Чернила, картридж для чернил, струйное записывающее устройство, печатный материал, фотополимеризуемое соединение, фотоотверждаемая композиция, материал для получения трехмерного объекта и трехмерный объект - RU2662521C2
Код документа: RU2662521C2
Чертежи

Описание
Область техники, к которой относится настоящее изобретение
Настоящее изобретение относится к чернилам, картриджу для чернил, струйному записывающему устройству и печатному материалу, использующему чернила, фотополимеризуемому соединению и фотоотверждаемой композиции, применяемой в чернилах, и материалу для получения трехмерного объекта и трехмерному объекту, полученному из фотоотверждаемой композиции.
Уровень техники настоящего изобретения
Способ струйной записи известен как способ получения изображения на материале для записи, таком как бумага. Данный способ записи обладает высокой эффективностью потребления чернил, является превосходным с точки зрения экономии ресурсов, и может сохранять низкую стоимость чернил на операцию единичной записи.
В последние годы привлекает внимание способ струйной записи, применяя чернила, отверждаемые ультрафиолетом.
Патентная литература 1 описывает (мет)акрилатное соединение, имеющее специфическую уретановую структуру, и отверждаемую лучами с активной энергией композицию, содержащую соединение, и чернильную композицию для струйной записи. Патентная литература 2 и 3 описывает отверждаемую лучами с активной энергией композицию, содержащую (мет)акрилатное соединение, исходным фрамгентом которого является углеводород, модифицированный алкоксигруппой, и чернильную композицию для струйной записи. Патентная литература 4 описывает композицию адгезионного средства для зубов, содержащую глицеринди(мет)акрилатное соединение. Патентная литература 5 описывает полимеризуемое по боковым группам соединение, имеющее эфирную структуру (-O-) или сложноэфирную структуру (―COO―) и в основной и в боковой цепи своей молекулы, и жидкокристаллическое устройство, применяя его.
Список ссылок
Патентная литература
патентная ссылка 1: выложенная японская патентная заявка (JP-A) No. 2013-256487
патентная ссылка 2: JP-A No. 2003-246818
патентная ссылка 3: JP-A No. 2005-239848
патентная ссылка 4: JP-A No. 09-227324
патентная ссылка 5: JP-A No. 06-32761
Сущность настоящего изобретения
Техническая проблема
Цель настоящего изобретения заключается в обеспечении чернил, в которых применяют фотополимеризуемое соединение, имеющее низкую вязкость и слабый запах по сравнению с общепринятыми соединениями, и которые обладают превосходной фотополимеризуемостью и фотоотверждаемостью.
Решение проблемы
Цель, описанную выше, достигают следующим изобретением 1).
1) Чернила, содержащие соединение, представленное общей формулой (1) ниже,

где в формуле выше, R1 представляет собой атом водорода или метильную группу, n представляет собой целое число, представляющее собой 2 или более, множество R1 могут быть одинаковыми или отличными друг от друга, X представляет собой углеводородную группу, содержащую 2-10 атомов углерода, Y представляет собой третичную гидроксильную группу или группу, имеющую сложноэфирную структуру, и m представляет собой целое 1 или больше.
Полезные эффекты настоящего изобретения
Настоящее изобретение может обеспечить чернилами, в которых применяют фотополимеризуемое соединение, имеющее низкую вязкость и слабый запах по сравнению с общепринятыми соединениями, и которые обладают превосходной фотополимеризуемостью и фотоотверждаемостью.
Краткое описание чертежей
Фигура 1 представляет собой схему, показывающую пример картриджа для чернил.
Фигура 2 представляет собой схему, объясняющую механизм печати струйного записывающего устройства.
Описание вариантов осуществления
(Чернила)
Соединение, представленное общей формулой (1) ниже, которое содержится в чернилах настоящего изобретения, содержит: две или более структур сложного эфира (мет)акриловой кислоты в качестве полимеризуемых функциональных групп; и одну или более третичных гидроксильных групп, или одну или более групп, имеющих сложноэфирную структуру, в качестве боковой структуры.

В формуле выше, R1 представляет собой атом водорода или метильную группу, n представляет собой целое число 2 или больше, множество R1 могут быть одинаковыми или отличными друг от друга, X представляет собой углеводородную группу, содержащую 2-10 атомов углерода, Y представляет собой третичную гидроксильную группу или группу, имеющую сложноэфирную структуру, и m представляет собой целое 1 или больше.
Соединение, содержащее несколько структур сложного эфира (мет)акриловой кислоты, которые представляют собой полимеризуемые функциональные группы, в своей молекуле, может образовывать сшитую структуру между своими молекулами при реакции полимеризации, и ее отверждаемость может улучшаться. Однако молекулярный вес и вязкость соединения будут увеличиваться по мере увеличения количества фрагментов сложного эфира (мет)акриловой кислоты в его молекуле, хотя его отверждаемость будет улучшаться. Следовательно, предпочтительно, чтобы n в общей формуле (1) выше было равно 2-4, и более предпочтительно 2 или 3.
Кроме того, ожидают, что введение полярной структуры в молекулы фотополимеризуемого соединения (мономера) будет усиливать взаимодействия между молекулами мономера и сближать их полимеризуемые функциональные группы друг с другом, посредством этого увеличивая реакционноспособность полимеризации мономера. Однако, например, введение первичной или вторичной гидроксильной группы (-OH) или протонной полярной структуры, такой как аминогруппа (-NH2), в мономер будет увеличивать вязкость мономера, и вызывать проблемы или накладывать ограничения в процессе применения мономера в качестве полимеризуемой композиции для различных типов чернил, и т.д. Кроме того, по мере увеличения вязкости мономера, подвижность молекул мономера снижается, что может ингибировать протекание реакции полимеризации мономера.
По сравнению с этим, введение третичной гидроксильной группы или апротонной полярной структуры в мономер будет приводить в результате к меньшему межмолекулярному взаимодействию, чем введение протонной полярной структуры, как выше, и будет обеспечивать одновременное удовлетворение подавления нарастания вязкости и увеличения реакционноспособности фотополимеризации и фотоотверждаемости. В частности, считают, что введение группы, имеющей эфирную структуру (эфирная группа или эфир угольной кислоты), будет подавлять нарастание вязкости, исходя из достаточной гибкости ее соединяющей части, соединяющей с исходной основной структурой, и подходящей степени полярности эфирной структуры, и будет обеспечивать одновременное удовлетворение увеличения реакционноспособности фотополимеризации и фотоотверждаемости, благодаря межмолекулярным взаимодействиям и снижению вязкости. Однако также, в данном случае, вязкость мономера будет увеличиваться по мере увеличения количества апротонных полярных структур, хотя реакционноспособность фотополимеризации и фотоотверждаемость мономера будут улучшаться. Следовательно, предпочтительно, чтобы m в общей формуле (1) выше было равно 1-3 и более предпочтительно 1 или 2.
Несмотря на изложенное выше, аналогично этому, считают, что введение эфирной структуры, которая представляет собой апротонную полярную структуру, будет менее способно увеличивать реакционноспособность фотополимеризации и фотоотверждаемости мономера, из-за полученных в результате слишком слабых межмолекулярных взаимодействий и большой свободы эфирной структуры. Кроме того, считают, что введение уретановой структуры в качестве апротонной полярной структуры будет увеличивать вязкость мономера из-за большей полярности уретановой структуры по сравнению с эфирной структурой, и жесткости уретановой структуры. Более того, та же сложноэфирная структура, как выше, которая, однако была присоединена наоборот по сравнению с настоящим изобретением (т.е., разветвляется через карбонильный углерод, а не через атом кислорода), будет вызывать увеличение вязкости мономера, поскольку данное связывание лишает сложноэфирную связь ее свободы, приводя в результате к жесткости молекул.
Как ясно из описания выше, соединение, представленное общей формулой (1) выше, обладает превосходной фотополимеризуемостью и фотоотверждаемостью, поскольку межмолекулярные взаимодействия и степень его молекулярной свободы можно регулировать до точного баланса, и обладает меньшим запахом. Кроме того, можно подавлять нарастание вязкости соединения, и оно будет иметь низкую вязкость, особенно когда его полярная группа представляет собой группу, имеющую сложноэфирную структуру. Следовательно, соединение, представленной общей формулой (1) выше, является пригодным для чернил.
В соединении, представленном общей формулой (1) выше, X представляет собой углеводородную группу, содержащую 2-10 атомов углерода. Его конкретные примеры включают группы, показанные ниже. Обратите внимание, что X также включает углеводородные цепи, присоединенные через гетероатом.

Среди них, группы, содержащие 2-8 атомов углерода, являются предпочтительными, и группы, показанные ниже, являются особенно предпочтительными.

В соединении, представленном общей формулой (1) выше, Y представляет собой третичную гидроксильную группу или группу, имеющую сложноэфирную структуру. Группа, представленная общей формулой (2) ниже, группа, представленная общей формулой (3) ниже, или обе являются предпочтительными в качестве группы, имеющей сложноэфирную структуру. В формуле, R2 представляет собой углеводородную группу, содержащую 1-15 атомов углерода, и предпочтительно углеводородную группу, содержащую 1-10 атомов углерода. Конкретные примеры R2 включают метильную группу, этильную группу, пропильную группу, бутильную группу, пентильную группу, гексильную группу, гептильную группу, октильную группу, нонильную группу и децильную группу. Данные группы могут быть линейными или разветвленными. Среди них, метильная группа и этильная группа являются предпочтительными.

Затем, конкретные примеры фотополимеризуемого соединения настоящего изобретения будут показаны ниже. Однако фотополимеризуемое соединение настоящего изобретения не ограничено ими. Обратите внимание, что R1 и R2 в данных примерах представляют собой, как описано выше.




Фотополимеризуемое соединение настоящего изобретения может представлять собой смесь двух или более различных соединений. В данном случае, примеры различных соединений включают структурные изомеры. Соотношение компонентов особым образом не ограничено.
Предпочтительный диапазон вязкости фотополимеризуемого соединения настоящего изобретения является различным, в зависимости от применения чернил. Кроме того, могут быть случаи, когда множество фотополимеризуемых соединений применяют в комбинации. Следовательно, предпочтительный диапазон вязкости нельзя определить абсолютно. Однако, его вязкость при 25°С обычно составляет приблизительно 50 мПа•с или ниже, предпочтительно 20 мПа•с или ниже, и более предпочтительно 15 мПа•с или ниже.
Содержание фотополимеризуемого соединения в чернилах обычно составляет от 20% по массе до 98% по массе, предпочтительно от 30% по массе до 90% по массе и более предпочтительно от 30% по массе до 80% по массе.
Предпочтительно, чтобы чернила дополнительно содержали инициатор фотополимеризации.
Примеры инициатора фотополимеризации включают инициатор фоторадикальной полимеризации, инициатор фотокатионной полимеризации (фотокислотный генератор) и инициатор фотоанионной полимеризации (фотоосновный генератор). Два или более типов можно применять в комбинации. Среди них, инициатор фоторадикальной полимеризации и инициатор фотоанионной полимеризации являются предпочтительными, и инициатор фоторадикальной полимеризации является особенно предпочтительным.
Инициатор фотополимеризации представляет собой соединение, которое генерирует частицы инициатора полимеризации, поглощением лучей с активной энергией.
Лучи с активной энергией конкретно не ограничены, и их примеры включают γ лучи, β лучи, электронные лучи, ультрафиолетовые лучи, видимый свет и инфракрасные лучи.
Инициатор фоторадикальной полимеризации конкретно не ограничен, и его примеры включают ароматические кетоны, ацилфосфиноксидное соединение, ароматическую ониевую соль, органический пероксид, тиосоединение, гексаарилбиимидазольное соединение, кетоксимное сложноэфирное соединение, боратное соединение, азиниевое соединение, металлоценовое соединение, активное сложноэфирное соединение, соединение, содержащее связь углерод-галоген и алкиламиновое соединение.
Конкретные примеры инициатора фоторадикальной полимеризации включает бензофенон, кетон Михлера, 4,4ʹ-бис(диэтиламино)бензофенон, ксантон, тиоксантон, изопропилксантон, 2,4-диэтилтиоксантон, 2-этилантрахинон, ацетофенон, 2-гидрокси-2-метил пропиофенон, 2-гидрокси-2-метил-4ʹ-изопропилпропиофенон, 1-гидроксициклогексилфенилкетон, изопропилбензоиновый эфир, изобутилбензоиновый эфир, 2,2-диэтоксиацетофенон, 2,2-диметокси-2-фенилацетофенон, камфорхинон, бензатрон, 2-метил-1-[4-(метилтио)фенил]-2-морфолинопропан-1-он, этил 2-бензил-2-диметиламино-1-(4-морфолинофенил)бутанон-1,4-диметиламинобензоат, изоамил 4-диметиламинобензоат, 4,4ʹ-ди(трет-бутилпероксикарбонил)бензофенон, 3,4,4ʹ-три(трет-бутилпероксикарбонил)бензофенон, 3,3ʹ,4,4ʹ-тетра(трет-бутилпероксикарбонил)бензофенон, 3,3ʹ,4,4ʹ-тетра(трет-гексилпероксикарбонил)бензофенон, 3,3ʹ-ди(метоксикарбонил)-4,4ʹ-бис(трет-бутилпероксикарбонил)бензофенон, 3,4ʹ-бис(метоксикарбонил)-4,3ʹ-бис(трет-бутилпероксикарбонил)бензофенон, 4,4ʹ-бис(метоксикарбонил)-3,3ʹ-бис(трет-бутилпероксикарбонил)бензофенон, 1,2-октандион,1-[4-(фенилтио)фенил]-2-(о-бензоилоксим), 2-(4ʹ-метоксистирил)-4,6-бис(трихлорметил)-s-триазин, 2-(3ʹ,4ʹ-диметоксистирил)-4,6-бис(трихлорметил)-s-триазин, 2-(2ʹ,4ʹ-диметоксистирил)-4,6-бис(трихлорметил)-s-триазин, 2-(2ʹ-метоксистирил)-4,6-бис(трихлорметил)-s-триазин, 2-(4ʹ-пентилоксистирил)-4,6-бис(трихлорметил)-s-триазин, 4-[п-N,N-ди(этоксикарбонилметил)]-2,6-ди(трихлорметил)-s-триазин, 1,3-бис(трихлорметил)-5-(2ʹ-хлорфенил)-s-триазин, 1,3-бис(трихлорметил)-5-(4ʹ-метоксифенил)-s-триазин, 2-(п-диметиламиностирил)бензоксазол, 2-(п-диметиламиностирил)бензотиазол, 2-меркаптобензотиазол, 3,3ʹ-карбонилбис(7-диэтиламинокумарин), 2-(o-хлорфенил)-4,4,5,5ʹ-тетрафенил-1,2ʹ-биимидазол, 2,2ʹ-бис(2-хлорфенил)-4,4ʹ,5,5ʹ-тетракис(4-этоксикарбонилфенил)-1,2ʹ-биимидазол, 2,2ʹ-бис(2,4-дихлорфенил)-4,4ʹ,5,5ʹ-тетрафенил-1,2ʹ-биимидазол, 2,2ʹ-бис(2,4-дибромфенил)-4,4ʹ,5,5ʹ-тетрафенил-1,2ʹ-биимидазол, 2,2ʹ-бис(2,4,6-трихлорфенил)-4,4ʹ,5,5ʹ-тетрафенил-1,2ʹ-биимидазол, 3-(2-метил-2-диметиламинопропионил)карбазол, 3,6-бис(2-метил-2-морфолинопропионил)-9-н-додецил карбазол, 1-гидроксициклогексилфенилкетон, бис(η5-2,4-циклопентадин-1-ил)-бис[2,6-дифтор-3-(1H-пиррол-1-ил)фенил]титан, бис(2,4,6-триметилбензоил)фенилфосфиноксид и 2,4,6-триметилбензоилдифенилфосфиноксид.
Среди них, бис(2,4,6-триметилбензоил)фенилфосфиноксид (IRGACURE 819), 2,4,6-триметилбензоилдифенилфосфиноксид (DAROCUR TPO), 1-гидроксициклогексилфенилкетон (IRGACURE 184), 2-метил-1-[4-(метилтио)фенил]-2-морфолинопропан-1-он (IRGACURE 907) и 2-диметиламино-2-(4-метилбензил)-1-(4-морфолин-4-илфенил)бутан-1-он (IRGACURE 379), все из которых получены у BASF Japan Ltd., являются предпочтительными, поскольку они обладают хорошей растворимостью в других компонентах, содержащихся в чернилах, и могут способствовать отверждению чернил при меньшем облучении ультрафиолетовыми лучами.
Отношение масс инициатора фотополимеризации относительно суммарного количества фотополимеризуемого соединения и красителя обычно составляет от 0,01 до 0,50, предпочтительно от 0,02 до 0,40, и более предпочтительно от 0,05 до 0,30.
Чернила могут дополнительно содержать краситель и могут, следовательно, давать цветное изображение.
Краситель конкретно не ограничен, и его примеры включают пигмент, жирорастворимый краситель, водорастворимый краситель и дисперсный краситель. Два или более типов можно применять в комбинации. Среди них, пигмент и жирорастворимый краситель являются предпочтительными, поскольку они обладают превосходной способностью выдерживать атмосферные воздействия и способностью воспроизводить насыщенный цвет, и пигмент является более предпочтительным.
Предпочтительно, чтобы краситель представлял собой соединение, которое не функционирует как ингибитор полимеризации для того, чтобы не снижать чувствительность к лучам с активной энергией для реакции фотополимеризации.
Примеры красного пигмента или пигмента маджента в качестве пигмента включают: пигмент красный 3, 5, 19, 22, 31, 38, 43, 48:1, 48:2, 48:3, 48:4, 48:5, 49:1, 53:1, 57:1, 57:2, 58:4, 63:1, 81, 81:1, 81:2, 81:3, 81:4, 88, 104, 108, 112, 122, 123, 144, 146, 149, 166, 168, 169, 170, 177, 178, 179, 184, 185, 208, 216, 226 и 257; пигмент фиолетовый 3, 19, 23, 29, 30, 37, 50 и 88; и пигмент оранжевый 13, 16, 20 и 36.
Примеры синего пигмента или голубого пигмента в качестве пигмента включают пигмент синий 1, 15, 15:1, 15:2, 15:3, 15:4, 15:6, 16, 17-1, 22, 27, 28, 29, 36 и 60.
Примеры зеленого пигмента в качестве пигмента включают пигмент зеленый 7, 26, 36 и 50.
Примеры желтого пигмента в качестве пигмента включают пигмент желтый 1, 3, 12, 13, 14, 17, 34, 35, 37, 55, 74, 81, 83, 93, 94, 95, 97, 108, 109, 137, 138, 139, 153, 154, 155, 157, 166, 167, 168, 180 и 193.
Примеры черного пигмента в качестве пигмента включают пигмент черный 7, 28 и 26.
Примеры белого пигмента в качестве пигмента включают пигмент белый 6, 18 и 21.
Примеры желтого жирорастворимого красителя включают: арильный или гетероарильный азокраситель, содержащий фенол, нафтол, анилин, пиразолон, пирролидон или активное метиленовое соединение с открытой цепью в качестве соединяющего компонента; метиновый краситель, содержащий активное метиленовое соединение с открытой цепью в качестве соединяющего компонента, такой как азометиновый краситель, бензилиденовый краситель и монометиновый оксоноловый краситель; краситель на основе хинона, такой как нафтохиноновый краситель и антрахиноновый краситель; хинофталоновый краситель; нитро-нитрозокраситель; акридиновый краситель; и акридиноновый краситель.
Примеры красного жирорастворимого красителя включают: арильный или гетероарильный азокраситель, содержащий фенол, нафтол или анилин в качестве соединяющего компонента; метиновый краситель, содержащий пиразолон или пиразолотриазол в качестве соединяющего компонента, такой как азометиновый краситель, арилиденовый краситель, стириловый краситель, мероцианиновый краситель и оксоноловый краситель; карбониевый краситель, такой как дифенилметановый краситель, трифенилметановый краситель и ксантеновый краситель; хиноновый краситель, такой как нафтохинон, антрахинон и антрапиридон; и конденсированный полициклический краситель, такой как диоксазин.
Примеры голубого жирорастворимого красителя включают: индоанилиновый краситель; индофенольный краситель; полиметиновый краситель, содержащий пирролотриазол в качестве соединяющего компонента, такой как азометиновый краситель, цианиновый краситель, оксоноловый краситель и мероцианиновый краситель; карбониевый краситель, такой как дифенилметановый краситель, трифенилметановый краситель и ксантеновый краситель; фталоцианиновый краситель; антрахиноновый краситель; арильный или гетероарильный азокраситель, содержащий фенол, нафтол или анилин в качестве соединяющего агента; и индиго или тиоиндиго краситель.
Конкретные примеры жирорастворимого красителя включают: C.I. жирорастворимый черный 3, 7, 27, 29, и 34; C.I. анилиновый желтый 14, 16, 19, 29, 30, 56, 82, 93, и 162; C.I. жирорастворимый красный 1, 3, 8, 18, 24, 27, 43, 49, 51, 72, 73, 109, 122, 132 и 218; C.I. жирорастворимый фиолетовый 3; C.I. жирорастворимый синий 2, 11, 25, 35, 38, 67, и 70: C.I. жирорастворимый зеленый 3, и 7; и C.I. жирорастворимый оранжевый 2.
Конкретные примеры дисперсного красителя включают: дисперсный желтый 5, 42, 54, 64, 79, 82, 83, 93, 99, 100, 119, 122, 124, 126, 160, 184:1, 186, 198, 199, 201, 204, 224 и 237; C.I. дисперсный оранжевый 13, 29, 31:1, 33, 49, 54, 55, 66, 73, 118, 119 и 163; C.I. дисперсный красный 54, 60, 72, 73, 86, 88, 91, 92, 93, 111, 126, 127, 134, 135, 143, 145, 152, 153, 154, 159, 164, 167:1, 177, 181, 204, 206, 207, 221, 239, 240, 258, 277, 278, 283, 311, 323, 343, 348, 356 и 362; C.I. дисперсный фиолетовый 33; C.I. дисперсный синий 56, 60, 73, 87, 113, 128, 143, 148, 154, 158, 165, 165:1, 165:2, 176, 183, 185, 197, 198, 201, 214, 224, 225, 257, 266, 267, 287, 354, 358, 365 и 368; и C.I. дисперсный зеленый 6:1 и 9.
Предпочтительно, чтобы пигмент диспергировали в чернилах в достаточной степени.
Диспергатор для диспергирования пигмента конкретно не ограничен, и его примеры включают шаровую мельницу, песочную мельницу, кольцевую мельницу, дробилку, вальцовую мельницу, мешалку, смеситель Хенкеля, коллоидную мельницу, ультразвуковой гомогенизатор, бисерную мельница, влажную струйную мельницу и шейкер для краски.
Диспергатор можно добавлять для диспергирования пигмента. Диспергатор конкретно не ограничен, но полимерный диспергатор является предпочтительным.
Отношение масс диспергатора к пигменту обычно составляет от 0,01 до 0,50.
Средний диаметр частиц пигмента в чернилах обычно составляет от 0,005 мкм до 0,5 мкм, предпочтительно от 0,01 мкм до 0,45 мкм, и более предпочтительно от 0,015 мкм до 0,4 мкм. Это позволяет подавить забивание форсунки головки и сохранить стабильность при хранении, прозрачность и фотоотверждаемость чернил.
Содержание красителя в чернилах обычно составляет от 0,5% по массе до 10% по массе, и предпочтительно от 1% по массе до 8% по массе.
Обратите внимание, что содержание красителя в белых чернилах, которые содержат белый пигмент, такой как оксид титана, в качестве красителя, обычно составляет от 5% по массе до 30% по массе, и предпочтительно от 10% по массе до 25% по массе. Это позволяет обеспечить укрывистость.
Чернила могут содержать любое другое фотополимеризуемое соединение, отличное от соединения, представленного общей формулой (1). Отношение масс любого другого фотополимеризуемого соединения к соединению, представленному общей формулой (1), обычно составляет от 0,01 до 100, и предпочтительно от 0,1 до 50.
Любое другое фотополимеризуемое соединение конкретно не ограничен, и его примеры включают фоторадикально полимеризуемое соединение, фотокатионно полимеризуемое соединение и фотоанионно полимеризуемое соединение. Два или более видов можно применять в комбинации.
Фоторадикально полимеризуемое соединение конкретно не ограничен, за исключением того, что оно должно представлять собой соединение, содержащее одну или более фоторадикально полимеризуемых этиленовых ненасыщенных групп, и оно включает мономер, олигомер, полимер и т.д. Его примеры включают: ненасыщенную карбоновую кислоту, такую как акриловая кислота, метакриловая кислота, итаконовая кислота, кротоновая кислота, изокротоновая кислота, малеиновая кислота и их соли, и соединения, полученные из них; ангидрид, содержащий этиленовую ненасыщенную группу; акрилонитрил; стирол; ненасыщенный полиэстер; ненасыщенный полиэфир; ненасыщенный полиамид; и ненасыщенный уретан.
Конкретные примеры фоторадикально полимеризуемого соединения включают: производные акриловой кислоты, такие как 2-гидроксиэтилакрилат, бутоксиэтилакрилат, карбитолакрилат, циклогексилакрилат, тетрагидрофурилакрилат, бензилакрилат, бис(4-акрилоксиполиэтоксифенил)пропан, неопентилгликольдиакрилат, этоксилированный неопентилгликольдиакрилат, пропоксилированный неопентилгликольдиакрилат, 1,6-гександиолдиакрилат, этиленгликольдиакрилат, диэтиленгликольдиакрилат, триэтиленгликольдиакрилат, тетраэтиленгликольдиакрилат, полиэтиленгликольдиакрилат, пропиленгликольдиакрилат, дипропиленгликольдиакрилат, трипропиленгликольдиакрилат, тетрапропиленгликольдиакрилат, полипропиленгликольдиакрилат, пентаэритритолтриакрилат, пентаэритритолтетраакрилат, дипентаэритритолтетраакрилат, триметилолпропантриакрилат, тетраметилолметантетраакрилат, акрилат олигоэстера и эпоксиакрилат; производные метакриловой кислоты, такие как метилметакрилат, н-бутилметакрилат, аллилметакрилат, глицидилметакрилат, бензилметакрилат, диметиламинометилметакрилат, 1,6-гександиолдиметакрилат, этиленгликольдиметакрилат, триэтиленгликольдиметакрилат, полиэтиленгликольдиметакрилат, полипропиленгликольдиметакрилат, триметилолэтантриметакрилат, триметилолпропанетриметакрилат и 2,2-бис(4-метакрилоксиполиэтоксифенил)пропан; производные акриламида, такие как N-метилолакриламид, диацетонакриламид, 2-гидроксиэтилакриламид и акрилоилморфолин; производное аллильного соединения, такое как аллилглицидиловый эфир, диаллилфталат и триаллилтримеллитат; ди- или тривинилэфирные соединения, такие как дивиниловый эфир этиленгликоля, моновиниловый эфир этиленгликоля, дивиниловый эфир диэтиленгликоля, моновиниловый эфир триэтиленгликоля, дивиниловый эфир триэтиленгликоля, дивиниловый эфир пропиленгликоля, дивиниловый эфир дипропиленгликоля, дивиниловый эфир бутандиола, дивиниловый эфир гександиола, дивиниловый эфир циклогександиметанола, моновиниловый эфир гидроксиэтила, моновиниловый эфир гидроксинонила и тривиниловый эфир триметилолпропана; моновинилэфирные соединения, такие как этилвиниловый эфир, н-бутилвиниловый эфир, изобутилвиниловый эфир, октадецилвиниловый эфир, циклогексилвиниловый эфир, гидроксибутилвиниловый эфир, 2-этилгексилвиниловый эфир, моновиниловый эфир циклогександиметанола, н-пропилвиниловый эфир, изопропилвиниловый эфир, изопропениловый эфир-о-пропиленкарбонат, додецилвиниловый эфир, моновиниловый эфир диэтиленгликоля и октадецилвиниловый эфир; и 2-этилгексилдигликольакрилат, 2-гидрокси-3-феноксипропилакрилат, 2-гидроксибутилакрилат, диакрилат неопентилгликоля и гидроксипивалевой кислоты, 2-акрилоилоксиэтилфталевая кислота, метоксиполиэтиленгликольакрилат, тетраметилолметантриакрилат, 2-акрилоилоксиэтил-2-гидроксиэтил фталевая кислота, диметилолтрициклодекандиакрилат, этоксилированный фенилакрилат, 2-акрилоилоксиэтилянтарная кислота, акрилат нонилфенолэтиленоксидного продукта присоединения, модифицированный глицеринтриакрилат, продукт присоединения диглицидильного эфира бисфенола A и акриловой кислоты, модифицированный бисфенол A диакрилат, феноксиполиэтиленгликольакрилат, 2-акрилоилоксиэтилгексагидрофталевая кислота, диакрилат продукта присоединения пропиленоксида к бисфенолу A, диакрилат продукта присоединения этиленоксида к бисфенолу A, дипентаэритритолгексаакрилат, пентаэритритолтриакрилат, толилендиизоцианатоуретановый преполимер, модифицированный лактоном эластичный акрилат, бутоксиэтилакрилат, продукт присоединения пропиленгликольдиглицидильного эфира к акриловой кислоте, пентаэритритолтриакрилат, гексаметилендиизоцианатоуретановый преполимер, 2-гидроксиэтилакрилат, метоксидипропиленгликольакрилат, дитриметилолпропантетраакрилат, пентаэритритолтриакрилат, гексаметилендиизоцианатоуретановый преполимер, стеарилакрилат, изоамилакрилат, изомиристилакрилат, изостеарилакрилат и модифицированный лактоном акрилат.
Примеры комбинации фотополимеризуемого соединения и инициатора фотополимеризации включают комбинацию фотокатионно полимеризуемого соединения и инициатора фотокатионной полимеризации, и комбинацию фотоанионнополимеризуемого соединения и инициатора фотоанионной полимеризации, в добавление к комбинации фоторадикально полимеризуемого соединения и инициатора фоторадикальной полимеризации.
Примеры фотокатионно полимеризуемого соединения включают эпоксисоединение, винилэфирное соединение и оксетановое соединение.
Примеры инициатор фотокатионной полимеризации включают: B(C6F5)4-, PF6-, AsF6-, SbF6- и CF3SO3- соли ароматических ониевых соединений, такие как диазоний, аммоний, йодоний, сульфоний и фосфоний; сульфированный продукт, который генерирует сульфокислоту; галогенид, который генерирует галогеноводород; и алленовый комплекс железа.
Примеры фотоанионно полимеризуемого соединения включают эпоксисоединение, лактоновое соединение, акриловое соединение и метакриловое соединение. Среди них, акриловые соединения и метакриловые соединения, представленные примерами фоторадикально полимеризуемого соединения, являются предпочтительными.
Примеры инициатора фотоанионной полимеризации включают о-нитробензилкарбаматное производное, о-ацилоксильное производное и о-карбамоилоксимамидиновое производное.
Чернила могут дополнительно содержать сенсибилизатор для того, чтобы способствовать разложению инициатора фотополимеризации при облучении лучами с активной энергией.
Сенсибилизатор поглощает лучи с активной энергией и переходит в электронно-возбужденное состояние, и контактирует с инициатором полимеризации в данном состоянии, посредством этого способствуя химическому изменению (разложению или генерированию радикала, кислоты или основания) инициатора полимеризации посредством таких эффектов, как миграция электронов, перенос энергии, выделение тепла и т.д.
Отношение масс сенсибилизатора к инициатору фотополимеризации обычно составляет от 5×10-3 до 200 и предпочтительно от 0,02 до 50.
Сенсибилизатор конкретно не ограничен, и сенсибилизирующий краситель, который поглощает длины волн в диапазоне длин волн от 350 нм до 450 нм. Его примеры включают: ароматическое соединение с конденсированными ядрами (например, пирен, перилен и трифенилен); ксантены (например, флуоресцеин, эозин, эритрозин, родамин B и бенгальский розовый); цианины (например, тиакарбоцианин и оксакарбоцианин); мероцианины (например, мероцианин и карбомероцианин); тиазины (например, тионин, метиленовый голубой и толуидиновый голубой); акридины (например, акридиновый оранжевый, хлорофлавин и акрифлавин); антрахиноны (например, антрахинон); скварилии (например, скварилий); и кумарины (например, 7-диэтиламино-4-метилкумарин).
Чернила могут дополнительно содержать косенсибилизатор.
Косенсибилизатор служат для дополнительного увеличения чувствительности сенсибилизирующего красителя к лучам с активной энергией, и подавляет ингибирование полимеризации фотополимеризуемого соединения в результате окисления.
Косенсибилизатор конкретно не ограничен, и его примеры включают: аминовые соединения, такие как триэтаноламин, этиловый эфир п-диметиламинобензойной кислоты, п-формилдиметиланилин и п-метилтиодиметиланилин; тиол, такой как 2-меркаптобензотиазол, 2-меркаптобензоксазол, 2-меркаптобензоимидазол, 2-меркапто-4(3H)-хиназолин и β-меркаптонафталин; и сульфиды.
Чернила могут дополнительно содержать инициатор полимеризации. Это позволяет улучшить стойкость при хранении (стабильность при хранении) чернил, и предотвратить забивание головки в результате термической полимеризации при впрыскивании чернил их нагреванием, и снизить их вязкость.
Инициатор полимеризации конкретно не ограничен, и его примеры включают гидрохинон, бензохинон, п-метоксифенол, TEMPO, TEMPOL и капферроновый комплекс алюминия.
Содержание инициатора полимеризации в чернилах обычно составляет от 200 частей на миллион до 20000 частей на миллион.
Вязкость чернил обычно составляет от 7 мПа•с до 30 мПа•с, и предпочтительно от 7 мПа•с до 25 мПа•с, в связи со способностью испускать струю из струйного записывающего устройства.
Предпочтительно, чтобы чернила не содержали растворителя, поскольку они представляют собой чернила, отверждаемые лучами с активной энергией. Однако, для того чтобы обеспечить лучшую адгезивность с материалом для записи после отверждения, чернила могут содержать растворитель, при условии, что это не влияет на скорость отверждения и т.д.
Растворитель конкретно не ограничен, и его примеры включают органический растворитель и воду.
Содержание органического растворителя в чернилах обычно составляет от 0,1% по массе до 5% по массе, и более предпочтительно от 0,1% по массе до 3% по массе.
Чернила могут дополнительно содержать поверхностно-активное соединение, выравнивающую добавку, матирующий агент и смолу на основе полиэстра, смолу на основе полиуретана, виниловую смолу, акриловую смолу на основе резины или воск для регулирования пленкообразующих свойств.
Чернила могут дополнительно содержать агент, придающий клейкость (агент, повышающий клейкость), не обладающий ингибирующим полимеризацию свойством для того, чтобы увеличить адгезивность с полиолефином, PET и т.д.
(Картридж для чернил)
Чернила можно содержать в контейнере и можно применять в виде картриджа для чернил. Это устраняет необходимость непосредственного контакта с чернилами при таких операциях, как замена чернил и т.д., и позволяет предотвратить загрязнение рук, пальцев и одежды. Это также предотвращает попадание чужеродного материала, такого как пыль, в чернила. Контейнер конкретно не ограничен, и его примеры включают пакет для чернил, изготовленный из воздухонепроницаемой алюминиевой многослойной пленки или полимерной пленки.
Фигура 1 показывает пример картриджа для чернил.
Отсек 11 для чернил содержит отверстие 12 для ввода чернил и отверстие 13 для выпуска чернил. Отсек 11 для чернил заполняют чернилами через отверстие 12 для ввода чернил, удаляют остаточный воздух из отсека 11 для чернил, и затем герметично закрывают отверстие 12 для ввода чернил наплавлением. Для применения отсека 11 для чернил, отверстие 13 для выпуска чернил прокалывают иголкой, имеющейся на корпусе струйного записывающего устройства, и чернила подают в струйное записывающее устройство. Отверстие 13 для выпуска чернил изготавливают из резинового материала.
Отсек 11 для чернил содержат в корпусе 14 картриджа, полученного из пластика, и он разъемно соединен со струйным записывающим устройством в виде картриджа 10 для чернил. Разъемная конфигурация позволяет увеличить эффективность работы по пополнению и замене чернил и т.д.
(Струйное записывающее устройство)
Струйное записывающее устройство включает картридж для чернил и струйную головку, рассчитанную на осуществление записи нанесением чернил.
Способ нанесения чернил конкретно не ограничен, и его примеры включают способ последовательного нанесения и способ печати по требованию. Примеры способа печати по требованию включают пьезоспособ, термический способ и электростатический способ.
Механизм печати струйного записывающего устройства будет описан со ссылкой на фигуру 2.
Номера позиций 23 обозначают печатающие элементы. Печатающие элементы 23a, 23b, 23c и 23d для желтых, красных, голубых и черных струйных чернил, соответственно, на материале 22 основы для печати, подаваемом барабаном для подачи материала 21 основы для печати. Желтые, красные, голубые и черные чернила наносятся отдельно. После этого, чернила облучают и отверждают источниками ультрафиолетовых лучей 24a, 24b, 24c и 24d для фотоотверждения чернил, посредством этого образуя цветное изображение. После этого, материал 22 основы для печати подают в блок 25 для обработки и приемный валик 26 для печатного материала.
Печатающие элементы 23a, 23b, 23c и 23d можно обеспечивать нагревающим механизмом для того, чтобы чернила были жидкими в области нанесения чернил.
Могут возникнуть случаи, когда температура материала основы становится высокой, что часто является случаем, когда площадь печати непосредственно напечатанного цвета является большой, или когда скорость подачи является высокой. Следовательно, в соответствии с необходимостью, можно обеспечивать контактный или бесконтактный механизм охлаждения материала основы до приблизительно комнатной температуры.
Материал 22 основы для печати конкретно не ограничен, и его примеры включают бумагу, пленку, метал и их составные материалы. Материал 22 основы для печати может иметь форму листа. Печать можно осуществлять на одной стороне или обеих сторонах.
Кроме того, ультрафиолетовое облучение источниками 24a, 24b и 24c света можно ослаблять или пропускать, и ультрафиолетовое облучение можно осуществлять только источником 24d света после печати нескольких цветов. Это обеспечивает энергосбережение и экономию расходов.
(Печатный материал)
Примеры печатного материала, на котором осуществляют запись чернилами настоящего изобретения, включают не только печатные материалы, для которых печать осуществляют на гладкой поверхности, такие как стандартная бумага и полимерная пленка, но также печатные материалы, для которых печать осуществляют на поверхности, имеющей шероховатости, и печатные материалы, для которых печать осуществляют на поверхности, изготовленной из различных материалов, таких как металл и керамика.
Фотополимеризуемое соединение и фотоотверждаемая композиция настоящего изобретения являются пригодными в качестве материала чернил, но их также можно применять для формовочной смолы, краски, адгезива, изолирующего материала, разделительного агента, материала для нанесения покрытия, герметизирующего материала, различных типов резистов и различных типов оптических материалов. Кроме того, фотоотверждаемую композицию настоящего изобретения можно применять в качестве материала для получения трехмерного объекта, и, например, можно применять в качестве связующего частиц порошка, применяемых в способе наложения слоев порошка, который представляет собой один из способов получения трехмерных объектов, или в качестве материала для получения трехмерного объекта способом нанесения материала для получения трехмерных объектов нанесением фотоотверждаемой композиции на предварительно определенную область, отверждая ее ультрафиолетовыми лучами, и затем складывая данные отвержденные продукты, или способом для получения трехмерных объектов последующим складыванием отвержденных слоев, имеющих заранее определенную форму, которые получают испусканием ультрафиолетовых лучей в пул хранения фотоотверждаемой композиции. Устройство для получения трехмерных объектов, когда фотоотверждаемую композицию настоящего изобретения применяют в качестве материала для получения трехмерного объекта, конкретно не ограничено, и может представлять собой общеизвестное устройство.
Примеры
Настоящее изобретение будет описано ниже более подробно представлением примеров и сравнительных примеров. Настоящее изобретение не ограничивается данными примерами. Обратите внимание, что ʺчастьʺ и ʺ%ʺ в примерах представляют собой ʺчасть по массеʺ и ʺ% по массеʺ.1H-ЯМР спектры регистрировали1H-ЯМР (500 МГц) (полученным JEOL Ltd.), и ИК спектры регистрировали FT-IR SPECTRUM GX (полученным Perkin Elmer Co., Ltd.).
Пример 1a
Соединение 1 получали согласно способу ниже.
1-(акрилоилокси)-3-(метакрилоилокси)-2-пропанол (5,4 г) (24 ммоль), полученный Tokyo Chemical Industry Co., Ltd., добавляли к сухому дихлорметану (100 мл), и после продувания колбы аргоном, добавляли в нее триэтиламин (3,6 г) (36 ммоль). Затем, после охлаждения ее до приблизительно -10°С, медленно прикапывали к ней хлорангидрид уксусной кислоты (2,4 г) (30 ммоль) так, чтобы внутренняя температура системы составляла от -10°С до -5°С, и затем их перемешивали при комнатной температуре в течение 2 часов. Затем, после удаления выпавшего продукта фильтрованием, фильтрат промывали водой, насыщенным водным раствором бикарбоната натрия и насыщенным водным раствором хлорида натрия. Затем, после сушки фильтрата сульфатом натрия, полученный в результате раствор концентрировали при пониженном давлении, посредством этого получая желтое маслянистое вещество. Затем, желтое маслянистое вещество очищали колоночной хроматографией, в которой колонку заполняли WAKOGEL C300 (полученным Wako Pure Chemical Industries, Ltd.) (200 г), и гексан и этилацетат применяли в качестве элюентов, посредством этого получая бесцветное маслянистое вещество (1,8 г) соединения 1, представленного химической формулой ниже (выход: приблизительно 28%).

Идентификационные данные были, как показано ниже.
1H-ЯМР (CDCl3): δ1,95 (с, 3H), 2,09 (д, 3H), 4,22-4,44 (м, 4H), 5,33-5,42 (м, 1H), 5,59-5,62 (м, 1H), 5,86-5,92 (м, 1H), 6,10-6,18 (м, 1H), 6,40-6,48 (м, 1H)
ИК (NaCl): 2961, 1720, 1637, 1454, 1409, 1372, 1322, 1296, 1232, 1164, 1099, 1066, 1022, 985, 809, 602 см-1
Пример 2a
Соединение 2 получали согласно способу ниже.
Диметакрилат глицерина (5,7 г) (25 ммоль), полученный Tokyo Chemical Industry Co., Ltd., добавляли к сухому дихлорметану (100 мл), и после продувания колбы аргоном, добавляли в нее триэтиламин (3,6 г) (36 ммоль). Затем, после охлаждения ее до приблизительно -10°С, медленно прикапывали в нее хлорангидрид уксусной кислоты (2,4 г) (30 ммоль) так, чтобы внутренняя температура системы составляла бы от -10°С до-5°С, и затем их перемешивали при комнатной температуре в течение 2 часов. Затем, после удаления выпавшего продукта фильтрованием, фильтрат промывали водой, насыщенным водным раствором бикарбоната натрия и насыщенным водным раствором хлорида натрия. Затем, после сушки фильтрата сульфатом натрия, полученный в результате раствор концентрировали при пониженном давлении, посредством этого получая желтое маслянистое вещество. Затем, желтое маслянистое вещество очищали колоночной хроматографией, в которой колонку заполняли WAKOGEL C300 (полученным Wako Pure Chemical Industries, Ltd.) (200 г), и гексан и этилацетат применяли в качестве элюентов, посредством этого получая бесцветное маслянистое вещество (3,2 г) соединения 2, представленного химической формулой ниже (выход: приблизительно 47%).

Идентификационные данные были, как показано ниже.
1H-ЯМР (CDCl3): δ1,95 (с, 6H), 2,09 (д, 3H), 4,23-4,42 (м, 4H), 5,35-5,42 (м, 1H), 5,59-5,63 (м, 2H), 6,10-6,15 (м, 2H)
ИК (NaCl): 2961, 1748, 1725, 1638, 1454, 1405, 1373, 1323, 1295, 1234, 1161, 1098, 1050, 1017, 946, 813, 651, 602 см-1
Пример 3a
Соединение 3 получали согласно способу ниже.
Диметакрилат глицерина (13,7 г) (60 ммоль), полученный Tokyo Chemical Industry Co., Ltd., добавляли к сухому дихлорметану (150 мл), и после продувания колбы аргоном, добавляли в нее триэтиламин (7,9 г) (78 ммоль). Затем, после охлаждения ее до приблизительно -10°С, медленно прикапывали в нее пропионилхлорид (7,2 г) (78 ммоль) так, чтобы внутренняя температура системы составляла бы от -10°С до -5°С, и затем их перемешивали при комнатной температуре в течение 2 часов. Затем, после удаления выпавшего продукта фильтрованием, фильтрат промывали водой, насыщенным водным раствором бикарбоната натрия и насыщенным водным раствором хлорида натрия. Затем, после сушки фильтрата сульфатом натрия, полученный в результате раствор концентрировали при пониженном давлении, посредством этого получая коричневое маслянистое вещество. Затем, коричневое маслянистое вещество очищали колоночной хроматографией, в которой колонку заполняли WAKOGEL C300 (полученным Wako Pure Chemical Industries, Ltd.) (360 г), и гексан и этилацетат применяли в качестве элюентов, посредством этого получая бесцветное маслянистое вещество (7,1 г) соединения 3, представленного химической формулой ниже (выход: приблизительно 42%).

Идентификационные данные были, как показано ниже.
1H-ЯМР (CDCl3): δ1,14 (т, 3H), 1,94 (с, 6H), 2,35 (кв, 2H), 4,24-4,42 (м, 4H), 5,36-5,42 (м, 1H), 5,58-5,62 (м, 2H), 6,10-6,15 (м, 2H)
ИК (NaCl): 2983, 2961, 1725, 1638, 1455, 1405, 1378, 1322, 1295, 1163, 1098, 1012, 945, 861, 813, 653 см-1
Пример 4a
Соединение 4 получали согласно способу ниже.
Диметакрилат глицерина (11,4 г) (50 ммоль), полученный Tokyo Chemical Industry Co., Ltd., добавляли к сухому дихлорметану (100 мл), и после продувания колбы аргоном, добавляли в нее триэтиламин (7,6 г) (75 ммоль). Затем, после охлаждения ее до приблизительно -10°С, медленно прикапывали в нее бутирилхлорид (6,9 г) (65 ммоль) так, чтобы внутренняя температура системы составляла бы от -10°С до -5°С, и затем их перемешивали при комнатной температуре в течение 2 часов. Затем, после удаления выпавшего продукта фильтрованием, фильтрат промывали водой, насыщенным водным раствором бикарбоната натрия и насыщенным водным раствором хлорида натрия. Затем, после сушки фильтрата сульфатом натрия, полученный в результате раствор концентрировали при пониженном давлении, посредством этого получая желтое маслянистое вещество. Затем, желтое маслянистое вещество очищали колоночной хроматографией, в которой колонку заполняли WAKOGEL C300 (полученным Wako Pure Chemical Industries, Ltd.) (300 г), и гексан и этилацетат применяли в качестве элюентов, посредством этого получая бесцветное маслянистое вещество (2,9 г) соединения 4, представленного химической формулой ниже (выход: приблизительно 19%).

Идентификационные данные были, как показано ниже.
1H-ЯМР (CDCl3): δ0,95 (т, 3H), 1,65 (кв, 2H), 1,94 (с, 6H), 2,29-2,34 (м, 2H), 4,24-4,42 (м, 4H), 5,36-5,42 (м, 1H), 5,58-5,62 (м, 2H), 6,10-6,14 (м, 2H)
ИК (NaCl): 2965, 2978, 1726, 1638, 1455, 1405, 1378, 1322, 1295, 1252, 1162, 1097, 1013, 945, 813, 652 см-1
Пример 5a
Соединение 5 получали согласно способу ниже.
Диметакрилат глицерина (9,1 г) (40 ммоль), полученный Tokyo Chemical Industry Co., Ltd., добавляли к сухому дихлорметану (100 мл), и после продувания колбы аргоном, добавляли в нее триэтиламин (6,1 г) (60 ммоль). Затем, после охлаждения ее до приблизительно -10°С, медленно прикапывали в нее пивалоилхлорид (6,0 г) (50 ммоль) так, чтобы внутренняя температура системы составляла бы от -10°С до -5°С, и затем их перемешивали при комнатной температуре в течение 2 часов, и затем перемешивали при от 35°С до 40°С в течение 3 часов. Затем, после удаления выпавшего продукта фильтрованием, фильтрат промывали водой, насыщенным водным раствором бикарбоната натрия и насыщенным водным раствором хлорида натрия. Затем, после сушки фильтрата сульфатом натрия, полученный в результате раствор концентрировали при пониженном давлении, посредством этого получая желтое маслянистое вещество. Затем, желтое маслянистое вещество очищали колоночной хроматографией, в которой колонку заполняли WAKOGEL C300 (полученным Wako Pure Chemical Industries, Ltd.) (300 г), и гексан и этилацетат применяли в качестве элюентов, посредством этого получая бесцветное маслянистое вещество (2,0 г) соединения 5, представленного химической формулой ниже (выход: приблизительно 16%).

Идентификационные данные были, как показано ниже.
1H-ЯМР (CDCl3): δ1,20 (с, 9H), 1,94 (с, 6H), 4,22-4,42 (м, 4H), 5,34-5,44 (м, 1H), 5,58-5,62 (м, 2H), 6,10-6,13 (м, 2H)
ИК (NaCl): 2976, 2932, 1728, 1637, 1558, 1481, 1456, 1399, 1368, 1322, 1294, 1155, 1096, 1029, 1011, 943, 813, 768 см-1
Пример 6a
Соединение 6 получали согласно способу ниже.
Диметакрилат глицерина (6,9 г) (30 ммоль), полученный Tokyo Chemical Industry Co., Ltd., добавляли к сухому дихлорметану (100 мл), и после продувания колбы аргоном, добавляли в нее триэтиламин (4,9 г) (48 ммоль). Затем, после охлаждения ее до приблизительно -10°С, медленно прикапывали в нее 2-этилгексаноилхлорид (6,5 г) (40 ммоль) так, чтобы внутренняя температура системы составляла бы от -10°С до -5°С, и затем их перемешивали при комнатной температуре в течение 2 часов. Затем, после удаления выпавшего продукта фильтрованием, фильтрат промывали водой, насыщенным водным раствором бикарбоната натрия и насыщенным водным раствором хлорида натрия. Затем, после сушки фильтрата сульфатом натрия, полученный в результате раствор концентрировали при пониженном давлении, посредством этого получая бесцветное маслянистое вещество. Затем, бесцветное маслянистое вещество очищали колоночной хроматографией, в которой колонку заполняли WAKOGEL C300 (полученный Wako Pure Chemical Industries, Ltd.) (300 г), и гексан и этилацетат применяли в качестве элюентов, посредством этого получая бесцветное маслянистое вещество (3,5 г) соединения 6, представленного химической формулой ниже (выход: приблизительно 33%).

Идентификационные данные были, как показано ниже.
1H-ЯМР (CDCl3): δ0,84-0,90 (м, 6H), 1,18-1,33 (м, 4H), 1,41-1,66 (м, 4H), 1,94 (с, 6H), 2,26-2,32 (м, 1H), 4,24-4,42 (м, 4H), 5,36-5,44 (м, 1H), 5,57-5,62 (м, 2H), 6,11-6,13 (м, 2H)
ИК (NaCl): 2962, 2933, 2875, 1727, 1638, 1456, 1403, 1379, 1322, 1294, 1264, 1159, 1096, 1011, 943, 855, 813, 749, 652 см-1
Пример 7a
Соединение 7 получали согласно способу ниже.
Диметакрилат глицерина (6,9 г) (30 ммоль), полученный Tokyo Chemical Industry Co., Ltd., добавляли к сухому дихлорметану (100 мл), и после продувания колбы аргоном, добавляли в нее триэтиламин (4,9 г) (48 ммоль). Затем, после охлаждения ее до приблизительно -10°С, медленно прикапывали в нее лауроилхлорид (додеканоилхлорид) (8,8 г) (40 ммоль) так, чтобы внутренняя температура системы составляла бы от -10°С до -5°С, и затем их перемешивали при комнатной температуре в течение 2 часов. Затем, после удаления выпавшего продукта фильтрованием, фильтрат промывали водой, насыщенным водным раствором бикарбоната натрия и насыщенным водным раствором хлорида натрия. Затем, после сушки фильтрата сульфатом натрия, полученный в результате раствор концентрировали при пониженном давлении, посредством этого получая бесцветное маслянистое вещество. Затем, бесцветное маслянистое вещество очищали колоночной хроматографией, в которой колонку заполняли WAKOGEL C300 (полученный Wako Pure Chemical Industries, Ltd.) (300 г), и гексан и этилацетат применяли в качестве элюентов, посредством этого получая бесцветное маслянистое вещество (1,5 г) соединения 7, представленного химической формулой ниже (выход: приблизительно 12%).

Идентификационные данные были, как показано ниже.
1H-ЯМР (CDCl3): δ0,88 (т, 3H), 1,20-1,34 (м, 16H), 1,57-1,64 (м, 2H), 1,94 (с, 6H), 2,30-2,34 (м, 2H), 4,23-4,42 (м, 4H), 5,36-5,43 (м, 1H), 5,58-5,63 (м, 2H), 6,10-6,13 (м, 2H)
ИК (NaCl): 2956, 2927, 2855, 1727, 1638, 1455, 1404, 1377, 1322, 1294, 1234, 1158, 1099, 1012, 942, 813, 722, 652 см-1
Пример 8a
Соединение 8 получали согласно способу ниже.
Диметакрилат глицерина (13,7 г) (60 ммоль), полученный Tokyo Chemical Industry Co., Ltd., добавляли к сухому дихлорметану (150 мл), и после продувания колбы аргоном, добавляли в нее триэтиламин (7,9 г) (78 ммоль). Затем, после охлаждения ее до приблизительно -10°С, медленно прикапывали в нее метилхлорформиат (7,4 г) (78 ммоль) так, чтобы внутренняя температура системы составляла бы от -10°С до -5°С, и затем их перемешивали при комнатной температуре в течение 2 часов. Затем, после удаления выпавшего продукта фильтрованием, фильтрат промывали водой, насыщенным водным раствором бикарбоната натрия и насыщенным водным раствором хлорида натрия. Затем, после сушки фильтрата сульфатом натрия, полученный в результате раствор концентрировали при пониженном давлении, посредством этого получая бледно-розовое маслянистое вещество. Затем, бледно-розовое маслянистое вещество очищали колоночной хроматографией, в которой колонку заполняли WAKOGEL C300 (полученный Wako Pure Chemical Industries, Ltd.) (390 г), и гексан и этилацетат применяли в качестве элюентов, посредством этого получая бесцветное маслянистое вещество (2,3 г) соединения 8, представленного химической формулой ниже (выход: приблизительно 13%).

Идентификационные данные были, как показано ниже.
1H-ЯМР (CDCl3): δ1,94 (с, 6H), 3,80 (д, 3H), 4,28-4,46 (м, 4H), 5,21-5,40 (м, 1H), 5,59-5,62 (м, 2H), 6,10-6,14 (м, 2H)
ИК (NaCl): 2960, 2931, 1755, 1725, 1638, 1444, 1404, 1378, 1325, 1270, 1160, 1098, 1012, 988, 947, 882, 817, 790, 653 см-1
Пример 9a
Соединение 9 получали согласно способу ниже.
Диметакрилат глицерина (13,7 г) (60 ммоль), полученный Tokyo Chemical Industry Co., Ltd., добавляли к сухому дихлорметану (150 мл), и после продувания колбы аргоном, добавляли в нее триэтиламин (7,9 г) (78 ммоль). Затем, после охлаждения ее до приблизительно -10°С, медленно прикапывали в нее метилхлорформиат (8,5 г) (78 ммоль) так, чтобы внутренняя температура системы составляла бы от -10°С до -5°С, и затем их перемешивали при комнатной температуре в течение 2 часов. Затем, после удаления выпавшего продукта фильтрованием, фильтрат промывали водой, насыщенным водным раствором бикарбоната натрия и насыщенным водным раствором хлорида натрия. Затем, после сушки фильтрата сульфатом натрия, полученный в результате раствор концентрировали при пониженном давлении, посредством этого получая бледно-розовое маслянистое вещество. Затем, бледно-розовое маслянистое вещество очищали колоночной хроматографией, в которой колонку заполняли WAKOGEL C300 (полученный Wako Pure Chemical Industries, Ltd.) (380 г), и гексан и этилацетат применяли в качестве элюентов, посредством этого получая коричневое маслянистое вещество (5,2 г) соединения 9, представленного химической формулой ниже (выход: приблизительно 29%).

Идентификационные данные были, как показано ниже.
1H-ЯМР (CDCl3): δ1,32 (дд, 3H), 1,94 (с, 6H), 4,18-4,26 (м, 2H), 4,28-4,35 (м, 2H), 4,40-4,46 (м, 2H), 5,22-5,40 (м, 1H), 5,58-5,62 (м, 2H), 6,10-6,14 (м, 2H)
ИК (NaCl): 2984, 2932, 1750, 1725, 1638, 1454, 1404, 1373, 1324, 1296, 1262, 1160, 1093, 1011, 945, 870, 813, 788, 653, 597 см-1
Пример 10a
Соединение 10 получали согласно способу ниже.
3-метилпентан-1,3,5-триол (6,7 г) (50 ммоль), полученный Tokyo Chemical Industry Co., Ltd., добавляли к сухому дихлорметану (100 мл), и после продувания колбы аргоном, добавляли в нее триэтиламин (12,1 г) (120 ммоль). Затем, после охлаждения ее до приблизительно -10°С, медленно прикапывали в нее хлорангидрид метакриловой кислоты (10,5 г) (100 ммоль) так, чтобы внутренняя температура системы составляла бы от -10°С до -5°С, и затем их перемешивали при комнатной температуре в течение 2 часов. Затем, после удаления выпавшего продукта фильтрованием, фильтрат промывали водой, насыщенным водным раствором бикарбоната натрия и насыщенным водным раствором хлорида натрия. Затем, после сушки фильтрата сульфатом натрия, полученный в результате раствор концентрировали при пониженном давлении, посредством этого получая коричневое маслянистое вещество. Затем, коричневое маслянистое вещество очищали колоночной хроматографией, в которой колонку заполняли WAKOGEL C300 (полученный Wako Pure Chemical Industries, Ltd.) (350 г) и гексан и этилацетат применяли в качестве элюентов, посредством этого получая бледно-желтое маслянистое вещество (8,9 г) соединения 10, представленного химической формулой ниже (выход: приблизительно 66%).
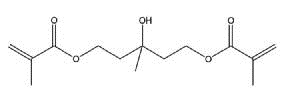
Идентификационные данные были, как показано ниже.
1H-ЯМР (CDCl3): δ 1,30 (с, 3H), 1,91-1,95 (с+т, 6H+4H), 2,15 (уш, 1H), 4,34 (т, 4H), 5,55-5,59 (м, 2H), 6,07-6,10 (м, 2H)
ИК (NaCl): 3504, 2972, 1717, 1637, 1453, 1376, 1325, 1298, 1163, 1013, 943, 815 см-1
Пример 11a
Соединение 11 получали согласно способу ниже.
3-Метилпентан-1,3,5-триол (13,4 г) (100 ммоль), полученный Tokyo Chemical Industry Co., Ltd., добавляли к сухому дихлорметану (100 мл), и после продувания колбы аргоном, добавляли в нее триэтиламин (24,3 г) (240 ммоль). Затем, после охлаждения ее до приблизительно -10°С, медленно прикапывали в нее хлорангидрид акриловой кислоты (21,7 г) (240 ммоль) так, чтобы внутренняя температура системы составляла бы от -10°С до -5°С, и затем их перемешивали при комнатной температуре в течение 2 часов. Затем, после удаления выпавшего продукта фильтрованием, фильтрат промывали водой, насыщенным водным раствором бикарбоната натрия и насыщенным водным раствором хлорида натрия. Затем, после сушки фильтрата сульфатом натрия, полученный в результате раствор концентрировали при пониженном давлении, посредством этого получая коричневое маслянистое вещество. Затем, коричневое маслянистое вещество очищали колоночной хроматографией, в которой колонку заполняли WAKOGEL C300 (полученный Wako Pure Chemical Industries, Ltd.) (350 г), и гексан и этилацетат применяли в качестве элюентов, посредством этого получая бесцветное маслянистое вещество (4,1 г) соединения 11, представленного химической формулой ниже (выход: приблизительно 17%).

Идентификационные данные были, как показано ниже.
1H-ЯМР (CDCl3): δ1,30 (с, 3H), 1,88-1,98 (м, 5H), 4,36 (т, 4H), 5,84 (дд, 2H), 6,08-6,15 (м, 2H), 6,40 (дд, 2H)
ИК (NaCl): 3491, 2972, 1724, 1636, 1619, 1463, 1410, 1298, 1277, 1199, 1057, 984, 812 см-1
Сравнительный пример 1a
Имеющийся в продаже диметакрилат 1,6-гександиола, представленный химической формулой ниже, применяли в качестве соединения сравнительного примера 1a.

Сравнительный пример 2a
Имеющийся в продаже диметакрилат 1,3-бутандиола, представленный химической формулой ниже, применяли в качестве соединения сравнительного примера 2a.

Сравнительный пример 3a
Имеющийся в продаже диметакрилат неопентилгликоля, представленный химической формулой ниже, применяли в качестве соединения сравнительного примера 3a.

Сравнительный пример 4a
Имеющийся в продаже диметакрилат диэтиленгликоля, представленный химической формулой ниже, применяли в качестве соединения сравнительного примера 4a.

Сравнительный пример 5a
Имеющийся в продаже диметакрилат полиэтиленгликоля (p=9), представленный химической формулой ниже, применяли в качестве соединения сравнительного примера 5a.

Сравнительный пример 6a
Имеющийся в продаже диметакрилат глицерина, представленный химической формулой ниже, применяли в качестве соединения сравнительного примера 6a.

Сравнительный пример 7a
Имеющийся в продаже 1-(акрилоилокси)-3-(метакрилоилокси)-2-пропанол, представленный химической формулой ниже, применяли в качестве соединения сравнительного примера 7a.
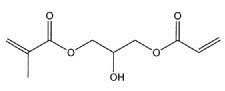
Сравнительный пример 8a
Сравнительное соединение 1 получали согласно способу ниже.
Диэтилкарбамоилхлорид (27,1 г, 200 ммоль) медленно добавляли к смеси глицерина (46,0 г, 540 ммоль) и пиридина (47 г) при комнатной температуре, и затем они реагировали при приблизительно 50°С в течение приблизительно 15 часов. После концентрирования реакционной смеси при пониженном давлении, удаляя избыток пиридина, добавляли к ней 10% хлористоводородную кислоту, подкисляя реакционную смесь, которую, затем, концентрировали при пониженном давлении, удаляя воду, посредством этого получая коричневое маслянистое вещество. Полученное маслянистое вещество экстрагировали этилацетатом, и слой экстракта сушили безводным сульфатом натрия. Этилацетатный раствор концентрировали, и полученное в результате желтое маслянистое вещество (27 г) очищали колоночной хроматографией (WAKOGEL C300, 400 г), посредством этого получая бесцветное маслянистое вещество (16,1 г), представленное химической формулой ниже, в качестве промежуточного продукта (выход: приблизительно 42%).
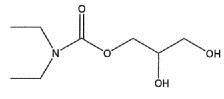
Идентификационные данные промежуточного продукта были, как показано ниже.
1H-ЯМР (CDCl3): δ 1,13 (т, 6H), 3,23-3,33 (м, 4H), 3,56-3,62 (м, 1H), 3,63-3,69 (м, 1H), 3,73 (д, 1H), 3,77-3,82 (м, 1H), 3,86-3,92 (м, 1H), 4,20 (уш с, 2H)
ИК (NaCl): 3419, 2974, 2936, 2878, 1681, 1485, 1457, 1431, 1381, 1365, 1316, 1280, 1225, 1180, 1071, 1009, 770 см-1
Затем, промежуточный продукт (6,7 г) (35 ммоль) добавляли к сухому дихлорметану (70 мл), и после продувания колбы аргоном, добавляли к ним триэтиламин (11,1 г) (110 ммоль). После охлаждения смеси до приблизительно -10°С, медленно прикапывали в нее хлорангидрид метакриловой кислоты (9,4 г) (90 ммоль) так, чтобы внутренняя температура системы составляла бы от -10°С до -5°С, и затем их перемешивали при комнатной температуре в течение 2 часов. Выпавший продукт удаляли фильтрованием, и фильтрат промывали водой, насыщенным водным раствором бикарбоната натрия и насыщенным водным раствором хлорида натрия, сушили сульфатом натрия, и затем концентрировали при пониженном давлении, посредством этого получая коричневое маслянистое вещество. Полученное масляное вещество очищали колоночной хроматографией (WAKOGEL C300, 250 г), посредством этого получая бесцветное маслянистое вещество (7,8 г) сравнительного соединения 1, представленного химической формулой ниже (выход: приблизительно 68%).

Идентификационные данные были, как показано ниже.
1H-ЯМР (CDCl3): δ 1,11 (уш с, 6H), 1,94 (с, 6H), 3,25 (д, 4H), 4,25-4,45 (м, 4H), 5,44 (м, 1H), 5,60 (м, 2H), 6,12 (м, 2H)
ИК (NaCl): 2977, 2933, 1724, 1706, 1638, 1479, 1456, 1428, 1379, 1319, 1294, 1274, 1226, 1164, 1097, 1074, 1013, 944, 854, 813, 767, 667 см-1
Сравнительный пример 9a
Сравнительное соединение 2 получали согласно способу ниже.
Диэтилкарбамоилхлорид (27,1 г) (200 ммоль) добавляли медленно к смеси триметилолпропана (67,0 г) (600 ммоль) и пиридина (47 г) при комнатной температуре, и затем они реагировали при приблизительно 50°С в течение приблизительно 15 часов. После концентрирования реакционной смеси при пониженном давлении, удаляя избыток пиридина, добавляли к ним 10% хлористоводородную кислоту, подкисляя реакционную смесь, которую, затем, концентрировали при пониженном давлении, удаляя воду, посредством этого получая коричневое маслянистое вещество. Полученное масляное вещество экстрагировали этилацетатом, и слой экстракта сушили безводным сульфатом натрия. Этилацетатный раствор концентрировали, и полученное в результате зеленое маслянистое вещество (32 г) очищали колоночной хроматографией (WAKOGEL C300, 400 г), посредством этого получая бесцветное маслянистое вещество (17,7 г), представленное химической формулой ниже в качестве промежуточного продукта (выход: приблизительно 38%).

Идентификационные данные промежуточного продукта были, как показано ниже.
1H-ЯМР (CDCl3): δ0,89 (т, 3H), 1,14 (т, 6H), 1,28 (кв, 2H), 3,23-3,34 (м, 4H), 3,48-3,59 (м, 4H), 3,62-3,66 (м, 2H), 4,23 (с, 2H)
ИК (NaCl): 3431, 2970, 2935, 2881, 1678, 1487, 1459, 1431, 1380, 1316, 1279, 1225, 1180, 1069, 1004, 771 см-1
Затем, промежуточный продукт (8,1 г) (35 ммоль) добавляли к сухому дихлорметану (70 мл), и после продувания колбы аргоном, добавляли в нее триэтиламин (11,1 г) (110 ммоль). После охлаждения смеси до приблизительно -10°С, медленно прикапывали к ней хлорангидрид метакриловой кислоты (11,1 г) (110 ммоль) так, чтобы внутренняя температура системы составляла бы от -10°С до -5°С, и затем их перемешивали при комнатной температуре в течение 2 часов. Выпавший продукт удаляли фильтрованием, и фильтрат промывали водой, насыщенным водным раствором бикарбоната натрия и насыщенным водным раствором хлорида натрия, сушили сульфатом натрия, и затем концентрировали при пониженном давлении, посредством этого получая коричневое маслянистое вещество. Полученное масляное вещество очищали колоночной хроматографией (WAKOGEL C300, 250 г), посредством этого получая бесцветное маслянистое вещество (10,4 г) сравнительного соединения 2, представленного химической формулой ниже (выход: приблизительно 80%).
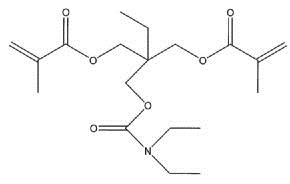
Идентификационные данные были, как показано ниже.
1H-ЯМР (CDCl3): δ0,95 (т, 3H), 1,11 (т, 6H), 1,56 (кв, 2H), 1,94 (с, 6H), 3,26 (д, 4H), 4,10 (с, 2H), 4,15 (с, 4H), 5,58 (м, 2H), 6,10 (уш с, 2H)
ИК (NaCl): 2974, 2933, 1722, 1705, 1636, 1558, 1540, 1473, 1457, 1428, 1379, 1321, 1294, 1273, 1226, 1162, 1073, 1014, 942, 813, 785, 768 см-1
Сравнительный пример 10a
Сравнительное соединение 3 получали согласно способу ниже.
DL-винную кислоту (7,5 г) (50 ммоль), полученную Tokyo Chemical Industry Co., Ltd., растворяли в метаноле (200 мл), добавляли к ней HfCl4 (THF)2 (0,46 г) (1 ммоль), и их перемешивали при комнатной температуре в течение 24 часов. Реакционную смесь фильтровали, удаляя нерастворимые вещества, и фильтрат концентрировали при пониженном давлении, посредством этого получая бесцветное маслянистое вещество (8,8 г), представленное химической формулой ниже? в качестве промежуточного продукта (выход: приблизительно 99%).
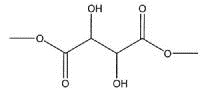
Идентификационные данные промежуточного продукта были, как показано ниже.
1H-ЯМР (CDCl3): δ3,50 (уш с, 2H), 3,84 (с, 6H), 4,55 (с, 2H)
ИК (NaCl): 3474, 2959, 1747, 1440, 1374, 1274, 1132, 1090, 1046, 1019, 979, 864, 826, 702, 605 см-1
Затем, промежуточный продукт (3,6 г) (20 ммоль) добавляли к сухому дихлорметану (100 мл), и после продувания колбы аргоном, добавляли в нее триэтиламин (6,1 г) (60 ммоль). После охлаждения ее до приблизительно -10°С, медленно прикапывали в нее хлорангидрид метакриловой кислоты (5,0 г) (48 ммоль) так, чтобы внутренняя температура системы составляла бы от -10°С до -5°С, и затем их перемешивали при комнатной температуре в течение 2 часов. После удаления выпавшего продукта фильтрованием, фильтрат промывали водой, насыщенным водным раствором бикарбоната натрия и насыщенным водным раствором хлорида натрия. Затем, после сушки фильтрата сульфатом натрия, полученный в результате раствор концентрировали при пониженном давлении, посредством этого получая красно-коричневое маслянистое вещество. Красно-коричневое маслянистое вещество очищали колоночной хроматографией, в которой колонку заполняли WAKOGEL C300 (полученным Wako Pure Chemical Industries, Ltd.) (250 г), и гексан и этилацетат применяли в качестве элюентов, посредством этого получая бесцветное маслянистое вещество (3,5 г) сравнительного соединения 3, представленного химической формулой ниже (выход: приблизительно 55%).

Идентификационные данные были, как показано ниже.
1H-ЯМР (CDCl3): δ1,97 (с, 6H), 3,76 (с, 6H), 5,67-5,70 (м, 2H), 5,74 (с, 2H), 6,22-6,24 (м, 2H)
ИК (NaCl): 2959, 2932, 2852, 1770, 1732, 1680, 1638, 1438, 1404, 1381, 1353, 1274, 1214, 1144, 1068, 1007, 950, 903, 854, 812, 706, 651 см-1
<Измерение вязкости >
Вязкость соединений примеров 1a-11a и сравнительных примеров 1a-10a измеряли прибором, измеряющим вязкоупругость VAR200AD (полученную Reologica Instruments, Inc.), применяя пластину, имеющую диаметр 40 мм, при 25°С. Результаты показаны в таблице 1.
<Оценка запаха>
Запах соединений примеров 1a-11a и сравнительных примеров 1a-10a оценивали согласно способам (1)-(3) ниже. Критерии оценки являются такими, как показано ниже. Результаты показаны в таблице 1.
(1) каждое соединение (приблизительно 100 мг) (0,1 г) взвешивали в 50 см3 бюксе (стеклянная колба), и бюксы закрывали крышкой.
(2) бюксы оставляли при комнатной температуре в течение приблизительно 30 минут.
(3) Анализатор подносил нос близко к бюксу (стеклянной колбе), нюхая запах после удаления крышки.
<Критерии оценки>
A: запах отсутствовал, или запах чувствовался, но не был неприятным.
B: чувство дискомфорта вызывалось характерным запахом.
C: сильное ощущение дискомфорта вызывалось характерным запахом.
Примеры 1b-11b и сравнительные примеры 1b-10b
<Получение фотоотверждаемой композиции>
Каждое из соединений примеров 1a-11a и сравнительных примеров 1a-10a (950 мг) и инициатор фотополимеризации IRGACURE 907 [2-метил-1-[4-(метилтио)фенил]-2-морфолинопропан-1-он] (полученный BASF Japan Ltd.) (50 мг) смешивали магнитной мешалкой, посредством этого получая фотоотверждаемые композиции примеров 1b-11b и сравнительных примеров 1b-10b.
Фотополимеризуемость и фотоотверждаемость фотоотверждаемых композиций примеров 1b-11b и сравнительных примеров 1b-10b оценивали, как описано ниже. Результаты показаны в таблице 1.
<Фотополимеризуемость>
Фотополимеризуемость каждой фотоотверждаемой композиции оценивали измерительным прибором, состоящим из DSC-7020 (полученного SII Inc.) и источника направленного света LA-410UV (полученного Hayashi Watch-Works Co., Ltd.).
Конкретно, количество выделяющейся теплоты фотополимеризуемого соединения, когда его облучали ультрафиолетовыми лучами, имеющими длину волны 365 нм, при 200 мВт/см2 в течение периода времени, достаточного для полной полимеризации фотополимеризуемого соединения, измеряли дважды для каждого образца. Количество выделяющейся теплоты, полученное первым измерением, включало количество выделяющейся теплоты в результате облучения ультрафиолетом, в добавление к количеству выделяющейся теплоты в результате полимеризации фотополимеризуемого соединения. Затем, образец, который был полностью полимеризован при первом измерении, снова облучали ультрафиолетовыми лучами при тех же условиях, измеряя количество выделяющейся теплоты, исключающее количество выделяющейся теплоты в результате полимеризации фотополимеризуемого соединения. Затем, количество выделяющейся теплоты в результате полимеризации фотополимеризуемого соединения рассчитывали, исходя из разницы первого и второго количеств выделяющейся теплоты. Здесь, продолжительность T1 [с], отсчитываемую от момента начала облучения ультрафиолетом до момента, когда достигали максимального количества выделяющейся теплоты, применяли в качестве коэффициента для сравнения скорости фотополимеризации.
<Фотоотверждаемость>
Фотоотверждаемость каждой фотоотверждаемой композиции измеряли измерительным прибором, состоящим из VAR200AD (полученного Reologica Instruments, Inc.) и источника света LED LIGHTNINGCURE LC-L1 (полученного Hamamatsu Photonics K.K.).
Конкретно, образец помещали в щель 10 мкм между конусом и пластиной, имеющей диаметр 20 мм, и затем облучали ультрафиолетовыми лучами, имеющими длину волны 365 нм, при 50 мВт/см2, измеряя изменения вязкоупругих свойств до того, как модуль упругости достигал предельной величины. Максимальную величину модуля упругости определяли из результата измерения и применяли в качестве показателя степени отверждаемости.
Обычно, модуль упругости 1×104 Па показывает достаточную степень отверждаемости. Фотоотверждаемые композиции всех примеров и сравнительных примеров имели модуль упругости 1×105 Па. Причина этого заключалась в том, что их модуль упругости по существу достигал предельного значения при 1×105 Па, и измерение модуля упругости вне данной величины, было невозможным. Результат показал, что все из образцов могут образовывать твердое состояние при облучении достаточным количеством света (получая много световой энергии). Образец, модуль упругости которого достигает 1×105 Па за более короткий период времени облучения светом, может отверждаться с меньшей энергией, и он обладает лучшей фотоотверждаемостью.
Энергию ультрафиолетовых лучей, излучаемых до того как модуль упругости достигает предельной величины, т.е., энергию отверждения рассчитывали в виде произведения интенсивности ультрафиолетовых лучей (50 мВт/см2) и периода времени [с], в течение которого образец облучали ультрафиолетовым светом.
[Таблица 1]
Из таблицы 1 можно видеть, что фотополимеризуемые соединения примеров 1a-9a имели низкую вязкость и слабый запах. Кроме того, можно видеть, что фотоотверждаемые композиции примеров 1b-9b, применяя фотополимеризуемые соединения примеров 1a-9a, обладали превосходными фотополимеризуемостью и фотоотверждаемостью. С другой стороны, можно видеть, что фотополимеризуемые соединения примеров 10a и 11a, содержащие третичную гидроксильную группу в их молекулах, имели слабый запах и очень хорошую фотоотверждаемость, хотя их вязкость была немного завышенной.
В настоящем изобретении, T1, который представляет собой показатель фотополимеризуемости, указывает на лучшую фотополимеризуемость, если величина является меньшей, и предпочтительно составляет 7 секунд или меньше, и более предпочтительно 5 секунд или меньше. При этом, энергия отверждения, которая представляет собой показатель фотоотверждаемости, аналогично указывает на лучшую фотоотверждаемость, если величина является меньшей, и предпочтительно составляет 350 мДж/см2 или меньше, и более предпочтительно 250 мДж/см2 или меньше.
Фотополимеризуемые соединения настоящего изобретения достигали эффектов, описанных выше, поскольку они содержали множество полимеризуемых функциональных групп и имели специфическую полярную структуру их молекулы. Среди них, фотополимеризуемые соединения, содержащие группу, имеющую эфирную структуру, имели слабый запах, превосходную фотополимеризуемость и фотоотверждаемость, и обладали особенно низкой вязкостью, как можно видеть.
По сравнению с этим, можно видеть, что хотя фотополимеризуемые соединения сравнительных примеров 1a-3a имели низкую вязкость, фотоотверждаемые композиции сравнительных примеров 1b-3b, применяя те же соединения, имели энергию отверждения, которая являлась показателем фотоотверждаемости, повышенную до высокой величины (т.е., требовалось много энергии для отверждения). Кроме того, данные фотополимеризуемые соединения не содержали полярной функциональной группы в их исходной основной структуре, и считали, что они обладали большей летучестью, чем фотополимеризуемые соединения примеров, что приводило к нежелательному запаху.
Фотополимеризуемые соединения сравнительных примеров 4a и 5a представляли собой бифункциональные метакрилатные соединения, содержащие этиленгликольную цепь в своей исходной основной структуре. В данном случае, сравнительный пример 4a, имеющий более короткую этиленгликольную цепь, имел меньшую вязкость, но фотоотверждаемая композиция сравнительного примера 4b, применяя то же соединение, имела плохие фотополимеризуемость и фотоотверждаемость. С другой стороны, сравнительный пример 5a, имеющий более длинную этиленгликольную цепь (p=9), имел немного большую вязкость, но соответствующая фотоотверждаемая композиция достигала большей фотоотверждаемости, вследствие влияния большего молекулярного веса мономера. Однако можно видеть, что его фотореактивность была низкой (T1=9,0 с). Это значит, что реакционные сайты мономера склонны оставаться неизменными в процессе фототверждения.
Кроме того, фотополимеризуемые соединения сравнительных примеров 6a и 7a, в которые вводили вторичную гидроксильную группу, которая представляла собой протонную полярную структуру, и фотополимеризуемое соединение сравнительного примера 8a, в которое вводили уретановую структуру, имели слабый запах, и фотоотверждаемые композиции сравнительных примеров 6b-8b, применяя те же соединения, достигали лучшей фотополимеризуемости и фотоотверждаемости, чем фотоотверждаемые композиции сравнительных примеров 1b-5b. Однако, трудно сказать, были ли лучшие фотополимеризуемость и фотоотверждаемость удовлетворительными, принимая во внимание то, что вязкость фотополимеризуемых соединений была немного завышенной.
Кроме того, фотоотверждаемые композиции сравнительных примеров 9b и 10b, применяя фотополимеризуемое соединение сравнительного примера 9a, в которое вводили уретановую структуру, которая представляла собой апротонную полярную структуру, и фотополимеризуемое соединение сравнительного примера 10a, в котором сложноэфирная структура присоединяли наоборот, по сравнению с примерами, достигали лучших фотополимеризуемости и фотоотверждаемости, но их соответствующие фотополимеризуемые соединения имели высокую вязкость, которая была выше чем 50 мПа•с.
Примеры 1c-11c
<Получение чернил>
Каждое из фотополимеризуемых соединений примеров 1a-11a (100 частей), инициатор фотополимеризации IRGACURE 907 (полученный BASF Japan Ltd.) (10 частей) и сажу MICROLITH BLACK C-K (полученную BASF Japan Ltd.) (3 части) смешивали, посредством этого получая чернила примеров 1c-11c.
Примеры 1d-11d
Каждое из фотополимеризуемых соединений примеров 1a-11a (100 частей), инициатор фотополимеризации IRGACURE 907 (полученный BASF Japan Ltd.) (10 частей) и пигмент голубой MICROLITH BLUE 4G-K (полученный BASF Japan Ltd.) (3 части) смешивали, посредством этого получая чернила примеров 1d-11d.
<Оценка чернил 1>
Каждые из чернил примеров 1c-11c и примеров 1d-11d наносили на предметное стекло, и затем облучали и отверждали ультрафиолетовыми лучами, имеющими длину волны 365 нм при 200 мВт/см2 УФ излучателем LH6 (полученным Fusion Systems Japan Co., Ltd.). Как результат, чернила можно наносить без проблем, и соответствующие чернильные изображения отверждались в достаточной степени.
Чернила по существу соответствуют продуктам, состоящим из фотоотверждаемых композиций примеров 1b-11b. Однако, для большей верности, фотополимеризуемость и фотоотверждаемость чернил измеряли тем же способом, как для фотоотверждаемых композиций. Как результат, подтверждалось, что чернила были так же превосходны, как фотоотверждаемые композиции.
<Оценка чернил 2>
Кончик пера перьевой ручки окунали в чернила примеров 1c-11c и примеров 1d-11d, и буквы писали на PET пленке и обычной бумаге. После этого, написанное чернилами облучали и отверждали ультрафиолетовыми лучами, имеющими длину волны 365 нм, при 200 мВт/см2 УФ излучателем LH6 (полученным Fusion Systems Japan Co., Ltd.). Как результат, соответствующие чернильные изображения отверждались в достаточной степени.
Аспекты настоящего изобретения являются, например, следующими.
<1> Чернила, содержащие:
Соединение, представленное общей формулой (1) ниже,
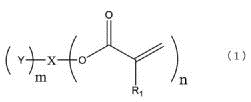
где в формуле выше, R1 представляет собой атом водорода или метильную группу, n представляет собой целое число, представляющее собой 2 или более, множество R1 могут быть одинаковыми или отличными друг от друга, X представляет собой углеводородную группу, содержащую 2-10 атомов углерода, Y представляет собой третичную гидроксильную группу или группу, имеющую сложноэфирную структуру, и m представляет собой целое 1 или больше.
<2> Чернила по <1>,
где Y в общей формуле (1) представляет собой группу, представленную общей формулой (2) ниже или общей формулой (3) ниже, или обеими,
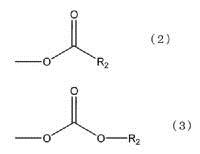
где в формулах выше, R2 представляет собой углеводородную группу, содержащую 1-15 атомов углерода.
<3> Чернила по <2>,
где R2 в общей формуле (2) или (3) представляет собой группу, представленную общей формулой (4) ниже,
-(CH2)aCH3 (4)
где в формуле выше a представляет собой целое от 0 до 2.
<4> Чернила по любому из <1>-<3>,
где в соединении, представленном общей формулой (1), n равно 2.
<5> Чернила по любому из <1>-<4>,
где в соединении, представленном общей формулой (1), n+m≤4.
<6> Чернила по любому из <1>-<5>,
где вязкость соединения, представленного общей формулой (1), при 25°С равна 20 мПа•с или меньше.
<7> Картридж для чернил, содержащий:
содержащиеся в нем чернила по любому из <1>-<6>.
<8> Струйное записывающее устройство, включающее:
установленный в него картридж для чернил по <7>.
<9> Печатный материал, включающий:
отпечаток, записанный чернилами по любому из <1>-<6>.
<10> Фотополимеризуемое соединение, представленное общей формулой (1) ниже,
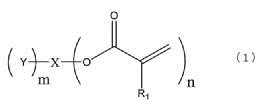
где в формуле выше R1 представляет собой атом водорода или метильную группу, n представляет собой целое 2 или больше, множество R1 могут быть одинаковыми или отличными друг от друга, X представляет собой углеводородную группу, содержащую 2-10 атомов углерода, Y представляет собой третичную гидроксильную группу или группу, имеющую сложноэфирную структуру, и m представляет собой целое число, представляющее собой 1 или более.
<11> Фотополимеризуемое соединение по <10>,
где Y в общей формуле (1) представляет собой группу, представленную общей формулой (2) ниже или общей формулой (3) ниже, или обеими,
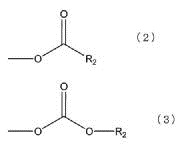
где в формулах выше, R2 представляет собой углеводородную группу, содержащую 1-15 атомов углерода.
<12> Фотополимеризуемое соединение по <11>,
где R2 в общей формуле (2) или (3) представляет собой группу, представленную общей формулой (4) ниже,
-(CH2)aCH3 (4)
где в формуле выше a представляет собой целое от 0 до 2.
<13> Фотополимеризуемое соединение по любому из <10>-<12>,
где n в общей формуле (1) равно 2.
<14> Фотополимеризуемое соединение по любому из <10>-<13>,
где в общей формуле (1), n+m≤4.
<15> Фотополимеризуемое соединение по любому из <10>-<14>,
где вязкость соединения, представленного общей формулой (1), при 25°С равна 20 мПа•с или меньше.
<16> Фотоотверждаемая композиция, содержащая:
фотополимеризуемое соединение по любому из <10>-<15>.
<17> Материал для получения трехмерного объекта, содержащий:
фотоотверждаемую композицию по <16>.
<18> Трехмерный объект, полученный отверждением материала для получения трехмерного объекта по <17>.
Реферат
Изобретение относится к чернилам для струйной печати. Чернила включают соединение формулы (1), где R- водород или метил, n целое число 2 или более, множество R1 могут быть одинаковыми или различными, X - углеводородная группа, содержащая 2-10 атомов углерода, Y - третичная гидроксильная группа формулы (2) или (3), или обе группы, m - 1 или более. Предложенные чернила обладают повышенной фотополимеризуемостью и фотоотверждаемостью, низкой вязкостью менее 50 мПа∙с при 25С и слабым запахом. 5 н. и 8 з.п. ф-лы, 2 ил., 1 табл., 11 пр.
Формула




Документы, цитированные в отчёте о поиске
Система на основе чернил, содержащая полимерные связующие вещества

Комментарии