Моноклональное антитело рам4 и его применение длядиагностики и лечения рака поджелудочной железы - RU2005100777A
Код документа: RU2005100777A
Реферат
1. Антитело или его фрагмент, который связывает домен, находящийся между N-концом и началом домена повторов MUC 1, где указанное антитело получено путем иммунизации муцином и/или селекции с его использованием.
2. Антитело или его фрагмент по п.1, где указанное антитело или его фрагмент получен против муцина рака поджелудочной железы.
3. Антитело или его фрагмент по п.1, где указанное антитело или его фрагмент представляет собой антитело PAM4 или его фрагмент.
4. Антитело или его фрагмент по п.3, где указанное антитело или его фрагмент химеризованы.
5. Химеризованное антитело или его фрагмент по п.3, содержащий определяющие комплементарность области (CDR) и каркасные области (FR) мышиного MAb PAM4 и константные области легких и тяжелых цепей человеческого антитела, где области CDR вариабельной области легкой цепи химеризованного MAb PAM4 включают в себя CDR1, содержащий аминокислотную последовательность SASSSVSSSYLY; CDR2, содержащий аминокислотную последовательность STSNLAS; и CDR3, содержащий аминокислотную последовательность HQWNRYPYT; и области CDR вариабельной области тяжелой цепи химеризованного Mab против PAM4 включают в себя CDR1, содержащий аминокислотную последовательность SYVLH; CDR2, содержащий аминокислотную последовательность YINPYNDGTQYNEKFKG и CDR3, содержащий аминокислотную последовательность GFGGSYGFAY.
6. Антитело или его фрагмент по п.4, где указанное антитело или его фрагмент включает в себя по меньшей мере одну из нуклеотидной последовательности VK PAM4 с фигуры 1A и нуклеотидной последовательности VH PAM4 с фигуры 1B.
7. Направленный на раковую клетку диагностический или терапевтический конъюгат, содержащий антительный компонент, который включает в себя антитело или его фрагмент по п.1, который связывается с указанной клеткой, где указанный антительный компонент связан по меньшей мере с одним средством диагностики/детекции и/или по меньшей мере с одним терапевтическим средством.
8. Диагностический конъюгат по п.7, где указанное средство диагностики/детекции выбрано из группы, включающей в себя радионуклид, контрастное средство и светочувствительное средство диагностики/детекции.
9. Диагностический конъюгат по п.8, где указанное диагностическое средство представляет собой радионуклид.
10. Диагностический конъюгат по п.9, где указанный радионуклид характеризуется энергией от 20 до 4000 кэВ.
11. Диагностический конъюгат по п.10, где указанный радионуклид представляет собой гамма-, бета-, или позитрон-излучающий изотоп.
12. Диагностический конъюгат по п.11, где указанный радионуклид выбран из группы, состоящей из110In,111In,177Lu,18F,52Fe,62Cu,64Cu,67Cu,67Ga,68Ga,86Y,90Y,89Zr,94m Tc,94Tc,99mTc,120I,123I,124I,125I,131I,154-158Gd,32P,11C,13N,15O,186Re,188Re,51Mn,52mMn,55Co,72As,75Br,76Br,82mRb,83Sr, или других гамма-, бета- или позитрон-излучающих элементов.
13. Диагностический конъюгат по п.8, где указанное средство диагностики/детекции представляет собой контрастное средство.
14. Диагностический конъюгат по п.13, где указанное контрастное средство представляет собой парамагнитный ион.
15. Диагностический конъюгат по п.14, где указанный парамагнитный ион представляет собой металл, включая хром (III), марганец (II), железо (III), железо (II), кобальт (II), никель (II), медь (II), неодимий (III), самарий (III), иттербий (III), гадолиний (III), ванадий (II), тербий (III), диспрозий (III), гольмий (III) и эрбий (III).
16. Диагностический конъюгат по п.13, где указанное контрастное средство представляет собой металл, включая лантан (III), золото (III), свинец (II), и особенно висмут (III).
17. Диагностический конъюгат по п.13, где указанное контрастное средство представляет собой средство усиления ультразвукового изображения.
18. Диагностический конъюгат по п.17, где указанное средство усиления ультразвукового изображения представляет собой липосому, которая содержит химеризованное антитело PAM4 или его фрагмент.
19. Диагностический конъюгат по п.18, где указанная липосома заполнена газом.
20. Диагностический конъюгат по п.13, где указанное контрастное средство представляет собой непроницаемый для излучения материал, выбранный из группы, включающей в себя соединения иода, соединения бария, соединения галлия и соединения таллия.
21. Диагностический конъюгат по п.20, где указанный непроницаемый для излучения материал выбран из группы, включающей в себя барий, диатризоат, этиодизированное масло, цитрат галлия, иокармовую кислоту, иоцетамовую кислоту, иодамид, иодипамид, иодоксамовую кислоту, иогуламид, иогексол, иопамидол, иопаноевую кислоту, иопроцемовую кислоту, иосефамовую кислоту, иосериновую кислоту, иосуламид-меглумин, иосеметовую кислоту, иотасул, иотетриновую кислоту, иоталамовую кислоту, иотроксовую кислоту, иоксаглиновую кислоту, иоксотризоевую кислоту, иподат, меглумин, метризамид, метризоат, пропилиодон, и хлорид таллия.
22. Диагностический конъюгат по п.8, где указанное средство диагностики/детекции представляет собой светочувствительное средство диагностики/детекции.
23. Диагностический конъюгат по п.22, где указанное светочувствительное средство диагностики/детекции представляет собой флуоресцентно меченое соединение, выбранное из группы, включающей в себя флуоресцеин-изотиоцианат, родамин, фикоэритрин, фикоцианин, аллофикоцианин, o-фталевый альдегид, и флуорескамин.
24. Диагностический конъюгат по п.22, где указанное светочувствительное средство диагностики/детекции представляет собой соединение для хемилюминесцентного мечения, выбранное из группы, включающей в себя люминол, изолюминол, ароматический сложный эфир акридина, имидазол, соль акридина и эфир щавелевой кислоты.
25. Диагностический конъюгат по п.22, где указанное светочувствительное средство диагностики/детекции представляет собой биолюминесцентное соединение, выбранное из группы, включающей в себя люциферин, люциферазу и экворин.
26. Диагностический конъюгат по пп. 8-25, где указанный конъюгат используют для диагностики опухоли во время операции, эндоскопической или внутрисосудистой диагностики опухоли.
27. Терапевтический конъюгат по п.7, где указанное терапевтическое средство выбрано из группы, состоящей из радионуклида, иммуномодулятора, гормона, антагониста гормона, фермента, ингибитора фермента, олигонуклеотида, светочувствительного терапевтического средства, цитотоксического средства, антитела, ингибитора ангиогенеза и их комбинации.
28. Терапевтический конъюгат по п.27, где указанный олигонуклеотид представляет собой антисмысловой олигонуклеотид.
29. Терапевтический конъюгат по п.28, где указанный олигонуклеотид представляет собой антисмысловой олигонуклеотид против онкогена.
30. Терапевтический конъюгат по п.29, где указанный онкоген представляет собой bcl-2 или p53.
31. Терапевтический конъюгат по п.27, где указанное терапевтическое средство представляет собой цитотоксическое средство.
32. Терапевтический конъюгат по п.31, где указанное цитотоксическое средство представляет собой лекарственное средство или токсин.
33. Терапевтический конъюгат по п.32, где указанное лекарственное средство обладает фармацевтическим свойством, выбранным из группы, состоящей из антимитотического, алкилирующего средства, средства-антиметаболита, антиангиогенного, апоптозного средства, средства-алкалоида и средства-антибиотика и их комбинаций.
34. Терапевтический конъюгат по п.32, где указанное лекарственное средство выбрано из группы, состоящей из азотистых ипритов, гемцитабина, производных этиленимина, алкилсульфонатов, нитрозомочевин, триазенов, аналогов фолиевой кислоты, антрациклинов, SN-38, таксанов, ингибиторов COX-2, аналогов пиримидина, аналогов пурина, антибитиотиков, ферментов, ингибиторов ферментов, эпиподофиллотоксинов, координатных комплексов платины, алкалоидов барвинка, замещенных мочевин, производных метилгидразина, средств, подавляющих адренокортикоиды, антагонистов гормонов, эндостатина, таксолов, камптотецинов, доксорубицинов и их аналогов, антиметаболитов, алкилирующих средств, антимитотических средств, антиангиогенных, апоптозных средств, метотрексата, CPT-11, и их комбинации.
35. Терапевтический конъюгат по п.32, где указанный токсин получен из источника, выбранного из группы, включающей в себя животный, растительный и микробный источник.
36. Терапевтический конъюгат по п.32, где указанный токсин выбран из группы, состоящей из рицина, абрина, альфа-токсина, сапорина, рибонуклеазы (РНКазы), ДНКазы I, стафилококкового энтеротоксина A, противовирусного белка фитолакки американской, гелонина, дифтерийного токсина, экзотоксина псевдомонады и эндотоксина псевдомонады.
37. Терапевтический конъюгат по п.27, где указанное терапевтическое средство представляет собой иммуномодулятор.
38. Терапевтический конъюгат по п.37, где указанный иммуномодулятор выбран из группы, состоящей из цитокина, фактора роста стволовых клеток, лимфотоксина, кроветворного фактора, колониестимулирующего фактора (CSF), интерферона (IFN), фактора роста стволовых клеток, эритропоэтина, тромбопоэтина, и их комбинации.
39. Терапевтический конъюгат по п.38, где указанный лимфотоксин представляет собой фактор некроза опухолей (TNF), указанный кроветворный фактор представляет собой интерлейкин (IL), указанный колониестимулирующий фактор представляет собой гранулоцитарный колониестимулирующий фактор (G-CSF) или гранулоцитарно-макрофагальный колониестимулирующий фактор (GM-CSF), указанный интерферон представляет собой интерфероны б, в или г, и указанный фактор роста стволовых клеток обозначен как "фактор S1".
40. Терапевтический конъюгат по п.37, где указанный иммуномодулятор включает в себя IL-1, IL-2, IL-3, IL-6, IL-10, IL-12, IL-18, IL-21, интерферон-г, TNF-б или их комбинацию.
41. Терапевтический конъюгат по п.27, где указанное терапевтическое средство представляет собой радионуклид.
42. Терапевтический конъюгат по п.41, где указанный радионуклид характеризуется энергией от 60 до 700 кэВ.
43. Терапевтический конъюгат по п.42, где указанный радионуклид выбран из группы, состоящей из32P,33P,47Sc,64Cu,67Cu,67Ga,86Y,90Y,111Ag,111In,125I,131 I,142Pr,153Sm,161Tb,166Dy,166Ho,177Lu,186Re,188Re,189Re,212Pb,212Bi,213Bi,211At,223Ra и225Ac, и их комбинаций.
44. Терапевтический конъюгат по п.27, где указанное терапевтическое средство представляет собой светочувствительное терапевтическое средство.
45. Терапевтический конъюгат по п.44, где указанное светочувствительное терапевтическое средство выбрано из группы, включающей в себя хромогены и красители.
46. Терапевтический конъюгат по п.27, где указанное терапевтическое средство представляет собой фермент.
47. Терапевтический конъюгат по п.46, где указанный фермент выбран из группы, включающей в себя малатдегидрогеназу, стафилококковую нуклеазу, дельта-V-стероидизомеразу, дрожжевую алкогольдегидрогеназу, б-глицерофосфатдегидрогеназу, триозофосфатизомеразу, пероксидазу хрена, щелочную фосфатазу, аспарагиназу, глюкозооксидазу, в-галактозидазу, рибонуклеазу, уреазу, каталазу, глюкозо-6-фосфатдегидрогеназу, глюкоамилазу и ацетилхолинэстеразу.
48. Мультивалентное мультиспецифическое антитело или его фрагмент, содержащий один или более антигенсвязывающих участков, характеризующихся сродством в отношении являющегося мишенью антигена MUC1, и один или более связывающих гаптен участков, характеризующихся сродством в отношении молекулы гаптена.
49. Антитело или его фрагмент по п.48, где указанное антитело химеризовано.
50. Антитело или его фрагмент по п.49, дополнительно включающий в себя диагностическое или терапевтическое средство.
51. Белок слияния антитела или его фрагмент, содержащий по меньшей мере два Mab PAM4 или их фрагмента по п.3.
52. Белок слияния антитела или его фрагмент, содержащий по меньшей мере одно первое MAb PAM4 или его фрагмент по п.1, и по меньшей мере одно второе MAb или его фрагмент, где указанное второе MAb или его фрагмент представляет собой не относящееся к PAM4 антитело или его фрагмент.
53. Белок слияния антитела или его фрагмент по п.52, где указанное второе MAb представляет собой ассоциированное с карциномой антитело.
54. Белок слияния антитела или его фрагмент по п.47, где указанное ассоциированное с карциномой антитело связывается с антигеном в ткани рака поджелудочной железы или происходящим из рака поджелудочной железы антигеном.
55. Белок слияния антитела или его фрагмент по п.47, где ассоциированное с карциномой антитело выбрано из группы, состоящей из CA19.9, DUPAN2, SPAN1, Nd2, B72.3, CC49, CEA, aLea, антител, определяемых антигеном Льюиса Le(y), и антител против CSAp, MUC1, MUC2, MUC3, MUC4, TAG-72, EGFR, CD40, факторов ангиогенеза (например, VEGF), инсулиноподобного фактора роста (IGF), тенасцина, фактора роста из тромбоцитов, IL-6, продуктов онкогенов и антигенов HER2/neu.
56. Белок слияния антитела или его фрагмент по п.51, где указанный белок слияния или его фрагмент содержит по меньшей мере одно средство диагностики/детекции и/или терапевтическое средство.
57. Последовательность ДНК, включающая в себя нуклеиновую кислоту, кодирующую MAb или его фрагмент, выбранный из группы, состоящей из MAb PAM4 или его фрагмента по п.1; белка слияния антитела или его фрагмента, содержащего по меньшей мере два из указанных MAb или их фрагментов; белок слияния антитела или его фрагмент, содержащий по меньшей мере одно первое MAb PAM4 или его фрагмент, включающие в себя указанное MAb или его фрагмент по п.1, и по меньшей мере одно второе MAb или его фрагмент, где указанное второе антитело представляет собой не относящееся к PAM4 антитело или его фрагмент; и белок слияния антитела или его фрагмент, содержащий по меньшей мере одно первое MAb или его фрагмент, включающие в себя указанное MAb или его фрагмент по п.1 и по меньшей мере одно второе MAb или его фрагмент, отличное от MAb или его фрагмента по п.1; где указанное второе MAb выбрано из группы, состоящей из CA19.9, DUPAN2, SPAN1, Nd2, B72.3, CC49, CEA, aLea, антител, определяемых антигеном Льюиса Le(y), и антител против CD40, факторов ангиогенеза (например, VEGF), продуктов онкогенов, MUC1, MUC2, MUC3, MUC4, TAG-72, EGFR, инсулиноподобного фактора роста (IGF), тенасцина, фактора роста из тромбоцитов, IL-6 и антигенов HER2/neu.
58. Экспрессирующий вектор, содержащий последовательность ДНК по п.57.
59. Клетка хозяина, содержащая последовательность ДНК по п.57.
60. Способ доставки диагностического или терапевтического средства или их комбинации к мишени, подразумевающий (i) предоставление композиции, которая включает в себя антитело PAM4 или его фрагмент, конъюгированный по меньшей мере с одним средством диагностики/детекции и/или терапевтическим средством, и (ii) введение субъекту, при необходимости, диагностического или терапевтического конъюгата по п.7.
61. Способ по п.60, где указанное средство диагностики/детекции выбрано из группы, состоящей из радионуклида, контрастного средства и светочувствительного средства диагностики/детекции.
62. Способ по п.61, где указанное средство диагностики/детекции представляет собой радионуклид.
63. Способ по п.62, где указанный радионуклид характеризуется энергией от 20 до 4000 кэВ.
64. Способ по п.63, где указанный радионуклид представляет собой гамма-, бета- или позитрон-излучающий изотоп.
65. Способ по п.64, где указанный радионуклид выбран из группы, состоящей из110In,111In,177Lu,18F,52Fe,62Cu,64Cu,67Cu,67Ga,68Ga,86Y,90Y,89Zr,94mTc,94Tc,99mTc,120I,123I,124I,125I,131I,154-158Gd,32P,11C,13N,15O,186Re,188Re,51Mn,52mMn,55Co,72As,75Br,76Br,82mRb,83Sr или других гамма-, бета- или позитрон-излучающих элементов.
66. Способ по п.61, где указанное средство диагностики/детекции представляет собой контрастное средство.
67. Способ по п.66, где указанное контрастное средство представляет собой парамагнитный ион.
68. Способ по п.67, где указанный парамагнитный ион представляет собой металл, включая хром (III), марганец (II), железо (III), железо (II), кобальт (II), никель (II), медь (II), неодимий (III), самарий (III), иттербий (III), гадолиний (III), ванадий (II), тербий (III), диспрозий (III), гольмий (III) и эрбий (III).
69. Способ по п.66, где указанное контрастное средство представляет собой металл, включая лантан (III), золото (III), свинец (II) и особенно висмут (III).
70. Способ по п.66, где указанное контрастное средство представляет собой средство усиления ультразвукового изображения.
71. Способ по п.70, где указанное средство усиления ультразвукового изображения представляет собой липосому, которая содержит химеризованное антитело PAM4 или его фрагмент.
72. Способ по п.71, где указанная липосома заполнена газом.
73. Способ по п.66, где указанное контрастное средство представляет собой непроницаемый для излучения материал, выбранный из группы, включающей в себя соединения иода, соединения бария, соединения галлия и соединения таллия.
74. Способ по п.73, где указанный непроницаемый для излучения материал выбран из группы, включающей в себя барий, диатризоат, этиодизированное масло, цитрат галлия, иокармовую кислоту, иоцетамовую кислоту, иодамид, иодипамид, иодоксамовую кислоту, иогуламид, иогексол, иопамидол, иопаноевую кислоту, иопроцемовую кислоту, иосефамовую кислоту, иосериновую кислоту, иосуламид-меглумин, иосеметовую кислоту, иотасул, иотетриновую кислоту, иоталамовую кислоту, иотроксовую кислоту, иоксаглиновую кислоту, иоксотризоевую кислоту, иподат, меглумин, метризамид, метризоат, пропилиодон и хлорид таллия.
75. Способ по п.61, где указанное диагностическое средство представляет собой светочувствительное диагностическое средство.
76. Способ по п.75, где указанное светочувствительное средство диагностики/детекции представляет собой флуоресцентно меченое соединение, выбранное из группы, включающей в себя флуоресцеин-изотиоцианат, родамин, фикоэритрин, фикоцианин, аллофикоцианин, o-фталевый альдегид и флуорескамин.
77. Способ по п.75, где указанное светочувствительное средство диагностики/детекции представляет собой соединение для хемилюминесцентного мечения, выбранное из группы, включающей в себя люминол, изолюминол, ароматический сложный эфир акридина, имидазол, соль акридина и эфир щавелевой кислоты.
78. Способ по п.75, где указанное светочувствительное средство диагностики/детекции представляет собой биолюминесцентное соединение, выбранное из группы, включающей в себя люциферин, люциферазу и экворин.
79. Способ по п.60, где указанное терапевтическое средство выбрано из группы, состоящей из радионуклида, цитотоксического средства, цитокина, иммуномодулятора, гормона, антагониста гормона, фактора роста, радионуклида, металла, олигонуклеотида, контрастного средства, фермента, ингибитора ферментов и светочувствительного терапевтического средства.
80. Терапевтический конъюгат по п.79, где указанный олигонуклеотид представляет собой антисмысловой олигонуклеотид.
81. Терапевтический конъюгат по п.80, где указанный олигонуклеотид представляет собой антисмысловой олигонуклеотид против онкогена.
82. Терапевтический конъюгат по п.81, где указанный онкоген представляет собой bcl-2 или p53.
83. Способ по п.79, где указанное терапевтическое средство представляет собой цитотоксическое средство.
84. Способ по п.83, где указанное цитотоксическое средство представляет собой лекарственное средство или токсин.
85. Способ по п.84, где указанное лекарственное средство обладает фармацевтическим свойством, выбранным из группы, состоящей из антимитотического, алкилирующего средства, средства-антиметаболита, антиангиогенного, апоптозного средства, средства-алкалоида и средства-антибиотика и их комбинаций.
86. Способ по п.84, где указанное лекарственное средство выбрано из группы, состоящей из азотистых ипритов, гемцитабина, производных этиленимина, алкилсульфонатов, нитрозомочевин, триазенов, аналогов фолиевой кислоты, SN-38, антрациклинов, таксанов, ингибиторов COX-2, аналогов пиримидина, аналогов пурина, антибитиотиков, ферментов, ингибиторов ферментов, эпиподофиллотоксинов, координатных комплексов платины, алкалоидов барвинка, замещенных мочевин, производных метилгидразина, средств, подавляющих адренокортикоиды, антагонистов гормонов, эндостатина, таксолов, камптотецинов, доксорубицинов и их аналогов, антиметаболитов, алкилирующих средств, антимитотических средств, антиангиогенных, апоптозных средств, метотрексата, CPT-11 и их комбинации.
87. Способ по п.84, где указанный токсин получен из источника, выбранного из группы, включающей в себя животный, растительный и микробный источник.
88. Способ по п.87, где указанный токсин выбран из группы, состоящей из рицина, абрина, альфа-токсина, сапорина, рибонуклеазы (РНКазы), ДНКазы I, стафилококкового энтеротоксина A, противовирусного белка фитолакки американской, гелонина, дифтерийного токсина, экзотоксина псевдомонады и эндотоксина псевдомонады.
89. Способ по п.79, где указанное терапевтическое средство представляет собой иммуномодулятор.
90. Способ по п.89, где указанный иммуномодулятор выбран из группы, состоящей из цитокина, фактора роста стволовых клеток, лимфотоксина, кроветворного фактора, колониестимулирующего фактора (CSF), интерферона (IFN), фактора роста стволовых клеток, эритропоэтина, тромбопоэтина и их комбинации.
91. Способ по п.90, где указанный лимфотоксин представляет собой фактор некроза опухолей (TNF), указанный кроветворный фактор представляет собой интерлейкин (IL), указанный колониестимулирующий фактор представляет собой гранулоцитарный колониестимулирующий фактор (G-CSF) или гранулоцитарно-макрофагальный колониестимулирующий фактор (GM-CSF), указанный интерферон представляет собой интефероны, в или и указанный фактор роста стволовых клеток обозначен как "фактор S1".
92. Способ по п.89, где указанный иммуномодулятор представляет собой цитокин.
93. Способ по п.90, где указанный иммуномодулятор включает в себя IL-1, IL-2, IL-3, IL-6, IL-10, IL-12, IL-18, IL-21, интерферон б, интерферон, интерферон г, TNF-б или их комбинацию.
94. Способ по п.79, где указанное терапевтическое средство представляет собой радионуклид.
95. Способ по п.94, где указанный радионуклид характеризуется энергией от 60 до 700 кэВ.
96. Способ по п.95, где указанный радионуклид выбран из группы, состоящей из32P,33P,47Sc,64Cu,67Cu,67Ga,86Y,90Y,111 Ag,111In,125I,131I,142Pr,153Sm,161Tb,166Dy,166Ho,177Lu,186Re,188Re,189Re,212Pb,212Bi,213Bi,211At,223Ra и225Ac и их комбинаций.
97. Способ по п.79, где указанное терапевтическое средство представляет собой светочувствительное терапевтическое средство.
98. Способ по п.97, где указанное светочувствительное терапевтическое средство выбрано из группы, включающей в себя хромогены и красители.
99. Способ по п.79, где указанное терапевтическое средство представляет собой фермент.
100. Способ по п.99, где указанный фермент выбран из группы, включающей в себя малатдегидрогеназу, стафилококковую нуклеазу, дельта-V-стероидизомеразу, дрожжевую алкогольдегидрогеназу, б-глицерофосфатдегидрогеназу, триозофосфатизомеразу, пероксидазу хрена, щелочную фосфатазу, аспарагиназу, глюкозооксидазу, в-галактозидазу, рибонуклеазу, уреазу, каталазу, глюкозо-6-фосфатдегидрогеназу, глюкоамилазу и ацетилхолинэстеразу.
101. Способ доставки средства диагностики/детекции, терапевтического средства или их комбинации к мишени, подразумевающий введение субъекту антитела или его фрагмента по п.48; выжидание в течение промежутка времени, достаточного для того, чтобы общее количество несвязавшегося белка было выведено из кровяного русла субъекта; и введение указанному субъекту молекулы-носителя, содержащей средство диагностики/детекции, терапевтическое средство или их комбинацию, которые связываются с участком связывания указанного антитела.
102. Способ по п.101, где указанная молекула-носитель связывается более чем с одним участком связывания указанного антитела.
103. Способ по п.101, где указанное средство диагностики/детекции или указанное терапевтическое средство выбрано из группы, включающей в себя изотопы, лекарственные средства, токсины, цитокины, гормоны, антагонисты гормонов, олигонуклеотиды, ферменты, ингибиторы ферментов, факторы роста, радионуклиды и металлы.
104. Терапевтический конъюгат по п.103, где указанный олигонуклеотид представляет собой антисмысловой олигонуклеотид.
105. Терапевтический конъюгат по п.104, где указанный олигонуклеотид представляет собой антисмысловой олигонуклеотид против онкогена.
106. Терапевтический конъюгат по п.105, где указанный онкоген представляет собой bcl-2 или p53.
107. Способ диагностики или лечения злокачественной опухоли, подразумевающий введение субъекту, при необходимости, антитела по п.50; выжидание в течение промежутка времени, достаточного для того, чтобы общее количество несвязавшегося белка было выведено из кровяного русла субъекта; и введение указанному субъекту молекулы-носителя, содержащей средство диагностики/детекции, терапевтическое средство или их комбинацию, которая связывается с участком связывания указанного антитела.
108. Способ по п.107, где указанная злокачественная опухоль представляет собой рак поджелудочной железы.
109. Способ по п.107, где указанный способ может использоваться для определения поврежденных тканей во время операции, эндоскопического определения поврежденных тканей или внутрисосудистого определения поврежденных тканей.
110. Способ лечения у субъекта злокачественного новообразования, подразумевающий
введение указанному субъекту терапевтически эффективного количества Mab PAM4 или его фрагмента или белка слияния антитела или его фрагмента по п.1, где указанное MAb PAM4 или его фрагмент или белок слияния антитела или его фрагмент связан по меньшей мере с одним терапевтическим средством, и необязательное получение препарата указанного антитела PAM4 или его фрагмента в фармацевтически приемлемом наполнителе.
111. Способ по п.110, дополнительно включающий в себя второе MAb или его фрагмент, который представляет собой не относящееся к MAb PAM4 антитело или его фрагмент.
112. Способ по п.111, где указанное второе MAb или его фрагмент представляет собой "голое" MAb или его фрагмент.
113. Способ по п.111, где указанное второе MAb или его фрагмент выбран из группы, состоящей из CA19.9, DUPAN2, SPAN1, Nd2, B72.3, CC49, CEA, aLea, антител, определяемых антигеном Льюиса Le(y), и антител против CSAp, MUC1, MUC2, MUC3, MUC4, TAG-72, EGFR, CD40, факторов ангиогенеза (например, VEGF), продуктов онкогенов, инсулиноподобного фактора роста (IGF), тенасцина, фактора роста из тромбоцитов, IL-6 и HER2/neu.
114. Способ по п.111, где указанное второе MAb конъюгировано с терапевтическим средством или средством диагностики/детекции.
115. Способ по п.110, дополнительно включающий в себя второе MAb PAM4 или его фрагмент.
116. Способ по п.110, где указанное антитело PAM4 вводят парентерально.
117. Способ по п.116, где указанное антитело PAM4 вводят в дозировке от 20 до 2000 мг белка на дозу.
118. Способ по п.117, где указанная дозировка вводится неоднократно.
119. Способ по п.110, где указанное антитело PAM4 представляет собой химеризованное антитело PAM4.
120. Способ по п.119, где константные и шарнирные области указанного химеризованного антитела PAM4 содержат константные и шарнирные области человеческого IgG.
121. Способ по п.110, где указанное антитело PAM4 вводят до введения указанному субъекту второго "голого" или конъюгированного антитела, способного взаимодействовать со вторым опухолевым маркером, экспрессируемым указанным злокачественным новообразованием, в сочетании с данным введением или после него.
122. Способ по п.110, где указанное антитело PAM4 вводят до введения указанному субъекту по меньшей мере одного терапевтического средства или средства диагностики/детекции, одновременно с данным введением или после него.
123. Способ диагностики у субъекта злокачественного новообразования, подразумевающий введение указанному субъекту диагностически эффективного количества диагностического конъюгата, содержащего MAb PAM4 или его фрагмент или белок слияния антитела или его фрагмент, где указанное MAb PAM4 или его фрагмент или белок слияния антитела или его фрагмент конъюгирован по меньшей мере с одним средством диагностики/детекции, и необязательное получение препарата указанного антитела PAM4 или его фрагмента или указанного белка слияния или его фрагмента в фармацевтически приемлемом наполнителе.
124. Способ лечения у субъекта раковой клетки, подразумевающий введение указанному субъекту терапевтически эффективного количества композиции, содержащей "голое" MAb PAM4 или его фрагмент или "голый" белок слияния антитела или его фрагмент по п.1, и необязательное получение препарата указанного "голого" MAb PAM4 или его фрагмента или указанного белка слияния антитела или его фрагмента в фармацевтически приемлемом наполнителе.
125. Способ по п.124, где указанная композиция дополнительно содержит второе "голое" антитело или его фрагмент.
126. Способ по п.125, где указанное второе антитело или его фрагмент связывает домен, находящийся между N-концом и началом домена повторов MUC 1.
127. Способ по п.125, где указанное второе антитело или его фрагмент не является Mab PAM4 или его фрагментом.
128. Способ по п.125, где указанное второе антитело или его фрагмент выбраны из группы, состоящей из CA19.9, DUPAN2, SPAN1, Nd2, B72.3, CC49, CEA, aLea, антител, определяемых антигеном Льюиса Le(y), и антител против CSAp, MUC1, MUC2, MUC3, MUC4, TAG-72, EGFR, CD40, факторов ангиогенеза (например, VEGF), инсулиноподобного фактора роста (IGF), тенасцина, фактора роста из тромбоцитов, IL-6, продуктов онкогенов и HER2/neu.
129. Способ по п.127, где указанное второе антитело или его фрагмент выбраны из группы, состоящей из CA19.9, DUPAN2, SPAN1, Nd2, B72.3, CC49, CEA, aLea, антител, определяемых антигеном Льюиса Le(y), и антител против CSAp, MUC1, MUC2, MUC3, MUC4, TAG-72, EGFR, CD40, факторов ангиогенеза (например, VEGF), инсулиноподобного фактора роста (IGF), тенасцина, фактора роста из тромбоцитов, IL-6, продуктов онкогенов и HER2/neu.
130. Способ по п.124, где указанное "голое" антитело PAM4 вводят парентерально.
131. Способ по п.130, где указанное "голое" антитело PAM4 вводят в дозировке от 20 до 2000 мг белка на дозу.
132. Способ по п.131, где указанная дозировка вводится неоднократно.
133. Способ по п.124, где указанное "голое" антитело PAM4 представляет собой химеризованное антитело PAM4 или его фрагмент.
134. Способ по п.133, где константные и шарнирные области указанного "голого" антитела PAM4 содержат константные и шарнирные области человеческого IgG.
135. Способ по п.125, где указанное второе "голое" антитело PAM4 вводят до введения указанному субъекту "голого" антитела, в сочетании с данным введением или после него.
136. Способ по п.124, где указанное "голое" антитело PAM4 вводят до введения указанному субъекту терапевтического средства и/или средства диагностики/детекции, одновременно с данным введением или после него.
137. Способ диагностики злокачественного новообразования у субъекта, подразумевающий проведение диагностического анализа in vitro на образце, полученном у указанного субъекта, с использованием композиции, содержащей "голое" MAb PAM4 или его фрагмент или "голый" белок слияния антитела или его фрагмент по п.1.
138. Способ по п.137, где указанное злокачественное новообразование представляет собой карциному.
139. Способ по п.138, где указанный рак представляет собой рак поджелудочной железы.
140. Способ по п.137, где указанный диагностический анализ in vitro выбран из группы, состоящей из иммунологических анализов, PCR, RT-PCR и иммуногистохимии.
141. Способ по п.140, где указанный диагностический анализ in vitro представляет собой RT-PCR или иммунологический анализ.
142. Способ по п.141, где указанный образец представляет собой жидкость организма или ткань.
143. Способ по п.140, где указанный диагностический анализ представляет собой иммуногистохимию.
144. Способ по п.143, где указанный образец представляет собой популяцию клеток или ткань.
145. Способ происходящего во время операции определения у субъекта поврежденных тканей, экспрессирующих антиген PAM4, подразумевающий
(A) введение эффективного количества биспецифического антитела или фрагмента антитела, включающего в себя по меньшей мере одно плечо, которое специфически связывается с экспрессирующимся в ткани-мишени антигеном PAM4, и по меньшей мере одно другое плечо, которое специфически связывается с нацеливаемым конъюгатом, где указанное одно плечо, которое специфически связывается с тканью-мишенью, представляет собой антитело cPAM4 или его фрагмент; и
(B) введение нацеливаемого конъюгата, выбранного из группы, состоящей из
(i) DOTA-Phe-Lys(HSG)-D-Tyr-Lys(HSG)-NH2;
(ii) DOTA-Phe-Lys(HSG)-Tyr-Lys(HSG)-NH2;
(iii) Ac-Lys(HSG)D-Tyr-Lys(HSG)-Lys(Tscg-Cys)-NH2;
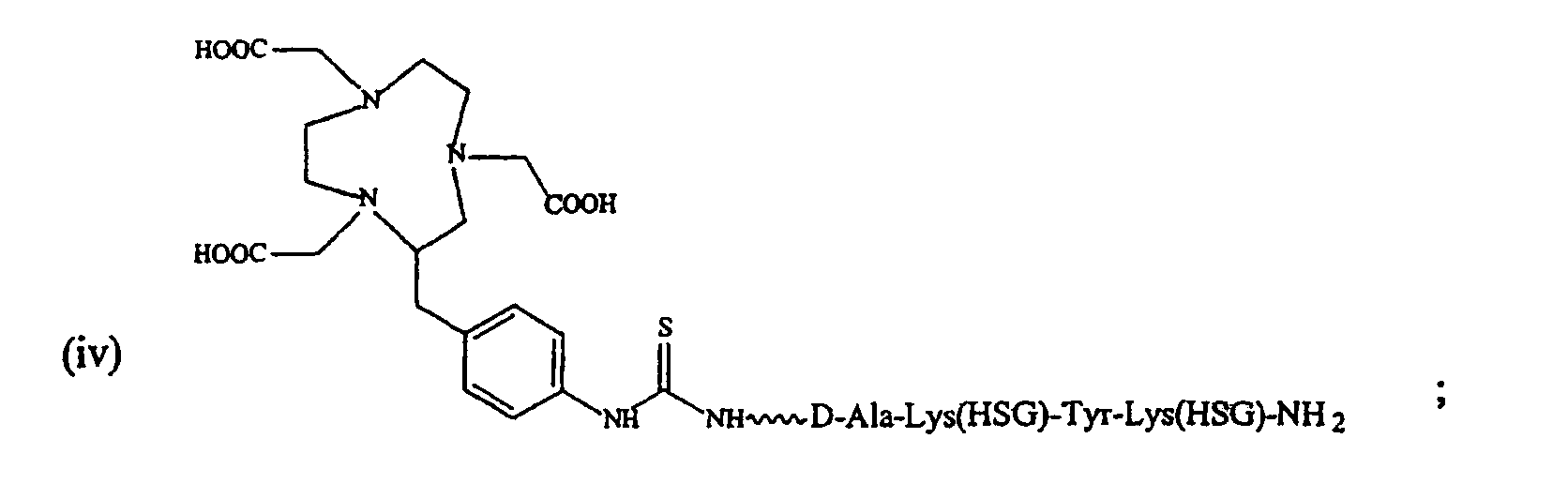
и

146. Способ эндоскопического определения у субъекта поврежденных тканей, экспрессирующих антиген PAM4, подразумевающий введение эффективного количества биспецифического антитела или фрагмента антитела, включающего в себя по меньшей мере одно плечо, которое специфически связывается с экспрессирующимся в ткани-мишени антигеном PAM4, и по меньшей мере одно другое плечо, которое специфически связывается с нацеливаемым конъюгатом, где указанное одно плечо, которое специфически связывается с тканью-мишенью, представляет собой антитело cPAM4 или его фрагмент; и
введение нацеливаемого конъюгата, выбранного из группы, состоящей из
(i) DOTA-Phe-Lys(HSG)-D-Tyr-Lys(HSG)-NH2;
(ii) DOTA-Phe-Lys(HSG)-Tyr-Lys(HSG)-NH2;
(iii) Ac-Lys(HSG)D-Tyr-Lys(HSG)-Lys(Tscg-Cys)-NH2;

и

147. Способ внутрисосудистого определения поврежденных тканей, экспрессирующих антиген PAM4, у субъекта, подразумевающий введение эффективного количества биспецифического антитела или фрагмента антитела, включающего в себя по меньшей мере одно плечо, которое специфически связывается с экспрессирующимся в ткани-мишени антигеном PAM4, и по меньшей мере одно другое плечо, которое специфически связывается с нацеливаемым конъюгатом, где указанное одно плечо, которое специфически связывается с тканью-мишенью, представляет собой антитело cPAM4 или его фрагмент; и
введение нацеливаемого конъюгата, выбранного из группы, состоящей из
(i) DOTA-Phe-Lys(HSG)-D-Tyr-Lys(HSG)-NH2;
(ii) DOTA-Phe-Lys(HSG)-Tyr-Lys(HSG)-NH2;
(iii) Ac-Lys(HSG)D-Tyr-Lys(HSG)-Lys(Tscg-Cys)-NH2;

и

148. Способ детекции очагов повреждения во время эндоскопической, внутрисосудистой катетерной или хирургической процедуры, где данный способ подразумевает инъекцию субъекту, который подвергается данной процедуре, биспецифического антитела, F(ab)2- или F(ab')2-фрагмента, ди-антитела, три-антитела или тетра-антитела, где указанное биспецифическое антитело или фрагмент характеризуется первым антительным участком связывания, который специфически связывается с антигеном PAM4, и характеризуется вторым участком связывания, который специфически связывается с гаптеном, и обеспечение накопления фрагмента антитела в участках-мишенях; необязательное выведение ненацеленных фрагментов антител с использованием галактозилированного антиидиотипического средства выведения, если данный биспецифический фрагмент большей частью не выводится из циркуляции примерно за 24 ч после инъекции, и инъекцию бивалентного меченого гаптена, который быстро локализуется в участке связывания и выводится через почки; выявление присутствия гаптена путем приближенной детекции повышенных уровней накопленной в участках-мишенях метки средствами детекции в пределах 48 ч после первой инъекции, и проведение указанной процедуры, где указанную детекцию проводят без применения контрастного средства или вычитающего средства.
149. Способ приближенной детекции во время операционной, внутрисосудистой или эндоскопической процедуры, где указанный способ подразумевает парентеральную инъекцию субъекту, подвергаемого такой процедуре, эффективного количества иммуноконъюгата cPAM4 или его фрагмента; проведение процедуры в пределах 48 ч после инъекции; приближенное сканирование оцениваемого внутреннего органа субъекта средствами детекции для выявления присутствия указанного меченого антитела или его фрагмента; и локализацию участков накопления указанного меченого антитела или его фрагмента путем выявления повышенных уровней указанного меченого антитела или его фрагмента в таких участках средствами детекции.

Комментарии