Функционализованный (мет) акрилатный мономер, полимер, покровное средство, способ получения и способ сшивания - RU2523549C9
Код документа: RU2523549C9
Описание
Настоящее изобретение относится к функционализованному (мет)акрилатному мономеру и способу его получения, а также к смеси мономеров, которая содержит указанный (мет)акрилатный мономер. Настоящее изобретение относится также к полимеру, который может быть получен с использованием указанного мономера или соответственно указанной смеси мономеров. Кроме того, настоящее изобретение относится к покровному средству и способу сшивания.
Покровные средства, в частности лаки, давно производят синтетическим путем. Новыми покровными средствами являются содержащие карбонильные группы полимеры, которые в присутствии сшивающих агентов способны отверждаться с образованием устойчивых по отношению к растворителям лаков. Указанные покровные средства известны, в частности, из международной заявки WO 94/025433. Однако комплекс свойств указанных покровных средств давно нуждается в усовершенствовании.
С учетом уровня техники в основу настоящего изобретения была положена задача предложить мономеры, которые можно было бы перерабатывать в обладающие отличными свойствами полимеры. Подобными свойствами, в частности, являются относящиеся к существу настоящего изобретения признаки покровных средств и покрытий, которые могут быть из них выполнены.
В частности, должна быть найдена возможность переработки указанных мономеров в дисперсии или соответственно полимеры, получаемые, например, путем эмульсионной полимеризации, которые обладают чрезвычайно низким содержанием остаточного мономера.
Кроме того, в основу настоящего изобретения была положена задача предложить пригодное для особо длительного хранения стабильное покровное средство. Наряду с этим должна быть найдена возможность варьирования в широком диапазоне твердости покрытий, которые могут быть выполнены из подобных покровных средств. Соответствующие покрытия, в частности, должны обладать особенно высокой твердостью и стойкостью к царапанью.
Другая задача настоящего изобретения состояла в том, чтобы предложить полимеры, покровные средства из которых можно было бы изготавливать без использования летучих органических растворителей. Покрытия, которые могут быть выполнены из подобных покровных средств, должны обладать высокой атмосферостойкостью и, в частности, высокой стойкостью к воздействию ультрафиолетовых лучей. Вместе с тем пленки, которые могут быть выполнены из подобных покровных средств, уже спустя небольшое время после изготовления должны обладать незначительной липкостью.
Покрытия, получаемые из полимеров, соответственно смесей мономеров, должны обладать также особенно высокой стойкостью к воздействию растворителей. Указанные покрытия должны обладать высокой стойкостью к воздействию множества самых разных растворителей. Вместе с тем они должны быть чрезвычайно стойкими по отношению к кислотным и щелочным средствам для очистки.
Кроме того, задача настоящего изобретения состояла в том, чтобы предложить мономеры, полимеры и покровные средства, которые можно было бы получать в соответствии с особенно экономичной технологией. В случае синтеза полимеров из смеси мономеров последняя (при условии одинаковой функциональной пригодности получаемых полимеров) должна содержать минимальные количества синтезируемых дорогостоящими методами компонентов.
Другая задача настоящего изобретения состояла в том, чтобы предложить экономичный способ получения указанных выше мономеров. Получаемые при этом мономеры должны обладать весьма незначительным содержанием побочных продуктов и остатков катализатора.
Предлагаемый в изобретении способ должен быть пригоден для получения мономеров, осуществляемого с чрезвычайно высокой селективностью. Получаемые мономеры должны быть пригодны для реализуемого без каких-либо проблем превращения на других технологических стадиях без предварительной дорогостоящей очистки.
Кроме того, в основу настоящего изобретения была положена задача предложить простой и экономичный способ получения мономеров. Способ должен отличаться возможностью реализации без значительного энергопотребления и должен обеспечивать максимально высокие выходы целевых мономеров.
Указанные выше, а также другие задачи настоящего изобретения, которые не были сформулированы, однако вытекают из контекста приведенного описания, решаются благодаря мономеру с представленными в пункте 1 отличительными признаками. Целесообразные варианты предлагаемого в изобретении мономера приведены в соответствующих зависимых пунктах. Решение задач настоящего изобретения, относящихся к смеси мономеров, полимеру, покровному средству, а также к способу получения мономера, приведены в пунктах 8, 15, 20 и 23 формулы изобретения.
Итак, объектом настоящего изобретения является (мет)акрилатный мономер общей формулы (I):

в которой
R1 означает водород или метильную группу,
Х означает кислород или группу формулы NR', в которой R' означает водород или остаток с 1-6 атомами углерода, и
R2 означает остаток с 3-31 атомами углерода и по меньшей мере одной альдегидной группой.
Благодаря реализации предлагаемых в изобретении технических мероприятий могут быть достигнуты, в частности, следующие преимущества.
Предлагаемые в изобретении смеси мономеров можно перерабатывать в полимеры, покровные средства и покрытия, которые обладают чрезвычайно низким остаточным содержанием мономеров.
Твердость покрытий, которые могут быть выполнены из предлагаемых в изобретении покровных средств, основанных на полимерах, соответственно смесях мономеров, можно варьировать в широком диапазоне. Согласно предпочтительному варианту осуществления изобретения могут быть выполнены особо твердые и стойкие к царапанью покрытия. Покрытия, которые могут быть выполнены из предлагаемых в изобретении покровных средств, неожиданно отличаются высокой устойчивостью к воздействию растворителей, в частности к воздействию метилизобутилкетона и этанола. Особенно высокими показателями устойчивости они отличаются в условиях принятого в мебельной промышленности испытания согласно DIN 68861-1.
Покровные средства, которые могут быть изготовлены с использованием предлагаемых в изобретении смесей мономеров, в общем случае не требуют присутствия летучих органических растворителей. Кроме того, предлагаемые в изобретении покровные средства отличаются высокой стойкостью при хранении и стабильностью, а также чрезвычайно высокой пригодностью к хранению. В частности, они характеризуются практически полным отсутствием склонности к образованию агрегатов.
Покрытия, которые могут быть выполнены из предлагаемых в изобретении покровных средств, отличаются высокой атмосферостойкостью, в частности высокой стабильностью в условиях воздействия ультрафиолетовых лучей. Кроме того, пленки, которые могут быть изготовлены из указанных покровных средств, отличаются незначительной липкостью уже по истечении небольшого времени после изготовления.
Предлагаемые в изобретении мономеры, смеси мономеров, полимеры и покровные средства можно экономично производить в промышленном масштабе. Полимеры с высокой функциональной пригодностью можно получать из смесей мономеров с незначительным содержанием подлежащих дорогостоящему синтезу компонентов. Функциональная пригодность полимеров определяется, в частности, свойствами изготавливаемых из них покровных средств и покрытий.
Предлагаемые в изобретении покровные средства не наносят ущерба окружающей среде и могут быть переработаны безопасными и экономичными методами. При этом они отличаются чрезвычайно высокой стабильностью в условиях воздействия усилий сдвига.
Кроме того, предлагаемый в изобретении способ пригоден для чрезвычайно экономичного синтеза функционализованных (мет)акрилатов. Получаемые согласно изобретению (мет)акрилаты неожиданно обладают чрезвычайно незначительным содержанием побочных продуктов и в общем случае характеризуются полным отсутствием остатков катализатора. Соответствующие смеси отлично пригодны для осуществления последующих технологических операций без необходимости предварительной дорогостоящей очистки.
Предлагаемый в изобретении способ позволяет с особенно высокой селективностью получать функционализованные (мет)акрилаты.
Предлагаемый в изобретении способ является простым и экономичным, причем целевой продукт можно получать с высокими выходами и при незначительном энергопотреблении.
Предлагаемый в изобретении (мет)акрилатный мономер обладает общей формулой (I):
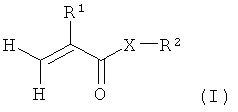
в которой
R1 означает водород или метильную группу,
Х означает кислород или группу формулы NR', в которой R' означает водород или остаток с 1-6 атомами углерода, и
R2 означает остаток с 3-31 атомами углерода и по меньшей мере одной альдегидной группой.
Согласно изобретению под остатком с 1-6 атомами углерода, соответственно остатком с 3-31 атомами углерода, подразумевают группу, которая содержит от 1 до 6 атомов углерода, соответственно от 3 до 31 атомов углерода. Речь при этом идет об ароматических или гетероароматических группах, а также об алкильных, циклоалкильных, алкоксильных, циклоалкоксильных, алкенильных, алканоильных или алкоксикарбонильных группах и о гетероалифатических группах. При этом указанные группы могут быть разветвленными или неразветвленными. Кроме того, указанные группы могут содержать заместители, которыми, в частности, являются атомы галогенов или гидроксильные группы.
Остатками R' предпочтительно являются алкильные группы. При этом к предпочтительным алкильным группам относятся метил, этил, пропил, изопропил, 1-бутил, 2-бутил, 2-метилпропил и трет-бутил.
Остаток R2 в формуле (I) означает группу с 3-31 атомами углерода, в частности с 3-25 атомами углерода, предпочтительно с 3-9 атомами углерода, особенно предпочтительно с 4-6 атомами углерода, которая содержит по меньшей мере одну альдегидную группу. Согласно другому варианту осуществления настоящего изобретения предпочтительными являются (мет)акрилатные мономеры, которые содержат от 10 до 25 атомов углерода. При этом остаток R2 может содержать одну, две, три или более альдегидных групп, а также может быть замещенным или может содержать другие функциональные группы, например, углерод-углеродные двойные связи. Согласно предпочтительному варианту осуществления настоящего изобретения остаток R2 означает алкильную или алкенильную группу, которая содержит одну или две альдегидные группы, причем особенно предпочтительными являются остатки с одной альдегидной группой. Подобные группы могут содержать гетероатомы, в частности атомы кислорода и/или азота, например, в виде сложноэфирных групп, групп простого эфира, аминогрупп и/или амидных групп.
К предпочтительным остаткам R2, в частности, относятся 2-формилэтил, 3-формилэтил, 2-формилпропил, 3-формилпропил, 2-формилокта-7-енил, 2,7-диформилоктил, 9-формилоктадецил и 10-формилоктадецил.
К предпочтительным (мет)акрилатным мономерам формулы (I), в частности, относятся (мет)акрилатные мономеры с 3-9 атомами углерода в остатке R2, например, такие как 3-оксопропил(мет)акрилат (2-формилэтил-(мет)акрилат), 4-оксобутил(мет)акрилат (3-формилпропил(мет)акрилат), 2-метил-3-оксопропил(мет)акрилат (2-формил-2-метилэтил(мет)акрилат), 2-формилоктенил(мет)акрилат, 3-формилоктенил(мет)акрилат, 8-формил-октенил(мет)акрилат, 7-формилоктенил(мет)акрилат, 2,8-диформилоктил-(мет)акрилат и 3,7-диформилоктил(мет)акрилат.
Кроме того, к (мет)акрилатным мономерам формулы (I) относятся (мет)-акрилатные мономеры с 10-25 атомами углерода в остатке R2, такие как (мет)акрилаты, являющиеся производными жирных кислот, жирных спиртов или амидов жирных кислот, в частности, 9-формилоктадекан-12-енил(мет)акрилат, 9,12-диформилоктадецил(мет)акрилат, 12-формилокта-декан-6,9-диенил(мет)акрилат, 9-формилгексадецил(мет)акрилат, 10-формилгексадецил(мет)акрилат, 9-формилоктадецил(мет)акрилат, 10-формилоктадецил(мет)акрилат, сложные эфиры (мет)акрилоилокси-2-гидроксипропил-9-формилоктадекановой кислоты, сложные эфиры (мет)-акрилоилокси-2-гидроксипропил-10-формилоктадекановой кислоты, амид (мет)акрилоилокси-2-гидроксипропил-9-формилоктадекановой кислоты и/или амид (мет)акрилоилокси-2-гидроксипропил-10-формилоктадекановой кислоты.
Кроме того, к (мет)акрилатным мономерам формулы (I) относятся (мет)-акрилаты, которые обладают формулой (II):

в которой
R1 означает водород или метильную группу,
Х означает кислород или группу формулы NR', в которой R' означает водород или остаток с 1-6 атомами углерода,
R3 означает алкиленовую группу с 1-22 атомами углерода,
Y означает кислород, серу или группу формулы NR", в которой R" означает водород или остаток с 1-6 атомами углерода, и
R4 означает остаток с 8 атомами углерода и по меньшей мере одной альдегидной группой.
Остатки R' и R" соответственно предпочтительно означают алкильную группу. При этом к предпочтительным алкильным группам относятся метил, этил, пропил, изопропил, 1-бутил, 2-бутил, 2-метилпропил и трет-бутил.
Остаток R3 в формуле (II) означает алкиленовую группу с 1-22 атомами углерода, предпочтительно с 1-10 атомами углерода, особенно предпочтительно с 2-6 атомами углерода. Согласно особому варианту осуществления настоящего изобретения остаток R3 означает алкиленовую группу с 2-4 атомами углерода, особенно предпочтительно с двумя атомами углерода. К алкиленовым группам с 1-22 атомами углерода, в частности, относятся метиленовая, этиленовая, пропиленовая, изопропиленовая, н-бутиленовая, изобутиленовая, трет-бутиленовая или циклогексиленовая группа, особенно предпочтительно этиленовая группа.
Остаток R4 содержит по меньшей мере одну альдегидную группу, предпочтительно две альдегидные группы. Согласно другому варианту остаток R4содержит одну альдегидную группу и одну двойную связь.
К (мет)акрилатам формулы (II) относятся, например, 2-[(2-формилокта-7-енил)метиламино]этил-2-метилпроп-2-еноат, 2-[(7-формилокта-2-енил)-метиламино]этил-2-метилпроп-2-еноат, 2-[(3-формилокта-7-енил)метил-амино]этил-2-метилпроп-2-еноат, 2-[(8-формилокта-2-енил)метиламино]-этил-2-метилпроп-2-еноат, 2-[(2,7-диформилоктил)метиламино]этил-2-метилпроп-2-еноат, 2-[(3,7-диформилоктил)метиламино]этил-2-метилпроп-2-еноат, 2-[(2,8-диформилоктил)метиламино]этил-2-метилпроп-2-еноат, 2-[(3,8-диформилоктил)метиламино]этил-2-метилпроп-2-еноат, амид 2-[(2-формилокта-7-енил)метиламино]этил(мет)акриловой кислоты, амид 2-[(7-формилокта-2-енил)метиламино]этил(мет)акриловой кислоты, амид 2-[(3-формилокта-7-енил)метиламино]этил(мет)акриловой кислоты, амид 2-[(8-формилокта-2-енил)метиламино]этил(мет)акриловой кислоты, амид 2-[(2,7-диформилоктил)метиламино]этил(мет)акриловой кислоты, амид 2-[(3,7-диформилоктил)метиламино]этил(мет)акриловой кислоты, амид 2-[(2,8-диформилоктил)метиламино]этил(мет)акриловой кислоты, амид 2-[(3,8-диформилоктил)метиламино]этил(мет)акриловой кислоты, сложные эфиры (мет)акрилоилокси-2-гидроксипропил-9-формилоктадека-12-еновой кислоты, сложные эфиры (мет)акрилоилокси-2-гидроксипропил-12-формилоктадека-9-еновой кислоты, сложные эфиры (мет)акрилоилокси-2-гидроксипропил-10-формилоктадека-12-еновой кислоты, сложные эфиры (мет)акрилоилокси-2-гидроксипропил-13-формилоктадека-9-еновой кислоты, сложные эфиры (мет)акрилоилокси-2-гидроксипропил-9,12-диформил-октадекановой кислоты, сложные эфиры (мет)акрилоилокси-2-гидроксипропил-10,13-диформилоктадекановой кислоты, сложные эфиры (мет)акрилоилокси-2-гидроксипропил-9-формилоктадекановой кислоты, сложные эфиры (мет)акрилоилокси-2-гидроксипропил-10-формилоктадекановой кислоты, амид (мет)акрилоилокси-2-гидроксипропил-9-формилоктадека-12-еновой кислоты, амид (мет)акрилоилокси-2-гидроксипропил-12-формилоктадека-9-еновой кислоты, амид (мет)акрилоилокси-2-гидрокси-пропил-10-формилоктадека-12-еновой кислоты, амид (мет)акрилоилокси-2-гидроксипропил-13-формилоктадека-9-еновой кислоты, амид (мет)акрилоилокси-2-гидроксипропил-9,12-диформилоктадекановой кислоты, амид (мет)акрилоилокси-2-гидроксипропил-10,13-диформилоктадекановой кислоты, амид (мет)акрилоилокси-2-гидроксипропил-9-формилоктадекановой кислоты и/или амид (мет)акрилоилокси-2-гидроксипропил-10-формилоктадекановой кислоты.
Указанные мономеры можно использовать по отдельности или в виде смесей двух или более соединений.
(Мет)акрилатные мономеры формулы (I) с преимуществами, которые не могли быть заранее предвидены, можно получать путем взаимодействия исходного продукта формулы (III):

в которой
Х означает кислород или группу формулы NR', в которой R' означает водород или остаток с 1-6 атомами углерода, и
R5 означает ненасыщенный остаток по меньшей мере с одной двойной связью и 2-30 атомами углерода, предпочтительно 2-24 атомами углерода,
с монооксидом углерода и водородом в присутствии катализатора.
Взаимодействие ненасыщенных соединений с монооксидом углерода и водородом в присутствии катализатора часто называют гидроформилированием. К предпочтительным катализаторам гидроформилирования, в частности, относятся соединения, которые содержат родий, иридий, палладий и/или кобальт, причем особенно предпочтительным является родий.
Согласно особому варианту осуществления изобретения для указанного катализа, в частности, можно использовать комплексы, в состав которых в качестве лиганда входит по меньшей мере одно фосфорсодержащее соединение. Предпочтительные фосфорсодержащие соединения включают ароматические группы и по меньшей мере один атом фосфора, особенно предпочтительно два атома фосфора. К пригодным фосфорсодержащим соединениям, в частности, относятся фосфины, фосфиты, фосфиниты и фосфониты. Примерами пригодных фосфинов является трифенилфосфин, трис(п-толил)фосфин, трис(м-толил)фосфин, трис(о-толил)фосфин, трис(п-метоксифенил)фосфин, трис(п-диметиламинофенил)фосфин, трициклогексилфосфин, трициклопентилфосфин, триэтилфосфин, три(1-нафтил)фосфин, трибензилфосфин, три-н-бутилфосфин и три-трет-бутилфосфин. Примерами пригодных фосфитов являются триметилфосфит, триэтилфосфит, три-н-пропилфосфит, триизопропилфосфит, три-н-бутилфосфит, триизобутилфосфит, три-трет-бутилфосфит, трис(2-этилгексил)фосфит, трифенилфосфит, трис(2,4-ди-трет-бутилфенил)-фосфит, трис(2-трет-бутил-4-метоксифенил)фосфит, трис(2-трет-бутил-4-метилфенил)фосфит и трис(п-крезил)фосфит. Примерами пригодных фосфонитов являются метилдиэтоксифосфин, фенилдиметоксифосфин, фенилдифеноксифосфин, 2-фенокси-2Н-дибенз[с,е][1,2]оксафосфорин и их производные, в которых атомы водорода полностью или частично заменены алкильными и/или арильными остатками или атомами галогена. Обычно используемыми фосфинитными лигандами являются дифенил-(фенокси)фосфин и его производные дифенил(метокси)фосфин и дифенил(этокси)фосфин.
К особенно предпочтительным лигандам, в частности, относятся 4,5-бис(дифенилфосфино)-9,9-диметилксантен (ксантофос), его производное 10,10'-(2,7-ди-трет-бутил-9,9-диметил-9Н-ксантен-4,5диил)бис(10Н-феноксафосфинин) (РОР-ксантофос) и бифефос:
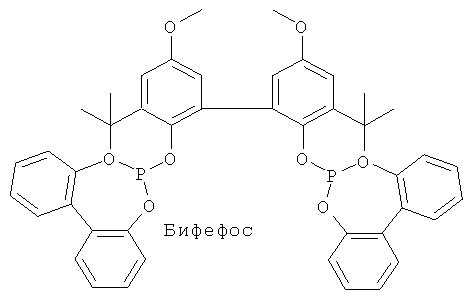
Пригодные для гидроформилирования катализаторы и лиганды приведены, например, в следующих зарегистрированных Европейским патентным ведомством документах: международной заявке WO 2008/071508 А1 (номер регистрации РСТ/ЕР 2007/062248 от 13.11.2007), европейском патенте ЕР 982314 В1 (номер регистрации 99116208 от 17.08.1999), а также в международных заявках WO 2008/012128 А1 (номер регистрации РСТ/ЕР 2007/055165 от 29.05.2007), WO 2008/006633 А1 (номер регистрации РСТ/ЕР 2007/054576 от 11.29.05.2007), WO 2007/036424 А1 (номер регистрации РСТ/ЕР 2006/066181 от 08.09.2006), WO 2007/028660 А1 (номер регистрации РСТ/ЕР 2006/062872 от 02.06.2006) и WO 2005/090276 А1 (номер регистрации РСТ/ЕР 2005/050347 от 27.01.2005), причем соответствующие публикации с указанными в них катализаторами и лигандами следует рассматривать в качестве ссылок, способствующих раскрытию сущности настоящего изобретения.
Согласно особому варианту осуществления предлагаемого в изобретении способа фосфорсодержащее соединение в качестве лиганда можно использовать в избытке по отношению к металлу. Благодаря этому неожиданно можно достичь преимуществ в отношении селективности и реакционной способности. При этом предпочтительное отношение металла к лиганду находится в интервале от 1:1 до 1:1000, особенно предпочтительно в интервале от 1:2 до 1:200.
К предпочтительным исходным веществам, которые можно использовать для получения (мет)акрилатов формулы (I), которым соответствует приведенная выше формула (II), относятся, в частности, (мет)акрилаты с 2-8 атомами углерода в алкильном остатке, являющиеся производными ненасыщенных спиртов, и (мет)акрилаты с 9-24 атомами углерода в алкильном остатке, содержащие по меньшей мере одну двойную связь.
К (мет)акрилатам с 2-8 атомами углерода в алкильном остатке, которые являются производными ненасыщенных спиртов, относятся 2-пропинил-(мет)акрилат, аллил(мет)акрилат и винил(мет)акрилат.
К (мет)акрилатам с 9-30 атомами углерода, предпочтительно с 9-24 атомами углерода, и по меньшей мере одной двойной связью в алкильном остатке, в частности, относятся (мет)акрилаты, которые являются производными ненасыщенных жирных кислот, жирных спиртов и амидов жирных кислот, такие как амид гептадеценилоилокси-2-этил(мет)акриловой кислоты, амид гептадекандиенилоилокси-2-этил(мет)акриловой кислоты, амид гептадекантриенилоилокси-2-этил(мет)акриловой кислоты, амид гептаде-ценилоилокси-2-этил(мет)акриловой кислоты, амид (мет)акрилоилокси-2-этилпальмитолеиновой кислоты, амид (мет)акрилоилокси-2-этилолеиновой кислоты, амид (мет)акрилоилокси-2-этиликозеновой кислоты, амид (мет)акрилоилокси-2-этилцетолеиновой кислоты, амид (мет)акрилоилокси-2-этилэруковой кислоты, амид (мет)акрилоилокси-2-этиллинолевой кислоты, амид (мет)акрилоилокси-2-этиллиноленовой кислоты, амид (мет)акрилоилокси-2-пропилпальмитолеиновой кислоты, амид (мет)акрилоилокси-2-пропилолеиновой кислоты, амид (мет)акрилоилокси-2-пропиликозеновой кислоты, амид (мет)акрилоилокси-2-пропилцетолеиновой кислоты, амид (мет)акрилоилокси-2-пропилэруковой кислоты, амид (мет)акрилоилокси-2-пропиллинолевой кислоты, амид (мет)акрилоилокси-2-пропиллиноленовой кислоты, сложные эфиры (мет)акрилоилокси-2-гидроксипропиллинолевой кислоты, сложные эфиры (мет)акрилоилокси-2-гидроксипропил-линоленовой кислоты, сложные эфиры (мет)акрилоилокси-2-гидрокси-пропилолеиновой кислоты, октадекандиенил(мет)акрилат, октадекантриенил(мет)акрилат, гексадеценил(мет)акрилат, октадеценил(мет)акрилат и гексадекандиенил(мет)акрилат.
Кроме того, к (мет)акрилатам с 9-30 атомами углерода, предпочтительно с 9-24 атомами углерода, и по меньшей мере одной двойной связью в алкильном остатке относятся, в частности, (мет)акрилатные мономеры общей формулы (IV):

в которой
R1 означает водород или метильную группу,
Х означает кислород или группу формулы NR', в которой R' означает водород или остаток с 1-6 атомами углерода,
R6 означает алкиленовую группу с 1-22 атомами углерода,
Y означает кислород, серу или группу формулы NR", в которой R" означает водород или остаток с 1-6 атомами углерода, и
R7 означает ненасыщенный остаток с 8 атомами углерода и по меньшей мере двумя двойными связями.
Предпочтительные остатки R6 такие, как указано выше для остатка R3.
К (мет)акрилатным мономерам общей формулы (IV) относятся, в частности, 2-[((2-Е)окта-2,7-диенил)метиламино]этил-2-метилпроп-2-еноат, 2-[((2-7)окта-2,7-диенил)метиламино]этил-2-метилпроп-2-еноат, 2-[((3-Е)-окта-3,7-диенил)метиламино]этил-2-метилпроп-2-еноат, 2-[((4-7)окта-4,7-диенил)метиламино]этил-2-метилпроп-2-еноат, 2-[(окта-2,6-диенил)метиламино]этил-2-метилпроп-2-еноат, 2-[(окта-2,4-диенил)метиламино]этил-2-метилпроп-2-еноат, 2-[(окта-3,5-диенил)метиламино]-этил-2-метилпроп-2-еноат, амид 2-[((2-е)окта-2,7-диенил)метиламино]этил(мет)акриловой кислоты, амид 2-[((2-Z)окта-2,7-диенил)метиламино]этил(мет)акриловой кислоты, амид 2-[((3-Е)окта-3,7-диенил)метиламино]этил(мет)акриловой кислоты, амид 2-[((4-Z)окта-4,7-диенил)метиламино]этил(мет)акриловой кислоты, амид 2-[(окта-2,6-диенил)метиламино]этил(мет)акриловой кислоты, амид 2-[(окта-2,4-диенил)метиламино]этил(мет)акриловой кислоты, амид 2-[(окта-3,5-диенил)метиламино]этил(мет)акриловой кислоты, 2-[((2-Е)окта-2,7-диенил)этиламино]этил-2-метилпроп-2-еноат, 2-[((2-7)окта-2,7-диенил)-этиламино]этил-2-метилпроп-2-еноат, 2-[((3-Е)окта-3,7-диенил)этиламино]-этил-2-метилпроп-2-еноат, 2-[((4-Z)окта-4,7-диенил)этиламино]этил-2-метилпроп-2-еноат, 2-[(окта-2,6-диенил)этиламино]этил-2-метилпроп-2-еноат, 2-[(окта-2,4-диенил)этиламино]этил-2-метилпроп-2-еноат, 2-[(окта-3,5-диенил)этиламино]этил-2-метилпроп-2-еноат, 2-[((2-Е)окта-2,7-диенил)-метиламино]этилпроп-2-еноат, 2-[((2-7)окта-2,7-диенил)метиламино]этил-проп-2-еноат, 2-[((3-Е)окта-3,7-диенил)метиламино]этилпроп-2-еноат, 2-[((4-2)окта-4,7-диенил)метиламино]этилпроп-2-еноат, 2-[(окта-2,6-диенил)метиламино]этилпроп-2-еноат, 2-[(окта-2,4-диенил)метиламино]-этилпроп-2-еноат, 2-[(окта-3,5-диенил)метиламино]этилпроп-2-еноат, 2-((2-Е)окта-2,7-диенилокси)этил-2-метилпроп-2-еноат, 2-((2-Z)окта-2,7-диенилокси)этил-2-метилпроп-2-еноат, 2-((3-Е)окта-3,7-диенилокси)этил-2-метилпроп-2-еноат, 2-((4-Z)окта-4,7-диенилокси)этил-2-метилпроп-2-еноат, 2-(окта-2,6-диенилокси)этил-2-метилпроп-2-еноат, 2-(окта-2,4-диенилокси)-этил-2-метилпроп-2-еноат, 2-(окта-3,5-диенилокси)этил-2-метилпроп-2-еноат, 2-((2-Е)окта-2,7-диенилокси)этилпроп-2-еноат, 2-((2-7)окта-2,7-диенилокси)этилпроп-2-еноат, 2-((3-Е)окта-3,7-диенилокси)этилпроп-2-еноат, 2-((4-7)окта-4,7-диенилокси)этилпроп-2-еноат, 2-(окта-2,6-диенилокси)этилпроп-2-еноат, 2-(окта-2,4-диенилокси)этилпроп-2-еноат и 2-(окта-3,5-диенилокси)этилпроп-2-еноат.
Исходные продукты формулы (III) можно использовать по отдельности или в виде смесей.
Часть указанных выше (мет)акрилатов, которые можно использовать в качестве исходных продуктов, являются коммерчески доступными соединениями. Кроме того, указанные выше (мет)акрилаты могут быть получены по реакции теломеризации, путем взаимодействия жирных кислот с глицидил(мет)акрилатом, по реакции этерификации или по реакции переэтерификации.
Взаимодействие глицидил(мет)акрилата с жирными кислотами описано, в частности, в международной заявке WO 2006/013061.
Указанные выше (мет)акрилаты, в частности, могут быть получены путем взаимодействия метакриловой кислоты, акриловой кислоты или смеси этих кислот (ниже их сокращенно называют (мет)акриловой кислотой) или (мет)акрилата, в частности метил(мет)акрилата или этил(мет)акрилата, со спиртом и/или амином. Переэтерификация спиртов (мет)акрилатами или получение амидов (мет)акриловой кислоты описаны также в патенте Канады CN 1355161, немецких патентах DE 2129425 (номер регистрации Немецким патентным ведомством Р 2129425.7 от 14.06.71) и DE 3423443 (номер регистрации Немецким патентным ведомством Р 3423443.8 от 26.06.84), европейской заявке на патент ЕР-А-0534666 (номер регистрации Европейским патентным ведомством ЕР 92308426.3 от 16.09.92), а также в немецком патенте DE 3430446 (номер регистрации Немецким патентным ведомством Р 3430446.0 от 18.08.84), причем соответствующие публикации с указанными в них реакционными условиями, катализаторами и так далее следует рассматривать в качестве ссылок, способствующих раскрытию сущности настоящего изобретения. Кроме того, указанные выше превращения описаны в Synthesis of Acrylic Esters by Transesterification, J. Haken, 1967.
Исходный продукт, подлежащий взаимодействию с (мет)акриловой кислотой или (мет)акрилатом, предпочтительно обладает формулой (V):

в которой
Х означает кислород или группу формулы NR', в которой R' означает водород или остаток с 1-6 атомами углерода,
R6 означает алкиленовую группу с 1-22 атомами углерода,
Y означает кислород, серу или группу формулы NR", в которой R" означает водород или остаток с 1-6 атомами углерода, и
R7 означает по меньшей мере сдвоенный ненасыщенный остаток с 8 атомами углерода.
Предпочтительные остатки R', R", R6, Y и R7 в формуле (V) такие, как указано в формуле (IV).
К предпочтительным исходным продуктам формулы (V) относятся (метил(окта-2,7-диенил)амино)этанол, (этил(окта-2,7-диенил)амино)этанол, 2-окта-2,7-диенилоксиэтанол, (метил(окта-2,7-диенил)амино)этиламин, (метил(окта-3,7-диенил)амино)этанол, (этил(окта-3,7-диенил)амино)этанол, 2-окта-3,7-диенилоксиэтанол, (метил(окта-3,7-диенил)амино)этиламин, (метил(окта-4,7-диенил)амино)этанол, (этил(окта-4,7-диенил)амино)этанол, 2-окта-4,7-диенилоксиэтанол, (метил(окта-4,7-диенил)амино)этиламин, (метил(окта-5,7-диенил)амино)этанол, (этил(окта-5,7-диенил)амино)этанол, 2-окта-5,7-диенилоксиэтанол, (метил(окта-5,7-диенил)амино)этиламин, (метил(окта-2,6-диенил)амино)этанол, (этил(окта-2,6-диенил)амино)этанол, 2-окта-2,6-диенилоксиэтанол, (метил(окта-2,6-диенил)амино)этиламин, (метил(окта-2,5-диенил)амино)этанол, (этил(окта-2,5-диенил)амино)этанол, 2-окта-2,5-диенилоксиэтанол, (метил(окта-2,5-диенил)амино)этиламин, (метил(окта-2,4-диенил)амино)этанол, (этил(окта-2,4-диенил)амино)этанол, 2-окта-2,4-диенилоксиэтанол, (метил(окта-2,4-диенил)амино)этиламин, (метил(окта-3,6-диенил)амино)этанол, (этил(окта-3,6-диенил)амино)этанол, 2-окта-3,6-диенилоксиэтанол, (метил(окта-3,6-диенил)амино)этиламин, (метил(окта-3,5-диенил)амино)этанол, (этил(окта-3,5-диенил)амино)этанол, 2-окта-3,5-диенилоксиэтанол, (метил(окта-3,5-диенил)амино)этиламин, (метил(окта-4,6-диенил)амино)этанол, (этил(окта-4,6-диенил)амино)этанол, 2-окта-4,6-диенилоксиэтанол и (метил(окта-4,6-диенил)амино)этиламин. Исходные продукты формулы (V) можно использовать по отдельности или в виде смесей.
Исходные продукты формулы (V) могут быть получены, в частности, известным методом теломеризации 1,3-бутадиена. При этом под теломеризацией подразумевают осуществляемое в присутствии нуклеофилов превращение соединений с сопряженными двойными связями. Метод теломеризации, в частности, используемые для теломеризации катализаторы и реакционные условия, например, давление и температура, приведены в зарегистрированных Европейским патентным ведомством международных заявках WO 2004/002931 (номер регистрации РСТ/ЕР 2003/006356 от 17.06.2003), WO 03/031379 (номер регистрации РСТ/ЕР 2002/10971 от 01.10.2002) и WO 02/100803 (номер регистрации РСТ/ЕР 2002/04909 от 04.05.2002), которые следует рассматривать в качестве ссылок, способствующих раскрытию сущности настоящего изобретения.
Теломеризацию 1,3-бутадиена предпочтительно можно осуществлять с использованием в качестве катализаторов соединений металлов, являющихся элементами от 8-й до 10-й групп Периодической системы, причем особенно предпочтительно можно использовать соединения палладия, в частности карбеновые комплексы палладия, более подробно рассмотренные в цитированных выше публикациях.
В качестве нуклеофилов, в частности, можно использовать двухатомные спирты, такие как этиленгликоль, 1,2-пропандиол или 1,3-пропандиол, диамины, такие как этилендиамин, N-метилэтилендиамин, N,N'-диметил-этилендиамин или гексаметилендиамин, или аминоалканолы, такие как аминоэтанол, N-метиламиноэтанол, N-этиламиноэтанол, аминопропанол, N-метиламинопропанол или N-этиламинопропанол.
В случае использования в качестве нуклеофила (мет)акриловой кислоты могут быть получены, например, октадиенил(мет)акрилаты, которые пригодны в качестве исходного продукта для получения мономеров формулы (I).
Температура, при которой осуществляют реакцию теломеризации, находится в интервале от 10 до 180°С, предпочтительно от 30 до 120°С, особенно предпочтительно от 40 до 100°С. Давление указанной реакции составляет от 1 до 300 бар, предпочтительно от 1 до 120 бар, особенно предпочтительно от 1 до 64 бар и еще более предпочтительно от 1 до 20 бар.
Изомеры содержащих окта-2,7-диенильную группу соединений можно получать путем изомеризации присутствующих в указанных группах двойных связей.
Помимо исходного продукта или соответственно исходных продуктов формулы (III) и указанных выше катализаторов для гидроформилирования используют водород (H2) и монооксид углерода (СО). Гидроформилирование предпочтительно осуществляют при общем давлении газов, составляющем от 1 до 200 бар, особенно предпочтительно от 1 до 150 бар, в частности предпочтительно от 1 до 100 бар.
Согласно особому варианту осуществления настоящего изобретения давление водорода, при котором осуществляют гидроформилирование, может превышать давление монооксида углерода.
Температура, при которой осуществляют взаимодействие исходного продукта формулы (III) с водородом и монооксидом углерода, не является критическим параметром. Особых преимуществ можно достичь, в частности, в том случае, если осуществлять реакцию в температурном интервале от 20 до 250°С, предпочтительно от 40 до 200°С, особенно предпочтительно от 150 до 160°С.
Согласно особому варианту осуществления настоящего изобретения взаимодействие можно осуществлять в инертном органическом растворителе. К подобным растворителям относятся, например, ароматические углеводороды, например, такие как толуол или ксилол, диоксан, а также сложные эфиры карбоновых кислот, например, такие как этилацетат. Особых преимуществ можно достичь в случае осуществления взаимодействия преимущественно без использования инертного органического растворителя. В этом случае функцию среды, в которой осуществляют реакцию, в частности, выполняют исходные продукты, а также лиганды.
Неожиданных преимуществ можно достичь также благодаря использованию стабилизаторов. К предпочтительным стабилизаторам относятся, в частности, гидрохиноны, простые эфиры гидрохинона, такие как монометиловый эфир гидрохинона или ди-трет-бутилпирокатехин, фенотиазин, метиленовый синий или пространственно затрудненные фенолы, например, 2,4-диметил-6-трет-бутилфенол, которые хорошо известны специалистам. Указанные соединения, которые в общем случае являются коммерчески доступными продуктами, можно использовать по отдельности или в виде смесей. Другие подробности содержатся в специальной литературе, в частности в справочнике Rompp-Lexikon Chemie (издатели J.Falbe, M.Regitz, Штутгарт, Нью-Йорк, 10-е издание, 1996) в разделе с ключевым словом «Антиоксиданты», и цитируемых в нем литературных источниках.
Указанный выше мономер формулы (I) предпочтительно можно использовать в смеси с одним или несколькими другими мономерами, способными к сополимеризации с мономером формулы (I).
Преимуществ, которые должны заинтересовать специалистов, можно достичь благодаря использованию смеси мономеров, содержащей по меньшей мере 0,5% масс., предпочтительно по меньшей мере 2% масс., особенно предпочтительно по меньшей мере 5% масс. мономеров формулы (I) в пересчете на общую массу указанной выше смеси.
Помимо по меньшей мере одного (мет)акрилатного мономера формулы (I) смесь мономеров содержит по меньшей мере один другой способный к сополимеризации мономер. К подобным способным к сополимеризации мономерам относятся, в частности, мономеры с кислотной группой, содержащие сложноэфирные группы мономеры А, которые отличаются от мономеров формулы (I), а также стирольные мономеры.
Содержащими кислотные группы мономерами преимущественно являются соединения, способные к радикальной сополимеризации с указанными выше (мет)акрилатными мономерами формулы (I). К подобным мономерам относятся, в частности, соединения с сульфокислотной группой, например, такие как винилсульфокислота, соединения с группой фосфоновой кислоты, например, такие как винилфосфоновая кислота, а также ненасыщенные карбоновые кислоты, например, такие как метакриловая кислота, акриловая кислота, фумаровая кислота и малеиновая кислота. При этом особенно предпочтительными соединениями являются метакриловая кислота и акриловая кислота. Содержащие кислотные группы мономеры можно использовать по отдельности или в виде смеси двух, трех или более содержащих кислотные группы мономеров.
К предпочтительным мономерам А, содержащим сложноэфирные группы, в частности, относятся (мет)акрилаты, которые отличаются от мономеров формулы (I), а также фумараты, малеаты и/или винилацетат. При этом под (мет)акрилатами подразумевают метакрилаты и акрилаты, а также их смеси. Указанные мономеры являются широко известными соединениями.
К подобным мономерам, в частности, относятся (мет)акрилаты с 1-6 атомами углерода в алкильном остатке, получаемые с использованием насыщенных спиртов, например, такие как метил(мет)акрилат, этил(мет)акрилат, н-пропил(мет)акрилат, изопропил(мет)акрилат, н-бутил(мет)акрилат, трет-бутил(мет)акрилат, пентил(мет)акрилат и гексил(мет)акрилат, а также циклоалкил(мет)акрилаты, например, такие как циклопентил(мет)акрилат и циклогексил(мет)акрилат.
Для получения полимеров особенно предпочтительно используют смеси, которые содержат метакрилаты и акрилаты. Так, например, в частности, можно использовать смеси метилметакрилата с акрилатами с 2-6 атомами углерода, такими как этилакрилат, бутилакрилат и гексилакрилат.
Кроме того, к пригодным сомономерам относятся, например, получаемые с использованием насыщенных спиртов (мет)акрилаты по меньшей мере с семью атомами углерода в алкильном остатке, например, такие как 2-этил-гексил(мет)акрилат, гептил(мет)акрилат, 2-трет-бутилгептил(мет)акрилат, октил(мет)акрилат, 3-изопропилгептил(мет)акрилат, нонил(мет)акрилат, децил(мет)акрилат, ундецил(мет)акрилат, 5-метилундецил(мет)акрилат, додецил(мет)акрилат, 2-метилдодецил(мет)акрилат, тридецил(мет)акрилат, 5-метилтридецил(мет)акрилат, тетрадецил(мет)акрилат, пентадецил(мет)акрилат, гексадецил(мет)акрилат, 2-метилгексадецил(мет)акрилат, гептадецил(мет)акрилат, 5-изопропилгептадецил(мет)акрилат, 4-трет-бутилоктадецил(мет)акрилат, 5-этилоктадецил(мет)акрилат, 3-изопропилоктадецил(мет)акрилат, октадецил(мет)акрилат, нонадецил(мет)акрилат, эйкозил(мет)акрилат, цетилэйкозил(мет)акрилат, стеарилэйкозил(мет)акрилат, докозил(мет)акрилат и/или эйкозилтетратриаконтил(мет)акрилат; циклоалкил(мет)акрилаты, такие как 3-винилциклогексил(мет)акрилат и борнил(мет)акрилат, циклоалкил(мет)акрилаты, такие как 2,4,5-три-трет-бутил-3-винилциклогексил(мет)акрилат и 2,3,4,5-тетра-трет-бутилцикло-гексил(мет)акрилат; гетероциклические (мет)акрилаты, такие как 2-(1-имидазолил)этил(мет)акрилат, 2-(4-морфолинил)этил(мет)акрилат и 1-(2-метакрилоилоксиэтил)-2-пирролидон; нитрилы (мет)акриловой кислоты и другие азотсодержащие метакрилаты, такие как N-(метакрилоилоксиэтил)-диизобутилкетимин, N-(метакрилоилоксиэтил)дигексадецилкетимин, метакрилоиламидоацетонитрил, 2-метакрилоилоксиэтилметилцианамид и цианометилметакрилат; арил(мет)акрилаты, такие как бензил(мет)акрилат и фенил(мет)акрилат, причем соответствующие арильные остатки могут быть незамещенными или могут содержать до четырех заместителей; (мет)акрилаты с двумя или более (мет)акрильными группами, гликольди(мет)акрилаты, такие как этиленгликольди(мет)акрилат, диэтиленгликольди(мет)акрилат, триэтиленгликольди(мет)акрилат, тетраэтиленгликольди(мет)акрилат, полиэтиленгликольди(мет)акрилат, 1,3-бутандиол(мет)акрилат, 1,4-бутандиол(мет)акрилат, 1,6-гександиолди(мет)акрилат и глицеринди(мет)акрилат; диметакрилаты этоксилированного бисфенола А; (мет)акрилаты с тремя или более двойными связями, например, такие как глицеринтри(мет)акрилат, триметилолпропантри(мет)акрилат, пентаэритриттетра(мет)акрилат и дипентаэритритпента(мет)акрилат, а также (мет)акрилаты, получаемые из амидов насыщенных жирных кислот, такие как амид пентадецилоилокси-2-этил(мет)акриловой кислоты, амид гептадецилоилокси-2-этил(мет)акриловой кислоты, амид (мет)акрилоилокси-2-этил-лауриновой кислоты, амид (мет)акрилоилокси-2-этилмиристиновой кислоты, амид (мет)акрилоилокси-2-этилпальмитиновой кислоты, амид (мет)акрилоилокси-2-этилстеариновой кислоты, амид (мет)акрилоилокси-2-пропиллауриновой кислоты, амид (мет)акрилоилокси-2-пропилмиристиновой кислоты, амид (мет)акрилоилокси-2-пропилпальмитиновой кислоты и амид (мет)акрилоилокси-2-пропилстеариновой кислоты.
Кроме того, к содержащим сложноэфирные группы мономерам А относятся (мет)акрилаты формулы (III), которые, в частности, можно использовать в качестве исходных соединений для получения указанных выше (мет)акрилатов формулы (I).
К содержащим сложноэфирные группы мономерам А относятся также сложные виниловые эфиры, такие как винилацетат, производные малеиновой кислоты, например, такие как малеиновый ангидрид, сложные эфиры малеиновой кислоты, в частности, сложный диметиловый эфир малеиновой кислоты и метилмалеиновый ангидрид, а также производные фумаровой кислоты, такие как сложный диметиловый эфир фумаровой кислоты.
Другую группу предпочтительных сомономеров образуют стирольные мономеры, например, такие как стирол, замещенные стиролы с алкильным заместителем в боковой цепи, например, такие как α-метилстирол и α-этилстирол, замещенные стиролы с алкильным заместителем в кольце, такие как винилтолуол и п-метилстирол, а также галогенированные стиролы, например, такие как монохлорстиролы, дихлорстиролы, трибромстиролы и тетрабромстиролы.
Помимо звеньев указанных выше мономеров предлагаемые в изобретении полимеры, которые получают путем полимеризации смесей мономеров, могут содержать звенья других мономеров. К последним относятся, например, гетероциклические виниловые соединения, такие как 2-винил-пиридин, 3-винилпиридин, 2-метил-5-винилпиридин, 3-этил-4-винил-пиридин, 2,3-диметил-5-винилпиридин, винилпиримидин, винилпиперидин, 9-винилкарбазол, 3-винилкарбазол, 4-винилкарбазол, 1-винилимидазол, 2-метил-1-винилимидазол, N-винилпирролидон, 2-винилпирролидон, N-винилпирролидин, 3-винилпирролидин, N-винилкапаролактам, N-винил-бутиролактам, винилоксолан, винилфуран, винилтиофен, винилтиолан, винилтиазолы, гидрированные винилтиазолы, винилоксазолы и гидрированные винилоксазолы, малеинимид, имид метилмалеиновой кислоты, простые виниловые и изопрениловые эфиры, а также винилгалогениды, например, такие как винилхлорид, винилфторид, винилиденхлорид и винилиденфторид.
Предпочтительные смеси мономеров согласно изобретению содержат от 0,1 до 90% масс., предпочтительно от 0,5 до 30% масс., особенно предпочтительно от 1 до 10% масс. и в частности от 1 до 6% масс. (мет)акрилатного мономера формулы (I), от 10 до 99,9% масс., предпочтительно от 40 до 90% масс. мономеров А со сложноэфирными группами, от 0 до 20% масс., предпочтительно от 1 до 8% масс. и в частности от 1 до 3% масс. мономера с кислотной группой, от 0 до 70% масс., предпочтительно от 0 до 50% масс. И, в частности, от 0 до 30% масс. стирольных мономеров, а также от 0 до 50% масс., предпочтительно от 0 до 30% масс. других сомономеров, причем приведенные выше данные соответственно относятся к общей массе мономеров.
Согласно особому варианту осуществления настоящего изобретения, в частности, можно использовать смеси, содержащие мономеры А со сложноэфирными группами, причем последние являются производными насыщенных спиртов, и мономеры формулы (III). Содержание мономеров формулы (III) в указанных смесях предпочтительно находится в интервале от 0,1 до 50% масс., особенно предпочтительно в интервале от 0,2 до 20% масс. и еще более предпочтительно в интервале от 1 до 10% масс. в пересчете на общую массу мономеров.
Особенно предпочтительно используют смеси с высоким содержанием мономеров А со сложноэфирными группами, являющимися производными насыщенных спиртов с 1-6 атомами углерода. Содержание мономеров А со сложноэфирными группами, являющихся производными насыщенных спиртов с 1-6 атомами углерода, предпочтительно находится в интервале от 10 до 99,9% масс., особенно предпочтительно в интервале от 40 до 90% масс. и еще более предпочтительно в интервале от 50 до 80% масс. в пересчете на общую массу мономеров.
Предлагаемые в изобретении (мет)акрилатные мономеры формулы (I) и смеси мономеров, в частности, предназначены для получения или для модифицирования полимеров. При этом полимеризацию можно осуществлять любыми известными методами. К последним, в частности, относятся радикальная, катионная или анионная полимеризация, причем можно использовать также варианты указанных методов полимеризации, например, такие как радикальная полимеризация с переносом атомов (ATRP), полимеризация под действием нитроксидов (NMP) или обратимое присоединение с переносом фрагментов цепи (RAFT).
Получаемые при этом продукты полимеризации являются новыми полимерами, которые также являются объектом настоящего изобретения. Предлагаемые в изобретении полимеры содержат звенья по меньшей мере одного мономера, который является производным (мет)акрилатного мономера общей формулы (I). Как указано выше, предлагаемые в изобретении мономеры можно использовать для осуществления радикальной полимеризации. Таким образом, мономерное звено указанного выше типа возникает вследствие превращения двойной связи, которое сопровождается образованием двух ковалентных связей. В случае присутствия в полимере двух или более подобных мономерных звеньев их обычно называют также повторяющимися структурными единицами.
Указанные выше мономеры, соответственно смеси мономеров, можно подвергать превращению, реализуемому, например, путем полимеризации в растворе, полимеризации в массе или эмульсионной полимеризации, причем преимуществ неожиданно достигают благодаря использованию метода радикальной эмульсионной полимеризации.
Методы эмульсионной полимеризации подробно описаны, в частности, в пятом издании Ullmann's Encyclopedia of Industrial Chemistry. При этом в общем случае сначала формируют водную фазу, которая помимо воды может содержать обычно используемые для стабилизации эмульсий добавки, в частности эмульгаторы и защитные коллоиды.
Затем к полученной водной фазе добавляют мономеры, которые подвергают последующей полимеризации в водной фазе. При этом для получения однородных полимерных частиц смесь мономеров можно добавлять к водной фазе в течение определенного промежутка времени непрерывно или порциями.
Эмульсионную полимеризацию можно осуществлять, например, в мини-эмульсии или в микроэмульсии (для получения более подробной информации по этому поводу смотри Chemistry and Technology of Emulsion Polymerisation, A.M.Van Herk (издатель), издательство Blackwell Publishing, Оксфорд, 2005, а также J.O'Donnell, E.W.Kaler, Macromolecular Rapid Communications, 2007, 28(14), 1445-1454). Для формирования мини-эмульсии обычно используют состабилизаторы или агенты набухания, которыми часто являются длинноцепные алканы или алканолы. Капельки мини-эмульсий предпочтительно обладают размерами, находящимися в интервале от 0,05 до 20 мкм. Размер капелек микроэмульсий предпочтительно составляет менее 1 мкм, что позволяет получать полимеры с размером частиц 50 нм. В случае микроэмульсий часто используют дополнительные поверхностно-активные вещества, например, гексанол или подобные соединения.
Диспергирование содержащей мономер фазы в водной фазе можно осуществлять известными методами. Речь при этом, в частности, идет о механическом диспергировании или о диспергировании с помощью ультразвука.
Для получения методом эмульсионной полимеризации однородного полимера предпочтительно следует использовать смесь мономеров, которая содержит от 1 до 50% масс., особенно предпочтительно от 1 до 10% масс., в частности от 1 до 6% масс. (мет)акрилатного мономера формулы (I).
В случае получения полимеров, обладающих структурой типа «ядро-оболочка», можно ступенчато изменять состав смеси мономеров, причем перед изменением состава полимеризацию осуществляют до степени превращения, предпочтительно составляющей по меньшей мере 80% масс., особенно предпочтительно по меньшей мере 95% масс. соответственно в пересчете на общую массу исходной смеси мономеров. В данном случае под полимером со структурой «ядро-оболочка» подразумевают продукт двухступенчатой или многоступенчатой эмульсионной полимеризации без обнаруживаемой, например, методом электронной микроскопии структуры «ядро-оболочка». Контроль за ходом процесса полимеризации на каждой его стадии можно осуществлять известными методами, например, гравиметрически или методом газовой хроматографии.
Для получения ядра используют смесь мономеров, которая предпочтительно содержит от 50 до 100% масс. (мет)акрилатов, причем особенно предпочтительной является смесь акрилатов и метакрилатов. После получения ядра к нему предпочтительно можно прививать смесь мономеров, которая содержит от 1 до 50% масс., особенно предпочтительно от 1 до 20% масс., в частности от 2 до 10% масс. (мет)акрилатного мономера формулы (I).
Эмульсионную полимеризацию предпочтительно осуществляют в температурном интервале от 0 до 120°С, особенно предпочтительно от 30 до 100°С. При этом особенно благоприятным является температурный интервал от 60 до 90°С, целесообразно от 70 до 85°С, предпочтительно от 75 до 85°С.
Инициирование полимеризации осуществляют посредством обычно используемых при эмульсионной полимеризации инициаторов. Пригодными органическими инициаторами являются, например, гидропероксиды, такие как трет-бутил-гидропероксид или гидропероксид кумола. К пригодным неорганическим инициаторам относится пероксид водорода, а также соли щелочных металлов или аммония с надсерной кислотой, в частности пероксодисульфат аммония, пероксодисульфат натрия и пероксодисульфат калия. Пригодными окислительно-восстановительными инициирующими системами являются, например, комбинации третичных аминов с пероксидами или дисульфитом натрия и солями щелочных металлов или аммония с надсерной кислотой, в частности пероксодисульфатом натрия и пероксодисульфатом калия. Другие подробности относительно инициирования полимеризации приведены в специальной литературе, в частности в Н.Rauch-Puntigam, Th Völker, "Acryl- und Methacrylverbindungen", издательство Springer, Гейдельберг, 1967, а также в Kirk-Othmer, Encyclopedia of Chemical Technology, том 1, сс.386 и следующие, издательство J.Wiley, Нью-Йорк, 1978. В соответствии с настоящим изобретением особенно предпочтительным является использование органических и/или неорганических инициаторов.
Указанные выше инициаторы можно использовать как по отдельности, так и в виде смесей. Инициаторы предпочтительно используют в количестве от 0,05 до 3,0% масс. в пересчете на общую массу полимеризуемых на соответствующей стадии мономеров. Для полимеризации предпочтительно можно использовать также смесь разных инициаторов полимеризации, обладающих разными периодами полураспада, что позволяет поддерживать постоянное количество радикалов в процессе полимеризации, а также при варьировании ее температуры.
Стабилизацию реакционной смеси предпочтительно осуществляют посредством эмульгаторов и/или защитных коллоидов. Эмульсию предпочтительно стабилизируют посредством эмульгаторов, что способствует образованию низковязких дисперсий. Общее количество используемого эмульгатора предпочтительно составляет от 0,1 до 15% масс., в частности от 1 до 10% масс., особенно предпочтительно от 2 до 5% масс. в пересчете на общую массу исходных мономеров. Согласно особому варианту осуществления настоящего изобретения часть эмульгаторов можно добавлять в процессе полимеризации.
Особенно пригодными являются анионные или неионные эмульгаторы или их смеси, к которым, в частности, относятся следующие соединения:
- алкилсульфаты, предпочтительно алкилсульфаты с 8-18 атомами углерода в алкильном остатке, а также алкилсульфоэфиры и алкиларилсульфоэфиры с 8-18 атомами углерода в алкильном остатке, содержащие от 1 до 50 этиленоксидных структурных единиц,
- сульфонаты, предпочтительно алкилсульфонаты с 8-18 атомами углерода в алкильном остатке, алкиларилсульфонаты с 8-18 атомами углерода в алкильном остатке, эфиры или кислые эфиры сульфоянтарной кислоты с одноатомными спиртами или алкилфенолами с 4-15 атомами углерода в алкильном остатке, причем указанные спирты или алкилфенолы при необходимости могут быть также этоксилированы посредством этиленоксида, используемого в количестве от 1 до 40 молей,
- неполные эфиры фосфорной кислоты и соответствующие соли щелочных металлов или аммония, предпочтительно алкилфосфаты и алкиларилфосфаты с 8-20 атомами углерода в алкильном, соответственно алкиларильном остатке, содержащие от 1 до 5 этиленоксидных структурных единиц,
- алкилполигликоли предпочтительно с 8-20 атомами углерода в алкильном остатке, содержащие от 8 до 40 этиленоксидных структурных единиц,
- алкиларилполигликоли предпочтительно с 8-20 атомами углерода в алкильном, соответственно алкиларильном остатке, содержащие от 8 до 40 этиленоксидных структурных единиц,
- сополимеры этиленоксида с пропиленоксидом, предпочтительно соответствующие блок-сополимеры, предпочтительно содержащие от 8 до 40 этиленоксидных или соответственно пропиленоксидных структурных единиц.
К особенно предпочтительным анионным эмульгаторам, в частности, относятся сульфоэфиры алифатических спиртов, диизооктилсульфосукцинат, лаурилсульфат и парафинсульфонат с 15 атомами углерода, причем указанные соединения в общем случае можно использовать в виде солей щелочных металлов, в частности в виде солей натрия. Указанные соединения являются коммерчески доступными продуктами, выпускаемыми фирмами Cognis GmbH, Cytec Industries, Inc. и BayerAG под торговыми названиями Disponil® FES 32, Aerosol® ОТ 75, Texapon® K1296 и Statexan® К1.
К используемым в целесообразном варианте неионным эмульгаторам относятся, в частности, трет-октилфенолэтоксилат с 30 этиленоксидными структурными единицами и простые эфиры на основе алифатических спиртов и полиэтиленгликоля предпочтительно с 8-20 атомами углерода в алкильном остатке, содержащие от 8 до 40 этиленоксидных структурных единиц. Указанные эмульгаторы являются коммерчески доступными продуктами, выпускаемыми под торговыми названиями Triton® X 305 (фирма Fluka), Tergitol® 15-S-7 (фирма Sigma-Aldrich Co.), Marlipal® 1618/25 (фирма Sasol, Германия) и Marlipal® O 13/400 (фирма Sasol, Германия).
В предпочтительном варианте можно использовать смеси анионных эмульгаторов с неионными эмульгаторами. Целесообразное массовое отношение анионного эмульгатора к неионному эмульгатору находится в интервале от 20:1 до 1:20, предпочтительно от 2:1 до 1:10, особенно предпочтительно от 1:1 до 1:5. При этом особенно предпочтительными являются смеси, которые в качестве анионного эмульгатора содержат сульфат, в частности сульфоэфир алифатического спирта, или лаурилсульфат, или сульфонат, в частности диизооктилсульфосукцинат или парафинсульфонат, а в качестве неионного эмульгатора алкилфенолэтоксилат или эфир на основе алифатического спирта и полиэтиленгликоля, соответственно предпочтительно содержащие от 8 до 20 атомов углерода в алкильном остатке и от 8 до 40 этиленоксидных структурных единиц.
Эмульгаторы при необходимости можно использовать также в смеси с защитными коллоидами. К пригодным защитным коллоидам относятся, в частности, частично гидролизованные поливинилацетаты, поливинилпирролидоны, карбоксиметилцеллюлоза, метилцеллюлоза, гидроксиэтилцеллюлоза, гидроксипропилцеллюлоза, крахмалы, белки, поли(мет)акриловая кислота, поли(мет)акриламид, поливинилсульфокислоты, меламинформальдегидсульфонаты, нафталинформальдегидсульфонаты, сополимеры стирола с малеиновой кислотой и сополимеры стирола с виниловыми эфирами малеиновой кислоты. В случае использования защитных коллоидов их количество в пересчете на общее количество мономеров предпочтительно составляет от 0,01 до 1,0% масс. Защитные коллоиды можно вводить в исходную смесь перед началом полимеризации или дозировать их в процессе полимеризации. Инициатор можно вводить перед началом полимеризации или дозировать в процессе полимеризации. Кроме того, перед началом полимеризации можно вводить часть инициатора, а остальное его количество можно добавлять в процессе полимеризации.
Полимеризацию предпочтительно инициируют путем нагревания исходной смеси до температуры полимеризации и ее подачи в реактор и/или путем дозирования инициатора предпочтительно в виде водного раствора. При этом в реактор можно ввести часть мономеров, а остальное количество добавлять по истечении определенного промежутка времени. Предпочтительным, как правило, является вариант, в соответствии с которым в реакторе полимеризуют введенную в него часть мономеров и лишь затем приступают к подаче мономеров. В соответствии с другим вариантом подачу мономеров можно прекратить на несколько минут, а затем добавить, например, от 1 до 5% мономеров. Дозирование эмульгатора и мономеров можно осуществлять по отдельности или предпочтительно в виде смеси, в частности в виде эмульсии в воде.
Эмульсионную полимеризацию можно осуществлять, варьируя показатель рН в широком диапазоне. Показатель рН при эмульсионной полимеризации предпочтительно находится в интервале от 2 до 9. В соответствии с особым вариантом осуществления изобретения полимеризацию осуществляют в диапазоне рН от 4 до 8, в частности от 6 до 8. Кроме того, показатель рН полученной в результате полимеризации дисперсии можно устанавливать в необходимом для ее конкретного применения предпочтительном интервале. В случае использования полученных дисперсий для изготовления пигментированных покровных систем их показатель рН в общем случае составляет от 8 до 9 или выше.
Молекулярная масса первоначально получаемых полимеров не является критическим параметром, и ее можно варьировать в широких пределах.
Для формирования особенно твердых и устойчивых к воздействию растворителей покровных средств с высоким уровнем механических свойств следует использовать полимеры, которые обладают максимально высокой молекулярной массой. Указанная выше технология эмульсионной полимеризации позволяет получать предпочтительные полимеры с высоким содержанием нерастворимых в тетрагидрофуране фракций. Условия полимеризации, которые следует использовать для синтеза полимеров с высокой молекулярной массой, известны специалистам. При этом, в частности, следует отказаться от использования регуляторов молекулярной массы.
Лаки, которые обладают особенно благоприятными технологическими свойствами, могут содержать также полимеры с более низкой молекулярной массой, и при этом может быть обеспечена относительно высокая устойчивость соответствующих покрытий к растворителям, а также высокая твердость. Полимеры с особенно высокой пригодностью для переработки могут обладать молекулярной массой менее 1000000 г/моль, предпочтительно менее 500000 г/моль и особенно предпочтительно менее 250000 г/моль. Молекулярную массу можно определять методом гель-проникающей хроматографии согласно стандарту Ассоциации изготовителей пластмасс.
Полимеры, которые обладают небольшой молекулярной массой, в частности полимеры, получаемые эмульсионной полимеризацией, можно синтезировать путем добавления к реакционной смеси регуляторов молекулярной массы до полимеризации или во время ее осуществления. При этом можно использовать не содержащие серу регуляторы молекулярной массы и/или серосодержащие регуляторы молекулярной массы.
К не содержащим серу регуляторам молекулярной массы относятся, например, димерный α-метилстирол (2,4-дифенил-4-метил-1-пентен), еноляты алифатических и/или циклоалифатических альдегидов, терпены, β-терпинен, терпинолы, 1,4-циклогексадиен, 1,4-дигидронафталин, 1,4,5,8-тетрагидронафталин, 2,5-дигидрофуран, 2,5-диметилфуран и/или 3,6-дигидро-2Н-пиран, предпочтительным из которых является димерный α-метилстирол, причем перечень возможных регуляторов молекулярной массы не ограничивается указанными выше соединениями.
В качестве серосодержащих регуляторов молекулярной массы предпочтительно можно использовать меркаптосоединения, диалкилсульфиды, диалкилдисульфиды и/или диарилсульфиды. Примерами пригодных регуляторов полимеризации подобного типа являются ди-н-бутилсульфид, ди-н-октилсульфид, дифенилсульфид, тиодигликоль, этилтиоэтанол, диизопропилдисульфид, ди-н-бутилдисульфид, ди-н-гексилдисульфид, диацетил-дисульфид, диэтанолсульфид, ди-трет-бутилтрисульфид и диметил-сульфоксид. Серосодержащими соединениями, предпочтительно используемыми в качестве регуляторов молекулярной массы, являются меркаптосоединения, диалкилсульфиды, диалкилдисульфиды и/или диарилсульфиды. Примерами подобных соединений являются этилтиогликолят, 2-этилгексилтиогликолят, цистеин, 2-меркаптоэтанол, 1,3-меркаптопропанол, 3-меркаптопропан-1,2-диол, 1,4-меркаптобутанол, меркаптоуксусная кислота, 3-меркаптопропионовая кислота, меркаптоянтарная кислота, тиоглицерин, тиоуксусная кислота, тиокарбамид, а также алкилмеркаптаны, такие как н-бутилмеркаптан, н-гексилмеркаптан или н-додецилмеркаптан. Особенно предпочтительно используемыми серосодержащими регуляторами полимеризации являются меркаптоспирты и меркаптокарбоновые кислоты.
Регуляторы молекулярной массы предпочтительно используют в количествах от 0,05 до 10% масс., особенно предпочтительно от 0,1 до 5% масс. в пересчете на подлежащие полимеризации мономеры. Для полимеризации, очевидно, можно использовать также смеси регуляторов молекулярной массы.
Кроме того, полимеризацию можно осуществлять с использованием регуляторов молекулярной массы, предназначенных для снижения минимальной температуры пленкообразования синтезируемых в их присутствии полимеров. В соответствии с подобным предпочтительным вариантом осуществления изобретения содержание регуляторов молекулярной массы может быть рассчитано таким образом, чтобы минимальная температура пленкообразования полимеров или соответственно предлагаемых в изобретении покровных средств, составляла не более 60°С, особенно предпочтительно не более 50°С и еще более предпочтительно не более 40°С (указанная температура может быть измерена согласно DIN ISO 2115). Чем выше содержание регулятора молекулярной массы, тем ниже минимальная температура пленкообразования.
Размер полимерных частиц можно регулировать, в частности, путем варьирования содержания эмульгаторов. Чем выше содержание эмульгатора, в особенности в начале полимеризации, тем меньше размер получаемых частиц.
Другим объектом настоящего изобретения являются полимеры, которые могут быть получены описанным выше способом, предпочтительно полимеры, которые могут быть получены путем эмульсионной полимеризации.
При этом предпочтительными являются несшитые продукты эмульсионной полимеризации или соответствующие слабосшитые полимеры, которые в пересчете на массу содержат свыше 60% масс. растворимых при 20°С в тетрагидрофуране фракций. В соответствии с другим предпочтительным вариантом осуществления изобретения получаемые эмульсионной полимеризацией полимеры могут содержать от 2 до 60% масс., особенно предпочтительно от 10 до 50% масс., еще более предпочтительно от 20 до 40% масс. растворимых при 20°С в тетрагидрофуране фракций (в пересчете на массу полимера). С целью определения содержания растворимых фракций образец полимера, подвергнутый сушке в исключающей доступ кислорода атмосфере, в течение 4 часов хранят при 20°С в 200-кратном избытке растворителя (в пересчете на массу образца). С целью исключения доступа кислорода образец сушат, например, в атмосфере азота или под вакуумом. Затем раствор отделяют от не растворившегося остатка, например, путем фильтрования. После испарения растворителя определяют массу остатка. Так, например, образец полученного эмульсионной полимеризацией и подвергнутого сушке под вакуумом полимера массой 0,5 г можно в течение 4 часов выдерживать в 150 мл тетрагидрофурана.
В соответствии с предпочтительным вариантом осуществления изобретения степень набухания получаемого эмульсионной полимеризацией полимера в тетрагидрофуране при 20°С может составлять по меньшей мере 800%, особенно предпочтительно по меньшей мере 1200% и еще более предпочтительно по меньшей мере 1300%. Верхнее предельное значение степени набухания не является критическим параметром и предпочтительно не превышает 5000%, особенно предпочтительно не превышает 3000%, еще более предпочтительно не превышает 2500%. Для определения степени набухания образец полимера, подвергнутый предварительной сушке без доступа кислорода, в течение 4 часов выдерживают при 20°С в 200-кратном избытке растворителя (в пересчете на массу образца). В течение указанного промежутка времени происходит набухание образца. Набухший образец отделяют от избыточного растворителя. Затем из образца удаляют растворитель. Основная часть растворителя может быть удалена из образца, например, путем испарения при комнатной температуре (20°С). Остаточный растворитель может быть удален путем сушки полимерного образца в сушильном шкафу (140°С), длительность которой в общем случае не превышает одного часа. Степень набухания вычисляют в виде разности между массой образца с поглощенным растворителем и массой сухого образца. Кроме того, по разности между массой образца перед осуществлением опыта по определению степени набухания и массой образца, подвергнутого сушке по завершении указанного опыта, можно установить содержание растворимых фракций в получаемом эмульсионной полимеризацией полимере.
Размер частиц получаемых эмульсионной полимеризацией полимеров, подлежащих использованию согласно изобретению, можно варьировать в широком диапазоне. Так, например, особенно пригодными являются получаемые эмульсионной полимеризацией полимеры, радиус частиц которых находится в интервале от 10 до 500 нм, предпочтительно от 10 до 100 нм, особенно предпочтительно от 20 до 60 нм. Радиус частиц полимера, особенно благоприятный в отношении пленкообразования и свойств соответствующих покрытий, предпочтительно может составлять менее 50 нм. Радиус частиц можно определять методом фотон-корреляционной спектроскопии, причем указанные выше данные относятся к показателю d50, при котором 50% частиц обладают размером меньше указанного, а 50% размером больше указанного. Для измерения радиуса частиц можно использовать, например, анализатор размеров субмикронных частиц Beckman Coulter N5.
Температура стеклования предлагаемых в изобретении полимеров предпочтительно составляет от - 30 до 70°С, особенно предпочтительно от - 20 до 40°С и еще более предпочтительно от 0 до 25°С. Температура стеклования указанных полимеров зависит от типа используемых для их получения мономеров и содержания соответствующих мономерных звеньев. При этом температуру стеклования Tg полимеров можно определять известным методом дифференциальной сканирующей калориметрии (ДСК). Кроме того, температуру стеклования Tg можно приближенно рассчитать по уравнению Фокса (Fox T.G., Bull. Am. Physics Soc. 1, 3, с.123, 1956):
,
в котором xn означает массовую долю мономера n (в % масс./100) и Tgn означает температуру стеклования гомополимера на основе мономера n (в градусах Кельвина). Другие вспомогательные данные специалисты могут найти в справочнике Polymer Handbook, 2-е издание, издательство J.Wiley & Sons, Нью-Йорк (1975), в котором приведены температуры стеклования Tg наиболее употребительных гомополимеров. При этом тот или иной полимер может обладать одной или несколькими разными температурами стеклования. Таким образом, соответствующие данные относятся к сегменту, который может быть получен в результате полимеризации по меньшей мере одного (мет)акрилатного мономера формулы (I), предпочтительно предлагаемой в изобретении смеси мономеров.
Структура полимера для многих сфер его использования и свойств не является критическим параметром. В соответствии с этим полимеры, в частности полимеры, получаемые эмульсионной полимеризацией, могут являться статистическими сополимерами, градиентными сополимерами, блок-сополимерами и/или привитыми сополимерами. Блок-сополимеры, соответственно градиентные сополимеры, могут быть получены, например, благодаря изменению состава мономеров, периодически осуществляемому в процессе роста полимерных цепей. В соответствии с предпочтительным вариантом осуществления изобретения получаемый эмульсионной полимеризацией полимер является статистическим сополимером, при получении которого состав мономеров остается преимущественно неизменным. Однако поскольку мономеры могут обладать разными параметрами сополимеризации, состав мономерных звеньев вдоль полимерной цепи может колебаться.
Полимер может являться однородным полимером, который, например, в водной дисперсии может образовывать частицы неизменного состава. В подобном случае получаемый предпочтительно эмульсионной полимеризацией полимер может состоять, например, из одного или нескольких сегментов, которые могут образоваться в результате полимеризации по меньшей мере одного (мет)акрилатного мономера формулы (I), предпочтительно смеси мономеров, предлагаемой в изобретении.
Согласно другому варианту осуществления изобретения получаемый эмульсионной полимеризацией полимер может обладать структурой типа «ядро-оболочка» и может содержать одну, две, три или более оболочек. При этом сегмент, который образуется в результате полимеризации предлагаемой в изобретении смеси мономеров или (мет)акрилатного мономера формулы (I), предпочтительно образует самую внешнюю оболочку полимера со структурой типа «ядро-оболочка». Указанная внешняя оболочка может быть соединена с ядром или внутренними оболочками полимера посредством ковалентных связей. Кроме того, указанная оболочка может быть также сополимеризована с ядром или внутренней оболочкой. В соответствии с подобным вариантом осуществления изобретения сегмент, который может быть получен, в частности, путем полимеризации предлагаемой в изобретении смеси мономеров, нередко можно отслоить от ядра и выделить с помощью соответствующего растворителя.
Массовое отношение сегмента, который может образоваться в результате полимеризации предлагаемой в изобретении смеси мономеров или (мет)акрилатного мономера формулы (I), к ядру предпочтительно находится в интервале от 6:1 до 1:6. В случае, если температура стеклования ядра превышает температуру стеклования оболочки, указанное массовое отношение составляет от 6:1 до 2:1, тогда как в случае обратного соотношения между температурами стеклования указанное массовое отношение особенно предпочтительно находится в интервале от 1:1 до 1:5.
Ядро предпочтительно может быть образовано полимером, содержащим от 50 до 100% масс., предпочтительно от 60 до 90% масс. мономерных звеньев (мет)акрилата. Предпочтительными являются мономерные звенья в виде сложных эфиров (мет)акриловой кислоты, спиртовой остаток которых предпочтительно содержит от 1 до 30 атомов углерода, особенно предпочтительно от 1 до 20 атомов углерода, еще более предпочтительно от 1 до 10 атомов углерода. К подобным мономерам, в частности, относятся (мет)акрилаты на основе насыщенных спиртов, такие как метил-(мет)акрилат, этил(мет)акрилат, н-пропил(мет)акрилат, изопропил(мет)-акрилат, н-бутил(мет)акрилат, трет-бутил(мет)акрилат, пентил(мет)-акрилат и гексил(мет)акрилат.
В соответствии с особым вариантом осуществления настоящего изобретения для формирования ядра можно использовать смесь, состоящую из метакрилатов и акрилатов. Так, например, в частности, можно использовать смеси, состоящие из метилметакрилата и акрилатов с 2-6 атомами углерода, таких как этилакрилат, бутилакрилат или гексилакрилат.
Кроме того, образующие ядро полимеры могут содержать звенья указанных выше сомономеров. Согласно предпочтительному варианту осуществления изобретения ядро может быть сшитым. При этом сшивание ядра может быть обеспечено благодаря использованию мономеров с двумя, тремя или более способными к радикальной полимеризации двойными связями.
Оболочка из полимера, получаемого в результате эмульсионной полимеризации предлагаемой в изобретении смеси мономеров, предпочтительно может содержать от 2 до 50% масс. мономерных звеньев (мет)акрилатных мономеров формулы (I).
В соответствии с особым вариантом осуществления настоящего изобретения температура стеклования ядра предпочтительно может составлять от -30 до 200°С, особенно предпочтительно от -20 до 150°С. Температура стеклования ядра особенно предпочтительно составляет более 50°С, в частности более 100°С. Температура стеклования оболочки из предлагаемого в изобретении полимера, который предпочтительно может быть получен эмульсионной полимеризацией предлагаемой в изобретении смеси мономеров, предпочтительно может составлять от -30 до 70°С, особенно предпочтительно от - 20 до 40°С и еще более предпочтительно от 0 до 25°С. Согласно особому варианту осуществления настоящего изобретения температура стеклования ядра превышает температуру стеклования оболочки. В целесообразном варианте температура стеклования ядра превышает температуру стеклования оболочки по меньшей мере на 10°С, предпочтительно по меньшей мере на 20°С.
Неожиданных преимуществ удается достичь в том случае, если йодное число предлагаемых в изобретении полимеров, измеренное согласно DIN 53241-1, предпочтительно находится в интервале от 0,1 до 300 г йода на 100 г полимера, особенно предпочтительно в интервале от 1 до 270 г йода на 100 г полимера и еще более предпочтительно от 5 до 250 г йода на 100 г полимера. Для измерения йодного числа, в частности, можно использовать также образцы предлагаемой в изобретении дисперсии.
Кислотное число полимеров в целесообразном варианте находится в интервале от 0 до 50 мг КОН/г, преимущественно от 0,1 до 40 мг КОН/г, предпочтительно от 1 до 20 мг КОН/г и еще более предпочтительно от 2 до 10 мг КОН/г. Кислотное число можно определять также согласно DIN EN ISO 2114, используя образцы дисперсии.
Гидроксильное число полимеров преимущественно находится в интервале от 0 до 200 мг КОН/г, особенно предпочтительно от 1 до 100 мг КОН/г и еще более предпочтительно от 3 до 50 мг КОН/г. Гидроксильное число можно определять также согласно DIN EN ISO 4629, используя образцы дисперсии.
Полимеры, получаемые полимеризацией (мет)акрилатного мономера формулы (I) или предлагаемой в изобретении смеси мономеров, можно выделять из продуктов полимеризации. Согласно особому варианту осуществления настоящего изобретения в качестве покровного средства можно использовать также получаемые эмульсионной полимеризацией дисперсии как таковые.
Объектом настоящего изобретения являются также покровные средства, которые содержат указанные выше полимеры или соединения, получаемые в результате реакций с указанными выше (мет)акрилатными мономерами. Под покровными средствами согласно изобретению подразумевают составы, которые пригодны для нанесения на соответствующие основы. Предлагаемые в изобретении покровные средства можно сшивать посредством сшивающего агента. Наряду с этим предпочтительные покровные средства обладают склонностью к самопроизвольному сшиванию. Сшитые пленки нередко отличаются высокой устойчивостью к действию растворителей. Особенно предпочтительные покровные средства обладают способностью к окислительному сшиванию, в связи с чем при воздействии кислорода из них образуются сшитые пленки. Окислительно сшиваемые покровные средства предпочтительно содержат полимеры с ненасыщенными боковыми цепями, которые, в частности, могут быть получены благодаря использованию мономеров формулы (III) или мономеров формулы (I), остаток R2 которых дополнительно содержит углерод-углеродные двойные связи.
Помимо покровных средств, содержащих указанные выше полимеры, хорошо пригодными являются также покровные средства на основе алкидных смол, которые могут быть модифицированы предлагаемыми в изобретении (мет)акрилатными мономерами или предлагаемыми в изобретении смесями мономеров. При этом под модифицированными алкидными смолами подразумевают алкидные смолы, содержащие одну или несколько структурных единиц или повторяющихся структурных единиц, которые являются производными (мет)акрилатных мономеров формулы (I). Кроме того, согласно изобретению модифицированными называют также алкидные смолы или дисперсии алкидных смол, которые содержат указанные выше полимеры.
Алкидные смолы давно известны, причем в общем случае под ними подразумевают продукты конденсации многоосновных карбоновых кислот и многоатомных спиртов, которые в общем случае модифицируют длинно-цепными спиртами (алифатическими спиртами) и жирными кислотами, соответственно содержащими жирные кислоты соединениями, например, жирами или маслами (DIN 55945, 1968). Информация об алкидных смолах приведена, например, в 5-м издании Ullmann's Encyclopedia of Industrial Chemistry (запись на CD-ROM). Помимо указанных выше классических алкидных смол можно использовать также смолы, которые обладают аналогичными свойствами. Подобные смолы также отличаются высоким содержанием групп, являющихся производными указанных выше длинно-цепных спиртов (алифатических спиртов) и жирных кислот, соответственно содержащих жирные кислоты соединений, например, жиров или масел. Однако подобные смолы не обязательно основаны на многоосновных карбоновых кислотах, а могут быть получены, например, путем взаимодействия многоатомных спиртов с изоцианатами. Используемые алкидные смолы предпочтительно можно смешивать с водой или разбавлять водой.
К предпочтительным многоосновным карбоновым кислотам, предназначенным для получения алкидных смол, подлежащих предпочтительному использованию в предлагаемой в изобретении дисперсии, относятся, в частности, дикарбоновые и трикарбоновые кислоты, например, такие как фталевая кислота, изофталевая кислота, 5-(натрийсульфо)изофталевая кислота, терефталевая кислота, тримеллитовая кислота, 1,4-циклогексан-дикарбоновая кислота, адипиновая кислота, малеиновая кислота, фумаровая кислота, себациновая кислота, адипиновая кислота или азелаиновая кислота. Указанные кислоты можно использовать для получения алкидных смол также в виде ангидридов. Для получения алкидных смол особенно предпочтительно используют ароматические дикарбоновые кислоты. Содержание многоосновных карбоновых кислот в пересчете на массу исходных продуктов, используемых в реакционной смеси для получения смолы, предпочтительно находится в интервале от 2 до 50% масс., особенно предпочтительно в интервале от 5 до 40% масс.
Кроме того, для получения алкидных смол используют многоатомные спирты. К пригодным спиртам относятся, в частности, триметилолпропан, пентаэритрит, дипентаэритрит, триметилолэтан, неопентилгликоль, этиленгликоль, 1,3-бутандиол, 1,4-бутандиол, 1,6-гександиол, 1,4-циклогексилдиметанол, диэтиленгликоль, триэтиленгликоль, полиэтиленгликоль, политетрагидрофуран, поликапролактондиол, поликапролактонтриол, простой триметилолмоноаллиловый эфир, простой триметилолдиаллиловый эфир, простой триаллиловый эфир пентаэритрита, простой диаллиловый эфир пентаэритрита, простой моноаллиловый эфир пентаэрита, 2-этил-2-(гидроксиметил)-1,3-пропандиол, 2-метил-1,3-пропандиол, 2,2,4-триметилпентандиол, 2,2,4-триметил-1,3-пентандиол, 2,2'-бис(4-гидроксициклогексил)пропан (гидрированный бисфенол А), пропиленгликоль, дипропиленгликоль, полипропиленгликоль, глицерин и сорбит. Предпочтительными многоатомными спиртами, в частности, являются триметилолэтан, триметилолпропан, пентаэритрит и сорбит. Согласно особому варианту предпочтительными, в частности, являются спирты с тремя или более гидроксильными группами. Содержание многоатомных спиртов в пересчете на массу исходных продуктов, используемых в реакционной смеси для получения смолы, предпочтительно находится в интервале от 2 до 50% масс., особенно предпочтительно в интервале от 5 до 40% масс.
Наряду с этим для получения указанных выше алкидных смол, в частности, можно использовать жирные кислоты. В частности, можно использовать насыщенные и ненасыщенные жирные кислоты, причем предпочтительными, в частности, являются содержащие ненасыщенные жирные кислоты смеси. Предпочтительные жирные кислоты содержат от 6 до 30 атомов углерода, особенно предпочтительно от 10 до 26 атомов углерода, еще более предпочтительно от 12 до 22 атомов углерода. Содержание жирных кислот в пересчете на массу исходных продуктов, используемых в реакционной смеси для получения смолы, предпочтительно находится в интервале от 2 до 90% масс., особенно предпочтительно в интервале от 10 до 70% масс.
К пригодным насыщенным жирным кислотам относятся, в частности, каприловая кислота, каприновая кислота, лауриновая кислота, миристиновая кислота, пальмитиновая кислота, маргариновая кислота, арахиновая кислота, бегеновая кислота, лигноцериновая кислота, церотиновая кислота, пальмитоловая кислота и стеариновая кислота.
К предпочтительным ненасыщенным жирным кислотам относятся, в частности, ундециленовая кислота, пальмитолеиновая кислота, олеиновая кислота, элаидиновая кислота, вакценовая кислота, икозеновая кислота, цетолеиновая кислота, эруковая кислота, нервоновая кислота, линолевая кислота, линоленовая кислота, арахидоновая кислота, тимнодоновая кислота, клупанодоновая кислота и/или цервоновая кислота.
Кроме того, указанные выше жирные кислоты можно использовать также в виде соответствующих сложных эфиров, например, в виде триглицеридов.
Указанные выше алкидные смолы могут содержать также другие компоненты. К другим компонентам относятся, например, одноосновные карбоновые кислоты, одноатомные спирты или соединения, которые способствуют образованию в алкидных смолах эмульгирующихся групп, например, такие как полиэтиленоксиды. Кроме того, алкидные смолы могут содержать гидроксикарбоновые кислоты, например, такие как 2-гидроксибензойная кислота, 3-гидроксибензойная кислота, 4-гидроксибензойная кислота, рицинолевая кислота, дигидроксипропионовая кислота, дигидроксиянтарная кислота, дигидроксибензойная кислота, 2,2-диметилолуксусная кислота, 2,2-диметилолпропионовая кислота, 2,2-диметилолмасляная кислота или 2,2-диментилолпентановая кислота.
Помимо указанных выше можно использовать также алкидные смолы, модифицированные другими смолами, в частности канифолью, полимерами стирола, акриловыми полимерами, эпоксидами, уретанами, полиамидами и/или силиконами. Подобные модифицированные алкидные смолы приведены, в частности, в цитированной выше патентной литературе, а также в 5-м издании Ullmann's Encyclopedia of Industrial Chemistry (в записи на CD-ROM). Благодаря подобному модифицированию, в частности, можно варьировать подсушку, адгезионную прочность, атмосферостойкость, пригодность к хранению, устойчивость к химикатам, полное отверждение, стабильность влажной пленки и сопротивление истиранию.
Так, например, предпочтительно можно использовать алкидные смолы, модифицированные полимерами, которые могут быть получены путем радикальной полимеризации. Указанные смолы известны, в частности, из патентов US 5538760 и US 6369135, а также из немецкой заявки на патент DE-A-19957161. Указанные в описании патента US 5538760 (соответствующая заявка зарегистрирована Бюро по патентам и товарным знакам США 22.05.95 под номером 446130) смолы включены посредством данной ссылки в описание настоящего изобретения. А также представленные в описании патента US 6369135 B1 (соответствующая заявка зарегистрирована Бюро по патентам и товарным знакам США 13.08.96 под номером 08/696 361) смолы включены посредством данной ссылки в описание настоящего изобретения. Кроме того, в описание настоящего изобретения включены посредством данной ссылки смолы, указанные в описании немецкой заявки на патент DE-A-199 57161, зарегистрированной Немецким бюро по патентам и товарным знакам 27.11.99 под номером DE 19957161.9.
Согласно патентам US 5538760 и US 6369135 модифицированные алкидные смолы можно получать, в частности, путем полимеризации смеси мономеров, осуществляемой в присутствии алкидной смолы. При этом массовое отношение смеси мономеров к алкидной смоле предпочтительно находится в интервале от 100:1 до 1:4, предпочтительно в интервале от 5:1 до 1:1.
В частности, особенно целесообразным является использование модифицированных акрилатами алкидных смол, описанных в немецкой заявке на патент DE-A-19957161. Помимо алкидного ядра указанные алкидные смолы содержат группы, получаемые путем полимеризации (мет)акрилатов.
Подобные модифицированные акрилатами алкидные смолы можно получать тем, что в присутствии по меньшей мере одного смешивающегося с водой диола:
(1) по меньшей мере одну алкидную смолу, которая в пересчете на ее общее количество содержит от 0,1 до 10% масс. боковых и/или концевых аллилоксильных групп, диспергируют в воде, получая дисперсию 1,
(2) в полученной дисперсии 1 реализуют привитую сополимеризацию смеси метакриловой кислоты по меньшей мере с одним другим олефинненасыщенным мономером, не содержащим групп карбоновой кислоты, получая дисперсию 2, и
(3) в дисперсии 2 или дисперсии от 2 до n-1, соответственно полученной на предшествующей технологической стадии (2) или от (2) до (n-1), однократно или n-кратно осуществляют привитую сополимеризацию:
(3.1) по меньшей мере одного не содержащего кислотных групп олефинненасыщенного мономера и/или
(3.2) по меньшей мере одной смеси, состоящей по меньшей мере из одного содержащего кислотные группы олефинненасыщенного мономера и по меньшей мере одного не содержащего кислотных групп олефинненасыщенного мономера,
при условии, что на технологической стадии (3) или одной из технологических стадий от (3) до (n) в полимерные цепи вводят кислотные группы, суммарное количество которых не превышает 90% мол. от количества введенных на технологической стадии (2) кислотных групп.
Содержание указанных выше боковых и/или концевых аллилоксигрупп в алкидной смоле может составлять от 0,1 до 10% масс., преимущественно от 0,2 до 9% масс., предпочтительно от 0,3 до 8% масс., особенно предпочтительно от 0,4 до 7% масс., еще более предпочтительно от 0,5 до 6% масс., в частности от 0,6 до 5% масс. соответственно в пересчете на алкидную смолу. Атом кислорода в аллилоксигруппе может являться компонентом уретановой группы, сложноэфирной группы или группы простого эфира, которая соединяет аллильный остаток с основной цепью алкидной смолы.
Примерами соединений, пригодных для введения боковых и/или концевых аллилоксигрупп, являются аллиловый спирт, простой 2-гидроксиэтилаллиловый эфир, простой 3-гидроксипропилаллиловый эфир, простой триметилолпропанмоноаллиловый эфир, простой триметилолпропандиаллиловый эфир, простой моноаллиловый эфир глицерина, простой диаллиловый эфир глицерина, простой моноаллиловый эфир пентаэритрита, простой диаллиловый эфир пентаэритрита, простой триаллиловый эфир пентаэритрита, простой моноаллиловый эфир маннита, простой диаллиловый эфир маннита, простой триаллиловый эфир маннита, простой тетрааллиловый эфир маннита, сложный аллиловый эфир дигидроксипропионовой кислоты, сложный аллиловый эфир дигидроксиянтарной кислоты, сложный аллиловый эфир дигидроксибензойной кислоты, сложный аллиловый эфир 2,2-диметилолуксусной кислоты, сложный аллиловый эфир 2,2-диметилолпропионовой кислоты, сложный аллиловый эфир 2,2-диметилолмасляной кислоты, сложный аллиловый эфир 2,2-диментилолпентановой кислоты или аллилуретан, предпочтительным из которых является простой моноаллиловый эфир триметилолпропана. С целью выполняемого на стадии (2) модифицирования алкидной смолы акрилатами можно осуществлять привитую сополимеризацию дисперсии 1 с метакриловой кислотой и по меньшей мере одним другим олефинненасыщенным мономером. Другие олефинненасыщенные мономеры наряду с олефиновыми двойными связями могут содержать помимо карбоксильных групп другие реакционно-способные функциональные группы, например, группы, реакционно-способные по отношению к изоцианатам, карбаматам, N-метилолу, простым эфирам N-метилола или алкоксикарбониламино. Важным обстоятельством при этом является отсутствие взаимодействия указанных реакционно-способных функциональных групп в данных реакционных условиях и при последующем хранении предлагаемых в изобретении дисперсий с карбоксильными группами метакриловой кислоты или другими при необходимости присутствующими реакционно-способными функциональными группами. Примером реакционно-способных функциональных групп, удовлетворяющих указанным требованиям, являются гидроксильные группы. Указанные мономеры являются известными соединениями (смотри приведенные в немецком патенте DE 19957161 примеры). К ним, в частности, относятся сложные гидроксиалкиловые эфиры акриловой кислоты, метакриловой кислоты или одной из других α,β-олефинненасыщенных карбоновых кислот, а также сложные эфиры акриловой кислоты, метакриловой кислоты, кротоновой кислоты или этакриловой кислоты, содержащие до 20 атомов углерода в алкильном остатке.
Кроме того, предпочтительными являются алкидные смолы, которые могут быть получены в соответствии с патентом US 5096959. Представленные в описании патента US 5096959 B1 (соответствующая заявка зарегистрирована Бюро по патентам и товарным знакам США 30.10.90 под номером 609024) смолы включены посредством данной ссылки в описание настоящего изобретения. Указанные алкидные смолы модифицированы циклоалифатической поликарбоновой кислотой, причем для модифицирования, в частности, пригодны циклогександикарбоновые и циклопентандикарбоновые кислоты.
Можно использовать также алкидные смолы, модифицированные полиэтиленгликолем. Получение эмульгируемых в воде алкидных смол путем модифицирования полиэтиленгликолем описано во многих патентных публикациях. При этом в большинстве случаев непосредственно в алкидную смолу путем переэтерификации или этерификации вводят примерно от 10 до 30% полиэтиленгликоля (смотри, например, патенты US 2634245, US 2853459, US 3133032, US 3223659, US 3379548, US 3437615, US 3437618, US 3442835, US 3457206 и US 3639315, выкладное описание к немецкой заявке на патент 1495032, а также описания патентов Великобритании №1038696 и №1044821).
Предпочтительные модифицированные полиэтиленгликолем алкидные смолы известны, в частности, из европейской заявки на патент ЕР-А 0029145. Представленные в описании указанной заявки, зарегистрированной Европейским патентным ведомством 30.10.80 под номером ЕР 80106672.1, смолы включены посредством данной ссылки в описание настоящего изобретения Согласно заявке ЕР-А 0029145. Сначала можно осуществлять взаимодействие полиэтиленгликоля с содержащей эпоксидные группы карбоновой кислотой. Затем полученный продукт можно вводить в реакционную смесь для синтеза алкидной смолы. Среднечисловая молекулярная масса полиэтиленгликолей, предпочтительно используемых для модифицирования алкидных смол, находится, например, в интервале от 500 до 5000 г/моль.
Кроме того, особенно предпочтительные модифицированные полиэтиленгликолем алкидные смолы могут быть модифицированы сополимерами, получаемыми путем полимеризации метакриловой кислоты, ненасыщенных жирных кислот и виниловых и/или винилиденовых соединений.
Целесообразным является также использование алкидных смол, модифицированных уретановыми группами. Подобные модифицированные алкидные смолы приведены, в частности, в международной заявке WO 2006/092211 и европейской заявке на патент ЕР-А 1533342.
Согласно целесообразному варианту осуществления настоящего изобретения можно использовать описанные в европейской заявке на патент ЕР-А 1533342 уретаналкидные смолы, которые содержат структурные элементы, производные ненасыщенных жирных кислот А1, не содержащих олефиновые двойные связи алифатических, ароматических или ароматических/алифатических монокарбоновых кислот А2, циклоалифатических дикарбоновых кислот A3 или их ангидридов, по меньшей мере трехатомных, предпочтительно по меньшей мере четырехатомных спиртов А4, и ароматических или алифатических полифункциональных, в частности бифункциональных изоцианатов А5. Уретаналкидную смолу предпочтительно получают в соответствии с двухстадийной реакцией, на первой стадии которой осуществляют этерификацию компонентов от А1 до А4, причем кислотное число образующегося на первой стадии продукта реакции предпочтительно не превышает 10 мг/г, особенно предпочтительно не превышает 5 мг/г. На второй стадии содержащий гидроксильные группы продукт первой стадии подвергают сопровождаемому ростом молекулярной массы взаимодействию с изоцианатом А5, которое осуществляют при добавлении незначительного количества третичного амина (до 1%, предпочтительно до 0,5% в пересчете на массу продукта первой стадии). Показатель вязкости Штаудингера предпочтительных уретаналкидных смол, измеренный в хлороформе при 23°С, составляет по меньшей мере 9 см3/г, предпочтительно по меньшей мере 11 с м3/г.
Раскрытые в описании европейской заявки на патент ЕР-А 1533342, зарегистрированной Европейским патентным ведомством 09.11.04 под номером ЕР 04026511.8 смолы посредством данной ссылки включены в описание настоящего изобретения.
Предпочтительному использованию подлежат уретаналкидные смолы, которые могут быть получены путем взаимодействия многоатомных спиртов А', модифицированных жирных кислот В', жирных кислот С' и полифункциональных изоцианатов D'. Модифицированные жирные кислоты В' могут быть получены путем взаимодействия ненасыщенных жирных кислот В1' с ненасыщенными карбоновыми кислотами В2'. Указанные уретаналкиды известны, в частности, из международной заявки WO 2006/092211. Раскрытые в описании указанной заявки, зарегистрированной Европейским патентным ведомством 20.02.06 под номером РСТ/ЕР 2006/001503, смолы посредством данной ссылки включены в описание настоящего изобретения. Кислотное число модифицированной жирной кислоты В' предпочтительно составляет по меньшей мере 80 мг/г. Обусловленное прививкой увеличение кислотного числа особенно предпочтительно составляет от 80 до 250 мг/г и еще более предпочтительно от 100 до 150 мг/г, причем кислотное число может быть определено согласно стандарту DIN EN ISO 2114. Йодное число жирных кислот С', используемых для получения уретаналкидных смол, преимущественно составляет по меньшей мере 80 г/100 г, предпочтительно по меньшей мере 120 г/100 г. Для получения описанной в международной заявке WO 2006/092211 уретаналкидной смолы в общем случае сначала осуществляют взаимодействие компонентов А', В' и С', причем гидроксильная функциональность продукта соответствующей конденсации предпочтительно составляет по меньшей мере 1,9, особенно предпочтительно по меньшей мере 2. Кроме того, продукт конденсации может содержать группы, производные многоосновных карбоновых кислот, в частности указанных выше дикарбоновых и трикарбоновых кислот. Полученный конденсат подвергают взаимодействию с полифункциональным изоцианатом. К предпочтительным полифункциональным изоцианатам относятся, в частности, 2,4-толуилендиизоцианат, 2,6-толуилендиизоцианат и их технические смеси, бис(4-изоцианатофенил)метан, изофорондиизоцианат, бис(4-изоцианатоциклогексил)метан, 1,6-диизоцианатогексан, а также изоцианураты, аллофанаты и биуреты, являющиеся производными указанных выше изоцианатов.
Помимо указанных выше классических алкидных смол, для получения которых в общем случае используют поликарбоновые кислоты, можно использовать также другие указанные выше алкидные смолы. К последним относятся, в частности, алкидные смолы на основе уретанов. Подобные уретаналкидные смолы могут быть получены, например, путем взаимодействия многоатомных спиртов с полифункциональными изоцианатами. Предпочтительные уретаналкидные смолы известны, например, из европейской заявки на патент ЕР-А 1129147. Они могут быть получены, например, путем взаимодействия сложных амидоэфирдиолов с многоатомными спиртами и полифункциональными изоцианатами. Сложные амидоэфирдиолы, подлежащие использованию согласно цитируемой заявке, могут быть получены путем взаимодействия растительных масел с N,N-диалканоламинами.
В соответствии с предпочтительным вариантом осуществления настоящего изобретения определяемое согласно DIN 53241 йодное число алкидной смолы может составлять по меньшей мере 1 г йода на 100 г смолы, предпочтительно по меньшей мере 10 г йода на 100 г смолы, особенно предпочтительно по меньшей мере 15 г йода на 100 г смолы. Согласно особому варианту осуществления изобретения йодное число алкидной смолы может составлять от 2 до 100 г йода на 100 г смолы, особенно предпочтительно от 15 до 50 г йода на 100 г смолы. Йодное число можно определять для находящейся в виде дисперсии алкидной смолы, причем результат определения относится к содержанию твердого вещества в подобной дисперсии.
В целесообразном варианте кислотное число алкидной смолы может составлять от 0,1 до 100 мг КОН/г, предпочтительно от 1 до 40 мг КОН/г, еще более предпочтительно от 2 до 10 мг КОН/г. Кислотное число может быть определено согласно стандарту DIN EN ISO 2114 для алкидной смолы, находящейся в виде дисперсии, причем результат соответствующего определения относится к содержанию твердого вещества в подобной дисперсии.
Гидроксильное число алкидной смолы предпочтительно может находиться в интервале от 0 до 400 мг КОН/г, особенно предпочтительно от 1 до 200 мг КОН/г, еще более предпочтительно от 3 до 150 мг КОН/г. Гидроксильное число может быть определено согласно стандарту DIN EN ISO 4629 для алкидной смолы, находящейся в виде дисперсии, причем результат соответствующего определения относится к содержанию твердого вещества в подобной дисперсии.
Получение алкидных смол осуществляют давно известными методами, предусматривающими конденсацию указанных выше спиртов и кислот, причем модифицирование алкидных смол можно осуществлять как в процессе конденсации, так и по ее завершении. В этой связи, в частности, следует сослаться на цитированную выше литературу.
Указанные выше алкидные смолы, не подвергая модифицированию, можно использовать в предлагаемых в изобретении покровных средствах совместно с предлагаемыми в изобретении полимерами. Модифицирование алкидных смол предпочтительно можно осуществлять путем полимеризации (мет)акрилатного мономера формулы (I) или предлагаемой в изобретении смеси мономеров, причем исчерпывающая информация относительно осуществления реакции может быть взята помимо прочего из европейской заявки на патент ЕР-А-0083137, причем приведенные в указанной заявке, зарегистрированной Европейским патентным ведомством 21.12.1987 под номером 82201642.4, реакционные условия и алкидные смолы посредством данной ссылки включены в описание настоящего изобретения.
Предлагаемое в изобретении покровное средство предпочтительно содержит лишь незначительное количество опасных для окружающей среды растворителей, причем особенно предпочтительные покровные средства являются водными дисперсиями. Содержание твердых веществ в подобных водных дисперсиях предпочтительно составляет от 10 до 70% масс., особенно предпочтительно от 20 до 60% масс. Динамическую вязкость дисперсий, которая зависит от содержания твердых веществ и размера полимерных частиц, можно варьировать в широких пределах. Так, например, динамическая вязкость тонкодисперсных дисперсий с высоким содержанием полимера в некоторых случаях может составлять более 10000 МПа·с. Целесообразная динамическая вязкость в большинстве случаев находится в интервале от 10 до 4000 МПа·с, предпочтительно от 10 до 1000 МПа·с и еще более предпочтительно от 10 до 500 МПа·с (измерения осуществляют посредством вискозиметра Брукфильда согласно DIN EN ISO 2555 при 25°С).
Для приведения свойств покровного средства в соответствие с теми или иными специфическими требованиями предлагаемые в изобретении водные дисперсии могут содержать также добавки или другие компоненты. К подобным добавкам, в частности, относятся используемые для отверждения вспомогательные средства, так называемые сиккативы, а также средства для улучшения текучих свойств, пигменты и красители.
Предлагаемые в изобретении покровные средства предпочтительно обладают минимальной температурой пленкообразования, которая может быть измерена согласно DIN ISO 2115, составляющей не более 50°С, особенно предпочтительно не более 35°С, еще более предпочтительно не более 25°С.
В соответствии с предпочтительным вариантом осуществления изобретения предлагаемое в изобретении покровное средство, в частности водная дисперсия, обладает йодным числом согласно DIN 53241, составляющим по меньшей мере 1 г йода на 100 г, предпочтительно по меньшей мере 10 г йода на 100 г, особенно предпочтительно по меньшей мере 15 г йода на 100 г. Йодное число может быть определено с использованием соответствующей дисперсии, причем результат определения относится к содержанию твердого вещества.
В целесообразном варианте кислотное число покровного средства, предпочтительно водной дисперсии, находится в интервале от 0,1 до 100 мг КОН/г, предпочтительно от 1 до 40 мг КОН/г и еще более предпочтительно от 2 до 10 мг КОН/г. Кислотное число может быть определено согласно DIN EN ISO 2114 с использованием соответствующей дисперсии, причем результат определения относится к содержанию твердого вещества.
Гидроксильное число предлагаемой в изобретении покровного средства, в частности водной дисперсии, предпочтительно находится в интервале от 0 до 400 мг КОН/г, особенно предпочтительно от 1 до 200 мг КОН/г и еще более предпочтительно в интервале от 3 до 150 мг КОН/г. Гидроксильное число может быть определено согласно DIN EN ISO 4629 с использованием соответствующей дисперсии, причем результат определения относится к содержанию твердого вещества.
Предлагаемые в изобретении покровные средств не нуждаются в использовании сиккативов, в связи с чем последние могут присутствовать в указанных композициях лишь в качестве используемых при необходимости компонентов. Сиккативы, в частности, целесообразно использовать в случае покровных средств, которые пригодны для окислительного сшивания. Сиккативы особенно предпочтительно следует добавлять к водным дисперсиям. К пригодным сиккативам, в частности, относятся металлоорганические соединения, например, мыла на основе переходных металлов, например, таких как кобальт, марганец, свинец и цирконий, или на основе щелочных и щелочноземельных металлов, например, таких как литий, калий и кальций. Примерами пригодных сиккативов являются, в частности, нафталат кобальта и ацетат кобальта. Сиккативы можно использовать по отдельности или в виде смеси, причем особенно предпочтительными, в частности, являются смеси, содержащие соли кобальта, циркония или лития.
Полимеры согласно настоящему изобретению, в частности, можно использовать в покровных средствах или в качестве добавок. Речь при этом, в частности, идет о лаках, средствах для пропитки, клеевых материалах и/или грунтовках. Покровные средства, в частности, водные дисперсии, особенно предпочтительно можно использовать для производства лаков или средств для пропитки, предназначенных для применения на древесине и/или металлах.
Покрытия, которые могут быть выполнены из предлагаемых в изобретении покровных средств, отличаются высокой устойчивостью по отношению к растворителям, причем последние, в частности, способны растворять лишь незначительную часть покрытий. Предпочтительные покрытия отличаются особенно высокой устойчивостью к метилизобутилкетону. Потери массы подобных покрытий в результате их обработки метилизобутилкетоном преимущественно составляют не более 50% масс., предпочтительно не более 35% масс. Поглощение метилизобутилкетона подобными покрытиями предпочтительно не превышает 1000% масс., особенно предпочтительно 600% масс. в пересчете на массу покрытия. Указанные значения определены при температуре около 25°С, длительности воздействия метилизобутилкетона по меньшей мере 4 часа и использовании для измерений совершенно сухого и сшитого покрытия.
Покрытия, выполняемые из предлагаемых в изобретении покровных средств, отличаются высокой стойкостью к механическим воздействиям. Твердость указанных покрытий, измеренная согласно DIN ISO 1522 по маятниковому прибору, предпочтительно составляет по меньшей мере 15 секунд, преимущественно по меньшей мере 25 секунд.
Предлагаемые в изобретении дисперсии помимо получаемых эмульсионной полимеризацией полимеров могут содержать также другие компоненты.
Сшивание предлагаемых в изобретении полимеров, соответственно покровных средств, можно осуществлять путем добавления сшивающих агентов. В качестве сшивающих агентов пригодны нуклеофильные соединения, содержащие несколько функциональных групп. В частности, особенно пригодными сшивающими агентами являются диамины, например, 2,2'-(этилендиокси)диэтиламин (Jeffamine® XTJ-504, CAS номер 929-59-9), а также дигидразиды, например, такие как дигидразид адипиновой кислоты.
Особенно предпочтительные сшивающие агенты приведены, в частности, в международной заявке WO 94/25433 (зарегистрирована Европейским патентным ведомством 25.04.1994 под номером РСТ/ЕР 94/01283), которые посредством данной ссылки включены в описание настоящего изобретения.
Количество используемого сшивающего агента не является критическим параметром и преимущественно зависит от конкретного полимера. Особенно предпочтительное молярное отношение содержащихся в полимере способных к сшиванию групп к реакционно-способным группам сшивающего агента составляет от 10:1 до 1:10, особенно предпочтительно от 4:1 до 1:4 и еще более предпочтительно от 2:1 до 1:2.
Приведенные ниже примеры и сравнительные примеры служат для более подробного пояснения настоящего изобретения и не ограничивают его объема.
Пример 1 (пример получения)
В автоклав фирмы Parr объемом 100 мл с системой стабилизации давления из термостатированной бюретки вводят 10 ммоль сложного аллилового эфира метакриловой кислоты в 25 мл тетрагидрофурана и под давлением 10 бар при температуре 65°С в течение 20 часов осуществляют взаимодействие указанного эфира с газовой смесью монооксида углерода с водородом (молярное отношение 1:1) в присутствии 0,1% мол. Rh(ацетил-ацетонат)(СО)2 и 0,2% мол. ксантофоса (соответственно в пересчете на исходный эфир). Выход достигает 90%, причем реакционная смесь содержит 4-оксобутилметакрилат и 2-метил-3-оксопропилметакрилат. Отношение 4-оксобутилметакрилата к 2-метил-3-оксопропилметакрилату составляет 92:8.
Пример 2 (пример получения)
В основном повторяют пример 1, однако используют 0,02% мол. Rh(ацетилацетонат)(СО)2 и 0,04% мол. ксантофоса (соответственно в пересчете на сложный аллиловый эфир метакриловой кислоты). Выход составляет 85% при соотношении 4-оксобутилметакрилата и 2-метил-3-оксо-пропилметакрилата 92:8.
Пример 3 (пример получения)
В основном повторяют пример 1, однако синтез осуществляют под давлением 20 бар. Выход составляет 95% при соотношении 4-оксобутилметакрилата и 2-метил-3-оксопропилметакрилата 88:12.
Пример 4 (пример получения)
В автоклав фирмы Parr объемом 100 мл с системой стабилизации давления из термостатированной бюретки вводят 50 ммоль сложного аллилового эфира метакриловой кислоты в 25 мл тетрагидрофурана и под давлением 20 бар при температуре 65°С в течение 2 часов осуществляют взаимодействие указанного эфира с газовой смесью монооксида углерода с водородом (молярное отношение 1:1) в присутствии 0,02% мол. (2,5 мг) Rh(ацетил-ацетонат)(СО)2 и 0,04% мол. бифефоса (соответственно в пересчете на исходный эфир). Выход достигает 99%, причем реакционная смесь содержит 4-оксобутил-метакрилат и 2-метил-3-оксопропилметакрилат. Отношение 4-оксобутилметакрилата к 2-метил-3-оксопропилметакрилату составляет 60:40.
Пример 5 (пример получения)
В основном повторяют пример 4, однако синтез осуществляют под давлением 10 бар. Выход составляет 99% при соотношении 4-оксобутилметакрилата и 2-метил-3-оксопропилметакрилата 68:32.
Пример 6 (пример получения)
В основном повторяют пример 5, однако используют 0,02% мол. Rh(ацетилацетонат)(СО)2 и 0,12% мол. бифефоса (соответственно в пересчете на сложный аллиловый эфир метакриловой кислоты). Выход составляет 99% при соотношении 4-оксобутилметакрилата и 2-метил-3-оксо-пропилметакрилата 73:27.
Пример 7. Получение дисперсии сополимера бутилакрилат/метилметакрилат/оксобутилметакрилат/метакриловая кислота с соотношением мономеров 53,9:43,1:2:1
Сначала в полиэтиленовом химическом стакане объемом 1 литр в 179,6 г воды в течение трех минут посредством ультраскоростной мешалки (4000 об/мин) эмульгируют 107,8 г бутилакрилата, 86,2 г метилметакрилата, 4 г оксобутилметакрилата, 2 г метакриловой кислоты, 0,6 г пероксодисульфата аммония и 6,0 г 30%-ного эмульгатора Disponil FES 32.
Затем в термостатируемый водяной баней стеклянный реактор объемом 1 литр, снабженный лопастной мешалкой, загружают 110 г воды и 0,15 г 30%-ного эмульгатора Disponil FES 32, реактор нагревают до 80°С и указанные компоненты смешивают с раствором 0,15 г пероксодисульфата аммония в 10 г воды. Через 5 минут приступают к подаче приготовленной выше эмульсии, которую осуществляют в течение последующих 240 минут (подача в течение трех минут, четырехминутная пауза, подача остального количества эмульсии в течение 237 минут).
По завершении подачи эмульсии реакционную смесь продолжают перемешивать при 80°С в течение 1 часа. Затем реактор охлаждают до комнатной температуры, и дисперсию отделяют путем фильтрования реакционной смеси через ситовую винилацетатную ткань с размером ячеек 0,09 мм.
Полученная эмульсия обладает содержанием твердого вещества 40±1%, показателем рН 2,6, вязкостью 16 МПа·с и показателем rN5 85 нм.
Пример 8. Получение дисперсии сополимера бутилакрилат/метилметакрилат/оксобутилметакрилат/метакриловая кислота с соотношением мономеров 52,8:42,2:4:1
Сначала в полиэтиленовом химическом стакане объемом 1 литр в 179,6 г воды в течение трех минут посредством ультраскоростной мешалки (4000 об/мин) эмульгируют 105,6 г бутилакрилата, 84,4 г метилметакрилата, 8 г оксобутилметакрилата, 2 г метакриловой кислоты, 0,6 г пероксодисульфата аммония и 6,0 г 30%-ного эмульгатора Disponil FES 32.
Затем в термостатируемый водяной баней стеклянный реактор объемом 1 литр, снабженный лопастной мешалкой, загружают 110 г воды и 0,15 г 30%-ного эмульгатора Disponil FES 32, реактор нагревают до 80°С и указанные компоненты смешивают с раствором 0,15 г пероксодисульфата аммония в 10 г воды. Через 5 минут приступают к подаче приготовленной выше эмульсии, которую осуществляют в течение последующих 240 минут (подача в течение трех минут, четырехминутная пауза, подача остального количества эмульсии в течение 237 минут).
По завершении подачи эмульсии реакционную смесь продолжают перемешивать при 80°С в течение 1 часа. Затем реактор охлаждают до комнатной температуры и дисперсию отделяют путем фильтрования реакционной смеси через ситовую винилацетатную ткань с размером ячеек 0,09 мм.
Полученная эмульсия обладает содержанием твердого вещества 40±1%, показателем рН 2,5, вязкостью 14 МПа·с и показателем rN5 84 нм.
Пример 9. Получение дисперсии сополимера бутилакрилат/метилметакрилат/оксобутилметакрилат/метакриловая кислота с соотношением мономеров 51,7:41,3:6:1
Сначала в полиэтиленовом химическом стакане объемом 1 литр в 179,6 г воды в течение трех минут посредством ультраскоростной мешалки (4000 об/мин) эмульгируют 103,4 г бутилакрилата, 82,6 г метилметакрилата, 12 г оксобутилметакрилата, 2 г метакриловой кислоты, 0,6 г пероксодисульфата аммония и 6,0 г 30%-ного эмульгатора Disponil FES 32.
Затем в термостатируемый водяной баней стеклянный реактор объемом 1 литр, снабженный лопастной мешалкой, загружают 110 г воды и 0,15 г 30%-ного эмульгатора Disponil FES 32, реактор нагревают до 80°С и указанные компоненты смешивают с раствором 0,15 г пероксодисульфата аммония в 10 г воды. Через 5 минут приступают к подаче приготовленной выше эмульсии, которую осуществляют в течение последующих 240 минут (подача в течение трех минут, четырехминутная пауза, подача остального количества эмульсии в течение 237 минут).
По завершении подачи эмульсии реакционную смесь продолжают перемешивать при 80°С в течение 1 часа. Затем реактор охлаждают до комнатной температуры и дисперсию отделяют путем фильтрования реакционной смеси через ситовую винилацетатную ткань с размером ячеек 0,09 мм.
Полученная эмульсия обладает содержанием твердого вещества 40±1%, показателем рН 2,5, вязкостью 14 МПа·с и показателем rN5 90 нм.
Примеры 10-12. Сшивание полученных в примерах 7-9 дисперсий дигидразидом
Полученные в примерах 7-9 дисперсии сшивают эквимолярным количеством дигидразида адипиновой кислоты. Для этого к дисперсии при перемешивании по каплям добавляют 15%-ный раствор дигидразида адипиновой кислоты, осуществляют двухчасовое перемешивание компонентов и пленку сушат при комнатной температуре.
Свойства полученного покровного средства исследуют разными методами. В частности, подвергнутые сушке пленки испытывают на устойчивость к растворителям, водопоглощение и твердость.
Устойчивость к растворителям определяют, используя метил изобутилкетон, в котором образец (А) набухает при комнатной температуре в течение 4 часов. Затем образец извлекают из растворителя, удаляют избыточный растворитель и определяют массу. После этого образец (В) сушат в течение 1 часа при температуре около 140°С. По разности А и В вычисляют массу поглощенных растворителем фракций образца. Рассчитывают набухание в пересчете на массу освобожденного от растворимых фракций образца В, причем полученный результат в дальнейшем тексте называют «истинным набуханием».
Для определения водопоглощения образец в течение 24 часов набухает при комнатной температуре в воде. Дальнейшие операции аналогичны указанным выше при определении устойчивости к растворителям. Полученный результат в дальнейшем тексте называют «истинным водопоглощением».
Кроме того, осуществляют испытание в соответствии с принятым в мебельной промышленности стандартом DIN 68861-1 (ниже называемое мебельным тестом). Результаты данного испытания оценивают по пятибалльной шкале, причем оценке 5 соответствует отсутствие видимых изменений, тогда как оценка 1 означает сильное изменение или разрушение испытуемой поверхности.
Результаты соответствующих испытаний приведены в таблице 1. В примере 10 используют дисперсию из примера 7, в примере 11 дисперсию из примера 8 и в примере 12 дисперсию из примера 9.
Примеры 13-15. Сшивание полученных в примерах 7-9 дисперсий диамином
Полученные в примерах 7-9 дисперсии сшивают эквимолярным количеством 2,2'-(этилендиокси)диэтиламина (Jeffamine® XTJ-504, CAS 929-59-9). Для этого к дисперсии при перемешивании по каплям добавляют диамин, осуществляют двухчасовое перемешивание компонентов и пленку сушат при комнатной температуре.
Свойства полученного покровного средства исследуют разными методами. В частности, подвергнутые сушке пленки испытывают на устойчивость к растворителям, водопоглощение и твердость.
Устойчивость к растворителям определяют, используя метилизобутилкетон, в котором образец набухает при комнатной температуре в течение 4 часов. Затем образец извлекают из растворителя и удаляют избыток последнего. После этого образец сушат в течение 1 часа при температуре около 140°С. По потере массы рассчитывают количество удаленных растворителем фракций образца.
Для определения водопоглощения образец в течение 24 часов набухают в воде при комнатной температуре. Затем образец извлекают из воды и удаляют избыточную воду. После этого образец сушат в течение 1 часа при температуре около 140°С. По потере массы рассчитывают количество удаленных водой фракций образца.
Полученные результаты приведены в таблице 1. Пример 13 выполнен с использованием дисперсии из примера 7, пример 14 с использованием дисперсии из примера 8 и пример 15 с использованием дисперсии из примера 9.
Сравнительный пример 1. Сополимер бутилакрилат/метилметакрилат/ацетоацетоксиэтилметакрилат/метакриловая кислота с соотношением мономеров 53,9:43,1:2:1
Для сравнения вместо оксобутилметакрилата в дисперсии вводят звенья коммерчески доступного ацетоацетоксиэтилметакрилата, причем сшивание осуществляют посредством дигидразида адипиновой кислоты.
Сначала в полиэтиленовом химическом стакане объемом 2 литра в 359,18 г воды в течение трех минут посредством ультраскоростной мешалки (4000 об/мин) эмульгируют 215,6 г бутилакрилата, 172,4 г метилметакрилата, 8 г ацетоацетоксиэтилметакрилата, 4 г метакриловой кислоты, 1,2 г пероксодисульфата аммония и 12,0 г 30%-ного эмульгатора Disponil FES 32.
Затем в термостатируемый водяной баней стеклянный реактор объемом 2 литра, снабженный лопастной мешалкой, загружают 230 г воды и 0,3 г 30%-ного эмульгатора Disponil FES 32, реактор нагревают до 80°С и указанные компоненты смешивают с раствором 0,3 г пероксодисульфата аммония в 10 г воды. Через 5 минут приступают к подаче приготовленной выше эмульсии, которую осуществляют в течение последующих 240 минут (подача в течение трех минут, четырехминутная пауза, подача остального количества эмульсии в течение 237 минут).
По завершении подачи эмульсии реакционную смесь продолжают перемешивать при 80°С в течение 1 часа. Затем реактор охлаждают до комнатной температуры и дисперсию отделяют путем фильтрования реакционной смеси через ситовую винилацетатную ткань с размером ячеек 0,09 мм.
Подвергнутые сушке пленки испытывают на устойчивость к растворителям, водопоглощение и стойкость к царапанью.
Полученная эмульсия обладает содержанием твердого вещества 40±1%, показателем рН 2,4 и показателем rN5 87 нм.
Сравнительный пример 2. Сополимер бутилакрилат/метилметакри-лат/ацетоацетоксиэтилметакрилат/метакри-ловая кислота с соотношением мономеров 52,8:42,2:4:1
Для сравнения вместо оксобутилметакрилата в дисперсии вводят звенья коммерчески доступного ацетоацетоксиэтилметакрилата, причем сшивание осуществляют посредством дигидразида адипиновой кислоты.
Сначала в полиэтиленовом химическом стакане объемом 2 литра в 359,18 г воды в течение трех минут посредством ультраскоростной мешалки (4000 об/мин) эмульгируют 211,1 г бутилакрилата, 168,8 г метилметакрилата, 16 г ацетоацетоксиэтилметакрилата, 4 г метакриловой кислоты, 1,2 г пероксодисульфата аммония и 12,0 г 30%-ного эмульгатора Disponil FES 32.
Затем в термостатируемый водяной баней стеклянный реактор объемом 2 литра, снабженный лопастной мешалкой, загружают 230 г воды и 0,3 г 30%-ного эмульгатора Disponil FES 32, реактор нагревают до 80°С и указанные компоненты смешивают с раствором 0,3 г пероксодисульфата аммония в 10 г воды. Через 5 минут приступают к подаче приготовленной выше эмульсии, которую осуществляют в течение последующих 240 минут (подача в течение трех минут, четырехминутная пауза, подача остального количества эмульсии в течение 237 минут).
По завершении подачи эмульсии реакционную смесь продолжают перемешивать при 80°С в течение 1 часа. Затем реактор охлаждают до комнатной температуры и дисперсию отделяют путем фильтрования реакционной смеси через ситовую винилацетатную ткань с размером ячеек 0,09 мм. Подвергнутые сушке пленки испытывают на устойчивость к растворителям, водопоглощение и стойкость к царапанью.
Полученная эмульсия обладает содержанием твердого вещества 40±1%, показателем рН 2,4 и показателем rN5 82 нм.
Сравнительный пример 3. Сополимер бутилакрилат/метилметакрилат/ацетоацетоксиэтилметакрилат/метакриловая кислота с соотношением мономеров 51,7:41,3:6:1
Для сравнения вместо оксобутилметакрилата в дисперсии вводят звенья коммерчески доступного ацетоацетоксиэтилметакрилата, причем сшивание осуществляют посредством дигидразида адипиновой кислоты.
Сначала в полиэтиленовом химическом стакане объемом 2 литра в 359,18 г воды в течение трех минут посредством ультраскоростной мешалки (4000 об/мин) эмульгируют 206,8 г бутилакрилата, 165,2 г метилметакрилата, 24 г ацетоацетоксиэтилметакрилата, 4 г метакриловой кислоты, 1,2 г пероксодисульфата аммония и 12,0 г 30%-ного эмульгатора Disponil FES 32.
Затем в термостатируемый водяной баней стеклянный реактор объемом 2 литра, снабженный лопастной мешалкой, загружают 230 г воды и 0,3 г 30%-ного эмульгатора Disponil FES 32, реактор нагревают до 80°С и указанные компоненты смешивают с раствором 0,3 г пероксодисульфата аммония в 10 г воды. Через 5 минут приступают к подаче приготовленной выше эмульсии, которую осуществляют в течение последующих 240 минут (подача в течение трех минут, четырехминутная пауза, подача остального количества эмульсии в течение 237 минут).
По завершении подачи эмульсии реакционную смесь продолжают перемешивать при 80°С в течение 1 часа. Затем реактор охлаждают до комнатной температуры и дисперсию отделяют путем фильтрования реакционной смеси через ситовую винилацетатную ткань с размером ячеек 0,09 мм.
Подвергнутые сушке пленки испытывают на устойчивость к растворителям, водопоглощение и стойкость к царапанью.
Полученная эмульсия обладает содержанием твердого вещества 40±1%, показателем рН 2,4 и показателем rN5 86 нм.
Сравнительные примеры 4-6. Сшивание полученных в сравнительных примерах 1-3 дисперсий дигидразидом
Полученные в сравнительных примерах 1-3 дисперсии сшивают эквимолярным количеством дигидразида адипиновой кислоты. Для этого к дисперсии при перемешивании по каплям добавляют 15%-ный раствор дигидразида адипиновой кислоты, осуществляют 30-минутное перемешивание компонентов и пленку сушат при комнатной температуре.
Свойства полученного покровного средства исследуют разными методами. В частности, подвергнутые сушке пленки испытывают на устойчивость к растворителям, водопоглощение и твердость.
Устойчивость к растворителям определяют, используя метилизобутилкетон, в котором образец набухает при комнатной температуре в течение 4 часов. Затем образец извлекают из растворителя, удаляют избыточный растворитель и определяют массу. После этого образец сушат в течение 1 часа при температуре около 140°С. По разности масс вычисляют массу поглощенных растворителем фракций образца.
Для определения водопоглощения образец в течение 24 часов набухает в воде при комнатной температуре. Затем образец извлекают из воды и удаляют избыточную воду. После этого образец сушат в течение 1 часа при температуре около 140°С. По потере массы рассчитывают количество удаленных водой фракций образца.
Полученные результаты приведены в таблице 1. Сравнительный пример 4 выполнен с использованием дисперсии из сравнительного примера 1, сравнительный пример 5 с использованием дисперсии из сравнительного примера 2 и сравнительный пример 6 с использованием дисперсии из сравнительного примера 3.
Пример 16 (пример получения)
В автоклав объемом 100 мл с системой стабилизации давления из термостатированной бюретки вводят 10 ммоль сложного аллилового эфира метакриловой кислоты в 25 мл тетрагидрофурана и под давлением 10 бар при температуре 65°С в течение 20 часов осуществляют взаимодействие указанного эфира с газовой смесью монооксида углерода с водородом (молярное отношение 1:1) в присутствии 0,1% мол. Rh(ацетил-ацетонат)(СО)2 и 0,2% мол. ксантофос (соответственно в пересчете на исходный эфир). Выход достигает 90%, причем реакционная смесь содержит 4-оксобутил-метакрилат и 2-метил-3-оксопропилметакрилат. Отношение 4-оксобутилметакрилата к 2-метил-3-оксопропилметакрилату составляет 92:8.
Пример 17
В инертизированный азотом автоклав фирмы Büchi объемом 3000 мл с системой стабилизации давления и газоплотной мешалкой загружают 1,03 ммоля бифефоса, 0,17 ммоля Rh(ацетилацетонат)(СО)2 и 2,08 ммоля бис(2,2,6,6-тетраметил-4-пиперидинил)себацината в виде раствора в 1200 мл толуола. Затем автоклав заполняют находящейся под давлением 5 бар газовой смесью монооксида углерода с водородом (молярное отношение 1:1) и в течение 60 минут нагревают до 80°С. После этого автоклав охлаждают до комнатной температуры и к находящемуся в нем толуольному раствору катализатора насосом подают 3 моля сложного аллилового эфира метакриловой кислоты, содержащего добавку 4-гидрокси ТЕМПО (3,2 ммоля). Последующее взаимодействие реагентов осуществляют при давлении указанной выше газовой смеси 5 бар. Температура в процессе взаимодействия повышается с 25 до 30°С. Через 100 минут в связи с отсутствием газопоглощения реакцию прекращают. После этого посредством насоса в систему дополнительно вводят раствор 1,7 ммоля бифефоса, 0,04 ммоля Rh(ацетилацетонат)(СО)2, 2,1 ммоля бис(2,2,6,6-тетраметил-4-пиперидинил)себацината и 0,6 ммоля 4-гидрокси ТЕМПО в 450 мл толуола, и вновь инициируют реакцию при давлении газовой смеси 5 бар и температуре 60°С. Через 72 минуты реакция прекращается. Выход достигает 61%, причем реакционная смесь содержит 4-оксобутил-метакрилат и 2-метил-3-оксопропилметакрилат. Отношение 4-оксобутилметакрилата к 2-метил-3-оксопропилметакрилату составляет 69:31.
Пример 18
В инертизированный азотом автоклав фирмы Büchi объемом 3000 мл с системой стабилизации давления и газоплотной мешалкой загружают 2,5 ммоля бифефоса, 0,17 ммоля Rh(ацетилацетонат)(СО)2 и 4,1 ммоля бис-(2,2,6,6-тетраметил-4-пиперидинил)себацината в виде раствора в 1500 мл толуола. Затем в автоклав вводят 3,5 моля сложного аллилового эфира метакриловой кислоты, содержащего добавку 4-гидрокси ТЕМПО (3,2 ммоля). Автоклав заполняют указанной в примере 1 газовой смесью под давлением 5 бар, которое поддерживают на постоянном уровне посредством системы стабилизации давления. Температуру автоклава повышают от комнатной до температуры реакции (60°С) посредством подключенного к двойной рубашке термостата мощностью 2 кВт. Через 105 минут в связи с отсутствием газопоглощения реакцию прекращают. Выход достигает 72%, причем реакционная смесь содержит 4-оксобутилметакрилат и 2-метил-3-оксопропилметакрилат. Отношение 4-оксобутилметакрилата к 2-метил-3-оксопропилметакрилату составляет 70:30.
Пример 19
В инертизированный азотом автоклав фирмы Büchi объемом 3000 мл с системой стабилизации давления и газоплотной мешалкой загружают 1,37 ммоля трифенилфосфина, 1,02 ммоля бифефоса, 0,17 ммоля Rh(ацетил-ацетонат)(СО)2 и 4,1 ммоля бис(2,2,6,6-тетраметил-4-пиперидинил)себацината в виде раствора в 1500 мл толуола. Затем в автоклав вводят 3,4 моля сложного аллилового эфира метакриловой кислоты, содержащего добавку 4-гидрокси ТЕМПО (3,2 ммоля). Автоклав заполняют указанной в примере 1 газовой смесью под давлением 5 бар, которое поддерживают на постоянном уровне посредством системы стабилизации давления. Температуру автоклава повышают от комнатной до реакционной (60°С) посредством подключенного к двойной рубашке термостата мощностью 2 кВт. Через 27 минут температура повышается до 70°С, еще через 49 минут до 75°С. Через 120 минут в связи с отсутствием газопоглощения реакцию прекращают. Выход достигает 74%, причем реакционная смесь содержит 4-оксобутилметакрилат и 2-метил-3-оксопропилметакрилат. Отношение 4-оксобутил-метакрилата к 2-метил-3-оксопропилметакрилату составляет 78:22.
Пример 20
В инертизированный азотом автоклав фирмы Büchi объемом 3000 мл с системой стабилизации давления и газоплотной мешалкой загружают 2,1 ммоля трифенилфосфина, 1,05 ммоля бифефоса, 0,17 ммоля Rh(ацетил-ацетонат)(СО)2 и 4,2 ммоля бис(2,2,6,6-тетраметил-4-пиперидинил)себацината в виде раствора в 1000 мл толуола. Затем в автоклав вводят 5,5 моля сложного аллилового эфира метакриловой кислоты, содержащего добавку 4-гидрокси ТЕМПО (6,6 ммоля). Автоклав заполняют указанной в примере 1 газовой смесью под давлением 5 бар, которое поддерживают на постоянном уровне посредством системы стабилизации давления. Температуру автоклава повышают от комнатной до реакционной (60°С) посредством подключенного к двойной рубашке термостата мощностью 2 кВт. Через 15 минут температура повышается до 70°С, еще через 20 минут до 75°С. Через 210 минут в связи с отсутствием газопоглощения реакцию прекращают. Выход достигает 60%, причем реакционная смесь содержит 4-оксобутилметакрилат и 2-метил-3-оксопропилметакрилат. Отношение 4-оксобутилметакрилата к 2-метил-3-оксопропилметакрилату составляет 82:18.
Пример 21
В инертизированный азотом автоклав фирмы Büchi объемом 3000 мл с системой стабилизации давления и газоплотной мешалкой загружают 2,1 ммоля трифенилфосфина, 1,05 ммоля бифефоса, 0,17 ммоля Rh(ацетил-ацетонат)(СО)2 и 4,2 ммоля бис(2,2,6,6-тетраметил-4-пиперидинил)себацината в виде раствора в 1000 мл толуола. Затем в автоклав вводят 6,3 моля сложного аллилового эфира метакриловой кислоты, содержащего добавку 4-гидрокси ТЕМПО (6,6 ммоля). Абсолютное давление в автоклаве трижды повышают до 6 бар посредством реакционной газовой смеси, а затем вновь снижают до 1 бар.
Автоклав заполняют указанной в примере 1 газовой смесью под давлением 5 бар, которое поддерживают на постоянном уровне посредством системы стабилизации давления. Температуру автоклава повышают от комнатной до реакционной (75°С) посредством подключенного к двойной рубашке термостата мощностью 2 кВт. Через 190 минут в связи с отсутствием газопоглощения реакцию прекращают.
Выход достигает 53%, причем реакционная смесь содержит 4-оксобутилметакрилат и 2-метил-3-оксопропилметакрилат. Отношение 4-оксобутилметакрилата к 2-метил-3-оксопропилметакрилату составляет 80:20.
Пример 22
В инертизированный азотом автоклав фирмы Büchi объемом 3000 мл с системой стабилизации давления и газоплотной мешалкой загружают 2,1 ммоля трифенилфосфина, 1,05 ммоля бифефоса, 0,17 ммоля Rh(ацетил-ацетонат)(СО)2 и 4,2 ммоля бис(2,2,6,6-тетраметил-4-пиперидинил)себацината в виде раствора в 1000 мл толуола. Затем в автоклав вводят 6,4 моля сложного аллилового эфира метакриловой кислоты, содержащего добавку 4-гидрокси ТЕМПО (0,47 ммоля).
Абсолютное давление в автоклаве трижды повышают до 6 бар посредством реакционной газовой смеси, а затем вновь снижают до 1 бар.
Автоклав заполняют указанной в примере 1 газовой смесью под давлением 5 бар, которое поддерживают на постоянном уровне посредством системы стабилизации давления. Температуру автоклава повышают от комнатной до реакционной (75°С) посредством подключенного к двойной рубашке термостата мощностью 2 кВт. Через 190 минут в связи с отсутствием газопоглощения реакцию прекращают.
Выход достигает 54%, причем реакционная смесь содержит 4-оксобутилметакрилат и 2-метил-3-оксопропилметакрилат. Отношение 4-оксобутилметакрилата к 2-метил-3-оксопропилметакрилату составляет 80:20.
Пример 23
В инертизированный азотом автоклав фирмы Büchi объемом 3000 мл с системой стабилизации давления и газоплотной мешалкой загружают 2,1 ммоля трифенилфосфина, 1,05 ммоля бифефоса, 0,17 ммоля Rh(ацетил-ацетонат)(СО)2 и 4,2 ммоля бис(2,2,6,6-тетраметил-4-пиперидинил)себацината в виде раствора в 1000 мл толуола. Затем в автоклав вводят 6,8 моля сложного аллилового эфира метакриловой кислоты, содержащего добавку 4-гидрокси ТЕМПО (0,53 ммоля). Абсолютное давление в автоклаве трижды повышают до 6 бар посредством реакционной газовой смеси, а затем вновь снижают до 1 бар.
Автоклав заполняют указанной в примере 1 газовой смесью под давлением 10 бар, которое поддерживают на постоянном уровне посредством системы стабилизации давления. Температуру автоклава повышают от комнатной до реакционной (75°С) посредством подключенного к двойной рубашке термостата мощностью 2 кВт. Через 190 минут в связи с отсутствием газопоглощения реакцию прекращают.
Выход достигает 61%, причем реакционная смесь содержит 4-оксобутилметакрилат и 2-метил-3-оксопропилметакрилат. Отношение 4-оксобутилметакрилата к 2-метил-3-оксопропилметакрилату составляет 80:20.
Пример 24
В инертизированный азотом автоклав фирмы Büchi объемом 3000 мл с системой стабилизации давления и газоплотной мешалкой загружают 2,1 ммоля трифенилфосфина, 1,05 ммоля бифефоса, 0,17 ммоля Rh(ацетил-ацетонат)(СО)2 и 4,2 ммоля бис(2,2,6,6-тетраметил-4-пиперидинил)себацината в виде раствора в 1000 мл толуола. Затем в автоклав вводят 6,8 моля сложного аллилового эфира метакриловой кислоты, содержащего добавку 4-гидрокси ТЕМПО (0,53 ммоля). Абсолютное давление в автоклаве трижды повышают до 6 бар посредством реакционной газовой смеси, а затем вновь снижают до 1 бар.
Автоклав заполняют указанной в примере 1 газовой смесью под давлением 5 бар, которое поддерживают на постоянном уровне посредством системы стабилизации давления. Температуру автоклава повышают от комнатной до реакционной (75°С) посредством подключенного к двойной рубашке термостата мощностью 2 кВт. Через 185 минут в связи с отсутствием газопоглощения реакцию прекращают. Выход достигает 57%, причем реакционная смесь содержит 4-оксобутилметакрилат и 2-метил-3-оксопропилметакрилат. Отношение 4-оксобутилметакрилата к 2-метил-3-оксо-пропилметакрилату составляет 80:20.
Реферат
Настоящее изобретение относится к способу получения (мет)акрилатного мономера. Описан способ получения (мет)акрилатного мономера общей формулы (I):в которой Rозначает водород или метильную группу, X означает кислород, Rозначает остаток алкильной группы с 3-6 атомами углерода и одной альдегидной группой, отличающийся тем, что исходный продукт формулы (III):в которой Rозначает водород или метильную группу, X означает кислород, и Rозначает ненасыщенный алкильный остаток по меньшей мере с одной двойной связью и 3-6 атомами углерода, подвергают взаимодействию с монооксидом углерода и водородом в присутствии катализатора, который является комплексом, содержащим родий, иридий, палладий и/или кобальт и фосфорсодержащее соединение в качестве лиганда, причем отношение металла к лиганду предпочтительно составляет от 1:1 до 1:1000, особенно предпочтительно от 1:2 до 1:200. Технический результат - получение (мет)акрилатного мономера способом, характеризующимся повышенной экономичностью, высокой селективностью, незначительным содержанием побочных продуктов. 7 з.п. ф-лы, 1 табл., 24 пр.
Формула
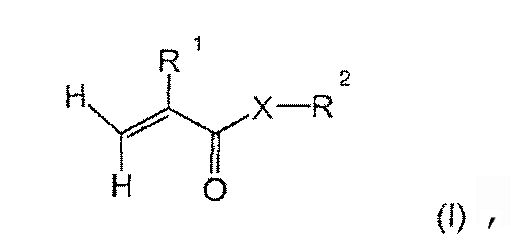
в которой
R1 означает водород или метильную группу,
X означает кислород,
R2 означает остаток алкильной группы с 3-6 атомами углерода и одной альдегидной группой,
отличающийся тем, что исходный продукт формулы (III):

в которой
R1 означает водород или метильную группу,
X означает кислород, и
R5 означает ненасыщенный алкильный остаток по меньшей мере с одной двойной связью и 3-6 атомами углерода,
подвергают взаимодействию с монооксидом углерода и водородом в присутствии катализатора, который является комплексом, содержащим родий, иридий, палладий и/или кобальт и фосфорсодержащее соединение в качестве лиганда, причем отношение металла к лиганду предпочтительно составляет от 1:1 до 1:1000, особенно предпочтительно от 1:2 до 1:200.

Комментарии