Кристаллическая бета - модификация (е)-диметилбутендиоата, способ её получения и фармацевтическая композиция на её основе - RU2616605C1
Код документа: RU2616605C1
Чертежи



Описание
Изобретение относится к органической химии и касается новой кристаллической модификации (Е)-диметилбутендиоата (диметилфумарат - международное непатентованное название, диметиловый эфир фумаровой кислоты - традиционное название), названной нами β-модификацией, способа ее получения и фармацевтической композиции на ее основе, которая может быть использована в фармацевтической промышленности и медицине в качестве средства для лечения тяжелых форм псориаза, рассеянного склероза, липоидного некробиоза, кольцевидной гранулемы, красного волосяного лишая и т.д.
Известны эфиры (помимо диметилового эфира фумаровой кислоты, который рассмотрен ниже) и соли фумаровой кислоты и их смеси. (US 5451667 В2 от 19.09.1995 г.; ЕР 2186819 А1 от 19.05.2010 г.; US 4851439 от 25.07.1989 г.; US 2006/0205659 А1 от 14.09.2006 г.; US 4515974 от 7.05.1985 г. и др.).
Однако эти соединения отличаются от заявляемой новой, не известной ранее кристаллической β-модификации (Е)-диметилбутендиоата химическим составом.
Наиболее близкими к заявляемой новой, не известной ранее кристаллической β-модификации (Е)-диметилбутендиоата являются кристаллические полиморфные модификации диметилфумарата: Форма I, которая характеризуется методом рентгенофазового анализа (РФА), параметрами решетки и значениями некоторых дифракционных максимумов, выраженных в углах 26: (10,96; 22,10; 24,07; 24,11; 24,17; 27,39) град (ЕА 2013/91638 А1 от 30.05.2014 г.). Не охарактеризованы эти модификации также и термоаналитическими исследованиями.
Известные кристаллические модификации диметилфумарата характеризуются физико-химическими методами анализа такими, как: ядерным магнитным резонансом (ЯМР)-совокупностью химических сдвигов (м.д.), высокоэффективной жидкостной хроматографией (ВЭЖХ) - временами удерживания (мин) и чистотой исследуемого вещества (%), методом рентгенофазового анализа (РФА) - наборами углов (2θ, град), межплоскостных расстояний (d, Å) и их интенсивностью (I, имп./мин; Iотн.=Ii/Imax×100, %) (получение дифрактограмм авторы вышеприведенных патентов проводили на Cu Kα-излучении), термоаналитическими исследованиями - температурами тепловых эффектов и др.
Сходство заявляемой новой, не известной ранее кристаллической β-модификации (Е)-диметилбутендиоата, с известными кристаллическими модификациями диметилфумарата заключается в идентичности их химических составов.
Отличие заявляемой новой, не известной ранее кристаллической β-модификации (Е)-диметилбутендиоата, от известных кристаллических модификаций диметилфумарата заключается в различии их дифрактограмм рентгенофазового анализа (РФА): определенного набора углов 2θ (град) - межплоскостных расстояний (d, Å) и их интенсивностью (Iотн.=Ii/Imax×100, %, а также в различии их кривых дифференциальной сканирующей калориметрии (ДСК).
Известные кристаллические модификации (Е)-диметилбутендиоата представляют собой порошки от белого до почти белого цвета, без запаха, растворимые в хлороформе, умеренно растворимые в низших спиртах и мало растворимые в воде.
Известные модификации (Е)-диметилбутендиоата получают эстерификацией фумаровой кислоты и метанола в присутствии серной кислоты в качестве кислотного катализатора и водного секвестранта с последующим выделением порошка диметилфумарата из раствора центрифугированием. Форму I получают перекристаллизацией диметилфумарата из растворов в органических растворителях или из их смесей (ЕА 2013/91638 А1 от 3.05.2014 г.).
Отличие способа получения заявляемой новой, не известной ранее кристаллической β-модификации (Е)-диметилбутендиоата от способов получения известных кристаллических модификаций диметилфумарата состоит в том, что субстанцию диметилфумарата испаряют при температуре (10…95)°С при остаточном давлении (4×10-2…5×10)-4 Торр и конденсируют на охлажденную до -40°С…-196°С поверхность.
Отличие заявляемой фармацевтической композиции в качестве средства для лечения тяжелых форм псориаза, рассеянного склероза, липоидного некробиоза, кольцевидной гранулемы, красного волосяного лишая и т.д. на основе (Е)-диметилбудендиоата от известной композиции [Регистр Лекарственных Средств России - Инструкция применения препарата Текфидера®/Tecfidera® (Dimetyl fumarat/Диметил фумарат)] состоит в том, что в качестве действующего вещества используют терапевтически эффективное количество новой, не известной ранее кристаллической β-модификации (Е)-диметилбутендиоата (диметилфумарата).
Целью изобретения является получение новой, не известной ранее кристаллической β-модификации (Е)-диметилбутендиоата, разработка способа ее получения и применение ее в фармацевтической композиции в качестве средства для лечения тяжелых форм псориаза, рассеянного склероза, липоидного некробиоза, кольцевидной гранулемы, красного волосяного лишая и т.д.
Поставленная цель достигнута настоящим изобретением, а именно получением новой, не известной ранее кристаллической β-модификации (Е)-диметилбутендиоата, характеризующейся следующим набором межплоскостных расстояний (d, Å) и их интенсивностью (Iотн.=Ii/Imax×100): 8,590-6,10%; 8,315-57,09%; 5,376-2,91%; 5,093-7,48%; 4,126-9,92%; 4,096-52,31%; 3,744-100,00%; 3,421-5,48%; 3,285-14,19%; 2,889-2,87%; 2,806-1,74%; 2,718-2,22%; 2,650-3,56%; 2,594-2,91%; 2,481-1,70%; 2,255-1,48%; 2,190-5,97%; 2,117-3,69%; 2,031-1,57%; 1,964-1,74%; 1,913-1,27%; 1,816-1,48%; 1,626-1,57% и двумя эндотермическими эффектами на кривой ДСК при температурах (104,4±0,5)°С и (161,8±0,5)°С.
Поставленная цель достигнута также разработкой способа получения новой, не известной ранее кристаллической β-модификации (Е)-диметилбутендиоата, который состоит в том, что кристаллическую субстанцию диметилфумарата испаряют при температуре (10…95)°С при остаточном давлении (4×10-2…5×10)-4 Торр и конденсируют на охлажденную до-40°С… -196°С поверхность.
Кроме того, поставленная цель достигнута применением новой, не известной ранее кристаллической β-модификации (Е)-диметилбутендиоата для приготовления фармацевтической композиции в качестве средства для лечения тяжелых форм псориаза, рассеянного склероза, липоидного некробиоза, кольцевидной гранулемы, красного волосяного лишая и т.д. Указанная композиция содержит β-модификацию диметилфумарата в терапевтически эффективном количестве и, по крайней мере, один фармацевтически приемлемый носитель, разбавитель, вспомогательное вещество или наполнитель.
Из патентной и научно-технической литературы не известна кристаллическая β-модификация (Е)-диметилбутендиоата, способ ее получения и применение ее в фармацевтической композиции в качестве средства для лечения тяжелых форм псориаза, рассеянного склероза, липоидного некробиоза, кольцевидной гранулемы, красного волосяного лишая и т.д.
Нами обнаружена новая, не известная ранее кристаллическая β-модификация (Е)-диметилбутендиоата, характеризующаяся определенным набором дифракционных максимумов (d, Å) и их интенсивностью (Iотн., %), и двумя эндотермическими эффектами на кривой ДСК при определенных температурах, предложены способ ее получения и применение ее для приготовления фармацевтической композиции в качестве средства для лечения тяжелых форм псориаза, рассеянного склероза, липоидного некробиоза, кольцевидной гранулемы, красного волосяного лишая и т.д.
Заявляемая новая, не известная ранее кристаллическая β-модификация (Е)-диметилбутендиоата представляет собой пушистый порошок от белого до почти белого цвета, без запаха, растворимый в хлороформе, умеренно растворимый в низших спиртах и мало растворимый в воде.
Для пояснения сущности заявляемого технического решения к описанию приложены следующие таблицы и рисунки:
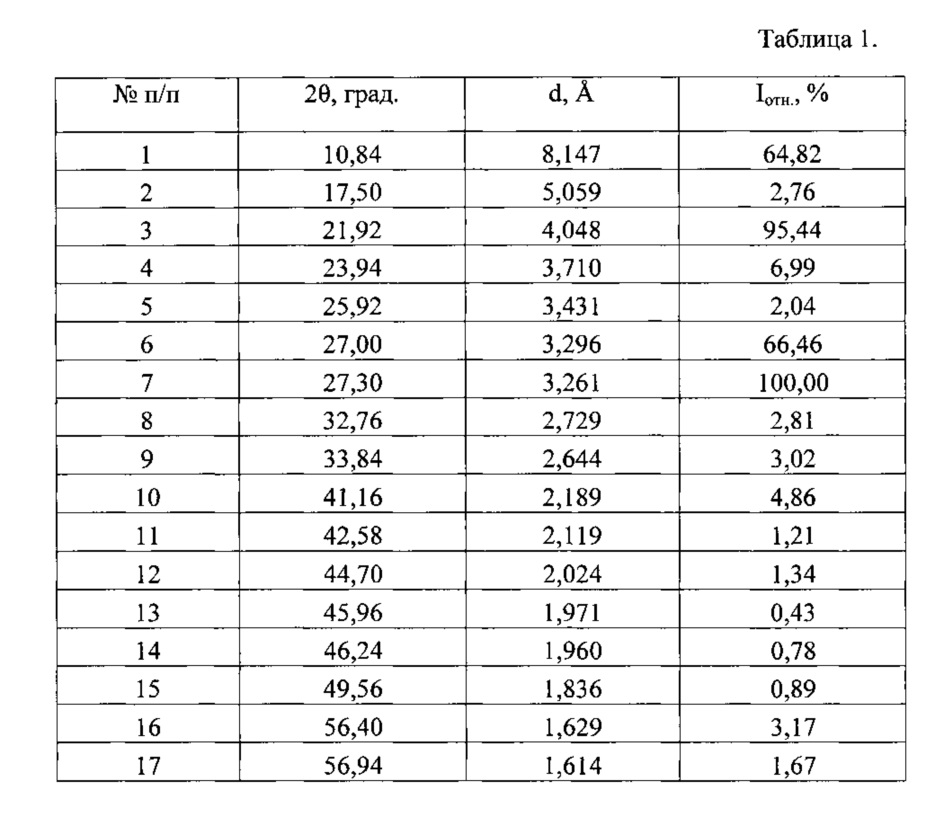
Таблица 1. Углы 2θ, град, межплоскостные расстояния (d, Å) и их интенсивности (Iотн., %) известной кристаллической модификации диметилфумарата, которую использовали в качестве исходного вещества.
Таблица 2. Углы 2θ, межплоскостные расстояния (d, Å) и их интенсивности (Iотн., %) новой, не известной ранее кристаллической β-модификации (Е)-диметилбутендиоата.
Рис. 1. ЯМР1Н-спектр известной кристаллической модификации диметилфумарата, которую использовали в качестве исходного вещества.
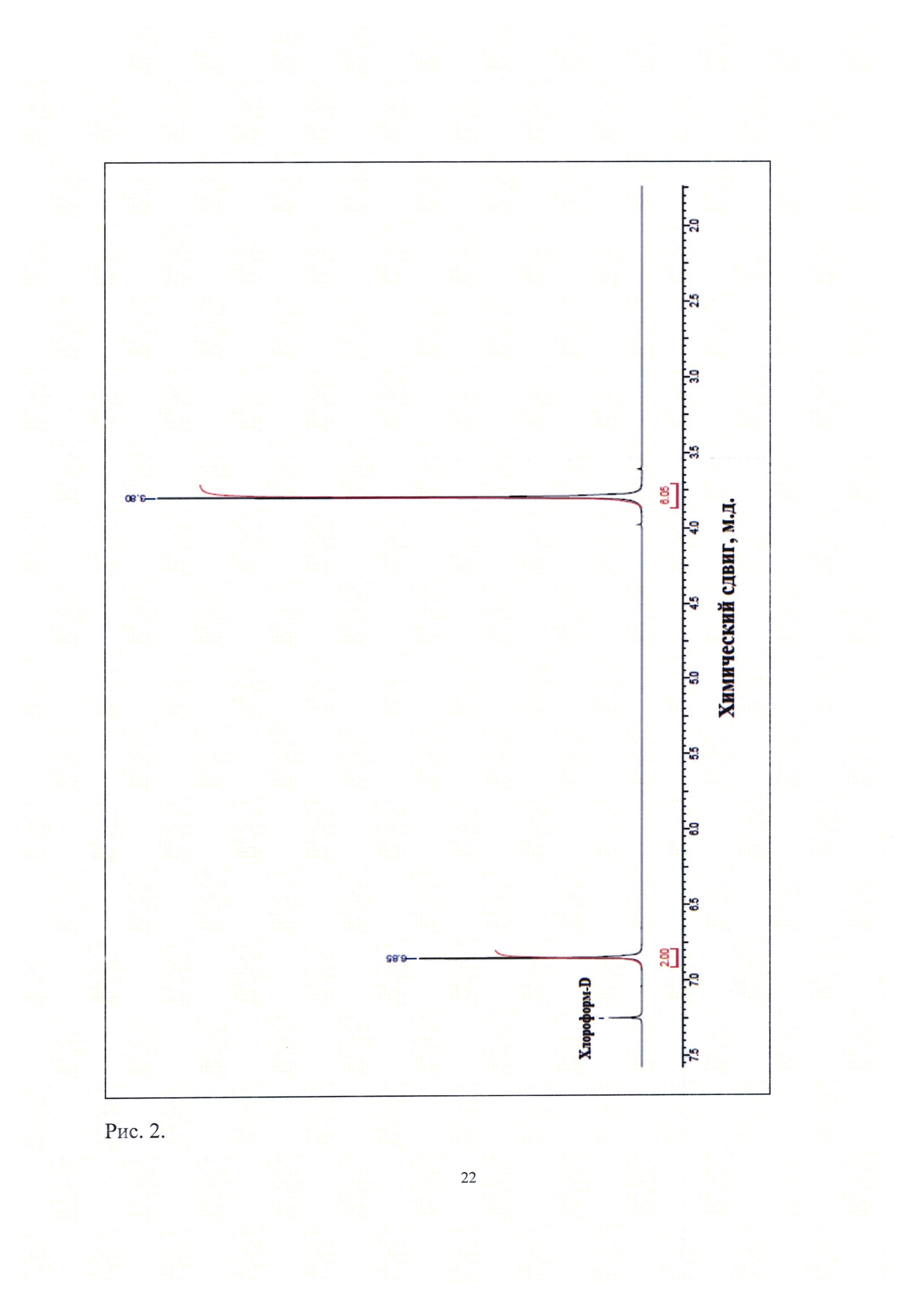
Рис. 2. ЯМР1Н-спектр новой, не известной ранее кристаллической β-модификации (Е)-диметилбутендиоата.
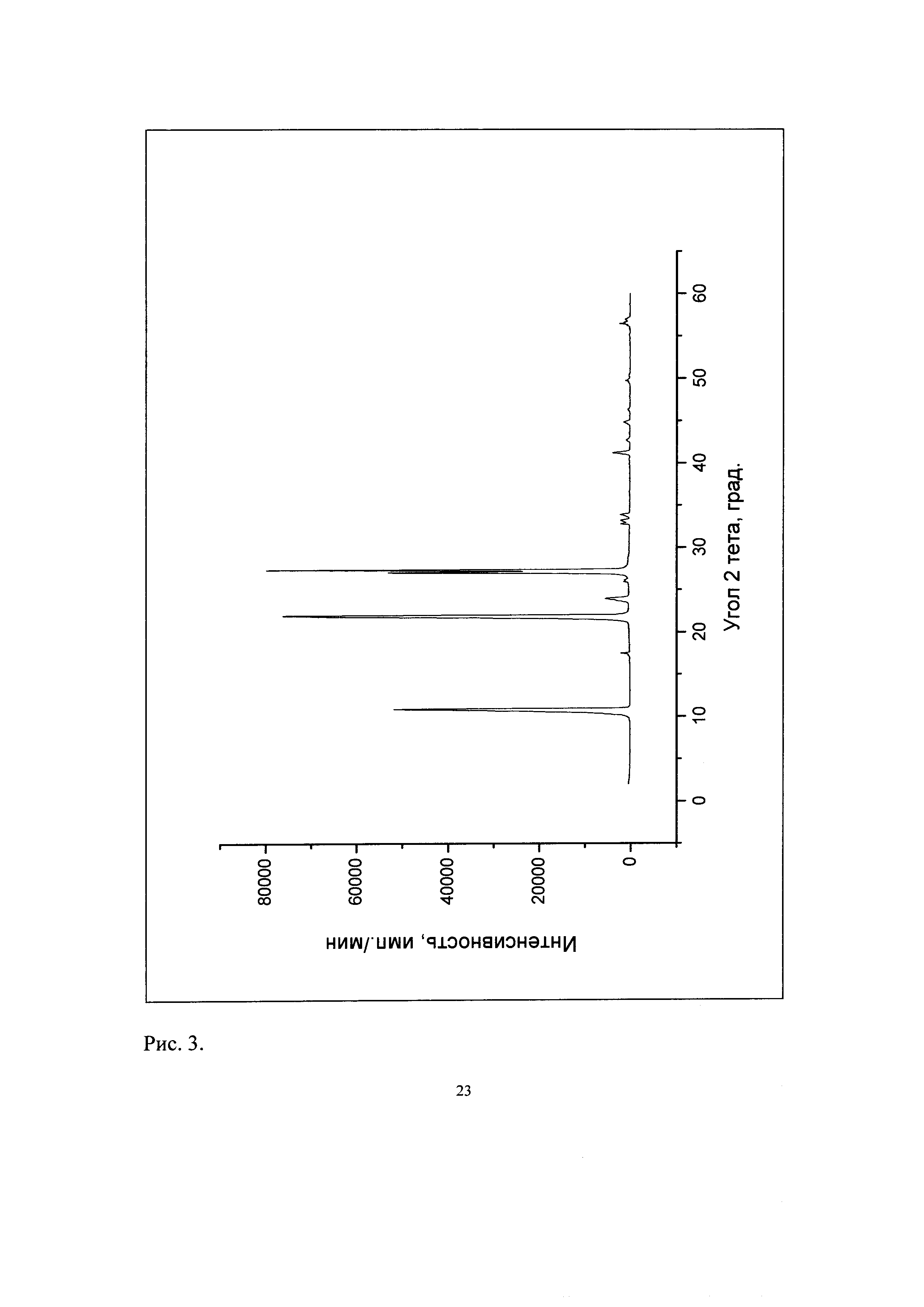
Рис. 3. Дифрактограмма известной кристаллической модификации диметилфумарата, которую использовали в качестве исходного вещества.
Рис. 4. Типичная дифрактограмма новой, не известной ранее кристаллической β-модификации (Е)-диметилбутендиоата.
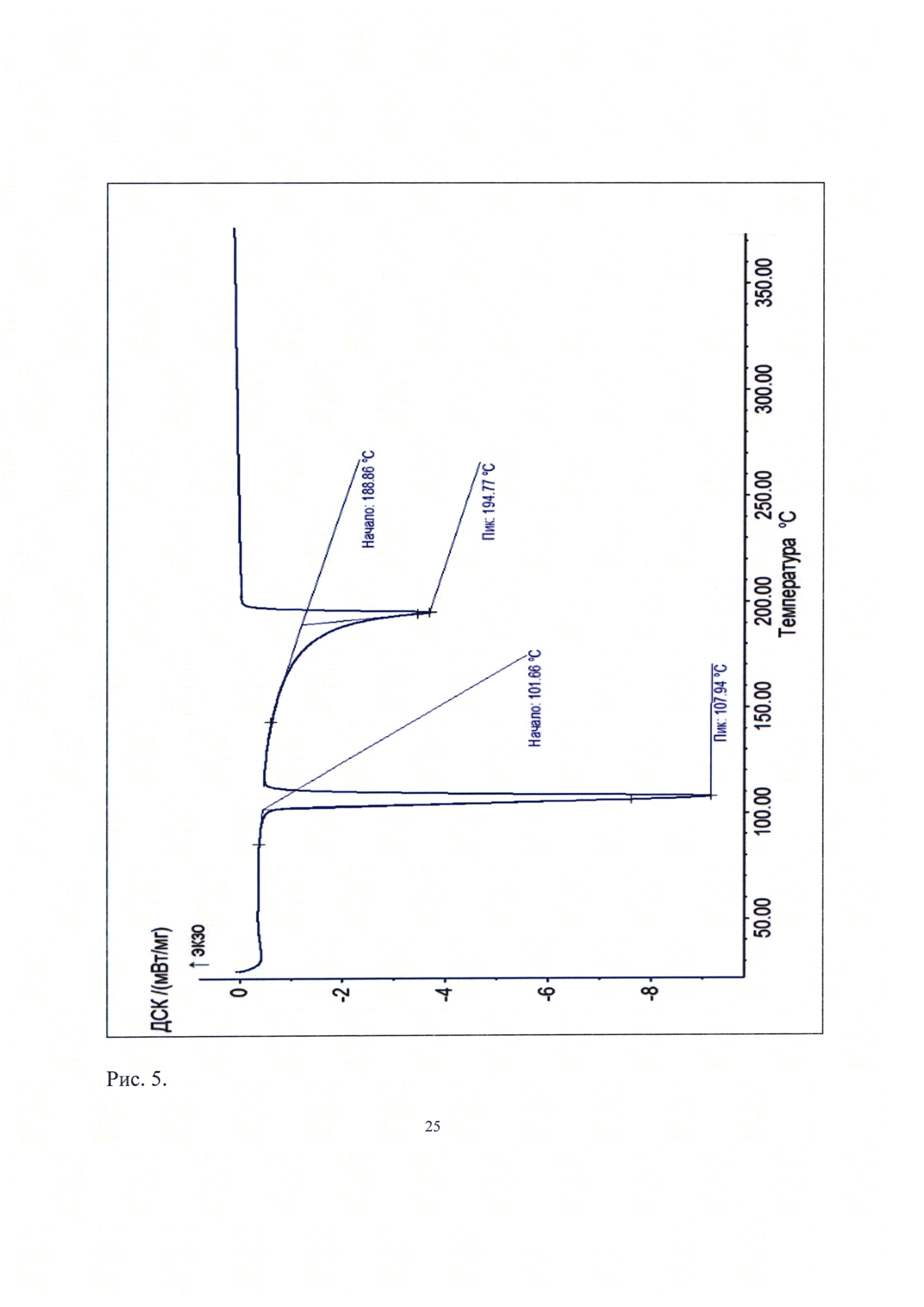
Рис. 5. Кривая дифференциальной сканирующей калориметрии известной кристаллической модификации диметилфумарата, которую использовали в качестве исходного вещества.
Рис. 6. Типичная кривая дифференциальной сканирующей калориметрии новой, не известной ранее кристаллической β-модификации (Е)-диметилбутендиоата.
Для идентификации полученного вещества был проведен комплекс физико-химических методов анализа.
Первоначально, методами ядерного магнитного резонанса (ЯМР1Н) и высокоэффективной жидкостной хроматографии (ВЭЖХ) была установлена идентичность химических формул известной кристаллической модификации диметилфумарата, которую использовали в качестве исходного вещества, и новой, не известной ранее кристаллической β-модификации (Е)-диметилбутендиоата.
Определение химических сдвигов исходного диметилфумарата и полученного из него вещества было проведено в его насыщенном растворе в дейтерированном хлороформе (хлороформ-d) на ЯМР-спектрометре высокого разрешения VXR-400 фирмы "VARIAN" (США). Полученные данные приведены на рис. 1 и 2 соответственно. Сравнение результатов, представленных на рис. 1 (известная кристаллическая модификация диметилфумарата), с данными, приведенными на рис. 2 [новая, не известная ранее кристаллическая β-модификация (Е)-диметилбутендиоата] показывает, что ЯМР-1Н-спектры исходного и полученного из него вещества практически идентичны, т.е. полученное вещество является (Е)-диметилбутендиоатом.
Хроматографическую подвижность известной кристаллической модификации диметилфумарата, которую использовали в качестве исходного вещества и, полученной из нее, новой, не известной ранее кристаллической β-модификации (Е)-диметилбудендиоата определяли методом ВЭЖХ на хроматографе Shimadzu LC - 20А с детектором SPD-M20A и с колонкой длиной 150 мм, сорбентом Grace Apollo CI 8 "Agilent" (США) с детектированием при длине волны 215,8 нм. В качестве подвижной фазы "А" использовали ацетонитрил (100%), а подвижной фазы "В" - фосфатный буферный раствор с рН=3, температура колонки была равна 42°С, а скорость потока - 1 мл/мин. Объем испытуемой пробы составил 3 мкл с концентрацией 0,5 мг/мл. Оказалось, что хроматограммы известной кристаллической модификации диметилфумарата, которую использовали в качестве исходного вещества, и новой, не известной ранее кристаллической β-модификации (Е)-диметилбутендиоата содержат по одному пику основного компонента с характерными временами удерживания 9,883 мин и 9,741 мин соответственно. Эти величины времен удерживания, в пределах ошибки определения, практически одинаковы. Чистота исследованных образцов, определенных методом ВЭЖХ составили 99,92% (исходное вещество) и 99,95% (новая, не известная ранее кристаллическая β-модификация диметилфумарата).
Проведенные методом ВЭЖХ эксперименты, свидетельствуют о том, что при получении новой, не известной ранее кристаллической β-модификации (Е)-диметилбутендиоата из исходного вещества - известной кристаллической модификации диметилфумарата, разложения исходного вещества не происходит.
Таким образом, экспериментальные результаты ядерного магнитного резонанса (ЯМР-!Н) и высокоэффективной жидкостной хроматографии (ВЭЖХ) однозначно свидетельствуют о том, что полученное вещество является (Е)-диметилбутендиоатом.
Для подтверждения того, что полученное вещество является новой, не известной ранее кристаллической β-модификацией (Е)- диметилбутендиоата, были проведены рентгенофазовый анализ (РФА) и термоаналитические исследования.
Рентгенофазовый анализ (РФА) известной кристаллической модификации диметилфумарата, которую использовали в качестве исходного вещества и полученного из нее порошка проводили на дифрактометре Rigaku D/MAX-2500 (Rigaku, Япония) на CuKα излучении (λ=1,54056 Å). Полученные данные РФА для известной кристаллической модификации диметилфумарата, который использовали в качестве исходного вещества, приведены в табл. 1 и на рис. 3, а полученного из него вещества - в табл. 2 и на рис. 4. Сравнение полученных данных, представленных в табл. 2, табл. 1 и в патенте (ЕА 2013/91638 А1 от 30.05.2014 г.), а также на рис. 3, рис. 4, свидетельствует о том, что полученный порошок диметилфумарата является новой, не известной ранее кристаллической β-модификацией (Е)-диметилбутендиоата.
Таким образом, экспериментальные результаты рентгенофазового анализа однозначно свидетельствуют о том, что полученное вещество является новой, не известной ранее кристаллической β-модификацией (Е)-диметилбутендиоата. Она характеризуется отличной от других кристаллических модификаций диметилфумарата, совокупностью межплоскостных расстояний (d, Å) и их интенсивностью (Iотн., %): 8,590-6,10%; 8,315-57,09%; 5,376-2,91%; 5,093-7,48%; 4,126-9,92%; 4,096-52,31%; 3,744-100,00%; 3,421-5,48%; 3,285-14,19%; 2,889-2,87%; 2,806-1,74%; 2,718-2,22%; 2,650-3,56%; 2,594-2,91%; 2,481-1,70%; 2,255-1,48%; 2,190-5,97%; 2,117-3,69%; 2,031-1,57%; 1,964-1,74%; 1,913-1,27%; 1,816-1,48%; 1,626-1,57%.
Термоаналитические исследования известной кристаллической модификации диметилфумарата, которую использовали в качестве исходного вещества и полученного из нее порошка, проводили на термоанализаторе DSC 204 Fl Poenix (NETZSCH) в токе аргона при повышении температуры 10 град/мин. В качестве держателей образцов использовали алюминиевые кюветы. Навеска пробы составляла 1,2-4,6 мг. Полученные данные приведены на рис. 5 и рис 6. Видно, что на кривых дифференциальной сканирующей калориметрии известной кристаллической модификации диметилфумарата и полученной из нее новой, не известной ранее кристаллической β-модификации (Е)-диметилбутендиоата присутствуют по два эндотермических эффекта при температурах (107,9±0,5)°С; (194,8±0,5)°С (известная модификация диметилфумарата, рис. 5) и при (104,4±0,5)°С; (161,8±0,5)°С (новая, не известная ранее β-модификация диметилфумарата, рис. 6). При этом на кривой ДСК новой, не известной ранее β-модификации (Е)-диметилбутендиоата (рис. 6) эндотермические эффекты находятся в более низкотемпературной области по сравнению с известной модификацией диметилфумарата (рис. 5). Отметим, что аналогичных термоаналитических исследований для известных кристаллических модификаций (Форма I и известного диметилфумарата) в имеющихся у авторов литературных источниках не обнаружено.
Таким образом, проведенные термоаналитические эксперименты показали, что новая, не известная ранее кристаллическая β-модификация (Е)-диметилбутендиоата характеризуется, отличными от других модификаций диметилфумарата, двумя эндотермическими эффектами на кривой ДСК при температурах (104,4±0,5)°С и (161,8±0,5)°С.
Приведенные экспериментальные данные рентгенофазового анализа и термоаналитических исследований однозначно свидетельствуют о том, что полученная новая, не известная ранее кристаллическая β-модификация (Е)-диметилбутендиоата характеризуется отличной от других кристаллических модификаций диметилфумарата, совокупностью межплоскостных расстояний и соответствующих им интенсивностей и эндотермическими эффектами при определенных температурах на кривой дифференциальной сканирующей калориметрии.
Способ получения новой кристаллической β-модификации (Е)-диметилбутендиоата заключается в том, что кристаллическую субстанцию диметилфумарата испаряют при температуре (10…95)°С при остаточном давлении (4×10-2…5×10-4) Торр и конденсируют на охлажденную до -40°С…-196°С поверхность.
Отличие способа получения заявляемой новой, не известной ранее кристаллической β-модификации (Е)-диметилбутендиоата от способов получения известных кристаллических модификаций диметилфумарата состоит в том, что субстанцию диметилфумарата испаряют при температуре (10…95)°С при остаточном давлении (4×10-2…5×10-4) Торр и конденсируют на охлажденную до -40°С…-196°С поверхность.
При уменьшении температуры испарения ниже 10°С скорость сублимации уменьшается и образование частиц новой фазы переходит из стадии образования зародышей в стадию их роста, что приводит к частичному образованию перекристаллизованной известной кристаллической модификации диметилфумарата. Получить новую кристаллическую β-модификацию (Е)-диметилбутендиоата в чистом виде не удается.
При увеличении температуры испарения выше 95°С скорость сублимации увеличивается что приводит к самопроизвольному захвату потоком молекул частиц исходной кристаллической модификации диметилфумарата. Получить новую кристаллическую β-модификацию (Е)-диметил-бутендиоата в чистом виде не удается.
При увеличении остаточного давления в системе выше 4×10-2 Торр процесс испарения замедляется и образование частиц новой фазы переходит из стадии образования зародышей в стадию их роста, что приводит к частичному образованию исходной кристаллической модификации диметилфумарата. Кристаллическую β-модификацию (Е)-диметилбутендиоата в чистом виде получить не удается.
Уменьшение остаточного давления в реакторе ниже 5×10-4 Торр нецелесообразно, из-за экономических и аппаратурных затруднений.
При повышении температуры конденсации получаемого порошка выше -40°С процесс образования кристаллитов на конденсаторе замедляется и переходит на стенки системы, и как следствие - происходит существенное уменьшение выхода получаемого продукта.
Понижение температуры конденсации ниже -196°С нецелесообразно из-за экономических и аппаратурных затруднений.
Возможность осуществления предлагаемого изобретения иллюстрируется следующими примерами, но не ограничивается ими.
Пример 1. 25,00 г субстанции диметилфумарата помещают на поддон из нержавеющей стали, переносят в сублимационную камеру и испаряют при 10°С при остаточном давлении 4×10-2 Торр и температуре на конденсаторе -40°С…-43°С. Выход продукта - пушистого порошка почти белого цвета - составил 23,75 г (91,0 мас. %). По данным РФА полученное вещество характеризуется типичной дифрактограммой, представленной на рис. 4 и набором межплоскостных расстояний и их интенсивностями, совпадающих с соответствующими значениями для новой, не известной ранее кристаллической β-модификации (Е)-диметилбутендиоата, представленными в табл. 2. По данным термоаналитических исследований полученное вещество характеризуется типичной кривой дифференциальной сканирующей калориметрии, представленной на рис. 6 и совпадающей, в пределах ошибки определения, с соответствующими значениями для новой, не известной ранее кристаллической β-модификации (Е)-диметилбутендиоата. Кривая ДСК характеризуется двумя эндотермическими эффектами на кривой ДСК при температурах (103,9±0,5)°С и (162,0±0,5)°С. По данным ВЭЖХ чистота полученной новой, не известной ранее кристаллической β-модификации диметилфумарата составляет 99,97%.
Пример 2. 37,00 г субстанции диметилфумарата помещают на поддон из нержавеющей стали, переносят в сублимационную камеру и испаряют при 50°С при остаточном давлении 7×10-3 Торр и температуре на конденсаторе -72°С…-75°С. Выход продукта - пушистого порошка белого цвета - составил 32,93 г (89,0 мас. %). По данным РФА полученное вещество характеризуется типичной дифрактограммой, представленной на рис. 4 и набором межплоскостных расстояний и их интенсивностями, совпадающих с соответствующими значениями для новой, не известной ранее кристаллической β-модификации (Е)-диметилбутендиоата, представленными в табл. 2. По данным термоаналитических исследований полученное вещество характеризуется типичной кривой дифференциальной сканирующей калориметрии, представленной на рис. 6 и совпадающей, в пределах ошибки определения, с соответствующими значениями для новой, не известной ранее кристаллической β-модификации (Е)-диметилбутендиоата. Кривая ДСК характеризуется двумя эндотермическими эффектами на кривой ДСК при температурах (104,6±0,5)°С и (161,6±0,5)°С. По данным ВЭЖХ чистота полученной новой, не известной ранее кристаллической β-модификации диметилфумарата составляет 99,93%.
Пример 3. 1,00 г субстанции диметилфумарата помещают на поддон из нержавеющей стали, переносят в сублимационную камеру и испаряют при 95°С при остаточном давлении 5×10-4 Торр и температуре на конденсаторе -196°С. Выход продукта - пушистого порошка белого цвета - составил 0,93 г (93,0 мас. %). По данным РФА полученное вещество характеризуется типичной дифрактограммой, представленной на рис. 4 и набором межплоскостных расстояний и их интенсивностями, совпадающих с соответствующими значениями для новой, не известной ранее кристаллической β-модификации (Е)-диметилбутендиоата, представленными в табл. 2. По данным термоаналитических исследований полученное вещество характеризуется типичной кривой дифференциальной сканирующей калориметрии, представленной на рис. 6 и совпадающей, в пределах ошибки определения, с соответствующими значениями для новой, не известной ранее кристаллической β-модификации (Е)-диметилбутендиоата. Кривая ДСК характеризуется двумя эндотермическими эффектами на кривой ДСК при температурах (104,4±0,5)°С и (161,8±0,5)°С. По данным ВЭЖХ чистота полученной новой, не известной ранее кристаллической β-модификации диметилфумарата составляет 99,95%).
Пример 4. Фармацевтическая композиция. Для приготовления 10,00 г композиции, включающей в качестве действующего вещества кристаллическую β-модификацию диметилфумарата и вспомогательные вещества в соотношении (мас. %):
6,50 г порошка новой, не известной ранее кристаллической β-модификации (Е)-диметилбутендиоата смешивают в течение 10 минут в керамической ступке с вспомогательными веществами: 2,89 г микрокристаллической целлюлозой (по фармакопее США и Европейской фармакопее), 0,50 г кроскармеллозой натрия (по фармакопее США и Европейской фармакопее), 0,06 г кремнием диоксидом коллоидным (по фармакопее США и Европейской фармакопее), 0,05 г магнием стеаратом (по ТУ 6-09-16-1533-90). Полученную смесь подвергали физико-химическим и биологическим методам анализа. По данным РФА в полученной смеси присутствует вещество, которое характеризуется набором межплоскостных расстояний и их интенсивностями, совпадающих с соответствующими значениями для новой, не известной ранее кристаллической β-модификации (Е)-диметилбутендиоата, представленными в таблице 2.
Аналогичным способом и идентичным по составу была приготовлена композиция на основе известной кристаллической модификации диметилфумарата, которую использовали в качестве исходного вещества. Полученную смесь подвергали физико-химическим и биологическим методам анализа. По данным РФА в полученной смеси присутствует вещество, которое характеризуется набором межплоскостных расстояний и их интенсивностями, совпадающих с соответствующими значениями для известной модификации (Е)-диметилбутендиоата, представленными в таблице 1.
Биологические эксперименты проводили на кроликах-самцах массой 2,0-2,5 кг. Для получения надежных результатов в параллельных сериях опытов использовали не менее 5ти кроликов. Определение времени появления диметилфумарата в крови проводили методом in vivo при пероральном введении композиции с последующим забором плазмы из ушной раковины. Во всех случаях количество вводимого в животное действующего вещества составляло 6,15 мг смеси (4,00 мг диметилфумарата). Оказалось, что для композиции, содержащей новую, не известную ранее кристаллическую β-модификацию (Е)-диметилбутендиоата время появления в крови кроликов равно 16±3 мин, а для известной композиции, содержащей в качестве действующего вещества известную кристаллическую модификацию диметилфумарата - 24±3 мин.
Таким образом, нами обнаружена новая, не известная ранее кристаллическая β-модификация (Е)-диметилбутендиоата, предложены способ ее получения и применение ее для приготовления фармацевтической композиции в качестве средства для лечения тяжелых форм псориаза, рассеянного склероза, липоидного некробиоза, кольцевидной гранулемы, красного волосяного лишая и т.д.
Полученная новая, не известная ранее кристаллическая β-модификация (Е)-диметилбутендиоата характеризуется, отличным от известных кристаллических модификаций диметилфумарата набором межплоскостных расстояний (d, Å) и соответствующих им интенсивностей (Iотн., %): 8,590-6,10%; 8,315-57,09%; 5,376-2,91%; 5,093-7,48%; 4,126-9,92%; 4,096-52,31%; 3,744-100,00%; 3,421-5,48%; 3,285-14,19%; 2,889-2,87%; 2,806-1,74%; 2,718-2,22%; 2,650-3,56%; 2,594-2,91%; 2,481-1,70%; 2,255-1,48%; 2,190-5,97%; 2,117-3,69%; 2,031-1,57%; 1,964-1,74%; 1,913-1,27%; 1,816-1,48%; 1,626-1,57% и двумя эндотермическими эффектами на кривой ДСК при температурах (104,4±0,5)°С и (161,8±0,5)°С.
Кроме того, новая, не известная ранее кристаллическая β модификация (Е)-диметилбутендиоата отличается повышенной биологической активностью в составе фармацевтической композиции по сравнению с действием известной кристаллической модификации диметилфумарата.
Из вышеизложенного можно сделать вывод о том, что заявляемая новая, не известная ранее кристаллическая β-модификация (Е)-диметилбутендиоата, способ ее получения и применение ее для приготовления фармацевтической композиции в качестве средства для лечения тяжелых форм псориаза, рассеянного склероза, липоидного некробиоза, кольцевидной гранулемы, красного волосяного лишая и т.д. являются новыми и удовлетворяют критериям «изобретательский уровень» и «промышленная применимость».

Реферат
Изобретение относится к органической химии и касается новой кристаллической модификации (Е)-диметилбутендиоата, названной β-модификацией, способа ее получения и фармацевтической композиции на ее основе, которая может быть использована в фармацевтической промышленности и медицине в качестве средства для лечения тяжелых форм псориаза, рассеянного склероза, липоидного некробиоза, кольцевидной гранулемы, красного волосяного лишая и т.д. Новая кристаллическая β-модификация диметилфумарата, характеризующаяся определенным набором дифракционных максимумов (d, Å) и их интенсивностью (I, %) и двумя эндотермическими эффектами на кривой ДСК при определенных температурах, предложены способ ее получения и применение ее для приготовления фармацевтической композиции. Заявляемая новая модификация представляет собой пушистый порошок от белого до почти белого цвета, без запаха, растворимый в хлороформе, умеренно растворимый в низших спиртах и малорастворимый в воде. 3 н.п. ф-лы, 6 ил., 2 табл., 4 пр.

Комментарии