Соли производного пиперазина с салициловой и гентизиновой кислотами - RU2412184C2
Код документа: RU2412184C2
Чертежи







Описание
Перекрестная ссылка на родственную заявку
Данная заявка претендует на приоритет согласно предварительной заявке на патент № 60/716161, поданной 12 сентября 2005 г., полное содержание которой включается в настоящий документ в виде ссылки.
Область техники, к которой относится изобретение
Настоящее изобретение обеспечивает солевые формы и композиции на их основе, применимые в качестве модуляторов одного или нескольких сопряженных с G-белком рецепторов (GPCR).
Предпосылки создания изобретения
Семейство сопряженных с G-белком рецепторов (GPCR) - это самое большое известное генное семейство, представляющее более чем 1% генома человека и осуществляющее широкий диапазон биологических функций (включая различные аутокринные, паракринные и эндокринные процессы). Суперсемейство GPCR является также самым задействованным генным семейством в фармацевтической промышленности для разработки терапевтических соединений. GPCR были классифицированы на родопсиноподобные GPCR, секретиноподобные GPCR, рецепторы цАМФ, грибковые сопряженные рецепторы феромонов и семейство метаботропных глутаматных рецепторов. Родопсиноподобные GPCR сами по себе представляют собой широко распространенное семейство белков, которое включает рецепторы гормонов, нейротрансмиттеров и световые рецепторы, которые преобразуют внеклеточные сигналы посредством взаимодействия с (G) белками, связывающими гуаниновые нуклеотиды. Несмотря на то, что активирующие их лиганды широко варьируются по структуре и характеру, аминокислотные последовательности родопсиноподобных GPCR очень похожи, и считается, что они принимают общее строение, включающее 7 трансмембранных (ТМ) перекрывающихся α-спиралей, и связываются с G-белками в клетке, которые диссоциируют от рецептора для связывания с агонистом и инициируют или ингибируют сигнальные механизмы вторичного посредника. См.: Lander et al. Nature 409:860 (2001); Basic and clinical pharmacology, 8th Ed., Katzung. USA: The McGraw Hill Companies, Inc. (2001).
Семейство родопсиноподобных GPCR включает несколько классов рецепторов, которые разнообразно распределяются по всей центральной нервной системе (ЦНС) и многим периферическим областям и непосредственно связаны с многообразием состояний ЦНС и психоневрологических состояний. Эти рецепторы включают дофаминовые («D») рецепторы и 6 из 7 главных подтипов серотониновых (5-гидрокситриптамин, «5HT») рецепторов (5HT1,2 и4-7 подтипы рецепторов являются рецепторами GPCR, тогда как 5HT3 подтипы рецепторов являются управляемыми лигандами Na+/K+ ионными каналами).
Дофаминовые нейроны позвоночной центральной нервной системы непосредственно связаны с инициированием и выполнением движения, поддержанием эмоциональной стабильности и регуляцией гипофизарной функции. Связывание дофамина с внеклеточной бороздкой связывания D-рецепторов активирует G-белки - подтипы рецепторов D1 и D5 («D1-подобные») связываются со стимулирующими G-белками, тогда как подтипы рецепторов 2-4 («D2-подобные») связываются с ингибирующими G-белками. D2-подобные рецепторы находятся по всему мозгу и в гладких мышцах и в пресинаптических окончаниях и оказывают ингибирующее действие на нейротрансмиссию при связывании с агонистом. В частности, D2-рецепторы имеются в изобилии и широко распространены в стриатуме, лимбической системе, таламусе, гипоталамусе и гипофизе. Связывание антагониста с D2-рецепторами ингибирует связывание агониста и, следовательно, предотвращает ингибирование последующих сигнальных механизмов. Антагонисты D2-рецепторов применяются в лечении психозов (например, шизофрении, маниакального синдрома, психотической депрессии и биполярного расстройства) и являются полезными для кратковременного седативного эффекта при агрессии или тревожном возбуждении (например, амисульприд, клозапин, галоперидол, немонаприд, пимозид, ремоксиприд, спиперон, сульпирид) и могут применяться для лечения лекарственного привыкания, тогда как агонисты D2-рецепторов применяются в лечении болезни Паркинсона и для подавления секреции пролактина из опухолей гипофиза (например, апоморфин, бромкриптин, дигидроэрготамин, пирибедил, хинпирол) и для лечения синдрома усталых ног (СУН; например, прамипексл, ропинирол). См.: Basic and clinical pharmacology, 8th Ed., Katzung. USA: The McGraw Hill Companies, Inc. (2001), Pharmacology 4th Ed., Rang et al. Edinburgh, UK: Harcourt Publishers Ltd. (2001); Sedvall et al. The Lancet, 346:743-749, (1995); Hietala. The Lancet, 346:1130-1131, (1995); Kemppainen et al. Eur J Neurosci., 18:149-154 (2003).
5-гидрокситриптамин распространен повсеместно в растениях и животных. Он является важным нейротрансмиттером и местным гормоном в ЦНС и кишечном тракте и непосредственно связан с обширным множеством физиологических и патофизиологических путей метаболизма. Связывание 5-гидрокситриптамина с внеклеточной бороздкой связывания 5HT-рецепторов активирует G-белки - подтипы рецепторов 5HT1, как известно, связываются с ингибирующими G-белками, тогда как подтипы 2, 4, 6 и 7, как известно, связываются со стимулирующими G-белками. Из них подтипы рецепторов 5HT1 (по меньшей мере, 5 известных), как известно, встречаются главным образом в мозге и мозговых кровеносных сосудах, где они способствуют нервному торможению и сужению кровеносных сосудов. Специфические агонисты 5HT1-рецепторов применяют в терапии мигрени (например, суматриптан) и в лечении стресса/тревожности (например, буспирон), тогда как антагонисты рекомендованы для лечения психоза (например, спиперон, метиотепин). Кроме того, регуляция подтипов рецепторов 5HT1непосредственно связана с лекарственным привыканием, болезнью Альцгеймера, болезнью Паркинсона, депрессией, рвотой и расстройствами пищевого поведения. Подтипы рецепторов 5HT2 (по меньшей мере, 3 известных) находятся по всей ЦНС и многим периферическим областям, где они производят возбуждающий неврональный и гладкомышечный эффекты. Антагонисты 5HT2-рецепторов применяются в терапии мигрени (например, метисергид) и проявили способность лечения склеродермии и феномена Рейно (например, кетансерин). 5HT3-рецепторы, как известно, встречаются главным образом в периферической нервной системе, а антагонисты применяются в качестве противорвотных средств (например, ондансетрон, трописетрон). 5HT4-рецепторы находятся в мозге, а также в сердце, мочевом пузыре и желудочно-кишечном (ЖК) тракте. В ЖК тракте они производят неврональное раздражение и способствуют эффекту 5HT на стимулирование перистальтики. Специфические антагонисты 5HT4-рецепторов применяются для лечения ЖК расстройств (например, метоклопрамид). Подтипы 5HT-рецепторов 5 (по меньшей мере, 5 известных), 6 и 7 также находятся по всей ЦНС и могут быть потенциальными мишенями для низкомолекулярных лекарственных средств. В частности, подтип рецепторов 5HT7 непосредственно связан с депрессией, психозом, болезнью Паркинсона, болезнью Альцгеймера, болезнью Гентингтона, мигренью, стрессом/тревожностью, расстройствами пищевого поведения и рвотой. См.: Basic and clinical pharmacology, 8th Ed., Katzung. USA: The McGraw Hill Companies, Inc. (2001), Pharmacology 4th Ed., Rang et al. Edinburgh, UK: Harcourt Publishers Ltd. (2001); Kleven et al. European Journal of Pharmacology, 281:219-228 (1995); U.S. Pat. No. 5162375; Leone et al. Neuro Report, 9:2605-2608 (1998); U.S. Pat. No. 4771053; WO 01/52855; De Vry et al. European Journal of Pharmacology, 357:1-8 (1998); Wolff et al. European Journal of Pharmacology, 340:217-220 (1997); Alfieri et al. British Journal of Cancer, 72:1013-1015 (1995); Wolff et al. Pharmacology Biochemistry and Behavior, 52:571-575 (1995); Lucot. European Journal of Pharmacology, 253:53-60 (1997); U.S. Pat. No. 5824680; U.S. Pat. No. 4687772; Rasmussen et al. Annual Reports in Medicinal Chemistry, 30:1-9 (1995); WO 00/16777; U.S. Pat. No. 4438119; Millan, Journal of Pharmacology and Experimental Therapeutics, 295:853-861 (2000); WO 93/04681; Miyamoto, et al. Current Opinion in CPNS Investigational Drugs, 2:25 (2000); Hagger, et al. Biol. Psychiatry, 34:702 (1993); Sharma et al. J. Clin. Psychopharmacol., 18:128 (1998); Lee et al. J. Clin. Psychiatry, 55:82 (1994); Fujii, et al. J. Neuropsychiatry Clin. Neurosci., 9:240 (1997); Mason et al. Eur. J. of Pharmacol., 221:397 (1992); Newman-Tancredi et al. Neuropharmacology, 35:119, (1996); Sumiyoshi et al. J. Clin. Pharmacol., 20:386 (2000); Carli et al. Eur. J. Neurosci., 10:221 (1998); Meneses et al. Neurobiol. Learn. Mem., 71:207 (1999); и Glennon et al. Neuroscience and Behavioral Reviews, 14:3547 (1990).
Действие 5HT в синапсах оканчивается его Na+/K+-опосредованным обратным захватом через пресинаптическую мембрану. Ингибиторы обратного захвата 5HT применяются для лечения депрессии, стресса/тревожности, панического расстройства, обсессивно-компульсивного расстройства, расстройств пищевого поведения и социофобий (например, циталопрам, кломипрамин, флуоксетин, флувоксамин, индатралин, зимелидин) и могут быть применимыми в лечении мигрени, психоза, болезни Альцгеймера, болезни Паркинсона, болезни Гентингтона, лекарственного привыкания, расстройств пищевого поведения, склеродермии и феномена Рейно, расстройств ЖК тракта, связанных с регуляцией перистальтики и/или рвоты. См.: Basic and clinical pharmacology, 8th Ed., Katzung. USA: The McGraw Hill Companies, Inc. (2001), Pharmacology 4th Ed., Rang et al. Edinburgh, UK: Harcourt Publishers Ltd. (2001); Masson et al. Pharm. Rev. 51:439 (1999); и, кроме того, ссылки на предыдущие пункты.
Таким образом, было бы желательно обеспечить соединения, которые модулируют GPCR, в форме подходящей для введения пациенту, нуждающемуся в лечении любого из указанных расстройств. В частности, было бы желательно, чтобы данные соединения проявляли дополнительные свойства, такие как хорошая растворимость, устойчивость и простота технологии приготовления лекарственного средства и т.д.
Сущность изобретения
В настоящее время было установлено, что новые солевые формы настоящего изобретения и композиции на их основе применимы в качестве модуляторов одного или нескольких GPCR и проявляют желаемые свойства для этого. В общем, данные солевые формы и фармацевтически приемлемые композиции на их основе применимы для лечения или уменьшения тяжести множества заболеваний или расстройств, включая, но не ограничиваясь, болезнь Паркинсона, психоз (например, шизофрения, маниакальный синдром, психотическая депрессия и биполярное расстройство), депрессию, стресс/тревожность, болезнь Альцгеймера, болезнь Гентингтона, паническое расстройство, обсессивно-компульсивное расстройство, расстройство пищевого поведения, лекарственное привыкание, социофобии, агрессию или тревожное возбуждение, мигрень, склеродермию и феномен Рейно, рвоту, расстройства ЖК тракта, связанные с регуляцией перистальтики, СУН и повышение секреции пролактина из опухолей гипофиза.
Краткое описание чертежей
На фиг.1 изображена порошковая рентгенограмма соединения 2.
На фиг.2 изображена порошковая рентгенограмма соединения 3.
На фиг.3 изображен1H ЯМР спектр соединения 2, полученный при 500 МГц в DMSO-d6.
На фиг.4 изображен1H ЯМР спектр соединения 3, полученный при 500 МГц в DMSO-d6.
На фиг.5 изображен1H ЯМР спектр соединения 1, полученный при 500 МГц в DMSO-d6.
Подробное описание изобретения
Общее описание некоторых аспектов изобретения:
Международная заявка на патент PCT/EP/00/08190 (международная публикация WO 01/14330) описывает разнообразные индолсодержащие производные пиперазина, включая соединение 1 (изображенный 8-{4-[3-(5-фтор-1H-индол-3-ил)пропил]пиперазин-1-ил}-2-метил-4H-бензо[1,4]оксазин-3-он), которое проявляет антагонистическую активность к D2-рецепторам и ингибирующую активность по отношению к обратному захвату 5HT в терапевтических моделях.

Кроме того, соединение 1 является активным в терапевтических моделях, которые чувствительны к клинически важным нейролептикам, антидепрессантам и анксиолитикам, а также при болезни Паркинсона. Таким образом, соединение 1 применимо для лечения болезни Паркинсона, психоза (например, шизофрении, маниакального синдрома, психотической депрессии и биполярного расстройства), депрессии, стресса/тревожности, панического расстройства, болезни Альцгеймера, обсессивно-компульсивного расстройства, расстройства пищевого поведения, лекарственного привыкания, социофобий, при агрессии или тревожном возбуждении, мигрени, склеродермии и феномена Рейно, рвоты, расстройств ЖК тракта, связанных с регуляцией перистальтики, СУН и для подавления повышения секреции пролактина из опухолей гипофиза. Кроме того, соединение 1 имеет низкую склонность вызывать каталепсию у грызунов и, следовательно, менее вероятно вызывать экстрапирамидные побочные эффекты, чем уже существующие нейролептики. См.: WO 01/14330; van der Heyden and Bradford. Behav. Brain Res. 31:61 (1988); van der Poel et al. Psychopharmacology, 97:147 (1989); и Ungerstredt. Acta Physiol. Scand. 82:(suppl. 367) 69 (1971).
Нестероидные противовоспалительные лекарственные средства, как известно, ингибируют синтез простагландина и других сопутствующих продуктов метаболизма арахидоновой кислоты посредством взаимодействия с ферментами циклооксигеназами (ЦОГ). Существует доказательство того, что сверхактивная интенсивность действия ЦОГ проявляется в мозгу пациентов, страдающих шизофренией, и, таким образом, расстройства в метаболическом пути простагландина непосредственно связаны с патогенезом шизофрении. Таким образом, не желая привязываться к какой-либо отдельной теории, считают, что применение солей, образованных из соединения 1 с кислотой, способных к взаимодействию с образованием простагландинов или взаимодействию с ЦОГ ферментом, обеспечило бы дополнительные преимущества и/или синергические эффекты в лечении пациентов с шизофренией и другими психотическими расстройствами. См.: Das and Khan. Prostaglandins Leukot Essent Fatty Acids 58:165 (1998).
В общем настоящее изобретение обеспечивает соли соединения 1 с салициловой или гентизиновой кислотами (2,5-дигидроксибензоат).
В некоторых вариантах осуществления настоящее изобретение обеспечивает салицилат соединения 1, представленный как соединение 2:
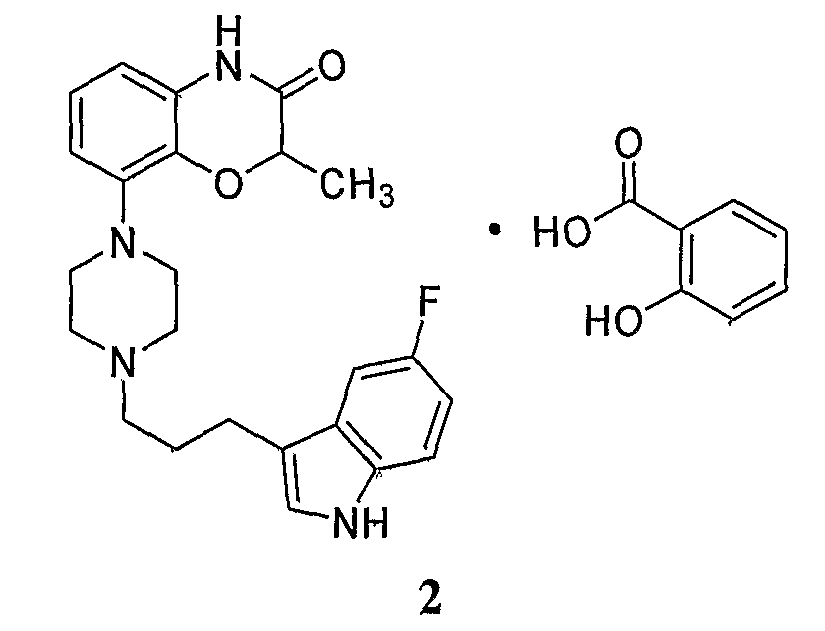
Любой специалист в данной области оценит, что салициловая кислота и соединение 1 связываются ионной связью с образованием соединения 2. Предполагают, что соединение 2 может существовать в виде многообразия физических форм. Например, соединение 2 может быть в растворе, суспензии или в твердой форме. В некоторых вариантах осуществления соединение 2 находится в твердой форме. Когда соединение 2 находится в твердой форме, то указанное соединение может быть аморфным, кристаллическим или их смесями.
В некоторых вариантах осуществления соединение 2 находится в кристаллической твердой форме. В других вариантах осуществления соединение 2 является кристаллическим твердым, по существу не содержащим аморфное соединение 2. Использованное в контексте данного документа понятие «по существу не содержащий аморфное соединение 2» означает, что соединение не содержит значительного количества аморфного соединения 2. В некоторых вариантах осуществления присутствует, по меньшей мере, 95% по массе кристаллического соединения 2. В еще одних вариантах осуществления изобретения присутствует, по меньшей мере, 99% по массе кристаллического соединения 2. Согласно одному аспекту соединение 2 имеет порошковую рентгенограмму, по существу совпадающую с порошковой рентгенограммой, изображенной на фиг.1. Согласно другому варианту осуществления соединение 2 является кристаллическим и характеризуется тем, что имеет один или несколько пиков, выбранных из пиков при примерно 8,2, 10,799 или 19,050 градуса 2-тета.
Согласно другому варианту осуществления настоящее изобретение обеспечивает соединение 2 в виде аморфного твердого вещества. Аморфные твердые вещества хорошо известны любому специалисту в данной области и обычно получаются такими способами, как лиофилизация, плавление или осаждение из надкритической жидкости наряду с прочим.
В других вариантах осуществления настоящее изобретение обеспечивает соединение 2, по существу свободное от примесей. Использованное в контексте данного документа понятие «по существу свободное от примесей» означает, что соединение не содержит значительного количества посторонних веществ. Данные посторонние вещества могут включать избыток салициловой кислоты, избыток соединения 1, остатки растворителей или любые другие примеси, которые могут появиться в результате получения и/или выделения соединения 2. В некоторых вариантах осуществления присутствует, по меньшей мере, примерно 95% по массе соединения 2. В еще одних вариантах осуществления изобретения присутствует, по меньшей мере, примерно 99% по массе соединения 2.
Согласно одному варианту осуществления соединение 2 присутствует в количестве, по меньшей мере, примерно 97, 97,5, 98, 98,5, 99, 99,5, 99,8 массовых процентов, причем процентные содержания основываются на общей массе композиции. Согласно другому варианту осуществления соединение 2 содержит не более чем примерно 2,0 процента площади пиков ВЭЖХ всех органических примесей и в некоторых вариантах осуществления не более чем примерно 1,5 процента площади пиков ВЭЖХ всех органических примесей относительно общей площади пиков ВЭЖХ хроматограммы. В других вариантах осуществления соединение 2 содержит не более чем примерно 0,6 процента площади пиков ВЭЖХ любой одной примеси и в некоторых вариантах осуществления не более чем 0,5 процента площади пиков ВЭЖХ любой одной примеси относительно общей площади пиков ВЭЖХ хроматограммы.
Подразумевается также, что структура, изображенная для соединения 2, включает все изомерные (например, энантиомерные или конформационные) формы структуры. Например, как R, так и S конфигурации при стереогенном атоме углерода включены в данное изобретение. Следовательно, отдельные стереохимические изомеры, также как энантиомерные и конформационные смеси настоящего соединения, находятся в рамках объема данного изобретения. Кроме того, все таутомерные формы соединения 2 находятся в рамках объема данного изобретения. Кроме того, подразумевается, что структуры, описанные в контексте данного документа, включают соединения, которые отличаются только присутствием одного или нескольких изотопно обогащенных атомов. Например, соединения, имеющие настоящую структуру, за исключением замещения водорода дейтерием или тритием или замещения углерода C13- или C14-обогащенным атомом углерода, находятся в рамках объема данного изобретения.
В некоторых вариантах осуществления настоящее изобретение обеспечивает гентизинат соединения 1, представленный как соединение 3:

Любой специалист в данной области примет во внимание, что гентизиновая кислота и соединение 1 связываются ионной связью с образованием соединения 3. Предполагают, что соединение 3 может существовать в многообразии физических форм. Например, соединение 3 может быть в растворе, суспензии или в твердой форме. В некоторых вариантах осуществления соединение 3 находится в твердой форме. Когда соединение 3 находится в твердой форме, то указанное соединение может быть аморфным, кристаллическим или их смесями.
В некоторых вариантах осуществления соединение 3 находится в кристаллической твердой форме. В других вариантах осуществления соединение 3 является кристаллическим твердым, по существу не содержащим аморфное соединение 3. Использованное в контексте данного документа понятие «по существу не содержащий аморфное соединение 3» означает, что соединение не содержит значительного количества аморфного соединения 3. В некоторых вариантах осуществления присутствует, по меньшей мере, 95% по массе кристаллического соединения 3. В еще одних вариантах осуществления изобретения присутствует, по меньшей мере, 99% по массе кристаллического соединения 3. Согласно одному аспекту соединение 3 имеет порошковую рентгенограмму, по существу совпадающую с порошковой рентгенограммой, изображенной на фиг.2. Согласно другому варианту осуществления соединение 3 является кристаллическим и характеризуется тем, что имеет один или несколько пиков, выбранных из пиков при примерно 19,080, 20,259 или 24,981 градуса 2-тета.
Согласно другому варианту осуществления настоящее изобретение обеспечивает соединение 3 в виде аморфного твердого вещества. Аморфные твердые вещества хорошо известны любому специалисту в данной области и обычно получаются такими способами, как лиофилизация, плавление или осаждение из надкритической жидкости наряду с прочим.
В других вариантах осуществления настоящее изобретение обеспечивает соединение 3, по существу свободное от примесей. Использованное в контексте данного документа понятие «по существу свободное от примесей» означает, что соединение не содержит значительного количества посторонних веществ. Данные посторонние вещества могут включать избыток салициловой кислоты, избыток соединения 1, остатки растворителей или любые другие примеси, которые могут появиться в результате получения и/или выделения соединения 3. В некоторых вариантах осуществления присутствует, по меньшей мере, примерно 95% по массе соединения 3. В еще одних вариантах осуществления изобретения присутствует, по меньшей мере, примерно 99% по массе соединения 3.
Согласно одному варианту осуществления соединение 3 присутствует в количестве, по меньшей мере, примерно 97, 97,5, 98, 98,5, 99, 99,5, 99,8 массовых процентов, причем процентные содержания основываются на общей массе композиции. Согласно другому варианту осуществления соединение 3 содержит не более 2,0 процентов площади пиков ВЭЖХ всех органических примесей и в некоторых вариантах осуществления не более чем 1,5 процента площади пиков ВЭЖХ всех органических примесей относительно общей площади пиков ВЭЖХ хроматограммы. В других вариантах осуществления соединение 3 содержит не более 0,6 процента площади пиков ВЭЖХ любой одной примеси и в некоторых вариантах осуществления не более чем 0,5 процента площади пиков ВЭЖХ любой одной примеси относительно общей площади пиков ВЭЖХ хроматограммы.
Подразумевается также, что структура, изображенная для соединения 3, включает все изомерные (например, энантиомерные или конформационные) формы структуры. Например, как R, так и S конфигурации при стереогенном атоме углерода включены в данное изобретение. Следовательно, отдельные стереохимические изомеры, также как энантиомерные и конформационные смеси настоящего соединения, находятся в рамках объема данного изобретения. Кроме того, все таутомерные формы соединения 3 находятся в рамках объема данного изобретения. Кроме того, подразумевается, что структуры, описанные в контексте данного документа, включают соединения, которые отличаются только присутствием одного или нескольких изотопно обогащенных атомов. Например, соединения, имеющие настоящую структуру, за исключением замещения водорода дейтерием или тритием или замещения углерода C13- или C14-обогащенным атомом углерода, находятся в рамках объема данного изобретения.
Общие способы получения настоящих соединений
Соединение 1 получают согласно способам, подробно описанным в PCT публикации номер WO 01/14330, полное содержание которой включается в настоящий документ в виде ссылки.
Другой аспект настоящего изобретения обеспечивает способ получения соединения 2:

включающий стадии:
предоставления соединения 1:

объединения соединения 1 с салициловой кислотой в подходящем растворителе; и,
необязательно, выделения соединения 2.
Подходящий растворитель может растворять один или несколько компонентов реакции, или наоборот, подходящий растворитель может способствовать получению суспензии одного или нескольких компонентов реакции. Примеры подходящих растворителей, применяемых в настоящем изобретении, представляют собой протонный растворитель, полярный апротонный растворитель или их смеси. В некоторых вариантах осуществления подходящие растворители включают простой эфир, сложный эфир, спирт, кетон или их смеси. В некоторых вариантах осуществления подходящим растворителем является метанол, этанол, изопропанол или ацетон, причем указанный растворитель является безводным или в сочетании с водой или гептаном. В других вариантах осуществления подходящие растворители включают тетрагидрофуран, диметилформамид, диметилсульфоксид, глим, диглим, метил-трет-бутиловый эфир, трет-бутанол, н-бутанол и ацетонитрил. В других вариантах осуществления подходящим растворителем является безводный этанол.
Согласно другому варианту осуществления настоящее изобретение обеспечивает способ получения соединения 2:

включающий стадии:
смешивания соединения 1:

с подходящим растворителем и нагревания с образованием раствора;
добавления салициловой кислоты к указанному раствору;
и, необязательно, выделения соединения 2.
В некоторых вариантах осуществления соединение 1 растворяют в подходящем растворителе при нагревании. В некоторых вариантах осуществления соединение 1 растворяют при температуре примерно 60°C. В других вариантах осуществления соединение 1 растворяют в подходящем растворителе при температуре примерно 40°C. В еще одних вариантах осуществления соединение 1 растворяют при температуре от 40°C до 60°C. В еще одних вариантах осуществления соединение 1 растворяют в подходящем растворителе при температуре дефлегмации подходящего растворителя. В других вариантах осуществления соединение 1 растворяют в подходящем растворителе без нагревания.
В некоторых вариантах осуществления раствор соединения 1 фильтруют перед добавлением салициловой кислоты. В других вариантах осуществления раствор соединения 1 не фильтруют перед добавлением салициловой кислоты.
В некоторых вариантах осуществления, в которых раствор соединения 1 нагревали до какой-либо температуры от примерно 40°C до примерно 60°C, раствор впоследствии охлаждают до какой-либо более низкой температуры, которая лежит от примерно 20°C до примерно 40°C, перед добавлением салициловой кислоты. В других вариантах осуществления, в которых раствор соединения 1 нагревали до какой-либо температуры от примерно 40°C до примерно 60°C, раствор впоследствии не охлаждают до какой-либо более низкой температуры перед добавлением салициловой кислоты.
В некоторых вариантах осуществления к соединению 1 добавляют примерно 1 эквивалент салициловой кислоты для получения соединения 2. В других вариантах осуществления к соединению 1 добавляют менее 1 эквивалента салициловой кислоты для получения соединения 2. В еще одних вариантах осуществления к соединению 1 добавляют более 1 эквивалента салициловой кислоты для получения соединения 2. В других вариантах осуществления к соединению 1 добавляют от примерно 1,0 до примерно 1,2 эквивалента салициловой кислоты для получения соединения 2. В еще одних вариантах осуществления к соединению 1 добавляют от примерно 0,9 до примерно 1,1 эквивалента салициловой кислоты для получения соединения 2. В другом варианте осуществления к соединению 1 добавляют от примерно 0,99 до примерно 1,01 эквивалента салициловой кислоты для получения соединения 2.
Будет принято во внимание, что салициловую кислоту можно добавлять к смеси соединения 1 и подходящего растворителя в любой подходящей форме. Например, можно добавлять салициловую кислоту в твердой форме или в виде раствора или суспензии в подходящем растворителе. Подходящим растворителем может быть тот же самый подходящий растворитель, как тот, который смешивают с соединением 1, или может быть другой растворитель. В некоторых вариантах осуществления салициловую кислоту смешивают с подходящим растворителем перед добавлением к соединению 1. Согласно другому варианту осуществления салициловую кислоту добавляют в виде раствора в подходящем растворителе. В других вариантах осуществления подходящий растворитель, в котором растворяют салициловую кислоту, является полярным протонным или полярным апротонным растворителем. Данные растворители включают спирты, простые эфиры и кетоны. Примеры подобных растворителей включают метанол, этанол, изопропанол, ацетон, тетрагидрофуран, диметилформамид, диметилсульфоксид, глим, диглим, метил-трет-бутиловый эфир, трет-бутанол, н-бутанол и ацетонитрил. В некоторых вариантах осуществления подходящий растворитель выбирают из указанных растворителей, и он является безводным. В других вариантах осуществления подходящий растворитель выбирают из указанных растворителей, и он является смесью с водой или гептаном. В другом варианте осуществления подходящим растворителем является безводный этанол.
В некоторых вариантах осуществления конечную смесь, содержащую соединение 2, охлаждают. В некоторых вариантах осуществления, в которых смесь, содержащую соединение 2, нагревают свыше примерно 20°C, раствор оставляют охлаждаться до температуры примерно 20°C. В других вариантах осуществления смесь, содержащую соединение 2, охлаждают ниже 20°C. В некоторых вариантах осуществления смесь, содержащую соединение 2, охлаждают до температуры от -15°C до 0°C перед добавлением к соединению 1.
В некоторых вариантах осуществления соединение 2 осаждается из смеси. В другом варианте осуществления соединение 2 кристаллизуется из смеси. В других вариантах осуществления соединение 2 кристаллизуется из раствора после внесения затравки в раствор (т.е. добавления кристаллов соединения 2 к раствору). В еще одних вариантах осуществления соединение 2 кристаллизуется из раствора на стеклянной фритте, которая погружена в раствор. В еще одних вариантах осуществления соединение 2 кристаллизуется из раствора после колебаний, причем давление воздуха над раствором варьируется от примерно 400 мм рт. ст. до примерно 760 мм рт. ст. В некоторых вариантах осуществления соединение 2 кристаллизуется при взбалтывании (например, перемешивании). В других вариантах осуществления соединение 2 кристаллизуется без взбалтывания. В некоторых вариантах осуществления соединение 2 кристаллизуется из раствора при добавлении подходящего смешивающегося антирастворителя. В другом варианте осуществления подходящим смешивающимся антирастворителем является гептан.
Как, в общем, описано выше, соединение 2 необязательно выделяют. Будет принято во внимание, что соединение 2 можно выделить любыми подходящими физическими способами, известными любому специалисту в данной области. В некоторых вариантах осуществления осажденное твердое соединение 2 отделяют от надосадочной жидкости фильтрацией. В других вариантах осуществления осажденное твердое соединение 2 отделяют от надосадочной жидкости декантированием надосадочной жидкости.
В еще одних вариантах осуществления выделенное соединение 2 необязательно промывают подходящим растворителем. В некоторых вариантах осуществления данный растворитель представляет собой метанол, этанол, пропанол, бутанол или трет-бутанол. В других вариантах осуществления выделенное соединение 2 не промывают после удаления надосадочной жидкости.
В некоторых вариантах осуществления выделенное соединение 2 сушат на воздухе при давлении окружающей среды. В других вариантах осуществления выделенное соединение 2 сушат при пониженном давлении. В некоторых вариантах осуществления выделенное соединение 2 сушат при пониженном давлении, причем давление в диапазоне от примерно 0,05 мм рт. ст. до примерно 50 мм рт. ст. В предпочтительном варианте осуществления выделенное соединение 2 сушат при пониженном давлении, причем давление составляет примерно 25 мм рт. ст.
В другом аспекте настоящего изобретения соединение 2 не выделяют из смеси.
В других вариантах осуществления в конечном соединении 2 полученное соотношение салициловой кислоты и соединения 1 находится в диапазоне от примерно 0,8 до примерно 2,0. В некоторых вариантах осуществления соотношение находится в диапазоне от примерно 0,9 до примерно 1,2. В других вариантах осуществления соотношение находится в диапазоне от примерно 0,94 до примерно 1,06.
Другой аспект настоящего изобретения обеспечивает способ получения соединения 3:

включающий стадии:
предоставления соединения 1:

объединения соединения 1 с гентизиновой кислотой в подходящем растворителе; и,
необязательно, выделения соединения 3.
Подходящий растворитель может растворять один или несколько компонентов реакции или, наоборот, подходящий растворитель может способствовать получению суспензии одного или нескольких компонентов реакции. Примеры подходящих растворителей, применяемых в настоящем изобретении, представляют собой протонный растворитель, полярный апротонный растворитель или их смеси. В некоторых вариантах осуществления подходящие растворители включают простой эфир, сложный эфир, спирт, кетон или их смеси. В некоторых вариантах осуществления подходящим растворителем является метанол, этанол, изопропанол или ацетон, причем указанный растворитель является безводным или в сочетании с водой или гептаном. В других вариантах осуществления подходящие растворители включают тетрагидрофуран, диметилформамид, диметилсульфоксид, глим, диглим, метил-трет-бутиловый эфир, трет-бутанол, н-бутанол и ацетонитрил. В другом варианте осуществления подходящим растворителем является безводный этанол.
Согласно другому варианту осуществления настоящее изобретение обеспечивает способ получения соединения 3:

включающий стадии:
объединения соединения 1:

с подходящим растворителем и нагревания с образованием раствора;
добавления гентизиновой кислоты к указанному раствору; и, необязательно, выделения соединения 3.
В некоторых вариантах осуществления соединение 1 растворяют в подходящем растворителе при нагревании. В некоторых вариантах осуществления соединение 1 растворяют при температуре примерно 60°C. В других вариантах осуществления соединение 1 растворяют в подходящем растворителе при температуре примерно 40°C. В еще одних вариантах осуществления соединение 1 растворяют при температуре от примерно 40°C до примерно 60°C. В еще одних вариантах осуществления соединение 1 растворяют в подходящем растворителе при температуре дефлегмации подходящего растворителя. В других вариантах осуществления соединение 1 растворяют в подходящем растворителе без нагревания.
В некоторых вариантах осуществления раствор соединения 1 фильтруют перед добавлением гентизиновой кислоты. В других вариантах осуществления раствор соединения 1 не фильтруют перед добавлением гентизиновой кислоты.
В некоторых вариантах осуществления, в которых раствор соединения 1 нагревали до какой-либо температуры от примерно 40°C до примерно 60°C, раствор впоследствии охлаждают до какой-либо более низкой температуры, которая составляет от примерно 20°C до примерно 40°C, перед добавлением гентизиновой кислоты. В других вариантах осуществления, в которых раствор соединения 1 нагревали до какой-либо температуры от примерно 40°C до примерно 60°C, раствор впоследствии не охлаждают до какой-либо более низкой температуры перед добавлением гентизиновой кислоты.
В некоторых вариантах осуществления к соединению 1 добавляют примерно 1 эквивалент гентизиновой кислоты для получения соединения 3. В других вариантах осуществления к соединению 1 добавляют менее 1 эквивалента гентизиновой кислоты для получения соединения 3. В еще одних вариантах осуществления к соединению 1 добавляют более 1 эквивалента гентизиновой кислоты для получения соединения 3. В других вариантах осуществления к соединению 1 добавляют от примерно 1,0 до примерно 1,2 эквивалента гентизиновой кислоты для получения соединения 3. В еще одних вариантах осуществления к соединению 1 добавляют от примерно 0,9 до примерно 1,1 эквивалента гентизиновой кислоты для получения соединения 3. В другом варианте осуществления к соединению 1 добавляют от примерно 0,99 до примерно 1,01 эквивалента гентизиновой кислоты для получения соединения 3.
Будет принято во внимание, что гентизиновую кислоту можно добавлять к смеси соединения 1 и подходящего растворителя в любой подходящей форме. Например, можно добавлять гентизиновую кислоту в твердой форме или в виде раствора или суспензии в подходящем растворителе. Подходящим растворителем может быть такой же подходящий растворитель, как тот, который смешивают с соединением 1, или может быть другой растворитель. В некоторых вариантах осуществления гентизиновую кислоту смешивают с подходящим растворителем перед добавлением к соединению 1. Согласно другому варианту осуществления гентизиновую кислоту добавляют в виде раствора в подходящем растворителе. В других вариантах осуществления подходящий растворитель, в котором растворяют гентизиновую кислоту, является полярным протонным или полярным апротонным растворителем. Данные растворители включают спирты, простые эфиры и кетоны. Примеры подобных растворителей включают метанол, этанол, изопропанол, ацетон, тетрагидрофуран, диметилформамид, диметилсульфоксид, глим, диглим, метил-трет-бутиловый эфир, трет-бутанол, н-бутанол и ацетонитрил. В некоторых вариантах осуществления подходящий растворитель выбирают из указанных растворителей, и он является безводным. В других вариантах осуществления подходящий растворитель выбирают из указанных растворителей, и он является смесью с водой или гептаном. В другом варианте осуществления подходящим растворителем является безводный этанол.
В некоторых вариантах осуществления конечную смесь, содержащую соединение 3, охлаждают. В некоторых вариантах осуществления, в которых смесь, содержащую соединение 3, нагревают свыше примерно 20°C, раствор оставляют охлаждаться до температуры примерно 20°C. В других вариантах осуществления смесь, содержащую соединение 3, охлаждают ниже 20°C. В некоторых вариантах осуществления смесь, содержащую соединение 3, охлаждают до температуры от -15°C до 0°C перед добавлением к соединению 1.
В некоторых вариантах осуществления соединение 3 осаждается из смеси. В другом варианте осуществления соединение 3 кристаллизуется из смеси. В других вариантах осуществления соединение 3 кристаллизуется из раствора после внесения затравки в раствор (т.е. добавления кристаллов соединения 3 к раствору). В еще одних вариантах осуществления соединение 3 кристаллизуется из раствора на стеклянной фритте, которая погружена в раствор. В еще одних вариантах осуществления соединение 3 кристаллизуется из раствора после колебаний, причем давление воздуха над раствором варьируется от примерно 400 мм рт. ст. до примерно 760 мм рт. ст. В некоторых вариантах осуществления соединение 3 кристаллизуется при взбалтывании (например, перемешивании). В других вариантах осуществления соединение 3 кристаллизуется без взбалтывания. В некоторых вариантах осуществления соединение 3 кристаллизуется из раствора при добавлении подходящего смешивающегося антирастворителя. В другом варианте осуществления подходящим смешивающимся антирастворителем является гептан.
Как, в общем, описано выше, соединение 3 необязательно выделяют. Будет принято во внимание, что соединение 3 можно выделить любыми подходящими физическими способами, известными любому специалисту в данной области. В некоторых вариантах осуществления осажденное твердое соединение 3 отделяют от надосадочной жидкости фильтрацией. В других вариантах осуществления осажденное твердое соединение 3 отделяют от надосадочной жидкости декантированием надосадочной жидкости.
В еще одних вариантах осуществления выделенное соединение 3 необязательно промывают подходящим растворителем. В некоторых вариантах осуществления данный растворитель представляет собой метанол, этанол, пропанол, бутанол или трет-бутанол. В других вариантах осуществления выделенное соединение 3 не промывают после удаления надосадочной жидкости.
В некоторых вариантах осуществления выделенное соединение 3 сушат на воздухе при давлении окружающей среды. В других вариантах осуществления выделенное соединение 3 сушат при пониженном давлении. В некоторых вариантах осуществления выделенное соединение 3 сушат при пониженном давлении, причем давление в диапазоне от примерно 0,05 мм рт. ст. до примерно 50 мм рт. ст. В другом варианте осуществления выделенное соединение 3 сушат при пониженном давлении, причем давление составляет примерно 25 мм рт. ст.
В другом аспекте настоящего изобретения соединение 3 не выделяют из смеси.
В других вариантах осуществления в конечном соединении 3 полученное соотношение гентизиновой кислоты и соединения 1 находится в диапазоне от примерно 0,8 до примерно 2,0. В некоторых вариантах осуществления соотношение находится в диапазоне от примерно 0,9 до примерно 1,2. В других вариантах осуществления соотношение находится в диапазоне от примерно 0,94 до примерно 1,06.
Применение соединений и фармацевтически приемлемых композиций
Как обсуждалось выше, настоящее изобретение обеспечивает соединения, которые применимы в качестве модуляторов D-рецепторов, 5HT-рецепторов, 5HT обратного захвата и синтеза простагландинов и оказались полезными в клинически важных моделях психоза, депрессии, стресса/тревожности и болезни Паркинсона. В некоторых вариантах осуществления данные соли применимы в качестве модуляторов одного или нескольких подтипов рецепторов D2, 5HT обратного захвата или синтеза простагландинов. В других вариантах осуществления данные соединения применимы для лечения психоза, депрессии, стресса/тревожности и болезни Паркинсона.
Таким образом, в другом аспекте настоящего изобретения обеспечены фармацевтически приемлемые композиции, причем данные композиции содержат соединение 2, соединение 3 или их смеси и необязательно фармацевтически приемлемый носитель, вспомогательное вещество или наполнитель. В некоторых вариантах осуществления данные композиции, кроме того, необязательно содержат один или несколько дополнительных терапевтических средств.
Как описано выше, фармацевтически приемлемые композиции настоящего изобретения, кроме того, содержат фармацевтически приемлемый носитель, вспомогательное вещество или наполнитель, которые использованы в контексте данного документа, включают какой-либо или все растворители, разбавители или другой жидкий наполнитель, дисперсионные или суспензионные вспомогательные средства, поверхностно-активные агенты, изотонические агенты, средства для сгущения или эмульгирующие агенты, консерванты, твердые связующие вещества, лубриканты и тому подобное, соответствующее частной желаемой лекарственной форме. Remington's Pharmaceutical Sciences, Sixteenth Edition, E.W. Martin (Mack Publishing Co., Easton, Pa., 1980) раскрывает различные носители, применимые в разработке рецептур фармацевтически приемлемых композиций, и известные методики их приготовления. За исключением того, когда какая-либо обычная среда носителя является несовместимой с солями данного изобретения, а именно из-за получения какого-либо нежелательного биологического эффекта или же взаимодействия губительным способом с любым другим компонентом(ами) фармацевтически приемлемой композиции, предполагают, что ее применение находится в рамках объема данного изобретения. Некоторые примеры веществ, которые могут служить в качестве фармацевтически приемлемых носителей, включают, но не ограничиваются ими, ионообменники, окись алюминия, стеарат алюминия, лецитин, сывороточные белки, такие как человеческий сывороточный альбумин, буферные вещества, такие как фосфаты, глицин, сорбиновая кислота или сорбат калия, смеси неполных глицеридов насыщенных растительных жирных кислот, воду, соли или электролиты, такие как протаминсульфат, гидрофосфат натрия, гидрофосфат калия, хлорид натрия, цинковые соли, коллоидная окись кремния, трисиликат магния, поливинилпирролидон, полиакрилаты, воски, полиэтилен-полиоксипропилен-блоксополимеры, ланолин, сахара, такие как лактоза, глюкоза и сахароза; крахмалы, такие как кукурузный крахмал и картофельный крахмал; целлюлозу и ее производные, такие как натриевая соль карбоксиметилцеллюлозы, этилцеллюлоза и ацетат целлюлозы; порошковый трагакант; солод; желатин; тальк; вспомогательные средства, такие как масло какао и суппозиторные воски; масла, такие как арахисовое масло, хлопковое масло; сафлоровое масло, кунжутное масло, оливковое масло, кукурузное масло и соевое масло; гликоли, такие как пропиленгликоль или полиэтиленгликоль; сложные эфиры, такие как этилолеат и этиллаурат; агар; буферные вещества, такие как гидроксид магния и гидроксид алюминия; альгиновую кислоту; апирогенную воду; изотонический раствор; раствор Рингера; этиловый спирт и фосфатные буферные растворы, а также другие нетоксические совместимые лубриканты, такие как лаурилсульфат натрия и стеарат магния, а также красящие вещества, разделительные средства, покровные вещества, подсластители, ароматизаторы и вкусовые добавки, также в композиции могут присутствовать консерванты и антиоксиданты на усмотрение разработчика.
В еще одном аспекте обеспечивается способ лечения или снижения тяжести расстройства, связанного с модуляцией D-рецепторов, 5HT-рецепторов, 5HT обратного захвата и синтеза простагландинов, и/или лечения или снижения тяжести психоза, депрессии, стресса/тревожности и/или болезни Паркинсона, включая введение эффективного количества соединения 2, соединения 3 или их смесей пациенту, который в этом нуждается. В некоторых вариантах осуществления настоящего изобретения «эффективным количеством» соединения или фармацевтически приемлемой композиции является количество, эффективное для лечения или снижения тяжести расстройства, связанного с модуляцией D-рецепторов, 5HT-рецепторов, 5HT обратного захвата и синтеза простагландинов, и/или лечения или снижения тяжести психоза, депрессии, стресса/тревожности и/или болезни Паркинсона. В других вариантах осуществления «эффективным количеством» соединения является количество, которое действует как модулятор одного или нескольких D-рецепторов, 5HT-рецепторов, 5HT обратного захвата и синтеза простагландинов. «Эффективное количество» соединения может достигать желаемого терапевтического и/или профилактического эффекта, как, например, количество, которое приводит к предотвращению или ослаблению симптомов, связанных с заболеванием, связанным с модуляцией одного или нескольких D-рецепторов, 5HT-рецепторов, 5HT обратного захвата и синтеза простагландинов и/или с психозом, депрессией, стрессом/тревожностью и/или болезнью Паркинсона.
Соединения и композиции согласно способам настоящего изобретения можно вводить, используя любое количество и любой путь введения, эффективные для лечения или снижения тяжести расстройства, связанного с модуляцией D-рецепторов, 5HT-рецепторов, 5HT обратного захвата и синтеза простагландинов, и/или лечения или снижения тяжести психоза, депрессии, стресса/тревожности и/или болезни Паркинсона. Точное требуемое количество будет варьироваться от пациента к пациенту в зависимости от вида, возраста и общего состояния пациента, тяжести инфицированности, специфического агента, его способа введения и тому подобное. Соединения данного изобретения предпочтительно формулируют в стандартную лекарственную форму (например, таблетку, капсулу или ампулу) для удобства введения и равномерности дозы. Выражение «стандартная лекарственная форма», использованное в контексте данного документа, относится к физически отдельной единице вещества, подходящего для лечения пациента. Будет понятно, однако, что суммарное ежедневное применение солей и композиций настоящего изобретения будет назначено лечащим врачом в рамках обоснованного медицинского заключения. Конкретный уровень эффективной дозы для любого отдельного пациента или организма будет зависеть от множества факторов, включая расстройство, которое лечат, и тяжесть данного расстройства; активность конкретного применяемого соединения; конкретную применяемую композицию; возраст, вес тела, общее состояние здоровья, пол и рацион пациента; время приема, путь введения и скорость экскреции конкретного применяемого соединения; продолжительность лечения; лекарственные средства, применяемые в комбинации или совместно с конкретным применяемым соединением и подобные факторы, хорошо известные в области медицины. Понятие «пациент», использованное в контексте данного документа, означает животное, предпочтительно млекопитающее, а предпочтительнее всего человека.
Фармацевтически приемлемые композиции данного изобретения можно вводить человеку или другим животным перорально, назально, ректально, парентерально, интрацистернально, интравагинально, внутрибрюшинно, местно (как например, порошки, мази или капли), трансбуккально или тому подобное, в зависимости от тяжести инфекции, которую лечат. В некоторых вариантах осуществления соли данного изобретения можно вводить перорально или парентерально при уровнях дозы примерно от 0,01 мг/кг до 50 мг/кг, а предпочтительно от 1 мг/кг до 25 мг/кг массы тела пациента в день, один или несколько раз в день для получения желаемого терапевтического эффекта.
Жидкие лекарственные формы для перорального или назального введения включают, но не ограничиваются ими, фармацевтически приемлемые эмульсии, микроэмульсии, растворы, суспензии, аэрозоли, гели, сиропы и эликсиры. Кроме активных солей, жидкие лекарственные формы могут содержать инертные разбавители, обычно применяемые в данной области техники, такие как, например, вода или другие растворители, солюбилизирующие агенты и эмульгаторы, такие как этиловый спирт, изопропиловый спирт, этилкарбонат, этилацетат, бензиловый спирт, бензилбензоат, пропиленгликоль, 1,3-бутиленгликоль, диметилформамид, масла (в частности, хлопковое, арахисовое, кукурузное, пшеничных зародышей, оливковое, касторовое и кунжутное масла), глицерин, тетрагидрофурфуриловый спирт, полиэтиленгликоли и сложные эфиры жирной кислоты сорбитана и их смеси. Кроме инертных разбавителей, пероральные композиции могут также содержать вспомогательные вещества, такие как увлажняющие средства, эмульгирующие и суспендирующие агенты, подсластители, ароматизаторы и вкусовые добавки. Составы аэрозолей обычно содержат раствор или тонкодисперсную суспензию активного вещества в физиологически приемлемом водном или неводном растворителе и обычно выпускаются в однократной или многократной дозах в стерильном виде в герметичном контейнере, который может принимать форму сменного баллончика для применения с распылительным механизмом. В качестве альтернативы, герметичный контейнер может быть единым устройством, таким как назальный ингалятор однократной дозы или дозатор аэрозоля, оборудованный дозирующим клапаном, который предназначен для употребления однократно содержимого контейнера, который нужно использовать. Поскольку лекарственная форма включает дозатор аэрозоля, то она будет содержать фармацевтически приемлемый пропеллент. Аэрозольные лекарственные формы могут также принимать форму насоса-пульверизатора.
Инъецируемые препараты, например, стерильные инъецируемые водные или маслянистые суспензии могут быть приготовлены согласно известному уровню техники, используя подходящие диспергирующие или увлажняющие средства и суспендирующие агенты. Стерильный инъецируемый препарат может также быть стерильным инъецируемым раствором, суспензией или эмульсией в нетоксическом парентерально приемлемом разбавителе или растворителе, например, в виде раствора в 1,3-бутандиоле. Среди приемлемых наполнителей и растворителей, которые можно применять, - вода, раствор Рингера, U.S.P. и изотонический раствор хлорида натрия. Кроме того, стерильные жирные масла применяются обычно в качестве растворителя или суспендирующей среды. Для этой цели можно применять любое смягчающее жирное масло, включая синтетические моно- или диглицериды. Кроме того, для приготовления инъекций применяют жирные кислоты, такие как олеиновая кислота.
Инъецируемые составы могут быть стерилизованы, например, посредством фильтрации через задерживающий бактерии фильтр или посредством включения стерилизующих агентов в форме стерильных твердых композиций, которые могут быть растворены или диспергированы в стерильной воде или другой стерильной инъецируемой среде перед применением.
Для того чтобы продлить эффект соединения настоящего изобретения, часто желательно замедлить всасывание соединения из подкожной или внутримышечной инъекции. Этого можно достичь применением жидкой суспензии кристаллического или аморфного вещества с плохой растворимостью в воде. Скорость всасывания соединения тогда зависит от скорости его диссоциации, которая в свою очередь может зависеть от размера кристалла и формы кристалла. В качестве альтернативы, замедленное всасывание парентерально введенного соединения достигается растворением или суспендированием соединения в масляной среде. Инъецируемые формы пролонгированного действия готовят посредством формирования микрокапсулированных матриц соединения в биоразлагаемых полимерах, таких как полилактид-полигликолид. В зависимости от соотношения соединения к полимеру и природы частного применяемого полимера можно контролировать скорость высвобождения соединения. Примеры других биоразлагаемых полимеров включают поли(ортоэфиры) и поли(ангидриды). Инъецируемые составы пролонгированного действия также готовят посредством включения соединения в липосомы или микроэмульсии, которые совместимы с тканями организма.
Обычные парентеральные композиции состоят из раствора или суспензии соединения или физиологически приемлемой соли в стерильном водном носителе или неводном или парентерально приемлемом масле, например, в полиэтиленгликоле, поливинилпирролидоне, лецитине, арахисовом масле или кунжутном масле. В качестве альтернативы раствор может быть лиофилизирован и затем перерастворен в другом подходящем растворителе прямо перед введением.
Композиции для ректального или вагинального введения обычно готовят в виде суппозиториев, пессариев, вагинальных таблеток, пен или клизм. Композиции для ректального или вагинального введения предпочтительно представляют собой суппозитории, которые можно приготовить смешиванием солей данного изобретения с подходящими нераздражающими вспомогательными веществами или носителями, такими как масло какао, полиэтиленгликоль или воск суппозитория, который является твердым при температуре окружающей среды, но жидким при температуре тела, а следовательно, плавится в прямой кишке или в вагинальной полости и высвобождает активное соединение.
Твердые лекарственные формы для перорального введения включают капсулы, таблетки, пилюли, порошки и гранулы. В подобных твердых лекарственных формах активное соединение смешивается, по меньшей мере, с одним инертным, фармацевтически приемлемым вспомогательным веществом или носителем, таким как цитрат натрия или дикальцийфосфат и/или a) наполнителями или разбавителями, такими как крахмалы, лактоза, сахароза, глюкоза, маннит и кремниевая кислота; b) связующими веществами, такими как, например, карбоксиметилцеллюлоза, альгинаты, желатин, поливинилпирролидон, сахароза и акация; c) увлажнителями, такими как глицерин; d) разрыхлителями, такими как агар-агар, карбонат кальция, картофельный крахмал или крахмал из тапиоки, альгиновая кислота, некоторые силикаты и карбонат натрия; e) замедлителями схватывания раствора, такими как парафин; f) ускорителями всасывания, такими как четвертичные аммониевые соли; g) увлажняющими средствами, такими как, например, цетиловый спирт и глицеринмоностеарат; h) абсорбирующими веществами, такими как каолин и бентонитовая глина; и i) лубрикантами, такими как тальк, стеарат кальция, стеарат магния, твердые полиэтиленгликоли, лаурилсульфат натрия и их смеси. В случае капсул, таблеток и пилюль лекарственная форма может также содержать буферные вещества.
Композиции, подходящие для трансбуккального или сублингвального введения, включают таблетки, леденцы и пастилки, в которых активный ингредиент формулируется с носителем, таким как сахароза и акация, трагакант или желатин и глицерин.
Твердые композиции подобного типа также могут применяться в качестве наполнителей в мягкие и твердые желатиновые капсулы, используя такие вспомогательные вещества, как лактоза или молочный сахар, а также полиэтиленгликоли с высокой молекулярной массой и тому подобное. Твердые лекарственные формы таблеток, драже, капсул, пилюль и гранул могут быть приготовлены с покрытиями и оболочками, такими как энтеросолюбильные покрытия и другие покрытия, хорошо известные в области техники фармацевтической разработки рецептур. Они могут необязательно содержать опалесцирующие компоненты, а также могут принадлежать к композиции, в которой они высвобождают только, или предпочтительно, активный ингредиент(ы) в определенной части кишечника, необязательно замедленным образом. Примеры капсулирующих составов, которые могут применяться, включают полимерные вещества и воски. Твердые композиции подобного типа также могут применяться в качестве наполнителей в мягкие и твердые желатиновые капсулы, используя такие вспомогательные вещества, как лактоза или молочный сахар, а также полиэтиленгликоли с высокой молекулярной массой и тому подобное.
Активные соли могут также быть в микрокапсулированной форме с одним или несколькими вспомогательными веществами, как отмечено выше. Твердые лекарственные формы таблеток, драже, капсул, пилюль и гранул могут быть приготовлены с покрытиями и оболочками, такими как энтеросолюбильные покрытия, контролирующие высвобождение покрытия и другие покрытия, хорошо известные в области техники фармацевтической разработки рецептур. В подобных твердых лекарственных формах активное соединение может быть смешано, по меньшей мере, с одним инертным разбавителем, таким как сахароза, лактоза или крахмал. Подобные лекарственные формы также могут содержать, что является обычной практикой, дополнительные вещества помимо инертных разбавителей, например, таблетированные лубриканты и другие таблетированные вспомогательные средства, такие как стеарат магния и микрокристаллическая целлюлоза. В случае капсул, таблеток и пилюль лекарственные формы могут также содержать буферные вещества. Они могут необязательно содержать опалесцирующие компоненты, а также могут принадлежать к композиции, в которой они высвобождают только, или предпочтительно, активный ингредиент(ы) в определенной части кишечника, необязательно замедленным образом. Примеры капсулирующих составов, которые могут применяться, включают полимерные вещества и воски.
Композиции для перорального введения могут быть разработаны таким образом, чтобы защищать активный ингредиент от разрушения, когда он проходит через пищеварительный тракт, например, посредством внешнего покрытия состава в таблетке или капсуле.
Соединение 2 и соединение 3 согласно настоящему изобретению могут быть обеспечены в композиции замедленного высвобождения. Данная композиция замедленного высвобождения содержит соединение 2 и/или соединение 3 в комбинации с компонентом замедленного высвобождения. Данная композиция позволяет целенаправленное высвобождение соединения 2 и/или соединения 3 в нижнем желудочно-кишечном тракте; например, в тонком кишечнике, толстом кишечнике, толстой кишке и/или прямой кишке. Композиция замедленного высвобождения может содержать соединение 2 и/или соединение 3 и энтеросолюбильное или pH-зависимое покрытие, такое как ацетатфталаты целлюлозы и другие фталаты (например, поливинилацетатфталат, метакрилаты (Eudragits)). В качестве альтернативы композиция замедленного высвобождения может обеспечивать контролируемое высвобождение в тонком кишечнике и/или в толстой кишке посредством обеспечения pH-чувствительных метакрилатных покрытий, pH-чувствительных полимерных микросфер или полимеров, которые подвергаются разрушению гидролизом. Композиция замедленного высвобождения может быть приготовлена с гидрофобными или гелеобразующими вспомогательными веществами или покрытиями. Кроме того, доставка к толстой кишке может быть обеспечена покрытиями, которые перевариваются бактериальными ферментами, такими как амилаза или пектин, pH-зависимыми полимерами, гидрогелевыми пробками, набухающими со временем (Pulsincap), изменяющимися со временем гидрогелевыми покрытиями и/или покрытиями акриловой кислоты, связанной азоароматическими связями.
Лекарственные формы для местного или трансдермального введения соединения данного изобретения включают мази, пасты, кремы, лосьоны, гели, порошки, растворы, спреи, лекарственные формы для ингаляции или пластыри. Активный компонент смешивают в стерильных условиях с фармацевтически приемлемым носителем и любыми необходимыми консервантами или буферными веществами при необходимости. Предполагается, что офтальмический состав, ушные капли и глазные капли также находятся в рамках объема данного изобретения. Кроме того, настоящее изобретение предполагает применение трансдермальных пластырей, которые имеют дополнительное преимущество обеспечения контролируемой доставки соединения в теле. Подобные лекарственные формы могут быть приготовлены растворением или разведением соединения в подходящей среде. Также для увеличения поступления соединения через кожу могут применяться усилители всасывания. Скорость можно контролировать либо обеспечением контролирующей скорость мембраны, либо диспергированием соединения в полимерной матрице или геле.
Композиции могут содержать от 0,1% до 99% (масс./масс.) предпочтительно 0,1-60% (масс./масс.), более предпочтительно 0,2-20% по массе и наиболее предпочтительно от 0,25 до 12% (масс./масс.) соединения 2 и/или соединения 3 в зависимости от способа введения.
Как, в общем, описано выше, соли настоящего изобретения применимы в качестве модуляторов одного или нескольких D-рецепторов, 5HT-рецепторов, 5HT обратного захвата и синтеза простагландинов, и, таким образом, изобретение, кроме того, относится к способу лечения (например, нерадикального, радикального, профилактического) заболевания или расстройства, связанного с модуляцией одного или нескольких D-рецепторов, 5HT-рецепторов, 5HT обратного захвата и синтеза простагландинов.
В одном варианте осуществления соли и композиции данного изобретения являются модуляторами одного или нескольких D-рецепторов, 5HT-рецепторов, 5HT обратного захвата и синтеза простагландинов, и, таким образом, не желая привязываться к какой-либо частной теории, соли и композиции, в частности, применимы для лечения или уменьшения тяжести заболевания, патологического состояния или расстройства, когда в данное заболевание, патологическое состояние или расстройство вовлечена модуляция одного или нескольких D-рецепторов, 5HT-рецепторов, 5HT обратного захвата и синтеза простагландинов. Когда модуляция одного или нескольких D-рецепторов, 5HT-рецепторов, 5HT обратного захвата и синтеза простагландинов вовлечена в частное заболевание, патологическое состояние или расстройство, то данное заболевание, патологическое состояние или расстройство может также быть названо «заболеванием, опосредованным D-рецептором, 5HT-рецептором, 5HT обратным захватом или синтезом простагландинов» или симптомом заболевания.
В некоторых вариантах осуществления соли и композиции настоящего изобретения обеспечивают способ лечения или уменьшения тяжести одного или нескольких расстройств, включая, но не ограничиваясь ими, болезнь Паркинсона, психоз (например, шизофрению, маниакальный синдром, психотическую депрессию и биполярное расстройство), депрессию, стресс/тревожность, болезнь Альцгеймера, болезнь Гентингтона, паническое расстройство, обсессивно-компульсивное расстройство, расстройство пищевого поведения, лекарственное привыкание, социофобии, агрессию или тревожное возбуждение, мигрень, склеродермию и феномен Рейно, рвоту, расстройства ЖК тракта, связанные с регуляцией перистальтики, СУН и повышение секреции пролактина из опухолей гипофиза, причем указанный способ включает введение пациенту соединения 2 и/или соединения 3 или их композиций.
Будет принято во внимание, что соединения и фармацевтически приемлемые композиции настоящего изобретения могут применяться в комбинированных терапиях, то есть соли и фармацевтически приемлемые композиции могут вводиться одновременно с, перед или после одного или нескольких других желаемых терапевтических средств или проведения медицинских манипуляций. Частная комбинация терапий (терапевтических средств или манипуляций) для применения в комбинированном режиме примет во внимание совместимость желаемых терапевтических средств и/или манипуляций и желаемый терапевтический эффект, которого необходимо достигнуть. Также будет принято во внимание, что применяемые терапии могут достигать желаемого эффекта для одного и того же расстройства (например, соединение изобретения может вводиться одновременно с другим средством, применимым для лечения того же самого расстройства) или они могут достигать различных эффектов (например, контроль любых нежелательных реакций). Как используется в контексте данного документа, дополнительные терапевтические средства, которые обычно вводят для лечения или предотвращения частного заболевания или патологического состояния, известны как «подходящие для лечения заболевания или патологического состояния».
Количество дополнительного терапевтического средства, присутствующего в композициях данного изобретения, будет не больше, чем количество, которое вводилось бы обычно в композиции, содержащей данное терапевтическое средство в качестве только активного компонента. Предпочтительно количество дополнительного терапевтического средства в раскрытых сейчас композициях будет находиться в диапазоне от 50% до 100% от количества, обычно присутствующего в композиции, содержащей данное средство только в качестве терапевтически активного средства.
Другой аспект данного изобретения относится к модуляции активности D-рецепторов, 5HT-рецепторов, 5HT обратного захвата и синтеза простагландинов в биологическом образце или у пациента, способ которой включает введение пациенту или взаимодействие указанного биологического образца с соединением 2 и/или соединением 3 или их композицией. Понятие «биологический образец», использованное в контексте данного документа, включает без ограничения клеточные культуры или их экстракты; материал биопсии, полученный из млекопитающего или его экстракты; и кровь, слюна, моча, экскременты, семенная жидкость, слезы или другие жидкости организма или их экстракты.
Модуляция активности D-рецепторов, 5HT-рецепторов, 5HT обратного захвата и синтеза простагландинов в биологическом образце применимы для многообразия целей, которые известны специалисту в данной области техники. Примеры подобных целей включают, но не ограничиваются ими, биологические анализы.
Количество соединения 2 и/или соединения 3, эффективное для лечения расстройства, как изложено выше, зависит от природы и тяжести расстройства, которое лечат, и веса пациента, который в этом нуждается. Однако однократная доза на 70 кг взрослого обычно содержит от 0,01 до 100 мг, например, от 0,1 до 50 мг, предпочтительно от 0,5 до 16 мг соединения данного изобретения в день. Однократные дозы можно вводить единожды или более чем один раз в день, например, 2, 3 или 4 раза в день, обычно от 1 до 3 раз в день, более предпочтительно 1 или 2 раза в день. Будет принято во внимание, что диапазоны доз, изложенные выше, только в случае показания к введению соединения 2 и/или соединения 3 взрослому. Количество, которое вводят, например, младенцу или ребенку, может быть определено врачом-терапевтом или специалистом в данной области техники и может быть ниже или таким же, как и количество, которое вводится взрослому. Однократная доза предпочтительно выпускается в виде капсулы или таблетки.
Все предпочтительные признаки каждого из аспектов данного изобретения распространяются на все другие аспекты с необходимыми изменениями.
Для того чтобы описанное в контексте данного документа изобретение можно было понять более полно, предложены следующие примеры. Следует понимать, что данные примеры служат только для иллюстративных целей, а не истолковываются как ограничивающие данное изобретение.
ПРИМЕРЫ
Общие процедуры
Порошковые рентгенограммы были получены на Rigaku Miniflex Diffraction System (Rigaku MSC Inc.). Порошковые образцы поместили на гладкий силиконовый держатель образцов нулевого уровня. В качестве источника рентгеновских лучей использовали медную рентгеновскую трубку с нормальным фокусом при 0,45 кВт, оснащенную Ni Kβ фильтром, сканирующим по 2 градуса в минуту от 3,00 до 40,00 градусов 2-тета. Обработка данных была произведена, используя программное обеспечение Jade 6.0.
Спектры протонного ядерного магнитного резонанса (1H ЯМР) были получены на Bruker model Avance DRX-500 MHz ЯМР-спектрометре, оснащенном 5 мм квадратурным ядерным датчиком. Примерно 5-25 мг солей растворили в 0,6 мл ДМСО-d6 (99,9% D), содержащем 0,05% TMS в качестве внутреннего источника.1H ЯМР спектры были записаны при 500,133 МГц, используя импульс 30 градусов, с задержкой импульса 20 секунд, 32 тысячи экспериментальных точек, 64 скана. Функцию экспоненциального окна с 0,3 Гц расширением спектральных линий применили к 16 тысячам экспериментальных точек для обработки данных без обнуления, а TMS приняли за 0,00 ч/млн.
Получение соединения 2
Способ A
Соединение 1 (50 мг) суспендировали в безводном этаноле (4 мл) и нагрели до 40°C для получения прозрачного раствора. К данному раствору добавили 16,3 мг салициловой кислоты (0,99 эквивалента). Конечный раствор охладили до 20°C и перемешивали магнитной мешалкой. В реактор внесли стеклянную фритту, а давление воздуха над раствором циклически изменяли от 760 мм рт. ст. до примерно 400 мм рт. ст. в течение 16 часов. Данный способ дает 2 фазы: масляную фазу, соприкасающуюся со стеклянным реактором, и твердую фазу на стеклянной фритте. Твердое вещество на стеклянной фритте высушили на воздухе при 23°C и проанализировали посредством рентгенографии (фиг.1) и выяснили, что это кристаллическое соединение 2.
Таблица 1 ниже показывает рентгенографические пики, наблюдаемые для соединения 2, причем каждая величина в градусах 2-тета.
Способ B
В качестве альтернативы соединение 2 приготовили следующим способом: соединение 1 (500 мг) суспендировали в 16 мл безводного этанола и нагрели до 60°C для получения прозрачного раствора. Раствор отфильтровали через 0,45 мкм фильтр и охладили до 40°C. К данному раствору добавили 164 мг салициловой кислоты (1,0 эквивалент) в виде раствора в 4 мл этанола. Добавили твердые затравочные кристаллы соединения 2 и суспензию перемешивали при температуре от примерно 20°C до примерно 40°C в течение 24 часов. Суспензию затем отфильтровывали и твердую фазу высушивали при 25°С и примерно 25 мм рт. ст. Сухое твердое вещество (372 мг, 56,1% выход) охарактеризовали посредством рентгенографии и1H ЯМР спектроскопии (фиг.3) и выяснили, что это кристаллическое соединение 2.
Приготовление гентизината 3
Способ A
Соединение 1 (50 мг) суспендировали в безводном этаноле (4 мл) и нагрели до 40°C для получения прозрачного раствора. К данному раствору добавили 18,2 мг гентизиновой кислоты (1,0 эквивалент). Конечный раствор охладили до 20°C и перемешивали магнитной мешалкой. В реактор внесли стеклянную фритту, а давление воздуха над раствором циклически изменяли от 760 мм рт. ст. до примерно 400 мм рт. ст. в течение 16 часов. Данный способ дает 2 фазы: одну - в стеклянном реакторе и вторую - на стеклянной фритте. Твердое вещество на стеклянной фритте высушили на воздухе при 23°C и проанализировали посредством рентгенографии (фиг.2) и выяснили, что это кристаллическое соединение 3.
Таблица 2 ниже показывает рентгенографические пики, наблюдаемые для соединения 3, причем каждая величина в градусах 2-тета.
Способ B
В качестве альтернативы гентизиновую соль 3 приготовили следующим способом: соединение 1 (500 мг) суспендировали в 16 мл безводного этанола и нагрели до 60°C для получения прозрачного раствора. Раствор отфильтровали через 0,45 мкм фильтр и охладили до 40°C. К данному раствору добавили 182 мг гентизиновой кислоты (1,0 эквивалент) в виде раствора в 4 мл этанола и раствор перемешивали при температуре от примерно 20°C до примерно 40°C в течение 16 часов. В течение данного периода выкристаллизовалась твердая фаза. Суспензию затем отфильтровали, а твердую фазу высушили при 25°C и примерно 25 мм рт. ст. Сухое твердое вещество (355 мг, 52,0% выход) охарактеризовали посредством рентгенографии и1H ЯМР спектроскопии (фиг.4) и выяснили, что это кристаллическое соединение 3.
Растворимость в воде
Растворимость в воде определяли смешиванием избыточного количества твердой соли с ~2 мл деионизированной воды в 4 мл стеклянном флаконе с завинчивающейся крышкой и уравновешиванием в течение, по меньшей мере, 24 часов на устройстве с вращением с донышка на крышку. Конечные суспензии отфильтровали через 0,22 мкм ПВДФ фильтр и проанализировали посредством высокоэффективной жидкостной хроматографии с количественным определением посредством УФ-облучения относительно стандартов соединения 1. Растворимость в воде соединения 2 составляет 1,6 мг/мл (эквивалент свободного основания) при конечном pH 5,8, тогда как растворимость соединения 3 составляет 0,5 мг/мл (эквивалент свободного основания) также при pH 5,8.
Результаты ЯМР
Интеграцию сигналов салициловой и гентизиновой кислоты сравнили с оригинальным пиком соединения 1 (фиг.5), для того чтобы получить молярные соотношения каждой кислоты к соединению 1 в соединении 2 и соединении 3. Результаты суммируются ниже в таблице 1.
Реферат
Описываются соединения формулы 2 и 3, способы их получения, фармацевтические композиции, а также их применение для получения лекарственного средства, обладающего антагонистической активностью к D2-рецепторам и модулирующей активностью по отношению к обратному захвату 5НТ. Настоящее изобретение обеспечивает солевые формы, применимые в качестве модуляторов одного или нескольких GPCR. 9 н. и 11 з.п. ф-лы, 3 табл., 5 ил.
Формула


включающий стадии:
предоставления соединения 1:

объединения соединения 1 с салициловой кислотой в подходящем растворителе; и,
необязательно, выделения соединения 2.
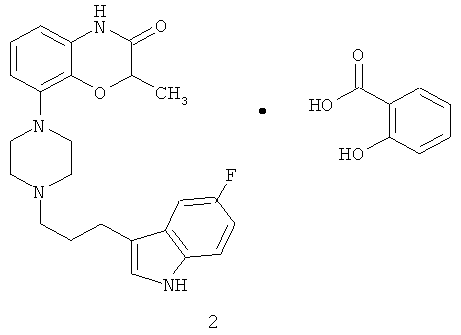
включающий стадии:
объединения соединения 1:

с подходящим растворителем и нагревание с образованием раствора;
добавления салициловой кислоты к указанному раствору; и, необязательно, выделения соединения 2.


включающий стадии:
предоставления соединения 1:

объединения соединения 1 с гентизиновой кислотой в подходящем растворителе; и,
необязательно, выделения соединения 3.

включающий стадии:
объединения соединения 1:

с подходящим растворителем и нагревания с образованием раствора;
добавления гентизиновой кислоты к указанному раствору; и,
необязательно, выделения соединения 3.
соединение 2:

или соединение 3:

или их смесь и фармацевтически приемлемый носитель, вспомогательное вещество или наполнитель.

Комментарии