Высокоафинные мутеины интерлейкина-4 - RU2202364C2
Код документа: RU2202364C2
Чертежи


















Описание
Изобретение относится, главным образом, к областям фармакологии и иммунологии. Более конкретно, изобретение направлено на новые варианты из семейства цитокинов и, в частности, человеческий интерлейкин-4 (IL-4). Интерлейкин-4 (IL-4) представляет собой гликопротеин массой 15 кДа, секретируемый активированными Т-клетками (Howard et al., J. Exp. Med. 155:914 (1982)), тучными клетками (Brown et al., Cell 50:809 (1987)) и базофилами (Seder et al. , Proc. Natl. Acad. Sci. USA 88:2835 (1991)), который регулирует широкий спектр клеточных функций кроветворных и некроветворных клеток. Последовательность описана в патенте США 5017691. Интерлейкин-4 (IL-4) представляет собой плейотропный цитокин, обладающий эффектами на клетки иммунной системы, эндотелия и на клетки ряда фибробластов. Описанные эффекты введения IL-4 in vitro включают в себя пролиферацию Т- и В-клеток, переключение классов иммуноглобулина в В-клетках, стимуляцию продукции молекул адгезии поверхности клеток эндотелиальными клетками и стимуляцию секреции IL-6. Что касается Т-клеток, IL-4 стимулирует пролиферацию Т-клеток после предварительной активации митогенами и ингибирует продукцию IFN-IFN-γ. В моноцитах IL-4 индуцирует экспрессию молекул МНС II класса, секрецию липополисахарид-индуцированного tPA и экспрессию CD23. В эндотелиальных клетках (ЭК) IL-4 индуцирует экспрессию VCAM-1 и секрецию IL-6. IL-4 снижает экспрессию ICAM-1. Maher, DW, et al., Human Interleukin-4: An Immunomodulator with Potential Therapeutic Applications, Progress in Growth Factor Research, 3:43-56 (1991).
По причине его способности к стимулированию пролиферации Т-клеток, активированных воздействием IL-2, исследовались терапевтические приложения IL-4. Например, IL-4 проявлял противоопухолевую активность в животных моделях злокачественных опухолей почки и вызывал регресс опухоли у мышей (Bosco M. et al. , Low Doses of IL-4 Injected Perilymphatically in Tumor-bearing Mice Inhibit the Growth of Poorly and Apparently Nonimmunogenic Tumors and Induce a Tumor Specific Immune Memory, J. Immunol., 145:3136-43 (1990)). Однако его токсичность ограничивает размер дозировки у людей (Margolin К. et al., Phase II Studies of Human Recombinant Interleukin-4 in Advanced Renal Cancer and Malignant Melanoma, J. immunotherapy, 15:147-153 (1994)).
В настоящее время известны общая структура и функция IL-4 и родственных мономерных лигандов, содержащих 4 антипараллельных α -спиральных домена (A-D). Была определена трехмерная структура IL-4 (Powers et al., Science 256: 1673, 1992). Белок содержит 4 левые α-спирали и две β-складки.
Рецептор IL-4 состоит, по крайней мере, из двух цепей. Первая цепь IL-4R, IL-4Rα, проявляет значительную гомологию с β-цепью IL-2R и с другими членами надсемейства рецепторов факторов роста (Ldzerda et al., J. Exp. Med. 171:861 (1990)). Была определена вторая цепь IL-4R, цепь IL-2R, также известная как "общая цепь", γc (Russel et al., Science, 262:1877 (1993)). Два участка связывания, вероятно, вовлечены в последовательный процесс двойного связывания, который приводит к образованию третичного 1:1:1 комплекса. Считается, что участок IL-4, вероятно ответственный за связывание с IL-4Rα, расположен либо на спиралях А и С, либо на них обеих, тогда как считается, что участок, взаимодействующий с γc, расположен на спирали D. В соответствии с данной теорией считается, что первое событие связывания включает в себя взаимодействие лиганда с IL-4Rα, первичным связывающим компонентом. С данным событием не связана какая-либо активность, выражающаяся в передаче сигнала. Второе событие связывания имеет место, когда комплекс IL-4/IL-4Rα укомплектовывается второй цепью, γc. После данного второго события связывания происходит передача сигнала и осуществляется клеточная активность. Антагонизм по отношению к IL-4 дикого типа обнаруживают, когда взаимодействия при связывании, опосредованные вторым участком (необходимым для клеточной активности), ослабляются или устраняются при сохраняющемся связывании с IL-4Rα. Агонизм имеет место в том случае, когда претендующий лиганд конструктивно взаимодействует посредством первого и второго участков с обоими рецепторными компонентами. В литературе есть сообщения об антагонистах IL-4. Мутанты IL-4, которые действуют как антагонисты, включают мутеин-антагонист IL-4 IL-4/Y124D (Kruse N, Tony HP, Sebald W, Conversion of human interleukin-4 into a high affinity antagonist by a single amino acid replacement. Embo J., 11: 3237-44 (1992)) и двойной мутеин IL-4[R121D/Y124D] (Tony H. et al., Design of Human Interleukin-4 Antagonists in Inhibiting Interleukin-4-dependent and Interleukin-13-dependent responses in T-cells and B-cells with high efficiency, Eur. J. Biochem. 225:659-664 (1994)). Одинарный мутеин представляет собой замену тирозина аспарагиновой кислотой в положении 124 в D-спирали. Двойной мутеин представляет собой замену аргинина аспарагиновой кислотой в положении 121 и тирозина аспарагиновой кислотой в положении 124 в D-спирали. Вариации в данной части D-спирали положительно коррелируют с изменениями во взаимодействиях во втором участке связывания.
Мутантные варианты IL-4, проявляющие агонизм или антагонизм по отношению к IL-4 дикого типа, могут быть применимы для лечения состояний, связанных с одним из множественных эффектов IL-4. Например, антагонисты IL-4 будут применимы для лечения состояний, обостряющихся при продукции IL-4, таких как бронхиальная астма, аллергия или иные состояния, связанные с воспалительной реакцией. Агонисты IL-4 могут быть применимы для лечения состояний, при которых присутствие IL-4 связано с улучшением состояния или ослаблением заболевания, например аутоиммунного заболевания, такого как ревматоидный артрит, рассеянный склероз, инсулинзависимый сахарный диабет и так далее. Данные аутоиммунные заболевания характеризуются поляризацией в продукции клеточных популяций Т-хелперов, типов 1 и 2 (Th1, Th2). Интактные CD4+ Т-клетки дифференцируются в подгруппы Th1 и Th2 в зависимости от присутствующего во время стимуляции цитокина. Агонист IL-4 идеально сдвинет продукцию желаемых Т-хелперных клеток, то есть в сторону Th2, оказывая, таким образом, терапевтический эффект.
В международной заявке на патент PCT/US93/03613 описан вариант IL-4, содержащий последовательность Phe-Leu или Tyr-Leu в альфа-спиральном домене и отрицательно заряженную аминокислоту на расстоянии не более двух аминокислот сразу слева или справа от последовательности Phe-Leu или Tyr-Leu, вариант, обладающий повышенным сродством к рецептору IL-4, благодаря замене отрицательно заряженной аминокислоты на электронейтральную аминокислоту. В нем также описано, что специфическая замена Trp-Leu или Phe-Leu в пределах α-спирали IL-4 на расстоянии 2 остатков от отрицательно заряженного остатка приводит к повышенному сродству. Вариант представляет собой гибридный белок IL-4 (с дифтерийным анатоксином).
Изобретение направлено на рекомбинантный мутеин человеческого IL-4, пронумерованный в соответствии с IL-4 дикого типа, где мутеин содержит, по крайней мере, одну аминокислотную замену в связывающей поверхности либо альфа-спирали А, либо альфа-спирали С IL-4 дикого типа, посредством которой мутеин связывается с рецептором IL-4Rα, по крайней мере, с большим сродством, чем нативный IL-4. Замену предпочтительно выбирают из группы положений, состоящей из положений 13 и 16 в спирали А, и положений 81 и 89 в спирали С. Наиболее предпочтительное осуществление представляет собой рекомбинантный мутеин человеческого IL-4, где замена в положении 13 представляет собой Thr на Asp. Также описаны фармацевтические композиции, аминокислотные и полинуклеотидные последовательности, кодирующие мутеины, трансформированные клетки-хозяева, антитела против мутеинов и способы лечения.
Изобретение также направлено на анализ для определения способности мутеина связываться с рецептором, включающий в себя следующие стадии: во-первых, внесение на FlashPlate, покрытый стрептавидином,
связывающего участка рецепторной цепи, причем связывающий участок рецепторной цепи содержит пептидную метку, способную связываться со стрептавидином; во-вторых, внесение на FlashPlate нативного
лиганда с радиоактивной меткой, обладающего сродством к связывающему участку рецепторной цепи; в-третьих, внесение на FlashPlate мутеина-лиганда, обладающего сродством к связывающему участку
рецепторной цепи; измерение значения сигнала, испускаемого FlashPlate после уравновешивания, и, наконец, расчет относительного сродства мутеина лиганда по сравнению с таковым нативного лиганда. В
предпочтительном методе в способе применяют рецеторную цепь IL-4Rα.
Изобретение также направлено на рекомбинантный мутеин-антагонист человеческого IL-4, пронумерованный в соответствии
с IL-4 дикого типа, где мутеин содержит: (а) замены R121D и Y124D в D-спирали IL-4 дикого типа и (б) по крайней мере, одну аминокислотную замену в связывающей поверхности либо альфа-спирали А, либо
альфа-спирали С IL-4 дикого типа, посредством которой мутеин связывается с рецептором IL-4Rα, по крайней мере, с большим сродством, чем нативный IL-4. Замену предпочтительно выбирают из группы
положений, состоящей из положений 13 и 16 в спирали А и положений 81 и 89 в спирали С. Наиболее предпочтительное осуществление представляет собой рекомбинантный мутеин-антагонист человеческого IL-4,
где замена в положении 13 представляет собой Thr на Asp. Также описаны фармацевтические композиции, аминокислотные и полинуклеотидные последовательности, кодирующие мутеины, трансформированные
клетки-хозяева, антитела против мутеинов и способы лечения.
На Фиг. 1 представлено схематическое изображение архитектуры лиганд/рецепторного комплекса IL-4. IL-4 представляет собой четырехспиральный белок и представлен здесь в виде изображения "концы вперед" четырех спиралей (А, В, С и D, от N- к С-концу соответственно). Первичным связывающим компонентом рецептора IL-4 является IL-4Rα, который взаимодействует с лигандом IL-4 посредством А- и С-спиралей IL-4. Образование третичного комплекса IL-4/IL-4Rα/IL-4Rγ вызывает передачу сигнала в клетке-мишени.
Фиг. 2 представляет собой X-Y график конкурентного связывания T13D-IL-4[R121D/Y124D] . Способность T13D-IL-4[R121D/Y124D] , •, конкурировать с125I-IL-4 в твердофазном анализе связывания показана относительно таковой IL-4[R121D/Y124D],o. Значение Кd, определенное с применением данного анализа для T13D-IL-4[R121D/Y124D], составляло 0,28 нМ, а для IL-4[R121D/Y124D] - 5,0 нМ.
Фиг. 3 представляет собой аналогичный X-Y график, описывающий антагонизм по отношению к IL-4 T13D-IL-4[R121D/Y124D] ,o. Способность T13D-IL-4[R121D/Y124D] ингибировать IL-4-индуцированную пролиферацию ФГА-бластов показана относительно таковой IL-4[R121D/Y124D], •. Значение ИК50, определенное с помощью данного анализа для T13D-IL-4[R121D/Y124D], составляло 2 нМ, а для IL-4[R121D/Y124D] - 13 нМ.
На Фиг. 4 представлен список аминокислотной последовательности sIL-4Rα-STX.
На Фиг. 5 представлен объединенный список последовательностей мутеина T13D-IL-4.
На Фиг. 6 представлен объединенный список последовательностей мутеина T13D-IL-4[R121D/Y124D].
В предпочтительных вариантах осуществления изобретения описаны новые мутеины и механизм получения новых мутеинов IL-4, обладающих более высокими значениями сродства к рецептору IL-4 д.т.
Термин "IL-4 дикого типа" или "IL-4 д.т." означает человеческий интерлейкин-4, нативный или рекомбинантный, обладающий последовательностью нативного человеческого IL-4, состоящей из 129 природных аминокислот, как описано в Патенте США 5017691, включенном сюда в качестве ссылки.
Термин "мутеин IL-4" означает полипептид, где в человеческом зрелом белке интерлейкин-4 произведены особые аминокислотные замены, конкретно, либо в А-, либо в С-спирали, и более предпочтительно тех аминокислот, которые содержатся в их связывающих поверхностях. Связывающая поверхность А-спирали, как правило, расположена от приблизительно 5 до приблизительно 16 аминокислотного положения, а в спирали С - от приблизительно 77 до приблизительно 89 положения. Данные изменения в одной из двух спиралей увеличивают сродство полученного мутеина к IL-4Rα, причем данный мутеин может представлять собой либо агонист, либо антагонист IL-4 д.т. в зависимости от итоговой природы дополнительных замен в молекуле.
Термин "мутеин-антагонист IL-4" означает полипептид, где в человеческом зрелом белке интерлейкин-4 произведены особые аминокислотные замены. Конкретно, представленные здесь мутеины-антагонисты содержат, по крайней мере, три отдельные замены. Пара замен "IL-4[R121D/Y124D]" присутствует во всех содержащихся мутеинах-антагонистах и отсылает к основной паре замен в D-спирали, R121D (Arg на Asp) и Y124D (Туг на Asp). В дополнение к этому третью замену вводили в связывающие поверхности либо А-, либо С-спирали в положении, которое увеличивает сродство связывания мутеина с рецепторной альфа-цепью. Помимо данных изменений большинство предпочтительных мутеинов-антагонистов IL-4 обладает аминокислотной последовательностью, идентичной таковой IL-4 дикого типа по другим, незамещенным остаткам.
Мутеины IL-4 по данному изобретению также могут характеризоваться вставками, делециями, заменами и модификациями аминокислот в одном или нескольких сайтах в других остатках полипептидной цепи нативного IL-4. В соответствии с данным изобретением любые такие вставки, делеции, замены и модификации должны приводить к образованию мутеина IL-4, который сохраняет активность, родственную таковой IL-4.
Авторы настоящего изобретения предпочитают консервативные модификации и замены в других положениях IL-4 (т.е. в тех,
которые обладают минимальным эффектом на вторичную и третичную структуру мутеина). Такие консервативные замены включают в себя таковые, описанные Dayhoff в The Atlas of Protein Sequence and Structure,
5 (1978), и Argos в ЕМВО J., 8:779-785 (1989). Например, аминокислоты, относящиеся к одной из следующих групп, представляют собой консервативные замены:
-ala, pro, gly, gln, asn, ser, thr;
-cys, ser, tyr, thr;
-val, ile, leu, met, ala, phe;
-lys, arg, his;
-phe, tyr, trp, his и
-asp, glu, tyr.
Авторы настоящего изобретения также предпочитают модификации или замены, которые устраняют сайты межмолекулярных сшивок или неправильного образования дисульфидных связей. Например, известно, что IL-4 содержит шесть остатков cys, в положениях белка дикого типа 3, 24, 46, 65, 99 и 127, одно или несколько из которых могут быть вовлечены в поперечно-сшивочные взаимодействия. Замены должны быть выбраны таким образом, чтобы сохранить третичную структуру белка дикого типа, насколько это возможно.
Под термином "пронумерованный в соответствии с IL-4 дикого типа" авторы настоящего изобретения подразумевают идентификацию выбранной аминокислоты относительно положения, которое данная аминокислота обычно занимает в IL-4 дикого типа. Если в мутеине IL-4 произведены вставки или делеции, для специалиста в данной области представится ценным тот факт, что, например, ser (S), обычно занимающий положение 125 при нумерации в соответствии с IL-4 дикого типа, может быть смещен в положение в мутеине. Однако локализация смещенного ser (S) может быть с легкостью определена путем проверки и корреляции фланкирующих аминокислот с таковыми, фланкирующими ser в IL-4 дикого типа.
Мутеины IL-4 по настоящему изобретению могут быть получены с помощью любого подходящего способа, известного в данной области. Такие способы включают в себя конструирование последовательности ДНК, кодирующей мутеины IL-4 по данному изобретению, и экспрессирование данных последовательностей в надлежащем образом трансформированном хозяине. Данный метод позволит получить рекомбинантные мутеины по данному изобретению. Однако мутеины по данному изобретению также могут быть получены, хотя и менее предпочтительно, с помощью химического синтеза и технологии рекомбинантных ДНК.
В одном варианте осуществления рекомбинантного метода получения мутеина по данному изобретению последовательность ДНК конструируют путем выделения или синтеза последовательности ДНК, кодирующей IL-4 дикого типа, с последующей заменой кодона, кодирующего треонин-13, на кодон, кодирующий аспарагиновую кислоту с помощью сайт-специфического мутагенеза. Данная методика хорошо известна. Смотри, например, Mark et al., Site-specific Mutagenesis of the Human Fibroblast Interferon Gene, Proc. Natl. Acad. Sci. USA 81:5662-66 (1984); патент США 4588585, включенные сюда в качестве ссылки.
Другой способ конструирования последовательности ДНК, кодирующей мутеины IL-4 по данному изобретению, представляет собой химический синтез. Например, ген, который кодирует желаемый мутеин IL-4, может быть синтезирован химическим путем с применением синтезатора олигонуклеотидов. Такие олигонуклеотиды обозначаются на основе аминокислотной последовательности желаемого мутеина IL-4 и предпочтительно выбирая те кодоны, которые являются предпочтительными в клетке-хозяине, в которой будет продуцироваться рекомбинантный мутеин. В отношении этого широко известно, что генетический код является вырожденным - что аминокислота может кодироваться несколькими кодонами. Например, Phe (F) кодируется двумя кодонами, ТТС или ТТТ, Туr (Y) кодируется ТАС или TAT, a His (Н) кодируется САС или CAT. Trp (W) кодируется единственным кодоном, TGG. Соответственно ценным представляется то, что для данной последовательности ДНК, кодирующей конкретный мутеин IL-4, будет множество вырожденных последовательностей ДНК, которые будут кодировать данный мутеин IL-4. Например, ценным представляется то, что в дополнение к предпочтительной последовательности ДНК, кодирующей мутеин T13D-IL-4[R121D/Y124D], показанной в ПОСЛ. ИД. :9, будет множество вырожденных последовательностей ДНК, которые кодируют показанный мутеин IL-4. Данные вырожденные последовательности ДНК рассматриваются в сфере данного изобретения. Таким образом, термин "его вырожденные варианты" в контексте данного изобретения означает все последовательности ДНК, которые кодируют конкретный мутеин.
Последовательность ДНК, кодирующая мутеин IL-4 по данному изобретению, полученная с помощью сайт-специфического мутагенеза, химического синтеза или других методов, может также включать или не включать последовательности ДНК, которые кодируют сигнальную последовательность. Такая сигнальная последовательность, при наличии, должна представлять собой последовательность, распознаваемую клеткой, выбранной для экспрессии мутеина IL-4. Она может являться прокариотической, эукариотической или представлять собой их комбинацию. Она также может представлять собой сигнальную последовательность нативного IL-4. Включение сигнальной последовательности зависит от того, является ли желаемой секреция мутеина IL-4 рекомбинантными клетками, в которых он продуцируется. Если выбранные клетки являются прокариотическими, как правило, предпочтительным является, чтобы последовательность ДНК не кодировала сигнальную последовательность, но включала в себя N-концевой метионин для направления экспрессии. Если выбранные клетки являются эукариотическими, как правило, предпочтительным является, чтобы сигнальная последовательность кодировалась и наиболее предпочтительно чтобы использовалась сигнальная последовательность IL-4 дикого типа.
Для синтеза гена, кодирующего мутеин IL-4 по данному изобретению, могут быть применены стандартные методики. Например, для конструирования обратнотранслируемого гена может быть применена полная аминокислотная последовательность. Может быть синтезирован олигомер ДНК, содержащий нуклеотидную последовательность, кодирующую мутеин IL-4. Например, несколько небольших олигонуклеотидов, кодирующих части желаемого полипептида, могут быть синтезированы и затем лигированы. Отдельные олигонуклеотиды обычно содержат 5'- или 3'-концевые избыточности для комплементарной сборки.
Собранные (с помощью синтеза, сайт-специфичного мутагенеза или другого метода) последовательности ДНК, кодирующие мутеин IL-4 по данному изобретению, будут вставлены в экспрессирующий вектор и оперативно пришиты к контролирующей экспрессию последовательности, подходящей для экспрессии мутеина IL-4 в желаемом трансформированном хозяине. Правильность сборки может быть подтверждена с помощью секвенирования нуклеиновой кислоты, рестрикционного картирования и экспрессии биологически активного полипептида в подходящем хозяине. Как хорошо известно в данной области, в целях достижения высоких уровней экспрессии внесенного по методу трансфекции гена в хозяине ген должен быть оперативно сшит с транскрипционными и трансляционными контролирующими экспрессию последовательностями, которые функционируют в выбранном экспрессирующем хозяине.
Выбор контролирующей экспрессию последовательности и экспрессирующего вектора будет зависеть от выбора хозяина. Может быть применен широкий спектр комбинаций хозяин/вектор. Применимые экспрессирующие векторы для эукариотических хозяев включают в себя, например, векторы, содержащие контролирующие экспрессию последовательности из SV40, вируса папилломы крупного рогатого скота, аденовируса и цитомегаловируса. Применимые экспрессирующие векторы для бактериальных хозяев включают в себя известные бактериальные плазмиды, такие как плазмиды из Е. coli, включая col El, pCRl, pER32z, pMB9 и их производные, плазмиды из более широкого спектра хозяев, такие как RP4, фаговые ДНК, например многочисленные производные фага лямбда, например NM989, и другие ДНК-содержащие фаги, такие как М13 и нитчатые фаги, содержащие одноцепочечную ДНК. Применимые экспрессирующие векторы для дрожжевых клеток включают в себя плазмиду 2μ и ее производные. Применимые векторы для клеток насекомых включают в себя pVL941. Авторы настоящего изобретения предпочитают pFastBacТМ1 (GibcoBRL, Gaithersburg, MD). Cate et al., Isolation of the Bovine and Human Genes for Mullerian Inhibiting Substance and Expression of the Human Gene in Animal Cells, Cell, 45:685-98 (1986).
В дополнение к этому в данных векторах может быть применена любая из большого многообразия контролирующих экспрессию последовательностей. Такие применимые контролирующие экспрессию последовательности включают в себя контролирующие экспрессию последовательности, ассоциированные со структурными генами указанных выше экспрессирующих векторов. Примеры применимых контролирующих экспрессию последовательностей включают в себя, например, ранние и поздние промоторы SV40 или аденовируса, lac-систему, trp-систему, ТАС- или TRC-систему, главные операторные и промоторные участки фага лямбда, например PL, регулярные участки белка оболочки fd, промотор 3-фосфоглицераткиназы или других гликолитических ферментов, промоторы кислой фосфатазы, например PhoA, промоторы системы α-спаривания дрожжей, polyhedron промотор бакуловируса и другие последовательности, контролирующие экспрессию генов прокариотических и эукариотических клеток или их вирусов, и различные их комбинации.
Для продукции мутеинов IL-4 по данному изобретению может быть применен любой подходящий хозяин, включая бактерии, грибы (включая дрожжевые), растение, насекомое, млекопитающее или другие подходящие животные клетки или клеточные линии, равно как и трансгенные животные или растения. Более конкретно, данные хозяева могут включать в себя хорошо известные эукариотические и прокариотические хозяева, такие как штаммы Е. coli, Pseudomonas, Bacillus, Streptomyces, клетки грибов, дрожжей, насекомых, таких как Spodoptera frugiperda (SF9), животные клетки, такие как яйцеклетки китайского хомячка (СНО) и мышиные клетки, такие как NS/О, клетки африканской зеленой мартышки, такие как COS 1, COS 7, BSC 1, BSC 40 и BNT 10, и человеческие клетки, равно как и растительные клетки в культуре клеток ткани. Для экспрессии в животных клетках авторы настоящего изобретения предпочитают применять клетки СНО и клетки COS 7 в культурах и, в особенности, СНО-клеточную линию СНО (DHFR-).
Разумеется следует понимать, что не все векторы и контролирующие экспрессию последовательности будут функционировать одинаково эффективно в экспрессии последовательностей ДНК, описанных здесь. Также не все хозяева будут функционировать одинаково эффективно с одной и той же экспрессирующей системой. Однако специалист в данной области способен сделать выбор между данными векторами, контролирующими экспрессию последовательностями и хозяевами без проведения излишней экспериментальной работы. Например, при выборе вектора должен приниматься во внимание фактор хозяина, поскольку вектору предстоит в нем реплицироваться. Также следует принимать во внимание факторы количества копий вектора, возможность контроля за данным количеством копий и экспрессии каких-либо других белков, кодируемых вектором, таких как маркеров антибиотиков. Например, предпочтительные векторы для применения по данному изобретению включают таковые, которые позволяют ДНК, кодирующей мутеины IL-4, быть амплифицированной в количестве копий. Такие многокопийные векторы хорошо известны в данной области. Они включают, например, векторы, способные амплифицироваться посредством DHFR-амплификации (смотри, например, Kaufman, патент Соединенных Штатов 4470461, Kaufman and Sharp, Construction of a Modular Dihydrofolate Reductase cDNA Gene: Analysis of Signals Utilized for Efficient Expression, Mol. Cell. Biol., 2:1304-19 (1982)) или глютаминсинтетазной ("GS") амплификации (смотри, например, патент США 5122464 и европейскую опубликованную заявку на патент ЕРО338841).
При выборе контролирующей экспрессию последовательности также следует учитывать множество факторов. Они включают в себя, например, относительную длину последовательности, ее контролируемость и ее совместимость с подлинной последовательностью ДНК, кодирующей мутеины IL-4 по данному изобретению, особенно это касается потенциальных вторичных структур. Хозяев следует выбирать, учитывая их совместимость с выбранным вектором, токсичность продукта, кодируемого последовательностями ДНК по данному изобретению, их характеристики секреции, их способность правильно сворачивать полипептиды, требования к их ферментации или культивированию и простоту очистки продуктов, кодируемых последовательностями ДНК.
В пределах данных параметров специалист может избрать различные комбинации вектор/контролирующая экспрессию последовательность/хозяин, которые будут экспрессировать желаемые последовательности ДНК в процессе ферментации либо в ходе широкомасштабного культивирования животных клеток, например, применяя клетки СНО или клетки COS 7.
Мутеины IL-4, полученные в соответствии с настоящим изобретением, могут быть гликозилированными либо негликозилированными в зависимости от организма-хозяина, применяемого для продукции мутеина. Если в качестве хозяина выбраны бактерии, продуцируемый мутеин IL-4 будет негликозилированным. С другой стороны, эукариотические клетки будут гликозилировать мутеины IL-4, хотя, возможно, не так, как гликозилируется нативный IL-4.
Мутеин IL-4, продуцируемый трансформированньм хозяином, может быть очищен в соответствии с любой подходящей методикой. Для очистки IL-4 известны различные методики. Смотри, например, патенты США 5013824; 5017691 и международную заявку на патент WО9604306-A2. Авторы настоящего изобретения предпочитают применять иммуноаффинную очистку. Смотри, например, Okamura et al., Human Fibroblastoid Interferon: Immunosorbent Column Chromatography and N-Terminal Ammo Acid Sequence, Biochem., 19:3831-35 (1980).
Биологическая активность мутеинов IL-4 по данному изобретению может быть проанализирована с помощью любой подходящей методики, известной в данной области. Такие анализы включают в себя антительную нейтрализацию противовирусной активности, индукцию протеинкиназной, олигоаденилат-2,5-А-синтетазной или фосфодиэстеразной активностей, как описано в европейской заявке на патент ЕР-В1-41313. Такие анализы также включают в себя иммуномодуляторные анализы (смотри, например, патент США 4753795), анализы подавления роста, пролиферации Т-клеток, индукции IL-6 и индукции МСР-1 в эндотелиальных клетках и определение связывания с клетками, которые экспрессируют рецепторы интерлейкина-4. Смотри также Spits H., Yssel Н., Takebe Y. et al., Recombinant Interleukin-4 Promotes the Growth of Human Т Cells, J. Immunol., 139:1142-47(1987).
Мутеин IL-4 будет вводиться в дозировках, соответствующих либо превышающих таковые, применяемые в лечении нативным дикого типа IL-4 или рекомбинантным IL-4. Предпочтительно вводят эффективное количество мутеина IL-4. Термин "эффективное количество" означает количество, способное предотвратить либо уменьшить тяжесть или распространение состояния или симптома, подвергающегося лечению. Для специалиста в данной области будет очевидно, что эффективное количество мутеина IL-4 будет зависеть, помимо прочего, от заболевания, дозировки, схемы введения мутеина IL-4, от того, вводят ли мутеин IL-4 отдельно или в сочетании с другими лекарственными средствами, от времени полужизни композиции в сыворотке и общего состояния здоровья пациента.
Мутеин IL-4 предпочтительно вводят в композиции, включающие в себя фармацевтически приемлемый носитель. Термин "фармацевтически приемлемый носитель" означает носитель, который не вызывает каких-либо неблагоприятных эффектов у пациентов, которым его вводят. Такие фармацевтически приемлемые носители хорошо известны в данной области. Авторы настоящего изобретения предпочитают применять 2% HSA/ФБР при рН 7,0.
Мутеины IL-4 по настоящему изобретению могут быть включены в состав фармацевтических композиций в соответствии с хорошо известными методиками. Смотри, например, подходящие составы, описанные E.W. Martin в Remington's Pharmaceutical Science, включенные сюда в качестве ссылки. Фармацевтическая композиция мутеина IL-4 может быть составлена в виде множества форм, включая жидкую, гелеобразную, лиофилизированную или любую другую подходящую форму. Предпочтительная форма будет зависеть от конкретного симптома, подвергающегося лечению, и будет очевидна для специалиста в данной области.
Фармацевтическая композиция мутеина IL-4 может быть введена перорально, в виде аэрозоля, внутривенно, внутримышечно, внутрибрюшинно, внутрикожно или подкожно или любым другим приемлемым образом. Предпочтительный способ введения будет зависеть от конкретного симптома, подвергающегося лечению, и будет очевиден для специалиста в данной области. Фармацевтическая композиция мутеина IL-4 может быть введена в сочетании с другими лекарственными средствами. Данные средства могут быть включены в виде части той же самой фармацевтической композиции или могут быть введены отдельно от мутеина IL-4 либо одновременно, либо в соответствии с любой другой приемлемой схемой лечения. К тому же фармацевтическая композиция мутеина IL-4 может быть применена в качестве дополнения к другим курсам лечения.
Соответственно данное изобретение обеспечивает композиции и способы лечения иммунных заболеваний, разновидностей рака или опухолей, аномального клеточного роста или иммуномодуляции у любого подходящего животного, предпочтительно млекопитающего, наиболее предпочтительно человека. Как указано выше, IL-4 обладает множеством эффектов. Некоторые из них представляют собой стимуляцию пролиферации Т-клеток, дифференцировки Т-хелперных клеток, индукцию активации и пролиферации человеческих В-клеток и лимфокин-направленное переключение классов иммуноглобулина. Эффекты, оказываемые на лимфоидную ткань, включают увеличение уровня экспрессии антигена МНС II класса (Noelle R. et al., Increased Expression of Ia Antigens on Resting В Cells: a New Role for В Cell Growth Factor, PNAS USA, 81:6149-53 (1984)), и CD23 на В-клетках (Kikutani H. et al., Molecular Structure of Human Lymphocyte Receptor for Immunoglobulin, Cell 47:657-61 (1986)). Таким образом, биология IL-4 предполагает, что он может играть значительную роль в развитии аллергии и аллергических воспалительных заболеваний, включая бронхиальную астму. Т-хелперные клетки 1 типа (Тh1) и 2 типа (Th2) вовлечены в иммунный ответ. Активированные клетки Th2 секретируют IL-4 и блокируют прогрессию Тh1. Любое Тh2-опосредованное заболевание поддается лечению антагонистом IL-4; также любое Тh1 - опосредованное заболевание поддается лечению агонистом IL-4.
Также рассматривается применение последовательностей ДНК, кодирующих мутеины IL-4 по данному изобретению, в геннотерапевтических приложениях. Рассматриваемые в отношении антагонистов IL-4 геннотерапевтические приложения включают лечение таких заболеваний, при которых ожидается, что IL-4 вызывает или усиливает имеющееся клиническое состояние, такое как состояние, связанное с воспалением, (бронхиальная астма) или аллергии. Показания для применения агонистов включают аутоиммунные заболевания, такие как ревматоидный артрит, рассеянный склероз и инсулинзависимый сахарный диабет. Данные аутоиммунные заболевания характеризуются поляризацией в продукции клеточных популяций Т-хелперов в сторону Т-хелперов 1 типа (Тh1).
Местная
доставка мутеинов IL-4, как агонистов, так и антагонистов, с применением генной терапии может обеспечить наличие лекарственного средства в области-мишени при избежании трудностей, сопряженных с
потенциальной токсичностью, связанных с неспецифическим введением агонистов. Рассматриваются методики генной терапии как in vitro, так и in vivo. Известно несколько способов переноса потенциально
лекарственных генов в определенные клеточные популяции. Смотри, например, Mulligan, The Basic Science of Gene Therapy, Science, 260:926-31 (1993). Данные способы включают:
1. Прямой перенос
генов. Смотри, например, Wolff et al., Direct Gene Transfer into Mouse Muscle In Vivo, Science, 247:1465-68 (1990).
2. Перенос ДНК с применением липосом. Смотри, например, Caplen et al., Liposome-mediated CFTR Gene Transfer to the Nasal Epithelium of Patients with Cystic Fibrosis, Nature Med. , 3:39-46 (1995); Crystal, The Gene As a Drug, Nature Med., 1:15-17 (1995); Gao and Huang, A Novel Cationic Liposome Reagent for Efficient Transfection of Mammalian Cells, Biochem. Biophys. Res. Comm., 179:280-85(1991).
3. Перенос ДНК с применением ретровирусов. Смотри, например, Кау et al., In Vivo Gene Therapy of Hemophilia B: Sustained Partial Correction in Factor IX-Deficient Dogs, Science, 262:117-19 (1993); Anderson, Human Gene Therapy, Science, 256:808-13 (1992).
4. Перенос ДНК с применением ДНК-содержащих вирусов. Такие ДНК-содержащие вирусы включают аденовирусы (предпочтительно, векторы на основе Ad-2 или Ad-5), вирусы герпеса (предпочтительно, векторы на основе вируса простого герпеса) и парвовирусы (предпочтительно векторы на основе неспособного воспроизводиться без вируса-помощника, или неавтономного, парвовируса, более предпочтительно векторы на основе аденоассоциированного вируса, наиболее предпочтительно, векторы на основе AAV-2). Смотри, например, Alt et al., The Use of DNA Viruses As Vectors for Gene Therapy, Gene Therapy, 1:367-84 (1994); патенты США 4797368, 5139941, включенные в качестве ссылки.
Выбор конкретной векторной системы для переноса интересующего гена будет зависеть от множества факторов. Одним важным фактором является природа популяции клеток-мишеней. Хотя ретровирусные векторы были тщательно изучены и применены в ряде геннотерапевтических приложений, данные векторы, как правило, не применимы для инфицирования неделящихся клеток. В дополнение к этому ретровирусы обладают потенциальной онкогенностью.
Аденовирусы имеют то преимущество, что обладая широким спектром хозяев, могут инфицировать покоящиеся, или окончательно дифференцированные, клетки, такие нейроны или гепатоциты, и являются, по существу, неонкогенными. Смотри, например, Ali et al., supra, p.367. Аденовирусы не интегрируются геном хозяина. Поскольку они находятся вне хромосом, риск инсерционного мутагенеза резко снижен. Ali et al., supra, p.373.
Аденоассоциированные вирусы проявляют преимущества, аналогичные таковым векторов на основе аденовирусов. Однако AAV проявляют сайт-специфичную интеграцию в человеческую хромосому 19. Ali et al., supra, p.377. В соответствии с данным осуществлением генную терапию ДНК, кодирующей мутеины IL-4 по данному изобретению, применяют к пациенту, нуждающемуся в ней, одновременно с или непосредственно после постановки диагноза.
Для специалиста в данной области ценным представляется то, что любой подходящий для генной терапии вектор, содержащий ДНК, кодирующую мутеин IL-4, может быть применен в соответствии с данным вариантом осуществления. Известны методики конструирования такого вектора. Смотри, например, Ohno et al., supra, p. 784; Chang et al., supra, p. 522. Введение вектора, содержащего ДНК, кодирующую мутеин IL-4, в сайт-мишень может быть проведено с применением известных методик, например, как описано в Ohno et al., supra, p.784.
Следующие примеры изложены в целях лучшего понимания данного изобретения. Данные примеры предназначены исключительно для иллюстрации и не должны быть истолкованы как ограничивающие каким-либо образом сферу изобретения.
Примеры.
Аланиновые замены вводят в последовательность IL-4 дикого типа с помощью сайт-специфичного мутагенеза в положения, соответствующие остаткам, для которых предсказана локализация на поверхности А- и С-спиралей IL-4 (Smith LJ; Redfield С; Boyd J; Lawrence GM; Edwards RG; Smith RA and Dobson CM, Human interleukin 4. The solution structure of a four-helix bundle protein, J. Mol. Biol., 224(4):899-904 (1992)). Наиболее вероятно, что именно данные остатки опосредуют взаимодействие IL-4 с IL-4Rα (Фиг. 1); эффекты на сродство связывания аланинзамещенного IL-4 с IL-4Rα указывают на то, что замещенные остатки могут быть вовлечены в процесс связывания. Остатки, замещенные аланином и оказывающие промежуточное влияние на сродство, широко замещаются в целях установления изменений, которые увеличивают сродство. Мутации, которые увеличивают сродство и объединены, могут позволить достичь комбинаторного увеличения сродства IL-4 (или родственных IL-4 пептидов) к IL-4Rα. Увеличение сродства должно коррелировать с увеличением силы действия.
Мутеины получают с помощью сайт-специфичного мутагенеза, экспрессируют в бакуловирусной системе, очищают до гомогенности, количественно оценивают с помощью аминокислотного анализа и исследуют в анализах рецепторного связывания. Аминокислотная последовательность зрелого человеческого IL-4 (ПОСЛ. ИД. : 1), примененного в данном исследовании, показана ниже; His в положении 1 представляет собой N-конец зрелого полипептида. А-, С- и D-спирали указаны над соответствующими им начальными точками и подчеркнуты. Аминокислоты, подходящая замена которых позволяла достичь вариантов с более высоким сродством, показаны жирным шрифтом (см. в конце описания).
Мутации, изученные в данном исследовании, вводят в известный вариант антагониста человеческого IL-4, содержащий две замены в D-спирали, R121D и Y124D (Tony HP et al., Design of Human Interieukin-4 Antagonists in Inhibiting Interleukin-4-dependent and Interleukin-13-dependent responses in T-cells and B-cells with high efficiency, Eur. J. Biochem., 225(2):659-65 (1994); данный мутеин обозначают как "IL-4[R121D/Y124D]"). Мутеины экспрессируют в бакуловирусной системе, очищают до гомогенности и оценивают в твердофазном анализе связывания IL-4Rα. Биологическую значимость увеличения сродства к IL-4Rα оценивают в анализах пролиферации Т-клеток. Поскольку мутеин IL-4[R121D/Y124D] является антагонистом IL-4, увеличенное сродство к IL-4Rα должно приводить к пониженным значениям ИК50 для мутеина-антагониста с повышенным сродством (ИК50 определяют как концентрацию антагониста, необходимую для ингибирования реакции на определенный агонист на 50%).
Пример 1. Продукция мутеинов.
Мутеины получают с помощью сайт-специфичного мутагенеза с применением праймеров, содержащих кодоны, соответствующие желаемой мутации,
по существу, так, как описано Kunkel ТА, Roberts JD and Zakour RA, "Rapid and efficient site-specific mutagenesis without phenotypic selection", Methods Enzymol. 154:367-382 (1987). Вкратце, кДНК
человеческого IL-4, содержащую сайты рестрикции Bam HI и Хbа I, субклонируют в вектор М13 mр19 фага М13 (New England Biolabs, Beverly, MA), применяя те же сайты. кДНК IL-4 дикого типа получают,
применяя полимеразную цепную реакцию (ПЦР, "PCR") с пула кДНК, полученного с мРНК, выделенной из лимфоцитов периферической крови человека, индуцированных в течение 24 часов
форбол-12-миристат-13-ацетатом (10 нг/мл). Примененные праймеры ПЦР представляют собой для 5'-конца открытой рамки считывания IL-4
5'-CGC GGA TCC ATG GGT СТС АСС ТСС-3' (ПОСЛ. ИД. :2)
и для 3'-конца открытой рамки считывания IL-4
5'-CGC TCT AGA СТА GCT CGA АСА СТТ TGA АТ-3'(ПОСЛ. ИД. :3).
Сайты рестрикции Bam HI (5'-конец) и Xba I (3'-конец) включают в каждый олигонуклеотид и обозначают курсивом. Примененные условия ПЦР представляют собой 1 минуту при 94oС, 1 минуту при 58,7oС и 1 минуту при 72oС в течение 25 циклов. Правильность полученной таким образом последовательности кДНК IL-4 подтверждает с помощью секвенирования с применением набора для секвенирования Sequenase® (Amersham Life Sciences, Arlington Heights, IL), как описано производителем. Урацилсодержащую одноцепочечную ДНК (U-ДНК) получают путем трансформации штамма Е. coli CJ236 (Bio-Rad Laboratories, Hercules, CA) M13 mpl9, содержащим кДНК IL-4. В сайт-специфичном мутагенезе, главным образом, применяют праймеры, содержащие 15 нуклеотидов, гомологичных матричной U-ДНК, расположенной на 5'-конце от кодона(ов), подвергающихся мутагенезу, нуклеотиды, которые заключают в себе желаемую замену, и дополнительные 10 нуклеотидов, гомологичных матричной U-ДНК, расположенной на 3'-конце от последнего заменяемого нуклеотида. Мутации в D-спирали Arg-121 на Asp и Туr-124 на Asp вводят в последовательность IL-4 дикого типа. Урацилсодержащую ДНК для данного варианта, обозначаемого "IL-4[R121D/Y124D]", получают, как описано выше. Все мутации, произведенные в данных исследованиях, производят с применением матрицы IL-4[R121D/Y124D].
Праймеры фосфорилируют, применяя полинуклеотидкиназу Т4 (New England Biolabs, Beverly, MA), используя протокол производителя. Затем фосфорилированный праймер гибридизуют с U-ДНК матрицей с последующим удлинением цепи с помощью ДНК-полимеразы Т7 (Bio-Rad Laboratories, Hercules, CA). Клетки штамма DH5αтм (GibcoBRL, Gaithersburg, MD) трансформируют 5 мкл реакционной смеси и высевают на планшет в среде LB, содержащей 0,7% агара. После инкубации при 37oС бляшки размножают путем взятия одной бляшки и переноса в 2 мл среды LB и культивируют в течение ночи при 37oС. Одноцепочечную ДНК выделяют, применяя набор для очистки M13 (Qiagen, Inc., Chatsworth, CA) в соответствии с протоколом производителя, и клоны, содержащие желаемую мутацию идентифицируют путем секвенирования одноцепочечной ДНК, применяя набор для секвенирования Sequenase® (Amersham Life Sciences, Arlington Heights, IL) в соответствии с протоколом производителя. Репликативную форму ДНК (двухцепочечную форму фага М13), соответствующую бляшкам, содержащим надлежащим образом мутировавшую последовательность IL-4, выделяют, применяя Qiagen Plasmid Miniprep Kit (Qiagen, Inc., Chatsworth, CA). кДНК мутеина IL-4 выделяют, применяя Bam HI и Xba I с очищенной репликативной формы ДНК, и субклонируют в плазмидный вектор pFastBacТМ1 (GibcoBRL, Gaithersburg, MD). По завершении субклонирования получают рекомбинантную бакуловирусную ДНК (на которую здесь далее ссылаются как на Bacmid) путем трансформации pFastBacТМ1, содержащим кДНК мутеина, штамма DH10BacТМ E. coli (GibcoBRL, Gaithersburg, MD), как описано производителем. Мутеины экспрессируют в Spodoptera frugiperda (Sf) 9 с применением бакуловирусной экспрессирующей системы Вас-to-Bac
Пример 2. Очистка мутеинов.
Моноклональные антитела С400.1 и С400.17 против человеческого IL-4 нарабатываются в организме мышей с применением стандартных протоколов с использованием в качестве иммуногена рекомбинантного человеческого IL-4 (Genzyme Diagnostics, Cambridge, МА), продуцируются в составе асцитической жидкости, подвергаются очистке и присоединяются к CNBr-активированной сефарозе (Pharmacia, Uppsala, Sweden) в соответствии с протоколом производителя. Супернатанты клеток Sf9, полученные в результате инфицирования клеток Sf9 рекомбинантным бакуловирусом, содержащие соответствующий мутеин IL-4, наносят на 1 мл колонку Sepharose, сшитой с MAT против IL-4, промывают 100 мМ NаНСО3, 500 мМ NaCl, pH 8,3, для удаления соли промывают водой и элюируют 8 объемами колонки 100 мМ глицина, pH 3,0. Фракции собирают в силиконизированные сосуды, содержащие 0,1 объема 1 М Триса, pH 8,0. Белок-мутеин далее очищают по методу обращенно-фазовой хроматографии, применяя колонку С 18

Пример 3. Анализы рецепторного связывания.
В целях определения влияния замены на способность мутеинов IL-4 связываться с IL-4Rα
(Ldzerda R.L. et al., Human interleukin 4 receptor confers biological responsiveness and defines a novel receptor superfamily, J. Exp. Med. 171: 861 (1990)) разрабатывают твердофазный анализ
рецепторного связывания. Сродство мутеинов измеряют по их способности вытеснять IL-4, помеченный радиоактивной меткой, с IL-4Rα, связанного с твердой поверхностью. На Фиг. 2 показана
способность T13D-IL-4[R121D/Y124D] конкурировать с125I-IL-4 в твердофазном анализе связывания по сравнению с IL-4[R121D/Y124D]. Анализ проводят с применением 96-луночных FlashPlates® (DuPont NEN®, Boston, MA), покрытых стрептавидином; внеклеточный домен IL-4Rα присоединяют к данным планшетам посредством пептидной метки, встроенной во
внеклеточный домен IL-4Rα, который связывается со стрептавидином. FlashPlates содержат сцинтиллирующее вещество, внедренное в пластик планшета, которое обладает свойством, что лишь соединение,
содержащее радиоактивную метку, находящееся в непосредственной близости от поверхности планшета, будет возбуждать сцинтилляцию. В каждую лунку добавляют образцы, содержащие IL-4 и мутеины-антагонисты
IL-4, содержащие радиоактивную метку, и инкубируют до
достижения равновесия. Поскольку несвязанное соединение, содержащее радиоактивную метку, не возбуждает сцинтилляционного сигнала, стадии
промывки до оценки количества связанной в каждой лунке радиоактивности не требуется. Измеренная таким образом радиоактивность представляет собой количество IL-4, содержащего радиоактивную метку,
связавшегося с IL-4Rα и при учете количества добавленного немеченого мутеина-антагониста IL-4 позволяет произвести расчет сродства немеченого мутеина-антагониста IL-4 к IL-4Rα.
Внутренний стандарт в каждом анализе получают путем измерения сродства IL-4[R121D/Y124D] параллельно с каждым мутеином. Таким образом, осуществляют конкретные относительные измерения сродства, которые
позволяют оценить влияние отдельных замен на сродство к IL-4Rα.
Внеклеточный домен IL-4Rα получают, применяя ПЦР с Jurkat cell Igtl1 library (Stratagene Cloning Systems, La
Jolla, CA). Праймеры ПЦР, примененные для выделения внеклеточного домена IL-4Rα, представляют собой для 5'-конца открытой рамки считывания IL-4
5'-GGC ATG GAT CCA TGG GGT GGC TTT GCT
CTG G-3' (ПОСЛ. ИД. :4)
и для 3'-конца внеклеточного домена IL-4Rα
5'-AAG CCG СТА GCG CTG TGC TGC TCG AAG GGC-3' (ПОСЛ. ИД. :5).
Примененные условия ПЦР представляют собой 1 минуту при 94oС, 1 минуту при 65,8oС и 1 минуту при 72oС в течение 30 циклов. Полученный продукт ПЦР расщепляют ферментами рестрикции BamHI и Есо47III и субклонируют в вектор pBluescript® (Stratagene Cloning Systems, La Jolla, CA), содержащий ДНК с кодонами, соответствующими последовательности Ser-Ala-Trp-Arg-His-Pro-Gln-Phe-Gly-Gly (ПОСЛ. ИД. : 6), расщепляемыми теми же ферментами. Сообщалось, что данная последовательность связывается со стрептавидином (Schmidt TG and Skerra A. , The random peptide library-assisted engineering of a C-terminal affinity peptide, useful for the detection and purification of a functional Ig Fv fragment, Protein Eng, 6(1):109-122 (1992)). Полученный таким образом внеклеточный домен IL-4Rα кодируют пептидную последовательность Ser-Ala-Trp-Arg-His-Pro-Gln-Phe-Gly-Gly (ПОСЛ. ИД. : 6) на С-конце внеклеточного домена и называют sIL-4Rα -STX (Met в положении 1 представляет собой N-конец зрелого IL-4Rα) и представляет собой ПОСЛ. ИД. :7.
Белок sIL-4Rα-STX продуцируют, применяя бакуловирусную систему, идентично тому, как продуцируют мутеины-антагонисты IL-4, очищают по методу афинной хроматографии с помощью сшитого с IL-4 носителя, как описано (Kruse N. et аl., "Two distinct functional sites of human interleukin 4 are identified by variants impaired in either receptor binding or receptor activation. " EMBO J., 12(13), p. 5121-9 (1993)), и хранили в ФБР. Сшитый с IL-4 носитель получают путем присоединения IL-4, продуцируемого в Е. coli, к CNBr Sepharose 4B, как описано производителем (Pharmacia, Uppsala, Sweden). Покрытые стрептавидином FlashPlates® (DuPont NEN®, Boston, MA) покрывают 100 мкл 2 мкг/мл sIL-4Rα-STX в 100 мМ Трисе, 0,1% BSA, pH 7,0, в течение 2 ч при 20oС, промывают ФБР, 0,1% BSA, рН 7,6, и инкубируют с 200 пМ125I-IL-4 (DuPont NEN®, Boston, MA) и варьирующими концентрациями мутеина-антагониста IL-4 в 100 мкл ФБР, 0,1% BSA, pH 7,6, в течение 1,5 ч при 20oС в четырех экземплярах. Анализы повторяют, по крайней мере, дважды. В качестве внутреннего контроля параллельно с каждым мутеином на том же FlashPlate® титруют IL-4[R121D/Y124D] . Связанную радиоактивность измеряют с помощью сцинтилляционного счетчика TopCountТМ (Packard Instrument Co., Meriden, CT) и значения Kd расчитывают с применением программы Ligand (Munson P.J. and Rodbard D. , "Computerized Analysis of Ligand Binding Data." Meth. Enzymol., 92, p. 543-576 (1983)); значения ошибки Kd, выражаемые как%CV, составляет 2-20%. Результаты выражают в виде отношения Kd мутеина/Kd IL-4[R121D/Y124D], используя данные, полученные по каждому анализируемому планшету. Различия между измеренными значениями Kd отражают либо относительное увеличение сродства соответствующего мутеина к IL-4Rα (т. е. Кd мутеина/Kd IL-4[R121D/Y124D] <1), либо относительное снижение сродства соответствующего мутеина к IL-4Rα (т.е. Kd мутеина/Kd IL-4[R121D/Y124D]>1).
Пример 4. Анализ пролиферации 1o Т-клеток.
Первичные Т-клетки получают из свежей крови здоровых доноров и очищают путем центрифугирования с применением Ficoll-Paque® Plus (Pharmacia, Uppsala, Sweden), по существу, как описано в Kruse N., Tony H.P. and Sebald W., Conversion of human interleukin-4 into a high affinity antagonist by a single amino acid replacement, Embo J. 11:3237-44 (1992). Очищенные мононуклеарные клетки периферической крови инкубируют в течение 7 суток с 10 мкг/мл фитогемагглютинина (Sigma Chemical Co., St. Louis, МО), собирают с помощью центрифугирования и промывают в среде RPMI 1640 (GibcoBRL, Gaithersburg, MD). 5•104 активированных Т-клеток/лунка (ФГА-бластов) инкубируют с варьирующими количествами IL-4 или мутеина в среде RPMI 1640, содержащей 10% околоплодной коровьей сыворотки, 10 мМ HEPES, рН 7,5, 2 мМ L-глютамин, 100 единиц/мл пенициллина G и 100 мкг/мл стрептомицина сульфата, в 96-луночных планшетах в течение 48 ч при 37oС, метят 1 мкКи3 H-тимидина (DuPont NEN®, Boston, МА)/лунка в течение 6 ч, собирают и радиоактивность измеряют с помощью сцинтилляционного счетчика TopCountТМ (Packard Instrument Co., Meriden, CT).
Пример 5. Влияние замены аланином на сродство IL-4 к IL-4Rα.
Влияние замены аланином поверхностно локализованных остатков в спиралях А и С IL-4 на
сродство IL-4 к IL-4Rα показано в Таблице 1.
Замены аланином, как правило, не вызывают структурных изменений в пространственной организации белка, влияние на активность, в данном случае на сродство, может быть приписано потере замещенной боковой цепи (Cunningham B. C. , Wells J.A., High-resolution epitope mapping of hGH-receptor interactions by alanine-scanning mutagenesis, Science 244(4908): 1081-5 (1989)). Незначительные изменения сродства (например, ~2-кратные), которые возникают в результате замены аланином, предполагают, что остаток/замещенное положение не вовлечены во взаимодействие; значительные эффекты (например, > 100-кратные) предполагают, что остаток/замещенное положение являются принципиально важными для взаимодействия (Lowman HB et al., "Selecting high-affinity binding proteins by monovalent phage display. " Biochemistry 30(45), p. 10832-8 (1991)). Lowman et al. (там же) обосновали, что исследовались остатки, оказывающие косвенное влияние на процесс связывания в результате замены аланином, в дополнение к наиболее чувствительным остаткам, вовлеченным во взаимодействие.
Применение данных заключений к результатам
данного сканирования с помощью аланина А- и С-спиралей IL-4, позволяет установить, что наиболее важными для взаимодействия IL-4 с IL-4Rα остатками являются Glu-9 и Arg-88; остатки с
промежуточным влиянием включают Ile-5>Asn-89>Lys-84~Arg-81>Thr-13~Gln-78~ Arg-85~ Lys-77; остатки, вероятно, не вовлеченные во взаимодействие включают Gln-8, Ile-11, Lys-12,
Asn-15, His-74, Phe-82 и Trp-91. Ser-16, на основании наблюдаемого увеличения сродства при замещении аланином, находится вблизи или в пределах области взаимодействия между IL-4 и IL-4Rα. Данные
результаты определяют возможную поверхность связывания IL-4 с IL-4Rα, которая, будучи воспринята в контексте структуры IL-4 (Smith LJ et аl., Human interleukin 4. The solution structure of a
four-helix bundle protein, J. Mol. Biol., 224(4): 899-904 (1992)), состоит из смежных частей А- и С-спиралей IL-4 и простирается приблизительно на три оборота каждой спирали, т.е. на положения 5-16
А-спирали и 77-89 С-спирали. Наиболее вероятные остатки, вовлеченные в контакт с альфа-субъединицей рецептора IL-4, представляют собой в А-спирали: Ile-5, Glu-9, Thr-13 и Ser-16; в С-спирали: Lys-77,
Gln-78, Arg-81, Lys-84, Arg-85, Arg-88 и Asn-89. Структурно принципиально важный центр взаимодействия состоит из остатков Glu-9, Arg-88 и Asn-89, и наблюдаемый эффект аланина обычно снижается при
смещении на один остаток от данной части молекулы. Таким образом, данный анализ описывает поверхность связывания IL-4 с IL-4Rα.
Пример 6. Замены мутеинов в выбранных положениях.
В предшествующем анализе гормона роста обнаружены остатки, замененные аланином, которые оказывают опосредованное влияние на сродство, и замены которых увеличивают сродство гормона роста к его рецептору (Lowman HB et аl., "Selecting high-affinity binding proteins by monovalent phage display." Biochemistry 30(45), p. 10832-8 (1991)). Установлено, что природу замен данного остатка, которые приводят к увеличению сродства, предсказать не представляется возможным. Таким образом, в представленном здесь анализе все замены, которые не оказывают характерных структурных эффектов (т.е. за исключением Cys, Gly, Pro) или не вступают легко в окислительные реакции (т. е. за исключением Met), вводят в положения-мишени (см. Таблицу 2).
Таким образом, цистеин, глицин, метионин и пролин исключают из дальнейшего анализа замен. Остатки выбирают для дальнейшего анализа, если при замене аланином наблюдают снижение сродства от 5 до 80 раз или какое-либо увеличение сродства; данный интервал выбирают на основании результатов, полученных Lowman et al. (там же). В дополнение к этому Ser-16 выбирают для дальнейшего анализа по причине наблюдаемого увеличения сродства, которое является результатом замены аланином; это позволяет предположить, что другие замены в данном положении могут также привести к увеличению сродства.
Пример 7. Замены, которые
приводили к увеличению сродства к IL-4Rα.
Мутеины, содержащие замены в отдельных положениях А- и С-спиралей, получают в сочетании с основой IL-4[R121D/Y124D]; анализы конкурентного
связывания проводят таким образом, что каждый мутеин параллельно сравнивают с IL-4[R121D/Y124D] . Это позволяет проводить непосредственное сравнение и, таким образом, делать заключения об эффекте
каждой замены на сродство отдельного мутеина к IL-4Rα.
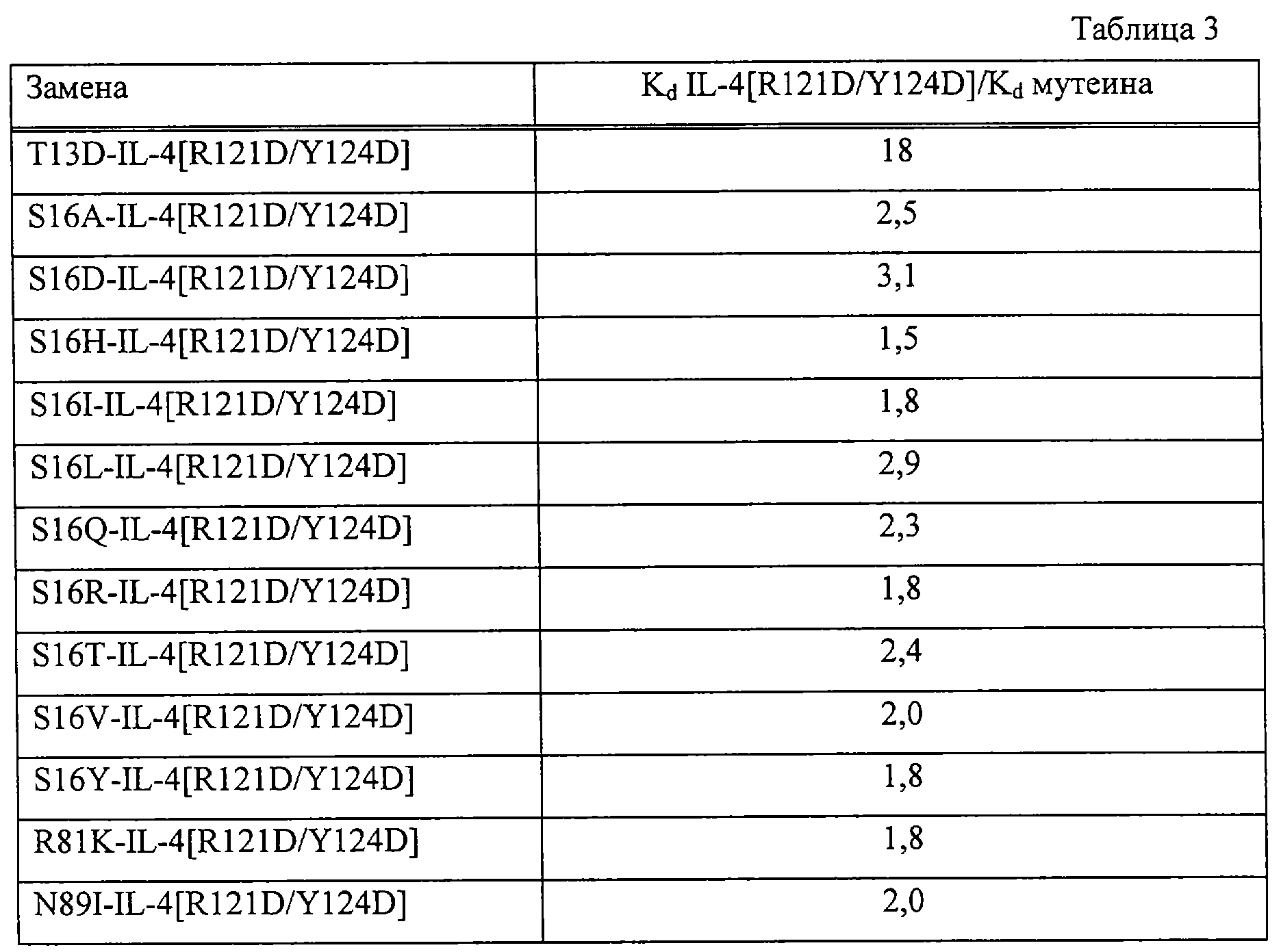
Все замены, которые приводят к увеличению сродства, показаны в Таблице 3. Отношение "Кd IL-4[R121D/Y124D]/Kd
мутеина" показывает относительное увеличение сродства, наблюдаемое в результате каждой замены.
Большинство замен оказывается либо вредным, либо не оказывает эффекта на сродство к IL-4Rα (данные не приведены). Однако несколько замен увеличивают сродство, наиболее заслуживающей внимания из которых является замена Thr-13 на Asp, которая приводит к удивительному 18-кратному увеличению сродства к IL-4Rα (Фиг. 2). Аминокислота Ser-16 оказывается уникальной в данном анализе, где большинство замен приводит к умеренному увеличению сродства. Сходные профили конкурентного связывания получают для данных других мутеинов в корреляции с их относительным сродством (данные не приведены). Значения сродства увеличиваются относительно белка-предшественника IL-4[R121D/Y124D] . Ожидается, что объединение данных замен в одном белке может привести к комбинаторному увеличению значений сродства; например, проведение замены [T13D/N89I] -IL-4[R121D/Y124D] может позволить получить мутеин с 36-кратным увеличением сродства по сравнению с IL-4[R121D/Y124D].
Замена остатков Thr-13 и Ser-16 позволяет получить наибольшее увеличение сродства, когда определяется подходящая замена. Это предполагает, что другие остатки, замещенные аланином, которые оказывали эффекты, аналогичные таковым мутеина Т13А либо S16A (6,4-кратное снижение и 2,5-кратное увеличение соответственно), также, вероятно, позволят получить варианты IL-4 с повышенным сродством при проведении надлежащей замены, применительно к данному ряду аланин-замещенных остатков таковые будут включать: Ilе-11, Lys-77, Gln-78, Lys-84 и Arg-85.
Что касается гормона роста, который широко исследовался, одинарные замены, которые приводят к увеличению сродства, оказывают эффект от 1,5- до 5-кратного порядка (Lowman НВ; Wells JA, "Affinity maturation of human growth hormone by monovalent phage display." J. Mol. Biol. 234(3), p. 564-78 (1993)). Однако недавно были идентифицированы замены, которые приводят к значительному увеличению либо активности (человеческий IL-3 (Olins PO et al. , Saturation mutagenesis of human interleukin-3, J. Biol. Chem. 270(40): 23754-60 (1995)) или сродства (человеческий цилиарный нейротрофный фактор (CNTF) (Saggio I et al., CNTF variants with increased biological potency and receptor selectivity define a functional site of receptor interaction, EMBO J. 14(13): 3045-54 (1995)). Что касается IL-3, одна мутация увеличивает биологическую активность in vitro ~26 раз; что касается CNTF, одна мутация увеличивает сродство ~ 32 раза. Что касается других цитокинов, описанных в литературе, большинство замен обычно не оказывает эффекта либо приводит к потере сродства/активности. Таким образом, абсолютный эффект любой данной замены на сродство и/или активность является непредсказуемым.
Пример 8. Эффект замены T13D на биологическую активность.
Мутеин-антагонист IL-4 IL-4[R121D/Y124D] является антагонистом IL-4 (Тоny HP, Shen BJ, Reusch P and Sebald W, "Design of Human Interleukin-4 Antagonists in Inhibiting Interleukin-4-dependent and Interleukin-13-dependent responses in T-cells and B-cells with high efficiency.", Eur. J. Biochem., 225(2), p. 659-665 (1994)) и применяется в данном исследовании в качестве контрольного пентида, благодаря своей неспособности к стимуляции активностей IL-4. Считается, что данный мутеин-антагонист является антагонистом, благодаря его способности связываться с IL-4Rα, но не задействовать γc таким образом, чтобы происходила передача сигнала, ингибируя, таким образом, связывание IL-4 с его собственным рецепторным комплексом. Таким образом, биологические эффекты IL-4[R121D/Y124D] (антагонизм по отношению к IL-4) выражаются в его взаимодействии с IL-4α, измеряемые сродством.
В целях доказательства того, что сродство рецептора коррелирует силу биологического эффекта, мутеин T13D-IL-4[R121D/Y124D] оценивают на предмет его способности ингибировать IL-4-индуцированную пролиферацию ФГА-бластов (Фиг. 3). Было установлено, что наблюдаемая ИК50 (концентрация, при которой наблюдается 50% ингибирование) относительно IL-4[R121D/Y124D] является приблизительно пропорциональной наблюдаемому относительному изменению сродства рецептора.
В заключение, несмотря на связывание с IL-4Rα с более высоким сродством, T13D-IL-4[R121D/Y124D] остается антагонистом IL-4. ИK50 T13D-IL-4[R121D/Y124D] по сравнению с IL-4[R121D/Y124D] является приблизительно пропорциональной относительным значениям Кd (измеренным в твердофазном анализе связывания), полученным для данных двух белков: Kd T13D-IL-4[R121D/Y124D] в ~18 раз меньше, чем Кd IL-4[R121D/Y124D] (0,28 нМ по сравнению с 5,0 нМ соответственно); ИК50 T13D-IL-4[R121D/Y124D] в ~5-10 раз меньше, чем ИК50 IL-4[R121D/Y124D] (2 нМ по сравнению с 13 нМ соответственно). Конкретные численные различия в относительном эффекте могут быть следствием конкретных условий каждого анализа: 1,5 ч инкубация в твердофазном анализе связывания при 20oС по сравнению с 48 ч инкубация в анализе пролиферации при 37oС. Способность других мутеинов, оцененных в данном исследовании, конкурировать с IL-4 в биологических анализах была пропорциональна их относительному Кd по сравнению с IL-4[R121D/Y124D] (данные не приведены). Данные результаты свидетельствуют, что связывание с IL-4Rα представляет собой явление, отделимое от активации рецептора IL-4; для данной активации требуется гетеродимеризация IL-4Rα и, по крайней мере, одной другой субъединицы (например, γc). Таким образом, модификация А- и С-спиралей IL-4 модулирует сродство IL-4 к IL-4Rα и делает это пропорционально способности указанного мутеина являться антагонистом IL-4 в биологическом смысле. Данное влияние на сродство, благодаря механизму взаимодействия IL-4 со своим рецептором, также будет преобразовываться в увеличение силы эффекта пептидов-агонистов, производных от IL-4.
Теория, развитая в данном изобретении, также может быть применена к другим цитокинам. Наиболее очевидной мишенью является IL-13 в силу того, что рецепторный комплекс IL-13 также задействует
IL-4Rα (Zurawski S.M. et al., The primary binding subunit of the human interleukin-4 receptor is also a component of the interleukin-13 receptor, J. Biol. Chem. 270:13869-78 (1995)). Таким
образом, мутирование А- и С-спиралей IL-13 с тем, чтобы они сильнее походили на таковые IL-4, приведет к увеличению сродства связывания с IL-4Rα.
Выравнивание последовательностей двух
интерлейкинов позволяет идентифицировать положения, которые будут являться аналогичными сайту мутации-мишени, например, Thr-13 в IL-4. Поверхности связывания двух интерлейкинов сравниваются в Таблице
4 ниже.
Наиболее важными остатками IL-4, опосредующими взаимодействие с IL-4Rα, идентифицированными путем сканирования с помощью аланина, Glu-9 и Arg-88, показаны жирным шрифтом, равно как и соответствующие остатки IL-13 на основании данного выравнивания последовательностей. Как указывалось ранее, IL-13 задействует в своем рецепторном комплексе цепь IL-4Rα (Zurawski S.M., supra). Таким образом, внесение изменений А- и С-спиралей IL-13 с тем, чтобы они сильнее походили на таковые IL-4, приведет к увеличению сродства связывания с IL-4Rα. В дополнение к этому, замена позиционно эквивалентных остатков IL-13 остатками, которые, как установлено, увеличивают сродство IL-4 к IL-4Rα (положения указаны двойным подчеркиванием для IL-4 и IL-13) также приведет к увеличению сродства IL-13 к своему рецепторному комплексу и, таким образом, к увеличенной силе эффекта.
Последовательности. В данной заявке содержатся следующие
биологические последовательности:
ПОСЛ. ИД. :1: аминокислотная последовательность, зрелый человеческий IL-4;
ПОСЛ. ИД. :2: нуклеотидная последовательность, праймеры ПЦР;
ПОСЛ. ИД. :3: нуклеотидная последовательность, праймеры ПЦР;
ПОСЛ. ИД. :4: нуклеотидная последовательность, праймеры ПЦР;
ПОСЛ. ИД. :5: нуклеотидная последовательность, праймеры ПЦР;
ПОСЛ. ИД. : 6: аминокислотная последовательность пептидной метки для стрептавидина;
ПОСЛ. ИД. :7: аминокислотная последовательность sIL-4Rα-STX;
ПОСЛ. ИД. :8:
аминокислотная последовательность, нуклеотидная последовательность T13D-IL-4 и
ПОСЛ. ИД. :9: аминокислотная последовательность, нуклеотидная последовательность Т13D-IL-4[R121D/Y124D].
Другие варианты осуществления изобретения будут очевидны специалисту в данной области. Концепция и экспериментальный подход, описанный здесь, будет применим к другим цитокинам, задействующим гетерологичные многомерные рецепторные системы, в частности IL-2 и родственные цитокины (например, IL-7, IL-9, IL-10, IL-13 и IL-15), альфа-интерферон и гамма-интерферон.
Реферат
Изобретение относится к области медицины. Сущностью изобретения является рекомбинантный мутеин человеческого IL-4, имеющий аминокислотную последовательность в соответствии с 1L-4 дикого типа, где мутеин содержит одну аминокислотную замену в связывающей поверхности либо альфа-спирали А, либо альфа-спирали С 1L-4 дикого типа, посредством которой мутеин связывается с рецептором IL-4Rα, по крайней мере, с большим сродством, нежели нативный IL-4. Замену предпочтительно выбирают из группы положений, состоящей из положений 13 и 16 в спирали А и положений 81 и 89 в спирали С. Наиболее предпочтительное осуществление представляет собой рекомбинатный мутеин человеческого IL-4, где замена в положении 13 представляет собой Thr на Asp. Также описаны фармацевтические композиции, аминокислотные и полинуклеотидные последовательности, кодирующие мутеины, трансформированные клеточные линии, антитела против мутеинов и способы лечения. Технический результат - расширение арсенала средств для поддержания и восстановления иммунной системы. 13 с. и 24 з.п.ф-лы, 4 табл., 6 ил.
Формула
25. Способ по п.23, где указанная пептидная метка содержит последовательность ДНК :6 или ее вырожденный вариант.

Комментарии