Процесс для производства полигидроксиалканоатов из прекурсоров, полученных с помощью анаэробной ферментации из ферментируемой биомассы - RU2682657C1
Код документа: RU2682657C1
Описание
Настоящее изобретение относится к процессу производства полигидроксиалканоатов из прекурсоров, полученных путем анаэробной ферментации из ферментируемой биомассы.
Здесь и далее для облегчения чтения полигидроксиалканоаты будут упоминаться по их аббревиатуре: ПГА. Это семейство включает несколько молекул в зависимости от количества атомов углерода.
ПГА представляют собой термопластичные полиэфиры, которые могут быть получены путем микробной ферментации сахаров растительного происхождения, в частности кукурузного крахмала или отходов растительного происхождения. Микроорганизмы вырабатывают ПГА, когда они попадают в условия дефицита определенных метаболитов, связанных с избытком углерода. Другими словами, микроорганизмы затем накапливают углерод, происходящий из сахаров, в форме гранул ПГА. ПГА используются, например, в качестве составного материала упаковки или в медицинской области в качестве шовного материала. Они заменяют полимеры на основе нефти.
Известны процессы ферментации с использованием чистых выбранных штаммов микроорганизмов, а также специфического субстрата для производства ПГА. Такое решение трудно использовать в промышленном масштабе для приемлемой себестоимости продукции.
Процесс, адаптированный к промышленному использованию, также известен из ЕР-А-2749650. Используемый субстрат получают из стоков и обогащают летучими жирными кислотами (ЛЖК), которые, как известно, являются предшественниками ПГА. Управляемым способом с использованием бактериального консорциума и чередования фаз роста биомассы и фаз дефицита стимулируется рост бактерий и производство ПГА. Однако такой способ предусматривает точный контроль условий ферментации и подходящую обработку для экстракции произведенных ПГА, что связано с относительно тяжелой установкой. Более того, такая экстракция не может выполняться непрерывно и не дает возможность производства всех видов ПГА. Другим недостатком этого процесса является его специфичность: с его помощью можно производить только микробные ПГА, то есть ПГА, продуцируемые микроорганизмами.
В частности, данное изобретение направлено на преодоление данных недостатков, предлагая способ получения ПГА, который позволяет производить различные типы ПГА, особенно непротеиногенные аминокислоты, легко и без ограничений, связанных с известными способами производства из предшествующего уровня техники.
С этой целью одним объектом изобретения является процесс получения полигидроксиалканоатов или ПГА из молекул летучих жирных кислот (ЛЖК), называемых прекурсорами, полученных анаэробной ферментацией из ферментируемой биомассы, отличающийся тем, что он включает в себя, по меньшей мере, следующие этапы:
- а) экстракцию молекул летучих жирных кислот (ЛЖК) без остановки ферментации с помощью экстракционного средства, выбранного из средств, которые, по меньшей мере, нерастворимы в ферментационной среде,
- b) сбор вне ферментационного реактора молекул летучих жирных кислот (ЛЖК) после их экстракции,
- с) синтез данной α-галогенированной кислоты путем галогенирования с использованием типа летучей жирной кислоты (ЛЖК), выбранной из летучих жирных кислот, собранных на этапе b), и определенной в соответствии с желаемым типом ПГА,
- d) синтез из этих молекул α-галогенированной кислоты данной α-гидроксикислоты путем взаимодействия с основанием,
- е) полимеризация с использованием полученной α-гидроксикислоты определенного полигидроксиалканоата (ПГА).
Таким образом, такой процесс дает возможность объединить фазу для непрерывного производства прекурсоров с помощью микроорганизмов с фазой синтеза, осуществляемой отдельно от ферментации, что позволяет легко управлять различными параметрами, и в то же время обеспечивая большую изменчивость в производстве полигидроксиалканоатов (ПГА).
Такой процесс позволяет непрерывно обеспечивать прекурсорами, то есть летучие жирные кислоты и в то же время сохранять производственную способность микроорганизмов, присутствующих в биореакторе.
В частности, этапы а) и b) экстракции и сбора дают возможность не только экстрагировать и непрерывно собирать молекулы летучих жирных кислот, образующихся в ферментационном реакторе, но и сохранять микроорганизмы, ответственные за их производство. В частности, экстракция и фактический сбор осуществляется в условиях, которые, по меньшей мере, являются нелетальными для всех микроорганизмов, то есть в биосовместимых условиях экстракции и сбора, поскольку экстракция сохраняет активность микроорганизмов, и сбор выполняется вне ферментационного реактора.
Таким образом, преодолеваются проблемы, связанные с накоплением метаболитов в ферментационном реакторе, например, подкисление ферментационной среды путем накопления образующихся летучих жирных кислот, которые вредны для микроорганизмов. Количество и активность микроорганизмов поддерживаются на более высоком уровне, близком к исходному уровню, в течение ферментационного цикла.
Предоставляя непрерывное и регулярное производство ЛЖК, предлагается легкий и быстро используемый источник разнообразных прекурсоров. В процессе, который является объектом изобретения, такое использование происходит на этапе с) с помощью химического синтеза и, следовательно, с легко регулируемыми и модифицируемыми условиями, что также обеспечивает большую изменчивость в типе синтезируемых молекул. В частности, на этапе с), в зависимости от ЛЖК, выбранного для осуществления галогенирования, получают данный тип α-галогенированной кислоты и, следовательно, после этого получают определенный тип α-гидроксикислот и, таким образом, получают данный тип α-ПГА. Изобретение также позволяет объединить несколько полученных таким образом α-гидроксикислот для производства гетерополимеров на конечном на этапе процесса.
Существует несколько типов ПГА, которые представляют интерес для промышленного, косметического, медицинского, пищевого или другого использования. Примерами, которые могут быть упомянуты, являются полигидроксибутират или ПГБ и поли(3-гидроксибутират-со-3-гидроксивалерат) или ПГБ-ГВ. Также среди типов ПГА можно указать производство полигликолевой кислоты или ПГК или полимолочной кислоты или ПМК, учитывая, что посредством известного процесса из предшествующего уровня техники невозможно напрямую получить ПМК, последняя должна быть полимеризована из продукции путем ферментации молочной кислоты.
Другими словами, посредством изобретения синтез нескольких типов ПГА, а именно гомо-, со- или гетерополимерных типов может осуществляться обычным и контролируемым образом из биоресурсного субстрата путем комбинирования биологического продуцирования с химическим производством.
Такой процесс позволяет использовать ферментируемую биомассу на этапе анаэробной ферментации. Термин «ферментируемая биомасса» в данном документе обозначает органический субстрат, который преимущественно не является пищевым, полученный из отходов, промежуточных продуктов и побочных продуктов, образованных из органического материала, то есть из биомассы, полученной от человеческой деятельности, будь то бытовая, промышленная, сельскохозяйственная, лесная, водная, агропромышленная, производная животноводства и т.п. Неограничивающие примеры органических субстратов, которые могут быть упомянуты, включают в себя навоз, органическую фракцию бытового мусора, отходы со скотобойни, остатки целлюлозы или лигноцеллюлозы, производные агропромышленности, такие как производные от переработки сахарного тростника (багасса), подсолнечника или сои.
Термин «анаэробная ферментация» означает ферментацию, выполняемую в анаэробных условиях эукариотическими или прокариотическими микроорганизмами, такими как бактерии, грибы, водоросли или дрожжи.
В соответствии с предпочтительными, но не обязательными аспектами данного изобретения такой процесс может включать одну или более из следующих характеристик:
- На этапе с) используемым галогенсодержащим соединением является дибром.
- На этапе с) используемое галогенсодержащее соединение не является дибромом.
- На этапе с) уксусный ангидрид используют в молярной процентной концентрации в области 12% относительно летучей жирной кислоты.
- На этапе с) используют ангидрид, соответствующий летучей жирной кислоте (ЛЖК), которая должна быть галогенирована.
- На этапе с) температура, при которой выполняется реакция бромирования, составляет от 20 до 40°С ниже точки кипения летучей жирной кислоты.
- На этапе d) используемое основание представляет собой гидроксид натрия.
- На этапе d) гидроксид натрия находится в эквимолярном количестве с α-галогенированной кислотой.
- На этапе d) реакцию α-галогенированной кислоты с гидроксидом натрия проводят при температуре от 20°С до 120°С, преимущественно от 50°С до 90°С.
- На этапе d) реакция α-галогенированной кислоты с гидроксидом натрия является оптимальной для температуры в области 50°С, если α-галогенированная кислота содержит по меньшей мере четыре атома углерода и для температуры в области 90°С, если α-галогенированная кислота содержит менее четырех атомов углерода.
Изобретение будет понято более четко, и другие его преимущества станут более ясными при чтении описания нескольких вариантов реализации изобретения, которое дается в виде неограничивающего примера.
Различные этапы процесса теперь описаны со ссылкой на несколько вариантов реализации изобретения, при этом понятно, что этапы, которые широко известны, не детализированы.
Во-первых, используемый субстрат преимущественно не обрабатывается, то есть он не подвергается какой-либо физико-химической или ферментативной предварительной обработке. Этот субстрат преимущественно состоит из ферментируемой биомассы. В качестве дополнительных неограничивающих примеров можно упомянуть сельскохозяйственные или растительные отходы (солома, багасса, отходы, образующиеся при дистилляции кукурузы, трава, древесина, скошенная трава), бумажные отходы (картон, бумага), агропродовольственные отходы, отходы со скотобойни, органическая часть бытовых отходов, отходы животноводства (навоз, навозная жижа, помет), водоросли, отходы аквакультуры, отходы лесной промышленности или ферментируемые побочные продукты косметической промышленности. Некоторые субстраты содержат органические молекулы, такие как органические кислоты, которые мало влияют или вообще не влияют на процесс ферментации. С другой стороны, эти молекулы могут быть найдены в ферментационной среде и могут участвовать, например, в получении определенных конечных органических молекул.
В качестве напоминания и известным способом субстрат вводят в ферментационный реактор, который широко известен и имеет размеры для желаемого производства, независимо от того, будет ли это производство осуществляться в лабораторном масштабе для проведения испытаний или в промышленном масштабе в случае производства. Другими словами, ферментационный реактор или биореактор имеет объем от нескольких литров до нескольких сотен кубических метров в зависимости от потребности.
Микроорганизмы преимущественно вводят в ферментационный реактор в количестве, достаточном для начала ферментации. Микроорганизмы преимущественно инокулируют в форме консорциума. Термин «консорциум» обозначает состав или смесь эукариотических и прокариотических микроорганизмов, будь то бактерии, дрожжи, грибы или водоросли. Эти различные микроорганизмы происходят главным образом из природных экосистем, преимущественно, но не исключительно, из анаэробных экосистем, неограничивающие примеры которых включают анаэробную зону водных сред, таких как бескислородная зона определенных озер, почв, болот, шлама очистных сооружений, рубца жвачных животных или кишечника термитов. Следует иметь в виду, что качественное и количественное распределение различных типов и видов микроорганизмов в консорциуме точно не известно и, в основном, может варьироваться в широких пределах. Оказывается, что это качественное и количественное разнообразие как ни странно обеспечивает устойчивость и адаптивность микроорганизмов, которые позволяют обеспечить оптимальное использование субстратов, независимо от состава этих субстратов и при изменяющихся условиях ферментации.
Кроме того, в связи с тем, что субстрат используется в немодифицированной форме, то есть его не стерилизуют, или, в более общем случае, не освобождают от содержащихся в нем микроорганизмов до его введения в биореактор, оказывается, что относящиеся к субстрату микроорганизмы фактически включены в консорциум или, по меньшей мере, объединены с ним в биореакторе.
Более того, ферментация происходит в анаэробных условиях, точнее, когда окислительно-восстановительный потенциал составляет менее -300 мВ, преимущественно от -550 мВ до -400 мВ и когда рН составляет менее 8, предпочтительно от 4 до 7. Ферментация преимущественно ограничивается выработкой "прекурсоров" ферментационных метаболитов, а именно летучих жирных кислот или ЛЖК, содержащих от двух до восьми атомов углерода, предпочтительно от двух до шести. Таким образом индуцируется реакция, которая подобна феномену ацидоза, встречающемуся у жвачных животных, но при которой продукция метана близка к нулю. Как правило, метан является одним из последних ферментационных метаболитов, полученных в результате анаэробной ферментации микроорганизмами, происходящими из природных экосистем.
На первом этапе ферментация приводит к образованию летучих жирных кислот, в основном содержащих от двух до четырех атомов углерода, например, уксусной кислоты, пропионовой кислоты и масляной кислоты. В меньшем количестве также получают длинноцепочечные летучие жирные кислоты, имеющие больше четырех атомов углерода, такие как валериановая кислота, капроновая кислота, гептановая кислота или октановая кислота. Продолжая ферментацию и/или увеличивая количество микроорганизмов в биореакторе, если необходимо с помощью выбранных микроорганизмов, можно стимулировать выработку ЛЖК с длинной углеродной цепью, имеющих более четырех атомов углерода.
Другими словами летучие жирные кислоты, образующиеся в количестве во время ферментации, по существу, представляют собой летучие жирные кислоты, имеющие от двух до шести атомов углерода.
Ферментация во всех случаях проводится для обеспечения производства ЛЖК в жидкой фазе. Как правило время ферментации составляет от 1 до 7 дней, предпочтительно от 2 до 4 дней. Концентрация метаболитов, полученных в ферментационной среде по завершению этого периода, является изменчивой, но для летучих жирных кислот, как правило, составляет от 10 до 20 г/л в зависимости от летучих жирных кислот, при этом понимается, что при определенных условиях она может составлять более 35 г/л, например, в области 50 г/л. В конце этапа ферментации рН ферментационной среды является кислым и обычно составляет от 4 до 6 из-за присутствия летучих жирных кислот в ферментационной среде.
Когда выработка ЛЖК достигает определенного количества, обычно в фазе постоянного режима ферментации, инициируется этап а) экстракции молекул. Предпочтительно, но не обязательно, это определенное количество ЛЖК соответствует замедлению роста микроорганизмов, таким образом, находясь в области порога ингибирования для микроорганизмов.
Экстракционное средство выбирают из жидкого или твердого экстракционного средства, которое, по меньшей мере, нерастворимо в ферментационной среде. В случае если экстракционное средство является жидким, таким образом оно является растворителем, предпочтительно плотность растворителя является меньшей, чем плотность ферментационной среды.
Точнее, экстракция осуществляется с помощью твердого или жидкого экстракционного средства, рабочие условия которого позволяют сохранить активность и/или рост микроорганизмов в условиях ферментации, преобладающих в биореакторе, и которые определены для осуществления ферментации. Молекулы ЛЖК предпочтительно экстрагируют с помощью молекулярных семейств и затем преимущественно разделяют индивидуально с помощью широко известных методов.
Когда молекулы, такие как летучие жирные кислоты, экстрагируются из ферментационной среды, фактически снижается создаваемая ими кислотность ферментационной среды. Таким образом, ферментация и, следовательно, выработка метаболитов продолжается в условиях, сходных с начальными условиями, причем ферментационная среда остается умеренно кислой.
Предпочтительно экстракцию проводят непрерывно или, по меньшей мере, последовательно, например, с экстракцией каждые 12 часов. Другими словами, можно продолжать ферментацию во время экстракции полученных метаболитов либо постепенно по мере их выработки, либо регулярно.
Жидкость-жидкостная экстракция органическими растворителями в качестве экстракционного средства представляет собой предпочтительный, но не исключительный способ экстракции.
В одном варианте реализации изобретения экстракция не выполняется в отдельном элементе реактора ферментации, но непосредственно в указанном реакторе. Растворитель вводят, например, с помощью устройства типа барботера, расположенного на дне реактора. Как вариант, экстракционный элемент соединяют с реактором, обеспечивая связь с ферментационной средой.
По завершении экстракции выполняют этап сбора b). На этом этапе ЛЖК собирают из органической фазы с помощью широко известных методов, таких как дистилляция или испарение.
Сбор осуществляется либо смеси ЛЖК, либо по типам ЛЖК. Очевидно, что выбор ЛЖК или смеси ЛЖК определяется типом конечных(ой) желательных(ой) молекул(ы). Для этого адаптируются условия сбора, в основном, параметры испарения или дистилляции.
После выполнения этого этапа сбора, выполняется следующий этап с). Это преимущественно, но не исключительно, выполняется после этапа сбора. Как вариант, он выполняется в другое время и/или в другом месте, причем выработанные ЛЖК транспортируются и/или хранятся в соответствии с широко известными методами.
Данный этап галогенирования заключается во взаимодействии галогена с ЛЖК с образованием α-галогенированной кислоты, которая является реакционноспособным типом молекулы и, таким образом, особенно предпочтительна для получения других молекул. Такая широко известная реакция осуществляется путем добавления брома, который является предпочтительным, при этом следует понимать, что могут быть использованы другие галогены, а именно хлор, фтор или йод или галогенированные молекулы, такие как тригалогениды фосфора, галогеновые кислоты или ацилгалогениды.
Был выбран дибром, поскольку бромированная α-галогенированная кислота является более реакционноспособной, чем соответствующая хлорированная α-галогенированная кислота, связь углерод-бром легче разрушается, чем связь углерод-хлор. Кроме того, дибром легче обрабатывать из-за его жидкой формы.
Для осуществления синтеза α-бромзамещенной кислоты был использован путь с использованием ангидрида, в данном случае уксусного ангидрида и пиридина. Понятно, что другие пути синтеза, например, с полифосфорной кислотой «или тригалогенидами фосфора являются широко известными. Проводились испытания с полифосфорной кислотой, но результаты были неопределенными, в частности, из-за высокой вязкости этого соединения, что затрудняет его обработку.
Испытания хлорирования также проводились Заявителем для синтеза α-хлорзамещенных кислот, например, с трихлоризоциануровой кислотой. Полученные результаты уступают с точки зрения выхода и простоты реализации результатам, полученным с дибромом.
Предпочтительным является синтетический путь с использованием ангидрида, соответствующего летучей жирной кислоте, которую желательно галогенировать, и дает возможность получить α-галогенированную кислоту, в данном случае α-бромзамещенную кислоту данного типа. Использование уксусного ангидрида с другими ЛЖК и/или со смесью ЛЖК с количеством атомов углерода от двух до шести позволяет получить смесь α-галогенированных кислот с количеством атомов углерода от двух до шести.
Испытания с использованием уксусной кислоты (ЛЖК, содержащей два атома углерода), пропионовой кислоты (ЛЖК, содержащей три атома углерода), масляной кислоты (ЛЖК, содержащей четыре атома углерода), капроновой кислоты (ЛЖК, содержащей шесть атомов углерода), а также смеси ЛЖК с числом атомов углерода от двух до шести проводились путем изменения количества уксусного ангидрида, а также других параметров, таких как температура.
Во время различных испытаний соблюдался протокол. Он включает в себя, в предварительной фазе, нагревание до рефлюкса исходной смеси ЛЖК, уксусного ангидрида и пиридина. Затем, во время фактического бромирования, дибром медленно добавляется в течение нескольких часов при температуре ниже точки кипения смеси и после добавления диброма смесь снова доводится до рефлюкса перед охлаждением. В конце реакции, предпочтительно, добавляется вода для разрушения присутствующего ангидрида. Затем α-бромзамещенную кислоту экстрагируют различными способами, в зависимости от кислоты. К таким способам относится, например, дистилляция или разделяющая экстракция.
Начальная температура доведения смеси до рефлюкса составляет от 120°С для ЛЖК, содержащих два атома углерода, и до 200°С для ЛЖК, содержащих шесть атомов углерода. Температура бромирования колеблется от 80°С до 180°С, в зависимости от того, содержат ли ЛЖК от двух до шести атомов углерода. Время реакции бромирования и, следовательно, фактическое время добавления диброма варьируется от около одного, часа для ЛЖК, содержащих шесть атомов углерода, до около четырех часов для ЛЖК, содержащих два атома углерода.
Проводились испытания бромирования летучих жирных кислот, содержащих два, три, четыре или шесть атомов углерода, а также испытание на смеси летучих жирных кислот:
уксусная кислота (С2): 0,53 моль
пропионовая кислота (С3): 0,53 моль
масляная кислота (С4): 0,53 моль
капроновая кислота (С6): 0,24 моль
Смесь ЛЖК от С2 до С6: 0,54 моль.
Количество добавляемого диброма составляет 0,21 моль или 0,11 моль, таким образом, что летучая жирная кислота находится в избытке. Предпочтительно, Заявитель обнаружил, что молярное соотношение 2:1 в пользу ЛЖК является оптимальным.
Количество добавляемого ангидрида для каждой кислоты составляет 0,06 моля для одного испытания и 0,03 моля для другого испытания. Смесь ЛЖК включает уксусную кислоту (С2), пропионовую кислоту (С3), масляную кислоту (С4), валериановую кислоту (С5) и капроновую кислоту (С6).
Температуры рефлюкса, в ходе предварительной фазы, изменяются в зависимости от ЛЖК: 120°С для уксусной кислоты; 120°С и 140°С для испытаний с пропионовой кислотой; 150°С и 160°С для масляной кислоты; 200°С для капроновой кислоты и 180°С для смеси.
Температуры бромирования для различных испытаний с каждой кислотой составляют от 10°С до 50°С и преимущественно от 20°С до 40°С ниже температуры рефлюкса и, следовательно, точки кипения летучей жирной кислоты.
Выходы и чистота α-бромзамещенных кислот, полученных по завершению различных испытаний, сопоставлены ниже в Таблице 1. Для простоты ЛЖК обозначены числом атомов углерода.


Анализ и расчеты выхода проводились с помощью широко известных аналитических методов, а именно с помощью ЯМР (ядерного магнитного резонанса) и ВЭЖХ (высокоэффективной жидкостной хроматографии). Выходы определялись относительно количества потребляемой ЛЖК.
Заявитель обнаружил, что реакция, проиллюстрированная путем обесцвечивания реакционной смеси после добавления диброма, протекает быстрее в случае большего количества ангидрида, в то же время чистота мало влияет на скорость протекания реакции. Тем не менее, это подходит для того, чтобы температура двух этапов, предварительного этапа и этапа бромирования, была оптимальной. Для этого Заявитель отметил, что необходимой является температура бромирования немного ниже точки кипения летучей жирной кислоты, не будучи слишком далекой от этой температуры.
Различные испытания позволили определить, что температура бромирования от около 10°С до 50°С ниже точки кипения летучей жирной кислоты, предпочтительно на 20°С ниже, позволила, при прочих равных условиях, получить оптимальный выход, как правило, от 60% до 100% при времени реакции от 1 часа до 4 часов.
Что касается роли уксусного ангидрида, то в свете результатов, приведенных в таблице, создается впечатление, что молярная процентная концентрация ангидрида по отношению к ЛЖК должна находиться в области 12% для оптимальной реакции бромирования, при этом следует понимать, что процент от 5% до 20% является приемлемым.
Используя полученные α-бромзамещенные кислоты или, точнее, используя данную α-бромзамещенную кислоту, затем на этапе d) проводится синтез данной α-гидроксилированной кислоты, также называемой α-гидроксикислотой. Для этого добавляется основание. Предпочтительно, но не исключительно, основание представляет собой гидроксид натрия.
Испытания проводились Заявителем путем замещения гидроксида натрия (NaOH) на α-бромзамещенные кислоты, а именно на бромуксусную кислоту, α-бромпропионовую кислоту, α-броммасляную кислоту, на α-бромкапроновую кислоту и на смесь α-бромзамещенных кислот, содержащих от двух до шести атомов углерода. Такая замена позволяет производить α-гидроксикислоты, содержащие углеродную цепь из, соответственно, двух, трех, четырех, пяти или шести атомов углерода, то есть гликолевую кислоту, молочную кислоту, α-гидроксимасляную кислоту, α-гидроксивалериановую кислоту или α-гидроксикапроновую кислоту.
После полимеризации эти α-гидроксикислоты относятся к числу наиболее широко используемых в производстве косметики или упаковки для пищевых продуктов. Нетрудно понять, что способ, являющийся предметом изобретения, позволяет производить другие типы кислот, которые позволяют полимеризовать другие типы ПГА. В качестве примера может быть упомянута α-гидроксидеценовая кислота.
Для различных испытаний протокол состоял в том, чтобы довести до рефлюкса эквимолярную смесь гидроксида натрия и α-бромзамещенных кислот в течение одного-двух часов. Температура нагрева находится в диапазоне от 80°С до 120°С. Образцы, взятые через равные промежутки времени, демонстрировали, что выход составляет от 60% до 100% и преимущественно от 80% до 100% для кислот, содержащих, по меньшей мере, три атома углерода.
Также видно, что оптимальный выход достигается при постепенном повышении температуры для соединений, содержащих более четырех атомов углерода. Таким образом, Заявитель обнаружил, что выход является оптимальным, когда температура остается ниже температуры, при которой и выше которой начинается деградация α-гидроксикислоты, причем эта температура фактически является меньшей, чем точка кипения α-бромзамещенной кислоты.
В частности, Заявитель неожиданно обнаружил, что температура, при которой достигается оптимальный выход, составляет от 20°С до 120°С, преимущественно от 50°С до 90°С.
В частности, Заявитель непредвиденно обнаружил, что температура, при которой достигается оптимальный выход, находится в области 50°С для α-бромзамещенных кислот, содержащих, по меньшей мере, четыре атома углерода, и в области 90°С для α-бромзамещенных кислот, содержащих менее четырех атомов углерода, при этом следует понимать, что для С2 и С3 α-гидроксикислот температура выше 100°С вызывает деградацию соединения.
В частности, как только достигается оптимальный выход, увеличение времени реакции дает лишь минимальную прибавку, например для α-бромзамещенной кислоты, содержащей четыре атома углерода, два часа времени реакции вместо одного часа приводят к увеличению выхода на 4%.
В Таблице 2 ниже обобщаются некоторые из проведенных испытаний.
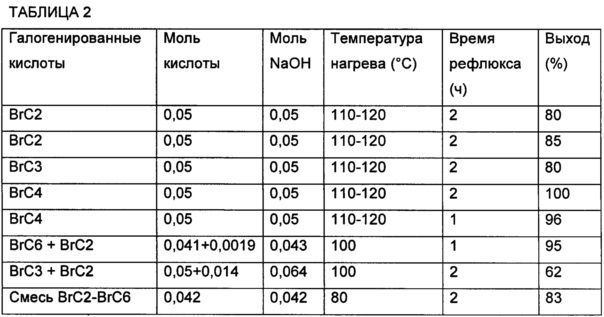
Анализ и расчеты выхода проводились с помощью упомянутых аналитических методов ЯМР и ВЭЖХ. Выходы определялись относительно исходного количества галогенированной кислоты.
Конечный этап процесса заключается в полимеризации соответствующего полигидроксиалканоата или ПГА, начиная с полученной α-гидроксикислоты. В качестве примера можно упомянуть полимолочную кислоту или ПМК, которая используется в упаковке для пищевых продуктов и полигликолевую кислоту или ПГК, используемую в медицинской области в качестве шовного материала. ПМК получают из молочной кислоты, полученной из α-бромпропионовой кислоты. ПМК получают из гликолевой кислоты, полученной из бромуксусной кислоты.
Такая полимеризация, которая является широко известной, предпочтительно выполняется тремя способами: путем дециклизации (полимеризации с раскрытием цикла), путем твердофазной полимеризации (полимеризации в твердом состоянии) или путем прямой поликонденсации. За этой полимеризацией следует восстановление ПГА, которое является широко известным.
Реферат
Изобретение относится к способу производства полигидроксиалканоатов. Процесс получения полигидроксиалканоатов (ПГА) осуществляют из молекул летучих жирных кислот (ЛЖК), называемых прекурсорами, которые получены анаэробной ферментацией из ферментируемой биомассы. Способ характеризуется тем, что он включает в себя, по меньшей мере, следующие этапы: а) экстракцию молекул летучих жирных кислот (ЛЖК) без остановки ферментации с помощью экстракционного средства, выбранного из средств, которые, по меньшей мере, нерастворимы в ферментационной среде, b) сбор вне ферментационного реактора молекул летучих жирных кислот (ЛЖК) после их экстракции, с) синтез данной α-галогенированной кислоты путем галогенирования с использованием типа летучей жирной кислоты (ЛЖК), выбранной из летучих жирных кислот, собранных на этапе b), и определенной в соответствии с желаемым типом ПГА, d) синтез из этих молекул α-галогенированной кислоты данной α-гидроксикислоты путем взаимодействия с основанием, е) полимеризация с использованием полученной α-гидроксикислоты определенного полигидроксиалканоата (ПГА). Технический результат – повышение технологичности способа за счет непрерывного производства ЛЖК и сохранения активности микроорганизмов, также технологичность обеспечивается объединением всех стадий до получения полимеров, при этом обеспечиваются хорошие выходы промежуточных продуктов. 9 з.п. ф-лы, 2 табл.

Комментарии