Детские каши, содержащие нереплицирующиеся пробиотические микроорганизмы - RU2549934C2
Код документа: RU2549934C2
Чертежи


Описание
Настоящее изобретение относится к области детских каш. В частности, настоящее изобретение относится к области изделий из дробленых зерновых для младенцев, которые могут быть применены для усиления иммунной системы младенца и/или могут быть использованы для лечения или профилактики воспалительных расстройств. Например, эти преимущества могут быть обеспечены пробиотическими микроорганизмами. Воплощение настоящего изобретения относится к детской каше, содержащей нереплицирующиеся пробиотические микроорганизмы, например, биоактивные подвергнутые тепловой обработке пробиотические микроорганизмы.
Новорожденные младенцы обычно находятся на грудном вскармливании или их кормят с помощью жидких детских смесей, которые напоминают содержание материнского молока настолько сильно, насколько это возможно. Грудное вскармливание и/или введение питательной смеси для младенцев, как правило, продолжается в течение первого года жизни младенца.
Однако, как правило, в возрасте 4-6 месяцев развивается потребность и готовность к другой пище. Признаки этого заключаются в том, что младенец начинает сидеть и контролировать движения головы. Он обретает способность продвигать пищу изо рта к горлу, так чтобы координация языком позволяла младенцу глотать с ложки.
Введение твердой пищи важно для младенца с целью построения позитивного отношения к пище. Это является первой стадией роста счастливого ребенка и развития долгосрочных привычек здорового питания.
На этом этапе рекомендуется, чтобы младенец начал потреблять детские каши.
Детские каши будут помогать младенцу экспериментировать со вкусом, текстурой и питанием. Однако пищеварительный тракт младенцев все еще развивается и ему придется иметь дело с новой задачей: твердая пища.
Пробиотики как часть флоры кишечника помогают желудку гораздо легче переносить пищу, а также могут, например, активизировать иммунную систему. В этом отношении, новым инновационным продуктом является, например, каша «Nestle Baby Cereal», содержащая культуры Bifidobacterium lactis. Эти культуры поддерживают здоровую флору пищеварительного тракта и помогают поддерживать здоровый рост и развитие.
Как правило, предполагается, что пробиотики безопасны для младенцев. Однако в особых обстоятельствах, целесообразно может быть не использовать пробиотики для младенцев без назначения врача, например, если младенец страдает нарушением иммунной системы.
Вследствие этого существует потребность в данной области в разработке детской каши, которая обеспечивает пользу пробиотиков и которая может потребляться без каких-либо проблем младенцами с нарушением иммунной системы.
Авторы изобретения взялись за решение этой потребности.
Следовательно, целью настоящего изобретения является предложение детской каши, которая легко переваривается младенцами, дает возможность эксперимента со вкусом, текстурой и питанием и обеспечивает пользу от пробиотиков, будучи при этом простой в получении в промышленном масштабе и в идеале не теряет активности при более продолжительном сроке хранения или при повышенных температурах.
Авторы изобретения неожиданно обнаружили, что они могут решить эту задачу с помощью объекта независимого пункта формулы изобретения. Зависимые пункты дополнительно развивают идею настоящего изобретения.
Авторы настоящего изобретения предложили детские каши, содержащие нереплицирующиеся пробиотические микроорганизмы.
Авторы неожиданно обнаружили, что, например, по показателю усиливающего иммунитет воздействия и/или по показателю противовоспалительного воздействия нереплицирующиеся пробиотические организмы могут быть еще более эффективными, чем реплицирующиеся пробиотические микроорганизмы.
Это удивительно, поскольку пробиотики часто определяются как «живые микроорганизмы, которые при введении в адекватных количествах приносят пользу здоровью организма-хозяина» (Руководство ПСО/ВОЗ). В подавляющем большинстве опубликованных работ имеют дело с живыми пробиотиками. Кроме того, в нескольких исследованиях показано, что благоприятные воздействия, привносятся нереплицирующимися бактериями и в большинстве из них указано, что инактивация пробиотиков, например, тепловой обработкой, приводит к потере ими предусмотренной пользы для здоровья (Rachmilewitz, D., et al., 2004, Gastroenterology 126:520-528; Castagliuolo, et al., 2005, FEMS Immunol. Med. Microbiol. 43:197-204; Gill, H. S. and K. J. Rutherford, 2001, Br. J.Nutr. 86:285-289; Kaila, M, et al., 1995, Arch. Dis. Child 72:51-53). Некоторые исследования, однако, демонстрируют, что инактивированные пробиотики могут сохранять некоторые воздействия на здоровье (Rachmilewitz, D., et al., 2004, Gastroenterology 126:520-528; Gill, H. S. and K. J. Rutherford, 2001, Br. J.Nutr. 86:285-289), но ясно, что живые пробиотики рассматривались в данной области до настоящего времени как более эффективные.
Поэтому авторы настоящего изобретения предлагают детскую кашу, содержащую нереплицирующиеся пробиотические микроорганизмы. Эти нереплицирующиеся пробиотические микроорганизмы все еще являются биоактивными.
Одно воплощение настоящего изобретения представляет собой детскую кашу, содержащую, по меньшей мере, 0,48 г/100 кДж источника белка, по большей части 1,1 г/100 кДж источника липидов, источника углеводов и нереплицирующиеся пробиотические микроорганизмы.
Детские каши известны в данной области. Детские каши представляют собой композиции, содержащие зерновые культуры, для введения младенцам. Они обычно вводятся с использованием ложки и могут предлагаться младенцам, например, в виде сухой каши. Готовые к употреблению детские каши также находятся в рамках настоящего изобретения. Кодекс Алиментариус (кодекс качества пищи) представляет руководство, согласно которому должны быть составлены ингредиенты детской каши.
Термин «младенец» означает ребенка в возрасте не более чем 12 месяцев.
Как правило, энергетическая ценность, а также количество и тип белков, углеводов и липидов, присутствующих в детской каше, должны быть тщательно отрегулированы соответственно потребностям младенца и зависят от степени развития младенца и его возраста.
Хорошо известны требования относительно питания при изменениях младенца, связанных с развитием и возрастом младенца, и композиция детской каши идеально отражает это изменение.
Следовательно, детская каша согласно изобретению, которую следует вводить младенцам в возрасте 4-6 месяцев, может иметь энергетическую ценность 220-240 кДж/15 г, 0,8-1,2 г/15 г источника белков, 0,1-0,3 г источника жиров и 12,3-12,7 г/15 г источника углеводов. Такая детская каша может содержать, например, рисовую муку, маисовый мальто декстрин, витамин С и железо.
Детская каша согласно настоящему изобретению, которую следует вводить младенцам в возрасте 6-12 месяцев, может иметь энергетическую ценность 220-240 кДж/15 г, 1,5-1,9 г/15 г источника белков, 0,2-0,4 г источника жиров и 11,1-11,5 г/15 г источника углеводов. Такая детская каша может содержать, например, пшеничную муку, манную крупу из пшеницы, железо, витамин С, ниацин, витамин В6, тиамин и маисовый мальтодекстрин.
Детские каши могут быть приготовлены из одной или нескольких перемолотых зерновых культур, которые могут составлять, по меньшей мере, 25 масс. % конечной смеси в пересчете на сухую массу.
Детские каши по настоящему изобретению предпочтительно получают из одного злака, типа рисовой каши или пшеничной каши - так как композиции из одного злака с меньшей вероятностью вызывают аллергические реакции.
Детские каши по настоящему изобретению могут дополнительно содержать пребиотики. Пребиотики могут поддерживать рост пробиотиков, до того как они станут нереплицирующимися. Под «пребиотиком» понимают неперевариваемые пищевые вещества, которые стимулируют рост полезных микроорганизмов и/или пробиотиков в кишечнике. Они не разрушаются в желудке и/или в верхней части кишечника или не адсорбируются в ЖК-тракте принимающей их персоны, но они ферментируются желудочно-кишечной микробиотой и/или пробиотиками. Пребиотики, например, определены в работе Glenn R. Gibson and Marcel B. Roberfroid, Dietary Modulation of the Human Colonic Microbiota: Introducing the Concept of Prebiotics, J. Nutr. 1995 125: 1401-1412.
Пребиотики, которые могут быть использованы в соответствии с настоящим изобретением ничем особенным не ограничены и включают все пищевые вещества, которые способствуют росту пробиотиков и микроорганизмов в кишечнике, приносящих пользу здоровью. Предпочтительно, они могут быть выбраны из группы, состоящей из олигосахаридов, необязательно содержащей фруктозу, галактозу, маннозу; пищевые волокна, в частности растворимые волокна, соевые волокна; инулин; или их смеси. Предпочтительными пребиотиками являются фруктоолигосахариды (ФОС), галактоолигосахариды (ГОС), изомальтоолигосахариды (ИМО), ксилоолигосахариды (КОС), арабино-ксилоолоигосахариды (АКОС), маннаноолигосахариды (МОС), олигосахариды сои, гликозилсахароза (ГС), лактосахароза (ЛС), лактулоза (ЛА), палатинозоолигосахариды (ПАО), мальтоолигосахариды, камеди и/или их гидролизаты, пектины и/или их гидролизаты. Например, детская каша может содержать олигофруктозу, инулин или их комбинацию.
Как правило, перед употреблением детские каши следует смешивать с водой. Например, 15 г детской каши согласно настоящему изобретению могут быть смешаны с 90 мл воды.
Детская каша согласно настоящему изобретению может содержать нереплицирующиеся пробиотические микроорганизмы в любом эффективном количестве, например, в количестве, соответствующем около 106-1012 КОЕ/г сухой массы.
«Нереплицирующиеся» пробиотические микроорганизмы включают пробиотические бактерии, которые были подвергнуты тепловой обработке. Они включают микроорганизмы, которые являются инактивированными, мертвыми, нежизнеспособными и/или которые представлены в виде фрагментов, таких как ДНК, метаболиты, цитоплазматические соединения и/или материалы клеточной стенки.
«Нереплицирующийся» означает, что невозможно обнаружить жизнеспособные клетки и/или колониеобразующие единицы классическими способами рассева на чашках. Такие классические способы рассева на чашках сведены вместе в книге о микробиологии:
James Monroe Jay, Martin J. Loessner, David A. Golden. 2005. Modem food microbiology. 7th edition, Springer Science, New York, N. Y. 790 p. Как правило, отсутствие жизнеспособных клеток может быть продемонстрировано следующим образом: на чашках с агаром отсутствует видимая колония или в жидкой среде для роста не увеличивается мутность после инокуляции различными концентрациями бактериальных препаратов («нереплицирующиеся» образцы) и инкубации в соответствующих условиях (аэробной и/или анаэробной атмосфере в течение, по меньшей мере, 24 часов).
Пробиотики определены для цели настоящего изобретения как «микробные клеточные препараты или компоненты микробных клеток с полезным воздействием на здоровье или самочувствие организма-хозяина» (Salminen S, Ouwehand A. Benno Y. et al "Probiotics: how should they be defined" Trends Food Sci. Technol. 1999:10 107-10).
Возможность применения нереплицирующихся пробиотических организмов дает некоторые преимущества. У младенцев с тяжелыми нарушениями иммунитета использование живых пробиотиков может быть ограничено в исключительных случаях благодаря потенциальному риску развития бактериемии. Нереплицирующиеся пробиотики могут быть применены без каких-либо проблем.
Кроме того, предоставление нереплицирующихся пробиотических микроорганизмов позволяет горячее восстановление с сохранением пользы для здоровья младенца.
Композиции по настоящему изобретению содержат нереплицирующиеся пробиотические микроорганизмы в количестве, достаточном, по меньшей мере, для частичного получения пользы для здоровья. Количество, достаточное для осуществления этого определяется как «терапевтически эффективная доза». Количества, эффективные для данной цели, будут зависеть от множества факторов известных специалистам в данной области, таких как масса и общее состояние здоровья младенца, и воздействие пищевой матрицы.
В профилактических применениях, композиции по изобретению вводят потребителю, восприимчивому к расстройству или в ином случае имеющему риск развития расстройства, в количестве, которое является достаточным, по меньшей мере, для частичного уменьшения риска развития данного расстройства. Такое количество определяется как «профилактически эффективная доза». Опять же, точное количество зависит от множества факторов, таких как состояние здоровья и масса младенца, и от воздействия пищевой матрицы.
Специалист в данной области будет способен скорректировать терапевтически эффективную дозу и/или профилактически эффективную дозу соответствующим образом.
Как правило, композиция по настоящему изобретению содержит нереплицирующиеся пробиотические микроорганизмы в терапевтически эффективной дозе и/или в профилактически эффективной дозе.
Как правило, терапевтически эффективная доза и/или профилактически эффективная доза находится в интервале около 0,005 мг-1000 мг нереплицирующихся пробиотических микроорганизмов в ежедневной дозе.
В численном выражении, нереплицирующиеся микроорганизмы после «высокотемпературной кратковременной» обработки могут присутствовать в композиции в количестве, соответствующем от 104 до 1012 эквивалентных КОЕ/г сухого композиции.
Очевидно, нереплицирующиеся микроорганизмы не образуют колоний, соответственно, данный термин понимается как количество нереплицирующихся микроорганизмов, которые получено из 104-1012 КОЕ/г реплицирующихся бактерий. Данный термин включает микроорганизмы, которые являются инактивированными, нежизнеспособными или мертвыми или присутствуют в виде фрагментов, таких как ДНК или клеточная стенка или питоплазматические соединения. Другими словами, количество микроорганизмов, которые содержит состав, выражается в виде колониеобразующей способности (КОЕ) того количества микроорганизмов, как если бы все микроорганизмы были живыми независимо от того, являются ли они, по сути, нереплицирующимися, то есть инактивированными или мертвыми, фрагментированными или являются смесью любых из представленных состояний.
Предпочтительно, если нереплицирующиеся микроорганизмы присутствуют в количественном эквиваленте от 104 до 109 КОЕ/г сухой композиции, а еще более предпочтительно в количественном эквиваленте в диапазоне от 105 до 109 КОЕ/г сухой композиции.
Пробиотики могут быть сделаны нереплицирующимися любым способом, известным в данной области.
Доступными в настоящее время технологиями приведения пробиотических штаммов в нереплицирующееся состояние являются термообработка, γ-облучение, УФ-обработка и применение химических агентов (формалина, парафармальдегида).
Было бы предпочтительно применить метод для приведения пробиотиков в нереплицирующееся состояние, который является относительно простьм в применении в производственной обстановке пищевой промышленности.
В настоящее время на рынке большинство содержащих пробиотики продуктов инактивируют тепловой обработкой в процессе их производства. Следовательно, было бы удобно, если бы было можно подвергать пробиотики тепловой обработке или вместе с полученным продуктом, или, по меньшей мере, аналогичным образом, с сохранением при этом или улучшением полезных свойств пробиотиков или даже с приобретением нового полезного для потребителя свойства.
Однако в литературе, как правило, инактивация пробиотических микроорганизмов тепловыми обработками связана, по меньшей мере, с частичной потерей пробиотической активности.
Авторы в настоящее время с удивлением обнаружили, что приведение пробиотических микроорганизмов в нереплицирующееся состояние, например, тепловой обработкой, не приводит к потере пробиотических благоприятных воздействий, но, наоборот, может усилить существующие благоприятные воздействия и даже создать новые благоприятные воздействия.
Поэтому одно воплощение настоящего изобретения представляет собой детскую кашу, где нереплицирующиеся пробиотические микроорганизмы были приведены в нереплицирующееся состояние тепловой обработкой.
Такая термообработка может быть проведена, по меньшей мере, при 71,5°С в течение, по меньшей мере, 1 секунды.
Могут быть применены длительные тепловые обработки или кратковременные тепловые обработки.
В настоящее время в промышленных масштабах, как правило, предпочтительными являются кратковременные тепловые обработки, такие как УВТ-подобные тепловые обработки. Данный тип тепловой обработки снижает бактериальную обсемененность и снижает время обработки, тем самым уменьшая порчу питательных веществ.
Авторы впервые демонстрируют факт того, что пробиотические микроорганизмы, подвергнутые тепловой обработке при высоких температурах в течение коротких периодов времени демонстрируют противовоспалительные иммунные профили независимо от их начальных свойств. Конкретно, либо развивается новый противовоспалительный профиль, либо существующий противовоспалительный профиль улучшается с помощью этой тепловой обработки.
Таким образом, стало возможным получение нереплицирующихся пробиотических микроорганизмов противовоспалительным иммунным профилем применением специфических параметров тепловой обработки, которые соответствуют типичной промышленно применяемой тепловой обработке, даже если живые эквиваленты не являются противовоспалительными штаммами.
Поэтому, например, такая тепловая обработка может представлять собой высокотемпературную обработку при около 71,5-150°С в течение около 1-120 секунд. Высокотемпературная обработка может являться высокотемпературной, кратковременной (ВТКВ) обработкой или ультравысокотемпературной (УВТ) обработкой.
Пробиотические микроорганизмы могут быть подвергнуты высокотемпературной обработке при около 71,5-150°С в течение короткого периода времени около 1-120 секунд.
Более предпочтительно, если микроорганизмы могут быть подвергнуты высокотемпературной обработке при около 90-140°С, например, 90-120°С в течение короткого периода времени около 1-30 секунд.
Данная высокотемпературная обработка приводит микроорганизмы, по меньшей мере, частично в нереплицирующееся состояние.
Высокотемпературная обработка может быть проведена при нормальной атмосферном давлении, но также может быть проведена при высоком давлении. Типичные диапазоны давления составляют от 1 до 50 бар, предпочтительно от 1 до 10 бар, еще более предпочтительно от 2 до 5 бар.
Очевидно, что предпочтительно, если пробиотики являются инактивированными тепловой обработкой в среде, которая является, либо жидкой, либо твердой, при применении тепла. Идеальное применяемое давление будет, следовательно, зависеть от природы композиции, в которой предоставлены микроорганизмы, и от используемой температуры.
Высокотемпературная обработка может быть проведена в температурном диапазоне около 71,5-150°С, предпочтительно около 90-120°С, еще более предпочтительно около 120-140°С.
Высокотемпературная обработка может быть проведена в течение короткого периода времени около 1-120 секунд, предпочтительно, около 1-30 секунд, еще более предпочтительно около 5-15 секунд.
Данные временные интервалы обозначают время, в течение которого Пробиотические микроорганизмы подвергают воздействию данной температуры. Следует отметить, что микроорганизмы предоставляются в зависимости от природы и количества композиции, и в зависимости от структуры используемого нагревательного прибора время нагревания может отличаться.
Однако, как правило, композицию по настоящему изобретению и/или микроорганизмы обрабатывают с помощью высокотемпературной кратковременной (ВТКВ) обработки, мгновенной пастеризации или с помощью ультравысокотемпературной (УВТ) обработки.
УВТ-обработка является ультравысокотемпературным технологическим процессом или ультравысокотемпературной обработкой (оба сокращенно УВТ), включающие, по меньшей мере, частичную стерилизацию композиции нагреванием в течение короткого периода времени, около 1-10 секунд, при температуре превышающей 135°С (275°F), которая является температурой, необходимой для уничтожения бактериальных спор в молоке. Например, технологическая обработка молока данным способом при использовании температуры, превышающей 135°С, позволяет снизить бактериальную обсемененность в течение необходимого периода удержания (до 2-5 сек), что позволяет проведение проточной операции.
Существует два основных типа систем УВТ: прямая и непрямая системы. В прямой системе продукты обрабатывают инъекцией пара, или нагнетанием пара, тогда как в непрямой системе продукты нагревают с помощью плоского теплообменника, трубчатого теплообменника или скребкового теплообменника. Комбинация систем УВТ может быть применена на любой стадии или множестве стадий в процессе приготовления продукта.
ВТКР-обработка определяется следующим образом (высокотемпературная/ кратковременная): Способ пастеризации для достижения 5 кратного логарифмического уменьшения, уничтожающий 99,9999% от числа жизнеспособных организмов в молоке. Способ считается достаточным для разрушения почти всех дрожжей, плесени и распространенных бактерий, вызывающих порчу, а также гарантирует достаточное разрушение распространенных патогенных термоустойчивых организмов. При ВТКВ-технологии молоко нагревают до 71,7°С (161°F) в течение 15-20 секунд.
Мгновенная пастеризация является способом тепловой пастеризации скоропортящихся напитков, таких как фруктовые и овощные соки, пиво и молочные продукты. Она осуществляется до заполнения в контейнеры для того, чтобы уничтожить микроорганизмы, вызывающие порчу, сделать продукты безопаснее и увеличить срок их хранения. Жидкость движется в контролируемом непрерывном потоке, в то же время подвергаясь нагреву до температур от 71,5°С (160°F) до 74°С (165°F) в течение около 15-30 секунд.
Для цели настоящего изобретения термин «кратковременная высокотемпературная обработка» должен включать высокотемпературные кратковременные (ВТКВ) обработки, УВТ-обработки, и, например, мгновенную пастеризацию.
Так как такая термообработка обеспечивает получение нереплицирующихся пробиотиков с улучшенным противовоспалительным профилем, то детская каша по настоящему изобретению может быть предназначена для применения при профилактике или при лечении воспалительных расстройств.
Воспалительные расстройства, которые могут быть подвергнуты лечению или профилактике с помощью композиции, полученной с применением настоящего изобретения, ничем конкретно не ограничены. Например, они могут быть выбраны из группы, состоящей из острых воспалений, таких как сепсис, ожоги, и хронических воспалений, таких как воспалительное заболевание кишечника, например, болезнь Крона, язвенный колит, научит; некротический энтероколит; кожных воспалений, таких как воспаление, индуцированное УФ или химическими соединениями, экзема, раздраженная кожа; из синдрома раздраженной толстой кишки; воспаления глаз; аллергии, астмы; и их комбинаций.
При применении продолжительных тепловых обработок для приведения пробиотических микроорганизмов в нереплицируемое состояние, такую тепловую обработку можно проводить в температурном диапазоне около 70-150°С в течение от около 3 минут до 2 часов, предпочтительно в диапазоне 80-140°С в течение 5-40 минут.
Хотя в предшествующем уровне техники известно, что бактерии, приведенные в нереплицирующееся состояние с помощью продолжительной тепловой обработки, как правило, менее эффективны, чем живые клетки по показателю их пробиотических свойств, авторам настоящего изобретения удалось продемонстрировать, что подвергнутые термообработке пробиотики являются лучшими при стимуляции иммунной системы по сравнению с их живыми эквивалентами.
Настоящее изобретение также относится к детской каше, содержащей пробиотические микроорганизмы, которые стали нереплицирующимися с помощью тепловой обработки, предпочтительно, с помощью высокотемпературной обработки, по меньшей мере, при 70°С в течение, по меньшей мере, 3 минут.
Иммуноусиливающие воздействия нереплицирующихся пробиотиков были подтверждены иммунопрофилированием in vitro, В использованной in vitro модели применено профилирование цитокинов из человеческих мононуклеарных клеток периферической крови (англ. Peripheral Blood Mononuclear Cell, PBMC) и данная модель популярна в данной области как стандартная модель для проверки иммуномодулирующих соединений (Schultz et al., 2003, Journal of Dairy Research 70, 165-173; Taylor et al., 2006, Clinical and Experimental Allergy, 36, 1227-1235; Kekkonen et al, 2008, World Journal of Gastroenterology, 14, 1192-1203).
In vitro анализ на РВМС использовался несколькими авторами/исследовательскими командами, например, для классификации пробиотиков в соответствии с их иммунным профилем, т.е. в соответствии с их противо- или провоспалительными характеристиками (Kekkonen et al., 2008, World Journal of Gastroenterology, 14, 1192-1203). Например, было продемонстрировано, что этот анализ дает возможность прогноза противовоспалительного воздействия пробиотических кандидатов в мышиных моделях кишечного колита (Foligne, В., et al., 2007, World J.Gastroenterol. 13:236-243). Более того, данный анализ регулярно используется для считывания данных при клинических испытаниях и было показано, что он дает результаты, которые согласуются с клиническими исходами (Schultz et al., 2003, Journal of Dairy Research 70, 165-173; Taylor et al., 2006, Clinical and Experimental Allergy, 36,1227-1235).
Аллергические заболевания неуклонно растут на протяжении последних десятилетий и в настоящее время они рассматриваются ВОЗ как эпидемия. В общем виде аллергию рассматривают как результат дисбаланса между Th1- и Th2-ответами иммунной системы, который приводит к сильному сдвигу по направлению к продупированию Th2-медиаторов. Следовательно, аллергия может быть смягчена, отрицательно регулирована или предотвращена путем восстановления соответствующего баланса между Th1 и Th2 плечами иммунной системы. Это подразумевает необходимость уменьшения Th2-ответов или увеличения, по меньшей мере, временно Th1-ответов. Последние, являясь предполагаемой характерной чертой вторичного иммунного ответа, часто сопровождаются, например, более высокими уровнями IFNγ, TNF-α и IL-12 (Kekkonen et al., 2008, World Journal of Gastroenterology, 14, 1192-1203; Viljanen M. et al., 2005, Allergy, 60,494-500).
Детская каша по настоящему изобретению, следовательно, дает возможность лечения или профилактики расстройств, которые связаны с ослабленной иммунной защитой.
Следовательно, расстройства, связанные с ослабленной иммунной защитой, которые могут быть подвергнуты лечению или профилактике с помощью композиции, полученной с применением настоящего изобретения, ничем конкретно не ограничены.
Например, они могут быть выбраны из группы, состоящей из инфекций, в частности, бактериальных, вирусных, грибковых и/или паразитарных инфекций; фагоцитарного дефицита; иммунодепрессии от легкой до тяжелой стадии, как например, иммунодепрессии, индуцированной стрессом или иммунодепрессивными лекарственными средствами, химиотерапией или лучевой терапией; естественных состояний менее иммуиокомпетентных иммунных систем, таких как иммунные системы новорожденных или пожилых людей; аллергий; и их комбинаций.
Детская каша, описанная в настоящем изобретении, также дает возможность усиления ответа младенца на вакцины, конкретно на пероральные вакцины.
Любое количество нереплицирующихся микроорганизмов будет эффективным. Однако, как правило, предпочтительно, если, по меньшей мере, 90%, предпочтительно, по меньшей мере, 95%, более предпочтительно, по меньшей мере, 98%, наиболее предпочтительно, по меньшей мере, 99%, идеально, по меньшей мере, 99,9%, в идеале все пробиотики являются нереплицирующимися.
В одном воплощении настоящего изобретения, все микроорганизмы являются нереплицирующимися.
Следовательно, в детской каше по настоящему изобретению, по меньшей мере, 90%, предпочтительно, по меньшей мере, 95%, более предпочтительно, по меньшей мере, 98%, наиболее предпочтительно, по меньшей мере, 99%, в идеале, по меньшей мере, 99,9%, наиболее идеально все пробиотики являются нереплицирующимися.
Все пробиотические микроорганизмы можно применять для цели настоящего изобретения.
Например, пробиотические микроорганизмы могут быть выбраны из группы, состоящей из бифидобактерий, лактобацилл, пропионовых бактерий или их комбинаций, например, Bifidobacterium longum, Bifidobacterium lactis, Bifidobacterium ш, Bifldobacterium breve, Bifidobacterium infantis, Bifidobacterium adolescentis, Lactobacillus acidophilus, Lactobacillus casei, Lactobacillus paracasei, Lactobacillus salivarius, Lactobacillus reuteri, Lactobacillus rhamnosus, Lactobacillus johnsonii, Lactobacillus plantarum, Lactobacillus fermentum, Lactococcus lactis. Streptococcus thermophilus, Lactococcus lactis, Lactococcus diacetylactis, Lactococcus cremoris, Lactobacillus bulgaricus, Lactobacillus helveticus, Lactobacillus delbrueckii, Escherichia coli и/или их смесей.
Детская каша согласно настоящему изобретению может, например, содержать нереплицирующиеся пробиотические микроорганизмы, выбранные из группы, состоящей из Bifidobacterium longum NCC 3001, Bifidobacterium longum NCC 2705, Bifidobacterium breve NCC 2950, Bifidobacterium lactis NCC 2818, Lactobacillus johnsonii LaI, Lactobacillus paracasei NCC 2461, Lactobacillus rhamnosus NCC 4007, Lactobacillus reuteri DSM17938, Laclobacillus reuteri ATCC55730, Streptococcus thermophilus NCC 2019, Streptococcus thermophilus NCC 2059, Lactobacillus easel NCC 4006, Lactobacillus acidophilus NCC 3009, Lactobacillus casei ACA-DC 6002 (NCC 1825), Escherichia coli Nissle, Lactobacillus bulgaricus NCC 15, Lactococcus lactis NCC 228, или из их комбинаций.
Все такие штаммы являются или депонированными согласно Будапештскому договору и/или являются коммерчески доступными.
Штаммы, депонированные согласно Будапештскому договору, представлены ниже:
Специалист в данной области поймет, что можно свободно комбинировать все признаки описанного в данном документе настоящего изобретения, не отходя от раскрытого объема притязаний изобретения.
Дополнительные преимущества и особенности настоящего изобретения очевидны из приведенных ниже Примеров и Фигур.
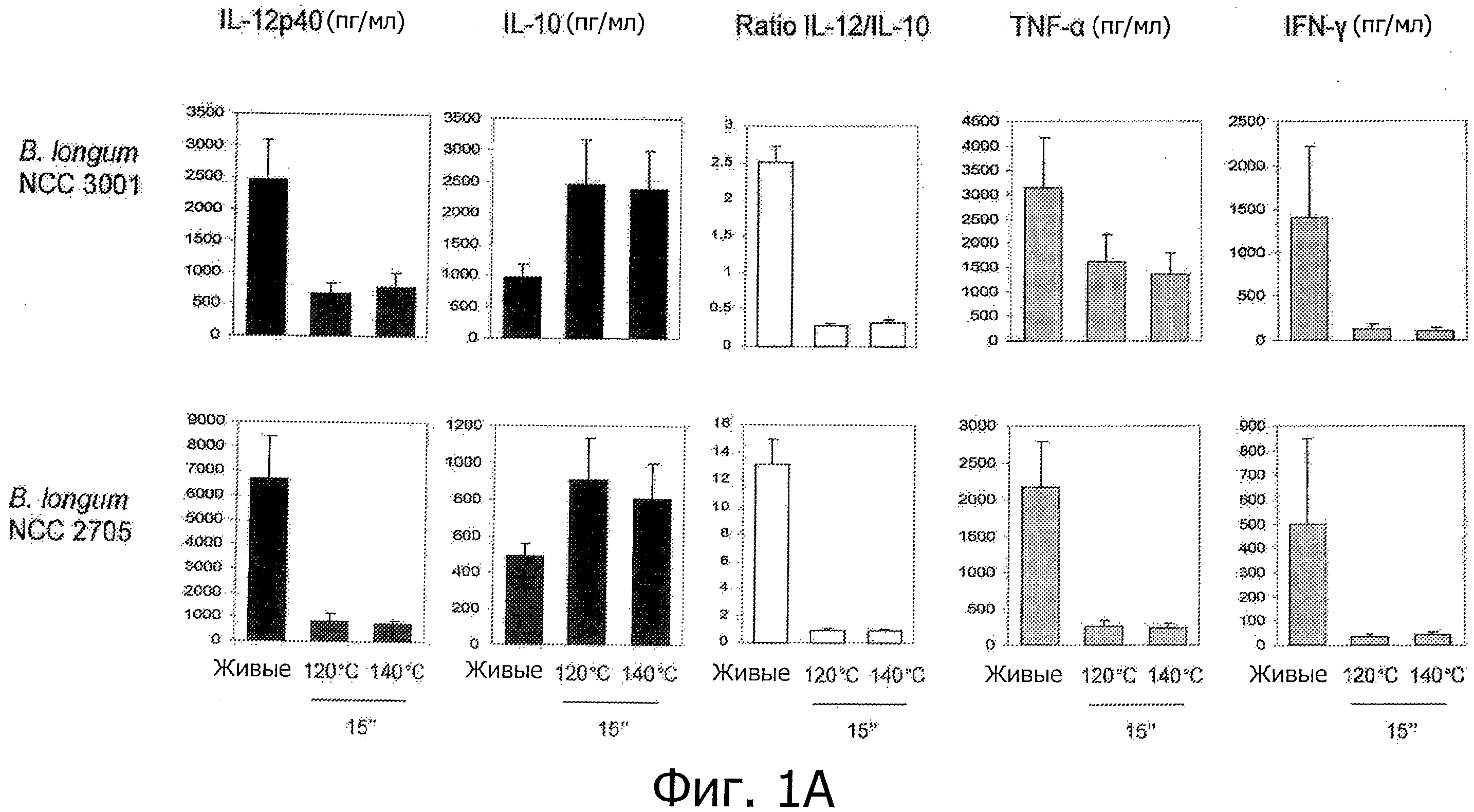
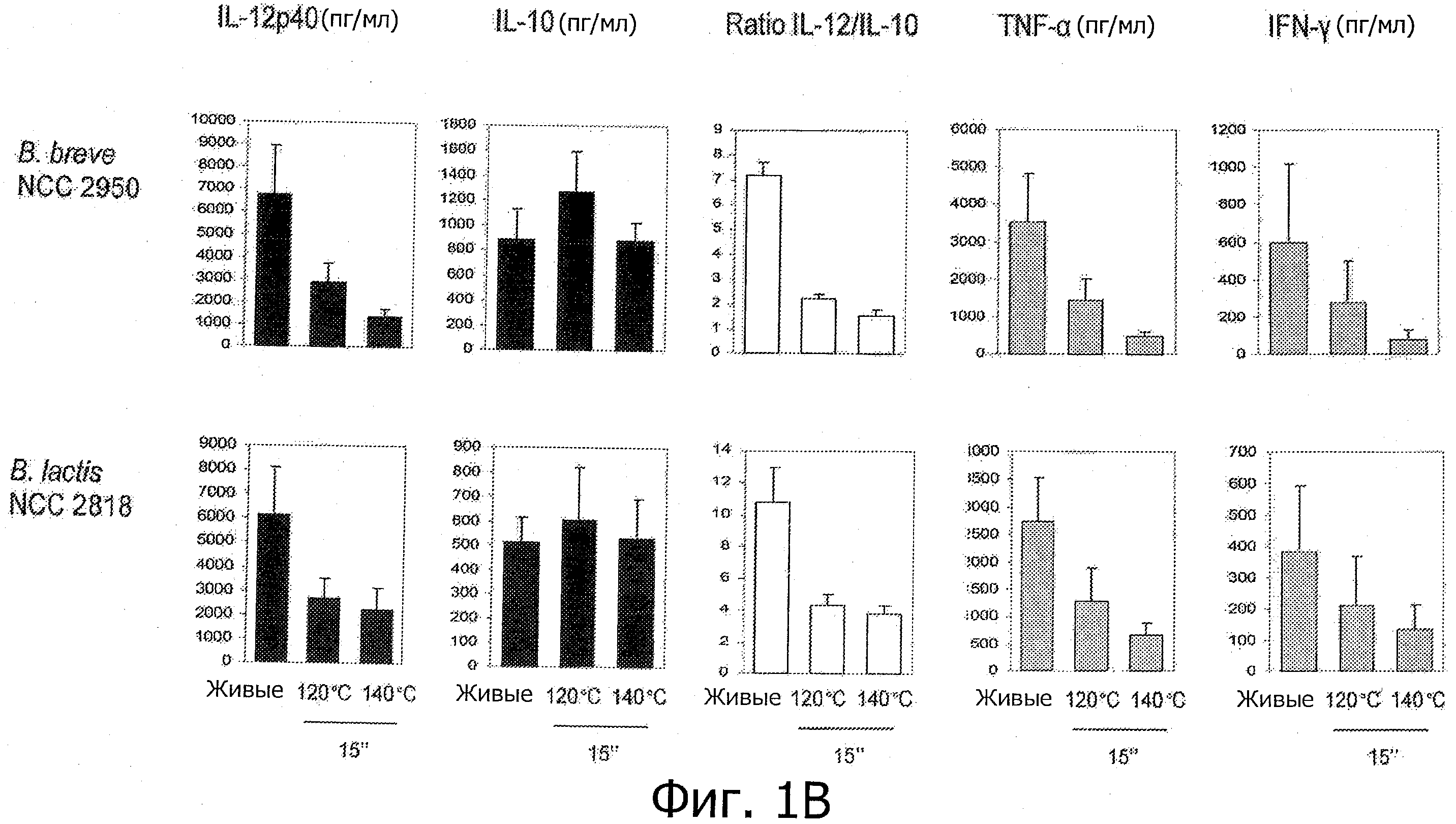
Фигуры 1А и В демонстрируют усиление противовоспалительных иммунных профилей пробиотиков, подвергнутых «высокотемпературной кратковременной обработке».
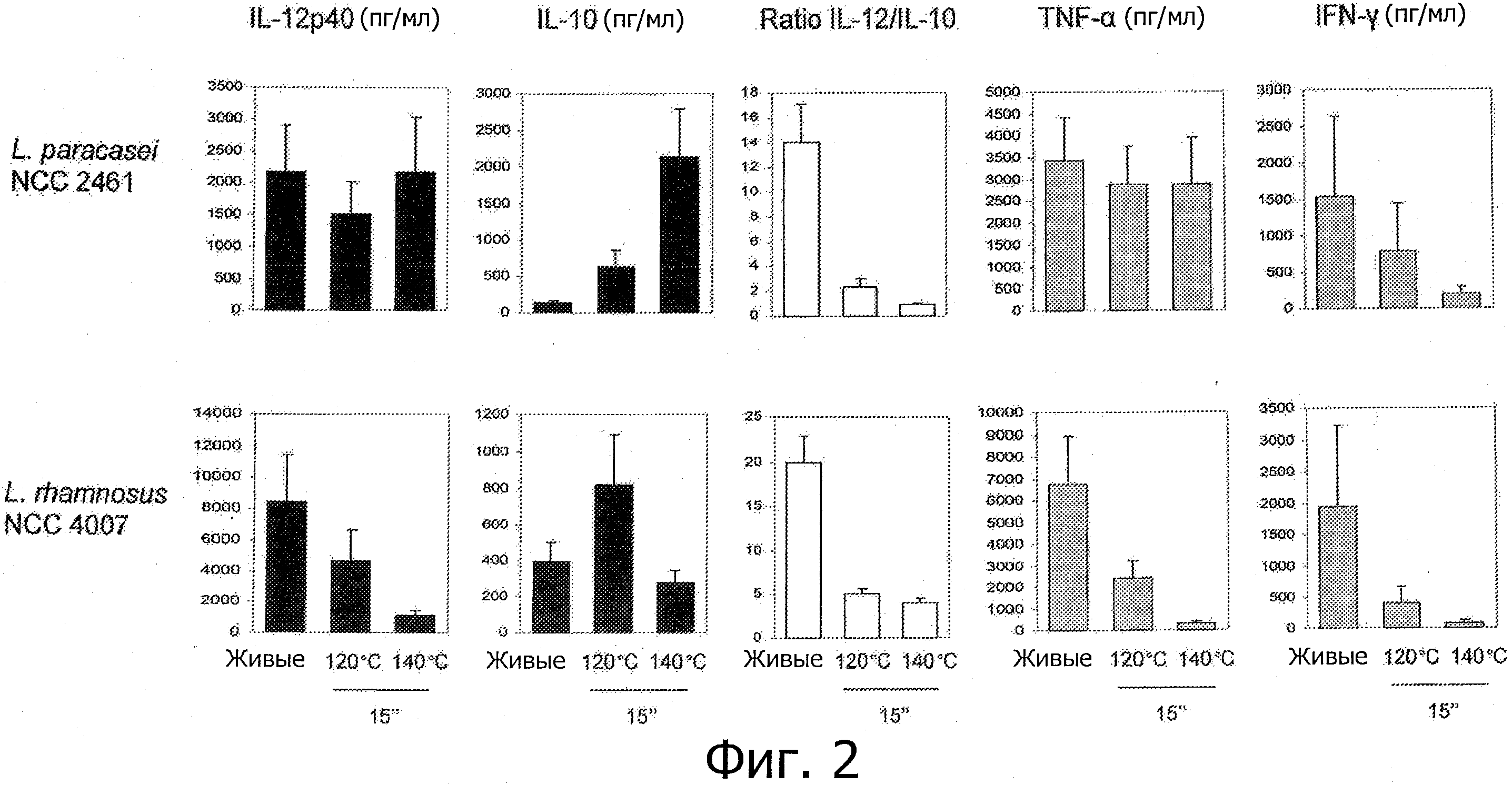
Фигура 2 демонстрирует непротивовоспалительные пробиотические штаммы, которые становятся противовоспалительными, т.е. которые демонстрируют ярко выраженные противовоспалительные иммунные профили in vitro после «высокотемпературной кратковременной обработки».
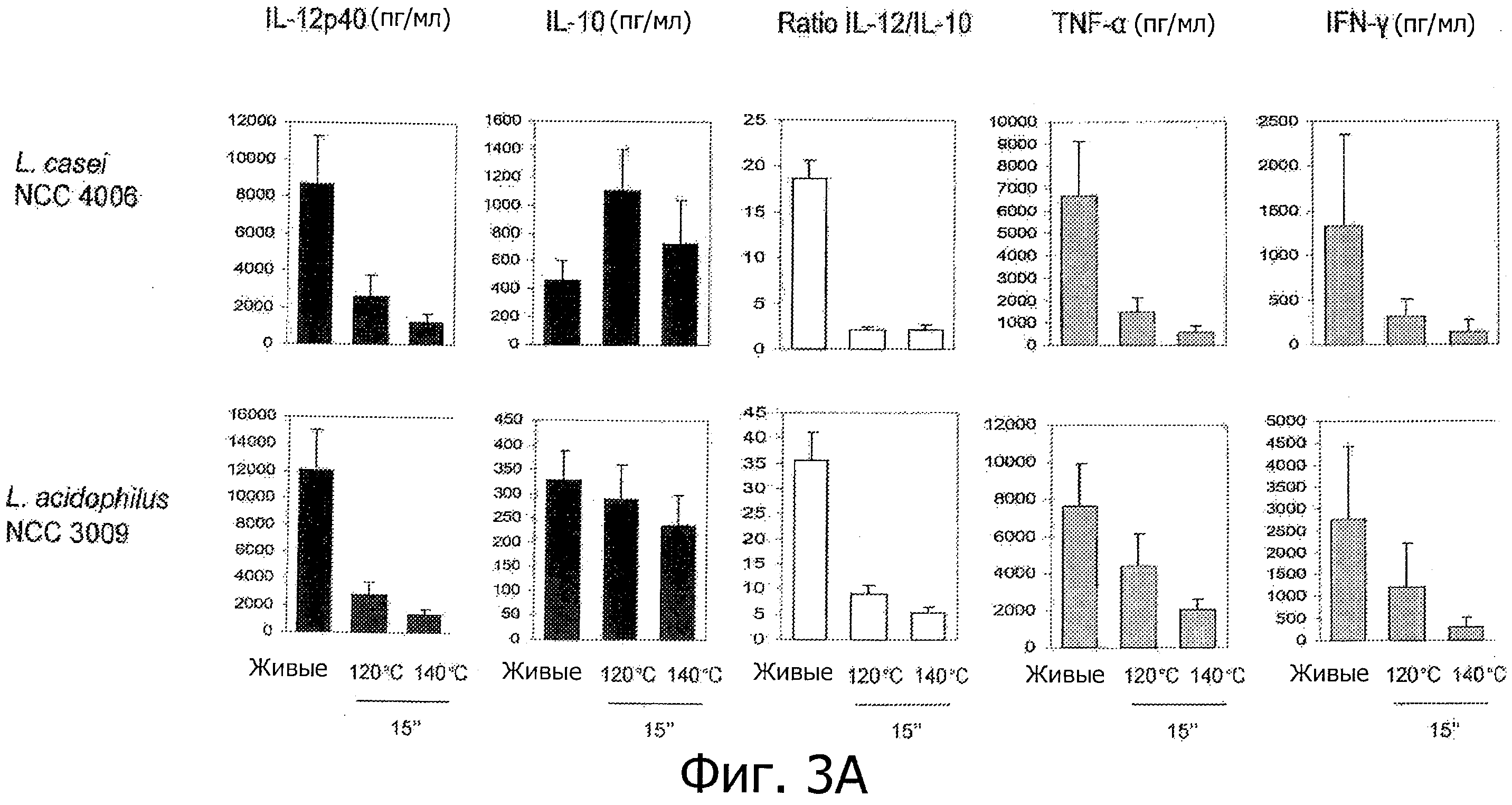
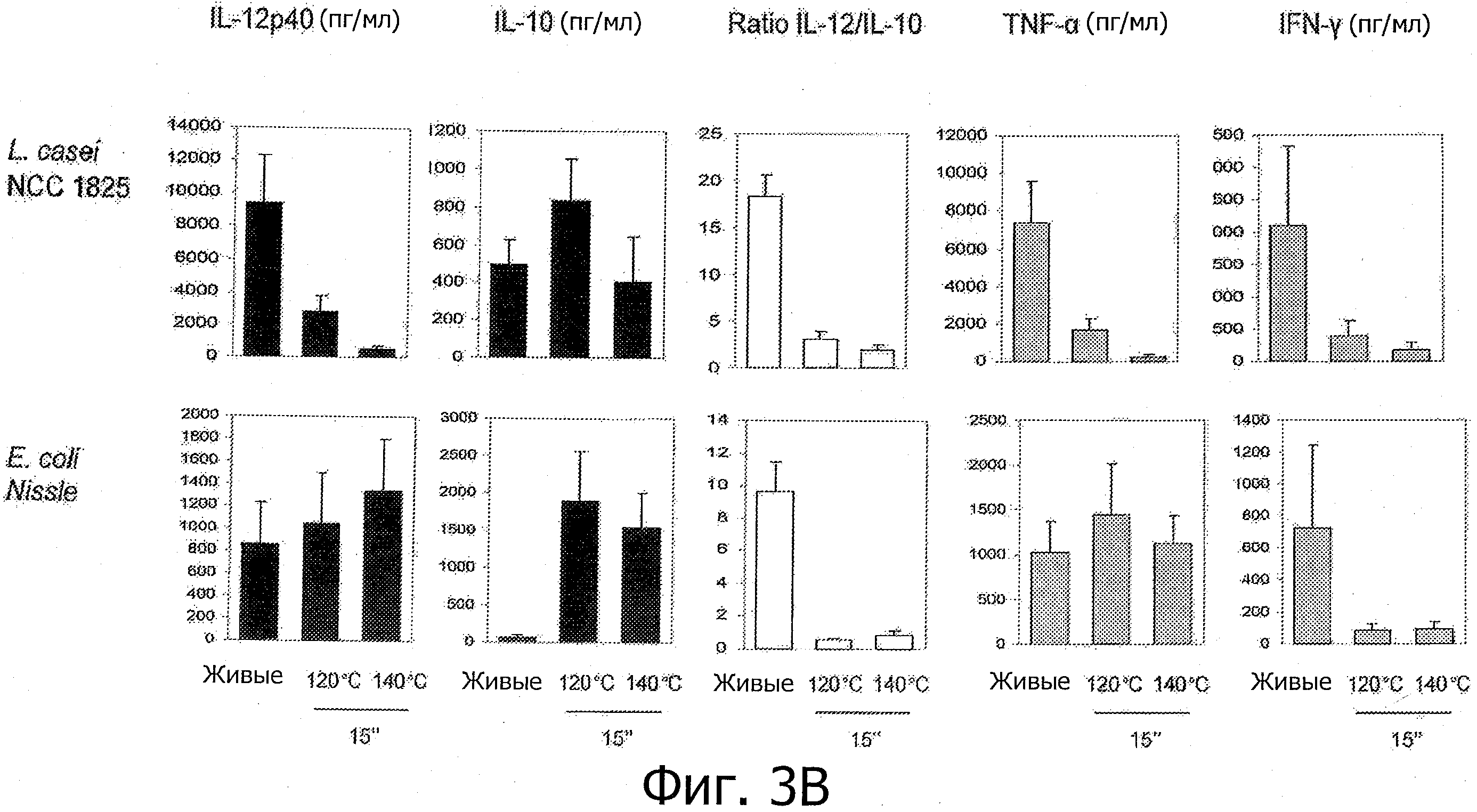
Фигуры 3А и В демонстрируют пробиотические штаммы, используемые в коммерчески доступных продуктах, которые демонстрируют усиление или появление новых противовоспалительных иммунных профилей in vitro после «высокотемпературной кратковременной обработки».
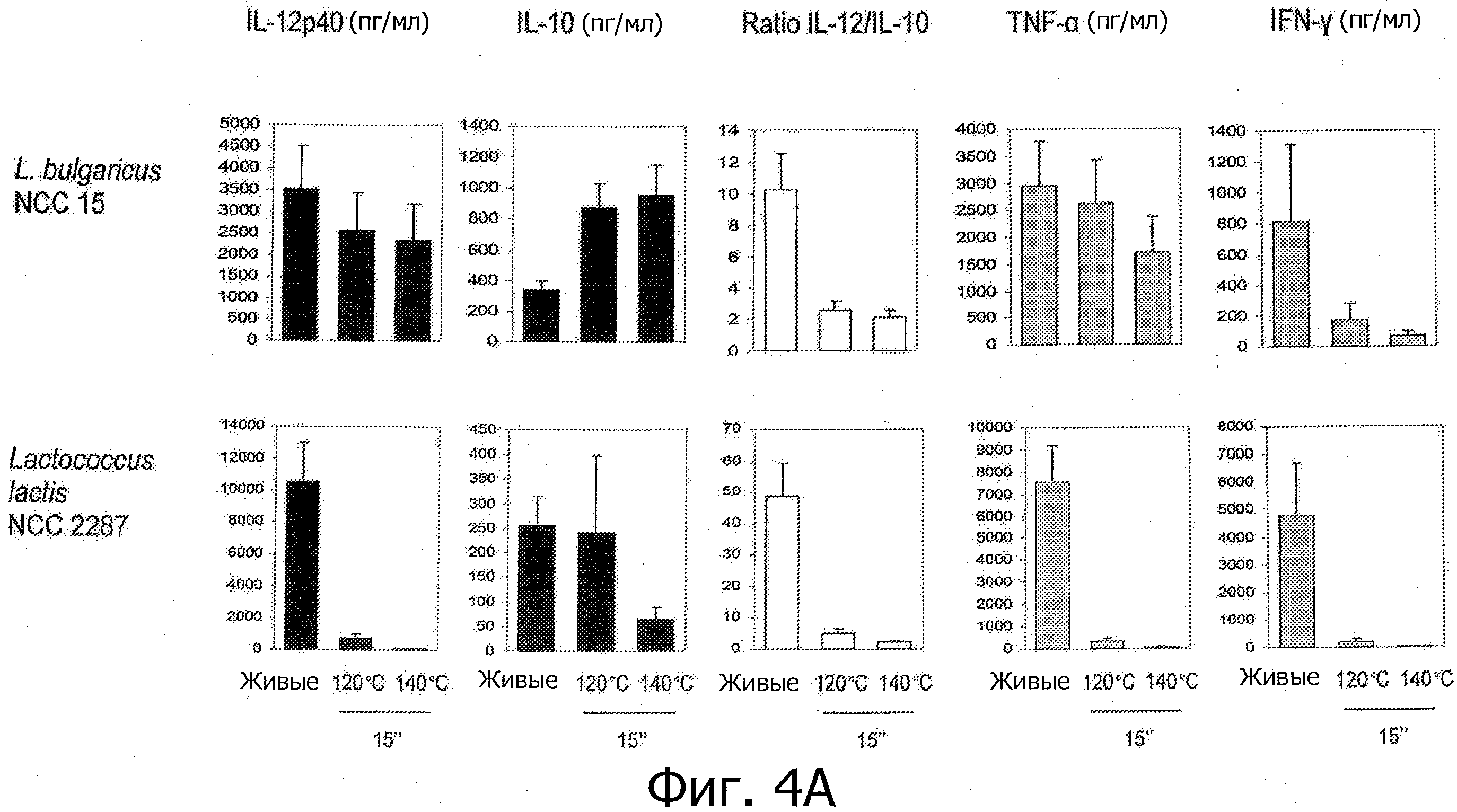
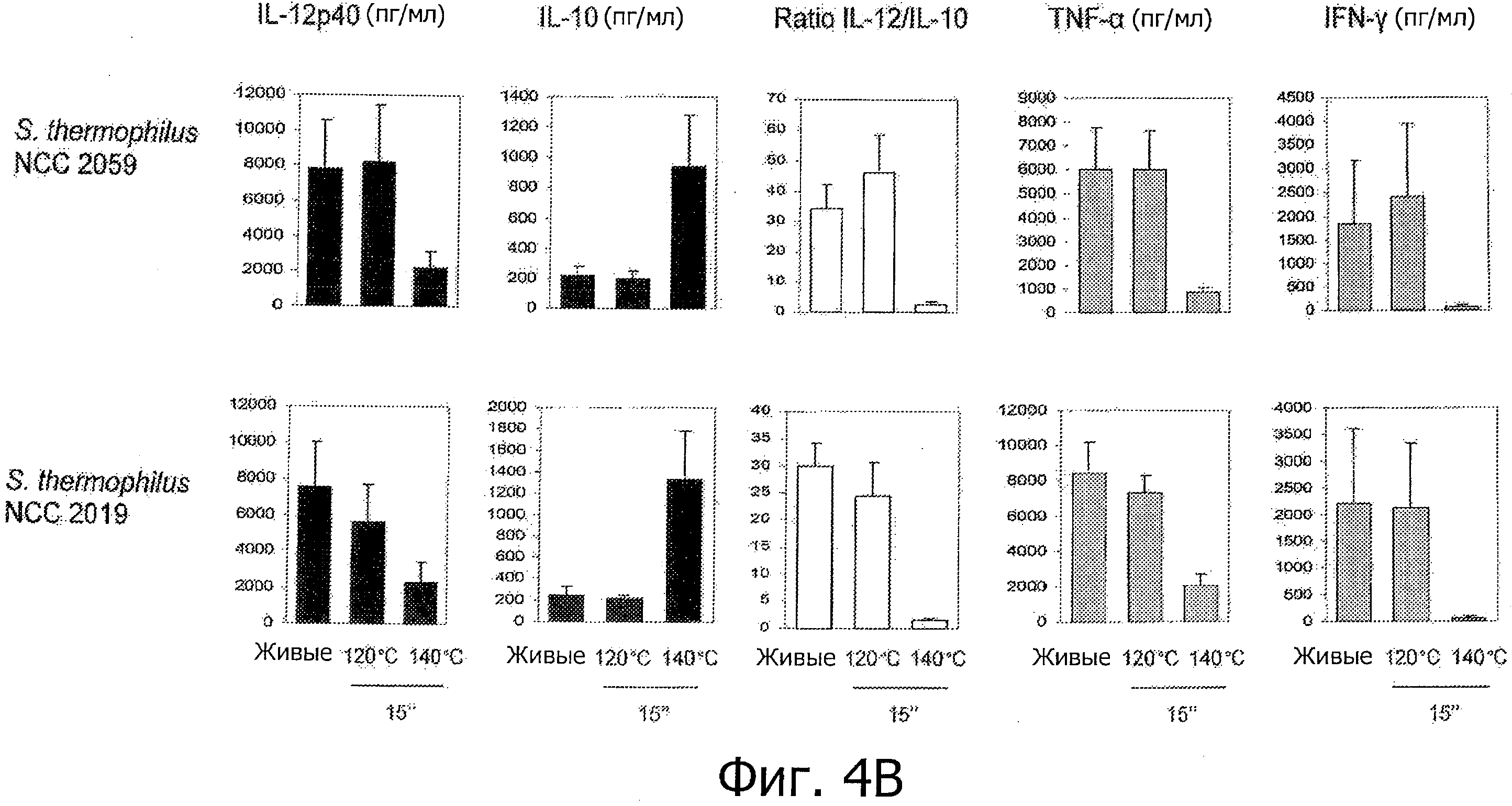
Фигуры 4А и В демонстрируют молочные заквасочные штаммы (т.е. заквасочные штаммы Lcl), которые демонстрируют усиление или появление новых противовоспалительных иммунных профилей in vitro при тепловой обработке высокими температурами.
Фигура 5 демонстрирует непротивовоспалительный пробиотический штамм, который демонстрирует противовоспалительный иммунный профиль in vitro после ВТКВ-обработки.
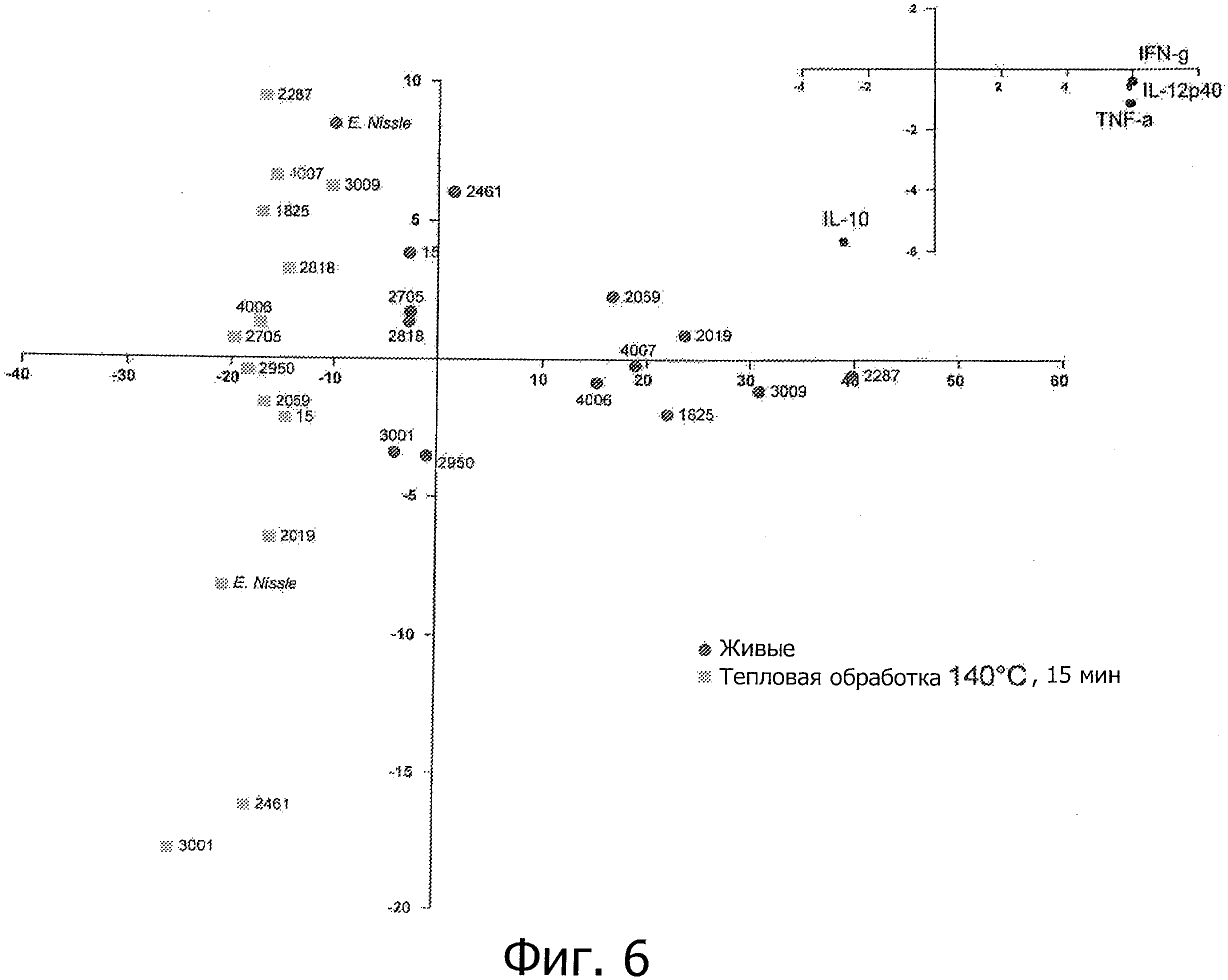
Фигура 6: анализ основных компонентов на основе данных РВМС (IL-12p40, IFN-γ, TNF-α, IL-10), полученных с использованием живых и подвергнутых термообработке (140°С в течение 15 секунд) форм пробиотических и молочных заквасочных штаммов. Все данные характеризуют один штамм, живой или подвергнутый тепловой обработке, идентифицированный по его NCC-номеру или по названию.
Фигура 7 демонстрирует соотношения IL-12p40/IL-10 живых и подвергнутых тепловой обработке штаммов (85°С, 20 мин). В целом, термообработка при 85°С в течение 20 мин приводит к увеличению соотношений IL-12p40/IL-10 в отличие от данных, соответствующих «высокотемпературной кратковременной обработке» по настоящему изобретению (Фигуры 1, 2, 3, 4 и 5).
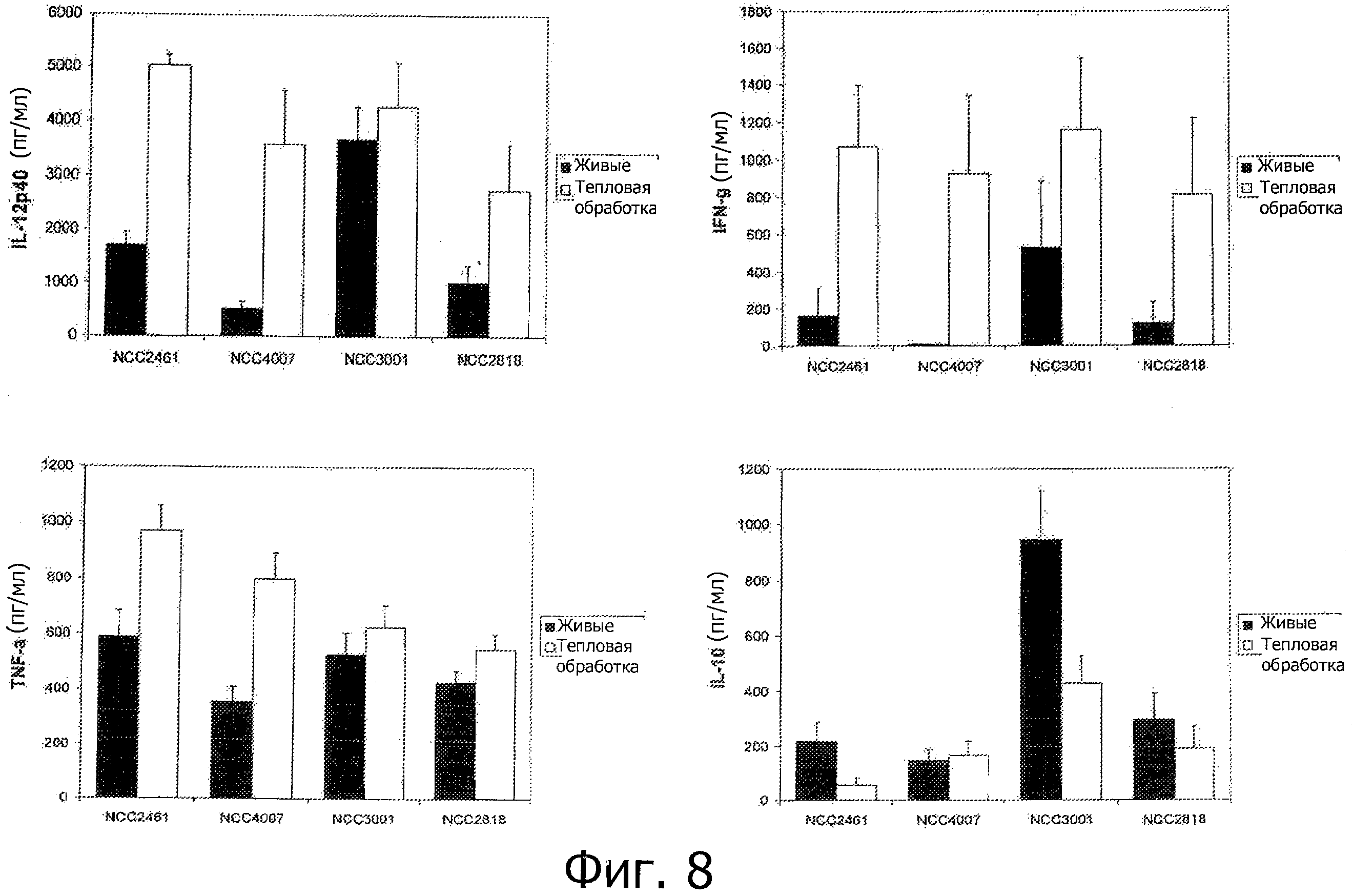
Фигура 8 демонстрирует усиление in vitro секреции цитокинов человеческими клетками РВМС, которые стимулировали бактериями, подвергнутыми тепловой обработке.
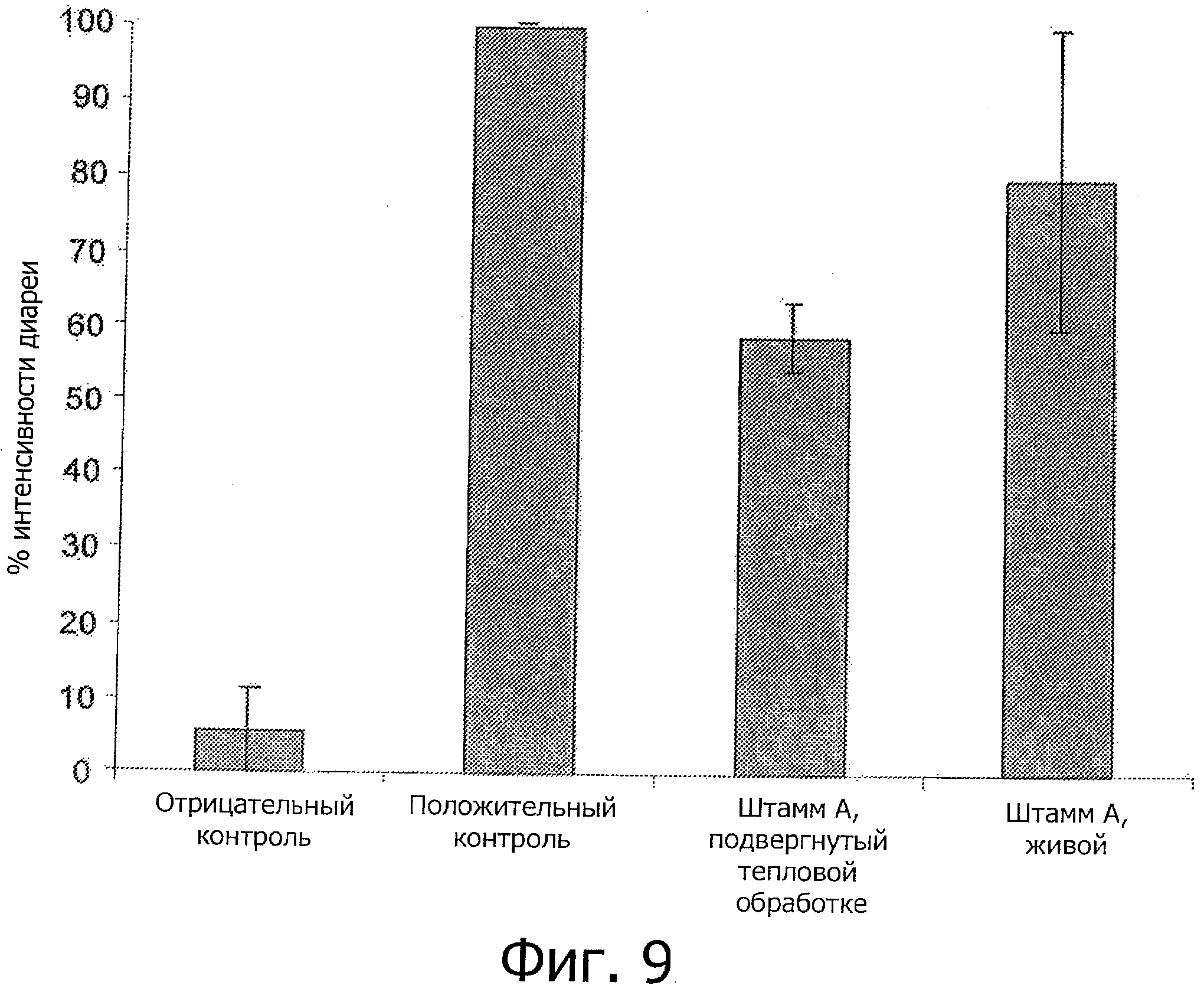
Фигура 9 демонстрирует процент интенсивности диареи, наблюдаемой у OVA-сенсибилизированных мышей, стимулированных с использованием физиологического раствора (отрицательный контроль), OVA-сенсибилизированных мышей, стимулированных с использованием OVA (положительный контроль) и у OVA-сенсибилизированных мышей, стимулированных с использованием OVA и обработанных бактериями Bifidobacterium breve NCC2950, которые были подвергнуты термообработке, или живыми бактериями. Результаты представлены в виде процента интенсивности диареи (Среднее значение±стандартная ошибка среднего, рассчитанные для 4 независимых экспериментов), при 100% интенсивности диареи, соответствующей симптомам, развившимся в группе положительного контроля (мыши, сенсибилизированные и стимулированные аллергеном).
Пример 1:
Методология
Бактериальные препараты:
Предполагается, что польза для здоровья, оказываемая живыми пробиотиками иммунной системе организма-хозяина, как правило, является штаммспецифичной. Было продемонстрировано, что пробиотики, индуцирующие IL-10 на высоком уровне и/или индуцирующие провоспалительные цитокины на низком уровне in vitro (РВМС-анализ), являются сильными противовоспалительными штаммами in vivo (Foligne, В., et al., 2007, World J.Gastroenterol. 13:236-243).
Для исследования противовоспалительных свойств пробиотиков, подвергнутых тепловой обработке, использовали несколько пробиотических штаммов. Это штаммы Bifldobacterium longum NCC 3001, Bifidobacterium longum NCC 2705, Bifidobacterium breve NCC 2950, Bifidobacterium lactis NCC 2818, Lactobacillus paracasei NCC 2461, Lactobacillus rhamnosus NCC 4007, Lactobacillus easel NCC 4006, Lactobacillus acidophilus NCC 3009, Lactobacillus easel ACA-DC 6002 (NCC 1825), и Escherichia coli Nissle. Также тестировали несколько штаммов заквасочных культур, включающих некоторые штаммы, коммерчески используемые для получения Lcl-ферментированных продуктов «Nestle»: Streptococcus thermophilus NCC 2019, Streptococcus thermophilus NCC 2059, Lactobacillus bulgaricus NCC 15 и Lactococcus lactis NCC 2287.
Бактериальные клетки культивировали в 5-15 л биореакторах в условиях, оптимизированных для каждого штамма. Применимы все типичные среды для бактериального роста. Такие среды известны специалистам в данной области. Когда рН доводили до значения 5,5, то непрерывно добавляли 30% раствор основания (или NaOH или Са(ОН)2). При поддержании адекватных, анаэробных условий в свободное пространство над продуктом выпускали CO2, E.coli при этом культивировали в стандартных аэробных условиях.
Бактериальные клетки собирали с помощью центрифугирования (5000×g, 4°C) и ресуспендировали в фосфатно-солевом буфере (PBS) в достаточном объеме с целью достижения конечной концентрации около 109-1010 КОЕ/мл. Часть препарата замораживали при -80°С в 15% глицерине. Другую часть клеток подвергали тепловой обработке с помощью:
- Ультравысокой температуры: 140°С в течение 15 сек; путем инжекции непрямого пара.
- Высокотемпературной Кратковременной обработки (ВТКВ): 74°С, 90°С и 120°С в течение 15 сек путем инжекции непрямого пара.
- Продолжительной низкотемпературной обработки (85°С, 20 мин) на водяной бане.
После тепловой обработки образцы держали замороженными при -80°С до использования.
In vitro иммунопрофилирование бактериальных препаратов:
Определяли иммунные профили живых и термообработанных бактериальных препаратов (т.е. способность индуцировать секрецию специфических цитокинов клетками крови человека in vitro). Человеческие мононуклеарные клетки перефирической крови (РВМС) выделяли из кровяных фильтров. После разделения клеток в градиенте плотности, мононуклеарные клетки собирали и отмывали дважды сбалансированным солевым раствором Хенкса. Затем клетки ресуспендировали в среде Дульбекко, модифицированной по способу Исков (Iscove's Modified Dulbecco's Medium) (IMDM, Sigma), дополненной 10% фетальной телячьей сывороткой (Bioconcept, Париж, Франция), 1% L-глутамином (Sigma), 1% пенициллином/стрептомицином (Sigma) и 0,1% гентамицином (Sigma). РВМС (7×105 клеток/на лунку) затем инкубировали с живыми и подвергнутыми тепловой обработке бактериями (эквивалентное количество 7×10 КОЕ/на лунку) в 48-луночных планшетах в течение 36 ч. Воздействия живых и подвергнутых тепловой обработке бактерий тестировали на РВМС из 8 доноров-индивидуумов, разделенных на два отдельных эксперимента. Через 36 часов инкубации культуральные чашки замораживали и хранили при -20°С до измерения цитокинов. Профилирование цитокинов осуществляли параллельно (т.е. в одном и том же эксперименте на одних и тех же партиях РВМС) для живых бактерий и для их подвергнутых тепловой обработке эквивалентов.
Уровни цитокинов (IFN-γ, IL-12p40, TNF-α и IL-10) определяли с помощью ИФА в надосадочных жидкостях клеточных культур через 36 часов инкубации (R&D DuoSet Human IL-10, BD OptEIA Human IL12p40, BD OptEIA Human TNF, BD OptEIA Human IFN-γ), следуя инструкциям изготовителей. IFN-γ, IL-12p40 и TNF-α являются провоспалительными цитокинами, тогда как IL-10 является мощным противовоспалительным медиатором. Результаты представлены в виде среднего (пг/мл)+/- стандартная ошибка среднего 4 индивидуальных доноров и являются репрезентативными для двух индивидуальных экспериментов осуществленных с 4 донорами в каждом. Соотношение IL-12p40/IL-10 рассчитывают для каждого штамма в качестве прогнозируемой величины in vivo противовоспалительного воздействия (Foligne, В., et al., 2007, World J.Gastroenterol. 13:236-243).
Числовые значения для цитокинов (пг/мл), определенные с помощью ИФА (см. выше) для каждого штамма, заносили в программу «BioNumerics v5.10 software» (Applied Maths, Синт-Мартенс-Латем, Бельгия). Анализ основных компонентов (РСА, расчетный метод) осуществляли на основе этой группы данных. Вычитание средних значений по признакам и деление на вариантность по признакам было включено в данный анализ.
Результаты
Противовоспалительные профили, полученные с помощью обработок типа ультравысокотемпературной обработки (УВТ)/высокотемпературной кратковременной обработки (ВТКВ).
Исследуемые пробиотические штаммы подвергали воздействию серии термообработок (ультравысокотемпературная (УВТ), высокотемпературная кратковременная (ВТКВ) и при 85°С в течение 20 мин), и сравнивали их иммунные профили с профилями живых клеток in vitro. При инкубации с человеческими клетками РВМС живые микроорганизмы (пробиотики и/или молочные заквасочные культуры) индуцировали продуцирование цитокинов на разном уровне (Фигуры 1, 2, 3, 4 и 5). Тепловая обработка этих микроорганизмов модифицировала уровни цитокинов, продуцируемых РВМС, зависимым от температуры образом. «Высокотемпературные кратковременные» обработки (120°С или 140°С в течение 15 сек) давали нереплицирующиеся бактерии с противовоспалительными иммунными профилями (Фигуры 1, 2, 3 и 4). Фактически, штаммы, подвергнутые обработке типа УВТ (140°С, 15 сек), индуцировали меньше провоспалительных цитокинов (TNF-α, IFN-γ, IL-12p40) при этом с сохранением или с индукцией дополнительного продуцирования IL-10 (по сравнению с живыми эквивалентами). Полученные в результате соотношения IL-12p40/IL-10 были ниже для любых штаммов, подвергнутых обработке типа УВТ, по сравнению с живыми клетками (Фигуры 1, 2, 3 и 4). Это наблюдение также было верным для бактерий, подвергнутых обработке типа ВТКВ, т.е. подвергнутых воздействию 120°С в течение 15 сек (Фигуры 1, 2, 3 и 4), или 74°С и 90°С в течение 15 сек (Фигура 5). Тепловые обработки (обработки типа УВТ или типа ВТКВ) обладали аналогичным эффектом в отношении in vitro иммунных профилей пробиотических штаммов (Фигуры 1, 2, 3 и 5) и молочных заквасочных культур (Фигура 4). Анализ основных компонентов на основе данных с РВМС, полученных с живыми и подвергнутыми тепловой обработке (140°С, 15 сек) пробиотическими и молочными заквасочными штаммами, выявил, что живые штаммы распространялись вдоль оси x, что говорит о том, что штаммы демонстрируют очень разные иммунные профили in vitro, от слабых (левая панель) до сильных (правая панель) индукторов провоспалительных цитокинов. Штаммы, подвергнутые тепловой обработке, кластеризуются на левой панели графика, демонстрируя, что провоспалительные цитокины гораздо слабее индуцируются штаммами, подвергнутыми тепловой обработке (Фигура 6). Напротив, бактерии, подвергнутые тепловой обработке при 85°С в течение 20 мин, индуцировали больше провоспалительных цитокинов и меньше IL-10 по сравнению с живыми клетками, которые приводят к получению более высоких соотношений IL-12p40/IL-10 (Фигура 7).
Противовоспалительные профили усиливаются или генерируются с помощью обработок типа УВТ и ВТКВ.
Штаммы, подвергнутые обработкам УВТ и ВТКВ, демонстрируют противовоспалительные профили независимо от их соответствующих исходных иммунных профилей (живые клетки). Было показано, что пробиотические штаммы, которые как известно, являются противовоспалительными in vivo и демонстрируют противовоспалительные профили in vitro (В. longum NCC 3001, В. longum NCC 2705, В. breve NCC 2950, В. lactis NCC 2818) демонстрируют усиление противовоспалительных профилей in vitro после «высокотемпературных кратковременных» обработок. Как показано на Фигуре 1, соотношения IL-12p40/IL-10 штаммов Bifidobacterium, подвергнутых обработке типа УВТ, были ниже, чем эти соотношения живых эквивалентов, демонстрируя, таким образом, улучшенные противовоспалительные профили образцов, подвергнутых обработке типа УВТ. Более удивительно то, что образование противовоспалительных профилей с помощью обработок типа УВТ и ВТКВ подтверждалось для непротивовоспалительных живых штаммов. Оба штамма, живые L. rhamnosus NCC 4007 и L. paracasei NCC 2461, демонстрируют высокие соотношения IL-12p40/IL-10 in vitro (Фигуры 2 и 5). Было показано, что два штамма не являются защитными против TNBS-индуцированного колита у мышей. Соотношения IL-12p40/IL-10, индуцированные с помощью L. rhamnosus NCC 4007 и L. paracasei NCC 2461, существенно снижались после «высокотемпературных кратковременных» обработок (УВТ или ВТКВ), достигая уровня настолько низкого, как тот, который получают с использованием штаммов Bifidobacterium. Эти низкие соотношения IL-12p40/IL-10 наблюдаются благодаря низкому уровню продуцирования IL-12p40, объединенному с отсутствием изменений (L. rhamnosus NCC 4007) или с мощной индукцией секреции IL-10 (L. paracasei NCC 2461) (Фигура 2).
Как следствие: - Противовоспалительные профили живых микроорганизмов могут быть усилены с помощью термообработок типа УВТ и типа ВТКВ (например, В. longum NCC 2705, В. longum NCC 3001, В. breve NCC 2950, В. lactis NCC 2818);
- Противовоспалительные профили могут быть получены из непротивовоспалительных живых микроорганизмов (например, L. rhamnosus NCC 4007, L. paracasei NCC 2461, молочных заквасочных культур S. thermophilus NCC 2019) с помощью термообработок типа УВТ и типа ВТКВ;
- Противовоспалительные профили также показаны для штаммов, выделенных из коммерчески доступных продуктов (Фигуры 3А и В), включая пробиотический штамм Е. coli.
Влияние обработок типа УВТ/ВТКВ было похожим для всех проверенных пробиотиков и молочных заквасочных культур, например, бифидобактерий и стрептококков.
Обработки типа УВТ/ВТКВ применяли к нескольким штаммам лактобацилл, бифидобактерий и стрептококков, демонстрирующим различные иммунные профили in vitro. Все штаммы индуцировали меньше провоспалительных цитокинов после обработок типа УВТ/ВТКВ, чем их живые эквиваленты (Фигуры 1, 2, 3, 4, 5 и 6), что говорит о том, что воздействие обработок типа УВТ/ВТКВ, оказываемое на иммунные свойства полученных в результате нереплицирующихся бактерий, может быть общим для всех пробиотиков, конкретно, для штаммов лактобацилл, бифидобактерий, и конкретных штаммов Е. coli, а также для всех молочных заквасочных культур, конкретно, для стрептококков, лактококков и лактобацилл.
Пример 2:
Методология
Бактериальные препараты:
Пять пробиотичесих штаммов использовали для исследования иммуностимулирующих свойств нереплицирующихся пробиотиков: 3 бифидобактерий (В. longum NCC3001, В. lactis NCC2818, В. breve NCC2950) и 2 лактобациллы (Z. paracasei NCC2461, L. rhamnosus NCC4007).
Бактериальные клетки выращивали на MRS при периодической ферментации при 37°С в течение 16-18 часов без контроля рН. Бактериальные клетки осаждали (5000×g, 40°С) и ресуспендировали в фосфатно-солевом буфере для разведения в соленой воде для достижения конечной концентрации около 1010 КОЕ/мл. В. longum NCC3001, В. lactis NCC2818, L. paracasei NCC2461, L. rhamnosus NCC4007 подвергали тепловой обработке при 85°С в течение 20 мин в водяной бане. В. breve NCC2950 подвергали тепловой обработке при 90°С в течение 30 минут на водяной бане. Повергнутые тепловой обработке бактериальные суспензии разделяли на аликвоты и хранили замороженными при -80°С до использования. Живые бактерии хранили при -80°С в PBS-15% глицерин до использования.
In vitro иммунопрофилирование бактериальных препаратов
Определяли иммунные профили живых и подвергнутых тепловой обработке бактериальных препаратов (т.е. способность индуцировать секрецию специфических цитокинов клетками крови человека in vitro). Человеческие мононуклеарные клетки перефирической крови (РВМС) выделяли из кровяных фильтров. После разделения клеток в градиенте плотности, мононуклеары собирали и отмывали дважды сбалансированным солевым раствором Хенкса. Затем клетки ресуспендировали в среде Дульбекко, модифицированной по способу Исков (Iscove's Modified Dulbecco's Medium) (IMDM, Sigma), дополненной 10% фетальной телячьей сывороткой. (Bioconcept, Париж, Франция), 1% L-глутамином (Sigma), 1% пенициллином/стрептомицином (Sigma) и 0,1% гентамицином (Sigma). РВМС (7×105 клеток/на лунку) затем инкубировали с живьми и подвергнутыми тепловой обработке бактериями (эквивалентное количество 7×106 КОЕ/на лунку) в 48-луночных планшетах в течение 36 часов. Воздействия живых и подвергнутых тепловой обработке бактерий тестировали на РВМС из 8 доноров-индивидуумов разделенных на два отдельных эксперимента. Через 36 часов инкубации культуральные чашки замораживали и хранили при -20°С до измерения цитокинов. Профилирование цитокинов осуществляли параллельно (т.е. в одном и том же эксперименте на одних и тех же партиях РВМС) для живых бактерий и для их подвергнутых тепловой обработке эквивалентов.
Уровни цитокинов (IFN-y, IL-12p40, TNF-α и IL-10) в надосадочных жидкостях клеточных культур через 36 часов инкубации определяли с помощью ИФА (R&D DuoSet Human IL-10, BD OptEIA Human IL12p40, BD OptEIA Human TNF, BD OptEIA Human IFN-γ), следуя инструкциям изготовителей. IFN-γ, IL-12p40 и TNF-α являются провоспалительными цитокинами, тогда как IL-10 является мощным противовоспалительным медиатором. Результаты представлены в виде среднего (пг/мл)+/- стандартная ошибка среднего 4 индивидуальных доноров и являются репрезентативными для двух индивидуальных экспериментов осуществленных с 4 донорами в каждом.
In vivo воздействие живых и подвергнутых тепловой обработке Bifidobacterium breve NCC2950 при предотвращении аллергической диареи
Мышиную модель аллергической диареи применяли для проверки промотирующего ТЫ воздействия В. breve NCC2950 (Brandt E.B et al. JCI 2003; 112(11); 1666-1667). После сенсибилизации (2 перитонеальные инъекции Овальбумина (OVA) и алюминиевокалиевыми квасцами с интервалом 14 дней; дни 0 и 14) самцов мышей Balb/c перорально стимулировали OVA 6 раз (дни 27, 29, 32, 34, 36, 39), что привело к временным клиническим симптомам (диарея) и изменениям иммунных параметров (концентрации в плазме общего IgE, OVA-специфичного IgE, мышиной протеазы 1 тучных клеток, т.е. ММСР-1). Bifidobacterium breve NCC2950 живые или термообработанные при 90°С в течение 30 минут вводили зондом за 4 дня до сенсибилизации OVA (дни -3, -2, -1, 0 и дни 11, 12, 13 и 14) и в течение периода стимулирования (дни с 23-39). Использовали ежедневную бактериальную дозу около 10 КОЕ или эквивалент КОЕ/мышь.
Результаты
Индукция секреции «провоспалительных» цитокинов после тепловой обработки.
Способность подвергнутых тепловой обработке бактериальных штаммов стимулировать секрецию цитокинов человеческими мононуклеарными клетками периферической крови (РВМС) оценивали in vitro. Иммунные профили, основанные на четырех цитокинах, в результате стимуляции РВМС инактивированными тепловой обработкой бактериями, сравнивали с профилями, индуцированными живыми бактериальными клетками в том же самом in vitro анализе.
Термообработанные препараты помещали на чашки и оценивали отсутствие каких-либо жизнеспособных единиц. Подвергнутые тепловой обработке бактериальные препараты не продуцируют колонии после рассевания.
Живые пробиотики индуцировали другие и штаммзависимые уровни продуцирования цитокинов при инкубации с человеческими РВМС (Фигура 8). Тепловая обработка пробиотиков модифицирует уровни цитокинов, полученных с помощью РВМС по сравнению с их живыми эквивалентами. Подвергнутые тепловой обработке бактерии индуцируют больше провоспалительных цитокинов (TNF-α, IFN-γ, IL-12p40), чем их живые эквиваленты. Напротив термообработанные бактерии индуцировали подобные или более низкие количества IL-10 по сравнению с живыми клетками (Фигура 8). Эти данные демонстрируют, что подвергнутые тепловой обработке бактерии способны сильнее стимулировать иммунную систему, чем их живые эквиваленты и, следовательно, способны лучше усиливать ослабленные иммунные защиты. Другими словами in vitro данные демонстрируют улучшенное иммунное усиливающее воздействие бактериальных штаммов после тепловой обработки.
Для иллюстрации усиленного воздействия термообработанных В. breve NCC2950 (по сравнению с живыми клетками) на иммунную систему, тестировали и живые и термообработанные B.breve NCC2950 (штамм А) в животной модели аллергической диареи.
По сравнению с положительной контрольной группой, интенсивность диареи значительно и сообразно снизилась после обработки подвергнутыми тепловой обработке В. breve NCC2950 (41.1%±4.8), тогда как интенсивность диареи снизилась только на 20±28.3% после обработки живыми В. breve NCC2950. Эти результаты показывают, что подвергнутые тепловой обработке В. breve NCC2950 демонстрируют более сильное защитное воздействие против аллергической диареи, чем их живые эквиваленты (Фигура 9).
Как следствие, было показано, что способность пробиотиков усиливать иммунную защиту стала лучше после тепловой обработки. Примеры 3 и 4:
Могут быть получены следующие композиции:
Для младенцев в возрасте 4-6 месяцев:
Ингредиенты: рисовая мука, мальтодекстрин, витамин С, минеральное вещество (железо).
Готовую к употреблению кашу получают путем смешивания 15 г состава с 90 мл воды.
Для младенцев в возрасте 6-12 месяцев:
Ингредиенты: пшеничная мука, манная крупа (пшеница), минеральное вещество (железо), витамины [С, ниацин, В6, тиамин], маисовый мальтодекстрин.
Готовую к употреблению кашу получают путем смешивания 15 г состава с 90 мл воды.
Реферат
Настоящее изобретение относится к области детских каш. Детская каша содержит, по меньшей мере, 0,48 г/100 кДж источника белков, по большей части 1,1 г/100 кДж источника жиров, источника углеводов и нереплицирующиеся пробиотические микроорганизмы. При этом нереплицирующиеся пробиотические микроорганизмы приводят в нереплицирующееся состояние тепловой обработкой, которая представляет собой высокотемпературную обработку при 71,5-150°C в течение около 1-120 секунд. Изобретение позволяет получить готовый продукт с повышенными противовоспалительными свойствами, а также усилить иммунную систему младенца. 13 з.п. ф-лы, 12 ил., 2 пр.

Комментарии