Соединения с группами сложных эфиров оксима и/или ацильными группами - RU2628076C2
Код документа: RU2628076C2
Чертежи









Описание
ПЕРЕКРЕСТНЫЕ ССЫЛКИ НА РОДСТВЕННЫЕ ЗАЯВКИ
Данное описание заявляет приоритет в соответствии с 35 U.S.С. §119(e), U.S. предварительными заявками серийных No. 61/489,910 и 61/489,892, поданы 25 мая 2011 г.
ОБЛАСТЬ ТЕХНИКИ
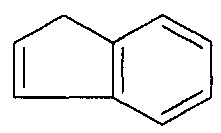
[0001] Настоящее изобретение относится к соединениям, содержащим, по крайней мере, одну группу сложного эфира оксима и/или ацильную группу. Более конкретно настоящее изобретение относится к соединениям на основе индена, сопряженного с флуореном или 9,10-дигидроантраценом и их производными.
ПРЕДПОСЫЛКИ СОЗДАНИЯ ИЗОБРЕТЕНИЯ
[0002] Фоточувствительные или фотополимеризуемые композиции, как правило, включают, к примеру, этиленненасыщенную связь полимеризуемого соединения и инициатор фотополимеризации. Такие фоточувствительные или фотополимеризуемые композиции полимеризуются и отверждаются при облучении светом, и, следовательно, используются, к примеру, в фотонаборах или фотоотверждаемых чернилах, фоточувствительных печатных платах, резистах цветофильтров, черноматричных полимерах, и множестве фоторезистов, включая сухой пленочный фоторезистор.
[0003] В последние годы возникла потребность в фоточувствительных или фотополимеризуемых композициях, которые чувствительны к источникам света с более короткой длиной волны (365 нм или 405 нм), и, следовательно, потребность в инициаторах фотополимеризации, чувствительных к таким источникам света, также увеличилась.
[0004] Инициаторы фотополимеризации также называются свободно радикальные фотоинициаторы. Под воздействием света с длиной волны, к которой они чувствительны, они генерируют свободные радикалы и таким образом инициируют свободнорадикальную полимеризацию окружающих полимеризуемых соединений.
[0005] Как правило, желательно, чтобы такие фотоинициаторы демонстрировали хорошую чувствительность к свету, в особенности в УФ-области спектра, низкое обесцвечивание при использовании, и хорошую термическую стабильность (при хранении и обработке).
[0006] Некоторые органические соединения, содержащие ацильные и/или группы сложного эфира оксима известны как свободнорадикальные фотоинициаторы. Они нашли применение в резистах цветовых фильтров в виду их поглощения в области ультрафиолетового излучения (между 300 и 450 нм). Irgacure OXE-01™ и ОХЕ-02™ (доступные от BASF, Германия) являются известными фотоинициаторами для некоторых применений, включая резисты цветовых фильтров. Некоторые соединения на основе триазина также известны как полезные фотоинициаторы.
[0007] Настоящее описание относится к количеству документов, содержание которых включено здесь в качестве ссылки в полном объеме.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
[0008] В соответствии с настоящим изобретением:
1. Соединение, содержащее, необязательно, замещенное


2. Соединение по п.1, где группа сложного эфира оксима представляет собой -CR6=N-O-(C=O)-R7 или =N-O-(C=O)-R7, где R6 и R7 представляют собой одинаковые или различные заместители.
3. Соединение по п.2, где R6 представляет собой:
- водород;
- C1-C12алкил, необязательно замещенный одним или более:
- фенилом,
- галогеном,
- -NR9R10,
- -O-L, и/или
- -S-L;
- C4-C10циклоалкил, C2-C12алкенил, C4-C10циклоалкенил, C2-C12алкинил, или C4-C10циклоалкенил, каждый из которых является необязательно замещенным алкилом и/или -O-L; или
- фенил, необязательно замещенный одним или более:
- C1-C6алкилом,
- галогеном,
- нитрилом,
- алкилокси,
- -COOR10, и/или
- C2-C12алкилкарбоксилом,
где L представляет собой водород или C1-C6алкил и где каждый из R8, R9 и R10 представляют собой независимо водород, C1-C12алкил; C4-C10циклоалкил; C1-C12алкенил; C4-C10циклоалкенил; C2-C12алкинил; C4-C10циклоалкинил; C1-C12галогеналкил; или необязательно замещенный арил.
4. Соединение по п.3, в котором R6 представляет собой алкил, необязательно замещенный -O-C1-6алкилом.
5. Соединение по п.4, в котором R6 представляет собой метил или бутил.
6. Соединение по п.5, в котором R6 представляет собой метил.
7. Соединение по любому из пп.2-6, где R7 представляет собой алкил, циклоалкил, алкенил или циклоалкенил, каждый из которых является необязательно замещенным арилом или галогеном, или R7 представляет собой арил, необязательно замещенный алкилом или галогеном.
8. Соединение по п.7, где R7 представляет собой C1-C12алкил, необязательно замещенный фенилом; C4-C10циклоалкил или фенил, необязательно замещенный C1-C6алкилом.
9. Соединение по п.8, где R7 представляет собой C1-C12алкил; C4-C10циклоалкил или фенил.
10. Соединение по п.9, где R7 представляет собой метил.
11. Соединение по любому из пп.1-10, где ацильная группа представляет собой -C(=O)-R30, где R30 представляет собой необязательно замещенный алкил, циклоалкил, алкенил, циклоалкенил, алкинил, циклоалкинил или арил, каждый из которых необязательно содержит один или больше атом кислорода, атом серы, атом азота, карбонильную группу, карбаматную группуа, карбамидную группу, и/или сложноэфирную группу.
12. Соединение по п.11, в котором указанный алкил, циклоалкил, алкенил, циклоалкенил, алкинил, циклоалкинил и арил в R30 является замещенным одной или более
- полиэтиленгликолевой цепью,
- C1-C12алкилом, необязательно замещенным одним или более:
- -NR8R9,
- -O-L,
- -S-L, и/или
- фенилом, необязательно замещенным одним или более: C1-C6алкилом, галогеном, нитрилом, алкилокси, COOR10, и/или C2-C12алкилкарбоксилом;
- C4-C10циклоалкилом, C2-C12алкенилом, C4-C10циклоалкенилом, C2-C12алкинилом, C4-C10циклоалкинилом, каждый из которых является необязательно замещенным алкилом и/или -O-L, и/или
- арилом, таким как фенил, тиофенил, бифенил и нафтил, каждый из которых является необязательно замещенным одним или более:
- C1-C6алкилом,
- галогеном,
- нитрилом,
- алкилокси,
- -COOR10, и/или
- C2-C12алкилкарбоксилом
где L, R8, R9 и R10 представляют собой, как опредено в п.3.
13. Соединение по п.12, где R30 представляет собой линейный алкил, фенил или тиофенил, все из которых являются необязательно замещенными линейным алкилом или -O-L.
14. Соединение по п.13, где R30 представляет собой метил, 2-метилфенил, фенил, тиофенил, или 4-метоксифенил.
15. Соединение по любому из пп.1-14, где, по крайней мере, одна группа сложного эфира оксима и/или ацильные группы являются прикрепленными к соединению через связь -LK-.
16. Соединение по п.15, где -LK- представляет собой необязательно замещенный алкилен, циклоалкилен, алкенилен, циклоалкенилен, алкинилен, циклоалкинилен, арилен, -S-арилен, -NH-арилен или -N(арил) -арилен, каждый из которых необязательно содержит один или больше атомов кислорода, атом серы, атом азота, карбонильную группу, карбаматную группу, карбамидную группу, и/или сложноэфирную группу.
17. Соединение по п.16, где алкилен, циклоалкилен, алкенилен, циклоалкенилен, алкинилен, циклоалкинилен, арилен, -S-арилен, -NH-арилен и -N(арил)-арилен являются замещенными одной или больше:
- полиэтиленгликолевой цепью,
- C1-C12алкилом, необязательно замещенным одним или более:
- -NR8R9,
- -O-L,
- -S-L, и/или
- фенилом, необязательно замещенным одним или более: C1-C6алкилом, галогеном, нитрилом, алкилокси, COOR10 и/или C2-C12алкилкарбоксилом;
- C4-C10циклоалкилом, C2-C12алкенилом, C4-C10циклоалкенилом, C2-C12алкинилом, C4-C10циклоалкинилом, каждый из которых является необязательно замещенным алкилом и/или -O-L, и/или
- арилом, таким как фенил, бифенил и нафтил, или арилоилом, таким как бензоил, каждый из которых является необязательно замещенным одним или больше:
- C1-C6алкилом,
- галогеном,
- нитрилом,
- алкилокси,
- -COOR10, и/или
- C2-C12алкилкарбоксилом.
где L, R8, R9 и R10 представляют собой как определено в п.3.
18. Соединение по любому из пп.1-17, где ФОРМУЛА I и/или одна из двух или обе ФОРМУЛЫ II представляют собой независимо замещенные одним или больше из следующих заместителей:
- C1-C12алкил, C1-C12алкилокси, C4-C10циклоалкил, C1-C12алкенил, C4-C10циклоалкенил, C4-C10циклоалкенил, C2-C12алкинил, и/или C4-C10циклоалкинил, каждый из которых является необязательно замещенным одним или больше:
- NR8R9,
- -O-L,
- -S-L, и/или
- фенилом, необязательно замещенным одним или более C1-C6алкилом, атомом галогена, нитрилом, алкилокси, COOR10 и/или C2-C12алкилкарбоксилом; и/или
- фенилом, бифенилом и/или нафтилом, каждый из которых является необязательно замещенным одним или больше:
- C1-C6алкилом,
- атомом галогена,
- нитрилом,
- алкилокси,
- -COOR10, и/или
- C2-C12 алкилкарбоксилом,
где L, R8, R9 и R10 представляют собой, как определено в п.3.
19. Соединение по любому из пп.1-18, содержащее одно необязательно замещенное соединение ФОРМУЛЫ II.
20. Соединение по п.19, содержащее необязательно замещенное


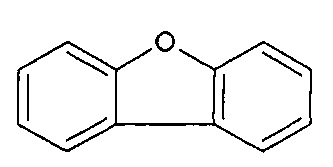
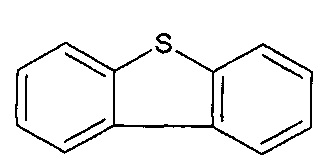





21. Соединение по п.20, содержащее необязательно замещенное



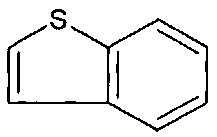
22. Соединение по п.20, содержащее необязательно замещенное
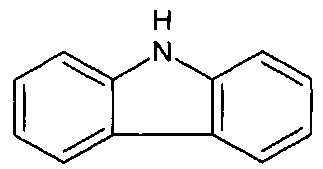


23. Соединение по п.20, содержащее необязательно замещенное


24. Соединение по п.20, содержащее необязательно замещенное



25. Соединение по п.20, содержащее необязательно замещенное


26. Соединение по любому из пп.1-18, содержащее две необязательно замещенные ФОРМУЛЫ II.
27. Соединение по п.26, содержащее необязательно замещенное


28. Соединение по п.26, содержащее необязательно замещенное



29. Соединение по любому из пп.1-18 представляет собой:






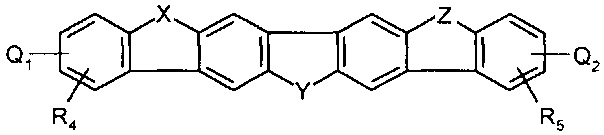
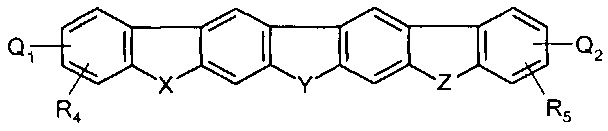

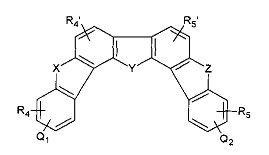
где:
- R4, R5, и являются необязательными и независимо представляют, в случает R4 и R5, от одного до четырех и, в случае и , один или два:
- C1-C12алкил или алкилокси, указанный алкил и алкилокси будут необязательно замещенные одним или более:
- -NR8R9,
- -O-L или -S-L, и/или
- фенилом, необязательно замещенным одним или более: C1-C6алкилом, атомом галогена, нитрилом, алкилокси, COOR10, и/или от C2 до C12алкилкарбоксилом;
- C4-C10циклоалкил, C2-C12алкенил, C4-C10циклоалкенил, C2-C12алкинил, C4-C10циклоалкинил, каждый из которых является необязательно замещенным алкилом и/или -O-L, и/или
- фенил, бифенил и нафтил, каждый из которых является необязательно замещенным одним или больше:
- C1-C6алкилом,
- галогеном,
- нитрилом,
- алкилокси,
- -COOR10, и/или
- C2-C12алкилкарбоксилом,
- Q1 и Q2 являются необязательными и независимо представляют от одной до четырех ацильных групп и/или группы сложного эфира оксима формулы
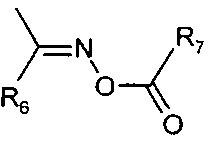
- каждый из X, Y и Z независимо представляют
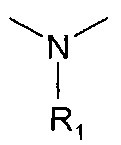



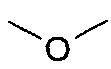


- R1, R2, и R3 каждый независимо представляет:
- атом водорода;
- C1-C12алкил, необязательно замещенный одним или более:
- -NR8R9,
- -O-L,
- -S-L, и/или
- фенилом, необязательно замещенным одним или более C1-C6алкилом, галогеном, нитрилом, алкилокси, -COOR10, и/или C2-C12алкилкарбоксилом;
- C4-C10 циклоалкил, C2-C12алкенил, C4-C10циклоалкенил, C2-C12алкинил, C4-C10циклоалкинил, каждый из которых является необязательно замещенным алкилом и/или -O-L, и/или
- фенил, бифенил или нафтил, каждый из которых является необязательно замещенным одним или больше:
- C1-C6алкилом,
- галогеном,
- нитрилом,
- алкилокси,
- -COOR10, и/или
- C2-C12алкилкарбоксилом,
- Q3 представляет собой атом водорода, ацильную группу, или группу сложного эфира оксима формулы:

- Q4 представляет собой сложный эфир оксима формулы:

- Ar представляет собой линкер -LK- как определено в одном из пп.15-17,
где L, R8, R9 и R10 представляют собой как определено в п.3, и где R6 и R7 представляют собой как определено в одном из пп.2-10.
30. Соединение по п.29 представляет собой:


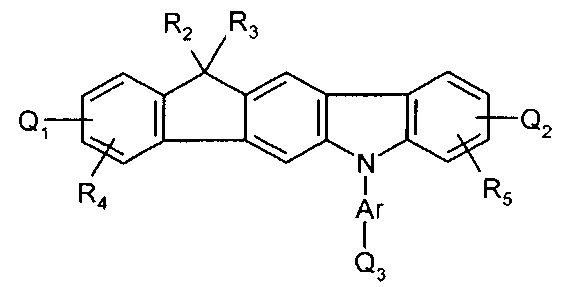
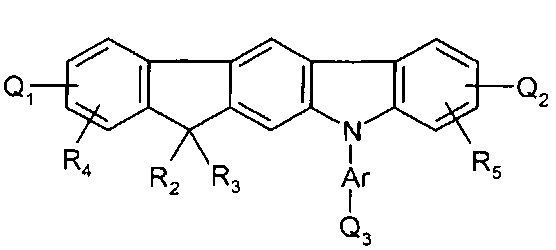








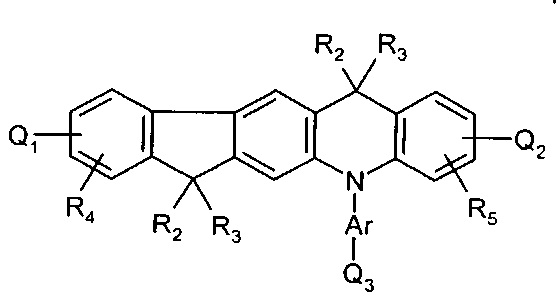



















где Q1, Q2, Q3, Q4, R1, R2, R3, R4, R5, и Ar представляют собой, как определено в п.29.
31. Соединение по п.29 или 30, где -Ar- представляет собой необязательно замещенный арилен, указанный арилен, необязательно содержит один или больше атом кислорода, атом серы, атом азота, карбонильную группу, карбаматную группу, карбамидную группу и/или сложноэфирную группу.
32. Соединение по п.31, где заместителями арилена являются один или больше:
- C1-C12алкил, необязательно замещенный одним или более:
- -NR8R9,
- -O-L,
- -S-L,
- фенил, необязательно замещенный одним или более: C1-C6алкилом, галогеном, нитрилом, алкилокси, COOR10, и/или C2-C12алкилкарбоксилом;
- C4-C10циклоалкил, C2-C12алкенил, C4-C10циклоалкенил, C2-С12алкинил, C4-С10циклоалкинил, каждый из которых является необязательно замещенным алкилом и/или -O-L, и/или
- фенил, бифенил и нафтил, каждый из которых является необязательно замещенным одним или больше:
- C1-C6алкилом,
- галогеном,
- нитрилом,
- алкилокси,
- -COOR10, и/или
- C2-C12алкилкарбоксилом.
где L, R8, R9 и R10 представляют собой как определено в п.3.
33. Соединение по любому из пп.29-32, где каждый -Ar-Q3 независимо представляет собой




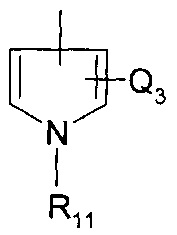


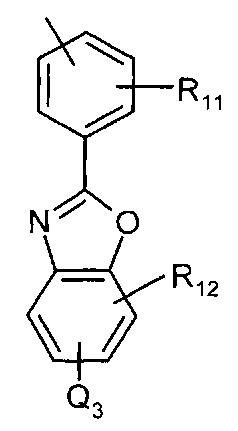



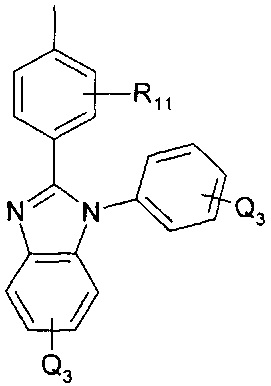

где R11 и R12 являются необязательными и независимо представляют один или больше:
- C1-C12алкил, необязательно замещенный одним или более:
- -NR8R9,
- -O-L,
- -S-L, и/или
- фенилом, необязательно замещенным одним или более:
- C1-C6алкилом, галогеном, нитрилом, алкилокси, COOR10, и/или C2-C12алкилкарбоксилом;
- C4-C10циклоалкил, C2-C12алкенил, C4-C10циклоалкенил, C2-C12алкинил и/или C4-C10циклоалкинил, каждый из которых является необязательно замещенным алкилом и/или -O-L; и/или
- фенил, бифенил и нафтил, каждый из которых является необязательно замещенным одним или больше:
- C1-C6алкилом,
- галогеном,
- нитрилом,
- алкилокси,
- -COOR10, и/или
- C2-C12алкилкарбоксилом.
где L, R8, R9 и R10 представляют собой как определено в п.3.
34. Соединение по любому из пп.29-33 представляет собой:








или

где:
- R4 и R5 являются необязательными и независимо представляют один C1-C12алкил или C1-C12алкилокси,
- Q1 и Q2 являются необязательными и независимо представляют одну группу сложного эфира оксима формулы

- R1, R2 и R3 каждый независимо представляет атом водорода или C1-C12алкил,
- Q3 представляет собой атом водорода или группу сложного эфира оксима формулы:

- Q4 представляет собой сложный эфир оксима формулы:
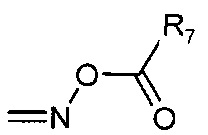
- Ar представляет собой

- R6 и R7 независимо представляет собой алкил.
35. Соединение по п.34 представляет собой:










36. Соединение по п.26, представляет собой труксен, труксенон, триазатруксен или их производное, указанные труксен, труксенон, триазатруксен или их производные имеют прикрепленный к нему, прямо или косвенно, по крайней мере, одну ацильную группу и/или группу сложного эфира оксима.
37. Соединение по п.36 представляет собой:
труксен:
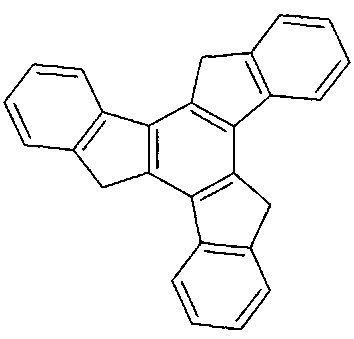
труксенон:

триазатруксен:

или их производные,
труксен, труксенон, триазатруксен или их производные имеют прикрепленные к ним, по крайней мере, один -E1, -LK-E1, -LK-(E1)2 или =E2,
-E1 представляет собой ацильную группу формулы -C(=O)-R30 или группу сложного эфира оксима формулы -CR6=N-O-(C=O)-R7, и =E2 представляет собой группу сложного эфира оксима формулы =N-O-(C=O)-R7,
где LK представляет собой как определено в одном из пп.15-17, R6 и R7 представляет собой как определено в одном из пп.2-10 и R30 представляет собой как определено в одном из пп.11-14.
38. Соединение по пп.36 или 37 представляет собой формулу:
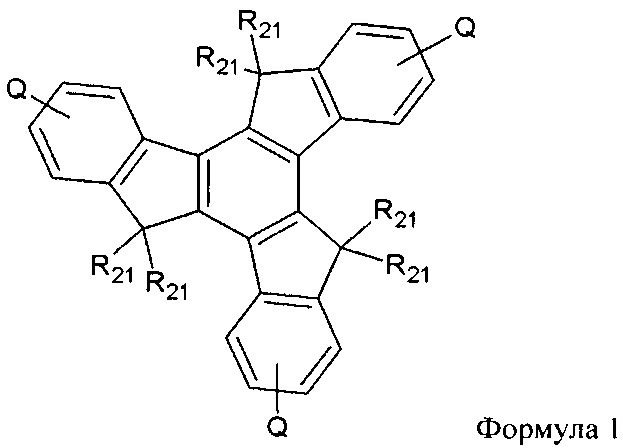


где:
каждый Q независимо представляет собой от 1 до 4:
- водород;
- -Е1;
- -LK-E1;
- -LK-(E1)2;
- C1-C12алкил, необязательно замещенный одним или более -NR19R20, -O-L и/или -S-L;
- C1-C12галогеналкил;
- C4-C8циклоалкенил;
- C2-C12алкинил;
- фенил или -N(R19)-фенил, каждый из которых является необязательно замещенным одним или больше C1-C6алкилом, галогеном, нитрилом, алкилокси, -COOR19, и/или C2-C12алкилкарбоксилом;
- бензоил, нафтил, фенилоксикарбонил, или нафтилоксикарбонил, каждый из которых является необязательно замещенным одним или больше C1-C20алкилом, C1-C4галогеналкилом, -SR19, -OR19, -NR19R20, галогеном, фенилом, -COOR19, -CONR19R20, -CN, -NO2 и/или C3-C10циклоалкилом, где C3-C10циклоалкил может быть прерван -O-, -(С=O)- или -N(R19)-;
- -NR16R17; и/или
- тиофенкарбонил или пирролидинил, каждый из которых является необязательно замещенным одним или больше C1-C6алкилом, галогеном, нитрилом, алкилокси, -COOR19, и/или C2-C12алкилкарбоксилом, и каждый R21 независимо представляет собой:
- водород;
- -E1;
- -LK-E1;
- -LK-(E1)2;
- C1-C12алкил, необязательно замещенный одним или более -NR19R20, -O-L и/или -S-L;
- C4-C8циклоалкенил;
- C2-C12алкинил; или
- фенил, необязательно замещенный одним или более C1-C6алкилом, нитрилом, алкилокси, -COOR16, и/или C2-C12алкилкарбоксилом, и/или два R21 прикрепленных к одному и тому же атому углерода представляют собой =O или =Е2,
где:
L представляет собой атом водорода или C1-C6алкил,
R16 и R17 независимо представляют:
- водород,
- C1-C12алкил, необязательно замещенный одним или более -NR19R20, -O-L и/или -S-L;
- C4-C10циклоалкил;
- C4-C10циклоалкенил;
- C2-C12алкинил;
- C1-C12галогеналкил; или
- фенил или бензоил, каждый из которых необязательно замещенный одним или более C1-C6алкилом, галогеном, нитрилом, алкилокси, -COOR19, и/или C2-C12алкилкарбоксильной группой, и
R19 и R20 независимо представляют собой водород, C1-C12алкил; C1-C12галогеналкил; C4-C8циклоалкенил; или C2-C12алкинил, при условии, что соединение содержит, по крайней мере, один сложный эфир оксима или ацильную группу, и при условии, что когда R21 является прикрепленным к атому азота и R21 представляет собой -E1, -E1 не является -CR6=N-O-(C=O)-R7.
39. Соединение по п.38 представляет собой формулы:

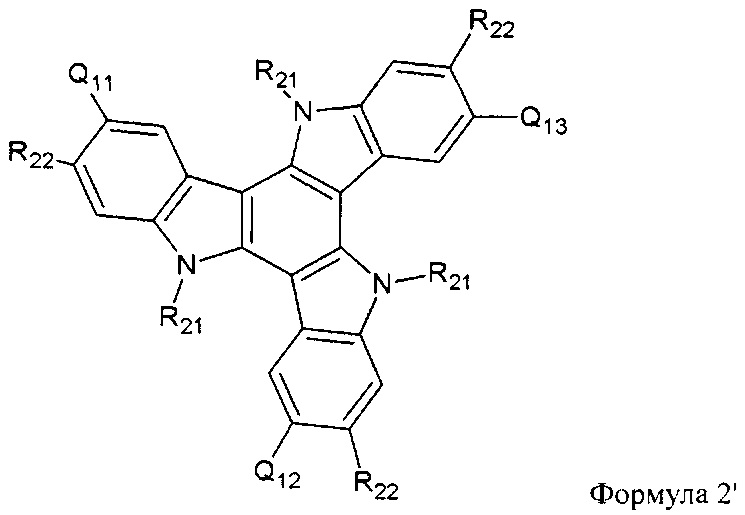

где:
каждый из Q11, Q12 и Q13 независимо представляют:
- водород;
- -E1;
- -LK-E1;
- -LK-(E1)2;
- C1-C12алкил, необязательно замещенный одним или более -NR19R20, -O-L и/или -S-L;
- C1-C12галогеналкил;
- C4-C8циклоалкенил;
- C2-C12алкинил;
- фенил или -N(R19)-фенил, каждый из которых является необязательно замещенным одним или больше C1-C6алкилом, галогеном, нитрилом, алкилокси, -COOR19, и/или C2-C12алкилкарбоксилом;
- бензоил, нафтил, фенилоксикарбонил или нафтилоксикарбонил, каждый из которых является необязательно замещенным одним или больше C1-C20алкилом, C1-C4галогеналкилом, -SR19, -OR19, -NR19R20, галогеном, фенилом, -COOR19, -CONR19R20, -CN, -NO2 и/или C3-C10циклоалкилом, где C3-C10циклоалкил может быть прерван -O-, -(С=O)- или -N(R19)-;
- -NR16R17; или
- тиофенкарбонил или пирролидинил, каждый из которых является необязательно замещенным одним или больше C1-C6алкилом, галогеном, нитрилом, алкилокси, -COOR19, и/или C2-C12алкилкарбоксилом,
каждый R22 независимо представляет собой:
- водород;
- C1-C12алкил, необязательно замещенный одним или более -NR19R20, -O-L и/или -S-L;
- C1-C12галогеналкил;
- C4-C8циклоалкенил;
- C2-C12алкинил;
- фенил или -N(R19)-фенил, каждый из которых является необязательно замещенным одним или больше C1-C6алкилом, галогеном, нитрилом, алкилокси, -COOR19, и/или C2-C12алкилкарбоксилом; или
- бензоил, нафтил, фенилоксикарбонил или нафтилоксикарбонил, каждый из которых является необязательно замещенным одним или больше C1-C20алкилом, C1-C4галогеналкилом, -SR19, -OR19, -NR19R20, галогеном, фенилом, -COOR9, -CONR19R20, -CN, -NO2 и/или C3-C10циклоалкилом, где C3-C10циклоалкил является прерванным -O-, -(С=O)- или -N(R19)-,
где R16, R17, R19, R20, R21 и L представляют собой как определено в п.38, при условии, что соединение содержит, по крайней мере, один сложный эфир оксима или ацильную группу, и при условии, что когда R21 является прикрепленным к атому азота и R21 представляет собой -Е1, -E1 не является -CR6=N-O-(C=O)-R7.
40. Соединение согласно п.38 или 39, где -LK-E1 представляет собой:









или

где R18 представляет собой водород или C1-C12алкил, необязательно замещенный одним или более -O-L и/или -S-L, и
где L, R16 и R17 представляют собой как определено в п.38.
41. Соединение по любому из пп.38-40, где
- каждый Q, Q1, Q2, и Q3, когда присутствует, представляет собой один -E1 формулы -CR6=N-O-(C=O)-R7, где R6 представляет собой C1-C12алкил, необязательно замещенный -O-L, где L представляет собой C1-C6алкил, и R7 представляет собой C1-C12алкил;
- все R22, когда присутствуют, представляют водород; и
- все R21, когда присутствуют, представляют водород или C1-C12алкил.
42. Соединение по любому из пп.38-40, где:
- каждый Q, Q11, Q12, и Q13, когда присутствует, представляет собой один -LK-E1, где E1 представляет собой формулу -CR6=N-O-(C=O)-R7, где R6 представляет собой C1-C12алкил, необязательно замещенный -O-L, где L представляет собой C1-C6алкил, и R7 представляет собой C1-C12 алкил;
- все R22, когда присутствуют, представляют водород;
- все R21, когда присутствуют, представляют водород или C1-C12алкил; и
- LK представляет собой




43. Соединение по любому из пп.38-40, где каждый из Q11, Q12, и Q13, когда присутствует, представляет собой водород, каждый из Q и R22, когда присутствует, представляет собой один -N(R19)-фенил, где R19 представляет собой C1-C12алкил, и каждая пара R21 прикрепленная к общему атому углерода представляет =E2, где R7 представляет собой C1-C12алкил.
44. Соединение по любому из пп.38-40, где
- каждый Q, Q1, Q2 и Q3, когда присутствует, представляет собой один -LK-E1 или -E1, где E1 представляет собой формулы -C(=O)-R30, где R30 представляет собой C1-C12 линейный алкил, фенил, фенил, замещенный алкилом или алкилокси, или тиофенил;
- все R22, когда присутствуют, представляют собой водород;
- все R21, когда присутствуют, представляют собой C1-C12алкил, и
- -LK- представляет собой 2-фенилен или 4-фенилен.
45. Соединение по любому из пп.36-40 представлено формулами:












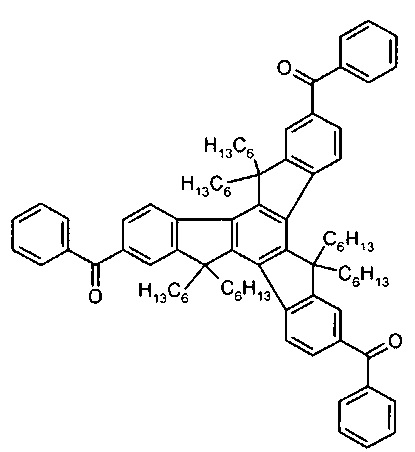



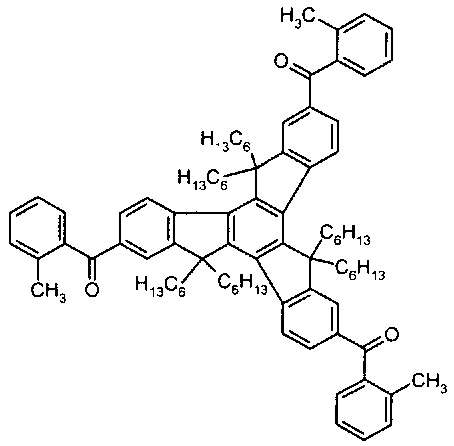
46. Соединение по любому из пп.1-45 для применения как фотоинициатор в фотополимеризуемой композиции.
47. Соединение по любому из пп.1-45 является содержащимся в фотополимеризуемой композиции.
48. Соединение по п.46 или 47, где фотополимеризуемая композиция представляет собой композицию офсетной печатной формы.
49. Соединение по п.46 или 47, где фотополимеризуемая композиция представляет собой резистную композицию цветного фильтра.
50. Соединение по п.46 или 47, где фотополимеризуемая композиция представляет собой полимерную композицию черной матрицы.
51. Соединение по п.46 или 47, где фотополимеризуемая композиция представляет собой фотонабор или фотоотверждаемые чернила.
52. Соединение по п.46 или 47, где фотополимеризуемой композицией является фотонабор для продувки кислородом.
53. Фотополимеризуемая композиция, содержащая соединение по одному из пп.1-45.
54. Фотополимеризуемая композиция по п.53, которая является композицией офсетной печатной формы.
55. Фотополимеризуемая композиция по п.53, которая является резистной композицией цветного фильтра.
56. Фотополимеризуемая композиция по п.53, которая является полимерной композицией черной матрицы.
57. Фотополимеризуемая композиция по п.53, которая является фотонабором или фотоотверждаемыми чернилами.
58. Фотополимеризуемая композиция по п.53, которая является фотонабором для продувки кислородом.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Соединения изобретения
[0009] Обращаясь теперь к соединению более подробно, тут предусмотрено соединение, содержащее необязательно замещенное
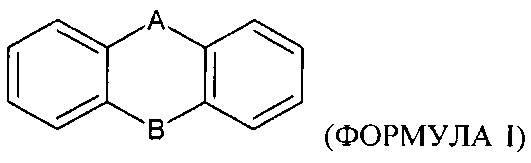

[0010] В ФОРМУЛЕ I, В может представлять связь, так что Формула также представляет собой соединения формулы



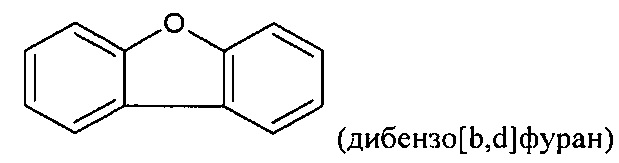













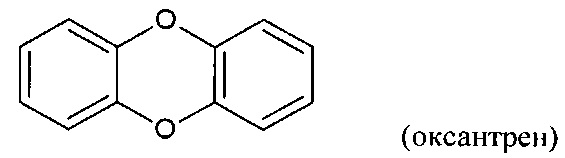

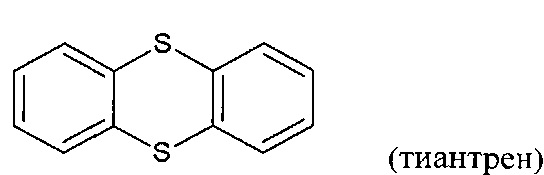
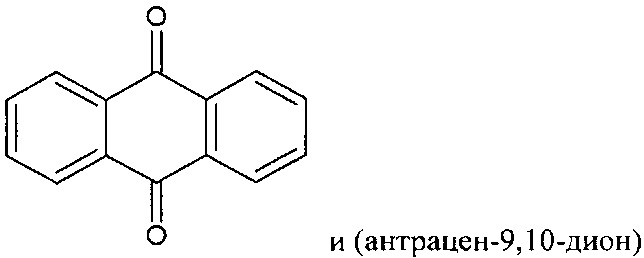
[0011] Подобным образом, ФОРМУЛА II включает:




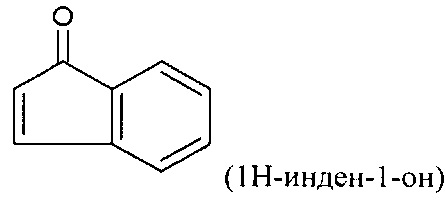
[0012] В соединении согласно изобретению ФОРМУЛА I является сопряженной с одной или двумя ФОРМУЛАМИ II. Тут, ФОРМУЛА I, будучи сопряженной с ФОРМУЛОЙ II, означает, что одно кольцо формулы I будет разделять связь с одним кольцом ФОРМУЛЫ II с образованием фенил /5-членное кольцо/ фенил структура, как, например, в следующем соединении:

[0013] Связи, которые участвуют в образовании ФОРМУЛЫ I с первой ФОРМУЛОЙ II, являются те, которые отмечены звездочками в следующих формулах:









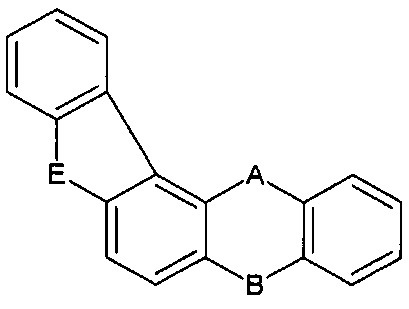



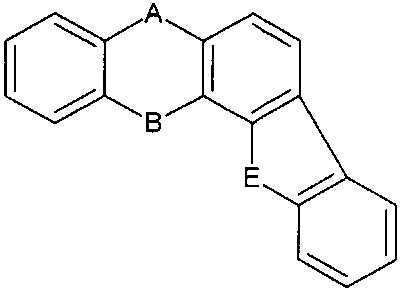
[0014] Когда вторая ФОРМУЛА II присутствует, то она может быть такой же или отличаться от первой ФОРМУЛЫ II. Также она может быть сопряженной с одной из двух фенильной группой формулы I или с фенильной группой первой ФОРМУЛЫ II. Например, для последних ФОРМУЛЫ I-ФОРМУЛЫ II структура показана в предыдущем параграфе, вторая ФОРМУЛА II может быть объединена при следующем расположении:

[0015] Снова, вторая ФОРМУЛА II является конденсированной, таким образом формируя фенил /5-членное кольцо/, фенильная структура. Следовательно, для каждого из ФОРМУЛЫ I-ФОРМУЛЫ II структуры, показанной в предыдущем параграфе, там есть 14 различных путей конденсирования второй ФОРМУЛЫ II. Эти 14 путей показаны ниже для последних ФОРМУЛЫ I - ФОРМУЛЫ II структур только предыдущего параграфа; специалист в данной области техники поймет из этого примера, как сконденсировать вторую ФОРМУЛУ II на любой из вышеуказанных структур ФОРМУЛЫ I - ФОРМУЛЫ II. Эти 14 путей тут:





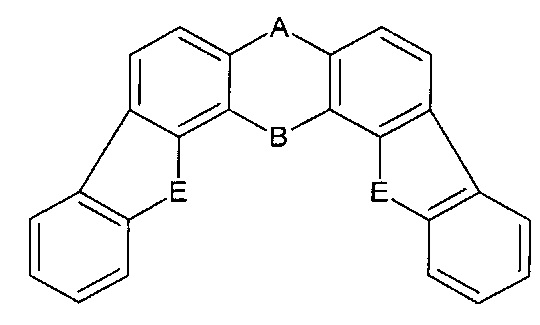






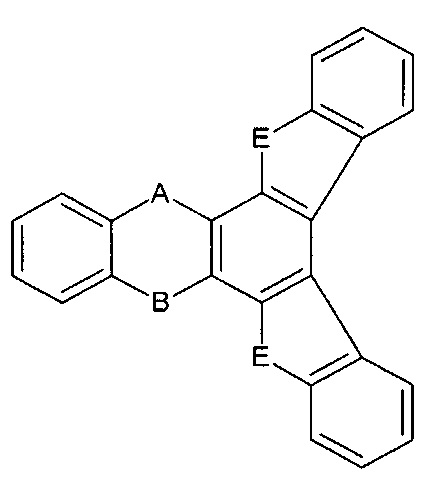

[0016] Следует отметить, что когда B представляет собой связь, последняя структура предыдущего параграфа соответствует труксен-подобным соединениям. В вариантах осуществления изобретения, соединение представляет собой труксен (то есть когда В представляет собой связь и A и E представляют собой -CH2-), труксенон (то есть когда В представляет собой связь и A и E представляют собой -С(=O)-), триазатруксен (то есть когда B представляет собой связь и A и E представляют собой -NH-), или их производные.
[0017] Для большей определенности, здесь, "труксен" относится к соединению формулы:


[0018] Тут, труксенон относится к соединении формулы:


[0019] Тут, "триазатруксен" относится к соединению, также известному как 5,10,15-триазатруксен, которое представляет собой формулы:


[0020] Труксен, труксенон и триазатруксен имеют CAS номера 548-35-6, 4430-15-3 и 109005-10-9 соответственно.
[0021] Варианты осуществления, в которых объединенные формулы I с двумя ФОРМУЛАМИ II вырабатывают труксен, труксенон, триазатруксен и их производные, будут обсуждаться дополнительно ниже после общего обсуждения соединений согласно изобретению.
[0022] В соединениях изобретения, ФОРМУЛА I и ФОРМУЛА II являются "необязательно замещенными". Это означат, что один или больше атомов водорода формулы I и/или ФОРМУЛА II (включая атомы водорода в A, B и E группах) могут быть заменены заместителями. Природа этих заместителей не имеет решающего значения для изобретения, если они не предотвращают соединение изобретения в качестве фотоинициатора.
[0023] В вариантах осуществления, ФОРМУЛА I и ФОРМУЛА II представляют собой необязательно замещенную одним или больше:
- C1-C12алкилом, C1-C12алкилокси, C4-C10циклоалкилом, C1-C12алкенилом, C4-C10циклоалкенилом, C4-C10циклоалкенилом, C2-C12алкинилом и/или C4-C10циклоалкинилом, каждый из которых является необязательно замещенным одним или больше:
- NR8R9,
- -O-L,
- -S-L, и/или
- фенилом, необязательно замещенным одним или более C1-C6алкилом, атомом галогена, нитрилом, алкилокси, COOR10 и/или C2-C12алкилкарбоксилом; и/или
- фенилом, бифенилом и/или нафтилом, каждый из которых является необязательно замещенным одним или больше:
- C1-C6алкилом,
- атомом галогена,
- нитрилом,
- алкилокси,
- -COOR10, и/или
- C2-C12алкилкарбоксилом,
где L представляет собой атом водорода или C1-C6алкил, и где каждый из R8, R9 и R10 представляет собой независимо атом водорода, C1-C12алкил; C4-C10 циклоалкил; C1-C12алкенил; C4-C10циклоалкенил; C2-C12алкинил; C4-C10циклоалкинил; C1-C12галогеналкил или необязательно замещенный арил, такой как незамещенный или замещенный фенил и нафтил. В вариантах осуществления, необязательно замещенный арил является замещенным алкилом или алкилокси.
[0024] В более конкретных вариантах осуществления, один или более этих заместителей расположены на фенильных кольцах ФОРМУЛЫ I и ФОРМУЛЫ II, которые не участвуют в объединении между ФОРМУЛОЙ I и ФОРМУЛОЙ II. Например, это будут фенильные кольца, окруженные следующей Формулой:

[0025] В этом же или других вариантах осуществления, один или больше этих заместителей расположены на углероде и атомах азота A, B и E групп. Следовательно, один или оба атомов водорода -CH2- в A, B и E могут независимо заменить такой заместитель. Кроме того, атом водорода -NH- в A, B и E может быть заменен таким заместителем.
[0026] В этом же или других вариантах осуществления, один или больше из указанных выше заместителей размещены на фенильных кольцах, которые включены в объединенные между ФОРМУЛОЙ I и ФОРМУЛОЙ II (это было бы фенильное кольцо, которое не отмечено выше, например). Там может быть от нуля до двух заместителей на фенильное кольцо.
[0027] Соединения по изобретению приложены к ней, прямо или косвенно, по крайней мере, к одному сложному эфиру оксима и/или ацильной группе. Здесь "имеющий прикрепленные к нему" означает, что один или два атома водорода на углероде или атом азота соединения (включая атомы водорода в A, B и E групп) размещен на сложном эфире оксима или ацильной группе.
[0028] Группы сложного эфира оксима и ацильные группы могут быть напрямую или косвенно прикрепленными. Здесь "прямо или косвенно прикрепленные" означает, что здесь может быть линкер (-LK-) между этой группой и ФОРМУЛОЙ I или ФОРМУЛОЙ II. Когда такой линкер присутствует, группа называется косвенно прикрепленной, в ином случае это непосредственно прикрепленная группа.
[0029] В вариантах осуществления, -LK- представляет собой необязательно замещенный алкилен, циклоалкилен, алкенилен, циклоалкенилен, алкинилен, циклоалкинилен, арилен, -S-арилен, -NH-арилен, или -N(арил)-арилен, каждый из которых необязательно содержит один или больше атомов кислорода, атомов серы, атомов азота, карбонильную группу, карбаматную группу, карбамидную группу, и/или сложноэфирную группу. Природа заместителей этих радикалов не является существенной для изобретения до тех пор, пока они не предотвращают соединение изобретения от воздействия в качестве фотоинициатора. Эти заместители могут замещать любые атомы водорода этих групп, в том числе включая атом водорода, который присоединен к атому азота в -NH-арилене. В вариантах осуществления, эти заместители представляют собой одну или более:
- полиэтиленгликолевую цепь,
- C1-C12алкил, необязательно замещенный одним или более:
- -NR8R9,
- -O-L,
- -S-L, и/или
- фенилом, необязательно замещенным одним или более: C1-C6алкилом, галогеном, нитрилом, алкилокси, COOR10, и/или C2-C12алкилкарбоксилом;
- C4-C10циклоалкил, C2-C12алкенил, C4-C10циклоалкенил, C2-C12алкинил, C4-C10циклоалкинил, каждый из которых является необязательно замещенным алкилом и/или -O-L, и/или
- арил, такой как фенил, бифенил и нафтил, или арилоил, такой как бензоил, каждый из которых является необязательно замещенным одним или больше:
- C1-C6алкилом,
- галогеном,
- нитрилом,
- алкилокси,
- -COOR10, и/или
- C2-C12алкилкарбоксилом.
где L, R8, R9 и R10 являются такими, как определено выше.
[0030] В вариантах осуществления, в которых линкер -LK- служит для присоединения ацильной группы, -LK- представляет собой арилен, такой как фенилен.
[0031] Здесь, группа сложного эфира оксима представляет собой -CR6=N-O-(C=O)-R7 или =N-O-(C=O)-R7, где R6 и R7 являются такими же или различными заместителями.
[0032] Природа группы R6 не является решающей для изобретения до тех пор, пока не предотвращает соединение изобретения к воздействию в качестве фотоинициатора. В вариантах осуществления, R6 представляет собой:
- водород;
- C1-C12алкил, необязательно замещенный одним или более:
- фенилом,
- галогеном,
- -NR9R10,
- -O-L, и/или
- -S-L;
- C4-C10циклоалкил, C2-C12алкенил, C4-C10циклоалкенил, C2-C12алкинил или C4-C10циклоалкенил, каждый из которых является необязательно замещенным алкилом и/или -O-L; или
- фенил, необязательно замещенный одним или более:
- C1-C6алкилом,
- галогеном,
- нитрилом,
- алкилокси,
- -COOR10, и/или
- C2-C12алкилкарбоксилом,
где L, R8, R9 и R10 являются такими, как определено выше.
[0033] В вариантах осуществления, представляет собой алкил необязательно замещенный -O-C1-C6алкилом. В более специфических вариантах осуществления R6 представляет собой метил или бутил. В вариантах осуществления, R6 представляет собой метил.
[0034] В группах сложного эфира оксима, группа R7 связана с производством свободных радикалов. Следовательно, она не будет содержать кислород, азот или атом серы, так как эти атомы гасят свободные радикалы. Также, более маленькие группы R7, хотя это и не существенно, являются предпочтительными, так как они имеют более высокие уровни диффузии и, следовательно, приводят к более быстрой полимеризации.
[0035] В вариантах осуществления, R7 представляет собой алкил, циклоалкил, алкенил, или циклоалкенил, каждый из которых является необязательно замещенным арилом или галогеном, или R7 представляет собой арил, необязательно замещенный алкилом или галогеном. В специфических вариантах осуществления, R7 представляет собой C1-C12алкил, необязательно замещенный фенилом; C4-C10циклоалкилом; или фенил, необязательно замещенный C1-C6алкилом. В вариантах осуществления, R7 представляет собой C1-C12алкил; C4-C10 циклоалкил; или фенил. В вариантах осуществления, R7 представляет собой метил.
[0036] Существует два варианта, при которых группа сложного эфира оксима может быть присоединена к ФОРМУЛЕ I или ФОРМУЛЕ II. Первый, когда группа сложного эфира оксима замещает два атома водорода, прикрепленные к такому же атому углерода в ФОРМУЛЕ I или ФОРМУЛЕ II, группа сложного эфира оксима может быть =N-O-(C=O)-R7, в которой атом азота (=N) является непосредственно прикрепленным посредством двойной связи к атому углерода (ФОРМУЛЫ I или ФОРМУЛЫ II) так, чтобы быть несущим два атома водорода. Второй, когда группа сложного эфира оксима замещает только один атом водорода на азот или атом углерода в ФОРМУЛЕ I или ФОРМУЛЕ II, группа сложного эфира оксима будет представлять собой -CR6=N-O-(C=O)-R7. В этом случае, группа сложного эфира оксима может быть присоединена непосредственно к атому, который будет несущим атом водорода, или она может быть присоединена к линкеру (-LK-), который сам присоединен к этому атому (то есть она может быть присоединена косвенно).
[0037] Следует отметить, что первый атом углерода группы сложного эфира оксима (то есть атом углерода, несущий группу R6 и тот, который подчеркнут в следующем звене -CR6=N-O-(C=O)-R7) должен предпочтительно быть присоединен к атому углерода ФОРМУЛЫ I или ФОРМУЛЫ II, скорее, чем к кислороду, азоту или атому серы, с целью увеличения термальной стабильности соединения. Следовательно, когда группа сложного эфира оксима замещает атом водорода на атом азота, оптимально должен быть использован линкер. Также, во всех случаях, где используется линкер, атом этого линкера, который является связанным с первым атомом углерода группы сложного эфира оксима как определено выше, должен оптимально быть атомом углерода. В противном случае, природа линкера не является существенной для изобретения.
[0038] Здесь, ацильная группа представляет собой группу формулы -С(=O)-R30, где R30 является заместителем. Природа R30 не является существенной для изобретения до тех пор, пока он не предотвращает соединение изобретения от воздействия в качестве фотоинициатора.
[0039] В вариантах осуществления, R30 представляет собой необязательно замещенный алкил, циклоалкил, алкенил, циклоалкенил, алкинил, циклоалкинил или арил, каждый из которых необязательно содержит один или больше атомов кислорода, атом серы, атом азота, карбонильную группу, карбаматную группу, карбамидную группу, и/или сложноэфирную группу. Природа заместителей этих радикалов не является существенной до тех пор, пока они не предотвращают соединение изобретения от воздействия в качестве фотоинициатора. В вариантах осуществления, эти заместители представляют собой один или более:
- полиэтиленгликолевую цепь,
- C1-C12алкил, необязательно замещенный одним или более:
- -NR8R9,
- -O-L,
- -S-L, и/или
- фенилом, необязательно замещенным одним или более: C1-C6алкилом, галогеном, нитрилом, алкилокси, COOR10, и/или C2-C12алкилкарбоксилом;
- C4-C10циклоалкил, C2-C12алкенил, C4-C10циклоалкенил, C2-C12алкинил, C4-C10циклоалкинил, каждый из которых является необязательно замещенным алкилом и/или -O-L, и/или
- арил, такой как фенил, тиофенил, бифенил и нафтил, каждый из которых является необязательно замещенным одним или больше:
- C1-C6алкилом,
- галогеном,
- нитрилом,
- алкилокси,
- -COOR10, и/или
- C2-C12алкилкарбоксилом.
где L, R8, R9 и R10 являются такими, как определено выше.
[0040] В варианте воплощения, R30 представляет собой алкил, фенил или тиофенил, все из которых являются необязательно замещенным линейным алкилом или -O-L.
[0041] В варианте воплощения, R30 представляет собой метил, 2-метилфенил, фенил, тиофенил, или 4-метоксифенил.
[0042] Здесь, "по крайней мере, один сложный эфир оксима и/или ацильная группа" подразумевает, что несколько атомов водорода в ФОРМУЛЕ I и/или ФОРМУЛЕ II могут быть замещены несколькими группами сложного эфира оксима, несколькими ацильными группами, или комбинацией групп сложного эфира оксима и ацильных групп (каждая будет либо непосредственно, либо косвенно присоединена). Каждая ФОРМУЛА I и/или ФОРМУЛА II имеет прикрепленный к ней один или больше, чем один сложный эфир оксима и/или ацильную группу, некоторые из этих групп могут быть прикреплены непосредственно, а другие прикреплены косвенно. В дополнение, различные косвенно присоединенные группы не должны быть прикрепленными с использованием идентичных линкеров (-LK-).
[0043] В вариантах осуществления, соединение изобретения имеет прикрепленные к ней прямо или косвенно, одну, две или три группы сложного эфира оксим или одну, две или три ацильные группы. В вариантах осуществления, соединение изобретения имеет прикрепленные к нему, прямо или косвенно, две или больше групп сложного эфира оксима или две или больше ацильных групп. В вариантах осуществления, соединение изобретения имеет прикрепленные к нему, прямо или косвенно, три группы сложного эфира оксима или три ацильные группы.
[0044] В более конкретных вариантах осуществления, сложный эфир оксима и ацильные группы являются расположенными на фенильных кольцах ФОРМУЛЫ I и ФОРМУЛЫ II, которые не участвуют в объединении между ФОРМУЛОЙ I и ФОРМУЛОЙ II. Например, это будет фенильным кольцом, окруженном следующей Формулой:

[0045] В том же или другом варианте осуществления, один или больше сложных эфиров оксима или ацильных групп расположены на фенильных кольцах, которые участвуют в объединении между ФОРМУЛОЙ I и ФОРМУЛОЙ II (это было бы не фенильное кольцо, которое не окружено в приведенном выше примере).
[0046] В этих и других вариантах осуществления, сложный эфир оксима и/или ацильные группы могут быть расположены на углероде и атомах азота A, B и E групп. Следовательно, один или оба атома водорода -CH2- в A, B и E могут быть независимо замещены такой группой. Также, атом водорода -NH- в A, B и E может быть заменен на сложный эфир оксима или ацильную группу.
[0047] В вариантах осуществления, ФОРМУЛА I представляет собой необязательно замещенное соединение





и ФОРМУЛА II представляет собой необязательно замещенное



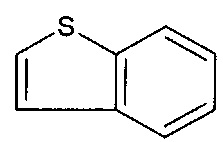
[0048] В вариантах осуществления, ФОРМУЛА I представляет собой необязательно замещенное
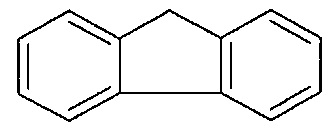



[0049] В вариантах осуществления, ФОРМУЛА I представляет собой необязательно замещенное


[0050] В вариантах осуществления, ФОРМУЛА I представляет собой необязательно замещенное

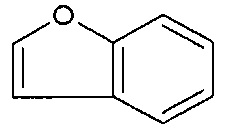
[0051] В вариантах осуществления, ФОРМУЛА I представляет собой необязательно замещенное

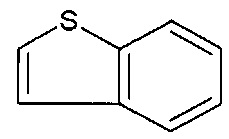
[0052] В вариантах осуществления, ФОРМУЛА I представляет собой необязательно замещенное


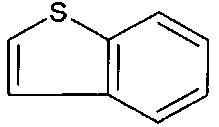
[0053] В вариантах осуществления, ФОРМУЛА I представляет собой необязательно замещенное


[0054] В вариантах осуществления, ФОРМУЛА I представляет собой необязательно замещенное


[0055] В вариантах осуществления, ФОРМУЛА I представляет собой необязательно замещенное
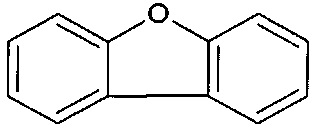

[0056] В вариантах осуществления, ФОРМУЛА I представляет собой необязательно замещенное

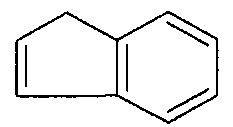
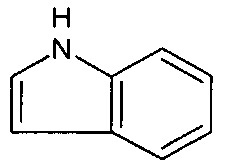
[0057] В вариантах осуществления, ФОРМУЛА I представляет собой необязательно замещенное


[0058] В вариантах осуществления, ФОРМУЛА I представляет собой необязательно замещенное
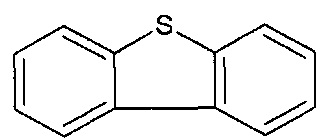

[0059] В вариантах осуществления, ФОРМУЛА I представляет собой необязательно замещенное
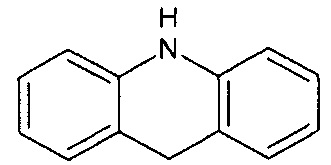

[0060] В вариантах осуществления, соединение содержит необязательно замещенное соединение



[0061] В вариантах осуществления, соединение содержит необязательно замещенное



[0062] В вариантах осуществления, соединение представляет собой:






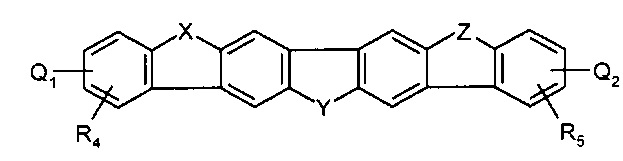



где:
- R4, R5, и являются необязательными и независимо представляют собой, в случае R4 и R5, от одного до четырех и, в случае и , один или два:
- C1-C12 алкил или алкилокси, указанный алкил и алкилокси являются необязательно замещенными одним или более:
- -NR8R9,
- -O-L или -S-L, и/или
- фенилом, необязательно замещенным одним или более: C1-C6алкилом, атомом галогена, нитрилом, алкилокси, COOR10, и/или от C2 до C12алкилкарбоксилом;
- C4-C10циклоалкил, C2-C12алкенил, C4-C10циклоалкенил, C2-C12алкинил, C4-C10циклоалкинил, каждый из которых является необязательно замещенным алкилом и/или -O-L, и/или
- фенил, бифенил и нафтил, каждый из которых является необязательно замещенным одним или больше:
- C1-C6алкилом,
- галогеном,
- нитрилом,
- алкилокси,
- -COOR10, и/или
- C2-C12алкилкарбоксилом,
где L, R8, R9 и R10 представляют собой как определено выше,
- Q1 и Q2 являются необязательными и независимо представляют от одной до четырех ацильных групп и/или группы сложного эфира оксимов формулы

- каждый из X, Y и Z независимо представляет собой






- R1, R2, и R3 каждый независимо представляет собой:
- атом водорода;
- C1-C12 алкил, необязательно замещенный одним или более:
- -NR8R9,
- -O-L,
- -S-L, и/или
- фенилом, необязательно замещенным одним или более C1-C6алкилом, галогеном, нитрилом, алкилокси, -COOR10, и/или C2-C12алкилкарбоксилом;
- C4-C10циклоалкил, C2-C12алкенил, C4-C10циклоалкенил, C2-C12алкинил, C4-C10циклоалкинил, каждый из которых является необязательно замещенным алкилом и/или -O-L, и/или
- фенил, бифенил или нафтил, каждый из которых является необязательно замещенным одним или больше:
- C1-C6алкилом,
- галогеном,
- нитрилом,
- алкилокси,
- -COOR10, и/или
- C2-C12алкилкарбоксилом,
где L, R8, R9 и R10 представляют собой как определено выше,
- Q3 представляет собой атом водорода, ацильную группу или группу сложного эфира оксима формулы:

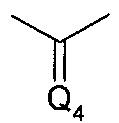
- Q4 представляет собой сложный эфир оксима формулы:

- -Ar- представляет собой линкер -LK- как определено выше и в более конкретных вариантах осуществления, необязательно замещенный арилен как определено выше в отношении -LK-,
при условии, что соединение содержит, по крайней мере, одну ацильную или группу сложного эфира оксима.
[0063] В более конкретных вариантах осуществления, соединение представляет собой:
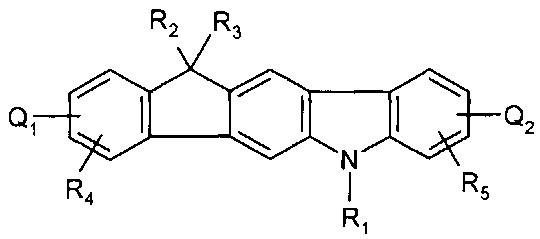
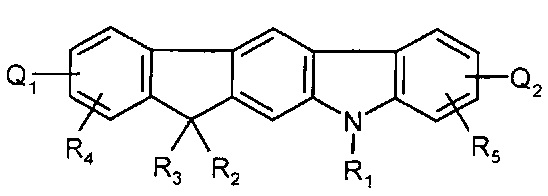


















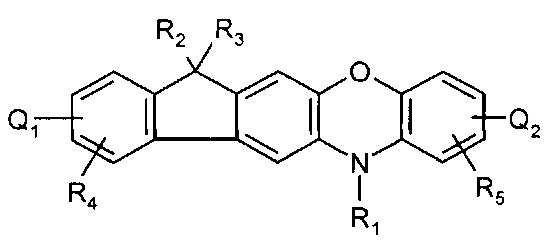



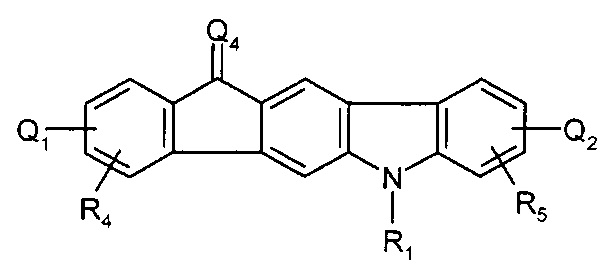


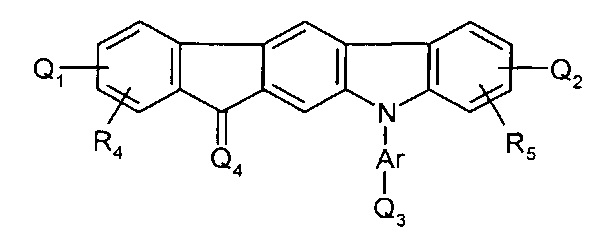



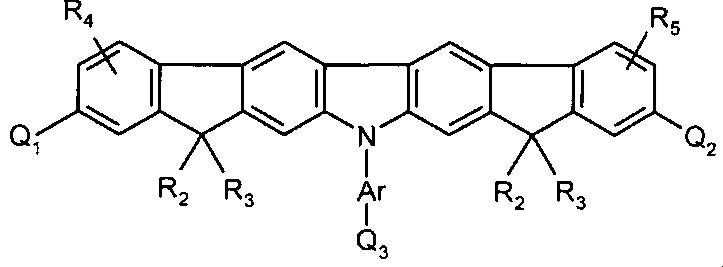
где Q1, Q2, Q3, Q4, R1, R2, R3, R4, R5, и Ar представляют собой, как определено выше.
[0064] В вариантах осуществления, -Ar- (то есть а линкер -LK-) представляет собой необязательно замещенный арилен как определено выше в отношении -LK-. Следует отметить, что хотя формулы выше и ниже показывают только один Q3, прикрепленный к -Ar-, они могут быть больше, чем один такой Q3. В вариантах осуществления, каждый -Ar-Q3 независимо представляет собой






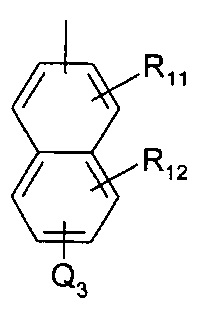





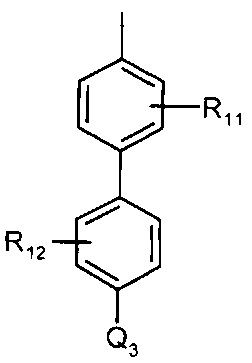
R11 и R12 являются необязательными и независимо представляют один или больше:
- C1-C12алкил, необязательно замещенный одним или более:
- -NR8R9,
- -O-L,
- -S-L, и/или
- фенилом, необязательно замещенным одним или более: C1-C6алкилом, галогененом, нитрилом, алкилокси, COOR10, и/или C2-C12алкилкарбоксилом;
- C4-C10циклоалкил, C2-C12алкенил, C4-C10циклоалкенил, C2-C12алкинил, и/или C4-C10циклоалкинил, каждый из которых является необязательно замещенным алкилом и/или -O-L; и/или
- фенил, бифенил и нафтил, каждый из которых является необязательно замещенным одним или больше:
- C1-C6алкилом,
- галогеном,
- нитрилом,
- алкилокси,
- -COOR10, и/или
- C2-C12алкилкарбоксилом,
где L, R8, R9 и R10 представляют собой как определено выше.
[0065] Что касается формул выше для Ar, следует также отметить, что в других вариантах осуществления, Q3 группа(ы) могут быть прикрепленными в положении Ar группы, которые отличаются от таких показанных выше групп.
[0066] В вариантах осуществления, соединения представляют собой:
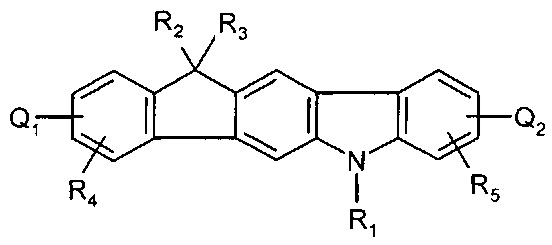





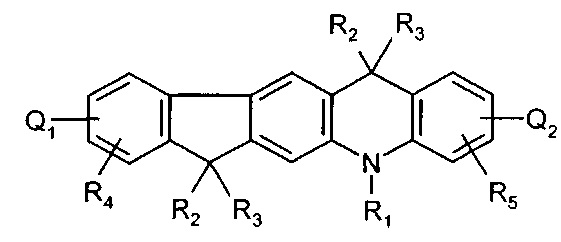

или

где:
- R4 и R5 являются необязательными и независимо представляют собой один C1-C12алкил или C1-C12алкилокси,
- Q1 и Q2 являются необязательными и независимо представляют собой одну ацильную группу или одну группу сложного эфира оксима формулы

- R1, R2 и R3 каждый независимо представляет атом водорода или C1-C12алкил,
- Q3 представляет собой атом водорода, ацильную группу, или группу сложного эфира оксима формулы:

- Q4 представляет собой ацил или сложный эфир оксима формулы:

- Ar представляет собой
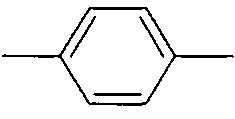
- R6 и R7 независимо представляет собой алкил, при условии, что соединение содержит, по крайней мере, одну ацильную группу или группу сложного эфира оксима.
[0067] В вышеуказанных вариантах осуществления, соединение содержит, по крайней мере, группу сложного эфира оксима, но не ацильную группу.
[0068] В вариантах осуществления, соединение представляет собой:





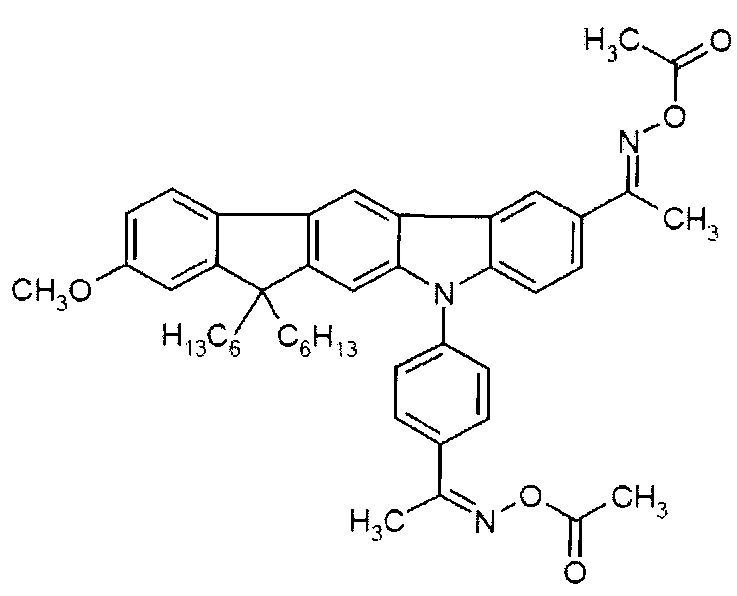

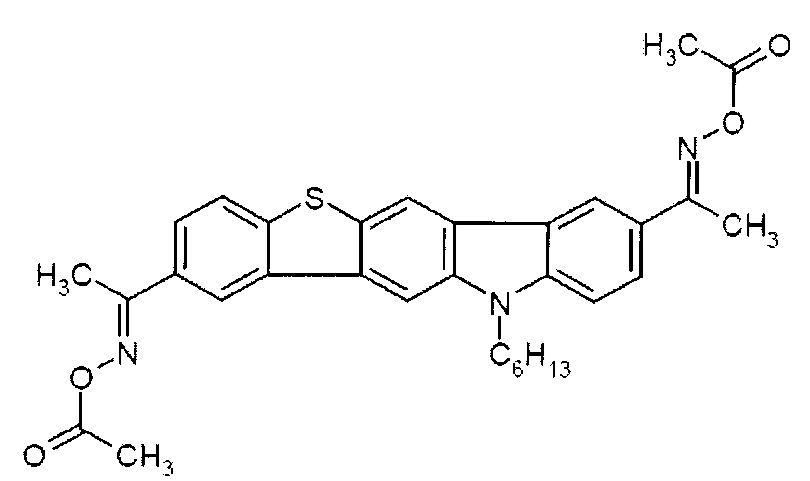


[0069] Конкретные варианты осуществления, в которых одна ФОРМУЛА I является сопряженной с двумя ФОРМУЛАМИ II для формирования труксена, труксенона, триазатруксена или их производных теперь будут рассмотрены. Для простоты, в последующей нумерации будет использоваться при обсуждении общая структура этих соединений:

Следует, однако, отметить, что нумерация в соответствии со стандартными правилами химической номенклатуры будет использоваться при именовании конкретных соединений (например, в "Описании иллюстративных вариантов осуществления" ниже).
[0070] Также, различные кольца в соединении изобретения будут представлены следующим образом: центральное фенильное кольцо (то есть фенильное кольцо, содержащее атомы углерода ном. 1-2, 6-7, и 11-12), три промежуточных пятичленных кольца (то есть пятичленные кольца, произведенные из атомов углерода ном. 2-6, атомов углерода ном. 7-11, и атомов углерода ном. 1, и 12-15 соответственно), и также три внешних фенильных кольца (то есть фенильные) кольца из атомов углерода ном. 3-4 и 16-19, атомов углерода ном. 8-9 и 20-23, и атомов углерода ном. 13-14 и 24-27 соответственное).
[0071] В вариантах осуществления, труксен, триазатруксен, труксенон или их производные имеют прикрепленные к нему к этому же, прямо или косвенно, один, два, три четыре, пять или шесть групп сложного эфира оксимов или один, два, три, четыре, пять или шесть ацильных групп. В вариантах осуществления, они содержат один, два, три, четыре, пять групп сложного эфира оксимов или больше и/или шесть, пять, четыре, две группы сложного эфира оксимов или меньше. В вариантах осуществления, они содержат один, два, три, четыре, пять ацильных групп или больше и/или шесть, пять, четыре, три, две ацильные группы или меньше.
[0072] В вариантах осуществления, некоторые или все группы сложных эфиров оксима или ацильные группы представляют собой прямо или косвенно прикрепленные к внешним фенильным кольцам труксена, труксенона, триазатруксена или их производных. Другими словами, некоторые или все сложные эфиры оксима или ацильные группы представляют собой прямо или косвенно прикрепленные к атомам углерода ном. 16-19, 20-23 и 24-27.
[0073] В тех же или других вариантах осуществления, некоторые или все сложные эфиры оксима или ацильные группы являются прямо или косвенно прикрепленными к промежуточным пятичленным кольцам труксена, триазатруксена или их производных. Другими словами, некоторые или все сложные эфиры оксима или ацильные группы представляют собой прямо или косвенно прикрепленные к углероду или атомам азота ном. 5, 10, и 15.
[0074] В вариантах осуществления, соединение содержит:
труксен:

труксенон:

триазатруксен:

или их производные,
труксен, труксенон, триазатруксен или их производные имеют присоединенную к нему, по крайней мере, одну -E1, -LK-E1, -LK-(E1)2 или =E2, где -LK- представляет собой как определено выше, -E1 представляет собой -CR6=N-O-(C=O)-R7 или -C(=O)-R30, и =E2 представляет собой =N-O-(C=O)-R7, где R6, R7 и R30 представляют собой, как определено выше.
[0075] В вариантах осуществления, соединение представляет собой формулы:



каждый Q независимо представляет собой от 1 до 4:
- водород;
- -E1,
- -LK-E1;
- -LK-(E1)2;
- C1-С12алкил, необязательно замещенный одним или более -NR19R20, -O-L и/или -S-L;
- C1-C12галогеналкил;
- C4-C8циклоалкенил;
- C2-C12алкинил;
- фенил или -N(R19)-фенил, каждый из которых является необязательно замещенным одним или больше C1-C6алкилом, галогеном, нитрилом, алкилокси, -COOR19, и/или C2-C12алкилкарбоксилом;
- бензоил, нафтил, фенилоксикарбонил, или нафтилоксикарбонил, каждый из которых является необязательно замещенным одним или более C1-C20алкилом, C1-C4галогеналкилом, -SR19, -OR19, -NR19R20, галогеном, фенилом, -COOR19, -CONR19R20, -CN, -NO2 и/или C3-C10циклоалкилом, где C3-C10циклоалкил может быть прерван -O-, -(С=O)- или -N(R19)-;
- -NR16R17; и/или
- тиофенкарбонил или пирролидинил, каждый из которых является необязательно замещенным одним или больше С1-С6алкилом, галогеном, нитрилом, алкилокси, -COOR19, и/или C2-C12алкилкарбоксилом, и каждый R21 независимо представляет собой:
- водород;
- -E1;
- -LK-E1;
- -LK-(E1)2;
- C1-C12алкил, необязательно замещенный одним или более фенилом, -NR19R20, -O-L и/или -S-L;
- C4-C8циклоалкенил;
- C2-C12алкинил; или
- фенил, необязательно замещенный одним или более C1-C6алкилом, нитрилом, алкилокси, -COOR16, и/или C2-C12алкилкарбоксилом,
и/или два R21 прикрепленных к одному и тому же самому атому углерода, представленному =O или =E2,
где:
- R16 и R17 независимо представляют собой:
- водород,
- C1-C12алкил, необязательно замещенный одним или более -NR19R20, -O-L и/или -S-L;
- C4-C10циклоалкил;
- C4-C10циклоалкенил;
- C2-C12алкинил;
- C1-C12галогеналкил; или
- фенил или бензоил, каждый из которых необязательно замещенный одним или более C1-C6алкилом, галогеном, нитрилом, алкилокси, -COOR19, и/или C2-C12алкилкарбоксильной группой,
- R19 и R20 независимо представляют собой водород, C1-C12алкил; C1-C12галогеналкил; C4-C8циклоалкенил или C2-C12 алкинил,
- L, -LK-, -E1, =E2, -R4 и -R5 представляют собой как определено выше, при условии, что соединение содержит, по крайней мере, один сложный эфир оксима или ацильную группу, и при условии, что когда R21 является прикрепленным к атому азота и R21 представляет собой -E1, -E1 не является -СR6=N-O-(С=O)R7.
[0076] Тут "каждый R21 независимо представляет собой [перечень заместителей] и/или два R21 прикрепленных к одному и тому же атому углерода, представленного =O или =E2" означает, что некоторые или все R21 группы могут представлять заместители, перечисленные, в то время как некоторые или все пары R21 прикреплены к общему атому углерода, могут быть =O или =E2.
[0077] Также, "каждый Q независимо представляет от 1 до 4 [список заместителей]" означает, что каждый Q может представлять 1, 2, 3 или 4 заместители, каждый независимо выбранный из списка. Также это означает, что заместители для каждого Q представляют собой выбранные независимо из тех, которые выбраны из других Q групп.
[0078] В вариантах осуществления, когда каждый Q представляет собой один заместитель, эти заместители являются прикрепленными к атомам углерода ном. 17 или 18, атомам углерода ном. 21 или 22, и атомам углерода ном. 25 или 26 соответственно.
[0079] В вариантах осуществления, соединение представляет собой формулы:



каждый из Q11, Q12 и Q13 независимо представляет собой:
- водород;
- -E1;
- -LK-E1;
- -LK-(E1)2;
- C1-C12алкил, необязательно замещенный одним или более -NR19R20, -O-L и/или -S-L;
- C1-C12галогеналкил;
- C4-C8циклоалкенил;
- C2-C12алкинил;
- фенил или -N(R19)-фенил, каждый из которых является необязательно замещенным одним или больше C1-C6алкилом, галогеном, нитрилом, алкилокси, -COOR19, и/или C2-C12алкилкарбоксилом;
- бензоил, нафтил, фенилоксикарбонил или нафтилоксикарбонил, каждый из которых является необязательно замещенным одним или больше C1-C20алкилом, C1-C4галогеналкилом, -SR19, -OR19, -NR19R20, галогеном, фенилом, -COOR19, -CONR19R20, -CN, -NO2 и/или C3-C10циклоалкилом, где C3-C10циклоалкил может быть прерван -O-, -(С=O)- или -N(R19)-;
- -NR16R17; и/или
- тиофенкарбонил или пирролидинил, каждый из которых является необязательно замещенным одним или больше C1-C6алкилом, галогеном, нитрилом, алкилокси, -COOR19, и/или C2-C12алкилкарбоксилом, каждый R22 независимо представляет собой:
- водород;
- C1-C12алкил, необязательно замещенный одним или более -NR19R20, -O-L и/или -S-L;
- C1-C12галогеналкил;
- C4-C8циклоалкенил;
- C2-C12алкинил;
- фенил или -N(R19)-фенил, каждый из которых является необязательно замещенным одним или больше C1-C6алкилом, галогеном, нитрилом, алкилокси, -COOR19, и/или C2-C12алкилкарбоксилом; или
- бензоил, нафтил, фенилоксикарбонил, или нафтилоксикарбонил, каждый из которых является необязательно замещенным одним или больше C1-C20алкилом, C1-C4галогеналкилом, -SR19, -OR19, -NR19R20, галогеном, фенилом, -COOR19, -CONR19R20, -CN, -NO2 и/или C3-C10циклоалкилом, где C3-C10циклоалкил прерывается -O-, -(С=O)- или -N(R19)-,
где R16, R17, R19, R20, R21, L, -LK-, -E1, =E2, -R4 и -R5 представляет собой как определено выше, при условии, что соединение содержит, по крайней мере, один сложный эфир оксима или ацильную группу, и при условии, что когда R21 является прикрепленной к атому азота и R21 представляет собой -E1, -E1 не является -CR6=N-O-(C=O)-R7.
[0080] В более конкретных вариантах осуществления вышеуказанных соединений, -LK-E1 представляет собой:






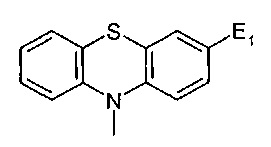



где R16 и R17 представляют собой как определено выше и где R18 представляют собой водород или C1-C12алкил, необязательно замещенный одним или более -O-L и/или -S-L, L представляющий собой как определено выше.
[0081] Следует также отметить, что в других вариантах осуществления, E1 группа(ы) могут быть прикреплены к другим позициям линкеров, показанных выше.
[0082] Для большей определенности, выше "два R21 прикрепленных таких же атомов углерода, представленных как =O или =Е2" означает, например, что Формула I выше представляет собой соединения Формулы:

[0083] В других вариантах осуществления вышеуказанные Формулы 1, 1', 2, 2', 3 и 3', соединение содержит один или больше групп сложного эфира оксима, но не ацильные группы.
[0084] В других вариантах осуществления вышеуказанные Формулы 1, 1', 2, 2', 3 и 3', соединение содержит одну или больше ацильных групп, но не групп сложных эфиров оксима.
[0085] В вариантах осуществления вышеуказанные Формулы 1, 1', 2, 2', 3 и 3':
- каждый Q, Q1, Q2, и Q3, когда присутствует, представляет собой одну -E1 формулы -CR6=N-O-(C=O)-R7, где R6 представляет собой C1-C12алкил необязательно замещенный -O-L, где L представляет собой C1-C6алкил, и R7 представляет собой C1-C12алкил;
- все R22, когда присутствуют, представляют водород; и
- все R21, когда присутствуют, представляют водород или C1-C12алкил.
[0086] В других вариантах осуществления вышеуказанных Формул 1, 1', 2, 2', 3 и 3':
- каждый Q, Q11, Q12, и Q13, когда присутствует, представляет собой один -LK-E1, где E1 представляет собой формулы -CR6=N-O-(C=O)-R7, где R6 представляет собой C1-C12алкил, необязательно замещенный -O-L, где L представляет собой C1-C6алкил, и R7 представляет собой C1-С12алкил;
- все R22, когда присутствуют, представляют собой водород;
- все R21, когда присутствует, представляют собой водород или C1-C12алкил; и
- LK представляет собой

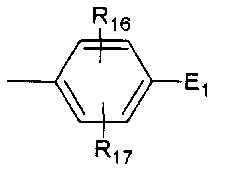

или

[0087] В других вариантах осуществления вышеуказанных формул 1 и 1', каждый из Q11, Q12, и Q13, когда присутствует, представляет собой водород, каждый из Q и R22 когда присутствует, представляет собой один -N(R19)-фенил, где R19 представляет собой C1-C12алкил, и каждая пара R21 прикрепленная к общему атому углерода, представляет собой =E2, где R7 представляет собой C1-C12алкил.
[0088] В вариантах осуществления вышеуказанных Формул 1, 1', 2, 2', 3 и 3':
- каждый Q, Q1, Q2 и Q3, когда присутствует, представляет собой один -LK-E1 или -E1, где E1 представляет формулы -C(=O)-R30, где R30 представляет собой C1-C12 линейный алкил, фенил, фенил, замещенный алкил или алкилокси, или тиофенил;
- все R22, когда присутствуют, представляют собой водород;
- все R21, когда присутствуют, представляют собой C1-C12алкил, и
- LK представляет собой 2-фенилен или 4-фенилен.
[0089] В вариантах осуществления, соединение представляет собой формулы:



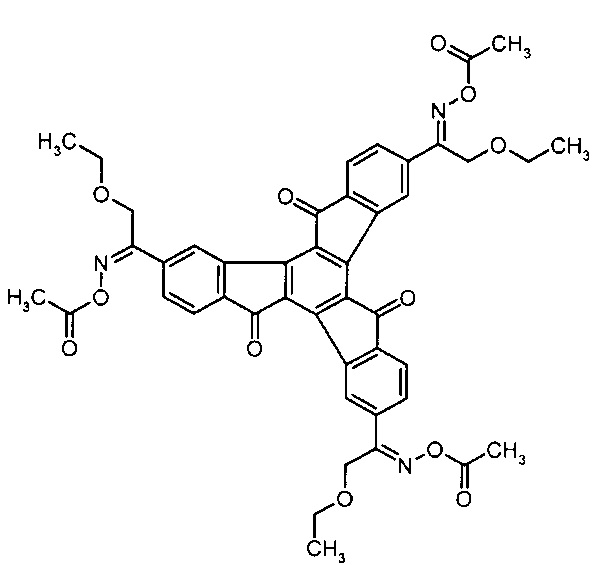

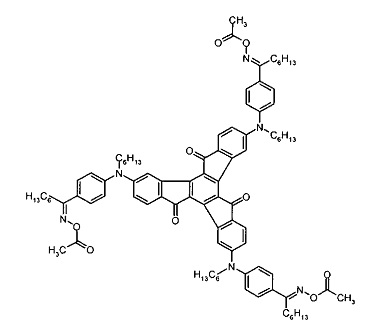

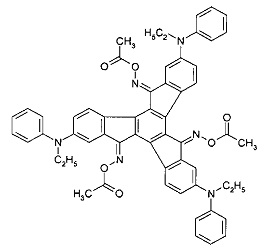



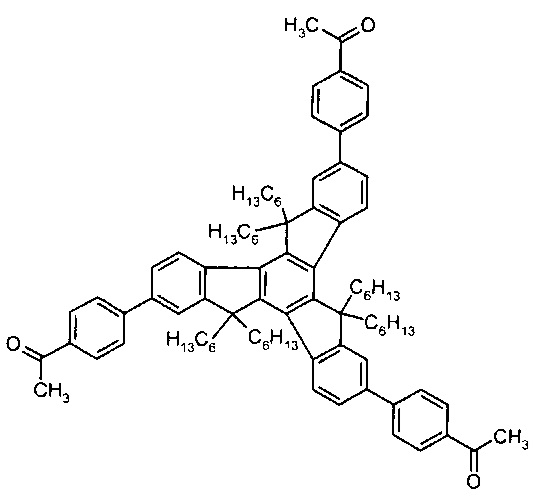





Применение соединений изобретения
[0090] Соединения настоящего изобретения являются полезными в качестве фотоинициаторов. Они поглощают УФ-свет и затем выделяют свободные радикалы. Как таковые, они являются полезными в фоточувствительных или фотополимеризуемых композициях. Такие композиции, как правило, содержат, вдобавок, к соединению настоящего изобретения, поляризуемое соединение со свободными радикалами. Такое поляризуемое соединение со свободными радикалами будет, как правило, этиленненасыщенным связьсодержащим полимеризуемым соединением. Эти композиции также часто содержат другие компоненты, которые являются известными для квалифицированного специалиста в данной области техники, который будет осуществлять их выбор в зависимости от предполагаемого применения полимеризуемой композиции.
[0091] Фоточувствительные или фотополимеризуемые композиции и полимеризуемые соединения для использования в них являются хорошо известными для квалифицированного специалиста в данной область техники. Неограничивающие примеры таких композиций включают фотонабор или фотоотверждаемые чернила (включая краски для струйной печати (к примеру, отверждаемые под действием УФ-краски для струйной печати), гравюры, и флексографская печать), фоточувствительные печатные пластины, защитные цветовые фильтры, черносмольную матрицу, литографические печатные пластины, и множество фототверждающих материалов, включая сухие пленочные резисты. Соединения изобретения могут также быть использованы в качестве фотоинициаторов в композициях для кислородочищающих пленок.
[0092] Соединения изобретения могут заменять фотоинициаторы, используемые в фоточувствительных или фотополимеризуемых композициях в существующем уровне техники.
[0093] В частности, соединения изобретения могут быть использованы в цветовых защитных фильтрах таких, которые описаны в Kura и др., "New Oxime Ester Photoinitiators for Color Filter Resists", Radtech Report, May/June 2004, стр.30-35.
[0094] Они также могут быть использованы в фотополимеризуемых композициях описанных на страницах 7-61 WO 2006/018405 и на страницах 22-65 WO 02/100903. Они также могут быть использованы в композиции, описанной в US 6,949,678.
[0095] Следует отметить, к примеру, что такие фотополимеризуемые композиции, вдобавок к соединению изобретения и полимеризуемому соединению, могут включать, кроме того, известные фотоинициаторы и другие добавки, такие как термические ингибиторы, соединения меди, ваксоподобные вещества, кислороднепроницаемый слой, светостабилизаторы, амины для усиления фотополимеризации, агенты переноса цепи, фотосенсибилизаторы, сшивающие агенты, co-инициаторы, фоторедукторные краски, улучшители текучести, усилители адгезии, поверхностно-активные вещества, оптические отбеливатели, пигменты, краски, смачивающий агент, выравнивающие помощники, дисперсанты, предотвратители агрегации, антиоксиданты, наполнители, микросферы, стекловолокна, связующие вещества и т.д.
[0096] Фотополимеризуемые композиции могут быть использованы для различных целей, к примеру, в качестве печатных чернил, к примеру, краски для трафаретной печати, краски для струйной печати, краски для офсетной или флексографской печати, как прозрачное покрытие, как белое или цветное покрытие, к примеру, для дерева или металла, как порошковое покрытие, как материал покрытия, между прочим, для бумаги, дерева, металла или пластика, как покрытия, отверждаемые при дневном свете для маркировки зданий и дорожной разметки, для фотографических репродуктивны технологий, для голографических записывающих материалов, для записывающих изображения технологий или для производства печатных пластин, которые могут быть разработаны с органическими растворителями или с водными щелочами, для изготовления масок для трафаретной печати, как стоматологические пломбировочные композиции, в качестве клеев, как чувствительные к давлению клеи, как смолы для ламинирования, как кислотостойкий копировальный слой, резист для пайки, резист для электролитического покрытия, или перманентные резисты, и жидкие и сухие пленки, как фотоструктурный диэлектрик, для печатных плат и электронных схем, как резисты для производства цветных фильтров для различных применений дисплеев или для получения структур в процессе производства плазменно-дисплейных панелей и электролюминесцентных дисплеев, (как, к примеру, описано в US 5,853,446; EP 863,534; JP 09-244230-A; JP 10-62980-А; JP 08-171863-А; US 5,840,465; EP 855,731; JP 05-271576-A; и JP 05-67405-A) для производства материала голографического хранения данных (HDS), для производства оптических переключателей, оптических решеток (интерференционные решетки), цепей освещения, для производства трехмерных изделий посредством выдерживания адиабатических условий (УФ-отверждение в прозрачных формах) или посредством стереолитографических технологий, как это описано, к примеру, в US 4,575,330, для производства композиционных материалов (к примеру, стирольные полиэфиры, которые могут, если необходимо, содержать стекловолокна и/или другие волокна и другие вспомогательные вещества) и другие толстослойные композиции, для покрытия или уплотнения электронных компонентов и интегральных микросхем, или в качестве покрытий для оптоволокно, или для изготовления оптических линз, к примеру, контактных линз или линз Френеля. Композиции в соответствии с настоящим изобретением являются, кроме того, подходящими для производства медицинского оборудования, вспомогательного оборудования или имплантов. Кроме того, композиции в соответствии с настоящим изобретением являются подходящими для приготовления гелей с термотропными свойствами, как, к примеру, описано в DE 19700064 и ЕР 678,534.
[0097] Фотоинициаторы могут дополнительно быть использованы в качестве инициаторов для эмульсионных полимеризаций, бисерных полимеризаций или суспензионных полимеризаций, как полимеризационные инициаторы для фиксирования упорядоченного состояния жидкокристаллических мономеров и олигомеров, или в качестве инициаторов для фиксирования красок на органических материалах. Они также могут быть использованы для полимеризации радиационно-отверждаемых порошковых покрытий. Кроме того, они находят применение в композициях с негативным резистом, подходящих для производства печатных форм для рельефной печати, плоской печати, фотогравюр или форм трафаретной печати, для производства рельефных копий, к примеру, для производства текстов шрифтом Брайля, для производства штампов, для использования в химическом измельчении или в качестве микрорезиста в производстве интегральных микросхем. Композиции, кроме того, могут использоваться в качестве фотолитографического диэлектрического слоя или покрытия, инкапсулированного материала и изоляционного покрытия в производстве компьютерных чипов, печатных плат и других электрических электронных компонентов. Возможные поддержки слоя, и условия обработки покрытия подложек столь же разнообразны.
[0098] Эти композиции могут также быть фоточувствительными термореактивными полимерными композициями, которые могут быть использованы для образования материала для нанесения паяльной маски. Они могут быть полезны в качестве материалов для производства печатных монтажных плат, прецизионного производства металлических изделий, травления стеклянных и каменных изделий, рельефа пластмассовых изделий, и также приготовления печатных форм. Защитная паяльная маска представляет собой вещество, которое используется по время пайки данной части к печатной плате с целью предотвращения расплавленного припоя от присоединения не относящихся к делу частей и защиты цепей.
[0099] Они являются подходящими для произведения цветных фильтров или цветных мозаичных систем, таких, которые описаны, к примеру, в EP 320,264. Цветные фильтры обычно используются в производстве LCD, проекционных систем и сенсоров изображения. Цветные фильтры могут быть использованы, к примеру, для дисплея и сканера изображения в телевизионных ресиверах, видеомониторах или компьютерах, в технологии плоскопанельных дисплеев и т.д.
[00100] Фоточувствительные композиции могут, кроме того, быть использованы для производства спейсеров, которые контролируют разрыв клеток жидкой части кристалла в жидкокристаллических панельных дисплеев. Фоточувствительные композиции являются также подходящими для производства массива микролинз, используемых в жидкокристаллических панельных дисплеях, сенсорах изображения и тому подобных. Они также являются пригодными для фотолитографических операций, используемых в процессах производства плазменных индикаторных панелей (PDP), в частности для визуализации процесса формирования барьерного ребра, слоя люминофора и электродов. Композиции также находят применение для производства одно- или многослойных материалов для записи изображения или воспроизведения изображения (копии, репрография), которое может быть моно- или полихроматическим. Кроме того, материалы являются пригодными для системы получения цветного пробного изображения. Соединения изобретения являются также подходящими в качестве фотоинициаторов в голографическом применении хранения данных. Фотоинициаторы являются подходящими для приготовления оптических изделий (к примеру, оптических волноводов) или голографических записывающих сред, к примеру, содержащих полимер и органический фотоинициатор. Как уже упоминалось выше, фотоинициаторы являются также подходящими для изготовления печатных форм. Также представляет интерес применение новых фотоинициаторов для отверждения формованных изделий, сделанных из композитных составов. Соединения в соответствии с настоящим изобретением могут быть использованы для произведения голографии, волноводов, оптических переключателей, где преимущества берутся из развития разницы в показателе преломления между облученной и необлученной площадями.
[00101] Соединения изобретения могут также быть использованы в фоточувствительных смоляных композициях, описанных в US 2010/0210749 и в способных к отверждению композициях, фотополимеризуемых композициях, цветовых фильтрах и тому подобных, описанных в US 2009/0023085, к примеру, в пунктах [0130]-[0342] и в пунктах [0407]-[0607].
[00102] Соединения изобретения могут также быть использованы в фоточувствительных композициях, описанных в US 7,556,910 и фотополимеризуемых композициях US 6,051,367.
[00103] Таким образом, аспект настоящего изобретения относится к использованию соединений в качестве фотоинициаторов в резистных композициях цветовых фильтров. Более конкретно, резистные композиции цветовых фильтров могут, в вариантах осуществления, содержать:
- от около 1 до около 5 мас.% соединения изобретения или ее смеси;
- щелочной растворимый полимер;
- реактивный олигомер;
- пигмент; и
- одну или более оптических добавок.
[00104] Таким образом, другой аспект настоящего изобретения относится к использованию соединения изобретения в покрытых композициях для производства литографических оффсетно-печатных плат, на которых может быть нанесено изображение цифровым образом при помощи луча лазера, который имеет длину волны излучения между 350 и 410 нм. Более конкретно, такие покрытые композиции могут, в вариантах осуществления, содержать:
- от около 1 до около 5 мас.% соединения изобретения или ее смеси;
- полимерную вяжущую смолу;
- реактивный олигомер;
- один или более красителей; и
- одну или более необязательных пленкообразующих добавок.
[00105] Эта покрытая композиция может быть покрыта на подложке из анодированного алюминия, который имеет вес покрытия между 0.8 и 3.0 грамм на квадратный метр.
[00106] Во многих вариантах осуществления изобретения, соединения изобретения относительно легко сделать. К примеру, некоторые из них легко очистить кристаллизацией, избегая, таким образом, потребность в флэш хроматографии. Кроме того, многие из них являются растворимыми в одном или более спиртов, которые являются относительно безвредными для окружающей среды растворителями. Кроме того, многие из них являются бесцветными, что делает их полезными в широком диапазоне применений. Другие виды легко окрашиваются и являются более полезными, к примеру, в черно полимерных матрицах и других применениях, где цвет не является проблемой. Кроме того, многие соединения изобретения не приводят к потере цвета при использовании.
[00107] При этом если не указано иное, "алкил" относится к однолистному насыщенному линейному или разветвленному C1-12 гидрокарбильный радикал формулы -CnH2n+1. Аналогичным образом, "алкенил" и "алкинил" относится к линейным или разветвленным C1-12 ненасыщенным (с двойной и тройной связью(ями), соответственно) одновалентным гидрокарбильным радикалам.
[00108] При этом если не указано иное, "алкилен" относится к двухвалентному насыщенному линейному или разветвленному C1-12 гидрокарбильному радикалу формулы . Аналогичным образом, "алкенилен " и "алкинилен" относится к линейным или разветвленным C1-12 ненасыщенным (с двойной и тройной связью(ями), соответственно) двухвалентным гидрокарбильным радикалам.
[00109] При этом, если не указано иное, "арил" и "арилен" относится соответственно к одновалентным и двухвалентным ароматическим радикалам, содержащим между 1 и четырьмя ароматических колец. Кольца могут быть склеены или прикреплены друг к другу посредством ковалентной связи.
[00110] При этом "около" имеет обычное значение. В вариантах осуществления изобретения, это может означать плюс или минус 5% от численного значения величины, которую оно определяет.
[00111] При этом "содержащие" является не ограничивающим термином, который означает "включая, но не ограничиваясь".
[00112] Другие объекты, преимущества и признаки настоящего изобретения станут более очевидными после прочтения следующих не ограничивающих описаний конкретных вариантов их осуществления, данных в качестве примеров со ссылкой на прилагаемые чертежи.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
[00113] На прилагаемых чертежах:
[00114] Фигура 1 иллюстрирует схему реакции для производства 3-ацетилоксим-O-ацетат-6,12-диэтил-12-метил-6,12-дигидро-6-аза-индено[1,2-b]флуорена;
[00115] Фигура 2 иллюстрирует схему реакции для производства 7-ацетилоксим-O-ацетат-10-этил-12,12-дигексил-10,12-дигидро-10-аза-индено[2,1-b]флуорена;
[00116] Фигура 3 иллюстрирует схему реакции для производства 9-ацетилоксим-O-ацетат-2-метокси-12,12-диэтил-6,12-дигидро-6-тиа-индено[1,2-b]флуорена;
[00117] Фигура 4 иллюстрирует схему реакции для производства 7-ацетилоксим-O-ацетат-12,12-диметил-10,12-дигидро-10-оксо-индено[2,1-b]флуорена;
[00118] Фигура 5 иллюстрирует схему реакции для производства 8-ацетилоксим-O-ацетат-11,13,13-триэтил-6,6-диметил-11,13-дигидро-6Н-11-аза-индено[2,1-b]антрацена;
[00119] Фигура 6 иллюстрирует схему реакции для производства 10-(4-ацетилоксим-O-ацетат фенил)-7-ацетилоксим-O-ацетат-2-метокси-12,12-дигексил-10,12-дигидро-10-аза-индено[2,1-b]флуорена;
[00120] Фигура 7 иллюстрирует схему реакции для производства 10-(4-ацетилоксим-O-ацетат фенил)-2,7-диацетилоксим-O-ацетат-12,12-дигексил-10,12-дигидро-10-аза-индено[2,1-b]флуорена;
[00121] Фигура 8 иллюстрирует схему реакции для производства 3,9-диацетилоксим-O-ацетат-6-гексил-6Н-12-тиа-6-аза-индено[1,2-b]флуорена;
[00122] Фигура 9 иллюстрирует схему реакции для производства 10-гексил-10Н-10-аза-индено[2,1-b]флуорен-12-O-ацетилоксима;
[00123] Фигура 10 иллюстрирует схему реакции для производства 7,7'-ацетилоксим-O-ацетат-1,1'-диметил-бисиндено[3,2-b:2',3'-h]-9-секс-бутил карбазола;
[00124] Фигура 11 иллюстрирует схему реакции для производства 4,9,13-триэтоксиацетилоксим-O-триацетаттруксенона;
[00125] Фигура 12 иллюстрирует спектры в УФ- и видимой области 3,8,13-триацетил-5,10,15-тригексил-10,15-дигидро-5Н-5,10,15-триазадииндено [1,2-a;1',2'-c]флуорен триоксим три-O-ацетата;
[00126] Фигура 13 иллюстрирует спектры в УФ- и видимой области Carba-05, Truxe-08, Truxe-07 и Truxe-12;
[00127] Фигура 14 иллюстрирует относительное поглощение в УФ- и видимой области Truxe-04 (INDENO 332), Truxe-13 (INDENO 336), Truxe-14 (INDENO 332B), Truxe-15 (INDENO 338) и Truxe-16 (INDENO 333);
[00128] Фигура 15 иллюстрирует потребление кислорода кислородочищающей пленкой, содержащей INDENO 332 как функция времени; и
[00129] Фигура 16 иллюстрирует потребление кислорода кислородочищающей пленкой, содержащей INDENO 336 как функцию времени.
ОПИСАНИЕ ИЛЛЮСТРАТИВНЫХ ВАРИАНТОВ ОСУЩЕСТВЛЕНИЯ
[00130] Настоящее изобретения проиллюстрировано более подробно следующими не ограничивающими примерами.
Глоссарий
[00131] Следующие были применены в приведенных примерах ниже:


Основной зеленый 4 (034): Пигмент, доступный от Spectra Colors, USA
BYK 307: Полисилоксановое поверхностно-активное вещество, модифицированное полиэтилен гликолем, доступный от BYK Chemie, USA
TRUXE-6H: 5,5',10,10',15,15'-Гексагексилтруксен (98%), доступный от American Dye Source, Inc., Canada.
TRUXA-3H: 5,10,15-Тригексил-10,15-дигидро-5Н-5,10,15-триазадииндено[1,2-a;1',2'-c]флуорен (98%), доступный от American Dye Source, Inc., Canada.
TRUXE-3Br: 2,7,12-Трибромо-5,5,10,10,15,15-гексагексилтруксен, доступный от American Dye Source, Inc., Canada.
TRUXE-3F: 4,9,14-Трифторотруксенон (98%), доступный от American Dye Source, Inc., Canada
TRUX-2Br: 2,2-Дибромо-5-фтороиндан-1-он (97%), доступный от American Dye Source, Inc., Canada
Silane: γ-Метакрилоксипропил триетоксисилан, доступный от Sigma Aldrich, Canada
BR07-001: Растворимая в щелочи полимерная вяжущая смола (MW=37,000 г/моль) доступная от American Dye Source, Inc., Canada и которая имеет следующую формулу:

UR07-015: Реактивный олигомер, доступный от American Dye Source, Inc., Canada и который имеет следующую Формулу:

АС07-001: Диспергатор сополимера ацеталя (MW=47,000 г/моль), доступный от American Dye Source, Inc., Canada и который имеет следующую формулу:

АС12-001: Сополимер ацеталя, содержащий циклогексенильную боковую группу (a=0.5, b=0.48 и c=0.02), доступный от Mylan Group, Travinh, Vietnam. Формула
Irgacure OXE-02: Фотоинициатор, доступный от BASF, Germany и который имеет следующую формулу:

BR10-010: Полимерная часть, 20% диспергатора в изопропаноле / водной смеси (80/20) (Размер частиц =150 нм; полидисперсность =0.08), доступный от America Dye Source, Inc., Canada и имеет следующую формулу:

UR07-009: Реактивный олигомер (60% в 1,3-раствор диоксолана), доступный от American Dye Source, Inc., Canada и имеет следующую формулу:

КОБАЛЬТ: Кобальтовая (II) соль масляной кислоты, доступная от Sigma Aldrich, Ontario, Canada.
ADD-2204: 2,4,6-Триметилбензоил-дифенил-фосфиноксид, доступный от Aceto Corporation, New York, USA.
ADD-9984: N-винилкапролактам, доступный от Sigma Adrich, Ontario, Canada.
ADD-9991: 1,6-гександиол диакрилат, доступный от Sigma Adrich, Ontario, Canada.
ADD-9992: 2-феноксиэтилакрилат, доступный от TCI America, USA.
ADD-9995: Пропоксилированный неопентилгликоль диакрилат, доступный от Sartomer, USA.
ADD-2614: 3-Метакрилоксипропил триметоксисилан, доступный от Polysciences, USA.
POL-0138: Алифатический полиэстер уретанакрилата, доступный от Mylan Group, Travinh, Vietnam.
POL-1001: Ароматический олигомер моноакрилата, доступный от Mylan Group, Travinh, Vietnam.
POL-0137: Стабилизатор для полностью отверждаемых красок, доступный от Mylan Group, Travinh, Vietnam.
600-B307: Силиконовая поверхностная добавка, доступная от Mylan Group, Travinh, Vietnam.
COL-1829: Пигмент Синий 15:4 - 25% диспергирован в ADD-9995, доступный от Mylan Group, Travinh, Vietnam.
ADD-9993: Триметилциклогексана акрилат, доступный от Sigma Aldrich, Ontario, Canada.
Yellow-150: Дисперсия желтого пигмента, содержащая 7.5 г CI Пигмента Желтого 150 (доступный от Hangzhou Multicolor Chemical Company, China), 2.5 г AC07-001 и 40 г циклогексанона. Смесь была диспергирована в течение 24 часов с использованием шариковой мельницы. Она была отфильтрована фильтром с размером пор 5 мкм, и был добавлен циклогексаном до получения 15% твердой массы.
Red-254: Дисперсия красного пигмента, содержащая 7.5 г CI Пигмента Красного 254 (Hostapern Red D2G 70 LV 2647, доступный от Clarian, Germany), 2.5 г AC07-001 и 40 г циклогексанона. Смесь была диспергирована в течение 24 часов с использованием шариковой мельницы. Она была отфильтрована фильтром с размером пор 5 мкм, и был добавлен циклогексанон до получения 15% твердой массы.
Green-36: Дисперсия зеленого пигмента, содержащая 7.5 г CI Пигмента Зеленого 36 (Heliogen Green K9360, доступный от BASF, Germany), 2.5 г АС07-001 и 40 г циклогексанона. Смесь была диспергирована в течение 24 часов с использованием шариковой мельницы. Она была отфильтрована фильтром с размером пор 5 мкм, и был добавлен циклогексанон до получения 15% твердой массы.
Blue-15: Дисперсия синего пигмента, содержащая 7.5 г CI Пигмента Синего 15:6 (Hangzhou Multicolor Chemical Company, China), 2.5 г AC07-001, и 40 г циклогексанона. Смесь была диспергирована в течение 24 часов с использованием шариковой мельницы. Она была отфильтрована фильтром с размером пор 5 мкм, и был добавлен циклогексанон до получения 15% твердой массы.
Black-250: Сажевая дисперсия, содержащая 7.5 г сажи (Special Black 250, доступный от Degussa, USA), 7.5 г AC07-001 и 40 г циклогексанона. Смесь была диспергирована в течение 24 часов с использованием шариковой мельницы. Она была отфильтрована фильтром с размером пор 5 мкм, и был добавлен циклогексанон до получения 15% твердой массы.
Резистентное связующее вещество: резистентное связующее вещество было приготовлено путем растворения 6.0 г BR07-001, 6.0 г UR07-015, 1.0 г Silane в 102 г циклогексаноне.
Синтез и исследование соединений изобретения
Пример 1.1 - 3-Ацетилоксим-O-ацетат-6,12-диетил-12-метил-6,12-дигидро-6-аза-индвно[1,2-b]флуорен
[00132] Синтез 3-ацетилоксим-O-ацетат-6,12-диетил-12-метил-6,12-дигидро-6-аза-индено[1,2-b]флуорена был выполнен согласно реакционной схеме, показанной на Фигуре 1.
(a) Синтез 3-ацетил-6,12-диетил-12-метил-6,12-дигидро-6-аза-индено[1,2-b]флуорена:
[00133] Хлорид алюминия (3.43 г, 25.6 ммоль) медленно добавляли в раствор дихлорметана (80 мл) в котором было растворено 6,12-диетил-12-метил-6,12-дигидро-6-аза-индено[1,2-b]флуорена (5.95 г, 20.0 ммоль) и ацетил хлорид (1.83 мл, 25.7 ммоль) при 0°C при атмосфере азота. После перемешивания при комнатной температуре в течение ночи, реакционную смесь выливали в воду со льдом. Продукт экстрагировали дважды дихлорметаном. Объединенный органический слой был промыт рассолом, и высушен над MgSO4. Дихлорметан был удален под высоким вакуумом и полученный таким образом продукт был использован на следующей стадии без дополнительной очистки.
(b) Синтез 3-Ацетилоксим-6,12-диетил-12-метил-6,12-дигидро-6-аза-индено[1,2-b] флуорена:
[00134] 3-Ацетил-6,12-диетил-12-метил-6,12-дигидро-6-аза-индено[1,2-b]флуорен (3.39 г, 10.0 ммоль) был добавлен в раствор смеси, содержащей 100 мл 1,3-диоксана, натрия ацетат (1.06 г, 13.0 ммоль), гидроксиаммония хлорид (0.83 г, 12.0 ммоль) и воду (60 мл). Реакционную смесь кипятили с обратным холодильником в течение ночи, охлаждают до комнатной температуры и затем выливают в воду. Продукт был экстрагирован этилацетатом. Объединенный органический слой был промыт дважды водой, высушен над MgSO4, и концентрирован до получения осадка, который затем сушили в вакуумном сушильном шкафу при 40 С. Полученный таким образом продукт был использован на следующей стадии без дополнительной очистки (3.22 г, 92% выход).
(c) Синтез 3-ацетилоксим-O-ацетат-6,12-диетил-12-метил-6,12-дигидро-6-аза-индено[1,2-b]флуорена:
[00135] Триэтиламин (1.7 мл, 12.2 ммоль) и ацетилхлорид (915 мкл, 12.8 ммоль) были медленно добавлены в 100 мл раствора тетрагидрофурана, содержащего 3-ацетилоксим-6,12-диетил-12-метил-6,12-дигидро-6-аза-индено[1,2-b]флуорен (3.54 г, 10.0 ммоль) при 0°C под атмосферным азотом. После 3 часового перемешивания при комнатной температуре, реакционная смесь была влита в воду. Продукт был экстрагирован этилацетатом. Объединенный органический слой был промыт дважды водой, высушен с MgSO4, и концентрирован посредством вакуумного выпаривания до получения осадка, который был очищен путем флэш-хроматографии на силикагеле с этилацетатом и гексаном в качестве элюентов. Растворитель был удален с использованием вакуумного выпаривания до получения белого порошкового продукта с 32% выходом и 99% чистотой.
Пример 1.2 - 7-Ацетилоксим-O-ацетат-10-этил-12,12-дигексил-10,12-дигидро-10-аза-индено[2,1-b]флуорен
[00136] Синтез 7-ацетилоксим-O-ацетат-10-этил-12,12-дигексил-10,12-дигидро-10-аза-индено[2,1-b]флуорена был выполнен согласно реакционной схеме, показанной на Фигуре 2.
(a) Синтез 7-ацетил-10-этил-12,12-дигексил-10,12-дигидро- 10-аза-ждено[2,1-b]флуорена:
[00137] Хлорид алюминия (3.43 г, 25.6 ммоль) был медленно добавлен в раствор дихлорметана (80 мл) в котором были растворены 10-этил-12,12-дигексил-10,12-дигидро-10-аза-индено[2,1-b]флуорен (5.95 г, 20.0 ммоль) и ацетилхлорид (1.83 мл, 25.7 ммоль) при 0°C под атмосферным азотом. При перемешивании при комнатной температуре в течение ночи, реакционная смесь была влита в ледяную воду. Продукт был дважды экстрагирован дихлорметаном. Объединенный органический слой был промыт рассолом, и высушен над MgSO4. Дихлорметан был извлечен под высоким вакуумом и полученный таким образом продукт был использован на следующей стадии без дополнительной очистки.
(b) Синтез 7-ацетилоксим-10-этил-12,12-дигексил-10,12-дигидро-10-аза-индено[2,1-b]флуорена:
[00138] 7-Ацетил-10-этил-12,12-дигексил-10,12-дигидро-10-аза-индено[2,1-b]флуорен (3.39 г, 10.0 ммоль) был добавлен в раствор смеси, содержащей 100 мл 1,3-диоксана, натрия ацетата (1.06 г, 13.0 ммоль), хлорида гидроксиламмония (0.83 г, 12.0 ммоль) и воды (60 мл). Реакционную смесь кипятили с обратным холодильником в течение ночи, охлаждали до комнатной температуры и затем выливают в воду. Продукт был экстрагирован этилацетатом. Объединенный органический слой был промыт дважды водой, высушен над MgSO4, и концентрирован до получения осадка, который был дополнительно высушен в вакуумном сушильном шкафу при 40°C. Полученный таким образом продукт был использован на следующей стадии без дополнительной очистки (3.22 г, 92% выход).
(c) Синтез 6-ацетилоксим-O-ацетат-1,1-дигексил индено-[2,3-b]-9-этилкарбазола:
[00139] Триэтиламин (1.7 мл, 12.2 ммоль) был медленно добавлен в 100 мл раствора тетрагидрофурана, содержащего 7-ацетилоксим-10-этил-12,12-дигексил-10,12-дигидро-10-аза-индено[2,1-b]флуорен (3.54 г, 10.0 ммоль) и ацетилхлорид (915 мкл, 12.8 ммоль) при 0°C под атмосферным азотом. После 3 часов перемешивания при комнатной температуре, реакционную смесь выливают в воду. Продукт был экстрагирован этилацетатом. Объединенный органический слой был промыт дважды водой, высушен с MgSO4, и концентрирован посредством вакуумного выпаривания до получения осадка, который был очищен посредством флэш-хроматографии на силикагеле этилацетатом и гексаном в качестве элюента. Растворитель был удален с использованием вакуумного выпаривания до получения белого порошкового продукта с 32% выходом и 99% чистотой.
Пример 1.3 - 9-Ацетилоксим-O-ацетат-2-метокси-12,12-диетил-6,12-дигидро-6-тиа-индено[1,2-b]флуорен
[00140] Синтез 9-ацетилоксим-O-ацетат-2-метокси-12,12-диетил-6,12-дигидро-6-тиа-индено[1,2-b]флуорена был выполнен согласно реакционной схеме, показанной на Фигуре 3.
(a) Синтез 9-ацетш-2-метокси-12,12-диетил-6,12-дигидро-6-тиа-индено[1,2-b]флуорена:
[00141] Хлорид алюминия (3.43 г, 25.6 ммоль) был медленно добавлен в раствор дихлорметана (100 мл), в котором был разбавлен 2-метокси-12,12-диетил-6,12-дигидро-6-тиа-индено[1,2-b]флуорен (6.60 г, 20.0 ммоль) и ацетилхлорид (1.83 мл, 25.7 ммоль) при 0°C под атмосферным азотом. После перемешивания при комнатной температуре в течение ночи, реакционная смесь была влита в ледяную воду. Продукт был дважды экстрагирован с дихлорметаном. Объединенный органический слой был промыт рассолом, и высушен над MgSO4. Дихлорметан был извлечен под высоким вакуумом и, полученный таким образом продукт, был использован на следующей стадии без дополнительной очистки.
(b) Синтез 9-ацетилоксим-2-метокси-12,12-диетил-б, 12-дигидро-6-тиа-индено[1,2-b]флуорена:
[00142] 9-Ацетил-2-метокси-12,12-диетил-6,12-дигидро-6-тиа-индено[1,2-b]флуорен (3.56 г, 10.0 ммоль) был добавлен в раствор смеси, содержащей 100 мл 1,3-диоксана, натрия ацетата (1.06 г, 13.0 ммоль), хлорида гидроксиламмония (0.83 г, 12.0 ммоль) и воды (60 мл). Реакционную смесь кипятили с обратным холодильником в течение ночи, охлаждают до комнатной температуры, и затем выливают в воду. Продукт был экстрагирован этилацетатом. Объединенный органический слой был промыт дважды водой, высушен над MgSO4, и концентрирован до получения осадка, который был дополнительно высушен в вакуумном сушильном шкафу при 40°C. Полученный таким образом продукт был использован на следующей стадии без дополнительной очистки.
(c) Синтез 9-Ацетилоксим-O-ацетат-2-метокси-12,12-диетил-6,12-дигидро-6-тиа-индено[1,2-b]флуорена:
[00143] Триэтиламин (1.7 мл, 12.2 ммоль) был медленно добавлен в 100 мл раствора тетрагидрофурана, содержащего 9-ацетилоксим-2-метокси-12,12-диетил-6,12-дигидро-6-тиа-индено[1,2-b]флуорен (3.87 г, 10.0 ммоль) и ацетилхлорид (915 мкл, 12.8 ммоль) при 0°C под атмосферным азотом. После 3 часов перемешивания при комнатной температуре, реакционную смесь выливают в воду. Продукт был экстрагирован этилацетатом. Объединенный органический слой был промыт дважды водой, высушен с MgS04, и концентрирован до получения осадка, который был очищен посредством флэш-хроматографии с использованием этилацетат-гексана в качестве элюента. Растворитель был удален с использованием вакуумного выпаривания до получения белого порошкового продукта с 32% выходом и 99% чистотой.
Пример 1.4 - 7-Ацетилоксим-O-ацетат-12,12-диметил-10,12-дигидро-10-оксо-индено[2,1-b]флуорен
[00144] Синтез 7-Ацетилоксим-O-ацетат-12,12-диметил-10,12-дигидро-10-оксо-индено[2,1-b]флуорена был выполнен в соответствии со схемой, показанной на Фигуре 4.
(a) Синтез 7-бутирил-12,12-диметил-10,12-дигидро-10-оксо-индено[2,1-b]флуорена:
[00145] Хлорид алюминия (3.43 г, 25.6 ммоль) был медленно добавлен в раствор дихлорметана (80 мл) в котором был разбавлен 12,12-диметил-10,12-дигидро-10-оксо-индено[2,1-b]флуорен (5.68 г, 20.0 ммоль) и ацетилхлорид (1.83 мл, 25.7 ммоль) при 0°C под атмосферным азотом. После перемешивания при комнатной температуре в течение ночи, реакционная смесь была влита в ледяную воду. Продукт был дважды экстрагирован с дихлорметаном. Объединенный органический слой был промыт рассолом, и высушен над MgSO4. Дихлорметан был извлечен под высоким вакуумом и, полученный таким образом продукт, был использован на следующей стадии без дополнительной очистки.
(b) Синтез 7-бутирилоксим-12,12-диметил-10,12-дигидро-10-оксо-индено[2,1-b]флуорена:
[00146] 7-Бутирил-12,12-диметил-10,12-дигидро-10-оксо-индено[2,1-b]флуорен (3.26 г, 10.0 ммоль) был добавлен в раствор смеси, содержащей 100 мл 1,3-диоксана, натрия ацетат (1.06 г, 13.0 ммоль), хлорида гидроксиламмония (0.83 г, 12.0 ммоль) и воды (60 мл). Реакционную смесь кипятили с обратным холодильником в течение ночи, охладили до комнатной температуры, и затем выливают в воду. Продукт был экстрагирован этилацетатом. Объединенный органический слой был промыт дважды водой, высушен над MgSO4, и концентрирован до получения осадка, который был дополнительно высушен в вакуумном сушильном шкафу при 40°C. Полученный таким образом продукт был использован на следующей стадии без дополнительной очистки.
(c) Синтез 7-бутирилоксим-O-ацетат-12,12-диметил-10,12-дигидро-10-оксо-индено[2,1-b]флуорена:
[00147] Триэтиламин (1.7 мл, 12.2 ммоль) был медленно добавлен в раствор тетрагидрофурана (100 мл), содержащего 7-бутирилоксим-12,12-диметил-10,12-дигидро-10-оксо-индено[1,2-b]флуорен (3.41 г, 10.0 ммоль) и ацетилхлорид (915 мкл, 12.8 ммоль) при 0°C под атмосферным азотом. После 3 часов перемешивания при комнатной температуре, реакционную смесь выливают в воду. Продукт был экстрагирован этилацетатом. Объединенный органический слой был промыт дважды водой, высушен с MgSO4, и концентрирован посредством вакуумного выпаривания до получения осадка, который был очищен посредством флэш-хроматографии на силикагеле этилацетатом и гексаном в качестве элюентов. Растворитель был удален с использованием вакуумного выпаривания до получения белого порошкового продукта с 37% выходом и 99% чистотой.
Пример 1.5 - 8-Ацетилоксим-O-ацетат-11,13,13-триэтил-6,6-диметил-11,13-дигидро-6Н-11-аза-индено[2,1-b]антрацен
[00148] Синтез 8-ацетилоксим-O-ацетат-11,13,13-триэтил-6,6-диметил-11,13-дигидро-6Н-11-аза-индено[2,1-b]антрацена был выполнен в соответствии со схемой, показанной на Фигуре 5.
(a) Синтез 8-ацетил-11,13,13-триэтил-6,6-диметил-11,13-дигидро-6H-11-аза-индено[2,1-b] антрацена
[00149] Хлорид алюминия (3.43 г, 25.6 ммоль) был медленно добавлен в раствор дихлорметана (80 мл) в котором был разбавлен 11,13,13-триэтил-6,6-диметил-11,13-дигидро-6Н-11-аза-индено[2,1-b]антрацен (6.80 г, 20.0 ммоль) и ацетилхлорид (1.83 мл, 25.7 ммоль) при 0°C под атмосферным азотом. После перемешивания при комнатной температуре в течение ночи, реакционная смесь была влита в ледяную воду. Продукт был дважды экстрагирован дихлорметаном. Объединенный органический слой был промыт рассолом, и высушен над MgSO4. Дихлорметан был извлечен под высоким вакуумом и полученный таким образом продукт был использован на следующей стадии без дополнительной очистки.
(b) Синтез 8-ацетилоксим-11,13,13-триэтил-6,6-диметил-11,13-дигидро-6Н-11-аза-индено[2,1-b]антрацена
[00150] 8-Ацетил-11,13,13-триэтил-6,6-диметил-11,13-дигидро-6Н-11-аза-индено[2,1-b]антрацен (3.82 г, 10.0 ммоль) был добавлен в раствор смеси содержащей 100 мл 1,3-диоксана, натрия ацетата (1.06 г, 13.0 ммоль), хлорида гидроксиламмония (0.83 г, 12.0 ммоль) и воды (60 мл). Реакционную смесь кипятили с обратным холодильником в течение ночи, охладили до комнатной температуры, и затем выливают в воду. Продукт был экстрагирован этилацетатом. Объединенный органический слой был промыт дважды водой, высушен над MgSO4, и концентрирован до получения осадка, который был дополнительно высушен в вакуумном сушильном шкафу при 40°C. Полученные таким образом продукты были использованы на следующей стадии без дополнительной очистки.
(c) Синтез 8-ацетипоксим-O-ацетат-11,13,13-триэтил-6,6-диметил-11,13-дигидро-6Н-11-аза-индено[2,1-b]антрацена
[00151] Триэтиламин (1.7 мл, 12.2 ммоль) был медленно добавлен в 100 мл раствора тетрагидрофурана, содержащего 8-ацетилоксим-11,13,13-триэтил-6,6-диметил-11,13-дигидро-6Н-11-аза-индено[1,2-b]антрацен (3.97 г, 10.0 ммоль) и ацетилхлорид (915 мкл, 12.8 ммоль) при 0°C под атмосферным азотом. После 3 часов перемешивания при комнатной температуре, реакционную смесь выливают в воду. Продукт был экстрагирован этилацетатом. Объединенный органический слой был промыт дважды водой, высушен с MgSO4, и концентрирован посредством вакуумного выпаривания до получения осадка, который был очищен посредством флэш-хроматографии на силикагеле этилацетатом и гексаном в качестве элюентов. Растворитель был удален с использованием вакуумного выпаривания до получения белого порошкового продукта с 46% выходом и 99% чистотой.
Пример 1.6 - 10-(4-Ацетилоксим-O-ацетат фенил)-7-ацетилоксим-O-ацетат-2-метокси-12,12-дигексил-10,12-дигидро-10-аза-индено[2,1-b]флуорен
[00152] Синтез 10-(4-ацетилоксим-O-ацетат фенил)-7-ацетилоксим-O-ацетат-2-метокси-12,12-дигексил-10,12-дигидро-10-аза-индено[2,1-b]флуорена был выполнен в соответствии со схемой, показанной на Фигуре 6.
(a) Синтез 10-(4-ацетил фенил)-7-ацетж-2-метокси-12,12-дигексил-10,12-дигидро-10-аза-индено[2,1-b]флуорена:
[00153] Хлорид алюминия (8.00 г, 60.0 ммоль) был медленно добавлен в раствор дихлорметана (120 мл) в котором был разбавлен 2-метокси-10-фенил-12,12-дигексил-10,12-дигидро-10-аза-индено[2,1-b]флуорен (7.47 г, 20.0 ммоль) и ацетилхлорид (3.56 мл, 50.0 ммоль) при 0°C под атмосферным азотом. После перемешивания при комнатной температуре в течение ночи, реакционная смесь была охлаждена до комнатной температуры и влита в ледяную воду. Продукт был дважды экстрагирован дихлорметаном. Объединенный органический слой был промыт рассолом, и высушен над MgSO4. Дихлорметан был извлечен под высоким вакуумом и, полученный таким образом продукт, был использован на следующей стадии без дополнительной очистки.
(b) Синтез 10-(4-Ацетилоксим фенил)-7-ацетилоксим-2-метокси-12,12-дигексил-10,12-дигидро-10-аза-индено[2,1-b]флуорена:
[00154] 10-(4-ацетил фенил)-7-ацетил-2-метокси-12,12-дигексил-10,12-дигидро-10-аза-индено[2,1-b]флуорен (4.58 г, 10.0 ммоль) был добавлен в раствор смеси, содержащей 120 мл 1,3-диоксана, натрия ацетат (2.46 г, 30.0 ммоль), хлорид гидроксиламмония (2.08 г, 30.0 ммоль) и воду (80 мл). Реакционную смесь кипятили с обратным холодильником в течение ночи, охладили до комнатной температуры, и затем выливают в воду. Продукт был экстрагирован этилацетатом. Объединенный органический слой был промыт дважды водой, высушен над MgSO4, и концентрирован до получения осадка, который был дополнительно высушен в вакуумном сушильном шкафу при 40°C. Полученный таким образом продукт был использован на следующей стадии без дополнительной очистки.
(c) Синтез 10-(4-ацетилоксим-O-ацетат фенил)-7-ацетилоксим-O-ацетат-2-метокси-12,12-дигексил-10,12-дигидро-10-аза-индено[2,1-b]флуорена:
[00155] Триэтиламин (4.18 мл, 30.0 ммоль) был медленно добавлен в 100 мл раствора тетрагидрофурана, содержащего 10-(4-Ацетилоксим фенил)-7-Ацетилоксим-2-метокси-12,12-дигексил-10,12-дигидро-10-аза-индено[2,1-b]флуорен (4.88 г, 10.0 ммоль) и ацетилхлорид (2.13 мл, 30.0 ммоль) при 0°C под атмосферным азотом. После 5 часов перемешивания при комнатной температуре, реакционную смесь выливают в воду. Продукт был экстрагирован этилацетатом. Объединенный органический слой был промыт дважды водой, высушен MgSO4, и концентрирован посредством вакуумного выпаривания до получения осадка, который был очищен посредством флэш-хроматографии на силикагеле с этилацетатом и гексаном в качестве элюентов. Растворитель был удален с использованием вакуумного выпаривания до получения белого порошкового продукта с 56% выходом и 99% чистотой.
Пример 1.7 - 10-(4-Ацетилоксим-O-ацетат фенил)-2,7-диацетилоксим-O-ацетат-12,12-дигексил-10,12-дигидро-10-аза-индено[2,1-b]флуорен:
[00156] Синтез 10-(4-Ацетилоксим-O-ацетат фенил)-2,7-диацетилоксим-O-ацетат-12,12-дигексил-10,12-дигидро-10-аза-индено[2,1-b]флуорена был выполнен в соответствии со схемой, показанной на Фигуре 7.
(a) Синтез 10-(4-ацетил фенил)-2,7-диацетил-12,12-дигексил-10,12-дигидро-10-аза-индено[2,1-b]флуорена:
[00157] Хлорид алюминия (12.0 г, 90.0 ммоль) был медленно добавлен в раствор дихлорметана (120 мл), в котором был разбавлен 10-этил-12,12-дигексил-10,12-дигидро-10-аза-индено[2,1-b]флурен (7.20 г, 20.0 ммоль) и ацетилхлорид (6.40 мл, 90.0 ммоль) при 0°C под атмосферным азотом. После кипячения в течение ночи, реакционная смесь была охлаждена до комнатной температуры и влита в ледяную воду. Продукт был дважды экстрагирован с дихлорметаном. Объединенный органический слой был промыт рассолом, и высушен над MgSO4. Дихлорметан был извлечен под высоким вакуумом и, полученный таким образом продукт, был использован на следующей стадии без дополнительной очистки.
(b) Синтез 10-(4-Ацетилоксим фенил)-2,7-диацетилоксим-12,12-дигексил-10,12-дигидро-10-аза-индено[2,1-b]флуорена:
[00158] 10-(4-Ацетилфенил)-2,7-диацетил-12,12-дигексил-10,12-дигидро-10-аза-индено[2,1-b]флуорен (4.86 г, 10.0 ммоль) был добавлен в раствор смеси, содержащей 150 мл 1,3-диоксана, натрия ацетат (4.92 г, 60.0 ммоль), хлорида гидроксиламмоний (4.17 г, 60.0 ммоль) и воду (100 мл). Реакционную смесь кипятили с обратным холодильником в течение ночи, охладили до комнатной температуры, и затем выливают в воду. Продукт был экстрагирован этилацетатом. Объединенный органический слой был промыт дважды водой, высушен над MgSO4, и концентрирован до получения осадка, который был дополнительно высушен в вакуумном сушильном шкафу при 40°C. Полученный таким образом продукт был использован на следующей стадии без дополнительной очистки.
(c) Синтез 10-(4-ацетилоксим-O-ацетат фенил)-2,7-диацетилоксим-O-ацетат-12,12-дигексил-10,12-дигидро-10-аза-индено[2,1-b]флуорена:
[00159] Триэтиламин (8.36 мл, 60.0 ммоль) был медленно добавлен в 100 мл раствора тетрагидрофурана содержащего 10-(4-ацетилоксим фенил)-2,7-диацетилоксим-12,12-дигексил-10,12-дигидро-10-аза-индено[2,1-b]флуорен (5.31 г, 10.0 ммоль) и ацетилхлорид (4.27 мл, 60.0 ммоль) при 0°C под атмосферным азотом. После 3 часов перемешивания при комнатной температуре, реакционную смесь выливают в воду. Продукт был экстрагирован этилацетатом. Объединенный органический слой был промыт дважды водой, высушен с MgSO4, и концентрирован посредством вакуумного выпаривания до получения осадка, который был очищен посредством флэш-хроматографии на силикагеле этилацетатом и гексаном в качестве элюентов. Растворитель был удален с использованием вакуумного выпаривания до получения белого порошкового продукта с 45% выходом и 99% чистотой.
Пример 1.8 - 3,9-Диацетилоксим-O-ацетат-6-гексил-6H-12-тиа-6-аза-индено[1,2-b]флуорен
[00160] Синтез 3,9-диацетилоксим-O-ацетат-6-гексил-6H-12-тиа-6-аза-индено[1,2-b]флуорена был выполнен в соответствии со схемой, показанной на Фигуре 8.
(a) Синтез 3,9-диацетил-6-гексил-6Н-12-тиа-6-аза-индено[1,2-b]флуорена:
[00161] Хлорид алюминия (8.00 г, 60.0 ммоль) был медленно добавлен в раствор дихлорметана (120 мл) в котором был разбавлен 6-гексил-6Н-12-тиа-6-аза-индено[1,2-b]флуорен (5.75 г, 20.0 ммоль) и ацетилхлорид (3.56 мл, 50.0 ммоль) при 0°C под атмосферным азотом. После перемешивания при комнатной температуре в течение ночи, реакционная смесь была охлаждена до комнатной температуры и влита в ледяную воду. Продукт был дважды экстрагирован дихлорметаном. Объединенный органический слой был промыт рассолом, и высушен над MgSO4. Дихлорметан был извлечен под высоким вакуумом и полученный таким образом продукт был использован на следующей стадии без дополнительной очистки.
(b) Синтез 3,9-диацетилоксим-6-гексил-6H-12-тиа-6-аза-индено[1,2-b]флуорена:
[00162] 3,9-диацетил-6-гексил-6Н-12-тиа-6-аза-индено[1,2-b]флуорен (3.71 г, 10.0 ммоль) был добавлен в раствор смеси, содержащей 120 мл 1,3-диоксана, натрия ацетат (3.28 г, 40.0 ммоль), хлорида гидроксиламмоний (2.78 г, 40.0 ммоль) и воду (80 мл). Реакционную смесь кипятили с обратным холодильником в течение ночи, охладили до комнатной температуры, и затем выливают в воду. Продукт был экстрагирован этилацетатом. Объединенный органический слой был промыт дважды водой, высушен над MgSO4, и концентрирован до получения осадка, который был дополнительно высушен в вакуумном сушильном шкафу при 40°C. Полученный таким образом продукт был использован на следующей стадии без дополнительной очистки.
(c) Синтез 3,9-диацетилоксим-O-ацетат-6-гексил-6H-12-тиа-6-аза-индено[1,2-b]флуорена:
[00163] Триэтиламин (5.78 мл, 40.0 ммоль) был медленно добавлен в 100 мл раствора тетрагидрофурана, содержащего 3,9-диацетилоксим-6-гексил-6Н-12-тиа-6-аза-индено[1,2-b]флуорен (4.01 г, 10.0 ммоль) и ацетилхлорид (3.45 мл, 40.0 ммоль) при 0°C под атмосферным азотом. После 3 часов перемешивания при комнатной температуре, реакционную смесь выливают в воду. Продукт был экстрагирован этилацетатом. Объединенный органический слой был промыт дважды водой, высушен с MgSO4, и концентрирован посредством вакуумного выпаривания до получения осадка, который был очищен посредством флэш-хроматографии на силикагеле этилацетатом и гексаном в качестве элюентов. Растворитель был удален с использованием вакуумного выпаривания до получения белого порошкового продукта с 68% выходом и 99% чистотой.
Пример 1.9 - 10-гексил-10Н-10-аза-индено[2,1-b]флуорен-12-O-ацетилоксим
[00164] Синтез 10-гексил-10Н-10-аза-индено[2,1-b]флуорен-12-O-ацетилоксим был выполнен в соответствии со схемой, показанной на Фигуре 9.
(a) Синтез 10-гексил-10H-10-аза-индено[2,1-b]флуорен-12-оксима:
[00165] 10-гексил-10H-10-аза-индено[2,1-b]флуорен-12-он (2.83 г, 10.0 ммоль) и хлорид гидроксиламмония (3.35 г, 40.0 ммоль) были растворены в 120 мл 1,3-диоксана. Пиридин (3.96, 50 ммоль) был добавлен в раствор с помощью шприца. Реакционную смесь перемешивали в течение ночи. Растворитель был удален посредством вакуумного выпаривания и затем вылит в воду. Продукт был экстрагирован этилацетатом. Объединенный органический слой был промыт дважды водой и рассолом, высушен над MgSO4 и концентрирован до получения осадка, который был дополнительно высушен в вакуумном сушильном шкафу при 40°C. Полученный таким образом продукт был использован на следующей стадии без дополнительной очистки.
(b) Синтез 10-гексил-10H-10-аза-индено[2,1-b]флуорен-12-O-ацетилоксима:
[00166] Триэтиламин (3.40 мл, 24.4 ммоль) был медленно добавлен в 80 мл раствора тетрагидрофурана, содержащего 10-гексил-10H-10-аза-индено[2,1-b]флуорен-12-оксим (2.98 г, 10.0 ммоль) и ацетилхлорид (1.83 мл, 25.6 ммоль) при 0°C под атмосферным азотом. После 3 часов перемешивания при комнатной температуре, реакционную смесь выливают в воду. Продукт был экстрагирован этилацетатом. Объединенный органический слой был промыт дважды водой, высушен с MgSO4, и концентрирован посредством вакуумного выпаривания до получения осадка, который был очищен посредством флэш-хроматографии на силикагеле этилацетатом и гексаном в качестве элюентов. Растворитель был удален с использованием вакуумного выпаривания до получения белого порошкового продукта с 86% выходом и 99% чистотой.
Пример 1.10 - 7,7'-Ацетилоксим-O-ацетат-1,1'-Диметил-бисиндено[3,2-b:2',3'-h]-9-сек-бутил карбазол
[00167] Синтез 7,7'-ацетилоксим-O-ацетат-1,1'-Диметил-бисиндено[3,2-b:2',3'-b]-9-сек-бутил карбазола был выполнен в соответствии со схемой, показанной на Фигуре 10.
(a) Синтез 7,7'-ацетил-1,1'-диметил-бисиндено[3,2-b:2',3'-h]-9-сек-бутил карбазола:
[00168] Хлорид алюминия (8.00 г, 60.0 ммоль) был медленно добавлен в раствор дихлорметана (150 мл), в котором был разбавлен 1,1'-диметил-бисиндено[3,2-b:2',3'-h]-9-сек-бутил карбазол (9.12 г, 20.0 ммоль) и ацетилхлорид (3.56 мл, 50.0 ммоль) при 0°C под атмосферным азотом. После перемешивания при комнатной температуре в течение ночи, реакционная смесь была охлаждена до комнатной температуры и влита в ледяную воду. Продукт был дважды экстрагирован дихлорметаном. Объединенный органический слой был промыт рассолом, и высушен над MgSO4. Дихлорметан был извлечен под высоким вакуумом и, полученный таким образом продукт, был использован на следующей стадии без дополнительной очистки.
(b) Синтез 7,7'-ацетилоксим-1,1'-диметил-бисиндено[3,2-b:2',3'-h]-9-сек-бутилкарбазола:
[00169] 7,7'-Ацетил-1,1'-диметил-бисиндено[3,2-b:2',3'-h]-9-сек-бутил карбазол (5.40 г, 10.0 ммоль) был добавлен в раствор смеси, содержащей 120 мл 1,3-диоксана, натрия ацетат (2.46 г, 30.0 ммоль), хлорид гидроксиламмония (2.08 г, 30.0 ммоль) и воду (80 мл). Реакционную смесь перемешивали при комнатной температуре в течение ночи, охлаждали до комнатной температуры, и затем выливали в воду. Продукт был экстрагирован этилацетатом. Объединенный органический слой был промыт дважды водой, высушен над MgSO4, и концентрирован до получения осадка, который был дополнительно высушен в вакуумном сушильном шкафу при 40°C. Полученный таким образом продукт был использован на следующей стадии без дополнительной очистки.
(c) Синтез 7,7'-ацетилоксим-O-ацетат-1,1'-диметил-бисиндено[3,2-b:2',3'-h]-9-сек-бутил карбазола:
[00170] Триэтиламин (4.18 мл, 30.0 ммоль) был медленно добавлен в 100 мл раствора тетрагидрофурана, содержащего 7,7'-Ацетилоксим-1,1'-диметил-бисиндено[3,2-b:2',3'-h]-9-сек-бутил карбазол (5.70 г, 10.0 ммоль) и ацетилхлорид (2.13 мл, 30.0 ммоль) при 0°C под атмосферным азотом. После 5 часов перемешивания при комнатной температуре, реакционную смесь выливают в воду. Продукт был экстрагирован этилацетатом. Объединенный органический слой был промыт дважды водой, высушен MgS04, и концентрирован посредством вакуумного выпаривания до получения осадка, который был очищен посредством флэш-хроматографии на силикагеле этилацетатом и гексаном в качестве элюентов. Растворитель был удален с использованием вакуумного выпаривания до получения белого порошкового продукта с 76% выходом и 99% частотой.
Примеры 1.11 и следующие
[00171] Синтез фотоинициаторов по примерам 1.11 и следующих был проведен в высушенной огнем стеклянной посуде, которая была снабжена механической мешалкой, конденсатором воды, нагревательным металлом, патрубком ввода азотного газа и температурным контролером. Полученные продукты и промежуточные продукты были охарактеризованы посредством УК Фурье-спектрофотометра (Perkin Elmer, Model Spectrum 100), ЯМР (Nicolet 500 МГц), спектрофотометра в УФ- и видимой ообластях света (Perkin Elmer, Model Lambda 25), ДСК (ТА Instruments, Model Q2000), ТГА (TA Instrument, Model Q500), и ВЭЖХ (Waters, Model Breeze 2).
Пример 1.11 - 2,7,12 Триацетилоксим-O-ацетат-5,5',10,10',15,15'-гексагексилтруксен
[00172] Синтез 2,7,12 триацетилоксим-O-ацетат-5,5',10,10',15,15'-гексагексилтруксена был выполнен, как указано далее.
(a) Синтез 2,7,12-триацетилоксим-5,5',10,10',15,15'-гексагексилтруксена:
[00173] 2,7,12-Триацетил-5,5',10,10',15,15'-гексагексилтруксен (получен в соответствии с Примером 1.16 ниже) был растворен в 180 мл диоксана в 500 мл колбе. Натрия ацетат (283 мг) и гидроксиламин HCl (256 мг) были растворены в 60 мл воды в 100 мл колбе. Этот раствор был добавлен к раствору триацетилгексагексилтруксена, которые затем нагревали при кипении в течение ночи. Большую часть диоксана удаляют при низком давлении (продукт осажденный), а затем было добавлено 300 мл воды. Суспензию перемешивали в течение 30 минут при комнатной температуре, и затем фильтровали до получения 950 мг (91%) желтоватого порошка.
[00174] H1 ЯМР (500 МГц, CDCl3) δ: 8.51-8.46 (m, 3H); 8.12-8.07 (m, 3H); 7.84-7.79 (m, 3H); 3.05-2.92 (m, 6H); 2.70-2.60 (m, 9H); 2.65-2.57 (m, 6H); 2.32-2.17 (m, 36H); 1.05-0.82 (m, 18H); 0.65-0.49 (m, 12H).
(b) Синтез 2,7,12-триацетилоксим-O-ацетат-5,5',10,10',15,15'-гексагексилтруксена:
[00175] 2,7,12-Триацетилоксим-5,5',10,10',15,15'-гексагексилтруксен был растворен в 60 мл ТГФ в высушенной огнем 100 мл колбе под N2. Раствор был охлажден до 0°C в ледяной бане. Триэтиламин (225 мкл) был добавлен, и затем ацетилхлорид (120 мкл) медленно добавляли. Образовался белый осадок. Ход реакции контролировали с помощью ТСХ с использованием 15% EtOAc в гексане. После 2 часов при комнатной температуре, реакционная смесь была извлечена с использованием EtOAc и воды, высушена над MgSO4, тщательно высушена под вакуумом, и затем суспендирована в метаноле. Эту суспензию обрабатывали ультразвуком в течение 30 минут и затем фильтровали до получения 235 мг (32%, ВЭЖХ чистота + 99%) белого порошка.
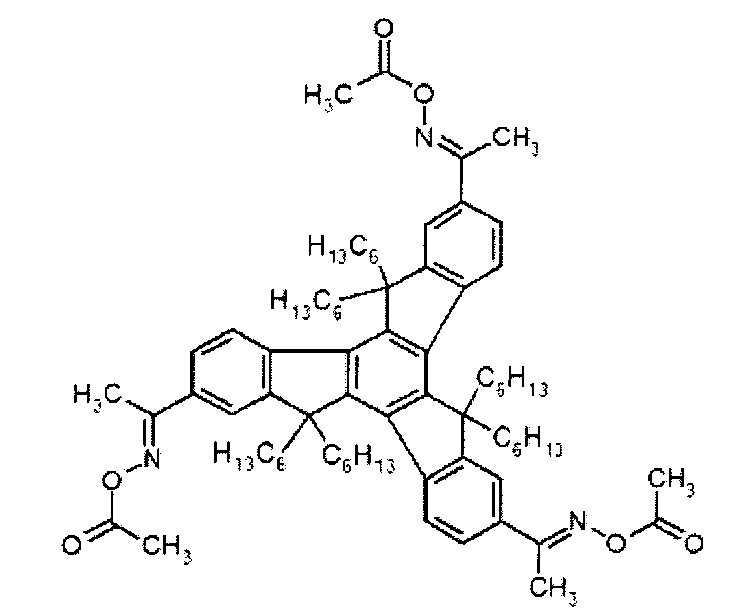
[00176] H1 ЯМР (500 МГц, CDCl3) δ 8.42 (d, J=8.5 Hz, 3H); 7.88 (dd, J1=1.7 Hz, J2=8.4 Hz, 3H); 7.82 (d, J=1.7 Hz, 3H); 2.97-2.91 (m, 6H); 2.54 (s, 9H); 2.35 (s, 9H); 2.18-2.11 (m, 6H); 0.98-0.80 (m, 36H); 0.62 (t, J=7.2 Hz, 18H); 0.52-0.45 (m, 12H).
Пример 1.12 - 3,8,13-Триацетил-5,10,15-Тригексил-10,15-дигидро-5H-5,10,15-триазадииндено[1,2-a;1',2'-c]флуорен триоксим три-O-ацетат (2E)
[00177] Синтез 3,8,13-триацетил-5,10,15-тригексил-10,15-дигидро-5Н-5,10,15-триазадииндено [1,2-a;1',2'-c]флуорен триоксим три-O-ацетата был выполнен как указано далее.
(a) Синтез
3,8,13-триацетил-5,10,15-тригексил-10,15-дигидро-5Н-5,10,15-триазадииндено [1,2-a;1',2'-c]-флуорен триоксима:
[00178] 3,8,13-Триацетил-5,10,15-тригексил-10,15-дигидро-5H-5,10,15-триазадииндено[1,2-a;1',2'-c]флуорена (800 г, 1.10 ммоль, из Примера 1.17 ниже) был растворен в 1,4-диоксане (120 мл) под азотом. Реакционная смесь была осторожно нагрета до растворения твердого вещества. Раствор натрия ацетата (285 мг, 4.32 ммоль) и гидроксил аммония хлорида (255 мг, 3.67 ммоль) в воде (40 мл) был добавлен в реакционную смесь, которую затем нагревают с обратным холодильником в течение 24 ч. Ход реакции контролировали с помощью ТСХ с использованием этилацетата (20%) и гексана (80%) в качестве элюента. После того, как реакция была завершена, продукт осаждают в холодной воде (200 мл). Бежевый твердый продукт, полученный посредством вакуумной фильтрации, обильно промывают водой и сушат под вакуумом при 30°C до постоянного веса (790 мг, 93% выход).
(b) Синтез
3,8,13-триацетил-5,10,15-тригексил-10,15-дигидро-5H-5,10,15-триазадииндено[1,2-a;1',2'-c]-флуорен триоксим три-O-ацетата:
[00179] Ацетилхлорид (167 мкл, 2.34 ммоль) был медленно добавлен в раствор тетрагидрофурана (500 мл) содержащий 3,8,13-триацетил-5,10,15-тригексил-10,15-дигидро-5H-5,10,15-триазадииндено [1,2-a;1',2'-c]флуорен триоксим (500 мг, 0.65 ммоль) и триэтиламин (312 мкл, 2.24 ммоль). Реакционную смесь перемешивали в течение ночи. Затем растворитель выпаривали при пониженном давлении до получения темно-коричневого масла. Оно было очищено с помощью колоночной хроматографии с использованием подвижной фазы силикагеля и смеси этилацетата и гексана в качестве элюента. Растворитель был выпарен в вакууме с получением бледно-коричневого твердого вещества (207 мг, 40%). Температура плавления и температура деструкции были определены с помощью дифференциального сканирующего калориметра и термогравиметрического анализа около 124°C и 260°C соответственно.

[00180]1H ЯМР (500 МГц, CDCl3) δ 8.71 (s, 3H), 7.88 (d, J=8.6 Hz, 3H), 7.66 (d, J=8.6 Hz, 3H), 4.98 (t, J=7.5 Hz, 6H), 2.60 (s, 9H), 2.36 (s, 9H), 1.95 (p, J=6.6 Hz, 6H), 1.20-1.11 (m, 18H), 0.76 (t, J=7.1 Hz, 9H).
Пример 1.13 - 4,9,13-триэтоксиацетилоксим-O-триацетаттруксенонон
[00181] Синтез 4,9,13-триэтоксиацетилоксим-O-триацетаттруксенона был выполнен в соответствии со схемой, показанной на Фигуре 11.
(a) Синтез 4,9,13-триэтоксиацетилтруксенона (3B):
[00182] Треххлористый алюминий (1.47 г, 11.02 ммоль) был медленно добавлен в раствор, содержащий дихлорметан (10 мл) и труксенон (3A, 1.29 г, 3.35 ммоль). Раствор становится темно-красным. Затем, этоксиацетилхлорид (1.81 г, 14.75 ммоль) был добавлен каплями в течение периода времени 2 минуты. Реакция продолжалась на протяжении 36 часов. Затем реакционная смесь была быстро отфильтрована и концентрирована под вакуумом до получения вязкого продукта. Обезвоженный этанол (15 мл) был добавлен для образования густой суспензии, которая была размещена в ультразвуковой бане в течение 30 минут. Твердый продукт был отфильтрован, обильно промыт этанолом и высушен под высоким вакуумом при 30°C в течение ночи до получения бледно-желтого твердого вещества (1.83 г, 85% выход).
(b) Синтез 4,9,13-триэтоксиацетилоксимтруксенона (3C):
[00183] 4,9,13-Триэтоксиацетилтруксенона (707 мг, 1.10 ммоль) был растворен в 1,4-диоксане (120 мл) под азотом. Реакционная смесь была осторожно нагрета до растворения твердого вещества. Раствор натрия ацетата (285 мг, 4.32 ммоль) и гидроксильного хлорида аммония (255 мг, 3.67 ммоль) в воде (40 мл) был добавлен в реакционную смесь, которую затем нагревают с обратным холодильником в течение 24 часов. Ход реакции контролировали с помощью ТСХ с применением этилацетата (20%) и гексана (80%) как элюента. После того, как реакция была завершена, продукт был осажден в холодной воде (200 мл). Бежевый твердый продукт был получен под вакуумной фильтрацией, обильно промыт водой и высушен под вакуумом при 30°C до постоянной массы (680 мг, 90% выход).
(c) Синтез 4,9,13-триэтоксиацетшоксим-O-триацетаттруксенона (3D):
[00184] Ацетилхлорид (167 мкл, 2.34 ммоль) был медленно добавлен в раствор тетрагидрофурана (500 мл), содержащего 4,9,13-триэтоксиацетилоксимтруксенона (447 мг, 0.65 ммоль) и триэтиламин (312 мкл, 2.24 ммоль). Реакционную смесь перемешивали в течение ночи. Затем растворитель был испарен при пониженном давлении с получением темно-коричневого масла. Он был очищен с помощью колоночной хроматографии с применением подвижной фазы силикагеля и смеси этилацетата и гексана в качестве элюента. Растворитель был испарен под вакуумом с получением бледного твердого продукта (158 мг, 30%).
Пример 1.14
3,8,13-Тригексаноил-5,10,15-тригексил-10,15-дигидро-5H-5,10,15-триазадииндено[1,2-a;1',2'-c]флуорен триоксим три-O-ацетат
[00185] Синтез
3,8,13-тригексаноил-5,10,15-тригексил-10,15-дигидро-5Н-5,10,15-триазадииндено [1,2-a;1',2'-c]флуорен триоксим три-O-ацетата (показано ниже) был выполнен подобно Примеру 1.11 за исключением того, что ацетилхлорид был заменен гексаноил хлоридом на этапе (b).

[00186] 3,8,13-Тригексаноил-5,10,15-тригексил-10,15-дигидро-5H-5,10,15-триазадииндено [1,2-a;1',2'-c]флуорен триоксим три-O-ацетат был получен как белое твердое вещество с 28% общего выхода.
[00187]1H ЯМР (500 МГц, CDCl3) δ: 8.69 (s, 3H), 7.83 (d, J=8.4 Hz, 3H), 7.67 (d, J=8.7 Hz, 3H), 5.00 (t, J=7.1 Hz, 6H), 3.05 (t, J=7.8 Hz, 6H), 2.35 (s, 9H), 1.95 (p, J=7.1 Hz, 6h), 1.72 (p, J=7.6 Hz, 6H), 1.50-1.44 (m, 6H), 1.41 (p, J=7.4 Hz, 6H), 1.25-1.13 (m, 18H), 0.94 (t, J=7.3 Hz, 9H), 0.76 (t, J=7.1 Hz, 9H).
[00188] Спектры в видимой и в УФ-области 3,8,13-триацетил-5,10,15-тригексил-10,15-дигидро-5Н-5,10,15-триазадииндено [1,2-a;1',2'-c]флуорен триоксим три-O-ацетата показаны на Фигуре 12. Этот спектр показал ссыльные полосы поглощения между 300 и 400 нм. Более конкретно, спектр показывает сильное поглощение при 365 нм, следующее за резким снижением. Это повышает чувствительность, избегая при этом помехи цвета.
Пример 1.15 - 2,7,12-три(4-ацетилфенил)-5,5,10,10,15,15-гексагексил-10,15-дигидро-5H-дииндено[1,2-a;1',2'-c]флуорен триоксим три-O-ацетат
(a) Синтез 2,7,12-три(4-ацетилфенил)-5,5,10,10,15,15-гексагексш-10,15-дигидро-5H-дииндено[1,2-a;1',2'-c]флуорен триоксима
[00189] В 100 мл 3-горлой колбе 2,7,12-три(4-ацетилфенил)-5,5',10,10',15,15'-гексагексилтруксен (6 г) был растворен в диоксане (50 мл) под атмосферой азота. Раствор хлорида гидроксиламмония (346 мг) и натрия ацетата (329 мг) в воде (15 мл) был добавлен к этому раствору. Реакционную смесь кипятили с обратным холодильником на протяжении 12 ч. Ход реакции мониторили с помощью ТСХ с использованием 5% этилацетата в толуоле. Растворитель был испарен при пониженном давлении. Затем вода (250 мл) была добавлена и соединение было отфильтровано до получения вязкого твердого вещества. Продукт был очищен перекристаллизацией в метаноле и оставлен при -20°С на всю ночь. Соединение (показано ниже) было отфильтровано до получения 4 г (65%) белого порошка.

[00190]1H ЯМР (500 МГц, CDCl3) δ 8.52-8.50 (m, 3H); 8.03-7.94 (m, 6H); 7.91-7.85 (m, 6H); 7.79-7.73 (m, 6H); 3.05 (s, 6H); 2.71 (s, 9H); 2.22 (s, 6H); 0.96-0.90 (m, 36H); 0.63-0.61 (m, 30H).
(b) 2,7,12-Три(4-ацетилфенил)-5,5,10,10,15,15-гексагексил-10,15-дигидро-5Н-дииндено[1,2-a;1',2'-c]флуорен триоксим три-O-ацетат
[00191] В высушенную в пламени 1 л 3-горлую колбу был добавлен сухой тетрагидрофуран и 2,7,12-Три(4-ацетилфенил)-5,5,10,10,15,15-гексагексил-10,15-дигидро-5H-дииндено[1,2-a;1',2'-c]флуорен триоксим (3 г) под азотом. Реакционная смесь была оставлена для охлаждения до 0°C в ледяной бане до добавления триэтиламина (1.1 мл). Реакционную смесь перемешивали на протяжении 5 мин до медленного добавления ацетилхлорида (0.591 мл). Реакционную смесь перемешивали 2 ч при 0°C и контролировали с помощью ТСХ с применением 5% этилацетата в толуоле как элюенте. Реакционная смесь была экстрагирована в этилацетат и воду, высушена над сульфатом магния и растворитель испаряли при пониженном давлении. Затем метанол (500 мл) был добавлен каплями к неочищенному продукту и раствор был нагрет и отфильтрован. Неочищенный продукт был растворен в 2-пропаноле, раствор был нагрет, и оставлен при -20°C на протяжении 1 ч и затем отфильтрован до получения 2 г (60%) белого порошка.

[00192]1H ЯМР (500 МГц, CDCl3) δ 8.48 (d, J=8.4 Hz, 3H); 7.94 (d, J=8.6 Hz, 6H); 7.84 (d, J=8.6 Hz, 6H); 7.74-7.72 (m, 6H); 3.08-3.01 (m, 6H); 2.50 (s, 9H); 2.34 (s, 9H) 2.24-2.15 (m, 6H); 1.03-0.85 (m, 36H); 0.64-0.58 (m, 30H).
[00193] Оптическая спектроскопия (ТГФ): 338 нм. DSC: 124°C. ИК (KBr): 2955, 2924, 2855, 1772, 1603, 1478, 1364, 1318, 1199, 984, 933, 890, 830, 808.
[00194] Фигура 13 иллюстрирует УФ-спектр Carba-05 (который представляет собой Irgacure ОХЕ-02 от BASF), и Truxe-08 и Truxe-07 (from above). Пример и и Truxe-12 (из Пример 1.15). Спектры нормированы так, что максимальное поглощение Carba-05 составляет 1. На этой фигуре, Carba-05 представляет собой кривую с максимумом поглощения при 277 нм относительной абсорбции при 365 нм или 0.161. Truxe-08 имеет два абсорбционных пика при 304 и 333 нм с относительной абсорбцией при 365 нм 0.754. Truxe-07 имеет один абсорбционный пик при 325 нм и относительное поглощение при 365 нм 0.043. Наконец, Truxe-12 имеет абсорбционный пик при 338 нм и относительную абсорбцию при 365 нм 0.666. Следует отметить, что Truxe-12 более высокую абсорбцию, чем ОХЕ-02.
Пример 1.16 - 2,7,12-триацетил-5,5',10,10',15,15'-гексагексилтруксена (INDENO 332)
[00195] Синтез 2,7,12-триацетил-5,5',10,10',15,15'-гексагексилтруксена был осуществлен растворением 4.3 грамм 5,5',10,10',15,15'-гексагексилтруксена в 250 мл высушенную пламенем колбу, содержащей 50 мл дихлорметана под N2. Ацетилхлорид (1.83 мл) был добавлен, и затем хлорид алюминия (3.27 г) был медленно добавлен в течение периода 15 минут. Реакционная смесь была перемешана при комнатной температуре в течение ночи. Реакция была проконтролирована ТСХ с применением 2.5% EtOAc в толуоле как элюенте. Экстракция была выполнена с применением дихлорметана и воды. Смесь затем была высушена над сульфатом магния. Неочищенный продукт был аккуратно высушен при высоком вакууме, осажден в метаноле и затем отфильтрован до получения белого порошка (5.5 г, 72%).

[00196] H1 ЯМР (500 МГц, CDCl3) δ 8.49 (d, J=8.4 Hz, 3H); 8.12 (d, J=1.7 Hz, 3H); 8.07 (dd, J1=1.7, J2=8.3 Hz, 3H); 3.00 2.94 (m, 6H); 2.76 (s, 9H); 2.25 2.19 (m, 6H); 0.98 0.79 (m, 36H); 0.61 (t, J=7.1, 18H); 0.52 0.44 (m, 12H).
[00197] Максимальный пик поглощения и абсорбционный пик 2,7,12-триацетил-5,5',10,10',15,15'-гексагексилтруксена в растворе тетрагидрофурана составляют 332 нм и 8.66×104 л/моль см, соответственно. Температура плавления была измерена и оказалась равной 217°C с помощью ДСК.
Пример 1.17 - 3,8,13-Триацетил-5,10,15-тригексил-10,15-дигидро-5H-5,10,15-триазадииндено[1,2-a;1',2'-c]-флуорен (INDENO 336)
[00198] Синтез 3,8,13-триацетил-5,10,15-тригексил-10,15-дигидро-5Н-5,10,15-триазадииндено [1,2-a;1',2'-c]-флуорена был сделан, медленно добавляя треххлористый алюминий (1.47 г, 11.02 ммоль) в растворе, содержащем дихлорметан (10 мл) и 5,10,15-тригексил-10,15-дигидро-5H-5,10,15-триазадииндено[1,2-a;1',2'-c]флуорен (2 г, 3.35 ммоль). Раствор становится темно-красным. Затем, ацетилхлорид (750 мкл, 14.75 ммоль) был добавлен каплями в течение периода 2 минут. Ход реакции мониторили с помощью ТСХ с применением смеси этилацетата (30%) и гексана (70%) как элюента. После того, как реакция завершена, реакционная смесь была быстро отфильтрована и концентрирована под вакуумом до получения вязкого красного продукта. Обезвоженный этанол (15 мл) был добавлен для формирования густой суспензии, которая была размещена в ультразвуковой бане на протяжении 30 минут. Твердое вещество было отфильтровано, обильно промыто этанолом и высушено под высоким вакуумом при 30°C в течение ночи до получения бледно-красного твердого вещества (1.93 г, 80% выход).

[00199]1H ЯМР (500 МГц, CDCl3) δ 9.02 (s, 3H), 8.13 (d, J=8.6 Hz, 3H), 7.66 (d, J=8.5 Hz, 3H), 5.00 (t, J=1.1 Hz, 6H), 2.80 (s, 9H), 1.99 (p, J=7.6 Hz, 6H), 1.33 (p, J=7.3 Hz, 6H), 1.26-1.17 (m, 12H), 0.78 (t,J=7.1 Hz, 9H).
[00200] Максимальный пик поглощения и абсорбционный пик
3,8,13-триацетил-5,10,15-тригексил-10,15-дигидро-5Н-5,10,15-триазадииндено[1,2-a; 1',2'-c]-флуорена в растворе тетрагидрофурана представляет собой 336 нм и 7.40×104 л моль-1см-1 соответственно.
Пример 1.18 - 2,7,12-три(4-ацетилфенил)-5,5',10,10',15,15'-гексагексилтруксен
[00201] TRUXE-03 или (8.5 г), 4-ацетилфенилбориновой кислоты (4.2 г) и толуола (500 мл) было введено в 500 мл колбу, промытую азотом. Карбонат калия (28 г), растворенный в воде (100 мл) был добавлен к этой смеси. Реакционную смесь барботируют азотом на протяжении 30 мин. Затем, ацетат палладия (52 мг) и трифенилфосфин (62 мг) были добавлены к раствору. Реакционную смесь нагревали с обратным холодильником в течение 2 дней до добавления 4-ацетилфенилбориновой кислоты (4.2 г). Реакционную смесь снова кипятили в течение 2 дней до окончательного добавления 4-ацетилфенилбориновой кислоты (4.2 г). Затем реакционную смесь кипятили с обратным холодильником на протяжении 4 дней. Ход реакции контролировали с применением 100% толуола как элюента. Реакционная смесь была промыта три раза водой, высушена над сульфатом магния и сконцентрирована при пониженном давлении. Смесь быстро пропускали через площадку силикагеля с применением 100% толуола как элюента до получения 7 г (75%) желаемого продукта.

[00202]]Н ЯМР (500 МГц, CDCl3) δ 8.50 (d, J=8.3 Hz, 3H); 8.14 (d, J=8.6 Hz, 6H); 7.89 (d, J=8.5 Hz, 6H); 7.77-7.75 (m, 6H); 3.08-3.02 (m, 6H); 2.72 (s, 9H); 2.25-2.19 (m, 6H); 1.05-0.85 (m, 36H); 0.64-0.58 (m, 30H).
[00203] Максимальный пик поглощения и абсорбционный пик 2C в растворе тетрагидрофурана представляет собой 340 нм и 12.64×104 л моль-1см-1, соответственно. Температура плавления составляет 85°C.
Пример 1.19 - 2,7,12-три-(о-toluloyl)-5,5',10,10',15,15'-гексагексилтруксен (INDENO 337)
[00204] 5,5',10,10',15,15'-Гексагексилтруксен (1.1 г) был растворен в 10 мл CH2Cl2 в 100 мл колбе под N2. o-Toluloyl chloride (638 мг, 3.20 экв.) был добавлен и затем хлорид алюминия (525 мг, 3.05 экв.) был медленно добавлен в течение периода 15 минут. Реакционную смесь перемешивали при комнатной температуре в течение ночи. Ход реакции мониторили с помощью ТСХ с применением 100% толуола как элюента. Если необходимо, хлорид алюминия (130 мг, 0.76 экв.) и o-toluloyl chloride (160 мг, 0.80 экв) был добавлен к реакционной смеси и реакционную смесь перемешивали при комнатной температуре в течение ночи. Реакцию гасили осторожным и медленным добавлением воды. Экстракция была выполнена с применением CH2Cl2 и воды. Затем смесь была высушена над MgSO4. Неочищенный продукт очищают на колонке силикагеля с применением 50% гексана в толуоле до 100% толуола. Полученное густое масло растирают в метаноле и фильтруют до получения светло-желтого порошка (720 мг, 46%).

[00205]1H ЯМР (500 МГц, CDCl3) δ 8.42 (d, J=8.4 Hz, 3H), 7.99 (d, J=1.5 Hz, 3H), 7.80 (dd, J1=1.4 Hz, J2=8.3 Hz, 3H), 7.47-7.41 (m, 6H), 7.35 (d, J=7.6 Hz, 3H), 7.31 (t, J=7.4 Hz, 3H), 2.95-2.86 (m, 6H), 2.40 (s, 9H), 2.17-2.09 (m, 6H), 0.97-0.79 (m, 36H), 0.61 (t, J=7.0 Hz, 18H), 0.53-0.44 (m, 12H).
[00206] Максимальный пик поглощения и абсорбционный пик 2,7,12-три-(о-толуол)-5,5',10,10',15,15'-гексагексилтруксена в растворе тетрагидрофурана представляет собой 336 нм и 7.90×104 л моль-1см-1, соответственно. Температура плавления составляет 125°C.
Пример 1.20 - 2,7,12-Три-(phenoyl)-5,5',10,10',15,15'-гексагексилтруксен (INDENO 333)
[00207] 5,5',10,10',15,15'-Гексагексилтруксен (5.0 г) был растворен в 50 мл CH2Cl2 в 100 мл колбе под N2. Бензоил хлорид (2.6 г, 3.20 экв.) был добавлен, и затем хлорид алюминия (3.3 г, 3.05 экв.) медленно добавляли в течение периода 5 минут. Реакционную смесь перемешивали при комнатной температуре на протяжении двух дней. Ход реакции мониторили с помощью ВЭЖХ (пик при 8 мин.) и ТСХ, применяя 100% толуол как элюент. Если необходимо, хлорид алюминия (825 мг, 0.76 экв.) и бензоил хлорид (650 мг, 0.80 экв.) были добавлены к реакционной смеси и реакционную смесь перемешивали при комнатной температуре в течение ночи. Реакцию гасили осторожным и медленным добавлением воды (ОСТОРОЖНО: очень экзотермично). Экстракция была выполнена с применением CH2Cl2 и воды. Органический слой был промыт 1М раствором NaHCO3 и затем высушен над MgSO4. Раствор был сконцентрирован при пониженном давлении. Полученное в результате твердое вещество растирают в метаноле в течение 1 ч и фильтруют. После фильтрации, неочищенный продукт был рекристализирован из 2-пропанола до получения 3.3 г (48%, 100%: 6.84 г). Дальнейшая очистка, при желании, была достигнута на колонке силикагеля с применением 50% гексана в толуоле до 100%) толуола (начиная с 500 мг, восстановлено 60 мг, 12%).

[00208]1H ЯМР (500 МГц, CDCl3) δ 8.48 (d, J=8.4 Hz, 3H), 7.96 (d, J=1.6 Hz, 3H), 7.93-7.88 (m, 9H), 7.65 (tt, J1=7.5 Hz, J2=1.3 Hz, 3H), 7.55 (t, J=7.7 Hz, 6H), 3.00-2.92 (m, 6H), 2.21-2.13 (m, 6H), 1.00-0.83 (m, 36H), 0.63 (t, J=7.3 Hz, 18H), 0.58-0.50 (m, 12H).
[00209] Максимальный пик поглощения и абсорбционный пик 2,7,12-три-(phenoyl)-5,5',10,10',15,15'-гексагексилтруксена в растворе тетрагидрофурана представляют собой 332 нм и 8.55×104 л моль-1см-1 соответственно. Температура плавления составляет 155°C.
Пример 1.21 - 2,7,12-три-(2-thienyloyl)-5,5',10,10',15,15'-гексагексилтруксен
[00210] 5,5',10,10',15,15'-Гексагексилтруксен (5.0 г) был растворен в 50 мл CH2Cl2 в 100 мл колбе под N2. 2-тиофенкарбонил хлорид (2.8 г, 3.20 экв.) был добавлен, и затем хлорид алюминия (3.3 г, 3.05 экв.) был медленно добавлен в течение периода времени 5 минут. Реакционную смесь перемешивали при комнатной температуре на протяжении двух дней. Ход реакции мониторили с помощью ВЭЖХ (пик при 5 мин.) и ТСХ с применением 100% толуола как элюента. Если необходимо, хлорид алюминия (825 мг, 0.76 экв.) и 2-тиофенкарбонил хлорид (700 мг, 0.80 экв.) был добавлен к реакционной смеси и реакционную смесь перемешивали при комнатной температуре в течение ночи. Реакцию гасили осторожным и медленным добавлением воды (ОСТОРОЖНО: очень экзотермично). Экстракция была выполнена с применением CH2Cl2 и воды. Органический слой был промыт 1М раствором NaHCO3 и затем высушен над MgSO4. Раствор был концентрирован при пониженном давлении. Полученное смолистое твердое вещество растирали в метаноле в течение 1 ч и фильтровали. После фильтрации, неочищенный продукт перекристаллизовывают из 2-пропанода до получения 580 мг (8%, 100%: 6.95 г) соединения, подходящего для анализа и 1.6 г (23%) приемлемого чистого соединения. Обе фракции показали лишь один пик с помощью ВЭЖХ, но 1.6 г фракции показали небольшие примеси на ТСХ.

[00211]1H ЯМР (500 МГц, CDCl3) δ 8.51 (d, J=8.2 Hz, 3H), 8.03-7.99 (m, 6H), 7.78 (dd, J1=4.9 Hz, J2=1.1 Hz, 3H), 7.77 (dd, J1=3.8 Hz, J2=1.1 Hz, 3H), 7.24 (dd, J1=4.8 Hz, J2=3.8 Hz, 3H), 3.00-2.95 (m, 6H), 2.24-2.17 (m, 6H), 1.01-0.82 (m, 36H), 0.62 (t, J=7.0 Hz, 18H), 0.58-0.49 (m, 12H).
[00212] Максимальный пик поглощения и абсорбционный пик 2,7,12-три-(2-thienyloyl)-5,5',10,10',15,15'-гексагексилтруксена в растворе тетрагидрофурана представляет собой 338 нм и 8.53×104 л моль-1см-1, соответственно. Температура плавления составляет 125°C.
Пример 1.22 - 2,7,12-три-(4-метоксифунилоил)-5,5',10,10',15,15'-гексагексилтруксен
[00213] 5,5',10,10',15,15'-Гексагексилтруксен (5.0 г) был растворен в 50 мл CH2Cl2 в 100 мл колбе под N2. 3-Метоксибензиол хлорид (3.2 г, 3.20 экв.) был добавлен, и затем хлорид алюминия (3.3 г, 3.05 экв.) был медленно добавлен в течение периода времени 5 минут. Реакционную смесь перемешивали при комнатной температуре в течение двух дней. Ход реакции мониторили с помощью ВЭЖХ (пик при 6 мин.) и ТСХ с применением 2% этилацетата в толуоле как элюенте. Если необходимо, хлорид алюминия (825 мг, 0.76 экв.) и 3-метоксибензиол хлорид (800 мг, 0.80 экв.) был добавлен в реакционную смесь и реакционную смесь перемешивали при комнатной температуре в течение ночи. Реакцию гасили осторожным и медленным добавлением воды (ОСТОРОЖНО: очень экзотермично). Экстракция была выполнена с применением CH2Cl2 и воды. Органический слой был промыт 1М раствором NaHCO3, затем высушен над MgSO4. Раствор был концентрирован при пониженном давлении. Полученное смолистое твердое вещество растирают в метаноле в течение 1 ч и фильтруют. После фильтрации, неочищенный продукт перекристаллизовывают из 2-пропанола до получения 700 мг (9%, 100%: 7.37 г). Дальнейшая очистка, при желании, была достигнута на колонке силикагеля с использованием 100% толуола до 10% этилацетата в толуоле (восстановлены 30 мг).
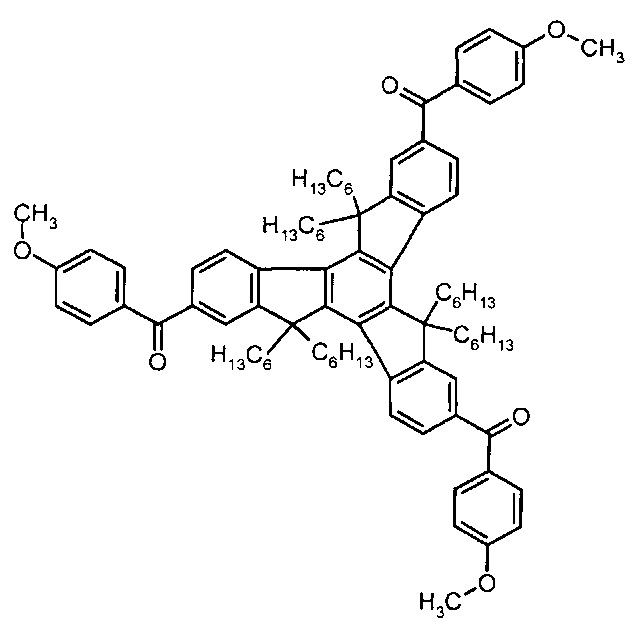
[00214]1H ЯМР (500 МГц, CDCl3) δ 8.48 (d, J=8.4 Hz, 3H), 7.95 (d, J1=1.5 Hz, 3H), 7.93 (dd, J1=8.3 Hz, J2=1.6 Hz, 3H), 7.46-7.42 (m, 9H), 7.21-7.18 (m, 3H), 3.91 (s, 9H), 3.00-2.93 (m, 6H), 2.20-2.13 (m, 6H), 1.00-0.82 (m, 36H) 0.63 (t, J=7.0 Hz, 18H), 0.59-0.48 (m, 12H).
[00215] Максимальный пик поглощения и абсорбционный пик 2,7,12-три-(4-метоксифенилоил)-5,5',10,10',15,15'-гексагексилтруксена в растворе тетрагидрофурана представляет собой 333 нм и 8.55×104 л моль-1см-1 соответственно. Температура плавления составляет 137°C.
Пример 1.23 - 2,7,12 три-(2-ацетилфенил)-5,5',10,10',15,15' гексагексилтруксен
[00216] 2,7,12-Трибромо-5,5',10,10',15,15'-гексагексилтруксен (1.7 г), 2-ацетилфенилбориновой кислоты (0.84 г) и толуола (100 мл) было введено в 500 мл колбу, наполненную азотом. Карбонат натрия (5.6 г) растворенный в воде (20 мл) и тетрабутиламмоний бромид (100 мг) были добавлены к этой смеси. Реакционную смесь барботируют азотом в течение 30 мин. Затем ацетат палладия (48 мг) и трифенилфосфин (60 мг) были добавлены к раствору. Реакционная смесь была нагрета с обратным холодильником в течение 2 дней. Реакционную смесь промывали водой три раза, высушивали над сульфатом магния и концентрировали при пониженном давлении. Смесь быстро пропускали через силикагель с применением 100% толуола, затем от 1 до 3% ацетона в толуоле как элюенте до получения 500 мг (21%) желаемого продукта.

[00217]1H ЯМР (500 МГц, CDCl3) δ 8.42 (d, J=8.2 Hz, 3H), 7.61-7.55 (m, 9Н), 7.48-7.45 (m, 6H), 7.42 (dd, J1=8.2 Hz, J2=1.7 Hz, 3H), 3.04-2.96 (m, 6H), 2.15-2.07 (m, 6H), 2.01 (s, 9H), 1.00-0.80 (m, 36H), 0.60 (t, J=7.3 Hz, 18H), 0.58-0.52 (m, 12H).
[00218] Максимальный пик поглощения и абсорбционный пик 2,7,12-три-(2-ацетилфенил)-5,5',10,10',15,15'-гексагексилтруксена в растворе тетрагидрофурана составляет 323 нм и 9.20×104 л моль-1см-1, соответственно. Температура плавления составляет 136°C.
[00219] Фигура 13 иллюстрирует относительное UV-Vis absorbance фотоинициаторов примеров 1.16 и 1.18 до 1.23.
КРАСНЫЙ, ЗЕЛЕНЫЙ, ГОЛУБОЙ И ЧЕРНЫЙ РЕЗИСТЫ ЦВЕТОВЫХ ФИЛЬТРОВ
Примеры 2.1 до 2.10 и Сравнительный Пример 1
[00220] Красный, зеленый, и синий резисты цветовых фильтров и черная матрица с различными фотоинициаторами были приготовлены смешиванием 1.0 части фотоинициаторов, 13 частей резистентных связующих веществ, 6.0 частей соответствующих дисперсий пигмента, то есть Red-254, Green-36, Blue-15 и Black-250 соответственно, с применением мешалки с большими сдвиговыми усилиями на протяжении 2 часов. Полученные смеси были отфильтрованы через фильтр с размером пор 1 мкм. Пигментированные растворы были нанесены на стекло с помощью спин-кутера, высушены при 100°C в течение 2 минут до получения однородных пленок, имеющих толщину около 3 мкм.
[00221] Цветные резистные пленки были облучены с использованием 250 В ртутной лампы сверхвысокого давления под воздухом с дозой 1,000 мДж/см2 через 21-полутоновый шаг заданной маски (Stouffer Graphic Arts Т2115). Облученную пленку обрабатывают с использованием водного раствора гидроксида калия (pH 12), обильно промывают деионизированной водой, и затем высушивают при 100°C на протяжении 30 минут. Результаты суммированы в таблице ниже.
[00222] В этой таблице, значение, приведенное для чувствительности, представляет собой минимальную дозу, необходимую для полного отверждения цветных резистных пленок. Это было рассчитано из коэффициента пропускания на более высшую ступень количества, оставшегося после выработки. Желательно, чтобы необходимая минимальная доза (мДж/см2) была как можно меньше, что свидетельствует о высокой чувствительности соединения. Как правило, чем более чувствительный фотоинициатор, тем меньше времени необходимо для отверждения композиции.
[00223] Из приведенной выше таблицы видно, что соединения согласно изобретению являются чувствительными, как Irgacure ОХЕ-2 и иногда даже более чувствительными.
Примеры 2.11 до 2.18 и Сравнительные Примеры (СЕ) от 2 до 5
[00224] Красный, зеленый, синий и черный цветной резисты были приготовлены смешиванием пигментной дисперсии, резистного вяжущего вещества и фотоинициаторов по примерам 1.11 и 1.12 с применением мешалки с большими сдвиговыми усилиями в течение 2 часов. Полученную смесь фильтровали через фильтр с размером пор 1 мкм. Пигментированные растворы были нанесены на стекло с помощью спин-кутера, высушены при 100°C на протяжении 2 минут до получения однородной пленки, имеющей толщину около 3 мкм. Для сравнения, имеющиеся в продаже фотоинициаторы Irgacure ОХЕ-02 были также использованы.
[00225] Цветные резистные пленки были облучены с использованием 250 В ртутной лампы сверхвысокого давления под воздухом с дозой 1,000 мДж/см2 через 21-полутоновый шаг заданной маски (Stouffer Graphic Arts Т2115). Облученную пленку обрабатывают с использованием водного раствора гидроксида калия (pH 12), обильно промывают деионизированной водой, и затем высушивают при 100°C на протяжении 30 минут. Результаты суммированы в таблице ниже.
[00226] В этой таблице значение, приведенное для чувствительности, представляет собой минимальную дозу, необходимую для полного отверждения цветных резистных пленок. Это было рассчитано из коэффициента пропускания на более высокую ступень количества, оставшегося после выработки. Желательно, чтобы необходимая минимальная доза (мДж/см2) была как можно меньше, что свидетельствует о высокой чувствительности соединения. Как правило, чем более чувствительный фотоинициатор, тем меньше времени необходимо для отверждения композиции.

[00227] Как можно увидеть из сказанного выше, испытанные соединения согласно изобретению во всех случаях являются более чувствительными, чем ОХЕ-02.
ЛИТОГРАФСКИЕ ОФФСЕТНЫЕ ПЕЧАТНЫЕ ПЛАСТИНЫ
Пример 3.1
[00228] Композиция покрытия была получена смешиванием 250 г BR10-010, 67 г UR07-009, 1.0 г основного зеленого 4, 33 г Blue-15, и 5.0 г фотоинициатора из примера 1.7, и 900 г раствора циклогексанона с применением мешалки с большими сдвиговыми усилиями на протяжении 5 часов. Полученный раствор фильтруют через фильтр с размером пор 5 мкм. Он был покрыт на подложке из анодизированного алюминия, который после этого был обработан фторидом фосфата (PF) с использованием проволочного стержня, затем высушен в печи с горячим воздухом при 100°C в течение 5 минут.
[00229] Пластина была облучена с использованием 250 В ртутной лампы сверхвысокого давления под воздухом с удельной энергией 100 мДж/см2 через 21-полутоновый шаг заданной маски (Stouffer Graphic Arts Т2115). Облученная пластина была обработана с водным раствором, содержащим 1% мыльного раствора с использованием обрабатывающего устройства Tung Sung 800 при 25°C и временем ожидания 20 секунд до получения изображения высокой четкости.
Обработанная пластина была помещена на пресс Heidelberg 46 с использованием черных чернил (Toyo Black) и увлажняющего раствора (UF300, доступный от Mylan Group, Vietnam) и произведено 20,000 копий с хорошим качеством.
Пример 3.2
[00230] Печатная пластина была приготовлена способом, аналогичным описанному в Примере 3.1, за исключением того, что Фотоинициатор из Примера 1.10 был использован вместо фотоинициатора из Примера 1.7.
[00231] Пластина была облучена с использованием 250 В ртутной лампы сверхвысокого давления под воздухом с удельной энергией 100 мДж/см2 через 21-полутоновый шаг заданной маски (Stouffer Graphic Arts Т2115). Облученная пластина была обработана водным раствором, содержащим 1% мыльного раствора с использованием обрабатывающего устройства Tung Sung 800 при 25°C и временем ожидания 20 секунд до получения изображения высокой четкости.
[00232] Обработанная пластина была помещена на пресс Heidelberg 46 с использованием черных чернил (Toyo Black) и увлажняющего раствора (UF300, доступный от Mylan Group, Vietnam) и произведено 20,000 копий с хорошим качеством.
Пример 3.3
[00233] Композиция покрытия были приготовлена путем смешивания 250 г BR10-010, 67 г UR07-009, 1.0 г основного зеленого 4, 33 г Blue-15, и 5.0 г фотоинициаторов 1Е (Пример 1.11) и 900 г раствора 2-метоксипропанола с использованием мешалки с большими сдвиговыми усилиями в течение 5 часов. Полученный в результате раствор фильтруют через фильтр с размером пор 5 мкм. Он был покрыт на подложке из анодизированного алюминия, который после этого был обработан фторидом фосфата (PF) с использованием проволочного стержня, затем высушен в печи с горячим воздухом при 100°C в течение 5 минут.
[00234] Пластина была облучена с использованием 250 В ртутной лампы сверхвысокого давления под воздухом с удельной энергией 100 мДж/см2 через 21-полутоновый шаг заданной маски (Stouffer Graphic Arts Т2115). Облученная пластина была обработана водным раствором, содержащим 1% мыльного раствора Mr. Clean с использованием обрабатывающего устройства Tung Sung 800 при 25°C и временем ожидания 20 секунд до получения изображения высокой четкости.
[00235] Обработанная пластина была помещена на пресс Heidelberg 46 с использованием черных чернил (Toyo Black) и увлажняющего раствора (UF300, доступный от Mylan Group, Vietnam) и произведено 20,000 копий с хорошим качеством.
Пример 3.4
[00236] Печатная пластина была приготовлена способом, аналогичным описанному в Примере 3.3, за исключением того, что Фотоинициатор из Примера 1.12 был использован вместо такого из Примера 1.11.
[00237] Пластина была облучена с использованием 250 В ртутной лампы сверхвысокого давления под воздухом с удельной энергией 100 мДж/см2 через 21-полутоновый шаг заданной маски (Stouffer Graphic Arts Т2115). Облученная пластина была обработана водным раствором, содержащим 1% мыльного раствора Mr. Clean с использованием обрабатывающего устройства Tung Sung 800 при 25°C и временем ожидания 20 секунд до получения изображения высокой четкости.
[00238] Обработанная пластина была помещена на пресс Heidelberg 46 с использованием черных чернил (Toyo Black) и увлажняющего раствора (UF300, доступного от Mylan Group, Vietnam) и произведено 20,000 копий с хорошим качеством.
УФ ОТВЕРЖДАЕМЫЕ КРАСКИ ДЛЯ СТРУЙНОЙ ПЕЧАТИ
Примеры 4.1-4.4
[00239] Отверждаемые ультрафиолетовым излучением краски для струйной печати, имеющие композиции, показанные в таблице ниже, были приготовлены с использованием мешалки с большими сдвиговыми усилиями до образования однородных растворов. Эти растворы были отфильтрованы через 1.0 мкм пропиленовый фильтр. Отфильтрованные чернила были напечатаны на полиэстерную пленку с различными данными тестирования и разрешающей способностью 300 точек на дюйм с использованием печатных головок Richol G4, которые были инъецированы при 50°C. Отпечатанные изображения были отверждены с УФ-светодиодной фотополимеризацией элементом (Модель: 8 Вт/см2 Fireline, доступный от Phoseon Technology, Oregon, USA) со скоростью десять метров в минуту. Элемент УФ-светодиодной фотополимеризации был помещен на растоянии 5 см около печатных пленок. Полностью отвержденные печатные изображения из чернил для струйной печати, содержащими фотоинициаторы изобретения были получены с высоким разрешением и хорошей адгезией к полиэстерной подложке.
АКЦЕПТИРУЮЩИЕ КИСЛОРОД ПЛАСТИЧЕСКИЕ ПЛЕНКИ
[00240] Акцептирующее кислород действие полимерных пленок, содержащих фотоинициаторы изобретения было продемонстрировано путем мониторинга снижения концентрации кислорода в результате потребления кислорода при приготовлении образца пленки. Таким образом, 1.0 грамм образца пленки, сделанного из сополимера ацеталя, содержащего подвесные группы циклогексана (РАСН-001), соль олеата кобальта(II) и фотоинициатор были помещены в стеклянную бутылку. Стеклянная бутылка была запечатана самодельной крышкой, содержащей кислородный флуоресцентный зонд. Стеклянная бутылка затем была промыта газом азота, содержащего около 21% кислорода. Затем бутылка была герметично закрыта и активирована под воздействием УФ-света при 254 нм при комнатной температуре с дозировкой 100 мДж/см2. Снижение концентрации кислорода с течением времени контролировали с помощью неинвазивной системы мониторинга и проникновения кислорода Oxysense's GEN III 5000.
Пример 4.1
[00241] Одна сотня частей сополимера ацеталя, содержащего боковую группу циклогексана (РАСН-001) была растворена в 1,3-диоксане до достижения 20% раствора. К этому раствору было добавлено 0.1 частей соли олеата кобальта(II) и 0.1 частей фотоинициатора Примера 1.16. Когда раствор стал прозрачным, его вылили на плоскую тефлоновую поверхность и растворитель был выпарен при комнатной температуре. Полученную полимерную пленку дополнительно сушили в вакууме в течение ночи, что дало оптически прозрачную пленку, имеющую толщину около 200 мкм. Эта пленка была использована для последующей демонстрации акцептирующего кислород воздействия. Результаты сокращения кислорода в зависимости от времени показаны на Фигуре 15.
[00242] Для сравнительных целей, аналогичная РАСН-001 пленка была приготовлена без фотоинициатора Примера 1.16. Акцептирующее кислород воздействие было также промониторено и также показано на Фигуре 15.
Пример 4.2
[00243] Одна сотня частей РАСН-001 была растворена в смеси растворителя, содержащей равные количества тетрагидрофурана и 2-метокси пропанола до достижения 20% раствора. К этому раствору было добавлено 0.1 частей соли олеата кобальта II и 0.2 частей фотоинициатора Примера 1.17. Когда раствор стал прозрачным, его вылили на плоскую тефлоновую поверхность и растворитель был выпарен при комнатной температуре. Полученную полимерную пленку дополнительно сушили в вакууме в течение ночи, что дало оптически прозрачную пленку, имеющую толщину около 200 мкм. Эта пленка была использована для последующей демонстрации акцептирующего кислород воздействия. Результаты сокращения кислорода в зависимости от времени показаны на Фигуре 16.
[00244] Результаты Примеров 4.1 и 4.2 показывают, что труксеновые фотоинициаторы являются очень эффективными в кислород акцептирующих композициях.
[00245] Объем формулы изобретения не должен быть ограничен предпочтительными вариантами осуществления, изложенных в примерах, а должен рассматриваться в самой расширенной интерпретации в соответствии с описанием целом.
Ссылки
[00246] Содержание следующих документов включено в настоящее описание в качестве ссылки во всей их полноте:
Реферат
Изобретение относится к соединениям формул 1 или 2:илиТехнический результат: получены новые соединения, полезные в качестве фотоинициаторов. 2 н. и 23 з.п. ф-лы, 16 ил., 2 табл., 31 пр.
Формула






























Комментарии