Способ получения 2,3,5-триметилбензохинона при помощи окисления 2,3,6-триметилфенола - RU2668962C2
Код документа: RU2668962C2
Описание
Предметом настоящего изобретения является способ получения 2,3,5-триметилбензохинона или смеси, содержащей 2,3,5-триметилбензохинон, включающий в себя следующую стадию: окисление 2,3,6-триметилфенола с помощью кислорода или кислородсодержащего газа в двух- или многофазной реакционной среде в присутствии катализатора или каталитической системы, содержащей по меньшей мере галогенид меди (II), с получением смеси, содержащей 2,3,5-триметилбензохинон, отличающийся тем, что реакционная среда содержит воду и по меньшей мере один вторичный алифатический ациклический спирт, имеющий 6 или более, предпочтительно 7 или более, атомов углерода.
Другой аспект настоящего изобретения касается смеси, содержащей 2,3,5-триметилбензохинон, причем эта смесь может получаться или получается при помощи способа согласно изобретению.
Предметом настоящего изобретения, кроме того, является применение вторичного алифатического ациклического спирта, имеющего 6 или более, предпочтительно 7 или более, атомов углерода, в качестве растворителя при окислении 2,3,6-триметилфенола до 2,3,5-триметилбензохинона.
Помимо этого, настоящее изобретение касается применения 2,3,5-триметилбензохинона, полученного по способу согласно изобретению, или полученной по способу согласно изобретению смеси, содержащей 2,3,5-триметилбензохинон, при синтезе витамина Е, в частности, для получения 2,3,6-триметилгидрохинона.
2,3,6-Триметилбензохинон (1) имеет большое значение в качестве промежуточного продукта для промышленного синтеза α-токоферола = витамина Е (3). Для этого (1) сначала каталитически гидрируется до 2,3,6-триметилгидрохинона (2), а затем с применением кислоты Льюиса в качестве катализатора конденсируется с изофитолом, с целью образования (3) (Схема 1).

Для синтеза (1) известен ряд технически реализованных синтезов. Почти все известные из уровня техники способы для синтеза (1) используют окисление 2,3,6-триметилфенола (4), который, в свою очередь, может получаться различными путями. Для окисления (4) с получением (1) в качестве недорогого окислителя предпочтительно применяется кислород (Схема 2).

Наиболее эффективные способы окисления (4) с получением (1) в качестве катализаторов используют галогениды меди (II) или комплексы галогенидов меди (II). Однако эти способы также сопряжены с проблемами. К примеру, следует назвать затратную рециркуляцию применяемого растворителя и/или применяемого катализатора и, прежде всего, образование нежелательных побочных продуктов. Особенно следует подчеркнуть образование галогенированных, как правило, хлорированных, побочных продуктов, которые в процессе обработки распадаются с высвобождением HCl и, таким образом, приводят к коррозии и к потерям производимого продукта (1).
Немецкий патент DE 2 221 624 описывает окисление 2,3,6-триметилфенола с помощью кислорода в присутствии галогенидов меди, прежде всего, дигидрата хлорида меди (II), в полярных, водорастворимых или неограниченно смешивающихся с водой растворителях, предпочтительно диметилформамиде. Однако этот способ обладает тем недостатком, что из реакционной смеси трудно выделить продукт и регенерировать катализатор.
Европейский патент ЕР 127 888 описывает применение комплексов галогенидов меди (II), имеющих общую формулу
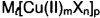
Европейский патент ЕР 167 153 описывает применение тех же самых катализаторов, как и в европейском патенте ЕР 127 888, в смеси из воды и алифатических спиртов, имеющих от 5 до 10 атомов углерода, в качестве растворителя. Предпочтительными называются первичные спирты, например, н-амиловый спирт, изоамиловый спирт, н-гексанол, 2-этилгексанол, н-гептанол, н-октанол, н-нонанол и н-деканол. Реакция проводится в «полунепрерывном» режиме, благодаря чему образуется меньше побочных продуктов. Кроме того, реакция может легче контролироваться, и требуется меньше катализатора.
Европейский патент ЕР 294 584 описывает применение смеси из хлорида меди (II) и хлорида лития в качестве катализатора, а в качестве растворителя водной смеси из ароматического углеводорода и алифатического спирта, имеющего от 1 до 4 атомов углерода. В качестве примеров называют первичные спирты - метанол, этанол, н-пропанол, изопропанол, н-бутанол, 2-бутанол и третбутанол. Хотя некоторые вторичные и третичные спирты также указываются, правда, только в комбинации с ароматическим углеводородом. Кроме того, эти спирты имеют максимум 4 атома углерода. Кроме того, сравнение примеров 9 и 11 европейского патента ЕР 294 584 показывает, что применение изопропанола в качестве вторичного спирта приводит к более низким выходам, чем применение н-пропанола (91,6 против 94,1% при идентичных в остальном условиях). Кроме того, применение смеси растворителей приводит к значительно усложненной рециркуляции растворителя.
Европейский патент ЕР 369 823 описывает применение хлорида меди (II) в комбинации с определенными соединениями азота (гидроксиламмониевыми солями, оксимами или солями аммония) в качестве катализатора. В качестве растворителя предпочтительно применяются алифатические спирты, имеющие от 3 до 10 атомов углерода, причем особенно предпочтительно используются разветвленные спирты, имеющие от 3 до 6 атомов углерода, и наиболее предпочтительно третичные спирты, такие как третбутанол или третамиловый спирт. Правда, наилучшие достигнутые здесь выходы (1) (Пример 55: 94,5% с третамиловым спиртом и 95% с третбутанолом) в лучшем случае лежат на том же уровне, как и в более ранних публикациях из уровня техники, которые не требуют добавления соединений азота.
М. Shimizu с соавт. (Bull. Chem. Soc. Jpn. 65 (1992) 1522) раскрывают способ окисления (4) с применением в качестве каталитических систем смесей из хлорида Cu (II) и гидрохлоридов различных аминов, гидроксиламина или оксимов. В данном случае в качестве растворителя также, помимо первичных спиртов, применяются вторичные спирты, такие как изопропанол, вторбутанол, 2-пентанол и 3-пентанол, третбутанол и третамиловый спирт, без того, чтобы особенное преимущество при использовании вторичных спиртов становилось очевидным. Предпочтительное применение гидроксиламина в качестве добавки, которая расходуется при окислении, делает этот способ непривлекательным.
Европейский патент ЕР 475 272 описывает применение смесей из хлорида меди (II) и хлоридов щелочноземельных металлов, в частности, MgCl2, в качестве катализатора. В качестве растворителя приводятся насыщенные алифатические спирты, имеющие от 5 до 10 атомов углерода. В качестве особенно предпочтительных называют 1-пентанол, 1-гексанол, 1-пентанол, 1-октанол, 1-нонанол, 1-деканол, 2-этил-1-гексанол и циклогексанол, то есть, за исключением циклогексанола, первичные спирты.
Европейский патент ЕР 1 092 701 описывает применение в качестве катализатора смесей из хлорида меди (II) и других хлоридов металлов из группы железа (Fe), хрома (Cr), марганца (Mn), кобальта (Со), никеля (Ni), цинка (Zn) или редкоземельных элементов. В качестве растворителя приводятся разветвленные и неразветвленные алифатические спирты, имеющие от 5 до 10 атомов углерода. В качестве особенно предпочтительных называют 1-пентанол, 1-гексанол, 1-гептанол, 1-октанол, 1-нонанол, 1-деканол, 2-этил-1-гексанол и циклогексанол, то есть, за исключением циклогексанола, первичные спирты.
Японский патент JP 55 072 136 описывает применение дигидрата хлорида меди (II) в качестве катализатора в полиэтиленгликолях, таких как, например, СН3О(CH2CH2O)9СН3, в качестве растворителя. Реакционная смесь может подвергаться водной обработке, чтобы регенерировать катализатор. Желаемый продукт отделяется перегонкой в виде легкокипящей фракции. Однако этот способ обладает тем недостатком, что высококипящие побочные продукты концентрируются в растворителе и могут удаляться лишь с трудом.
Как и все способы, основанные на галогенидах Cu в качестве катализаторов, описанные выше способы также имеют принципиальные недостатки, которые берут начало из образования хлорорганических побочных продуктов. Эти побочные продукты образуются в процессе проведения реакции окисления и являются результатом хлорирования исходного вещества (4), продукта (1), а при необходимости растворителя - 1-гексанола. Рисунок 1 показывает некоторые типичные побочные продукты, однако без того, чтобы давать полный список.

Рисунок 1: Типичные побочные продукты при окислении 2,3,6-триметилфенола (4) до 2,3,6-триметилбензохинона (1).
Возникающие реакции хлорирования являются причиной непосредственной потери селективности в желаемой реакции окисления и, кроме того, при необходимости потери растворителя, которая должна компенсироваться при помощи добавления свежего растворителя. Одновременно фаза катализатора обедняется по содержанию хлорида, из-за чего эта фаза катализатора через определенные промежутки должна обрабатываться соляной кислотой для регенерации.
Кроме того, хлорорганические побочные продукты, в частности, при термической нагрузке, отщепляют хлороводород, который в соответствующих частях установки (например, в перегонных колоннах, в которых нагревается реакционная смесь) приводит к существенным проблемам с коррозией, из-за чего почти для всех зон установки должны применяться дорогостоящие специальные стали. Кроме того, хлороводород индуцирует реакции разложения получаемого продукта (1), что приводит к потерям выхода, в частности, в кубовой части перегонной колонны. Хлорорганические побочные продукты (например, представленные на Рис. 1 соединения (7)-(11)), как правило, имеют температуры кипения, которые аналогичны температурам кипения растворителя или температурам кипения продукта, что затрудняет разделение реакционной смеси перегонкой и обусловливает потери как продукта, так и растворителя во фракциях, имеющих промежуточные температуры кипения. Хлорсодержащие загрязнения также отравляют катализатор гидрирования из последующего превращения хинона (1) в гидрохинон (2).
Для предотвращения этих недостатков, как правило, проводятся дополнительные стадии обработки. Европейский патент ЕР 0 216351 раскрывает концепцию отделения хлорорганических побочных продуктов от необработанной выгружаемой массы из осуществляемого с помощью CuCl2 окисления (4) до (1). Обеднение по содержанию побочных продуктов здесь осуществляется при помощи промывки основанием. Однако промывка основанием является не особенно эффективной и всегда означает компромисс между снижением содержания хлорорганических соединений и потерями продукта. Хотя в целом эта операция делает возможной техническую реализацию способа согласно Схеме 3, однако промывка основанием в результате дополнительной стадии процесса приводит к более высоким инвестиционным и производственным затратам, к потерям выхода, а, следовательно, в общей сложности, только к смягчению описанной здесь проблемы.
Следовательно, первичной задачей настоящего изобретения является предоставление способа получения 2,3,5-триметилбензохинона или смеси, содержащей 2,3,5-триметилбензохинон, при помощи окисления 2,3,6-триметилфенола в присутствии катализатора или каталитической системы, содержащей по меньшей мере галогенид меди (II), который обладает всеми преимуществами способов, известных из уровня техники, однако минимизирует образование нежелательных хлорированных побочных продуктов.
Предпочтительной задачей настоящего изобретения является предоставление способа получения 2,3,5-триметилбензохинона или смеси, содержащей 2,3,5-триметилбензохинон, при помощи окисления 2,3,6-триметилфенола в присутствии катализатора или каталитической системы, содержащей по меньшей мере галогенид меди (II), который в максимальной степени предотвращает образование хлорированных побочных продуктов, чтобы таким образом улучшить селективность реакции, минимизировать потери растворителя в результате хлорирования этого растворителя, а при необходимости избежать потребности в дополнительных стадиях обработки, а также применения специальных конструкционных материалов.
Так, неожиданно было обнаружено, что в результате применения вторичного алифатического ациклического спирта, имеющего 6 или больше, предпочтительно 7 или больше, атомов углерода, в качестве растворителя при окислении 2,3,6-триметилфенола в присутствии катализатора или каталитической системы, содержащей по меньшей мере галогенид меди (II), может сильно подавляться образование хлорированных побочных продуктов при одновременном сохранении всех известных из уровня техники преимуществ.
Следовательно, предметом изобретения является способ получения 2,3,5-триметилбензохинона или смеси, содержащей 2,3,5-триметилбензохинон, включающий в себя следующую стадию: окисление 2,3,6-триметилфенола с помощью кислорода или кислородсодержащего газа в двух- или многофазной реакционной среде в присутствии катализатора или каталитической системы, содержащей по меньшей мере галогенид меди (II), с получением смеси, содержащей 2,3,5-триметилбензохинон, отличающийся тем, что реакционная среда содержит воду и по меньшей мере один вторичный алифатический ациклический спирт, имеющий 6 или более, предпочтительно 7 или более, атомов углерода.
При способе согласно изобретению можно отказаться от применения специальных сталей, а также от промывки основанием. Сырой продукт при термической нагрузке в процессе очистки перегонкой является заметно более устойчивым, благодаря чему минимизируются потери выхода и одновременно получается более чистый, а следовательно, более высококачественный продукт.
В принципе, для способа согласно изобретению подходят все алифатические ациклические спирты, которые содержат 6 или больше, предпочтительно 7 или больше, атомов углерода. Особенно предпочтительным является применение 3-гептанола.
В одном предпочтительном оформлении способа согласно изобретению окисление 2,3,6-триметилфенола (4) проводится с помощью кислородсодержащего газообразного азота в двухфазной реакционной среде в присутствии менее чем стехиометрических количеств катализатора CuCl2 и стехиометрических количеств LiCl (Схема 3).

При способе согласно изобретению заметно сокращается образование хлорорганических побочных продуктов в реакции окисления 2,3,6-триметилфенола (4) до 2,3,5-триметилбензохинона (1).
Помимо значительного сокращения содержания хлорорганических побочных продуктов в выгружаемых массах проводимой во вторичных спиртах реакции окисления обнаруживаются заметно сниженные количества ионов металлов или соответственно хлорид-ионов, а также заметно меньше воды. Это облегчает экстракцию для регенерации растворенного в органической фазе катализатора. Поскольку разделение фаз в процессе водной обработки осуществляется заметно быстрее, значительно сокращается и упрощается концепция обработки в сравнении с применением первичного спирта в качестве растворителя. К тому же, поскольку растворимость в воде вторичного спирта, по сравнению с первичными спиртами с одинаковым числом атомов углерода, ниже, также сокращается потеря растворителя в процессе экстракции.
В описанном выше предпочтительном оформлении способа согласно изобретению реакционная смесь состоит из нижней водной фазы катализатора и верхней органической фазы, которая содержит растворитель, исходное вещество и продукты реакции. В эту двухфазную смесь при перемешивании подается поток кислород/азот. Способ предпочтительно осуществляется в периодическом режиме.
В одном предпочтительном оформлении способа согласно изобретению смесь, содержащая 2,3,5-триметилбензохинон, на стадии (ii) промывается водным щелочным раствором.
Кроме того, согласно изобретению предпочтительно, чтобы окисление проводилось при температуре между 50°С и 65°С, предпочтительно при температуре между 53 и 58°С.
Кроме того, согласно изобретению предпочтительно, чтобы окисление проводилось на протяжении промежутка времени от 4 до 8 часов, предпочтительно на протяжении промежутка времени 5-7 часов.
В одном предпочтительном оформлении способа согласно изобретению реакционная среда после проведенного окисления на стадии (iii) подвергается разделению фаз, и органическая фаза для регенерации растворенного в этой органической фазе катализатора подвергается экстракции.
Предметом настоящего изобретения также является смесь, содержащая 2,3,5-триметилбензохинон, причем эта смесь может получаться или получается при помощи способа согласно изобретению.
При помощи способа согласно изобретению может получаться смесь, содержащая 2,3,5-триметилбензохинон, которая имеет содержание хлора меньше чем 0,5 г/100 г и/или содержание лития меньше чем 0,3 г/100 г и/или содержание меди меньше чем 240 мг/кг.
Предметом настоящего изобретения, кроме того, является применение вторичного ал иератического ациклического спирта, имеющего 6 или более, предпочтительно 7 или более, атомов углерода, в качестве растворителя при окислении 2,3,6-триметилфенола до 2,3,5-триметилбензохинона.
Помимо этого, настоящее изобретение касается применения 2,3,5-триметилбензохинона, полученного по способу согласно изобретению, или полученной по способу согласно изобретению смеси, содержащей 2,3,5-триметилбензохинон, при синтезе витамина Е, в частности, для получения 2,3,6-триметилгидрохинона.
Изобретение поясняется более подробно на основании следующих ниже Примеров.
Метод анализа:
В конце приведенных в качестве примеров экспериментов фазы разделяли, взвешивали раздельно, а органические фазы анализировали. Количественное определение содержания (1) и (4) в органических фазах осуществлялось газовой хроматографией. Определение общего содержания хлора осуществлялось при помощи элементного анализа, а содержание хлорид-ионов определялось при помощи потенциометрического титрования с раствором нитрата серебра. Разность этих двух величин дает содержание органически связанного хлора. Количественное определение меди и лития осуществлялось при помощи атомной эмиссионной спектроскопии с индуктивно-связанной плазмой (ICP-OES).
Примеры с 1 по 10:
В стальной реактор объемом 4 л загружают 657 г водной реакционной среды, состоящей из 151 г CuCl2⋅2H2O, 150 г LiCl и 365 г воды, а также 818 г служащего в качестве растворителя спирта. Эту двухфазную смесь при перемешивании доводят до желаемой исходной температуры ТD и при нормальном давлении пропускают через нее кислородсодержащую газовую смесь. При достижении температуры ТD в течение промежутка времени tD с постоянной скоростью подают имеющий концентрацию 60% масс. раствор 500 г 2,3,5-триметилфенола (4) в спирте, служащем в качестве растворителя. Для полного завершения реакцию дополнительно перемешивают в течение промежутка времени tR при температуре TR.
После оконченной реакции и охлаждения до комнатной температуры фазы разделяют, взвешивают по отдельности и органическую фазу анализируют. Степень превращения (4) во всех случаях является полной (>99,9%). Выход хинона (1) варьируется лишь незначительно и во всех экспериментах лежит в диапазоне 90-95%. Результаты приводятся в Таблице 1.
Как показывает сравнение Примеров согласно изобретению (Е 2, 4, 6, 8, 10) с соответствующими Примерами для сравнения (С 1, 3, 5, 7, 9), содержание органически связанного хлора при проведении реакции во вторичном спирте, который следует применять согласно изобретению, в среднем составляет в 3,5 раза меньше, чем в случае применения первичного спирта. Общее содержание хлора, меди и лития в органической фазе так же заметно ниже (в среднем в 6 раз для общего хлора, в 4,5 раза для меди и в 18 раз для лития).

Пример 11:
Выгружаемую реакционную массу, полученную из Примера Е7 (реакция в 3-гептаноле), сначала промывают водой. После проведенного разделения фаз органическую фазу в делительной воронке встряхивают с водной HCl (25% масс.), а затем снова промывают водой. При помощи добавления водного раствора едкого натра (2% масс.) раствор доводят до рН=6 и удаляют растворитель в вакууме так, что получается раствор триметилхинона (1) с концентрацией примерно 75% масс.
Для определения термической устойчивости этого сырого продукта этот продукт нагревается до 110°С и через определенные промежутки времени при помощи газовой хроматографии определяется содержание (1). Спустя 125 часов разложилось только 8% от первоначально полученного (1).
Пример для сравнения 12:
Пример 11 повторяли с выгружаемой массой из Примера С1 (реакция в 1-гексаноле в качестве растворителя). При нагревании до 110°С спустя 125 часов разлагались 44% от первоначально полученного хинона (1).
Реферат
Настоящее изобретение относится к способу получения 2,3,5-триметилбензохинона или смеси, содержащей 2,3,5-триметилбензохинон, которые используются для получения витамина Е. Способ включает стадию окисления 2,3,6-триметилфенола до 2,3,5-триметилбензохинона с помощью кислорода или кислородсодержащего газа в двух- или многофазной реакционной среде в присутствии катализатора или каталитической системы, содержащей по меньшей мере галогенид меди (II), так что образуется смесь, содержащая 2,3,5-триметилбензохинон. При этом реакционная среда содержит воду и по меньшей мере один вторичный алифатический ациклический спирт, имеющий 6 или более атомов углерода. Также изобретение относится к смеси для синтеза витамина Е, содержащей 2,3,5-триметилбензохинон, к применению вторичного алифатического ациклического спирта, имеющего 6 или более атомов углерода, и к применению получаемой предлагаемым способом смеси. Предлагаемый способ позволяет в максимальной степени предотвратить образование хлорированных побочных продуктов, чтобы таким образом улучшить селективность процесса. 4 н. и 14 з.п. ф-лы, 1 табл., 12 пр.

Комментарии