Способ получения альдегидного соединения и ацетального соединения - RU2693040C1
Код документа: RU2693040C1
Описание
Область техники, к которой относится настоящее изобретение
[0001]
Настоящее изобретение относится к способу получения 3-метилглутаральдегида и нового ацетального соединения.
Уровень техники настоящего изобретения
[0002]
3-Метилглутаральдегид (3-метил-1,5-пентандиаль, в настоящем изобретении ниже сокращен до "MGL") является полезным соединением в качестве отверждающего агента для фоточувствительного материала, дубильного вещества для кожи и синтетического промежуточного соединения (смотри, например, PTL 1-3). В качестве способа получения MGL, является известным способ гидролиза пиранильного эфира, который получают реакцией Дильса-Альдера между кротоновым альдегидом и метилвиниловым эфиром (смотри NPL 1 и 2).
Список цитируемой литературы
Патентная литература
[0003]
PTL 1: JP 07-281342 A PTL 2: DE 2137603 A PTL 3: JP 2009-102244 A Непатентная литературы [0004]
NPL 1: Organic Syntheses, Vol. 34, p,29 (1954) NPL 2: Organic Syntheses, Vol. 34, p,71 (1954) Сущность настоящего изобретения Техническая проблема
[0005]
Согласно приведенным выше стандартным способам, способность реагировать кротонового альдегида и метилвинилового эфира в реакции Дильса-Альдера является низкой, требуются жесткие условия высокой температуры и высокого давления, и выход MGL является низким. Таким образом, есть возможность для улучшения. Вследствие этого, цель настоящего изобретения заключается в обеспечении способа получения MGL с хорошим выходом в мягких условиях и нового ацетального соединения, которое является пригодным для осуществления приведенного выше способа.
Решение проблемы
[0006]
Согласно настоящему изобретению, приведенную выше цель достигают следующими [1]-[3].
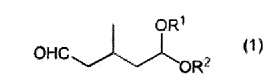
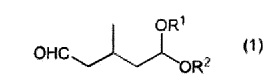
[1] способ получения 3-метилглутаральдегида, включающий стадию гидролиза соединения, представленного следующей общей формулой (1) (называют в настоящем изобретении ниже "ацетальным соединением (1)"):
[0007]
[0008]
где каждый R1 и R2 независимо представляет собой алкильную группу, содержащую 1-6 атомов углерода, или они соединены вместе, представляя собой алкиленовую группу, содержащую 2-6 атомов углерода.
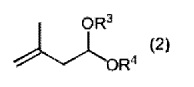
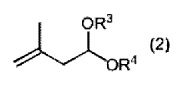
[2] способ получения по [1], дополнительно включающий стадию применения соединения, представленного следующей общей формулой (2) (называют в настоящем изобретении ниже "ацетальным соединением (2)"):
[0009]
[0010]
где каждый R3 и R4 независимо представляет собой алкильную группу, содержащую 1-6 атомов углерода, или они соединены вместе, представляя собой алкиленовую группу, содержащую 2-6 атомов углерода,
в гидроформилировании, получая ацетальное соединение (1).
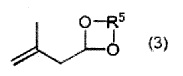
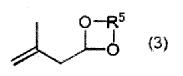
[3] соединение, представленное следующей общей формулой (3) (называют в настоящем изобретении ниже "ацетальным соединением (3)"):
[0011]
[0012]
где R5 представляет собой линейную алкиленовую группу, содержащую 2-6 атомов углерода.
Полезные эффекты настоящего изобретения
[0013]
Согласно настоящему изобретению, обеспечивают способ получения MGL с хорошим выходом в мягких условиях и нового ацетального соединения, которое является пригодным для осуществления приведенного выше способа.
Описание вариантов осуществления
[0014]
В настоящем изобретении, MGL получают гидролизом ацетального соединения (1). Ацетальное соединение (1) можно подходящим способом получить реакцией
гидроформилирования ацетального соединения (2).
[0015]
В ацетальном соединении (1) и ацетальном соединении (2), алкильная группа, содержащая 1-6 атомов углерода, как представлено R1-R4, может быть линейной, разветвленной или циклической, и ее примеры включают метильную группу, этильную группу, н-пропильную группу, изопропильную группу, н-бутильную группу, изобутильную группу, трет-бутильную группу, н-пентильную группу, циклогексильную группу и подобные. Среди них, метильная группа, этильная группа и н-пропильная группа
являются предпочтительными, и метильная группа и этильная группа являются более предпочтительными.
Примеры алкиленовой группы, в которой R1 и R2, или R3 и R4 соединены вместе,
включают этиленовую группу, н-пропиленовую группу, н-бутиленовую группу, н- пентиленовую группу, н-гексиленовую группу, 2-метилэтиленовую группу, 1,2- диметиленовую группу, 2-метил-н-пропиленовую группу, 2,2-диметил-н-пропиленовую группу, 3-метил-н-пентиленовую группу и подобные. Среди них, этиленовая группа, н- пропиленовая группа, 2-метил-н-пропиленовая группа, 2,2-диметил-н-пропиленовая группа, 2-метилметиленовая группа и 1,2-диметиленовая группа являются предпочтительными; этиленовая группа, н-пропиленовая группа, 2-метил-н-пропиленовая группа и 2,2-диметил-н-пропиленовая группа являются более предпочтительными; и этиленовая группа и н-пропиленовая группа являются особенно предпочтительными.
[0016]
(Получение ацетального соединения (2))
Способ получения ацетального соединения (2) не ограничен, и его примеры включают способ применения 3-метил-3-бутен-1-аля в реакции получения ацеталей в присутствии спирта, соответствующего приведенным выше R1-R4. В настоящем изобретении, 3-метил-3-бутен-1-аль, который будут применять, можно получить из
изопренола согласно способу, описанному, например, в JP 2007-525522 A или WO
08/037693 A. [0017]
Хотя реакция получения ацеталей протекает даже в отсутствии катализатора, можно применять кислотный катализатор, при необходимости. Кислота, которую будут применять, конкретно не ограничена, и ее примеры включают неорганические кислоты и их соли, такие как серная кислота, фосфорная кислота, азотная кислота, хлороводородная кислота, борная кислота и т.д.; органические кислоты и их соли, такие как муравьиная кислота, уксусная кислота, пропионовая кислота, щавелевая кислота, метансульфоновая кислота, п-толуолсульфоновая кислота, п-толуолсульфонат пиридиния и т.д.; твердые кислоты, такие как катионообменная смола, алюмосиликат, цеолит, активированная глина и т.д.; и подобные.
Хотя применяемое количество приведенного выше катализатора изменяется в зависимости от типа применяемой кислоты или количества воды, поскольку описывают случай применения хлористоводородной кислоты, катализатор применяют в количестве предпочтительно в диапазоне от 0,00001% по массе до 10% по массе, и более предпочтительно в диапазоне от 0,0001% по массе до 5% по массе реакционного раствора, как выражено в единицах молекулы хлороводорода. Когда применяемое количество катализатора является меньшим, чем 0,00001% по массе, часто не достигают достаточной скорости реакции, тогда как в случае применения катализатора в количестве более чем
10% по массе, применяемое количество основания в случае нейтрализации увеличивается, так что загрузка в способе постобработки увеличивается.
[0018]
Можно проводить реакцию получения ацеталей всей партией и непрерывными способами. Кроме того, можно также применять режим экстракции воды, полученной при превращении 3-метил-3-бутен-1-аля в ацетальное соединение (2), из системы одновременно с реакцией. После реакции, при необходимости, кислотный катализатор можно удалять и применять в следующей реакции, или ацетальное соединение (2) можно очищать стандартным способом очистки, таким как перегонка и т.д.
Среди ацетальных соединений (2), ввиду простоты получения, следующее ацетальное соединение (3):
[0019]

[0020]
В котором R5 представляет собой линейную алкиленовую группу, содержащую 2-6 атомов углерода, является особенно предпочтительным. В данном случае, данное ацетальное соединение (3) представляет собой новое соединение.
[0021]
(Получение ацетального соединения (1))
Ацетальное соединение (1) подходящим образом получают способом применения ацетального соединения (2) в гидроформилировании.
Реакцию гидроформилирования проводят реакцией ацетального соединения (2) с монооксидом углерода и водородом в присутствии металлического соединения, принадлежащего к группам 8-10, и при необходимости, лиганда.
[0022]
Примеры металлического соединения принадлежащего к группам 8-10, включают родиевое соединение, кобальтовое соединение, рутенивое соединение, железное соединение и подобные. Примеры родиевого соединения включают Rh(acac)(CO)2, Rh(acac)3, RhCl(CO)(PPh3)2, RhCl(PPh3)3, RhBr(CO)(PPh3)2, Rh4(CO)12, Rh6(CO)16 и подобные. Примеры кобальтового соединения включают HCo(CO)3, HCo(CO)4, Co2(CO)8, HCo3(CO)9 и подобные. Примеры рутениевого соединения включают Ru(CO)3(PPh3)2, RuCl2(PPh3)3, RuCl3(PPh3)3, Ru3(CO)12 и подобные. Кроме того, примеры железного соединения включают Fe(CO)5, Fe(CO)4PPh3, Fe(CO)4(PPh3)2 и подобные. Среди них, предпочтительно применять родиевое соединение, для которого легко выбрать сравнительно мягкие условия, и с точки зрения доступности особенно предпочтительно применять Rh(acac)(CO)2 и Rh(acac)3.
Применяемое количество металлического соединения, принадлежащего к группам
8-10, предпочтительно находится в диапазоне 0,0001-100 ммоль, и более предпочтительно в диапазоне 0,005-10 ммоль как выражено в единицах атома металла на литр реакционной смеси. Когда применяемое количество металлического соединения, принадлежащего к группам 8-10, является меньшим, чем 0,0001 ммоль, как выражено в единицах атома металла на литр реакционной смеси, скорость реакции становится крайне низкой, тогда как даже когда она является большей чем 100 ммоль, не достигают соответствующий эффект, и стоимость катализатора просто возрастает.
[0023]
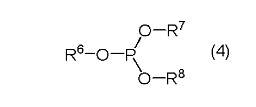
Лиганд, который будут применять, конкретно не ограничена, и можно применять общеизвестные лиганды. Примеры данного лиганда, который можно применять, включают соединения, представленные следующими общими формулами (4)-(6);
фосфорамидиты (смотри WO 03/018192 A, WO 02/083695 A, WO 04/026803 A, WO
06/045597 A, WO 03/06642 A, WO 00/005641 A, WO 99/65606 A, и WO 99/46044 A);
фосфиты, содержащие указанную сшитую структуру (смотри WO 95/00525 A и WO
01/58589 A); фосфины, содержащие указанный заместитель (смотри WO 03/053571 A, WO
03/053572 A, WO 09/059963 A, и WO 00/69801 A); фосфабензол (смотри WO 97/46507 A и
WO 00/55164 A); фосфины, содержащие указанную сшитую структуру (смотри WO
01/85661 A); и подобные.
Конкретно, можно применять, например, соединения, описанные на страницах 9-40
JP 2007-506691 A.
Лиганды можно применять отдельно, или можно применять комбинацию двух или
более.
[0024]
[0025]
Здесь, каждый R6-R8 независимо представляет собой необязательно замещенную углеводородную группу, содержащую 1-24 атома углерода, и они могут быть соединены вместе.
[0026]
[0027]
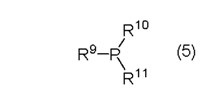
Здесь, каждый R9-R11 независимо представляет собой необязательно замещенную углеводородную группу, содержащую 1-24 атома углерода, и они могут быть соединены вместе.
[0028]
[0029]
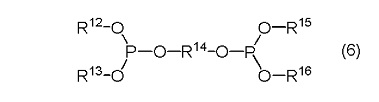
Здесь, каждый R12, R13, R15 и R16 независимо представляет собой необязательно замещенную углеводородную группу, содержащую 1-40 атомов углерода, и R12 и R13, или
R15 и R16, могут быть соединены вместе; и R14 представляет собой необязательно замещенную углеводородную сшивающую группу, содержащую 1-40 атомов углерода.
[0030]
В приведенной выше общей формуле (4) и общей формуле (5), необязательно замещенная углеводородная группа, содержащая 1-24 атома углерода, которую каждый R6-R8 независимо представляет, может быть линейной, разветвленной или циклической, и ее примеры включают алкильную группу, такую как метильная группа, этильная группа, н-пропильная группа, изопропильная группа, н-бутильная группа, изобутильная группа, трет-бутильная группа, н-пентильная группа, циклогексильная группа и т.д.; арильную группу, такую как фенильная группа, нафтильная группа, антраценильная группа и т.д.; и подобные. Среди них, предпочтительными являются фенильная группа и нафтильная
группа.
[0031]
Приведенная выше углеводородная группа может содержать любой заместитель при условии, что не ухудшается реакция гидроформилирования, и ее примеры включают алкильную группу, арильную группу, алкокси группу, силильную группу, аминогруппу, ацильную группу, карбокси группу, ацилоксигруппу, амидную группу, ионную группу, такую как -SO3M (где M представляет собой неорганический или органический катион) и т.д., сульфонильную группу, галоген, нитро группу, циано группу, фторалкильную группу, гидрокси группу и подобные.
[0032]
Примеры соединения, представленного общей формулой (4), которое применяют в качестве лиганда в настоящем изобретении, включают трис(2-метилфенил)фосфит, трис(2,6-диметилфенил)фосфит, трис(2-изопропилфенил)фосфит, трис(2- фенилфенил)фосфит, трис(2-трет-бутилфенил)фосфит, трис(2-трет-бутил-5- метилфенил)фосфит, трис(2,4-ди-трет-бутилфенил)фосфит, ди(2-метилфенил)(2-трет- бутилфенил)фосфит, ди(2-трет-бутилфенил)(2-метилфенил)фосфит и подобные, но соединение не ограничено ими. Среди них, трис(2-трет-бутилфенил)фосфит, трис(2-трет- бутил-5-метилфенил)фосфит и трис(2,4-ди-трет-бутилфенил)фосфит являются предпочтительными с точки зрения промышленной реализации настоящего изобретения.
[0033]
В общей формуле (4), конкретные примеры соединения, в которых R6-R8
соединены вместе, показаны ниже, но соединение не ограничено ими.
[0034]
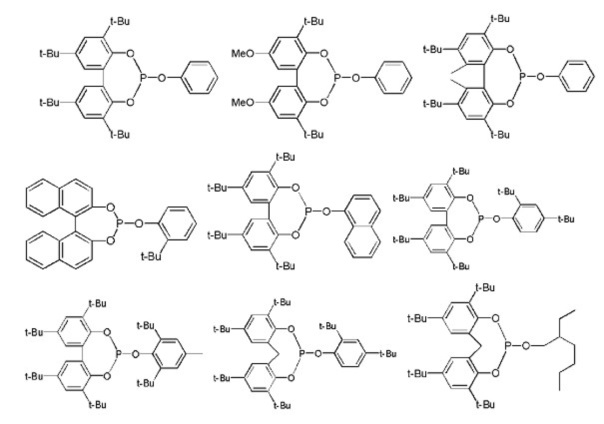
[0035]
Примеры соединения, представленного общей формулой (5), которое применяют в качестве лиганда в настоящем изобретении, включает соли щелочных металлов и соли щелочноземельных металлов трифенилфосфина, три(п-толил)фосфин, три(п- метоксифенил)фосфин, три(п-фторфенил)фосфин, три(п-хлорфенил)фосфин, три(диметиламинофенил)фосфин, пропилдифенилфосфин, трет-бутилдифенилфосфин, н- бутилдифенилфосфин, н-гексилдифенилфосфин, циклогексилдифенилфосфин, дициклогексилфенилфосфин, трициклогексилфосфин, трибензилфосфин, сульфированный трифенилфосфин, (три-м-сульфонил)фосфин, (м- сульфонил)дифенилфосфин и т.д., и подобные, но соединение не ограничено ими.
[0036]
Среди соединений, представленных общими формулами (4) и (5), соединения, попадающие в такой диапазон, что электронный параметр (ν-величины) составляет 2,080-
2,090 см-1, и пространственный параметр (θ-величины) составляет 135-190°, являются
предпочтительными. Приведенные выше два типа параметров представляют собой величины, определяемые согласно описанию в литературе [C.A. Tolman, Chem. Rev., 177,
313 (1977)]. Электронный параметр представляет собой параметр, определяемый в терминах частоты A1 ИК-спектра поглощения CO Ni(CO)3L (L представляет собой фосфорный лиганд), как измерено в дихлорметане; и пространственный параметр определяют в терминах угла при вершине конуса, нарисованного так, чтобы окружать радиус ван-дер-ваальса атома, находящегося на наиболее удаленном от центра месте группы, соединяющей фосфор в положении 2,28 ангстрем от центра атома фосфора.
[0037]
В приведенной выше общей формуле (6), необязательно замещенная углеводородная группа, содержащая 1-40 атомов углерода, которую представляет каждый из R12, R13, R15 и R16, может быть линейной, разветвленной или циклической, и ее примеры включают алкильную группу, такую как метильная группа, этильная группа, н- пропильная группа, изопропильная группа, н-бутильная группа, изобутильная группа, трет-бутильная группа, н-пентильная группа, циклогексильная группа и т.д.; и арильную группу, такую как фенильная группа, нафтильная группа, антраценильная группа и т.д. Среди них, предпочтительными являются фенильная группа и нафтильная группа.
[0038]
Приведенная выше углеводородная группа может содержать любой заместитель при условии, что не ухудшается реакция гидроформилирования, и ее примеры включают алкильную группу, арильную группу, алкокси группу, силильную группу, аминогруппу, ацильную группу, карбокси группу, ацилоксигруппу, амидную группу, ионную группу, такую как -SO3M (где M представляет собой неорганический или органический катион) и т.д., сульфонильную группу, галоген, нитро группу, циано группу, фторалкильную группу, гидрокси группу и подобные.
[0039]
В качестве R12 и R13, которые соединены вместе, R15 и R16, которые соединены вместе, и R14, примеры включают алкиленовую группу, циклоалкиленовую группу, фениленовую группу, нафтиленовую группу, двухвалентную сшивающую группу, представленную следующей общей формулой (7) и подобные.
[0040]
-R17 1
2 18
m-Ar -(CH2)x-Qp-(CH2)y-Ar -R
[0041]
n- (7)
Здесь, каждый R17 и R18 независимо представляет собой необязательно замещенную алкиленовую группу, содержащую 1-6 атомов углерода; каждый Ar1 и Ar2 независимо представляет собой необязательно замещенную ариленовую группу; каждый m, n, p, x, и y равен 0 или 1; Q представляет собой двухвалентную сшивающую группу, выбранную из -CR19R20-, -O-, -S-, -NR21-, -SiR22R23- и -CO-; и каждый из R19-R23 независимо представляет собой любую группу из галогена, необязательно замещенной
алкильной группы, содержащей 1-12 атомов углерода, фенильной группы, толильной группы и анизильной группы.
[0042]
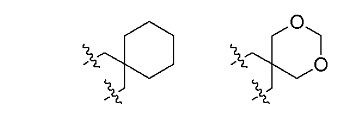
Примеры алкиленовой группы включают этиленовую группу, триметиленовую
группу, тетраметиленовую группу, пентаметиленовую группу, группы, представленные следующими формулами, и подобные.
[0043]
[0044]
В формулах, волнистая линия представляет собой место присоединения.
[0045]
Примеры циклоалкиленовой группы включают циклопропиленовую группу, 1,2- циклопентиленовую группу, 1,3-циклопентиленовую группу, 1,2-циклогексиленовую группу, 1,3-циклогексиленовую группу, 1,4-циклогексиленовую группу и подобные.
Примеры фениленовой группы включают 1,2-фениленовую группу, 1,3-
фениленовую группу, 1,4-фениленовую группу и подобные.
Примеры нафтиленовой группы включают 1,2-нафтиленовую группу, 1,8-
нафтиленовую группу и подобные.
[0046]
Все из R12 и R13, которые соединены вместе, R15 и R16, которые соединены вместе, и R14 могут содержать заместитель. Примеры данного заместителя включают алкильную группу, предпочтительно содержащую 1-5 атомов углерода, такую как метильную группу, этильную группу, пропильную группу, бутильную группу, пентильную группу и т.д.;
алкокси группу, предпочтительно содержащую 1-4 атома углерода, такую как метокси группу, этокси группу, пропокси группу, бутокси группу и т.д.; арильную группу, такую как фенильную группу, нафтильную группу и т.д.; и подобные.
[0047]
В общей формуле (7), примеры необязательно замещенной алкиленовой группы, содержащей 1-6-атомов углерода, как представлено R17 и R18, включают этиленовую группу, н-пропиленовую группу, н-бутиленовую группу, н-пентиленовую группу, н- гексиленовую группу, 2-метил-этиленовую группу, 1,2-диметилэтиленовую группу, 2- метил-н-пропиленовую группу, 2,2-диметил-н-пропиленовую группу, 3-метил-н- пентиленовую группу и подобные. Примеры ариленовой группы, представленной Ar1 и Ar2, включают фениленовую группу, нафтиленовую группу, антрацениленовую группу и подобные. Примеры необязательно замещенной алкильной группы, содержащей 1-12 атомов углерода, как представлено R19-R23, включают метильную группу, этильную
группу, н-пропильную группу, изопропильную группу, н-бутильную группу, изобутильную группу, трет-бутильную группу, н-пентильную группу и циклогексильную группу.
[0048]
Каждый из R17-R23, Ar1 и Ar2 может содержать любой заместитель при условии, что реакция гидроформилирования не ухудшается, и его примеры включают алкильную группу, арильную группу, алкокси группу, силильную группу, аминогруппу, ацильную группу, карбокси группу, ацилокси группу, амидную группу, ионную группу, такую как - SO3M (где M представляет собой неорганический или органический катион) и т.д., сульфонильную группу, галоген, нитро группу, циано группу, фторалкильную группу, гидрокси группу и подобные.
[0049]
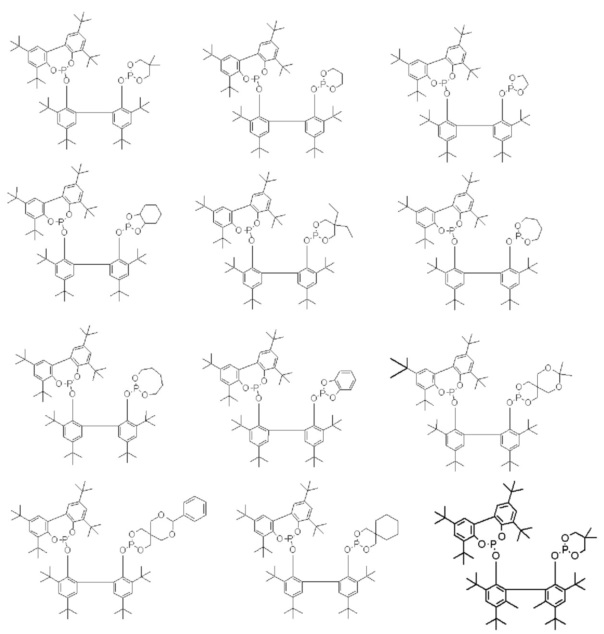
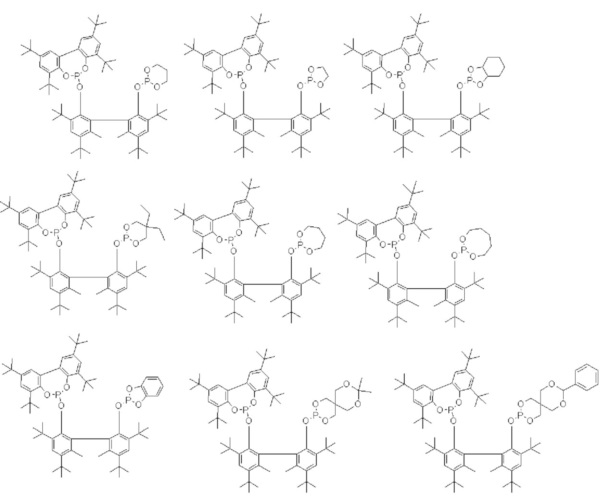
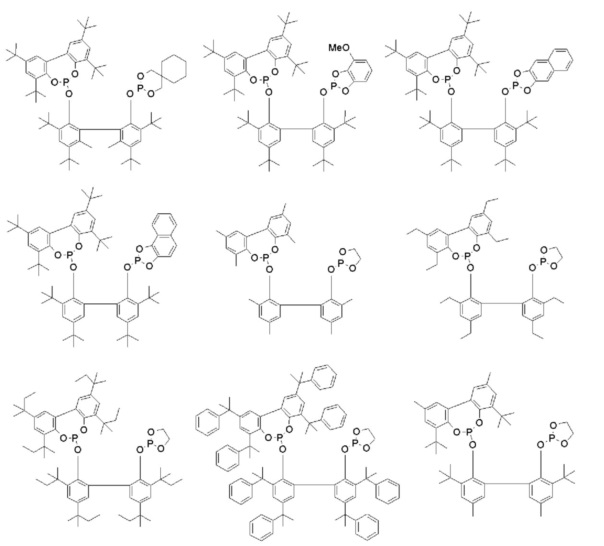
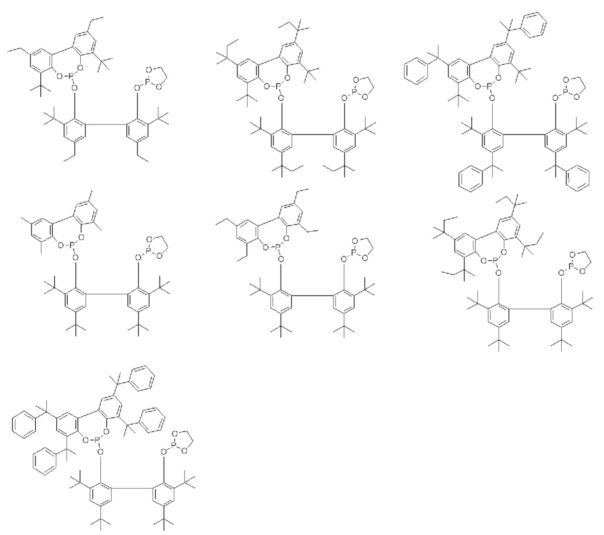
Примеры соединения, представленного общей формулой (6), включают следующие соединения, но соединение не ограничено ими.
[0050]
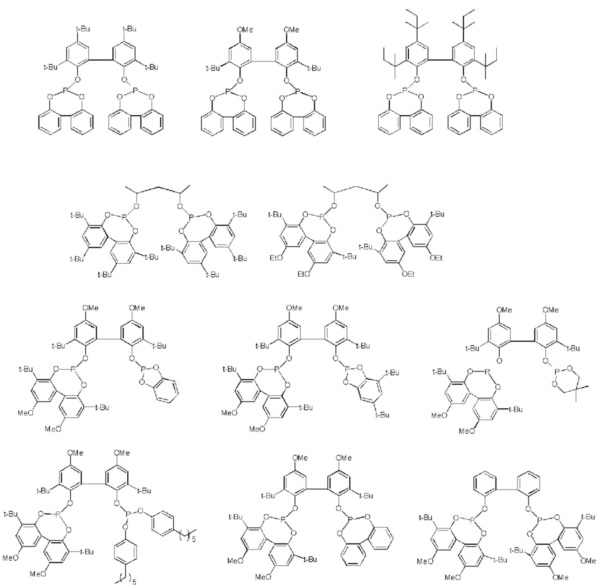
[0051]
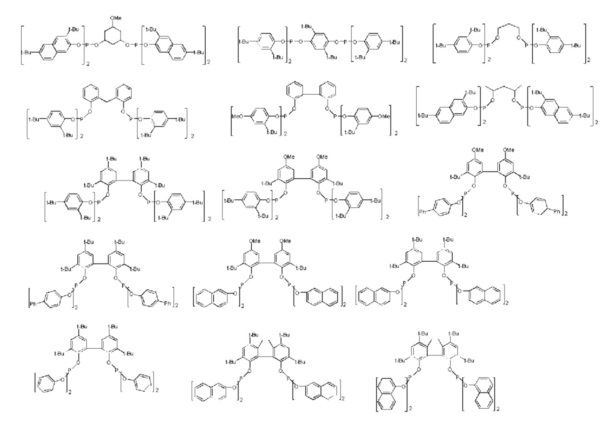
[0052]
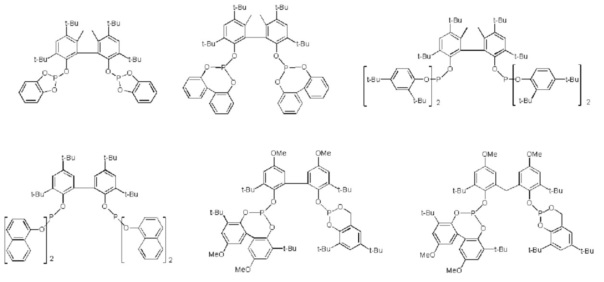
[0053]
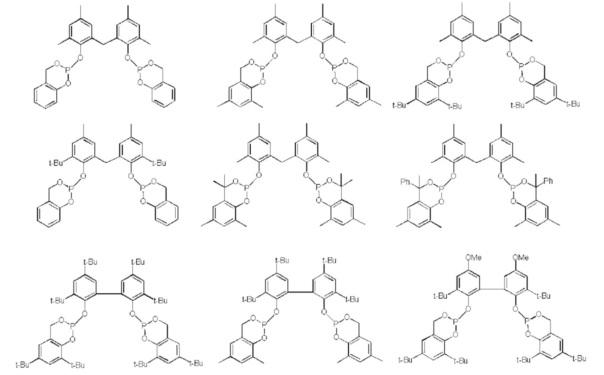
[0054]
[0055]
[0056]
[0057]
[0058]
Среди приведенных выше лигандов, с точки зрения скорости реакции, соединения, представленные формулой (4), являются особенно предпочтительными.
[0059]
Хотя применяемое количество лиганда конкретно не ограничено, оно предпочтительно находится в диапазоне 1-1000 моль, и более предпочтительно в диапазоне 2-500 моль, и с точки зрения скорости реакции, еще более предпочтительно в диапазоне 3-200 моль, как выражено в единицах координирующего атома в лиганде на моль металла в металлическом соединении, принадлежащего к группам 8-10. В случае, когда применяемое количество лиганда является меньшим, чем 2 моль, как выражено в единицах координирующего атома в лиганде на моль металла в металлическом соединении, принадлежащего к группам 8-10, стабильность катализатора ухудшается, тогда как в случае, когда он является большим, чем 1000 моль, скорость реакции становится низкой.
[0060]
Реакцию гидроформилирования можно проводить в присутствии или отсутствии растворителя. Примеры данного растворителя включают насыщенные алифатические углеводороды, такие как пентан, гексан, гептан, октан, нонан, декан, циклогексан и т.д.; ароматические углеводороды, такие как бензол, толуол, этилбензол, пропилбензол, ксилол, этилтолуол и т.д.; спирты, такие как изопропанол, изобутанол, изопентанол, неопентиловый спирт, этиленгликоль, 1,2-пропандиол, 1,3-пропандиол, 1,2-бутандиол,
1,4-бутандиол, диэтиленгликоль, триэтиленгликоль и т.д.; эфиры, такие как диметиловый эфир, этилметиловый эфир, диэтиловый эфир, дипропиловый эфир, бутилметиловый эфир, трет-бутилметиловый эфир, дибутиловый эфир, этилфениловый эфир, дифениловый эфир, тетрагидрофуран, 1,4-диоксан, диметиловый эфир диэтиленгликоля, диметиловый эфир триэтиленгликоля, диметиловый эфир тетраэтиленгликоля и т.д.; кетоны, такие как ацетон, этилметилкетон, метилизопропилкетон, диэтилкетон, этилпропилкетон, дипропилкетон и т.д.; и подобные. Данные растворители можно применять отдельно или можно применять в комбинации два или более. В случае применения растворителя, хотя применяемое количество растворителя конкретно не ограничено, в общем, оно предпочтительно находится в диапазоне 1-90% по массе относительно всей реакционной
смеси.
[0061]
Температура реакции в реакции гидроформилирования предпочтительно находится в диапазоне 40-170°C, и с точки зрения подавления дезактивации катализатора, более предпочтительно в диапазоне 50-150°C. Кроме того, давление реакции предпочтительно находится в диапазоне 0,01-15 МПа (манометрическое давление), и более предпочтительно в диапазоне 0,5-10 МПа (манометрическое давление). Продолжительность реакции обычно находится в диапазоне 0,5-20 часов и предпочтительно в диапазоне 0,5-10 часов.
[0062]
Способ осуществления реакции гидроформилирования конкретно не ограничен. Например, ацетальное соединение (2) загружают в присутствии газовой смеси монооксида углерода/водорода 1/1 (молярное соотношение), смешанный раствор лиганда, металлического соединения, принадлежащего к группам 8-10, и растворитель добавляют при перемешивании, и содержимое реагирует друг с другом при заранее определенной температуре и заранее определенном давлении в течение заранее определенного периода времени.
Реакцию можно проводить или в периодическом режиме или в непрерывном режиме, применяя реактор с перемешиванием, реактор с циркулированием, реактор типа
ректификационная колонна или подобный. При необходимости, реакцию можно осуществлять извлечением непрореагировавшего ацетального соединения (2) из реакционного раствора после реакции и рециклированием его в реактор. Непрерывный режим можно осуществлять, применяя один реактор или несколько реакторов, установленных последовательно или параллельно.
[0063]
Способ разделения и очистки ацетального соединения (1) из реакционной смеси, получаемой приведенным выше способом, конкретно не ограничен, и можно вводить способ, который введен для стандартного разделения и очистки органического соединения. Например, ацетальное соединение (1) с высокой чистотой можно получить упариванием растворителя, основных веществ и подобных из реакционной смеси при пониженном давлении, и затем перегонкой остатка при пониженном давлении. Кроме того, перед данной перегонкой, применяя на остатке способ, такой как упаривание, экстракция, адсорбция и т.д., можно отделить лиганд и металлическое соединение, принадлежащее к группам 8-10. Отделенный лиганд и металлическое соединение, принадлежащее к группам 8-10, можно снова применять в реакции гидроформилирования.
[0064]
(Получение MGL)
Далее, описан способ получения MGL гидролизом ацетального соединения (1). MGL можно получить реакцией ацеталя (1) с водой. Реакцию с водой можно осуществлять в отсутствии катализатора, и при необходимости, кислоту можно применять в качестве катализатора. Кислота, которую будут применять, конкретно не ограничена, и ее примеры включают неорганические кислоты и их соли, такие как серная кислота, фосфорная кислота, азотная кислота, соляная кислота, борная кислота и т.д.; органические кислоты и их соли, такие как муравьиная кислота, уксусная кислота, пропионовая кислота, щавелевая кислота, метансульфоновая кислота, п-толуолсульфоновая кислота, п- толуолсульфонат пиридиния и т.д.; твердые кислоты, такие как катионообменная смола, алюмосиликат, цеолит, активированная глина т.д.; и подобные.
Хотя применяемое количество приведенной выше кислоты изменяется в зависимости от типа применяемой кислоты или количества воды, поскольку рассматривается случай применения хлористоводородной кислоты, кислоту применяют в количестве предпочтительно в диапазоне от 0,0001% по массе до 10% по массе, и более предпочтительно в диапазоне от 0,001% по массе до 5% по массе реакционного раствора. Когда применяемое количество кислоты является меньшим, чем 0,0001% по массе, часто не получают достаточной скорости реакции, тогда как в случае применения кислоты в
количестве большем, чем 10% по массе, применяемое количество основания в случае нейтрализации увеличивается, так что загрузка в способе постобработки увеличивается.
[0065]
Хотя количество воды, которое будут применять, конкретно не ограничено, оно обычно является 0,1-10000 кратным по массе, предпочтительно 0,2-5000 кратным по массе и более предпочтительно 0,3-1000 кратным по массе относительно ацетального соединения (1). В случае, когда количество воды является меньшим чем 0,1 кратное по массе, часто не получают достаточный выход, тогда как в случае применения воды в количестве большем, чем 10000 кратное по массе, энергозатраты, необходимые для извлечения целевого вещества, увеличиваются.
[0066]
Реакцию можно проводить в присутствии или отсутствии растворителя. Хотя растворитель, который будут применять, конкретно не ограничен, его примеры включают эфиры, такие как тетрагидрофуран, диэтиловый эфир, диизопропиловый эфир, трет- бутилметиловый эфир, метилтетрагидропиран, диметиловый эфир этиленгликоля и т.д.; алифатические или ароматические углеводороды, такие как гексан, гептан, циклогексан, толуол, ксилол, мезитилен и т.д.; кетоны, такие как ацетон, метилизопропилкетон, метилизобутилкетон и т.д.; и подобные. Их можно применять отдельно, или можно применять в комбинации двух или более. Применяемое количество растворителя конкретно не ограничено.
[0067]
Хотя продолжительность реакции конкретно не ограничена, она обычно составляет
5 секунд или более, предпочтительно 1 минуту или более и более предпочтительно 10 минут или более. Хотя температура реакции конкретно не ограничена, она обычно составляет -200°C-350°C, предпочтительно 0°C-250°C и более предпочтительно 10°C-
100°C.
[0068]
MGL в реакционной смеси, полученной приведенным выше способом, можно выделить и очистить, при необходимости. Способ выделения и очистки конкретно не ограничен, и можно применять способ, который приспособлен для стандартного выделения и очистки органического соединения. Например, MGL с высокой чистотой можно получить упариванием растворителя или спирта, полученного гидролизом, из реакционной смеси при пониженном давлении, и затем перегонкой остатка при пониженном давлении. Кроме того, перед данной перегонкой, применяя на остатке способ, такой как нейтрализация, поглощение, промывка и т.д., можно удалить кислоту.
Для того чтобы избежать мультимеризации, полученный в результате MGL можно также хранить разбавленным растворителем, таким как вода и т.д., при необходимости.
Примеры
[0069]
Настоящее изобретение далее конкретно описано со ссылкой на примеры и так далее, но не следует считать, что настоящее изобретение никоим образом не ограничено данными примерами.
[0070]
(Пример 1: получение соединения A)
[0071]
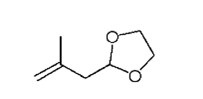
Соединение A
[0072]
В реактор помещали 1,390 г циклогексана, 618,0 г (9,96 моль) этиленгликоля и 0,3 г (3,1 ммоль) серной кислоты и нагревали до 90°C. 686,0 г (8,16 моль) 3-метил-3-бутен-1- аля добавляли порциями в течение 4 часов, удаляя получаемую воду из системы посредством азеотропного осушения. После завершения добавления порциями, содержимое перемешивали при 90°C в течение 1 часа, и затем реакционную смесь охлаждали до комнатной температуры и нейтрализовали метоксидом натрия. Растворитель упаривали при пониженном давлении из полученного в результате реакционного раствора, и остаток перегоняли и очищали, получая 969,0 г (7,56 ммоль, выход: 92,6%) целевого соединения A.
1H-ЯМР (400 МГц, CDCl3, TMS) δ: 1,805 (с, 3H), 2,382 (д, 2H), 3,843-4,008 (м, 4H),
4,828 (кв, 1H), 4,868 (т, 1H), 4,982 (т, 1H)
[0073]
(Пример 2: Получение соединения B)
[0074]
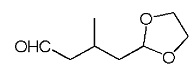
Соединение B
[0075]
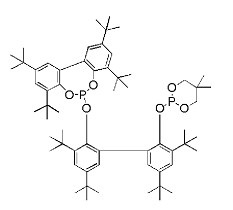
бисфосфит A
[0076]
Получали раствор 1,08 г бисфосфита A и 14,2 мг Rh(acac)(CO)2, растворенного в
100 мл толуола [(атом родия)/(атом фосфора)]=1/20 (молярное соотношение)]. В автоклаве с электромагнитным перемешиванием с входным отверстием для газа и отверстием для отбора проб, 45 мл соединения A и 10 мл полученного выше каталитического раствора (концентрация родиевого соединения в реакционной системе: 0,1 ммоль/л) добавляли в атмосфере азота; давление в автоклаве регулировали равным 8 МПа (манометрическое давление) смесью газов монооксида углерода/водорода 1/1 (молярное соотношение); затем, температуру в автоклаве повышали до 130°C при перемешивании; и содержимое реагировало в течение 4 часов. В процессе реакции, смесь газов монооксида углерода/водорода 1/1 (молярное соотношение) непрерывно подавали, поддерживая давление внутри реактора равным фиксированному значению. Как результат анализа полученного в результате реакционного раствора посредством газовой хроматографии, конверсия соединения A составляла 90,0%, и селективность соединения B составляла
97,0%.
[0077]
(Пример 3: Получение соединения B)
Реакцию осуществляли тем же способом, как в примере 2, за исключением применения 3,56 г трис(2,4-ди-трет-бутилфенил)фосфита вместо бисфосфита A, регулируя соотношение (атом родия)/(атом фосфора) 1/100 (молярное соотношение) и заменяя продолжительность реакции на 2 часа. Конверсия соединения A составляла 99,2%, и селективность соединения B составляла 94,3%.
[0078]
(Пример 4: Получение соединения B)
Реакцию осуществляли тем же способом, как в примере 2, исключением применения 1,44 г трифенилфосфина вместо бисфосфита A, регулируя соотношение (атом родия)/(атом фосфора) 1/100 (молярное соотношение) и заменяя продолжительность реакции на 3,5 часа. Конверсия соединения A составляла 80,0%, и селективность
соединения B составляла 94,1%.
[0079]
(Пример 5: получение MGL)
В трехгорлую колбу загружали 636,4 мг 1 моль/л хлористоводородной кислоты
(хлористоводородная кислота: 0,64 ммоль, 23,3 мг), 600 мл дистиллированной воды и
100,8 г (636,9 ммоль) соединения B, и содержимое перемешивали в атмосфере азота при
60°C в течение 3,5 часов. Как результат анализа полученного в результате реакционного раствора посредством газовой хроматографии, конверсия соединения B составляла 97,2%, и селективность MGL составляла 99,8%. Реакционный раствор охлаждали до комнатной температуры, затем нейтрализовали гидрокарбонатом натрия и экстрагировали три раза
600 мл этилацетата. Полученные в результате органические слои объединяли, растворитель упаривали при пониженном давлении, и затем остаток перегоняли и очищали, получая 65,8 г (576,4 ммоль, выход: 90,5%) MGL.
Промышленная применимость
[0080]
3-Метилглутаральдегид (MGL), получаемый настоящим изобретением, является полезным соединением в качестве отверждающего агента для фоточувствительного материала, дубильного агента для кожи и синтетического промежуточного соединения.
Реферат
Предложен способ получения 3-метилглутаральдегида, включающий стадию гидролиза соединения, представленного следующей общей формулой (1):где Rи Rсоединены вместе, представляя собой алкиленовую группу, содержащую 2-6 атомов углерода, и стадию, где подвергают взаимодействию соединение, представленное следующей общей формулой (2):где Rи Rсоединены вместе, представляя собой алкиленовую группу, содержащую 2-6 атомов углерода, для гидроформилирования, получая соединение, представленное следующей общей формулой (1). Также предложено соединение, представленное следующей общей формулой (3):В которой Rпредставляет собой линейную алкиленовую группу, содержащую 2 или 4-6 атомов углерода. Технический результат – обеспечение способа получения MGL (3-метил-1,5-петандиаль) с хорошим выходом в мягких условиях и нового ацетального соединения. 2 н. и 1 з.п. ф-лы, 5 пр., 6 ил.
Формула

Комментарии