Устройство для нейрохирургической аспирации со спектроскопическим и электрофизиологическим контролем - RU183278U1
Код документа: RU183278U1
Чертежи
Описание
Описание полезной модели
Полезная модель относится к области медицинской техники, а именно к устройствам для проведения интраоперационной навигации с использованием методов оптической спектроскопии и нейрофизиологической стимуляции.
Спектроскопический анализ биологических сред позволяет определять как структурные изменения тканей, так и их метаболическую активность, не повреждая сами ткани. Методы спектроскопического анализа, такие как флуоресцентная спектроскопия и спектроскопия диффузного отражения, отличаются высокой скоростью, значительной чувствительностью и хорошим пространственным разрешением, что приобретает особое значение в микрохирургии и в нейроонкологии. В современной клинической практике активно применяются различные методы интраоперационной диагностики, одним из которых является флуоресцентная навигация [А.А. Потапов, С.А. Горяйнов, В.А. Охлопков и др. [Клинические рекомендации по использованию интраоперационной флуоресцентной диагностики в хирургии опухолей головного мозга]. Журнал «Вопросы нейрохирургии» имени Н.Н. Бурденко. 2015; 79(5): 91-101] с использованием в качестве опухолевого маркера протопорфирина IX (Пп IX). Значительную диагностическую ценность представляют и такие параметры как уровень кровенаполнения и оксигенации гемоглобина в сосудах опухоли и в окружающей ткани [А.А. Потапов, С.А. Горяйнов, В.Б. Лощенов и др. [Интраоперационная комбинированная спектроскопия (оптическая биопсия) глиом головного мозга]. Журнал «Вопросы нейрохирургии» имени Н.Н. Бурденко. 2013; 77(2): 3-10]. В то время как для оценки концентрации опухолевого маркера Пп IX используется метод флуоресцентной спектроскопии (с использованием лазерного возбуждающего излучения), для оценки степени кровенаполнения и оксигенации гемоглобина необходимо производить анализ диффузно отраженного тканью излучения в широком спектральном диапазоне.
На данный момент в клинической практике интраоперационная спектроскопическая диагностика осуществляется последовательно - сначала происходит регистрация спектров флуоресценции, а затем регистрация спектров диффузного отражения - с использованием одного оптоволоконного устройства [Pablo A. Vald'es et al., Combined fluorescence and reflectance spectroscopy for in vivo quantification of cancer biomarkers in low- and high-grade glioma surgery, Journal of Biomedical Optics, November 2011, 16(11)]. Недостатком этого подхода является невозможность однозначно сопоставить область, где проводится регистрация спектров флуоресценции, и область, где проводится регистрация спектров диффузного отражения.
Известным устройством, относящимся к системам для определения границ опухоли с помощью флуоресцентной диагностики и наиболее близким к предлагаемой полезной модели является спектральное устройство для контроля и мониторинга процесса фотодинамической терапии, описанное в патенте РФ №2169590 (МПК A61N 5/06, от 27.06.2001). Устройство содержит спектрометр, включающий полихроматор с волоконно-оптическим вводом излучения, в котором установлен специальный фильтр, ослабляющий интенсивность рассеянного излучения лазера, блок регистрации и программно-аппаратный компьютерный модуль, лазер и широкополосный источник света, оснащенные устройствами ввода излучения в световод, волоконно-оптический зонд, включающий световод для доставки лазерного излучения, световод для доставки широкополосного излучения и приемный световод.
Недостатком описанного устройства является невозможность однозначно сопоставить область анализа спектроскопического зонда и область работы канюли аспиратора ввиду поочередного использования сначала устройства для спектроскопического анализа и затем устройства для удаления участков опухоли.
Известно устройство для осуществления удаления опухолей мозга с выделением границ опухоли флуоресцентной диагностикой с одновременной коагуляцией и аспирацией, описанное в патенте РФ №2510248 (МПК А61В 17/3205, от 23.04.2012). Устройство включает сапфировый зонд с продольными каналами, в которых размещены оптические волокна, одни из которых предназначены для подачи излучения, возбуждающего флуоресценцию и коагулирующего излучения в зону деструкции ткани от присоединенных источников излучения, другие предназначены для передачи излучения флуоресценции на средство, регистрирующее это излучение. Сапфировый зонд также имеет открытый канал для аспирации, соединенный с аспиратором посредством шланга. Одним из недостатков этого устройства является его форма (цилиндр), поскольку в поле зрения нейрохирургического микроскопа попадает не только дистальная часть зонда, но и рукоятка вместе с рукой хирурга, что сужает обзор операционной зоны и существенно ограничивает подвижность инструмента в операционном поле. При этом материал, из которого изготовлено устройство (сапфир), не позволяет изготавливать зонды иной формы.
Задачей настоящего технического решения является создание устройства, которое обеспечивает повышение точности спектроскопической диагностики в зоне нейрохирургической аспирации, а также повышает качество работы хирурга.
Поставленная задача решается тем, что предложенное устройство для нейрохирургической аспирации со спектроскопическим и электрофизиологическим контролем, содержащее спектрометр, источники оптического излучения и волоконно-оптический зонд, содержит рабочую часть волоконно-оптического зонда, выполненную как наконечник нейрохирургического аспиратора, что позволяет проводить спектроскопический анализ в области, совпадающей с областью аспирации тканей.
Также задача решается тем, что предложенное устройство содержит как узкополосный световой источник для возбуждения флуоресценции, так и световой источник широкополосного излучения для регистрации спектров диффузного отражения, что позволяет определять степень злокачественности исследуемых тканей одновременно по нескольким параметрам : накопление Пп IX, концентрация гемоглобина, степень оксигенации гемоглобина, оптическая плотность тканей, для повышения точности определения границ опухоли.
Также задача решается тем, что предложенное устройство изготовлено из проводящего материала и выполняет функцию монополярного стимулятора для системы интраоперационного нейромониторинга, что позволяет определять функциональность нервных тканей в исследуемой области во избежание повреждения функционально-значимых нервных тканей.
Также задача решается тем, что предложенное устройство имеет форму, позволяющую наблюдать в поле зрения нейрохирургического микроскопа только дистальный конец рабочей части, что обеспечивает максимально возможный обзор операционного поля и свободу манипуляций хирурга.
Работа устройства поясняется на фиг. 1 и фиг. 2.
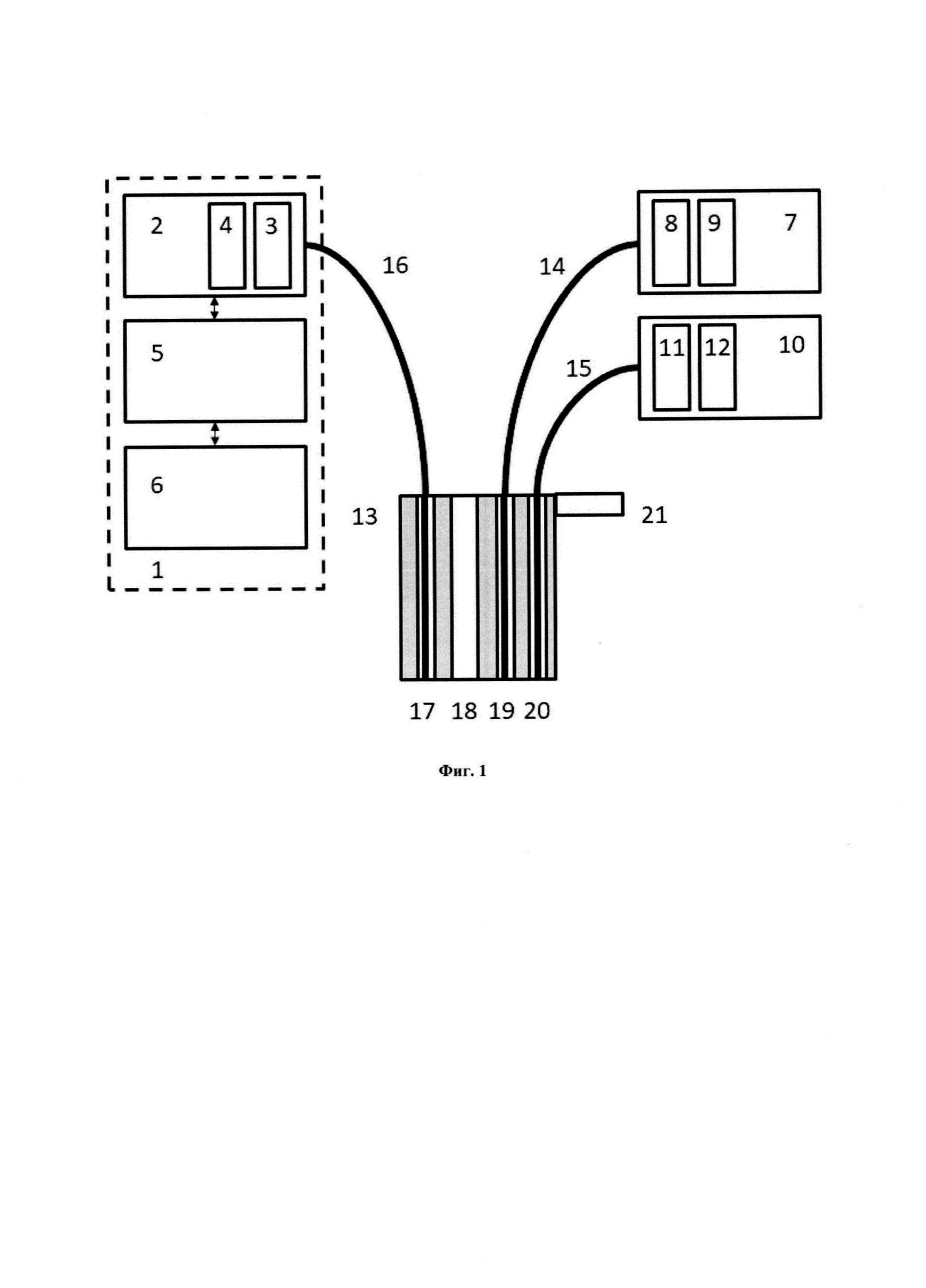
На Фиг. 1 приведена блок-схема предлагаемого устройства, где:
1 - спектрометр;
2 - полихроматор;
3 - волоконно-оптический ввод;
4 - фильтр;
5 - блок регистрации;
6 - вычислительный модуль;
7 - источник узкополосного светового излучения;
8 - устройство ввода излучения;
9 - фильтр;
10 - источник широкополосного светового излучения;
11 - устройство ввода излучения;
12 - фильтр;
13 - рабочая часть волоконно-оптического зонда;
14 - световод для доставки узкополосного излучения;
15 - световод для доставки широкополосного излучения;
16 - приемный световод;
17 - канал для приемного световода;
18 - канал для аспирации;
19 - канал для световода узкополосного светового излучения;
20 - канал для световода широкополосного светового излучения;
21 - разъем для соединения с системой нейромониторинга.
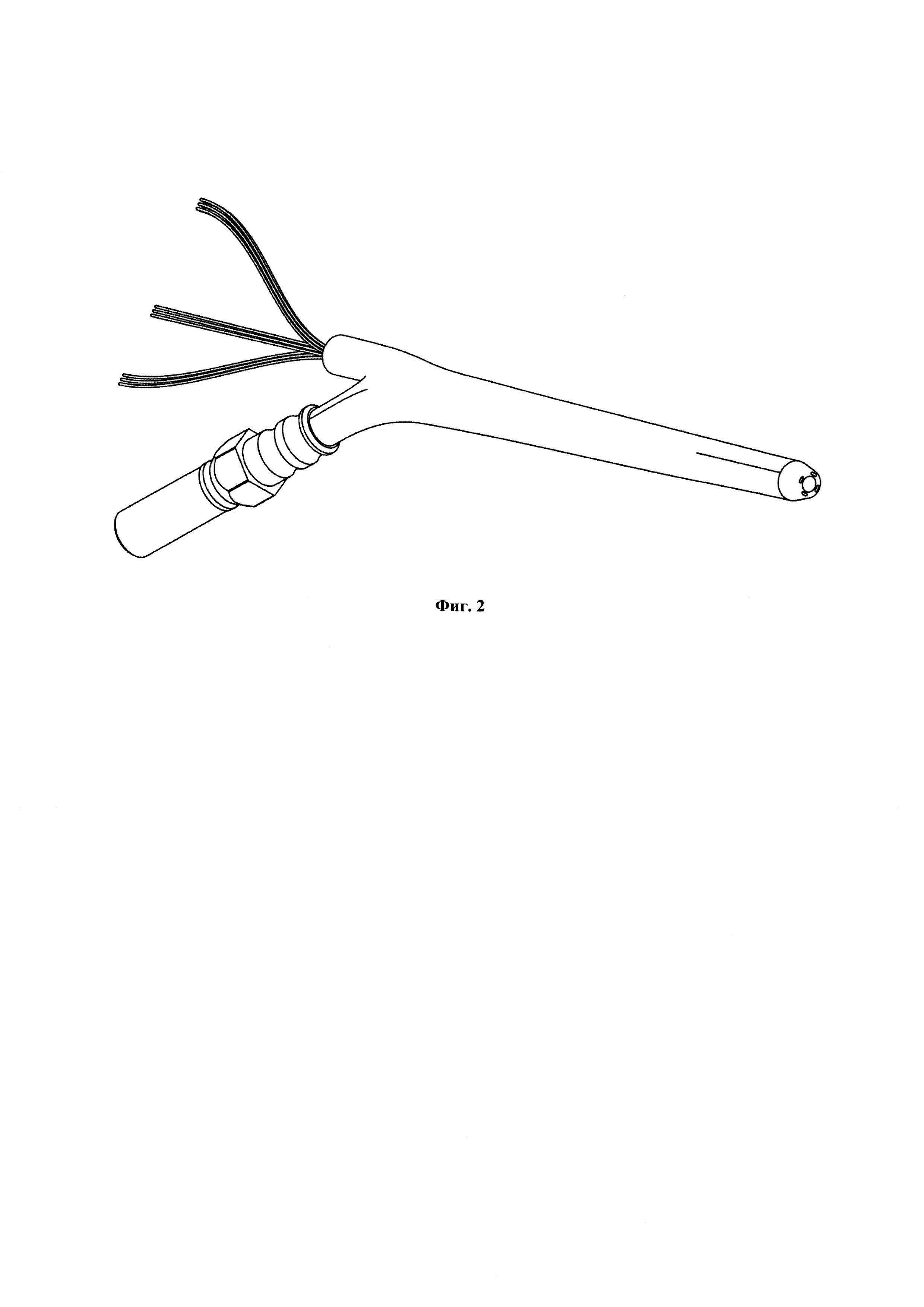
На фиг. 2 приведен эскиз рабочей части предлагаемого устройства.
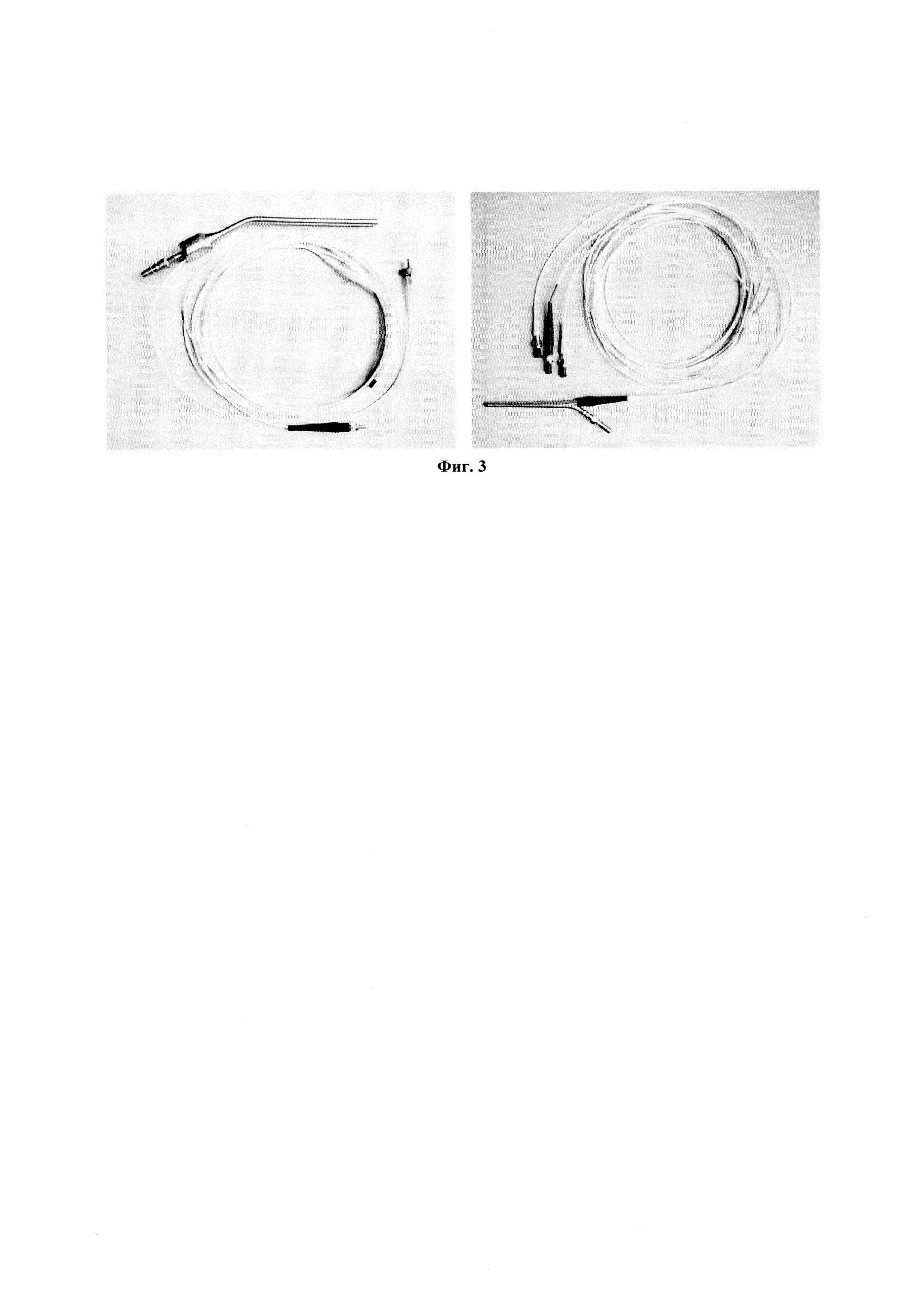
На фиг. 3 показаны рабочая часть и оптоволоконный зонд устройства для нейрохирургической аспирации со спектроскопическим и электрофизиологическим контролем в двух вариантах исполнения: слева - с одним осветительным каналом и одним приемным, справа - с двумя осветительными каналами и одним приемным.
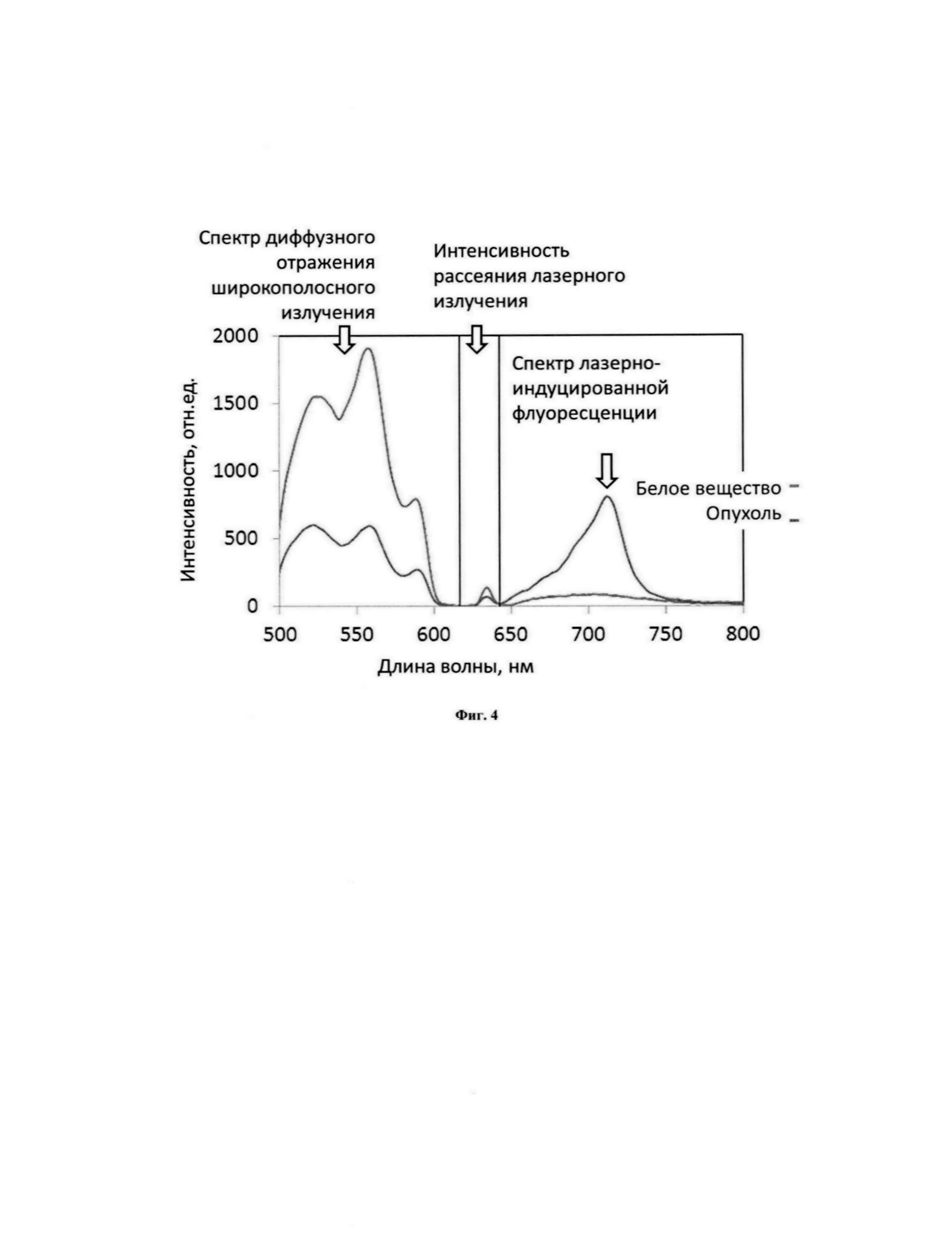
На фиг. 4 приведены результаты апробации разработанного устройства на оптических фантомах.
Предлагаемое устройство содержит (Фиг. 1) спектрометр (1), включающий полихроматор (2) с волоконно-оптическим вводом излучения (3), в котором установлен фильтр (4), ослабляющий интенсивность рассеянного излучения узкополосного источника, блок регистрации (5) и вычислительный модуль (6), узкополосный источник излучения (7) и широкополосный источник света (10), оснащенные устройствами ввода излучения в световоды (8, 11) и фильтрами (9, 12), волоконно-оптический зонд с рабочей частью (13), включающий один или несколько световодов для доставки узко полосного излучения (14), один или несколько световодов для доставки широкополосного излучения (15) и один или несколько приемных световодов (16), рабочая часть волоконно-оптического зонда (13) содержит канал для приемного световода (17), канал для аспирации (18), канал для световода узкополосного излучения (19), канал для световода широкополосного излучения (20), разъем для соединения с системой нейромониторинга (21).
Предлагаемое устройство работает следующим образом. Выходящее из узкополосного источника света (7) излучение проходит через полосовой светофильтр (9), подавляющий паразитное излучение в спектральных диапазонах регистрации флуоресцентного излучения и сигнала диффузного отражения. Выходящее из широкополосного источника света (10) излучение проходит через краевой/полосно-пропускающий фильтр (12), подавляющий паразитное излучение в спектральном диапазоне возбуждения и регистрации флуоресцентного излучения. Подвергшееся фильтрации узкополосное и широкополосное излучение подается по разным каналам (14, 15) на дистальный конец рабочей части волоконно-оптического зонда (13). Рабочая часть волоконно-оптического зонда (13) выполнена как наконечник нейрохирургического аспиратора, содержащий каналы для световодов (17, 19, 20) и канал для аспирации (18), а также контакт для подключения к системе нейромониторинга (21). Оптические волокна расположены на торце рабочей части волоконно-оптического зонда в соответствии с оптимальной для конкретного использования схемой освещения и регистрации излучения.
Излучение, подвергшееся взаимодействию с биологической тканью в зоне аспирации, подается на вход спектрометра (1) посредством волоконно-оптического ввода (3), на проксимальном конце которого приемные волокна формируют линию. При этом узкополосное излучение подвергается ослаблению за счет использования полосового ослабляющего фильтра (4) для реализации возможности регистрации флуоресцентного и возбуждающего его узкополосного излучения в одном динамическом диапазоне. Излучение подвергается в полихроматоре (2) разложению в спектр, после чего поступает в блок регистрации (5). Данные из блока регистрации поступают в вычислительный модуль (6), где подвергаются обработке для определения физиологических параметров на основании анализа регистрируемых спектральных зависимостей. Полученная информация позволяет формировать рекомендации для регулировки скорости/мощности аспирации тканей. Спектроскопические характеристики дают информацию о степени озлокачествления тканей, в то время как данные нейромониторинга свидетельствуют об их функциональной целостности, что позволяет избежать удаления здоровых тканей и сохранения злокачественных.
На Фиг. 2 приведен эскиз рабочей части волоконно-оптического зонда.
На Фиг. 3 приведен внешний вид волоконно-оптического зонда в различных исполнениях.
Предложенное устройство было апробировано на образцах биологических тканей, полученных при удалении глиальной опухоли ex vivo (спектральные зависимости приведены на Фиг. 4). По результатам апробации показана способность одновременной регистрации спектральных зависимостей от биологических тканей, проведения нейромониторинга и аспирации тканей.
Таким образом, устройство обеспечивает одновременность спектроскопического анализа тканей с их аспирацией и нейромониторингом, что приводит к повышению точности спектроскопической диагностики в зоне нейрохирургической аспирации, а также повышает качество работы хирурга.
Реферат
Устройство относится к области медицинской техники, а именно к устройствам для проведения интраоперационной навигации с использованием методов оптической спектроскопии и нейрофизиологической стимуляции. Устройство содержит спектрометр, включающий полихроматор с волоконно-оптическим вводом излучения, блок регистрации с фотоприемником и программно-аппаратный модуль, узкополосный световой источник для возбуждения флуоресценции и световой источник широкополосного излучения для регистрации спектров диффузного отражения для определения степени злокачественности исследуемых тканей одновременно по нескольким параметрам для повышения точности определения границ опухоли, волоконно-оптический зонд, рабочая часть которого выполнена в одном корпусе с канюлей нейрохирургического аспиратора и может быть использована в качестве монополярного стимулятора для системы интраоперационного нейромониторинга. Устройство обеспечивает повышение точности спектроскопической диагностики в зоне нейрохирургической аспирации, а также повышает качество работы хирурга.

Комментарии