Способ определения тромбина, плазмина, трипсина и тромбиноподобных ферментов в биологических жидкостях - SU1099839A3
Код документа: SU1099839A3
Описание
со
со
00
со со Изобретение относится к медицине а именно биологическим методам иссле ;:;ования биологических жидкостей. Известен способ определения тромбина , плазммна, трипсина и тромбиноподобных ферментов в биологических жидкостях путем взаимодействия пробы биологической жидкости с субстратом с последующим определением продуктов гидролиза фотометрически, спектрометрически или флюорографически 1 Однако известный способ недостаточно чувствителен. Цель изобретения - , повьшление чувствительности способа. Поставленная цель достигается тем что согласно способу определения тромбина, плазмина, трипсина и тром биноподобных ферментов в биологичес ких жидкостях путем взаимодействия пробы биологической жидкости с субс ратом с последующим определением про дуктов гидролиза фотометрически, спе трометрически или флюоресцентноспектрофотометрически в качестве субстра та используют вещество общей формулы R -гли-про-X-NH-R (1) или общей формулы R-гли-про-арг-NH-R (2) где R - водород .или блокирующая ацильная или сульфанильная группа; - - замещенный ароматический углеводородный остаток; X - аргинильная или лизильная группа. Субстрат может быть протонизован минеральной кислотой, например HCI;,. НВг, H2SO или .,или органической кислотой, например муравьиной, щавелевой или винной. R - ацильная группа может быть изображена частичной формулой где алифатический углеводородный остаток с 1-17, предпочтительно 1-8 атомами С; аралифатический углеводородный остаток, алифатическая груп па которого содержит 1-6 атомов С; циклоалифатический углеводородный остаток; ароматический углеводородный остаток; алкилоксигруппа с 1-17 предпочтительно 1-6, атомами С, или ,бензилоксигруппа„ R может обозначат неразветвленную или разветвленную алкильную группу, например метил, этил, пропил, бутил, пентил, гексил гептил, октил и т.д. до гептадецила бензильную 2-фенилэтильную, 3-фенилпропильную и т.д« до 11-фенилундецильной группы; циклогексильную или фенильную, oi - нафтильную, р -нафтильную или бифенильную группу, а также бенэилоксигруппу. R - сульфонильная группа - может представлять собой алкансульфонилгруппу , алкановый остаток которой содержит 1-17, предпочтительно 1-6, атомов С, например метан- или этансульфонильную группу или арсульфонильную группу, ароматическое ядро которой может быть замещено одной или несколькими {например, тремя) алкильными группами, например бензолсульфонильную , п-толуолсульфонильную или нафталинсуль фонильную группу, R может представлять собой, например , п-нитрофенильную, 2-нафтильную или 4-метокси-2-нафтильную группу. Субстрат можно получать различны-ми известными методами, например, согласно одному из них связывают хромофорные группы (R в формуле 1) с С-концевой аминокислотной группой. Эти группы одновременно имеют функцию С-концевых групп, защйщакжшх карбоксильную группу во время ступенчатого соединения аминокислот при образовании желаемой пептидной цепи. Остальные защитные группы селективно отщепляют от целевого продукта без влияния на хромофорную группу. Анализ элкхатов и продуктов проводят путем тонкослойной хроматографии. Для этой цели п зименяют покрытые гелем двуокиси кремния Ф 254 стеклянные пластинки. Для проявления тонкослойных хроматограмм применяют следующие системы раст ворителей : хлороформ :метанол 9:1; н-пропанол:этиловый эфир уксусной кислоты; вода 7:1:2; н-бутанол:уксусная кислота; вода 3:1:1. Хроматограммы проявляют сначала в ультрафиолетовом свете и потом путем реакции с хлором/толуидином. Подгруппа определенных формулой I субстратов соответствует веществу, описанному следующей формулой R-гли-про-арг-R где R - алкилоксикарбонильная группа , алкилостаток которой содержит 1-6 атомов С, аралкилоксикарбонилгруппа , алкиленовый остаток которой содержит 1-6 атомов С, алкансульфонильная группа, алканостаток которой содержит 1-6 атомов С, арилсульфониягруппа , арилостаток которой содержит в соответствующем случае заместители, или алкансильная группа, алканостаток которой содержит 1-6 атомов С; К - h-нитрофенильная, 2-нафтильная или 4-метокси-2-нафтильная группа. Субстраты этой формулы имеют высокую восприимчивость не только в отношении плазмина и трипсина, а также и в отношении тромбина и тромбиноподобных энзимов. Пример 1. К -Кбо-гли-про-арг-пНА-НС ; кбо-арг-рНА-HCI.
В круглодонной трехгорлой колбе емкостью 250 мл растворяют 16,0 г высушенного пятиокисью фосфора кбоapr-OK-HCJ в 90 мл абсолютного ГМПТА (триамид N, N, N , N, N - гексаметилфосфорной кислоты) без доступа влаги при 20°С. К полученному раствору прибавляют при комнатной температуре сначала раствор 4,74 г триэтиламина в 10 мл ГМПТА и затем 1б,4 г п-нитрофенилизоцианата (100%-ный избыток) по порциям.
После 24 ч при 20°С ГМПТА большей частью отгоняют в вакууме. Остаток экстрагируют неоднократно 30%-ной уксусной кислотой-. Остаток выбрасывают .
Соединенные экстракты уксусной кислоты для дальнейшей очистки наносят на.уравновешенную 30%-ной уксусной кислотой колонку -Сефадекс Г-15 и элюируют 30%-ной уксусной кислотой. Ту фракцию элюата уксусной кислоты, которую можно расщеплять обработкой трипсином при освобождении п-нитроанилина, подвергают сушке вымораживанием. Получают 12,6 г аморфного порошка, который однороден в тонкослойной хроматограм ме в системе растворителей В.
Элементный ; анализ,: С 51,2у (51,67); Н 5,48 (5,42); N 17.,92 (18,08) ; С 7,50 (7,73) .
Пример 2. N -Кбо-гли-про-арг-пНА-НС .
4,65 г соединения примера 1 обрабатыБают 40 мл 2 н. НВг в ледяной уксусной кислоте без доступа влаги при перемешивании в течение 1 ч при 20°С. Пептидное производное при этом растворяется при выделении СО2 . Реак ционный раствор при сильном перемешиваиии прибавляют по каплям к 250 мл абсолютного эфира, причемвыпадает (2НВг) Н-арг-пНА. Эфирную фазу отсасывают , после чего промывают твердую фазу еще 4 раза, применяя по 100 мл абсолютного эфира, с целью удаления образовавшегося в качестве побочного продукта бензилбромида, а также избыток НВг и уксусной кислоты
Путем сушки в вакууме пластинками NaOH получают деблокированный продукт с количественным выходом. Сухой (2НВг) Н-арг-рНА растворяют в 25 мп диметилформалида. К охлажденному до раствору прибавляют 1,40 мл триэтиламина. Образуется осадок, который отфильтровывают и дополнительно промывают небольшим количеством холодного диметилформамида. К фильтрату прибавляют при 4,70 г кбо-гли-про-п-нитрофенокси. Через несколько часов температура реакционного раствора поднимается до 20 С. Раствор опять охлаждают до -10 С и буферуют 0,35 мл триэтиламина. Через 16 ч прибавляют еще раз 0,35 мл триэтиламина при . Еще через 24 ч концентрируют реакционный раствор в вакууме досуха.Остаток растворяют в 50 мл метанола. После прибавления 0,8 мл кон::: чтрированной поляной кислоты концентрируют раствор досуха в вакууме при- 20°С. Эту операцию повторяют 3 раза с целью перевода гидг робромида трипептида в гидрохлорид. Сырой гидрохлорид трипептида растворяют в 50 мл метанола и предварительно очищают при помощи фильтрации гелем через колонку Сефадекс ЛХ-20 .
Для дальнейшей очистки концентрируют в вaкyy ie ту фракцию метанола, которую можно расщеплять обработкой трипсином с освобождением п-иитроанилина . Остаток растворяют в 30%-ной уксусной кислоте. Раствор очищают путем фильтрации гелем на уравндвешенной 30%-ной уксусной кислотой колонке Сефацекс Г-15. Ту фракцию элюата уксусной кислоты, которую можно расщеплять обработкой трипсином с освобождением п-нитроанилина , после прибавления 0,80 мл концентрированной соляной кислоты подвергают сушке вымораживанием. Получа ют 3,64 г (58,8% от теоретического) аморфного легкого порошка, который однороден в тонкослойной хроматограмме в системе растворителей В.
Элементный анализ,%: С 52,09 (52,38); Н 5,33 .(5,70); N 18,33 (18,10); сг 5,75 (5,73).
С2 з5«зО,СЕ
Анализ дает аминокислоты в прдвильном соотношении: арг: 0,96-гли: :1,00-про:О,96.
Пример 3. Н-Гли-про -арг-пНА2НС .
61,91 г полученного по примеру 2 соединения без доступа влаги обрабатывают 300 мл 3 н.соляной кислоты в ледяной уксусной кислоте с перемешиванием в течение 2 ч при 35°С. Пептидное производное при этом растворяется при выделении СО2. Реакционный раствор при сильном перемешивании прибавляют по каплям к 2 л абсолютного эфира, причем выпадает Н-гли-про-арг-пН-2НСЕ в виде хлопьев . Эфирную фазу отсасывают, после чего промывают твердую фазу еще 4 раза, применяя по 0,5 л абсолютного эфира, с целью удаления образовавшегося в качестве продукта расщепления бензилхлорида и избытка соляной и уксусной кислот.
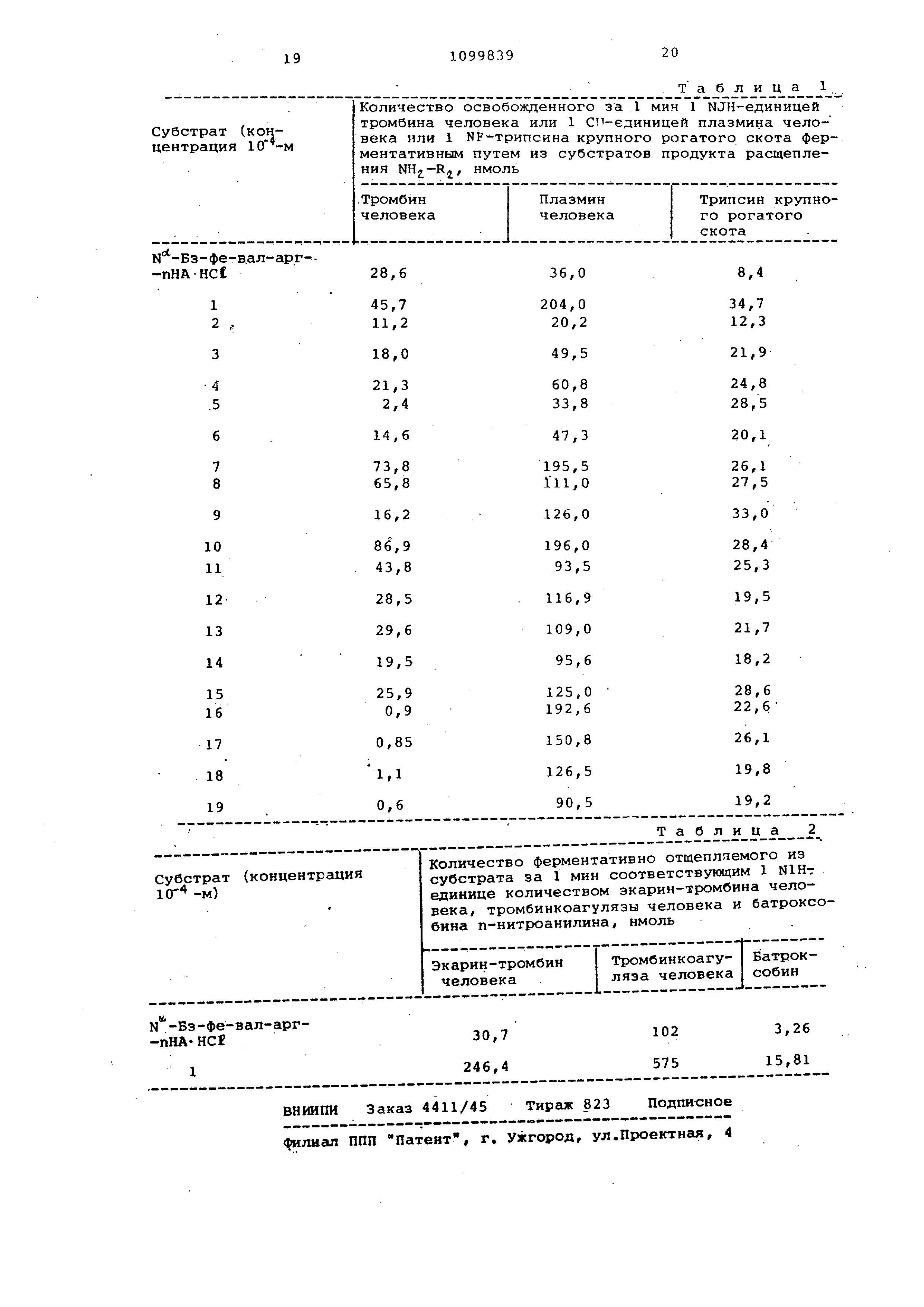
Путем сушки в вакууме плитками NaOH получают деблокированный продукт с количественным выходом. Для дальнейшей очистки растворяют высушенный продукт в 900 мл 30%-ной уксусной кислоты. Раствор очищают путем фильтрации гелем на уравновешенной 30%-ной уксусной кислотой колонке Сефадекс Г-15. При этом, Г;азделяют элюат уксусной кислоты на 2 фракции, которые обе можно расщеплять обработкой трипсином с освобождением п-нитроанилина. Главная фракция содержит желаемый продукт, а побочная фракция - исход-ный материал. После прибавления 8 мл концентрированной соляной кислоты к главной фракции ее подвергают сушке вымораживаЕ1ием. Получают 43,5 г аморфного nopoiuK i который однороден в тонкослойной хро матограмме в системе растворителей В Элементный анализ,%: С 43,38 (43,77); Н 5,88 (5,80); N 21,72 (21,49); СЕ 13,41 (13,60). VboNgO.CE. Пример 4. 2,09 г полученног „соединения из примера 3 растворяют в 25 мл диметилформамида. После охлаждения до -10°С прибавляют 555 мкл триэтиламина и непосредствен но- после этого 1,13 г п-нитрофенило-вого эфира фенилуксусной кислоты. Реакционный продукт обрабатывают, ка описано выше. Очистка. Фильтрацию гелем осуш.ест вляют на уравновешенной 30%-ной уксу ной кислотой колонке Сефадекс Г-15 Ту фракцию элюата уксусной кислоты, которую можно расщеплять обработкой трипсином с освобождением п-нитроани лина, после прибавления 320 мкл кон центрированной соляной кислоты подве гают сушке вымораживанием. . Выход 1,99 г (82,5% от теоретичес кого) аморфного порошка, который однороден в тонкослойной хроматограм ме в системе растворителей В. Элементный анализ,%: С 54,06 (53,77); Н 5,78 (5,85); N 18,83 (18,58); CI 5,79 (5,88), Cj H NgOfcCE Пример 5. № -Фенилпропионил -гли-про-арг-пНА-НСЕ. 2,09 г полученного по примеру 3 соединения растворяют в 25 мл димети формамида . После охлаждения до -10°С прибавляют 555 мкл триэтиламина и после этого 1,19 г п-нитрофенилового эфира 3-фенилпропионовой кислоты (т,пл. 97-98,5 С). Продукт реакции обрабатывают, как описано выше. Филь трацию гелем осу11 ествляют на уравновешенной 30%-ной уксусной кислотной колонке Сефадекс Г-15, Фракцию элюата уксусной кислоты, которую мож . но расщеплять обработкой трипсином с выделением п-нитроанилина, после при бавления 320 мкл концентрированной соляной кислоты подвергают сушке вымораживанием . Выход 2,06 г (83,5% от теоретического ) аморфного порошка, который однороден в тонкослойной хроматограмме в системе растворителей В. Элементный анализ,; С 54.2 (54,50); Н 5,98 (6,04); N 18,29 ); (18,16); CI 5,63 (5,75). C gH NgOfeCr Пример 6. N -Циклогексилкарбонил-гли-про-арг-пНА-НС1 . 2,09 г полученного по примеру 3 соединения растворяют в 25 мл диметилформамида . После охлаждения до -10°С прибавляют 555 мкл триэтиламина и после этого 1,10 г п-нитрофенилового эфира циклогексикарбоновой кислоты. Продукт реакции обрабатывают даль:;1е, как описано выше. Фильтрацию гелем осуществляют на уравновешенном 30%-ной уксусной кислотой колонке Сефадекс Г-15. Фракцию элюата уксусной кислоты, можно расщеплять обработкой трипсином с освобождением п-нитроанилина, после прибавления 320 мкл концентрированной соляной кислоты подвергают сушке вымораживанием. Выход 1,87 г (78,6% от теоретического ) аморфного порошка, который однороден в тонкослойной хроматограмме в системе растворителей В. Элементный анализ,%: С 52,70 (52,47); Н 6,72 (6,61); N 19,03 (18,83) ; CI 5,83 (5,96) . С2бН, Пример 7. N -Каприлокл-гли-про-арг-пКА-НС1 . 2,09 г полученного по примеру 3 соединения растворяют в 25 мл диметилформамида . После охлаждения до -10С прибавляют 555 мкл триэтиламина и непосредственно после этого I, 17 г п-нитрофенилового эфира каприловой кислоты. Реакционный продукт обрабатывают, как описано выше. Фильтрование гелем осуществляют на уравновешенной 30%-ной уксусной кислотой колонке Сефадекс Г-15, Фракцию элюата уксусной кислоты, которую можно расщеплять путем обработки трипсином с освобождением п-нитроанилина , после прибавления 320 мкл концентрированной соляной кислоты подвергают сушке вьзмораживанием . Выход 1,99 г (81,4% от теоретического ) аморфного порошка, который однороден в тонкослойной хроматограмме в системе растворителей В. Элементный анализ,%: С 52,84 (53,06); Н 7,15 (7,09); N 18,58 (18,34); сг 5,73 (5,80). С,Н4эНдОбС Пример 8, N -Моз-гли-про-арг-пНАHCJ . 2,09 г полученного по примеру 3 соединения растворяют в 25 мл диметилформймида . После охлаждения до -10°С прибавляют 555 мкл триэтиламина и непосредственно после этого 840 мл хлорангидрида п-толуолсульфоновой кислоты (тозилхлорида). Продукт реакции перерабатывают дальше как описано выше. Фильтрование гелем осуществляют на уравновешенной 30%-ной уксусной кислотой колонке Сефадекс Г-15. Фракцию элюата уксусной кислоты, которую можно расщеплять обработкой трипсином с освобождением п-нитроанилина, после прибавления 320 мкл концентрирован ной соляной кислоты подвергают сушке вымораживанием. Выход 2,17 г (84,9% от теоретического ) аморфного порошка, которы однороден в тонкослойной хроматогр ме в системе растворителей В. Элементный анализ,%: С 48,50 {48,8б);Н 5,60 (5,52).; N 17,73 (17,53); S 5,19 (5,02); С1 5,49 (5,55). .sc. Пример 9. N -Бензолсульфонил-гли-про-арг-пНАНС . 2,09 г полученного по примеру 3 соединения растворяют в 25 мл диме тилформамида. После охлаждения до -10°С прибавляют 555 мкл триэтилам на и после этого 780 мг хлорангидрида бензолсульфоновой кислоты. Продукт реакции перерабатывают дальше, как описано выше. Фильтрова ние гелем осуществляют на уравновешенной 30%-ной уксусной кислотой ко лонке Сефадекс Г-15. Фракцию эл ата уксусной кислоты, которую можно расщеплять обработкой трипсином с освобождением п-нитроанилина, посл прибавления 320 мкл концентрированной соляной кислоты подвергают сушк вымораживанием. Выход 1,95 г (78% от теоретического ) аморфного порошка, который однороден в тонкослойной хроматогра ме в системе растворителей В. Элементный анализ,%: С 47,79 (48,03); Н 5,40 (5,32); N 18,11 (17,93); S 5,06 (5,13); СГ 5,61(5, С25«33 80г5С. Пример 10. N -Метансульфо нил-гли-про-арг-пНАНС. 2,09 г полученного по примеру 3 соединения растворяют в 25 мл диметилформамида . После охлаждения до -10°С прибавляют 555 мкл триэтилами на и после этого 345 мкл хлорангидр да метансульфоновой кислоты. Продук реакции обрабатывают дальше, как описано выше. Фильтрование гелем осуществляют на уравновешенной 30%-ной уксусной кислотой колонке Сефадекс Г-15 Фракции элюата уксусной кислоты, которую можно расщеплять обработко трипсином с освобождением п-нитроа лина, после прибавления 320 мкл концентрированной соляной кислоты подвергают сушке вымораживанием. Выход 1,70 г (75,5% от теоретического ) аморфного порошка, к -/гпрыП однороден в тонкослойной хромачограмме в сист-еме растворителей В. Элементный анализ, С 42,88 (42,66); Н 5,63(5,55); N 20,08 (19,90); S 5,62 (5,70); СР 6,21 (6,30) . С2оНз, NgO.,SCf Пример 11. N -2-Нафталинсульфонил-гли-про-арг-пНАHCf . 2,09 г полученного по примеру 3 соединения растворяют в 25 мл диметилформамида. После охлаждения до прибавляют 555 мкл триэтиламина и после этого 1,0 г хлорангидрида нафталин -2-сульфоновой к ислоты Продукт реакции обрабатывают, как описано выше. Фильтрование гелем осуществляют на уравновешенной 30%-ной уксусной кислотой колонке Сефадекс Г-15. Фракцию элюата уксусной кислоты, которую можно расщеплять обработкой трипсином с освобождением п-нитроани лина, после прибавления 320 мкл концентрированной соляной кислоты подвергают сушке вымораживанием. Выход, 1,81 г (66,8% от теоретического ) аморфного порошка, который однороден в тонкослойной хрома тограмме в системе растворителей В. Элементный анализ,%: С 51,88 (51,59); Н 5,19 (5,23); N 16,75 (16,60); S 4,62 (4,75); С 5,12 (5,25). Пример 12, N -Изобутилоксикарбонил-гли-про-арг-пНАНСБ . 2,09 г полученного по примеру 3 соединения растворяют в 25 мл диметилформамида . После охлаждения до -10°С прибавляют 555 мкл триэтиламина и после этого 650 мкл изобутилового эфира хлормуравьиной кислоты. Реакционный продукт перерабатыгают дальше, как Описано выше. Фильтрование гелем осутцествляют на уравновешенной 30%-нбй уксусной кислотой колонке Сефадекс Г-15. Фракцию элюата уксусной кислоты, которую можно расщеплять обработкой трипсином с освобождением п-нитроанилина , после прибавления 320 мкл концентрированной соляной кислоты подвергают сушке вымораживанием. Выход 1,71 (73,1% от теоретического ) аморфного порошка, который однороден в тонкослойной хроматограмме в системе растворителей В. Элементный анализ,%: С 49,06 (49,27); Н 6,42 (6,37); N 19,33 (19,15) ; С 5,98 (6,06) . ., Пример 13. N -Кбо-гли-про-арг-2-НА HCI; к -кбо-арг (Юг ) -2-НА. 3,53 г хорошо высушенного кбо-арг (NOji-OH без доступа влаги растворяют в 150 мл тетрагидрофурана/диметилформамида (3:1), После охлаждения до -10°С к раствору прибавляют 1,39 мл триЭтиламина и потом по каплям в течение 15 мин раствор 1,35 г изобутилового эфира хлормуравьиной кислоты в 20 мл тетрагидрофурана, причем температуру выдерживают от -10°до -5®С. К полученному раствору затем прибавляют по каплям раствор 1,72 г п-нафтиламина в 15 мл тетрагидрофурана , причем поддерживают указанную температуру. Реакционную смесь составляют стоять в течение 24 ч при комнатной температуре. После отгонки растворителя в вакууме промывают остаток подряд три раза дистиллированной водой, три раза 5%-ным раствором гидрогенкарбоната натрия и опять три раза дистиллированной водой. После сушки в вакууме растворяют сырой продукт в метаноле и хроматографируют через уравновешенную метанолом колонку Сефадекс ЛХ-20. Из одной фракции элюата получают 3,75 г кристаллического соединения N -кбо-арг-(NOg) (78,4% от теоретического) с т.пл. 173-174,, которое однородно в тонкослойной хроматограмме в системах растворителей А и Б. Элементный анализ,%: С 60,82 (60,24); Н 5,63/ (5,48); N 17,48 ,.(16,72). .НгнМдОс При мер 14. ,н-арг-2-НАНСГ. 957 мг соединения ы -кбо-арг (N022-2 -НА навешивают в раакдионном сосуде аппарата Сакакибара. 15 мл высушенного фтористоводородного газа конде сируют в реакционном сосуде. После реакции через 1 ч при 0 С при перем шивании отщепляют нитрозащитную гру пу аргинина, а также карбобензоксигруппу . Конденсированный фтористово дородный газ отгоняют в вакууме из реакционной смеси и остаток раствор ют в диметилформамиде. Для перевода производного амино кислоты в солянокислую соль прибавляют 0,5 мл концентрированной солян кислоты и раствор концентрируют досуха . После двукратного повторения этого процесса растворяют остаток в 50 мл 40%-ной уксусной кислоты. Д очистки наносят раствор уксусной ки лоты на уравновешенную 30%-ной уксу ной кислотой колонку Сефадекс Г-1 и элюируют 30%-ной уксусной кислотой . Фракцию элюата, которую можно расщеплять обработкой трипсином с освобождением п-нитроанилина, после прибавления 320 мкл концентрированной соляной кислоты подвергают сушк вымораживанием. Выход 473 мг (63,5% от теоретического ) аморфного порошка, который однороден в тонкослойной хроматограмме в системе растворителей в. Элементный анализ, %: С 51,82 (51,62J; Н 6,18(6,23); N.17,08 (18,81); ,75 (19,05)„ Пример 15. Н -Кбо-гли-проарг-2-HAHCl . ,. 372 мг соединения по примеру 14 подвергают взаимодействию с 470 мг кбо-гли-про-ОпНП, получая соединения ы -кбо-гли-арг-2-НА- НС1. Фильтрование гелем осуществляют на уравновешенной уксусной кислотой колонке Сефадекс Г-15. Фракцию элюата уксусной кислоты , которую можно расщеплять обработкой трипсином с освобождением пнафтиламина , после прибавления 80 Мкл концентрированной соляной кислоты подвергают сушке вымораживанием. Выход 425 мг (68,1% от теоретического ) аморфного порошка, который од 5/ороден в тонкослойной хроматограмме в системе растворителей В. Элементный анализ,%: С 60,11 (59,65); Н 6,25 (6,14); N 16,07 (15,71) ; .сг 5,59 (5,68) . C.JjH. Пример 16. Ы -Гли-про-арг-2-HA-HCj , 625 мг соединения N-кбо-гли-про-а рг-2-Н -НС1 деблокируют, как oni caно выше, и растворяют в В мл ди- метилформамида. После охлаждения до -10°с прибавляют 140 мкл триэтиламина и после этого 210 мг хлорангидрида п-толуолсульфоновой кислоты(т.пл. 67-69с) . Реакционный продукт обрабатывс1ют известными приемами. Фильтрование гелем осуществляют на уравновешенной 30%-ной уксусной кислотой колонке Сефадекс Г-15. Фракцию злюата уксусной кислоты, которую можно расщеплять обработкой трипсином с освобождением /3 -нафтиламина , после прибавления 80 мкл концентрированной соляной кислоты подвергают сушке вымораживанием. Выход 500 мг аморфного порошка. Элементный анализ,%: С 56,13 (55,93); Н 5,86 (5,95); N 15,48 15,22); S 5,07 (4,98); С 5,39 (5,50). Пример 17. м -Кбо-гли-про-арг-4-МеО-2-НА- к -кбо-арг (N02)-4-MeO-2-HA. 3,53 г кбо-арг(NO2)-ОН согласно примеру 13 подвергают взаимодействию с 2,17 г 4-метокси-2-нафтиламина и перерабатывают, как описано в этом примере. Фильтрование гелем осуществляют на уравновешенной метанолом колонке Сефадекс ЛХ 20. Из одной фракции элюата получают 3,35 г (65,9% ст теоретического) кристаллического соединения N -K6oарг (NQj)-4-МеО-2-НА, которое олнородно в тонкослойной хроматограмме в системах растворителей А и Б. Элементный анализ,%: С 59,18 (59,05); Н 5,43 (5,55); N 16,49 (16,23). CjsHjgN O Пример 18. Н-Арг-4-Мео-2-НА-2НС2 . 1,02 г соединения N-кбо-арг (NO -4-МеО-2-НА подвергают взаимодейств получая соединение Н-арг-4-МеО-2-НА- 2НС. Фильтрование гелем осуществляют на уравновешенней 30%-ной уксусной КИСЛО1ОЙ колонке Сефадекс Г-15 Фракцию элюата уксусной кислоты, ко торую можно расщеплять обработкой трипсином с освобождением 4-метокси -2-нафтиламина, после прибавления 320 мкл концентрированной соляной кислоты подвергают сушке вfclI Opaживa нием. Выход 570 мг (71,0% от теоретического ) аморфного порошка, который однороден в тонкослойной хромат грамме в системе растворителей В. Элементный анализ,%: С 51,08 (50,88); Н 5,98 (6,03); N 17,75 (17,45); сг 17,55 (17,67). С, Н,,, N OjCE Пример 19. 402 мг соединения Н-арг-4-МеО-2-НАHCJ подвергают взаимодействию с 470 мг кбо-гли-про -ОпНП, получая соединение №-кбо-гли-про-арг-4-МеО-2-НА-НС2 . Фильтрование гелем осуществляют на уравновешенной 30%-ной уксусной кислотой колонке Сефадекс Г-15 Фракцию элюата уксусной кислоты, которую можно расщеплять обработкой трипсином с освобождением 4-метокси 2-нафтиламина, после приб,авления J 80 мкл концентрированной соляной кислоты подвергают сушке выморажива нием . Выход 493 мг (75,4% от теорети 1е кого) аморфного порошка, который однороден в тонкослойной хроматогра ме в системе растворителей В. Элементный анализ,%: С 59,01 (58,75); Н 6,10 (6,16); N 15,19 (14,99); С1 5,35 (5,42). , Пример 20. 655мг соединения М --кбо-гли-про-арг-4-МеО-2-НА НС2 деблокируют и растворяют в 80 м диметилформалина. После охлаждения до -10°С прибавляют 140 мкл триэтил амина и после этого 210 мг хлорангидрида п-толуолсульфоновой кислоты Продукт реакции перерабатывают даль ше. Фильтрование гелем осуществляют на уравновешенной 30%-ной уксусной кислотой колонке Сефадекс Г-15. Фракцию элюата уксусной кислоты, которую можно расщеплять обработкой трипсином с освобождением 4-метокси-2-нафтиламина , после прибавления 80 мкл концентрированной соляной кислоты подвергают сушке вымораживанием . Выход 465 мг (69,4% от теоретического ) аморфного порошка, который однороден в тонкослойной хроматограмме в системе растворителей В. Элементный анализ,%: С 55,75 (55,72); Н 6,01 (5,98); N 14,98 (14,54); S 4,59 (4,76); СР 5,16 (5,26). С,, . Пример 21. N -Моз-гли-пролиз-пНА-ПС ; Н-БОК-Ы -кбо-лиз-пНА. 19,0 г соединения Ы -БОК-М -кбо-лиэ-ОН растворяют в 100 мл ГМПТА и прибавляют 5,06 г триэтиламина и потом 16,4 г п-нитрофенилизоцианата. По истечений 24 ч реакционный раствор с перемешиванием прибавляют по каплям к 1 л 2%-ного раствора гидрогенкарбоната натрия. Осажден-, ный продукт отфильтровывают и промывают трижды по 0,5 л 2%-ного раствора гидрогенкарбоната натрия, трижды по 0,5 л дистиллированной воды, трижды по 0,5 л 0,5 н. соляной кислоты и трижды по 0,5 л дистиллированной воды. Полученный продукт высуши-г вают в вакууме при 40°С и после этого экстрагируют дважды, применяя по 30 мл нагретого до диметилформамида , причем желаемый продукт полностью растворяется, в то время как побочный продукт, NN-бис-п-питрофенилмочевина , остается в нерастворенном виде. Раствор диметилформамида концентрируют в вакууме 40 С. Остаток растворяют в метаноле и путем фильтрования гелем через уравновешенную метанолом колонку Сефадекс ЛХ-20 получают 18,85 (75,3% от теоретического) кристаллического соединения ы -БОК-Ы -кбо-лиз-пНА с т.пл. 125-125,5°С, которое однородно в тонкослойной хроматограмме в системах растворителей А и В. Элементный анализ,%: С 60,49 (59,99); Н 6,35 (6,44); N 11,48 1 (11,19) . С25НзаЫ407 П р и м е р 22. ы -Моз-гли-про-лиз (-кбо)-пНА. 1,5 г соединения N -БОК-N -кбо-лиз-пНА обрабатывают, перемешивая 1 ч при 20°С, 20 мл трифторуксусной кислоты без доступа влаги, причем производное аминокислоты растворяется с выделением СО. Реакционный раствор при сильном перемешивании медленно прибавляют по каплям к 150 мл высушенного эфира, причем выпадает Н-лиз (е-кбо)-пНА-трифторацетат . Эфирную фазу отсасывают фильтровальной палкой. Оставшийся осадок промывают еще 4 раза, примен:яя по 50 мл сухого эфира для удале ния избыточной трифторуксусной кислоты . Сушкой в вакууме плитками едкого натра получают деблокированный продукт с количественным выходом . Сухой трифторацетат производно го аминокислоты растворяют в 15 мл диметилформамида. После охлаждения до -10°С прибавляют к раствору 415 мкл триэтиламина для освобождения производного аминокислоты из трифторацетата. К реакционной смеси прибавляют 1,48 г моз-гли-про-ОпНП„ Продукт реакции перерабатывают дальше, как описано выше. Фильтрова ние гелем осуществляют на уравновешенной метанолом колонке Сефадекс ЛХ--20 , Выход 1,77 г (83,2% от теоретического ) аморфного вешества, которо однородно в тонкослойной хроматограмме в системах растворителей А и Б. Пример 23. н -Моз-гли-про--ЛИЗ-ПНА-НС1 . If 42 г соединения N -моз-гли-про-лиз (Е-кбо)-пНА деблокируют. Фильтрование гелем осуществляют на уравновешенной 30%-ной уксусной кио лстой колонке Сефадекс Г-15. Фракцию элюата уксусной кислоты, ;:оторую можно расщеплять обработкой трипсином с освобождением пт нитро а-нилина, после прибавления 160 мкл концентрированной соляной кислотгл подвергают сушке вымораживанием. Выход 1040 мг (85,1% от теоретического ) аморфного порошка, который однороден в тонкослойной хроматограмме в системе растворителей В, Пример 24. N -Изобутоксикарбонил-гли-про-лиз- гНА НСУ.; N БОК-гли-про-лиз- (-кбо) -nf.LA. 20 г соединения №-БОК-Ы -кбо-лиз (8-кбо)-ПКА деблокируют и раст воряют в 20 мл диметилформамида. После охлаждения до -10с к раствор прибавляют 555 мкл триэтиламина и после этого 1,73 г БОК-гли про О-НП Реакционный продукт перерабатывают, как описано выше. Фильтрование геле осуществляют на уравновешенной мета нолом колонке Сефадекс ЛХ-20 . Выход 2,20 г (84„0% от теоретиче кого) аморфного вещества, которое од нородно в тонкослойной хромс;тограм-ме в системах растворителей А и Б. Пример 25 „N -Изобутоксикар бонил-гли-про-лиз(-кбо)-л НА, 1,31 г соединения N -БОК-гли-про-лиз (8-кбо)-пНА деблокируют и раств ряют в 12 мл диметилформамида« Посл охлаждения до к раствору при бавляют 280 мкл триэтиламина и посл этого 285 мкл изобутилового эфира хлормуравьиной кислоты. Продукт реакции обрабатывают, как описано выше . Фильтрование гелем осуществляют на уравновешенной метанолом колонке Сефадекс ЛХ-20 . Выход 1,15 г (87,8% от теоретического ) аморфного вещества, которое однородно в тонкослойной хроматограмме в системах растворителей А и Б. Пример 26.№ -изобутоксикарбонил-гли-про-лиз-пНА-НС . 660 мг соединения N -изобутоксикарбонил-гли-про-лиз (Е-кбо) -Г:НА деблокируют. Фильтрование гелем осуществляют на уравновешенной 30%-ной уксусной кислоты колонке Сефадекс Г-15. Фракцию элюата уксусной кислоты , которую можно расщеплять Обработкой трипсином с освобождением п нитроанилина , после прибавления 80 мкл концентрированной соляной кислоты подвергают сушке вымораживанием. Выход 430 мг (77,2% от теоретического ) аморфного порошка, который однороден в тонкослойной хроматограмме в системе растворителей В. Пример 27. А -Моз-гли-про-ЛИЗ-2-НА-НС1; Ц -БОК-М кбо-лиз-2-НА 1,30 г соединения М -БОК-Ы -кбо ЛИЗ-ОН подвер ают взаимодействию, как указано при получении №-кбо-арг- (NOa )-2-НА, соединения Ы -БОК-н -кбо-лиэ-2-НА. Фильтрование гелем осуществляют на уравновешенной метанолом колонке Сефадекс ЛХ-20 . Выход 1,60 г (63,3% от теоретического ) аморфного соединения, которое однородно в тонкослойной хроматограмме в системах растворителей А и Б, Пример 28.N Моз-гли-про--ЛИЗ (f-кбо) 2-НА, 1,05 г соединения И -БОК-fi -кбо лиз -2-НА деблокируют, как указано при получении Н -моз-гли-пролиз- (-кбо)-пНА, и растворяют в 20 мл диметилформамида. После охлаждения до -10°С к раствору прибавляют 280 мкл триэтиламина и непосредственно после этого 985 мг моз-гли Про-ОпНП . Продукт реакции перерабатывают дальше, как указано выше. Фильтрование гелем осуществляют на уравновешенной метанолом колонке Сефадекс ЛХ-20. Выход 1,14 г аморфного вещества, которое однородно в тонкослойной хромаTorpaKSMe. Пример 29, №-моз-гли-про лиз-2-НА-НС2„ 715 мг соединения N -моз-гли-про Лиз (-кбо)-2-НА деблокируют, как указано выше. Фильтрование гелем осуществляют на уравновешенной 30%-ной уксусной кислотой колонке Сефадекс Г-15. Фракцию элюата уксусной кислоты, которую можно расщеплять обработкой трипсином с освобождением 2-нафтиПамина , после прибавления 80 мкл кон центрированной соляной кислоты подвергают сушке вымораживанием. Выход 470 мг (76,3% от теоретиче кого)аморфного порошка, который одн роден в.тонкослойной хроматограмме в системе растворителей В. Пример 30. Ы -Моз-гли-про-лиз .-4-МеО-2НА НС2; N -БОК- МЕ кбо-лиэ-4-ЛеО-2-НА . 1,90 г соединенияN -BOK-N -KCo-лиз-ОН подвергают взаимодействию с 1,22 г 4-метокси-2-нафтиламина согласно примеру 13. Фильтрование гелем осуществляют на уравнове-иенной метанолом колонке Сефадекс ЛХ-20. Выход 1,82 г {168,0% от теоретического ) аморфного соединения, кото рое однородно в тонкослойной хромаTorpciMMe в системах растворителей. Пример 31.N -Моз-гли-про-лиз )4-МеО-2-НА. 1,07 г соединения N --БОК-М -кбо-лиз-4-МеО-2-НА деблокируют согласно примеру 18 и растворяют в 20 мл диметилформамида . После охлаждения до -10°С к раствору прибавляют 280 мкл триэтиламина и после этого 985 мг моз-гли-про-ОоНБ. Реакционными продук перерабатывают согласно примеру 1. Фильтрование гелем осуществляют на уравногеыенной метанолом колонке Сефадекс ЛХ-20. Выход 895 мг (60,2% от теоретичес кого) с1морфного вещества, которое однородно а тонкослойной хроматограм ме в системах растворителей. Пример 32. N -Моз-гли-про-лиз-4-МеО-2-НАНС . 745 мг соединения по примеру 31 деблокируют, как указано выше. Филь трование гелем осуществляют на урав новешенной 30%-ной уксусной кислото колонке Сефадекс Г-15. Фракцию элюата уксусной кислоты, которую можно расщеплять обработкой трипсин с освобождением 4-метоксИ-2-нафтиламина , после прибавления 80 мкл кон центрировайной соляной кислоты подвергают сушке вымораживанием. Выход 470 мг (72,74 от теоретиче кого) аморфного порошка, который од нороден в тонкослойной хроматограмме в системе растворителей В. Субстраты формулы 1 пригодны для определения энзимов, расщепляющих пептидные цепи на карбоксильной стороне как аргинина, так и лизина. К этой группе энзимов относятся тром бчн и тромбиноподобные энзимы, экар тромбин, плазмин и трипсин. При помотл субстратов можно также определять проэнзимы, например протромбин плазмипоген и трипсиноген, активатор и ингибиторы энзимов, например антитромбины, в частности софактор гепарина (антитромбин 111) и гепарин далее антиплазмип (iv.j-макрохлобулин / , ингибиторы трипсина ( ,-антитрипсин), апротинин, ингибиторы трипсина соевых бобов и ингибиторы плазмина. При полн.. активировании проэнзи-( мов активаторами или смесями активаторов образуется эквивалентное количество энзима, которое можно измерять. Измерение концентрации активаторов проводят таким образом, что определяют скорость образования энзима из проэнзима. Эта скорость пропорциональна концентрации активатора.; Пример JJ. Субстрат, например -кбо-гли-про-арг- НА-НС.Е, применяют для определения различных энзимов в плазме крови. Определение основывается на-том принципе, что образованный ферментативны гидролизом субстрата продукт расщепления имеет УФ-спек.тр, который отличается от УФ -спектра, субстрата и смещен в направлении болыяих длин волн. Так, субстрат N -кбо-гли-про-арг-рНА- НСЕ имеет макс -1мум поглощения при 302 нм и молярный коэффициент экстинкции 12920. Поглощеьше субстрата при 405 нм практически равно 0. Образованный при ферментативном гидролизе субстрата продукт расщепления , т.е. п-нитроанилии, имеет максимум поглощения 380 нм и молярный коэффициент экстинкции 13200. При 405 нм коэффициент экстинкции мало понижается, т.е. до 9650. Путем спектрофотометрического измерения при 405 нм можно легко определять степень Ферментативного гидролиза субстрата, которая пропорциональна кол - честву отщепленного п-нитроанилина . Имеющийся в избытке субстрат не мешает измерению при 405 нм. Спектрофотометркческое измерение но всех случаях проводят при 405 нм. Повышенная водорастворимость соединения обеспечивает определение энзимов в более широких пределах концентрации. Это важно при стандартных способах исследования, так как в этих случаях можно точно определять крайние величины, без предварительного разбавления или концентрирования биологических проб. Измерения проводят следующим образом. 0,25 мл раствора энзима (0,56 N1 Н/мл тромбина человека, 0,28 NJ Н/м экарин-тромбина человека 1,05 NJ Н/мл стафило-тромбина чело- , века, 4,0 NJ Н/мл батроксобина, 0,4 си/мл плазмина человека и 1,8 NF/мл трипсина крупного рогатого скота) прибавляют к 2,0 мл буфера трисимидазола (рП-8,4, ионная сила,0 ,15). Смесь инкубируют в течение 2 мин при 37°С. Потом к смеси прибавляют 0,25 мл водного раствора суб страта {1 ммоль/мл субстрата по примеру 33 или известного субстрата N бз-фе-вал-арг-pFIAHCE ) при 37°С. Повышение поглощения измеряют спектр фотометрически при 405 ни и за ним непрерывно следят при помощи самопис ца« Количество образовавшегося продукта расщепления представляют собой меру чувствительности субстратов к энзимам. При вычислении образующегося за 1 мин п-иитроанилина применяют молярный коэффициент зкстинкции 10 00 вместо 9620, так как отношение между расщепляемостью различных субстратов энзимами этим не изменяется. Для вычисления образовавшегося за 1 мин количества -нафтиламина или 4-метокси-/ -нафтиламина пробу облучают во флуоресцентном фотометре светом длины волн 350 им. Количество образовавшегося продукта расщепления определяют измерением интенсивности испущенного при 420 им. света. В табл.1 представлена активность тромбина человека, плазмина человека и трипсина крупного рогатого скота, измеронная при помощи субстратов сог ласно изобретению при постоянной кон центрации субстрата и энзимов; для сравнения даны соответствующие значе ния, определенные при помощиN -63-фе-вал- дрг-рНА -HCj. Из табл,1 видно, что субстраты показывают улучшенную по отношению к плазмину человека, а в большинстве случаев значительно улучшенную восприимчивость , чем известный -вал-арг рНАНС. Перечисленные cs6страты имеют значительно лучшую восприимчивость к трипсину крупного рогатого скота, чем известный сравни тельный субстрат Пример 34. В табл, 2 представлена активность зкарин-тромбина человека, тромбинкоагулязы человека и батроксобина (из яда Bothrops moojeni), измеренная посредством субстрата 1 при постоянной концентрации субстрата и энзима Контролем служат соответствующие измеренные М -бз-фе-вал-арг-пНА- НС -значения. пример 35. Субстраты можно например, применять также для определения протромбина и антитромбина о Для определения протромбина к 0,5 м 1лицинового буфера с рН 8,4 и конно силой 0,3 прибавляют 5 мкл цитратно плазмы. Смесь инкубируют в течение 30 с при 37°С. Затем к инкубирован ной смеси прибавляют 100 мкл водног раствора тромбопластина кальция ( тромбопластин кальция представляет собой активатор протромбина). Полученную смесь инкубируют при . После инкубации в течение 2,5 мин активация протромбина окончена. После инкубации более чем 5 мин исчезает часть активированного тромбина вследствие воздействия содержащихся в плазме антитромбинов.После инкубации через 4 мин к указанной смеси прибавляют 1 мл глицинового буфера с рН 8,4, ионной силой 0,3 и температурой и затем 0,25 мл 1, 510-молярного водного раствора субстрата 1. За ходом гидролиза субстрата следят фотометрическим измерением количества освобожденного за 1 мин n-нктpoaнил 5мa при 40-5 нм. Повышение оптической плотности составляет 0,162 за 1 мин. Из этого значения и молярного коэффициента экстинкции п-нитрофениланилина при 405 нм 10000 вычисляют значение 5,99 mU образовавшегося из протромбина тромбина ка 1 мкл плазмы. Из этого вытекает, что 5,99 ед. субстрата 1 тромбина было образовано из протромбина на 1 мл плаз1лы, что соответствует 162,3 & 1Н-едини1ды тромбина на 1 мл плазмы. Для определения антитромбина к 1 мл содержащего . 3 USP-единицы гепарина глицинового буфера с рН 8,4 и ионной; силой 0,3 прибавляют 0,1 мл водного раствора тромбина концентрацией 25-40 NlH-еДипиц на 1 мл при З7с. К полученной смеси прибавляют 2,5-10 мкл цитратовой плазмы, после чего инкубируют смесь в течение 30 с при . К инкубированной смеси сразу прибавляют Of 25 мл раствора полибрена (концентрация 1 мг полибрена на 1 мл 0,3-молярного раствора поваренной соли, полибрен представляет собой состоящий из 1,5-диметил-1,5-диазаундекаметиленполиметобромида продукт. Полученную смесь инкубируют в течение -,j 30 с при 37°с. Затем к смеси прибавляют 0,5 мл О, 75 10 -молярного водного раствора субстрата 1. За ходом гидролиза субстрата ненейтрализованным антитромбином тромбином следят фотометрическим измерением количества освобожденного за 1 мин п нитроанилина при 405 нм. При этом оказывается , что торможение применяемого тромбина различными количествами цитратовой плазма пропорционально этим количествам. Предлагаемый способ по сравнению с известным является высокочувствительным и позволяет определять небольшие количества , что очень важно в клинической практике.
Таблица









Реферат
СПОСОБ ОПРЕДЕЛЕНИЯ ТРОМБИНА, ПЛАЗМИНА, ТРИПСИНА И ТРОМБИНОПОДОБНЫХ ФЕРМЕНТОВ В БИОЛОГИЧЕСКИХ ЖИДКОСТЯХ путем взаимодействия пробы биологической жидкости с субстратом с последующим определением продуктов гид ролиза фотометрически, спектрометрически или флюоресцентноспектрофотометрически , отличающийся тем, тем, что, с целью повышения чувствительности способа, в качестве субстрата используют вещество общей формулы R гли-про-X-NH-R или овщей-формулы R -гли-про-арг-NH-R , где R - водород или блокирующая ацильная или сульфанильная группа; R - замещенный ароматический а углеводородный остаток; (О X - аргинильнан или лизильная со группа.


Комментарии