Способ получения трихлорметилкарбиноленов или их сложных эфиров - SU1530092A3
Код документа: SU1530092A3
Описание
Изобретение относится к усовершенствованному способу получения три- клорметилкарбиноленов общей формулы
С1
,
С1-С-СН-СН-С СН
XI III С ОЯч RI RT, 3
которые находят применение в синтезе инсектицидов.
Цель изобретения - повышение выхода целевых продуктов и упрощение процесса .
Способ иллюстрируется нижеприведенными примерами.
Пример 1. К97,5мл (1 моль) безводного хлораля добавляют 0,5 г гексагидрата хлорида железа (III). В прозрачный раствор желтого цвета вводят 58-59 г изобутена с такой скоростью , чтобы его температура не поднялась выие 15-20°(. В реакционную смесь вливают раствор из 35 мл воды и 15 мл концентрированной соляной кислоты. Фазы разделяют. Органическую фазу сначала прои лпают водой.
со
N3
С/4
после этого смепшвают с бензолом и далее обезвоживают при пониженном давлении (100 мм рт.ст.). Получают 194,6 г 1,1,1-трихпор-4-метил-4-пен- тен-2-ола при выходе 96,5%. Содержание биологически активного вещества 98,2%.-Далее продукт подвергают вакуумной дистилляции для последующей очистки.
Аналитические данные;
Н-ЯМР CDC1,): 4,97 (широкий s, 1Н, СНО); 4,08-4,4 (dq, 2Н, -СНг); 2,25-3,0 (п, 2Н, CHj CHOCH); 1,93 (s, ЗН, СН,).
Тонкослойная хроматография Rr 0,37 (бензол).
Силикагельную пластинку обрабатывают фосформолибденкислим реактивом.
ОУ - 225/15/, 120°С - мин; 225,2 с.
Пример 2. Опыт проводят аналогично примеру 1, лишь с той разницей , что в реакционную смесь в качестве катализатора вводят 0,5 г ди- гидрата сульфата железа (II). При зтом получают 189,5 г 1,1,1-трихлор- 4-иетил-4-пентен-2-ола, выход 94%. Аналитические характеристики продукт идентичны характеристикам соединения полученного в примере 1.
Пример 3. В 3,9мл (0,04 моль хлоралп растворяют 0,1 г гексагидрат хлорида железа (III) , после чего при 10-25 0 в раствор добавляют 3,95 мл (0,04 моль) циклогексена. В течение 2 ч реакционную смесь медленно перемешиваю т, после чего в нее доливают 20 мл воды и 4 мл концентрированной соляной кислоты. Фазы отделют и водньш слой экстрагируют четы- реххлористым углеро дом. Органические фазы объединяют, сушат, фильтруют и растворитель при пониженном давлении удаляют методом дистилляции. Получаю 7,6 г 1 ,1,1-трихлорметил-2-циклогек- СИЛ-1-ИЛ карбинола. Выход 82,8%.
Аналитические характеристики: тонкослойная хроматография R 0,71 (бензол).
Силикагельную пластину обрабатывают до получения прозрачности фос- формолибденовып реактивом.
Пример 4. Опыт проводят аналогично примеру 1, с той разницей, что для разложения реакционной смеси вместо смеси соляной кислоты и воды в нее в течение 1 ч при 35 С добавля
0
5
0
5
55
ют 124 мл (1,3 моль) уксуснокислого ангидрида при условии, что после добавки первых 10 МП этого количества в смесь капают 3 капли концентрированной серной кислоты. В эту смесь далее вливают 200 мл дихлорэтана , ее пpoмывaюt 40 мл воды и 15 мл концентрированной соляной кислоты, сушат, фильтруют и при пониженном давлении отдистиллировывают. органический растворитель. Полученный сырец (270 г) очищают методом фракционной дистилляции. В качестве основного дистиллята собирается дистиллят , перетекающий при температуре 94-98°С при давлении 10 мм рт.ст.По- лучают 228,2 г 1,1,1-трихлор-4-метил- 2-ацетокси-4-пентена, выход 93%.
Аналитические характеристики
Rf « 0,88 (бензол).
Н-ЯМР (СНС1,): 2,.2 (s, ЗН, ОН СО); 4,87 (широкий 8, 2Н«СН); 5,7 (dd, 1Н, СКОАс).
Пример 5. Реакция хлораля и изобутена в условиях строгого соблюдения безводного режима и в присутствии в качестве катализатора безводного хлорида железа (III) (сравни тельный пример).
В смесь из 78,5 г (48,5 мл, 0,5 моль) хлораля и 0,5 г безводного хлорида железа (III) вводят при 40 С 29 г (0,5 моль) изобутена. К реакци- юнной смеси добавляют 200 мл эфира. -, Смесь фильтруют, эфирную фазу экстрагируют водой, сушат сульфатом натрия и выпаривают. В полученное вязкое
масло добавляют 3 мл н-гексана. 00- разовавшуюся кристаллическую субстанцию фильтруют, дважды промывают каждый раз 20 мл п-гексана и сушат при комнатной температуре. Получают 57,0 г продукта, выход 65%.
Продукт, полученный таким образом, перекристаллизовывают в смеси из п-гексана и эфира, составленной в соотношении 10:1. Получают 50,8 г продукта, выход 5,8%.
Тонкослойная хроматография: растворитель - п-гексан, проявитель 50 20%-ньп1 кислый раствор фосформолиб- дена Rf 0,55.
Н-ЯМР: 5,06 (s, 0-СН-О, 1Н); 4,325 (d, 0-CH-CoI, 1Н); 1,99 (d, СН,-, 2Н); 1,425 (s, С(СН,)4 , |Й).
Мол. вес: 350,9; F: 112-114 С.
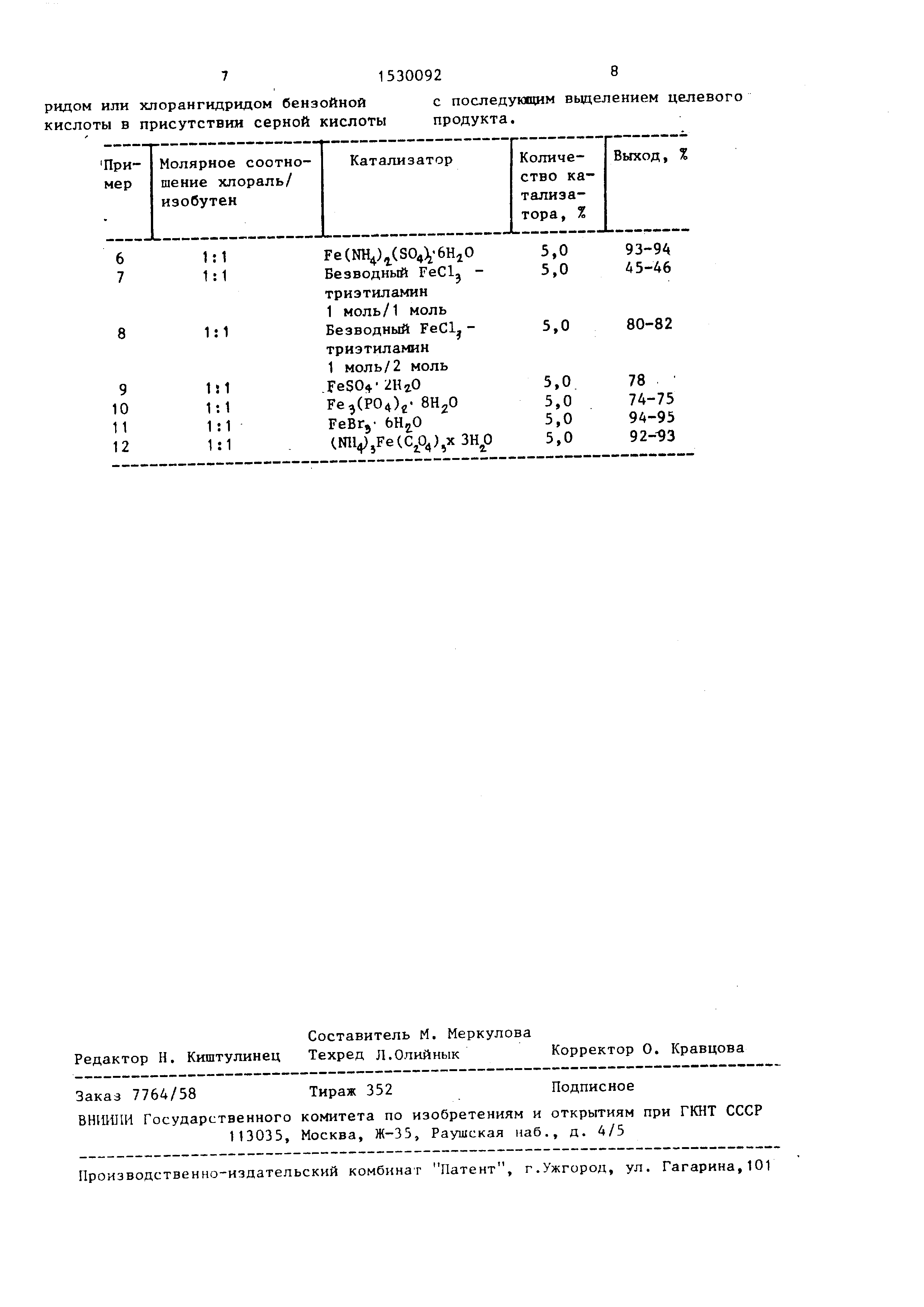
Примеры 6-12. Процесс проводят аналогично примеру 1, с той лишь разницей, что применяются другие катализаторы, которые перечислены в таблице.
Характерные аналитические константы продукта соответствуют константам продукта, полученного в примере 1.
Пример 13. 203,5 г (1 моль) 1,1,1-трихлор-4-метил-4-пентен-2-ола растворяют в 300 мл пиридина, и при наружном охлазкдении холодной водой закапьшают 154,6 мл (1,1 моль) хлоритого бензола. Затем перемешивают реакционную смесь при 30-35 с 1 ч. За ходом реакции наблюдают при помощи тонкослойной хроматографии (бензол). Коэффициенты 0,7 (силикагель на G-пластине, проявитель: 10%-ная фос- формолибденовая кислота).
Реакционную смесь выливают на смесь 1000 г воды и льда и добавляют 500 мл этилацетата. Разделяют фазы, органическую фазу промьшают 3x200 мл 10%-ной соляной кислоты, 100 мл 5%-ного раствора бикарбоната натрия до нейтрального состояния. Затем сушат над сульфатом натрия и выпаривают при пониженном давлении.
Получают 295,2 г (96%) 1,1,1-три- хлор-4-метил-2-бензоилокси-4-пентена
Аналитические характеристики:
Н-ЯМР (СПС1з): 4,85 (ширина s, 2Н, -СН); 5,76 (dd, 1Н, ); 7,8-7,3 (т, 5Н, ароматический).
Таким образом, предлагаемый спосо по сравнению с известным позволяет упростить процесс за счет применения более доступных катализаторов на основе железа вместо тетрахлорида олова , количество используемого катализатора уменьшается в 8 раз при сокращении времени процесса с 5 ч до 30 мин.
Формула изобретения
Способ получения трихлорметилкарб ноленов или их сложных зфиров общей формулы I
где
R - 4сг
н;
Н, алканоилгруппа
или бензоин, путем взаимодействия хпораля и олефи- нов общей формулы II
9
R
СН С-СН
где R, Rrt и R имеют указанные значения ,
в присутствии катализатора и при необходимости ацилирования продукта реакции , отличающийся тем, что, с целью упрощения процесса, катализатор общей формулы III
Fe
п
m
Р
где Y - галогенид, сульфат, фосфат или оксалат; или (R5)jN, где Rj.-€,-0 ;
1-3;
1-3;
А
m п Р
1-6,
растворяют в хлорале при концентрации 0,34-5,0 мас.% по отношению к массе хлораля, к полученному комплексному соединению общей формулы IV
/сн
5
ч
С1 С1
I
Fe
п
Ф Ym
О
д где Y, А, п, m и р имеют указанные
;значения
добавляют олефин общей формулы II в эквимолярном по отношению к хлоралю количестве при 10-25°С, причем образуется комплексное соединение общей
5
формулы V
0
сг ,сн-сн- р/
Х DH RI
С1 С1
iJi 1
C-R.
0-R,
Гё
п
Y.
Р
где
R
(
5
m
1, К, п, т, р, Y и А имеют
указанные значения, или разлагают смесью сокоторое
ляной кислоты и воды с последующим отделением органической фазы, сушкой и перегонкой, или подвергают ацилированию уксусным ангидРИДОМ или хлорангидридом бензойной кислоты в присутствии серной кислоты
с последующим вьщелением целевого продукта.



Реферат
Изобретение относится к ненасыщенным спиртам, в частности к получению трихлорметилкарбиноленов или их сложных эфиров ф-лы (CL)3C - CH(OR4) - CH(R) - C(R2) = CH(R3), где R1 - H
R2 - C1 - C4
R3 - H или R1+R3 - алкиленовая группа C4
R2 - H
R4 - H, алканоилгруппа C1 - C4 или бензоил, которые находят применение в синтезе инсектицидов. С целью упрощения процесса катализатор ф-лы FEN.YM.PA где Y - галогенид, сульфат, фосфат или оксалат
A - H2O или (R5)3N, где R5 - C1 - C4 - алкил
M=1-3
N=1-3
P=1-6, растворяют в хлорале (0,34-5,0 мас.% по отношению к массе хлораля), к полученному комплексному соединению добавляют олефин ф-лы (R1)CH = C(R2) - CH2(R3), где R1, R2, R3 имеют указанные значения, в эквимолярном по отношению к хлоралю количестве при 10-25°С. Образующееся комплексное соединение или разлагают смесью HCL и H2O с последующим отделением органической фазы, сушкой и перегонкой, или подвергают ацилированию уксусным ангидридом или хлорангидридом бензойной кислоты в присутствии H2SO4. Количество катализаторов уменьшается в 8 раз при сокращении времени процесса до 30 мин (против 5 ч при известном способе). 1 табл.

Формула


Комментарии