Способ получения кремниевого композиционного материала и устройство для получения кремниевого композиционного материала - RU2714070C1
Код документа: RU2714070C1
Чертежи

Описание
Область техники
Настоящее изобретение относится к способу получения кремниевого композиционного материала и к устройству для получения кремниевого композиционного материала, более конкретно, оно относится к способу и устройству для получения такого кремниевого композиционного материала, как композит с керамической матрицей на основе карбида кремния.
Уровень техники
Кремниевые композиционные материалы, в частности, композиты с керамической матрицей (CMC), представляют интерес как легкие материалы, обладающие высокой механической прочностью даже при высокой температуре, поэтому исследовалась возможность их массового производства в ближайшем будущем. Композиты с керамической матрицей представляют собой композиционные материалы, получаемые пропиткой преформы (ткани), образованной из керамических волокон (армирующий материал) керамикой в качестве матрицы. Из них композиты с керамической матрицей на основе карбида (SiC-based CMC), в которых карбид кремния (SiC) используется как для ткани, так и для матрицы, имеет отличные свойства в отношении легкости и высокой термостойкости и считается лидирующим материалом следующего поколения.
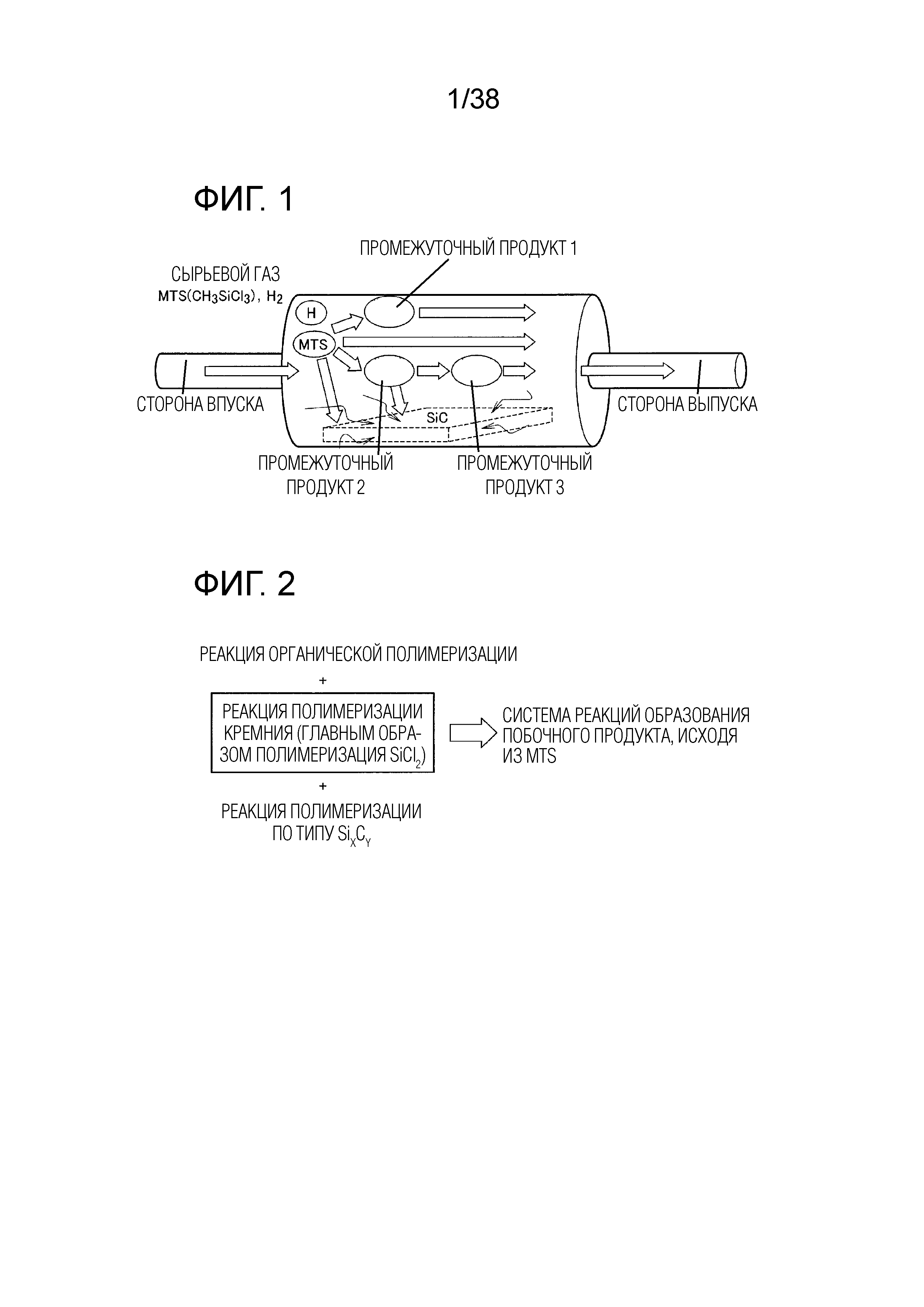
До сих пор получение композита с керамической матрицей на основе карбида кремния включало стадию химической инфильтрации из паровой фазы (CVI), показанную на фиг. 1. На стадию CVI подают метилтрихлорсилан (CH3SiCl3, MTS) и газообразный водород (H2) в качестве сырьевого газа, и сырьевой газ проникает в преформу из карбида кремния, выдерживаемую в реакционной печи типа печи с горячими стенками, атмосфера в которой поддерживается при температуре от примерно 800°C до примерно 1100°C, а давление от примерно нескольких торр до примерно нескольких десятков торр. В результате матрица карбида кремния осаждается на преформу. В реакционной печи MTS образует матрицу, осаждаясь в преформе в виде карбида кремния, проходя через различные промежуточные соединения (молекулы). Однако часть MTS образует матрицу, а оставшаяся его часть выводится из реакционной печи. Некоторые из этих разных выводимых молекул при охлаждении до комнатной температуры превращаются в полимеры высших хлорсиланов и осаждаются на выпускной трубе или насосе.
Между тем, для способа получения трихлорсилана по реакции тетрахлорсилана и водорода уже была описана технология подавления образования полимеров высших хлорсиланов путем обработки реакционного газа из реакционной печи на первой ступени охлаждения, промежуточной реакционной стадии и второй ступени охлаждения (смотри патентный документ 1).
Список цитирования
Патентная литература
Патентный документ 1: выложенная заявка на патент Японии JP 2010-132536
Непатентная литература
Непатентный документ 1: D. Togel, A. Antony, j. Bill, Petra Scheer, A. Eichhofer, G. Fritz, Journal of Organometallic Chemistry 521 (1996) 125.
Непатентный документ 2: Investigative Report of the Explosion & Fire Accident occurred in the High-Purity Polycrystalline Silicon Manufacturing Facility at Yokkaichi Plant of Mitsubishi Materials Corporation http://www.mmc.co.jp/corporate/ja/news/press/2014/14-0612.html
Непатентный документ 3: Frisch, M.J.; Trucks, G.W.; Schlegel, H.B.; Scuseria, G.E.; Robb, M.A.; Cheeseman, J.R.; Scalmani, G.; Barone, V.; Mennucci, B.; Petersson, G.A. et al. Gaussian 09, revision D.01; Gaussian, Inc.: Wallingford, CT, 2009.
Непатентный документ 4: A. Miyoshi, GPOP software, rev. 2013.07.15m5, http://www.frad.t.u-tokyo.ac.jp/~miyoshi/gpop/.
Непатентный документ 5: A. Miyoshi, SSUMES software, rev. 2010.05.23m4, http://www.frad.t.u-tokyo.ac.jp/~miyoshi/ssumes/.
Непатентный документ 6: CHEMKIN-PRO 15131, Reaction Design: San Diego, 2013.
Непатентный документ 7: Yang-Soo Won, J. Ind. Eng. Chem., Vol. 13, No. 3, (2007) 400-405
Непатентный документ 8: E. A. CHERNYSHEV, et. al., Journal of Organometallic Chemistry 271 (1984) 129.
Сущность изобретения
Техническая задача
На стадии CVI получения композита с керамической матрицей на основе карбида кремния газ, выходящий из реакционной печи, содержит различные молекулы, полученные из MTS, и некоторые из этих различных молекул, охлаждаясь, осаждаются как жидкий побочный продукт в выпускной трубе. Побочный продукт содержит высшие хлорсиланы и, следовательно, может гореть при воспламенении или превращаться во взрывоопасное вещество в твердой форме при окислении в контакте с атмосферой. Кроме того, при контакте с воздухом побочный продукт также образует газы, такие, как HCl и H2.
Таким образом, необходимо разбирать трубу и погружать трубу в воду для гидролиза побочного продукта с образованием диоксида кремния (кремнезем) с последующей промывкой. Если количество осажденного побочного продукта велико, и он недостаточно окислен внутри, побочный продукт иногда воспламеняется при промывке. Кроме того, собранный побочный продукт необходимо помещать в резервуар и утилизировать работниками, занимающимися захоронением промышленных отходов. Как описано выше, техническое обслуживание выпускных труб на стадии CVI является очень трудоемким и также требует затрат.
Между тем, технология, описанная в патентном документе 1, который направлен на подавление образования полимеров высших хлорсиланов в реакционном газе из реакционной печи, основана на реакции тетрахлорсилана и водорода. Следовательно, эта технология не применима к газу, выходящему из реакционной печи стадии CVI, для композита с керамической матрицей на основе карбида кремния.
Настоящее изобретение предоставлено с учетом вышеупомянутых текущей ситуации, и его целью является разработать способ получения кремниевого композиционного материала и устройство для получения кремниевого композиционного материала, способные снизить образование жидкого или твердого побочного продукта из газа, выпускаемого из реакционной печи, в которой кремниевый композиционный материал, такой как композит с керамической матрицей на основе карбида кремния, производится способом CVI.
Решение задачи
Для решения вышеуказанных задач в соответствии с одним вариантом осуществления настоящего изобретения предлагается способ получения кремниевого композиционного материала, включающий стадии: выдерживание преформы из карбида кремния (SiC) в реакционной печи; подача сырьевого газа, содержащего метилтрихлорсилан (MTS), в реакционную печь для пропитки преформы карбидом кремния; и контроль и изменение температуры газа, выпускаемого из реакционной печи, с заданной скоростью, чтобы подвергнуть газ непрерывному изменению температуры во времени, снижая тем самым образование жидкого или твердого побочного продукта из газа.
Стадия контроля и изменения температуры газа, выпускаемого из реакционной печи, может включать этап поддержания газа, выпускаемого из реакционной печи, при заданной температуре. Заданная температура может лежать в интервале от 500°C или выше, но меньше 950°C, или быть больше или равной 1500°C. Заданная температура может составлять от 600°C или выше, но меньше 800°C. Этап снижения образования жидкого или твердого побочного продукта может включать поддержание газа, выпускаемого из реакционной печи, при заданной температуре в течение заданного периода времени, составляющего от 0 до 8 сек. Этап снижения образования жидкого или твердого побочного продукта может включать ступенчатое изменение температуры газа до нескольких значений температур.
Жидкий или твердый побочный продукт может содержать высший хлорсилан. Этап снижения образования жидкого или твердого побочного продукта может включать превращение SiCl2, являющегося предшественником жидкого или твердого побочного продукта, в стабильное соединение, чтобы тем самым снизить образование жидкого или твердого побочного продукта. Стабильное соединение может включать по меньшей мере одно соединение из метилтрихлорсилана, диметилдихлорсилана ((CH3)2SiCl2), дисилана (Si2H6), дихлорсилана (SiH2Cl2), трихлорсилана (SiHCl3) или тетрахлорсилана (SiCl4).
Этап снижения образования жидкого или твердого побочного продукта может включать добавление заданного дополнительного газа в газ, выпускаемый из реакционной печи. Этап снижения образования жидкого или твердого побочного продукта может включать добавление дополнительного газа так, чтобы количество дополнительного газа было больше количества жидкого или твердого побочного продукта.
Этап снижения образования жидкого или твердого побочного продукта может включать добавление хлора таким образом, чтобы количество хлора было больше количества кремния, содержащегося в жидком или твердом побочном продукте.
Этап снижения образования жидкого или твердого побочного продукта может включать стадию поддержания газа, выпускаемого из реакционной печи, при заданной температуре, и стадия поддержания выпускаемого из реакционной печи газа при заданной температуре может включать добавление заданного дополнительного газа.
Стадия поддержания газа, выпускаемого из реакционной печи, при заданной температуре может включать использование печи риформинга (= печь для конверсии газа), и период времени, в течение которого газ, выпускаемый из реакционной печи, поддерживается при заданной температуре, может соответствовать времени пребывания газа в печи риформинга.
Заданная температура может быть больше или равной 200°C, но меньше 1100°C.
Заданная температура может быть больше или равной 750°C, но меньше 850°C.
Дополнительный газ может включать газ, содержащий хлорсодержащую молекулу. Дополнительный газ может включать по меньшей мере одно вещество из газообразного азота (N2), газообразного водорода (H2), хлористого водорода (HCl), хлорметана (CH3Cl), тетрахлорметана (CCl4), трихлорэтилена (C2HCl3), трихлорэтана (C2H3Cl3), этилена (C2H4), этанола (C2H6O), ацетона (C3H6O), метанола (CH4O), водяного пара (H2O), дихлорметана (CH2Cl2) или хлороформа (CHCl3).
Кроме того, дополнительный газ может содержать хлорметан или дихлорметан, и на стадии поддержания газа, выпускаемого из реакционной печи, при заданной температуре, период времени, в течение которого выпускаемый из реакционной печи газ вместе с добавленным к нему дополнительным газом поддерживается при заданной температуре, можно установить больше или равным 0,08 сек.
Кроме того, дополнительный газ может включать хлорметан или дихлорметан, и на стадии поддержания газа, выпускаемого из реакционной печи, при заданной температуре период времени, в течение которого выпускаемый из реакционной печи газ вместе с добавленным к нему дополнительным газом поддерживается при заданной температуре, может составлять 1 сек или больше.
Кроме того, дополнительный газ может включать хлорметан, и на стадии поддержания газа, выпускаемого из реакционной печи, при заданной температуре, количество добавляемого хлорметана может быть больше или равно количеству метилтрихлорсилана в загружаемом сырьевом газе.
Кроме того, дополнительный газ может включать хлорметан, и на стадии поддержания газа, выпускаемого из реакционной печи, при заданной температуре заданная температура может быть больше или равной 750°C, но меньше 850°C, количество добавляемого хлорметана может составлять от одного до полутора количеств метилтрихлорсилана в загружаемом сырьевом газе, и период времени, в течение которого выпускаемый из реакционной печи газ вместе с добавленным к нему дополнительным газом поддерживается при заданной температуре, может быть установлен в интервале от 1 сек или больше, но меньше 10 секунд.
Кроме того, дополнительный газ может включать дихлорметан, и на стадии поддержания выпускаемого из реакционной печи газа при заданной температуре количество добавляемого дихлорметана может составлять от 0,25 или больше от количества метилтрихлорсилана в загружаемом сырьевом газе.
Кроме того, дополнительный газ может включать дихлорметан, и на стадии поддержания выпускаемого из реакционной печи газа при заданной температуре заданная температура может быть больше или равной 750°C, но меньше 850°C, количество добавляемого дихлорметана может составлять от 0,25 до полутора количеств метилтрихлорсилана в загружаемом сырьевом газе, и период времени, в течение которого выпускаемый из реакционной печи газ вместе с добавленным к нему дополнительным газом поддерживается при заданной температуре, может быть установлен в интервале от 1 сек или больше, но меньше 10 сек.
Кроме того, дополнительный газ может включать любое соединение из хлористого водорода, тетрахлорметана, трихлорэтилена, трихлорэтана и этилена, заданная температура может составлять 975°C, количество добавляемого газа может быть равным количеству метилтрихлорсилана в загружаемом сырьевом газе, и период времени, в течение которого выпускаемый из реакционной печи газ вместе с добавленным к нему дополнительным газом поддерживается при заданной температуре, можно установить равным 1 сек.
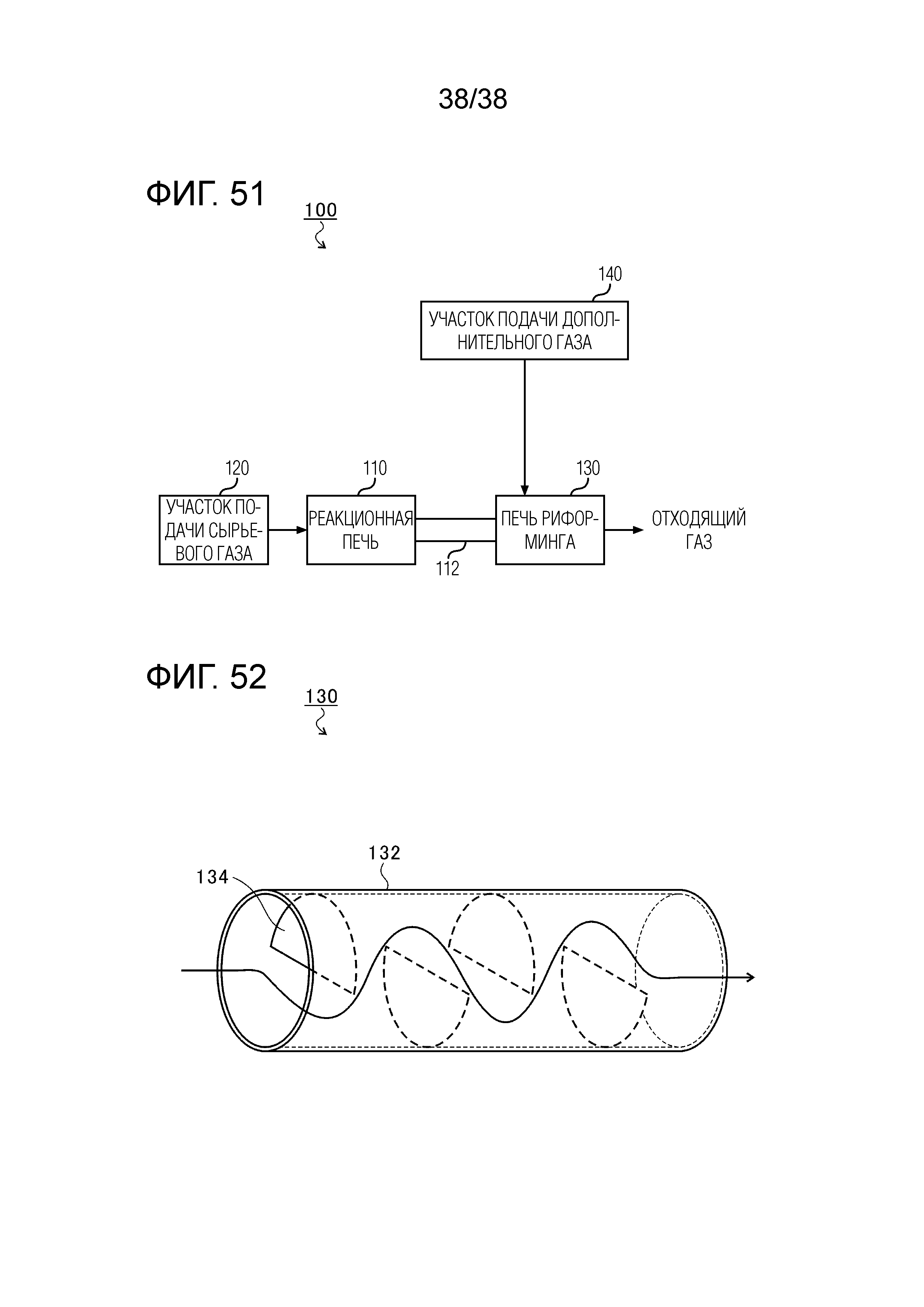
Для решения вышеуказанных задач в одном варианте осуществления настоящего изобретения предлагается устройство для получения кремниевого композиционного материала, содержащее: реакционную печь, предназначенную для выдерживания преформы; участок подачи сырьевого газа, предназначенный для подачи сырьевого газа, содержащего метилтрихлорсилан, в реакционную печь; печь риформинга, предназначенную для поддержания газа, выпускаемого из реакционной печи, при заданной температуре, и участок подачи дополнительного газа, предназначенный для подачи заданного дополнительного газа в печь риформинга.
Кроме того, печь риформинга может быть печью с горячими стенками.
Кроме того, в печи риформинга может быть установлена отражательная перегородка.
Кроме того, печь риформинга может быть образована из трубы круглого сечения, и труба круглого сечения может иметь удельную поверхность, определенную делением объема трубы круглого сечения на площадь поверхности трубы круглого сечения, в интервале от 5 мм до 15 мм.
Эффекты от изобретения
Благодаря настоящему изобретению можно уменьшить образование из газа, выпускаемого из реакционной печи, в которой способом CVI производится кремниевый композиционный материал, такой как композит с керамической матрицей на основе карбида кремния, жидкого или твердого побочного продукта, который может превратиться во взрывоопасное вещество в результате реакции с атмосферой.
Краткое описание чертежей
Фиг. 1 показывает концептуальную схему способа CVI.
Фиг. 2 иллюстрирует пояснение структуры механизма реакции образования побочного продукта.
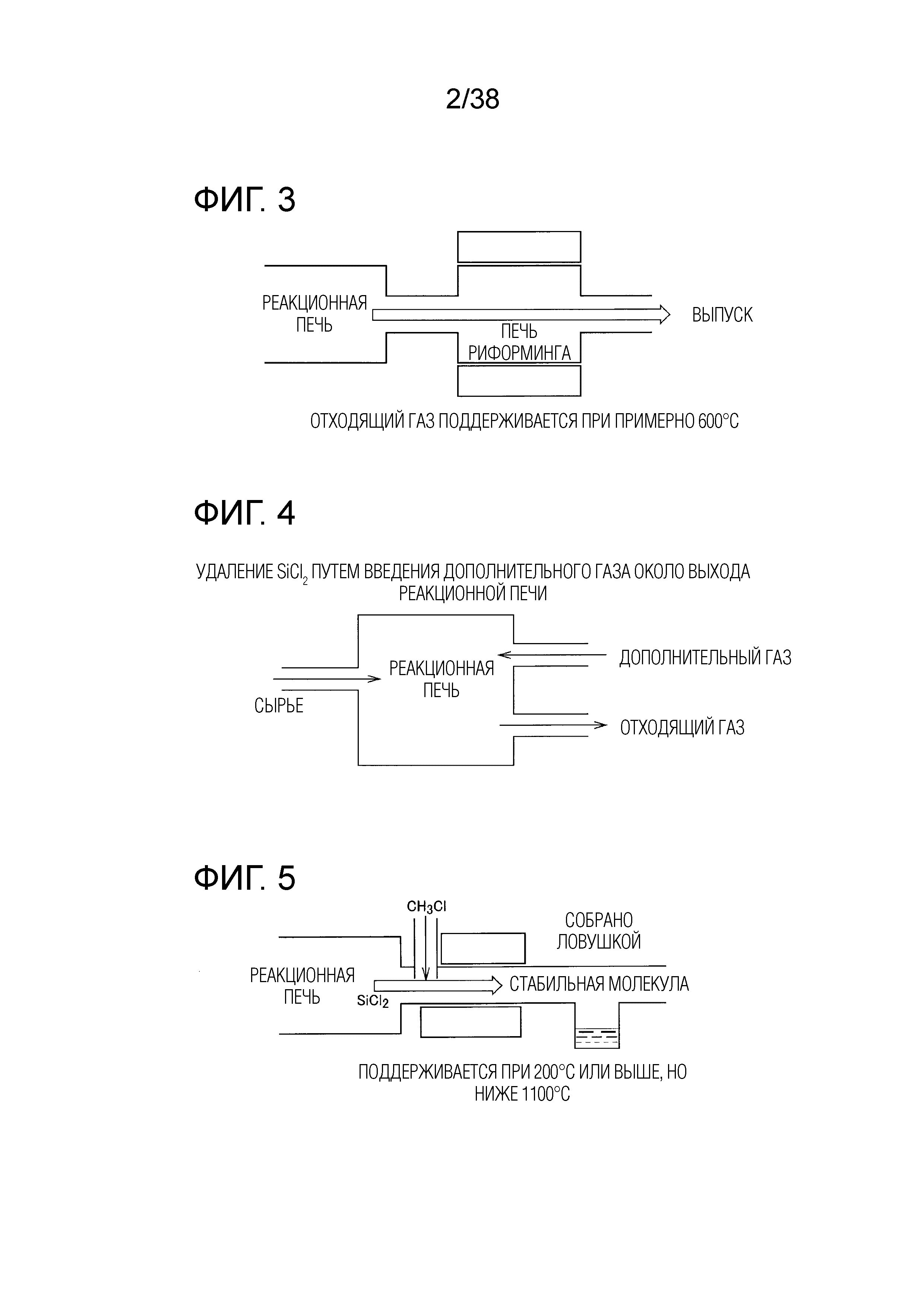
Фиг. 3 иллюстрирует способ снижения образования побочного продукта благодаря использованию печи риформинга.
Фиг. 4 иллюстрирует способ снижения образования побочного продукта благодаря введению дополнительного газа.
Фиг. 5 иллюстрирует способ снижения образования побочного продукта благодаря использованию печи риформинга и дополнительного газа.
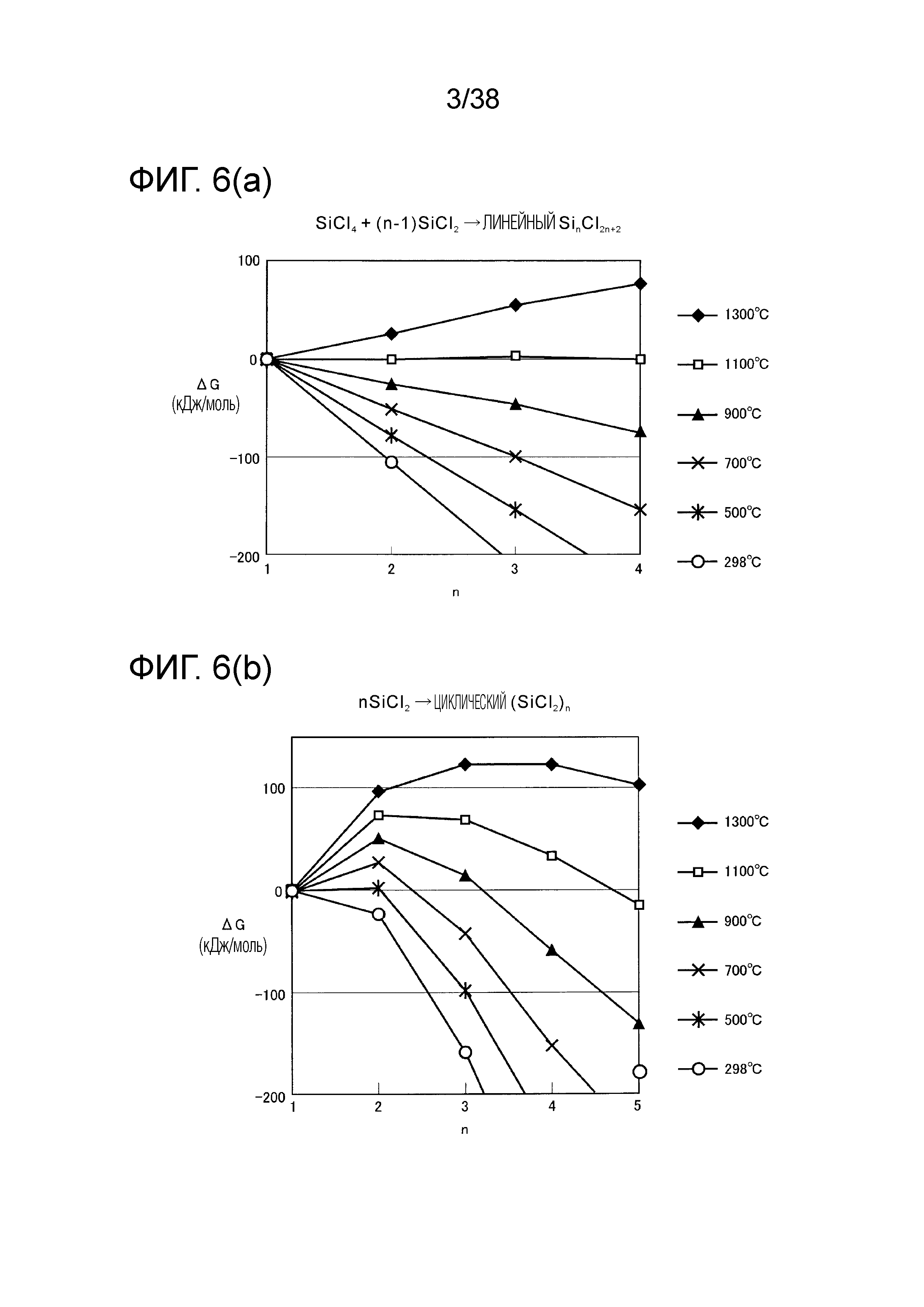
Фиг. 6(a) является первым графиком, показывающим изменение свободной энергии высших хлорсиланов.
Фиг. 6(b) является вторым графиком, показывающим изменение свободной энергии высших хлорсиланов.
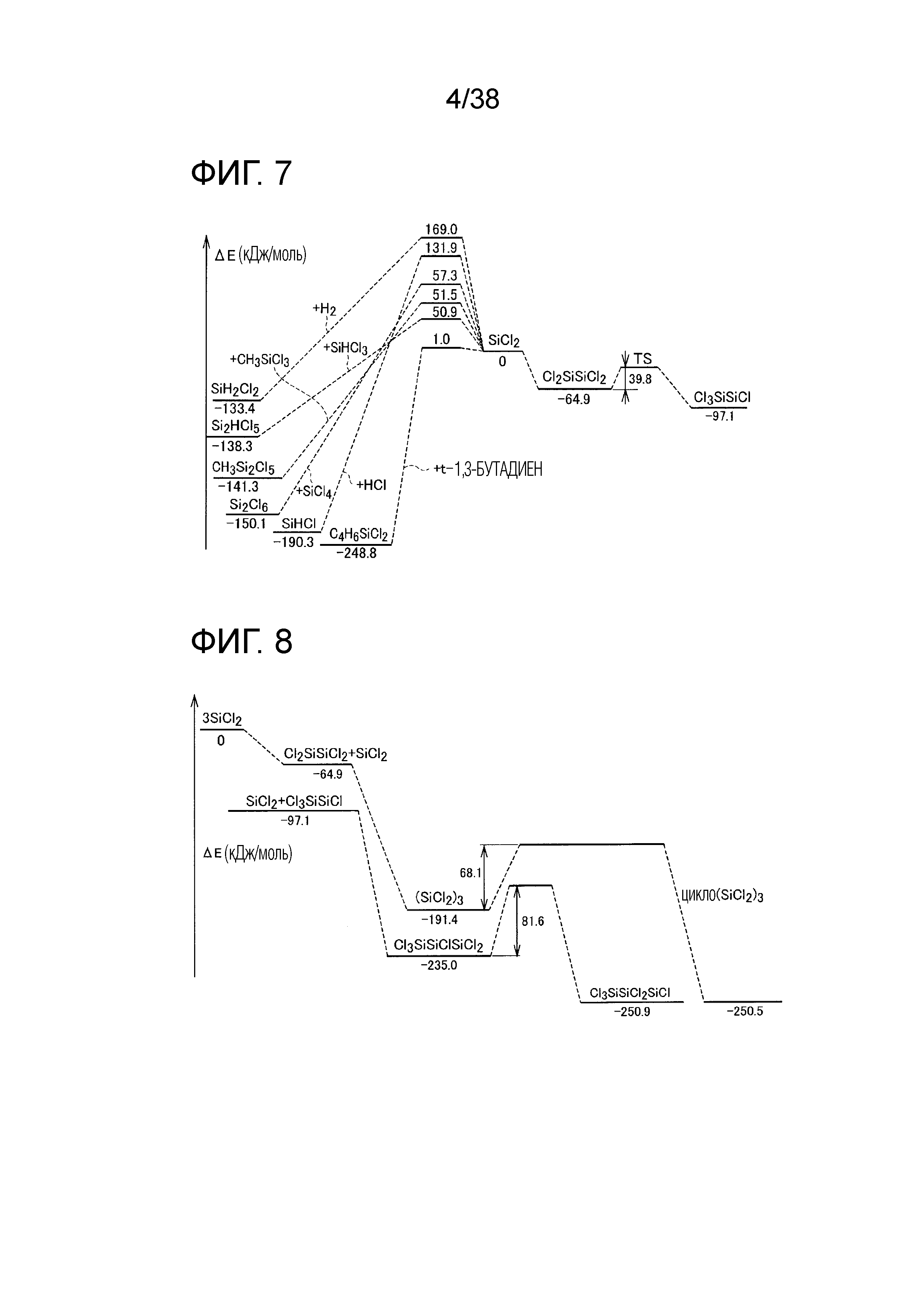
Фиг. 7 иллюстрирует маршрут реакции между SiCl2 и другими газообразными веществами.
Фиг. 8 иллюстрирует маршрут реакции от 3SiCl2 к (SiCl2)3.
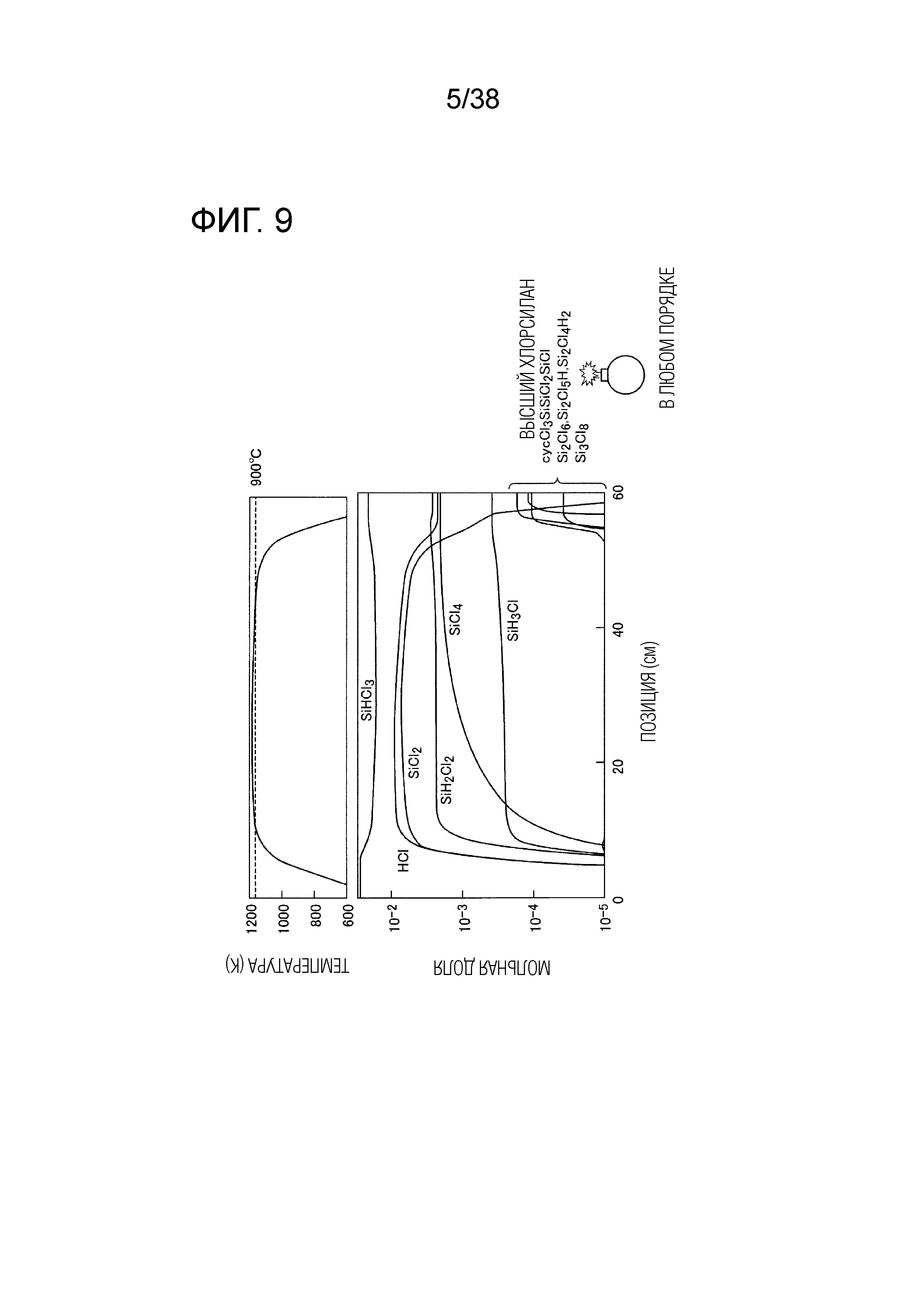
Фиг. 9 содержит графики для анализа температуры полимеризации SiCl2.
Фиг. 10(a) является первой иллюстрацией основной реакции SiCl2 при снижении температуры.
Фиг. 10(b) является второй иллюстрацией основной реакции SiCl2 при снижении температуры.
Фиг. 10(c) является третьей иллюстрацией основной реакции SiCl2 при снижении температуры.
Фиг. 11(a) является первым изображением для анализа условий термообработки на стороне выпуска газов.
Фиг. 11(b) является вторым изображением, включающим графики для анализа условий термообработки на стороне выпуска газов.
Фиг. 12(a) показывает первый график для сравнения количеств образованных высших хлорсиланов в зависимости от температуры поддерживания.
Фиг. 12(b) показывает второй график для сравнения количеств образованных высших хлорсиланов в зависимости от температуры поддерживания.
Фиг. 12(c) показывает третий график для сравнения количеств образованных высших хлорсиланов в зависимости от температуры поддерживания.
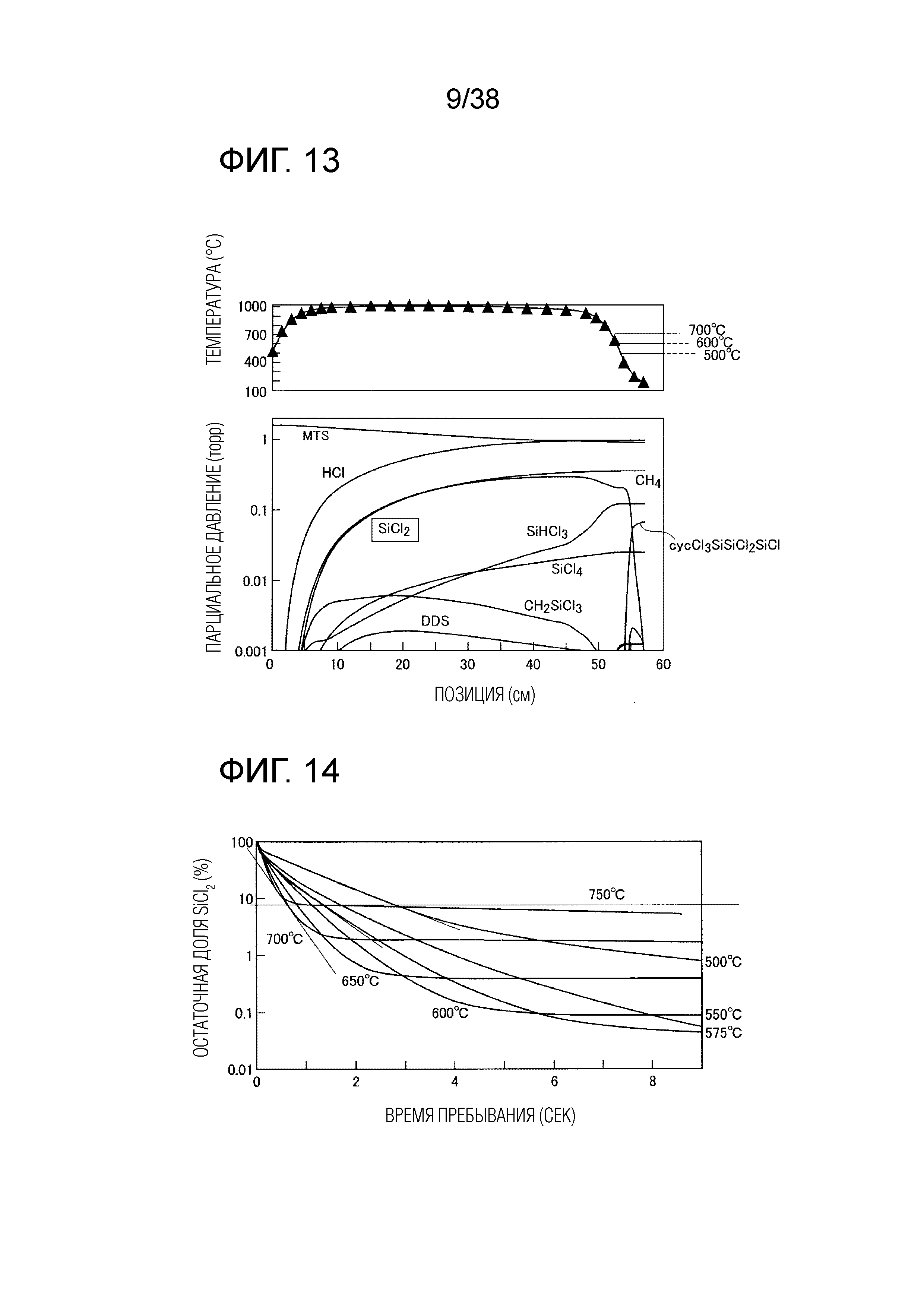
Фиг. 13 показывает графики, предсказывающие полимеризацию SiCl2 в системе MTS/H2.
Фиг. 14 показывает график скорости уменьшения количества SiCl2 при поддерживании отходящего газа при разных температурах.
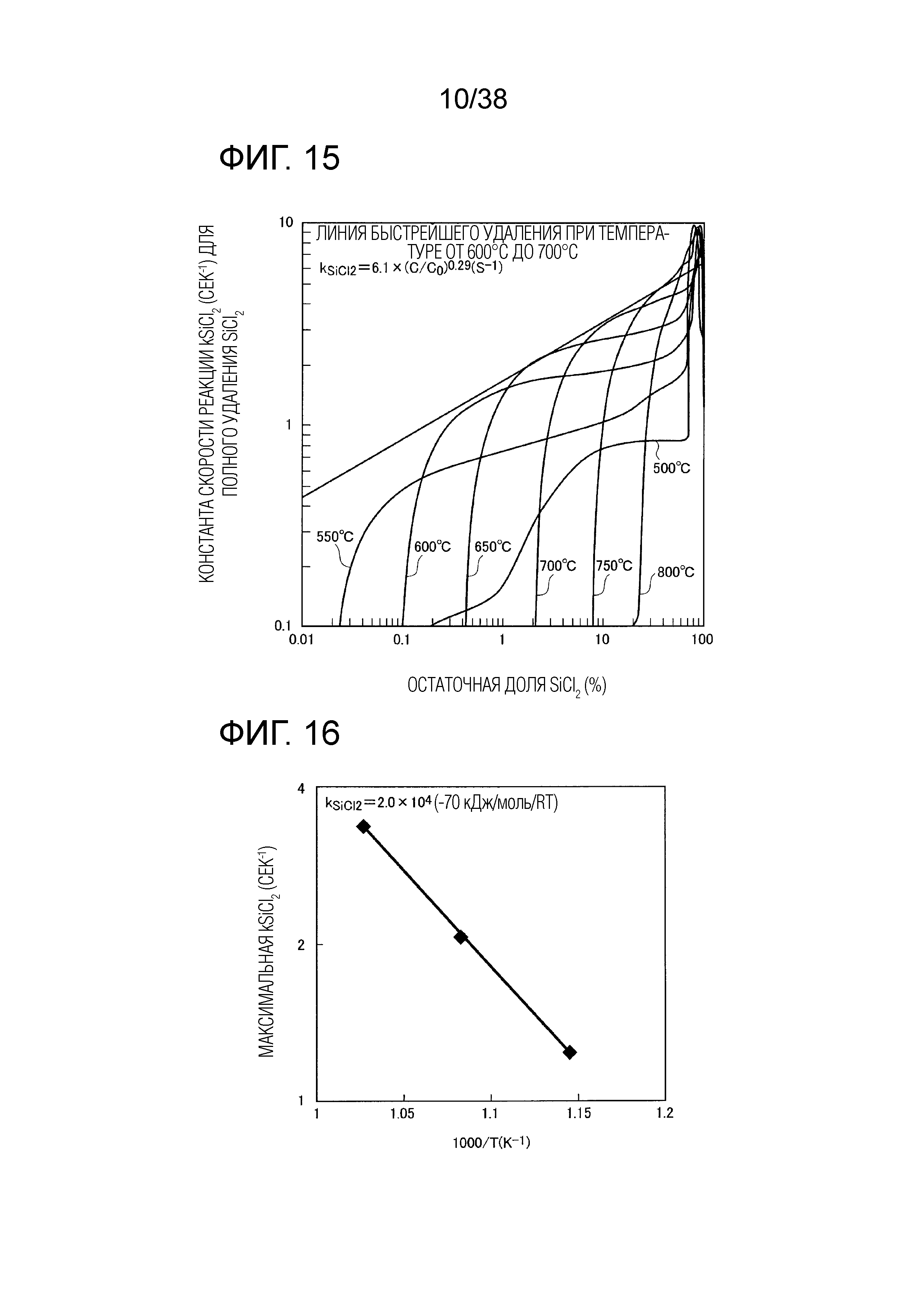
Фиг. 15 является графиком, показывающим константу kSiCl2 скорости реакции полного удаления, когда побочный продукт может быть удален быстрее всего благодаря сочетанию оптимальных условий при каждой температуре поддерживания.
Фиг. 16 является графиком, показывающим зависимость от температуры максимальной константы kSiCl2 скорости реакции полного удаления, показаннй на фиг. 15.
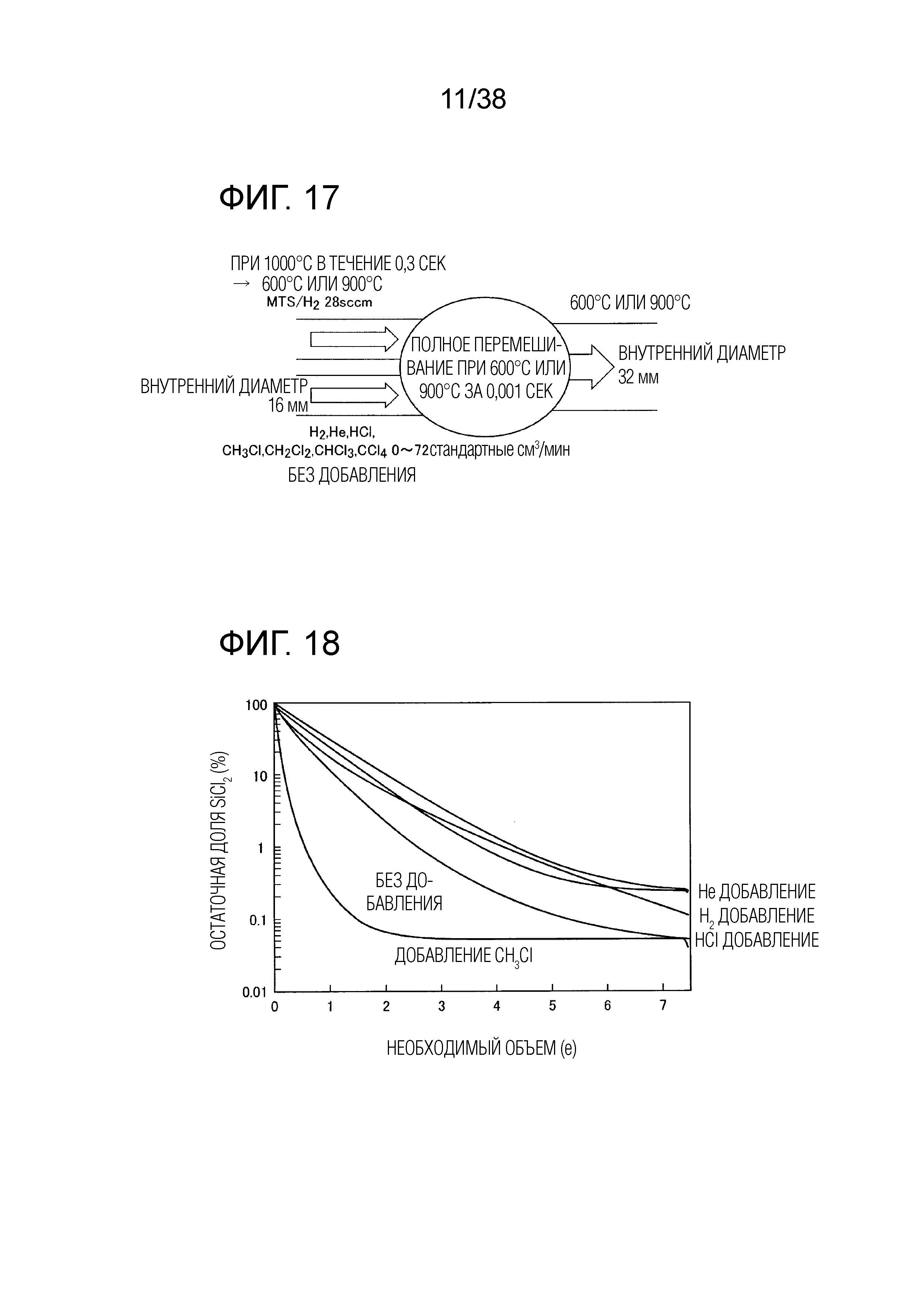
Фиг. 17 иллюстрирует совокупность условий для расчета реакции при добавлении газа.
Фиг. 18 является графиком, показывающим эффект добавления первого газа при 600°C.
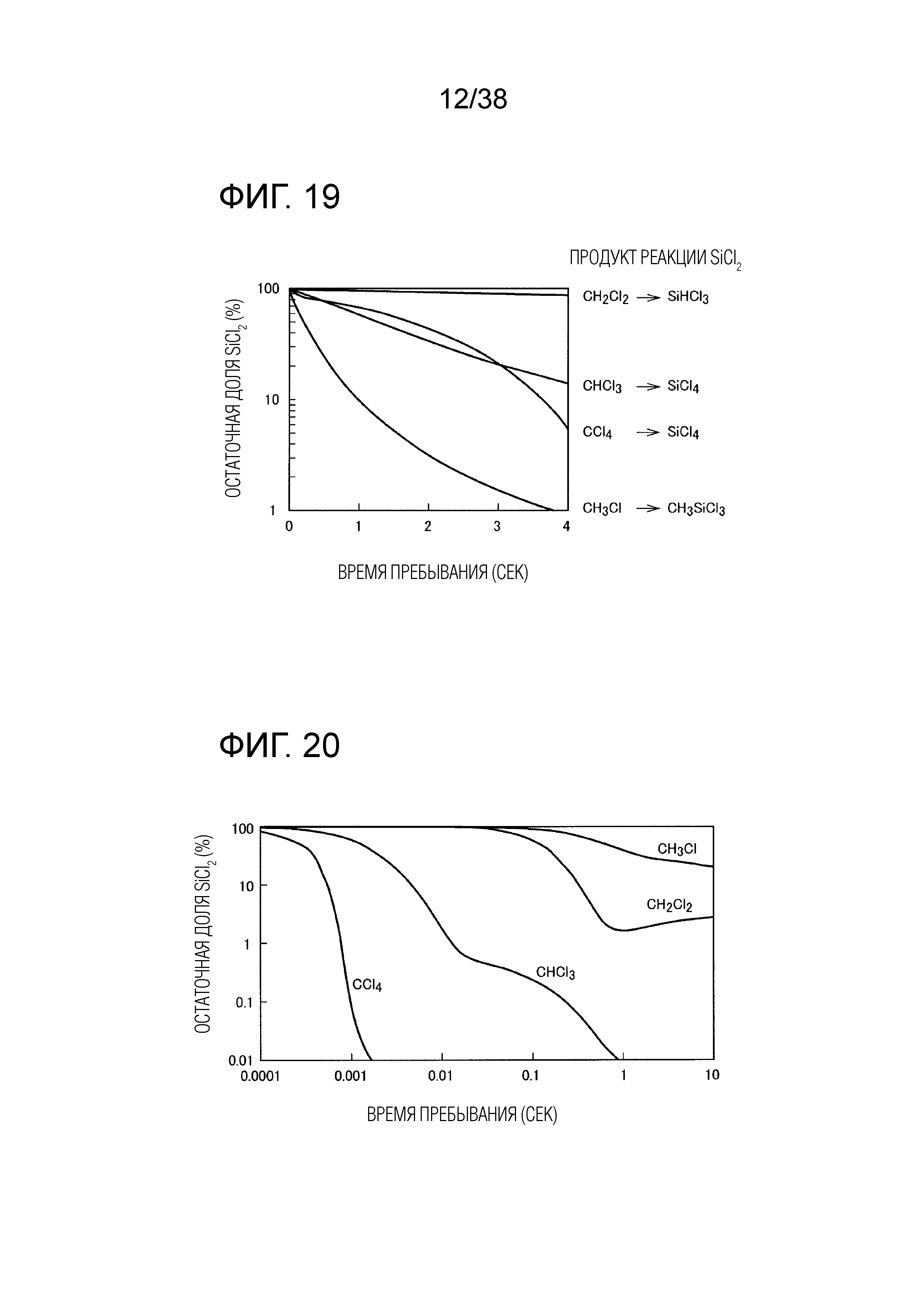
Фиг. 19 является графиком, показывающим эффект добавления второго газа при 600°C.
Фиг. 20 является графиком, показывающим эффект добавления газа при 900°C.
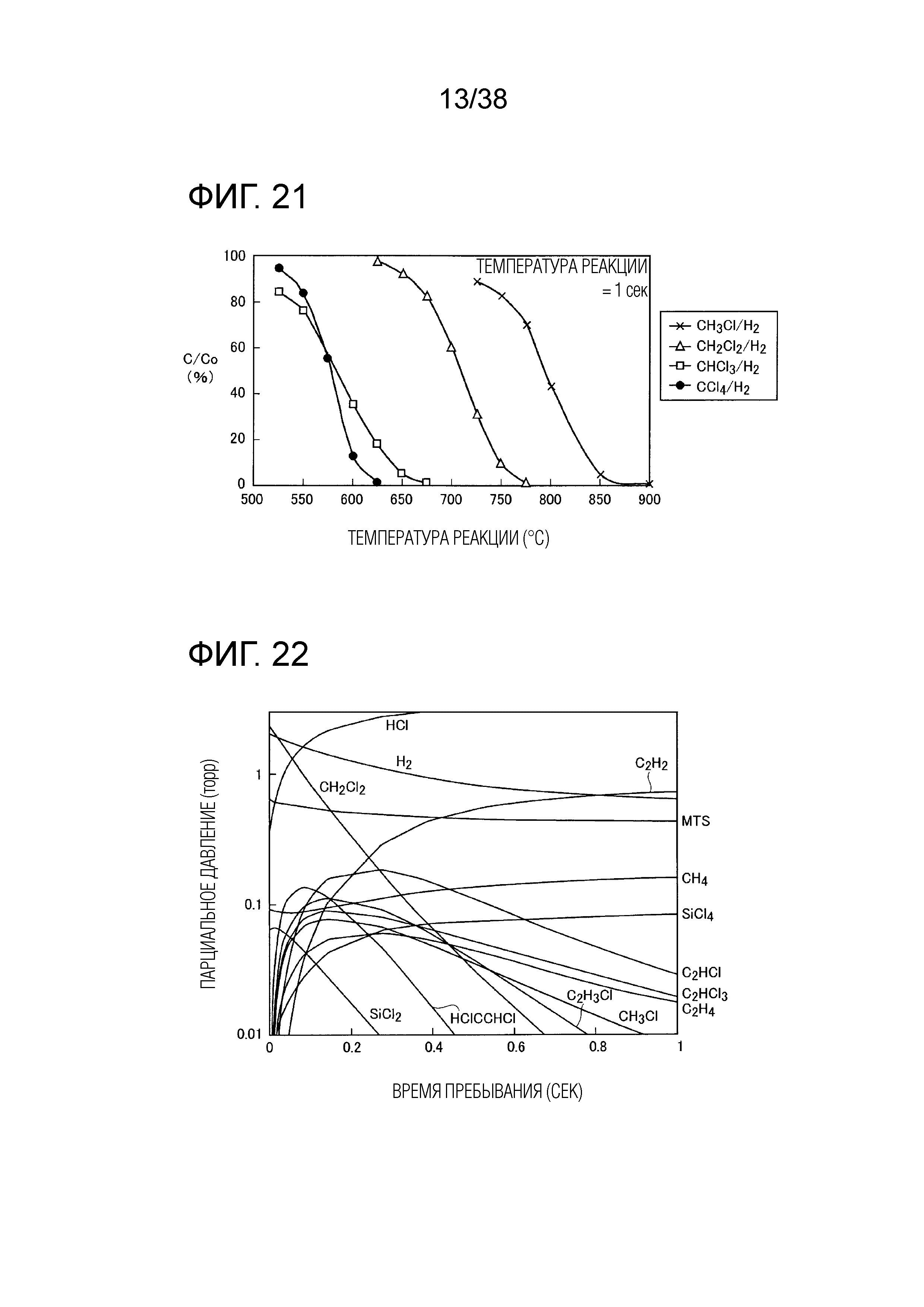
Фиг. 21 является графиком, показывающим остаточный уровень CH4-nCln после реакции CH4-nCln/H2 в течение 1 секунды при различных температурах.
Фиг. 22 является графиком, показывающим изменение парциальное давление газообразных веществ при добавлении CH2Cl2 и поддерживании при 900°C.
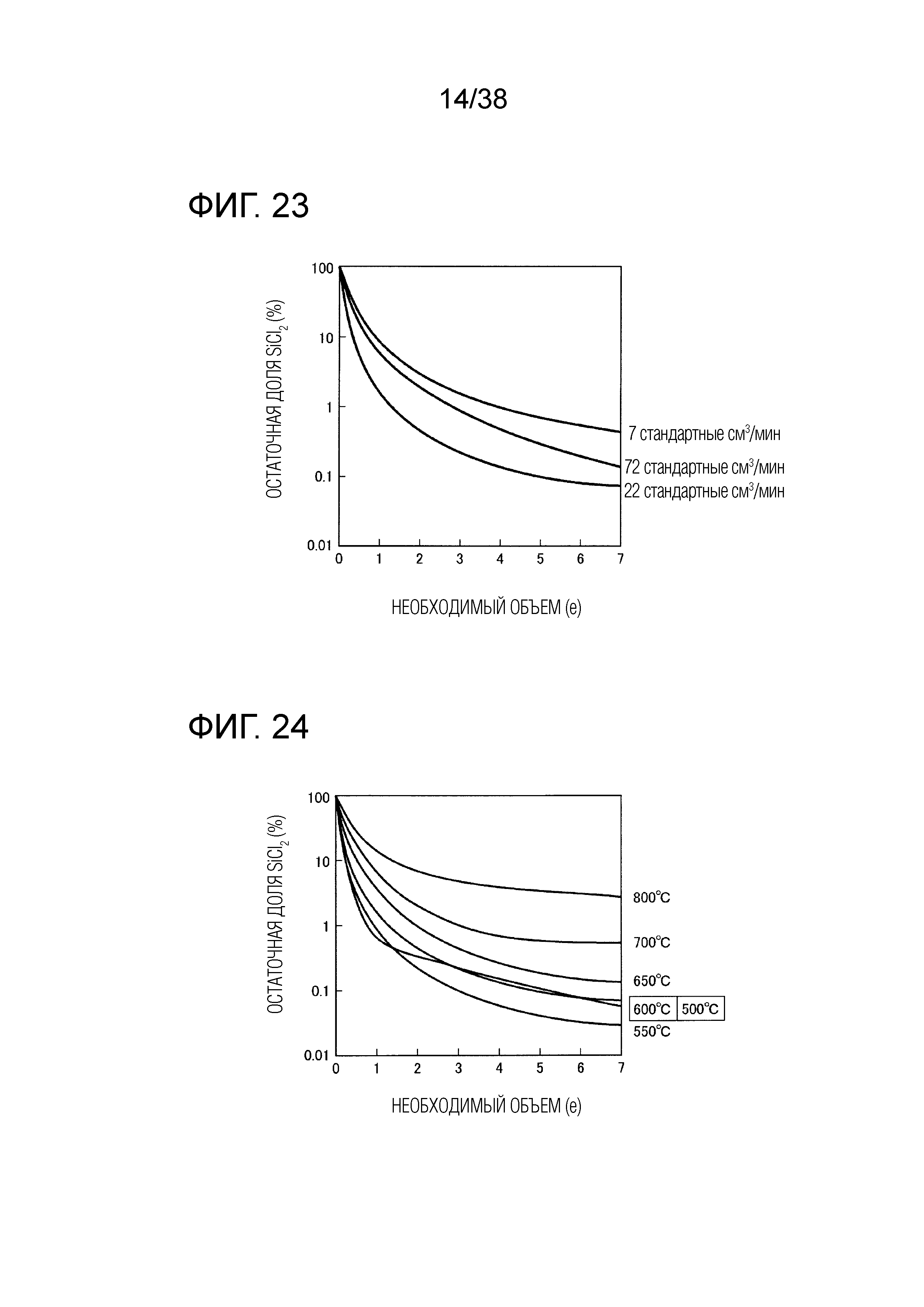
Фиг. 23 является графиком для анализа оптимального количества добавленного CH3Cl.
Фиг. 24 является графиком для анализа оптимальной температуры при добавлении CH3Cl.
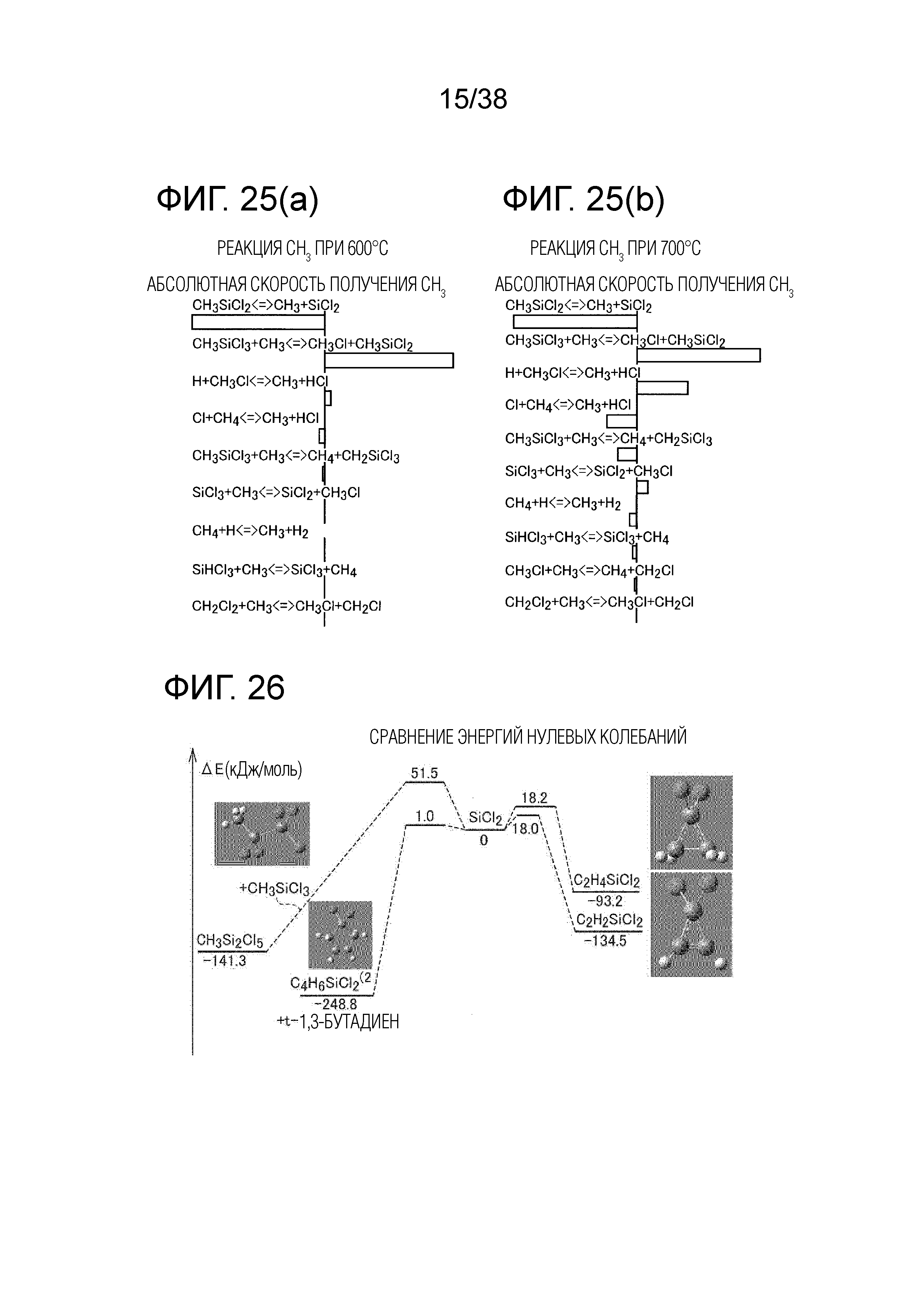
Фиг. 25(a) является первой иллюстрацией основной реакции радикала CH3 при разных температурах.
Фиг. 25(b) является второй иллюстрацией основной реакции радикала CH3 при разных температурах.
Фиг. 26 иллюстрирует энергию реакции между SiCl2 и молекулой на основе C.
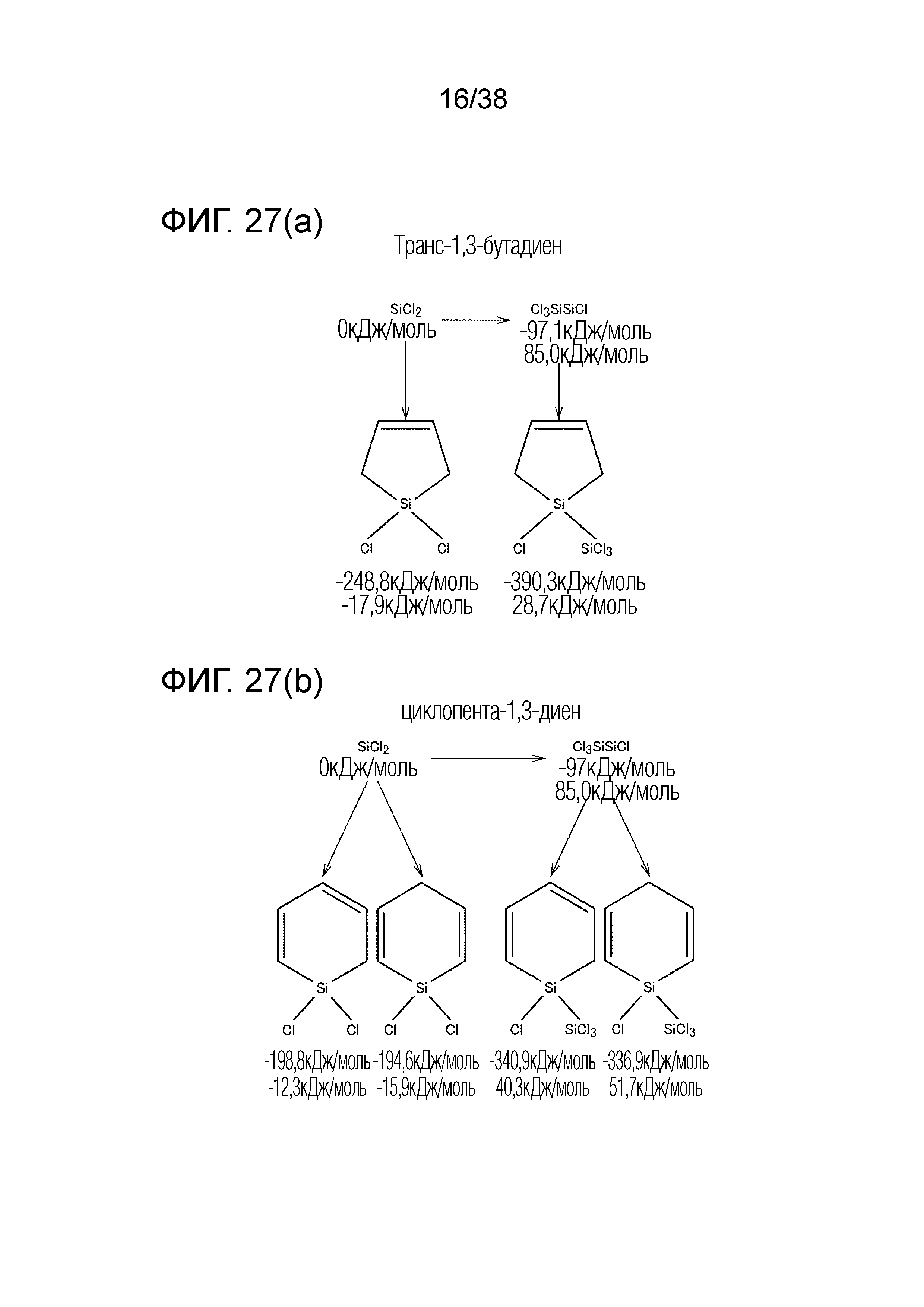
Фиг. 27(a) является первой иллюстрацией, показывающей энергию реакции между SiCl2 и диеном.
Фиг. 27(b) является второй иллюстрацией, показывающей энергию реакции между SiCl2 и диеном.
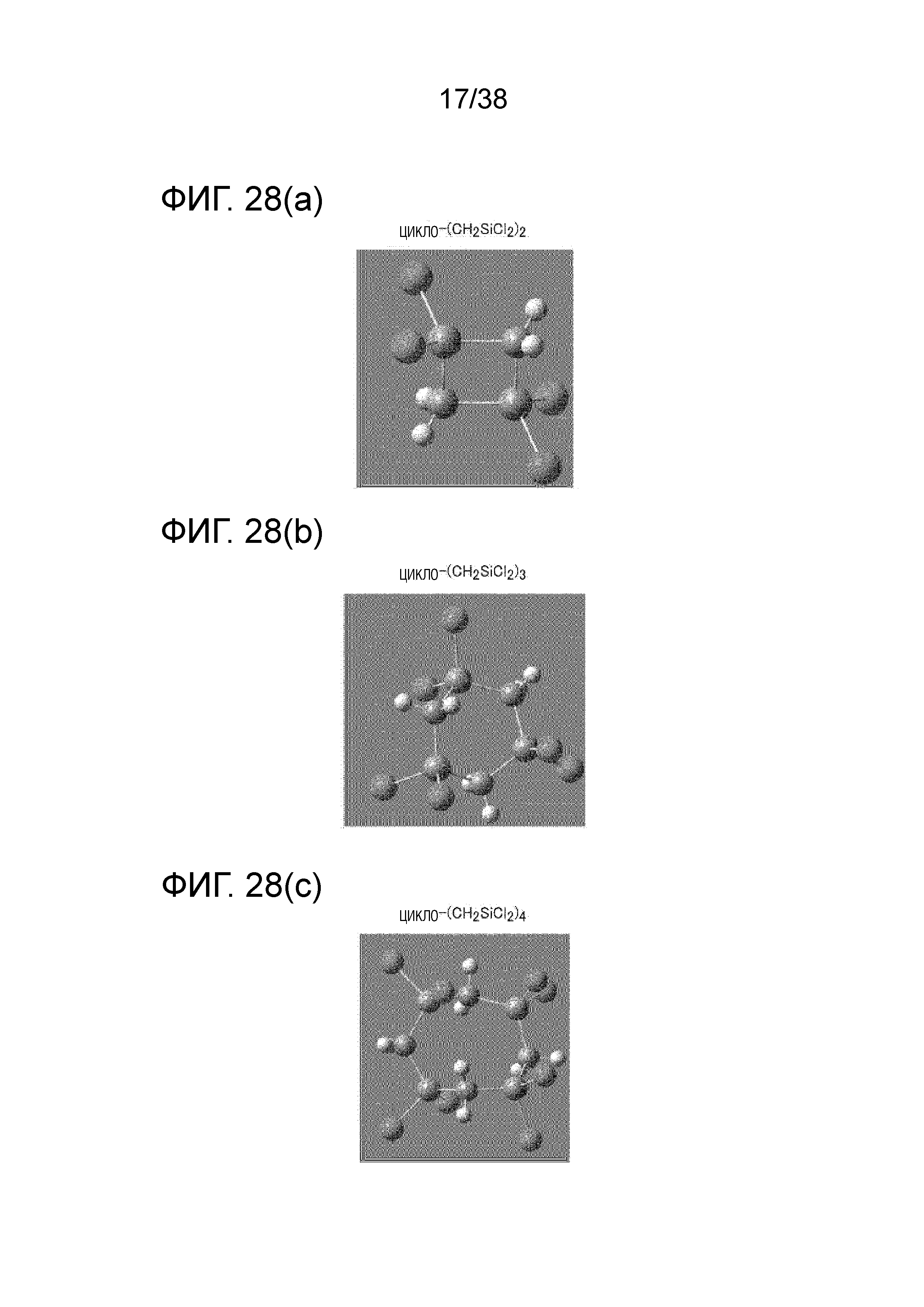
Фиг. 28(a) является первой иллюстрацией, показывающей циклическую структуру (CH2SiCl2)n.
Фиг. 28(b) является второй иллюстрацией, показывающей циклическую структуру (CH2SiCl2)n.
Фиг. 28(c) является третьей иллюстрацией, показывающей циклическую структуру (CH2SiCl2)n.
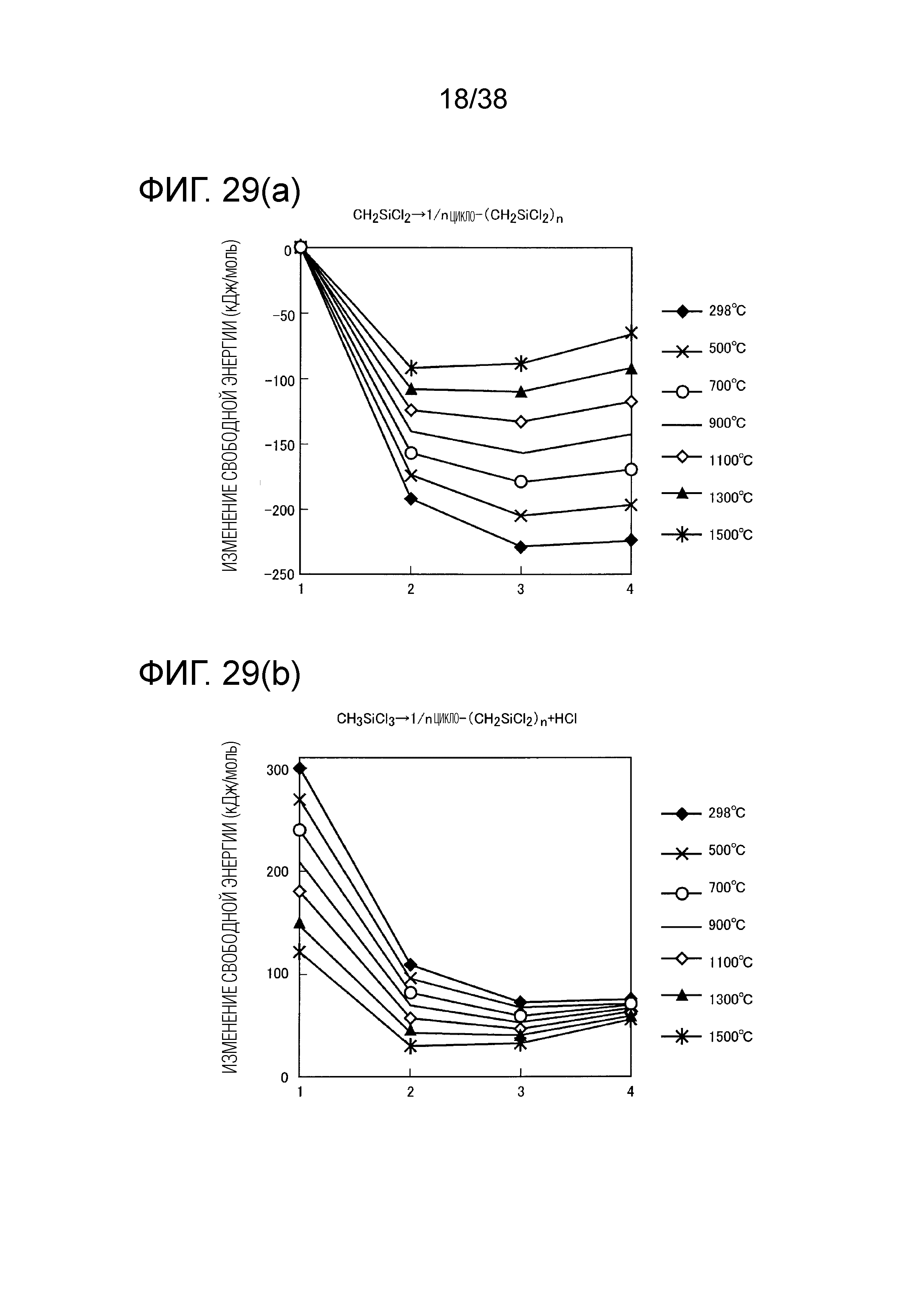
Фиг. 29(a) является первым графиком, показывающим изменение свободной энергии циклического (CH2SiCl2)n при разных температурах (K).
Фиг. 29(b) является вторым графиком, показывающим изменение свободной энергии циклического (CH2SiCl2)n при разных температурах (K).
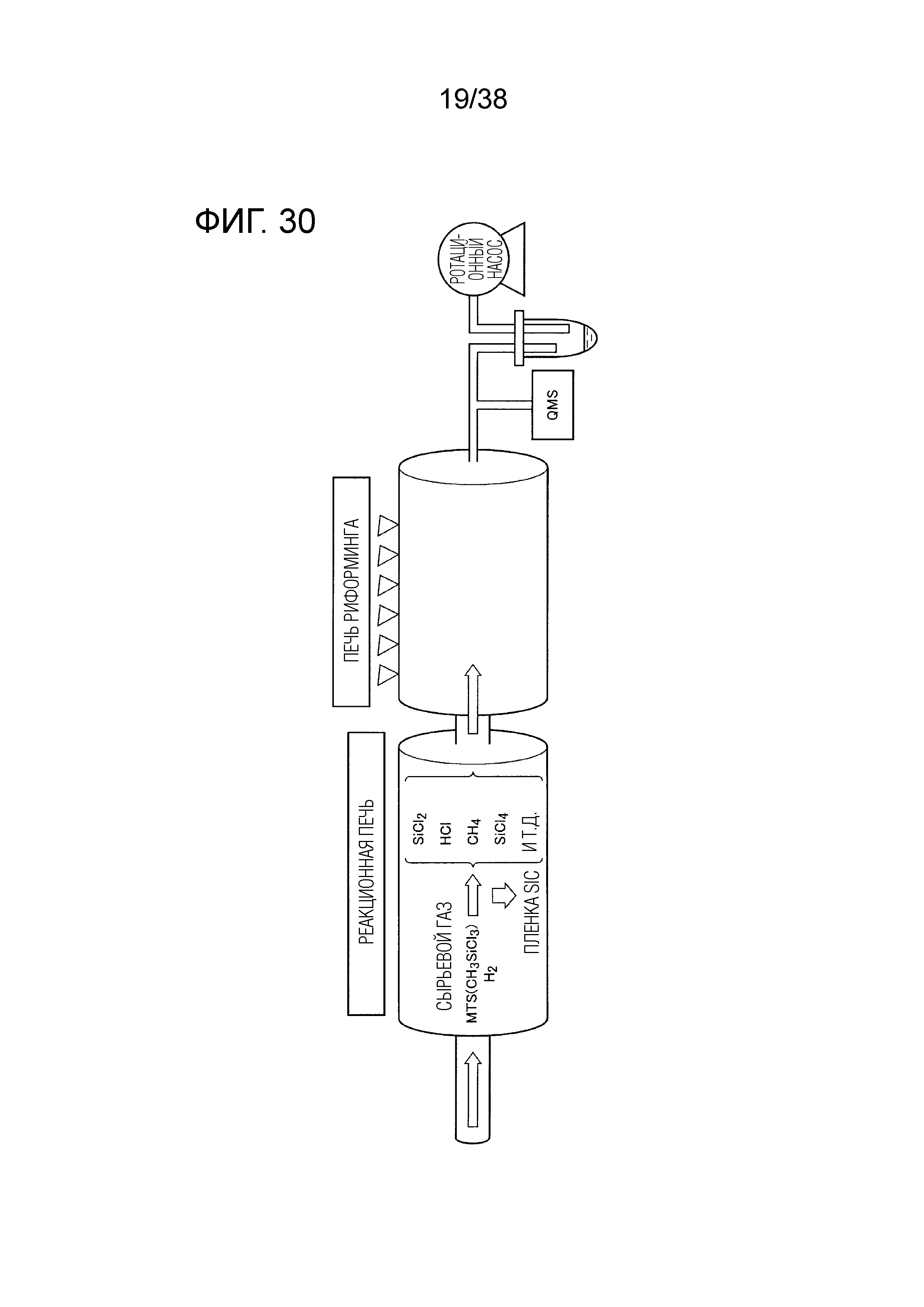
Фиг. 30 показывает схему экспериментального устройства для риформинга отходящего газа.
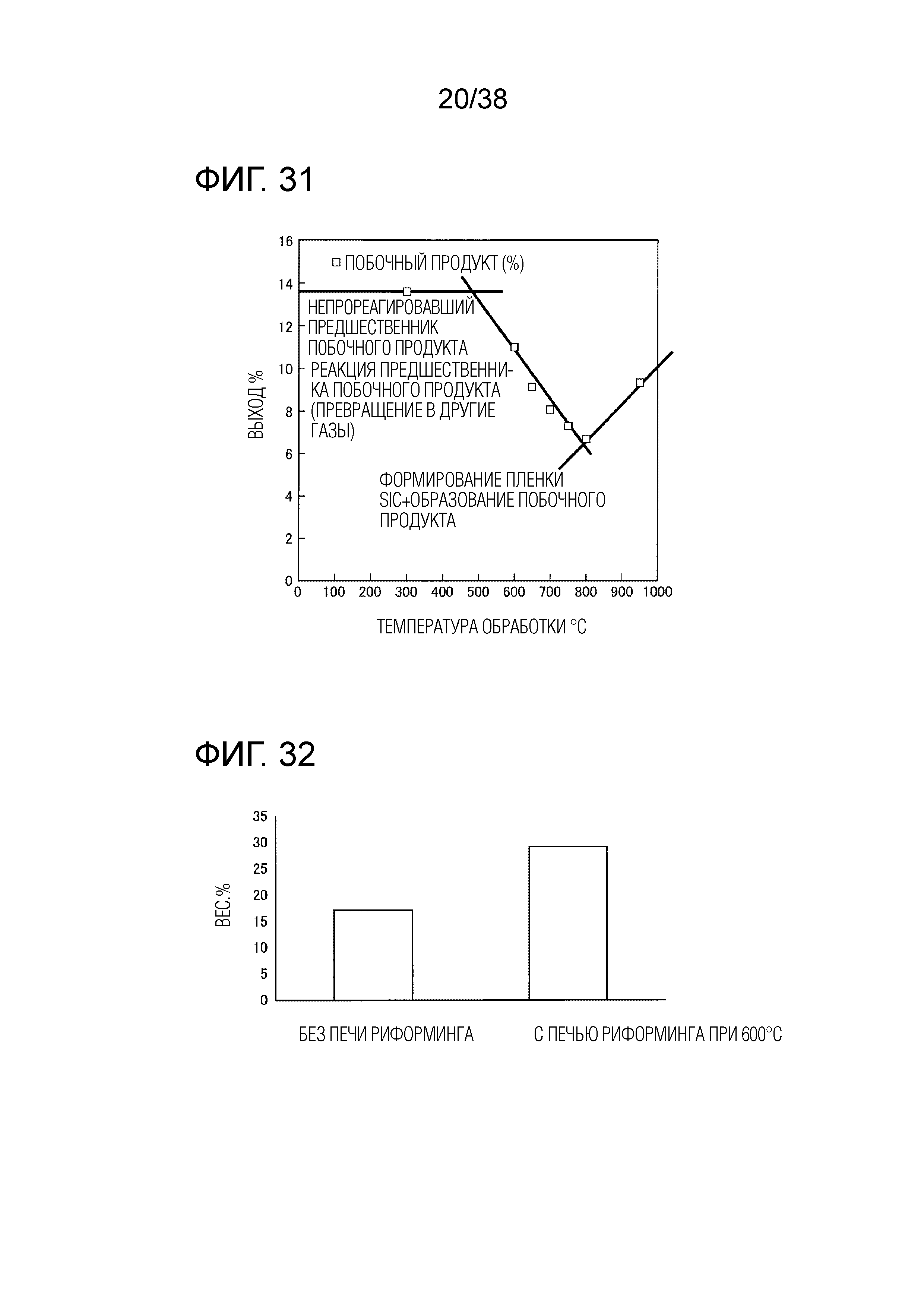
Фиг. 31 является графиком, показывающим соотношение между количеством собираемого побочного продукта и температурой обработки.
Фиг. 32 является графиком, показывающим связь между наличием или отсутствием печи риформинга и содержанием MTS.
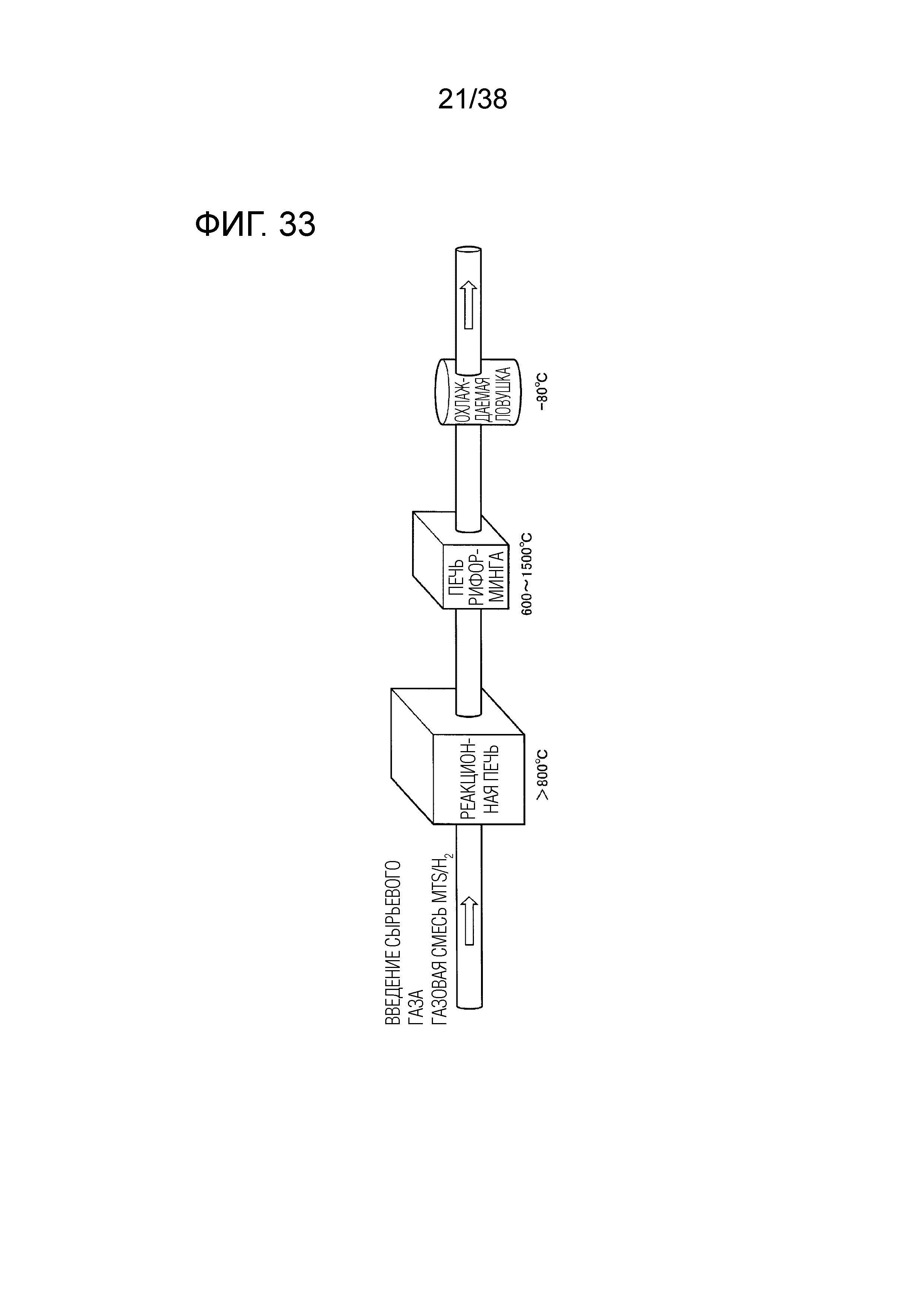
Фиг. 33 иллюстрирует схему эксперимента для многообразия побочных продуктов в зависимости от температуры печи риформинга.
Фиг. 34 показывает фотографии внешнего вида жидкого побочного продукта и окиси кремния.
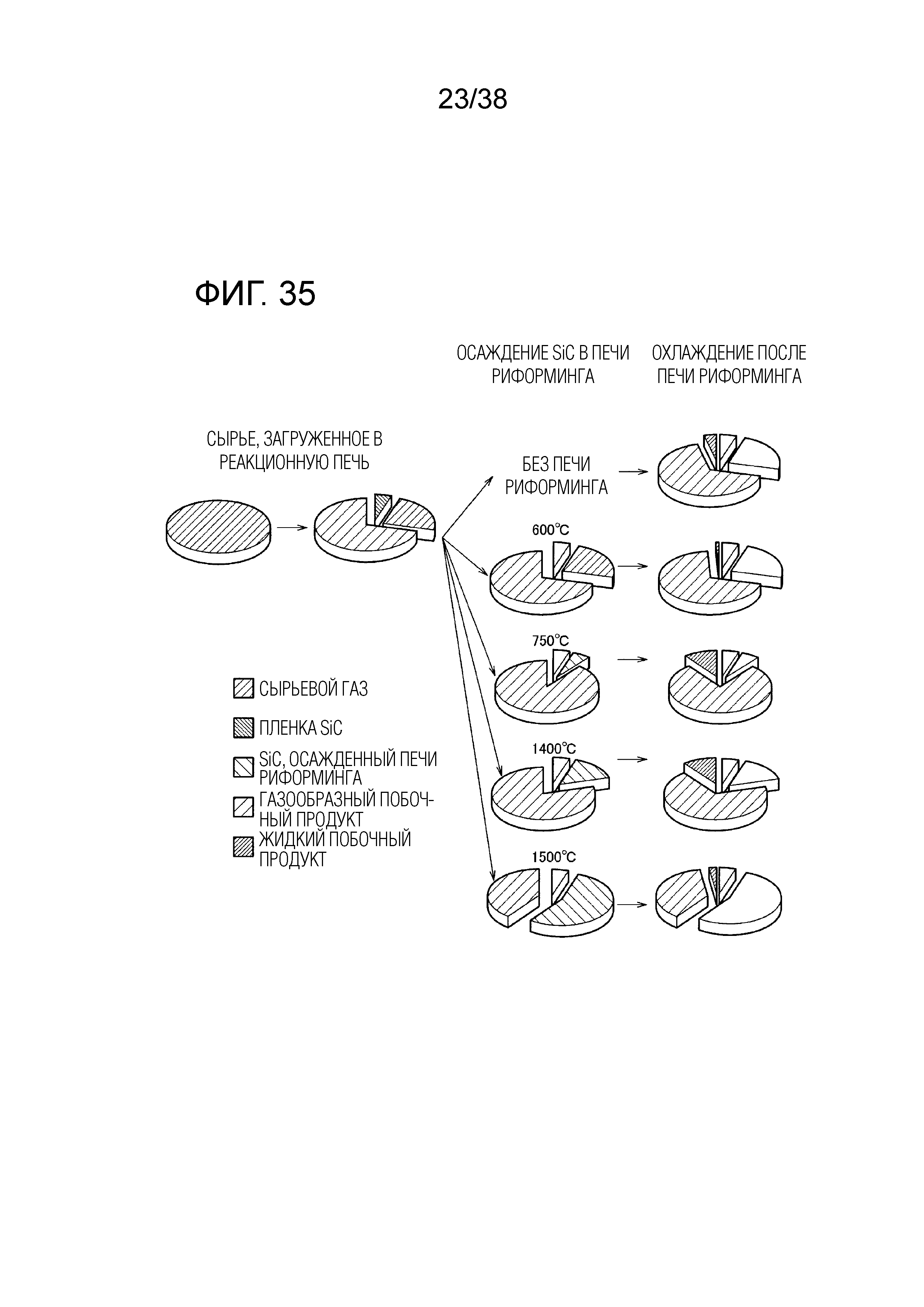
Фиг. 35 содержит диаграммы, показывающие разнообразие побочных продуктов в зависимости от температуры в печи риформинга.
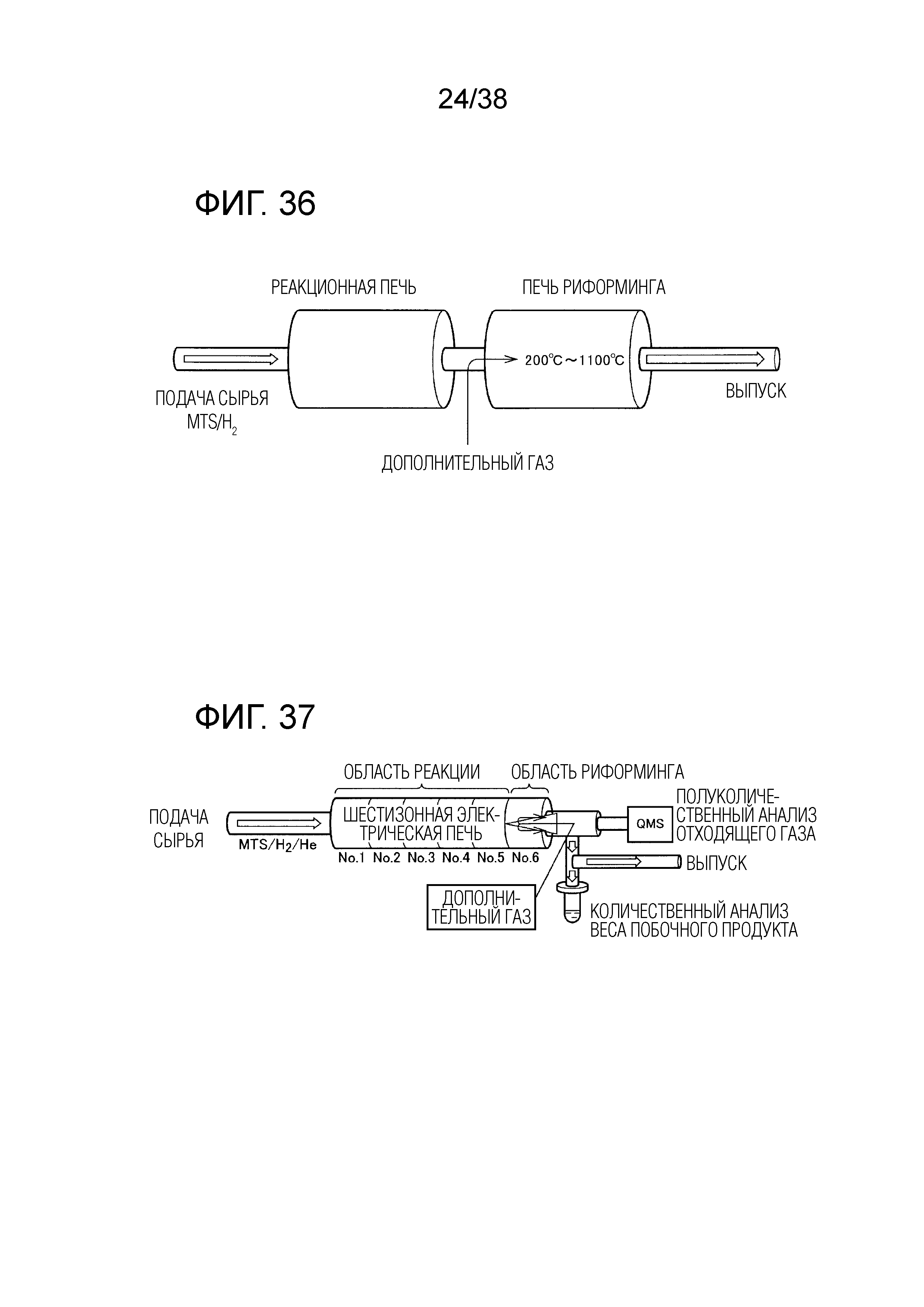
Фиг. 36 показывает концептуальную схему обработки отходящего газа дополнительным газом.
Фиг. 37 иллюстрирует схему эксперимента.
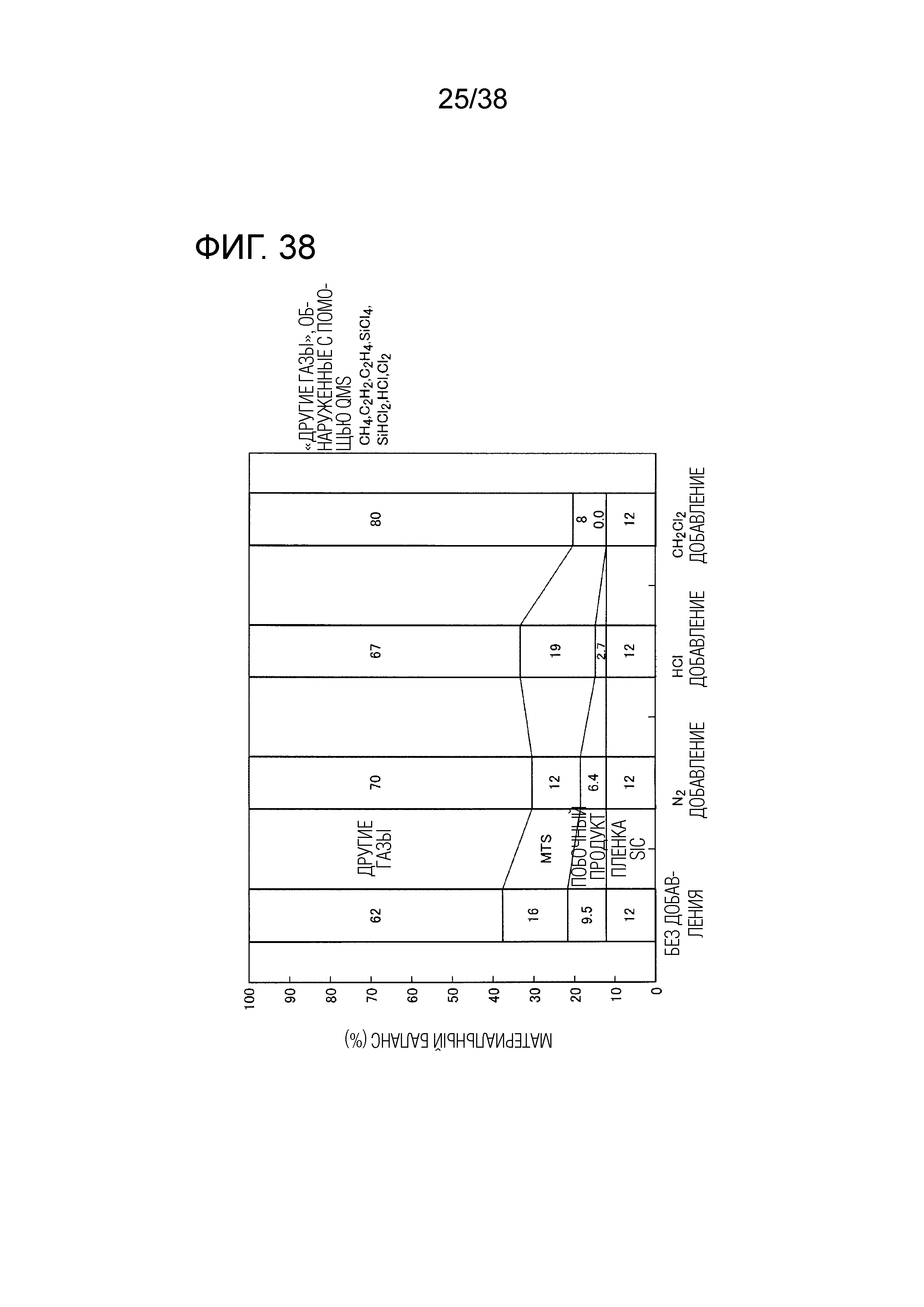
Фиг. 38 является диаграммой, показывающей материальный баланс.
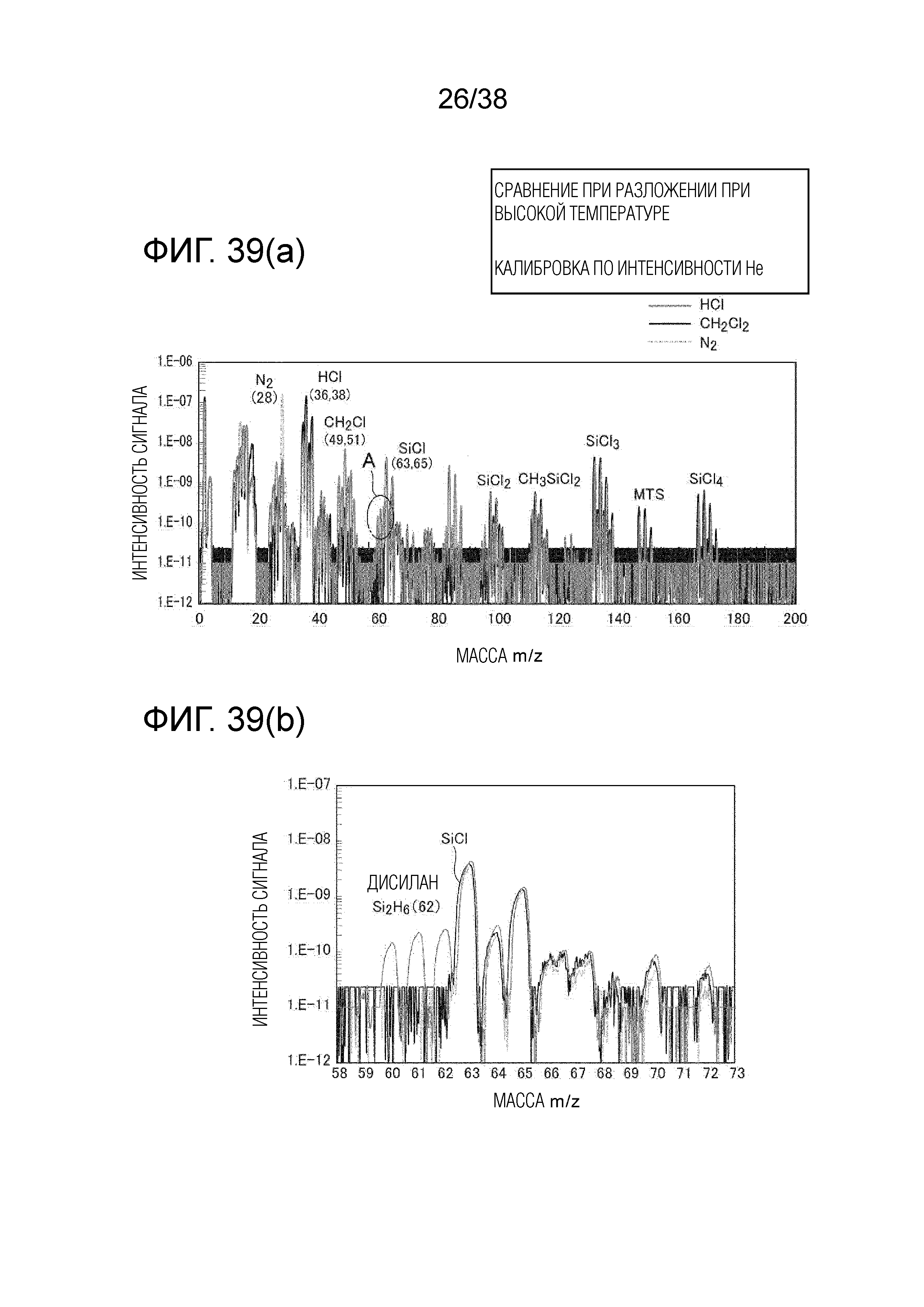
Фиг. 39(a) является первым графиком, показывающим сравнение составов отходящего газа во время разложения при высокой температуре для случаев использования HCl, CH2Cl2 и N2 в качестве дополнительного газа.
Фиг. 39(b) является вторым графиком, показывающим сравнение составов отходящего газа во время разложения при высокой температуре при использовании HCl, CH2Cl2 и N2 в качестве дополнительного газа.
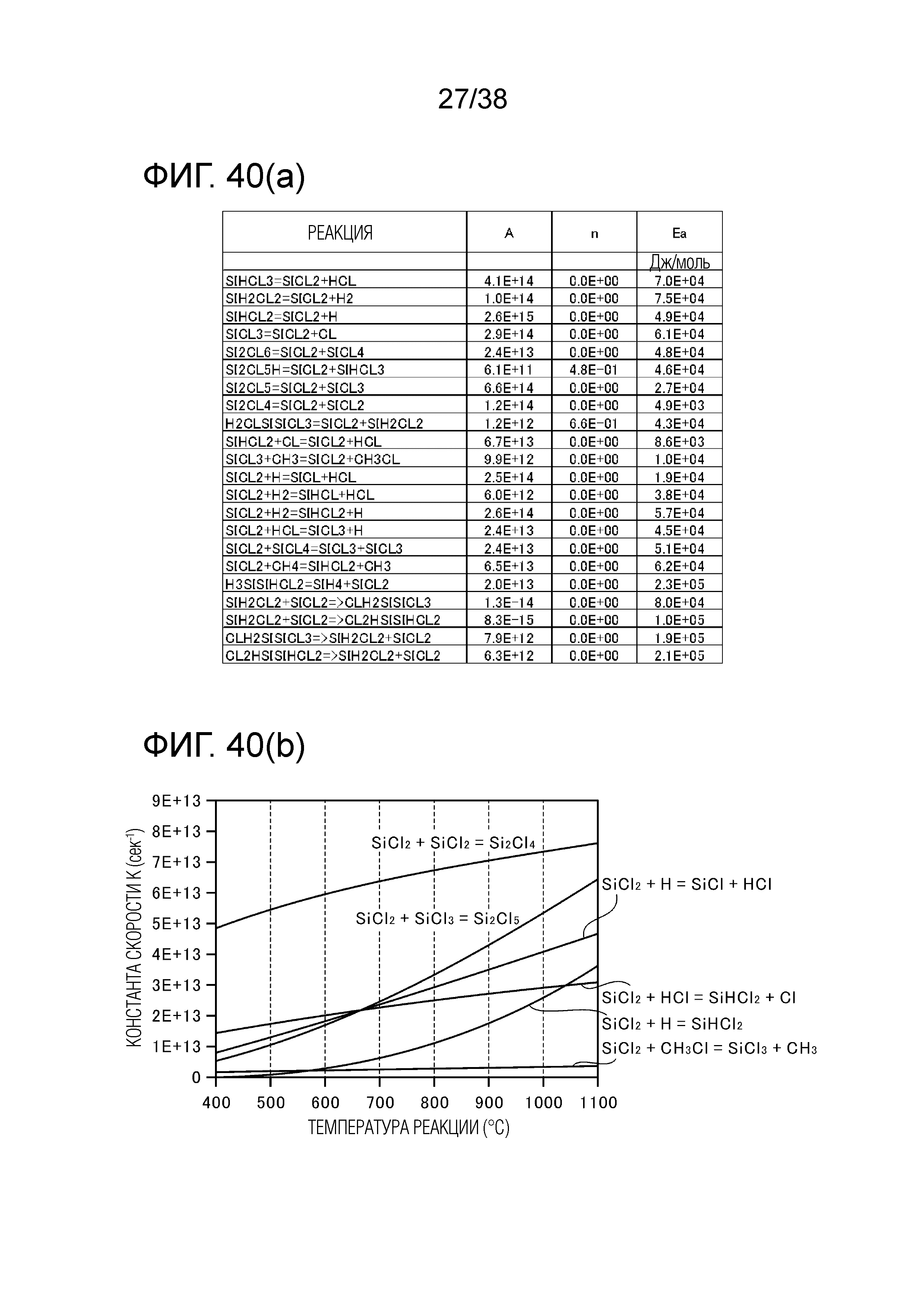
Фиг. 40(a) приводит таблицу, показывающую примеры элементарных реакций, относящихся к SiCl2, и их константы.
Фиг. 40(b) является графиком, сравнивающим константы скоростей элементарных реакций, перечисленных как возможные.
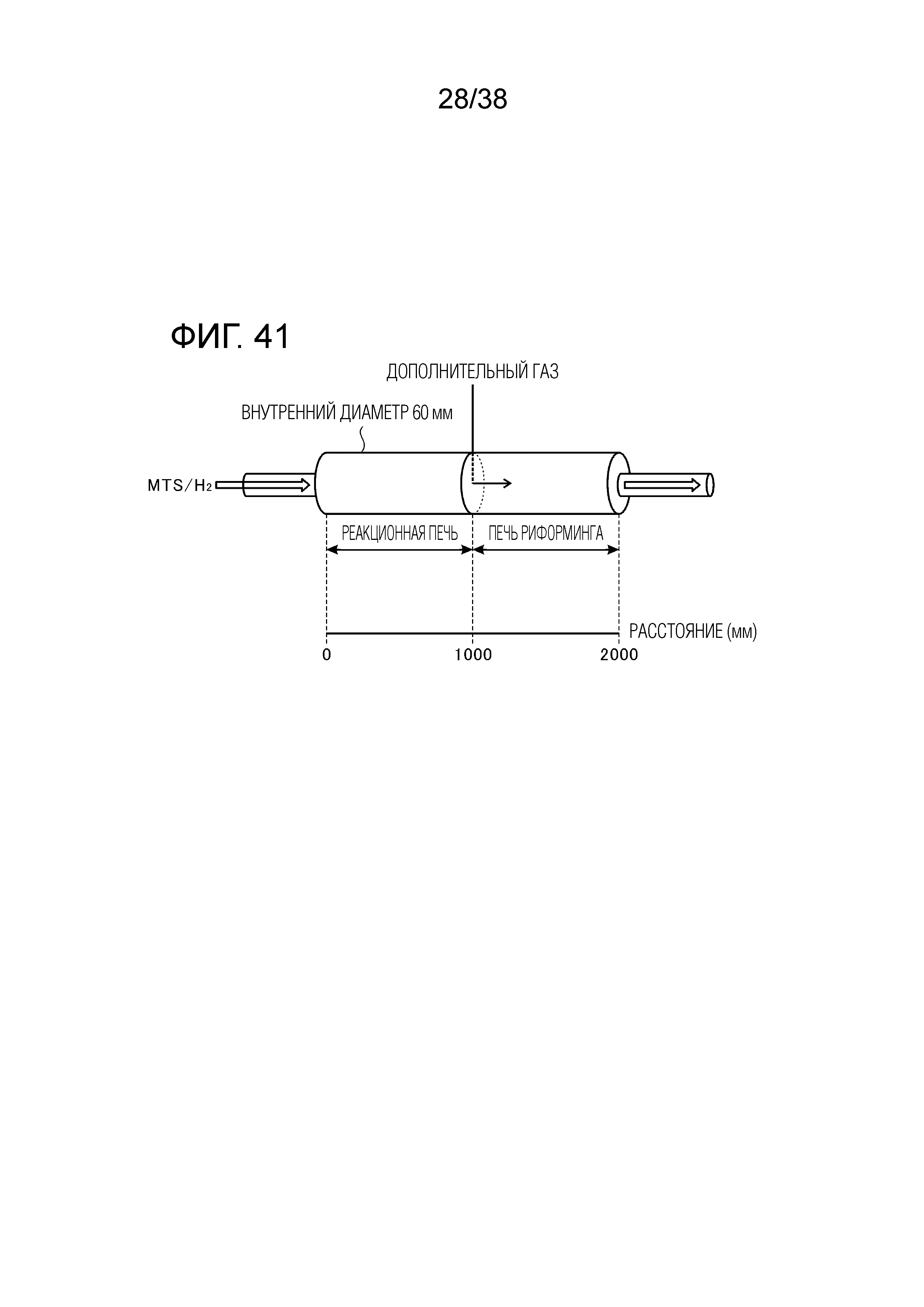
Фиг. 41 иллюстрирует условия моделирования.
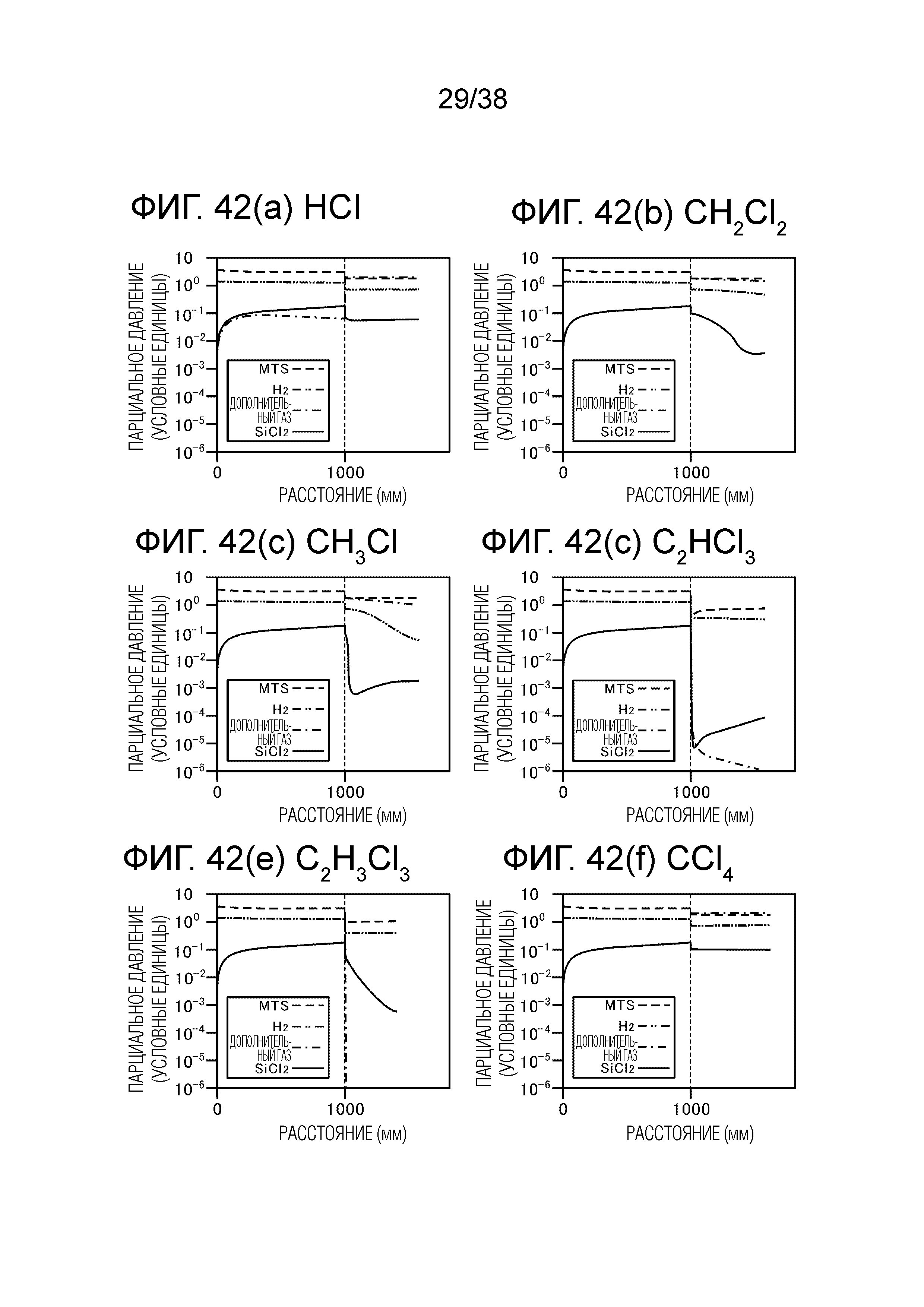
Фиг. 42(a) является графиком, показывающим результаты моделирования в случае добавления HCl в качестве дополнительного газа.
Фиг. 42(b) является графиком, показывающим результаты моделирования в случае добавления CH2Cl2 в качестве дополнительного газа.
Фиг. 42(c) является графиком, показывающим результаты моделирования в случае добавления CH3Cl в качестве дополнительного газа.
Фиг. 42(d) является графиком, показывающим результаты моделирования в случае добавления C2HCl3 в качестве дополнительного газа.
Фиг. 42(e) является графиком, показывающим результаты моделирования в случае добавления C2H3Cl3 в качестве дополнительного газа.
Фиг. 42(f) является графиком, показывающим результаты моделирования в случае добавления CCl4 в качестве дополнительного газа.
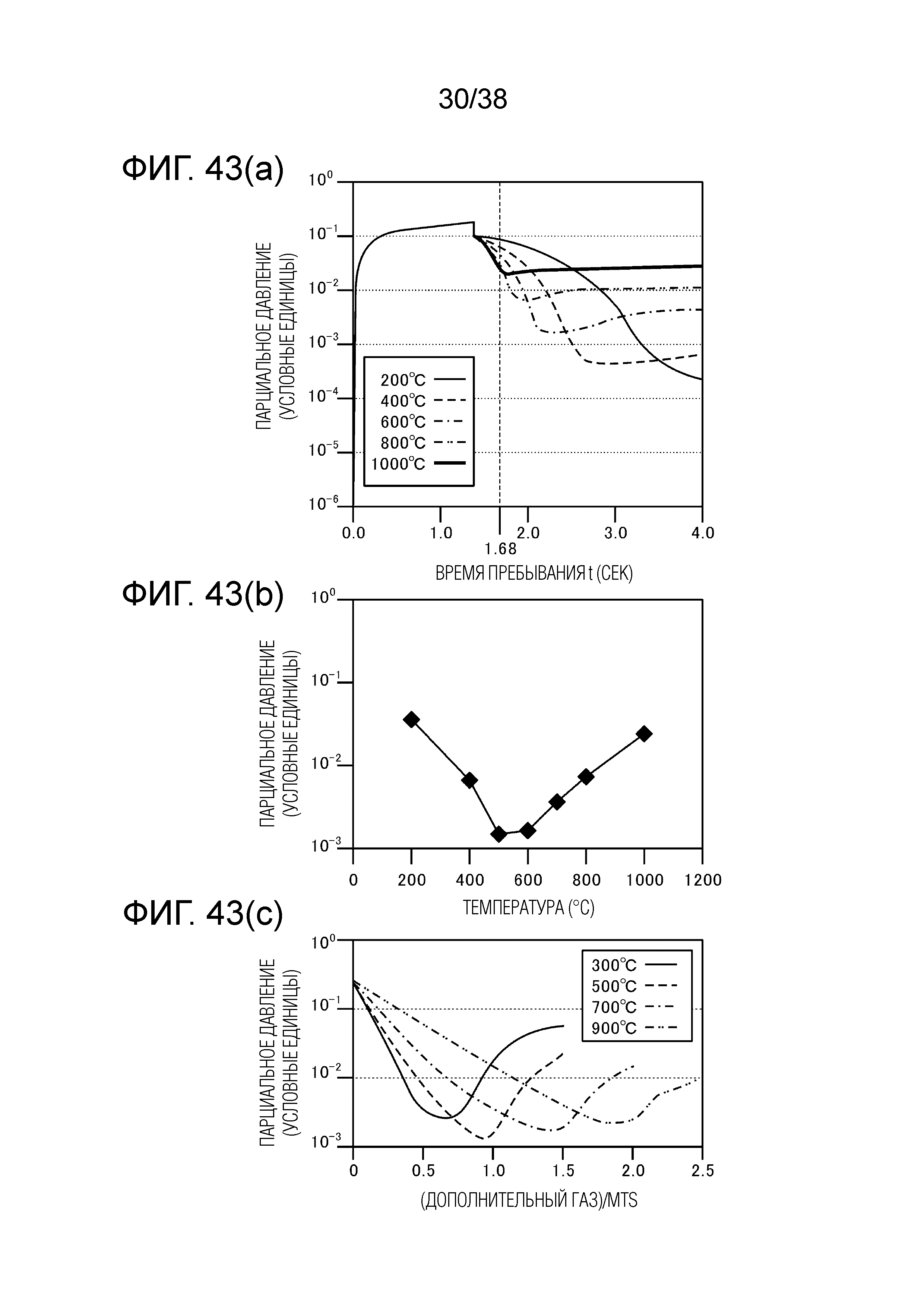
Фиг. 43(a) является графиком, показывающим изменение парциального давления SiCl2 в зависимости от времени пребывания при разных температурах в случае использования CH2Cl2 в качестве дополнительного газа.
Фиг. 43(b) является графиком, показывающим парциальное давление SiCl2 на выходе печи риформинга.
Фиг. 43(c) является графиком, показывающим изменение парциального давления SiCl2 в зависимости от отношения расходов дополнительного газа и MTS при разных температурах.
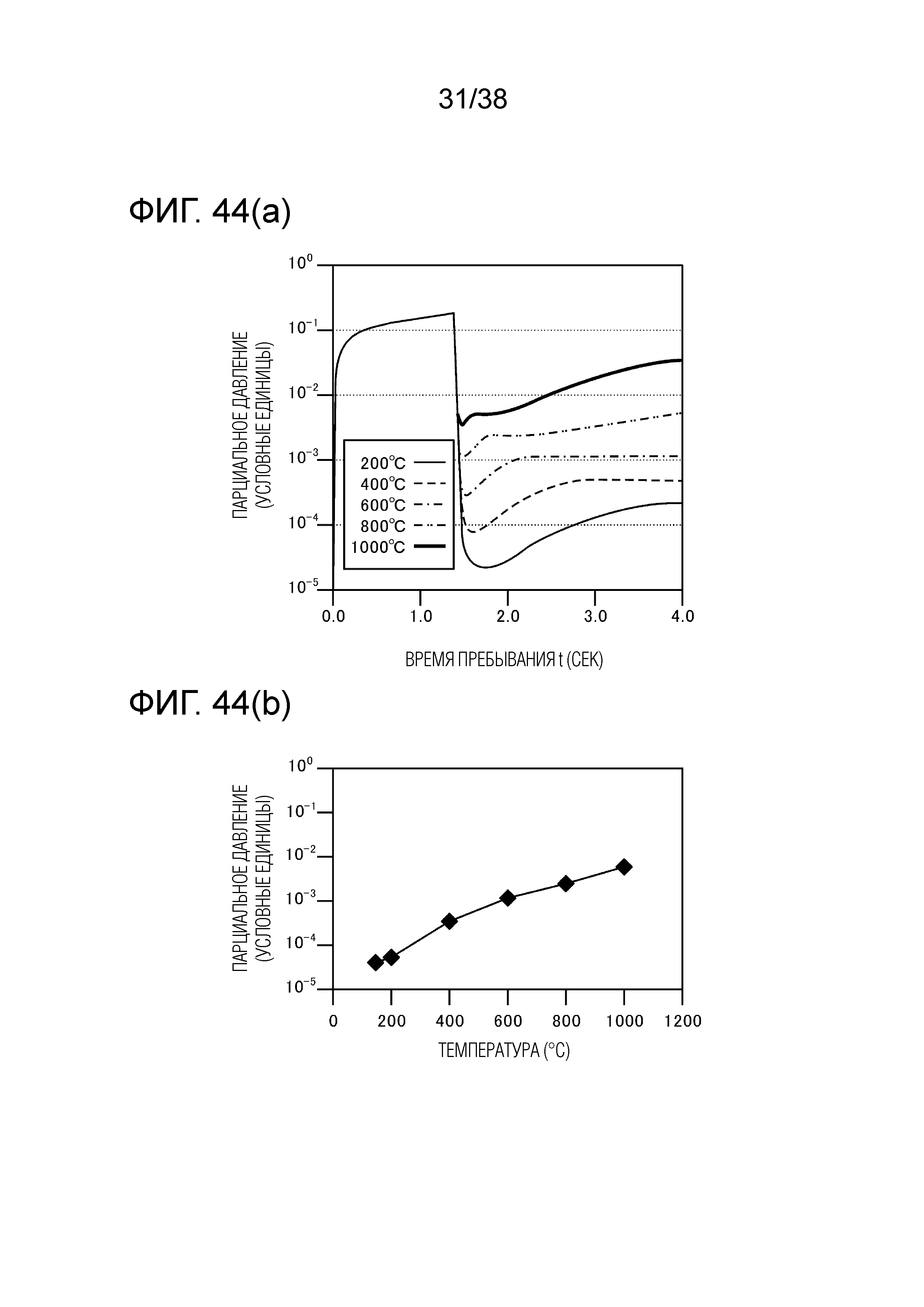
Фиг. 44(a) является графиком, показывающим изменение парциального давления SiCl2 в зависимости от времени пребывания при разных температурах в случае использования CH3Cl в качестве дополнительного газа.
Фиг. 44(b) является графиком, показывающим парциальное давление SiCl2 на выходе печи риформинга.
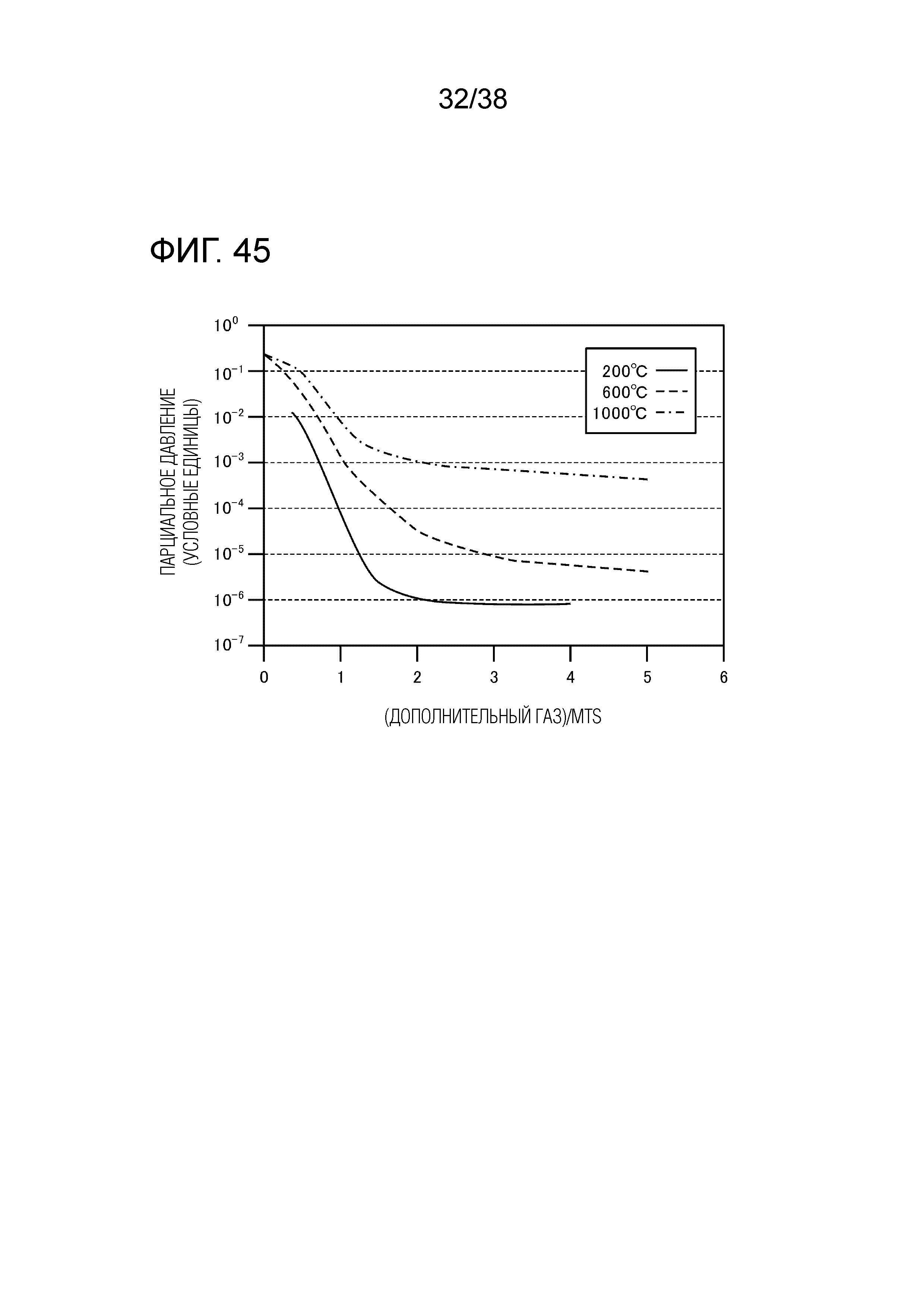
Фиг. 45 является графиком, показывающим парциальное давление SiCl2 при изменении количества добавленного CH3Cl, использующегося в качестве дополнительного газа.
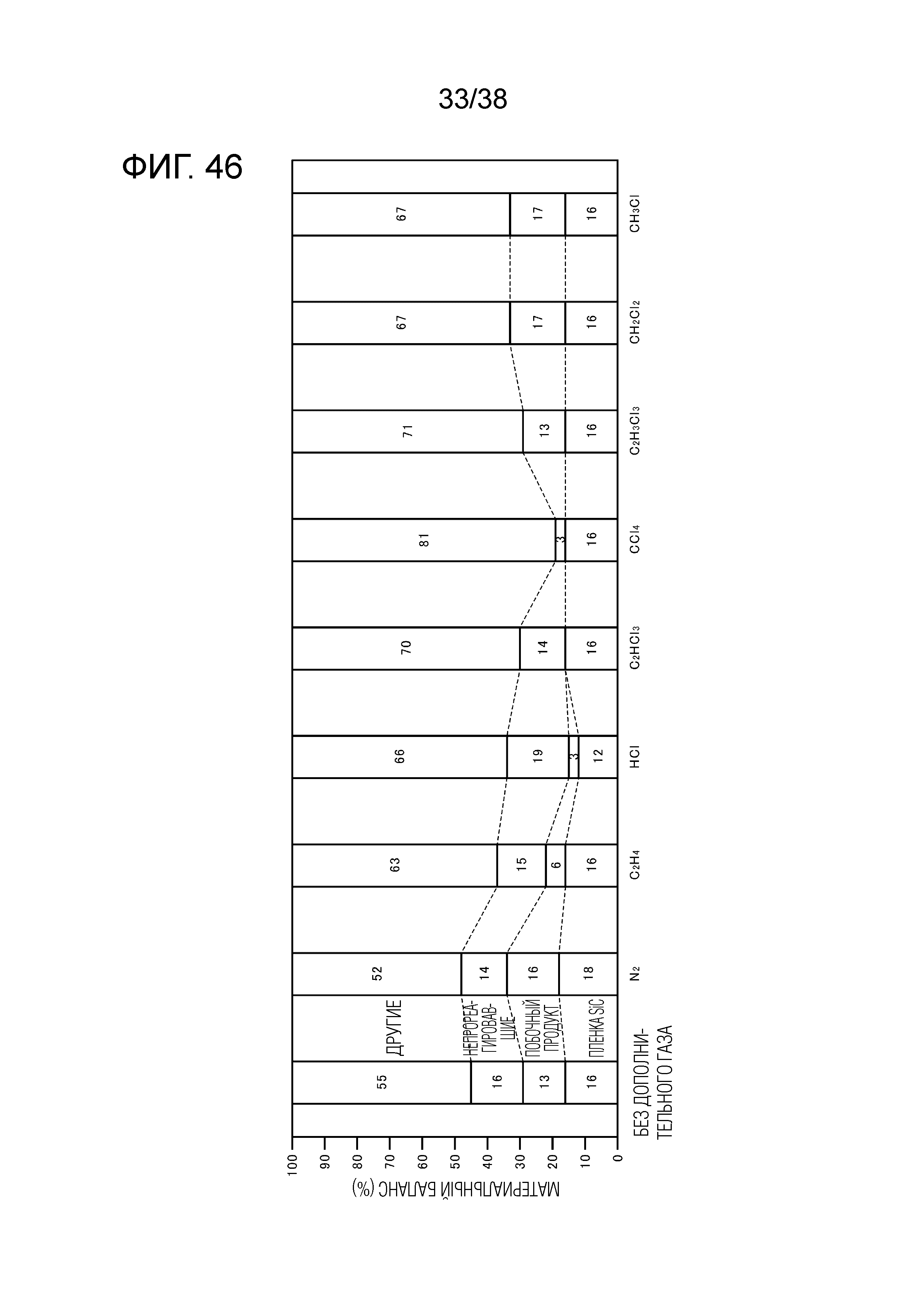
Фиг. 46 является графиком, показывающим материальный баланс, рассчитанный для примера 4.
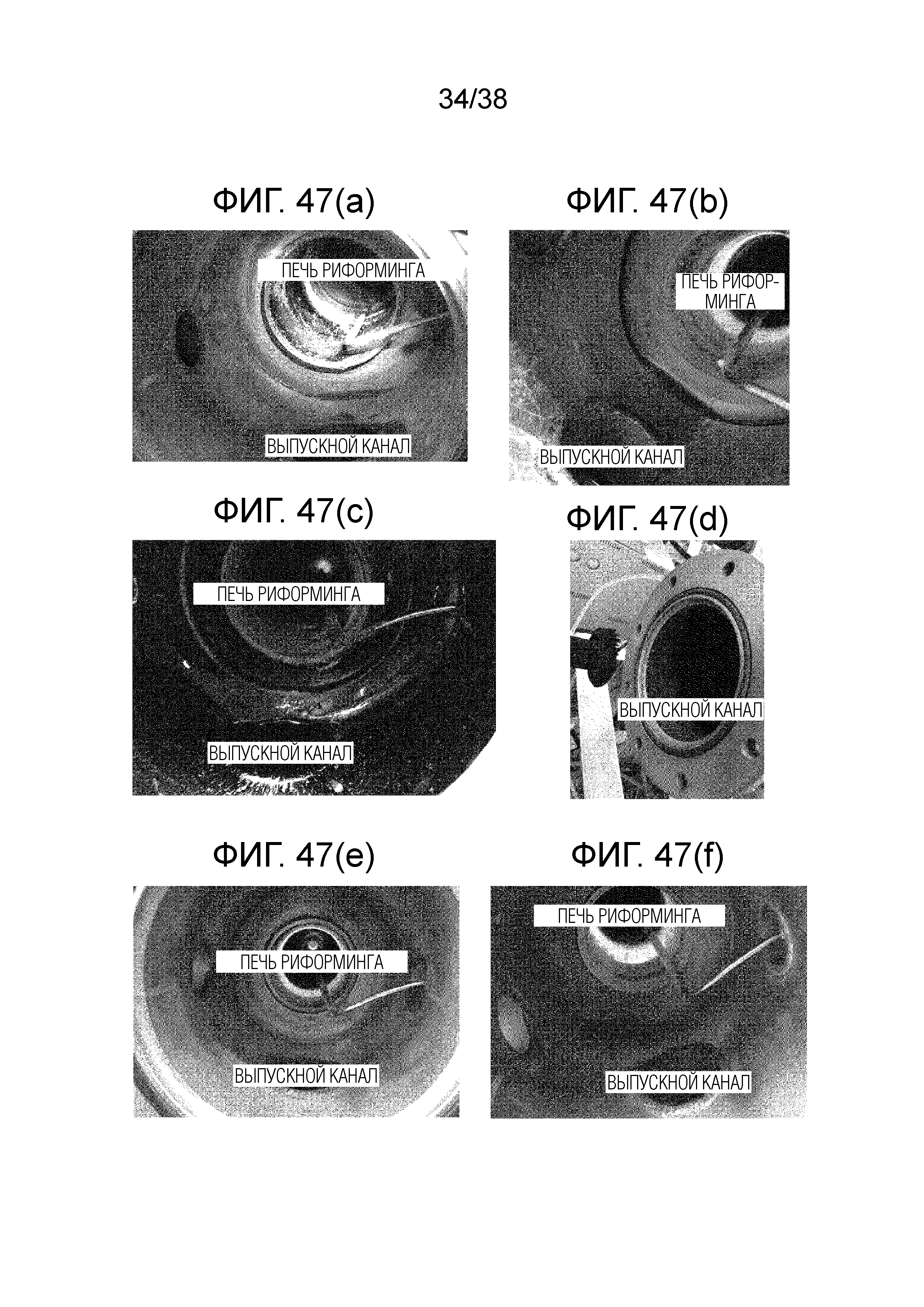
Фиг. 47(a) показывает фотографию для случая без добавления дополнительного газа.
Фиг. 47(b) показывает фотографию для случая добавления HCl в качестве дополнительного газа.
Фиг. 47(c) показывает фотографию для случая добавления C2HCl3 в качестве дополнительного газа.
Фиг. 47(d) показывает фотографию для случая добавления CCl4 в качестве дополнительного газа.
Фиг. 47(e) показывает фотографию для случая добавления CH3Cl в качестве дополнительного газа.
Фиг. 47(f) показывает фотографию для случая добавления CH2Cl2 в качестве дополнительного газа.
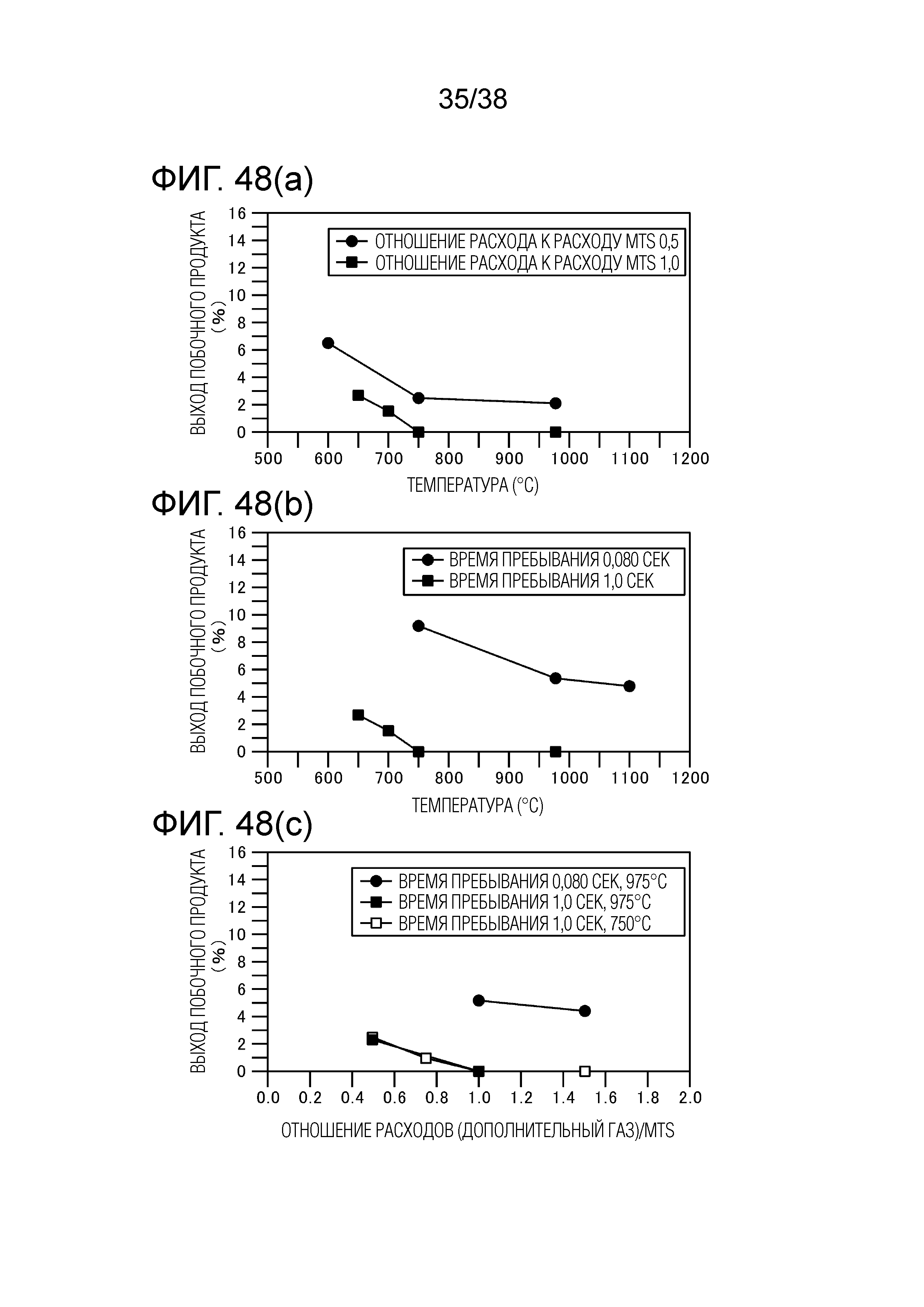
Фиг. 48(a) является графиком, показывающим связь между добавленным количеством CH3Cl, температурой печи риформинга и выходом побочного продукта.
Фиг. 48(b) является графиком, показывающим связь между временем пребывания CH3Cl, температурой печи риформинга и выходом побочного продукта.
Фиг. 48(c) является графиком, показывающим связь между временем пребывания CH3Cl, температурой печи риформинга и выходом побочного продукта.
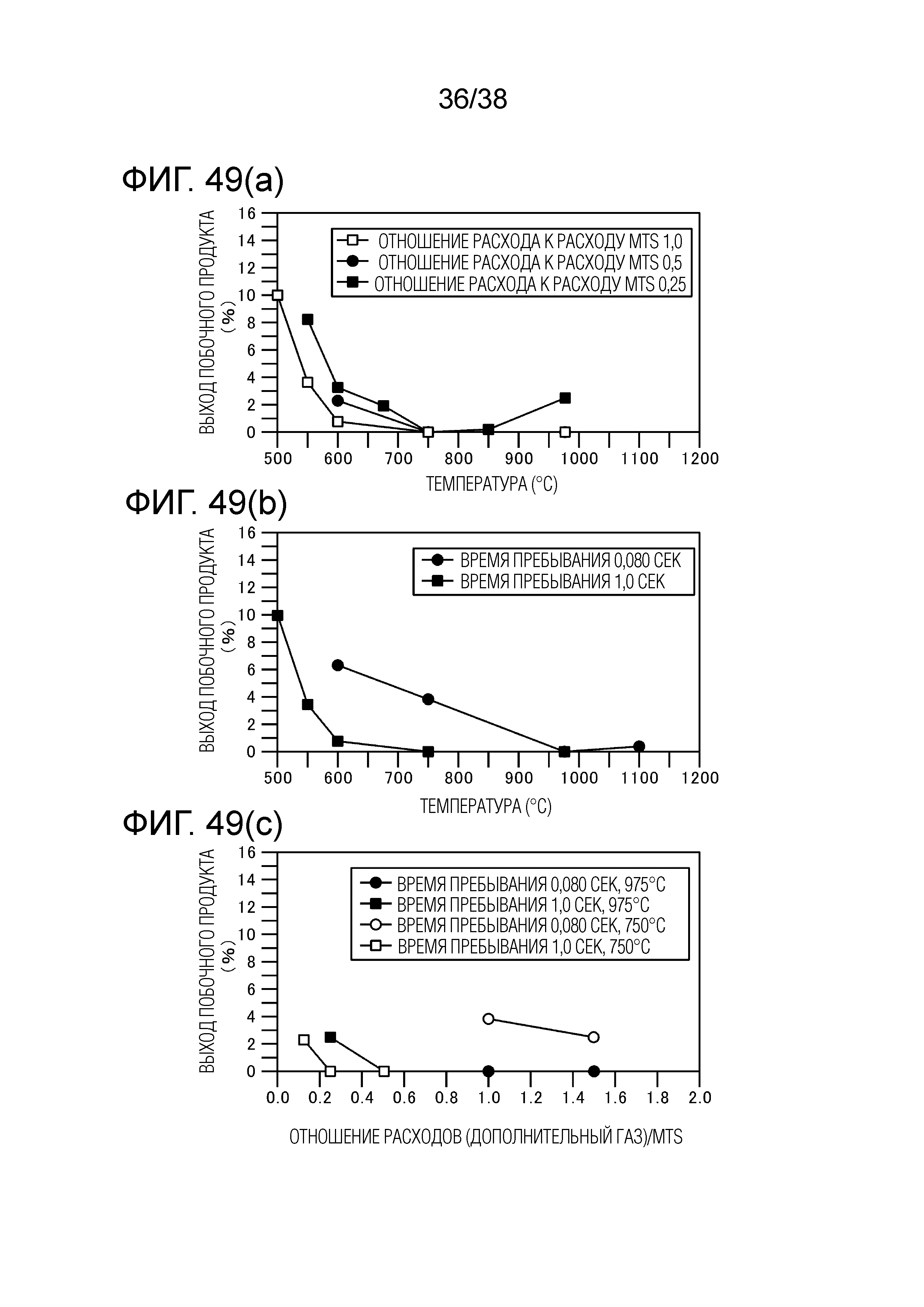
Фиг. 49(a) является графиком, показывающим связь между добавленным количеством CH2Cl2, температурой печи риформинга и выходом побочного продукта.
Фиг. 49(b) является графиком, показывающим взаимосвязь времени пребывания CH2Cl2, температурой печи риформинга и выходом побочного продукта.
Фиг. 49(c) является графиком, показывающим взаимосвязь времени пребывания CH2Cl2, температурой печи риформинга и выходом побочного продукта.
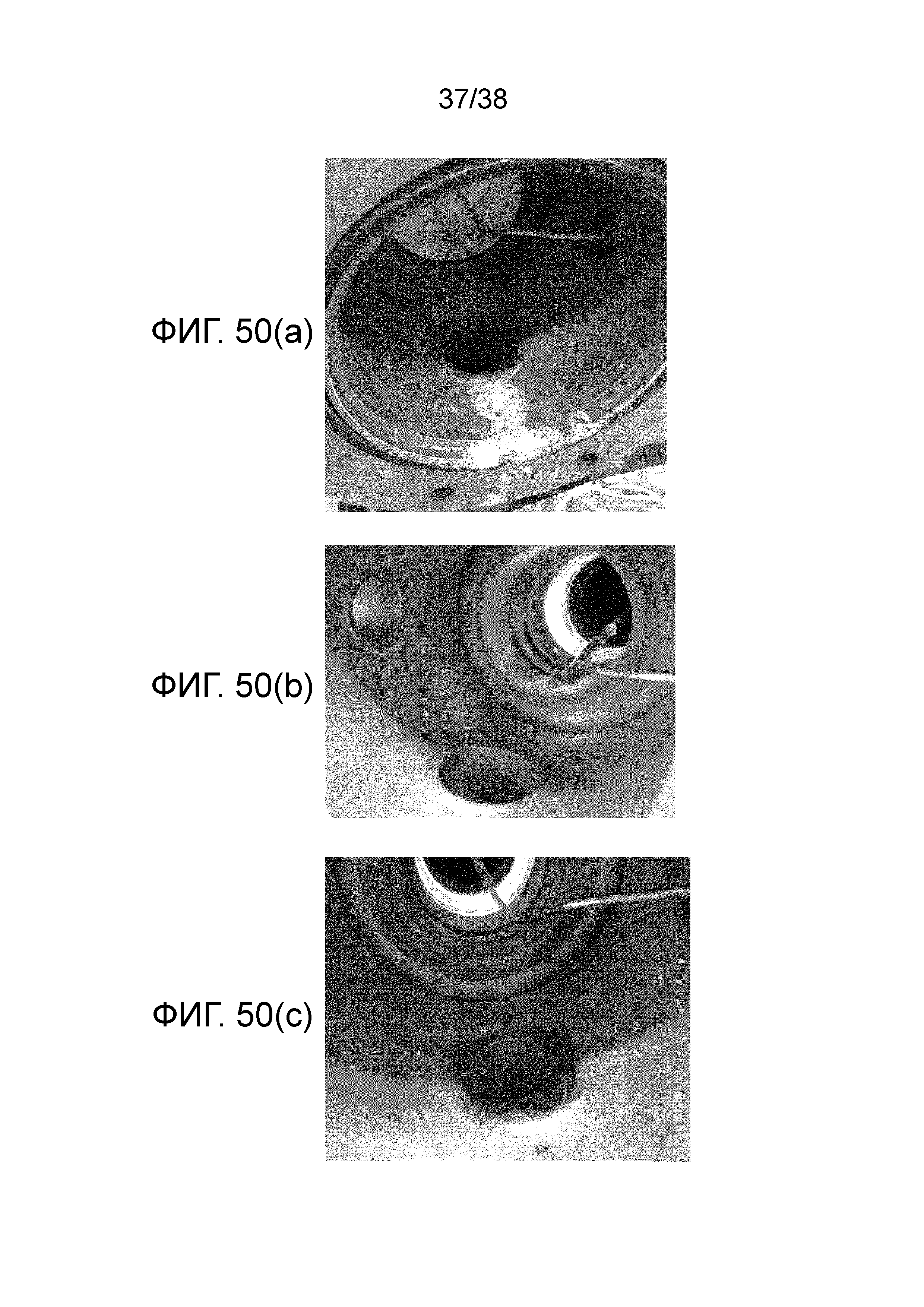
Фиг. 50(a) показывает фотографию для случая без добавления дополнительного газа.
Фиг. 50(b) показывает фотографию для случая добавления CH3Cl в качестве дополнительного газа.
Фиг. 50(c) показывает фотографию для случая добавления CH2Cl2 в качестве дополнительного газа.
Фиг. 51 иллюстрирует устройство для получения кремниевого композиционного материала в соответствии с одним вариантом осуществления настоящего изобретения.
Фиг. 52 иллюстрирует пример модифицированной печи риформинга.
Описание вариантов осуществления
Далее с обращением к прилагаемым чертежам подробнее описывается один вариант осуществления настоящего изобретения. Размеры, материалы и другие конкретные числовые значения в этом варианте осуществления являются просто примерами, использующимися для облегчения понимания настоящего изобретения, и, если не указано иное, не ограничивают изобретение. Компоненты, имеющие по существу одинаковые функции и форму, обозначены одинаковыми позициями в описании и на чертежах, чтобы избежать излишнего описания. Кроме того, иллюстрации компонентов, не имеющих прямого отношения к настоящему изобретению, опущены.
Ниже с обращением к чертежам подробно описываются способ получения кремниевого композиционного материала и устройство для получения кремниевого композиционного материала в одном варианте осуществления настоящего изобретения. В этом варианте осуществления в качестве кремниевого композиционного материала предполагается получение композита с керамической матрицей на основе карбида кремния с использованием карбида кремния как для преформы, так и для матрицы.
Расчет реакции снижения образования побочного продукта
Реакция образования побочного продукта анализируется с использованием реакционного механизма, основанного на квантово-химических расчетах, анализируются также реакционные условия для уменьшения количества образованного побочного продукта и для полного избавления от побочного продукта.
Считается, что предшественником побочного продукта, образуемого из газовой смеси метилтрихлорсилана и газообразного водорода (иногда обозначаемой ниже "MTS/H2"), является SiCl2, и побочный продукт образуется в результате полимеризации SiCl2 (смотри непатентный документ 1). Примеры детального исследования молекулярного веса, структуры и других характеристик побочного продукта в системе MTS/H2 отсутствуют, но подробно изучалась смешанная газовая система из трихлорсилана и газообразного водорода (ниже иногда обозначаемая "SiHCl3/H2") (смотри непатентный документ 2). Сообщалось, что побочный продукт в смешанной газовой системе SiHCl3/H2 содержит SinCl2n+2 и (SiCl2)n (n=3-6). Предполагается, что в побочном продукте в смешанной газовой системе MTS/H2, в которой, как и в системе SiHCl3/H2, образуется SiCl2, также будет образовываться SinCl2n+2 или (SiCl2)n. Исходя из сказанного выше, в данном варианте осуществления рассматривается система (SiCl2)n, как показано на фиг. 2.
В данном варианте осуществления предложены три следующих способа снижения образования побочного продукта, показанные на фигурах 3-5. Их детали подробнее описаны ниже.
1) Как показано на фиг. 3, отходящий газ поддерживается при температуре примерно 600°C (от 500°C или выше, но ниже 950°C) в печи риформинга.
2) Как показано на фиг. 4, на выходе реакционной печи добавляют по меньшей мере один из следующих газов: N2, H2, HCl, CH3Cl, CCl4, C2HCl3, C2H3Cl3, C2H4, C2H6O, C3H6O, CH4O, H2O, CH2Cl2 или CHCl3.
3) Как показано на фиг. 5, добавляют по меньшей мере один из газов: N2, H2, HCl, CH3Cl, CCl4, C2HCl3, C2H3Cl3, C2H4, C2H6O, C3H6O, CH4O, H2O, CH2Cl2 или CHCl3, и отходящий газ поддерживается в печи риформинга при температуре, больше или равной 200°C, но меньше 1100°C.
Разработка механизма реакции побочного продукта
Хотя SinCl2n+2 и (SiCl2)n многие годы считались проблемными, термодинамические данные побочного продукта и данные о скорости реакции образования побочного продукта и т.д. отсутствуют. Термодинамические данные по SinCl2n+2 и (SiCl2)n (n≥3) и их константы скорости реакции образования определяли путем квантово-химических расчетов. Для расчетов молекулярной структуры, энергии и частоты использовали пакет программ Gaussian 09D (смотри непатентный документ 3) на уровне CBS-QB3//B3LYP/CBSB7. Константы скоростей реакции были рассчитаны с использованием программ GPOP (смотри непатентный документ 4) и SSUMSE (смотри непатентный документ 5).
Изменение свободной энергии из-за полимеризации SiCl2 показано на фигурах 6(a) и 6(b). В случаях линейной полимеризации, показанной на фиг. 6(a), SiCl2 в несвязанном состоянии имеет более низкую свободную энергию и является более стабильным при температуре 1100K или выше, а SiCl2 в полимеризованном состоянии имеет более низкую свободную энергию и постепенно становится стабильным при температурах 1100 K или ниже. Между тем, в случаях циклической полимеризации, показанных на фиг. 6(b), SiCl2 имеет самую высокую свободную энергию и наиболее нестабилен при определенной степени полимеризация, и имеет более низкую свободную энергию и становится более стабильным с повышением степени полимеризации. Степень полимеризации и свободная энергия, при которых SiCl2 является наиболее нестабильным, меняются с температурой.
Энергия реакции и энергетический барьер реакции между SiCl2 и другой молекулой при 0K показаны на фиг. 7 (смотри непатентные документы 1 и 2). Если сравнить вариант, в котором SiCl2 следует маршруту реакции, показанному в правой части фиг. 7, где SiCl2 реагирует с другой молекулой SiCl2, превращаясь в Si2Cl4 (Cl2SiSiCl2, Cl3SiSiCl), и вариант, в котором SiCl2 следует маршруту реакции, показанному в левой части фиг. 7, где SiCl2 реагирует с H2, HCl и т.д., то видно, что продукт реакции между двумя молекулами SiCl2 имеет более высокую энергию и является более нестабильным, чем любой из продуктов реакции в левой части. Однако, если сравнить энергетические барьеры реакции SiCl2 и этих продуктов, то все продукты в левой части, за исключением варианта с бутадиеном, имеют барьер не ниже 50 кДж/моль, при этом барьер для образования Si2Cl4 является низким по сравнению с исходным SiCl2 и ниже, чем барьеры для продуктов в левой части.
Из вышеуказанных результатов следует, что когда температуру SiCl2, который стабилен при высокой температуре, снижают со значения больше или равного 1000°C и поддерживают при определенной температуре, SiCl2 превращается в основном в Si2Cl4, который имеет низкий энергетический барьер реакции. Однако, сам Si2Cl4 нестабилен по сравнению с SiHCl3 или SiH2Cl2 и, следовательно, со временем ожидается реакция, в которой Si2Cl4 превращается в SiHCl3 или SiH2Cl2.
Маршрут реакции из SiCl2 в (SiCl2)3 при 0K показан на фиг. 8. Каждый продукт на маршруте из SiCl2 в (SiCl2)3 имеет низкую энергию и низкий энергетический барьер реакции по отношению к SiCl2, и поэтому ожидается, что SiCl2 будет легче превращаться в (SiCl2)3 при 0K. Исходя из этих энергетических маршрутов, можно рассчитать константу скорости реакции полимеризации SiCl2.
Предсказание особенностей реакции образования побочных продуктов
Рассмотренный выше механизм реакции был введен в механизм реакции MTS/H2. Расчет реакции осуществляли, используя указанный механизм реакции и программу CHEMKIN (смотри непатентный документ 6). Чтобы понять особенности SiCl2, сначала рассматривали газовую смесь SiHCl3/H2. В качестве распределения температуры использовали распределение, показанное в верхней части фиг. 9. Распределение температуры соответствует распределению в золотоплавильной печи, фактически использовавшейся в качестве реакционной печи, и температура резко снижается на стороне выхода. Расчет реакции осуществляли в условиях, в которых газовая смесь SiHCl3/H2 течет в поршневом режиме в цилиндрической трубе с внутренним диаметром 16 мм в условиях отношения парциальных давлений газов SiHCl3 и H2 1:37 (при пониженном давлении) и расхода 1,08 стандартных л/мин.
Изменение мольной доли газа показано в нижней части фиг. 9. Как показано на фиг. 9, ожидается, что высший хлорсилан (SiCl2)n, который считается одним из побочных продуктов, будет образовываться в ходе снижения температуры, а не в режиме томления при примерно 900°C в печи для реакции CVI. При этом ожидается, что температура образования побочного продукта ниже 600°C. Изображение бомбы на фиг. 9 указывает, что высший хлорсилан может стать взрывоопасным веществом при окислении в контакте с атмосферой. Это же используется и ниже.
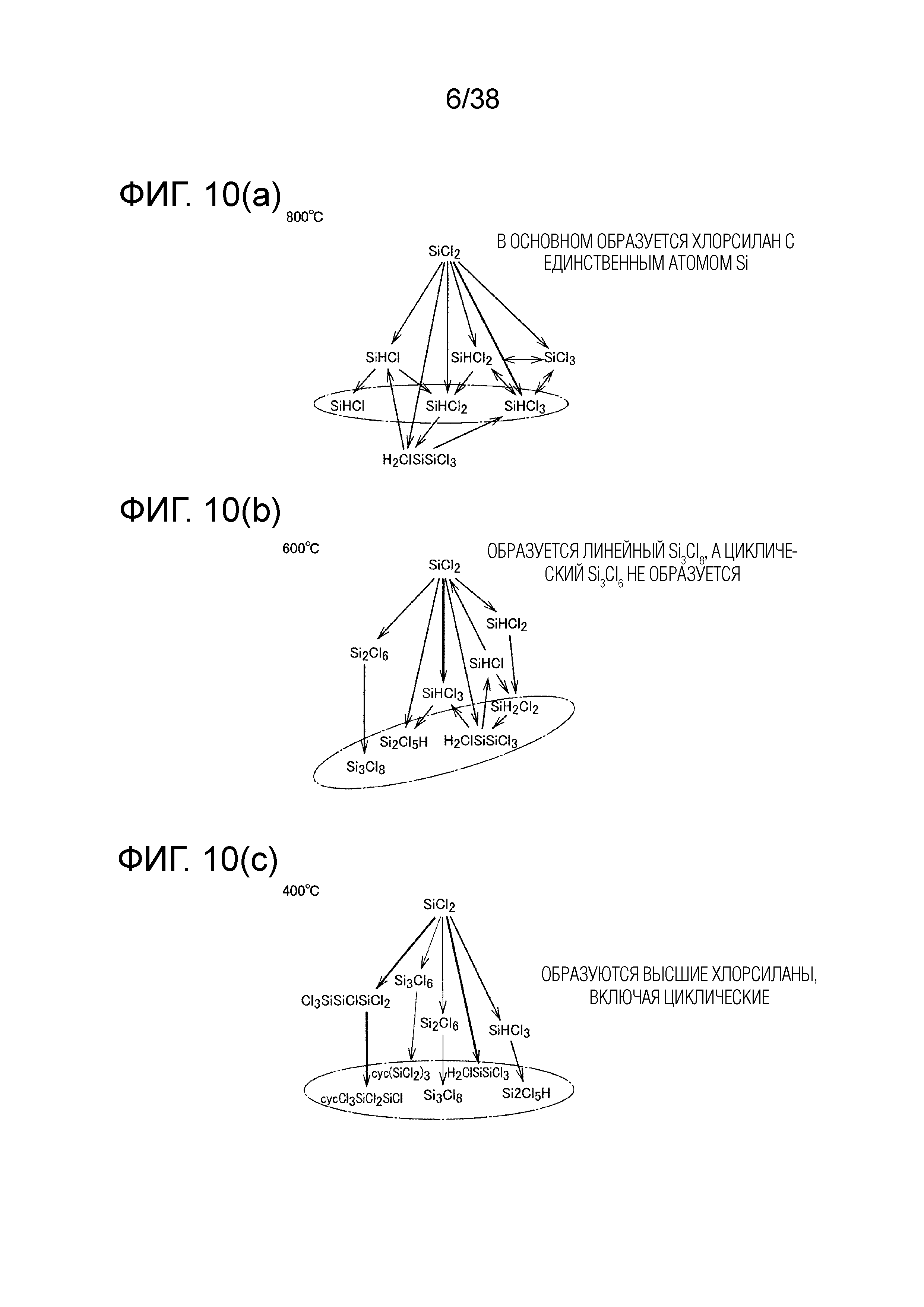
Основная реакция SiCl2, протекающая при температурах от 400°C до 800°C в ходе снижения температуры с фиг. 9, показана на фигурах 10(a), 10(b) и 10(c). При этих температурах идет следующая реакция (смотри непатентный документ 1):
линейный SinCl2n+2 → SiCl4+(n-1)SiCl2
Как показано на фиг. 10(a), при 800°C полимеризация не идет, и образуется мономерная молекула, содержащая единственный атом Si. Когда температура снижается до 600°C, то, как показано на фиг. 10(b), образуется линейное соединение SiCl. Когда температура падает до 400°C, то, как показано на фиг. 10(c), образуется циклическое соединение.
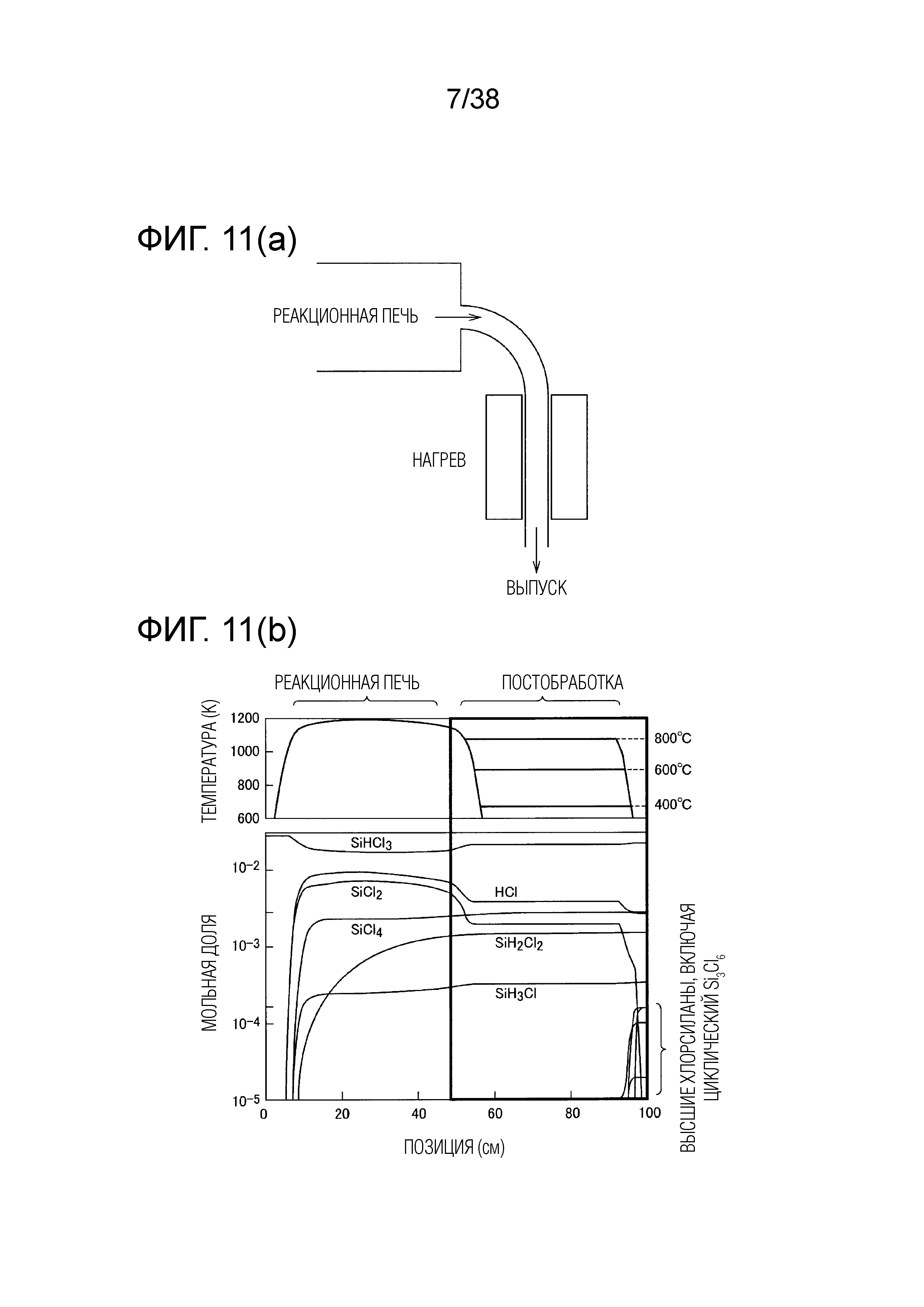
Как правило, на эксперименте в процессе CVD с использованием смеси SiHCl3/H2 количество побочного продукта снижают, нагревая выпускную трубу. Поэтому был проведен расчет для случая, когда температура терморазлагаемой газовой смеси SiHCl3/H2 поддерживается со стороны выпуска. Фиг. 11(a) и фиг. 11(b) соответствуют примеру, когда температура поддерживается на уровне 800°C. На фиг. 11(a) показана конфигурация на стороне выпуска, где для постобработки на стадии, следующей за реакционной печью, предусмотрена печь риформинга. Распределение температуры и содержания высших хлорсиланов показаны на фиг. 11(b).
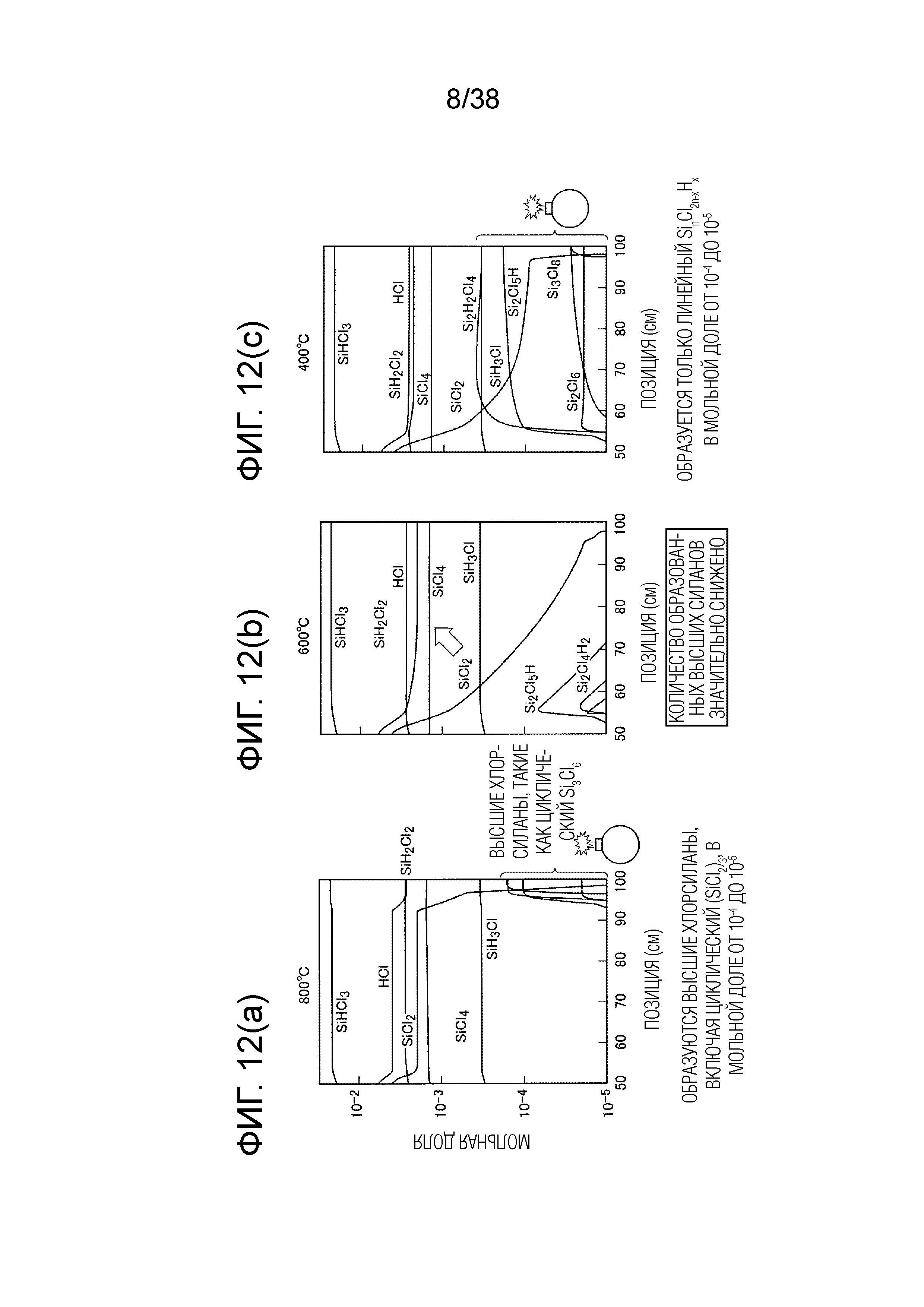
Результаты расчета реакции для разных температур поддерживания: 800°C, 600°C и 400°C, показаны на фигурах 12(a), 12(b) и 12(c), соответственно. Каждая из фигур 12(a), 12(b) и 12(c) соответствует стадии постобработки в условиях фиг. 11(a) и фиг. 11(b). Как показано на фиг. 12(a), при 800°C SiCl2 является стабильным из-за высокой температуры, таким образом, SiCl2 не вступает в реакцию, но в конечном счете превращается в побочный продукт при охлаждении. Напротив, при 400°C, как показано на фиг. 12(c), побочный продукт является стабильным вследствие низкой температуры, поэтому SiCl2 становится побочным продуктом. При 600°C, как показано на фиг. 12(b), SiHCl3 образуется по нижеследующей реакции, предположительно потому, что и SiCl2, и побочный продукт являются нестабильными, а SiHCl3 является стабильным.
SiCl2+HCl → SiHCl3
Из вышеуказанных результатов можно ожидать, что температура около 600°C подходит для превращения SiCl2 в SiHCl3, который является энергетически стабильным.
Расчет реакции снижения образования побочного продукта без добавления газа
Чтобы проанализировать условия снижения образования SiCl2 для газовой смеси MTS/H2, расчет реакции проводили аналогичным образом. Расчетные условия были следующими: отношение парциальных давлений MTS, H2 и He 2:5:18 (при пониженном давлении), внутренний диаметр 16 мм и суммарный расход 100 стандартных кубических сантиметров в минуту (sccm). Результат для прямого снижения температуры показан на фиг. 13. Считается, что, как и в системе SiHCl3/H2, образуются высшие хлорсиланы.
Предполагается, что остаточное количество SiCl2 напрямую связано с количеством образованных высших хлорсиланов, поэтому рассматривается только остаточный уровень SiCl2. Изменение остаточного уровня SiCl2 при изменении температуры поддерживания отходящего газа в интервале от 500°C до 750°C показано на фиг. 14. Когда отходящий газ поддерживается при температуре от 700°C до 750°C, скорость уменьшения содержания SiCl2 является высокой, но SiCl2 остается в большем количестве. Между тем, когда отходящий газ поддерживается при температуре ниже 600°C и подвергается реакции в течение достаточного времени, остаточный уровень значительно снижается, но скорость снижения становится меньше. Например, тогда как количество SiCl2 снижается быстрее всего при обработке при 700°C с остаточным уровнем SiCl2 около 10%, количество SiCl2 снижается быстрее всего при обработке при 650°C с остаточным уровнем SiCl2 около 1%. Таким образом, можно полагать, что если температуру обработки SiCl2 постепенно снизить с 700°C или выше, продолжительность обработки уменьшится, и объем печи риформинга, требуемый для обработки, уменьшится по сравнению со случаем поддержания постоянной температуры.
На фиг. 14 скорость уменьшения количества SiCl2 при каждой температуре определена из следующего уравнения
В этом уравнении C означает концентрацию SiCl2, а t означает время пребывания (сек). Фиг. 15 является графиком, показывающим кривые зависимости kSiCl2 для разных температур от остаточного уровня (%) SiCl2 (C/C0). Как можно видеть из фиг. 15, когда, например, остаточный уровень SiCl2 больше или равен 15%, максимальное значение kSiCl2 достигается при температуре поддерживания 750°C, но когда остаточный уровень SiCl2 составляет от 9% до 15%, максимальное значение kSiCl2 достигается при температуре поддерживания 700°C. Таким образом, ожидается, что температура достижения максимального значения kSiCl2 снижается при снижении остаточного уровня SiCl2.
Соответственно, когда температура отходящего газа контролируется так, чтобы достигалась максимальная константа скорости kSiCl2 в соответствии с остаточным уровнем SiCl2, этот остаточный уровень SiCl2 может снижаться быстрее всего, а значит, можно уменьшить образование жидкого побочного продукта. Другими словами, когда температуру отходящего газа контролируют и снижают с заданной скоростью, подвергая отходящий газ непрерывному изменению температуры во времени, скорость уменьшения остаточного уровня SiCl2 можно повысить. Для этого температуру отходящего газа устанавливают следующим образом: температуру отходящего газа постепенно и непрерывно снижают с 700°C так, чтобы можно было получить непрерывную кривую снижения температуры. Можно также подобрать кривую снижения температуры, в соответствии с которой температура отходящего газа надлежащим образом снижается ступенчато до нескольких дискретных значений температуры. Кроме того, жидкий побочный продукт иногда становится твердым, когда его приводят в контакт с другим веществом (например, кислородом) в окружающей среде. Ниже жидкий или твердый побочный продукт иногда называется просто побочным продуктом.
Линию на фиг. 15 получают, придерживаясь максимального значения kSiCl2 при соответствующих остаточных уровнях SiCl2. При этом между kSiCl2 и C/C0 установлено следующее соотношение
Из фиг. 15 следует, что температура, при которой достигается максимум kSiCl2, меняется в зависимости от остаточного уровня. График зависимости максимального значения kSiCl2 от обратной температуры T ((1000/T по абсциссе) показан на фиг. 16. Из фиг. 16 можно вывести следующее уравнение связи между максимумом kSiCl2 и T
где R означает газовую постоянную, равную 8,314 Дж/моль/K.
Если уравнение (2) подставить в уравнение (1), получится следующее уравнение
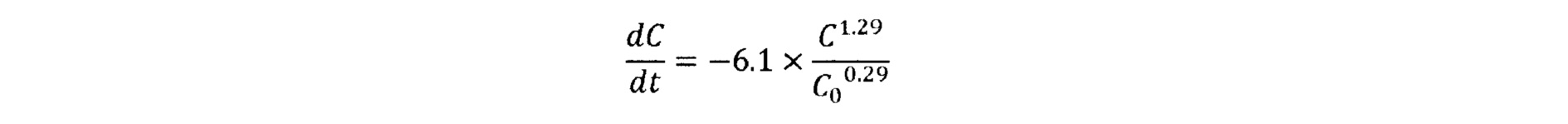
или, эквивалентно
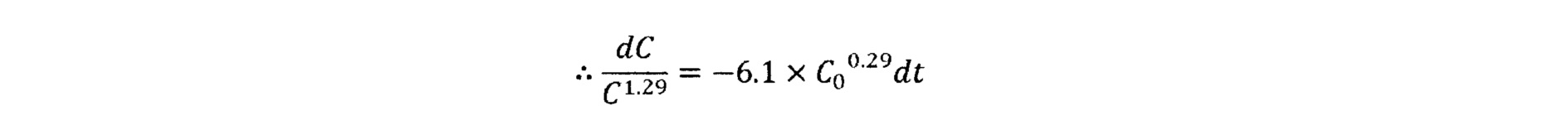
При интегрировании обеих сторон получается следующее уравнение
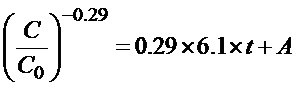
A равно 1, так как C/C0 стремится к 1, когда t стремится к 0, таким образом, получаем уравнение (4).
Если уравнение (4) подставить в уравнение (2) и полученный результат сравнить с уравнением (3), получится следующее уравнение
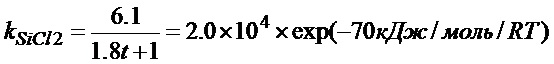
что равносильно
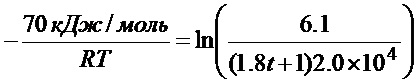
т.е.
Уравнение (5) показывает, как должна изменяться во времени температура отходящего газа для достижения максимума kSiCl2. Если температура отходящего газа изменяется в соответствии с уравнением (5), считается, что остаточный уровень SiCl2 (C/C0) уменьшается согласно уравнению (4). Хотя считается, что числовые коэффициенты в уравнениях (4) и (5) меняются в зависимости от условий отходящего газа, т.к. каждый параметр в уравнении (5) задается процессом, осуществляемым в этой секции, можно полагать, что найденный способ снижения температуры является оптимальным для этих условий.
Первая схема реакции снижения образования побочного продукта с добавлением газа
Было проанализировано, приводит ли добавление в отходящий газ другого газа к снижению количества SiCl2. Были рассмотрены He, H2, HCl и CH3Cl. Кроме того, были рассмотрены также CH2Cl2, CHCl3 и CCl4, которые, как ожидается, оказывают аналогичные эффекты. Расчетные условия проиллюстрированы на фиг. 17.
Описанный выше результат сравнения остаточных уровней SiCl2 в диапазоне 600°C проиллюстрирован на фиг. 18 и фиг. 19. Сравнение варианта без добавления газа и вариантов с добавлением H2, He, HCl и CH3Cl в добавленном количестве 72 sccm показано на фиг. 18. На фиг. 18 сравнение проводится по отношению к отложенной по абсциссе переменной "время пребывания, умноженное на текущий расход". Сравнение вариантов добавления CH3Cl, CH2Cl2, CHCl3 и CCl4 в количестве 22 sccm показано на фиг. 19. На фиг. 19 сравнение проводится по отношению к отложенному по абсциссе времени пребывания, так как во всех случаях расходы газов были одинаковыми. Из фиг. 18 и фиг. 19 следует, что самая высокая скорость уменьшения количества SiCl2 получается при добавлении CH3Cl. He, H2, и HCl вносят меньший вклад в реакцию и, напротив, повышают суммарный расход, что требует дополнительного объема. Это же относится к CH2Cl2, но ожидается, что CHCl3, CCl4 и т.п. вносят вклад в реакцию.
Анализировалась основная реакция SiCl2 при добавлении CH3Cl, результаты расчетов показывают, что количество SiCl2 уменьшалось вследствие следующей радикально-цепной реакции.
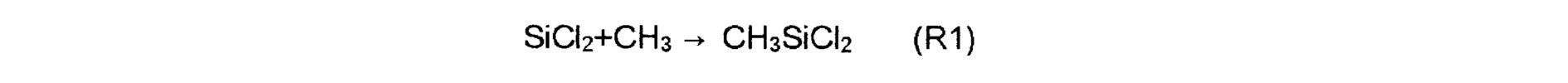
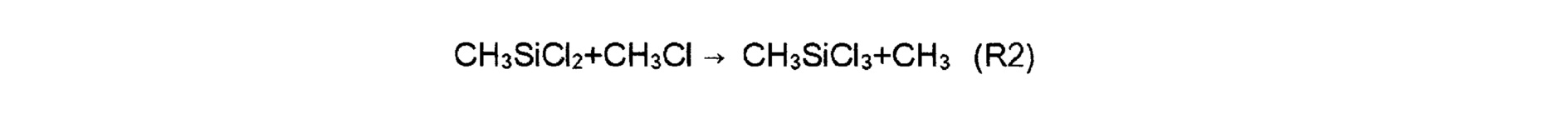
Считается, что SiCl2 может превратиться в CH3SiCl3 при добавлении CH3Cl в диапазоне 600°C. Хотя указывается, что процесс CVI с использованием MTS/H2 имеет низкую конверсию исходного материала, существует возможность, что можно добиться процесса с несколько более высокой конверсией, если позволить CH3Cl и SiCl2 реагировать друг с другом, снова превращая SiCl2 в CH3SiCl3 и собирая CH3SiCl3. Это же относится к случаю добавления CH2Cl2.
Далее, результат расчета для случая добавления газообразного CH4-nCln при 900°C показан на фиг. 20. При этом, когда n увеличивается на единицу, скорость реакции возрастает от 10 или более раз до 100 или более раз. При этом количество SiCl2 резко снижается, в основном в результате следующей реакции
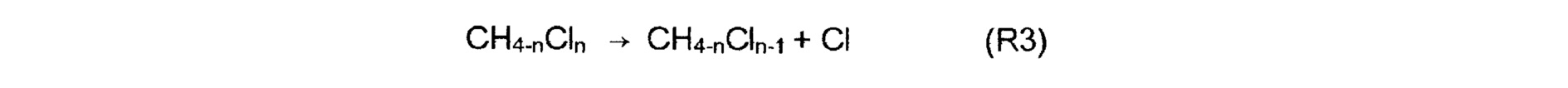
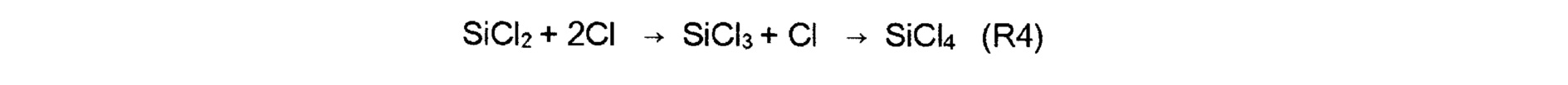
Считается, что скорость, с которой CH4-nCln выделяет радикал Cl, пропорционально зависит от скорости уменьшения количества SiCl2.
Согласно Yang Soo Won (смотри непатентный документ 7), и как видно из фиг. 21, стабильность этих хлорметанов повышается в порядке, указанном ниже.
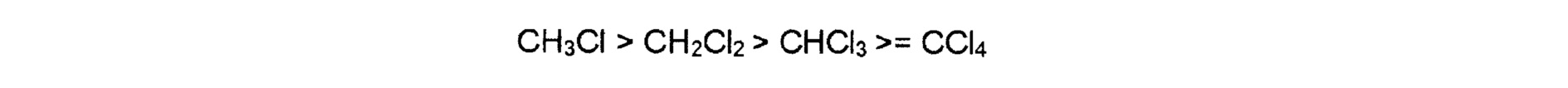
Считается, что вышеуказанный результат вычислений объясняется тем, что CCl4, являющийся наиболее нестабильным, высвобождает радикалы быстрее всех.
На фиг. 22 для случая добавления CH2Cl2 показано изменение парциального давления газообразного вещества, содержащего другие газы. Парциальное давление CH2Cl2 снижается до 1% или ниже от исходного парциального давления за примерно 0,6 сек, и соответственно возрастает парциальное давление C2H2. Ожидается, что избыточный Cl, образующийся в этом случае, реагирует с SiCl2 или H2, образуя SiCl4 или HCl.
Проводилось уточнение оптимальных условий в случае CH3Cl, что дает возможность повторного использования MTS в реакции при 600°C. Во-первых, что касается температуры загрузки CH3Cl, считается, что CH3Cl желательно добавлять, когда температура отходящего газа составляет порядка 600°C, так как при температурах 750°C или выше CH3Cl подвержен термическому разложению, хотя, как видно из фиг. 21, CH3Cl является более стабильным по сравнению с другими CH4-nCln.
Результаты расчетов при изменении расхода CH3Cl показаны на фиг. 23. Когда расход повышается с 7 sccm до 22 sccm, скорость уменьшения количества повышается в соответствии с повышением парциального давления CH3Cl, и объем газа, требующийся для реакции, уменьшается. Однако, когда расход повышается с 22 sccm до 72 sccm, объем газа, требующийся для реакции, напротив, увеличивается из-за повышения расхода. Это указывает, что существует оптимальный расход для исходного отходящего газа, и ожидается, что оптимальный расход будет, вероятно, сопоставим с расходом отходящего газа.
Результат для случая изменения температуры при фиксированном расходе CH3Cl, равном 22 sccm, показан на фиг. 24. Скорость реакции обычно возрастает с повышением температуры, поэтому ожидается, что скорость уменьшения количества SiCl2 будет повышаться с повышением температуры. Однако, результаты расчетов показывают, что скорость разложения уменьшается с повышением температуры.
Возможной причиной этого является то, что, как показывают реакции (R1) и (R2), реакции между CH3Cl и SiCl2 являются цепными реакциями через радикал CH3. Основные реакции с участием радикала CH3 при 600°C и 700°C показаны на фиг. 25(a) и фиг. 25(b), соответственно. Левая гистограмма показывает потребление CH3 в реакции, а правая гистограмма показывает образование CH3 в реакции. Как видно из фиг. 25(a), при 600°C радикал CH3 реагирует почти исключительно с SiCl2. Однако, при 700°C радикал CH3 реагирует с HCl, H2, CH3SiCl3 и т.п. При более высокой температуре большее количество CH3 расходуется в реакциях с другими молекулами, и CH3 не может вносить вклад в реакцию с SiCl2. Соответственно, считается, что смесь отходящего газа и CH3Cl желательно поддерживать при температуре больше или равной примерно 500°C и меньше или равной примерно 600°C.
Резюме
Исходя из вышеуказанных результатов, ниже описываются возможные способы снижения образования побочного продукта и их ожидаемые преимущества и недостатки.
1) В отсутствие добавления газа температуру поддерживают на уровне примерно 600°C или постепенно снижают, начиная с примерно 700°C. Этот способ имеет следующие преимущества по сравнению с другими способами: способ не требует затрат на дополнительный газ, так как газ добавлять не нужно. Однако скорость реакции ниже, чем в других случаях с добавлением газа, поэтому предусмотрена печь риформинга, предназначенная для осуществления обработки при температурах от 600°C до 700°C (смотри фиг. 3).
2) В случае добавления CH2Cl2, CHCl3 или CCl4 реакция завершается за время от 1/1000 сек до 0,1 сек, поэтому считается, что реакцию желательно проводить с остаточным теплом реакционной печи, разместив входной канал для введения дополнительного газа на выходе реакционной печи. Считается, что от SiCl2 можно в достаточной мере избавиться с помощью остаточного тепла за время прохождения от входного канала для введения дополнительного газа до выпускного канала, поэтому ожидаются меньшие затраты на оборудование и меньшее потребление энергии по сравнению со случаем дополнительной установки печи риформинга, предназначенной для поддержания температуры снаружи реакционной печи. Однако этот способ предполагает затраты на дополнительный газ, в отличие от способа без добавления газа. Кроме того, как показано на фиг. 20, из C2H2 и хлоруглеродного соединения, такого как CxHyClz, например, мономера винилхлорида (C2H3Cl), образуется сажа в соответствии с загружаемым количеством CH4-nCln, и ожидается появление довольно беспорядочных реакций. Ожидается, что соответственно возрастает нагрузка на устройство обработки отходящего газа.
3) В случае добавления CH3Cl и поддержания температуры при 500°C-600°C в печи риформинга, обработку можно завершить за более короткий период времени по сравнением со случаем без добавления газа. Кроме того, SiCl2 превращается в MTS. Кроме того, из фиг. 22 следует, что CH3Cl не разлагается при температуре меньше или равной 600°C и остается около 99%, в отличие от ситуации в пункте 2), поэтому считается, что накапливается мало сажи.
В этом варианте осуществления способ снижения образования побочного продукта рассматривался с акцентом на SiCl2. Термодинамическую константу и константу скорости реакции SiCl2 определяли путем квантово-химических расчетов. При этом предполагалось, что побочный продукт образуется в основном при температуре 500°C или ниже, и приводится три примера способа снижения образования SiCl2 в интервале температур от 500°C до 600°C или выше.
В этом варианте осуществления расчеты проводились в предположении механизма реакции образовании (SiCl2)n, где n не превышает 3, поэтому реальный характер образования (SiCl2)n может отличаться от расчета. Таком образом, можно повысить точность, чтобы предсказать способ снижения образования побочного продукта, используя граничные условия, при каких побочный продукт почти не образуется. Например, можно предложить механизм реакции, в котором n больше или равен 4.
Кроме того, учитывается также побочный продукт, в котором имеются смешанные связи Si-C. Рассчитаны энергии реакции между SiCl2 и углеродсодержащими молекулами, результаты приведены на фиг. 26, фиг. 27(a) и фиг. 27(b). На фиг. 27(a) и фиг. 27(b) сравнивается энергия нулевых колебаний (жирный шрифт) и свободная энергия (КДж/моль) при 1300K. Энергия SiCl2 снижается, и SiCl2 стабилизируется при любой реакции с углеродсодержащими химическими соединениями (MTS, C2H4, C2H2, или трет-1,3-C4H6), поэтому SiCl2 может реагировать с этими молекулами. При этом реакции между диенами и SiCl2 уже были описаны ранее в литературе (смотри непатентный документ 8), и ожидается, что SiCl2 будет довольно легко реагировать с диенами вследствие низкого энергетического барьера реакции.
Сообщалось, что в побочном продукте имеется большое число связей Si-C, поэтому рассматривались также циклическая структура (CH2SiCl2)n и изменение энергии. Структуры с n, равными 2, 3 и 4, показаны на фигурах 28(a), 28(b) и 28(c), соответственно. Что касается изменения энергии, из фиг. 29(a) и фиг. 29(b) следует, что энергия циклического (CH2SiCl2)n уменьшается с повышением степени полимеризации, и ожидается, что циклический (CH2SiCl2)n наиболее стабилен, когда n равно 3. Можно придумать механизм реакции, в котором такая молекула образуется в побочном продукте, в котором имеются смешанные связи Si-C.
Пример 1
В качестве примера 1 применения данного варианта осуществления проводили эксперимент для случая наличия печи риформинга, предназначенной поддерживать газ, выходящий из реакционной печи, при заданной температуре.
Схема эксперимента показана на фиг. 30. На стадии после реакционной печи предусмотрена печь риформинга, имеющая такой же объем. Печь риформинга была печью с горячими стенками. На стадии после печи риформинга был установлен квадрупольный масс-спектрометр (QMS) для анализа газа, охлаждаемая ловушка, предназначенная для сбора побочного продукта при комнатной температуре, и ротационный насос (RP) в качестве вакуумного насоса. В такой конфигурации проводили эксперимент, изменяя температуру печи риформинга с 300°C до 950°C, и определяли температуру печи риформинга, при которой образование побочного продукта снижалось больше всего.
Сырьевой газ, использованный в эксперименте, имел отношение расходов MTS:H2:He=1:1:0,05. Использовали реакционную печь, выполненную из кварцевой трубки. Реакционная печь имела следующие размеры: внутренний диаметр 60 мм и длина 2100 мм, ее область нагрева была разделена на шесть зон (по 350 мм на зону). Три зоны со стороны впуска использовались как реакционная печь, а три зоны со стороны выпуска использовались как печь риформинга.
Связь между собранным побочным продуктом и температурой обработки в печи риформинга показана на фиг. 31. Показан выход побочного продукта, при этом количество (число молей) подаваемого MTS было принято за 100%. Случай температуры обработки в печи риформинга, равной 300°C, когда сырьевой газ не разлагался, и никакого побочного продукта не образовывалось, рассматривался как случай "без обработки". Кроме того, полученная разность с количеством побочного продукта использовалось при этом в качестве "уменьшения количества побочного продукта" при температуре обработки в интервале от 600°C до 800°C.
Как видно из фиг. 31, когда температура обработки в печи риформинга составляла от 600°C до 800°C, результатом было уменьшение количества побочного продукта при повышении температуры обработки. При 950°C образовывался SiC, следовательно, количество вещества, используемого для образования пленки SiC, велико по сравнению с другие температурами. Таким образом, количество побочного продукта меньше, чем в случае 300°C, рассматриваемого как "без обработки". Например, в диапазоне температур 500°C-950°C также наблюдается снижение образования побочного продукта.
В каждом из варианта с отсутствием печи риформинга и варианта с установкой печи риформинга, предназначенной для поддерживания температуры 600°C, жидкость, полученную путем сбора отходящего газа, отличного от побочного продукта, полученного при низкой температуре, анализировали методом газовой хроматографии в сочетании с масс-спектроскопией (ГХ/МС) на стадии после печи риформинга, результат приведен в таблице 1. Обнаружение газа представлено символом "○". Число видов газов увеличивалось при температуре в печи риформинга 600°C, таким образом, было подтверждено, что SiCl2, являющийся предшественником побочного продукта, превращался в другие газы.
Таблица 1
Кроме того, на фиг. 32 показана концентрация MTS в собранной жидкости. Концентрация MTS повышалась в 1,7 раз в случае температуры в печи риформинга 600°C, таким образом, было подтверждено, что SiCl2 превращался в MTS.
Время пребывания газа MTS в печи риформинга составляет около 1,5 сек. Когда температурный режим в печи риформинга был установлен так, чтобы иметь градиент температуры в области трех зон со стороны впуска (800°C, 700°C и 600°C со стороны впуска), время пребывания газообразного MTS в каждой зоне составляло около 0,5 сек. Выход побочного продукта по отношению к количеству загружаемого MTS для варианта с градиентом температуры составил 7,2%.
Анализировалось уменьшение образования побочного продукта благодаря размещению печи риформинга на стадии после реакционной печи. Образование побочного продукта снижалось, когда температура печи риформинга падала в пределах заданного диапазона. Кроме того, было подтверждено, что предшественник побочного продукта превращался в MTS.
Пример 2
В качестве примера 2 применения данного варианта осуществления проводили эксперимент на многообразие побочных продуктов в случае, когда печь риформинга находилась при высокой температуре.
Схема эксперимента показана на фиг. 33. Печь риформинга была установлена на стадии после реакционной печи. В реакционную печь подавали газовую смесь MTS/H2. Печь риформинга поддерживали при температуре в интервале от 600°C до 1500°C. Анализировали эффект от установки охлаждаемой ловушки, поддерживаемой при температуре -80°C, на стадии после печи риформинга.
В охлаждаемой ловушке отходящий газ, выходящий из печи риформинга, конденсировался и затем доходил до комнатной температуры, а газифицированный компонент (сырьевой газ или подобное) испарялся. Остаток, полученный после испарения газообразного компонента, оценивали как жидкий побочный продукт, способный прилипать к трубопроводу при комнатной температуре.
Фотография внешнего вида жидкого побочного продукта, полученного в температурных условиях печи риформинга, и фотография внешнего вида побочного продукта, стабилизированного до оксида кремния в результате гидролиза, показаны на фиг. 34. Результат измерения веса оксида кремния после стабилизации и его доля в загружаемом сырье, полученная делением числа молей оксида кремния на полное число молей MTS, загруженного на стадию CVI, приведены в таблице 2.
Таблица 2
Согласно таблице 2, в условиях, когда температура печи риформинга составляла 1500°C, количество жидкого побочного продукта удалось уменьшить вдвое по сравнению с вариантом без печи риформинга. Однако в условиях, когда температура печи риформинга составляла 750°C или 1400°C, количество жидкого побочного продукта удваивалось, т.е. получался неблагоприятный эффект.
Возможная причина этого описывается ниже. Непрореагировавший MTS, выходящий из реакционной печи, разлагался в печи риформинга и осаждался в виде SiC. Однако существует интервал температуры, в котором доля непрореагировавшего MTS, разложившегося с образованием SiCl2, являющегося предшественником побочного продукта, превышает долю непрореагировавшего MTS, осажденного в виде SiC. Считается, что температуры 750°C и 1400°C входят в этот интервал, а температура 1500°C, при которой скорость реакции образования SiC является высокой, находится за пределами этого интервала. Многообразие побочных продуктов в зависимости от температуры печи риформинга, определенное по модели, предполагающей такой механизм, проиллюстрировано на фиг. 35. Таким образом, в качестве способа, в котором расходуется SiCl2, являющийся предшественником побочного продукта, одним из эффективных способов является также способ, включающий осаждение SiCl2 в форме твердого вещества SiC при 1500°C или выше.
Считается, что когда печь риформинга имеет температуру в пределах заданного диапазона, включающего 750°C и 1400°C, доля непрореагировавшего MTS, разложившегося до SiCl2, который является предшественником побочного продукта, превышает долю непрореагировавшего MTS, разложившегося и осажденного в виде SiC в печи риформинга, что способствует увеличению количества жидкого побочного продукта.
Пример 3
В качестве примера 3 применения данного варианта осуществления проводился эксперимент для случая добавления N2, HCl или CH2Cl2 и осуществления обработки в печи риформинга.
Фиг. 36 показывает принцип обработки отходящего газа дополнительным газом. Печь риформинга была установлена на стадии после реакционной печи, и дополнительный газ подавался на вход печи риформинга. Дополнительный газ предпочтительно является газом на основе хлора, содержащим хлор. В печи риформинга газовая смесь, состоящая из газа, выходящего из реакционной печи, и дополнительного газа, подвергается обработке при заданной температуре в интервале от 200°C до 1100°C. Дополнительный газ не ограничен описанными выше CH2Cl2, CHCl3, CCl4 и CH3Cl и может включать N2, H2, HCl, спирт (этанол, ацетон или метанол) и водяной пар. Известно, что спирт или водяной пар активно реагирует с побочным продуктом при комнатной температуре и, следовательно, их можно добавлять при комнатной температуре. Кроме того, дополнительный газ можно добавлять так, чтобы количество дополнительного газа было больше, чем количество жидкого или твердого побочного продукта.
Схема эксперимента показана на фиг. 37. Электрическая печь, использующаяся в этом эксперименте, является шестизонной печью, в которой шесть электрических печей непрерывно соединены друг с другом. Температуру можно устанавливать в каждой зоне. Каждая электрическая печь имеет длину 350 мм и внутренний диаметр ϕ60 мм. Первые пять из этих зон служат реакционной зоной, что соответствует реакционной печи, а последняя зона служит зоной риформинга, что соответствует печи риформинга.
Электрическая печь содержит реакционную трубку, выполненную из кварцевой трубы круглого сечения, и является печью с горячими стенками, когда нагревается вся труба. В качестве сырья использовали газовую смесь MTS/H2/He. Она является стандартным газом для калибровки квадрупольного масс-спектрометра (QMS) для анализа газов. QMS устанавливали на выпускную трубу вблизи реакционной трубки. Газ анализировали с помощью QMS для определения остаточного уровня газообразного MTS и для качественного анализа газов, образующихся при термическом разложении газовой смеси MTS/H2.
Побочный продукт собирается в трубе-ловушке, установленной на выпускной трубе, и исходя из его веса, рассчитывается скорость образования побочного продукта. Дополнительный газ добавляли от середины электрической печи номер шесть (вблизи центра трубы круглого сечения реакционной печи и на расстоянии 175 мм от конца электрической печи номер шесть), являющейся самой близкой к выходу из шести зон на фиг. 37. Дополнительный газ вводился в направлении вверх по потоку. В примере 3 оценивалось увеличение или уменьшение количества побочного продукта в зависимости от дополнительного газа, поэтому определяли материальный баланс для газов и пленки, образующейся в результате реакции из MTS, служащего сырьем. Материальный баланс определяли, принимая количество (число молей) загружаемого MTS (CH3SiCl3) за 100%.
1) Экспериментально определяли количество образующейся пленки SiC.
Количество образующейся пленки SiC представляло собой суммарное количество вещества пленок SiC, образующихся на кварцевой трубке, подложке Si и войлока, но для простоты предполагалось, что выход пленки SiC в каждом случае соответствовал одному и тому же экспериментальному значению (12%).
2) Экспериментально определяли остаточный уровень MTS.
При анализе газа на QMS-спектрометре интенсивность сигнала QMS при комнатной температуре принимали равной 100%, и остаточный уровень MTS рассчитывали из отношения интенсивности сигнала QMS при комнатной температуре к интенсивности сигнала при термическом разложении при высокой температуре.
3) Экспериментально определяли количество побочного продукта.
Для количественного анализа количества побочного продукта использовали трубу для сбора побочного продукта, установленную на выпускной трубе, исходя из веса собранного вещества.
В расчетах количество побочного продукта определяли в предположении, что побочный продукт представлял собой SiCl2 (молекулярный вес: 98,5 г/моль).
4) Количества других газов рассчитывали как остаток, полученный после вычитания значений, определенных в вышеуказанных пунктах 1), 2) и 3), из 100.
Оценивали также типы образованных газов путем качественной оценки на с помощью QMS.
В примере 3 сравнивались четыре условия эксперимента "без дополнительного газа", "добавление N2", "добавление HCl" и "добавление CH2Cl2", эти условия указаны в таблице 3. Газовая смесь, использовавшаяся в примере 3, имела отношение расходов MTS:H2:He=1:1:0,05, и дополнительные газы добавляли в одинаковых количествах.
Таблица 3
Результаты по материальному балансу при CVI сведены на фиг. 38. Из количественного анализа с помощью QMS выявилось, что в качестве "других газов" в результате термического распада MTS образовывались по меньшей мере газы CH4, C2H2, C2H4, SiCl4, SiHCl2, HCl и Cl2.
В отсутствие дополнительного газа побочный продукт образовывался на уровне 9,5% по отношению к балансу массы. Напротив, при добавлении N2 уровень образования снизился до 6,4%. Вероятно, это связано с тем, что скорость течения газа повышается в результате добавления дополнительного газа, и побочный продукт вытесняется к выпуску выпускной трубы, а не с тем, что количество побочного продукта уменьшается в результате реакции и подобного. Таким образом, в примере 3 в эксперименте с дополнительным газом наличие или отсутствие эффекта сравнивали, используя в качестве точки отсчета результат для случая добавления N2. Однако нельзя отрицать, что изменение механизма реакции в результате добавления N2 может иметь эффектом существенное снижение образования побочного продукта.
При добавлении CH2Cl2 образования побочного продукта не наблюдалось, не образовывались также другие остатки и т.п. Сравнение результатов газового анализа с помощью QMS-спектрометра в случаях добавления N2, добавления HCl и добавления CH2Cl2 показано на фиг. 39(a) и фиг. 39(b). Общие данные показаны на фиг. 39(a), а данные вблизи области A с фиг. 39(a) показаны в увеличении на фиг. 39(b).
При добавлении CH2Cl2 была обнаружена молекула газа, имеющая массовое число 62 m/z, которая не наблюдалась при добавлении N2 и при добавлении Cl. Если бы молекула газа, имеющая массовое число 62 m/z, содержала Cl, спектр характеризовался бы присутствием в соответствующем отношении изотопов Cl (35 г/моль и 37 г/моль). В результате удалось определить, что молекула, имеющая массовое число 62 m/z, не содержит Cl. Таким образом, принимая во внимание молекулярный вес, предполагается, что молекула с массовым числом 62 m/z является дисиланом (Si2H6). Разумно предположить, что молекулы с массовым числом 59 m/z, 60 m/z и 61 m/z представляют собой фрагменты дисилана (Si2H6), то есть, молекулы, в каждой из которых H удален из дисилана.
При добавлении HCl уровень образования побочного продукта в расчете на полную массу снизился до 2,7%. Количество побочного продукта снизилось до половины или ниже по сравнению со случаем добавления N2 (6,4%). Между тем остаточный уровень MTS повысился с 12% до 19%. Этот результат указывает, что реакция, в которой предшественник побочного продукта снова превращается в MTS, промотируется за счет добавления HCl. Кроме того, как показано на фиг. 39(a) и фиг. 39(b), в случае добавления HCl анализ отходящего газа на QMS-спектрометре не позволил подтвердить образование конкретной молекулы газа. Исходя из того, что количество побочного продукта уменьшилось вдвое, остаточный уровень MTS повысился, и состав газа не претерпел особых изменений, можно предположить, что в результате добавления HCl реакция, в которой SiCl2, являющийся предшественником побочного продукта, снова превращается в MTS (CH3SiCl3), превалирует над реакцией, в которой SiCl2 полимеризуется, образуя побочный продукт. В этом случае считается, что речь идет о сложных маршрутах реакции.
Дисилан представляет собой горючий газ, легко сгорающий при комнатной температуре на воздухе и представляющий опасность, но он также является малотоксичным газом (обычно указывается как нетоксичный) и обычно применяется в полупроводниковой промышленности и т.п., и легко детоксифицируется. Дисилан с большой вероятностью можно обрабатывать, по крайней мере с большей безопасностью, чем жидкий побочный продукт, осажденный в трубе. Было обнаружено, что способ снижения образования побочного продукта путем использования дополнительного газа был высокоэффективным.
В примере 3 рассматривалось уменьшение образования побочного продукта путем добавления дополнительного газа в газ, выпускаемый из реакционной печи. Было обнаружено, что при добавлении CH2Cl2 можно было почти полностью избавиться от побочного продукта. При добавлении HCl количество побочного продукта снижалось до половины или ниже, а остаточный уровень MTS возрастал. Однако HCl повлек за собой увеличение объема обработки в детоксифицирующем устройстве вследствие повышения концентрации HCl в отходящем газе, к том же он является более дорогостоящим газообразным веществом, и оказывает низкий эффект на снижение образования побочного продукта по сравнению с другими газами (сравнимо с эффектом от обработки при 600°C).
Вторая схема реакции снижения образования побочного продукта с добавлением газа
Было выведено уравнение (6) для расчета константы элементарной реакции с использованием SiCl2 в качестве исходного вещества. Элементарная реакция, имеющая более высокую константу скорости k, была предположена в результате теоретических расчетов с использованием уравнения для расчета константы скорости (6).
В уравнении (6) для расчета константы скорости параметры A, n и Ea (Дж/моль) являются постоянными в каждой элементарной реакции.
На фиг. 40(a) представлена таблица, показывающая примеры элементарных реакций, связанных с SiCl2, и их константы. Фиг. 40(b) показывает график сравнения констант скоростей элементарных реакций, перечисленных как потенциально возможные. Как видно из фиг. 40(a) и фиг. 40(b), в результате теоретических расчетов было предсказано, что количество SiCl2 можно уменьшить, если реакцию, в которой из SiCl2 образуется любая одна или более из молекул SiCl, H, HCl и CH3Cl, можно промотировать путем добавления дополнительного газа. При этом предполагалось, что когда в качестве дополнительного газа использовалось три типа газов: газообразный HCl, газ на основе CxHy и газ на основе CxHyClz, проявлялся эффект снижения количества SiCl2.
Выбор возможных кандидатов в качестве дополнительного газа
Исходя из результатов раздела "Вторая схема реакции снижения образования побочного продукта", из трех видов газов (газообразный HCl, газ на основе CxHy и газ на основе CxHyClz), которые, как предполагалось, приводят к уменьшению количества SiCl2, были выбраны вещества, отличающиеся высокой безопасностью (низкая токсичность, низкая нагрузка на окружающую среду, простое детоксифицирующее устройство), простотой в обработке (высокое давление паров) и низкой стоимостью (широко распространенный продукт, низкий молекулярный вес (г/моль)).
В частности, в качестве кандидатов на дополнительный газ было выбрано шесть следующих веществ: HCl (хлористый водород), CH3Cl (хлорметан), CH2Cl2 (дихлорметан), CCl4 (тетрахлорметан, четыреххлористый углерод), C2H3Cl3 (трихлорэтан) и C2HCl3 (трихлорэтилен).
Моделирование побочного продукта в случае добавления дополнительного газа
Аналогично тому, как это делалось в разделе "Предсказание свойств реакции образования побочных продуктов", реакцию рассчитывали, используя механизм реакции MTS/H2 и программу CHEMKIN (смотри непатентный документ 6). Условия моделирования показаны на фиг. 41. Как следует из фиг. 41, расчет реакции проводили для условий, когда газовая смесь MTS/H2 (сырьевой газ) течет в поршневом режиме в цилиндрической трубе, имеющей внутренний диаметр 60 мм и полную длину 2000 мм при отношении расходов MTS:H2=1,0:0,4 при пониженном давлении. В цилиндрической трубе область от концевого участка (0 мм) со стороны входа в направлении течения сырьевого газа до точки, отстоящей от концевого участка на 1000 мм, служит в качестве реакционной печи, а область от точки, отстоящей от концевого участка на 1000 мм, до точки, отстоящей от него на 2000 мм, служит в качестве печи риформинга. Кроме того, расчет реакции проводился для условий, когда температура печи риформинга была установлена на 975°C, а дополнительный газ добавлялся в печь риформинга (в позиции, соответствующей расстоянию 1000 мм и времени пребывания t=1,36 сек) при отношении расходов MTS:дополнительный газ=1,0:1,0. Реакцию рассчитывали для каждого из шести веществ (HCl, CH3Cl, CH2Cl2, CCl4, C2H3Cl3 и C2HCl3) в качестве дополнительного газа.
Фиг. 42(a) является графиком, показывающим результат моделирования в случае добавления HCl в качестве дополнительного газа. Фиг. 42(b) является графиком, показывающим результат моделирования в случае добавление CH2Cl2 в качестве дополнительного газа. Фиг. 42(c) является графиком, показывающим результат моделирования в случае добавление CH3Cl в качестве дополнительного газа. Фиг. 42(d) является графиком, показывающим результат моделирования в случае добавление C2HCl3 в качестве дополнительного газа. Фиг. 42(e) является графиком, показывающим результат моделирования в случае добавление C2H3Cl3 в качестве дополнительного газа. Фиг. 42(f) является графиком, показывающим результат моделирования в случае добавление CCl4 в качестве дополнительного газа. На каждой из фигур 42(a) - 42(f) пунктирные линии показывают парциальное давление MTS, линии, состоящие из последовательностей штриха и двух точек, показывают парциальное давление H2, штрих-пунктирные линии показывают парциальное давление дополнительного газа, и сплошная линия показывает парциальное давление SiCl2.
Результат проведенного моделирования побочного продукта (SiCl2) состоял в том, что образование SiCl2 подавлялось благодаря добавлению дополнительного газа в каждом из случаев HCl, CH3Cl, CH2Cl2, CCl4, C2H3Cl3 и C2HCl3. Кроме того, результатом было то, что из этих шести веществ C2HCl3, показанный на фиг. 42(d), оказывал наибольшее влияние на уменьшение количества SiCl2. Кроме того, результатом было то, что CH2Cl2, показанный на фиг. 42(b), CH3Cl, показанный на фиг. 42(c), и C2H3Cl3, показанный на фиг. 42(e), оказывали большое влияние на уменьшение количества SiCl2.
Из указанных выше результатов можно сделать вывод, что количество SiCl2 можно эффективно снизить, если использовать в качестве дополнительного газа соединение на основе CxHyClz (0≤x+y+z≤1, 0≤x, y≤1, 0 Анализ температуры печи риформинга при добавлении дополнительного газа Аналогично тому, как это делалось в разделе "Моделирование побочного продукта в случае добавления дополнительного газа", реакцию рассчитывали, используя механизм реакции MTS/H2 и программу CHEMKIN (смотри непатентный документ 6). Условия моделирования были теми же, что и в разделе "Моделирование побочного продукта в случае добавления дополнительного газа", за исключением температуры печи риформинга и полной длины печи риформинга. Рассчитывали парциальное давление SiCl2 для вариантов температуры печи риформинга 200°C, 400°C, 600°C, 800°C и 1000°C. Кроме того, расчет реакции проводили при условии, что каждый из CH2Cl2 и CH3Cl добавляли в качестве дополнительного газа в месте, соответствующем времени пребывания t=1,37 сек. Фигуры 43(a), 43(b) и 43(c) являются графиками показывающими парциальное давление SiCl2 в случае добавления CH2Cl2 в качестве дополнительного газа и изменения температуры печи риформинга. Фиг. 43(a) является графиком, показывающим для разных температур изменение парциального давления SiCl2 в зависимости от времени пребывания. Фиг. 43(b) является графиком, показывающим парциальное давление SiCl2 на выходе печи риформинга. Фиг. 43(c) является графиком, показывающим изменение парциального давления SiCl2 в зависимости от разницы отношений расходов дополнительного газа и MTS при разных температурах. На фиг. 43(a) сплошная линия соответствует температуре 200°C, пунктирная линия температуре 400°C, штрих-пунктирная линия температуре 600°C, линия из последовательности штриха и двух точек - температуре 800°C, и сплошная линия температуре 1000°C. Кроме того, на фиг. 43(c) сплошная линия соответствует температуре 300°C, пунктирная линия температуре 500°C, штрих-пунктирная линия температуре 700°C и линия из последовательности штриха и двух точек температуре 900°C. Как показано на фиг. 43(a), полученным результатом было то, что при времени пребывания t=1,68 сек эффект уменьшения количества SiCl2 усиливается с повышением температуры. То есть, полученный результат состоял в том, что эффект уменьшения количества SiCl2 становился сильнее, когда температура повышалась через 0,31 сек после добавления CH2Cl2, служащего дополнительным газом. Между тем, когда время пребывания t превышало 1,68 сек, был получен другой результат: температура, при которой достигался повышенный эффект снижения количества SiCl2, менялся в зависимости от времени пребывания. Кроме того, как показано на фиг. 43(b), полученный результат состоял в том, что парциальное давление SiCl2 на выходе печи риформинга было самым низким, когда температура печи риформинга составляла 500°C. Кроме того, результатом было то, что парциальное давление SiCl2 на выходе печи риформинга повышалось в порядке возрастания температуры 500°C, 600°C, 700°C, 400°C, 800°C, 1000°C и 2000°C. Было теоретически обнаружено существование оптимального температурного диапазона в случае добавления CH2Cl2 в качестве дополнительного газа. Кроме того, как показано на фиг. 43(c), когда отношение расходов CH2Cl2 и MTS (CH2Cl2/MTS) было меньше 0,7, полученный результат состоял в том, что эффект уменьшения количества SiCl2 усиливался при снижении температуры печи риформинга. Кроме того, при отношении расходов 1,6 или больше полученный результат состоял в том, что эффект уменьшения количества SiCl2 усиливался с повышением температуры печи риформинга. Далее, когда отношение расходов составляло 0,7 или больше, но менее 1,6, результат состоял в том, что температура печи риформинга, при которой достигался повышенный эффект уменьшения количества SiCl2, менялся в зависимости от отношения расходов. На фигурах 44(a) и 44(b) приведены графики, показывающие парциальное давление SiCl2 в случае добавления CH3Cl в качестве дополнительного газа и изменения температуры печи риформинга. Фиг. 44(a) показывает график изменения парциального давления SiCl2 в зависимости от времени пребывания при разных температурах. Фиг. 44(b) показывает график парциального давления SiCl2 на выходе печи риформинга. На фиг. 44(a) сплошная линия относится к температуре 200°C, пунктирная линия к температуре 400°C, штрих-пунктирная линия к температуре 600°C, линия из последовательностей штриха и двух точек к температуре 800°C и сплошная линия к температуре 1000°C. Как видно из фиг. 44(a) и фиг. 44(b), результат состоит в том, что самое низкое парциальное давление SiCl2 достигалось при времени пребывания t=1,5 сек, независимо от температуры печи риформинга. Таким образом, полученный результат состоял в том, что парциальное давление SiCl2 было самым низким через 0,1 сек после добавления CH3Cl в качестве дополнительного газа. Кроме того, как показано на фиг. 44(b), полученный результат состоял в том, что парциальное давление SiCl2 на выходе печи риформинга снижалось при снижении температуры печи риформинга. В частности, результатом было то, что парциальное давление SiCl2 на выходе печи риформинга повышалось в порядке возрастания температуры: 150°C, 200°C, 400°C, 600°C, 800°C и 1000°C. Анализ добавленного количества дополнительного газа Аналогично тому, как это делалось в разделе "Анализ температуры печи риформинга при добавлении дополнительного газа", реакцию рассчитывали, используя механизм реакции MTS/H2 и программу CHEMKIN (смотри непатентный документ 6). Условия моделирования были теми же, что и в разделе "Анализ температуры печи риформинга при добавлении дополнительного газа", за исключением количества добавляемого дополнительного газа. График на фиг. 45 показывает парциальное давление SiCl2 при изменении оптимального количества добавленного CH3Cl, использующегося в качестве дополнительного газа. На фиг. 45 сплошная линия относится к случаю, когда температура печи риформинга была установлена на уровне 200°C, пунктирная линия соответствует установке температуры печи риформинга на 600°C, и штрих-пунктирная линия соответствует установке температуры печи риформинга на 1000°C. Как следует из фиг. 45, парциальное давление SiCl2 снижается при увеличении количества дополнительного газа независимо от температуры печи риформинга. Кроме того, результат состоял в том, что парциальное давление SiCl2 заметно снижалось, когда отношение количеств дополнительного газа и MTS (дополнительный газ/MTS) было больше или равно 1. Пример 4 Эксперимент, в котором в качестве дополнительного газа добавляли N2, C2H4, HCl, CH3Cl, CH2Cl2, CCl4, C2H3Cl3 или C2HCl3 и осуществляли обработку в печи риформинга, проводили с использованием устройства, аналогичного устройству из примера 3, показанному на фиг. 37. В примере 4 зоны с номерами 1-3 служили реакционной областью, соответствующей реакционной печи, а зоны 4-6 служили областью риформинга, соответствующей печи риформинга. Таким образом, реакционная печь имела длину 1,05 м (350мм×3), а печь риформинга имела длину 1,05 м (350 мм×3). Температуру печи риформинга устанавливали на уровне 975°C. Кроме того, реакционная печь и печь риформинга находились при пониженном давлении. Кроме того, в качестве сырьевого газа в реакционную печь подавали газовую смесь MTS/H2/He. Сырьевой газ имел отношение расходов MTS:H2:He=1,0:1,0:0,05. Кроме того, в печь риформинга в качестве дополнительного газа подавали HCl, CH3Cl, CH2Cl2, CCl4, C2H3Cl3 или C2HCl3. Отношение расходов MTS и дополнительного газа было следующим: MTS:(дополнительный газ)=1,0:1,0. Чтобы оценить эффект уменьшения количества побочного продукта, оказываемый дополнительным газом, рассчитывали материальный баланс для пленки SiC и газов, образующихся из MTS, содержащегося в сырьевом газе, по реакции, соответствующей типу дополнительного газа. Материальный баланс рассчитывали, принимая количество (число молей) подаваемого MTS (CH3SiCl3) за 100%. 1) Количество пленки SiC (%) Количество пленки SiC рассчитывали, исходя из полного количества пленок SiC, образованных на основном материале, находящемся в реакционной печь или печи риформинга, и на поверхности стенок кварцевой трубки. 2) Количество побочного продукта (%) Количество побочного продукта рассчитывали, исходя из веса вещества, собранного в трубе для сбора побочного продукта, установленной на выпускной трубе. Количество побочного продукта рассчитывали в предположении, что побочный продукт представлял собой SiCl2 (молекулярный вес 98,5 г/моль). 3) Количество непрореагировавшего MTS (%) При газовом анализе на QMS-спектрометре интенсивность QMS-сигнала при комнатной температуре принимали за 100%, и количество непрореагировавшего MTS рассчитывали из отношения интенсивности сигнала QMS при комнатной температуре и интенсивности сигнала во время термического разложения при высокой температуре. 4) Количество других газов (%) Количества других газов получали, вычитая значения, рассчитанные выше в пунктах 1), 2) и 3), из 100%. На фиг. 46 показан график материального баланса, рассчитанного для примера 4. Как видно из фиг. 46, в варианте "без дополнительного газа" побочный продукт (SiCl2) образовывался на уровне 13%. Кроме того, в варианте "добавление газообразного азота (N2)" в качестве дополнительного газа уровень образования побочного продукта составил 16%. В варианте "добавление C2H4 (этилен)" в качестве дополнительного газа уровень образования побочного продукта составил 6%. Кроме того, в варианте "добавление HCl" в качестве дополнительного газа уровень образования побочного продукта составлял 3%. Далее, в каждом из вариантов добавления "C2HCl3", "CCl4", "C2H3Cl3", "CH2Cl2" и "CH3Cl" в качестве дополнительного газа побочный продукт не образовывался (0%). Вышеуказанные результаты подтверждают, что когда добавляли любое, по меньшей мере одно, вещество из шести избранных веществ и C2H4, можно было снизить образование SiCl2 по сравнению со случаем добавления газообразного азота при том же расходе газа. Кроме того, было установлено, что образование SiCl2 можно было избежать, когда в качестве дополнительного газа добавляли по меньшей мере одно вещество, выбранное из C2HCl3, CCl4, C2H3Cl3, CH2Cl2 и CH3Cl. На фигурах 47(a) - 47(f) показаны снимки выпускной трубы (труба, соединенная с выходом печи риформинга) в примере 4. Фиг. 47(a) показывает фотографию для случая без добавления дополнительного газа. Фиг. 47(b) показывает фотографию для случая добавления HCl в качестве дополнительного газа. Фиг. 47(c) показывает фотографию для случая добавления C2HCl3 в качестве дополнительного газа. Фиг. 47(d) показывает фотографию для случая добавления CCl4 в качестве дополнительного газа. Фиг. 47(e) показывает фотографию для случая добавления CH3Cl в качестве дополнительного газа. Фиг. 47(f) показывает фотографию для случая добавления CH2Cl2 в качестве дополнительного газа. Фотографии на фиг. 47(a) и фиг. 47(b) подтверждают, что в отсутствие дополнительного газа и при добавлении HCl в качестве дополнительного газа побочный продукт (SiCl2) прилипает к выпускной трубе. Кроме того, как показано на фиг. 47(c) и фиг. 47(d), прилипания побочного продукта (SiCl2) не наблюдалось, но в случаях добавления C2HCl3 и CCl4 в качестве дополнительного газа наблюдалось прилипание углерода. Между тем, как видно из фиг. 47(e) и фиг. 47(f), для случаев добавления CH3Cl и CH2Cl2 в качестве дополнительного газа не наблюдалось прилипания ни побочного продукта (SiCl2), ни углерода. Указанные выше результаты подтверждают, что когда в качестве дополнительного газа добавляли по меньшей мере один из CH3Cl или CH2Cl2, образования SiCl2 удалось избежать и, кроме того, удалось избежать осаждения углерода в выпускной трубе. Пример 5 Ниже обсуждается отношение расходов в предположении, что расход MTS принят за 1,0. Эксперимент, в котором в качестве дополнительного газа добавляли CH3Cl и осуществляли обработку в печи риформинга, проводили с использованием устройства, похожего на устройство из примера 4. Реакционная печь и печь риформинга находились при пониженном давлении. Кроме того, в реакционную печь в качестве сырьевого газа подавали газовую смесь MTS/H2/He. Сырьевой газ имело отношение расходов MTS:H2:He=1:1:0,05. Кроме того, в печь риформинга в качестве дополнительного газа добавляли CH3Cl. Далее, для анализа времени пребывания эксперимент проводили в вариантах введения трубки, выполненной из углерода (ниже называемой "карбоновой трубкой"), в печь риформинга и без введения карбоновой трубки в печь риформинга. Карбоновая трубка имела размеры, составляющие: длина 1,05 м, наружный диаметр 60 мм и внутренний диаметр 20 мм. Таким образом, когда печь риформинга была образована из трубы круглого сечения, эксперимент проводили для случаев, когда удельная поверхность, полученная делением объема трубы круглого сечения на площадь поверхности трубы круглого сечения, составляла 5 мм и 15 мм. Фигуры 48(a), 48(b) и 48(c) являются графиками, показывающими результаты примера 5. График на фиг. 48(a) показывает соотношение между добавленным количеством CH3Cl, температурой печи риформинга и выходом побочного продукта. График на фиг. 48(b) показывает соотношение между временем пребывания CH3Cl, температурой печи риформинга и выходом побочного продукта. График фиг. 48(c) показывает соотношение между временем пребывания CH3Cl, температурой печи риформинга, отношением расходов и выходом побочного продукта. Для случая, когда CH3Cl добавляли при отношении расходов 0,5 (50% от количества MTS), и для случая, когда CH3Cl добавляли при отношении расходов 1,0 (в том же количестве, что и MTS), выход (%) побочного продукта (SiCl2) измеряли в условиях изменения температуры печи риформинга. Как результат, в случае добавления CH3Cl в печь риформинга при отношении расходов 0,5 (показано черными кружками на фиг. 48(a)), было подтверждено, что выход побочного продукта снижался с повышением температуры печи риформинга вплоть до достижения температуры печи риформинга 750°C. Кроме того, было установлено, что степень снижения выхода побочного продукта уменьшалась, когда температура печи риформинга превышала 750°C. Для случая, когда CH3Cl добавляли в печь риформинга при отношении расходов 1,0 (т.е. в том же количестве, что и MTS) (показано черными квадратами на фиг. 48(a)), было установлено, что выход побочного продукта снижался с повышением температуры печи риформинга. Кроме того, было установлено, что при температуре печи риформинга больше или равной 750°C побочный продукт не образовывался (нулевой выход). Из приведенных выше результатов для случая использования CH3Cl в качестве дополнительного газа было подтверждено, что образование побочного продукта (SiCl2) можно предотвратить, если установить температуру печи риформинга больше или равной 750°C. Кроме того, когда температура печи риформинга больше или равна 850°C, образуется пленка SiC. Соответственно, при использовании CH3Cl в качестве дополнительного газа было подтверждено, что предпочтительно устанавливать температуру печи риформинга больше или равной 750°C, но меньше 850°C. Кроме того, в случаях, когда время пребывания CH3Cl в печи риформинга было установлено равным 0,080 сек (вставлена карбоновая трубка) и 1,0 сек (без вставки карбоновой трубки), выход (%) побочного продукта (SiCl2) измеряли при изменении температуры печи риформинга. В результате было установлено, что в случае, когда время пребывания в печи риформинга было равно 0,080 сек (показано черным кружками на фиг. 48(b)), выход побочного продукта снижался с повышением температуры печи риформинга. Между тем, в случае, когда время пребывания CH3Cl в печи риформинга было установлено равным 1,0 сек (показано черными квадратами на фиг. 48(b)), было обнаружено, что выход побочного продукта снижался с повышением температуры печи риформинга. Кроме того, было установлено, что когда температура печи риформинга была больше или равна 750°C, побочный продукт вообще не образовывался (выход равен 0%). Из приведенных выше результатов было установлено, что в случае использования CH3Cl в качестве дополнительного газа образование побочного продукта можно предотвратить, если установить время пребывания дополнительного газа в печи риформинга больше или равным 1,0 сек. Исходя из того, что эффект уменьшения количества побочного продукта наблюдался и в том случае, когда время пребывания было установлено равным 0,080 сек, можно предположить, что при использовании CH3Cl в качестве дополнительного газа образование побочного продукта можно предотвратить, если установить время пребывания дополнительного газа в печи риформинга больше или равным 0,2 сек. Кроме того, чтобы установить время пребывания дополнительного газа в печи риформинга больше или равным 10 сек, сама печь риформинга должна иметь увеличенный размер. Соответственно, при использовании CH3Cl в качестве дополнительного газа было установлено, что время пребывания дополнительного газа в печи риформинга предпочтительно должно быть больше или равным 0,2 сек, но меньше 10 секунд. Таким образом, когда время пребывания дополнительного газа в печи риформинга установлено больше или равным 0,2 сек, но меньше 10 сек, образование побочного продукта можно предотвратить при одновременном уменьшении размера печи риформинга. Кроме того, выход (%) побочного продукта (SiCl2) измеряли при изменении отношения расходов дополнительного газа (CH3Cl) и MTS (дополнительный газ/MTS). Когда время пребывания CH3Cl в печи риформинга было установлено равным 0,080 сек, а температура печи риформинга равной 975°C (показано черными кружками на фиг. 48(c)), оказалось, что выход побочного продукта снижался с увеличением отношения расходов (отношение количеств веществ). В случае, когда время пребывания CH3Cl в печи риформинга было установлено равным 1,0 сек, а температура печи риформинга равной 975°C (показано черными квадратами на фиг. 48(c)), оказалось, что выход побочного продукта снижался с увеличением отношения расходов. Кроме того, было установлено, что когда отношение расходов составляло 1,0 или больше, побочный продукт вообще не образовывался (выход равен 0%). В случае, когда время пребывания CH3Cl в печи риформинга было установлено равным 1,0 сек, а температура печи риформинга равной 750°C (показано белыми квадратами на фиг. 48(c)), оказалось, что выход побочного продукта снижался с увеличением отношения расходов. Кроме того, было установлено, что когда отношение расходов составляло 1,0 или больше, побочный продукт вообще не образовывался (выход равен 0%). Приведенные выше результаты подтверждают, что образование побочного продукта (SiCl2) можно предотвратить, если установить отношение расходов CH3Cl и MTS (CH3Cl/MTS) больше или равным 1,0. Пример 6 Ниже рассматривается отношение расходов при условии, что расход MTS принят за 1,0. Эксперимент, в котором в качестве дополнительного газа добавляли CH2Cl2 и осуществляли обработку в печи риформинга, проводили с использованием устройства, похожего на устройство из примера 4. Реакционная печь и печь риформинга находились при пониженном давлении. Кроме того, в реакционную печь в качестве сырьевого газа подавали газовую смесь a MTS/H2/He. Сырьевой газ имел отношение расходов MTS:H2:He=1:1:0,05. Кроме того, в печь риформинга в качестве дополнительного газа добавляли CH2Cl2. Далее, чтобы проанализировать влияние времени пребывания, эксперимент проводили в варианте с введением карбоновой трубки в печь риформинга и в варианте без введения карбоновой трубки в печь риформинга. Размеры карбоновой трубки были такими же, как в примере 5, т.е., длина 1,05 м, наружный диаметр 60 мм и внутренний диаметр 20 мм. Таким образом, когда печь риформинга была выполнена из трубы круглого сечения, эксперимент проводили для случаев, для которых удельная поверхность, полученная делением объема трубы круглого сечения на площадь поверхности трубы круглого сечения, составляла 5 мм и 15 мм. Фигуры 49(a), 49(b) и 49(c) представляют собой графики, показывающие результаты примера 6. График на фиг. 49(a) показывает связь между добавленным количеством CH2Cl2, температурой печи риформинга и выходом побочного продукта. График на фиг. 49(b) показывает связь между временем пребывания CH2Cl2, температурой печи риформинга и выходом побочного продукта. График на фиг. 49(c) показывает связь между временем пребывания CH2Cl2, температурой печи риформинга, отношением расходов и выходом побочного продукта. Для случая, когда CH2Cl2 добавляли при отношении расходов 0,25 (в количестве 25% от MTS), а также для случая, когда CH2Cl2 добавляли при отношении расходов 0,5 (в количестве 50% от MTS), и случая, когда CH2Cl2 добавляли при отношении расходов 1,0 (в том же количестве, что и MTS), измеряли выход (%) побочного продукта (SiCl2) при изменении температуры печи риформинга. В результате было установлено, что когда CH2Cl2 добавляли в печь риформинга при отношении расходов 0,25 (показано черными квадратами на фиг. 49(a)), выход побочного продукта снижался с повышением температуры печи риформинга вплоть до достижения температуры печи риформинга 750°C. Кроме того, было установлено, что когда температура печи риформинга была больше или равна 750°C, но меньше 850°C, побочный продукт не образовывался (выход равен 0%). Между тем, было установлено, что при температуре печи риформинга больше или равной 850°C выход побочного продукта повышался. Было установлено, что когда CH2Cl2 добавляли при отношении расходов 0,5 (показано черными кружками на фиг. 49(a)), выход побочного продукта снижался с повышением температуры печи риформинга вплоть до достижения температуры печи риформинга 750°C. Кроме того, было установлено, что когда температура печи риформинга составляла 750°C или выше, побочный продукт не образовывался (выход равен 0%). При добавлении CH2Cl2 в печь риформинга при отношении расходов 1,0 (показано белыми квадратами на фиг. 49(a)), было установлено, что выход побочного продукта снижался с повышением температуры печи риформинга. Кроме того, было установлено, что когда температура печи риформинга составляла 750°C или выше, побочный продукт не образовывался (выход равен 0%). Из приведенных выше результатов следует, что при использовании CH2Cl2 в качестве дополнительного газа можно предотвратить образование побочного продукта (SiCl2), если установить температуру печи риформинга больше или равной 750°C, но меньше 850°C. Кроме того, для случаев, когда время пребывания CH2Cl2 в печи риформинга было установлено равным 0,080 сек (вставлена карбоновая трубка) и 1,0 сек (без вставки карбоновой трубки), измеряли выход (%) побочного продукта (SiCl2) при изменении температуры печи риформинга. В результате было обнаружено, что когда время пребывания в печи риформинга было установлено равным 0,080 сек (показано черным кружками на фиг. 49(b)), выход побочного продукта снижался с повышением температуры печи риформинга вплоть до достижения температуры печи риформинга 975°C. Кроме того, было установлено, что когда температура печи риформинга составляла 975°C, побочный продукт вообще не образовывался (выход равен 0%). В то же время было установлено, что когда температура печи риформинга превышала 975°C, выход побочного продукта чуть повышался (примерно 0,1%). Для случая, когда время пребывания в печи риформинга было установлено равным 1,0 сек (показано черными квадратами на фиг. 49(b)), было обнаружено, что выход побочного продукта снижался с повышением температуры печи риформинга. Кроме того, было установлено, что когда температура печи риформинга была больше или равна 750°C, побочный продукт вообще не образовывался (выход равен 0%). Из приведенных выше результатов было подтверждено, что при использовании CH2Cl2 в качестве дополнительного газа образование побочного продукта (SiCl2) можно предотвратить, если установить время пребывания дополнительного газа в печи риформинга больше или равным 0,080 сек, но меньше 1,0 сек, и установить температуру печи риформинга больше или равной 975°C, но меньше 1100°C. Кроме того, было обнаружено, что образование побочного продукта (SiCl2) можно предотвратить, если установить время пребывания дополнительного газа в печи риформинга больше или равным 1,0 сек и температуру печи риформинга больше или равной 750°C, но меньше 850°C. Далее, как описано выше, чтобы можно было установить время пребывания дополнительного газа в печи риформинга больше или равным 10 сек, сама печь риформинга должна иметь увеличенный размер. Соответственно, если при использовании CH2Cl2 в качестве дополнительного газа установить время пребывания дополнительного газа в печи риформинга больше или равным 1,0 сек, но меньше 10 секунд, а температуру печи риформинга больше или равной 750°C, но меньше 850°C, образование побочного продукта можно предотвратить при одновременном уменьшении размера печи риформинга. Кроме того, измеряли выход (%) побочного продукта (SiCl2) при изменении отношения расходов дополнительного газа (CH2Cl2) и MTS (дополнительный газ/MTS). Было обнаружено, что когда время пребывания CH2Cl2 в печи риформинга установлено равным 0,080 сек, а температура печи риформинга равной 975°C (показано черными кружками на фиг. 49(c)), побочный продукт не образовывался, если отношение расходов (отношение количеств веществ) составляло 1 или больше. Для случая, когда время пребывания CH2Cl2 в печи риформинга было установлено равным 1,0 сек, а температура печи риформинга равной 975°C (показано черными квадратами на фиг. 49(c)), было обнаружено, что выход побочного продукта снижался с увеличением отношения расходов. Кроме того, было установлено, что когда отношение расходов составляло 0,5 или больше, побочный продукт не образовывался. Для случая, когда время пребывания CH2Cl2 в печи риформинга было установлено равным 0,080 сек, а температура печи риформинга равной 750°C (показано белыми квадратами на фиг. 49(c)), было обнаружено, что выход побочного продукта снижался с увеличением отношения расходов. Для случая, когда время пребывания CH2Cl2 в печи риформинга было установлено равным 1,0 сек, а температура печи риформинга равной 750°C (показано белыми квадратами на фиг. 49(c)), было обнаружено, что выход побочного продукта снижался с увеличением отношения расходов. Кроме того, было установлено, что когда отношение расходов составляло 0,25 или больше, побочный продукт не образовывался. Из приведенных выше результатов следует, что образование побочного продукта (SiCl2) можно предотвратить, если установить отношение расходов CH2Cl2 и MTS (CH2Cl2/MTS) больше или равным 0,5. На фигурах 50(a), 50(b) и 50(c) показаны фотографии выпускной трубы (труба, соединенная с выходом печи риформинга) для примеров 5 и 6. Фиг. 50(a) показывает фотографию для случая без добавления дополнительного газа. Фиг. 50(b) показывает фотографию для случая добавления CH3Cl в качестве дополнительного газа. Фиг. 50(c) показывает фотографию для случая добавления CH2Cl2 в качестве дополнительного газа. Фигуры 50(a), 50(b) и 50(c) показывают снимки выпускной трубы для случая, когда температура печи риформинга установлена равной 750°C. Как видно из фиг. 50(a), для варианта без добавления дополнительного газа было установлено, что побочный продукт (SiCl2) скапливался в выпускной трубе. Кроме того, как видно из фиг. 50(b), при добавлении CH3Cl в качестве дополнительного газа было установлено, что осаждается сильнокислое (негорючее) вещество, отличное от SiCl2. Между тем, как показано на фиг. 50(c), при добавлении CH2Cl2 в качестве дополнительного газа не наблюдалось прилипания ни побочного продукта (SiCl2), ни других веществ. Устройство 100 для получения кремниевого композиционного материала На фиг. 51 показано устройство 100 для получения кремниевого композиционного материала в соответствии с данным вариантом осуществления. Как видно из фиг. 51, устройство 100 для получения кремниевого композиционного материала включает реакционную печь 110, участок 120 подачи сырьевого газа, печь риформинга 130 и участок 140 подачи дополнительного газа. На фиг. 51 течение газа показано сплошной стрелкой. Реакционную печь 110 поддерживают при заданной температуре и заданном давлении (пониженное давление). Преформу помещают в реакционную печь 110. Сырьевой газ подают в реакционную печь 110 от участка 120 подачи сырьевого газа. Сырьевой газ содержит метилтрихлорсилан (MTS). В реакционной печи 110 преформа пропитывается карбидом кремния. Газ, выпускаемый из реакционной печи 110, подают в печь риформинга 130 по трубе 112. Печь риформинга 130 способна поддерживать газ, выпускаемый из реакционной печи 110, при температуре больше или равной 200°C и меньше 1100°C. Участок 140 подачи дополнительного газа предназначен для подачи дополнительного газа в печь риформинга 130. Дополнительный газ является одним или более газом, выбранным из группы, состоящей из CH3Cl (хлорметан), CH2Cl2 (дихлорметан), CCl4 (четыреххлористый углерод), C2H3Cl3 (трихлорэтан) и C2HCl3 (трихлорэтилен). Когда дополнительный газ добавляют в газ, выпускаемый из реакционной печи 110, и газ, выпускаемый из реакционной печи 110, поддерживается при температуре больше или равной 200°C, но меньше 1100°C в печи риформинга 130, образование SiCl2 можно предотвратить. Тем самым можно избежать ситуации, когда SiCl2 прилипает к выпускной трубе, соединенной со следующей стадией печи риформинга 130. Соответственно, печь риформинга 130 и выпускную трубу легко промывать. В результате можно снизить нагрузку и расходы на техническое обслуживание выпускного канала реакционной печи 110, и в более широком смысле, можно достичь безопасного ведения работ. Дополнительный газ предпочтительно представляет собой один или оба из CH3Cl и CH2Cl2. Когда дополнительный газ является одним или обоими газами из CH3Cl и CH2Cl2, можно избежать осаждения углерода в выпускной трубе. Кроме того, когда участок 140 подачи дополнительного газа предусмотрен для добавления CH3Cl, печь риформинга 130 выполнена с возможностью поддерживать газ, выпускаемый из реакционной печи 110, и дополнительный газ при температуре больше или равной 750°C, но меньше 850°C. В случае добавления CH3Cl образование SiCl2 можно предотвратить, если установить температуру печи риформинга 130 больше или равной 750°C. Кроме того, при температуре печи риформинга 130 больше или равной 850°C образуется пленка SiC. Соответственно, если при добавлении CH3Cl установить температуру печи риформинга 130 в интервале от 750°C или выше, но меньше 850°C, можно предотвратить образование SiCl2 при одновременном улучшении эксплуатационных качеств печи риформинга 130. Далее, если участок 140 подачи дополнительного газа предназначен для добавления CH3Cl, время пребывания CH3Cl в печи риформинга 130 устанавливают в интервале от 0,2 сек или выше и до 10 секунд. Если установить время пребывания больше или равным 0,2 сек, можно предотвратить образование SiCl2. Кроме того, если установить время пребывания менее 10 секунд, можно уменьшить размеры печи риформинга 130. Кроме того, если участок 140 подачи дополнительного газа предусмотрен для добавления CH3Cl, CH3Cl добавляют так, чтобы отношение (CH3Cl/MTS) расходов CH3Cl и MTS, подаваемого от участка 120 подачи сырьевого газа, было больше или равно 1,0. Этим можно предотвратить образование SiCl2. Между тем, если участок 140 подачи дополнительного газа предусмотрен для подачи CH2Cl2, печь риформинга 130 выполнена с возможностью поддерживать газ, выпускаемый из реакционной печи 110, а также дополнительный газ при температуре больше или равной 750°C, но меньше 850°C. Если при добавлении CH2Cl2 установить температуру печи риформинга 130 больше или равной 750°C, можно предотвратить образование SiCl2. Кроме того, при температуре печи риформинга 130 больше или равной 850°C образуется пленка SiC. Соответственно, если в случае добавления CH2Cl2 установить температуру печи риформинга 130 в интервале от 750°C или более и до менее 850°C, можно предотвратить образование SiCl2 при одновременном улучшении эксплуатационных качеств печи риформинга 130. В этом случае время пребывания CH2Cl2 в печи риформинга 130 устанавливают в интервале от 0,2 сек или больше, но меньше 10 сек. При установке времени пребывания больше или равным 0,2 сек можно предотвратить образование SiCl2. Кроме того, если установить время пребывания меньше 10 сек, можно уменьшить размеры печи риформинга 130. Кроме того, если участок 140 подачи дополнительного газа предусмотрен для добавления CH2Cl2, CH2Cl2 добавляют так, чтобы отношение (CH2Cl2/MTS) расходов CH2Cl2 и MTS, подаваемого от участка 120 подачи сырьевого газа, было больше или равно 0,25, предпочтительно больше или равно 0,5. Этим можно предотвратить образование SiCl2. Кроме того, в печи риформинга 130 можно разместить отражательную перегородку. Фиг. 52 иллюстрирует пример модифицированной печи риформинга 130. Как показано на фиг. 52, корпус 132 печи риформинга 130 имеет трубчатую форму (например, форму трубы круглого сечения). Корпус 132 является печью с горячими стенками, обогреваемой снаружи нагревательным устройством (не показано). Внутри корпуса 132 расположено множество отражательных перегородок 134. Все отражательные перегородки 134 представляют собой полукруглую пластину, проходящую от внутренней периферийной поверхности корпуса 132 до его середины. Отражательные перегородки 134 размещены в корпусе 132 в разных местах в направлении течения газа (в направлении оси корпуса 132). Кроме того, соседние отражательные перегородки 134 размещены в корпусе 132 так, чтобы их точки контакта с корпусом 132 были разными. В результате размещения отражательных перегородок 134 газ, выпускаемый из реакционной печи 110, и дополнительный газ могут эффективно перемешиваться друг с другом. Соответственно, можно предотвратить образование SiCl2. Как описано выше, устройство 100 для получения кремниевого композиционного материала в соответствии с данным вариантом осуществления позволяет предотвратить образование SiCl2 благодаря использованию простой схемы добавления дополнительного газа. Вариант осуществления был описан выше с обращением к прилагаемым чертежам, однако настоящее изобретение, разумеется, не ограничено этим вариантом осуществления. Очевидно, что специалисты в данной области могут придумать различные изменения и модификации в рамках формулы изобретения, и эти изменения и модификации истолковываются как естественным образом охватываемые техническим объемом настоящего изобретения. Например, в вышеописанном варианте осуществления, когда участок 140 подачи дополнительного газа в устройстве 100 для получения кремниевого композиционного материала предусмотрен для добавления CH2Cl2, печь риформинга 130 выполнена с возможностью поддерживать газ, выпускаемый из реакционной печи 110, а также дополнительный газ при температуре больше или равной 750°C, но меньше 850°C. Однако, когда участок 140 подачи дополнительного газа предназначен для добавления CH2Cl2, печь риформинга 130 может поддерживать газ, выпускаемый из реакционной печи 110, а также дополнительный газ при температуре, больше или равной 975°C, но меньше 1000°C. В этом случае желательно устанавливать время пребывания CH2Cl2 в печи риформинга 130 больше или равным 0,080 сек, но меньше 0,2 сек. Тем самым можно предотвратить образование SiCl2. Кроме того, при описании вышеуказанного варианта в качестве примера была взята конфигурации, в которой устройство 100 для получения кремниевого композиционного материала включает участок 140 подачи дополнительного газа. Однако участок 140 подачи дополнительного газа не является существенным компонентом. Когда устройство для получения кремниевого композиционного материала не содержит участка 140 подачи дополнительного газа, желательно выполнить печь риформинга 130 так, чтобы она поддерживала газ, выпускаемый из реакционной печи 110, при заданной температуре больше или равной 500°C, но меньше 950°C. Тем самым можно предотвратить образование SiCl2. Промышленная применимость Настоящее изобретение применимо к способу получения кремниевого композиционного материала и к устройству для получения кремниевого композиционного материала. Список позиций
Реферат
Изобретение может быть использовано в химической промышленности. Способ получения композиционного материала на основе карбида кремния включает стадии: выдерживания преформы из карбида кремния в реакционной печи; подачу сырьевого газа, содержащего метилтрихлорсилан, в реакционную печь для пропитки преформы карбидом кремния; контроль и снижение температуры газа, выпускаемого из реакционной печи, с заданной скоростью. Предложенная группа изобретений обеспечивает снижение образования жидкого или твердого побочного продукта из газа. 2 н. и 39 з.п. ф-лы, 6 пр., 52 ил., 3 табл.
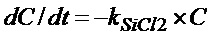
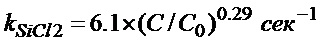
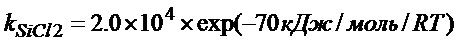
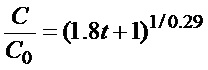
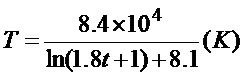
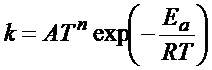

Комментарии