Способ получения металлического магния, способ получения чистого оксида магния (варианты) и способ переработки исходного материала - RU2109078C1
Код документа: RU2109078C1
Чертежи








Описание
Изобретение относится к способам переработки исходного материала, выбранного из группы, состоящей из оксида магния, содержащего незначительные количества оксидов Fe, Si, Ca и Al природных и промышленно полученных магнийсиликатных минералов и их смесей, например оливина, путем углеродотермического восстановления и к способам производства металлического магния, чистого оксида магния (MgO) и огнеупорных масс, состоящих из MO, Mg2 SiO4 и SiC, путем углеродотермического восстановления исходных материалов, выбранных из вышеприведенной группы.
1. Магний.
В общем металлический магний получают посредством электролитических и термических способов. При применении термических способов в качестве исходных материалов используют две группы минералов/горных пород.
Первая группа, в которой оксид магния связан с диоксидом углерода, включает, например, минералы магнезит и доломит.
Вторая группа, в которой оксид магния связан с диоксидом кремния, включает, например, минерал оливин.
Хотя минералы во второй группе, например оливин, встречаются в большом количестве отложений и имеют высокое содержание магния, в промышленности для производства магния используют главным образом магнезит и доломит, т.е. исходные материалы из первой группы.
Это обусловлено тем фактом, что было найдено, что можно более легко удалить и отделить CO2 из членов первой группы, чем удалить и отделить SiO2 из членов второй группы.
В общем для удаления и отделения SiO2 из второй группы было предложено два класса способов: мокрые методы, в которых руды обрабатывают сильными минеральными кислотами, и прямые методы восстановления, в которых магнийоксидный компонент руды восстанавливают и удаляют в виде газообразного Mg.
Прямые методы можно разделить на две группы. В первой группе прямых методов восстановления, которые предлагались только в связи с восстановлением оксидов металлов, т. е. несиликатов металла, использовали восстановители, образующие газообразные продукты реакции, содержащие кислород, например восстановление MgO углеродом в качестве восстановителя при атмосферном давлении и температуре 1850oC приводит к образованию Mg и CO в качестве газообразного продукта реакции, содержащего кислород, или применяли другие способы углеродотермического восстановления [например, USPS N 2268779 (SEIFERT) и US PS NN 2582119 и 2582120 (HANSGIRG)].
Когда смесь силиката магния, например оливина (Mg2-xFexSiO4; SiO4; x:0 - 1), и углерода нагревают до температуры в интервале 1300 - 2200oC, происходят следующие реакции:
(1) (Mg2-xFex)
SiO4(тв) + (1 + x(1 + 2)) C(тв) <-> (2 - x)MgO(тв) + (1 - zx) SiO (г) + (1 + x(1 +z)) CO (г) + x''SizFe'' (сплав Si и Fe)
(1') Mg2SiO4
(тв) + 3 C (тв) < - > 2MgO (тв) + SiC (тв) + 2 CO (г)
(1'') Mg2SiO4(тв) + 3 C (тв) < - > 2Mg (г) + SiO (г) + 3 CO (г)
(1''') Mg2SiO4 (тв) + 5C (тв) < - > 2Mg (г) + SiC (тв) + 4 CO (г)
(2) MgO (тв) + C (тв) < - > Mg (г) + CO (г)
(3) SiO (г) + C (тв) <
- > Si (тв/ж) + CO (г)
(4) Si (тв/ж) + C (тв) < - > SiO (тв)
где
(тв), (ж) и (г) обозначают соответственно твердую, жидкую и газообразную фазы.
При возрастании температуры и уменьшении давления эти равновесия кроме равновесия (4) сдвигаются вправо.
Подобные реакции происходят при углеродотермическом восстановлении MgO, содержащего примеси, например оксидов Fe, Si, Ca и Al, и который в последующем будет отнесен в "сырому MgO".
Благодаря образованию газообразных компонентов Mg (г) и SiO (г), может происходить перемещение Mg и SiO в пределах реакционной смеси и Mg и SiO можно даже удалить из нее путем испарения.
Таким образом, твердый Mg можно собрать путем конденсации испарившегося металлического Mg в отдельной зоне конденсации, т.е. в конденсаторе, расположенном на расстоянии от реакционной смеси.
Проблема, неотъемлемо связанная с первой группой прямых методов, заключается в возможности обратной реакции [см. уравнение (2)], между магнием и продуктом реакции, содержащим газообразный кислород, посредством чего магний окисляется до оксида магния.
Данную проблему можно решить во второй группе прямых методов при использовании восстановителей, которые образуют негазообразные продукты реакции, например при восстановлении магнийсодержащих руд кремнием, алюминием, карбидом кальция или карбидом кремния.
Методы, принадлежащие ко второй группе прямых методов восстановления, представлены в ряде описаний к патентам например, N 2372571, 2379576, 2527722, 2527724 и 2570232 (HANSGIRG), а также используются на практике, например в способе HANSGIRGA, упомянутом выше, способах Pilgeona и Bolzana (реакция между обожженным доломитом и ферросилицием при температуре около 1200oC и пониженным давлением) и в магнийтермическом способе (восстановление обожженного доломита ферросилицием в присутствии оксида алюминия при температуре около 1600oC и давлении 4 КРа).
В способах, относящихся к предшествующему уровню техники, предлагались другие различные решения
проблемы избежания обратной реакции: в связи с углеродотермическим восстановлением MgO, например, следующим образом:
свести к минимуму обратную реакцию выходящего газа, получающегося при
углеродотермическом восстановлении MgO путем
мгновенного резкого охлаждения газа, выходящего из углеродотермической зоны, например ударного охлаждения путем инжектирования охлаждающей среды
или путем быстрого адиабатического охлаждения (см. например, US PS NN 2582119 и 2582129 (HANSGIRC), описание Европейской заявки на патент N 75836 (AVERY) и US PS N 4200264 (HORI) или
осаждения Mg при пониженном давлении (см. например, DE PS N 49329 (KNOFLER), US PS N 2257910 (KIRK) и Trans. Insti. Min. Metal. 99, May-August 1990, с. 105-111 (WINAND et al).
При углеродотермическом восстановлении силикатов магния количество полученного CO возрастает пор сравнению с количеством CO, полученного при углеродотермическом восстановлении оксида магния, потому что CO получается не только при восстановлении MgO, но также и при восстановлении SiO2.
Если во время углеродотермического восстановления Mg2SiO4 увеличить давление, из реакционной смеси будут испаряться возрастающие количества SiO, что приведет к увеличению соотношения SiO/Mg в газе, выходящем из реакционной смеси.
Первая задача, которую
необходимо решить с помощью предлагаемого изобретения, состоит в обеспечении углеродотермического способа получения Mg из исходных материалов, выбранных из группы, состоящей из оксиды магния,
содержащего незначительные количества оксидов Fe, Si, Ca и Al; природных и промышленно полученных магнийсиликатных материалов и их смесей, например оливина, при использовании которого избегают
загрязнения конечного магниевого продукта
(I) MgO и C, полученными посредством вышеупомянутой обратной реакции; и
(II) продуктами конденсации, получающимися из SiO, например Mg2SiO4, S, SiC, SiO2 и т.д.
2. Оксид магния
В соответствии с предшествующим уровнем техники сырой оксид магния, т.е. оксид магния, содержащий
примеси, например оксиды Fe, Si, Ca и Al, получают путем обжатия гидроксида магния, карбоната магния или основного карбоната магния.
Гидроксид магния получают в большом масштабе из морской воды с помощью способа, в котором Mg (OH)2 осаждают путем добавления гидроксида кальция.
Осажденный гидроксид магния обычно содержит в качестве примесей следовые количества оксидов B, Ca, Si, Al и Fe. Эти загрязняющие примеси оказывают вредное воздействие на поведение оксида магния во время спекания и при последующих применениях, в связи с чем были предприняты значительные усилия для удаления этих примесей, что привело к высоким расходам, связанным с переработкой.
Высокочистый оксид магния получают при расплавлении оксида магния (MgO) путем электродуговой плазмы.
В этом способе, который описан, например, в Radex Rundshau 1958, Heft 2, p.91-104 (EIPELTAUER et al), очистки MgO достигают вследствие миграции примесей через жидкую или газообразную фазу в направлении поверхности перед и после охлаждения расплавленной загрузки MgO. После затвердевания привесные частицы твердого блока MgO удаляют механическими средствами.
Таким образом, когда используют этот способ, кроме неотъемлемых высоких расходов энергии, необходимых для расплавления MgO, получают относительно высокое соотношение отходов производства к продукту.
Кроме того, известно получение тонкого порошка оксида магния (периклаза), подходящего для производства качественной керамики, с помощью способа, в котором металлический магний испаряют при 700oC или выше в потоке инертного газа и смешивают с кислородсодержащим газом для обеспечения потока реакционной смеси, в котором пары магния окисляются до тонких частиц оксида магния, которые собирают из реакционной смеси, например с помощью фильтра [см. заявку GB (Великобритания) на патент N 2183622 (YOSHIDA).
Недостатками способов производства высокочистого оксида магния в предшествующей области заключаются в необходимости использования в качестве исходного материала дорогостоящего магния.
Вторая задача, которую можно решить с помощью предлагаемого изобретения, состоит в обеспечении способа получения высокочистого магния из недорогостоящих исходных материалов, при этом высокочистый продукт окись магния по существу не содержит оксиды Ca, Si, Al и Fe.
3. Переработка силикатов магния.
Хорошо известно, что огнеупорные материалы получают путем спекания порошка оливина при температуре в интервале 1540 - 1710oC в окислительных условиях и при атмосферном давлении. Чтобы избежать образования легкоплавких фаз, содержание оксидов кальция, алюминия и железа в исходном оливине должно быть достаточно низким, обычно менее чем 7 мас.% (см. Ullmann Encyklopadie der Technischen chemie, 4th Edition, v. II p. 561 -562), но даже когда используют эти количества оливина, полученный спеченный продукт не может быть классифицирован как огнеупорный материал, обладающий высокими эксплуатационными качествами.
SiC является примером огнеупорного материала с высокими эксплуатационными качествами. Он может быть получен в электрической ночи путем восстановления SiO2 углеродом при температуре около 2200 - 2400o C.
Оксид магния технического срока может быть, кроме того, обработан путем спекания при температуре до 1900oC до получения обожженного намертво оксида магния, который является важным огнеупорным материалом, используемым при производстве стали.
Возрастающая потребность в огнеупорных материалах с высокими эксплуатационными качествами, используемых в современном производстве стали, переключила потребности рынка на числе высокоплотные спекшиеся материалы.
Третья задача, которую можно решить с помощью предлагаемого изобретения, состоит в обеспечении простого и недорогостоящего способа получения огнеупорных материалов с высокими эксплуатационными качествами, в котором используют недорогостоящее сырье, выбранное из группы, состоящей из оксида магния, содержащего незначительные количества оксиды Fe, Si, Ca и Al, природных и промышленно полученных магнийсиликатных минералов; и их смесей, например оливина.
Кроме того, желательно обеспечить общий способ переработки членов вышеупомянутой группы, позволяющий извлечь ценные металлические элементы, содержащиеся в магнийсиликатных горных породах и минералах в низких концентрациях, например Mn, Cr, Ni, Au, и члены группы платины.
2. Магний
Предлагаемое изобретение доказывает, что первую задачу можно решить с помощью способа
получения металлического магния путем углеродотермического восстановления исходного материала, выбранного из группы, состоящей из оксида магния, содержащего незначительные количества оксидов Fe, Si,
Ca и Al; природных и промышленного полученных магнийсиликатных минералов; и их смесей, например оливина, который включает:
смешивание исходного материала с углеродом в количестве: по крайней
мере 1 моль C/моль SiO2 плюс по крайней мере 1 моль C/моль FeO плюс по крайней мере 1,3 моль C/моль Fe2O3 плюс по крайней мере 1 моль C/моль MgO;
предпочтительно в количестве по крайней мере 2 моль C/моль SiO2 плюс по крайней мере 1 моль C/моль FeO плюс по крайней мере 1,3 моль C/моль Fe2O3 плюс по крайней мере
1 моль C/моль MgO;
в особенности в количестве по крайней мере 3 моль С/моль SiO2 плюс 1 моль C/моль FeO плюс 1,3 моль С/моль Fe2O3 плюс 1 моль С/моль MgO;
предпочтительно в количестве менее, чем 4 моль C/моль SiO2 плюс 2 моль С/моль FeO плюс 4 моль С/моль Fe2O3 плюс 2 моль С/моль MgO;
нагревание смеси в
восстановительной зоне до температуры Tr в интервале 1400-1700oC, предпочтительно менее чем 1500oC, при давлении pr 0,01-1,75 кPa, предпочтительно 0,2-1,1, в частности
0,3-0,7 кPa;
восстановление оксида железа, содержащегося в исходном материале, в восстановительной зоне до железа;
восстановление диоксида кремния, содержащегося в исходном материале,
до SiO, который частично превращается в SiC и сплав Si и Fe, "SizFe" в восстановительной зоне, частично испаряется из восстановительной зоны и превращается в SiC, Si и/или Mg2
SiO4 путем взаимодействия с углеродом в отдельной первой зоне конденсации при давлении p1 в интервале 0,01-1,1 kPa, предпочтительно 0,2-0,8, в частности 0,3-0,7 кРа, при
температуре T1 выше чем:

где p1 выражено в кРа,
и ниже (Tмин+100oC), предпочтительно (Tмин + 50oC), в частности (Tмин + 25oC) и в любом случае ниже Tr;
восстановление оксида магния исходного материала до газообразного металлического магния в восстановительной зоне;
испарение упомянутого газообразного металлического магния из восстановительной зоны и конденсацию газообразного металлического магния в отдельной второй зоне конденсации, расположенной за первой зоной конденсации, при давлении p2 внутри интервала 0,01-1,1 кPa, предпочтительно 0,2-0,8, в частности 0,3-0,7 кPa, при температуре T2 менее чем 638oC, предпочтительно в интервале 200-600, в частности в интервале 250-540oC;
удаление CO, образованного посредством вышеупомянутых способов восстановления, из второй зоны конденсации и поддержание давления p2 при предварительном выбранном значении путем использования насоса;
посредством чего температурный градиент между первой зоной конденсации и второй зоной конденсации поддерживают настолько большим, насколько это возможно;
посредством чего p2≤ p1 ≤pr.
Основная мысль первого аспекта изобретения состоит в регулировании способов переноса газообразного магния и SiO путем углеродотермической реакции сырого оксида магния магнийсиликатных минералов, как минералов, т.е. регулировании местонахождения образования продуктов и побочных продуктов путем выбора соответствующих значений и градиентов следующих параметров процесса: давления (значения и градиента), температуры (значения и градиента) и процентного содержания углерода в загрузке (значения) в реакционной зоне и в первой и второй зоне конденсации.
Испарившийся материал извлекают путем конденсации при пониженных температурах. Таким образом, испарившийся SiO (г) извлекают по существу в виде Si (тв) или SiC (тв) в
сконструированном подходящим образом первом конденсаторе, работающем при температуре ниже, чем температура слоя, и выше, чем температура (Tмин), где MgO (тв) может образовываться путем
обратной реакции в соответствии с
(2) Mg(г)+CO(r) _→ MgO(тв)+C(тв).
Испарившийся M (г) можно затем извлечь в сконструированном подходящим образом втором конденсаторе,
работающем при температуре ниже Tмин в виде Mg (тв), при этом обратной реакции (2') избегают посредством работы при низком давлении и посредством поддержания большого температурного
градиента между первым и вторым конденсатором.
При этом выгодно использовать 5 молей углерода (C) или более на каждую молекулу оливина (Mg2SiO4), когда целью являются получение чистого Mg (тв), хорошо отделенного от кремний содержащих фаз путем углеродотермического превращения оливина.
Реакция будет происходить в соответствии с

Это обеспечивает полное испарение магния и максимальное удержание кремния в слое в виде карбида кремния (и SizFe, когда присутствует железо). Таким образом, количество SiO (г), которое будет сконденсировано в виде Si (тв) или SiC в первом конденсаторе, будет возможно очень незначительным.
Предлагаемое изобретение, касающееся получения чистого M (тв), основано на очистке газовой фазы, образованной путем углеродотермической переработки магнийсиликатных материалов и горных пород,
а также загрязненного оксида магния, путем конденсации испарившегося SiO (г) в виде Si (тв) или SiC (тв) в сконструированном подходящим образом первом конденсаторе. Это наиболее эффективно
осуществляют путем образования SiC (тв) в соответствии с
(3) SiO+2C _→ SiC+CO
при температуре выше Tмин, где MgO (тв) может образовываться путем обратной
реакции между Mg (г) и CO (г). Tмин определяют с помощью следующего уравнения (Pобщ в кРа):
TминoC = -32217(2log (Pобщ) - 19,
92)-1- 273,15
Как упоминалось выше, SiO взаимодействует с углеродом в первой зоне конденсации. Упомянутой зоне выгодно придают форму одиночной трубы или ее выполняют в виде
множества параллельно расположенных труб, выполненных из химически активного углерода или покрытых химически активного углерода или покрытых химически активным углеродом.
Исходными
материалами, подходящими для использования в вышеупомянутом способе, являются:
сырой оксид магния, т.е. оксид магния, содержащий незначительное количество примесей, например оксиды Fe, Si, Ca
и Al;
силикаты магния, т. е. природные и промышленно полученные магнийсиликатные минералы.
Сырой оксид магния содержит обожженные (обработанные нагревом при температуре приблизительно 1000oC) соединения, полученные из магнезита, брусита, кизерита или подобные промышленно полученные материалы, например отработанную футеровку печи, выполненную из периклаза, или пыли фильтров с фабрик обжига магнезита.
Сырой оксид магния содержит более 50% MgO, в частности более 80% MgO. Предпочтительно содержание CaO будет составлять менее 1%, в частности менее 0,5%.
Предпочтительно содержание щелочных металлов будет составлять менее 1%, в частности менее 0,3% в пересчете на оксиды.
Предпочтительно сумма других летучих элементов, например S и Cl, и металлов, подобных Zn, Cd, Hg и т.д., будет менее 1%, в частности менее 0,5%.
Силикаты магния включают природные или обожженные (обработанные нагревом при 1000oC) силикатные минералы, например оливины, серпентины, вермикулиты, антофиллиты, кумингтониты, энстатиты, пиропы, шпинели и подобные промышленно полученные соединения, содержащие Mg в качестве основного компонента, которые определены ниже.
Предпочтительно силикаты магния содержат более 25% MgO, в частности более 40% MgO.
Предпочтительно содержание CaO составляет менее 1%, в частности менее 0,5%.
Предпочтительно содержание щелочных металлов составляет менее 1%, в частности менее 3% в пересчете на оксиды.
Если содержание Al2O3 выше чем 3%, температура реакции в восстановительной зоне должна быть менее 1550oC для того, чтобы избежать образования карбида алюминия.
Предпочтительно сумма других летучих элементов, например S и Cl и металлов, подобных Zn, Cd, Hg и т.д., должна быть менее 1%, в частности менее 0,5%.
Силикаты магния, кроме того, включают природные горные породы, состоящие из более чем 50% силикатов магния, которые определены выше, предпочтительно из более чем 80%, в частности горные породы, состоящие из более чем 90% силикатов, и промышленные отходы, богатые силикатом магния высокого качества, например использованные форстеритовые футеровки печи.
В настоящем контексте термин "углерод" включает материалы, богатые углеродом, например антрацит, углеродную сажу и кокс.
Эти богатые углеродом материалы в общем имеют следующий состав,%:
Содержание углерода - > 90
Зольность - < 2
Летучие компоненты - < 8
Предпочтительно:
Содержание углерода - > 96
Зольность - < 1
Летучие компоненты
- < 3
В частности
Содержание углерода - > 98,5
Зольность - < 0,5
Летучие компоненты - < 1
Исходный материал предпочтительно
измельчают до средней крупности частиц, менее чем 45 мкм. Материал, богатый углеродом, имеет предпочтительно среднюю крупность частиц около 100 нм. Реакционную смесь вводят предпочтительно в
восстановительную зону в виде брикетов, имеющих пористость около 57%.
Большой температурный градиент между первой и второй зоной конденсации может быть получен посредством методов закалки, предложенных для использования в углеродотермическом способе переработки, который описан в описании патента, обсужденного выше.
В соответствии с предпочтительными
вариантами:
большой температурный градиент между первой и второй зоной конденсации обеспечивают путем быстрого охлаждения, включающего введение газа из первой зоны конденсации в рассеивающее
сопло, работающее в условиях недостаточного расширения, эжектирование смешанного газа через рассеивающее сопло и создание возможности смешанному газу адиабатически расширяться при сверхзвуковой
скорости, вследствие чего коэффициент расширения в сопле выбирают в интервале 12,5-2, предпочтительно в интервале 12,5-6;
диоксидкремниевый компонент исходного материала превращают в
реакционной смеси по существу в SiO путем использования добавленного углерода в количестве, взятом в интервале 3-4 моль С/моль SiO2 плюс 1-2 моль C/моль FeO, плюс 3-4 моль C/моль Fe2O3, плюс 1-2 моль C/моль MgO;
температурный градиент между восстановительной зоной и первой зоной конденсации поддерживают настолько большим, насколько это возможно;
в качестве исходного материала используют оксид магния, содержащий незначительные количества оксидов Fe, Si, Ca и Al;
в качестве исходного материала используют оливин;
когда
содержание Al2O3 в исходной реакционной смеси более 1 мас.%, Tr менее чем 1550oC;
"SizFe" и металлическое железо отделяют от остатка в
восстановительной зоне традиционными способами, например магнитным или электростатическим разделением или флотацией, после чего Au и переходные элементы, например Mn, Cr, Ni, и металлы из платиновой
группы извлекают общепринятыми способами, например выщелачиванием;
SiС, образованный в восстановительной зоне и первой зоне конденсации, извлекают в виде побочного продукта из остатка
соответственно в восстановительной зоне и первой зоне конденсации.
Извлеченный SiС представляет микропродукт высокой чистоты.
Магний в зависимости от условий во второй зоне конденсации может осаждаться в виде макрокристаллов, а также в виде пирофорной массы, которую можно расплавить и сформовать в слитки общепринятыми способами.
2. Оксид магния.
Кроме того, было найдено, что вторую задачу можно решить способом получения чистого оксида магния путем углеродотермического восстановления исходного материала, выбранного из группы,
состоящей из оксида магния, содержащего незначительные количества оксидов Fe, Si, Ca и Al, природных и промышленно полученных магнийсиликатных минералов и их смесей, например оливина, который
включает:
смешивание исходного материала с углеродом в количестве по крайней мере 1 моль С/моль SiO2 плюс по крайней мере 1 моль С/моль FeO плюс по крайней мере 3 моль С/моль
Fe2O3 плюс по крайней мере 1 моль С/моль MgO;
предпочтительно в количестве по крайней мере 2 моль С/моль SiO2 плюс по крайней мере 1 моль С/моль FeO плюс по
крайней мере 3 моль С/моль Fe2O3 плюс по крайней мере 1 моль С-моль MgO, в частности в количестве по крайней мере 3 моль С/моль SiO2 плюс 1 моль С/моль FeO плюс 3 моль
С/моль Fe2O3 плюс 1 моль С/моль MgO, предпочтительно в количестве менее чем 4 моль С/моль SiO2 плюс 2 моль С/моль FeO плюс 4 моль С/моль Fe2O3
плюс 2 моль С/моль MgO;
нагрев смеси в восстановительной зоне до температуры Tr в интервале 1400 - 1700oC, предпочтительно менее чем 1500oC, при давлении
pr в интервале

предпочтительно

в частности
0,3 - 1,75 kPa;
восстановление железооксидного компонента в реакционной смеси до железа;
восстановление диоксидкремниевого компонента исходного материала до SiO, который частично превращают в восстановительной зоне в SiC и сплав SiC, Si и/или Mg2SiO4 путем взаимодействия с углеродом в отдельной первой зоне конденсации при давлении p1, где p1 ≤ pr и при температуре T1 выше чем

где
p1 выражено в kPa, и ниже чем (Tмин + 100oC), предпочтительно (Tмин + 50oC), в частности (Tмин + 25oC), и в любом случае ниже Tr;
восстановление магнийоксидного компонента исходного материала, по крайней мере частично, до газообразного металлического магния в восстановительной зоне;
испарение газообразного металлического магния из восстановительной зоны и взаимодействие газообразного металлического магния с CO, образованным в восстановительной зоне, до MgO и C, и осаждение этих продуктов реакции в виде смеси углерода и оксида магния в отдельной зоне окисления и зоне конденсации, расположенной за первой зоной конденсации, при давлении p2, где p2 ≤ p1, и при температуре T2 в интервале от 638oC до T1, предпочтительно от 650oC до T1 - 50, в частности 800 - 1000oC;
удаление смеси углерода и оксида магния из зоны окисления и конденсации и удаление углерода из удаленного продукта, например окислением;
удаление той части CO, которая была образована в результате вышеупомянутых способов восстановления, и не расходуется при реакции с Mg, из зоны окисления и конденсации и поддержание давления p2 при предварительно выбранном значении путем использования насоса;
посредством чего p2 ≤ p1 ≤ pr.
Кроме того было найдено, что вторая задача может быть также решена способом производства чистого оксида магния путем углеродотермического восстановления исходного материала, выбранного из
группы, состоящей из оксида магния, содержащего незначительные количества оксидов Fe, Si, Ca и Al, природных и промышленно полученных магнийсиликатных минералов, и их смесей, например оливина, который
включает:
смешивание исходного материала с углеродом в количестве по крайней мере 1 моль С/моль SiO2 плюс по крайней мере 1 моль С/моль FeO плюс по крайней мере 3 моль С/моль
Fe2O3 плюс по крайней мере 1 моль С/моль MgO, предпочтительно в количестве по крайней мере 2 моль С/моль SiO2 плюс по крайней мере 1 моль С/моль FeO плюс по крайней
мере 3 моль С/моль Fe2O3 плюс по крайней мере 1 моль С/моль MgO, в частности в количестве по крайней мере 3 моль С/моль SiO2 плюс 1 моль С/моль FeO плюс 3 моль С/моль
Fe2O3 плюс 1 моль С/моль MgO, предпочтительно в количестве менее, чем 4 моль С/моль SiO2 плюс 2 моль С/моль FeO, плюс 4 моль С/моль Fe2O3: плюс 2
моль С/моль MgO;
нагрев смеси в восстановительной зоне до температуры Tr в интервале 1400 - 1700oC, предпочтительно менее чем 1500oC, при давлении pr в интервале

предпочтительно

в частности
0,3 - 1,75 kРа;
восстановление железооксидного компонента исходного материала в восстановительной зоне до железа;
восстановление диоксидкремниевого компонента исходного материала до SiO, который частично превращают в восстановительной зоне в SiC и сплав Si и Fe, SizFe частично испаряют из восстановительной зоны и превращают в SiC, и/или Mg2SiO4 путем взаимодействия с углеродом в отдельной первой зоне конденсации при давлении p1, где p1 ≤ pr и при температуре выше, чем

где
p1 выражено в kPa, и ниже (Tмин + 100oC), предпочтительно (Tмин + 50oC), в частности (Tмин + 25oC) и в любом случае ниже Tr;
восстановление магнийоксидного компонента исходного материала, по крайней мере частично, до газообразного металлического магния в восстановительной зоне;
испарение упомянутого газообразного металлического магния из восстановительной зоны и взаимодействие газообразного металлического магния с отдельно добавленным кислородсодержащим газом, например молекулярным кислородом, воздухом, CO2, CO, H2O и их смесями, до образования оксида магния и осаждения оксида магния в отдельной зоне окисления и конденсации, расположенной после первой зоны конденсации, при давлении p2, где p2 ≤ p1, и при температуре T2 в интервале от 638oC до T1, предпочтительно от 650oC до T1 - 50, в частности от 800 - 1000oC;
удаление оксида магния из зоны окисления и конденсации и, если необходимо, удаление углерода из удаленного продукта путем окисления;
удаление газов, образованных при вышеупомянутых процессах восстановления и окисления, из зоны окисления и конденсации и поддержание давления p2 при предварительно выбранном значении путем использования насоса;
посредством чего P2 ≤ p1 ≤pr.
Основная мысль второго аспекта изобретения является по существу той же самой, что и первого.
Испарившийся материал извлекают путем конденсации при пониженных температурах. Таким образом, испарившийся SiO (г) может быть извлечен в виде SI (тв) в
сконструированном соответствующим образом первом конденсаторе, работающем при температуре ниже температуры слоя и выше чем температура (Tмин), где MgO (тв) может образоваться посредством
обратной реакции в соответствии с
(2′) Mg(г)+CO(r) _→ MgO(тв)+C(тв).
Испарившийся Mg (г) может быть затем извлечен в сконструированном соответствующим образом
втором конденсаторе, работающем при температуре ниже Tмин, или в виде MgO (тв), смешанного с C (тв) в соответствии с обратной реакцией, приведенной выше, или в виде MgO (тв), когда отдельно
добавляют молекулярный кислород, воздух, CO, H2O и их смеси.
Выгодно использовать 5 моль углерода (C) или более на каждый моль оливина (Mg2SiO4), когда целью является получение чистого Mg (тв) или MgO (тв), хорошо отделенного от кремнийсодержащих фаз путем углеродотермического превращения оливина.
Реакция будет происходить в
соответствии с

Это обеспечивает полное испарение магния и максимальное удержание кремния в слое в виде карбида кремния (и "SizFe", когда присутствует железо). Таким образом, количество SiO (тв), которое конденсируется в виде Si (тв) или SiC в первом конденсаторе, будет возможно очень незначительным.
Предлагаемое изобретение, касающееся производства чистого MgO (тв), основано на очистке газовой фазы, образованной при углеродотермической переработке
магнийсиликатных минералов и горных пород, а также загрязненного оксида магния путем конденсации испарившегося SiO (г) в виде Si (тв) или SiC (тв) в сконструированном соответствующим образом первом
конденсаторе. Это наиболее эффективно осуществляют путем образования SiC (тв) в соответствии с
SiO + 2C _→ SiC + CO
при температуре выше Tмин, где MgO (тв)
может образоваться путем обратной реакции между Mg (г) и CO (г). Tмин определяют с помощью следующего уравнения (Pобщ в kPa):
TминoC =
-32217 (2log (Pобщ - 19,92-1 - 273,15.
Как упоминалось выше, SiO взаимодействует с углеродом в первой зоне конденсации. Упомянутую зону выгодно выполняют в виде одиночной трубы или в виде множества параллельно расположенных труб, изготовленных из химически активного углерода или покрытых химически активным углеродом.
Исходными материалами,
подходящими для использования в вышеупомянутом способе, являются:
сырой оксид магния, т.е. оксид магния, содержащий незначительные количества примесей, например оксиды Fe, Si, Ca и Al;
силикаты магния, т.е. природные или промышленно полученные магнийсиликатные минералы.
Сырой оксид магния включает обожженные (обработанные нагревом при температуре приблизительно 1000oC) соединения, полученные из магнезита, брусита, низерита или подобные промышленно полученные материалы, например отработанную футеровку печи, выполненную из периклаза, и пыли фильтров с фабрик обжига магнезита.
Сырой оксид магния содержит более чем 50% MgO, в частности более 80% MgO. Предпочтительно содержание CaO будет составлять менее 1%, в частности менее 0, 5%.
Предпочтительно содержание щелочных металлов будет составлять менее 1%, в частности менее 0,3% в пересчете на оксиды.
Предпочтительно сумма других летучих элементов, например S и Cl, и металлов, подобных Zn, Cd, Fe и т.д., будет составлять менее 1%, в частности менее чем 0,5%.
Силикаты магния включают природные или обожженные (обработанные нагревом при 1000oC) силикатные минералы, например оливины, серпентины, вермикулиты, антофиллиты, нумингтониты, энстатиты, пиропы, шпинели и подобные промышленно полученные соединения, содержащие Mg в качестве основного компонента, которые определены ниже.
При этом предпочтительно силикаты магния содержат более чем 25% MgO, в частности более чем 40% MgO.
Предпочтительно содержание CaO составляет менее 1%, в частности менее чем 0,5%.
Предпочтительно содержание щелочных металлов составляет менее 1%, в частности менее 0,3% в пересчете на оксиды.
Если содержание Al2O3 выше, чем 3%, температура реакции в восстановительной зоне должна быть менее 1550oC для того, чтобы избежать обрезания карбида алюминия.
Предпочтительно сумма других летучих элементов, например S и Cl, и металлов, подобных Zn, Cd, Hg и т.д., должна быть менее чем 1%, в частности менее чем 0, 5%.
Силикаты магния, кроме того, включают природные горные породы, состоящие из более чем 50% силикатов, которые определены выше, предпочтительно из более чем 80%, в частности горные породы, состоящие из более чем 90% силикатов, и промышленные отходы, богатые силикатом магния высокого качества, например использованные форстеритовые футеровки печи.
В настоящем контексте термин "углерод" включает материалы, богатые углеродом, например антрацит, углеродную сажу и кокс.
Эти богатые углеродом материалы в общем имеют следующий состав,%:
Содержание углерода - >90
Зольность - <2
Летучие компоненты - <8
Предпочтительно:
Содержание углерода - >96
Зольность - <
1
Летучие компоненты - <3
В частности:
Содержание углерода - >98,5
Зольность - <0,5
Летучие компоненты - <1
Исходный
материал предпочтительно измельчают до средней крупности частиц, менее чем 45 мкм. Материал, богатый углеродом, имеет предпочтительно среднюю крупность частиц около 100 нм. Реакционную смесь вводят
предпочтительно в восстановительную зону в виде брикетов, имеющих пористость около 57%.
В соответствии с предпочтительными вариантами:
диоксидкремниевый компонент исходного
материала превращают по существу в реакционной смеси в SiC путем использования добавленного углерода в количестве, взятом в интервале 3 - 4 моль C/моль SiO2 плюс 1 - 2 моль C/моль FeO, плюс
3 - 4 моль C/моль Fe2O3 плюс 1 - 2 моль C/моль MgO;
температурный градиент между восстановительной зоной и первой конденсацией поддерживают настолько большим, насколько
это возможно;
в качестве исходного материала используют оксид магния, содержащий незначительные количества оксидов Fe, Si, Ca и Al;
в качестве исходного материала используют оливин;
когда содержание Al2O3 в реакционной смеси более 1 мас.%, Tr менее чем 1550oC;
SizFe и металлическое железо отделяют от
остатка в восстановительной зоне традиционными методами, например магнитным или электрическим разделением или флотацией, после чего Au и переходные элементы, например Mn, Cr, Ni и металлы из группы
платины, извлекают общепринятыми способами, например выщелачиванием; и
SiC, образованный в восстановительной зоне и первой зоне конденсации, извлекают в виде побочного продукта из остатка
соответственно в восстановительной зоне и первой зоне конденсации.
Извлеченный SiC представляет микропродукт высокой чистоты.
3. Переработка силикатов магния.
Кроме того, было найдено, что третью задачу можно решить способом переработки исходного материала, выбранного из группы, состоящей из оксида магния, содержащего незначительные количества
оксидов Fe, Si, Ca и Al, природных и промышленно полученных магнийсиликатных минералов, и их смесей, например оливина, который включает:
смешивание исходного материала с углеродом в
количестве по крайней мере 1 моль C/моль SiO2 плюс по крайней мере 1 моль C/моль FeO плюс по крайней мере 3 моль C/моль Fe2O3 плюс по крайней мере 1 моль C/моль MgO;
предпочтительно в количестве по крайней мере 2 моль C/моль SiO2 плюс по крайней мере 1 моль C/моль FeO плюс по крайней мере 3 моль C/моль fe2O3 плюс по
крайней мере 1 моль C/моль MgO;
предпочтительно в количестве менее чем 4 моль C/моль SiO2 плюс 2 моль C/моль FeO плюс 4 моль C/моль Fe2O3 плюс 2 моля C/моль
MgO;
нагревание смеси в реакционной зоне до температуры Tr в интервале 1400 - 1800oC, предпочтительно менее чем 1700oC, при давлении pr в
интервале

предпочтительно при 1700 - 1750oC и около 101 kPa (1 атм), посредством чего:
железооксидный компонент исходного материала восстанавливают в реакционной смеси до железа,
диоксидиркремниевый компонент исходного материала по крайней мере частично превращают в реакционной зоне в SiC и сплав Si и Fe, SizFe и
магнийоксидный компонент исходного материала превращают по крайней мере частично, в оксид магния(периклаз);
удаление по существу полностью превращенной смеси в качестве конечного продукта из реакционной зоны;
удаление CO, образованного посредством вышеупомянутых способов восстановления, из реакционной зоны и поддержание давления pr в реакционной зоне при предварительно выбранном значении путем использования насоса;
по желанию осаждения смеси MgO, Mg2, SiO4, Si и SiC при удалении газа из реакционной зоны в отдельной зоне конденсации, расположенной перед насосом, при давлении p1 ≤ pr и при температуре в интервале 800 - 1500oC и извлечение упомянутого осажденного материала.
Исходными материалами, подходящими для использования в вышеупомянутом способе, являются:
сырой оксид магния, т.е. оксид магния, содержащий незначительные количества примесей, например оксидов Fe, Si, Ca и Al;
силикаты магния, т.е. природные или промышленно полученные
магнийсиликатные минералы.
Сырой оксид магния содержит обожженные (обработанные нагревом при температуре приблизительно 1000oC) соединения, полученные из магнезита, брусита, кизерита или подобные промышленно полученные материалы, например отработанную футеровку печи, выполненную из периклаза, и пыли фильтров с фабрик обжига магнезита.
Сырой оксид магния содержит более 50% MgO, в частности более 80% MgO.
Предпочтительно содержание CaO будет составлять менее 1%, в частности менее 0,5%.
Предпочтительно содержание щелочных металлов должно быть менее 1%, в частности менее 0,3% в пересчете на оксиды.
Предпочтительно сумма других летучих элементов, например S и Cl, и металлов, подобных Zn, Cd, Hg и т.д., должна быть менее 1%, в частности менее 0,5%.
Силикаты магния включают природные или обожженные (обработанные нагревом при 1000oC) силикатные минералы, например оливины, серпентины, вермикулиты, антофиллиты, кумингтониты, энстатиты, пиропы, шпинели и подобные промышленно полученные соединения, содержащие Mg в качестве основного компонента, которые определены ниже.
Предпочтительно силикаты магния содержат более чем 25% MgO, в частности более чем 40% MgO.
Предпочтительно содержание CaO составляет менее 1%, в частности менее чем 0, 5%.
Предпочтительно содержание щелочных металлов составляет менее, чем 1%, в частности менее чем 0,3% в пересчете на оксиды.
Если содержание Al2O3 выше чем 3%, то для того, чтобы избежать образования карбида алюминия, температуры реакции в реакционной зоне должны быть ниже 1550oC.
Предпочтительно сумма других летучих элементов, например S и Cl и металлов, подобных Zn, Cd, Hg и т.д., должно быть менее 1%, в частности менее 0,5%.
Силикаты магния, кроме того, включают природные горные породы, состоящие из более чем 50% силикатов Mg, которые определены выше, предпочтительно из более чем 80%, в частности горные породы, состоящие из более чем 90% силикатов, и промышленные отходы, богатые силикатом магния высокого качества, например использованные форстеритовые футеровки печи.
В настоящем контексте термин "углерод" включает материалы, богатые углеродом, например антрацит, углеродную сажу и кокс.
Эти богатые углеродом материалы в общем имеют следующий состав, %:
Содержание углерода - >90
Зольность - <2
Летучие компоненты - <8
Предпочтительно:
Содержание углерода - >96
Зольность - <1
Летучие компоненты - <3
В частности:
Содержание углерода - > 985
Зольность - <0,5
Летучие компоненты - <1
Исходный материал предпочтительно измельчают до средней крупности частиц, менее чем
45 мкм. Материал, богатый углеродом, имеет предпочтительно среднюю крупность частиц около 100 нм. Реакционную смесь вводят предпочтительно в восстановительную зону в виде брикетов, имеющих пористость
около 57%.
В соответствии с первым предпочтительным вариантом исходный материал смешивают с углеродом:
в количестве 2,9 - 3,3 моль C/моль SiO2 плюс 1,0 - 1,3 моль
C/моль FeO плюс 3,0 - 3,4 моль C/моль Fe2O3 плюс 0,0 - 0,25 моль C/моль MgO;
предпочтительно в количестве 2,9 - 3,2 моль C/моль SiO2, плюс 1,0 - 1,2 моль
C/моль FeO плюс 3,0 - 3,2 моль C/моль Fe2O3 плюс 0,0 - 0,2 - моль C/моль MgO;
в частности в количестве 2,9 - 3,1 моль C/моль SiO2 плюс 1,0 - 1,05 моль C/соль
FeO, плюс 3,0 - 3,1 моль C/моль Fe2O3, плюс 0,0 - 0,15 моль C/моль MgO.
В соответствии с другими предпочтительными вариантами:
реакционную температуру
Tr поддерживают в интервале 1400 - 1500oC, и MgO и Mg2SiO4 осаждают в зоне конденсации путем инжекции кислородсодержащего газа, например молекулярного
кислорода, воздуха, CO2, CO, H2O и их смесей;
в качестве исходного материала используют оксид магния, содержащий незначительные количества оксидов Fe, Si, Ca и Al;
в качестве исходного материала используют оливин;
когда содержание Al2O3 в реакционной смеси более 1 мас.%, Tr меньше чем 1500oC;
SirFe и металлическое железо отделяют от остатка в восстановительной зоне традиционными способами, например магнитным или электростатическим разделением или флотацией, после чего A и
переходные элементы, например Mn, Cr, Ni и металлы из платиновой группы извлекают общепринятыми способами, например выщелачиванием;
SiC, образованный в восстановительной зоне и первой зоне
конденсации, извлекают в виде побочного продукта из остатка соответственно в восстановительной зоне и первой зоне конденсации;
MgO, образованный в восстановительной зоне и первой зоне
конденсации, извлекают в виде побочного продукта из остатка собственно в восстановительной зоне и первой зоне конденсации.
Изобретение поясняется чертежом, где:
фиг. 1
- экспериментальная аппаратура лабораторного масштаба, используемая для экспериментов, представленных в примерах 1 - 5;
фиг. 2 - экспериментальная аппаратура лабораторного масштаба,
используемая для экспериментов, представленных в примере 6;
фиг. 3 - аппаратура для углеродотермической переработки магнийсиликатных минералов и горных пород;
фиг. 4
- фотографические снимки прореагировавшего слоя материала из примера 1, полученные на сканирующем электронном микроскопе;
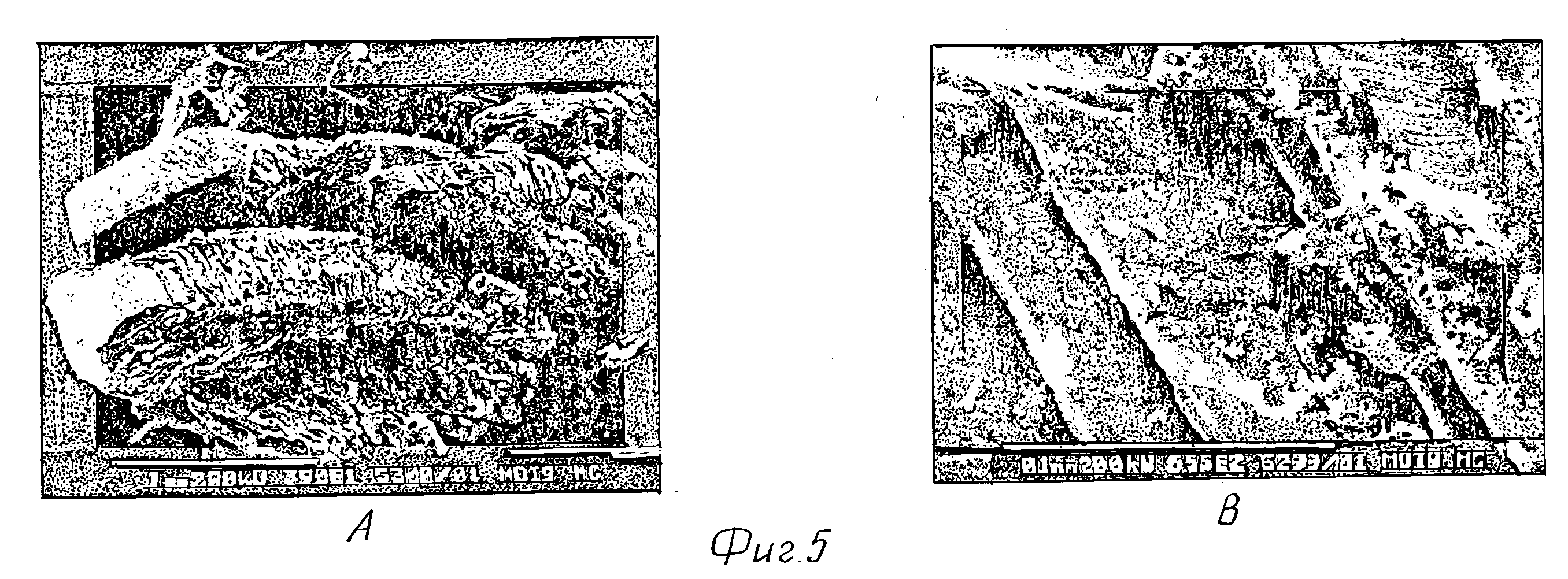
фиг. 5 - фотографические снимки столбчатых кристаллов магния из
примера 5, полученные на сканирующем электронном микроскопе;
фиг. 6 - показывает диаграммы, иллюстрирующие выход MgO (тв) из слоя MgO, перешедшего в паровую фазу, в виде функции пониженного
давления при углеродотермическом превращении оливина 613 при 1508±2oC (примеры 1, 4 и 5).
Фиг. 1 представляет экспериментальную аппаратуру лабораторного масштаба, и
используемую для экспериментов (примеры 1 - 5 и имеющую:
электрически нагреваемую камерную печь 1, рассчитанную на 1600oC, показана только теплоизоляция;
камеру печи 2;
термопару 3 для измерения температуры печи;
милливольтметр 4, соединенный с термопарой 3;
реактор и трубку 5 конденсатора, состоящую из графитовой трубки с закрытым концом,
расположенной в трубке из оксида алюминия с закрытым концом, имеющий загрузку 6 в конце трубки 5 реактора, первый конденсат 7 в нагретом конце трубки 5 конденсатора и второй конденсат 8 в холодном
конце трубки 5 конденсатора;
прессостат 9 для регулирования давления газа в реакторе и трубке 5 конденсатора;
пневматический клапан 10, регулируемый прессостатом 9,
пылевой
фильтр 11;
вакуумный насос 12;
резервуар газа 13 для сбора отходящего газа из реактора/трубки 5 конденсатора;
монитор CO 14.
Фиг. 2 показывает
экспериментальную аппаратуру лабораторного масштаба, используемую для экспериментов, представленных в примере 6, и имеющую:
электрически нагреваемую печь 1, рассчитанную 1600oC,
для нагрева части реактора/трубки конденсатора реактора;
электрически нагреваемую печь 2, рассчитанную на 1400oC, для нагрева первой части конденсатора реактора/трубки конденсатора;
электрически нагреваемую печь 3, рассчитанную на 1200oC, для нагрева второй части конденсатора реактора/трубки конденсатора;
теплоизоляцию 4, между тремя элементами печи;
реактор и трубку конденсатора, состоящую из графитовой трубки с закрытым концом, расположенной внутри трубки на оксиде алюминия с закрытым концом, имеющий часть 6 реакционной камеры в конце
трубки 5 реактора;
первую часть 7 трубки 5 конденсатора;
вторую часть 8 трубки 5 конденсатора;
фильтр частиц 9 для сбора порошка MgO-C, образованного во второй части 8
трубки 5 конденсатора;
вакуум-плотную удаляемую крышку 10;
вакуумную трубу 11, ведущую к пневматическому клапану, регулируемому с помощью прессостата, между конденсатором и вакуумным
насосом.
Фиг. 3 представляет аппаратуру для углеродотермической переработки магнийсиликатных минералов и горных пород, имеющую:
вакуумную замкнутую систему 1 для загрузки
гранулированной сырьевой смеси, расположенной на вершине;
электрически нагреваемую печи 2, рассчитанную по крайней мере на 1400 и предпочтительно на 1800oC, с графитовой футеровкой
для углеродотермической переработки сырьевой смеси;
вакуумную замкнутую систему 3 для выгрузки остаточного слоя материала из печи 2;
электрически нагреваемый первый конденсатор 4 с
системой регулирования температуры для поддержания постоянной температуры в диапазоне 1000-1500oC, имеющий углеродную футеровку и содержащий химически активный углерод в форме, подходящей
для образования SiO путем взаимодействия с SiO-компонентом газовой фазы, генерированной в печи 2;
электрически нагреваемый второй конденсатор 5 для получения тонкого порошка MgO или
металлического магния.
Для получения тонкого порошка MgO второй конденсатор снабжают системой регулирования температуры для поддержания постоянной температуры в диапазоне 600-1500oC и системой фильтрации для сбора тонких частиц и необязательно системой для регулируемого введения кислородсодержащего газа.
Для производства металлического магния второй конденсатор снабжают системой регулирования температуры для поддержания постоянной температуры в диапазоне 200-650oC и системой сбора сконденсированного металла.
Аппаратура имеет также зону большого температурного градиента 6, расположенную между первым конденсатором 4 и вторым конденсатором 5. Эта зона может быть сконструирована в виде рассеивающего сопла для сверхзвукового адиабатического охлаждения газа, проходящего из первого конденсатора 4 во второй конденсатор 5.
В заключение аппаратура имеет циклон 7 для осаждения частиц, увлеченных отходящим газом из второго конденсатора 5, фильтр 8 для тонких частиц, вакуумный насос 9, дающий возможность поддерживать давление в диапазоне 10 - 155 Pa в печи 2, в первом конденсаторе 4 и во втором конденсаторе 5, вакуумную замкнутую систему 10 для выгрузки металлического магния, образованного во втором конденсаторе.
Фиг. 4 показывает фотографические снимки прореагировавшего слоя материала из примера 1, полученные на сканирующем электронном микроскопе (методика 1 : 1506oC, Pобщ/Pравн=0,79; 320 мин).
A) Просмотр (N 5359/01).
B) Микронные сортированные по величине кристаллы MgO и SiC вместе с 5-микронной капелькой "Siz Fe", показанные крупным планом (N 5357/01).
Фиг. 5 показывает фотографические снимки столбчатых кристаллов магния из примера 5, полученные на сканирующем электронном микроскопе (Методика 1: 1510oC, Pобщ/Pравн=0,029; 115 мин).
Кристаллы Mg образовались путем осаждения из первой фазы в самой колодной части конденсаторе (< 650oC).
A) Просмотр (N 5300/01).
B) Крупный план (N 5299/01).
Фиг. 6 показывает диаграммы, иллюстрирующие выход MgO (тв) из слоя, и Mg), перешедшего в паровую фазу, в виде функции пониженного давления при углеродотермическом превращении оливина 613 при 1508±2oC (примеры 1, 4 и 5).
В дальнейшем основная мысль изобретения будет, кроме того, объявлена со ссылкой на фиг. 6.
Продукты реакции, образующиеся при соответствующем нагреве смесей, например оливина (Mg2SiO4) и углерода (C), зависят от
молярного соотношения между реагентами и давления газа во время переработки. Так например, смесь 1 моля оливина (Mg2CiO4) и 3 моль углерода (C) может взаимодействовать в
соответствии с реакцией (I') или (I'') в зависимости от общего давления газа
(1') Mg2SiO4(тв) + 3C(тв) _→ 2MgO(тв) + SiC(тв) + 2C(г)
(2') Mg2SiO4(тв) + 3C(тв) _→ 2Mg(г) + SiO(г) + 3CO(г)
Уравнения для вычисления равновесного парцианального давления всех основных разновидностей газа, включенных в
реакцию между 1 молем Mg2SiO4 и 3 моль C при 1400 - 1750oC:
(a) log PCO = -17196T-1 + 10,746
(b) log PMg =
-15021T-1 + 8,526
(c) log PSiO = -21473T-1 +10,886
(d) log PO2 = -46405T-1 + 10,536
Термодинамическое вычисление
показывает, что реакция (1') будет происходить слева направо в температурном диапазоне от 1400-1750oC, если парциальное давление CO(PCO) меньше или равно давлению (kPa),
определенному выше уравнением (a). При термодинамическом равновесии одновременные парциальные давления всех других важных разновидностей газа Mg(г), SiO(г), O2(г), включенных в реакцию,
определяются уравнениями (b), (c) и (d). Из определенного таким образом парциального давления основных разновидностей газа и массового баланса включенных реакций можно вычислить общее давление газа
(Pравн), состав и количество летучего материала и остаточный состав слоя для равновесного превращения Mg2SiO4(тв) в MgO(тв) и SiC(тв) в соответствии с уравнением (1'),
при этом можно вычислить минимальный избыток добавленного углерода, необходимый для образования равновесного количества Mg (г) и SiO (г). Общее равновесное давление газа Oравн, вычисленное
таким образом, может быть представлено
(Pравн) = -17043 T-1 + 10,705.
Если общее давление пара (Pобщ) существующей газовой фазы над реакционной смесью выше чем (Oравн), реакция не будет происходить.
При равновесных условиях (Pобщ/Pравн) = 1 вычисленный выход MgO (тв) из слоя изменяется от 86,4% при 140oC до 91,8% при 1700oC.
Когда Oобщ станет ниже Pравн, дальнейшее испарение загрузки будет происходить в соответствии с реакцией (1'') и выход MgO(тв) и SiC(тв) в слое уменьшится. Таким образом, когда давление постоянно снижается ниже Pравн, реакция (1'')становится все более и более значительной по сравнению с реакцией (1').
Эксперименты показывают, что реакция (1'') является преобладающей, когда (Pобщ/Pравн) < 0,7, и что выход MgO (тв) из слоя (реакция 1') составляет < 5%, когда (Pобщ/Pравн) < 0,2 (фиг. 6), т.е. во время переработки из оливина испаряется более чем 95% MgO.
При этом следует понимать, что хотя номинальная температура печи, которую используют для вычисления Oравн (1508±2oC на фиг. 6) равна действительной температуре слоя, когда (Pобщ/Pравн) ≥ 1, этот случай не является таким случаем, когда общее давление уменьшается и парообразование становится преобладающим. При этом условиях испарение приводит к охлаждению слоя до температуры, когда Pобщ равно давлению газа при устойчивом испарении, или до температуры, когда парообразование уменьшается по кинетическим причинам (≈ 1400oC, пример 3). При номинальных температурах печи выше ≈ 1500oC и (Pобщ/Pравн) < ≈ 0,1 скорость испарения будет в значительной степени регулирования скоростью, при которой подводят нагрев. Это в общем подобно тому, что происходит во время процессов возгонки. При этих условиях номинальная температура печи отражает скорость подвода нагрева, а не температуру слоя.
Таким образом, температура, равная 1508oC, приводит в Pобщ ≤ 1,1 кРа (Pобщ/Pравн) < ≈ 0,1). Примеры 4, 5 и 6 являются характерными примерами того, что происходит при том же самом Pобщ и номинальной температуре печи в диапазоне 1400-1750oC.
Последующие примеры описывают более подробно предпочтительные варианты способа, изобретенного для превращения силикатов магния (например, оливина) в:
A) огнеупорные массы, состоящие из
периклаза, карбида кремния и необязательно форстерите, обогащенного оксидом магния;
B) хорошо разделенные металлический магний и карбид кремния;
C) хорошо разделенные оксид магния и
карбид кремния.
Химический состав и физические данные сырья, использованного в примерах 1 - 6, даны в табл. 1. Состав и физические данные гранулированного углерод-форстеритовых смесей, полученных из этого сырья и использованных в экспериментах, представлены в табл. 2.
Эксперименты осуществляли в соответствии со следующими методиками.
Методика 1.
Экспериментальная аппаратура лабораторного масштаба, использованная в этой части работы для углеродотермического превращения при температуре 1200 - 1500oC и давлениях 0,4 - 10,4 kPa брикетированной сырьевой смеси, показано на фиг. 1.
Загрузки известной массы поместили в реактор/конденсатор, графитовую трубку с закрытым концом расположенную внутри трубки из оксида алюминия с закрытым концом. Затем реактор/конденсатор вакуумировали, заполнили Ar до желательного давления и ввели в предварительно нагретую печь со скоростью, соответствующей скорости нагрева около 50oC/мин. Для поддержания постоянного давления в реакторе/конденсаторе во время углеродотермической реакции использовали пневматический клапан, расположенный перед вакуумным насосом, которые регулировал давление. Потом собрали газ, выделенный в процессе и проверили концентрацию CO.
После углеродотермической обработки продукты реакции в слое и различные фракции, конденсированные из первой фазы, отдельно собрали, взвесили и исследовали XRD (дифракцией рентгеновский лучей), TG (термогравиметрией) и SEM/EDS (сканирующей электронной микроскопией EDS).
Методика 2.
Экспериментальная аппаратура лабораторного масштаба, использованная в этой части работы для углеродотермического превращения при 1510oC и давлении 1,1 kPa брикетированной сырьевой смеси, показана на фиг. 2.
Загрузки известной массы поместили в реактор/конденсатор, графитовую трубку с закрытым концом, расположенную внутри трубки из оксида алюминия с закрытым концом. Затем реактор/конденсатор вакуумировали, заполнили Ar до желательного давления и ввели в предварительно нагретую секцию печи со скоростью, соответствующей скорости нагрева около 50oC/мин. Для поддержания постоянного давления в реакторе/конденсаторе во время углеродотермической реакции использовали пневматический клапан, расположенный перед вакуумным насосом, который регулировал давление. Потом собрали газ, выделенный в процессе, и проверили концентрацию CO.
После углеродотермической обработки продукты реакции в слое и различные фракции, конденсированные из паровой фазы, отдельно собрали, взвесили и исследовали XRDTG и SEM/EDS.
A) Получение
огнеупорных масс, состоящих из периклаза (MgO), карбида кремния (SiC) и следов форстерита Mg2SiO4), обогащенных оксидов магния
Пример 1.
В этом эксперименте 11,2 г углерод-оливиновых брикетов смеси A (табл. 2) обработали в соответствии с методикой 1 при 1506oC и давлении газа (Pобщ) 10,4 kPa в течение 320 мин.
Давление (Pобщ) выбрали равным 0,84 от равновесного давления газа (Pравн), как было вычислено из термодинамических данных. Конец реакции определили через 320 мин посредством постепенного повышения выделения CO, которое определили в выкаченном отходящем газе.
Аналитические данные фазового состава прореагировавшего слоя и осажденных продуктов в конденсаторе сведены в табл. 3.
Прореагировавший слой состоял из высокопористых брикетов зеленоватого цвета. Присутствующие фазы сортировали по величине на MgO, SiO, капельки "SizFe" и незначительные остатки Mg2SiO4 (фиг. 4). Выход MgO (тв) из слоя составил 67%.
Часть превращенного материала слоя измельчили и капельки Si2 Fe удалили магнитом. На основе пространственного распределения фаз и общего веса пробы установили, что более чем 95 мас.%. первоначальных 8,62 мас.% оксидов железа было удалено таким путем.
Анализ SEM/EDS показывает, что переходные элементы (Cr, Mn, Ni и Pt), которые встречаются в следовых количествах в оливине 613, сконцентрированы в капельках "SizFe". Полуколичественный анализ EDS показывает средние концентрации в капельках "SizFe":2 мас.% C, 0,3 мас.% Mn, 3 мас.% Ni и 0,1 мас. % Pt.
Пример 2. В этом эксперименте 12,5 г углерод-оливиновых брикетов смеси A (табл. 2) обработали в соответствии с методикой 1 при 1580oC и давлении газа (Pобщ) 31,3 kPa в течение 260 мин.
Давление (Pобщ) выбрали равным 0,97 от равновесного давления газа (Pравн), как было вычислено из термодинамических данных. Конец реакции определили через 260 мин посредством постепенного понижения выделения CO, которое определили в выкаченном оходящем газе.
Прореагировавший слой состоял из высокопористых брикетов зеленоватого цвета. Присутствующие фазы сортировали по величине на MgO, SiO, капельки "SizFe" и незначительные остатки Mg2SiO4. Материал в виде пара подробно не анализировали. Выход MgO (тв) из слоя составил 82%.
Пример 3. В этом эксперименте 13,5 г углерод-оливиновых брикетов смеси A (табл. 2) обработали в соответствии с методикой 1 при 1405oC и давлении газа (Pобщ) 3,4 кРа в течение 180 мин.
Давление (Pобщ) выбрали равным 0,97 от равновесного давления газа (Pравн), как было вычислено из термодинамических данных.
Через 180 мин эксперимент прекратили, несмотря на то, что все еще наблюдали выделение CO, которое определили в выкаченном отходящем газе.
Наблюдаемая потеря веса составила 18,7 мас.%, включая MgO, который не был извлечен.
Прореагировавший слой состоял из высокопористых брикетов черно-зеленоватого цвета. Присутствующие фазы представляли оливины (39 мас.%), периклаз (17 мас.%), SiC(11 мас.%), "SizFe" (3 мас.%) и углерод (11 мас.%).
Выход MgO (тв) из слоя составил 44%, в то время как непрореагировавший оливин содержал около 50% первоначального содержания MgO.
Кроме того, исследования брикетов смеси A (табл. 2) с использованием DTA/TG (дифференциального термического анализа/термогравиметрии) Mettler показали, что когда для удаления газообразных продуктов реакции использовали поток чистого аргона (подсчитано: (Pобщ-PAr)/Pравн≈0,97), при 1200oC происходило очень незначительное взаимодействие. Через 120 мин общая потеря веса составила только 4 мас.% и образование периклаза (MgO) не наблюдали.
B) Получение хорошо разделенных металлического магния (Mg) и карбида кремния (SiC).
Пример 4. В этом эксперименте 15 г углерод-оливиновых брикетов смеси A (табл. 2) обработали в соответствии с методикой 1 при 1510oC и давлении газа (Pобщ) 1,1 kPa в течение 103 мин.
Давление (Pобщ) выбрали равным 0,079 от равновесного давления газа (Pравн), как было вычислено из термодинамических данных. Конец реакции определяли через 103 мин посредством постепенного понижения выделения CO, которое определили в выкачанном отходящем газе.
Аналитические данные фазового состава реагирующего слоя и осажденных продуктов в конденсаторе сведены в таблицу 4.
Остаточный слой материала состоял, главным образом, из капелек "SizFe" вместе с незначительным количеством периклаза (MgO), следами SiC, при этом он не содержал форстерит.
Благодаря низкому давлению и молярному отношению между Mg2SiO4 и углеродом, равному 1:3, большая часть кремния и магния из оливина 613 в сырьевой смеси быстро испарялась в соответствии с реакцией:
Mg2SiO4(тв)
_→ 3C(тв)2Mg(г)+SiO(г)+3CO(г)
Кремний вновь осаждали в виде SiC в самой натриевой части конденсатора (1480±20oC) вместе с периклазом (MO)и некоторым
количеством форстарита, образованного посредством обратной реакции.
Выход металлического магния, образованного в самой холодной части конденсатора (< 650oC), составил 23 мас.%. Металлический магний содержал около 4,4 мас.% периклаза (MgO) в качестве основной примеси.
Пример 5. В этом эксперименте 9,4 г углерод-оливиновых брикетов смеси A (табл. 2) обработали в соответствии с методикой 1 при 1510oC и давлении газа (Pобщ) 0,4 kPa в течение 115 мин.
Давление (Pобщ) выбрали равным 0,029 от равновесного давления газа (Pравн), как было вычислено из термодинамических данных. Конец реакции определяли через 115 мин. посредством постепенного понижения выделения CO, которое определили в выкачанном отходящем газе.
Аналитические данные фазового состава реагирующего слоя и осажденных продуктов в конденсаторе сведены в табл. 5.
Остаточный слой материала состоял главным образом из капелек "SizFe" и небольшого количества SiC.
Благодаря низкому давлению и молярному отношению между Mg2SiO4
частью сливина и углеродом, равному ≈1:3, большая часть кремния и магния из оливина 613 в сырьевой смеси быстро испарялась в соответствии с реакцией
Mg2SiO4(тв)
_→ 3С(тв)2Mg(г)+SiO(г)+3CO(г)
Кремний повторно осаждали, главным образом в виде Si, в самой нагретой части конденсатора (1300oC) вместе с форстеритом, образованным
путем обратной реакции, небольшим количеством периклаза (MgO) и следами SiC.
Выход металлического магния, образованного в самой холодной части конденсатора (<650oC), составил 74,6%. Магний осадили в виде столбчатых кристаллов (фиг. 5). Металлический магний содержал около 4,9 мас.% периклаза (MgO) в качестве основной примеси.
C) Получение хорошо разделенных оксида магния и карбида кремния.
Пример 6. В этом эксперименте 14,2 г углерод-оливиновых брикетов смеси A (табл. 2) обработали в соответствии с методикой 2 при 1510oC и давлении газа (Pобщ) 1,1 kPa в течение 120 мин.
Давление (Pобщ) выбрали равным 0,079 от равновесного давления газа (Pравн), как было вычислено из термодинамических данных. Конец реакции определили через 120 мин посредством постепенного понижения выделения CO, которое определили в выкачанном отходящем газе.
Аналитические данные фазового состава прореагировавшего слоя и осажденных продуктов в конденсаторе сведены в табл. 6.
Остаточный слой материала состоял из SiC, капелек "Siz Fe" и небольшого количества остаточного углерода.
Единственной фазой, обнаруженной в конденсаторе II, удержанной при 1360oC, был SiC.
Материал, собранный из конденсатора II, удержанный при 800oC, представлял тонкой черный порошок, состоящий из периклаза (MgO) и углерода (C). Углерод удалили путем нагрева порошка до 800oC на воздухе в течение 5 ч.
Полученный порошок был белым, и единственная фаза, обнаруженная с помощью XRD (дифракции рентгеновских лучей), представляла периклаз (MO). Выход периклаза составил 95 мас.%.
В вышеприведенных экспериментах в качестве исходного материала использовали оливины. Подобные результаты можно получить с другими магнийсиликатными минералами и сырой окисью магния.
Реферат
Металлический магний и чистый оксид магния получают углеродотермическим восстановлением исходного материала, например оксида магния, содержащего незначительные количества оксидов Fe, Si, Ca и Al и/или магнийсиликатных минералов, например оливина, при давлении ниже атмосферного. Металлический магний испаряют из восстановительной зоны и во второй зоне конденсации осаждают чистый металлический магний и чистый оксид магния. Кремний частично испаряют в виде SiO, который осаждают в первой зоне конденсации, расположенной перед второй зоной конденсации, частично превращают в реакционной смеси в SiC и сплав Si и Fe. Исходные материалы можно также переработать способом, в котором их магниевый компонент превращают в реакционной смеси в оксид магния, в то время как оставшиеся компоненты превращают в SiC и сплав Si и Fe, Au, а ценные переходные элементы извлекают путем выщелачивания сплава Si и Fe. 4 с. и 21 з.п.ф-лы, 6 ил. 6 табл.

Формула

где P1 выражено в кПа,
и ниже значения Tмин + 100oС, предпочтительно Тмин + 50oС, в частности Тмин + 25oС и обязательно ниже Tr, восстановленный газообразный металлический магний испаряют из восстановительной зоны и конденсируют в отдельной второй зоне конденсации, расположенной за первой зоной конденсации, при давлении P2 в интервале 0,01 - 1,1 кПа, предпочтительно 0,2 - 0,8 кПа, в частности 0,3 - 0,7 кПа, при температуре Т2 менее 638oС, предпочтительно в интервале 200 - 600oС, в частности в интервале 250 - 540oС, удаляют образованный в указанных процессах восстановления CO из второй зоны конденсации и поддерживают давление P2 при предварительно выбранном значении посредством использования насоса с обеспечением максимального градиента температуры между первой и второй зонами конденсации при соотношении P2 ≤ P1 ≤ Pr.

предпочтительно

в частности 0,3 - 1,75 кПа, осуществляют восстановление диоксидкремниевого компонента исходного материала до SiO, который в восстановительной зоне частично превращают в SiC и в сплав Si и Fe - Si2Fe, частично испаряют из восстановительной зоны и превращают в SiC, Si и/или Mg2SiO4 путем реакции с углеродом в отдельной первой зоне конденсации при давлении P1, где P1 ≤ Pr, и при температуре T1 выше, чем
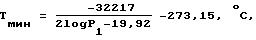
где P1 выражено в кПа,
и ниже значения Тмин + 100oС, предпочтительно Тмин + 50oС, в частности Тмин + 25oС и обязательно ниже Tr, восстановленный газообразный металлический магний подвергают испарению из восстановительной зоны и взаимодействию с CO, образованным в восстановительной зоне, до MgO и C, и осаждают MgO и C в отдельной зоне окисления и конденсации, расположенной за первой зоной конденсации, при давлении P2, где P2 ≤ P1, и при температуре T2 в интервале от 638oС до T1, предпочтительно от 650oС до Т1 - 50, в частности от 800 до 1000oС, удаляют смесь углерода и оксида магния из зоны окисления и конденсации, удаляют смесь углерода и диоксида магния из зоны окисления и конденсации, удаляют углерод из смеси предпочтительно путем окисления, удаляют часть CO, образованного в процессах восстановления и не потребленного в реакции с Mg, из зоны окисления и конденсации, поддерживают выбранное давление P2 посредством использования насоса, причем P2 ≤ P1 ≤ Pr.

предпочтительно

в частности 0,3 - 1,75 кПа, осуществляют восстановление диоксидкремниевого компонента исходного материала до SiO, который в восстановительной зоне частично превращают в SiC и в сплав Si и Fe - Si2Fe, частично испаряют из восстановительной зоны и превращают в SiC, Si и/или Mg2SiO4 путем реакции с углеродом в отдельной первой зоне конденсации при давлении P1, где P1 = Pr, и при температуре T1 выше, чем
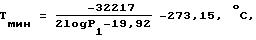
где P1 выражено в кПа,
и ниже значения Тмин + 100oС, предпочтительно Тмин + 50oС, в частности Тмин + 25oС и обязательно ниже Tr, восстановленный газообразный металлический магний подвергают испарению из восстановительной зоны и взаимодействию с отдельно введенным кислородсодержащим газом, таким как молекулярный кислород, воздух, CO2, CO, H2O и их смеси, до оксида магния, осаждают указанный оксид магния в отдельной зоне окисления и конденсации, расположенной за первой зоной конденсации, при давлении P2 ≤ P1 и при температуре T1 в интервале от 638oС до T1, предпочтительно от 650oС до Т1 - 50, в частности от 800 до 1000oС, удаляют оксид магния, углерод и образовавшийся газ из зоны окисления и конденсации и поддерживают выбранное давление P2 посредством использования насоса, причем P2 ≤ P1 ≤ Pr.

предпочтительно при 1700 - 1750oС и 101 кПа (1 атм), после восстановления железа диоксидкремниевый компонент исходного материала переводят в реакционной зоне в SiC и в сплав Si и Fe - Si2Fe, магнийоксидный компонент исходного материала частично переводят в оксид магния (периклаз), осуществляют удаление конечного продукта из реакционной зоны, удаляют из реакционной зоны CO, образованный путем процессов восстановления, поддерживают выбранное давление Pr в реакционной зоне с помощью насоса и осуществляют осаждение смеси MgO, Mg2SiO4, Si и SiC из газа, удаленного из реакционной зоны, в отдельной зоне конденсации, расположенной до насоса при давлении P1 ≤ Pr, и при температуре в интервале 800 - 1500oС, с последующим извлечением осажденных веществ.

Комментарии