Новое органическое соединение, органическое светоизлучающее устройство и дисплейное устройство - RU2570577C2
Код документа: RU2570577C2
Чертежи
Описание
Область техники, к которой относится изобретение
Настоящее изобретение предоставляет новое органическое соединение, а также органическое светоизлучающее устройство и дисплейное устройство, содержащее данное соединение.
Уровень техники
Органическое светоизлучающее устройство (также называется органическое электролюминесцентное устройство или органическое устройство EL) представляет собой элемент, включающий пару электродов и слой органического соединения, расположенный между этими электродами.
Электроны и дырки выходят из пары электродов в слой органического соединения, производя экситоны светоизлучающего органического соединения в слое органического соединения, и органическое светоизлучающее устройство излучает свет, когда экситоны возвращаются в основное состояние.
В последнее время наблюдается значительное развитие органических светоизлучающих устройств, и становятся возможными низкие возбуждающие напряжения, разнообразные длины волны излучения, быстрый отклик и уменьшение размера и массы светоизлучающих устройств.
Для изготовления высокоэффективных органических светоизлучающих устройств важно получение соединений, имеющих превосходные светоизлучающие характеристики и свойства переноса носителей заряда. Соответственно, активно создаются органические соединения для органических светоизлучающих устройств.
Что касается соединений, которые были получены до настоящего времени, известны, например, соединение 1-A, описанное в патентном документе 1 как синтетическое промежуточное соединение и в патентном документе 2 как органический транзисторный материал.
[Химическая формула 1]
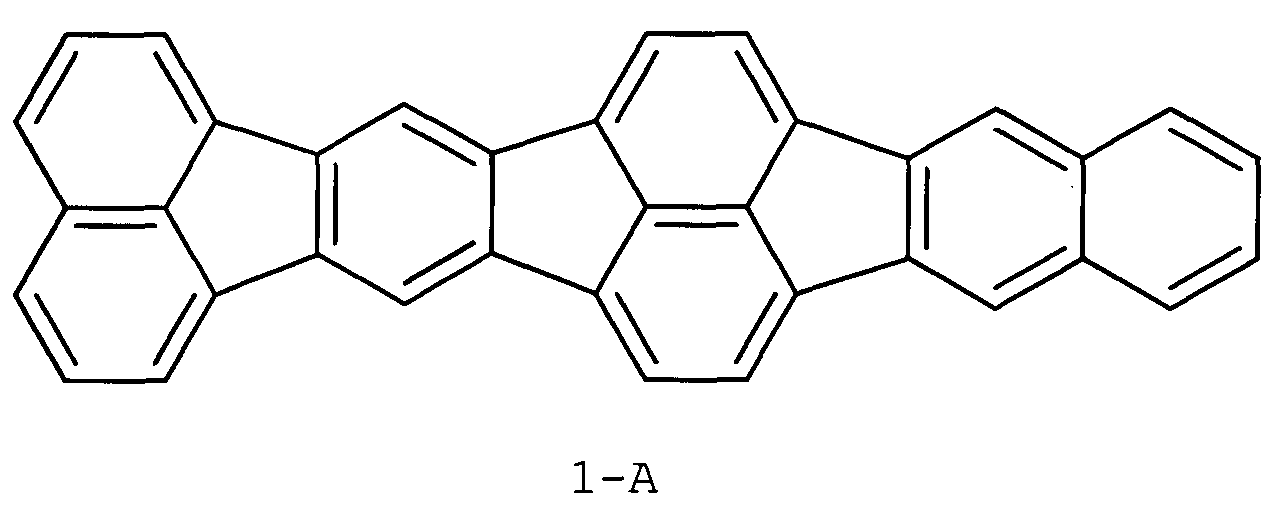
Данные о светоизлучающих характеристиках соединения 1-A не описаны, но цвет люминесценции является желтым, и интенсивность излучения является чрезмерно низкой, и поэтому оно излучает очень мало света.
Основная структура соединения, описанного в патентном документе 1, излучает желтый свет, как описано выше. Кроме того, не получено световое излучение с высоким квантовым выходом.
Список цитируемой литературы
Патентная литература
Патентный документ 1 - японская выложенная патентная заявка № 2002-110354 (отсутствует соответствующая иностранная заявка)
Патентный документ 2 - японская выложенная патентная заявка № 2009-182039 (отсутствует соответствующая иностранная заявка)
Сущность изобретения
Настоящее изобретение предлагает органическое соединение, которое имеет высокий квантовый выход и излучает свет в зеленой области только за счет своей основной структуры.
Соответственно, настоящее изобретение предлагает органическое соединение, представленное следующей формулой (1).
[Химическая формула 2]
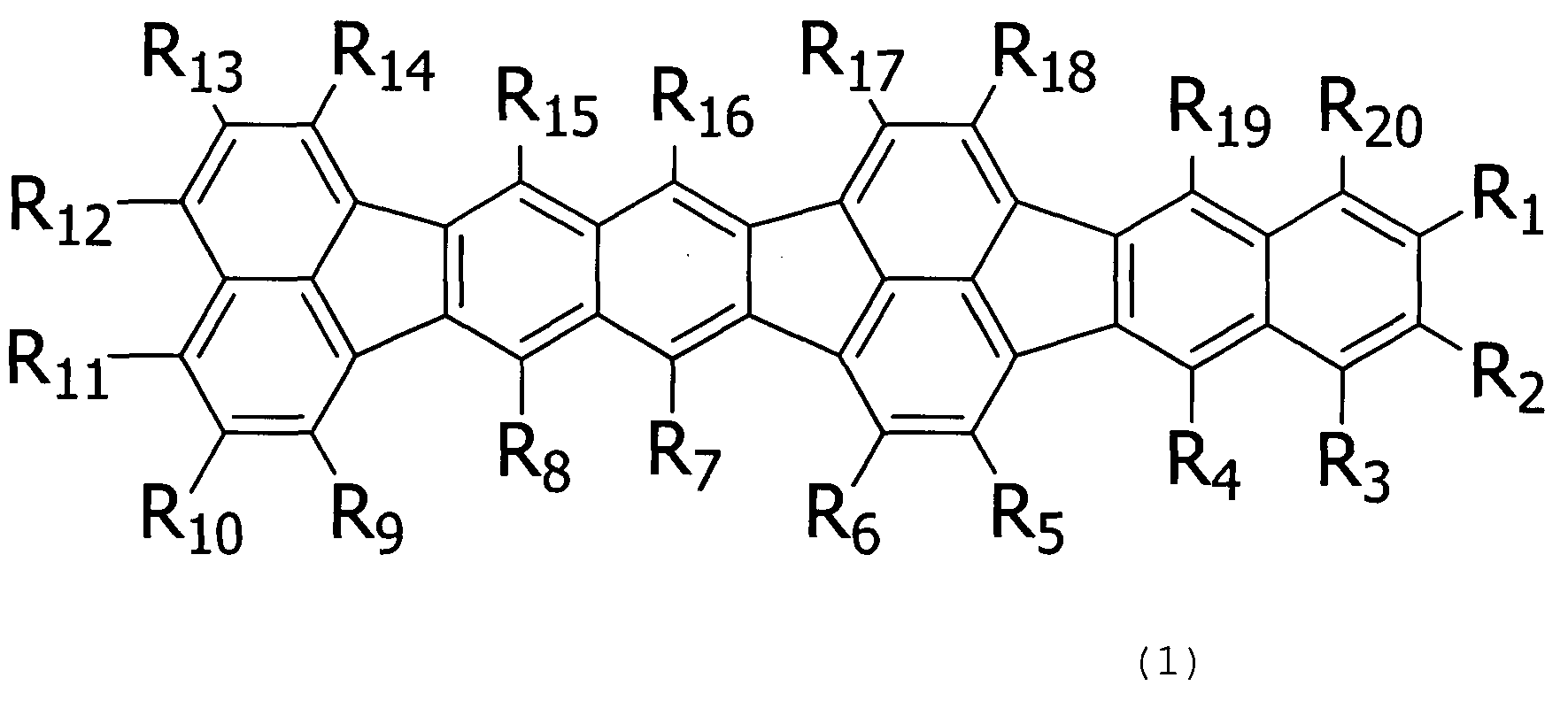
В формуле (1) каждый R1-R20 независимо выбирают из атомов водорода, атомов галогена, замещенных или незамещенных алкильных групп, замещенных или незамещенных алкоксигрупп, замещенных или незамещенных аминогрупп, замещенных или незамещенных арильных групп, замещенных или незамещенных гетероциклических групп, замещенных или незамещенных арилоксигрупп, замещенных или незамещенных тиоловых групп, силильных групп и цианогрупп.
Настоящее изобретение может предоставить органическое соединение, способное излучать свет в зеленой области за счет своей основной структуры и способное обеспечивать высокий квантовый выход. Настоящее изобретение также может предоставить органическое светоизлучающее устройство, включающее данное соединение и в результате этого имеющее высокую эффективность излучения.
Краткое описание чертежей
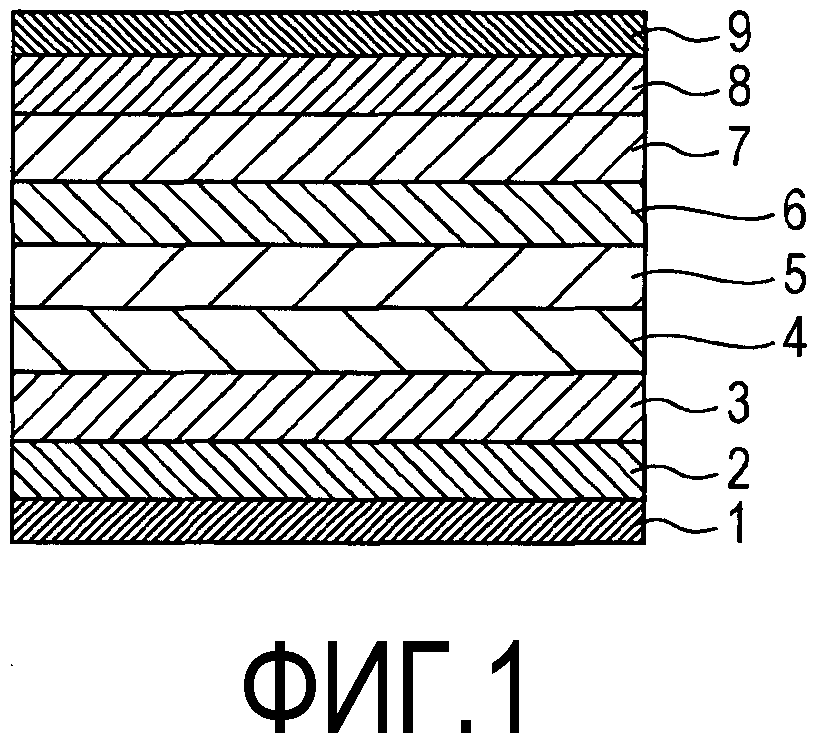
Фиг. 1 представляет схематическое изображение, иллюстрирующее пример светоизлучающего слоя органического светоизлучающего устройства многослойного типа согласно варианту осуществления.
Фиг. 2 представляет схематическое изображение поперечного сечения, иллюстрирующее дисплейное устройство, содержащее органические светоизлучающие устройства согласно варианту осуществления и тонкопленочные транзисторные устройства (TFT) в качестве примера переключающих устройств, электрически присоединенных к органическим светоизлучающим устройствам.
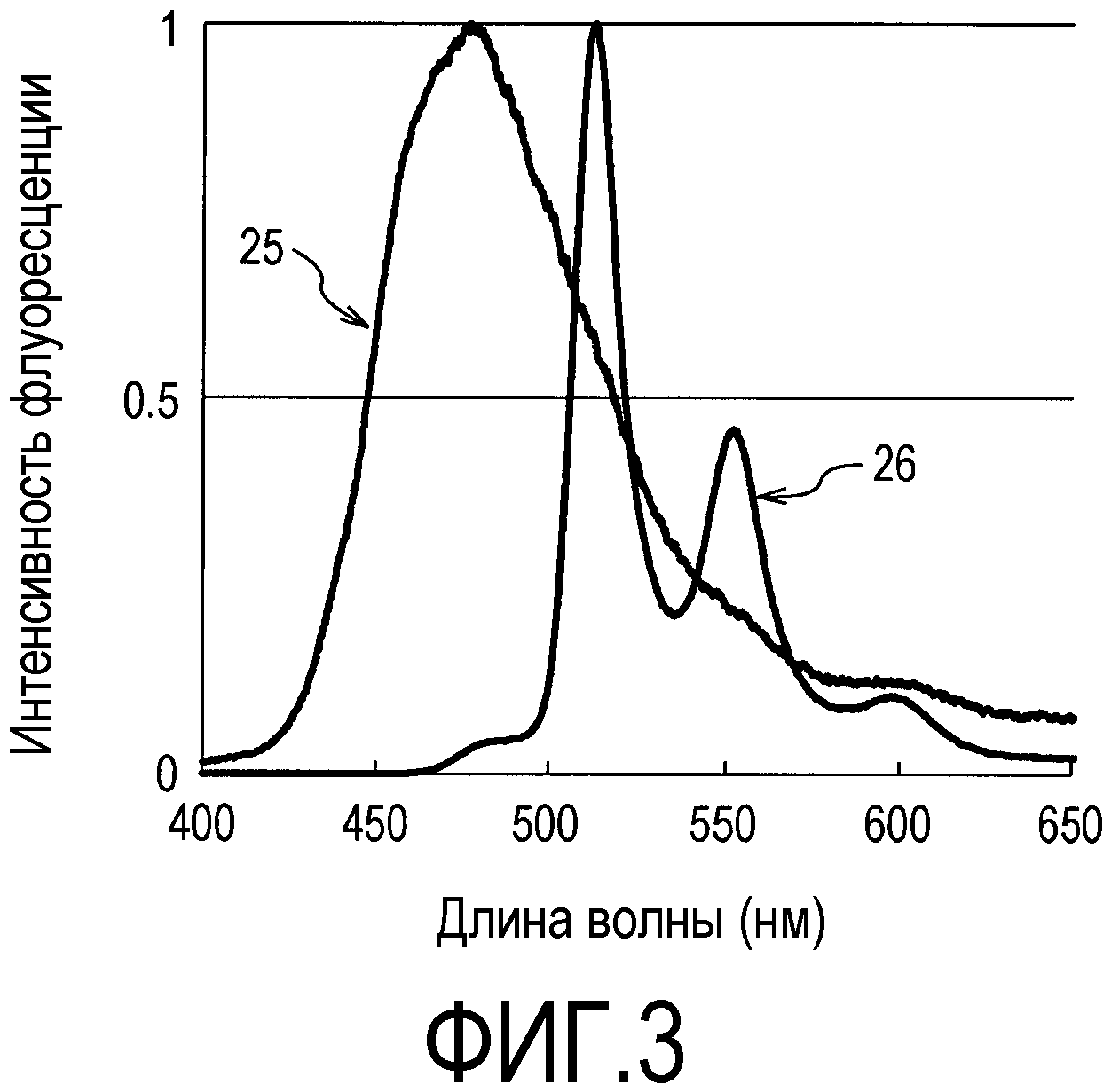
Фиг. 3 представляет спектры излучения органического соединения согласно варианту осуществления и сравнительного органического соединения.
Описание варианта осуществления
Настоящее изобретение относится к органическому соединению, представленному следующей формулой (1).
[Химическая формула 3]
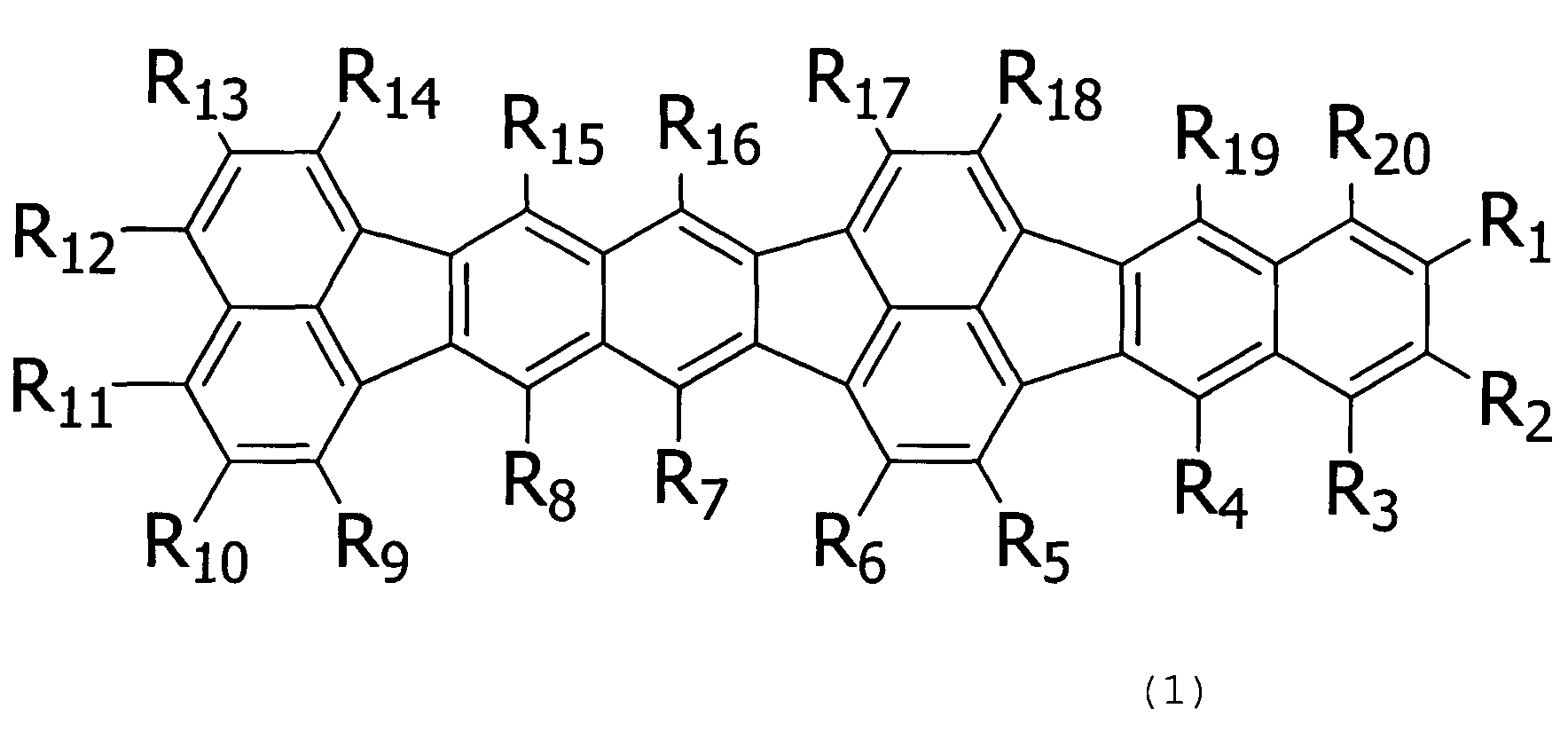
В формуле (1) каждый R1-R20 независимо выбирают из атомов водорода, атомов галогена, замещенных или незамещенных алкильных групп, замещенных или незамещенных алкоксигрупп, замещенных или незамещенных аминогрупп, замещенных или незамещенных арильных групп, замещенных или незамещенных гетероциклических групп, замещенных или незамещенных арилоксигрупп, замещенных или незамещенных тиоловых групп, силильных групп и цианогрупп.
Согласно одному аспекту, каждый R1-R20 в формуле (1) независимо выбирают из атомов водорода, замещенных или незамещенных алкильных групп и замещенных или незамещенных арильных групп.
Примеры атомов галогенов, представленных посредством R1-R20, включают, но не ограничиваются этим, фтор, хлор, бром и йод.
Примеры алкильных групп, представленных посредством R1-R20, включают, но не ограничиваются этим, метильные, этильные, н-пропильные, изопропильные, н-бутильные, втор-бутильные, трет-бутильные, октильные, циклогексильные, 1-адамантильные и 2-адамантильные группы.
Примеры алкоксигрупп, представленных посредством R1-R20, включают, но не ограничиваются этим, метокси, этокси, пропокси, 2-этил-октилокси и бензилоксигруппы.
Примеры аминогрупп, представленных посредством R1-R20, включают, но не ограничиваются этим, N-метиламино, N-этиламино, N,N-диметиламино, N,N-диэтиламино, N-метил-N-этиламино, N-бензиламино, N-метил-N-бензиламино, N,N-дибензиламино, анилино, N,N-дифениламино, N,N-динафтиламино, N,N-дифлуорениламино, N-фенил-N-толиламино, N,N-дитолиламино, N-метил-N-фениламино, N,N-дианизолиламино, N-мезитил-N-фениламино, N,N-димезитиламино, N- фенил-N-(4-трет-бутилфенил)амино, N-фенил-N-(4-трифторметилфенил)амино и N-пиперидильные группы.
Примеры арильных групп, представленных посредством R1-R20, включают, но не ограничиваются этим, фенильные, нафтильные, инденильные, бифенильные, терфенильные и флуоренильные группы.
Примеры гетероциклических групп, представленных посредством R1-R20, включают, но не ограничиваются этим, пиридильные, оксазолильные, оксадиазолильные, тиазолильные, тиадиазолильные, карбазолильные, акридинильные и фенантролильные группы.
Примеры арилоксигрупп, представленных посредством R1-R20, включают, но не ограничиваются этим, фенокси и тиенилоксигруппы.
Примеры силильных групп, представленных посредством R1-R20, включают, но не ограничиваются этим, трифенилсилильные группы.
Примеры заместителей, которые могут содержать алкильные группы, алкоксигруппы, аминогруппы, арильные группы, гетероциклические группы и арилоксигруппы включают, но не ограничиваются этим, алкильные группы, такие как метильная, этильная, н-пропильная, изопропильная, н-бутильная и трет-бутильная группы; аралкильные группы, такие как бензильная группа; арильные группы, такие как фенильная и бифенильная группы; гетероциклические группы, такие как пиридильная и пирролильная группы; аминогруппы, такие как диметиламино, диэтиламино, дибензиламино, дифениламино и дитолиламиногруппы; алкоксигруппы, такие как метокси, этокси и пропоксигруппы; арилоксигруппы, такие как феноксигруппа; атомы галогенов, такие как фтор, хлор, бром и йод; и цианогруппу.
Согласно данному варианту осуществления, каждый R1-R20 в формуле (1) может быть независимо выбран из атомов водорода, замещенных или незамещенных алкильных групп и замещенных или незамещенных арильных групп.
Органическое соединение согласно варианту осуществления может ингибировать концентрационное гашение посредством введения заместителя в основную структуру. Такое соединение имеет высокую сублимационную способность при сублимации и высокую растворимость в растворителе для нанесения покрытия.
С точки зрения ингибирования концентрационного гашения по меньшей мере один из R1-R20 в формуле (1) может быть замещен алкильной группой.
Согласно варианту осуществления, основная структура представляет собой конденсированную циклическую структуру, имеющую сопряженное строение. То есть основная структура органического соединения согласно варианту осуществления имеет структуру, представленную соединением, где все R1-R20 в формуле (1) представляют собой атомы водорода.
Далее будут описаны свойства основной структуры органического соединения согласно варианту осуществления.
Авторы настоящего изобретения сосредоточили свое внимание именно на основной структуре при разработке органического соединения, представленного формулой (1). В частности, авторы настоящего изобретения делали попытки получения соединения, где молекула основной структуры имеет длину волны излучения только в желательном диапазоне длин волн излучения.
Согласно варианту осуществления, область желательной длины волны излучения представляет собой зеленую область. В частности, длина волны максимума излучения в разбавленном толуольном растворе составляет 490 нм или более и 530 нм или менее.
Свойства основной структуры органического соединения согласно варианту осуществления будут описаны посредством сопоставления со сравнительными контрольными соединениями, имеющими структуры, аналогичные структуре органического соединения согласно настоящему изобретению. В частности, сравнительные контрольные соединения представлены формулами (2) и (3).
[Химическая формула 4]
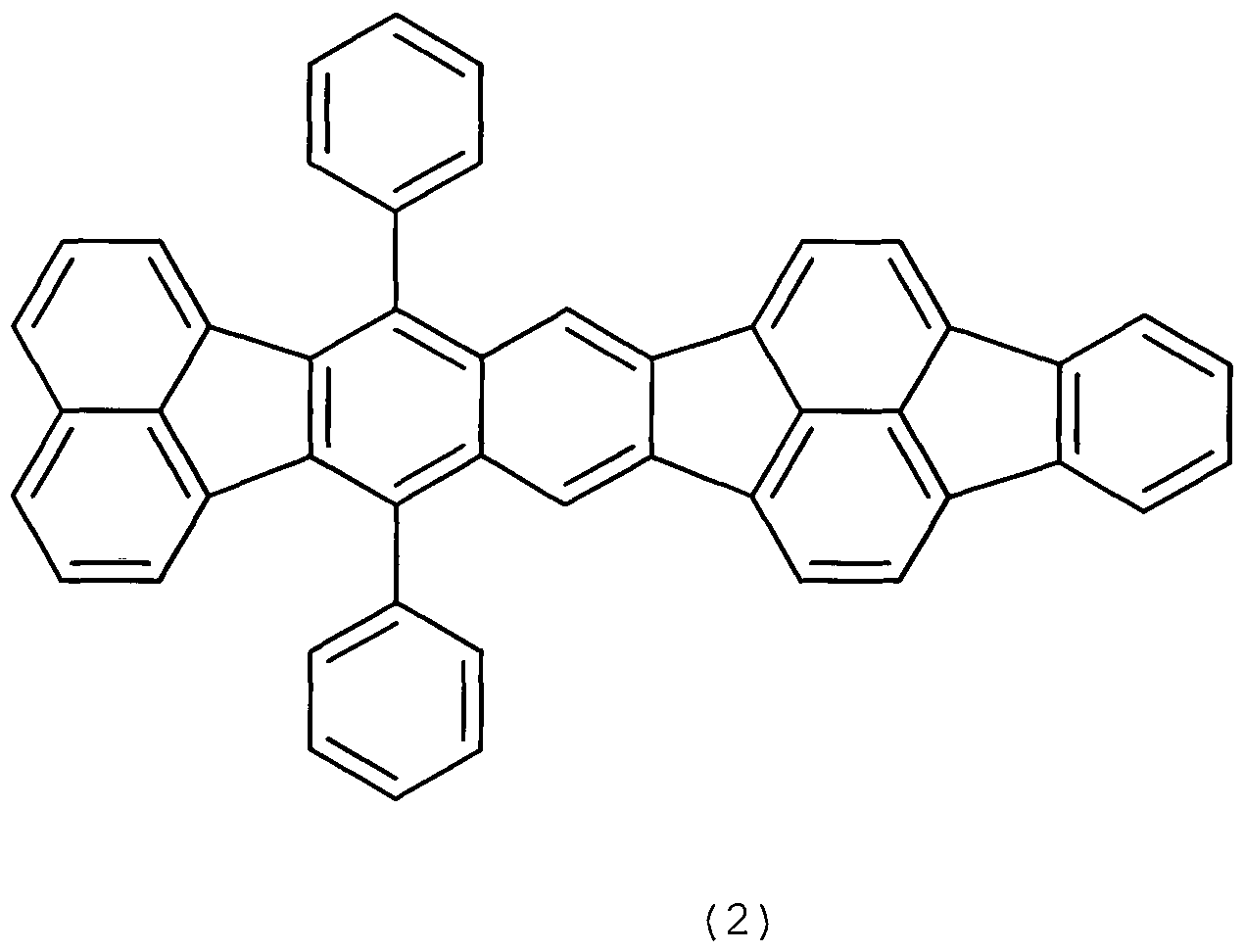
[Химическая формула 5]
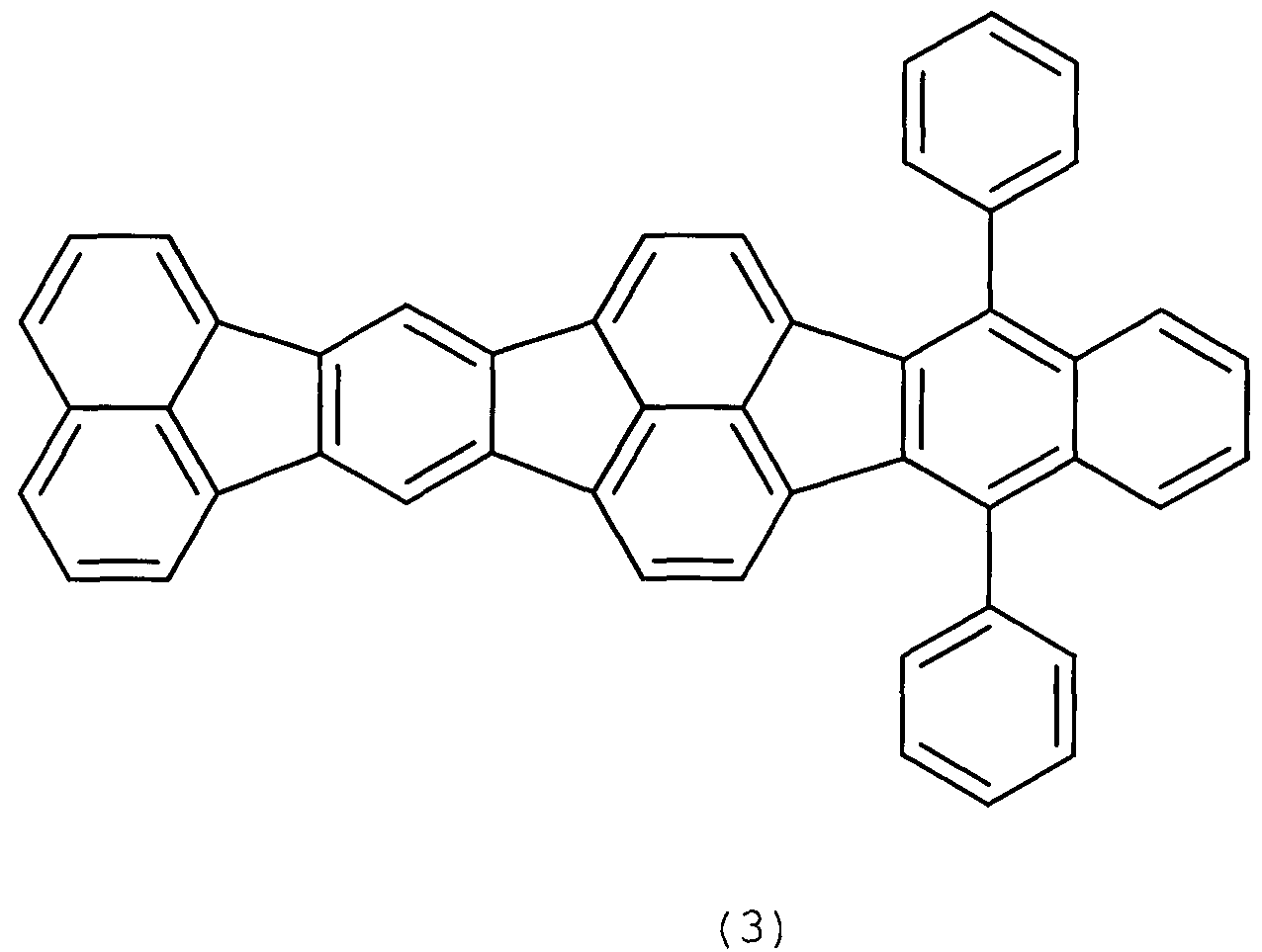
Один пример органического соединения согласно варианту осуществления представляет собой соединение, представленное формулой (4), где основная структура представлена формулой (1); группы R1-R3, R5-R7, R9-R14, R16-R18 и R20 представляют собой атомы водорода; и группы R4, R8, R15 и R19 представляют собой фенильные группы.
[Химическая формула 6]
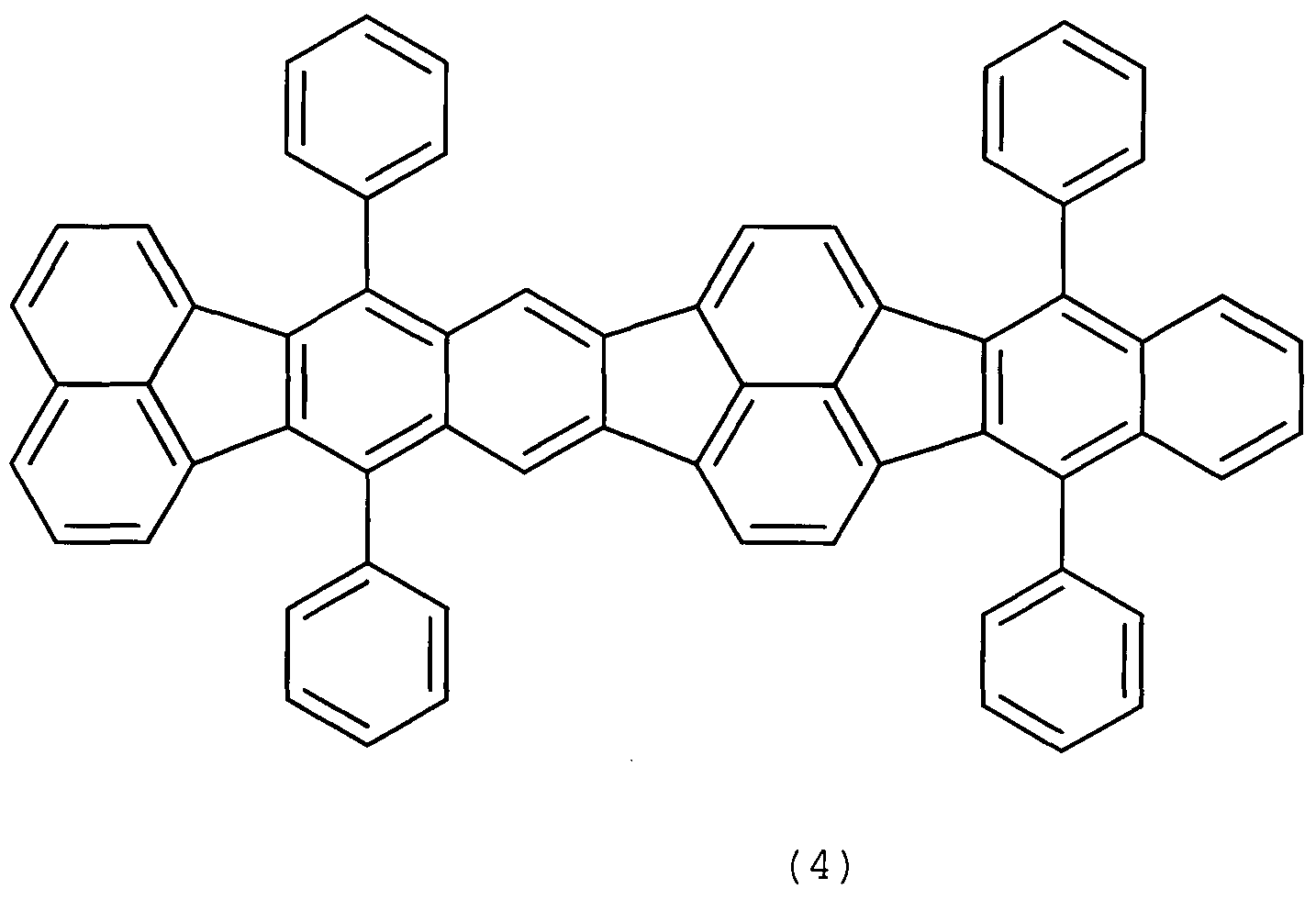
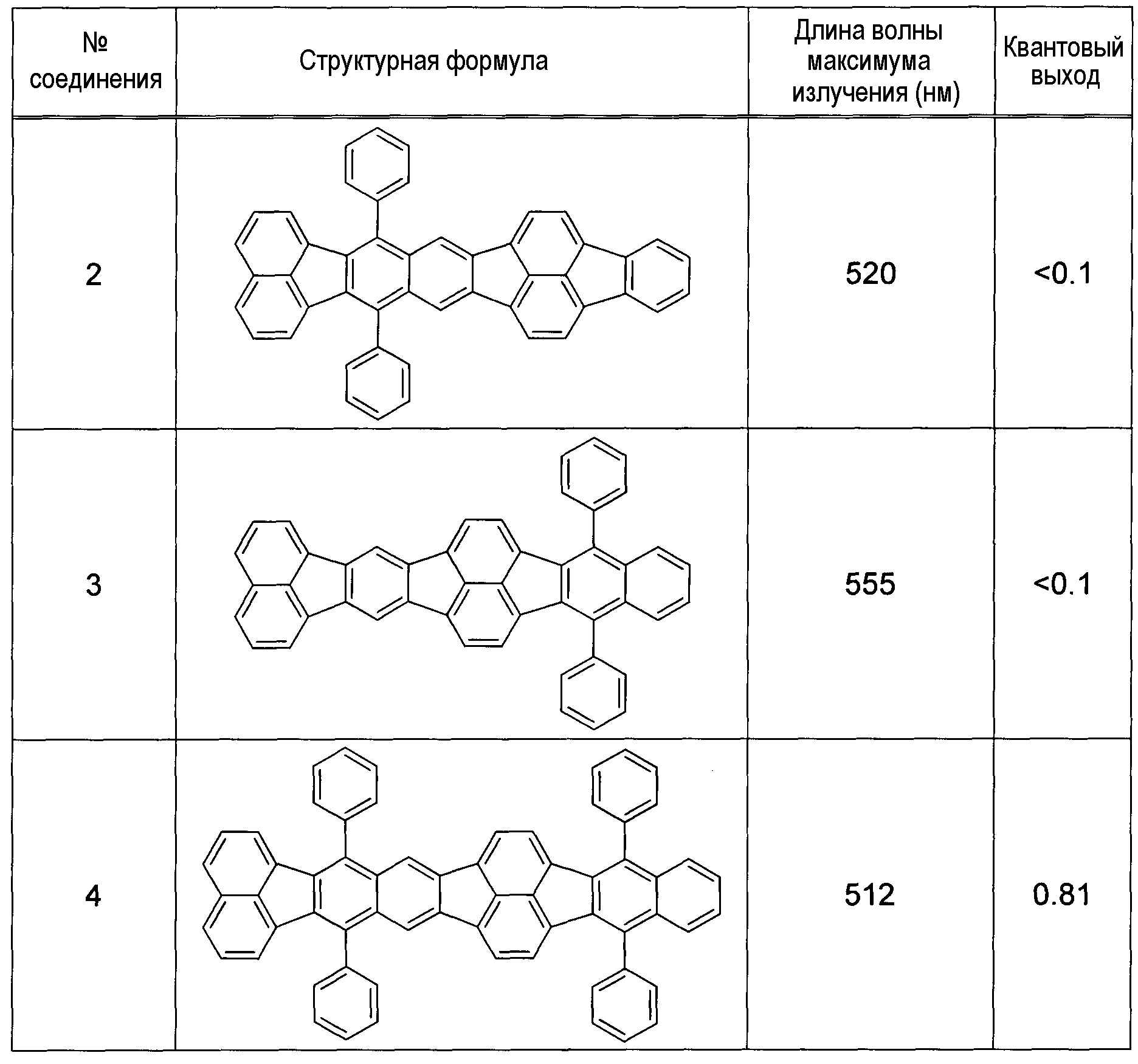
Авторы настоящего изобретения сравнивали органическое соединение, представленное формулой (4), с органическими соединениями, представленными формулами (2) и (3), в отношении длины волны излучения и квантового выхода в разбавленном толуольном растворе. Результаты представлены в таблице 1.
Цвет люминесценции соединения 2, которое представлено в таблице 1, является зеленым, но его квантовый является низким, составляя менее чем 0,1, то есть приблизительно одну десятую квантового выхода, который имеет соединение 4. Это означает, что энергия, производимая в результате рекомбинации дырок и электронов, не может быть эффективно преобразована в свет.
Цвет люминесценции соединения 3, которое представлено в таблице 1, является не зеленым, а желтым, и его квантовый выход низким, составляя менее чем 0,1, то есть приблизительно одну десятую квантового выхода, который имеет соединение 4.
Соединение 4, которое представлено в таблице 1, представляет собой органическое соединение согласно варианту осуществления и имеет высокий квантовый выход по сравнению с вышеупомянутыми материалами, а также имеет цвет люминесценции, подходящий для зеленого стандартного цвета дисплейных устройств.
Фиг. 3 представляет спектры соединения 4 в качестве органического соединения согласно варианту осуществления и соединения 3 в качестве сравнительного соединения.
В спектре соединения 4, который обозначен ссылочной позицией 26, полная ширина на полувысоте максимума спектра при длине волны максимума излучения составляет 30 нм или менее. С другой стороны, в спектре соединения 3, который обозначен ссылочной позицией 25, полная ширина на полувысоте максимума при длине волны максимума излучения составляет 50 нм или более.
Данное различие ширины влияет на цветовую чистоту цвета люминесценции. Чем меньше ширина, тем более высокой является чистота цвета, и чем больше ширина, чем ниже чистота цвета.
Согласно варианту осуществления, полная ширина на полувысоте максимума, когда интенсивность излучения пика при длине волны максимума излучения спектра излучения нормирована как 1, представляет собой разность значений длины волны справа и слева от пика, соответствующих интенсивности излучения на уровне 0,5.
При этом цвет люминесценции органического соединения согласно варианту осуществления имеет высокую чистоту по отношению к желательному цвету. Таким образом, данное органическое соединение обеспечивает превосходные характеристики.
Органическое соединение согласно варианту осуществления представляет собой материал, имеющий высокий квантовый выход, составляющий 0,7 или более, и, таким образом, данное соединение является превосходным в качестве зеленого светоизлучающего материала для органического светоизлучающего устройства. В случае органического светоизлучающего устройства с использованием соединения, имеющего высокий квантовый выход, потребление электроэнергии устройства является низким.
Основная структура органического соединения согласно варианту осуществления имеет высокую плоскостность и может, таким образом, вызывать образование эксимеров вследствие межмолекулярного взаимодействия в укладке.
Соответственно, чтобы ингибировать образование эксимеров, в данное соединение может быть введен заместитель. Высокий эффект ингибирования может быть получен посредством введения заместителя по меньшей мере в одно из положений R4, R7, R8, R15, R16 и R19, причем данный заместитель должен, как правило, ориентироваться перпендикулярно плоскости, в которой находится основная структура.
Таким образом, органическое соединение может содержать заместитель, такой как алкильная группа или арильная группа, в данных положениях.
В качестве альтернативы, заместитель можно вводить в любое из положений R5, R6, R9, R10, R13, R14, R17 и R18, которые представляют собой эффективные положения для увеличения межмолекулярного расстояния.
Межмолекулярное взаимодействие в укладке можно также ингибировать посредством введения алкильной группы в положение R1, R2, R10 или R13 органического соединения согласно варианту осуществления.
Введение арильной группы, гетероциклической группы или замещенной или незамещенной аминогруппы в положение R11 или R12 органического соединения согласно варианту осуществления может уменьшать реакционную способность молекулы, и в результате этого получается стабильная молекула.
Органическое соединение согласно варианту осуществления содержит три пятичленных цикла в основной структуре, и в результате этого оно имеет низкий энергетический уровень низшей свободной молекулярной орбитали НСМО. Это означает, что окислительный потенциал данного соединения является низким. Таким образом, органическое соединение согласно варианту осуществления является стабильным в отношении окисления.
В органическом соединении согласно варианту осуществления основную структуру составляют только атомы углерода, и в ней отсутствуют любые гетероатомы, такие как атомы азота. Это также способствует низкому окислительному потенциалу, то есть представляет собой одну причину стабильности органического соединения согласно варианту осуществления по отношению к окислению.
Кристаллизацию молекул органического соединения согласно варианту осуществления можно ингибировать посредством введения заместителя в соединение. Ингибирование кристаллизации приводит к ингибированию концентрационного гашения и к повышению сублимационной способности.
Конкретные примеры алкильной группы в качестве вводимого заместителя включают метильную, этильную, пропильную, бутильную, гексильную и октильную группы. В частности, заместитель может представлять собой стерически крупную алкильную группу, такую как изопропильная или трет-бутильная группа.
Конкретные примеры арильной группы в качестве вводимого заместителя включают фенильную и бифенильную группы. В частности, заместитель может представлять собой арильную группу, содержащую алкильную группу, такую как метильная, изопропильная или трет-бутильная группа.
Такие же эффекты можно получать посредством введения атома фтора в органическое соединение согласно варианту осуществления. Введение атома фтора также приводит к ингибированию концентрационного гашения к повышению сублимационной способности.
Кроме того, введение заместителя в основную структуру также приводит к улучшению способности образования мембраны в способе нанесения покрытия.
Конкретные примеры органического соединения согласно варианту осуществления представлены ниже, но настоящее изобретение не ограничивается данными примерами.
[Химическая формула 7]
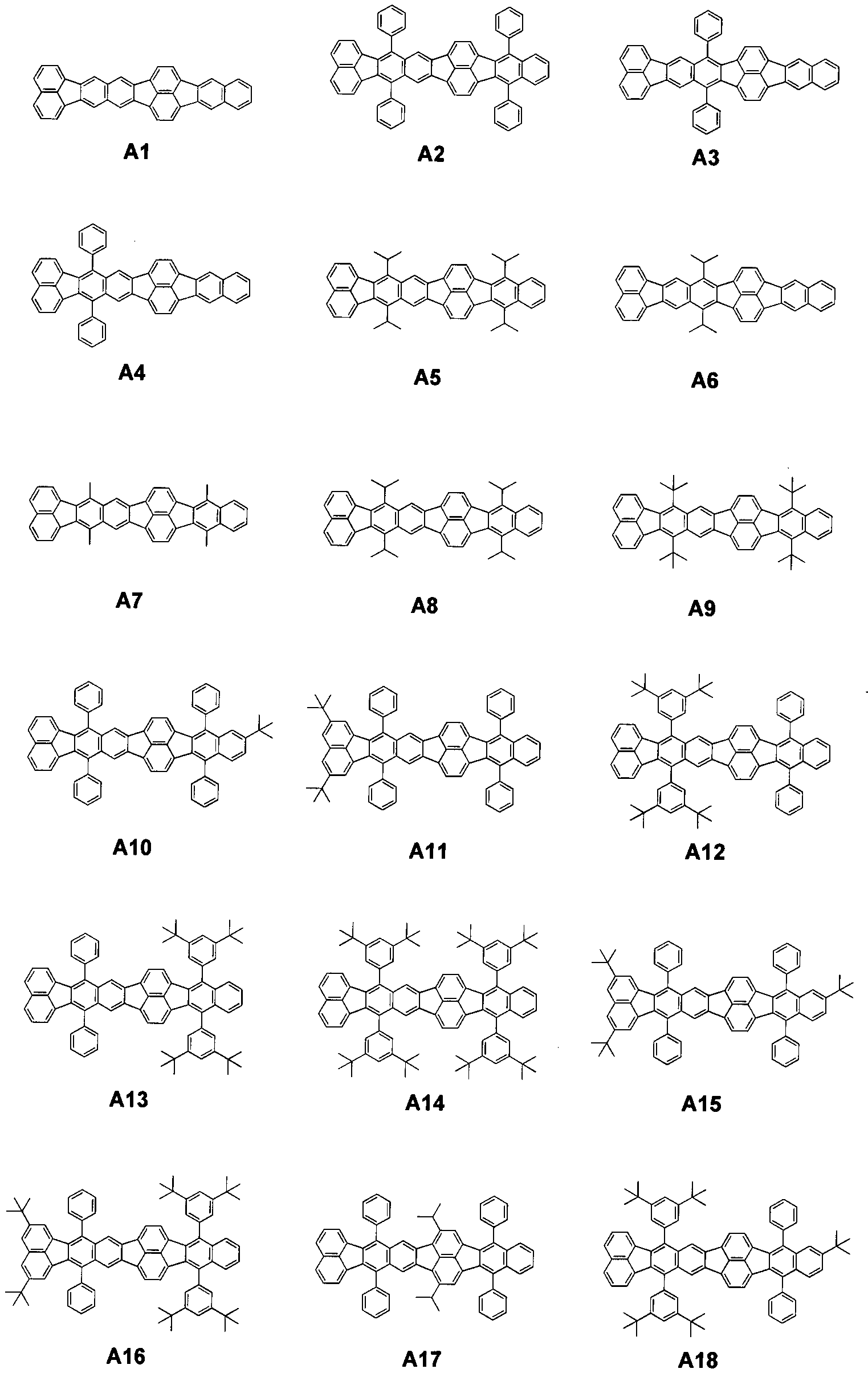
[Химическая формула 8]
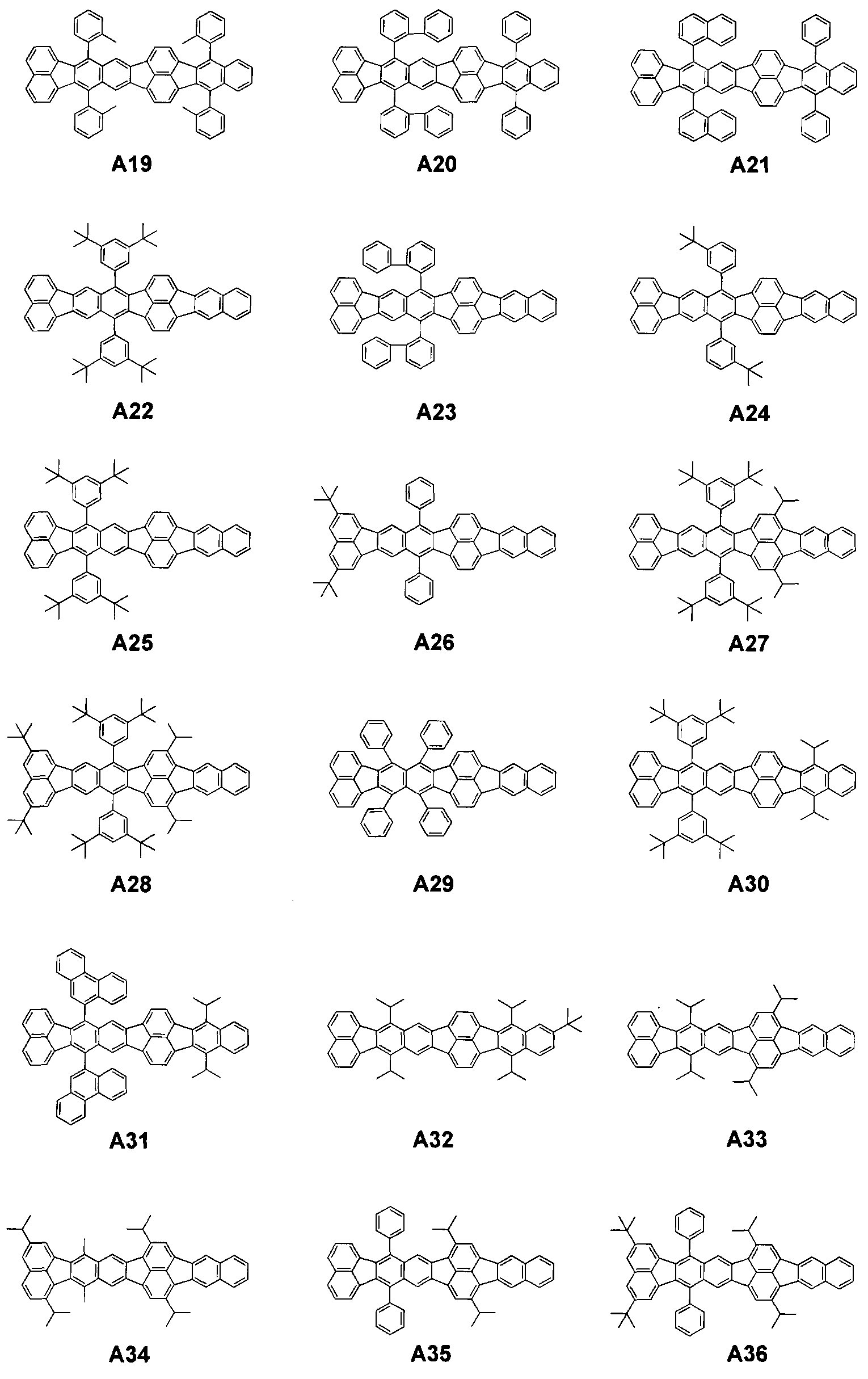
[Химическая формула 9]
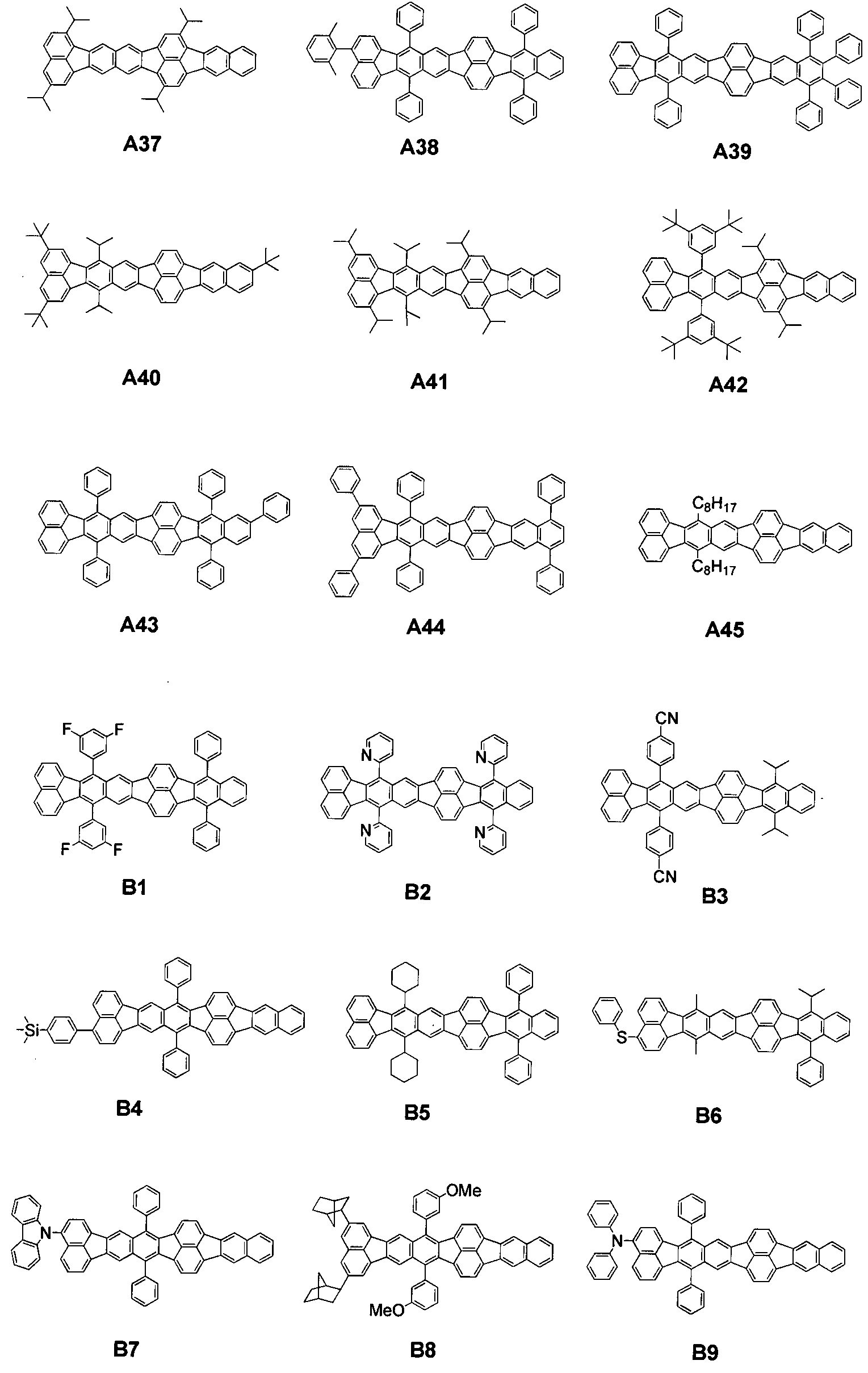
В примерных соединениях, принадлежащих к группе A, молекулу составляют только углеводороды. Согласно настоящему изобретению, соединения, которые составляют только углеводороды, как правило, имеют низкие энергетические уровни НСМО и, таким образом, являются стабильными в отношении окисления.
Соответственно, среди органических соединений согласно варианту осуществления, соединения, которые составляют только углеводороды, т.е., соединения, принадлежащие к группе A, имеют высокую молекулярную стабильность.
Органические соединения, принадлежащие к группе A, можно использовать в светоизлучающем слое, проводящем слое или инжекционном слое в высокой концентрации, составляющей 100%, но при их использовании в светоизлучающем слое концентрация может быть низкой.
В примерных соединениях, принадлежащих к группе B, заместители содержат гетероатомы. Это вызывает изменение окислительного потенциала молекулы или межмолекулярного взаимодействия.
Кроме того, органические соединения, принадлежащие к группе B, в которых заместители содержат гетероатомы, пригодны в качестве проводящих электроны, проводящих дырки или захватывающих дырки светоизлучающих материалов.
В частности, во фторированных соединениях межмолекулярное взаимодействие является слабым, и таким образом, можно предполагать повышение сублимационной способности. Органические соединения, принадлежащие к группе B, можно использовать в высокой концентрации, составляющей 100%.
Синтез органического соединения согласно варианту осуществления
Далее будет описан способ синтеза органического соединения согласно варианту осуществления. Органическое соединение согласно варианту осуществления можно синтезировать, например, в соответствии со следующей схемой реакции.
[Химическая формула 10]
[Химическая формула 11]
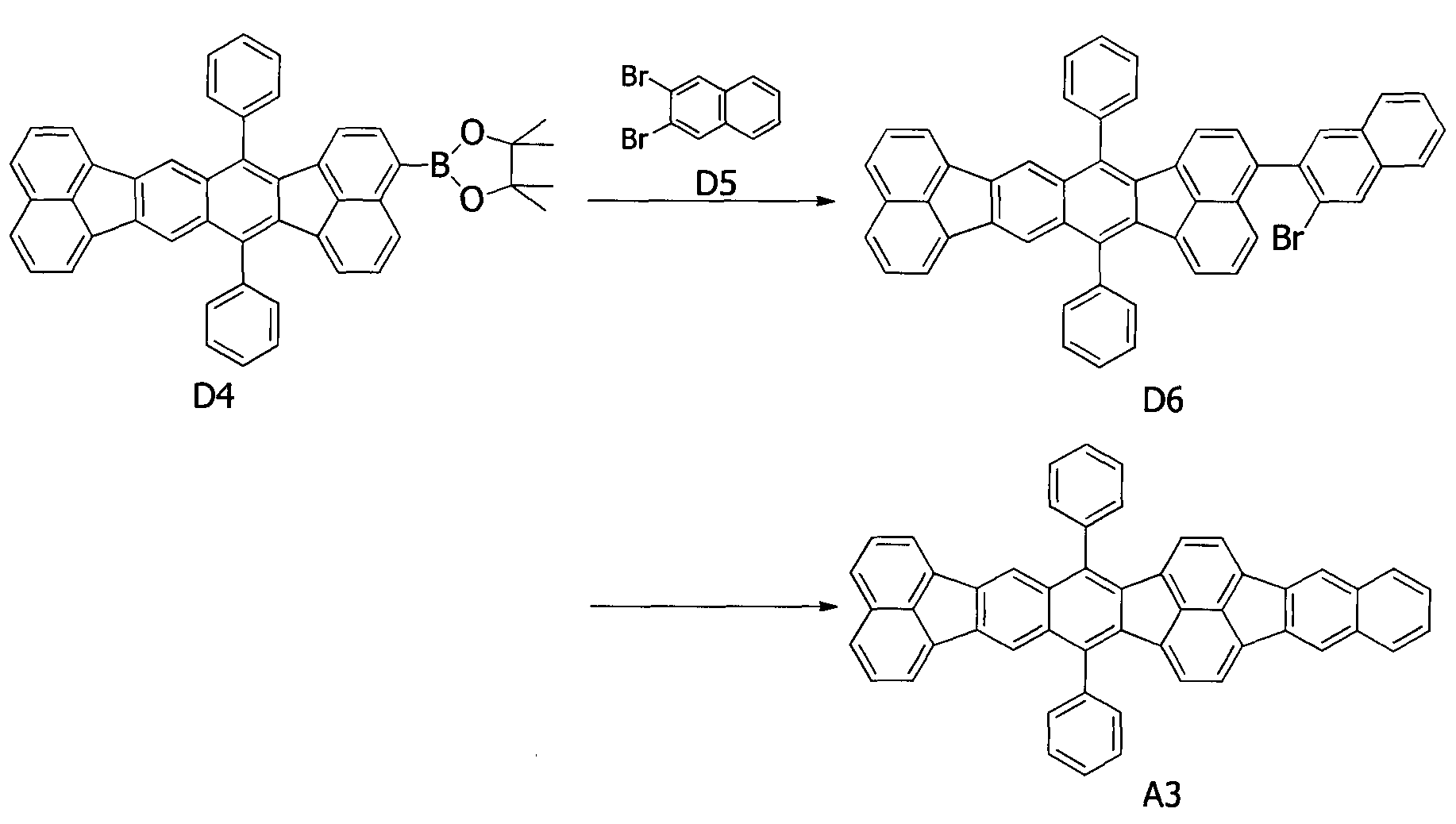
Как представлено в схеме синтеза, органическое соединение согласно варианту осуществления синтезируют, используя следующие соединения (a)-(d) в качестве исходных веществ:
(a) производное бенз[k]флуорантена (D1),
(b) производное бенз[k]флуорантена (D2),
(c) производное флуорантено[8,9-k]флуорантена (D4), и
(d) производное нафталина (D5).
Любой из атомов водорода в положениях R1-R20 в формуле (1) замещается заданным заместителем посредством соответствующего введения заместителя в любое из соединений (a)-(d). Примеры вводимого заместителя включают алкильные группы, атомы галогенов и фенильные, метоксигруппы и цианогруппы.
Разнообразные органические соединения можно синтезировать посредством замены D1-D4 в схеме синтеза.
Свойства органического светоизлучающего устройства согласно варианту осуществления
Далее будет описано органическое светоизлучающее устройство согласно варианту осуществления.
Органическое светоизлучающее устройство согласно варианту осуществления включает анод и катод в качестве примера пары электродов и слой органического соединения, расположенный между этими электродами.
Слой органического соединения органического светоизлучающего устройства согласно варианту осуществления может представлять собой одиночный слой или многослойную систему из множества слоев при том условии, что в ней содержится светоизлучающий слой.
Когда слой органического соединения представляет собой многослойную систему, состоящую из множества слоев, слой органического соединения может включать, в дополнение к светоизлучающему слою, например, инжектирующий дырки слой, проводящий дырки слой, блокирующий электроны слой, блокирующий дырки/экситоны слой, проводящий электроны слой, и инжектирующий электроны слой. Светоизлучающий слой может представлять собой одиночный слой или многослойную систему из множества слоев.
В органическом светоизлучающем устройстве согласно варианту осуществления органическое соединение согласно варианту осуществления содержится в по меньшей мере одном слое из слоев органических соединений.
В органическом светоизлучающем устройстве согласно варианту осуществления органическое соединение согласно настоящему изобретению может содержаться в любом из слоев, и в частности, может содержаться в светоизлучающем слое.
Когда органическое соединение согласно варианту осуществления содержится в светоизлучающем слое органического светоизлучающего устройства согласно варианту осуществления, светоизлучающий слой может быть образован только из органического соединения согласно варианту осуществления, или он может быть образован из органического соединения согласно варианту осуществления и другого соединения.
В случае светоизлучающего слоя, полученного из органического соединения согласно варианту осуществления и еще одного соединения, органическое соединение согласно варианту осуществления можно использовать в качестве легируемого материала или легирующего материала светоизлучающего слоя, или его можно использовать в качестве вспомогательного материала, который может содержаться в светоизлучающем слое.
В настоящем описании легируемый материал представляет собой соединение, имеющее наибольшее массовое соотношение среди соединений, которые составляют светоизлучающий слой, и легирующий материал представляет собой соединение, имеющее наименьшее массовое соотношение по сравнению с легируемым материалом среди соединений, составляющих светоизлучающий слой и производящих основное световое излучение.
Вспомогательный материал представляет собой соединение, имеющее меньшее массовое соотношение, чем легируемый материал, среди соединений, которые составляют светоизлучающий слой, и содействует световому излучению легирующего материала. Вспомогательный материал также обозначается как «второй легируемый материал».
Когда органическое соединение согласно варианту осуществления используется в качестве легирующего материала светоизлучающего слоя, концентрация легирующего материала может составлять 0,01 масс.% или более и 20 масс.% или менее, в частности, 0,1 масс.% или более и 5 масс.% или менее по отношению к суммарной массе светоизлучающего слоя.
Когда органическое соединение согласно варианту осуществления используется в качестве легирующего материала светоизлучающего слоя, материал, имеющий более высокий уровень НСМО, чем уровень органического соединения согласно варианту осуществления (материал, имеющий уровень НСМО, близкий к уровню вакуума) можно использовать в качестве легируемого материала.
Это объясняется тем, что поскольку органическое соединение согласно варианту осуществления имеет низкий уровень НСМО, органическое соединение согласно варианту осуществления может легко принимать электроны, которые поставляет легируемый материал светоизлучающего слоя, когда легируемый материал имеет более высокий уровень НСМО, чем уровень органического соединения согласно варианту осуществления.
Когда органическое соединение согласно варианту осуществления используется в качестве легируемого или легирующего материала светоизлучающего слоя органического светоизлучающего устройства, в частности, используется в качестве легирующего материала светоизлучающего слоя, органическое светоизлучающее устройство имеет оптический выход с высокой эффективностью и высокой яркостью и проявляет высокую долговечность.
Органическое светоизлучающее устройство согласно варианту осуществления может излучать зеленый свет, но цвет люминесценции не ограничивается зеленым и может представлять собой, например, белый или промежуточный цвет.
Когда органическое светоизлучающее устройство согласно варианту осуществления излучает белый свет, светоизлучающие слои излучают свет цветов, отличающихся друг от друга, т.е., красный, зеленый и синий, и белый свет излучается посредством смешивания соответствующих цветов люминесценции. Органическое соединение согласно варианту осуществления может представлять собой материал, излучающий зеленый свет.
Органическое белое светоизлучающее устройство согласно варианту осуществления может представлять собой конфигурацию, содержащую множество светоизлучающих слоев, или конфигурацию, содержащую светоизлучающую часть, которая включает множество светоизлучающих материалов.
Фиг. 1 представляет собой схематическое изображение поперечного сечения, которое иллюстрирует конфигурацию устройства, имеющего светоизлучающий слой многослойного типа и представляющего собой пример органического белого светоизлучающего устройства согласно варианту осуществления. Данная фигура изображает органическое светоизлучающее устройство, имеющее три светоизлучающих слоя, которые излучают свет цветов, отличающихся друг от друга. Данная структура будет подробно описана ниже.
Это органическое светоизлучающее устройство имеет конфигурацию устройства, в котором анод 1, инжектирующий дырки слой 2, проводящий дырки слой 3, синий светоизлучающий слой 4, зеленый светоизлучающий слой 5, красный светоизлучающий слой 6, проводящий электроны слой 7, инжектирующий электроны слой 8 и катод 9, ламинированы на подложку, такую как стеклянная подложка. Можно изменять последовательность ламинирования синего, зеленого и красного светоизлучающих слоев.
Конфигурация светоизлучающих слоев не ограничивается ламинированием, и слои могут быть расположены горизонтально. В горизонтальной конфигурации каждый светоизлучающий слой находится в контакте с прилегающими слоями, такими как проводящий дырки слой и проводящий электроны слой.
Светоизлучающий слой может иметь конфигурацию, в которой светоизлучающий слой, который излучает свет одного цвета, включает область светоизлучающего слоя, который излучает свет другого цвета.
Светоизлучающие материалы синего светоизлучающего слоя и красного светоизлучающего слоя не ограничиваются конкретным образом, и соответствующие примеры включают соединения, имеющие основную структуру хризена, основную структуру флуорантена или основную структуру антрацена; комплексы бора и комплексы иридия.
Согласно настоящему изобретению, в дополнение к органическому соединению согласно варианту осуществления, можно необязательно использовать, например, известное низкомолекулярное или высокомолекулярное инжектирующее или проводящее дырки соединение, легируемый материал, светоизлучающее соединение или инжектирующее или проводящее электроны соединение.
Примеры этих соединений будут представлены ниже.
В качестве инжектирующего или проводящего дырки соединения можно использовать материал, имеющий высокую подвижность дырок. Примеры низкомолекулярного или высокомолекулярного материала, имеющего способность инжектировать или проводить дырки, включают, но не ограничиваются этим, производные триариламина, производные фенилендиамина, производные стильбена, производные фталоцианина, производные порфирина, поливинилкарбазол, политиофен и другие электропроводящие полимеры.
Конкретные примеры легируемых материалов включают соединения, представленные в таблице 2.
Настоящее изобретение не ограничивается данными примерами. Кроме того, производные соединений, представленных в таблице 2, также можно использовать в качестве легируемых материалов. Кроме того, соединения, отличающиеся от соединений, представленных в таблице 2, можно использовать в качестве легируемых материалов. Примеры таких соединений включают, но не ограничиваются этим, конденсированные циклические соединения (например, производные флуорена, производные нафталина, производные антрацена, производные пирена, производные карбазола, производные хиноксалина и производные хинолина), органические комплексы алюминия, такие как трис(8-хинолинолят) алюминия, органические комплексы цинка, производные трифениламина и производные полимеров, такие как производные полифлуорена и производные полифенилена.
Инжектирующее или проводящее электроны соединение выбирают соответствующим образом, принимая во внимание, например, баланс с подвижностью дырок инжектирующего или проводящего дырки соединения. Примеры соединения, имеющего способность инжектировать или проводить электроны, включают, но не ограничиваются этим, производные оксадиазола, производные оксазола, производные пиразина, производные триазола, производные триазина, производные хинолина, производные хиноксалина, производные фенантролина и органические комплексы алюминия.
В качестве составляющего материала анода используют материал, имеющий более высокую работу выхода. Соответствующие примеры включают элементарные металлы, такие как золото, платина, серебро, медь, никель, палладий, кобальт, селен, ванадий и вольфрам; сплавы двух или более элементарных металлов; а также оксиды металлов, такие как оксид олова, оксид цинка, оксид индия, оксид индия и олова (ITO) и оксид индия и цинка. Кроме того, можно использовать электропроводящие полимеры, такие как полианилин, полипиррол и политиофен. Эти электродные материалы можно использовать индивидуально или в комбинации. Анод может иметь однослойную структуру или многослойную структуру.
С другой стороны, в качестве составляющего материала катода используют материал, имеющий низкую работу выхода, и соответствующие примеры включают щелочные металлы, такие как литий; щелочноземельные металлы, такие как кальций; элементарные металлы, такие как алюминий, титан, марганец, серебро, свинец и хром; и сплавы двух или более элементарных металлов, такие как сплавы магния и серебра, алюминия и лития, алюминия и магния. Кроме того, можно использовать оксиды металлов, такие как оксид индия и олова (ITO). Эти электродные материалы можно использовать индивидуально или в комбинации. Катод может иметь однослойную структуру или многослойную структуру.
В органическом светоизлучающем устройстве согласно варианту осуществления слой, содержащий органическое соединение согласно варианту осуществления, и слои других органических соединений формируют, используя следующие способы. Как правило, тонкие пленки формируют, используя вакуумное осаждение, осаждение ионизированного пара, напыление, плазменное покрытие или известные способы нанесения покрытия (например, центрифугирование, погружение, литье, способ Ленгмюра-Блоджетт (Langmuir-Blodgett, LB) или краскоструйное покрытие) соединений, растворенных в соответствующих растворителях. В случае вакуумного осаждения, нанесения покрытия из раствора или подобного процесса вероятность кристаллизации является низкой, и получаемый в результате слой проявляет превосходную стабильность в течение продолжительного времени. Кроме того, при нанесении покрытия можно формировать пленку в комбинации с соответствующим связующим полимером.
Примеры связующего полимера включают, но не ограничиваются этим, полимеры поливинилкарбазола, поликарбонатные полимеры, сложнополиэфирные полимеры, сополимеры акрилонитрила, бутадиена и стирола (ABS), акриловые полимеры, полиимидные полимеры, фенольные полимеры, эпоксидные полимеры, кремнийорганические полимеры и полимеры мочевины. Эти связующие полимеры можно использовать индивидуально в форме гомополимера или сополимера или в комбинации двух или более полимеров. Кроме того, в пленках могут необязательно содержаться известные добавки, такие как пластификаторы, антиоксиданты и поглощающие ультрафиолетовое излучение.
Использование органического светоизлучающего устройства согласно варианту осуществления
Органическое светоизлучающее устройство согласно варианту осуществления можно использовать в качестве составляющего элемента дисплейного устройства или системы освещения. Другие примеры использования включают облучающие источники света, создающие электрофотографическое изображение устройства, заднее освещение жидкокристаллических дисплейных устройств и источники белого света. Органическое светоизлучающее устройство может дополнительно включать цветной светофильтр.
Дисплейное устройство включает органическое светоизлучающее устройство согласно варианту осуществления в дисплейной секции. Эта дисплейная секция включает множество элементов изображения, и каждый из элементов изображения включает органическое светоизлучающее устройство согласно варианту осуществления и активное устройство. Анод или катод органического светоизлучающего устройства присоединяется к электроду стока или к электроду истока активного устройства. Здесь дисплейное устройство можно использовать в качестве блока экрана, например, персонального компьютера (PC).
Примеры активного устройства включают переключающие устройства и усилительные устройства, более конкретно, транзисторы и устройства со структурой типа металл-диэлектрик-металл (MIM). Примеры транзисторов включают устройства TFT.
Дисплейное устройство может представлять собой устройство обработки видеоинформации, которое включает вводящую изображение секцию для ввода видеоинформации, например, из двухмерного устройства с зарядной связью (CCD), одномерного CCD или карты памяти и демонстрирует введенное изображение на дисплейной секции.
Дисплейное устройство может представлять собой тип с использованием сенсорной панельной системы для ввода информации.
Система освещения представляет собой устройство, которое освещает, например, помещение. Система освещения может излучать свет, имеющий белый, натуральный белый или любой цвет от синего до красного. Система освещения включает органическое светоизлучающее устройство согласно варианту осуществления и преобразователь переменного тока в постоянный (AC/DC), присоединенный к устройству. Белый цвет имеет цветовую температуру, составляющую приблизительно 4200 К, и натуральный белый свет имеет цветовую температуру, составляющую приблизительно 5000 К. Система освещения может содержать цветной светофильтр.
Преобразователь переменного тока в постоянный (AC/DC) согласно варианту осуществления преобразует переменное напряжение (AC) в постоянное напряжение (DC). Преобразователь переменного тока в постоянный подает возбуждающее напряжение на систему освещения.
Органическое светоизлучающее устройство согласно варианту осуществления можно использовать в облучающем блоке устройства формирования изображения, которое включает светочувствительный элемент, зарядный блок для зарядки светочувствительного элемента, облучающий блок для облучения светочувствительного элемента и проявляющее устройство для проявления электростатического скрытого изображения, формируемого на поверхности светочувствительного элемента.
Облучающий блок имеет облучающий источник света для облучения светочувствительного элемента. Облучающий источник света имеет множество светоизлучающих точек расположенных рядами. Световой поток каждой из этих светоизлучающих точек можно регулировать независимо.
Далее дисплейное устройство с использованием органического светоизлучающего устройства согласно варианту осуществления будет описано со ссылкой на Фиг. 2.
Фиг. 2 представляет схематическое изображение поперечного сечения дисплейного устройства, имеющего органические светоизлучающие устройства согласно варианту осуществления и устройства TFT, присоединенные к органическим светоизлучающим устройствам.
Дисплейное устройство включает подложку 10, такую как стеклянная подложка и влагонепроницаемую пленку 11, расположенную на подложке 10 для защиты устройства TFT или слоя органического соединения. Ссылочная позиция 12 обозначает металлический электрод затвора, ссылочная позиция 13 обозначает изолирующую пленку затвора, и ссылочная позиция 14 обозначает полупроводниковый слой.
Устройство TFT 17 включает полупроводниковый слой 14, электрод стока 15 и электрод истока 16. На устройство TFT 17 нанесена изолирующая пленка 18. Анод 20 органического светоизлучающего устройства и электрод истока 16 присоединены посредством контактного окна 19.
Дисплейное устройство согласно варианту осуществления не ограничивается данной конфигурацией при том условии, что анод или катод присоединяется к электроду истока или электроду стока устройства TFT.
На Фиг. 2 слой органического соединения 21 многослойной структуры представлен как одиночный слой. Слой органического соединения может представлять собой одиночный слой или многослойную систему. Кроме того, на катод 22 нанесены первый защитный слой 23 и второй защитный слой 24 для защиты органического светоизлучающего устройства от разрушения.
Когда свет, излучаемый дисплейным устройством согласно варианту осуществления, является, например, белым, светоизлучающий слой, имеющий многослойную конструкцию, которая представлена на Фиг. 1, используется в качестве слоя органического соединения 21 на Фиг. 2.
В органическом светоизлучающем устройстве согласно варианту осуществления яркость регулирует устройство TFT в качестве примера переключающего устройства. Органические светоизлучающие устройства, расположенные во множестве плоскостей, могут демонстрировать изображения с соответствующей яркостью.
Переключающее устройство органического светоизлучающего устройства согласно варианту осуществления не ограничивается устройством TFT и может представлять собой транзистор, устройство MIM или активный матричный формирователь, нанесенный на подложку, такую как кремниевая подложка. Транзистор, нанесенный на подложку, представляет собой транзистор, непосредственно нанесенный на подложку, такую как кремниевая подложка. Выбор осуществляется в зависимости от разрешения. Например, при разрешении, составляющем приблизительно 320×240 точек на дюйм (http://www.multitran.ru/c/m.exe?a=116&&UserName=lainQVGA) активные устройства могут быть нанесены на кремниевую подложку.
Дисплей, имеющий хорошее качество изображения и стабильность даже в случае продолжительной работы, можно получить посредством управления дисплейным устройством с использованием органических светоизлучающих устройств согласно варианту осуществления.
Примеры
Далее настоящее изобретение будет описано посредством примером, но оно не ограничивается данными примерами.
Пример 1
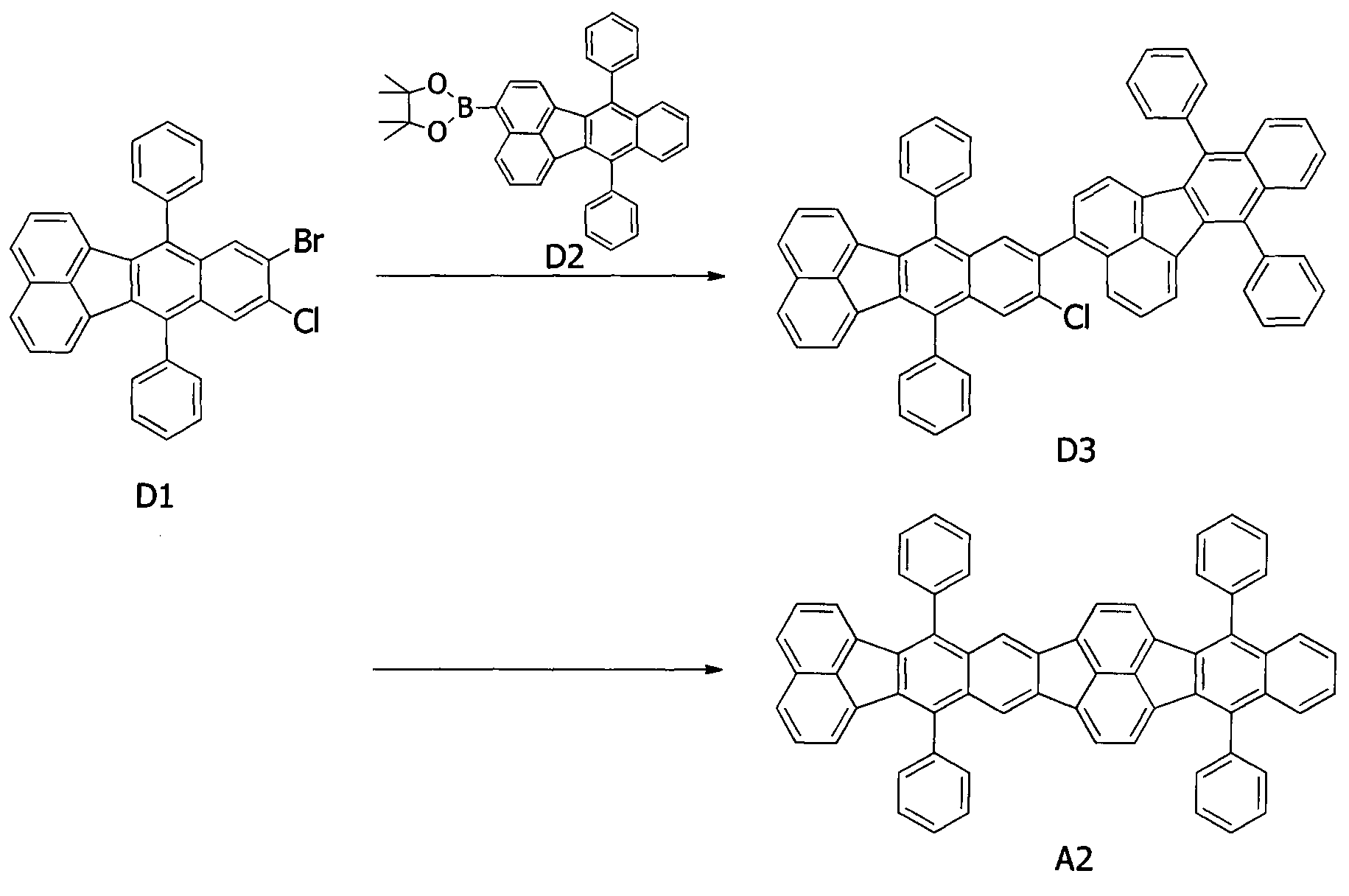
Синтез примерного соединения A2
[Химическая формула 12]
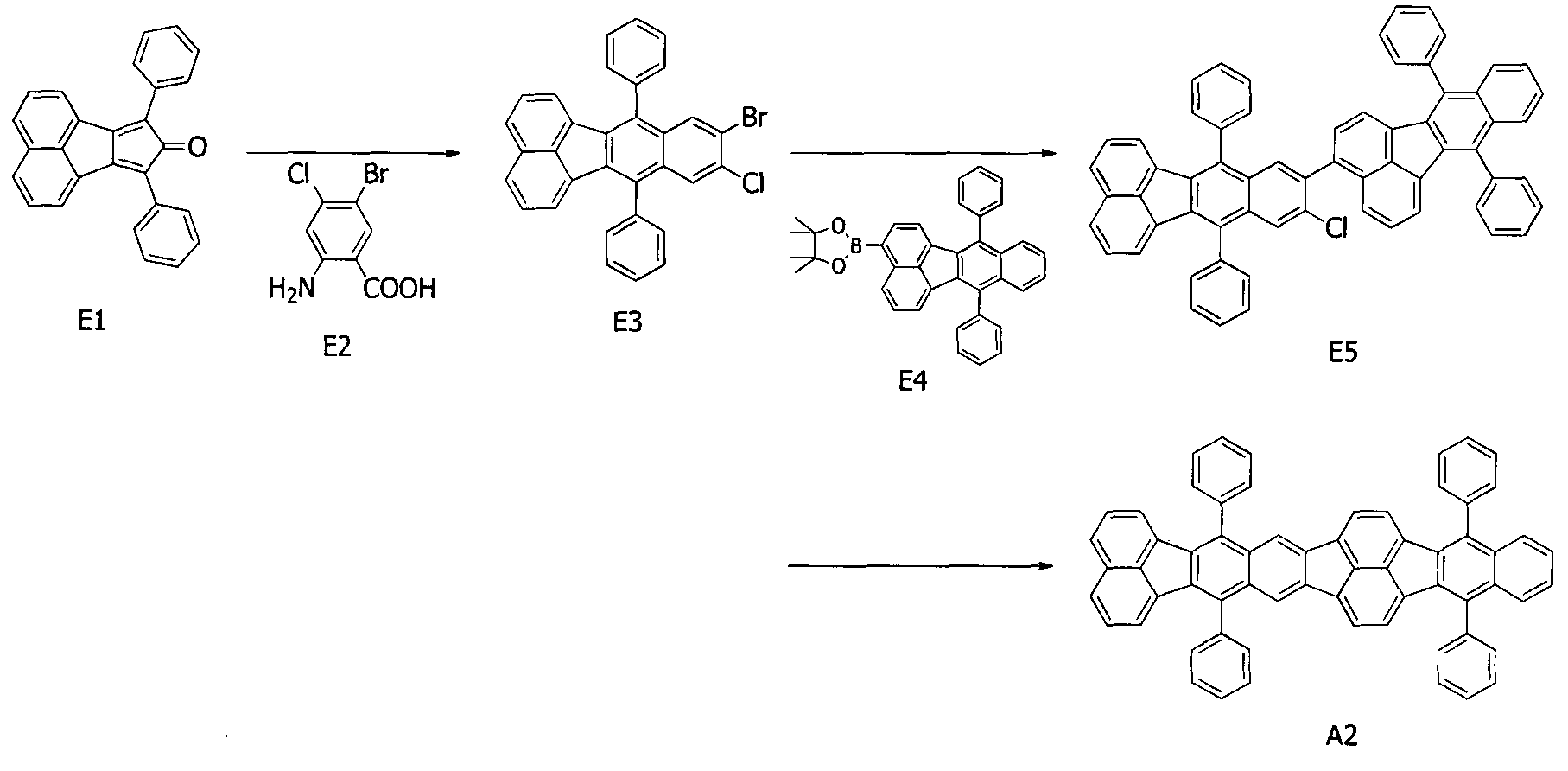
(1) Синтез соединения E3
В испарительную колбу объемом 100 мл помещали следующие реагенты и растворители:
соединение E1: 3,56 г (10 ммоль),
соединение E2: 3,25 г (13 ммоль),
изоамилнитрит: 1,52 г (13 ммоль) и
толуол: 50 мл.
Затем реакционный раствор нагревали до 110°C и перемешивали при данной температуре (110°C) в течение 3 часов в потоке газообразного азота. После завершения реакции органический слой промывали два раза, используя по 50 мл воды, а затем насыщенным раствором хлорида натрия и высушивали над сульфатом магния. Получаемый в результате раствор фильтровали, и фильтрат концентрировали, получая темно-коричневый раствор. Данный раствор очищали посредством колоночной хроматографии (хлороформ:гептан=1:4), после чего осуществляли перекристаллизацию из смеси хлороформ/метанол, получая 4,3 г (выход 83%) соединения E3 в форме желтых кристаллов.
(2) Синтез соединения E5
В испарительную колбу объемом 200 мл помещали следующие реагенты и растворители:
соединение E4: 2,59 г (5 ммоль),
соединение E5: 2,65 г (5 ммоль),
Pd(PPh3)4: 0,1 г,
толуол: 50 мл,
этанол: 20 мл и
водный раствор 2 М карбоната натрия: 50 мл
Затем реакционный раствор нагревали до 80°C и перемешивали при данной температуре (80°C) в течение 8 часов в потоке газообразного азота. После завершения реакции этанол добавляли в реакционный раствор для осаждения кристаллов. Кристаллы собирали посредством фильтрования и промывали путем последовательного диспергирования в воде, этаноле и гептане. После этого получаемые в результате кристаллы растворяли в толуоле при нагревании, и раствор очищали посредством колоночной хроматографии (толуол:гептан=1:3), после чего осуществляли перекристаллизацию из смеси хлороформ/метанол, получая 3,28 г (выход 78%) желтых кристаллов соединения E5.
(3) Синтез примерного соединения A2
В испарительную колбу объемом 20 мл помещали следующие реагенты и растворители:
соединение E5: 841 мг (1 ммоль),
Pd(dba)2: 238 мг,
P(Cy)3 (трициклогексилфосфин): 280 мг,
DBU (диазабициколоундецен): 0,15 мл и
DMF: 5 мл
Затем реакционный раствор нагревали до 145°C и перемешивали при данной температуре (145°C) в течение 6 часов в потоке газообразного азота. После завершения реакции этанол добавляли в реакционный раствор для осаждения кристаллов. Кристаллы собирали посредством фильтрования и промывали путем последовательного диспергирования в воде, этаноле и гептане. После этого получаемые в результате фиолетовые кристаллы растворяли в толуоле при нагревании, и раствор фильтровали в горячем состоянии, после чего осуществляли перекристаллизацию из смеси толуол/метанол, получая 0,60 г (выход 75%) оранжевых кристаллов примерного соединения A2.
Методом высокоэффективной жидкостной хроматографии (ВЭЖХ) подтверждено, что чистота данного соединения составляла 99% или более. Спектр излучения толуольного раствора примерного соединения A2 при концентрации, составляющей 1×10-5 моль/л, показывал максимальную интенсивность при 512 нм, когда фотолюминесценцию измеряли при длине волны возбуждения 350 нм, используя флуоресцентный спектрофотометр F-4500, изготовленный компанией Hitachi, Ltd. Массу примерного соединения A2 анализировали методом времяпролетной масс-спектрометрии с лазерной ионизацией и десорбцией из жидкой матрицы (MALDI-TOF-MS), используя прибор Autoflex LRF, изготовленный компанией Bruker.
MALDI-TOF-MS
Наблюдаемое значение: m/z = 804,11, вычисленное значение: C64H36 = 804,28.
Пример 2
Синтез примерного соединения A3
[Химическая формула 13]
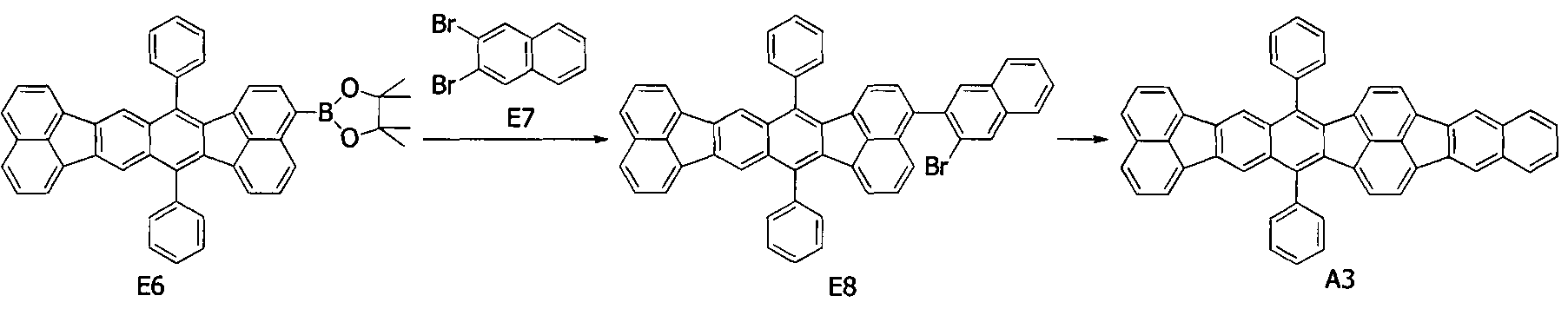
(1) Синтез соединения E8
В испарительную колбу объемом 200 мл помещали следующие реагенты и растворители:
соединение E6: 3,27 г (5 ммоль),
соединение E7: 1,43 г (5 ммоль),
Pd(PPh3)4: 0,1 г,
толуол: 50 мл,
этанол: 20 мл и
водный раствор 2 М карбоната натрия: 50 мл.
Затем реакционный раствор нагревали до 60°C и перемешивали при данной температуре (60°C) в течение 5 часов в потоке газообразного азота. После завершения реакции этанол добавляли в реакционный раствор для осаждения кристаллов. Кристаллы собирали посредством фильтрования и промывали путем последовательного диспергирования в воде, этаноле и гептане. После этого получаемые в результате кристаллы растворяли в толуоле при нагревании, и раствор очищали посредством колоночной хроматографии (толуол:гептан=1:3), после чего осуществляли перекристаллизацию из смеси хлороформ/метанол, получая 2,1 г (выход 58%) желтых кристаллов соединения E8.
(2) Синтез примерного соединения A3
В испарительную колбу объемом 20 мл помещали следующие реагенты и растворители:
соединение E5: 734 мг (1 ммоль),
Pd(dba)2: 238 мг,
P(Cy)3 (трициклогексилфосфин): 280 мг,
DBU (диазабициколоундецен): 0,15 мл и
DMF: 5 мл
Затем реакционный раствор нагревали до 145°C и перемешивали при данной температуре (145°C) в течение 6 часов в потоке газообразного азота. После завершения реакции этанол добавляли в реакционный раствор для осаждения кристаллов. Кристаллы собирали посредством фильтрования и промывали путем последовательного диспергирования в воде, этаноле и гептане. После этого получаемые в результате фиолетовые кристаллы растворяли в толуоле при нагревании, и раствор фильтровали в горячем состоянии, после чего осуществляли перекристаллизацию из смеси толуол/метанол, получая 0,43 г (выход 66%) оранжевых кристаллов примерного соединения A3.
Методом ВЭЖХ подтверждено, что чистота получаемого в результате соединения составляла 99% или более.
Спектр излучения толуольного раствора примерного соединения A3 (концентрация: 1×10-5 моль/л), показывал максимальную интенсивность при 511 нм при измерении таким же способом, как в примере 1.
Массу примерного соединения A3 анализировали методом MALDI-TOF-MS (Autoflex LRF, изготовленный компанией Bruker).
MALDI-TOF-MS
Наблюдаемое значение: m/z = 652,46, вычисленное значение: C52H28 = 652,22.
Пример 3
Синтез примерного соединения A4
Примерное соединение A4 получали таким же способом, как в примере 2, за исключением того, что соединение E9, представленное ниже, использовали вместо соединения E6 на стадии (1) примера 2.
[Химическая формула 14]
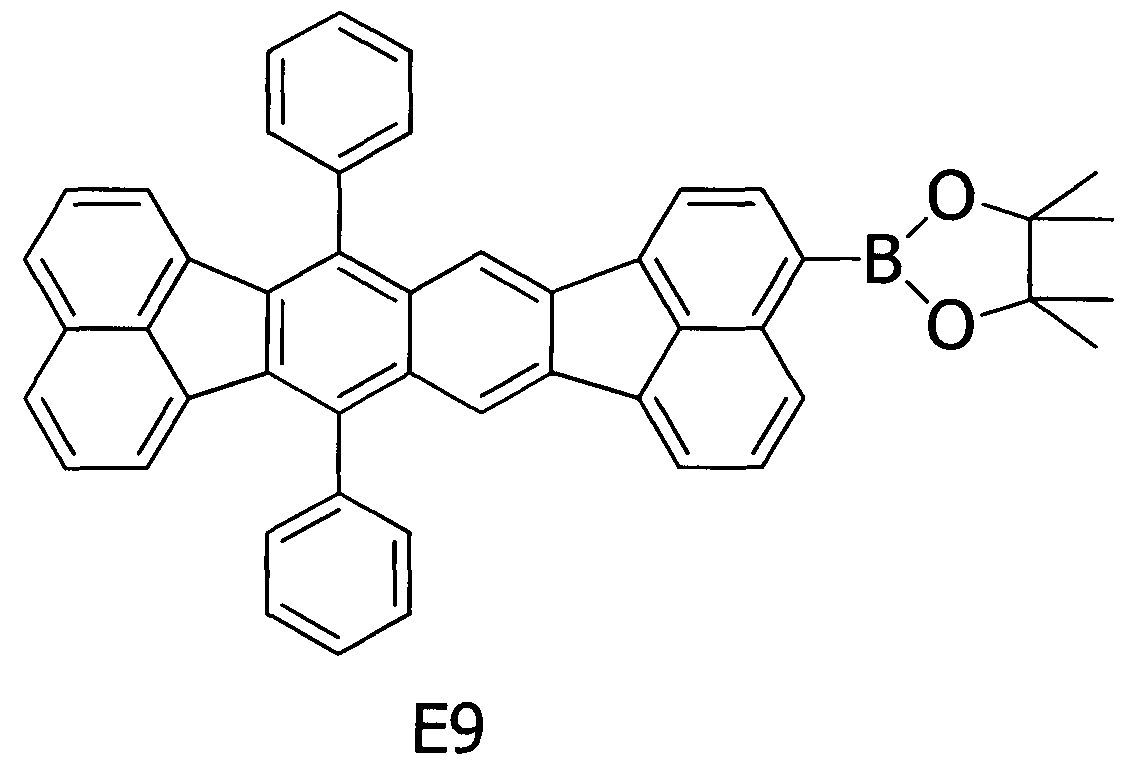
Методом ВЭЖХ подтверждено, что чистота получаемого в результате соединения составляла 99% или более.
Спектр излучения толуольного раствора примерного соединения A4 (концентрация: 1×10-5 моль/л), показывал максимальную интенсивность при 511 нм при измерении таким же способом, как в примере 1.
Массу примерного соединения A4 анализировали методом MALDI-TOF-MS (Autoflex LRF, изготовленный компанией Bruker).
MALDI-TOF-MS
Наблюдаемое значение: m/z = 652,48, вычисленное значение: C52H28 = 652,22.
Пример 4
Синтез примерного соединения A5
Примерное соединение A5 получали таким же способом, как в примере 1, за исключением того, что соединения E10 и E11, представленные ниже, соответственно, использовали вместо соединения E1 на стадии (1) и соединения E4 на стадии (2) примера 1.
[Химическая формула 15]
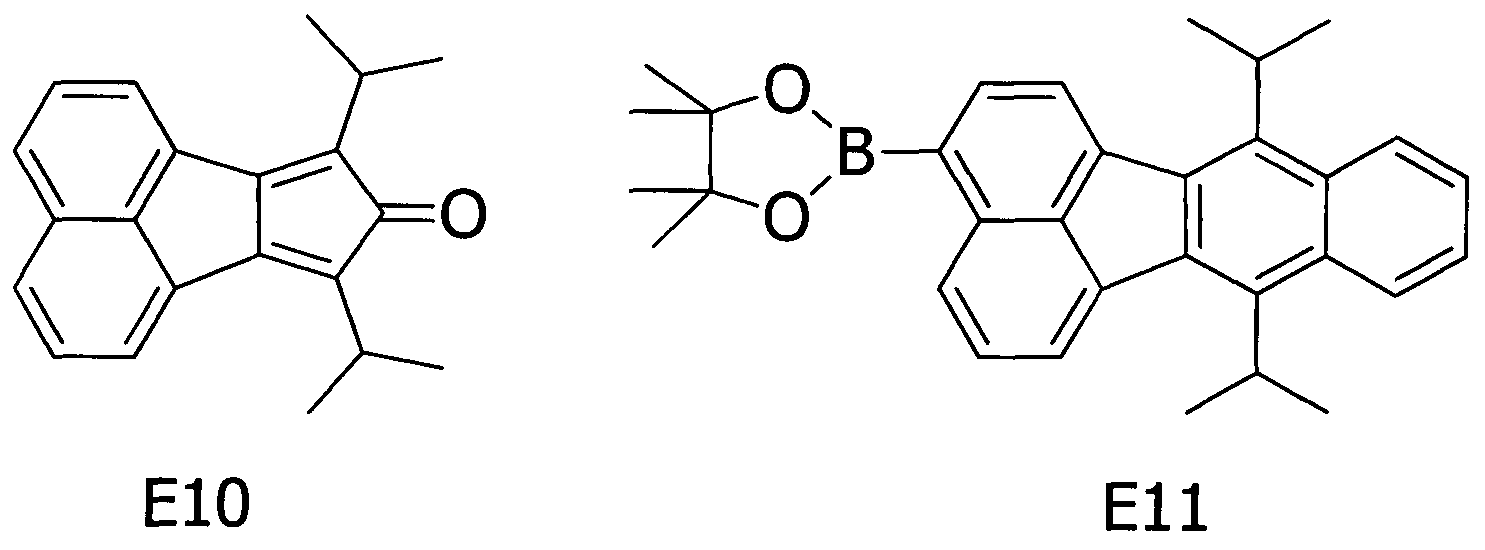
Методом ВЭЖХ подтверждено, что чистота получаемого в результате соединения составляла 99% или более.
Спектр излучения толуольного раствора примерного соединения A5 (концентрация: 1×10-5 моль/л), показывал максимальную интенсивность при 513 нм при измерении таким же способом, как в примере 1.
Массу примерного соединения A5 анализировали методом MALDI-TOF-MS (Autoflex LRF, изготовленный компанией Bruker).
MALDI-TOF-MS
Наблюдаемое значение: m/z = 668,50, вычисленное значение: C53H44 = 668,34.
Пример 5
Синтез примерного соединения A12
Примерное соединение A12 получали таким же способом, как в примере 1, за исключением того, что соединение E12, представленное ниже, использовали вместо соединения E1 на стадии (1) примера 1.
[Химическая формула 16]
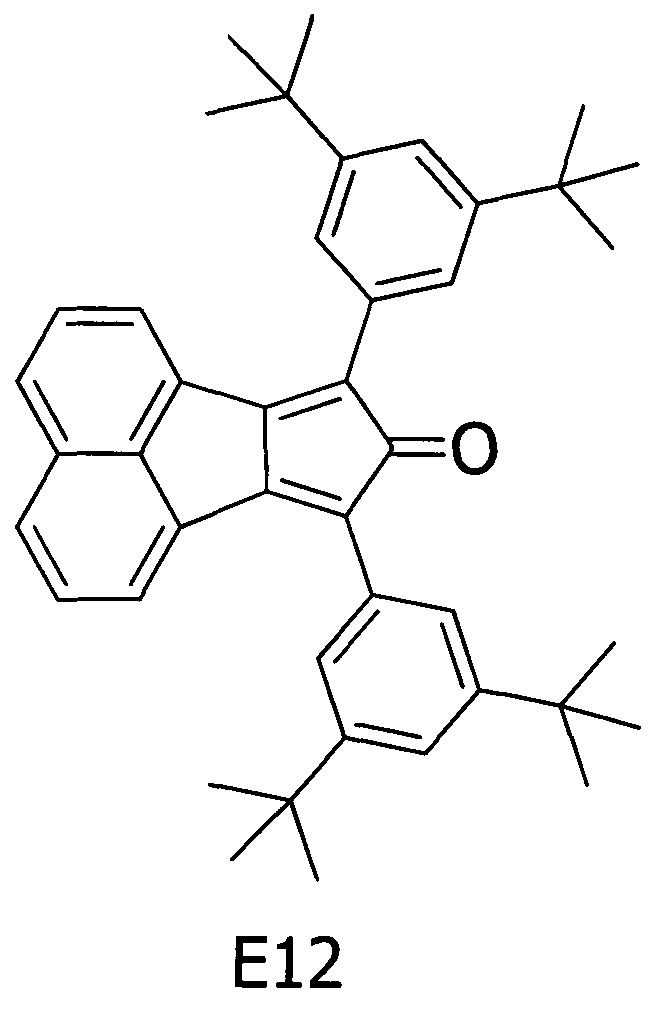
Методом ВЭЖХ подтверждено, что чистота получаемого в результате соединения составляла 99% или более.
Спектр излучения толуольного раствора примерного соединения A12 (концентрация: 1×10-5 моль/л), показывал максимальную интенсивность при 515 нм при измерении таким же способом, как в примере 1.
Массу примерного соединения A12 анализировали методом MALDI-TOF-MS (Autoflex LRF, изготовленный компанией Bruker).
MALDI-TOF-MS
Наблюдаемое значение: m/z = 1028,66, вычисленное значение: C80H68 = 1028,53.
Пример 6
Синтез примерного соединения A14
Примерное соединение A14 получали таким же способом, как в примере 1, за исключением того, что соединения E13 и E14, представленные ниже, соответственно, использовали вместо соединения E1 на стадии (1) и соединения E4 на стадии (2) примера 1.
[Химическая формула 17]
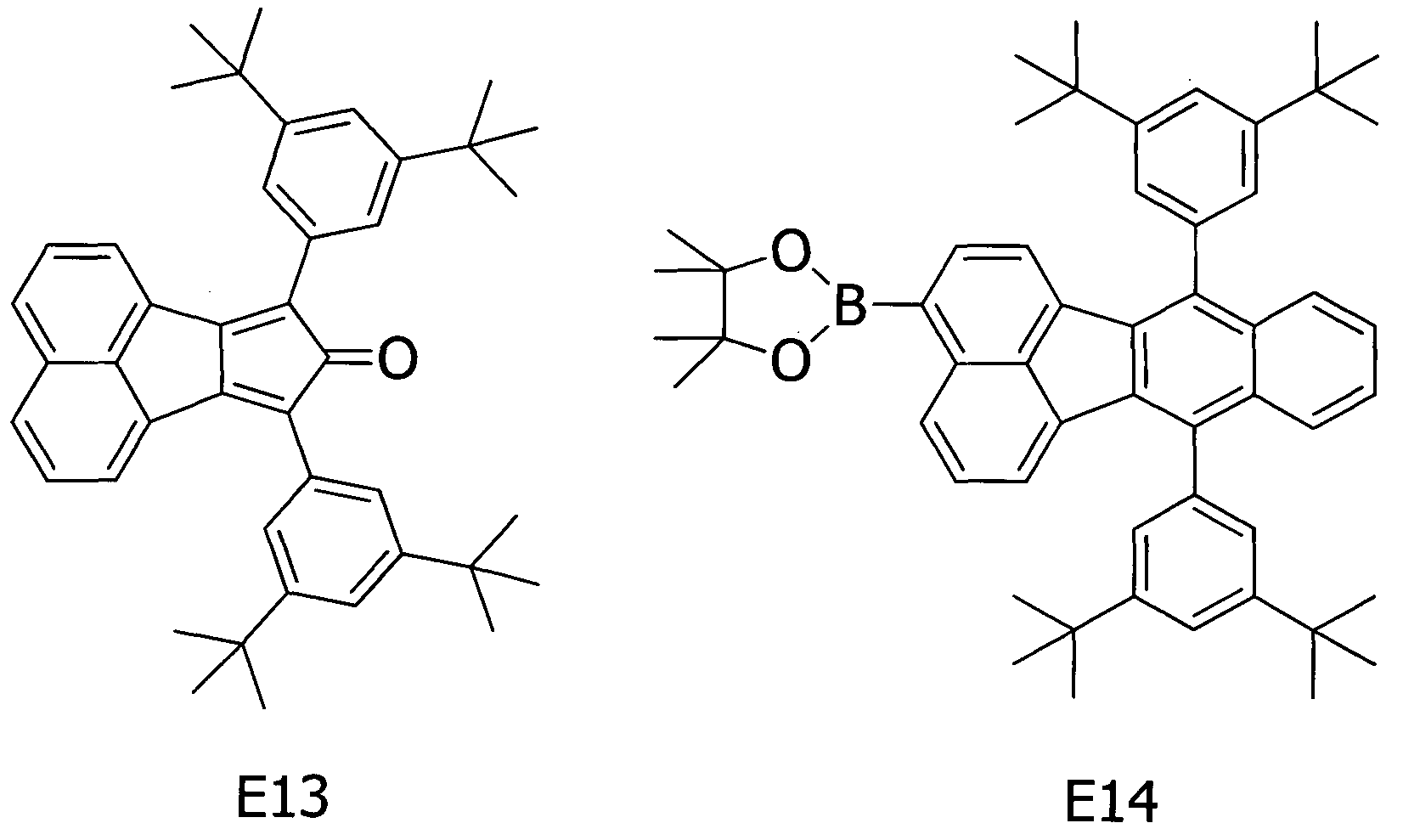
Методом ВЭЖХ подтверждено, что чистота получаемого в результате соединения составляла 99% или более.
Спектр излучения толуольного раствора примерного соединения A14 (концентрация: 1×10-5 моль/л) показывал максимальную интенсивность при 517 нм при измерении таким же способом, как в примере 1.
Массу примерного соединения A14 анализировали методом MALDI-TOF-MS (Autoflex LRF, изготовленный компанией Bruker).
MALDI-TOF-MS
Наблюдаемое значение: m/z = 1252,12, вычисленное значение: C96H100 = 1252,78.
Пример 7
Синтез примерного соединения A15
Примерное соединение A15 получали таким же способом, как в примере 1, за исключением того, что соединения E15 и E16, представленные ниже, соответственно, использовали вместо соединения E1 на стадии (1) и соединения E4 на стадии (2) примера 1.
[Химическая формула 18]
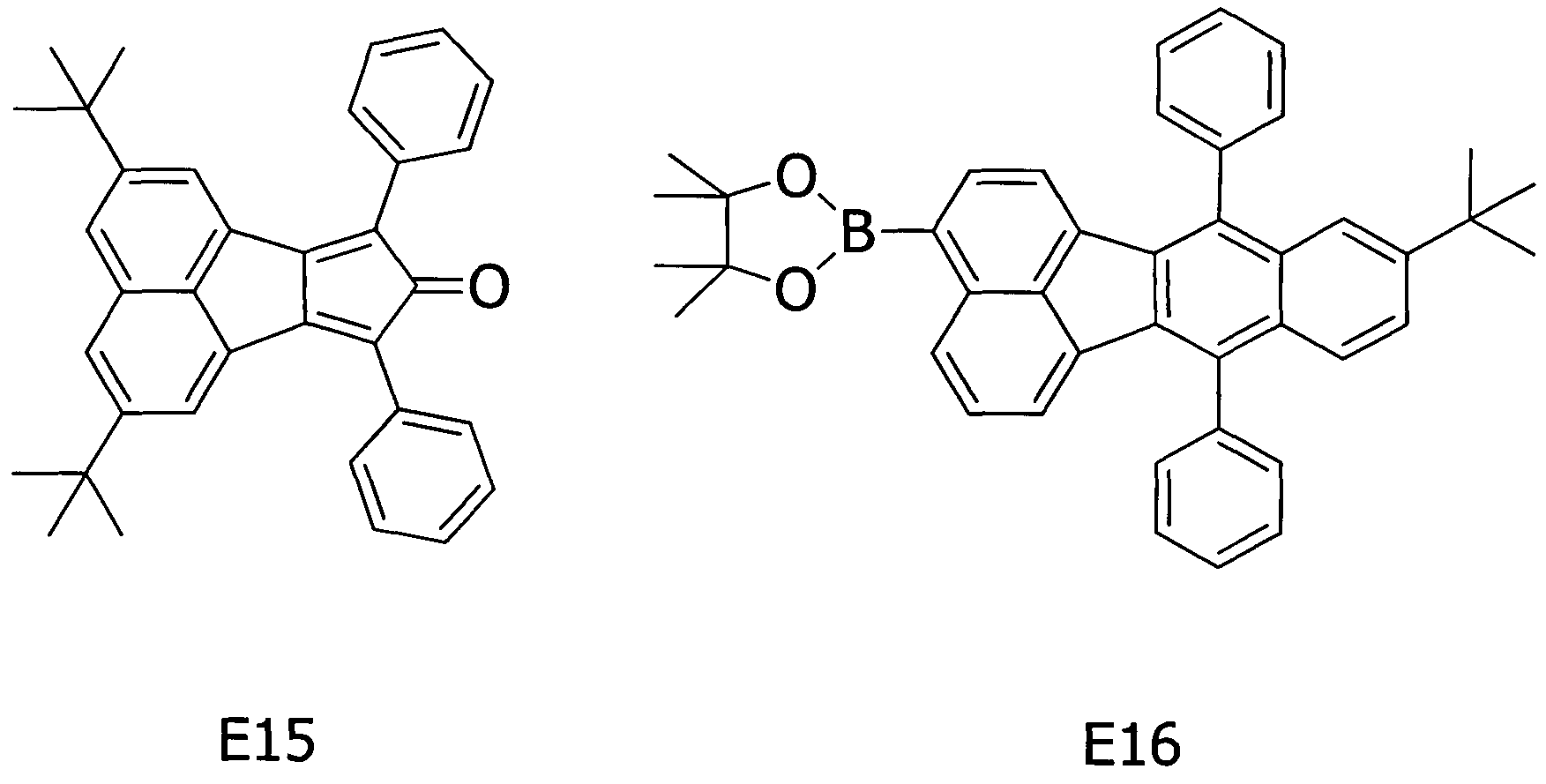
Методом ВЭЖХ подтверждено, что чистота получаемого в результате соединения составляла 98% или более.
Спектр излучения толуольного раствора примерного соединения A15 (концентрация: 1×10-5 моль/л) показывал максимальную интенсивность при 516 нм при измерении таким же способом, как в примере 1.
Массу примерного соединения A15 анализировали методом MALDI-TOF-MS (Autoflex LRF, изготовленный компанией Bruker).
MALDI-TOF-MS
Наблюдаемое значение: m/z = 972,18, вычисленное значение: C76H60 = 972,47.
Пример 8
Синтез примерного соединения A16
Примерное соединение A16 получали таким же способом, как в примере 1, за исключением того, что соединения E17 и E18, представленные ниже, соответственно, использовали вместо соединения E1 на стадии (1) и соединения E4 на стадии (2) примера 1.
[Химическая формула 19]
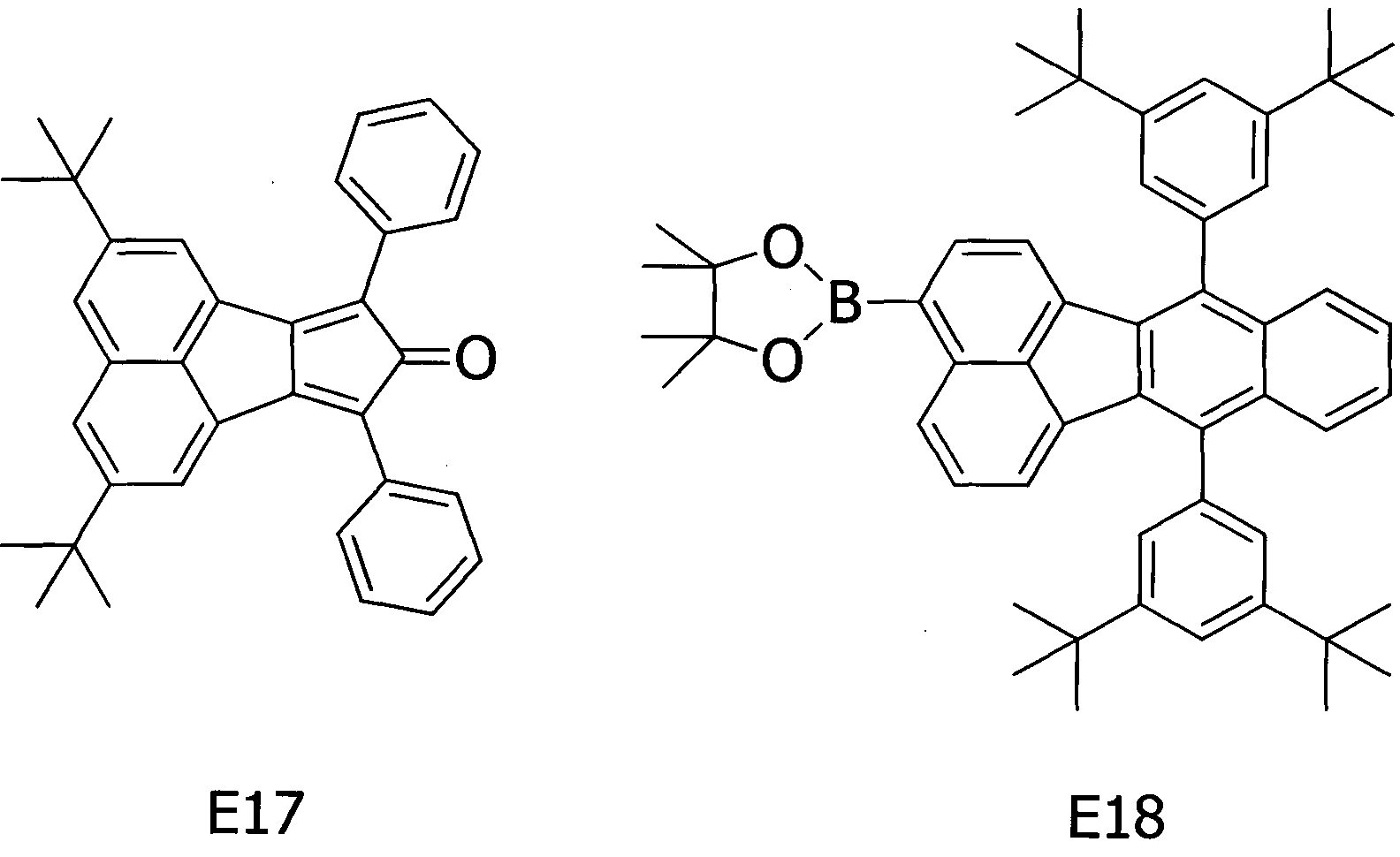
Методом ВЭЖХ подтверждено, что чистота получаемого в результате соединения составляла 99% или более.
Спектр излучения толуольного раствора примерного соединения A16 (концентрация: 1×10-5 моль/л) показывал максимальную интенсивность при 516 нм при измерении таким же способом, как в примере 1.
Массу примерного соединения A16 анализировали методом MALDI-TOF-MS (Autoflex LRF, изготовленный компанией Bruker).
MALDI-TOF-MS
Наблюдаемое значение: m/z = 1140,21, вычисленное значение: C88H84 = 1140,66.
Пример 9
Синтез примерного соединения A22
Примерное соединение A22 получали таким же способом, как в примере 2, за исключением того, что соединение E19, представленное ниже, использовали вместо соединения E6 на стадии (1) примера 2.
[Химическая формула 20]
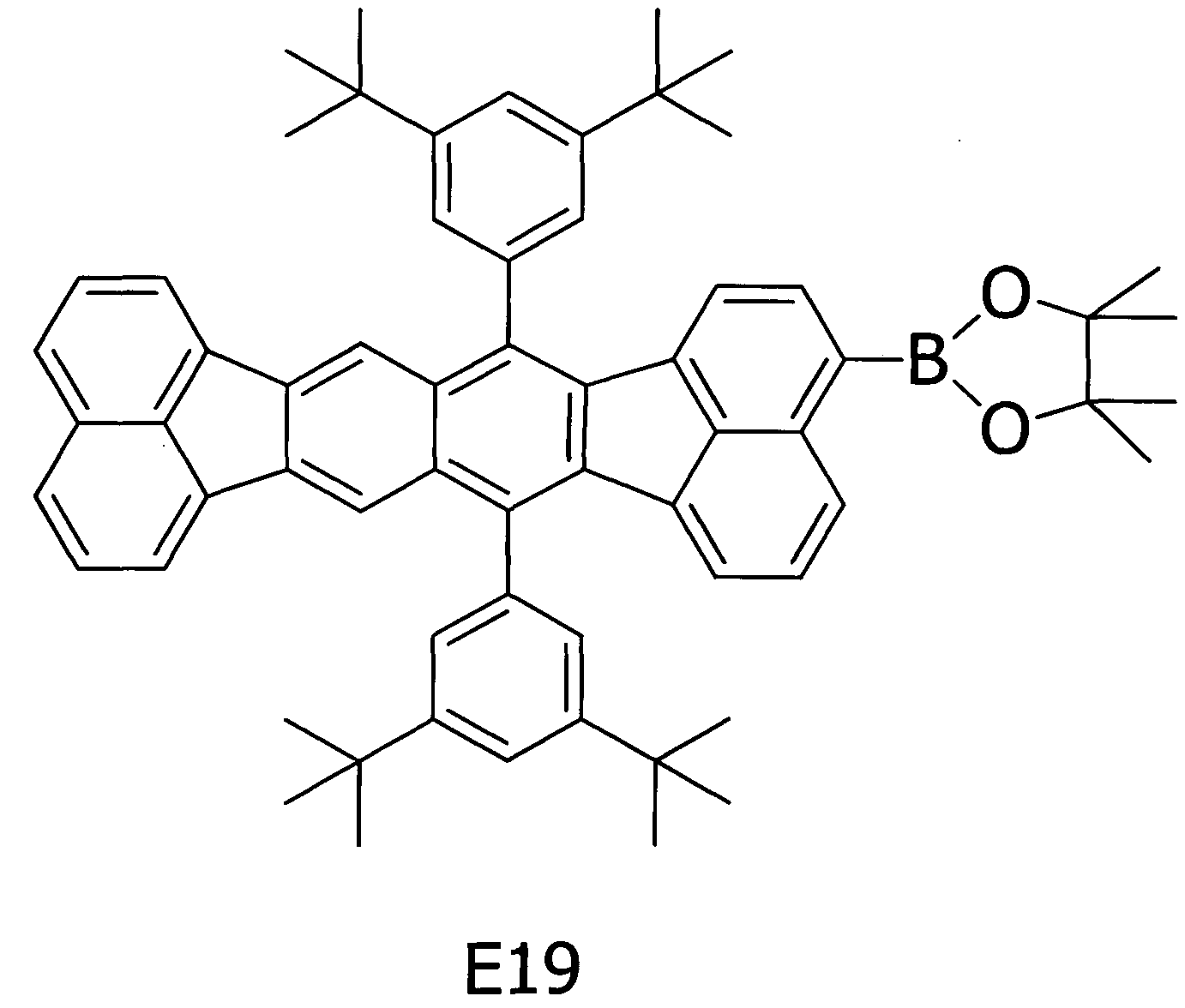
Методом ВЭЖХ подтверждено, что чистота получаемого в результате соединения составляла 99% или более.
Спектр излучения толуольного раствора примерного соединения A22 (концентрация: 1×10-5 моль/л) показывал максимальную интенсивность при 514 нм при измерении таким же способом, как в примере 1.
Массу примерного соединения A22 анализировали методом MALDI-TOF-MS (Autoflex LRF, изготовленный компанией Bruker).
MALDI-TOF-MS
Наблюдаемое значение: m/z = 876,44, вычисленное значение: C68H60 = 876,47.
Пример 10
Синтез примерного соединения A23
Примерное соединение A23 получали таким же способом, как в примере 2, за исключением того, что соединение E20, представленное ниже, использовали вместо соединения E6 на стадии (1) примера 2.
[Химическая формула 21]
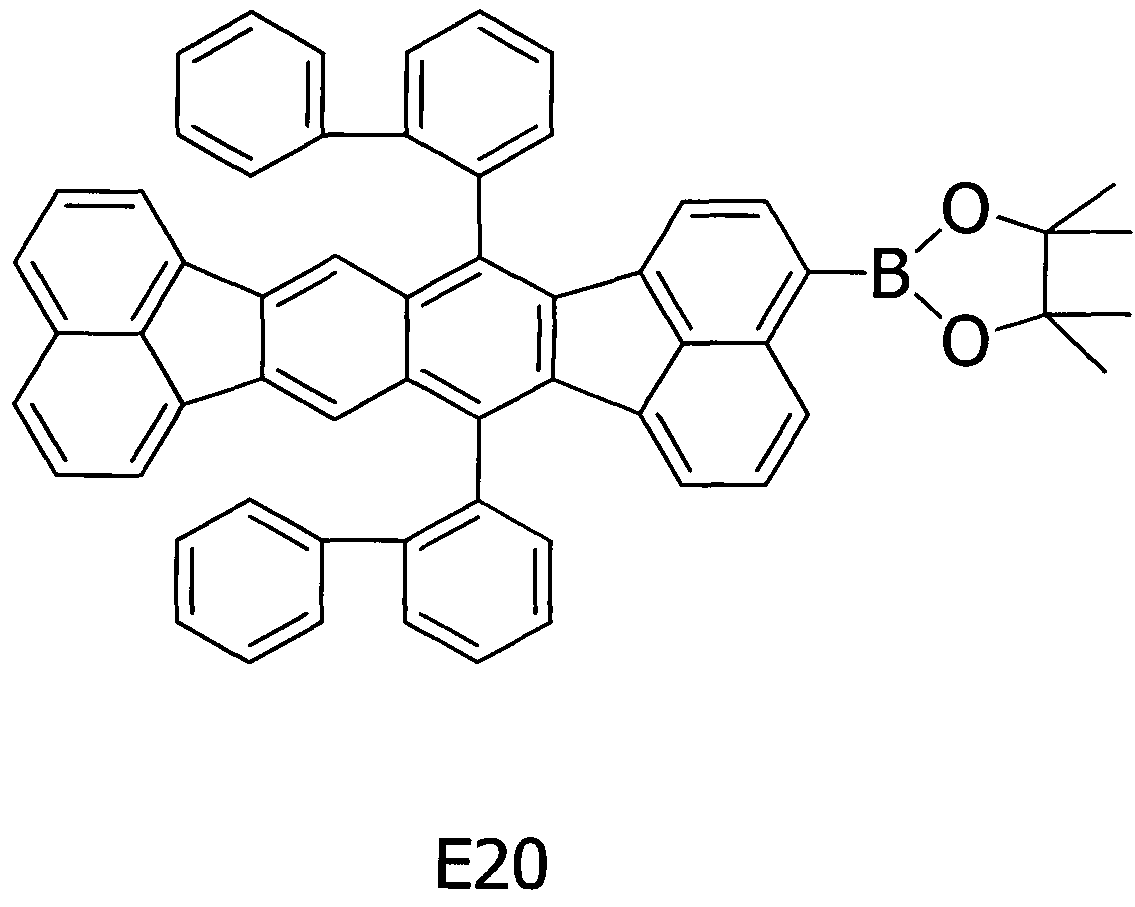
Методом ВЭЖХ подтверждено, что чистота получаемого в результате соединения составляла 97% или более.
Спектр излучения толуольного раствора примерного соединения A23 (концентрация: 1×10-5 моль/л) показывал максимальную интенсивность при 514 нм при измерении таким же способом, как в примере 1.
Массу примерного соединения A23 анализировали методом MALDI-TOF-MS (Autoflex LRF, изготовленный компанией Bruker).
MALDI-TOF-MS
Наблюдаемое значение: m/z = 804,82, вычисленное значение: C64H36 = 804,28.
Пример 11
Синтез примерного соединения A33
Примерное соединение A33 получали таким же способом, как в примере 2, за исключением того, что соединение E21, представленное ниже, использовали вместо соединения E6 на стадии (1) примера 2.
[Химическая формула 22]
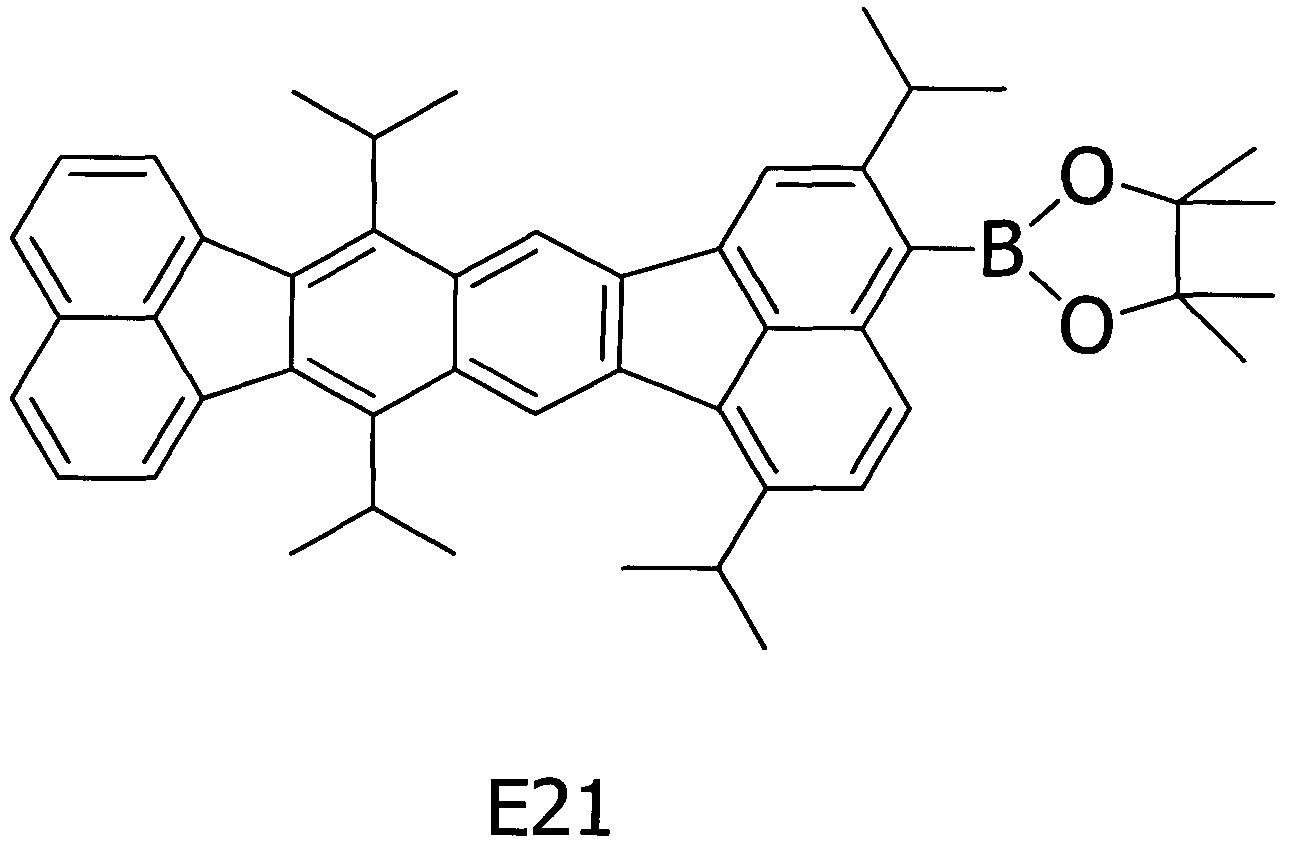
Методом ВЭЖХ подтверждено, что чистота получаемого в результате соединения составляла 99% или более.
Спектр излучения толуольного раствора примерного соединения A33 (концентрация: 1×10-5 моль/л) показывал максимальную интенсивность при 516 нм при измерении таким же способом, как в примере 1.
Массу примерного соединения A33 анализировали методом MALDI-TOF-MS (Autoflex LRF, изготовленный компанией Bruker).
MALDI-TOF-MS
Наблюдаемое значение: m/z = 668,56, вычисленное значение: C52H44 = 668,34.
Пример 12
Синтез примерного соединения A42
Примерное соединение A42 получали таким же способом, как в примере 2, за исключением того, что соединение E22, представленное ниже, использовали вместо соединения E6 на стадии (1) примера 2.
[Химическая формула 23]
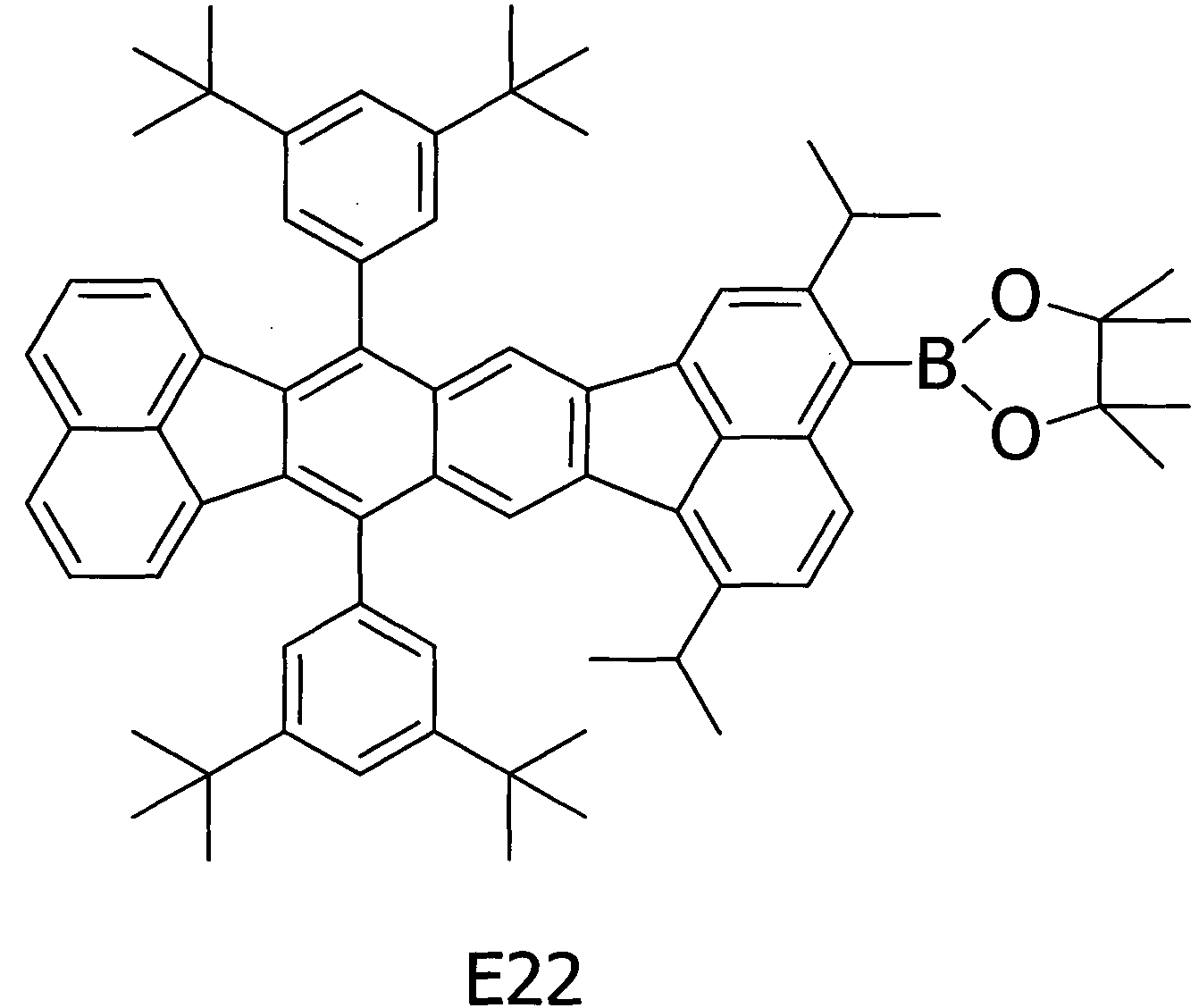
Методом ВЭЖХ подтверждено, что чистота получаемого в результате соединения составляла 98% или более.
Спектр излучения толуольного раствора примерного соединения A42 (концентрация: 1×10-5 моль/л) показывал максимальную интенсивность при 516 нм при измерении таким же способом, как в примере 1.
Массу примерного соединения A42 анализировали методом MALDI-TOF-MS (Autoflex LRF, изготовленный компанией Bruker).
MALDI-TOF-MS
Наблюдаемое значение: m/z = 960,05, вычисленное значение: C74H72 = 960,56.
Пример 13
Синтез примерного соединения A45
Примерное соединение A45 получали таким же способом, как в примере 2, за исключением того, что соединение E23, представленное ниже, использовали вместо соединения E6 на стадии (1) примера 2.
[Химическая формула 24]
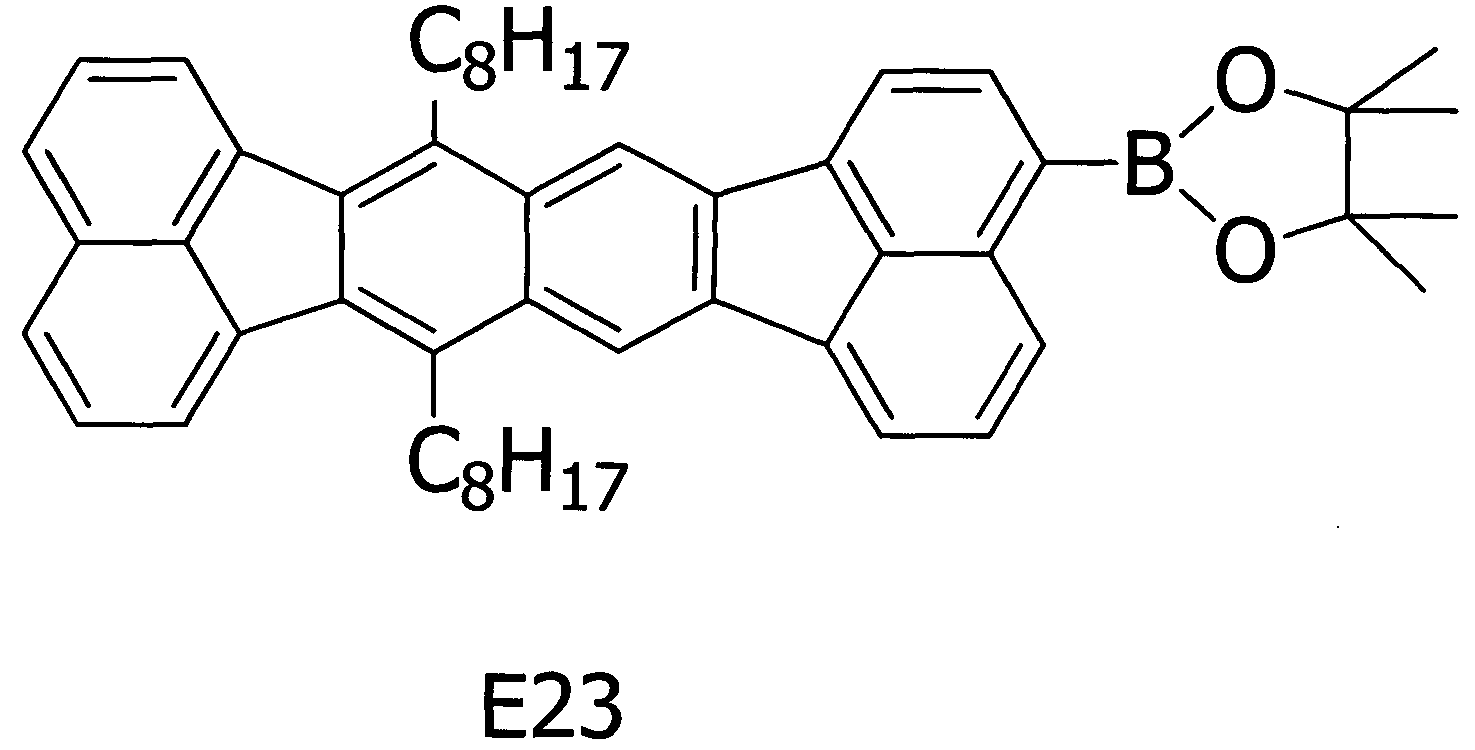
Методом ВЭЖХ подтверждено, что чистота получаемого в результате соединения составляла 98% или более.
Спектр излучения толуольного раствора примерного соединения A45 (концентрация: 1×10-5 моль/л) показывал максимальную интенсивность при 517 нм при измерении таким же способом, как в примере 1.
Массу примерного соединения A45 анализировали методом MALDI-TOF-MS (Autoflex LRF, изготовленный компанией Bruker).
MALDI-TOF-MS
Наблюдаемое значение: m/z = 724,88, вычисленное значение: C56H52 = 724,41.
Пример 14
Синтез примерного соединения B1
Примерное соединение B1 получали таким же способом, как в примере 1, за исключением того, что соединение E24, представленное ниже, использовали вместо соединения E1 на стадии (1) примера 1.
[Химическая формула 25]
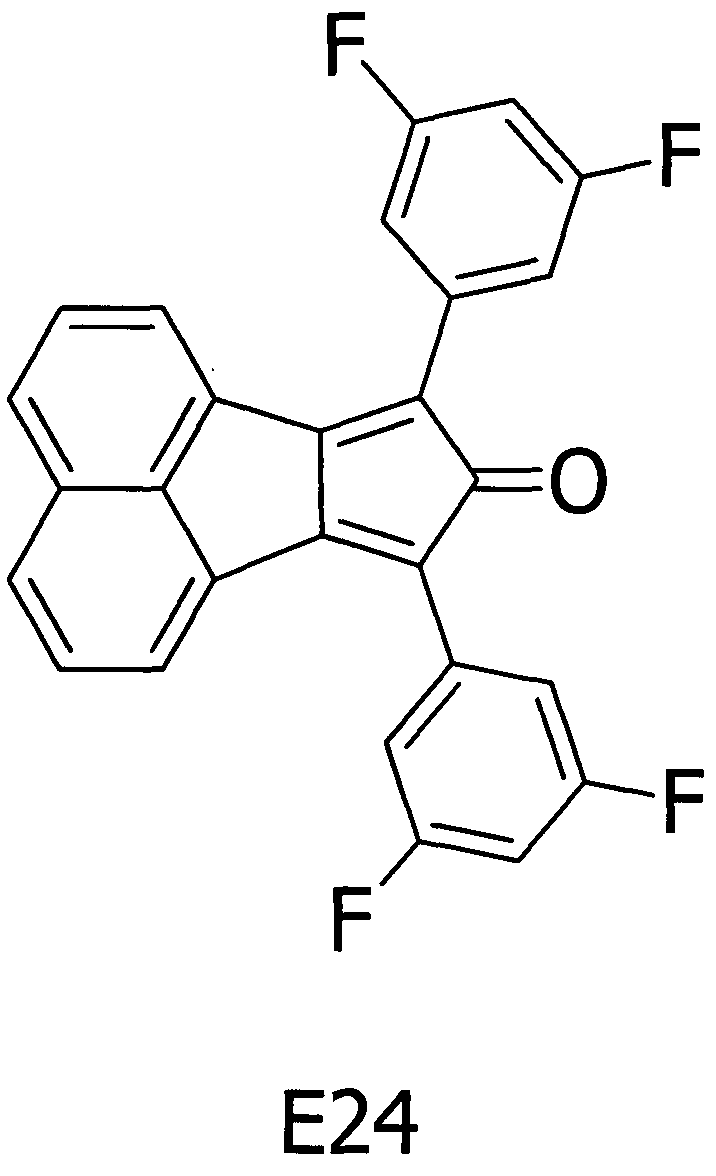
Методом ВЭЖХ подтверждено, что чистота получаемого в результате соединения составляла 99% или более.
Спектр излучения толуольного раствора примерного соединения B1 (концентрация: 1×10-5 моль/л) показывал максимальную интенсивность при 510 нм при измерении таким же способом, как в примере 1.
Массу примерного соединения B1 анализировали методом MALDI-TOF-MS (Autoflex LRF, изготовленный компанией Bruker).
MALDI-TOF-MS
Наблюдаемое значение: m/z = 807,55, вычисленное значение: C58H36F4 = 808,28.
Пример 15
Синтез примерного соединения B9
Примерное соединение B9 получали таким же способом, как в примере 2, за исключением того, что соединение E25, представленное ниже, использовали вместо соединения E6 на стадии (1) примера 2.
[Химическая формула 26]
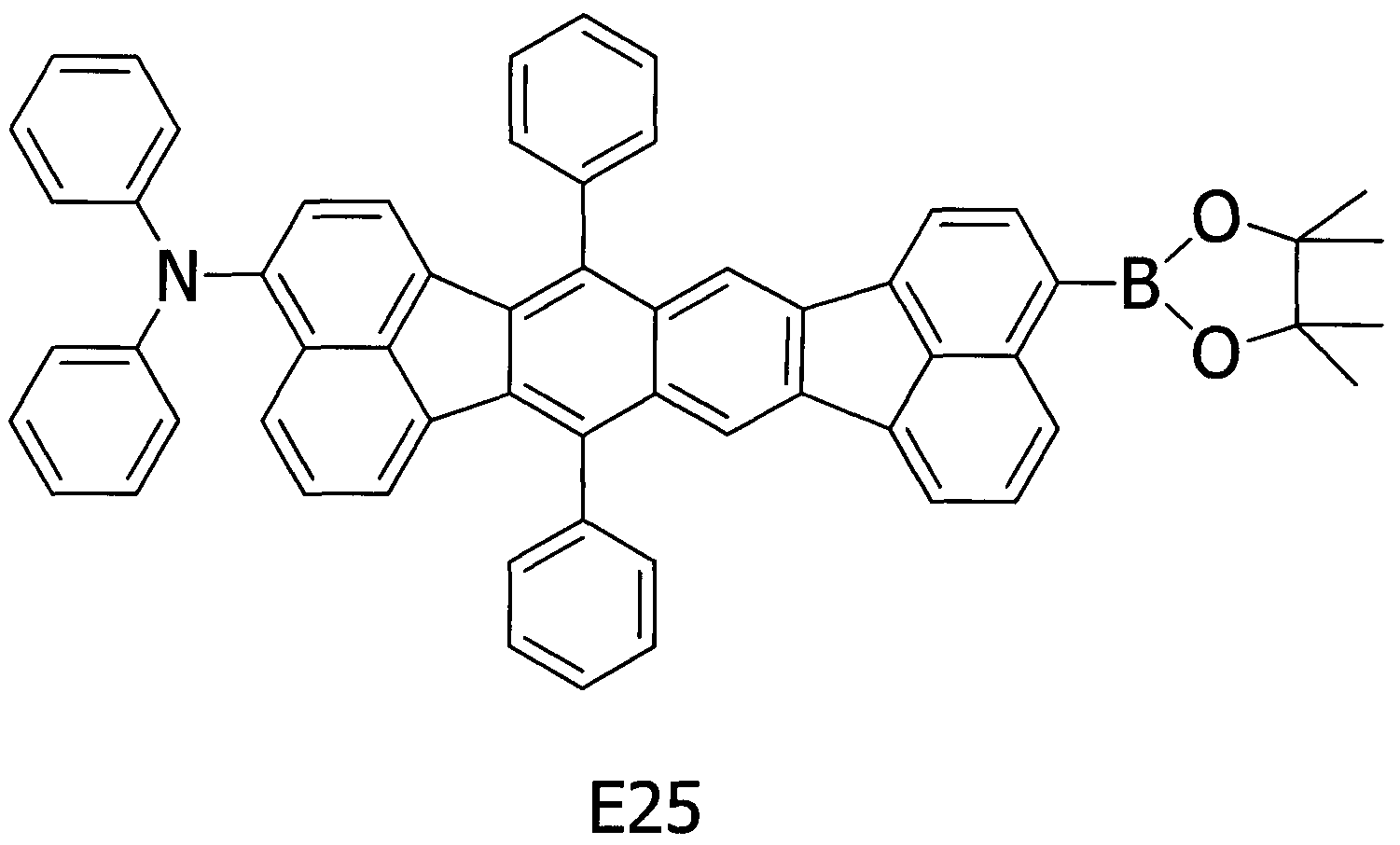
Методом ВЭЖХ подтверждено, что чистота получаемого в результате соединения составляла 98% или более.
Спектр излучения толуольного раствора примерного соединения B9 (концентрация: 1×10-5 моль/л) показывал максимальную интенсивность при 533 нм при измерении таким же способом, как в примере 1.
Массу примерного соединения B9 анализировали методом MALDI-TOF-MS (Autoflex LRF, изготовленный компанией Bruker).
MALDI-TOF-MS
Наблюдаемое значение: m/z = 819,86, вычисленное значение: C64H37N = 819,29.
Пример 16
В данном примере получали органическое светоизлучающее устройство, в котором анод, проводящий дырки слой, блокирующий электроны слой, светоизлучающий слой, блокирующий дырки/экситоны слой, проводящий электроны слой и катод были нанесены на подложку в данной последовательности. Ниже представлены некоторые из материалов, используемых в данном примере.
[Химическая формула 27]
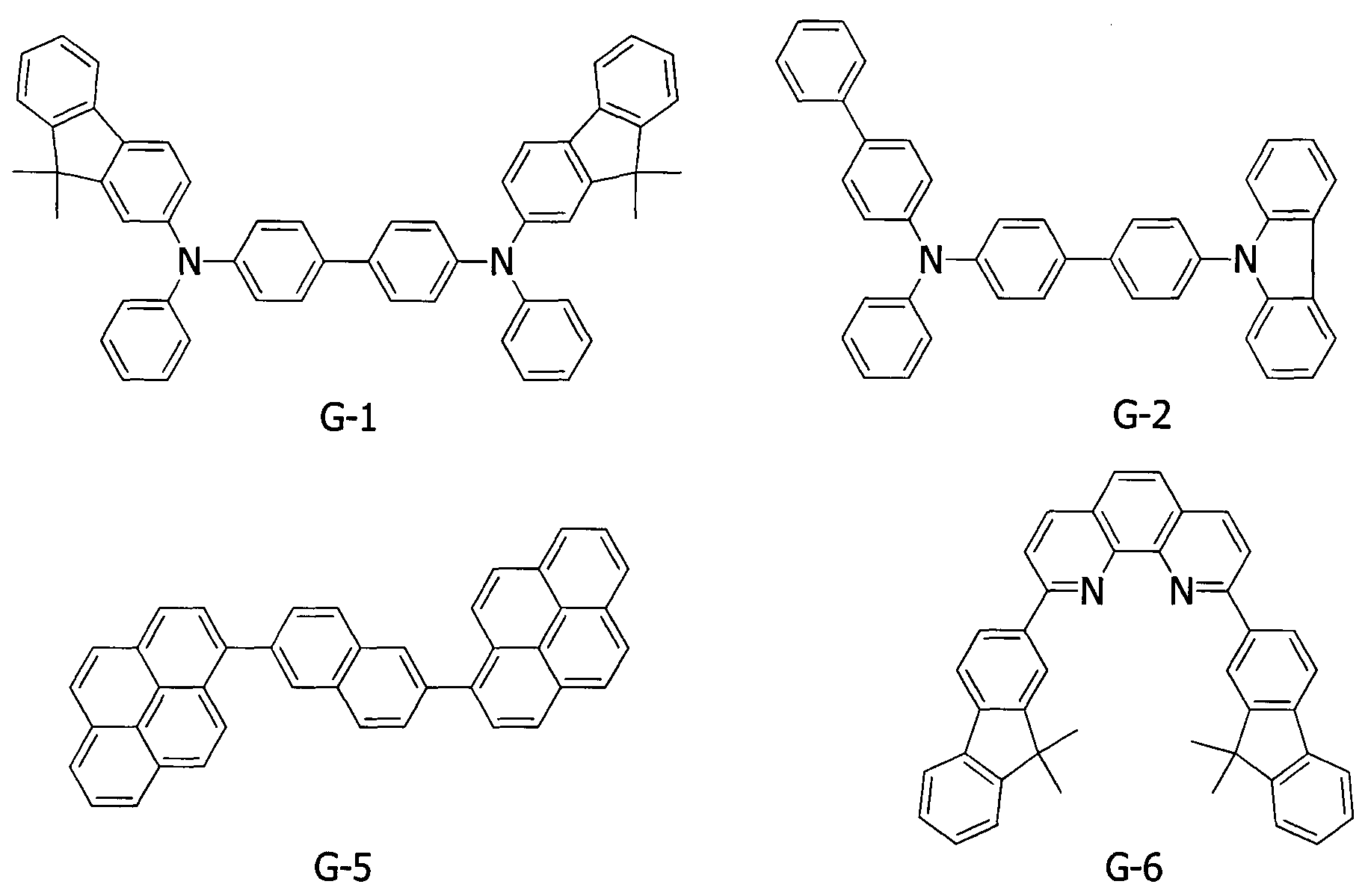
Пленку ITO, толщина которой составляла 100 нм, наносили на стеклянную подложку и превращали в электрод (анод) ITO посредством трафаретирования. Полученную таким способом подложку с электродом ITO использовали в качестве подложки ITO на следующих стадиях.
На данную подложку ITO последовательно наносили слои органического соединения и электродные слои, которые представлены в таблице 3. В данном случае площадь, которую занимали обращенные друг к другу электроды (металлический электродный слой, катод), составляла 3 мм2.
В данном примере соединения G-3 и G-4 соответствуют соединениям H10 и H21, соответственно, которые представлены в таблице 2.
Характеристики получаемого в результате устройства измеряли и оценивали. В частности, характеристики тока и напряжения измеряли, используя микроамперметр 4140B, изготовленный компанией Hewlett-Packard Company, и яркость измеряли, используя измеритель яркости BM7, изготовленный компанией Topcon Corp. Результаты измерений представлены в таблице 4.
Примеры 17-27
Органические светоизлучающие устройства получали таким же способом, как в примере 16, за исключением того, что G-3, G-4 и легирующий материал, соответственно, заменяли на соединения, которые представлены в таблице 4. Характеристики получаемых в результате устройств измеряли и оценивали таким же способом, как в примере 16. Результаты измерений представлены в таблице 4. В таблице 4 соединения G-3 и G-4 представляют собой соединения, приведенные в таблице 2. В том случае, когда G-3 и G-4 представляют собой одно и то же соединение, легируемый материал и вспомогательный материал представляют собой один и тот же материал.
Пример 28
В данном примере получали органическое светоизлучающее устройство, в котором анод, инжектирующий дырки слой, проводящий дырки слой, светоизлучающий слой, проводящий электроны слой, инжектирующий электроны слой и катод были нанесены на подложку в данной последовательности. Органическое светоизлучающее устройство, полученное в данном примере, имеет резонансную структуру. Ниже представлены некоторые из материалов, используемых в данном примере.
[Химическая формула 28]
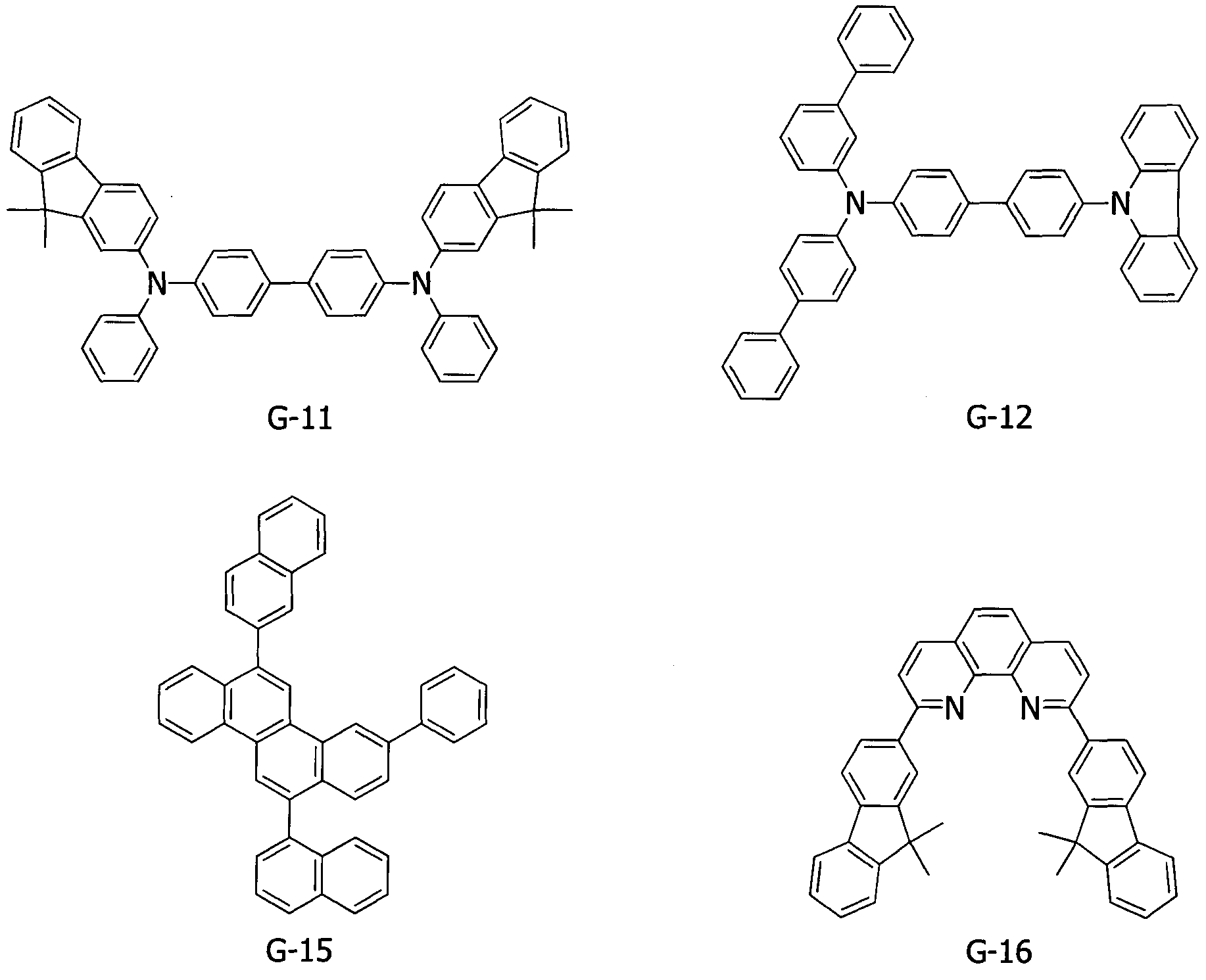
Сначала пленку, которая служила в качестве отражающего анода и имела толщину 100 нм, наносили на стеклянную подложку (носитель) посредством напыления алюминиевого сплава (AlNd). Затем пленку, которая служила в качестве прозрачного анода и имела толщину, составляющую 80 нм, наносили на отражающий анод посредством напыления ITO.
Кроме того, изолирующую устройство акриловую пленку, толщина которой составляла 1,5 мкм, наносили на периферию анода, и отверстие, радиус которого составлял 3 мм, получали посредством трафаретирования.
Подложку с нанесенным анодом промывали при воздействии ультразвука ацетоном и затем изопропиловым спиртом (IPA), после чего промывали посредством кипячения в IPA с последующим высушиванием. Кроме того, поверхность данной подложки промывали при воздействии ультрафиолетового излучения и озона.
Затем слои органического соединения, которые представлены в таблице 5, последовательно наносили на подложку ITO методом парофазного осаждения с резистивным нагреванием в вакуумной камере при давлении 1×10-5 Па.
В данном примере соединения G-13 и G-14 соответствуют соединениям H5 и H19, соответственно, которые представлены в таблице 2.
Затем пленку, которая служила в качестве катода и имела толщину 30 нм, наносили на инжектирующий электроны слой посредством напыления ITO. Наконец, осуществляли герметизацию в атмосфере азота. Таким образом, получали органическое светоизлучающее устройство.
Характеристики получаемого в результате устройства измеряли и оценивали. В частности, характеристики тока и напряжения измеряли, используя микроамперметр 4140B, изготовленный компанией Hewlett-Packard Company, и яркость измеряли, используя измеритель яркости BM7, изготовленный компанией Topcon Corp. Результаты измерений представлены в таблице 6.
Примеры 29-32
Органические светоизлучающие устройства получали таким же способом, как в примере 28, за исключением того, что соединения G-13, G-14 и легирующий материал, соответственно, заменяли на соединения, которые представлены в таблице 7. Характеристики получаемых в результате устройств измеряли и оценивали таким же способом, как в примере 28. Результаты измерений представлены в таблице 6.
В таблице 6, в том случае, когда соединения G-13 и G-14 представляют собой одно и то же вещество, легируемый материал и вспомогательный материал представляют собой один и тот же материал, и G-13 и G-14 представляют собой легируемые материалы, приведенные в таблице 2.
Пример 33
В данном примере получали органическое светоизлучающее устройство, в котором анод, проводящий дырки слой, первый светоизлучающий слой, второй светоизлучающий слой, блокирующий дырки/экситоны слой, проводящий электроны слой и катод были нанесены на подложку в данной последовательности. Органическое светоизлучающее устройство в данном примере имеет множество светоизлучающих слоев. Ниже представлены некоторые из материалов, используемых в данном примере.
[Химическая формула 29]
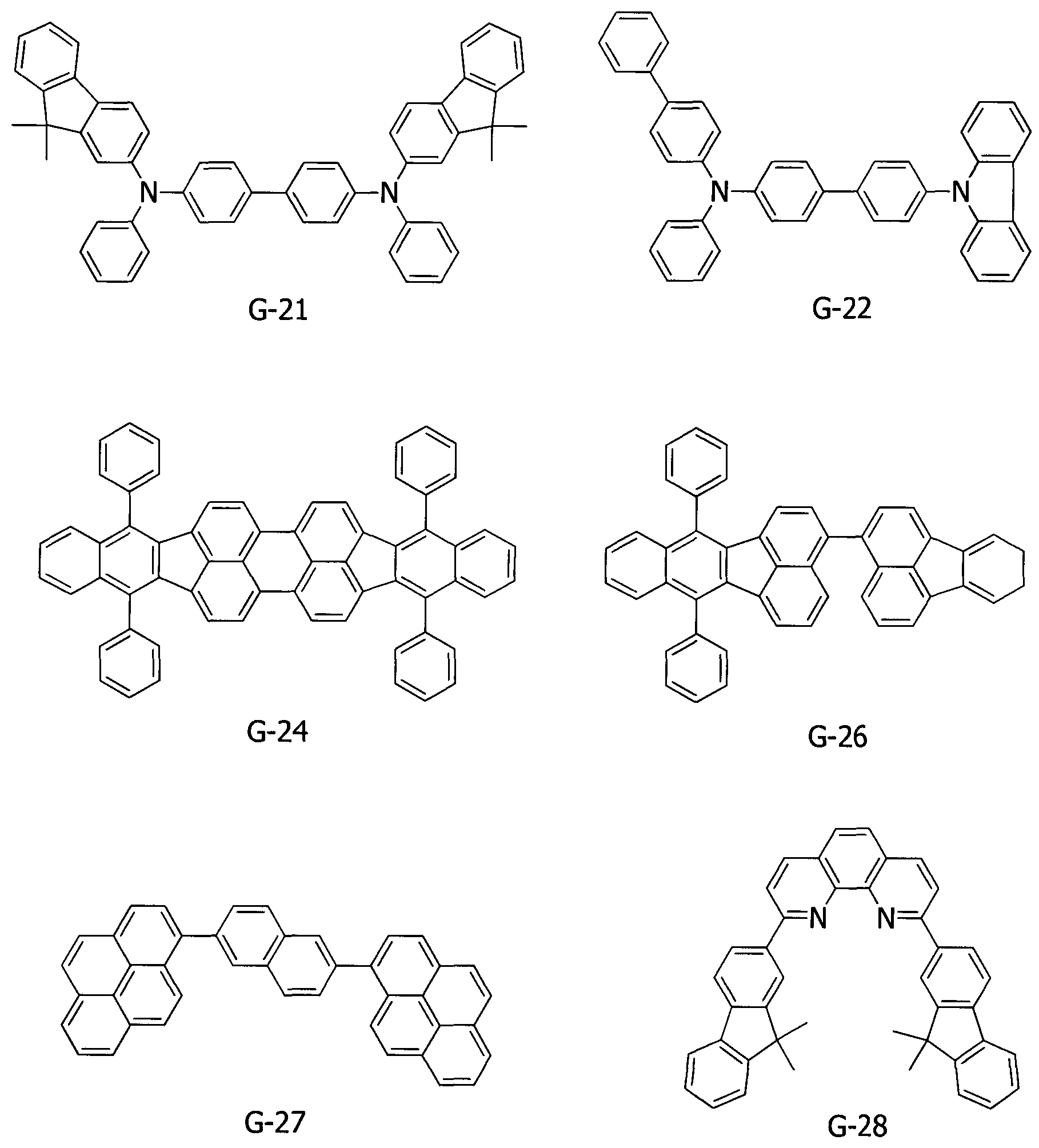

Сначала пленку ITO, которая имела толщину 100 нм, наносили на стеклянную подложку и превращали в электрод ITO (анод) посредством трафаретирования. Полученную таким способом подложку с электродом ITO использовали в качестве подложки ITO на следующих стадиях.
Затем слои органического соединения и электродные слои, которые представлены в таблице 7, последовательно наносили на подложку ITO методом парофазного осаждения с резистивным нагреванием в вакуумной камере при давлении 1×10-5 Па. В данном случае площадь, которую занимали обращенные друг к другу электроды (металлический электродный слой, катод), составляла 3 мм2.
В данном примере соединения G-23 и G-25 представляют собой, соответственно, соединения H10 и H14, приведенные в таблице 2.
Характеристики получаемого в результате устройства измеряли и оценивали. В частности, характеристики тока и напряжения измеряли, используя микроамперметр 4140B, изготовленный компанией Hewlett-Packard Company, и яркость измеряли, используя измеритель яркости BM7, изготовленный компанией Topcon Corp. Результаты измерений представлены в таблице 8.
Примеры 34 и 36
Органические светоизлучающие устройства получали таким же способом, как в примере 33, за исключением того, что соединения G-23, G-25 и легирующий материал, соответственно, заменяли на соединения, которые представлены в таблице 8. Характеристики получаемых в результате устройств измеряли и оценивали таким же способом, как в примере 33. Результаты измерений представлены в таблице 8.
В таблице 8 соединения G-23 и G-25 представляют собой легируемые материалы, приведенные в таблице 2.
Как показывают данные примеры, органические соединения согласно настоящему изобретению, которые используются в светоизлучающих устройствах, обеспечивают цветность, подходящую для излучения зеленого света с малой полной шириной на полувысоте максимума и высокой эффективностью и, таким образом, представляют собой превосходные зеленые светоизлучающие материалы. Когда только соединение согласно настоящему изобретению используется в качестве светоизлучающего материала, максимальная эффективность излучения является высокой, составляя 54 кд/А.
Органические соединения согласно настоящему изобретению имеют высокий квантовый выход и излучают свет, подходящий для излучения зеленого света. Соответственно, органические светоизлучающие устройства, включающие органические соединения согласно настоящему изобретению в качестве составляющих материалов, могут иметь превосходные светоизлучающие характеристики.
Хотя настоящее изобретение описано в отношении примерных вариантов осуществления, следует понимать, что настоящее изобретение не ограничивается описанными примерными вариантами осуществления. Объем приведенной ниже формулы изобретения следует истолковывать в максимально широкой интерпретации, таким образом, чтобы объединять все возможные модификации и эквивалентные структуры и функции.
Настоящая заявка испрашивает приоритет японской патентной заявки № 2011-207325, поданной 22 сентября 2011 г., которая во всей своей полноте включается в настоящий документ посредством ссылки.
Список ссылочных позиций
4 - синий светоизлучающий слой
5 - зеленый светоизлучающий слой
6 - красный светоизлучающий слой
17 - устройство TFT
20 - анод
21 - слой органического соединения
22 - катод
Реферат
Изобретение относится к органическому соединению, представленному формулой (1), в которой каждый R-Rнезависимо выбирают из атомов водорода, замещенных или незамещенных алкильных групп, замещенных аминогрупп, замещенных или незамещенных арильных групп. При этом алкильную группу выбирают из группы, состоящей из метильных, этильных, н-пропильных, изопропильных, н-бутильных, втор-бутильных, трет-бутильных, октильных, циклогексильных, 1-адамантильных и 2-адамантильных групп; аминогруппу выбирают из группы, состоящей из N,N-дифениламино, N,N-динафтиламино, N,N-дифлуорениламино, N-фенил-N-толиламино, N,N-дитолиламино, N-метил-N-фениламино, N,N-дианизолиламино, N-мезитил-N-фениламино, N,N-димезитиламино, N-фенил-N-(4-трет-бутилфенил)амино, N-фенил-N-(4-трифторметилфенил)амино групп; арильную группу выбирают из группы, состоящей из фенильных, нафтильных, инденильных, бифенильных, терфенильных и флуоренильных групп. В случае когда алкильная группа или арильная группа замещены, заместитель выбирают из группы, состоящей из алкильных групп, алкоксигрупп, аминогрупп, арильных групп, гетероциклических групп и арилоксигрупп. Также изобретение относится к органическому светоизлучающему устройству, дисплейному устройству, устройству обработки видеоинформации, системе освещения, устройству формирования изображения, облучающему источнику света. Предлагаемое соединение имеет высокий квантовый выход и излучает свет в зеленой области только за счет своей основной структуры. 7 н. и 9 з.п. ф-лы, 36 пр., 8 табл., 3 ил.
Формула
[Химическая формула 2]
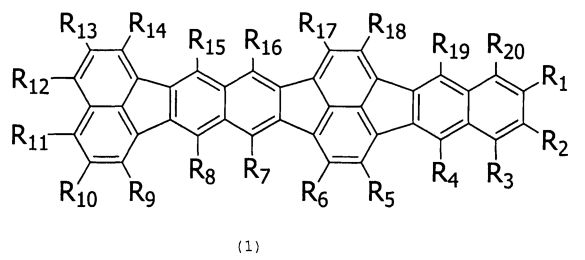
в формуле (1) каждый R1-R20 независимо выбирают из атомов водорода, замещенных или незамещенных алкильных групп, замещенных аминогрупп, замещенных или незамещенных арильных групп,
причем алкильную группу выбирают из группы, состоящей из метильных, этильных, н-пропильных, изопропильных, н-бутильных, втор-бутильных, трет-бутильных, октильных, циклогексильных, 1-адамантильных и 2-адамантильных групп;
аминогруппу выбирают из группы, состоящей из N,N-дифениламино, N,N-динафтиламино, N,N-дифлуорениламино, N-фенил-N-толиламино, N,N-дитолиламино, N-метил-N-фениламино, N,N-дианизолиламино, N-мезитил-N-фениламино, N,N-димезитиламино, N-фенил-N-(4-трет-бутилфенил)амино и N-фенил-N-(4-трифторметилфенил)амино групп;
арильную группу выбирают из группы, состоящей из фенильных, нафтильных, инденильных, бифенильных, терфенильных и флуоренильных групп;
в случае, когда алкильная группа или арильная группа замещены, заместитель выбирают из группы, состоящей из алкильных групп, алкоксигрупп, аминогрупп, арильных групп, гетероциклических групп и арилоксигрупп.
алкильные группы содержат от 1 до 4 атомов углерода; и
арильные группы представляют собой фенильную группу или нафтильную группу и необязательно содержат алкильные группы, содержащие от 1 до 4 атомов углерода.
слой органического соединения представляет собой светоизлучающий слой, включающий легируемый материал и легирующий материал, и
легирующий материал представляет собой органическое соединение.
слой органического соединения включает множество светоизлучающих слоев;
по меньшей мере один слой из множества светоизлучающих слоев содержит органическое соединение; и
множество светоизлучающих слоев излучают свет цветов, отличающихся друг от друга.
вводную секцию для ввода видеоинформации; и
дисплейную секцию для показа изображения,
где дисплейная секция представляет собой дисплейное устройство по п. 12.
органическое светоизлучающее устройство по любому из пп. 7-11; и
преобразователь переменного тока в постоянный для подачи возбуждающего напряжения на органическое светоизлучающее устройство.
светочувствительный элемент;
зарядный элемент для зарядки поверхности светочувствительного элемента;
облучающий элемент для облучения светочувствительного элемента; и
проявляющее устройство для проявления электростатического скрытого изображения, формируемого на светочувствительном элементе,
где облучающий элемент включает органическое светоизлучающее устройство по любому из пп. 7-11.
множество светоизлучающих точек, расположенных на линии, где
каждая светоизлучающая точка имеет независимо регулируемый световой поток; и
каждая светоизлучающая точка включает органическое светоизлучающее устройство по любому из пп. 7-11.
Документы, цитированные в отчёте о поиске
Электролюминесцентный материал, содержащий органическое люминесцентное вещество
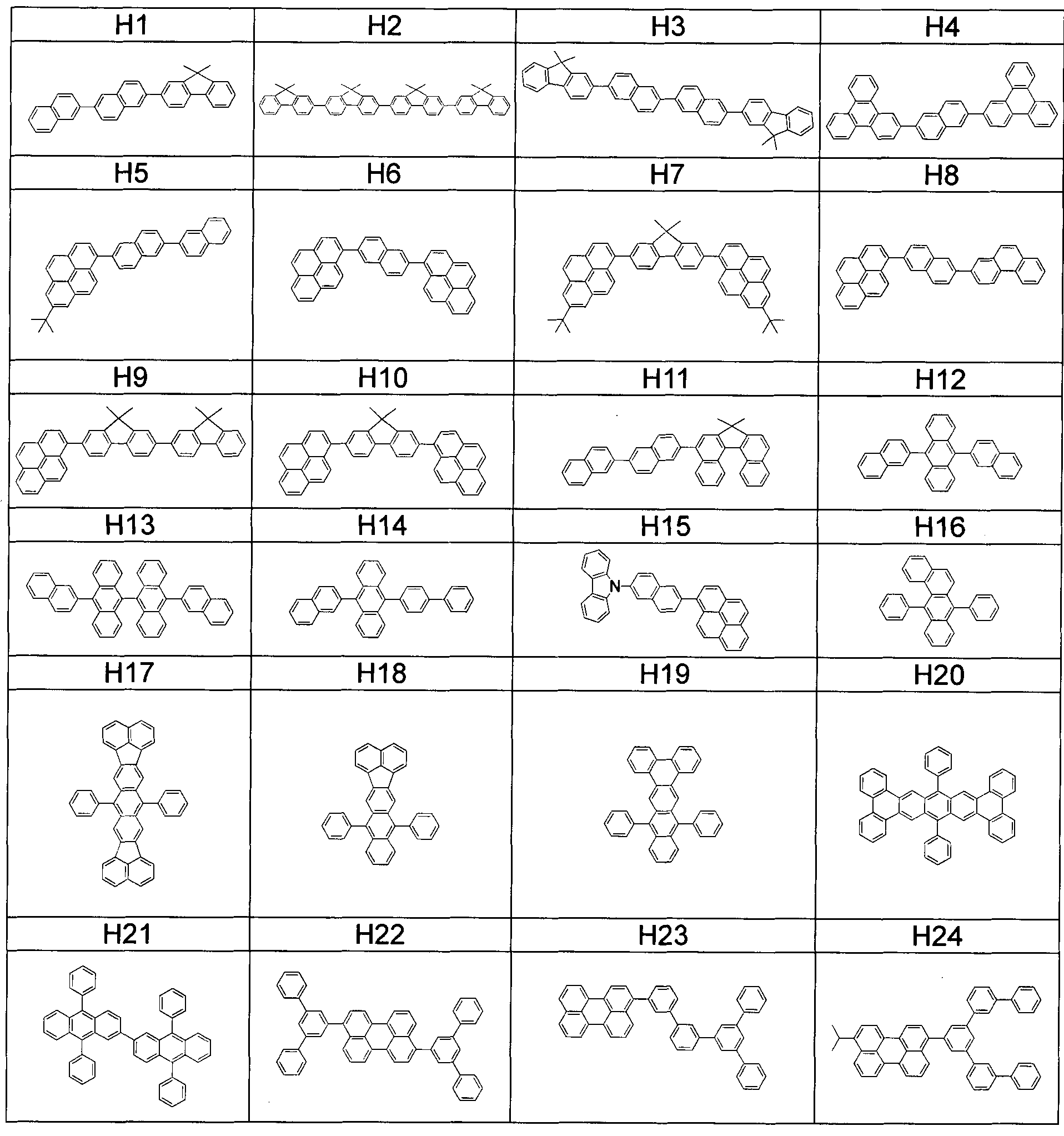

Комментарии