Способ получения аддукта перфторалкилиодида-олефина - SU420162A3
Код документа: SU420162A3
Описание
1
Изобрете;1ие относится к области получения аддуктов перфторалки.тиоднда-олеф:}и1а, имеющих в перфторалкильном остатке 6-24 атомов углерода и замещенных алифатическим или ци.клоалифатическим олефином с числом углеродиых атомов яе более 12.
Эти соединения, раиее не описанные в литературе , представляют собой важные промежуточные продукты, которые используются в качестве новых мономеров. Наличие в указанных соединениях та;ких функциональных групп как амидная, сложноэфирная позволяет получать поли.меры с улучщенными свойствами . Эти соединения используются для отделки текстильных материалов, бумаги и т. д.
Способ получения указаиных соединений основан на известной взаимодействия перфторалкилиодида с олефином в присутствии катализатора-соли металла и амина при повыщенных температуре .И давлении.
Ио предлагаемому способу перфторалкиллодид с числом углеродных атомов в перфторалкильном остатке подвергают взаимодействию с алифатическим или циклоалифатическим .или замещенным алифатическим или циклоалифатическим олефином с числом угеродных атомов не более 12 с последующим выделе}1ием целевого продукта известными приемам.
Процесс осуществляют при температуре 0°-350°С, дапленщ О-200йгг/ в пржутствии амина и соли металлов групп 1а-IV а или 16-Vni6 периодической системы элементов. 1 моль нерфторалкилиодида подвергают взаимодействию с 1 -10 молями соединения, содержащего двойиую связь, в присутствии 0,05-10 молей амина и 0,003-20 молей соли металла.
Используемые в данном процессе перфторалкилиодиды могут быть моно-, так и диидидамн . Эти нерфторалкилиодиды представляют собой разветвлеииые ил)1 иеразветвле)ные перфторалкилаюдиды с 16-18, предпочтительно с 6-14 атомами углерода.
В качестве второго компонента используют замещенные функциональными группами а.ткеиы , содержащие 2-6 атомов углерода, или замещенный стирол.
Замещенными функциональными группами алкенами являются, например аллиловый
спирт, ВИИИЛХЛОрИД, ВИИИЛИДеНХЛОрИД, В31НИЛфторид , винилиденфторид, винилацетат, 1/ 2-дихлорэтен; сложные эфиры, например низшие алкиловые эфиры, и амащы акриловой, метакриловой, кротоиовой, малеиновой, фумаровой или нтаконовой кислот, в частности алл;;1лфармиат, и аллилацетат, диаллилфумарат и диаллилитаконат дивипилфумарат и дивинилитаконат .
Полученные в данном процессе аддукты часто являются изомерными смесями, в которых перфторалкилостато.к может присоеднпяться, как к а - так и ,к р-атому углерода этиленовоненасыщекной связи олефииа. Для ясности в большинстве случаев указана только одна изомерная форма.
Амины, которые п рименяют в данном ироцеосе-тпервнч«ы€ , вт оричмые третичные алифатические, гетероциклические или ароматические амины. Предпочитают амины, которые содержат по меньшей мере один атом кислорода -в молекуле. Особенно пригодны а.мины , которые содержат одну гидроксильную группу в молекуле. Амины, способные к образованию амфотерпых конфигураций, как например ал:каноламины, особенно интересны.
Такие алканоламмны содержат пред почтительно 2-б атомов углерода.
Следует назвать, например, следующи-еа.мины: N-этилэтаноламин, аминоэтилизопропаноламин , днэтилэтаноламин, Н-(2-оксиэт1Ил)этнлендиамин , .изопропаноламин, триизопропаноламин; К-этилэтаноламии, N-метилэтаноламин , в частности диэтаноламин, триэтаноламин , .и предпочтительно моноэтаноламин. Кроме того, принимают во вннмание и такие амины, как N-оксиэтилморфолнн, морфолин, Ы-0;КСиэтилп1И1пераз 1н, 3-диэтиламинофенол, глицин или диэтил-амии.
В числе применимых в данном процессе солей металлов пригодны прежде всего соли металлов лрупп 16-VII16, в частности с 4-го ио 6-ой периоды периодической системы. Соли металлов прупп 16 и 116 особенно пригодны, как например, соли меди {), серебра, золота, дин«а, кадмия или ртути. Другими предпочтительными солями металлов являются соли металлов групп III6 или VIII6, в частности 4-го или 5-го периода, или металлов групп IV6 или V6, в частности с 4-го по 6-ой периоды периодической системы. Речь здесь.идет о солях кттр я , титана, циркония, ниобия, тантала, маргатца , железа, рутения ИЛ1И родия.
Пригодными представителями металлов группы la являются, например натрий или .калий и группы На, например магний, кальций, стронций или барий. К металлам группы Illo принадлежит галлий, таллий и индий и к прутпе IVa германий, олово или свинец.
Особенно пригодными оказались такие галогениды , как бромиды, йодиды или предпочтительно хлориды соответствующих металлов . Кроме того, могут быть применены и соответствующие фосфаты, карбонаты, нитраты, сульф,аты, цианиды, гидриды, ацетил ацетон аты пли алкоголяты, например этплаты или метилаты . Можно также применять смеси солей, даже металлов разной валентности.
Особенно пригодным оказался хлорид меДИ (I).
Реакцию можно проводить в отсутствии или в присутствии растворителя. Подходящими растворителями являются, например, фторированные галоидалканы, спирты, простые эфиры , ароматические углеводороды или циклоал .кен.
Пример 1. 500 г теломеризата перфторалкилиодида , состоящего из 30%; н-перфторгексилиодида , 46%; н-перфтороктилиодида, 20,5% н-лерфтордецилиодида и смеси перфторалкилиодндов €4, , Си, загружают вместе с 1 г CuCl и 5 г этанола.мина в авто-клав из стали высокого качества емкостью л. Потом .подают избыток этилена. Автоклав нагревают до 140°С в течение 45 ишн и выдерживагот при этой температуре в течение 45 мин. Уже незадолго до получееия реа;кц«онтой температуры да/влевне в автоклаве нач:итает .снижаться от 138 до 130 ати «i через 30 мин Становится постоялнькм.
530 г твердого, воскообразного вещества выгружают из автоклава и дистиллируют в вакууме . При этом выделяют общую фракцию 484 г (т. кип. 29 до 150°С при 5 мм рт. ст.) полутвердого , белого вещества.
22 г ИСХОД1ЮГО материала выделяют из холодильной ка.меры. Газохроматографические и масс-.снектрометрические анализы дают следующие результаты:
М 474 СРз(СР2)5СН2СН2Л 36%, М 574 CF3(CF2)7CH2CH2J 34,5%. М 674 CF3(CF2)9CH2CH2J 9,8%. М 502 CF3(CF2)5(CH2)4J 8,2% М 602 CF3(CF2)7(Cl-l2)4J 8,7%. М 702 CF3(CF2)9(CH2)4J 2,0%+за рязнения , где М - молекулярный вес.
Выход перфторалкилнодида (М 574), рассчитанный на прореалировавщий исходный материал () но исходному уравнению
484 пг л го/
-, „ 90,41 7о от теоретического.
Пример 2. 500 г теломеризата перфторалкилиодида , состоящего ai3 30% н-нерфторгексилиодида , 46% н-иерфтороктилиодида, 20,5% н-.перфтор.децилнодида ш с.меси перфторалкилиодидов С4, Ci2, Си, загружают -вместе с 1 г CuCl и 5 г этанола мина в автоклав емкостью il л из стал.и повышенного качества и подают избыток пропилена. В течение 45 мин автоклав иагревают до 140°С и оставляют при этой тем.пературе в течение еще 45 мин. По достиженни реакционной температуры давлениеснижается в течение20 мин от 20 до 15 аги 31 до о.кончания реакции остается постоянным.
500 г светло-коричневого вязкого вещества выгружают из автоклава и дистиллируют в вакууме . При этом выделяют общую фракцию 460 г (т. кип. 33-150°С, 10 мм рт. ст.) жидкотвердого вещества. 33 г исходного материала выделяют из холодильной камеры. Газохроматограф ич еские ;и .масс-спектрометрические анализы дают следующие результаты:
СНз
М 488 CF3(CF2)5-СИ.-СН-J 40% . М 588 СРз(СР2)7-СНз-СН-J 51,3% СНз -J 8,7%. (CF2)o-СНг-СИ688 С Fa Вы.ход надфторалкилиодида () рассчитан ia прореагировавший исходный материал () по исходному уравнению. т 96,27%: от теоретического. При м е р 3. 54,6 г теломеризата перфторалкилиодида , состоящего из 30% н-перфторгексилиодида , 46% и-перфтороктилиодпда 20,5% н-перфтордецилиодида и смеои перфторалкилиодидов С, Ci2, См вместе с 11,2 г Л тетрагидробе1 зиловым спиртом загружают в автоклав емкостью 3000 мл из стал-и повышенного качества. В качестве катализатора берут 100 лг CiiCl и 1 г этаноламина. Реакционную массу нагревают до 100°С, вследствие чего быстро повышается температура в автоклаве до 150-160°С. В течение 90 мин реакиия идет при этой температуре. Давление составляет 2 ати. По охлаждении автоклава получают 5 г темпо-коричневого жидкого вешества. Этот продукт-сырец растворяют в 250 мл диэтилового эфира и трижды промывают 50 .1/л воды, сушат над сульфатом натрия и простой эфир дистиллируют. Дистилляцией в вакууме 58 г очиш.енного вещества получают: Отброшен На основании масс-спектра фракции 2, имеющего характерные пики (М 558, 658, 758), соединение можно идентифицировать и представить формулой |.где п--5,7,9 CHgOHj Выход продуктов из фракций I и 2 описанной реакции, рассчитанный на средннй молекулярныи вес Ьо8, составляет , - 33,5% от теоретического. Пример 4. 54,6 г теломеризата перфторалкиллодида , состоящего из 30% н-перфторгексилиодпда , 46% н-перфтороктилиодида, 20,5% н-перфтордецплиодида н смеси перфторалкилподидов С4, Cjo, Ci4 загружают .вместе с эноксило г в автоклав из сн-сн сн. СНтО/ стаЛП новышеиного качества емкостью 300 .и.г. В качестве катализатора берут 100 мл CuCl и 1 г траэтаноламнна. В Teneiine 135 .i/;/M реакцню проводят при 40-158°С и потом прекращают . Давление 1 атм. 97 г KOpiiMiicBoro продукта-сырца растворяют в 250 мл простого эфира }1 П|рол1ЫБают три раза водо11 по 50 ..ы, сушат над сульфатом натрня и отгоняют простой эфир. Выход 95 г, что составляет 937о от теоретического. Рассчитан на соедипс-ше формулы IJ / -fH-CH..jjCF, . V 742 п 7. Содержаиле эноксида составляет 100%. Записью массового спектра получают М+Н 643, 743, 843 М-Н 641, 741, 841, а также относящийся сюда ряд распада, который нач.инается с М 515, 615, 715. npiiMep 5. 54,6 г теломернзата перфторалкилиодида , состоящего из 30% н-перфторгексилиодида , 46% и-перфтороктилиодида, 20,5% н-перфтордецилиодида и смеси перфт0 ралкил;1одндов С, , Си, загружают в.месте с 5,8 г аллилового спирта в автоклав из стаЛИ повышенного качества емкостью 300 мл. в качестве катализатора используют 100 мг Cud и 1 г этаюламнна. Автоклав нагревают до 100°С, вследствие чего температура реакции быстро повышается до 140-155°С. Эта температура сохраняется в течение 120 мин. Давление 2 атм. По охлаждении автоклава получают 50 г коричневого вяЗКОго вещества. Это вещество дистиллируют в вакууме. ХолодильнаяИс.ходиый камера 17 гматсрма.ч фракция 1 29 ; 2 мм рт, ст. 40-ПО С Реакционный с помощью масс-снектроскопни фракции 1 идентифицируют соединение формулы СРз(СР-,)пСИ,-СН-СН.ОИ , J
где n 3, 5, 7,
М 504, 604, 704.
Выход, рассчитанный «а средний .молекулярный вес 604, составляет
29 ,0% от теоретического.
Пример 6. 55 г соединения формулы
J
СРз(СР2)п-СН2-С-СООСНз ,
СНз
где , 7, 9, растворяют в смеси 100 мл этил ацетата и 20 мл ледя-ной уксусной кислоты .
К раствору Прибавляют 6 г цинковой пыли и в течение 5 мин вводят газообразный НС1 со скоростью 20 пузырьков в 1 мин. Реакционную смесь в течение 5 мин выдерживают гари температуре обратного потока, потом охлаждают , фильтруют л раствор концентрируют . Остаток дистиллируют в высоком вакууме и получают 18,6 г вещества кремового цвета. Т. пл. 167-204°С при 0,1 мм рт. ст.
Выход составляет 42%; от теоретического.
Записью массового oneKTipa (М 420, 520, 620) подтверждается следующая структура
CF. (CFs) n-СН,-СН-СООСНз
СНз « 5,7, 9
Приведенный сложный эфир можно перевести в свободную кислоту путем омыления.
По описанному примеру получают л другие сложные эфиры, например
Нг-СНг-СН--СООСНз- RF-СН,-СН,-СООСНз
Rr-СНг-СН-(СН2)8-СООСНз--Rr-(СНо),о
J -СООСНз
j-C J-сооснГЧ ЛсоосНз
RF GF3(CF,)n п 5, 7, 9, 11
Примеры 7-72. Вычисление оптимального выхода по примеру 7.
Во всех примерах (7-72) берут для реакции 150 г (0,3 ) теломеризата 5 перфторалкилиодида, состоящего «з 23,5%, н-перфторгексил«одида (), 44,9%: иперфтороктилиодида (М -546), 32,1%; н-перфтордецилиодида (М 646), 2,0%: н-перфтордиодецилиодида и смеси других перфториро0 ванных соединений, и 68 г (0,6 ) октена-, проводят опыт по примеру 1 и получают 36,04 г октеиа-1 (107%), 5 г перфторалкилиодида (3,4%) и 141,25 г реакционного продукта.
5 Продукт идентифицируЕОт с помощью газовой хроматографии и масс-спектрометрии.
Оптимальный выход продукта, полученного из 145 г (150-5) исходного перфторалкилиодида составляет n
141,25 . -pry-- 79,58% от теоретического.
177,48 г соответствуют теоретическому (выходу при 100%,-ном взаимодействии. Выходы рассчитаны на средний молекулярный вес перфторалкилиодида 546, используемое количество перфторалкилиодида составляет 96,6%, да.нные в процентах для используемыхолефинов указаны.
В примерах 7-72 в качестве исходного продукта применяют перфторалкилиодиды СРз(СР2)пЛ, где п 5, 7, 9, 11.
В . 1 приведены названия ил.и форму5 лы использованных в примерах 7-72 олефинов и конечных продуктов.
В табл. 2 приведеиы условия и результатг Е опытов примеров 7-72. В табл. 3 приведены данные по проведению опыта примера 73. 0
Обозначения, принятые в табл. 2:
ЭА - этаиоламии ДЭА - диэтаноламин ТЭА - триэтаиоламин
- окись алюм1иния для хроматографии
SiOo-силикагель для использования в распределительной хроматографии, кизельгур или молекулярное сито
Rf - перфторалкилостаток.
Использзе.мый олефмп
Пример Л2
Октен-1
Т а б л 11 ц а I
Конечный продукт
СРз(СР2)п-СН-СН (СН,)5СНз
I J
О СНгОС-СНf Bf- iiil
j-fjLcH.occH-,









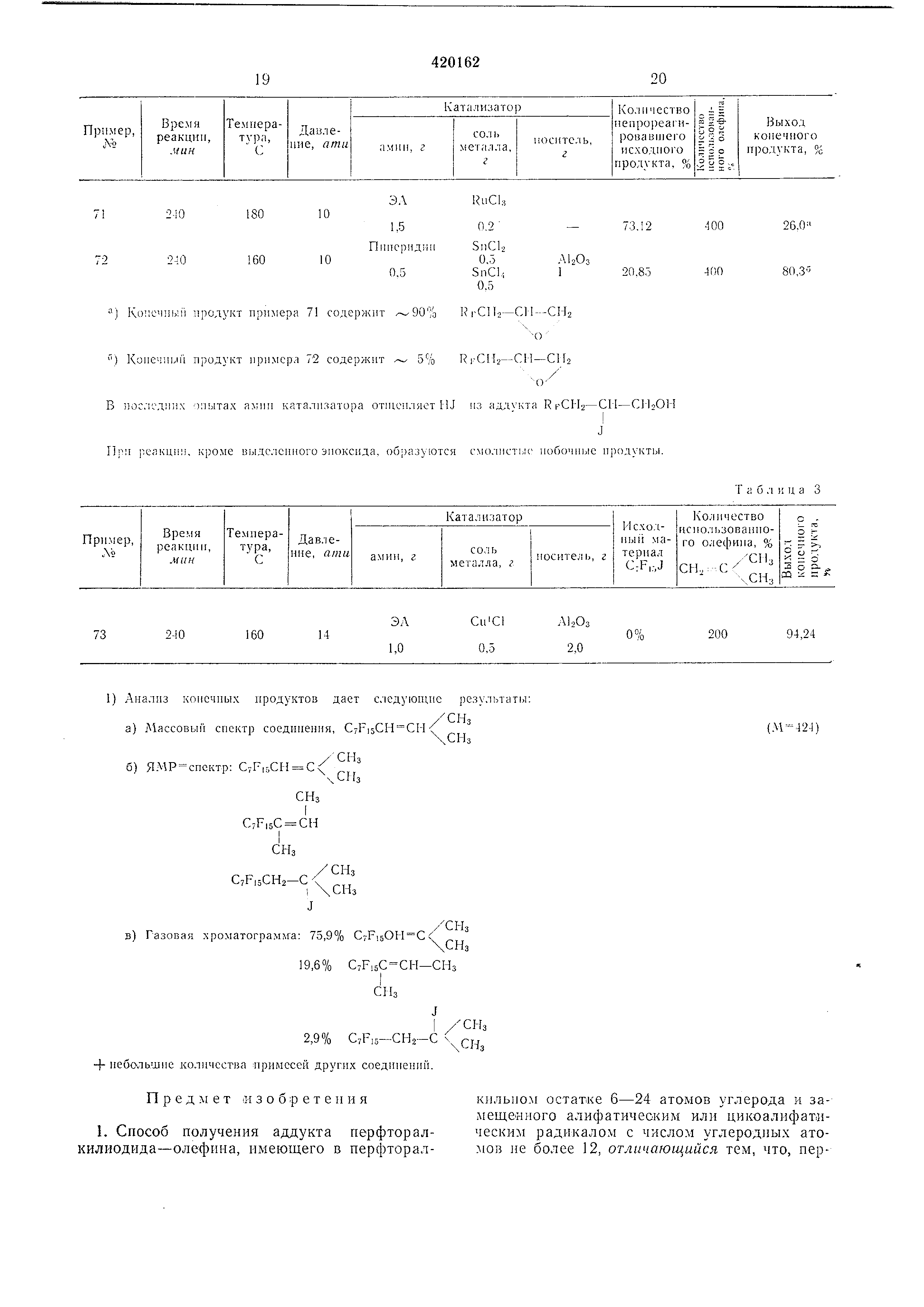
Реферат

Формула
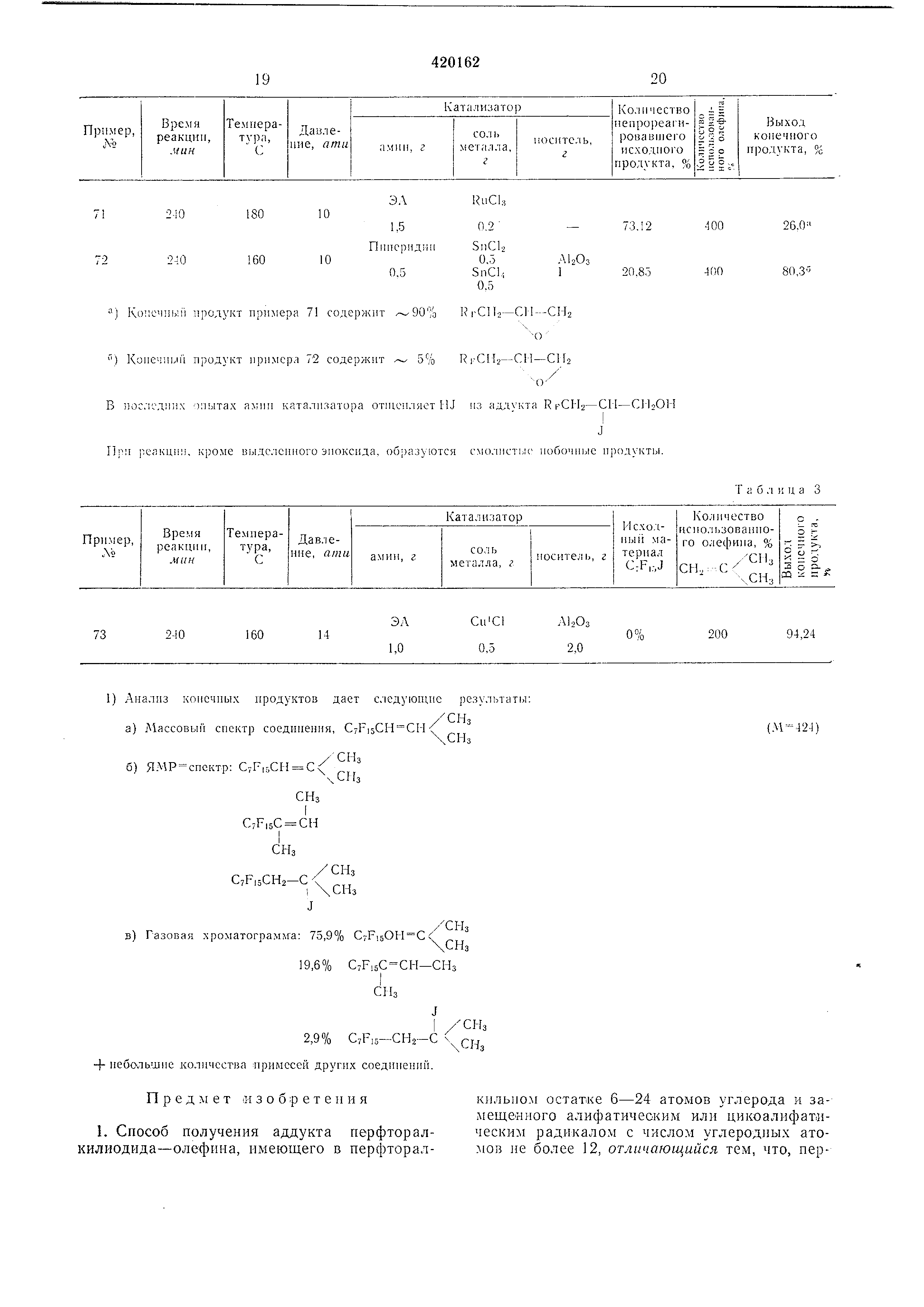


Комментарии