Фториодированные соединения для фторполимеров - RU2645156C2
Код документа: RU2645156C2
Описание
ТЕХНИЧЕСКАЯ ОБЛАСТЬ
[0001] Фториодированные соединения описаны вместе со способами их получения. Эти фториодированные соединения могут использоваться при получении фторполимеров.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
[0002] Существует необходимость найти альтернативу фториодированным соединениям для использования в полимерном синтезе. Существует также необходимость в получении этих фториодированных соединений с нечетным количеством атомов углерода. Также было бы желательно идентифицировать способы получения этих фториодированных соединений, которые могут быть более эффективными и/или более дешевыми, чем традиционные способы.
[0003] В одном аспекте описывается способ получения частично фторированного соединения, включающий: (а) восстановление перфтордисульфонилфторида с получением дисульфината; (b) реакцию дисульфината с йодом с получением перфторированного двуйодистого соединения; и (с) реакцию перфторированного двуйодистого соединения с этиленом с получением замещенного этиленом перфтордииодида. В одном варианте осуществления изобретения замещенный этиленом перфтордииодид вступает в реакцию с основанием с получением частично фторированного иодалкена.
[0004] В другом аспекте описывается состав, включающий частично фторированное соединение йода, выбранное из группы, состоящей из I(CF2)xCH=CH2 и I(CF2)xCH2CH2I, где х является нечетным целым числом от 3 до 11.
[0005] В одном аспекте описывается полимерный состав, включающий полимеризованный продукт реакции состава, включающего частично фторированное соединение йода, выбранное из группы, состоящей из I(CF2)xCH=CH2 и I(CF2)xCH2CH2I, где х является нечетным целым числом от 3 до 11, и фторированного олефинового мономера.
[0006] В другом аспекте описан способ получения полимера, включающий: (а) обеспечение частично фторированного соединения I(CF2)xCH=CH2, где х является нечетным целым числом от 3 до 11; фторированного олефинового мономера; и инициатора; и (b) полимеризацию частично фторированного соединения и фторированного олефинового мономера с получением полимера.
[0007] Вышеупомянутая сущность изобретения не предназначена для описания каждого варианта осуществления изобретения. Детали одного или нескольких вариантов осуществления изобретения также сформулированы в описании ниже.
Другие характеристики, объекты и преимущества очевидны из описания и из формулы изобретения.
ПОДРОБНОЕ ОПИСАНИЕ
[0008] В данном контексте
формы единственного и множественного числа используются взаимозаменяемо и означают один или несколько; и
«и/или» используется для указания одного или обоих изложенных случаев, которые могут произойти, например А и/или В включает (А и В) и (А или В).
[0009] Также в настоящем документе указание диапазонов их граничными значениями включает все числа, включенные в такой диапазон (например, диапазон 1-10 включает 1.4, 1.9, 2.33, 5.75, 9.98, и т.д.).
[0010] Также в настоящем документе выражение «по крайней мере, одного» включает все числа от одного и больше (например, по крайней мере 2, по крайней мере 3, по крайней мере 4, по крайней мере 6, по крайней мере 8, по крайней мере 10, по крайней мере 25, по крайней мере 50, по крайней мере 100 и т.д.).
[0011] α,ω-Дииодоперфторалканы являются важными структурными элементами при получении других фторированных соединений и полимеров. Во фторполимерах α,ω-дииодоперфторалканы используются в качестве агентов передачи цепи, помогая управлять молекулярной массой полимера. Как правило, эти α,ω-дииодоперфторалканы получают олигомеризацией тетрафторэтилена и йода, приводящей к четному количеству единиц CF2. См., например J. Org. Chem., т.42, №11, с. 1985-1990 (1977). Далее, соединения йода могут полимеризоваться в полимер, и наличие йодида во фторполимере используется для вулканизации.
[0012] Получение фторированных двуйодистых соединений с нечетным количеством единиц CF2 было трудным и дорогостоящим. Фторированные двуйодистые соединения с нечетным числом единиц CF2 получали путем реакции ICF2I с тетрафторэтиленом, однако, тетрафторэтилен трудно использовать, a ICF2I труднодоступен.
[0013] Настоящее изобретение направлено на однореакторный двухступенчатый синтез для получения α,ω-дииодоперфторалканов (т.е. I(CF2)nI, где n - по крайней мере 1). Этот способ может использоваться для получения α,ω-дииодоперфторалканов с высоким выходом. Предпочтительно, этот способ может использоваться для получения α,ω-дииодоперфторалканов с нечетным количеством единиц CF2. Также в настоящем документе описывается способ получения частично фторированного α,ω-дииодоалкана и частично фторированных иодоолефинов из α,ω-дииодоперфторалканов.
[0014] Способ I
[0015] В настоящем документе раскрыт эффективный (однореакторный, двухступенчатый) синтез для получения перфторированных двуйодистых соединений, в котором перфтордисульфонилфторид восстанавливают с получением дисульфината, далее вступающего в реакцию с йодом с получением перфторированного двуйодистого соединения. В одном варианте осуществления изобретения перфторированное двуйодистое соединение является α,ω-дииодоперфторалканом (т.е. I(CF2)nI, где n по крайней мере 1, например, n является 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11 и т.д.). В другом варианте осуществления изобретения перфторированное двуйодистое соединение включает циклическую группу и/или разветвляющие и/или встроенные в цепь гетероатомы.
[0016] Первая стадия синтеза в Способе I включает восстановление перфтордисульфонилфторида.
[0017] Перфтордисульфонилфторид в настоящем изобретении является соединением формулы FSO2-Rf-SO2F, где Rf является двухвалентной перфторированной связывающей группой. Перфтордисульфонилфторид можно получить с помощью способов, известных из уровня техники, включая, например, электрохимическое фторирование. Как правило, перфторированная связывающая группа включает, по крайней мере, 2, 3, 4, 5, 7 или даже 9 атомов углерода. В одном варианте осуществления изобретения перфторированная связывающая группа является линейной. В другом варианте осуществления изобретения перфторированная связывающая группа может содержать разветвляющие группы, имеющие 1-5 атомов углерода и, если размеры позволяют, циклические группы. В одном варианте осуществления изобретения перфторированная связывающая группа является перфторированным углеводородом. В альтернативном варианте осуществления изобретения перфторированная связывающая группа включает встроенные в цепь гетероатомы, такие как азот или кислород.
[0018] Примерные перфтордисульфонилфториды включают FSO2-CF2CF2CF2-SO2F, FSO2-CF2CF2CF2CF2-SO2F и FSO2-CF2CF2CF2CF2CF2-SO2F.
[0019] Восстанавливающие агенты, известные в уровне техники, могут использоваться для восстановления перфтордисульфонилфторида. Иллюстративные восстанавливающие агенты, применимые в настоящем изобретении, включают агенты, представленные формулой M'Y'H4, где М' является щелочным металлом или щелочноземельным металлом, и Y' является алюминием или бором, включая, например, борогидрид натрия, цианоборогидрид натрия, борогидрид калия, борогидрид лития и алюмогидрид лития. Приемлемые гидридные восстанавливающие агенты также включают агенты, представленные формулой М''Hn, где М'' является щелочным металлом, и n является целым числом, выбранным из 1 или 2, включая, например, гидрид натрия, гидрид лития, гидрид калия, гидрид бария и гидрид кальция. Другие пригодные восстанавливающие агенты включают моно- ди- или три-(низший алкокси)алюмогидриды щелочных металлов, моно- ди- или три-(низший алкокси низший алкокси)алюмогидриды щелочных металлов, ди(низший алкил)алюмогидриды, цианоборогидриды щелочных металлов, три(низший алкил)гидриды олова, три(арил)гидриды олова, Li(C2H5)3BH и (((СН3)2СНС2)2AlH)2. Другим пригодным восстанавливающим агентом для перфтордисульфонилфторида является щелочной сульфит. Подходящие щелочные сульфиты включают сульфиты щелочных и щелочноземельных металлов, например K2SO3, Na2SO3, KHSO3 и NaHSO3.
[0020] Восстановление перфтордисульфонилфторида может быть сделано в присутствии растворителя. Выбор растворителя зависит от используемого восстанавливающего агента. Растворитель должен быть инертным к реагентам и продукту; и реагент, и продукт должны обладать, по крайней мере, некоторой растворимостью в этом растворителе. Примерные растворители включают полярные апротонные растворители, например, CH3CN, диметилформамид, диметилсульфоксид и другие растворители, такие как диалкиловые эфиры (например, диэтиловый эфир, т-бутилметиловый эфир, диалкиловый эфир гликоля (например, СН3ОСН2СН2ОСН3), диоксан и тетрагидрофуран), и их комбинации. Иллюстративные растворители также включают полярные протонсодержащие растворители, такие как низшие алканолы, имеющие 1-4 атома углерода (например, метанол, этанол, изопропанол, н-бутанол и т.д.), кислоты (например, уксусная кислота), вода и их комбинации.
[0021] Восстановление перфтордисульфонилфторида может быть проведено при температуре по меньшей мере 10, 20, 23, 25, 30 или даже 35°С; максимальные значения - 70, 80, 90, 100, 150, 200 или даже 220°С.
[0022] Восстановленный перфторсульфонилфторид далее вступает в реакцию с йодом с получением перфторированного двуйодистого соединения (например, α,ω-дииодоперфторалканы).
[0023] В одном варианте осуществления изобретения перед реакцией с йодом продукт реакции со стадии восстановления, указанной выше, сначала может быть окислен для получения дисульфиновой кислоты. Окисление продукта реакции позволяет удалить нерастворимые соли до контакта с йодом. При окислении для достижения желаемой кислотности могут использоваться кислоты, известные в уровне техники, включая соляную кислоту, серную кислоту и фосфорную кислоту.
[0024] Для получения желаемого перфторированного двуйодистого соединения продукт реакции, представляющий собой дисульфинат, вступает в реакцию с йодом.
[0025] Чтобы вызывать реакцию замещения, используют радикалобразующее соединение (радикальный инициатор или донор электронов) и/или нагревание. Например, персульфат может использоваться для разъединения сульфиновой группы, образующей радикал, который может затем вступать в реакцию с йодом с получением перфторированного двуйодистого соединения. В другом примере реакционную смесь, включающую дисульфинат, можно нагреть выше температуры разложения сульфиновой группы для генерации радикала, который может затем вступать в реакцию с йодом с получением перфторированного двуйодистого соединения.
[0026] В одном варианте осуществления изобретения реакция с йодом проводится в присутствии растворителя. Типичные растворители включают, например, воду, ацетонитрил, изопропанол, уксусную кислоту и их комбинации.
[0027] В одном варианте осуществления изобретения реакция с йодом может быть проведена при температуре от по меньшей мере 10, 20, 23, 25, 30 или даже 35°С; при этом максимальная температура может быть 70, 80, 90, 100, 150, 200 или даже 220°С.
[0028] Полученное перфторированное двуйодистое соединение может быть изолировано и очищено известными способами.
[0029] Количество атомов углерода в полученном перфторированном двуйодистом соединении идентично количеству атомов углерода, присутствующих в исходном перфтордисульфонилфториде. Поэтому Способ I, как раскрыто выше, может использоваться для генерации как нечетных, так и четных α,ω-дииодоперфторалканов, в зависимости от длины углеродной цепи начального исходного материала. Например, если перфтордисульфонилфторид включает две группы CF2, то полученный α,ω-дииодоперфторалкан будет иметь две группы CF2. Аналогично, если перфтордисульфонилфторид включает три группы CF2, то полученный α,ω-дииодоперфторалкан будет иметь три группы CF2. Кроме того, если перфтордисульфонилфторид включает группу -CF2CF(CF2)CF2-, то полученное перфторированное двуйодистое соединение будет также включать группу -CF2CF(CF2)CF2-.
[0030] Иллюстративные перфторированные двуйодистые соединения, полученные способом, описанным выше, включают α,ω-дииодоперфторалканы со структурой: I-CF2CF2CF2-I, I-CF2CF2CF2CF2-I, I-CF2CF2CF2CF2CF2-I, I-CF2CF2CF2CF2CF2CF2-I, и т.д.
[0031] В одном варианте осуществления изобретения перфторированные двуйодистые соединения по настоящему изобретению могут использоваться в качестве агентов передачи цепи в полимерных синтезах или, как будет описано ниже, могут использоваться для генерации других фторированных соединений.
[0032] Способ II
[0033] Также в настоящем документе раскрыт способ получения этилензамещенного перфтордииодида (например, α,ω-дииодогидрофторалканов), где перфторированное двуйодистое соединение вступает в реакцию с этиленом с получением α этилензамещенного перфтордииодида. Например, соединение Формулы I вступает в реакцию с этиленом с получением соединения Формулы II.

где n является по крайней мере 1. В одном варианте осуществления настоящего изобретения n является нечетным целым числом, составляющим, по крайней мере, 3, 5, 7 или даже 9. Следует обратить внимание на то, что, несмотря на то, что Способ II иллюстрирует линейные алкановые соединения, химические процессы, описанные в Способе II, также могут быть применены к другим перфторированным двуйодистым соединениям, раскрытым в настоящем описании.
[0034] В одном варианте осуществления изобретения α,ω-дииодоперфторалкан (например, соединение Формулы I) может быть получен согласно Способу I, раскрытому выше, или может быть получен взаимодействием оксида гексафторпропилена с йодом, как раскрыто, например, в заявке США №61/715059 (поданной 17.10.2012), включенной посредством ссылок в настоящий документ. Альтернативно, α,ω-дииодоперфторалкан может быть получен способом, включающим известные процессы получения α,ω-дииодоперфторалканов, например, теломеризацией TFE. Однако эти альтернативные способы могут не привести к формированию углеродной цепи с четным количеством атомов углерода, которая является желательной в некоторых случаях.
[0035] Этилен затем добавляют к перфторированному двуйодистому соединению (например, α,ω-дииодоперфторалканам). Для достижения вставки этилена используют радикалобразующее соединение, свет (например, УФ-излучение) и/или нагревание.
[0036] Иллютративные радикалобразующие соединения включают пероксиды или азо-соединения. Пероксиды включают, например, органические пероксиды, такие как диацилпероксиды, пероксиэфиры, диалкиловые пероксиды и гидропероксиды. Азо-соединения включают, например, азоизобутиронитрил и азо-2-циановалериановую кислоту. Другие радикалобразующие соединения являются донорами электронов, такими как комплексные соединения металла или комплексные соединения металла с лигандами, также известные в литературе. Иллюстративный донор электронов для такого соединения перфторированного йодида с ненасыщенной углерод-углеродной связью представляет собой Cu, Zn, Mg, Pd(0), Fe, Ni, Pt(P(C6H5)3)4, Ir(CO)H(P(C6H5)3)3, Pb(C2H3O2)4 и RhCl(P(C6H5)3)2.
[0037] В одном варианте осуществления изобретения реакция может быть проведена при температуре по крайней мере 10, 25, 50, 100, или даже 125°С; максимум - 140, 150, 200 или даже 220°С.
[0038] В одном варианте осуществления изобретения отношение этилена к α,ω-дииодоперфторалкану составляет 1:2-2:1, более предпочтительно 1:0.8-1:1.1, еще более предпочтительно, 1:0.9. [0039] В одном варианте осуществления изобретения реакция с этиленом проводится без примесей. В другом варианте осуществления изобретения реакция с этиленом проводится в присутствии растворителя. Типичные растворители включают инертные растворители, например фторированные растворители, такие как "3М FLUORINERT ELECTRONIC LIQUID" и "3М NOVEC ENGINEERED FLUID" от 3М Co., Сен-Пол, Миннесота.
[0040] Полученный этилензамещенный перфтордииодид (например, α,ω-дииодогидротфторалкан) может быть изолирован и очищен известными способами.
[0041] Иллюстративные этилен замещенные перфтордииодиды включают I-CH2CH2CF2CF2CF2-I, I-CH2CH2CF2CF2CF2CF2-I, I-CH2CH2CF2CF2CF2CF2CF2-I, и т.д.
[0042] В одном варианте осуществления изобретения Формула II представляет собой I(CF2)xCH2CH2I, где х является нечетным целым числом от 3 до 11 (другими словами, 3, 5, 7, 9, или 11).
[0043] В одном варианте осуществления изобретения замещенные этиленом перфтордииодиды по настоящему изобретению могут использоваться в качестве агентов передачи цепи в полимерных синтезах или могут также использоваться для генерации других фторированных соединений.
[0044] Способ III
[0045] Также в настоящем документе раскрыт способ получения частично фторированных концевых иодалкенов, которые в одном варианте осуществления изобретения могут использоваться в качестве мономеров-модификаторов.
[0046] В Способе III по настоящему изобретению замещенный этиленом перфтордииодид является дегидроиодизированным для получения частично фторированного иодалкена. Например, соединение Формулы II является дегидроиодизированным для получения соединения Формулы III.

где n является по крайней мере 1. В одном варианте осуществления изобретения n является нечетным целым числом, составляющим по крайней мере 3, 5, 7 или даже 9.
[0047] В настоящем изобретении замещенный этиленом перфтордииодид из Способа II может быть дополнительно обработан основным или основоподобным соединением в спиртовом растворе с получением частично фторированного концевого иодалкена.
[0048] Обычно, по крайней мере, мольные эквиваленты основного или основоподобного соединения к замещенному этиленом перфтордииодиду должны использоваться для получения частично фторированного иодалкена.
[0049] Основные и основоподобные соединения включают известные в уровне техники, например, метилаты, KOH, NaOH, алкиламины, LiCl в диметилформамиде и т.д.
[0050] В одном варианте осуществления изобретения реакция может быть проведена при температуре, по крайней мере, 10, 20, 23, 25, 30, или даже 35°С; максимальная температура составляет 70, 80, 90, 100, 150, 200, или даже 220°С.
[0051] В одном варианте осуществления изобретения реакция проводится в присутствии растворителя. Типичные растворители включают, например, водные и полярные органические растворители, такие как низшие алканолы, включающие этанол, метанол, изопропанол, бутанол, и т.д.
[0052] Полученные частично фторированные концевые соединения иодалкена могут быть изолированы и очищены известными способами.
[0053] Иллюстративные частично фторированные соединения иодалкена включают CH=CH2CF2CF2CF2-I, CH2=CH2CF2CF2CF2CF2-I, CH2=CH2CF2CF2CF2CF2CF2-I и т.д.
[0054] В одном варианте осуществления изобретения Формула III представляет собой I(CF2)xCH2=CH2, где х является нечетным целым числом от 3 до 11 (другими словами, 3, 5, 7, 9 или 11).
[0055] В одном варианте осуществления изобретения частично фторированные концевые соединения иодалкена по настоящему изобретению могут использоваться в качестве мономеров-модификаторов в полимерном синтезе.
[0056] Полимерный синтез
[0057] В одном варианте осуществления изобретения соединения Формул I, II, и III могут использоваться по отдельности или вместе во время полимеризации фторполимера (например, как мономеры-модификаторы или агенты передачи цепи).
[0058] При получении фторполимеров соединения Формул I, II и/или Формулы III могут полимеризоваться с одним или несколькими фторированными олефиновыми мономерами с получением полимера.
[0059] Фторированный олефиновый мономер является мономером, имеющим двойную связь углерод-углерод, и включает по крайней мере один атом фтора. Фторированный олефиновый мономер может быть перфторированным (или полностью фторированным) или частично фторированным (включающим, по крайней мере один атом водорода и один атом фтора).
[0060] Иллюстративные перфторированные олефиновые мономеры включают гексафторпропен (HFP), тетрафторэтилен (TFE), пентафторпропилен, трифторхлороэтилен (CTFE), перфтор(алкилвиниловый эфир), хлортрифторэтилен, перфтор(метилвиниловый эфир) (PMVE), перфтор(пропилвиниловый эфир) (PPVE), перфтор(метоксипропилвиниловый эфир), перфтор(этоксиметилвиниловый эфир), CF2=CFOCFCF2CF2OCF3, CF2=CFOCF2OCF2CF2CF3, CF2=CFOCF2OCF2CF3, CF2=CFOCF2OCF3 и их комбинации.
[0061] Иллюстративные частично фторированные олефиновые мономеры включают винилфторид (VF), винилиденфторид (VDF), фторэтилен, пентафторпропилен (например, 2-гидропентафторпропилен), трифторэтилен и их комбинации.
[0062] В дополнение к фторированному олефиновому мономеру дополнительные мономеры могут быть добавлены, такие как нефторированные олефиновые мономеры. Иллюстративные нефторированные олефиновые мономеры включают пропилен, этилен, изобутилен и их комбинации. Обычно эти дополнительные мономеры использовались бы в количествах менее чем 25 мольных процентов фторполимера, предпочтительно менее 10 мольных процентов, и даже меньше чем 3 мольных процента.
[0063] В настоящем изобретении соединение Формулы I и/или II может использоваться в полимеризации в качестве агента передачи цепи. Агенты передачи цепи добавляют к полимеризации для контроля молекулярной массы растущей полимерной цепи.
[0064] В настоящем изобретении соединение Формулы III может использоваться в полимеризации в качестве мономера-модификатора. Мономеры-модификаторы полимеризуются в полимер во время полимеризации и затем используются в качестве сайтов для последующей поперечной сшивки полимерных цепей.
[0065] Инициаторы, известные в уровне техники, могут быть использованы для инициирования полимеризации фторированных олефиновых мономеров с мономерами-модификаторами и/или агентами передачи цепи по настоящему изобретению.
[0066] При использовании мономера-модификатора Формулы III во время полимеризации может использоваться агент передачи цепи Формулы II, и/или агент передачи цепи, выбранный из (i) C1 - С10 α,ω-дииодоперфторалкана; (ii) I(CF2)yCH2CH2I, где у является целым числом от 2 до 10; (iii) CH2I2; и (iv) их комбинации. Иллюстративные агенты передачи цепи включают 1,3-дииодоперфторпропан, 1,4-дииодоперфторбутан, 1,6-дииодоперфторгексан и 1,8-дииодоперфтороктан.
[0067] После полимеризации полимерная дисперсия может быть коагулирована и промыта известными способами с получением полимерного каучука.
[0068] В одном варианте осуществления изобретения полимер по настоящему изобретению включает по крайней мере 0,05, 0,1, 0,2 или даже 0,4% по весу йода относительно общей массы полимерного каучука. В одном варианте осуществления изобретения, полимерный каучук по настоящему изобретению включает максимум 0.5, 0.75, 1 или даже 1,5% по весу йода относительно общей массы полимерного каучука.
[0069] Полимерные каучуки по настоящему изобретению являются частично фторированными эластомерами. Как раскрыто в настоящем документе, частично фторированный эластомер является аморфным полимером, включающим, по крайней мере, один атом водорода и по крайней мере один атом фтора на цепи полимера.
[0070] Иллюстративные фторполимеры включают сополимер TFE/пропилен, сополимер TFE/пропилен/VDF, сополимер VDF/HFP, сополимер TFE/VDF/HFP, сополимер TFE/PMVE, сополимер TFE/CF2=CFOC3F7, сополимер TFE/CF2=CFOCF3/CF2=CFOC3F7, сополимер TFE/CF2=C(OC2F5)2, сополимер TFE/этилвинилового эфира (EVE), сополимер TFE/бутилвинилового эфира (BVE), сополимер TFE/EVE/BVE, сополимер VDF/CF2=CFOC3F7, сополимер этилен/HFP, сополимер TFE/HFP, сополимер CTFE/VDF, сополимер TFE/VDF, сополимер TFE/VDF/PMVE/этилена и сополимер TFE/VDF/CF2=CFO(CF2)3OCF3.
[0071] Вулканизация
[0072] Фторполимер по настоящему изобретению может быть вулканизирован пероксидными вулканизирующими агентами, включающими органические пероксиды. Во многих случаях предпочтительней использовать трет-бутилпероксид, имеющий четвертичный атом углерода, присоединенный к пероксидному кислороду.
[0073] Иллюстративные пероксиды включают 2,5-диметил-2,5-ди(т-бутилперокси)гексан; дикумилпероксид; ди(2-т-бутилпероксиизопропил)бензол; диалкилпероксид; бис(диалкилпероксид); 2,5-диметил-2,5-ди(трет-бутилперокси)3-гексин; дибензоилпероксид; 2,4-дихлоробензоилпероксид; трет-бутилпербензоат; α,α'-бис(т-бутилперокси-диизопропилбензол); т-бутилпероксиизопропилкарбонат, т-бутилперокси-2-этилгексилкарбонат, т-амилперокси-2-этилгексилкарбонат, т-гексилпероксиизопропилкарбонат, ди[1,3-диметил-3-(т-бутилперокси)бутил]карбонат, карбонопероксидная кислота, O,O'-1,3-пропандиилOO,OO'-бис(1,1-диметилэтил)эфир и их комбинации.
[0074] Количество используемого пероксидного вулканизирующего агента обычно составляет по крайней мере 0,1, 0.2, 0.4, 0.6, 0.8, 1, 1.2 или даже 1.5; максимум 2, 2.25, 2.5, 2.75, 3, 3.5, 4, 4.5, 5 или даже 5,5 весовых частей на 100 частей фторполимера.
[0075] В пероксидные системы вулканизации зачастую желательно включать соагент. Специалисты в области могут выбрать стандартные соагенты на основе желаемых физических свойств. Иллюстративные соагенты включают три(метил)аллилизоцианурат (TMAIC), триаллилизоцианурат (TAIC), три(метил)аллилцианурат, поли-триаллилизоцианурат (поли-TAIC), триаллилцианурат (ТАС), ксилилен-бис(диаллилизоцианурат) (XBD), N,N'-m-фениленбисмалеимид, диаллилфталат, трис(диаллиламин)-s-триазин, триаллилфосфит, 1,2-полибутадиен, этиленгликольдиакрилат, диэтиленгликольдиакрилат и их комбинации. Другой приемлемый соагент может быть представлен формулой CH2=CH-Rfl-CH=CH2, где Rfl может быть перфторалкиленом из 1-8 атомов углерода. Такие соагенты обеспечивают улучшенную механическую прочность полностью вулканизированному эластомеру. Они обычно используются в количестве по крайней мере 0,5, 1, 1.5, 2, 2.5, 3, 4, 4.5, 5, 5.5, или даже 6; максимум 4, 4.5, 5, 5.5, 6, 7, 8, 9, 10, 10.5 или даже 11 весовых частей на 100 частей фторполимера.
[0076] Составы фторполимера могут также содержать большое разнообразие добавок, обычно используемых в получении эластомерных составов, таких как пигменты, наполнители (например, углеродная сажа), порообразующие агенты и другие агенты, известные в уровне техники.
[0077] Оксиды металла традиционно используются при пероксидной вулканизации. Иллюстративные оксиды металла включают Са(ОН)2, СаО, MgO, ZnO и PbO. В одном варианте осуществления изобретения вулканизируемый фторполимер, по существу, не содержит оксида металла (т.е. состав включает меньше, чем 1, 0.5, 0.25, 0.1, или даже меньше 0,05 частей на 100 частей фторэластомера). В одном варианте осуществления изобретения вулканизируемый фторполимер включает оксид металла. Например, по крайней мере 1,5, 2, 4, 5, или даже 6 частей оксида металла на 100 частей фторполимера.
[0078] В процессе вулканизации каучуковый фторполимер, вместе с необходимыми количествами пероксида, соагентов и других компонентов смешивают стандартными средствами, например, в двухвалковом вальце, при повышенных температурах. Каучуковый фторполимер затем обрабатывают и формуют (например, в форме покрытия шланга или шланга) или отливают в форму (например, в форме кольцевого уплотнителя). Формованное изделие далее может подлежать термической обработке, чтобы вулканизировать состав каучука и получить вулканизированное резиновое изделие.
[0079] Вулканизированные фторэластомеры часто используются в качестве герметиков (изоляций), уплотнителей и формованных частей в системах, подверженных воздействию повышенных температур и/или коррозийных материалов, например, в автомобильной, химической обработке, полупроводниках, космической промышленности и нефтяной промышленности и т.д. Поскольку фторэластомеры могут использоваться в герметизации (изолировании), важно, чтобы эластомеры проявляли хорошие свойства при сжатии. Компрессионная герметизация основывается на способности эластомера легко сжиматься и разжиматься, и производить усилие обратного давления на сопряженных поверхностях. Способность материала сохранять эту равнодействующую силу во времени в различных условиях окружающей среды важна для долгосрочной стабильности. В результате теплового расширения, уменьшения напряжения и теплового старения, начальные герметизирующие усилия ослабевают со временем. Путем определения сохраненной герметизирующей силы резиновые материалы можно оценить на герметизирующее задержание силы в различных условиях, особенно при условиях высокой температуры, например 200°С, 225°С, 250°С, и даже 275°С.
[0080] Иллюстративные варианты осуществления настоящего изобретения включают:
[0081] Пункт 1. Состав, включающий частично фторированное соединение, выбранное из группы, состоящей из I(CF2)XCH=CH2 (Формула III); и I(CF2)xCH2CH2I (Формула II), где х является нечетным целым числом от 3 до 11.
[0082] Пункт 2. Полимерный состав, включающий полимеризованный продукт реакции частично фторированного соединения по пункту 1 и фторированного олефинового мономера.
[0083] Пункт 3. Полимерный состав по пункту 2, в котором фторированный олефиновый мономер выбран из группы, состоящей из гексафторпропилена, трифторэтилена, фторэтилена, винилиденфторида, тетрафторэтилена, перфтор(метилвинилового эфира), перфтор(пропилвинилового эфира), перфтор(метоксипропилвинилового эфира), перфтор(этоксиметилвинилового эфира), хлортрифторэтилена и их комбинаций.
[0084] Пункт 4. Полимерный состав по любому из пунктов 2 или 3, в котором полимеризованный продукт реакции дополнительно включает агент передачи цепи, где агент передачи цепи выбран из группы, состоящей из С1-С10 α,ω- дииодоперфторалкана; I(CF2)yCH2CH2I, где у является целым числом от 2 до 10; CH2I2; и их комбинации.
[0085] Пункт 5. Полимерный состав по пункту 4, в котором агент передачи цепи является 1,3-дииодоперфторпропаном или 1,4-дииодоперфторбутаном.
[0086] Пункт 6. Полимерный состав по любому из пунктов 2-5, где х равняется 3.
[0087] Пункт 7. Полимерный состав по любому из пунктов 2-6, в котором полимеризованный продукт реакции дополнительно включает нефторированный олефиновый мономер.
[0088] Пункт 8. Полимерный состав по любому из пунктов 2-7, в котором полимерный состав включает 0.05-1% йода по весу.
[0089] Пункт 9. Изделие, включающее вулканизированный полимерный состав по любому из пунктов 2-8.
[0090] Пункт 10. Способ получения полимера, включающий обеспечение частично фторированного соединения I(CF2)XCH=CH2 (Формула III) по пункту 1; фторированного олефинового мономера; и инициатора; и полимеризацию частично фторированного соединения и фторированного олефинового мономера с получением полимера.
[0091] Пункт 11. Способ по пункту 10, дополнительно включающий полимеризацию в присутствии агента передачи цепи.
[0092] Пункт 12. Способ по пункту 11, в котором агент передачи цепи является 1,3-дииодоперфторпропаном или 1,4-дииодоперфторбутаном.
[0093] Пункт 13. Способ по любому из пунктов 10-12, в котором фторированный олефиновый мономер выбран из группы, состоящей из гексафторпропилена, трифторэтилена, фторэтилена, винилиденфторида, тетрафторэтилена, перфтор(метилвинилового эфира), перфтор(пропилвинилового эфира), перфтор(метоксипропилвинилового эфира), перфтор(этоксиметилвинилового эфира), хлортрифторэтилена и их комбинаций.
[0094] Пункт 14. Способ получения перфторированного соединения, включающий восстановление перфтордисульфонилфторида с получением дисульфината; и реакцию дисульфината с йодом с получением α,ω-дииодоперфторалкана.
[0095] Пункт 15. Способ получения перфторированного соединения, включающий следующие стадии по порядку: обеспечение оксида гексафторпропилена и йода; и реакцию оксида гексафторпропилена с йодом с получением α,ω-дииодоперфторалкана формулы I(CF2)XI, где х является нечетным целым числом от 3 до 11.
[0096] Пункт 16. Способ получения частично фторированного соединения, включающий реакцию α,ω-дииодоперфторалкана из Пунктов 14 или 15 с этиленом с получением α,ω-дииодоперфторалкана.
[0097] Пункт 17. Способ по пункту 16, дополнительно включающий дегидроиодирование α,ω-дииодоперфторалкана с получением йодированного частично фторированного олефина формулы I(CF2)xCH=CH2, где х является по крайней мере 1.
ПРИМЕРЫ
[0098] Преимущества и варианты осуществления настоящего изобретения далее проиллюстрированы следующими примерами, но определенные материалы и объемы, раскрытые в этих примерах, а также в других условиях и деталях, не следует толковать для несоответствующего ограничения настоящего изобретения. В этих примерах все проценты, пропорции и отношения приведены по весу, если иначе не обозначено.
[0099] Все материалы коммерчески доступны от разных производителей, например, Sigma-Aldrich Chemical Company; Милуоки, Висконсин или известны специалистам в данной области, если не указано иное.
[00100] Указанные сокращения используются в следующих примерах: г = грамм, мин = минута, моль = моль, ч = час, мл = миллилитр; вес = вес.
Материалы

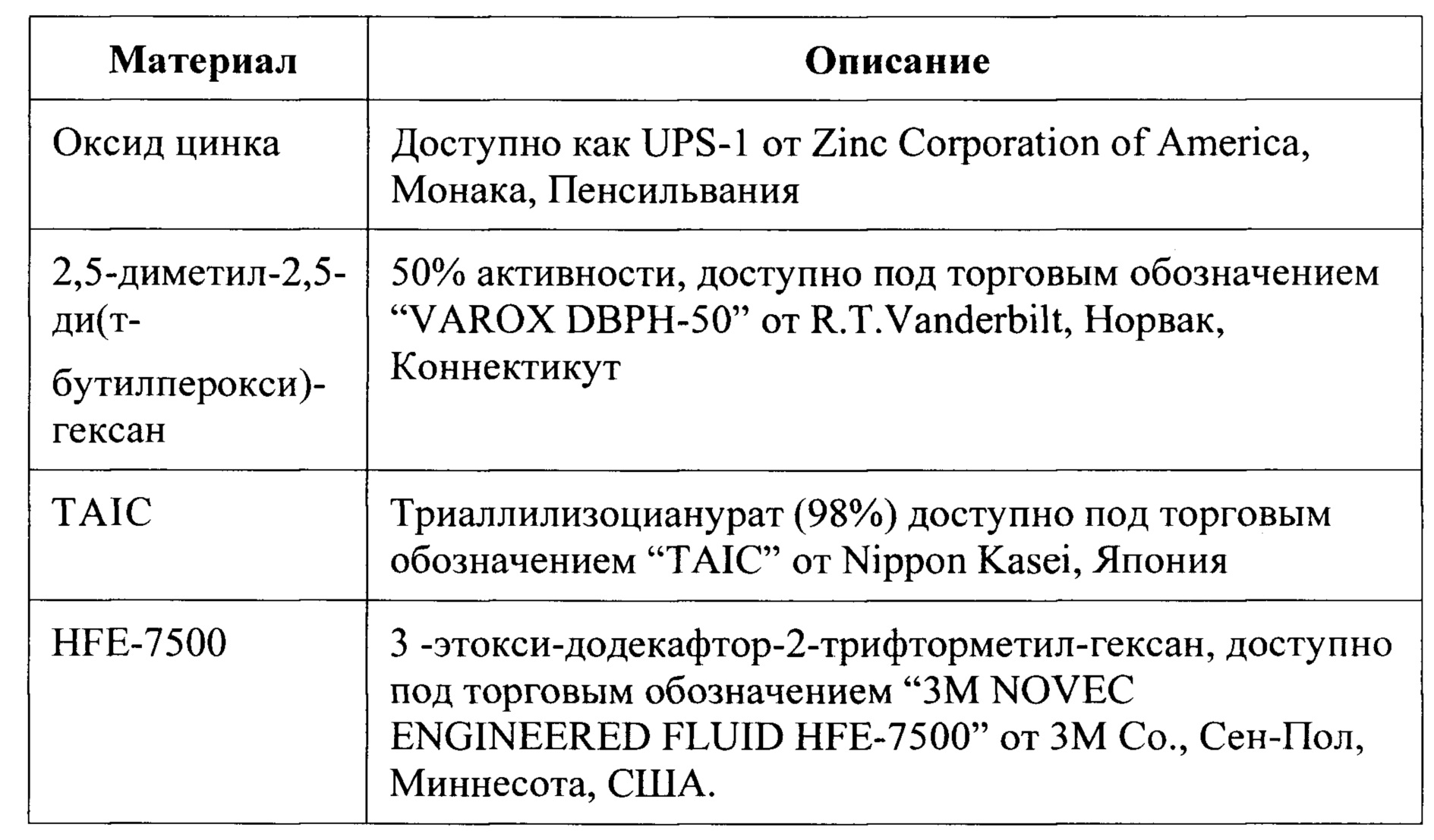
[00101] Реология вулканизации
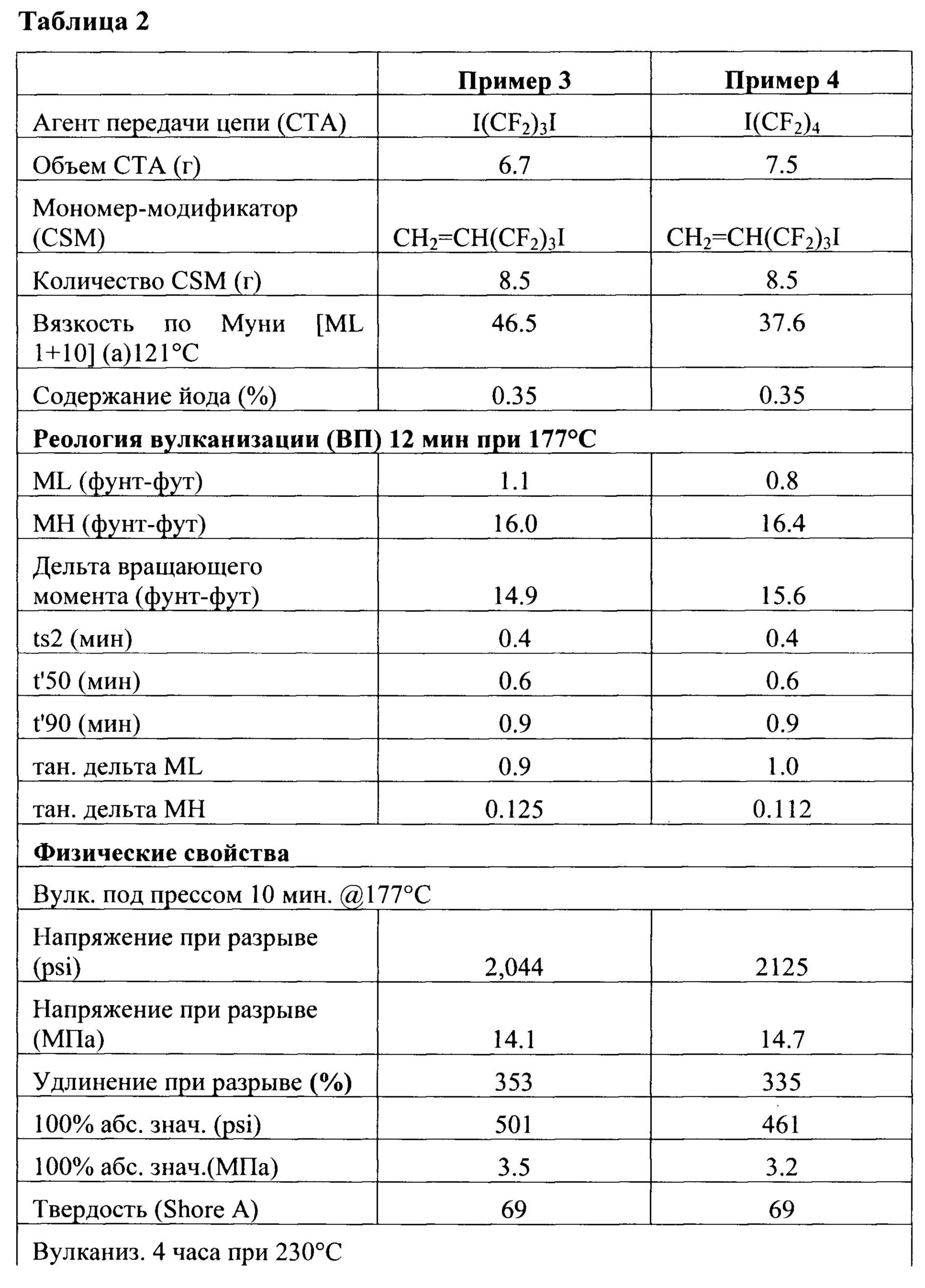
[00102] Анализы реологии вулканизации были выполнены с помощью невулканизированных образцов с помощью реометра (Alpha Technology RPA 2000 в вискозиметре с пуансоном (ВП) Alpha Technology, Dynisco Company, Акрон, Огайо) в соответствии с ASTM D 5289-12 в 177°С, без предварительного нагрева, с 12-минутной выдержкой и дугой 0,5 градуса. Были измерены и минимальный вращающий момент (ML), и самый высокий вращающий момент, достигнутые во время установленного периода времени, когда не было получено пологой части графика или максимального вращающего момента (МН). Также измеряли время увеличения вращающего момента на 2 единицы выше ML (ts2); время достижения вращающего момента значения ML+0.5 (МН - ML), (t '50); и время достижения вращающего момента ML+0.9 (МН - ML), (t '90), а также тангенс дельта в МН и ML. Результаты приведены в Таблице 2.
[00103] Физические свойства
[00104] Вязкость по вискозиметру Муни была определена согласно ASTM 1646-00 (ML 1+10 121°С). Результаты приведены в единицах Муни.
[00105] Данные прессовой вулканизации являются данными, полученными из анализа механических свойств, после прессования листов (150 мм × 150 мм × 2 мм) и проведения вулканизации в течение 10 минут при температуре формы 177°С. Данные последующей вулканизации были получены из листов, подготовленных, как описано для прессовой вулканизации, которые далее обработаны путем нагревания листов в термостате с циркулирующим воздухом приблизительно при 230°С в течение 4 часов.
[00106] Предел прочности на разрыв, относительное удлинение при разрыве и 100% абсолютные значения (последние для предела прочности при 100% удлинении) были определены с помощью механического тестера Tensometer 2000 с датчиком нагрузки на 100 кгс в соответствии с ASTM D 412-92. Заготовки для физических свойств были вырезаны из вулканизированных листов формой ASTM D. Все испытания проводились при постоянной скорости выдавливания поперечной головки 500 мм/минут. Представленные значения являются средними значениями трех анализов. Дюрометр, или твердость, определялась с помощью Метода А по ASTM D 2240-02 дюрометром Типа а-2 Shore. Единицы указаны в баллах.
[00107] Сопротивление пластичной деформации было измерено на кольцевых уплотнителях согласно ASTM D395-03 (способ В (25% деформация)) и ASTM D 1414-94. Кольцевые уплотнители были вулканизированы под прессом с использованием формы 214 для кольцевых уплотнителей (AMS AS568) при 177°С в течение 10 минут и далее вулканизировались в течение 4 часов приблизительно при 230°С. Вулканизированные под прессом и дополнительно вулканизированные кольцевые уплотнители были проверены на пластичную деформацию в течение 22 часов приблизительно при 200°С.
[00108] Пример 1А: Получение 1,3-дииодогексафторпропана из FSO2C3F6SO2F
[00109] Перфторпропандисульфонилфторид FSO2C3F6SO2F, 200 г (0.63 моль) был восстановлен в 3-литровой колбе с круглым дном с 3 горлышками, оборудованной механической мешалкой, конденсатором, дополнительным раструбом и термопарой путем добавления 97 г (2.55 моль) борогидрида натрия в 690 г 2-пропанола. Скорость добавления составляла три часа с сохранением температуры реакции ниже 40°С. После добавления реакцию нагрели до 75°С в течение одного часа. Реакцию охладили до 25°С и добавили 375 г 33% серной кислоты с последующей фильтрацией для получения раствора HOSOC3F6SO2H. В 3-литровую колбу с круглым дном с 3 горлышками добавили 400 г йода (1.58 моль), 376 г персульфата натрия (1.58 моль), 600 г дистиллированной воды и 200 г 2-пропанола размешали и нагрели до 55°С. Затем через час добавили раствор HOSOC3F6SO2H. После добавления реакцию нагрели до 75°С и выдерживали в течение одного часа. Дистиллят продукта и растворителя собирали в приемнике путем нагревания смеси до 108°С. Смесь продукта и растворителя обработали сульфитом натрия (70 г 10% водного раствора) для получения светло-желтого раствора. Добавили еще воды, чтобы получить фторсодержащее соединение, чтобы сформировать низшую фазу, и фторсодержащее соединение дважды промыли 100 г воды. Вакуумная дистилляция дала 1,3-дииодогексафторпропан, I-C3F6-I 165 г (0,41 моль) с точкой кипения 72°С/100 торр для 65%-ного выхода, подтвержденного F19 ЯМР.
[00110] Пример 1 В: получение 1,3-дииодогексафторпропана из HFPO
[00111] Паровой стерилизатор Hastelloy В-2 на 300 мл (производитель Superpressure Division, Newport Scientific Inc., Джессапа, Мэриленд) наполнили 24,5 г йода и 2,5 г катализатора никеля. Паровой стерилизатор наполнили азотом и очистили три раза. Паровой стерилизатор охладили сухим льдом и наполнили 58 г HFPO. Паровой стерилизатор поместили в шейкер, где его нагревали до 170°С в течение 12 часов. Паровой стерилизатор охладили до комнатной температуры, до выведения образованных газов и получили 36 г темной жидкости. Сырую смесь проанализировалиl9F и1Н ЯМР (ядерный магнитный резонанс) со следующими результатами: I-CF2-I (0,0036% абсолютного веса), I-(CF2)2-I (0,00005%), I-(CF2)3-I (92,2%), I-(CF2)4-I (0,41%), I-(CF2)5-I (5,4%), I-(CF2)8-I (0,27%) плюс небольшое количество различных других монойодистых и двуйодистых соединений, частично фторированных соединений, фторангидридных кислот, карбоновых кислот, алкенов и т.д.
[00112] Пример 2А: получение CH2=CH-C3F6-I
[00113] Реактор Parr™ на 600 мл очистили и наполнили 100 г 1,3-дииодогексафторпропана I-C3F6-I (0.25 моль, полученного из Примера 1А) и 2 г т-амил-2-этилгексаноатпероксида (0.01 моль) и размешали. Реактор нагрели до 65°С и добавили этилен, 6.9 г (0.25 моль) при 18 фунтах на квадратный дюйм (ppsi) через один час и реакцию продолжали в течение 20 часов. Реактор охладили до 25°С, и 85 г смеси продукта дренировали из реактора. Вакуумная дистилляция привела к получению ICH2CH2C3F6I, 53 г (0.13 моль), кипящего в вакууме при 95°С/15 торр. 50 г (0.12 моль) ICH2CH2C3F6I использовали для реакции в 25 г метанола с 28 г (0.13 моль), 25% по весу метоксида натрия в метаноле, при 65°С в течение одного часа, что привело к получению 1-иодо-1,1,2,2,3,3-гексафторпентена IC3F6CH=CH2, 29 г (0.1 моль), подтвержденного19F и1Н NMR, с точкой кипения 106°С.
[00114] Пример 2 В: получение CH2=CH-C3F6-I
[00115] Реактор Parr™ на 600 мл очистили и наполнили 95 г 1,3-дииодогексафторпропана I-C3F6-I (0.24 моль, полученного из Примера IB) и 3 г т-амил-2-этилгексаноатпероксида (0,01 моль) и размешали. Реактор нагрели до 65°С и добавили 6 г этилена (0.21 моль) при 18 фунтах на квадратный дюйм через один час и реакцию продолжали в течение 20 часов. Реактор охладили до 25°С, и 93 г смеси продукта дренировали из реактора. Вакуумная дистилляция привела к получению 51 г ICH2CH2C3F6I (0.12 моль), кипящего при 84°С/6 тор вакуума. Наполнили 37 г (0.09 моль) ICH2CH2C3F6I и начали реакцию в 25 г метанола с 28 г (0.12 моль), 25% по весу метоксида натрия в метаноле, при 65°С в течение одного часа, что привело к получению 24 г 1-иодо-1,1,2,2,3,3-гексафторпентана, IC3F6CENCH2 (0.08 моль), как подтвержденоl9F и1Н NMR, с точкой кипения 106°С.
[00116] Пример 3: получение фторэластомера
[00117] 4-литровый реактор наполнили 2,250 г воды, 2 г персульфата аммония (APS, (NH4)2S2O8), 8 г водного раствора 50% по весу фосфата калия двухосновного (K2HPO4), и 3,3 г олигомерной сульфиновокислой аммониевой соли (сульфиновокислый олигомер 1, Пример 1 от WO 2012/082707 (Фукуши и др.)). После очистки реактора вакуум нарушили и реактор герметизировали азотом до 25 фунтов на квадратный дюйм (0,17 МПа). Эту очистку и герметизацию повторили три раза. Реактор снова очистили и нагрели до 80°С. Вакуум нарушили, и реактор герметизировали до 40 фунтов на квадратный дюйм (0,28 МПа) смесью HFP.
[00118] Смесь HFP состояла из гексафторпропилена (HFP); 1,3-дииодогексафторпропана из Примера 1А; 5-иодогексафторпентена (CH2=CH(CF2)3I) из Примера 2 В; и HFE-7500. Смесь HFP подготовили путем очистки цилиндра из нержавеющей стали объемом 1 литр и троекратной очистки азотом. После добавления 6,7 г (0,0181 моль) 1,3-дииодогексафторпропана, 8,5 г 5-иодогексафторпентена и 16 г HFE-7500 в реактор добавили 1000 г HFP. Эту смесь HFP использовали в полимерном синтезе.
[00119] Затем реактор наполнили тетрафторэтиленом (TFE), винилиденфторидом (VDF) и вышеупомянутой смесью гексафторпропилена (HFP), доводя давление реактора до 200 фунтов на квадратный дюйм (1,38 МПа). Общая предварительная масса смеси TFE, VDF и HFP составила 31,6 г, 96,4 г и 229,5 г соответственно. Реактор размешивали на скорости 650 об/мин (оборотов в минуту). По мере снижения реакторного давления из-за потребления мономера в реакции полимеризации смесь TFE, VDF и HFP постоянно подавалась в реактор, чтобы поддерживать давление 200 фунтов на квадратный дюйм (1,38 МПа). Отношение смеси HFP/VDF, и TFE/VDF составляли 0.61 и 0.23 по весу соответственно. Спустя 4,5 часа подача мономеров и смеси HFP была прекращена, и реактор охладили. Полученная дисперсия имела содержание твердых частиц 31,6% по весу и рН 3,1. Размер дисперсной частицы составлял 80 нм, и общее количество дисперсии составляло 3 878 г.
[00120] Для коагуляции 942 г дисперсии, проведенной, как описано выше, добавили к 2 320 мл 1,25% по весу MgCl2 в водном растворе. Частицы извлекли путем фильтрации коагулянта через ткань и мягко сжали для удаления лишней воды. Частицы ополоснули деионизированной водой и отфильтровали в общей сложности 3 раза. После заключительного полоскания и фильтрации, частицы высушили при 130°С в термостате в течение 16 часов. Полученный каучук из фторэластомера имел вязкость по вискозиметру Муни 46,5 при 121°С.
[00121] Содержание йода по данным радиоактивационного анализа с облучением медленными нейтронами составило 0,35% по весу. Анализ FT-IR показал, что фторэластомер содержал 13,2% по весу сополимеризованных единиц TFE, 53,2% по весу сополимера VDF и 33,6% по весу сополимера HFP. Содержание фтора составило 67,1% по весу.
[00122] Вязкость по вискозиметру Муни или вязкость соединения по вискозиметру Муни определяли в соответствии с ASTM D1646-06 TYPE инструментом MV 2000 (производитель Alpha Technologies, Огайо, США) с использованием большого ротора (ML 1+10) при 121°С. Результаты приведены в единицах Муни.
[00123] Соединение фторэластомера изготовили с помощью 15,2 см (6 дюймов) двухвалкоого вальца путем смешивания 100 частей каучука сырого фторэластомера с 30 частями углеродной сажи N990, 3 частями оксида цинка, 2 частями 2,5-диметил-2,5-ди(т-бутилперокси)-гексана и 3 частями соагента TAIC. Во время смешивания полимер было просто обрабтывать, и соединение не прилипало к вальцу.
[00124] Реологию вулканизации фторэластомера исследовали путем тестирования невулканизованных соединений смесей с помощью механического реометра (доступного под торговым обозначением "RPA, 2000" от Alpha Technology, Dynisco Company, Акрон, Огайо) в режиме ВП (вискозиметр на пуансоне) и согласно процедуре, описанной в ASTM D 5289-95. Фторэластомер показал хорошие свойства вулканизации, и 90% время отверждения (t '90) составляло 0,9 минуты, и вращающий момент трехгранной поверхности (MH-ML) составил 14.9 фунт-фут (16.8 дНм). Результаты испытаний приведены в Таблице 2.
[00125] Фторэластомер вулкалинизировали под прессом с использованием формы 214 для кольцевых уплотнителей (AMS AS568) при 177°С в течение 2 минут. Далее кольцевые уплотнители снова вулканизирвали под прессом при 230°С в течение 4 часов. Вулканизированные под прессом и вулканизированные кольцевые уплотнители проверили на пластичную деформацию в течение 22 часов и 70 часов при 200°С в соответствии со Способом В по ASTM D395-03 и ASTM D 1414-12. Отношение отклонения составляло 25%. Результаты испытаний приведены в Таблице 2.
[00126] Пример 4: получение FKM из I-C4F8-I и Примера 2 В CH2=CH-C3F6-I
[00127] Каучуковый фторэластомер получили и испытали как в Примере 3, кроме того, что 7,5 г (0,0181 моль) 1,4-дииодоостафторбутана (I(CF2)4I) использовали вместо 1,3-дииодогексафторпропана. Общая предварительная масса смеси TFE, VDF и HFP составила 26,5 г, 79,7 г и 241,7 г соответственно. Время полимеризации составляло 3,3 часа и в результате дисперсии получено содержание твердого вещества 30,1% по весу с рН 3,2. Размер дисперсной частицы составлял 78 нм, и общее количество дисперсии составило приблизительно 3 652 г. Полученный каучуковый фторэластомер имел вязкость по вискозиметру Муни 37,6 при 121°С.
[00128] Каучуковый фторэластомер анализировали методом FT-IR, содержащим 14,9% по весу сополимера TFE, 51,5% по весу сополимера VDF и 33,6% по весу сополимера HFP. Содержание фтора составило 67,4% по весу. Содержание йода по данным нейтронно-активационного анализа (NAA) было 0.35%. Содержание фторэластомера в этом примере показало хорошие свойства вулканизации, и 90% время отверждения (t '90) составляло 1,0 минуты, и вращающий момент трехгранной поверхности (MH-ML) составил 15.6 фунт-фут (17.6 дНм). Результаты испытаний приведены в Таблице 2.

[00129] Прогнозируемые модификации и изменения данного изобретения будут очевидны для специалиста в данной области, не отступая от объема и духа настоящего изобретения.
Настоящее изобретение не ограничивается вариантами осуществления, сформулированными в настоящей заявке в иллюстративных целях. В случае противоречия или несоответствия между настоящим описанием и раскрытием в любом документе, включенном посредством ссылок в настоящий документ, настоящее описание является преобладающим.
Реферат
Настоящее изобретение относится к частично фторированному соединению I(CF)СН=СН, где х представляет собой 3, а также к способу его получения, включающему взаимодействие соединения формулы I(CF)I с этиленом с получением соединения формулы I(CF)CHCHI и дегидройодирование его с получением заявленного соединения (значение х в указанных формулах представляет собой 3). Изобретение имеет отношение к фторполимеру для вулканизации, включающему полимеризованный продукт реакции: (a) частично фторированного соединения и (b) фторированного олефинового мономера; к резиновому изделию для герметизации и уплотнения, сформованному из вулканизированного фторполимера; к способу получения фторполимера, включающему: (a) обеспечение частично фторированного соединения, фторированного олефинового мономера и инициатора; и (b) полимеризацию частично фторированного соединения и фторированного олефинового мономера с получением фторполимера. Технический результат – хорошие физические свойства, свойства вулканизации и время отверждения, долгосрочная стабильность. 5 н. и 8 з.п. ф-лы, 2 табл., 4 пр.
Формула


Комментарии