Каталитические системы для олигомеризации этиленав линейные альфа-олефины - RU2315658C2
Код документа: RU2315658C2
Описание
Настоящее изобретение относится к каталитическим системам для олигомеризации этилена в линейные альфа-олефины с высоким выходом и очень высокой селективностью и способу получения упомянутых линейных альфа-олефинов.
Известны различные способы получения высших линейных альфа-олефинов (например, D.Vogt, Oligomerisation of ethylene to higher α-olefins в Applied Homogeneous Catalysis with Organometallic Compounds Ed. B.Cornils, W.A. Herrmann, 2nd Edition, Vol.1, Ch. 2.3.1.3, с. 240-253, Wiley-VCH 2002). Данные коммерческие способы обеспечивают распределение олигомерного продукта либо по типу Пуассона, либо по типу Шульца-Флори.
Для того чтобы получить распределение Пуассона, во время олигомеризации не должен происходить обрыв цепи. Напротив, по способу Шульца-Флори происходит обрыв цепи, который не зависит от длины цепи. Стадия Ni-катализируемой олигомеризации этилена в Shell Higher Olefins Process (SHOP) является типичным примером способа Шульца-Флори.
По способу Шульца-Флори обычно получается широкий диапазон олигомеров, в котором фракцию каждого олефина можно определить путем вычисления на основе так называемого К-фактора. К-фактор, который показывает относительные пропорции олефинов в продукте, представляет собой молярное отношение [Cn+2]/[Cn], вычисленное из наклона графика log[Cn %мол] от n, где n обозначает число атомов углерода в отдельном олефине продукта. К-фактор определяется таким образом для каждого n. Путем вариации лиганда и регулирования параметров реакции можно регулировать К-фактор к большим или меньшим значениям. Таким образом, процесс можно проводить так, чтобы получать состав продукта с оптимальным экономическим эффектом.
Так как потребность в С6-С18 фракции намного выше, чем в С>20 фракции, процессы направляют таким образом, чтобы производить олефины с меньшим количеством углеродных чисел. Тем не менее, образование олефинов с высшими углеродными числами неизбежно и без дополнительной переработки образование этих продуктов убыточно для рентабельности способа. Для того чтобы снизить отрицательное влияние олефинов с высшими углеродными числами и низшей С4 фракции, была разработана дополнительная технология для переработки этих потоков и их превращения в более ценные химические продукты, такие как внутренние С6-С18 олефины, как осуществлено на практике в Shell Higher Olefins Process.
Тем не менее, данная технология является дорогостоящей с точки зрения инвестирования и эксплуатации и, следовательно, приводит к дополнительным расходам. Поэтому значительные усилия направлены на то, чтобы свести образование олефинов с высшими углеродными числами к абсолютному минимуму, т. е. не больше, чем неотъемлемо связано с К-фактором Шульца-Флори.
В связи с этим, ряд опубликованных патентных заявок описывает каталитические системы для полимеризации или олигомеризации 1-олефинов, особенно этилена, которые содержат азотсодержащие соединения переходного металла. Смотри, например, следующие патентные заявки, которые представлены здесь ссылками во всей полноте: WO 92/12162, WO 96/27439, WO 99/12981, WO 00/50470, WO 98/27124, WO 99/02472, WO 99/50273, WO 99/51550, EP-A-1127987, WO 02/12151, WO 02/06192, WO 99/12981, WO 00/24788, WO 00/08034, WO 00/15646, WO 00/20427, WO 01/58874 и WO 03/000628.
В частности, недавно опубликованные заявки Shell WO 01/58874, WO 02/00339, WO 02/28805 и WO 03/011876, которые все представлены здесь ссылками во всей их полноте, обнаруживают новые классы катализаторов, основанные на бисиминопиридиновых соединениях железа, которые высокоактивны в олигомеризации олефинов, особенно этилена, и которые дают линейные альфа-олефины С6-С30 диапазона с распределением Шульца-Флори, причем упомянутые линейные альфа-олефины имеют высокую чистоту.
Тем не менее, все еще есть необходимость улучшения селективности по линейным альфа-олефинам в способах олигомеризации, описанных в предшествующем уровне техники.
Известно, что в соединении с катализатором полимеризации олефинов применяют сокатализатор, такой как алкилалюминий или алюмоксан. Неожиданно было найдено, что замена части алкилалюминиевого или алюмоксанового сокатализатора одним или более соединением цинка, таким как ZnEt2, приводит к улучшению селективности по линейным альфа-олефинам в вышеупомянутом способе олигомеризации, катализируемом бисарилиминопиридиновыми соединениями железа. Одновременно уменьшается количество нежелательных побочных продуктов, таких как внутренние и разветвленные олефины и диены.
Статья в Angew. Chem. Int. Ed. 2002, 41 No.3, c.489-491, озаглавленная "Рост катализируемой железом полиэтиленовой цепи на цинке: линейные альфа-олефины с распределением Пуассона" George J.P. Britovsek, Steven A. Cohen, Vernon C. Gibson, Peter J. Maddox и Martin van Meurs раскрывает процесс роста цепи на цинке, катализируемый бис(имино)пиридином железа. Тем не менее, анализ полимера, полученного в результате данной реакции, после гидролиза показывал полностью насыщенный линейный алкановый продукт предпочтительнее, чем альфа-олефиновый продукт. Для того чтобы получить альфа-олефин, в данной ссылке описывается катализируемое никелем замещение выросшей алкильной цепи в присутствии этилена для регенерации диэтилцинка. Распределение полученных альфа-олефинов, как упомянуто, является скорее Пуассоновым, чем распределением Шульца-Флори.
Настоящее изобретение представляет каталитическую систему содержащую:
(а) один или несколько катализаторов на основе бисарилиминопиридина железа или кобальта;
(b) первое соединенние сокатализатор, которое выбрано из алюминийалкилов, алюмоксанов и их смесей; и
(с) второе соединение сокатализатор, которое содержит одно или несколько соединений формулы ZnR'2, в котором каждый R', который может быть одинаковым или разным, выбирают из водорода, необязательно замещенного С1-С20 углеводорода, фенила, F, Cl, Br, I, SR'', NR''2, OH, OR'', CN, NC, где R'', который в той же молекуле может быть одинаковым или разным, представляет собой необязательно замещенный С1-С20 углеводород.
В дополнительном аспекте настоящего изобретения обеспечивается способ получения линейных альфа-олефинов, включающий взаимодействие этилена в условиях олигомеризации в присутствии эффективного количества каталитической системы, описанной здесь.
Первым существенным компонентом в каталитической системе настоящего изобретения является один или несколько катализаторов на основе бисарилиминопиридина железа или кобальта. Любой катализатор на основе бисарилиминопиридина железа или кобальта, подходящий для использования в реакциях олигомеризации этилена для получения линейных альфа-олефинов, может быть применен здесь.
Подходящие катализаторы на основе бисарилиминопиридина железа или кобальта, используемые в настоящем изобретении, включают в себя, но не ограничиваются этим, бисарилиминопиридиновые MXn комплексы и/или [бисарилиминопиридин MYp·Lb+ ][NC-]q комплексы, причем упомянутые бисарилиминопиридиновые комплексы содержат бисарилиминопиридиновый лиганд, в котором M представляет собой атом металла, выбранный из Fe или Co, n равно 2 или 3 и Х представляет собой галогенид, необязательно замещенный углеводород, алкоксид, амид или гидрид, Y представляет собой лиганд, который может включать в себя олефин, NC- представляет собой некоординированный анион, p+q равно 2 или 3, согласно формальной степени окисления упомянутого атома металла; L представляет собой молекулу нейтрального основания Льюиса; b равно 0, 1 или 2. Катализаторы на основе бисарилиминопиридина железа или кобальта данного типа описаны в WO 01/58874, WO 02/00339, WO 02/28805 и WO 03/011876, которые все представлены здесь ссылками во всей их полноте.
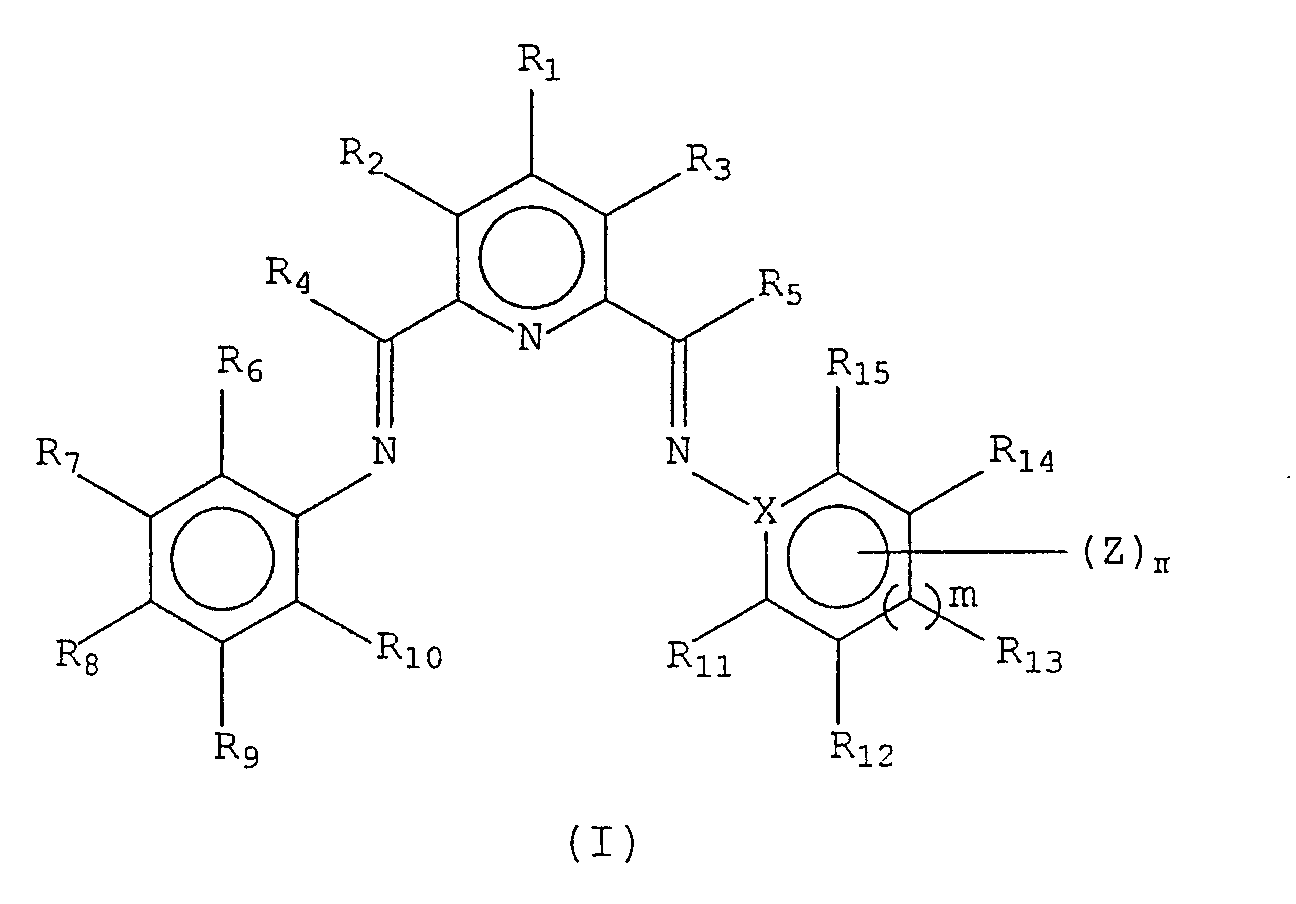
Особенно подходящие бисарилиминопиридиновые лиганды, используемые в каталитических системах настоящего изобретения, включают в себя такие, которые имеют формулу (I), приведенную ниже:

в которой Х представляет собой углерод или азот,
n равно 0 или 1,
m равно 0 или 1,
Z представляет собой π-координированный фрагмент металла, R1-R5, R7-R9 и R12-R14 представляют собой каждый независимо водород, необязательно замещенный углеводород, инертную функциональную группу или любые два из R1-R5, R7-R9 и R12-R14, вицинальные друг другу, взятые вместе, могут образовывать цикл; R6 представляет собой водород, необязательно замещенный углеводород, инертную функциональную группу или взятый вместе с R7 или R4 образует цикл; R10 представляет собой водород, необязательно замещенный углеводород, инертную функциональную группу или взятый вместе с R9 или R4, образует цикл; R11 представляет собой водород, необязательно замещенный углеводород, инертную функциональную группу или, взятый вместе с R5 или R12, образует цикл; и R15 представляет собой водород, необязательно замещенный углеводород, инертную функциональную группу или, взятый вместе с R5 или R14, образует цикл.
В настоящем изобретении некоторые термины используются следующим образом.
Термин "фрагмент π -координированного металла" по отношению к группе Z означает, что группа Z вместе с циклом, содержащим атом Х, представляет собой металлоценовую часть или сандвич или металл-ареновый комплекс, который необязательно замещен. Группа Z содержит атом металла, который π-координирован с ароматическим кольцом, содержащим атом Х. Группа Z может также содержать один или несколько лигандов, которые координированы с атомом металла, такие как, например, (СО) лиганды, так, что группа Z образует фрагмент металла Fe(CO)x. Предпочтительно, тем не менее, если группа Z содержит необязательно замещенное ароматическое кольцо, которое π-координировано с металлом. Упомянутое необязательно замещенное ароматическое кольцо может быть любым подходящим моноциклическим или полициклическим, ароматическим или гетероароматическим кольцом, имеющим от 5 до 10 атомов в кольце, необязательно содержащим от 1 до 3 гетероатомов, выбранных из N, O и S. Ароматическое кольцо, предпочтительно, является моноциклическим ароматическим кольцом, содержащим от 5 до 6 атомов углерода, таким как фенильное или циклопентадиенильное. Неограничивающие примеры комбинаций ароматических углеводородных колец, содержащих атом Х, и фрагментов π-координированного металла включают в себя ферроцен, кобальтоцен, никелецен, хромоцен, титаноцен, ванадоцен, бисбензолхром, бисбензолтитан и подобные гетероареновые комплексы металла, трикарбонил монокатионного аренмарганца, дихлорид аренрутения.
Термин "углеводородная группа" в отношении групп от R1до R15 формулы (I), приведенной выше, означает группу, содержащую только атомы углерода и водорода. Если не оговорено особо, число атомов углерода находится, предпочтительно, в интервале от 1 до 30, особенно от 1 до 6. Углеводородная группа может быть насыщенной или ненасыщенной, алифатической, циклоалифатической или циклоароматической (например, фенил), но предпочтительно является алифатической. Подходящие углеводородные группы включают в себя группы с первичным, вторичным или третичным атомом углерода такие, как описанные ниже.
В настоящем изобретении фраза "необязательно замещенный углеводород" в отношении групп от R1 до R15 формулы (I), приведенной выше, используется для описания углеводородных групп, необязательно содержащих одну или несколько "инертных" функциональных групп, содержащих гетероатом. Под "инертными" понимается, что функциональные группы не влияют в какой-либо заметной степени на процесс (со-)олигомеризации. Неограничивающими примерами таких инертных групп являются фториды, хлориды, силаны, станнаты, простые эфиры, алкоксиды и амины с соответствующим стерическим экранированием, все хорошо известные специалистам в данной области. Некоторые примеры таких групп включают в себя метокси, триметилсилокси и эйкозаноксигруппы. Упомянутый необязательно замещенный углеводород может включать в себя группы с первичным, вторичным или третичным атомом углерода описанного выше типа.
Термин "инертная функциональная группа" в отношении групп от R1до R15 формулы (I), приведенной выше, означает группу, иную, чем необязательно замещенный углеводород, которая здесь является инертной в условиях процесса олигомеризации. Под "инертной" понимается, что функциональная группа не влияет в какой-либо заметной степени на процесс (со-)олигомеризации. Примеры инертных функциональных групп, подходящие для использования здесь, включают в себя галогенид, простые эфиры и амины, такие как третичные амины, особенно фтор и хлор.
Термин "группа с первичным атомом углерода", используемый здесь, означает группу -CH2-R, в которой R выбран из водорода, необязательно замещенного углеводорода или инертной функциональной группы. Примеры подходящих групп с первичным атомом углерода включают в себя, но не ограничены, -CH3, -C2H5, -CH2Cl, -CH2OCH3, -CH2N(C2 H5)2 и -CH2Ph. Предпочтительными группами с первичным атомом углерода для использования здесь являются такие, в которых R выбран из водорода или С1-С6 незамещенного углеводорода, предпочтительно, в которых R представляет собой водород или С1-С3 алкил.
Термин "группа с вторичным атомом углерода", используемый здесь, означает -CH(R)2 группу, в которой каждый R независимо выбран из необязательно замещенного углеводорода или инертной функциональной группы. Альтернативно, две группы R могут вместе представлять собой часть двойной связи, например, =СН2 или циклоалкильную группу. Примеры групп с вторичным атомом углерода включают в себя, но не ограничены, -CH(CH3)2, -CHCl2, -CHPh2, -CH=CH2 и циклогексил. Предпочтительными группами с вторичным атомом углерода для использования здесь являются такие, в которых R представляет собой С1-С6 незамещенный углеводород, предпочтительно С1-С3 алкил.
Термин "группа с третичным атомом углерода", применяемый здесь, означает -C(R)3 группу, в которой каждый R независимо выбран из необязательно замещенного углеводорода или инертной функциональной группы. Альтернативно, три группы R могут вместе представлять собой часть тройной связи, например, -С≡CPh или циклическую систему, содержащую третичные атомы углерода, такую как производные адамантила. Примеры групп с третичным атомом углерода включают в себя, но не ограничены, -C(CH3)3, -CCl3, -C≡CPh, 1-адамантил и -С(СН3 )2(ОСН3). Предпочтительными группами с третичным атомом углерода для использования здесь являются такие, в которых каждый R представляет собой С1-С6 незамещенную углеводородную группу, предпочтительно, в которых каждый R представляет собой С1-С3 алкильную группу, более предпочтительно, в которых каждый R представляет собой метил. В случае, если каждый R является метильной группой, группа с третичным атомом углерода является трет-бутилом.
Под "лигандом, который может вставить олефин", понимают лиганд, который координирован с ионом металла, в который связанная молекула этилена или альфа-олефина может быть вставлена, чтобы инициировать или продолжить реакцию (со -)олигомеризации. В [бисарилиминопиридин MYp·Lb+][NC-]q комплексах по настоящему изобретению Y может быть гидридом, алкилом или любым другим анионным лигандом, который может вставлять олефин.
Под "некоординирующим анионом" понимают анион, который не координирует по существу с атомом металла М. Некоординирующие анионы (NC-), которые могут быть использованы, включают в себя объемистые анионы, такие как тетракис[3,5-бис(трифторметил)фенил]борат (BAF-), (C6F5)4B- и анионы соединений алкилалюминия, включающие в себя R3AlX-, R2AlClX-, RAlCl2X- и " RAlOX-", в которых R представляет собой водород, необязательно замещенный углеводород или инертную функциональную группу, и Х представляет собой галоген, алкоксид или кислород.
Специалисты в данной области оценят, что в вышеописанных ограничивающих условиях заместители R1-R15 могут быть легко выбраны таким образом, чтобы оптимизировать производительность каталитической системы и ее экономическое применение.
В одном предпочтительном варианте осуществления данного изобретения катализатор на основе бисарилиминопиридина металла представляет собой катализатор на основе бисарилиминопиридина железа.
Предпочтительный бисарилиминовый лиганд для использования здесь представляет собой лиганд формулы (I), в котором Х означает С, m равно 1 и n равно 0, так что цикл, содержащий атом Х, представляет собой 6-членную ароматическую группу.
Другой предпочтительный бисарилиминовый лиганд для использования здесь представляет собой лиганд формулы (I), в котором Х означает С, m равно 0, n равно 1, и цикл, содержащий атом Х, вместе с группой Z представляет собой металлоценовую группу.
Еще один предпочтительный бисарилиминовый лиганд для использования здесь представляет собой лиганд формулы (I), в котором Х означает N, m равно 0, n равно 0, так что цикл, содержащий атом Х, представляет собой 1-пиррольную группу.
Для ограничения продуктов олигомерами предпочитают, чтобы не больше, чем один из R6, R10, R11 и R15 представлял собой группу с третичным атомом углерода. Предпочитают также, чтобы не больше, чем два из R6, R10, R11 и R15 представляли собой группу с вторичным атомом углерода.
Предпочтительные лиганды для использования здесь включают в себя лиганды формулы (I) со следующими ортозаместителями:
(i) R6, R10, R11 и R15 каждый независимо представляет собой F или Cl;
(ii) R6 и R10 представляют собой группы с первичным атомом углерода, R11 представляет собой Н или F и R15 представляет собой Н, F или группу с первичным атомом углерода;
(iii) R6 и R10 каждый независимо представляет собой Н или F, R11 и R15 каждый независимо представляет собой F, Cl или группу с первичным атомом углерода;
(iv) R6 представляет собой Н или F, R10 представляет собой Н, F или группу с первичным атомом углерода, R11 и R15 представляют собой группу с первичным атомом углерода;
(v) R6 представляет собой группу с первичным или вторичным атомом углерода, R10 представляет собой Н, R11 и R15 представляют собой H, F, Cl, группы с первичным или вторичным атомом углерода;
(vi) R6 представляет собой группу с третичным атомом углерода, R10 представляет собой Н, R11 представляет собой H, F, Cl, группу с первичным атомом углерода и R15 представляет собой H или F;
(vii) R6 представляет собой группу с третичным атомом углерода, R10 представляет собой группу с первичным атомом углерода, R11 и R15 представляют собой H или F;
(viii) R6 и R10 представляют собой H, F, Cl, группу с первичным атомом углерода, группу с вторичным атомом углерода, R11 представляет собой группу с первичным или вторичным атомом углерода и R15 представляет собой H;
(ix) R6 представляет собой H, F, Cl, R10 представляет собой H, F, Cl или группу с первичным атомом углерода, R11 представляет собой группу с третичным атомом углерода и R15 представляют собой H;
(x) R6 и R10 представляют собой H, F или Cl, R11 представляет собой группу с третичным атомом углерода, R15 представляет собой группу с первичным атомом углерода.
Особенно предпочтительные лиганды для использования здесь включают в себя лиганды формулы (I), в которых R1-R3 представляют собой водород и R4 и R5 представляют собой метил, Н, бензил или фенил, предпочтительно, метил.
Особенно предпочтительные лиганды для использования здесь включают в себя:
лиганд формулы (I), в котором R1-R3 представляют собой водород; R4 и R5 представляют собой метил; R6 и R10 представляют собой метил; R8 представляет собой метил или водород, R7 и R9 представляют собой водород; R11 и R15 представляют собой водород; R12, R13 и R14 независимо представляют собой водород, метил или трет-бутил; Х представляет собой С, m равно 1, n равно 0;
лиганд формулы (I), в котором R1-R3 представляют собой водород; R4 и R5 представляют собой метил; R6, R8 и R10 представляют собой метил; R7 и R9 представляют собой водород; R11 представляет собой фтор; и R12-R15 представляют собой водород; и Х представляет собой С, m равно 1, n равно 0;
лиганд формулы (I), в котором R1-R3 представляют собой водород; R4 и R5 представляют собой метил; R7-R9 и R12-R14 представляют собой водород; R6, R10, R11 и R15 представляют собой фтор; Х представляет собой С, m равно 1, n равно 0;
лиганд формулы (I), в котором R1 -R3 представляют собой водород, R4 и R5 представляют собой метил, R6, R8 и R10 представляют собой метил, R7 и R9 представляют собой водород, m равно 1, n равно 0, Х представляет собой С, R11, R12, R14 и R15 представляют собой водород, R13 представляет собой метокси или триметилсилокси;
лиганд формулы (I), в котором R1-R3 представляют собой водород; R4 и R5 представляют собой метил; R6 и R10 представляют собой метил; R8 представляет собой метил или водород, R7 и R9 представляют собой водород; R11 и R15 представляют собой водород; R12, R13 и R14 независимо представляют собой водород, метил или фтор; Х представляет собой С, m равно 1, n равно 0;
лиганд формулы (I), в котором R1-R3 представляют собой водород, R4 и R5 представляют собой метил, R6, R8 и R10 представляют собой метил, R7 и R9 представляют собой водород, m равно 1, n равно 0, Х представляет собой С, R11 и R15 представляют собой водород, R12 и R14 представляют собой фенил, R13 представляет собой метокси, триметилсилокси и эйкозанокси.
В бисарилиминопиридиновом МХn комплексе Х может быть галогенидом, предпочтительно хлоридом.
В предпочтительном варианте осуществления бисарилиминопиридинового МХn комплекса атом металла М представляет собой Fe и n равно 2. В другом предпочтительном варианте осуществления атом металла М представляет собой Fe и n равно 3.
Нейтральная донорная молекула Льюиса представляет собой соединение, которое может действовать как основание Льюиса, такое как простые эфиры, амины, сульфиды и органические нитрилы, например триэтиламин или 2,6-дитрет-бутилпиридин.
В [бисарилиминопиридин MYp· Lb+][NC-]q комплексе по настоящему изобретению L может быть нейтральной донорной молекулой Льюиса, способной к замещению этиленом, или вакантным координационным местом.
В [бисарилиминопиридин MYp·Lb+][NC-]q комплексе по настоящему изобретению атом металла М представляет собой, предпочтительно, Fe и формальная степень окисления упомянутого атома металла может быть равна 2 или 3.
Соединения сокатализаторы
Второй существенный компонент каталитических систем здесь представляет собой соединение сокатализатор, выбранное из алкилалюминия или алюмоксана. Любой алкилалюминий или алюмоксан, пригодный для использования в качестве сокатализатора, может быть использован здесь. Смеси двух или нескольких алкилалюминиев и/или алюмоксанов также могут быть использованы здесь. Пригодные для использования здесь соединения алкилалюминия или алюмоксана включают в себя метилалюмоксан (МАО) и модифицированный метилалюмоксан (ММАО). Модифицированный метилалюмоксан представляет собой производное метилалюмоксана, в котором часть метильных групп замещена другими алкильными группами, например изобутильными группами. В особенно предпочтительных вариантах осуществления первое соединение сокатализатор представляет собой модифицированный метилалюмоксан, в котором, предпочтительно, около 25% метильных групп замещены изопропильными группами.
Третий существенный компонент каталитических систем здесь представляет собой второе соединение сокатализатор, выбранное из соединений формулы ZnR'2, в которых каждый R', который может быть одинаковым или разным, выбран из водорода, необязательно замещенного С1-С20 углеводорода, фенила, Cl, Br, I, SR'', NR''2, OH, OR'', CN, NC, где R'', который в той же молекуле может быть одинаковым или разным, представляет собой С1 -С20 углеводород.
В предпочтительных каталитических системах настоящего изобретения второе соединение сокатализатор представляет собой ZnR'2, где R' представляет собой С1-С20 углеводород, более предпочтительно, С1-С20 алкил, еще более предпочтительно, С1-С6 алкил. Пригодные алкильные группы включают в себя метил, этил, пропил, бутил и им подобные. Особенно предпочтительно, если R' группа представляет собой С1-С3 алкил, особенно этил.
Второй сокатализатор особенно полезен в сочетании с первым сокатализатором для увеличения селективности по линейным альфа-олефинам в реакциях олигомеризации этилена и снижения количества нежелательных побочных продуктов, таких как разветвленные олефины, внутренние олефины, 2,2-дизамещенные олефины и диены.
Было отмечено, что особенно высокая селективность по линейным альфа-олефинам достигается, когда молярное отношение металла первого сокатализатора к металлу второго сокатализатора находится в диапазоне от 5:1 до 1:5, предпочтительно, от 3:1 до 1:3, более предпочтительно от 2:1 до 1:2 и, особенно, 1:1.
Можно добавлять дополнительные возможные компоненты к каталитическим системам здесь, например кислоты и основания Льюиса такие, как изложены в WO 02/28805.
Каталитическая система может быть образована смешиванием вместе комплекса бисиминопиридина железа или кобальта, или смеси соли ацетилацетоната железа или кобальта и соответствующего бисиминопиридинового лиганда, первого соединения сокатализатора, второго соединения сокатализатора и любых возможных дополнительных соединений, предпочтительно, в растворителе, таком как толуол или изооктан.
Реакции олигомеризации
Количество каталитической системы в реакционной смеси олигомеризации обычно выбирается таким образом, чтобы содержать от 10-4 до 10-9 грамм-атома атомов металла М, в частности Fe [II] или [III], на моль реагирующего этилена.
Реакцию олигомеризации наиболее удобно проводить в диапазоне температур от -100°С до +300°С, предпочтительно, в диапазоне от 0°С до 200°С, и более предпочтительно, в диапазоне от 50°С до 150°С.
Реакцию олигомеризации удобно проводить при давлениях от 0,01 до 15 мПа (от 0,1 до 150 бар(атм)), более предпочтительно, от 1 до 10 мПа (от 10 до 100 бар(атм)), и наиболее предпочтительно, от 1,5 до 5 мПа (от 15 до 50 бар(атм)).
Оптимальные условия по температуре и давлению, применяемые для особых каталитических систем с целью максимизировать выход олигомера и минимизировать конкурирующие реакции, такие как димеризация и полимеризация, могут быть легко установлены специалистом в данной области.
Условия по температуре и давлению выбирают так, чтобы достичь распределения продукта с К-фактором, предпочтительно, в диапазоне от 0,40 до 0,90, наиболее предпочтительно, в диапазоне от 0,60 до 0,80. В настоящем изобретении считается, что полимеризация происходит, когда распределение продукта имеет К-фактор больше 0,9.
Реакция олигомеризации может проводиться в газовой фазе или в жидкой фазе, или смешанной газово-жидкостной фазе в зависимости от летучести исходных и конечных олефинов.
Реакция олигомеризации проводится в присутствии инертного растворителя, который может также быть носителем для катализатора и/или исходного олефина. Подходящие растворители включают в себя алканы, алкены, циклоалканы и ароматические углеводороды. Например, растворители, которые могут быть использованы по настоящему изобретению, включают в себя гептан, изооктан, циклогексан, бензол, толуол и ксилол.
Найдено, что пригодно время реакции от 0,1 до 10 часов в зависимости от активности катализатора. Реакция, предпочтительно, проводится в отсутствие воздуха или влаги.
Реакция олигомеризации может проводиться обычным способом. Она может проводиться в перемешиваемом баковом реакторе, когда олефин и катализатор или предшественники катализатора непрерывно добавляются в перемешиваемый бак, и реагент, продукт, катализатор и неиспользованный реагент удаляют из перемешиваемого бака с отделенным продуктом и неиспользованный реагент и, необязательно, катализатор возвращают обратно в перемешиваемый бак.
Альтернативно, реакция может проводиться в реакторе периодического действия, когда предшественники катализатора и реагирующий олефин загружают в автоклав и после проведения реакции в течение определенного времени продукт отделяют от реакционной смеси обычным способом, таким как дистилляция.
После подходящего времени реакции реакция олигомеризации может быть закончена быстрым выпусканием этилена, для того чтобы дезактивировать каталитическую систему.
Полученные альфа-олефины имеют длину цепи от 4 до 100 атомов углерода, предпочтительно, от 4 до 30 атомов углерода, и наиболее предпочтительно, от 4 до 20 атомов углерода.
Олефины продукта могут быть приемлемо выделены дистилляцией и, в дальнейшем, разделены, как требуется, с помощью технологий дистилляции в зависимости от намеченного конечного применения олефинов.
Теперь настоящее изобретение будет проиллюстрировано следующими примерами, которые не следует рассматривать как ограничивающие область настоящего изобретения каким-либо образом.
Экспериментальные данные
Общие методики и отличительные особенности
Все операции с каталитическими системами проводили в атмосфере азота. Все используемые растворители сушили с применением стандартных методик.
Безводный толуол (99,8% чистоты) (ex. Aldrich) сушили над 4 Å молекулярными ситами (содержание воды после сушки около 3 м.д.).
Этилен (99,5% чистоты) чистили на колонке с 4 Å молекулярными ситами и BTS катализатором (ex. BASF) для того, чтобы уменьшить содержание воды и кислорода до < 1 м.д.
Полученные олигомеры характеризовали с помощью газовой хроматографии (ГХ), для того чтобы оценить распределение олигомеров, использовали HP 5890 серии II хроматограф и следующие условия хроматографирования:
Колонка: HP-1 (сшитый метилсилоксан) толщина пленки=0,25 мкм, внутренний диаметр=0,25 мм, длина колонки=60 м (Hewlett Packard); температура испарителя: 325°С; температура детектора: 325°С; начальная температура: 40°С в течение 10 минут;программирование температуры со скоростью: 10,0°С/минута; конечная температура: 325°С в течение 41,5 минут; внутренний стандарт н-гексилбензол.
Выход олефинов С4-С30 определяли с помощью ГХ анализа. Данные ЯМР получали при комнатной температуре на приборе VARIAN от 300 МГц до 400 МГц.
Катализатор, используемый для описанных ниже экспериментов по олигомеризации, представлял собой комплекс хлорида железа [II] с 2-[1-(2,4,6-триметилфенилимино)этил]-6-[1-(4-третбутилфенилимино)этил]пиридином, который получали, следуя способу, изложенному в WO02/28805, и который имел формулу, представленную ниже:

Альтернативный катализатор, используемый в описанных ниже экспериментах по олигомеризации, представлял собой комплекс хлорида железа [II] с 2,6-бис[1-(2, 6-дифторфенилимино)этил]пиридином, который получали, следуя способу, изложенному в WO02/00339, и который имел формулу, представленную ниже:

Альтернативный катализатор, используемый в описанных ниже экспериментах по олигомеризации, представлял собой комплекс хлорида железа [II] с 2-[1-(2,4,6-триметилфенилимино)этил]-6-[1-(3,5-дитрет-бутилфенилимино)этил]пиридином, который получали, следуя способу, описанному ниже:
Получение 2-[1-(2,4, 6-триметилфенилимино)этил]-6-[1-(3,5-дитрет-бутилфенилимино)этил]пиридина

2-[1-(2,4,6-триметилфенилимино)этил]-6-ацетилпиридин (1,3 г, 4,64 ммоль), полученный, следуя способу, изложенному в WO02/28805, и 3,5-дитрет-бутиланилин (1 г, 4,87 ммоль) растворяли в 100 мл толуола. К полученному раствору добавляли 4 Å молекулярные сита. После стояния в течение 2 суток смесь отфильтровывали. Растворитель удаляли в вакууме. Остаток промывали метанолом и кристаллизовали из этанола. Выход 1,1 г (51%) 2-[1-(2,4,6-триметилфенилимино)этил]-6-[1-(3,5-дитрет-бутилфенилимино)этил]пиридина.
1Н-ЯМР (CDCl3) δ 8,43 (δ, 1Н, Py-Hm), 8,37 (д, 1H, Py-Hm), 7,87 (т, 1H, Py-Hp), 7,16 (т, 1H, ArH), 6,89 (с, 2H, ArH), 6,69 (д, 2H, ArH), 2,42 (с, 3H, Me), 2,29 (с, 3H, Me), 2,22 (c, 3H, Me), 2,01 (c, 6H, Me), 1,33 (c, 18H, But).
Получение комплекса хлорида железа [II] с 2-[1-(2,4,6-триметилфенилимино)этил]-6-[1-(3, 5-дитрет-бутилфенилимино)этил]пиридином

В инертной атмосфере раствор 400 мг диимина (0,855 ммоль) в 20 мл дихлорметана добавляли к 100 мг FeCl2 (0,789 ммоль) в 30 мл дихлорметана. Смесь перемешивали в течение 16 часов. Небольшое количество осадка удаляли центрифугированием. В раствор добавляли 40 мл пентана. Осадок голубого цвета отфильтровывали и сушили в вакууме. Выход 0,420 г (90%) комплекса железа.
1Н-ЯМР (Cl2 CDCDCl2, уширенные сигналы) δ 78,6 (1Н, Ру-Нm), 76,8 (1Н, Ру-Нm), 29,7 (1Н, Ру-Нр), 20,9 (3Н, Ме), 18,3 (6Н, Ме), 15,2 (2Н, ArH), 0,7 (18Н, But), -4,1 (3Н, МеС=N), -11,5 (1Н, ArH), -15,6 (2Н, о-ArH), -30,7 (3Н, МеС=N).
Альтернативный катализатор, используемый в описанных ниже экспериментах по олигомеризации, представлял собой комплекс хлорида железа [II] c 2-[1-(2,4,6-триметилфенилимино)этил]-6-[1-(4-эйкозанокси-3,5-дифенилфенилимино)этил]пиридином, который получали, следуя способу, описанному ниже:
Получение 4-гидрокси-3,5-дифенилацетанилида

К 4-гидрокси-3,5-дифениланилину (4 г, 15,3 ммоль) в 30 мл этанола добавляли 1,6 мл уксусного ангидрида. Реакционную смесь перемешивали в течение 16 часов. Полученную смесь выливали в воду. Продукт (6 г) розового цвета отфильтровывали, промывали водой, сушили и использовали без дальнейшей очистки.
1Н-ЯМР (CDCl3), (выборочные данные) δ,31 (с, ОН), 2,16 (с, Ме).
Получение 4-эйкозанокси-3,5-дифенилацетанилида

Смесь 4-гидрокси-3,5-дифенилацетанилида (6 г), 1-бромэйкозана и 10 г карбоната калия кипятили с обратным холодильником в ацетоне (70 мл) в течение 16 часов. Реакционную смесь выливали в воду. Продукт отфильтровывали, промывали водой и сушили. Кристаллизацией из пентана получали 7,2 г 4-эйкозанокси-3,5-дифенилацетанилид в виде белого твердого вещества.
1 Н-ЯМР (CDCl3), (выборочные данные) δ,13 (т, СН2О), 2,17 (с, Ме).
Получение 4-эйкозанокси-3,5-дифениланилина
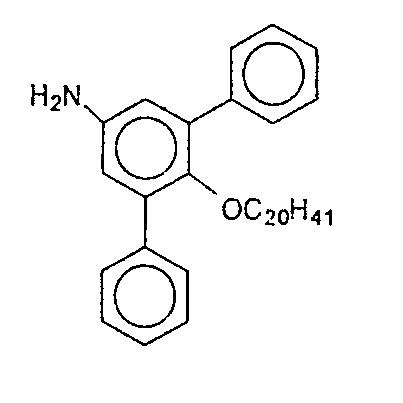
К 4-эйкозанокси-3,5-дифенилацетанилиду (7,2 г) добавляли 24 г NaOH в 30 мл H2O и 40 мл этанола. Полученную смесь кипятили с обратным холодильником в течение 16 часов. Реакционную смесь выливали на лед. Продукт отфильтровывали и промывали водой. Кристаллизацией из этанола получали 5,9 г (10,9 ммоль) 4-эйкозанокси-3,5-дифениланилин в виде белого твердого вещества.
1Н-ЯМР (CDCl3) δ 7,27-7,63 (м, 10H, ArH), 6,67 ( с, 2H, ArH), 3,60 (ушир. с, 2H, NH2), 3,09 (т, 2H, CH2O), 0,8-1,4 (м, 39H, алкил).
Получение 2-[1-(2,4,6-триметилфенилимино)этил]-6-[1-(4-эйкозанокси-3, 5-дифенилфенилимино)этил]пиридина

2-[1-(2,4, 6-триметилфенилимино)этил]-6-ацетилпиридин (3 г, 10,7 ммоль), полученный, следуя способу, изложенному в WO02/28805, и 4-эйкозанокси-3,5-дифениланилин (5,8 г, 10,7 ммоль) растворяли в 200 мл толуола. К полученному раствору добавляли 4 Å молекулярные сита. После стояния в течение 1 дня смесь отфильтровывали. Растворитель удаляли в вакууме. Остаток перекристаллизовывали из холодного этанола. Продукт выделяли в виде желтой вязкой жидкости (6,5 г, 8,1 ммоль, 76%) после сушки в вакууме при 60°С.
1Н-ЯМР (CDCl3) δ 8,45 (д, 1H, Py-Нm ), 8,37 (д, 1H, Py-Hm), 7,89 (т, 1H, Py-Hp), 7,67 (д, 4H, ArH), 7,1-7,5 (м, 16H, ArH), 6,90 (c, 2H, ArH), 6,86 (c, 2H, ArH), 3,19 (т, 2H, CH2O), 2,51 (c, 3H, Me), 2,29 (c, 3H, Me), 2,22 (c, 3H, Me), 2,01 (c, 6H, Me), 0,8-1,4 (м, 39H, алкил).
Получение комплекса хлорида железа [II] c 2-[1-(2,4, 6- триметилфенилимино)этил]-6-[1-(4-эйкозанокси-3,5-дифенилфенилимино)этил]пиридином

В инертной атмосфере раствор 5 г описанного выше диимина в 20 мл дихлорметана добавляли к 788 мг FeCl2 в 30 мл дихлорметана. Смесь перемешивали в течение 16 часов. Раствор фильтровали. Растворитель удаляли в вакууме. Полученный зеленовато-голубой продукт промывали пентаном, отфильтровывали и сушили в вакууме. Выход 5 г (86%) комплекса железа.
1Н-ЯМР (CD2Cl2, широкие сигналы, выборочные данные) δ 81,4 (1Н, Ру-Нm), 80,5 (1Н, Ру-Нm), 21,1 (3Н, Ме), 17,3 (6Н, Ме), 16,0 (2Н, ArH), 0, 21 (3Н, Ме), -13,8 (2Н, ArH), -30,4 ( 3Н, Ме).
Альтернативно, когда любые каталитические соединения, полученные в WO 02/28805, WO 02/00339, WO 01/58874 или WO 03/011876, могут быть использованы для экспериментов по олигомеризации, представленных ниже.
Первым соединением сокатализатором, использованным в описанных ниже экспериментах, был модифицированный метилалюмоксан (ММАО), в котором около 25% метильных групп замещены на изобутильные группы. ММАО-3А в гептане ([Al]=6,42% мас.), который использовали в примерах 1-19 таблицы 1, был закуплен у AKZO-NOBEL Chemical B. V., Amersfoort, The Netherlands. В экспериментах в автоклаве на 0,5 литра (позиция 20 и выше в таблице 1) используемый метилалюмоксан (МАО) в толуоле был поставлен торговой фирмой Eurecen AL 5100/10T, партия: B7863; [Al]=4,88% мас. TMA 35,7% мас. (вычислено), молекулярная масса=900 г/моль, и [Al]=4,97% мас. был поставлен Witco Gmbh, Bergkamen, Germany.
Вторым сокатализатором, использованным в описанных ниже экспериментах по олигомеризации, был чистый диэтилцинк, поставленный Ethyl Corporation, Baton Rouge, LA, U.S.A.
Получение каталитической системы
В сухой камере Braun MB 200-G помещали комплекс хлорида железа [II] с 2-[1-(2,4, 6-триметилфенилимино)этил]-6-[1-(4-третбутил-фенилимино)этил]пиридином, или
комплекс хлорида железа [II] с 2,6-бис[1-(2,6-дифторфенилимино)этил]пиридином, или
комплекс хлорида железа [II] с 2-[1-(2,4,6-триметилфенилимино)этил]-6-[1-(3, 5-дитрет-бутилфенилимино)этил]пиридином, или
комплекс хлорида железа [II] c 2-[1-(2,4, 6-триметилфенилимино)этил]-6-[1-(4-эйкозанокси-3,5-дифенилимино)этил]пиридином,(обычно 22,5 мкмоль) помещали в стеклянную колбу, закрытую мембраной; добавляли толуол (обычно около 10 мл). Полученную смесь перемешивали в течение нескольких часов. Это приводило к образованию тонко распределенной окрашенной суспензии. В случае комплекса хлорида железа [II] c 2-[1-(2,4, 6-триметилфенилимино)этил]-6-[1-(4-эйкозанокси-3,5-дифенилфенилимино)этил]пиридином в толуоле сразу получали прозрачный темно-зеленый раствор. Часть полученной суспензии или раствора использовали в реакции олигомеризации.
Эксперименты по олигомеризации с использованием устройства Edeavor
Эксперименты по олигомеризации были проведены с использованием устройства Endeavor® (Argonaut Technologies), содержащего восемь независимо нагреваемых и с независимо устанавливаемым давлением реакторов из нержавеющей стали объемом 20 мл. Каждый реактор был оборудован стеклянной втулкой, мешалкой и отверстием для ввода пробы.
Для того, чтобы удалить следы воды из реактора, его три раза промывали сухим азотом при температуре 150°С. Затем реактор промывали этиленом при комнатной температуре. Потом 2 мл толуола с соответствующим количеством ММАО и Et2Zn (таблица 1) были добавлены через отверстие для ввода пробы реактора. Реактор нагревали до желаемой температуры (таблица 1) и заполняли этиленом до давления, указанного в таблице 1. Суспензию комплекса железа вводили через отверстие для ввода пробы (обычное количество: 0,45 мкмоль в 0,2 мл толуола). Перемешивание 500 об/мин продолжалось при постоянном давлении этилена, по меньшей мере, в течение 2 ч. После этого периода подачу этилена перекрывали, перемешивание прекращали, и реактор автоматически охлаждался. После охлаждения до комнатной температуры этилен выдували воздухом и н-гексилбензол (45 мг, внутренний стандарт) в 0,2 мл толуола добавляли через отверстие для ввода пробы реактора к сырому продукту. Стеклянную втулку удаляли из реактора. Количество и чистоту олефинов определяли с помощью газовой хроматографии. Данные представлены в таблице 1.
Эксперименты по олигомеризации в автоклаве объемом 0,5 литра
Эксперименты по олигомеризации проводились в автоклаве объемом 0,5 литра, снабженном оболочкой для охлаждения, нагрев/охлаждение баней (Julabo, model no ATS-2) и турбинной/газовой мешалкой и перегородками.
Для удаления следов воды из реактора его оставляли в течение ночи в вакууме <10 Па при температуре 70°С. Реактор очищали введением 250 мл толуола, МАО (0,3 г раствор) и последующим перемешиванием при 70°С в атмосфере азота при давлении 0,4-0,5 МПа в течение 30 мин. Содержимое реактора удаляли с помощью вентиля в основании автоклава. Откачку реактора проводили до 0,4 кПа, загружали 125 мл толуола и нагревали до температуры, указанной в таблице 1 ( позиция 20 и выше) и заполняли этиленом до давления, указанного в таблице 1.
Раствор МАО (обычно 140 мг) и диэтилцинк (обычно 10 мг) затем добавляли в реактор с помощью толуола (суммарный объем введенной смеси составлял 30 мл при использовании методики, аналогичной вводу раствора катализатора; смотри ниже) и перемешивание со скоростью 800 об/мин продолжали в течение 30 минут.
0,40 мкмоль каталитической системы, полученной как описано выше, вводили в реактор при перемешивании, используя систему ввода с помощью толуола (суммарный введенный объем составлял 30 мл: вводили раствор катализатора, разбавленного толуолом до 10 мл, и систему ввода дважды промывали 10 мл толуола).
Добавление каталитической системы приводило к подъему температуры (обычно 5-25°С), который обычно достигал максимума в пределах 1 минуты и за которым обычно следовало установление температуры и давления, указанных в таблице 1 (позиция 20 и выше).
После поглощения определенного объема этилена олигомеризацию прекращали, быстро перекрывая подачу этилена, и смесь продуктов декантировали в сборную колбу, используя вентиль в основании автоклава. Контакт смеси с воздухом приводил к быстрой дезактивации катализатора.
После добавления к сырому продукту н-гексилбензола (0,5-3,5 г) как внутреннего стандарта количество и чистоту олефинов С6, С8 и С10определяли с помощью газовой хроматографии. Данные представлены в таблице 1 (позиция 20 и выше).
Из экспериментальных данных, представленных в таблице 1, можно видеть, что имеется ряд преимуществ от замены некоторого количества ММАО и МАО сокатализатора диэтилцинком. Наблюдается значительное увеличение селективности линейных альфа олефинов (измеренное в % чистоты вещества), а количество нежелательных (метил-)разветвленных побочных продуктов уменьшается. В то время как селективность по линейным альфа олефинам увеличивается, суммарный выход олефинов остается, по меньшей мере, равным суммарному выходу, полученному в экспериментах без добавления диэтилцинка, как это ясно из выхода С6,С8 и С10олигомеров (количество С6, С8 и С10 продуктов измеряли в мг) в позициях 1-19 таблицы 1.
Эксперименты, проведенные в устройстве Endeavor с использованием 0,45 мкмоль комплекса хлорида железа [II] с 2-[1-(2,4,6-триметилфенилимино)этил]-6-[1-(4-трет-бутилфенилимино)этил]пиридином или в автоклаве емкостью 0,5 литра (позиция 20 и выше) с использованием 0,40 мкмоль альтернативных Fe-каталитических систем.
Таблица 1


*) Сравнительный эксперимент.
**) Использованиекомплекса хлорида железа [II] с 2,6-бис[1-(2, 6-дифторфенилимино)этил]пиридином.
***) использование МАО вместо ММАО
#) полностью разветвленные децены.
##) использование комплекса хлорида железа [II] с 2-[1-(2,4,6-триметилфенилимино)этил]-6-[1-(3,5-дитрет-бутилфенилимино)этил]пиридином.
S) использование растворимого комплекса хлорида железа [II] c 2-[1-(2,4, 6-триметилфенилимино)этил]-6-[1-(4-эйкозанокси-3,5-дифенилфенилимино.
Реферат
Настоящее изобретение относится к каталитическим системам для олигомеризации этилена в линейные альфа-олефины с высоким выходом и очень высокой селективностью и способу получения упомянутых линейных альфа-олефинов. Каталитическая система содержит: (а) один или несколько катализаторов на основе бисарилиминопиридина железа или кобальта; причем упомянутые бисарилиминопиридиновые комплексы содержат бисарилиминопиридиновые лиганды общей формулы:

(b) первое соединение сокатализатор, которое выбрано из алкилов алюминия, алюмоксанов или их смесей; (с) второе соединение сокатализатор, которое содержит одно или несколько соединений формулы ZnR'2, в которой каждый R', который может быть одинаковым или разным, выбран из водорода, необязательно замещенного С1-С20 углеводорода, фенила, Cl, Br, I, SR'', NR''2, OH, OR'',CN, NC, в котором R'', который в той же молекуле может быть одинаковым или разным, является С1 -С20 углеводородом. Способ получения альфа-олефинов заключается в реагировании этилена в условиях олигомеризации в присутствии эффективного количества указанной каталитической системы. 2 н. и 18 з.п. ф-лы, 1 табл.
Формула

Комментарии