Дегидрирование алканов до алкенов - RU2692254C2
Код документа: RU2692254C2
Чертежи





Описание
Настоящее изобретение относится к способу дегидрирования алканов до алкенов, в первую очередь, дегидрирования этана, пропана и бутана до соответствующих алкеновых продуктов (олефинов) - этилена, пропилена и бутилена. Настоящее изобретение также относится к дегидрированию алкенов до соответствующего ненасыщенного химического соединения. В частности, настоящее изобретение также относится к дегидрированию алкилбензола до соответствующих ненасыщенных химических соединений, в первую очередь, дегидрированию этилбензола до стирола. Более конкретно, это дегидрирование проводится каталитически путем контактирования алканов, алкенов или алкилбензола с сульфидом металла (MeS) в присутствии сероводорода (H2S), однако при этом сероводород (H2S) не образуется, и в процессе в качестве газа-носителя не используется водяной пар. Вместо водяного пара в качестве газа-носителя используются или могут использоваться газы-носители, имеющие более высокое соотношение теплоемкости и теплоты испарения и которые образуются в процессе.
Современное уровень техники в промышленных процессах дегидрирования алканов представляют собой высокотемпературные процессы, обычно работающие при температуре выше 500°С, и во всех случаях также идущие при низком давлении процессы, исходящие из того факта, что реакция дегидрирования AH2=А+Н2 является эндотермической, требующей около 120 кДж/моль, и включает в себя образование количества моль продукта, большего, чем реагентов. Таким образом, как повышение температуры, так и низкое давление приводят к более высокой конверсии. А представляет собой ненасыщенное соединение и в качестве такового является высокореакционноспособным. Дегидрирование алканов обычно осуществляется без разбавителей или с водородом в качестве разбавителя. Для дегидрирования этилбензола при производстве стирола текущий уровень техники промышленных процессов осуществляется с использованием промотированного катализатора из оксида железа и с водой/водяным паром в качестве газа-носителя (разбавителя) и средства для подавления образования углерода.
Одной из нежелательных реакций при дегидрировании является образование углерода, который приводит к быстрой деактивации катализатора. Таким образом, в отдельных случаях применения может быть необходима частая регенерация. Образование углерода является проблемой не только для катализатора. Материал, используемый для реактора дегидрирования и для трубопроводов, приходится выбирать внимательно, обычно с использованием весьма дорогостоящих сплавов, чтобы избежать повреждения от углерода, приводящего к катастрофической форме коррозии, известной как металлическое запыливание.
Использование сульфидов металлов для дегидрирования алканов известно в технике. Например, известно, что для дегидрирования изобутана используют катализаторы из сульфидированного металла на носителе из диоксида кремния, в которых металл представляет собой (Zn), (Cu) или (Mn), (Mo), (Fe), (Со), (Ni). Однако эти сульфиды металлов демонстрируют низкую устойчивость, поскольку в противном случае высокая каталитическая активность обычно имеет тенденцию быстро спадать в процессе дегидрирования.
Патент US 3,787,517 раскрывает окислительное дегидрирование парафинов, при котором парафин (алкан) вступает в реакцию с карбонилсульфидом (COS) в качестве окислителя и в присутствии катализатора из тяжелых металлов на носителе, таком как железо на диоксиде кремния. Также раскрывается конверсия этилбензола в стирол согласно данному способу.
Заявка на патент US 2004/0092784 раскрывает способ каталитического превращения алканов в алкены путем реакции алкана с серосодержащим соединением в присутствии катализатора из сульфида металла, однако при получении сероводорода в процессе, то есть, при образовании сероводорода в качестве продукта реакции.
Патент US 3,787,517 раскрывает применение смешанного катализатора из оксида/сульфида основного металла для производства стирола из толуола в результате окислительного соединения с метаном, причем избегают использования этилбензола в качестве подаваемого сырья и использования перегретого водяного пара, что является обычным в промышленном производстве стирола.
Патент US 3,801,661 раскрывает дегидрирование неароматических алканов до алкенов при помощи катализаторов из сульфида металла, в котором присутствуют H2S и водяной пар, хотя и не в качестве дополнительных реагентов.
Патент US 4,420,649 раскрывает дегидрирование пригодных для дегидрирования углеводородов с использованием компонента пиролизованного карбонила рутения, компонента рения и компонента платиновой группы. Таким образом, этот катализатор является дорогостоящим и, кроме того, не предусмотрено использование сероводорода (H2S) в дегидрировании.
Заявка на патент US 2015/0018593 раскрывает катализаторы для превращения алканов с 2-4 атомами углерода в олефины, в котором катализаторами являются карбид металла, нитрид металла, силицид металла, фосфид металла, сульфид металла или их смеси, в сочетании со связующим средством, не обладающим свойствами кислоты Бренстеда, выбираемым среди AlPO4, бентонита, AlN и N4Si3. Использование сероводорода (H2S) в дегидрировании не предусмотрено.
Заявка на патент US 2014/0114107 раскрывает разновидность общепринятого способа дегидрирования этилбензола в присутствии водяного пара, в котором бензол и толуол подвергаются рециркуляции. Использование сероводорода (H2S) в дегидрировании не предусмотрено.
Катализаторы из сульфидов металлов являются хорошо известными для способов переработки нефти, таких как гидрообработка и так называемые процессы конверсии серосодержащих соединений и конверсии водяного газа. При этом данные способы обычно происходят при температурах в районе около 300°С, в то время как дегидрирование имеет место при температурах около 600°С. Таким образом, к устойчивости таких катализаторов предъявляются гораздо более жесткие требования, в частности, к термической устойчивости носителя, а также устойчивости сульфидного катализатора.
Таким образом, известный уровень техники содержит достаточное количество ссылок, в которых алканы или этилбензол дегидрируются с помощью катализаторов из сульфидов металлов в присутствии: серосодержащих соединений в форме COS или серосодержащих соединений, которые дают сероводород во время процесса дегидрирования, или которые дают SO2 во время процесса дегидрирования, или в которых дегидрирование проводится в присутствии сероводорода и водяного пара.
Использование водяного пара в процессе дегидрирования, хотя он не действует как реагент в дегидрировании, является нежелательным, поскольку водяной пар требует производства при помощи затратного по энергии испарения, и его приходится снова конденсировать в процессе. Теплота испарения не может быть полностью рекуперирована. Например, в современных способах превращения этилбензола в стирол к этилбензолу добавляется большое количество водяного пара, чтобы подавить образование углерода на катализаторе, разбавить газ, тем самым снижая парциальное давление этилбензола для благоприятствования равновесию и, наконец, обеспечить теплоту реакции, путем действия в качестве теплоносителя.
Следовательно, задачей настоящего изобретения является предоставить альтернативный способ дегидрирования алканов, алкенов или алкилбензолов до соответствующих ненасыщенных химических продуктов, который способен обеспечивать высокую устойчивость катализатора.
Другой задачей настоящего изобретения является предоставить альтернативный способ дегидрирования алканов, алкенов или алкилбензолов до соответствующих ненасыщенных химических продуктов, который является более простым и более энергетически эффективным, и который в то же самое время обеспечивает возможность сохранение высокой устойчивости катализатора.
Другой задачей настоящего изобретения является предоставить альтернативный способ дегидрирования алканов, алкенов или алкилбензолов, который является более дешевым, чем способы из известного уровня техники.
Эти и другие задачи решаются с помощью настоящего изобретения.
Неожиданно мы обнаружили, что металлические сульфидированные катализаторы (пассивированные серой катализаторы) могут дегидрировать алканы или алкилбензолы соответственно до алкенов, как, например, пропан до пропена и этилбензол до стирола, эффективно, с высокой устойчивостью и селективностью, если реакция дегидрирования проводится в присутствии небольших количеств H2S, даже без использования водяного пара в качества газа-носителя. В частности, в этом способе дегидрирования в качестве реагента не требуется никакого серосодержащего соединения в форме COS или SO2 или элементарной серы. Соответственно, в результате этого способа дегидрирования H2S не образуется.
Оказывается, что устойчивость катализатора из сульфида металла является функцией молярного соотношения H2S/H2. Поскольку мы имеем дело с возможными реакциями MeS+Н2=Me+H2S, причем Me, как правило, представляет собой Fe, Со, Ni, Mo, W, причем все являются потенциальными углеродообразующими агентами в углеводородных потоках, тогда как их сульфиды и их смеси являются катализаторами гидрирования/дегидрирования.
Ключевым элементом в существующих способах дегидрирования, и тем, который касается настоящего изобретения, является передача тепла в реакцию. В частности, в общепринятом способее получения стирола это осуществляется с использованием водяного пара в качестве газа-носителя. Реакция часто проводится с помощью 2-3 адиабатических каталитических слоев с повторным нагревом в промежутке между ними до 600-650°С.
Способ дегидрирования на основе сульфидов согласно настоящему изобретению предлагает другие существенные преимущества. Помимо исключения ненужного образования СО2 в результате парового риформинга, поскольку в способе отсутствует использование водяного пара, очень важным преимуществом является гибкость и улучшение энергетической эффективности в способе в результате использования в качестве газа-носителя, вместо водяного пара, ароматических углеводородов, образующихся во время процесса превращения этилбензола в стирол, таких как бензол или толуол. Они имеют очень высокую теплоемкость и являются очень устойчивыми с термической точки зрения. Более конкретно, соотношение теплоемкости/теплоты испарения для смеси бензол - толуол выше, чем для воды - водяного пара, таким образом, приводя к значительно более низкой потребности в нагревательной энергосреде, которая должна быть обеспечена путем сжигания дополнительного топлива в котельном агрегате. Хотя потребность в охлаждающей энергосреде возрастает, эта энергосреда имеет намного меньшую стоимость. Полученный в этом процессе газообразный водород легко отделить от остатка просто путем конденсации бензола, толуола, этилбензола и стирола. Конденсированный продукт направляют на перегонку, а бензол, толуол и этилбензол возвращают обратно в цикл.
Соответственно, изобретение в самом широком своем аспекте представляет собой способ дегидрирования алканов, алкенов или алкилбензолов с получением соответствующих ненасыщенных химических продуктов и водорода (H2), включающий приведение в контакт алкана, алкена или алкилбензола с катализатором на основе сульфида металла (MeS), в котором дегидрирование проводится в одном или нескольких реакторах дегидрирования без использования водяного пара (Н2О) в качестве газа-носителя для алканов, алкенов или алкилбензолов и в присутствии сероводорода (H2S), без образования H2S в качестве продукта реакции.
Таким образом, в отличие от известного уровня техники, настоящее изобретение избегает использования таких соединений как COS, которые приводят к получению H2S в качестве продукта в способе. Также предпочтительно, чтобы не происходило получение диоксида серы (SO2). Также, в отличие от известного уровня техники, нет необходимости использовать водяной пар в процессе в качестве газа-носителя при дегидрировании этилбензола до стирола.
Сульфиды металлов (MeS) также предпочтительно получаются посредством стадии предсульфидирования.
Используемые в данном документе термины «металлический сульфид» и «сульфид металла» используются взаимозаменяемо.
Используемое в данном документе термин «газ-носитель» означает газ, который вносит значительный вклад в разбавление реагента для поддержания термодинамического равновесия реакции дегидрирования, подавление образования углерода на катализаторе и обеспечение теплоты реакции, действуя в качестве теплоносителя. Соответственно, газ-носитель представляет собой газ, который по меньшей мере составляет 20% (в расчете на массу) подаваемого сырья, которое следует подвергнуть дегидрированию, такого как подаваемое сырье из алканов, алкенов или алкилбензола, или смеси этих соединений. Несколько газов-носителей могут быть объединены, чтобы образовать газ-носитель, так что газ-носитель в таком случае может составлять по меньшей мере 90% (в расчете на массу) подаваемого сырья, подвергаемого дегидрированию, предпочтительно по меньшей мере 100%, более предпочтительно, свыше 200%, то есть, общее количество газа-носителя по меньшей мере в 2 раза больше, чем подаваемого сырья, подвергаемого дегидрированию.
Термин «без использования водяного пара (H2O) в качестве газа-носителя» обозначает, что водяной пар составляет менее 10% (объемного расхода) от используемого газа-носителя, поскольку признают, что небольшие количества водяного пара могут переноситься или получаться в любом технологическом потоке. Например, водяной пар может составлять 0,5-10% от газа-носителя. Более конкретно, водяной пар может составлять даже менее 5% от газа-носителя, например 1-5% или 0,5-5%. В любом случае, основной вклад в разбавление реагента, для поддержания термодинамического равновесия реакции дегидрирования, подавления образования углерода на катализаторе и обеспечения теплоты реакции, действуя в качестве теплоносителя, обеспечивается не водяным паром. В конкретном варианте исполнения исходя из вышеуказанных или нижеследующих вариантов исполнения количество водяного пара в газе-носителе равно нулю или находится ниже определяемых пределов.
В одном конкретном варианте исполнения исходя из вышеуказанных или нижеследующих вариантов исполнения молярное соотношение сероводорода (H2S) к алканам, алкенам или алкилбензолам (в подаваемом сырье) находится между 0,01 и 0,2, предпочтительно 0,01-0,1. Следовательно, небольшие количества H2S используются в способе, в частности, на уровне частей на миллион по объему. В одном конкретном варианте исполнения молярное соотношение H2S к алканам или алкилбензолам составляет 0,02-0,05. Например, концентрация алканов, таких как пропан, может составлять 10%, в то время как H2S присутствует в количестве 2000 частей на миллион по объему.
В другом варианте исполнения в связи с одним из вышеуказанных или нижеследующих вариантов исполнения молярное соотношение сероводорода (H2S) к водороду (Н2) находится между 0,01 и 0,2, предпочтительно между 0,01 и 0,1, более предпочтительно, когда температура процесса дегидрирования составляет 600°С или выше. Это начальное молярное соотношение H2S к H2. Было обнаружено, что при поддержании H2S в таких пропорциях, таким образом, получая небольшие количества H2S в способе, теперь возможно поддерживать высокую устойчивость катализатора, так как катализаторы в процессе дегидрирования сохраняются в виде сульфидов металлов. Таким образом подавляется образование углерода, которое является основным двигателем дезактивации катализатора и сопутствующих нежелательных эффектов, таких как металлическое запыливание.
Присутствие H2S в процессе дегидрирования поддерживается с помощью проведения процесса в непрерывном режиме. Таким способом катализатор сохраняется в сульфидированном состоянии в виде MeS. Например, для Me=Со, применяется следующее уравнение реакции:

Для которого константа равновесия может быть рассчитана из уравнения Kp=0,004907*ехр(98105/Т).
Подаваемое в процесс сырье в форме алканов, алкенов или алкилбензолов, вместе с газом-носителем, отличающимся от водяного пара, объединяется с непрерывным потоком H2S, который является достаточно сильным, чтобы сохранять металл, в данном случае кобальт, в сульфидированном состоянии. Специалист поймет, что это количество H2S должно быть выше по сравнению с равновесной константой Kp при соответствующей температуре, которая предпочтительно является температурой на входе в реактор (реакторы) дегидрирования. Соответственно, начальное молярное соотношение H2S к Н2, например, на входе в реактор (реакторы) дегидрирования, будет поддерживаться примерно на таком же низком уровне в процессе дегидрирования и достаточно высоким, чтобы сохранять сульфид металла (MeS), несмотря на то, что в процессе дегидрирования образуется водород.
В частном варианте исполнения в связи с одним из вышеуказанных или нижеследующих вариантов исполнения молярное соотношение сероводорода (H2S) к водороду (Н2) составляет 0,05-0,06, например, 0,055. Опять-таки, это начальное молярное соотношение H2S к Н2. В этом конкретном диапазоне мы обнаружили неожиданно высокую степень конверсии и селективность, в частности, для производства стирола из этилбензола. Предпочтительно, температура составляет 600°С или выше, например, вплоть до 650°С или 700°С, а молярное соотношение сероводорода к этилбензолу составляет 0,05-0,06, например, 0,055. Предпочтительно, катализатор представляет собой СоМо-оксиды на носителе из MgAl2O4, где катализатор перед использованием был сульфидирован, то есть, предсульфидирован.
В другом варианте исполнения в связи с одним из вышеуказанных или нижеследующих вариантов исполнения металл (Me) металлического сульфида (MeS) выбирается из Fe, Со, Ni, Mn, Cu, Mo, W и их комбинаций. Предпочтительно, металл представляет собой комбинацию Со и Мо. Предпочтительно сульфиды металлов нанесены на носитель из оксида алюминия или шпинелей, таких как магний-алюминиевая шпинель (MgAl2O4).
В другом варианте исполнения в связи с одним из вышеуказанных или нижеследующих вариантов исполнения способ проводится при температурах в диапазоне 450-700°С, предпочтительно 500-650°С. Эти температуры обеспечивают надлежащие условия для эндотермических реакций дегидрирования.
Подаваемое сырье, подлежащее дегидрированию, состоит из алканов, алкенов, этил бензолов и их комбинаций. Предпочтительно подаваемое сырье является одним из алканов, алкенов или этилбензолов.
В другом варианте исполнения в связи с одним из вышеуказанных или нижеследующих вариантов исполнения алкан выбирается из этана, пропана, бутана, пентана и их комбинаций.
В другом варианте исполнения в связи с одним из вышеуказанных или нижеследующих вариантов исполнения алкен выбирается из этилена, пропилена, бутена, пентена и их комбинаций. Дегидрирование дает в результате соответствующий ненасыщенный химический продукт, например, пропадиен/пропин, когда алкен в подаваемом сырье является пропиленом.
В другом варианте исполнения в связи с одним из вышеуказанных или нижеследующих вариантов исполнения алкилбензол представляет собой этилбензол, а соответствующим ненасыщенным химическим продуктом является стирол.
В другом варианте исполнения в связи с одним из вышеуказанных или нижеследующих вариантов исполнения не вступившие в реакцию алканы, алкены, алкилбензолы и побочные продукты возвращают обратно в цикл, в один или несколько реакторов дегидрирования. Не вступившие в реакцию алканы и побочные продукты включают в себя метан, этан, этилбензол, бензол, толуол и их комбинации.
В частности, когда способ относится к дегидрированию этилбензола до стирола, в побочных реакциях получаются бензол и толуол. Поэтому, в другом варианте исполнения в связи с одним из вышеуказанных или нижеследующих вариантов исполнения бензол, толуол или комбинации их обоих используются в качестве газа-носителя. Благодаря очень высокой теплоемкости бензола и толуола, а также их термической устойчивости, их использование в способе в качестве газа-носителя вместо водяного пара обеспечивает огромные преимущества в том, что касается энергетической эффективности, то есть, имеется неожиданно резкое сокращение потребления энергии, выраженное в потребностях в нагревательной энергосреде.
В дополнение, побочная реакция, дающая бензол, также дает этилен, а побочная реакция дающая толуол, также дает метан. Этан также может получаться в этом способе в качестве побочного продукта. Поэтому, в другом варианте исполнения в связи с одним из вышеуказанных или нижеследующих вариантов исполнения метан, этан или комбинации их обоих используются в качестве газа-носителя. Эти соединения также имеют более высокие соотношения теплоемкости и теплоты испарения, чем водяной пар, и обеспечивает аналогичные преимущества в том, что касается энергетической эффективности.
В частности, в способе производства стирола путем дегидрирования этилбензола, полученный газообразный водород просто отделять от остальных продуктов (и побочных продуктов) при помощи простой конденсации бензола, толуола, этилбензола и стирола. Полезный водород может использоваться в качестве продукта, а не разбавителя, как в современных общепринятых способах дегидрирования, в то время как конденсированный продукт направляется на перегонку, а бензол, толуол и этилбензол подаются обратно в цикл в реакторы дегидрирования.
В другом конкретном варианте исполнения в связи с одним из вышеуказанных или нижеследующих вариантов исполнения дегидрирование проводится в адиабатических реакторах со стадией повторного подогрева и селективным окислением водорода, полученного в способе, в промежутке между реакторами. Этот вариант исполнения обеспечивает даже более высокую энергетическую эффективность. Селективное окисление водорода, полученного в первом реакторе, предпочтительно проводится над катализатором из благородного металла, таком как катализатор на основе платины (Pt).
В еще одном конкретном варианте исполнения в связи с одним из вышеуказанных или нижеследующих вариантов исполнения отходящий газ, содержащий H2 и CH4, полученный в способе, используется в качестве газа-носителя, а селективное окисление водорода проводится перед входом в первый реактор дегидрирования. Таким образом, селективное окисление водорода может проводиться перед входом в первый реактор дегидрирования и/или перед входом во второй реактор дегидрирования. В частности, во время получения стирола из этилбензола использование бензола-толуола и отходящего газа, содержащего H2 и CH4, полученных в способе, в качестве газов-носителей, совместно с использованием селективного окисления водорода перед входом в первый реактор дегидрирования и предпочтительно также в промежутке между реакторами (например, перед входом во второй реактор дегидрирования), приносит даже более высокую энергетическую эффективность. Использовать такую установку для селективного окисления перед входом в первый реактор дегидрирования не предполагается, поскольку водород не получали как таковой, и, следовательно, нет необходимости в такой установке, однако же в результате этого получается неожиданно более высокая энергетическая эффективность. Специалиста в данной области техники обычно отговаривали бы создавать установку селективного окисления перед входом в первый реактор дегидрирования. Типичные способы с использованием водяного пара в качестве газа-носителя требовали бы молярного соотношения водяного пара и этилбензола, составляющего 5-6. Используемый в цикле отходящий газ в сочетании с воздухом, использованным для окисления, поступают вдобавок к этому, что означает, что рециркуляционный компрессор должен сжимать до значительно более высоких давлений, чем в настоящем изобретении. Другими словами, то, что, казалось бы, дает вредное высокое потребление энергии, в настоящем изобретении оборачивается появлением существенного преимущества в энергетической эффективности.
Таким образом, простым и оригинальным образом обеспечивается способ, в котором не только катализатор остается устойчивым, то есть, отсутствует дезактивация в результате образовании кокса/углерода, тем самым обеспечивая катализатору функционирование в течение длительных периодов времени без регенерации, но этот способ превосходит и известный уровень техники с точки зрения энергетической эффективности, в частности, во время производства стирола из этилбензола.
Прилагаемые фигуры 1-4 служат для иллюстрации настоящего изобретения. Фиг. 1 соответствует Примеру 3 и показывает способ согласно известному уровню техники для превращения этилбензола в стирол, где в качестве газа-носителя используется водяной пар. Фиг. 2 соответствует Примеру 4 и показывает способ согласно настоящему изобретению, где этилбензол превращается в стирол, в котором газ-носитель представляет собой смесь бензола/толуола, и в этом способе также используется H2S. Фиг. 3 соответствует Примеру 5 и показывает способ согласно известному уровню техники для превращения этилбензола в стирол, где в качестве газа-носителя используется водяной пар и где проводится селективное окисление водорода, полученного в первом реакторе. Фиг. 4 соответствует Примеру 6 и показывает способ согласно настоящему изобретению, где этилбензол превращается в стирол, в котором газ-носитель представляет собой смесь бензола/толуола, также в этом способе используется H2S, и проводится селективное окисление водорода, полученного в первом реакторе. Фиг. 5 соответствует Примеру 7 и показывает способ согласно настоящему изобретению, где этилбензол превращается в стирол, в котором газ-носитель представляет собой смесь бензола/толуола и рециркулирующего отходящего газа, содержащего Н2 и CH4, также в этом способе используется H2S и проводится селективное окисление перед первым и вторым реактором.
Пример 1 - Согласно изобретению
Дегидрирование этилбензола
Использованный катализатор состоял из СоМо-оксидов, нанесенных на носитель из MgAl2O4, причем этот катализатор был перед использованием сульфидирован, то есть, предсульфидирован. Загруженное в реактор количество составляло 10 г катализатора, смешанного с 10 г инертного материала, также состоящего из носителя из MgAl2O4 (шпинели).

Зона загрузки в реакторе составляла от 635 мм до 244 мм от верхнего фланцевого соединения. Общий расход составлял около 48 Нл/ч на всем протяжении испытательного периода дегидрирования этилбензола. Давление составляло 3 бар изб., что является минимальным давлением, при котором эксперимент мог проводиться с использованием данных установок. Неселективными продуктами были бензол, толуол, метан, этан и этилен. В качестве газа-носителя использовали азот. Сероводород добавляли из смеси сероводород/водород, таким образом, добавляя водород. Излишек водорода может приводить к увеличенному крекингу, помимо ограничения конверсии, которая является относительно близкой к расчетному равновесному значению. Использовали лишь небольшие количества H2S, если измерять с помощью молярного (объемн.) соотношения H2S/H2, и в отсутствие водяного пара. Как показано в Таблице 1, высокие степени конверсии по стиролу (близкие к равновесному значению) и высокие селективности по стиролу получаются без образования углерода на катализаторе. Особенно высокие степень конверсии и селективность получаются при более высоких температурах, что ожидаемо, поскольку реакция является эндотермической, еще неожиданны высокая степень конверсии и селективность, если значение H2S/H2 находится, в частности, в диапазоне 0,05-0,06, а именно, в данном случае 0,054 (третья от конца строчка в Таблице 1). Молярное соотношение сероводорода (H2S) к водороду (Н2) представляет собой начальное молярное соотношение, а не после того, как реакция была осуществлена.
Пример 2 - Согласно изобретению
Дегидрирование пропана
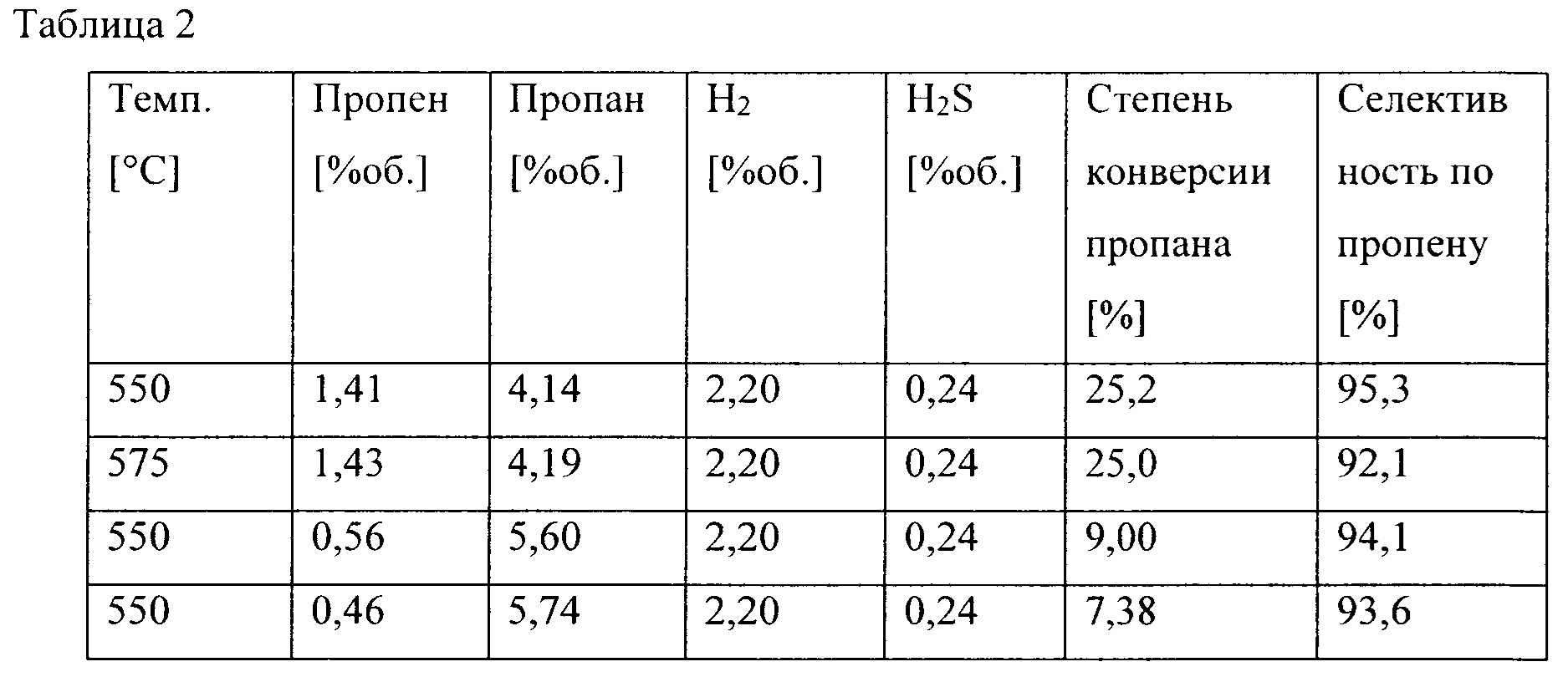
Дегидрирование пропана проводилось на том же катализаторе, что и дегидрирование этилбензола в Примере 1. Условия в отношении давления и азота в качестве разбавителя, а также добавления смеси водорода и сероводорода для сохранения катализатора в сульфидированном состоянии, были теми же самыми. Обнаруженные побочные продукты представляли собой метан, этан и этилен. Меркаптаны не обнаруживались. Как показано в Таблице 2, могут быть получены степени конверсии, близкие к равновесным, и высокие селективности. Образование углерода на катализаторе не было обнаружено.
Пример 3 - Согласно уровню техники
Классический способ получения стирола
Стирол производится в очень больших количествах по всему миру и используется во множестве продуктов. Преобладающий на сегодня способ основан на каталитическом дегидрировании этилбензола с использованием катализатора на основе железа.
Фиг. 1 показывает типичную технологическую схему. Фигуры в этой заявке на патент представлены без детализированной теплообменной схемы, например, потоки, подлежащие нагреванию и охлаждению, делятся на удобные сегменты, где нагревание и охлаждение проводят до точек росы или начала кипения, чтобы обеспечить входные данные для пинч-анализа. Пинч-анализ дает ответы на то, какой будет минимальная потребность в нагревательной и охлаждающей энергосреде, обеспечивающая предварительно заданный минимальный перепад температур на входе и выходе в теплообменной сети. Во всех случаях использовался минимальный перепад температур на входе и выходе, равный 20°С (Примеры 3-7).
На Фиг. 1 этилбензол 1 смешивают с водяным паром 2 для образования смешанного подаваемого потока 3 и предварительно нагревают до температуры на входе в первый реактор 20, составляющей 645°С. В результате реакции температура на протяжении первого реактора адиабатически снижается до 542°С. Вытекающий поток 4 из реактора 20 повторно нагревается до 645°С, прежде чем входит во второй реактор 30, из которого выходящий поток 5 выходит при 600°С. Он охлаждается до 20°С перед разделительным устройством 40, где вода декантируется, а сырая смесь стирола/бензола/толуола 6 совместно с не вступившим в реакцию этилбензолом отделяется. Оставшиеся следы ароматических соединений 7 улавливаются с помощью цеолитов или тому подобного в установке 50 и добавляются к потоку сырого стирола 6. Отходящий газ 8, состоящий главным образом из водорода, метана, этилена и диоксида углерода, сжимается до давления, слегка превышающего давление окружающей среды, и используется в качестве топлива 9.
Поток сырого стирола направляется в секцию перегонки 60, где получается продукт - стирол 10. Первая колонна (не показана) отделяет бензол/толуол от этилбензола/стирола, а вторая колонна (не показана) отделяет этилбензол от стирола. Конечную очистку стирола и разделение бензола/толуола не включали в сравнение способов, поскольку они принимаются как идентичные во всех случаях.
Степень конверсии этилбензола в стирол фиксировалась при 70% путем варьирования содержания водяного пара, что выражалось в соотношении водяного пара и углерода около 1 или массовом соотношении водяного пара и масла около 1,4, как это обычно выражается в промышленном производстве стирола.
Потери этилбензола в результате побочных реакций, где этилбензол соответственно превращается в бензол, этилен и в толуол, метан рассчитываются путем преобразования 2% стирола в этилен и бензол и 3% в толуол и метан.
Все расчеты выполнялись при получении 100 метрических тонн в час стирола, выходящего из разделительной колонны для этилбензола/стирола второй перегонной колонны.
Результат пинч-анализа процесса показан в Таблице 3. Потребность в нагревательной энергосреде составляет 307 МВт (сравнительная потребность в нагревательной энергосреде = 100).
Пример 4 - Согласно изобретению
Новый способ получения стирола
В этом примере две другие функции водяного пара, а именно, разбавление реакционной смеси и подведение тепла, исполняются в результате рециркуляции смеси бензола/толуола, то есть, смесь бензола/толуола используется в качестве газа-носителя. Этот поток может получаться путем возвращения обратно в цикл из колонн для отделения продукта, то есть, первой перегонной колонны.
Этот способ иллюстрируется с помощью Фиг 2.
Возвращенный в цикл поток бензола/толуола 2 вместо водяного пара добавляется к свежему и возвращенному в цикл этилбензолу 1 совместно с достаточным количеством H2S в потоке 11, чтобы сохранять сульфид катализатора на всем протяжении реакторной линии согласно уравнению

Для которого константа равновесия может определяться из соотношения Kp=0,004907*ехр(98105/Т).
Следовательно, подаваемый в первый реактор поток содержит этилбензол, небольшое количество H2S и бензол/толуол в качестве газа-носителя. Сероводород регенерируется в виде потока 12 после регенерации бензола/толуола 50.
Результат пинч-анализа процесса в Таблице 3 показывает, что потребность в нагревательной энергосреде составляет только 278 МВт или примерно на 9% меньше, чем у способа из Примера 4 (из уровня техники).
Пример 5 - Согласно уровню техники
Улучшенный классический способ получения стирола
В улучшенной версии классического способа (Пример 3, Фиг. 1) повторное нагревание между двумя реакторами обеспечивается с помощью селективного окисления части водорода, полученного в первом реакторе, в установке 70 с использованием воздуха 13, над катализатором из благородного металла. Фиг. 3 иллюстирует этот подход. Результат пинч-анализа (Таблица 3) показывает, что эта конфигурация процесса снижает потребность в нагревательной энергосреде до 263 МВт, что является существенным улучшением в сравнении с классическим способом из Примера 3 (энергетическая эффективность на 14% лучше, со 100 до 86 в пересчете на сравнительную потребность в нагревательной энергосреде), в частности, потому, что среда, использованная для повторного нагревания между двумя реакторами в Примере 3, представляет собой водяной пар, перегретый до очень высокой температуры, вплоть до 890°С, что, однако также требует для конструкции дорогих высоколегированных сталей.
Пример 6 - Согласно изобретению
Новый способ получения стирола с селективным окислением водорода
В этом варианте исполнения селективное окисление водорода 70 с использованием воздуха 13 в промежутке между реакторами дегидрирования сочетается с рециркуляцией бензола/толуола в качестве газа-носителя 2 и добавлением небольших количеств H2S в поток 11 согласно изобретению. Это проиллюстрировано на Фиг. 4. Результат пинч-анализа в Таблице 3 показывает неожиданно более высокий эффект для энергетической эффективности, дающий улучшение примерно на 23 процента (с 278 МВт до 214 МВт потребности в нагревательной энергосреде). Ожидаемый результат улучшился бы на 14% относительно способов из известного уровня техники, как описано в Примере 5.
Пример 7 - Согласно изобретению
Новый способ получения стирола с селективным окислением водорода перед обоими реакторами Даже более хорошая энергетическая эффективность достигается также в результате внедрения возврата отходящего газа обратно в цикл, в первый реактор. Принцип проиллюстрирован на Фиг. 5. Рециркулирующий отходящий газ 14, состоящий преимущественно из Н2, CH4 и N2, также служит в качестве разбавителя и теплоносителя, однако также используется небольшое количество бензола/толуола 2. Также перед входом в первый реактор 20 добавляется установка селективного окисления 70. Результат пинч-анализа в Таблице 3 показывает, что потребность в нагревательной энергосреде снижается на всем протяжении, до 186 МВт и составляет на 29% меньше потребности в нагревательной энергосреде улучшенного способа из уровня техники из Примера 5 (потребность в нагревательной энергосреде 263 МВт). Потребность в энергии для сжатия увеличивается с 1 до 8,5 МВт, однако преимущества в энергетической эффективности все еще являются неожиданно высокими.
Результаты расчетов обобщаются в Таблице 3:

Преимуществами способа согласно изобретению с использованием пассивированного серой катализатора дегидрирования, среди прочих, являются:
A) Потребность в нагревательной энергосреде, которая должна быть обеспечена за счет сжигания дополнительного топлива в котельном агрегате, значительно ниже, если в качестве газа-носителя избегают использования водяного пара, а вместо него используют смесь бензола/толуола.
B) Если внедряется рециркуляция отходящего газа и селективное окисление водорода (Прим. 7), потребность в нагревательной энергосреде снижается даже более значительно и составляет почти на 40% (Прим. 3) или на 29% меньше, чем в способах из уровня техники, Прим. 3 и Прим. 5 соответственно.
Реферат
Предложен способ дегидрирования алканов или алкилбензолов до соответствующих алкенов и водорода (Н), включающий приведение в контакт алкана или алкилбензола с катализатором на основе сульфида металла (MeS), в котором дегидрирование проводят в одном или нескольких реакторах дегидрирования в присутствии сероводорода (HS) без образования HS в качестве продукта реакции, водяной пар (HO) составляет менее 10% (объемного расхода) от используемого газа-носителя для алканов или алкилбензолов, молярное соотношение сероводорода к алканам или алкилбензолам находится между 0,01 и 0,2, молярное соотношение сероводорода (HS) к водороду (Н) находится между 0,01 и 0,2, и либо бензол, толуол или комбинации их обоих, либо метан, этан или комбинации их обоих используют в качестве газа-носителя. Технический результат - обеспечение высокой устойчивости катализатора. 6 з.п. ф-лы, 5 ил., 3 табл., 7 пр.

Комментарии