Способ получения композиции с использованием спирта в качестве исходного вещества - RU2467057C2
Код документа: RU2467057C2
Описание
Область техники
[0001]
Настоящее изобретение относится к способу получения композиций, содержащих органические соединения и пригодных в качестве химического промышленного материала или топливной композиции с использованием спирта, например этанола, в качестве исходного вещества.
Предшествующий уровень техники
[0002]
Бензин представляет собой жидкую нефтяную фракцию, которая является летучей в диапазоне точки кипения приблизительно 30-200°С. С точки зрения состава бензин является смесью углеводородов с 4-12 атомами углерода (см. непатентный документ 1). Соединенные Штаты Америки, которые являются самым большим в мире потребителем бензина, в 2004 году расходовали приблизительно 380 миллионов галлонов (1436,4 миллиона литров) в день, и этот расход составляет 40% или более мирового потребления бензина (см. непатентный документ 2). Бензин имеет очень большое влияние на экономику и энергетическую стратегию каждой страны, хотя и по-иному, чем в Соединенных Штатах Америки. В настоящее время бензин синтезируют из нефти, и большую важность представляет собой проблема будущего истощения запасов нефти (энергетическая безопасность). Кроме того, распространенность автомобилей как признак цивилизации считается основной причиной глобального потепления из-за выбросов диоксида углерода в результате массового расхода ископаемых топлив, и необходимо снизить выбросы диоксида углерода. Чтобы справиться с этой ситуацией, производители автомобилей разработали гибридные автомобили, автомобили с гибким выбором топлива, автомобили на топливных элементах, электромобили и т.д., среди которых гибридные автомобили и автомобили с гибким выбором топлива уже проникли на рынок, несмотря на их довольно высокие цены.
[0003]
С другой стороны, технология синтеза бензина из метанола с использованием цеолита в качестве катализатора, разработанная Мобил Корпорейшн (MTG), технология синтеза жидких топлив из синтез-газа (GTL) и подобное известны как синтетические технологии для нового типа топлив (см. непатентные документы 3-5). Метанол, материал MTG, в настоящее время синтезируют главным образом из природного газа, то есть из ископаемых ресурсов. Синтез-газ, как материал GTL, получают из природного газа и биомассы, но сжиженное топливо является альтернативным топливом для легкой нефти и не может использоваться непосредственно для автомобилей с бензиновым двигателем.
[0004]
Газовый двигатель, четырехтактный двигатель, дизельный двигатель, реактивный двигатель и т.д. хорошо известны в качестве двигателя внутреннего сгорания, т.е. устройства для выработки энергии. Текущая ситуация и проблемные вопросы, касающиеся четырехтактного двигателя, являются следующими. Этанол, бутанол, метил-трет-бутиловый эфир (МТБЭ) и этил-трет-бутиловый эфир (ЭТБЭ) известны в качестве добавок к бензину в четырехтактном двигателе (см. непатентные документы 6-10). Когда этанол добавляют к бензину, существующие автомобили с бензиновым двигателем считаются свободными от влияния этанола, если количество добавленного этанола составляет приблизительно до 10%. Поэтому бензин, содержащий 10% этанола, продается в Соединенных Штатах Америки как бензоспирт (Е10).В Бразилии общеупотребительный бензин содержит уже 22-26% этанола. Бензин, содержащий около 85% этанола (Е85), и топлива из 100% этанола требуют специализированных автомобилей. Этанол, однако, имеет более низкую теплотворную способность по сравнению с бензином, и сообщалось, что потребление топлива Е10 и Е85 ниже, чем бензина. Кроме того, смешение с водой приводит к отделению слоев топлива в бензине, смешанном с этанолом, что считается причиной повреждения двигателя. МТБЭ использовался во всем мире в 1980-х как средство контроля оксидов азота NOx в выхлопных газах и в качестве увеличителя октанового числа, который был заменителем известного тетраэтилсвинца. Однако в Соединенных Штатах Америки выявлено, что МТБЭ является веществом, загрязняющим подземные воды, и все больше штатов приходят к тому, что запрещают использование МТБЭ. По-видимому, МТБЭ будет полностью запрещен в ближайшем будущем. ЭТБЭ синтезируют из этанола и изобутилена, и в настоящее время он преобладает главным образом в Европе в обоих аспектах: как заменитель МТБЭ и как добавка к топливу, имеющая растительное происхождение. Однако изобутилен - одно из исходных веществ для ЭТБЭ - получают из нефти, так что он не отвечает требованиям мер против глобального потепления, и проблемы экологической безопасности и стоимости производства остаются.
[0005]
Предполагается, что объем производства этих новых типов автомобилей и новых топлив в будущем будет увеличиваться. С другой стороны, существующие в настоящее время автомобили с бензиновым двигателем, без сомнения, останутся на рынке в следующие 20 лет или около того. Соответственно, желательно разработать заменяющие топлива, которые подходят к этим существующим автомобилям с бензиновым двигателем.
[0006]
С другой стороны, в качестве способа синтеза высокооктанового топлива с использованием этанола как исходного вещества предлагается способ с использованием гидроксиапатитового катализатора, в котором на поверхности катализатора регулируют твердую кислоту и основность (см. патентный документ 1). В этом способе, однако, молярное отношение фосфора и кальция в катализаторе требует тщательного регулирования. Поэтому была проблема в трудности приготовления катализатора. Кроме того, полученное топливо имеет недостаточную устойчивость к окислению и образует много смол.
[0007]
[Патентный документ 1] WO 99/38822
[Непатентный документ 1] Gasoline Blending Streams Test Plan, Submitted to US EPA by The American Petroleum Institute Petroleum HPV Testing Group, AR201-13409A, 2001.
[Непатентный документ 2] Motor Fuels Understanding the Factors That influence the Retail Price of Gasoline, the United States Government Accountability Office, GAO-05-525SP, May 2005.
[Непатентный документ 3] Meisel L.S., McCullough P.J., Lechthaler Н/ С/ and Weisz, B.P. Gasoline from methanol in one step. Chemtech 1976, February, 86-89.
[Непатентный документ 4] Maiden J.С.. The New Zealand Gas-to-Gasoline Project, Methane Conversion, Elsevier Science Publishers В.V., Amsterdam, 1988, 1-16.
[Непатентный документ 5] Baker G.B. And Clark J.N. Synthesis Gas to Motor Fuel via Light Alkenes, Methane Conversion, Elsevier Science Publishers В.V., Amsterdam, 1988, 497-501.
[Непатентный документ 6] Demirbas A. Progress and recent trends in biofuels. Progress in Energy and Combustion Science, 2007, 33, 1-18.
[Непатентный документ 7] Ancillotti F. and Fattore V. Oxygenate fuels: Market expansion and catalyst aspect of synthesis. Fuel Processing Technology, 1998, 57, 163-194.
[Непатентный документ 8] Malca J. And Freire F.Renewability and life-cycle energy efficiency of bioethanol and bio-ethyl tertiary butyl ether (bioETBE): Assessing the implications of allocation. Energy, 2006, 31, 3362-3380.
[Непатентный документ 9] Snelling J., Curtis W.C. And Park Y-K. Synthesis of higher carbon ethers from olefins and alcohols. I. Reactions with methanol. Fuel Processing Technology, 2003, 83, 219-234.
[Непатентный документ 10] Hamelinck N.С, P. С.A., Outlook for advanced biofuels. Energy Policy, 2006, 34, 3268-3283.
Раскрытие изобретения
Задача, решаемая изобретением
[0008]
Задачей настоящего изобретения является обеспечение способа получения композиций, содержащих парафины и спирты и полезных в качестве химического промышленного материала или топливной композиции с использованием спирта в качестве исходного вещества.
Средство решения задачи
[0009]
Поскольку биоэтанол получают из растений, нет необходимости беспокоится об истощении из-за производства его плановым образом. Кроме того, источники энергии растительного происхождения считаются углеродно-нейтральными, как принято в Киотском протоколе СОР-3 (1997), так что они не создают новых выбросов диоксида углерода. Общемировой объем производства этанола в 2006 году составил 51 миллион килолитров, что на 11% больше по сравнению с объемом производства в предыдущем году. Соединенные Штаты Америки, Бразилия, Китай, Индия являются, в этом порядке самыми большими в мире производителями этанола, а другие страны следуют после этих стран. В Бразилии, которая является страной, где производство этанола преобладает более всего в мире, стоимость производства этанола уже намного ниже международной цены нефти благодаря их замкнутой инфраструктуре от выращивания сахарного тростника до распределения этанола. В Соединенных Штатах Америки объем производства этанола быстро увеличивается, что объясняется государственной политикой. В своем послании к нации в январе 2007 года президент Буш настаивал на ускорении разработок новых технологий для производства этанола из различных сельскохозяйственных и лесных целлюлозных отходов, включая багассу (выжатый сахарный тростник - примеч. перевод.), рисовую солому, пшеничную солому, кукурузные стебли и листья, макулатуру, отходы и кухонные отходы. Таким образом ожидается, что выходы этанола на единицу площади будут увеличиваться в ближайшем будущем более чем вдвое, так что можно предположить увеличение объема производства этанола и снижение стоимости производства. Более того, непохоже, что стоимость производства этанола будет увеличиваться в будущем.
[0010]
В этих условиях авторы настоящего изобретения начали разрабатывать замещающее топливо, которое может быть использовано для существующих автомобилей с бензиновым двигателем. Они первыми сосредоточились на использовании биоэтанола растительного происхождения в качестве исходного вещества. Поскольку этанол уже использовался в качестве добавки к бензину, по этанолу провели небольшие исследования или не проводили дальнейших исследований. При продвижении исследований авторы настоящего изобретения обнаружили, что топливная композиция, синтезированная из этанола в качестве исходного вещества, имеет высокое содержание диенов и альдегидов и что содержание диенов и альдегидов вызывает снижение устойчивости к окислению и образование смол в топливе. Авторы настоящего изобретения также обнаружили, что когда водород добавляют после обеспечения контакта этанола с катализатором превращения спирта, можно получить топливо, которое имеет значительно повышенную устойчивость к окислению, пониженное образование смол и высокую теплотворную способность. Таким образом было сделано настоящее изобретение. При последующей разработке было также обнаружено, что за счет использования этого способа может быть получен спирт с высоким выходом. Кроме того, авторы настоящего изобретения обнаружили, что когда смешанный спирт желателен в качестве конечной композиции, полученной реакцией гидрирования, предпочтителен низкий процент превращения этанола, например рекомендуется процент превращения этанола 0,3-90 масс.%, предпочтительно 0,3-57,3 масс.%. Также было обнаружено, что, когда желательно получить в большом количестве смешанный парафин, рекомендуется процент превращения этанола 50 масс.% или более, предпочтительно 82,6 масс.% или более.
[0011]
Настоящее изобретение относится к (1) способу получения композиции с использованием спирта в качестве исходного вещества, при этом композиция содержит, по меньшей мере, один компонент, выбранный из группы, состоящей из парафинов и спиртов, а способ содержит первый этап, на котором обеспечивают контакт спирта с катализатором превращения спирта, и второй этап, на котором продукт, полученный на первом этапе, подвергают реакции гидрирования; (2) способу получения органического соединения в соответствии с (1), в котором исходным веществом является этанол; (3) способу получения композиции в соответствии с (1) или (2), в котором катализатор превращения спирта одновременно вызывает обезвоживание и дегидрирование спирта; (4) способу получения композиции в соответствии с любым из (1)-(3), в котором катализатор превращения спирта является фосфатом кальция; (5) способу получения композиции в соответствии с (4), в котором фосфат кальция является гидроксиапатитом; (6) способу получения композиции в соответствии с любым из (1)-(3), в котором катализатор превращения спирта является глинистым минералом; (7) способу получения композиции в соответствии с (6), в котором глинистый минерал является гидротальцитом; (8) способу получения композиции в соответствии с любым из (1)-(7), в котором реакцию на первом этапе проводят при давлении 1-200 атм; (9) способу получения композиции в соответствии с любым из (1)-(8), в котором реакцию на первом этапе проводят при температуре 100-600°С; (10) способу получения композиции в соответствии с любым из (1)-(9), в котором реакцию на первом этапе проводят в течение 0,1-600 секунд; (11) способу получения композиции в соответствии с любым из (1)-(10), в котором в качестве газа-носителя для спирта как исходного вещества в реакции на первом этапе используют водород; (12) способу получения композиции в соответствии с любым из (1)-(11), в котором процент превращения спирта на первом этапе составляет 0,3%-100%; (13) способу получения композиции в соответствии с любым из (1)-(12), в котором в качестве продукта на первом этапе используют одно из следующего: все продукты реакции, состоящие из жидкой фазы, включающей спирты, воду и углеводороды с 4-12 атомами углерода, и газовой фазы, которая представляет собой легкий газ, содержащий парафины, спирты и олефины; все жидкофазные продукты реакции, состоящие из всех продуктов реакции, из которых удален легкий газ; продукты реакции обезвоживания жидкой фазы, состоящие из всех продуктов реакции, из которых удалены легкий газ, непрореагировавший этанол и вода как продукт реакции; и легкий газ; (14) способу получения композиции в соответствии с (13), в котором все продукты реакции на первом этапе соответственно содержат парафины в количестве 0-1,7 масс.%, олефины в количестве 0-60,3 масс.%, диены в количестве 0-19,8 масс.%, ароматические соединения в количестве 0-11,4 масс.%, спирты в количестве 0-37,4 масс.%, альдегиды в количестве 0-5,4 масс.%, простые эфиры в количестве 0-2,2 масс.% и воду как продукт реакции в количестве 0,1-38,8 масс.% по отношению к этанолу как исходному веществу; (15) способу получения композиции в соответствии с (13) или (14), в котором спирты в жидкой фазе, полученные превращением из этанола на первом этапе, содержат, по меньшей мере, один из следующих: бутанол, гексанол и октанол; (16) способу получения композиции в соответствии с любым из (1)-(15), в котором на этапе реакции гидрирования используют катализатор гидрирования; (17) способу получения композиции в соответствии с любым из (1)-(16), в котором реакцию на втором этапе проводят при давлении 1-200 атм; (18) способу получения композиции в соответствии с любым из (1)-(17), в котором реакцию на втором этапе проводят при температуре 0-400°С; (19) способу получения композиции в соответствии с любым из (13)-(18), в котором второй этап является этапом, на котором проводят реакцию гидрирования одного из следующего: всех продуктов реакции на первом этапе; всех жидкофазных продуктов реакции, состоящих из всех продуктов реакции на первом этапе, из которых удален легкий газ; продуктов реакции обезвоживания жидкой фазы, состоящих из всех продуктов реакции на первом этапе, из которых удалены легкий газ, непрореагировавший этанол и вода как продукт реакции; и легкий газ; (20) способу получения композиции в соответствии с любым из (1)-(19), в котором на первом этапе водород используют в качестве газа-носителя для спирта как исходного вещества, а на втором этапе водород используют в качестве газа-носителя в реакции гидрирования; и (21) способу получения композиции в соответствии с любым из (1)-(20), в котором водород, образовавшийся на первом этапе, используют в реакции гидрирования на втором этапе.
[0012]
Настоящее изобретение также относится к (22) композиции, полученной способом получения, в котором проводят реакцию гидрирования для всех продуктов реакции на первом этапе в соответствии с любым из (13)-(21); (23) композиции в соответствии с (22), содержащей парафины в количестве 0,5-64,0 масс.%, олефины в количестве 0-6,3 масс.%, диены в количестве 0-2,1 масс.% и альдегиды в количестве 0,1-0,4 масс.% по отношению к этанолу как исходному веществу; (24) композиции в соответствии с (23), содержащей парафины С1 в количестве 0,1-2,5 масс.%, парафины С2 в количестве 0,2-62,2 масс.%, парафины С4 в количестве 0,1-7,6 масс.%, парафины С6 в количестве 0-10,3 масс.% и парафины С8 в количестве 0-4,5 масс.% по отношению к этанолу как исходному веществу; (25) композиции, полученной способом получения, в котором реакцию гидрирования проводят для всех жидкофазных продуктов реакции, состоящих из всех продуктов реакции, из которых удален легкий газ на первом этапе в соответствии с любым из (13)-(21); (26) композиции в соответствии с (25), содержащей парафины в количестве 0,3-28,9 масс.%, олефины в количестве 0-1,6 масс.%, диены в количестве 0-0,7 масс.% и альдегиды в количестве 0,1-0,2 масс.% по отношению к этанолу как исходному веществу; (27) композиции в соответствии с (26), содержащей парафины С1 в количестве 0-1,9 масс.%, парафины С2 в количестве 0,1-2,2 масс.%, парафины С4 в количестве 0,1-2,4 масс.%, парафины С6 в количестве 0-12,2 масс.% и парафины С8 в количестве 0-5,5 масс.% по отношению к этанолу как исходному веществу; (28) композиции, полученной способом получения, в котором реакцию гидрирования проводят для всех продуктов реакции обезвоживания жидкой фазы, состоящих из всех продуктов реакции, из которых удалены легкий газ, непрореагировавший этанол и вода как продукт реакции на первом этапе в соответствии с любым из (13)-(21); (29) композиции в соответствии с (28), содержащей парафины в количестве 0,2-29,2 масс.%, олефины в количестве 0-1,3 масс.%, диены в количестве 0-0,4 масс.% и альдегиды в количестве 0-0,1 масс.% по отношению к этанолу как исходному веществу; (30) композиции в соответствии с (29), содержащей парафины С1 в количестве 0,1-1,3 масс.%, парафины С2 в количестве 0,1-1,4 масс.%, парафины С4 в количестве 0-1,9 масс.%, парафины С6 в количестве 0-13,3 масс.% и парафины С8 в количестве 0-6,5 масс.% по отношению к этанолу как исходному веществу; (31) композиции, полученной способом получения, в котором реакцию гидрирования проводят для легкого газа на первом этапе в соответствии с любым из (13)-(21); (32) композиции в соответствии с (31), содержащей парафины в количестве 1,2-64,2 масс.%, олефины в количестве 0-0,5 масс.% и диены в количестве 0-0,5 масс.% по отношению к этанолу как исходному веществу; (33) композиции в соответствии с (32), содержащей парафин С1 в количестве 0-0,3 масс.%, парафин С2 в количестве 0,4-64,2 масс.% и парафин С4 в количестве 0-7,7 масс.% по отношению к этанолу как исходному веществу; (34) композиции в соответствии с любым из (22)-(33), содержащей олефины в количестве 0-10,0 масс.% по отношению к этанолу как исходному веществу; (35) композиции в соответствии с любым из (22)-(34), содержащей диены в количестве 0-3,0 масс.% по отношению к этанолу как исходному веществу; (36) композиции в соответствии с любым из (22)-(35), содержащей альдегиды в количестве 0-1,0 масс.% по отношению к этанолу как исходному веществу; (37) композиции в соответствии с любым из (22)-(36), содержащей парафины в количестве 0,2-70,0 масс.% по отношению к этанолу как исходному веществу; и (38) композиции в соответствии с любым из (22)-(37), содержащей спирты в количестве 0-50,0 масс.% по отношению к этанолу как исходному веществу.
[0013]
Настоящее изобретение далее относится к (39) топливной композиции для двигателя внутреннего сгорания с повышенной устойчивостью к окислению топлива, содержащей композицию в соответствии с любым из (22)-(38), в которой содержание олефинов и диенов снижено, а содержание парафина повышено; (40) топливной композиции для двигателя внутреннего сгорания с повышенной устойчивостью к окислению топлива, содержащей композицию в соответствии с любым из (22)-(38), в которой содержание альдегидов снижено, а содержание спирта повышено; и (41) топливной композиции для двигателя внутреннего сгорания, содержащей композицию в соответствии с любым из (22)-(38), в которой содержание смол ниже уровня промышленного стандарта Японии для топливных композиций благодаря реакции гидрирования на втором этапе.
Краткое описание чертежей
[0014]
[Фиг.1] Фиг.1 представляет собой схематическое изображение, поясняющее устройство для использования в способе получения органических соединений в способе по настоящему изобретению.
Лучший пример осуществления изобретения
[0015]
С точки зрения способа получения композиций по настоящему изобретению нет особого ограничения, поскольку он является способом получения композиций с использованием спирта как исходного вещества, содержащим первый этап, на котором обеспечивают контакт спирта с катализатором превращения спирта, и второй этап, на котором проводят реакцию гидрирования продукта, полученного на первом этапе, при этом композиции содержат, по меньшей мере, один компонент, выбранный из группы, состоящей из парафинов и спиртов. Парафины в настоящем изобретении означают алкан (углеводороды с насыщенной цепью общей формулы CnH2n+2).
[0016]
Способ получения по настоящему изобретению дает высокие выходы парафинов и спиртов, которые могут быть соответственно использованы в качестве химического промышленного материала и подобного. Состав, полученный способом получения по настоящему изобретению, очень полезен как топливная композиция для двигателя внутреннего сгорания, потому что, как указано выше, такая композиция имеет высокое содержание парафинов и спиртов, наиболее предпочтительных для топливной композиции для двигателя внутреннего сгорания, и потому что в ней почти не содержатся диены, альдегиды и т.д., неблагоприятные для топливной композиции для двигателя внутреннего сгорания. Таким образом, эта композиция может быть использована в качестве заменителя бензинового топлива или добавки к бензину. Топливная композиция для двигателя внутреннего сгорания имеет значительно повышенную устойчивость к окислению, пониженное образование смол и высокую теплотворную способность. Особенно устойчивость к окислению намного превосходит ту, которая оговорена промышленным стандартом Японии.
[0017]
В общем, когда нефтяные продукты подвергаются окислению, вязкость увеличивается, а цвет становится темнее. Кроме того, уже не могут выполняться основные требования к качеству из-за образования осаждаемых полимеров (осадка). Для определения степени устойчивости нефтяных продуктов к окислению проводят испытания на устойчивость к окислению. Нефтяные продукты с низкой устойчивостью к окислению с большей вероятностью ухудшают качество продукта из-за нахождения на воздухе в течение длительного времени, нежели нефтяные продукты с высокой устойчивостью к окислению. Способ испытаний на устойчивость к окислению бензина для двигателей внутреннего сгорания в Японии оговорен в промышленном стандарте Японии К2287 «Способ испытаний на устойчивость бензина к окислению (Способ индукционного периода)», а стандартный уровень составляет «240 мин или более».
[0018]
Кроме того, непромытые фактические растворенные смолы означают осадки после выпаривания такого бензина для двигателей внутреннего сгорания, а высокое содержание смол вызывает осаждение в индукционной системе, защемление индукционного клапана и т.д. Способ испытаний на фактические растворенные смолы оговорен в промышленном стандарте Японии К2261 «Способ испытаний нефтяных продуктов - Бензин для двигателей внутреннего сгорания и авиационное горючее - Фактические растворенные смолы (Метод выпаривания струей)», а стандартный уровень непромытых фактических растворенных смол составляет «20 мг/100 мл или менее».
[0019]
Спирт как исходное вещество по настоящему изобретению может быть линейным спиртом или спиртом с разветвленной цепью, а также может быть насыщенным спиртом или ненасыщенным спиртом. Кроме того, число атомов углерода особо не ограничивается, но с точки зрения простоты доступности предпочтительны спирты с 1-22 атомами углерода и более предпочтительны спирты с 1-8 атомами углерода. Особенно предпочтительные примеры включают линейные спирты, например метанол, этанол, 1-пропанол, 1-бутанол, 1-пентанол, 1-гексанол, 1-гептанол, 1-октанол, среди которых чрезвычайно предпочтителен этанол с точки зрения реакционной способности и того, что он может быть получен из растений. Спирт как исходное вещество может быть одного вида спиртов или может быть двумя или более видами спиртов. Когда используются два или более видов спиртов, предпочтительно использовать этанол в качестве, по меньшей мере, одного вида спиртов.
[0020]
Катализатор превращения спирта, используемый на первом этапе, особенно не ограничивается, поскольку он является катализатором, который одновременно вызывает обезвоживание и дегидрирование спирта и который может синтезировать углеводороды, такие как олефины и диены, и кислородсодержащие соединения, такие как альдегиды и спирты. Конкретные примеры включают фосфат кальция, глинистые минералы с каолином, глинистые минералы с пирофиллитом, глинистые минералы со смектитом, гидротальцит, силикат кальция, фторид кальция, сульфат кальция, гидроксид магния, хитин, фосфат лития, фосфат алюминия, фосфат магния, оксид титана, гидроксид кальция и сепиолит. Они могут использоваться в смеси.
[0021]
Фосфат кальция, использующийся в настоящем изобретении, включает гидроксиапатит Ca10(PO4)6(OH)2, трехзамещенный фосфат кальция Са3(PO4)2, двузамещенный фосфат кальция СаНРО4·0~2Н2О, однозамещенный фосфат кальция Са(Н2РО4)2·0~1Н2О, дифосфат кальция Ca2P2O7, метафосфат кальция Са(PO3)2, фторапатит Ca10(PO4)5F2, фосфат тетракальция Са4(PO4)2O, фосфат октакальция Са8Н2(PO4)5·5H2O. Среди них предпочтителен гидроксиапатит, так как он может эффективно превращать спирт как вещество, а также проявляет каталитическую активность в реакции гидрирования.
Кальциевофосфатный катализатор можно использовать даже для спирта, содержащего около 50% или менее, предпочтительно около 10% или менее воды, поэтому он особенно предпочтителен для использования для биоэтанола, который обычно получается как водосодержащие продукты.
[0022]
Гидроксиапатит является одним из видов фосфата кальция, и стехиометрически может быть представлен составом Са10(PO4)6(ОН)2, как указывалось выше. Даже гидроксиапатит, у которого молярное отношение Са/Р составляет менее 1,67 и не является стехиометрическим, проявляет свойства гидроксиапатита и может приобрести апатитовую структуру. Поэтому такие синтезированные гидроксиапатиты с молярным отношением Са/Р приблизительно 1,4-1,8 также включаются. В способе получения композиций по настоящему изобретению главным образом предпочтительны гидроксиапатиты с молярным отношением Са/Р, равным 1,50-1,80, особенно предпочтительно молярное отношение, равное 1,60-1,70. Гидроксиапатит может быть использован в любой форме: гранулах, сферах, таблетках, пористых структурах и т.д.
[0023]
Кроме того, гидроксиапатит может быть носителем металлического катализатора или ионно-металлического катализатора, которые действуют на спирт. Что касается металлического катализатора или ионно-металлического катализатора, действующих на спирт, то в качестве примеров можно привести мета или ион металла, описанные в выложенной патентной заявке Японии №5-305238.
[0024]
Глинистый минерал каолин представляет собой глинистый минерал, имеющий основную структуру из тетраэдрического слоя и октаэдрического слоя в соотношении 1:1. Примеры глинистых минералов каолинов включают лизардит [Mg3Si2O5(OH)4], бертьерин [(Fe2+, Fe3+, Mg)2-3(Si, Al)2O5(ОН)4], амезит [Mg2Al(Si, Al)O5(ОН)4], кронстедит [Fe2+Fe3+(SiFe3+)O5(OH)4], непуит [Ni3Si2O5(OH)4], келлиит [(Mn2+, Mg, Al)3(Si, Al)2O5(ОН)4], фрэпонит [(Zn, Al)3(Si, Al)2O5(OH)4], бриндлиит [(Ni, Mg, Fe2+)3(Si, Al)O5(ОН)4], каолинит [Al2Si2O5(OH)4], диккит [Al2Si2O5(OH)4], накрит [Al2Si2O5(OH)4], галуазит [Al2Si2O5(OH)4] и одинит [(Fe3+, Mg, Al, Fe2+)2-3>(Si, Al)2O5(ОН)4].
[0025]
Глинистый минерал пирофиллит представляет собой глинистый минерал, имеющий основную структуру из тетраэдрического слоя и октаэдрического слоя в соотношении 2:1. Примеры глинистых минералов пирофиллитов включают: тальк [Mg3Si4O10(OH)2], виллемсеит [(Ni, Mg)3Si4O10(OH)2], керолит [Mg3Si4O10(OH)2], пимелит [Ni3Si4O10(OH)2], пирофиллит [Al2Si4O10(OH)2] и феррипирофиллит [Fe3+Si4O10(ОН)2].
[0026]
Глинистый минерал смектит представляет собой глинистый минерал, имеющий основную структуру из тетраэдрического слоя и октаэдрического слоя в соотношении 2:1. Примеры глинистых минералов смектитов включают:
сапонит [(Са/2, Na)0,3(Mg, Fe2+)3(Si, Al)4О10(ОН)2·4Н2О],
гектолит [Na0,3(Mg, Li)3Si4O10(Fe, ОН)2·4H2O],
соконит [Na0,3Zn3(Si, Al)4О10(ОН)2·4Н2О],
стивенсит [(Ca/2)0,3Mg3Si4O10(OH)2·4H2O],
свайнфордит [(Са/2, Na)0,3(Li, Mg)2(Si, Al)4О10(ОН, F)2·2H2O],
монмориллонит [(Са/2, Na)0,3(Al, Mg)2(Si)4O10(OH)2·nH2O],
байделит [(Са/2, Na)0,3Al2(Si, Al)4О10(ОН)2·nH2O],
нонтронит [Na0,3Fe3+(Si, Al)4О10(ОН)2·nH2O] и
волконскоит [Ca0,3(Cr3+, Mg, Fe3+)3(Si, Al)4О10(ОН)2·nH2O].
[0027]
Гидротальцит представляет собой глинистый минерал, имеющий состав из Mg6Al2(OH)16CO3·4H2O. Сепиолит представляет собой глинистый минерал, имеющий состав из Si12Mg8O30(OH)4(H2O)4·8H2O.
[0028]
Хитин является мукополисахаридом, в котором N-ацетил-β-D-глюкозамин связан 1,4 связями. Особых ограничений на молекулярную массу хитина нет, и обычно молекулярная масса составляет приблизительно 100000 - 1 миллион.
[0029]
Процент превращения спиртов, например этанола, на первом этапе составляет обычно 0,3-100,0%. Примерами продуктов, полученных на первом этапе, для которых на втором этапе проводится реакция гидрирования, служат все продукты реакции, состоящие из жидкой фазы, содержащей кислородсодержащие соединения, например спирты и альдегиды, воду, углеводороды с 4-12 атомами углерода и т.д., и газовой фазы, которая представляет собой легкий газ, содержащий парафины, олефины, диены, спирты и т.д.; все жидкофазные продукты реакции, состоящие из всех продуктов реакции, из которых удален легкий газ; и продукты реакции обезвоживания жидкой фазы, состоящие из всех продуктов реакции, из которых удалены легкий газ, непрореагировавший спирт и вода как продукт реакции. Легкий газ, используемый здесь, означает газофазный компонент, который получают путем пропускания всех реагентных продуктов на первом этапе через охлаждаемую ловушку при температуре 10°С и нормальном давлении и который содержит, по меньшей мере, один компонент, выбранный из группы газов, состоящей из метана, этана, этилена, пропана, пропилена, бутана, бутена, бутадиена и т.д.
[0030]
При использовании этанола в качестве исходного вещества примерами продуктов реакции на первом этапе могут служить композиции, соответственно содержащие парафины в количестве 0-1,7 масс.%, олефины в количестве 0-60,3 масс.%, диены в количестве 0-19,8 масс.%, ароматические соединения в количестве 0-11,4 масс.%, спирты в количестве 0-37,4 масс.%, альдегиды в количестве 0-5,4 масс.%, простые эфиры в количестве 0-2,2 масс.% и воду как продукт реакции в количестве 0,1-38,8 масс.% по отношению к этанолу как исходному веществу. По существу, на первом этапе синтезируют различные углеводороды, например парафины, олефины, диены, триены, спирты, простые эфиры, кетоны, альдегиды и сложные эфиры, но предпочтительно регулировать условия синтеза так, чтобы получать углеводород с 4-12 атомами углерода в качестве основного компонента. Кроме того, поскольку на первом этапе в качестве исходного вещества используется этанол, можно с высоким выходом синтезировать спирты (линейные спирты), например бутанол, гексанол и октанол в жидкой фазе.
[0031]
Если конечный продукт используется как топливная композиция для двигателя внутреннего сгорания, второй этап оказывается этапом по улучшению свойств топлива, а также этапом по повышению устойчивости топлива к окислению. Другими словами, как упоминалось выше, первый этап дает различные углеводороды. А на втором этапе можно уменьшить количество соединений, например диенов и альдегидов, которые неблагоприятны для топливной композиции, а также соединений, например олефинов, которые весьма неблагоприятны с точки зрения устойчивости топлива, и одновременно увеличить количество соединений, например парафинов и спиртов, которые благоприятны для топлива. По существу, можно получить топливо, которое имеет замечательно высокую устойчивость к окислению, сниженное образование смол и высокую теплотворную способность. В частности, резко повышается устойчивость к окислению. Кроме того, на втором этапе повышается выход спирта, полезного в качестве химического промышленного материала.
[0032]
Целесообразно проводить реакцию гидрирования с катализатором гидрирования на втором этапе. В качестве катализатора гидрирования может быть использован любой известный катализатор гидрирования, который действует на диены, альдегиды или ароматические соединения, и примеры включают металлы, например Pd, Pt, Ru, Rh, Fe, Ni, Cu, Co, Cr, W и Mo, или металлонесущие катализаторы, несущие эти металлы, предпочтительно пористые катализаторы с этими металлами (катализаторы Ренея), использующие дешевые переходные металлы. Среди них предпочтительны катализаторы гидрирования, действующие на диены и альдегиды, и более предпочтительны такие катализаторы гидрирования, которые действуют на диены, альдегиды и ароматические соединения. А именно особенно предпочтительны металлические катализаторы, содержащие Pt, Ni, Со, Pd или Cu. Реакцию гидрирования можно проводить как двухстадийную реакцию с использованием двух типов катализаторов.
[0033]
Реакция по настоящему изобретению может проводиться либо периодическим образом либо последовательным образом, но с точки зрения промышленной экономической эффективности предпочтительна реакция последовательным образом. Кроме того, предпочтительна газофазная реакция. Ракции на первом и втором этапах можно проводить в одном и том же реакционном сосуде или в разных реакционных сосудах.
[0034]
При газофазной реакции в реакционный сосуд могут подавать только исходный спирт в газообразном состоянии либо исходный спирт в газообразном состоянии вместе с газом-носителем. В последнем случае предпочтительно использовать водород как весь газ-носитель или часть газа-носителя для спирта в газообразном состоянии, поскольку это делает возможным использование водорода как газа-носителя в реакции гидрирования на втором этапе и таким образом служит для легкого и эффективного протекания реакции по настоящему изобретению. Когда на первом этапе в качестве катализатора превращения спирта используется гидроксиапатит, реакция гидрирования происходит также и на первом этапе благодаря тому, что гидроксиапатитовый катализатор действует еще и как катализатор гидрирования. Поэтому эффективность гидрирования может быть повышена. Предпочтительно на первом этапе водород подают в реакционный сосуд в качестве газа-носителя, как упоминалось выше, или его могут подавать после завершения первого этапа (только на втором этапе). Что касается количества вводимого водорода, то оно составляет предпочтительно 10-1000 об.% и более предпочтительно-20-500 об.% по отношению к исходному спирту в газообразном состоянии. Как альтернатива водород, образовавшийся в реакции на первом этапе, может быть использован в реакции гидрирования без отдельного введения водорода.
[0035]
Температура реакции, использующаяся в настоящем изобретении, обычно составляет 100-600°С и более предпочтительно 200-500°С на первом этапе. А именно, если желательно получить спирт с высоким выходом, предпочтительна температура реакции 100-450°С и более предпочтительна температура 200-450°С. На втором этапе предпочтительная температура реакции обычно составляет 0-600°С, при этом предпочитается температура 0-400°С, в частности 80-300°С.
[0036]
Далее, давление в реакции по настоящему изобретению на первом этапе может быть нормальным, повышенным или пониженным, а реакция может проводиться, например, при 1-200 атм. На втором этапе, который может проводиться при нормальном давлении, предпочитается проведение реакции при повышенном давлении, предпочтительно при 2-200 атм. Еще более предпочтительно проведение реакции при 10 атм или выше, поскольку можно снизить количество ароматических соединений, которые содержат токсичный бензол и дают сажу. Когда первый и второй этапы проводят в одном и том же реакционном сосуде, реакции проводят при одинаковом давлении на первом и втором этапах. Время контакта с катализатором на первом и втором этапах обычно составляет приблизительно 0,1-600 секунд и предпочтительно - приблизительно 0,4-60 секунд.
[0037]
Композиции по настоящему изобретению особенно не ограничиваются, так как композиции получают способом получения, в котором реакцию гидрирования проводят для всех продуктов реакции на первом этапе. При использовании этанола в качестве исходного вещества конкретными примерами служат композиции, содержащие парафины в количестве 0,5-64,0 масс.%, олефины в количестве 0-6,9 масс.%, диены в количестве 0-2,1 масс.% и альдегиды в количестве 0,1-0,4 масс.% по отношению к этанолу как исходному веществу. Частными примерами среди них являются такие композиции, которые содержат парафины С1 в количестве 0,1-4,3 масс.% (метан), парафины С2 в количестве 0,2-62,2 масс.% (этан), парафины С4 в количестве 0,1-12,9 масс.% (бутан), парафины С6 в количестве 0-10,3 масс.% и парафины С8 в количестве 0-4,5 масс.% по отношению к этанолу как исходному веществу.
[0038]
Далее, композиции по настоящему изобретению особенно не ограничиваются, так как композиции получают способом получения, в котором реакцию гидрирования проводят для всех жидкофазных продуктов реакции, состоящих из всех продуктов реакции, из которых удален легкий газ на первом этапе. При использовании этанола в качестве исходного вещества конкретными примерами служат композиции, содержащие парафины в количестве 0,3-28,9 масс.%, олефины в количестве 0-1,6 масс.%, диены в количестве 0-0,7 масс.% и альдегиды в количестве 0,1-0,2 масс.% по отношению к этанолу как исходному веществу. Частными примерами среди них являются такие композиции, которые содержат парафины С1 в количестве 0-1,9 масс.%, парафины С2 в количестве 0,1-2,2 масс.%, парафины С4 в количестве 0,1-2,4 масс.%, парафины С6 в количестве 0-12,2 масс.% и парафины С8 в количестве 0-5,5 масс.% по отношению к этанолу как исходному веществу.
[0039]
Далее, композиции по настоящему изобретению особенно не ограничиваются, так как композиции получают способом получения, в котором реакцию гидрирования проводят для продуктов реакции обезвоживания жидкой фазы, состоящих из всех продуктов реакции, из которых удалены легкий газ, непрореагировавший этанол и вода как продукт реакции на первом этапе. При использовании этанола в качестве исходного вещества конкретными примерами служат композиции, содержащие парафины в количестве 0,2-29,2 масс.%, олефины в количестве 0-1,3 масс.%, диены в количестве 0-0,4 масс.% и альдегиды в количестве 0-0,1 масс.% по отношению к этанолу как исходному веществу. Частными примерами среди них являются такие композиции, которые содержат парафины С1 в количестве 0,1-1,3 масс.%, парафины С2 в количестве 0,1-1,4 масс.%, парафины С4 в количестве 0-1,9 масс.%, парафины С6 в количестве 0 - 13,3 масс.% и парафины С8 в количестве 0-6,5 масс.% по отношению к этанолу как исходному веществу.
[0040]
Еще далее, композиции по настоящему изобретению особенно не ограничиваются, так как композиции получают способом получения, в котором реакцию гидрирования проводят для легкого газа на первом этапе. При использовании этанола в качестве исходного вещества конкретными примерами служат композиции, содержащие парафины в количестве 1,2-64,2 масс.%, олефины в количестве 0-0,5 масс.%, диены в количестве 0-0,5 масс.% по отношению к этанолу как исходному веществу. Частными примерами среди них являются такие композиции, которые содержат парафины С1 в количестве 0-0,3 масс.%, парафины С2 в количестве 0,4-64,2 масс.%, парафины С4 в количестве 0-7,7 масс.% по отношению к этанолу как исходному веществу.
[0041]
Далее, предпочтительные примеры композиций по настоящему изобретению с использованием этанола в качестве исходного вещества включают: композиции, содержащие парафины в количестве 0,2-70,0 масс.%, предпочтительно 0,2-64,2 масс.% по отношению к этанолу как исходному веществу; композиции, содержащие спирты в количестве 0-50,0 масс.%, предпочтительно 0-40,4 масс.% по отношению к этанолу как исходному веществу; и композиции, содержащие парафины в количестве 0,2-70,0 масс.%, предпочтительно 0,2-64,2 масс.%, и спирты в количестве 0-50,0 масс.%, предпочтительно 0-40,4 масс.% по отношению к этанолу как исходному веществу.
[0042]
Далее, предпочтительные примеры композиций по настоящему изобретению с использованием этанола в качестве исходного вещества включают: композиции, содержащие олефины в количестве 0-10 масс.%, предпочтительно 0-6,3 масс.% по отношению к этанолу как исходному веществу; композиции, содержащие диены в количестве 0-3 масс.%, предпочтительно 0-2,1 масс.% по отношению к этанолу как исходному веществу; композиции, содержащие альдегиды в количестве 0-1 масс.%, предпочтительно 0-0,4 масс.% по отношению к этанолу как исходному веществу; композиции, содержащие олефины в количестве 0-10 масс.%, предпочтительно 0-6,3 масс.%, и диены в количестве 0-3 масс.%, предпочтительно 0-2,1 масс.% по отношению к этанолу как исходному веществу; композиции, содержащие олефины в количестве 0-10 масс.%, предпочтительно 0-6,3 масс.%, и альдегиды в количестве 0-1 масс.%, предпочтительно 0-0,4 масс.% по отношению к этанолу как исходному веществу; композиции, содержащие диены в количестве 0-3 масс.%, предпочтительно 0-2,1 масс.%, и альдегиды в количестве 0-1 масс.%, предпочтительно 0-0,4 масс.% по отношению к этанолу как исходному веществу; и композиции, содержащие олефины в количестве 0-10 масс.%, предпочтительно 0-6,3 масс.%, диены в количестве 0-3 масс.%, предпочтительно 0-2,1 масс.%, и альдегиды в количестве 0-1 масс.%, предпочтительно 0-0,4 масс.% по отношению к этанолу как исходному веществу.
[0043]
Вышеуказанные композиции по настоящему изобретению могут использоваться в качестве топливной композиции и т.д., в качестве смеси как таковой. Как альтернатива они могут использоваться как химический промышленный материал за счет выделения и очистки представляющего интерес органического соединения с помощью обычно применяемых способов выделения и очистки, включающих дистилляцию, разделение посредством микропористой мембраны, экстракцию и адсорбцию.
[0044]
Когда композиции по настоящему изобретению, для которых этанол является исходным веществом, используются в качестве топливной композиции для двигателя внутреннего сгорания, они показывают замечательную полезность как топливной композиции для двигателя внутреннего сгорания с повышенной устойчивостью к окислению топлива, в которой содержание олефинов и диенов уменьшено, а содержание парафинов увеличено, и как топливной композиции для двигателя внутреннего сгорания с повышенной устойчивостью к окислению топлива, в которой содержание альдегидов уменьшено, а содержание спиртов увеличено. Кроме того, композиции полезны как топливная композиция для двигателя внутреннего сгорания, в которой содержание смол ниже уровня, оговоренного промышленным стандартом Японии для топливных композиций благодаря реакции гидрирования на втором этапе.
[0045]
Пример осуществления способа получения композиций по настоящему изобретению поясняется со ссылкой на чертеж. Фигура 1 представляет собой схематическое изображение, поясняющее устройство для использования в способе по настоящему изобретению для получения композиций. Как показано на фигуре 1, устройство в примере осуществления представляет собой устройство с использованием той же реакционной трубы (реакционного сосуда). Используемый на первом этапе катализатор превращения спирта загружен в верхнюю часть реакционной трубы, расположенную в центре устройства, а используемый на втором этапе катализатор гидрирования расположен в нижней части. Далее, каждый участок, где проводятся реакции на первом и втором этапах, соответственно снабжен электропечью, так что температуры реакций на первом и втором этапах могут соответствующим образом регулироваться.
[0046]
В этом примере осуществления этанол в газообразном состоянии в качестве исходного вещества подают вместе с водородом сверху реакционной трубы. Другими словами, этанол в газообразном состоянии, введенный в реакционную трубу, вступает в контакт с катализатором превращения спирта, в результате чего происходит синтез главным образом углеводородов с 4-12 атомами углерода (топливный компонент) (первый этап). Затем водород, введенный с исходным веществом, становится активным за счет контактирования с катализатором гидрирования, и происходит реакция гидрирования топливного компонента, синтезированного на первом этапе (второй этап). Таким образом получают топливную композицию. Все продукты реакции или их часть могут временно храниться в резервуаре и подаваться по необходимости на второй этап для проведения реакции гидрирования.
[0047]
Настоящее изобретение будет пояснено ниже более подробно со ссылками на примеры. Технический объем настоящего изобретения, однако, не будет ограничиваться только этими примерами.
[Пример 1]
[0048]
[Катализатор]
(Катализатор превращения спирта: гидроксиапатитовый катализатор)
Гидроксиапатитовый катализатор (НАР-катализатор) был приготовлен в соответствии с методом осаждения. Все использованные вещества являются первоклассными реагентами, производимыми фирмой Wako Pure Chemical Industrial Ltd. Порядок действий является следующим.
[0049]
Исходными веществами были 0,60 моль/л водного раствора тетрагидрата нитрата кальция, отрегулированного на pH 10 с помощью аммиачной воды, и 0,40 моль/л водного раствора водородфосфата диаммония, отрегулированного на pH 10 с помощью аммиачной воды. Растворы веществ закапаны отдельно в дистиллированную воду с помощью раствороподающих насосов после регулирования скорости подачи раствора, чтобы можно было синтезировать гидроксиапатит с определенным молярным отношением Са/Р. После того как определенные количества были закапаны, результирующий раствор был хорошо перемешан в течение 24 часов, затем отфильтрован, промыт водой и высушен при 140°С. К полученным таким образом порошкам была добавлена деионизированная (ion-exchanged) вода для получения суспензии с концентрацией гидроксиапатита 10%. Затем суспензию выдержали и высушили при 140°С в сушильной камере, измельчили в ступке и прокалили в течение 2 часов при 600°С в атмосфере для получения порошкового гидроксиапатитового катализатора.
[0050]
Синтезированный таким образом гидроксиапатитовый катализатор был идентифицирован с помощью порошковой рентгеновской дифракции, и была определена величина удельной площади поверхности (БЭТ). Молярное отношение Са/Р катализатора определили методом калибровочной кривой с использованием флюоресцентного рентгеновского анализа. С помощью порошковой рентгеновской дифракции идентифицировали, что катализатор состоит из однофазного гидроксиапатита и что величина удельной площади поверхности (БЭТ) составляет 33 м2/г, а молярное отношение Са/Р составляет 1,64. Гидроксиапатитовые порошки были сформованы в таблетки с помощью таблетировочного компрессора, эти таблетки затем без труда размололи до размера 14-26 меш для использования в реакции превращения этанола.
[0051]
(Катализатор гидрирования)
В качестве катализатора гидрирования использовали пористый никелевый катализатор (NDT-90) от Kawaken Fine Chemicals Co., Ltd. Было принято во внимание выделение тепла в реакции гидрирования, и использовались порошки никелевого катализатора, 4-кратно разбавленные фосфатом кальция (β-трикальций фосфатом (β-ТСР)), который инертен к этанолу. Порошки были сформованы в таблетки с помощью таблетировочного компрессора, эти таблетки затем без труда размололи до размера 14-26 меш для использования.
[0052]
[Получение топливной композиции]
Использовали проточный реактор с неподвижным слоем. В верхнюю часть реакционной трубы с внутренним диаметром 10 мм, выпускаемой фирмой SUS, загрузили 1,8 г вышеупомянутого гидроксиапатитового катализатора в качестве катализатора первой стадии, а в нижнюю часть реакционной трубы загрузили 1,0 г вышеупомянутого катализатора гидрирования в качестве катализатора второй стадии. Сверху реакционной трубы ввели смешанный газ из этанола и водорода и проанализировали продукт реакции. Этанол в газообразном состоянии подавали с расходом 67 мл/мин, а водород подавали при двух уровнях расхода: 0 мл/мин и 200 мл/мин. Давление в реакции было установлено на двух уровнях: 1,0 атм и 7,9 атм. Конкретные условия реакции показаны в таблице 1. Пробные примеры 1-1 и 1-3 представляют собой примеры, в которых водород вводят на первой стадии смешанным с этанолом в газообразном состоянии как исходным веществом. Пробный пример 1-2 представляет собой пример, в котором водород добавляют на второй стадии. Пробный пример 1-4, который проводили при подаче водорода 0 мл/мин, представляет собой пример, в котором реакция гидрирования проводится с использованием водорода, образовавшегося в реакции первой стадии, и без введения водорода. В этом случае в качестве газа-носителя использовали газ гелий.
[0053]
С целью сравнения получили топливную композицию без проведения реакции гидрирования на втором этапе путем использования реакционной трубы (внутренний диаметр 10 мм; SUS), загруженной 1,8 г вышеупомянутого гидроксиапатитового катализатора. Затем проанализировали продукты реакции. Сравнительный пример 1-1 представляет собой пример, в котором этанол в газообразном состоянии был введен с водородом сверху реакционной трубы, а сравнительный пример 1-2 представляет собой пример, в котором этанол в газообразном состоянии был введен с газом гелием сверху реакционной трубы.
[0054]
Полученные таким образом продукты подвергли качественному анализу с использованием газового хромато-масс-спектрометра (GC-MS) с диапазоном масс M/Z=100-400, а количественный анализ осуществили с использованием газовой хроматографии (GC-FID (газовая хроматография с пламенно-ионизационной детекцией - примеч. перевод.)). Для определения количества кислородсодержащих соединений использовали коэффициент коррекции чувствительности моля углерода. Для обоих устройств использовали колонны от J&W Scientific (жидкая фаза: DB-1, толщина пленки: 5,0 мкм, размер колонны: 30 м × 0,323 мм). Проценты селективности продуктов реакции были вычислены по следующему уравнению.
[0055]
Процент селективности продукта реакции (С - масс.%) = моль углерода каждого продукта/моль углерода прореагировавшего спирта × 100.
Выход продуктов реакции был рассчитан путем вычисления массы продукта на основании результата FID (пламенно-ионизационной детекции - примеч. перевод.) (С - масс.%) при условии, что поданный этанол принят за 100%.
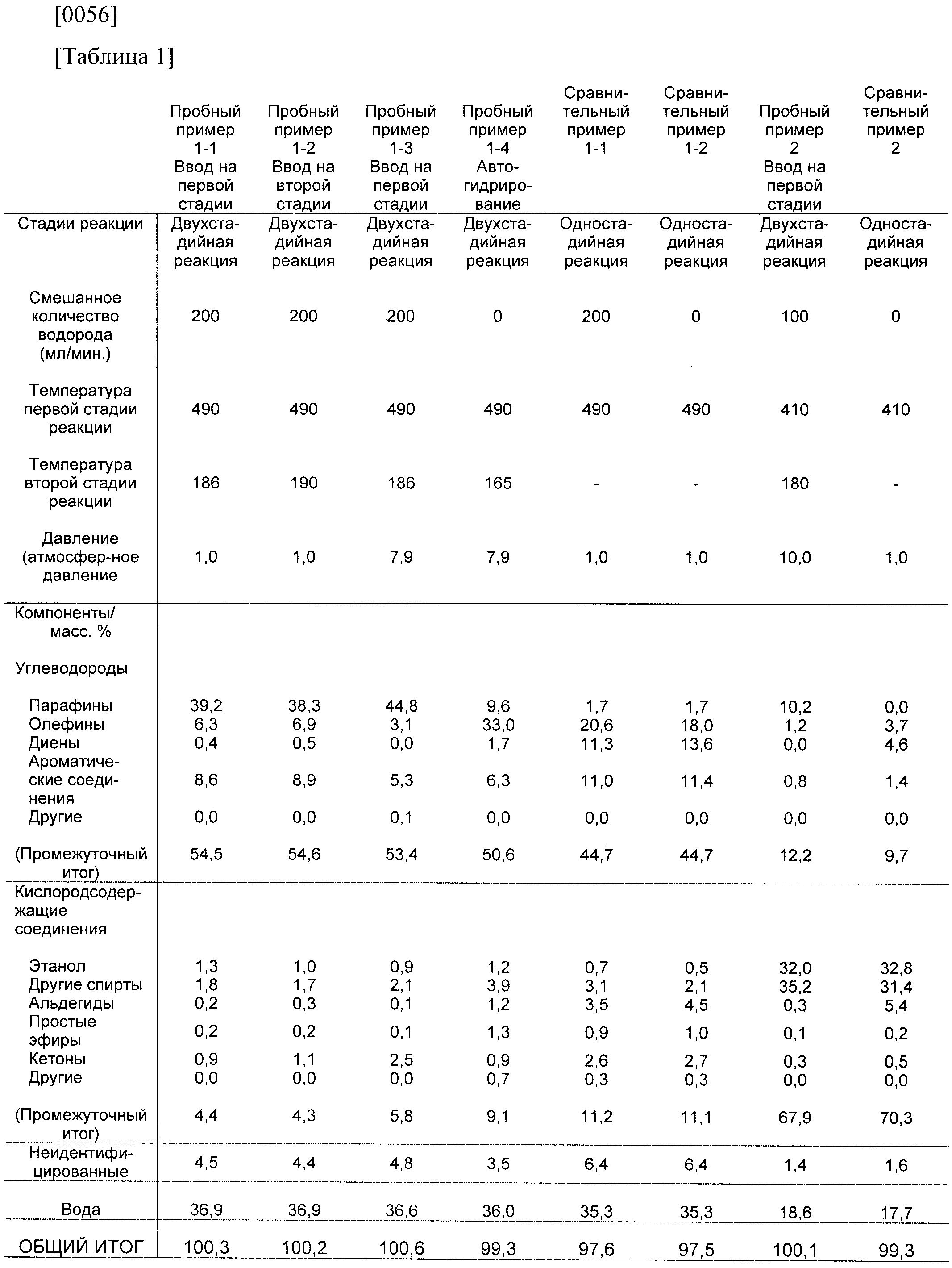
Результаты показаны ниже. В таблице 1 показан процентный состав топливных композиций в каждом из пробных примеров. В таблицах 2-7 показан более подробный процентный состав в каждом опыте.
[0057]
[0058]
[0059]
[0060]
[0061]
[0062]
[0063]
Сравнение пробных примеров и сравнительных примеров в таблице 1 обнаруживает, что в способе с 2-стадийной реакцией, осуществленном в пробных примерах, количество диенов и альдегидов, неблагоприятных для топливной композиции, значительно уменьшилось, а количество парафинов и спиртов, благоприятных для топливной композиции, увеличилось. Из пробных примеров 1-1 и 1-3 видно, что за счет повышения давления количество неблагоприятных для топливной композиции диенов еще больше уменьшается и также уменьшается количество ароматических соединений, дающих сажу. Пробные примеры 1-1 и 1-2 также демонстрируют, что ввод водорода на первой стадии приводит к снижению количества диенов и альдегидов и повышению количества парафинов и спиртов. А именно можно видеть, что реакция гидрирования проходит также в реакции первой стадии, доказывая что гидроксиапатитовый катализатор действует как катализатор гидрирования. Аналогично, на сравнительных примерах 1-1 и 1-2 показано, что гидроксиапатитовый катализатор действует как катализатор гидрирования. Кроме того, на опробном примере 1-4 и сравнительном примере 1-2 показано, что гидрирование возможно на второй стадии (втором этапе) за счет использования водорода, образовавшегося на первой стадии (первом этапе), без отдельного добавления водорода.
[0064]
Далее пробный пример 1-1 и сравнительный пример 1-2 увеличили приблизительно в 6 раз, а продукты реакции были сжижены с помощью охлаждаемой ловушки при 0°С и нормальном давлении. Образцы получили, подвергнув жидкую фракцию простой перегонке при температуре от комнатной до 210°С, затем для этих образцов определили показатели (октановое число по исследовательскому методу, устойчивость к окислению, непромытые и фактические смолы, теплотворная способность), предусмотренные промышленным стандартом Японии (JIS К 2202). Результаты показаны в таблице 8.
[0065]
[0066]
Из таблицы 8 ясно, что октановое число по исследовательскому методу (RON) образца в пробном примере 1-1 ниже, чем в сравнительном примере 1-2, но все же выше значения 89,0, которое является требуемым октановым числом для рядового бензина. Устойчивость к окислению образца в пробном примере 1-1 повысилась до 1440 мин или более с 60 мин. образца в сравнительном пример 1-2, что оказалось удивительно высокой устойчивостью даже по отношению к стандарту JIS. Количество непромытых и фактических смол также намного снизилось до пределов диапазона стандарта JIS. Теплотворная способность образца в пробном примере 1-1 составила 31,6 МДж/л (39620 Дж/г), что было ниже уровня в 34,6 МДж/л, являющегося теплотворной способностью бензина, но выше, чем уровни в 22,7 МДж/л для этанола и 26,8 МДж/л для бутанола.
[0067]
Далее провели серию испытаний с мотоциклами, оборудованными одноцилиндровым четырехтактным двигателем объемом 49 см3 с верхним распределительным валом и воздушным охлаждением АА01Е, который заправили образцом топлива по пробному примеру 1-1. В результате подтвердилось, что ходовые характеристики были аналогичны тем, что были при использовании товарного бензина.
[Пример 2]
[0068]
[Катализатор]
Использовали катализатор, аналогичный тому, что использовался в примере 1.
[Получение топливной композиции (получение спирта)]
Использовали проточный реактор с неподвижным слоем. В верхнюю часть реакционной трубы с внутренним диаметром 10 мм (SUS) загрузили 2,0 г гидроксиапатитового катализатора в качестве катализатора первой стадии, а в нижнюю часть реакционной трубы загрузили 1,0 г вышеупомянутого катализатора гидрирования в качестве катализатора второй стадии. Сверху реакционной трубы ввели смешанный газ из этанола и водорода и проанализировали продукт реакции. Этанол в газообразном состоянии подавали с расходом 26 мл/мин, а водород подавали с расходом 100 мл/мин. Давление в реакции было установлено в 10 атм.
[0069]
С целью сравнения получили топливную композицию без проведения реакции гидрирования на втором этапе. В реакционную трубу с внутренним диаметром 10 мм (SUS) загрузили 2,0 г гидроксиапатитового катализатора. Этанол в газообразном состоянии ввели с газом-носителем сверху реакционной трубы и продукт реакции проанализировали.
[0070]
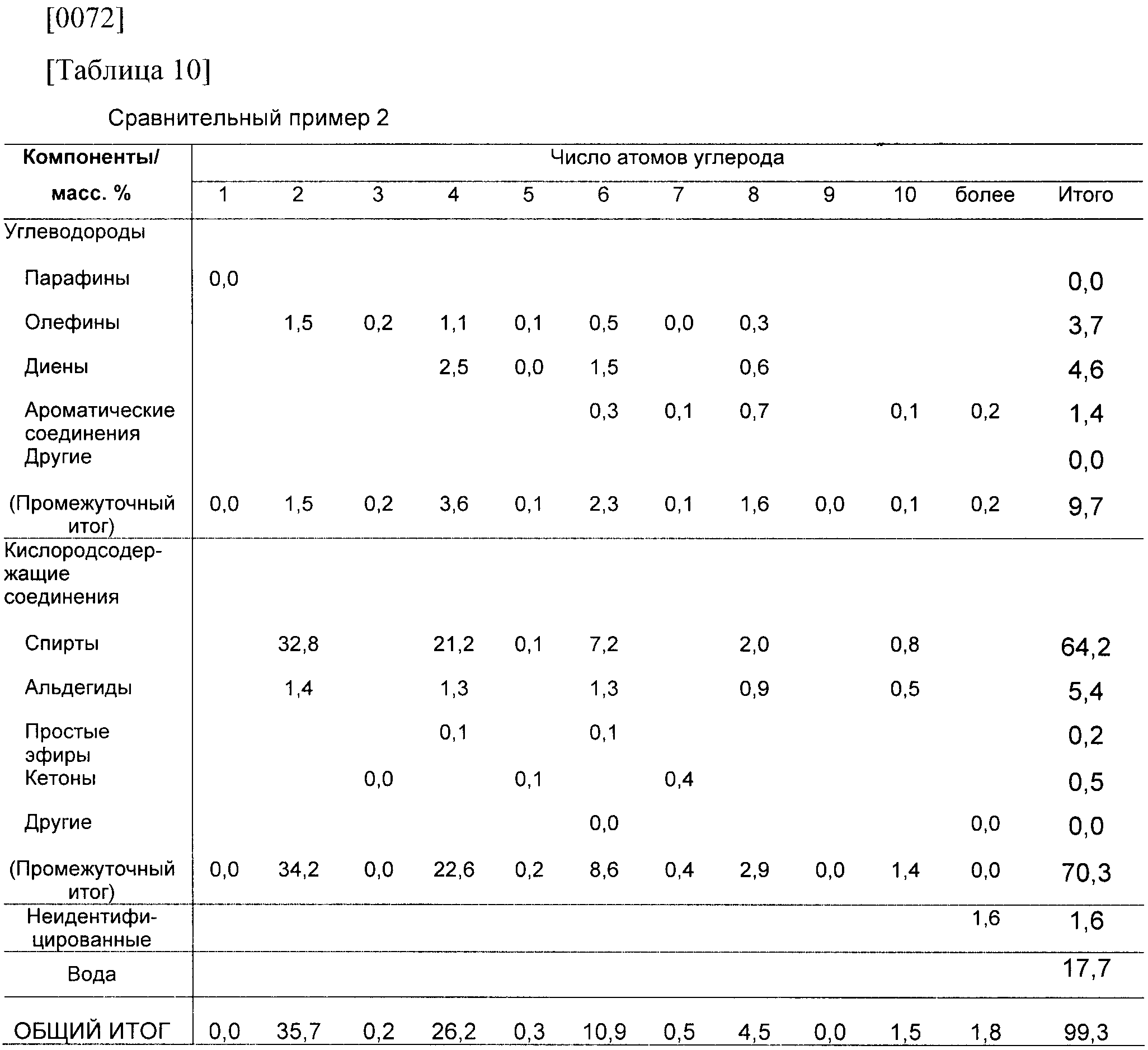
Результаты анализа вышеупомянутых образцов показаны в таблице 1 (пробный пример 2, сравнительный пример 2), таблице 9 и таблице 10.
[0071]
[0073]
Из пробных примеров и сравнительных примеров в таблицах 1, 9 и 10 было обнаружено, что в способе с 2-стадийной реакцией, осуществленном в пробных примерах, по сравнению со способом с одностадийной реакцией, осуществленном в сравнительных примерах, количество диенов и альдегидов, неблагоприятных для топливной композиции, значительно уменьшилось, а количество парафинов и спиртов, благоприятных для топливной композиции, увеличилось. А именно показано, что спирты (бутанол, гексанол, октанол и т.д.) могут быть получены с высоким выходом в соответствии с пробными примерами. Здесь бутанолом был в основном 1-бутанол.
[Пример 3]
[0074]
[Катализатор]
(Катализатор превращения спирта: гидротальцитовый катализатор)
Использованный гидротальцитовый катализатор был первоклассным реагентом, выпускаемым Wako Pure Chemical Industrial Ltd.
(Катализатор гидрирования)
Использовался катализатор гидрирования, аналогичной тому, что в примере 1.
[Получение топливной композиции]
Использовали проточный реактор с неподвижным слоем. В верхнюю часть реакционной трубы с внутренним диаметром 10 мм (SUS) загрузили 1,3 г гидротальцитового катализатора в качестве катализатора первой стадии, а в нижнюю часть реакционной трубы загрузили 1,0 г вышеупомянутого катализатора гидрирования в качестве катализатора второй стадии. Сверху реакционной трубы ввели смешанный газ из этанола и водорода и проанализировали продукт реакции. Этанол в газообразном состоянии подавали с расходом 26 мл/мин, а водород подавали с расходом 100 мл/мин. Давление в реакции было установлено в 1 атм.
[0075]
С целью сравнения получили топливную композицию без проведения реакции гидрирования на втором этапе. В реакционную трубу с внутренним диаметром 10 мм (SUS) загрузили 1,3 г гидротальцитового катализатора. Этанол в газообразном состоянии (26 мл/мин) ввели с газом-носителем сверху реакционной трубы и продукт реакции проанализировали.
[0076]
Результаты анализа вышеупомянутых образцов показаны в таблице 11.
[0077]
[0078]
Как и в случае, когда в качестве катализатора используется гидроксиапатит, в способе с 2-стадийной реакцией, осуществленном в пробном примере, по сравнению со способом с одностадийной реакцией, осуществленном в сравнительном примере, количество диенов и альдегидов, неблагоприятных для топливной композиции, значительно уменьшилось, а количество парафинов и спиртов, благоприятных для топливной композиции, увеличилось.
[Пример 4]
[0079]
Реакцию провели тем же образом, что и в примере 3, за исключением того, что в качестве катализатора превращения спирта использовали смешанный катализатор из оксида кальция и фосфата магния (CaO:Mg3(PO4)2·8H2O=1:1). В таблице 12 показаны результаты анализа, полученные для образцов.
[0080]
[0081]
Как и в случае, когда в качестве катализатора используется гидроксиапатит, в способе с 2-стадийной реакцией, осуществленном в пробных примерах, по сравнению со способом с одностадийной реакцией, осуществленном в сравнительных примерах, количество диенов и альдегидов, неблагоприятных для топливной композиции, значительно уменьшилось, а количество парафинов и спиртов, благоприятных для топливной композиции, увеличилось.
[Пример 5]
[0082]
[Катализатор]
(Катализатор превращения спирта)
В качестве катализатора превращения спирта использовали гидроксиапатитовый катализатор-1 (НАР-1) (молярное отношение Са/Р равно 1,67), гидроксиапатитовый катализатор-2 (НАР-2) (молярное отношение Са/Р равно 1,62) и гидроксиапатитовый катализатор-3 (НАР-3) (молярное отношение Са/Р равно 1,52), которые были получены способом, подобным тому, что в примере 1.
[0083]
(Катализатор гидрирования)
В качестве катализатора гидрирования использовали никелевый катализатор Ренея, палладиевый катализатор и медный катализатор Ренея. В качестве никелевого катализатора Ренея использовали пористый никелевый катализатор (NDT-90; Kawaken Fine Chemicals Co., Ltd.); в качестве палладиевого катализатора использовали углерод-палладиевый катализатор (N. Е. Chemcat Corporation); а в качестве медного катализатора Ренея использовали пористый медный катализатор (CDT-90; Kawaken Fine Chemicals Co., Ltd.). Никелевый катализатор Ренея и медный катализатор Ренея разбавили в 4 раза фосфатом кальция ((β-ТСР), который инертен к этанолу в температурном диапазоне реакции гидрирования с учетом тепла, выделяемого в реакции гидрирования. Эти каталитические порошки были сформованы в таблетки с помощью таблетировочного компрессора, затем эти таблетки без труда размололи до размера 14-26 меш для использования.
[0084]
[Получение топливной композиции]
(Все продукты реакции на первом этапе)
Использовали проточный реактор с неподвижным слоем. В реакционную трубу с внутренним диаметром 10 мм (SUS) загрузили 0,8 г гидроксиапатитового катализатора. В реакционную трубу ввели газ, разбавленный гелием, чтобы обеспечить концентрацию этанола 20 об.%, при расходе 50 мл/мин. В таблице 13 показаны конкретные условия реакции для пробных примеров с 5-1 по 5-7 и составы А-G всех продуктов реакции.
[0085]
[0086]
(Все жидкие продукты реакции на первом этапе)
Все продукты реакции А-G на первом этапе были соответственно поданы в охлаждаемую ловушку при 10°С и нормальном давлении, а все жидкофазные продукты реакции Н-N на первом этапе были получены сжижением. В таблице 14 показаны конкретные условия реакции для пробных примеров с 5-8 по 5-14 и процентное содержание всех жидкофазных продуктов реакции Н-N.
[0087]
[0088]
(Продукты реакции обезвоживания жидкой фазы на первом этапе)
Все жидкофазные продукты реакции I-N на первом этапе соответствующим образом пропустили через ректификационную колонну, из которой путем удаления в основном непрореагировавшего этанола и воды как продукта реакции получили продукты обезвоживания О-Т жидкой фазы на первом этапе. В таблице 15 показаны конкретные условия для пробных примеров с 5-15 по 5-20 и процентное содержание всех продуктов реакции обезвоживания О-Т жидкой фазы.
[0089]
[0090]
(Реакция гидрирования на втором этапе)
Представляющие интерес композиции, содержащие алканы, были получены путем проведения реакции гидрирования с использованием всех продуктов реакции на первом этапе (В, С, D, F, G), всех жидкофазных продуктов реакции на первом этапе (I, J, K, М) и продуктов реакции обезвоживания жидкой фазы на первом этапе (О, Р, Q, S) в качестве соответствующего исходного вещества и с использованием в качестве никелевого катализатора Ренея, палладиевого катализатора или медного катализатора Ренея. Для реакций использовали проточный реактор с неподвижным слоем.
[0091]
При использовании всех продуктов реакции на первом этапе (В, С, D, F, G) в качестве исходного вещества реактор для второго этапа был встроен в последнюю часть реактора для первого этапа, и никелевый катализатор Ренея, палладиевый катализатор или медный катализатор Ренея загрузили в кварцевую реакционную трубу с внутренним диаметром 5 мм и использовали в качестве катализатора второго этапа. Сверху реакционной трубы подавали газ водород с расходом 50 мл/мин и смешивали его с газом, который прошел через реактор первого этапа, смешанный газ затем вводили в реакционную трубу. Композиции, полученные реакцией гидрирования, проанализировали. Когда все жидкофазные продукты реакции (I, J, K, М)на первом этапе и продукты реакции обезвоживания жидкой фазы (О, Р, Q, S) на первом этапе использовали в качестве исходных веществ, никелевый катализатор Ренея, палладиевый катализатор или медный катализатор Ренея загрузили в реакционную трубу с внутренним диаметром 10 мм (SUS) для использования в качестве катализатора второго этапа. Все жидкофазные продукты реакции (I, J, K, М) на первом этапе и продукты реакции обезвоживания жидкой фазы (О, Р, Q, S) на первом этапе соответствующим образом газифицировали с помощью карбюратора сверху реакционной трубы и добавили газ водород и газ-носитель гелий с расходом 50 мл/мин и 40 мл/мин соответственно. Композиции, полученные реакцией гидрирования, проанализировали. В таблице 16 показаны конкретные условия реакции и процентное содержание композиций, полученных реакцией гидрирования на втором этапе. Кроме того, в проверке реакции гидрирования на легкий газ был встроен другой реактор для второго этапа, при этом в качестве катализатора второго этапа в кварцевую реакционную трубу с внутренним диаметром 5 мм загрузили никелевый катализатор Ренея или медный катализатор Ренея. Затем сверху реакционной трубы подали газ водород с расходом 50 мл/мин и легкий газ, образовавшийся на первом этапе (J-абгаз, K-абгаз, L-абгаз, М-абгаз, N-абгаз), подвергли реакции гидрирования. Полученные таким образом композиции проанализировали. В таблице 17 показаны конкретные условия реакции и процентное содержание композиций, полученных реакцией гидрирования на втором этапе.

Промышленная применимость
[0093]
Способ получения композиций по настоящему изобретению обеспечивает получение композиций, содержащих алканы или спирты, которые полезны в качестве химического промышленного материала или топливной композиции, путем использования спиртов, например этанола, в качестве исходного вещества. А именно способ обеспечивает получение топливной композиции для двигателя внутреннего сгорания, имеющей значительно повышенную устойчивость к окислению, сниженное образование смол и высокую теплотворную способность. Кроме того, могут быть получены с высоким выходом спирты, такие как бутанол, гексанол и октанол.
Реферат
Настоящее изобретение относится к способу получения композиций, содержащих органические соединения и пригодных в качестве химического промышленного материала или топливной композиции с использованием спирта, например этанола в качестве исходного вещества. Способ получения содержит первый этап, на котором обеспечивают контакт по меньшей мере одного спирта, выбранного из метанола, этанола, пропанола, бутанола, пентанола, гексанола, гептанола и октанола, по меньшей мере с одним катализатором превращения спирта, выбранным из фосфата и глинистого минерала. Катализатор превращения спирта одновременно вызывает обезвоживание и дегидрирование спирта. Далее способ получения содержит второй этап, на котором продукт, полученный на первом этапе, подвергают реакции гидрирования, чтобы получить композицию. При этом полученная композиция содержит по меньшей мере один компонент, выбранный из группы, состоящей из парафинов и спиртов. Изобретение также относится к композициям, которые получены указанным способом и применяются в качестве топливных композиций для двигателей внутреннего сгорания. 8 н. и 45 з.п. ф-лы, 1 ил., 17 табл., 5 пр.

Комментарии