Ванадийфосфатные соединения - RU2263069C2
Код документа: RU2263069C2
Описание
Настоящее изобретение относится к катализаторам для осуществления селективного окисления углеводородного сырья, более конкретно к ванадийфосфатным соединениям, представляющим собой предшественник ванадийфосфатных катализаторов для селективного окисления углеводородного сырья, в частности селективного окисления бутана до малеинового ангидрида. Одним из катализаторов, показывающих высокую каталитическую активность, является пирофосфат ванадия ((VO)2P2O7), который обычно получают термическим превращением VOHPO4·1/2H2O. Фосфат ванадила может быть получен с использованием известных способов, которые раскрыты в публикации G.J.Hutchings, C.J.Kiely, M.T.Sananes-SchuIz, y A.Burrows и J.C.Volta, Catalysis Today 40 (1998) 372. Первый способ представляет собой восстановление V2O5 водной HCl с последующим превращением реакцией с Н3PO4 с образованием VOHPO4·1/2H2O. Второй способ включает восстановление V2O5 изобутанолом в присутствии Н3PO4. Еще один способ относится к двухстадийному процессу, в котором VOPO4·2H2O получают из V2O5 и Н3PO4 в водной среде с стоследующим восстановлением VOPO4·2H2O до VOHPO4·1/2H2O в изобутаноле. Современный подход, включающий водные способы, включает не только HCl как восстанавливающий агент, но также, например, щавелевую кислоту (немецкая заявка на патент DE 19645066 А1), Н3РО3 (патент DD 256659 А1) и гидразин (японская заявка на патент 59132938).
Задачей изобретения является представление высокоактивных предшественников ванадийфосфатных катализаторов для селективного окисления углеводородного сырья.
Поставленная задача решается предлагаемым ванадийфосфатным соединением β-VOHPO4·2H2O, характеризующимся порошковой дифракцией рентгеновских лучей, показывающих моноклинную ячейку с пространственной группой Р21/с, а=6,90 Å; b=7,36 Å; с=9,27 Å; β=104,8°; V=455,3 Å3 , где а, b, с, β, V - параметры моноклинной ячейки, а также ванадийфосфатным соединением (VO)3(PO4)2·5Н2O, характеризующимся порошковой дифракцией рентгеновских лучей, показывающих моноклинную ячейку с пространственной группой P21/c, а=19,77 Å; b=7,303 Å; с=9,226 Å; β=100,07°; V=1311,5 Å3, где а, b, с, β, V - параметры моноклинной ячейки.
Предлагаемые ванадийфосфатные соединения можно использовать как таковые или же перед применением превращать до VOHPO4·1/2H2O.
Предлагаемые ванадийфосфатные соединения можно получать известными приемами. Так, например, их получают в смесях муравьиной кислоты и воды, которые способны восстанавливать ванадий (V) до ванадия (IV). В общем, использование муравьиной кислоты в получении фосфатов ванадия как катализаторов окисления известно специалистам, как раскрыто, например, в патенте US 4016105, в котором муравьиную кислоту используют в сочетании со вторичным спиртом. Другой подход раскрыт в японской заявке на патент 53060391, описывающей смеси муравьиной кислоты и воды, содержащие соединения железа (Fe), предпочтительно, в сочетании с носителем. Аналогично патенты US 4388221, 4481363, 4562269, 4599477, 4639530 и 4801567 описывают восстановление V (V) смесями муравьиной кислоты и воды, содержащими олово (Sn) (II), с целью получения нанесенных на носитель катализаторов для окисления углеводородов от С4 до С10 в малеиновый ангидрид (патенты US 4388221, 4481363, 4562269, 4639530, 4801567) или нанесенных на носитель катализаторов для окислительного дегидрогенирования моноолефинов от С4 до C8 (патент US 4599477). В патенте US 4179404 описано применение муравьиной кислоты в менее чем стехиометрическом количестве, чтобы предотвратить 100% восстановление ванадия (V) до ванадия (IV). Другая методология раскрыта в европейской заявке на патент ЕР 0071140. Получение предшественника катализатора включает две стадии: синтез фосфата ванадия (V) и последующее восстановлением V (V) до V (IV) с использованием, например, смесей муравьиной кислоты и воды, дающее смешанный ванадийфосфороксид.
В нижеследующем описываются предпочтительные способы получения предлагаемых ванадийфосфатных соединений.
Синтез предшественников VOHPO4·1/2H2O, β-VOHPO4·H2O и (VO)3(PO4)2·5Н2O.
Настоящее изобретение основано на том, что различные продукты могут быть выделены из реакционных смесей, содержащих соединение ванадия и соединение фосфора в растворителе муравьиная кислота - вода. Таким образом, состав реакционной смеси и особенное проведение экспериментального метода решающим образом влияют на образование продукта. Подходящими соединениями ванадия (V) в этих способах являются V2O5, соли, содержащие структуру VO3-, такие как NH4VO3, и соли, содержащие структуру VO3+ такие как VOPO4·2H2O. Однако предпочтительна V2O5. Подходящими соединениями фосфора Р (V) являются Н3PO4 и Р2O5. Однако предпочтительна Н3PO4. Могут различаться три основных способа, включающие предпочтительные исходные соединения:
Способ А. Реакционную смесь, содержащую V2O5, Н3PO4, НСООН и Н2О, нагревают с обратным холодильником до кипения определенный период времени.
Способ Б. Реакционную смесь, содержащую V2O5, НСООН и Н2О, нагревают с обратным холодильником до кипения определенный период времени; Н3PO4 добавляют позднее.
Способ В. Реакционную смесь, содержащую V2O5, НСООН и Н3PO4, нагревают с обратным холодильником до кипения определенный период времени; Н2О добавляют позднее.
В качестве основного экспериментального метода с использованием муравьиной кислоты согласно способу А реагенты смешивают при комнатной температуре и затем кипятят с обратным холодильником период времени в интервале 20-170 часов. Полученный продукт выделяют фильтрованием, промывают водой и сушат ночь при 110°С. Обзор методов получения, включающий две ссылки, представлен в Таблице 1. В ссылках вещество получали согласно методам, уже известным специалистам, то есть с использованием смеси изобутанола и бензилового спирта (R-1, ср. патент США US 4132670) и с использованием водной HCl (R-2, C.J.Kiely, A.Burrows, S.Sajip, G.J.Hutchings, M.T.Sananes, A.Tuel и J.C.Volta, J. Catal. 162 (1996) 31).
Приложенная Таблица 1 показывает полное восстановление ванадия (V) до ванадия (IV) в смесях муравьиной кислоты и воды, имеющих концентрацию муравьиной кислоты от 5% (Р-15) до 91% (Р-2, 3, 4). Неполное восстановление наблюдается в отсутствии воды (Р-1), как представляется из среднего окислительного состояния ванадия (4,52). Метод порошковой дифракции рентгеновских лучей показывает присутствие VOHPO4·1/2H2O и (VO)(VO2)2H4(PO4)2(P2 O7)0,5×H2O (0,01<×<2). Последнее соединение известно специалистам (патент США 4374756) и, как запатентовано, полезно в частичном окислении углеводородов. Влияние воды на восстановление V2O5 может быть объяснено с учетом того, что на протеолитическое равновесие Н3PO4 и НСООН сильно влияет энергетически благоприятное гидратирование протонов водой (ур. 1 и 2). Повышение концентрации Н+ благоприятствует восстановлению V2O5, как это видно из уравнения окисления-восстановления (3). Ванадий присутствует как VO2+ при рН около 2,0 (C.F.Tsang, J.Kim и A.Manthiram, J. Mater. Chem. 8 (1998) 425).
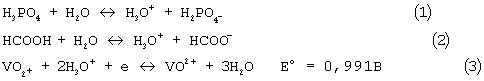
Как видно из Таблицы 1, состав реакционной смеси не только влияет на степень восстановления, но также и на кристаллизацию получаемого фосфата ванадия. Образование VOHPO4·1/2H2O наблюдается в реакционных смесях, содержащих от 35% до 91% муравьиной кислоты. Продукты анализировали методами, которые хорошо известны специалистам, то есть порошковой дифракции рентгеновских лучей, элементного анализа, спектроскопии комбинационного рассеяния и Брунауэра-Эммета-Теллера. Анализ на Р и V Р-3, 5, 6, 10 показывает приемлемое согласие с ожидаемыми величинами для VOHPO4·1/2H2O. На основе порошковой дифракции рентгеновских лучей были рассчитаны размеры кристаллитов (D001) полученных VOHPO4·1/2H2O и было найдено, что они больше 300 Å. Спектроскопия комбинационного рассеяния показывает присутствие неизвестной фазы Х в образцах Р-2, 5, 6, не наблюдаемой порошковой дифракцией рентгеновских лучей. Эта фаза, вероятно, ответственна за цвет продуктов, который был зелено-серым вместо ожидаемого голубого цвета. Продукт Р-10 был чистым VOHPO4·1/2H2O. Приготовление в 91% муравьиной кислоте, включающее способы А (Р-2), Б (Р-3) и В (Р-4), показывает, что VOHPO4·1/2H2O получают независимо от специфического метода. Специалистам будет понятно, что для практической выгоды предпочтителен только способ А, а не способы Б и В. Это явно ни ограничивает, ни исключает применение способов Б и В в большом интервале смесей муравьиной кислоты и воды. Более того, специалистам будет понятно, что в способе Б полное восстановление ванадия (V) до ванадия (IV) предшествует реакции с Н3PO4. Чтобы доказать это, был выделен и подробно охарактеризован продукт, полученный согласно способу Б после полного восстановления V (V) до V (IV) в отсутствии Н3РО4. Порошковая дифракция рентгеновских лучей показала чистую фазу, характеризующуюся моноклинной ячейкой (а=8,474 Å, b=8,385 Å, с=7,409 Å, β=90,44°) и пространственной группой Р21/с. Обзор данных порошковой дифракции рентгеновских лучей представлен в приложенной Таблице 2.
Кроме того, элементный анализ ясно показал образование VO(HCOO)2·11/2H2O (рассчитано С 13,06%; Н 2,74%; V 27,69%, найдено С 12,8%; Н 2,84%; V 28,5%), которое известно в литературе (Gmelins Handbuch der Anorganischen Chemie, ванадий, часть Б, издательство Шпрингер, Вайнхайм, 1967, страница 345). Таким образом, очевидно, что способ Б фактически является эквивалентом способу, в котором соединение ванадия (IV) реагирует с Н3PO4 в определенной смеси муравьиной кислоты и воды. Это заключение поддерживается экспериментом, использующим "VO2", то есть оксид, содержащий ванадий в среднем окислительном состоянии, существенно ниже 5 (V7O13, V4O9, VO2 вместо V2O5 P-18, см. ниже). Получение VOHPO4·1/2H2O также возможно в присутствии агентов кристаллизации наподобие H2SO4 (Р-7), Н3CSO3Н (Р-8) и п-толуолсульфокислоты (Р-9). Использование этих материалов хорошо известно специалистам (P.U.Wolf, U.Rodemerck, A.Brückner, M.Meisel и B.Kubias, Catal. Lett. 46 (1997) 113) и имеет существенное влияние на каталитическую активность (см. ниже). Иные продукты, отличные от VOHPO4·1/2H2O, наблюдали в реакционных смесях, содержащих 5-27% муравьиной кислоты. В 27%-ной муравьиной кислоте (Р-12) наблюдали кристаллизацию нового соединения (VO)3(PO4)2·5Н2O. Этот продукт был охарактеризован порошковой дифракцией рентгеновских лучей, показавшей моноклинную ячейку с пространственной группой P21/c (a=19,77 Å, b=7,303 Å, с=9,226 Å, β=100,07°). Обзор данных порошковой дифракции рентгеновских лучей представлен в приложенной Таблице 3.
ТГА (термогравиметрический анализ) Р-12 дает потерю массы 21,12% из-за дегидратации: 3,73% между 60 и 120°С за счет физически сорбированной воды и 17,39% между 120 и 500°С за счет кристаллизационной воды. Это объясняет, что результаты элементного анализа (Таблица 1) находятся в соответствии с составом (VO)3(PO4)2·6Н2O (расч. V 30,63%, Р 12,42%). Однако ТГА дает решающее свидетельство приписывать химический состав Р-12 химической формуле (VO)3(PO4)2·5Н2O. Хотя образование (VO)3(PO4)2·5Н2O также наблюдали в 5%-ной муравьиной кислоте (Р-15), было найдено, что на процесс кристаллизации в 27%-ной муравьиной кислоте может влиять добавление H2SO4 как агента кристаллизации. Этот процесс дает новое соединение β-VOHPO4·H2O (Р-13), которое структурно ясно отличается от модификаций VOHPO4·Н2О, описанных в литературе. В литературе указаны три типа VOHPO4·H2O, обозначенные здесь αI- (P.Amoros, R.Ibanez, E.Martinez-Tamayo, D.Beltran-Porter, A.Beltran-Porter, Mater.Res. Bull. 24 (1989) 1347), αII- (D.Beltran-Porter, A.Beltran-Porter, P.Amoros, R.Ibanez, E.Martinez, A.Le Bail, G.Ferey и G.Villeneuve, Eur. J. Solid St. Inorg. Chem. 28 (1991) 131), и αIII-VOHPO4·H2O (V.V.Gulliants, J.B.Benziger, S.Sundaresan, I.E.Wachs, J.M.Jehng и J.E.Roberts, Catal. Today 28 (1996) 275). Постоянные решеток различных систем, включающие нашу модификацию, представлены в приложенной Таблице 4, в то время как приложенная Таблица 5 дает обзор данных порошковой дифракции рентгеновских лучей Р-13.
Специалистам будет понятно, что анализ порошковой дифракции рентгеновских лучей недвусмысленно показывает структурное разнообразие модификаций VOHPO4·2H2O, указанных в Таблице 4. Элементный анализ (расч. V 28,2%, Р-17,1%, смотри таблицу 1) и ТГА были использованы для определения элементного состава β-VOHPO4·2H2O. ТГА показывает потерю веса 14,82% относительно дегидратации, тогда как ожидалось 14,94% для конверсии VOHPO4·2H2O в (VO)2P2О7. Таким образом, как ТГА, так и элементный анализ недвусмысленно подтверждают элементный состав β-VOHPO4·2H2O.
Независимо от получения с использованием V2O5 и Н3PO4 можно также использовать другие исходные материалы. Обзор способов с альтернативными исходными материалами V и Р представлен в приложенной Таблице 6.
Таблица 6 показывает выгодность альтернативных исходных материалов в процессах получения в соответствии со способом А, как подчеркивалось выше. Показано, что вместо V2О5 могут быть использованы для получения VOHPO4·1/2H2O в смесях муравьиной кислоты и воды соединения ванадия наподобие NH4VO3 (P-16), VOPO4·2H2O (Р-17) и "VO2" (Р-18). Необходимо заметить, что получение с использованием NH4VO3 (P-16) требует добавки H2 SO4 как агента кристаллизации. Кроме того, получение, исходя из VOPO4·2H2O (Р-17), требует добавки Н3PO4, чтобы избежать нежелательной кристаллизации VO(HCOO)2·11/2Н2O. Получение, включающее "VO2" (Р-18), подразумевает использование оксидов ванадия, содержащих ванадий в среднем окислительном состоянии существенно ниже 5, и включает, например, V7O13, V4O9, VO2. Только для краткости эти окислы или смеси их обозначают "VO2". Получение с VO2 (Р-18) показывает, что успешное использование смесей муравьиной кислоты и воды не зависит от степени восстановления, имеющей место в течение этого процесса. Относительно соединений Р было показано, что вместо Н3PO4 можно использовать P2O5 (Р-19). Это соответствует ожиданиям, так как P2 O5 превращается в Н3РО4 при реакции с водой. Применение β-VOHPO4·2H2O как предшественника для получения VOHPO4·1/2H2O было инициировано наблюдением, что применение непосредственно β-VOHPO4·2H2O как предшественника для селективного окисления бутана в малеиновый ангидрид не приводило к улучшению дела (см. ниже). Неожиданно было найдено, что β-VOHPO4·2H2O (Р-13) можно превратить в VOHPO4·1/2H2O (P-20) посредством процесса рекристаллизации в уксусной кислоте. Таким образом, новый предшественник P-20 был получен из β-VOHPO4· 2H2O (Р-13), показывая интересные каталитические свойства (см. ниже). Другая цель настоящего изобретения состоит в том, что принцип рекристаллизации может быть применен не только к β -VOHPO4·2H2O, но также и к (VO)3(PO4)2·5Н2O (Р-12, Р-14, Р-15). Специалистам хорошо известно, что лучшие промышленные ванадийфосфатные катализаторы имеют атомное отношение P/V немного выше единицы (D.Wang, M.C.Kung и H.H.Kung, Catal. Lett. 65 (2000) 9). Исследования, включающие предшественники с отношением P/V менее 1, показали, что это оказывает отрицательное влияние как на конверсию бутана, так и на селективность образования малеинового ангидрида. (N.Yamazoe, H.Morishige и Y.Teraoka, Stud. Surf. Sci. Catal. 44 (1988) 15). Так, (VO)3(PO4)2·5Н2O является невыгодным предшественником катализатора с атомным отношением P/V, равным 0,67. В этом отношении превращение (VO)3(PO4)2·5Н2O реакцией с Н3PO4 в VOHPO4·1/2H2O в уксусной кислоте (Р-21) является очень интересным. Более того, было показано, что превращение (VO)3(PO4)2·5Н2O в VOHPO4·1/2H2O может также быть проведено с использованием 60%-ной муравьиной кислоты (Р-22). Таким образом, интересующие предшественники катализаторов могут быть получены в смесях муравьиной кислоты и воды, содержащих 91-5% муравьиной кислоты, если это применять в сочетании с процессом рекристаллизации.
Резюмируя, мы показали успешное получение VOHPO4·1/2H2O или β- VOHPO4·2H2O или (VO)3(PO4)2·5Н2O с использованием:
1)способов А, Б, В;
2) смесей муравьиной кислоты и воды с содержанием муравьиной кислоты 91-5%;
3) V2O5, NH4VO3, VO2 и VOPO4·2H2O как предшественников соединений ванадия;
4) P2O5 и Н3PO4 как предшественников соединений фосфора;
5) рекристаллизацией β-VOHPO4·2H2O (с использованием уксусной кислоты) и (VO)3(PO4)2·5Н2O (с использованием уксусной кислоты или смеси муравьиной кислоты и воды).
Каталитическая активность предшественников VOHPO4·1/2H2O, β-VOHPO4·2H2O или (VO)3(PO4)2·5Н2O.
Каталитическую активность предшественников VOHPO4 ·1/2H2O или β-VOHPO4·2H2O рассчитывали относительно селективного окисления бутана. Предшественники прессовали в таблетки после того, как получали их просеянную фракцию 0,3-0,7 мм. Этот материал активировали в соответствии с общими принципами, раскрытыми в патенте США US 4132670, то есть окислительным кальцинированием на воздухе с последующим приведением в равновесие с подаваемым газом.
Условия активации были следующими:
- нагревание на воздухе 1 час при данной температуре;
- конверсия газа до 1,29% н-бутана в искусственном воздухе с потоком 100 мл/мин·г,
- нагревание до данной равновесной температуры за 17 часов;
- охлаждение до 400°С и измерение каталитической активности при объемной скорости 6000 ч-1.
Анализ каталитической активности различных предшественников, включая ссылки, представлен в приложенной Таблице 7 и в приложенном чертеже.
Чертеж и Таблица 7 показывают явное улучшение каталитической активности большинства предшественников, полученных из процесса в муравьиной кислоте по сравнению с R-1 (современный спиртовый катализатор) и R-2 (современный водный катализатор). Низкая активность Р-13 показывает, что β-VOHPO4·2H2O не может быть использован как предшественник катализатора. Р-3, Р-16 и Р-22 показывают невысокую активность, которая еще сравнима с R-1 и явно лучше, чем у R-2. Следовательно, очевидно, что процессы получения в соответствии с Р-3, Р-16 и Р-22 менее предпочтительны. Обычно с предшественниками в муравьиной кислоте наблюдали селективность по малеиновому ангидриду 60%, которая слегка выше, чем R-1. Однако высокую селективность поддерживают при уровнях конверсии между 47 и 84%. Это является критическим свойством предшественников, полученных в муравьиной кислоте, которое очевидно из 14 предшественников, показанных в Таблице 7 и чертеже. Таким образом, целый ряд процессов может быть использован для получения предшественников, являющихся существенно более активными по сравнению с настоящим состоянием дел по ссылкам.
Примеры
Пример 1
Способ А, общий метод: синтез Р-2.
Суспензию V2O5 (9,10 г) нагревали при кипячении с обратным холодильником 44 ч в смеси муравьиной кислоты (250 мл), Н3PO4 (7,5 мл) и воды (25 мл). Затем зелено-серую суспензию охлаждали до комнатной температуры и фильтровали. Зеленовато-серое твердое вещество промывали водой и сушили при 110°С 16 часов.
Пример 2
Способ Б: синтез Р-3.
Суспензию V2O5 (3,64 г) нагревали при кипячении с обратным холодильником 72 ч в смеси муравьиной кислоты (100 мл) и воды (10 мл). Затем добавляли к темно-зеленой суспензии 1 мл Н3PO4 и кипячение продолжали 24 ч. Затем синюю суспензию охлаждали до комнатной температуры и фильтровали. Синее твердое вещество промывали водой и сушили при 110°С 16 часов.
Пример 3
Способ В: синтез Р-4.
Суспензию V2O5 (1,82 г) нагревали при кипячении с обратным холодильником 144 ч в смеси муравьиной кислоты (50 мл) и Н3 PO4 (1,5 мл). Затем добавляли H2O (5 мл) к зеленой суспензии и кипячение продолжали 20 часов. Затем синюю суспензию охлаждали до комнатной температуры и фильтровали. Синее твердое вещество промывали водой и сушили при 110°С 16 часов.
Пример 4
Конверсия β-VOHPO4·2H2O (Р-13) в VOHPO4 ·1/2H2O (P-20). Суспензию β-VOHPO4·2H2O (11,60 г) в уксусной кислоте (400 мл) нагревали до кипения с обратным холодильником 20 часов. Светло-зеленую суспензию охлаждали до комнатной температуры и фильтровали. Слегка зеленовато-серое твердое вещество промывали водой и сушили при 110°С 16 часов.
Пример 5
Конверсия (VO)3(PO4)2·5Н2O (Р-12) в VOHPO4·1/2H2O (P-22). Суспензию (VO)3(PO4)2·5Н2O (3,21 г) в смеси Н3PO4 (590 мкл) и 60%-ной муравьиной кислоты (100 мл) нагревали до кипения с обратным холодильником 20 часов. Голубую суспензию охлаждали до комнатной температуры и фильтровали. Синее твердое вещество промывали водой и сушили при 110°С 16 часов.
Хотя характер этого изобретения описан с многочисленными примерами, это было сделано только как иллюстрация и без ограничения изобретения. Специалистам будет очевидно, что определенные особенности изобретения могут быть изменены, хотя они остаются внутри основного духа изобретения, который более точно определен в следующих пунктах формулы изобретения.
Реферат
Заявленное изобретение относится к ванадийфосфатному соединению β-VOHPO4*Н2О, характеризующемуся порошковой дифракцией рентгеновских лучей, показывающих моноклинную ячейку с пространственной группой P21/c, а-6,90 Å; b=7,36 Å; с=9,27 Å; β=104,8°; V=455,3 Å3, где а, b, с, β, V - параметры моноклинной ячейки. Изобретение также относится к ванадийфосфатному соединению (VO)3(PO4)3*5H2О, характеризующемуся порошковой дифракцией рентгеновских лучей, показывающих моноклинную ячейку с пространственной группой Р21/с, а=19,77 Å; b=7,303 Å; с-9,226 Å; β=104,07°; V=1311,5 Å3, где а, b, с, β, V - параметры моноклинной ячейки. Задачей изобретения является представление высокоактивных предшественников ванадийфосфатных катализаторов для селективного окисления углеводородного сырья. 2 н.п., 7 табл., 1 ил.


Комментарии