Катализатор дегидрирования метанола, используемый для получения метилформиата, и способ получения метилформиата - RU2489208C2
Код документа: RU2489208C2
Описание
Область техники, к которой относится изобретение
Настоящее изобретение относится к катализатору, используемому для получения метилформиата реакцией дегидрирования метанола в газовой фазе, и к способу получения метилформиата с использованием этого катализатора.
Уровень техники
Метилформиат получают как промежуточный продукт в органическом синтезе, и он является важным сырьевым материалом для промышленного получения высокочистого монооксида углерода, муравьиной кислоты, формальдегида, уксусной кислоты, N,N-диметилформамида и тому подобных.
В литературе описано большое число катализаторов для синтеза метилформиата дегидрированием метанола в газовой фазе. Большинство катализаторов сформировано на основе меди в качестве основного компонента. Например, Патентный Документ 1 раскрывает катализатор, состоящий из меди, цинка, циркония и алюминия, а Патентный Документ 2 представляет катализатор, состоящий из оксида меди, оксида цинка и оксида алюминия.
Также предложены катализаторы, каждый из которых содержит сокатализатор. Например, Патентный Документ 3 раскрывает способ получения катализатора добавлением фосфата меди или тому подобного, хлорида щелочного металла, щелочноземельного металла или тому подобного, и соединения щелочного металла или щелочноземельного металла, за исключением галогенидов, к смеси оксида меди, оксида цинка и оксида алюминия. Патентный Документ 4 представляет катализатор, состоящий из оксидов меди, цинка и алюминия, соединения фосфорной кислоты и двух или более видов соединений щелочных металлов, включающих литий.
В катализаторе, описанном в Патентном Документе 1 или 2, среди других катализаторов, содержание меди должно быть повышено для улучшения выхода и селективности образования метилформиата. Поэтому механическая прочность катализатора после восстановительной активации значительно снижается.
Согласно способу, описанному в Патентном Документе 3, отмечено, что получение катализатора, имеющего высокую механическую прочность даже после восстановительной активации, и обеспечивающего высокие выход и селективность образования метанола, может быть достигнуто действием добавки. Для катализатора, описанного в Патентном Документе 4, еще больше повышены начальная активность и селективность образования метилформиата, и предполагается, что это главным образом обусловлено действием, которое достигнуто добавлением лития.
Однако для практического применения таких катализаторов требуется дополнительное усовершенствование в плане селективности образования метилформиата, долговечности и термостойкости.
Прототипные документы
Патентные документы
[Патентный документ 1] JP-А-53-71008
[Патентный документ 2] JP-А-54-12315
[Патентный документ 3] JP-А-58-163444
[Патентный документ 4] JP-А-3-151047
Сущность изобретения
Техническая проблема
Цель настоящего изобретения состоит в том, чтобы предложить катализатор дегидрирования метанола, используемый для получения метилформиата, который обеспечивает высокую селективность образования метанола и имеет превосходные долговечность и термостойкость, и способ получения метилформиата с использованием катализатора.
Разрешение проблемы
Авторы настоящего изобретения провели обширные исследования катализатора, который сформирован на основе оксидов меди, цинка и алюминия, соединения фосфорной кислоты и соединения щелочного металла, чтобы разрешить вышеупомянутую проблему. В результате авторы настоящего изобретения нашли, что катализатор, содержащий бромид щелочного металла в качестве соединения щелочного металла, обеспечивает явно более высокую селективность образования метилформиата, чем традиционный катализатор, содержащий хлорид щелочного металла в качестве соединения щелочного металла, и имеет превосходные долговечность и термостойкость, то есть малые степени сокращения срока службы и термостойкости со временем при испытании на продолжительность срока службы и испытании на термостойкость. Таким образом было создано настоящее изобретение.
То есть настоящее изобретение представляет собой следующее:
катализатор дегидрирования метанола, используемый для получения метилформиата, который содержит оксиды меди, цинка и алюминия, соединение фосфорной кислоты и бромид щелочного металла; и способ получения метилформиата, включающий стадию, в которой проводят дегидрирование метанола в газовой фазе с использованием такого катализатора.
Преимущества, обеспечиваемые изобретением
Катализатор согласно настоящему изобретению имеет превосходные долговечность и термостойкость и обеспечивает высокую селективность образования метилформиата. Дегидрированием метанола в газовой фазе с помощью катализатора согласно настоящему изобретению метилформиат может быть получен с высокой селективностью при высоком выходе.
Описание вариантов исполнения
Катализатор согласно настоящему изобретению проявляет активность, в особенности высокую селективность образования метилформиата и термостойкость, в получении метилформиата дегидрированием метанола в газовой фазе. Как представляется, причина того, что получен такой эффект, обусловливается содержанием бромида щелочного металла в качестве соединения щелочного металла. Причина того, что катализатор, содержащий бромид щелочного металла в качестве соединения щелочного металла, превосходит катализатор, содержащий хлорид щелочного металла, в отношении селективности образования метилформиата и термостойкости неизвестна. Однако представляются возможными следующие обоснования.
(1) Катализатор, содержащий бромид щелочного металла, имеет более низкую степень возгонки галогена во время реакции, чем катализатор, содержащий хлорид щелочного металла. Поэтому возрастание реакционной активности в отношении разложения метилформиата щелочным металлом в качестве побочной реакции подавляется переносом электрона с галогена на щелочный металл, что приводит к высокой селективности образования.
(2) Катализатор, содержащий бромид щелочного металла, вряд ли изменяет свой состав даже во время реакции. Поэтому практически не происходит разрушения на поверхности катализатора, чем улучшается термостойкость.
Способ получения оксидов меди, цинка и алюминия в качестве основы каталитического компонента в катализаторе согласно настоящему изобретению не является специально ограниченным, если медный, цинковый и алюминиевый каталитические компоненты однородно смешаны между собой. Для получения однородной смеси медного, цинкового и алюминиевого каталитических компонентов, может быть использован, например, способ, в котором, например, водный раствор водорастворимой соли каждого каталитического компонента и щелочный водный раствор смешивают друг с другом для получения осадков, и затем осадки смешивают между собой; способ, в котором проводят совместное осаждение осадков из водорастворимых солей двух каталитических компонентов из меди, цинка и алюминия, и осадок другого (оставшегося) каталитического компонента смешивают с совместным осадком, и способ, в котором получают совместный осадок водорастворимых солей трех каталитических компонентов меди, цинка и алюминия. Следует отметить, что осадок или совместный осадок каждого каталитического компонента не обязательно должен быть оксидом в стадии осаждения или совместного осаждения, если он может быть преобразован в оксид при последующей стадии высушивания или обжига (прекурсор оксида).
В качестве сырьевого материала, который может превращаться в оксид меди, могут быть использованы, например, водорастворимые органические соли, такие как ацетат меди, или водорастворимые неорганические соли, такие как хлорид меди, сульфат меди и нитрат меди.
В качестве сырьевого материала, который может превращаться в оксид цинка, могут быть использованы, например, оксид цинка и водорастворимые органические соли, такие как ацетат цинка, или водорастворимые неорганические соли, такие как хлорид цинка, сульфат цинка и нитрат цинка.
В качестве сырьевого материала, который может превращаться в оксид алюминия, могут быть использованы, например, в дополнение к оксиду алюминия и золю оксида алюминия, водорастворимые органические соли, такие как ацетат алюминия, или водорастворимые неорганические соли, такие как хлорид алюминия, сульфат алюминия и нитрат алюминия.
В качестве осаждающего реагента, используемого для получения осадка или совместного осадка, применяют, например, гидроксид щелочного металла, карбонат щелочного металла и бикарбонат щелочного металла, и конкретные примеры их включают гидроксид натрия, карбонат натрия, карбонат калия, бикарбонат натрия и бикарбонат аммония.
Катализатор дегидрирования метанола, используемый для получения метилформиата согласно настоящему изобретению, может быть получен добавлением соединения фосфорной кислоты и бромида щелочного металла к вышеупомянутым оксидам меди, цинка и алюминия или прекурсору оксида, и высушиванием и обжигом полученной смеси.
Способ добавления соединения фосфорной кислоты и бромида щелочного металла не является специально ограниченным, если они однородно смешаны друг с другом, и может представлять собой «мокрый» или «сухой» способ. Температура высушивания предпочтительно составляет от около 70 до 150°С, и температура обжига предпочтительно варьирует от около 350 до 650°С.
Катализатор согласно настоящему изобретению перед применением подвергают гранулированию. Перед реакцией предпочтительно проводят восстановление.
В качестве соединения фосфорной кислоты предпочтительно используют фосфат, моногидрофосфат, дигидрофосфат, пирофосфат или тому подобные соли меди, цинка или алюминия, и конкретные примеры их включают фосфат двухвалентной меди, пирофосфат меди, фосфат цинка, фосфат алюминия, моногидрофосфат алюминия и дигидрофосфат алюминия.
Примеры бромида щелочного металла включают бромид лития, бромид натрия и бромид калия. С позиции селективности образования метилформиата, термостойкости и долговечности предпочтительным является бромид лития или бромид натрия, и в особенности предпочтителен бромид натрия.
С позиции реакционной способности катализатора является предпочтительным, чтобы было проведено надлежащее спекание атома меди. «Спекание» означает то явление, что частицы катализатора образуют крупнозернистый агломерат. Когда частицы катализатора собираются в крупнозернистый агломерат, площадь контактной поверхности для реакции между частицами катализатора и метанолом сокращается, и число мест, служащих в качестве активных каталитических центров, уменьшается, в результате чего может падать степень превращения метанола. Между тем, надлежащее спекание ненамного сокращает площадь поверхности катализатора, тем самым обеспечивая возможность стабилизировать катализатор в плане устойчивости к окислению и тому подобного.
Из этих соображений, в том, что касается уровня содержания каждого компонента в катализаторе согласно настоящему изобретению, если общее число атомов меди, содержащейся в катализаторе, составляет 10, то атомное отношение цинка предпочтительно варьирует от 0,1 до 10, более предпочтительно от 0,15 до 5, и еще более предпочтительно от 0,2 до 2, и атомное отношение алюминия предпочтительно составляет от 0,1 до 10, более предпочтительно от 0,15 до 5, и еще более предпочтительно от 0,2 до 2. Кроме того, в отношении уровня содержания соединения фосфорной кислоты в катализаторе согласно настоящему изобретению, если общее число атомов меди, содержащейся в катализаторе, составляет 10, то атомное отношение фосфора предпочтительно составляет от 0,1 до 5, более предпочтительно от 0,15 до 5, и еще более предпочтительно от 0,2 до 2. Что касается уровня содержания бромида щелочного металла, то если общее число атомов меди, содержащейся в катализаторе, составляет 10, атомное отношение брома предпочтительно составляет от 0,02 до 0,5, более предпочтительно от 0,03 до 0,4, и в особенности предпочтительно от 0,05 до 0,3.
Следует отметить, что уровень содержания каждого компонента в оксидах меди, цинка и алюминия надлежащим образом определяют так, чтобы гарантировать, что уровень содержания каждого компонента в катализаторе согласно настоящему изобретению находится в пределах вышеуказанного диапазона с учетом числа атомов меди, цинка или алюминия, содержащихся в соединении фосфорной кислоты.
Метилформиат может быть получен с высокой селективностью при высоком выходе дегидрированием метанола в газовой фазе с использованием катализатора согласно настоящему изобретению. Условия реакции надлежащим образом определяют из соображений выхода метилформиата, стоимости производства и тому подобных. Температура реакции предпочтительно варьирует от 100 до 400°С, более предпочтительно от 150 до 350°С. Величина объемного расхода потока (среднечасовая скорость подачи газа: GHSV) метанола предпочтительно составляет от 100 до 100000/час, более предпочтительно от 500 до 30000/час. Реакционное давление предпочтительно составляет 5 МПа (избыточных) или менее, более предпочтительно 1 МПа (избыточный) или менее, и предпочтительно 0,01 МПа (избыточного) или более, более предпочтительно 0,1 МПа (избыточного) или более, в единицах манометрического давления.
Примеры
Нижеследующие примеры и сравнительные примеры приведены в целях дополнительного иллюстрирования настоящего изобретения, но никоим образом не должны толковаться как ограничивающие.
<Получение катализатора>
Пример 1
186,6 г (0,772 моля) тригидрата нитрата меди, 11,5 г (0,039 моля) гексагидрата нитрата цинка и 28,9 г (0,077 моля) нонагидрата нитрата алюминия растворяли в 1600 г деминерализованной ионным обменом воды и нагревали до температуры 40°С. Полученный раствор при температуре 40°С вливали в водный раствор, полученный растворением 108,0 г (1,019 моля) безводного карбоната натрия в 1600 г деминерализованной ионным обменом воды, в течение 1 минуты при перемешивании. Полученный раствор оставляли для старения с нагреванием при температуре 40ºС в течение 60 минут и дополнительно при температуре 80ºС в течение 30 минут, и осадок отделяли фильтрованием и промывали водой для получения 282 г совместного осадка.
К совместному осадку добавляли и тщательно перемешивали 20,3 г (0,020 моля в расчете на Al2O3) золя оксида алюминия с концентрацией 10% масс., 4,9 г (0,013 моля) фосфата двухвалентной меди, 2,5 г (0,006 моля) додекагидрата тринатрийфосфата и 0,8 г (0,008 моля) бромида натрия, и тестообразный продукт сушили при температуре 115ºС в течение 12 часов и затем подвергали обжигу при температуре 600ºС в течение 2 часов. Полученный оксид измельчали, к измельченному продукту добавили 3% масс. графита, и полученную смесь гранулировали в таблетировочной машине для получения катализатора в виде столбчатых таблеток, имеющих диаметр 6 мм и высоту 5,5 мм. По результатам элементного анализа, число атомов брома составляло 0,10 (атомное отношение), когда общее число атомов меди, содержащейся в полученном катализаторе, было равно 10. Для элементного анализа использовали эмиссионный спектральный анализ с индуктивно-связанной плазмой (ICP).
Пример 2
Катализатор получали в соответствии с методикой получения, описанной в Примере 1, за исключением того, что вместо 0,8 г бромида натрия добавляли 1,6 г (0,016 моля) бромида натрия. По результатам элементного анализа, число атомов брома составляло 0,20 (атомное отношение), когда общее число атомов меди, содержащейся в полученном катализаторе, было равно 10.
Пример 3
Катализатор получали в соответствии с методикой получения, описанной в Примере 1, за исключением того, что вместо 0,8 г бромида натрия добавляли 2,5 г (0,024 моля) бромида натрия. По результатам элементного анализа, число атомов брома составляло 0,30 (атомное отношение), когда общее число атомов меди, содержащейся в полученном катализаторе, было равно 10.
Пример 4
Катализатор получали в соответствии с методикой получения, описанной в Примере 1, за исключением того, что вместо 0,8 г бромида натрия добавляли 0,7 г (0,008 моля) бромида лития. По результатам элементного анализа, число атомов брома составляло 0,10 (атомное отношение), когда общее число атомов меди, содержащейся в полученном катализаторе, было равно 10.
Пример 5
Катализатор получали в соответствии с методикой получения, описанной в Примере 1, за исключением того, что вместо 0,8 г бромида натрия добавляли 1,0 г (0,008 моля) бромида калия. По результатам элементного анализа, число атомов брома составляло 0,10 (атомное отношение), когда общее число атомов меди, содержащейся в полученном катализаторе, было равно 10.
Сравнительный Пример 1
Катализатор получали в соответствии с методикой получения, описанной в Примере 1, за исключением того, что бромид натрия не добавляли.
Сравнительный Пример 2
Катализатор получали в соответствии с методикой получения, описанной в Примере 1, за исключением того, что вместо 0,8 г бромида натрия добавляли 0,34 г (0,008 моля) хлорида лития. По результатам элементного анализа, число атомов хлора составляло 0,10 (атомное отношение), когда общее число атомов меди, содержащейся в полученном катализаторе, было равно 10.
Сравнительный Пример 3
Катализатор получали в соответствии с методикой получения, описанной в Примере 1, за исключением того, что вместо 0,8 г бромида натрия добавляли 0,2 г (0,008 моля) фторида лития. По результатам элементного анализа, число атомов фтора составляло 0,10 (атомное отношение), когда общее число атомов меди, содержащейся в полученном катализаторе, было равно 10.
Сравнительный Пример 4
Катализатор получали в соответствии с методикой получения, описанной в Примере 1, за исключением того, что вместо 0,8 г бромида натрия добавляли 1,1 г (0,008 моля) иодида лития. По результатам элементного анализа, число атомов иода составляло 0,10 (атомное отношение), когда общее число атомов меди, содержащейся в полученном катализаторе, было равно 10.
Сравнительный Пример 5
Катализатор получали в соответствии с методикой получения, описанной в Примере 1, за исключением того, что вместо 0,8 г бромида натрия добавляли 0,5 г (0,008 моля) хлорида натрия. По результатам элементного анализа, число атомов хлора составляло 0,10 (атомное отношение), когда общее число атомов меди, содержащейся в полученном катализаторе, было равно 10.
<Испытание для первичной оценки катализатора (отборочное)>
Для оценки активности и термостойкости катализатора, измеряли степень конверсии метанола и селективность образования метилформиата в условиях более высокой температуры и более высокой среднечасовой скорости подачи газа (GHSV), чем при обычных условиях проведения реакции.
Более конкретно, полученную сформованную таблетку сначала измельчили, и просеиванием отобрали измельченные кусочки, имеющие размер от 20 до 30 меш. Измельченный продукт подвергли восстановлению при температуре 220ºС в потоке водорода, и 0,5 мл продукта взвесили и поместили в реакционную трубку, имеющую внутренний диаметр 6 мм. Реакцию проводили при контрольной реакционной температуре 360ºС, реакционном давлении 0,49 МПа (манометрическое), и среднечасовой скорости подачи метанола (GHSV) 100000/час в течение 20 часов, для измерения степени конверсии метанола и селективности образования метилформиата.
Степень превращения метанола (МеОН) и селективность образования метилформиата (MF) определяли по составу газа на выходе из реактора, основываясь на следующем уравнении. [СО], [СН4], [СО2], [DME], [МеОН] и [MF] в уравнении означают концентрации (в мольных процентах) монооксида углерода, метана, диоксида углерода, диметилового простого эфира, метанола и метилформиата в газе на выходе из реактора соответственно.
Степень превращения метанола (мольных процентов)
=([СО]+[СН4]+[СО2]+([DME]+[MF])Ч2)/
([СО]+[СН4]+[СО2]+([DME]+[MF])Ч2+[МеОН])Ч100
Селективность образования метилформиата (мольных процентов)
=([MF]Ч2)/([СО]+[СН4]+[СО2]+([DME]+[MF])Ч2)Ч100
Результаты испытания для первичной оценки катализаторов из Примеров 1-5 и Сравнительных Примеров 1-5 показаны в Таблице 1. Значения представляют собой средние величины в течение 20 часов.
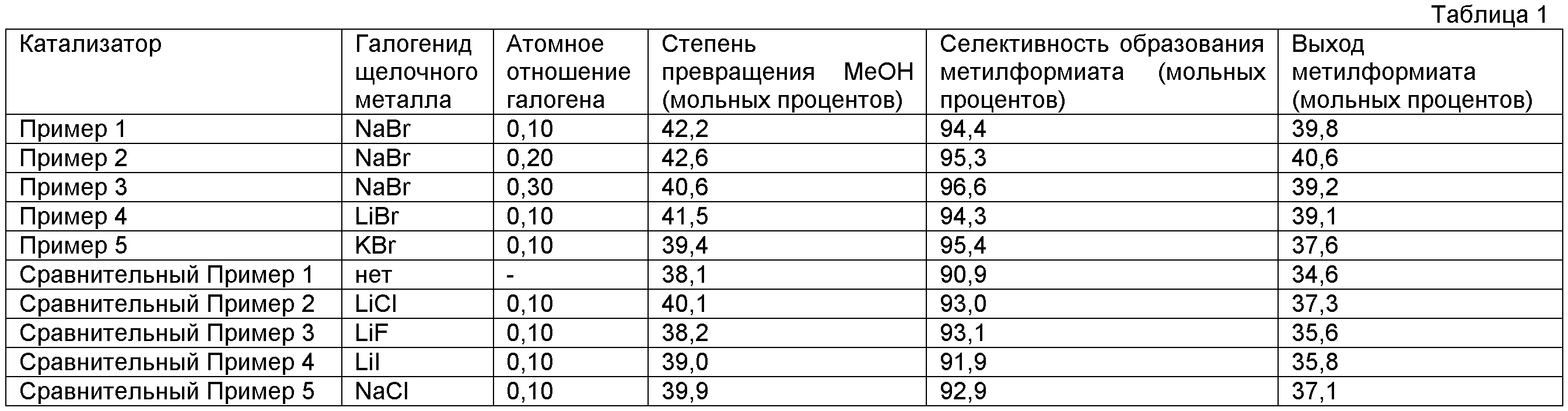
Атомное отношение галогена представляет собой число атомов галогена, когда общее число атомов меди, содержащейся в катализаторе, составляло 10.
Как показано в Таблице 1, каждый из катализаторов в Примерах 1-5, в каждом из которых был добавлен бромид щелочного металла, показал более высокие степень превращения МеОН и селективность образования MF, чем катализатор из Сравнительного Примера 1, в котором бромид щелочного металла не был добавлен. Каждый катализатор из Примеров 1-5 показал лучшие селективность образования MF и выход MF, чем катализаторы из Сравнительных Примеров 2, 3, 4 и 5, в каждом из которых частицы галогена не были бромом.
<Испытание долговечности>
В соответствии с таким же методом, как в испытании для первичной оценки, исследовали изменение каждого выхода в зависимости от времени в условиях высокой температуры и большой величины объемного расхода потока (GHSV), с увеличением продолжительности реакции до 40 часов. Долговечность катализатора выражали как среднюю скорость ухудшения характеристик (%/час). Среднюю скорость ухудшения характеристик определяли расчетом снижения выхода в единицу времени по разнице между выходом MF через 5 часов реакции и выходом MF после 40 часов реакции. Более низкая скорость ухудшения характеристик означает улучшенную долговечность.
Результаты испытания долговечности Примеров 1, 4 и 5 и Сравнительных Примеров 2 и 5 показаны в Таблице 2.
Как показано в Таблице 2, каждый катализатор в Примерах 1, 4 и 5, в каждый из которых добавили бромид щелочного металла, показал меньшую скорость ухудшения характеристик, представленную как изменение выхода со временем, чем катализаторы из Сравнительных Примеров 2 и 5, к каждому из которых добавляли хлорид щелочного металла. Поэтому катализатор согласно настоящему изобретению, полученный добавлением бромида в качестве частиц галогена, превосходит по долговечности катализаторы Сравнительных Примеров 2 и 5, в каждый из которых в качестве частиц галогена добавляли хлорид.
<Испытание для оценки срока службы катализатора>
Для сравнения и оценки термостойкости и долговечности катализаторов Примера 1 и Сравнительного Примера 2, изменения степени превращения метанола и селективности образования метилформиата в зависимости от времени измеряли в условиях более высокой температуры, чем для обычных реакционных условий.
Более конкретно, полученную сформованную таблетку сначала измельчили, и просеиванием отобрали измельченные кусочки, каждый из которых имел размер от 0,85 до 1,4 мм. Измельченный продукт подвергли восстановлению при температуре 220ºС в потоке водорода, и 3 мл продукта взвесили и поместили в реакционную трубку, имеющую внутренний диаметр 10 мм. Испытание проводили при контрольной реакционной температуре 360ºС (измеренной в диапазоне от 260 до 280ºС только во время измерения), реакционном давлении 0,49 МПа (манометрическое), и среднечасовой скорости подачи метанола (GHSV) 4000/час, пока выход метилформиата (MF) при каждой реакционной температуре не достигал 20%. Результаты испытания показаны в Таблицах 3 и 4.
Как показано в Таблицах 3 и 4, с катализатором из Примера 1, в который добавляли бромид щелочного металла, время, прошедшее до того, как выход MF достигал 20%, было более продолжительным в 2 раза или более при более высокой температуре, например, 270ºС или 280ºС, по сравнению с катализатором из Сравнительного Примера 2, в который добавляли хлорид щелочного металла. Поэтому катализатор согласно настоящему изобретению является превосходным по термостойкости.
Промышленная применимость
Катализатор согласно настоящему изобретению является превосходным по долговечности и термостойкости и может быть использован для получения метилформиата из метанола с высокой селективностью при высоком выходе.
Метилформиат, полученный с использованием катализатора согласно настоящему изобретению, может быть применен в промышленности в качестве сырьевого материала для получения высокочистого монооксида углерода, муравьиной кислоты, формальдегида, уксусной кислоты, N,N-диметилформамида или тому подобных.
Реферат
Настоящее изобретение относится к катализатору, используемому для получения метилформиата реакцией дегидрирования метанола в газовой фазе, и к способу получения метилформиата с использованием этого катализатора. Описан катализатор дегидрирования метанола, используемый для получения метилформиата, который содержит оксиды меди, цинка и алюминия, соединение фосфорной кислоты и бромид щелочного металла. Описан также способ получения метилформиата, включающий стадию дегидрирования метанола в газовой фазе с использованием описанного выше катализатора дегидрирования метанола. Технический эффект - улучшение выхода и селективности образования метилформиата и превосходные долговечность и термостойкость предложенного катализатора. 2 н. и 6 з.п. ф-лы, 4 табл., 5 пр.

Комментарии