Высокоактивное производное нуклеозида для лечения hcv - RU2015148010A
Код документа: RU2015148010A
Формула
1. Соединение формулы I или его фармацевтически приемлемая соль, причем формула I представляет собой

где R1 и R2 каждый представляют собой водород или D; и каждое положение, представленное в виде D, характеризуется дейтериевым обогащением, составляющим по меньшей мере 50%.
2. Соединение или соль по п. 1 формулы
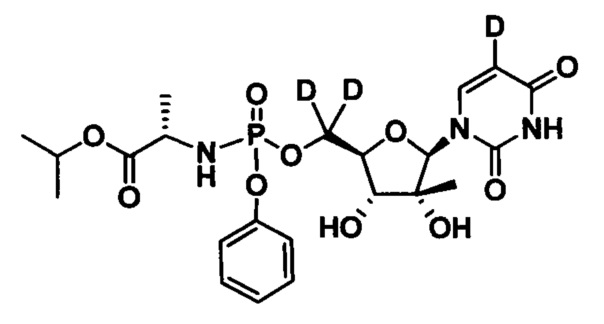
3. Соединение или соль по п. 2 формулы

4. Соединение или соль по п. 2 формулы

5. Соединение или соль по п. 2, в котором каждое положение, представленное в виде D, характеризуется дейтериевым обогащением, составляющим по меньшей мере 90%.
6. Соединение или соль по п. 2, в котором каждое положение, представленное в виде D, характеризуется дейтериевым обогащением, составляющим по меньшей мере 95%.
7. Смесь 50/50 стереоизомеров соединения по п. 2, причем смесь содержит

8. Фармацевтическая композиция, содержащая активный агент, в которой активный агент представляет собой соединение или соль по п. 2, а также содержащая фармацевтически приемлемый носитель.
9. Фармацевтическая композиция по п. 8, содержащая один или несколько дополнительных активных агентов.
10. Фармацевтическая композиция по п. 9, в которой один или несколько дополнительных активных агентов представляют собой ингибитор протеазы NS3 HCV, ингибитор NS5A HCV, ингибитор NS5B HCV или комбинацию вышеперечисленного.
11. Фармацевтическая композиция по п. 9, в которой один или несколько дополнительных активных агентов представляют собой ингибитор NS5A и по меньшей мере одно из совапревира и АСН-2684.
12. Способ лечения инфекции HCV у пациента, предусматривающий введение терапевтически эффективного количества соединения или соли по п. 2 пациенту.
13. Способ лечения инфекции HCV у пациента, предусматривающий введение терапевтически эффективного количества фармацевтической композиции по п. 8 пациенту.
14. Способ лечения инфекции HCV у пациента, предусматривающий введение терапевтически эффективного количества первого активного агента и терапевтически эффективного количества одного или нескольких дополнительных активных агентов пациенту, причем первый активный агент представляет собой соединение или соль по п. 1 и один или несколько дополнительных активных агентов выбирают из ингибитора NS3 и ингибитора NS5A.
15. Способ лечения вирусной инфекции Flaviviridae у пациента, предусматривающий введение терапевтически эффективного количества соединения или соли по п. 2 пациенту, причем вирусная инфекция Flaviviridae представляет собой лихорадку денге, вирусную инфекцию Западного Нила, желтую лихорадку или вирусную инфекцию диареи крупного рогатого скота.
16. Способ получения соединения формулы

предусматривающий
(I) взаимодействие сложного аминоэфира (100), в котором сложный аминоэфир представляет собой изопропиловый эфир аланина L, с дихлорфосфатом (200) с образованием реакционной смеси

(II) добавление к реакционной смеси (I) R-LH, где L представляет собой S или О и R представляет собой необязательно замещенный арильную, гетероарильную или гетероциклоалкильную группу, или R-LH, где R-LH представляет собой N-гидроксиимид; с образованием промежуточного соединения (300)

(III) взаимодействие промежуточного соединения (300) с нуклеозидом (400)


в котором каждое положение D, представленное в виде D, характеризуется дейтериевым обогащением, составляющим по меньшей мере 50%.
17. Способ по п. 16 для получения соединения формулы
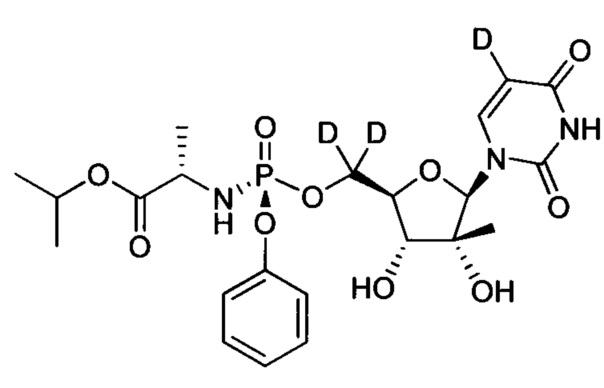

18. Способ по п. 16, при котором сложный аминоэфир (100) и дихлорфосфат (200) объединяют при температуре менее чем -20°C и R-LH выбирают из



19. Способ по п. 16, при котором сложный аминоэфир (100) и дихлорфосфат (200) объединяют при температуре от -40°C до приблизительно -60°C.
20. Способ по п. 18, при котором основание добавляют к смеси аминоэфира (100) и дихлорфосфата (200).
21. Способ по п. 20, при котором основание представляет собой триэтиламин, и добавление основания к смеси происходит в органическом растворителе, выбранном из дихлорметана, 2-метилтетрагидрофурана или тетрагидрофурана.

Комментарии