Способ получения гидроксиламинсульфата - RU2717515C1
Код документа: RU2717515C1
Чертежи
Описание
Изобретение относится к химической промышленности, а именно - к способу получения гидроксиламинсульфата (ГАС) гидрированием оксида азота (II) водородом в присутствии катализатора «платина на электрографите» в водном растворе серной кислоты. ГАС является одним из основных прекурсоров в синтезе капролактама. Обычно процесс получения ГАС рассматривают вместе с процессом получения оксида азота (II) парокислородной конверсией аммиака. Полученный таким образом оксид азота (II) используют в процессе синтеза ГАС.
Парокислородную конверсию аммиака проводят на платинородиевой сетке при повышенном давлении и температуре 800-950°С с получением целевого продукта оксида азота (II).
Основная реакция:
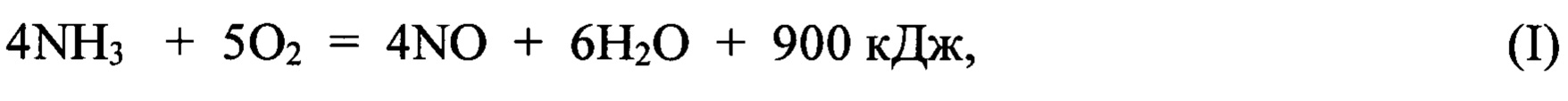
Побочные реакции:
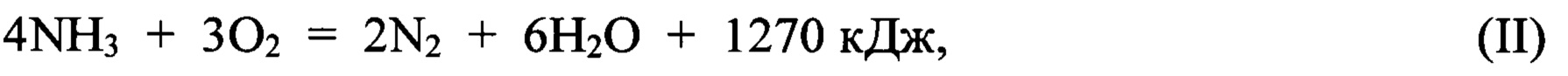
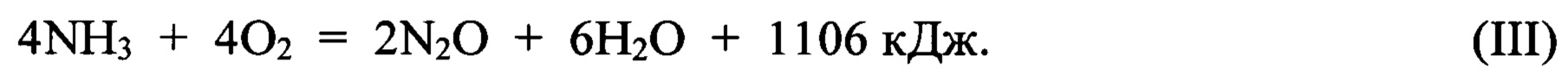
Для смещения равновесия основной реакции (I) в сторону образования целевого продукта оксида азота (II) процесс проводят при избытке кислорода. Содержащийся в продуктах реакции избыточный кислород гидрируют водородом на Ag-Mn-катализаторе при температуре 400-450°С, при этом протекают следующие основные реакции:

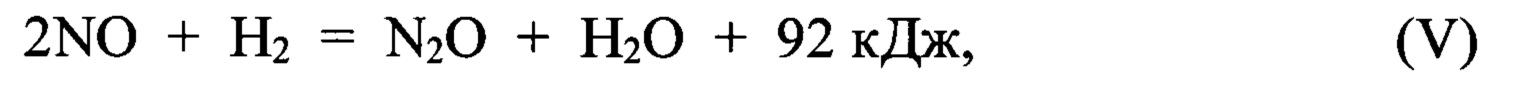

Водяной пар, используемый в исходной смеси в качестве защитного компонента для понижения температуры реакции и повышения нижнего предела взрываемости по аммиаку, конденсируется с получением слабой азотной кислоты при температуре не более 40°С, при этом процесс охлаждения и конденсации сопровождается реакциями, описываемыми следующими уравнениями:



Полученный оксид азота (II) отделяют от оксида азота (IV) промывкой газовой смеси слабой азотной кислотой.
Оптимальное соотношение аммиак : кислород в исходной смеси, поступающей на парокислородную конверсию, равно 1:1,35, что несколько выше стехиометрического по основной реакции, равного 1:1,25. Изменение этого соотношения в сторону уменьшения объемной доли кислорода ведет к снижению конверсии аммиака и, как следствие, снижению выхода оксида азота (II). Изменение соотношения увеличением объемной доли кислорода приводит к повышенному расходу водорода в процессе гидрирования кислорода или увеличению выхода азотной кислоты при конденсации водяного пара.
Известен способ получения ГАС [Патент РФ 2324645 МПК С01В 21/14, 2006]. Способ включает приготовление реакционной смеси аммиака, кислорода и водяного пара, каталитическое окисление аммиака, концентрирование нитрозного газа за счет конденсации водяных паров, смешение сконцентрированного нитрозного газа с водородом, смесью серной кислоты, воды и конденсата концентрирования нитрозного газа и синтез ГАС. Каталитическое окисление аммиака осуществляют под давлением 3-3,5 атм., тепло нитрозного газа используют для концентрирования азотнокислого конденсата (АКК) и раствора ГАС, при этом АКК концентрируют до массовой доли азотной кислоты не менее 40%, а раствор ГАС концентрируют до массовой доли 40% за счет тепла конденсации паров дистиллята, образующихся при концентрации АКК.
Для получения 1 тонны ГАС в час по этому способу в смесителе приготавливают реакционную смесь из 817,5 кг/час аммиака, 2052,6 кг/час кислорода и 4021 кг/час водяного пара и направляют в реактор, где на платиноидных сетках осуществляют парокислородную конверсию аммиака под давлением 3-3,5 атм. Тепло реакции окисления аммиака используют для получения пара, охлаждая нитрозный газ в котловой части реактора. Полученный нитрозный газ (NOx) далее поступает в кипятильник колонны дистилляции АКК, где конденсируются пары воды с выделением АКК и концентрируется нитрозный газ. Тепло конденсации паров воды используют для концентрирования АКК от массовой доли 7-8,5% до массовой доли 40%. Образующийся при этом газообразный дистиллят, содержащий азотную кислоту с массовой долей до 0,25%, поступает в теплообменник, куда в качестве охлаждающей жидкости подают раствор ГАС с массовой долей около 24%. Нагретый за счет конденсации водяных паров дистиллята раствор ГАС поступает в сепаратор, где под разрежением из раствора испаряются водяные пары при температуре 60-85°С. Сконцентрированный раствор содержит ГАС с массовой долей около 40%. Нитрозный газ после кипятильника колонны дистилляции поступает в теплообменник, где происходит конденсация остаточных паров воды с образованием АКК с массовой долей 7-8,5% и охлаждение концентрированного нитрозного газа до 40°С, затем он очищается от оксида азота (IV) в скруббере и подается на стадию синтеза ГАС в количестве 1092 кг/час. Сконденсированный дистиллят с массовой долей азотной кислоты 0,25%, а также часть конденсата вторичного пара после сепаратора и конденсатора вторичного пара направляются на разбавление концентрированной серной кислоты в стадию синтеза ГАС. Кубовый остаток из колонны дистилляции с массовой долей азотной кислоты около 40% в количестве 1138 кг/час выдается как готовый продукт. Хвостовые газы реакторов синтеза ГАС направляют на сжигание в рекуперативную установку.
Недостатком данного способа является отсутствие стадии гидрирования АКК с получением дополнительного количества синтез-газа (NO+Н2) для производства ГАС, что не позволяет в полной степени перерабатывать имеющееся сырье.
Известен способ получения ГАС [Патент РФ 2241662 МПК С01В 21/14, 2004]. Способ включает приготовление реакционной смеси аммиака, кислорода и водяного пара, каталитическое окисление аммиака, смешение полученного нитрозного газа с водородом, стабилизацию состава нитрозного газа путем гидрирования на серебряно-марганцевом катализаторе, его двух стадийное концентрирование конденсацией паров воды, очистку концентрированного нитрозного газа от оксида азота (IV), смешение его с водородом, смесью серной кислоты, воды, конденсата первой стадии концентрирования нитрозного газа и продукта, образующегося при каталитическом гидрировании азотной кислоты, содержащейся в конденсате второй стадии концентрирования нитрозного газа и синтез ГАС. При стабилизации состава нитрозного газа гидрируют 70-75 об. % свободного кислорода. Образующийся при каталитическом гидрировании азотной кислоты, содержащейся в конденсате второй ступени концентрирования нитрозного газа, чистый оксид азота (II) в смеси с водородом направляют в один из реакторов синтеза ГАС.
Процесс проводят следующим образом. Реакционную смесь аммиака, кислорода и водяного пара, приготовленную в смесителе, направляют в реактор, где аммиак окисляют кислородом до оксида азота (II) при соотношении аммиака и кислорода выше стехиометрического на 8-10%, т.е. (1,35-1,37):1, чтобы достичь максимального выхода оксида азота (II). Образовавшийся нитрозный газ охлаждают в котловой части реактора до температуры 260-280°С, смешивают в смесителе с водородом и направляют в реактор для стабилизации состава. Здесь избыточный кислород на серебряно-марганцевом катализаторе гидрируют в воду. Степень гидрирования кислорода достигает 75%. Тепло реакций окисления аммиака и гидрирования кислорода используют для получения пара.
Стабилизированный нитрозный газ с температурой 150°С подают в конденсатор первой стадии, где при температуре 93-95°С выделяют 70-75% конденсата, содержащего до 0,3% масс, азотной кислоты, а затем в конденсатор второй стадии, где выделяют 25-30% конденсата с содержанием азотной кислоты более 5% масс. Конденсат первой стадии направляют через холодильник в смеситель для получения 19% масс, раствора серной кислоты, необходимой для синтеза ГАС. Концентрированный оксид азота (II) из конденсатора компрессором направляют в абсорбер, орошаемый азотнокислым конденсатом второй стадии, в котором его очищают от оксида азота (IV), после чего направляют в смеситель для смешения с водородом и далее в каскад реакторов, где в среде разбавленной серной кислоты синтезируют ГАС.
Конденсат второй стадии концентрирования нитрозного газа после охлаждения в холодильнике направляют в реактор, где при температуре 80-90°С азотную кислоту, содержащуюся в этом конденсате, гидрируют на платиновом катализаторе. Образующуюся в результате гидрирования азотной кислоты, содержащейся в конденсате второй стадии концентрирования нитрозного газа, газовую смесь, состоящую из чистого оксида азота (II) и водорода, подают в последний реактор каскада реакторов синтеза ГАС, а катализат, выходящий из реактора и содержащий до 0,45% масс, азотной кислоты, используют при получении водного раствора серной кислоты в смесителе. Отходящие газы реакторов синтеза ГАС направляют на сжигание в рекуперативную установку.
Недостатками данного способа являются:
1) не оптимальный состав синтез-газа (NO+Н2), подаваемого в последний реактор каскада стадии синтеза ГАС;
2) отсутствие контроля за взрывобезопасностью синтез-газа на всей технологической цепочке его получения и применения;
3) не полное гидрирование кислорода и попадание до 25% остаточного кислорода в газообразные продукты реакции, что увеличивает взрывоопасность процесса.
Известен способ получения ГАС [Патент РФ 2257339 МПК С01В 21/14, 2005]. Способ включает приготовление реакционной смеси из аммиака, кислорода и паров воды, каталитическое окисление аммиака, смешение нитрозного газа с водородом, стабилизацию нитрозного газа путем гидрирования избыточного кислорода на серебряно-марганцевом катализаторе, двухступенчатое концентрирование его конденсацией паров воды, очистку концентрированного нитрозного газа от оксида азота (IV), каталитическое жидкофазное гидрирование АКК второй ступени концентрирования нитрозного газа на платиновом катализаторе, смешение концентрированного нитрозного газа с водородом и оксидом азота (II), полученным в результате гидрирования азотнокислого конденсата второй ступени концентрирования нитрозного газа, и прямой синтез ГАС на платиновом катализаторе в среде 19% масс, серной кислоты, полученной смешением концентрированной серной кислоты, конденсата первой ступени концентрирования нитрозного газа, продукта гидрирования конденсата второй ступени концентрирования нитрозного газа и обессоленной и очищенной воды. 19% масс, серную кислоту готовят из концентрированной серной кислоты, разбавляя ее сначала конденсатом первой ступени концентрирования нитрозного газа и обессоленной водой до 21,1-22,3% масс, затем очищают и смешивают очищенную серную кислоту с продуктом гидрирования АКК второй ступени концентрирования нитрозного газа.
Недостатком этого способа является отсутствие контроля за взрывобезопасностью синтез-газа, получаемого после смешения его основного потока с газообразными продуктами, образующимися на стадии гидрирования азотной кислоты.
Известен способ получения ГАС [Патент РФ 2257340 МПК С01В 21/14, 2005]. Способ включает приготовление реакционной смеси аммиака, кислорода и водяного пара, каталитическое парокислородное окисление аммиака, концентрирование нитрозного газа конденсацией паров воды, гидрирование АКК, очистку концентрированного нитрозного газа от примесей оксида азота (IV), смешение его с водородом, смесью серной кислоты, воды и продуктом гидрирования АКК и синтез ГАС. Каталитическое парокислородное окисление аммиака и синтез ГАС осуществляют под давлением более 2,5 атм., при этом давление стадии синтеза аммиака превышает давление стадии синтеза ГАС на величину, равную аэродинамическому сопротивлению оборудования и трубопроводов газового тракта между стадиями. Концентрирование нитрозного газа осуществляют в одну стадию, используя весь избыточный кислород для получения азотной кислоты. АКК подвергается жидкофазному гидрированию в присутствии платинового катализатора, образующийся чистый оксид азота (II) используется для получения ГАС, а продукт гидрирования с массовой долей азотной кислоты до 0,45% используется для разбавления концентрированной серной кислоты.
Способ осуществляют следующим образом. Реакционную смесь аммиака, кислорода и водяного пара, приготовленную в смесителе, направляют в реактор, где аммиак окисляют кислородом до оксида азота (II) под давлением 3-3,5 атм. Тепло реакции окисления аммиака используют для получения пара, охлаждая нитрозный газ в котловой части реактора. Полученный нитрозный газ концентрируют, конденсируя пары воды в теплообменнике, очищают от примесей оксида азота (IV), промывая частью АКК, смешивают с водородом в смесителе и направляют в каскад реакторов, где в среде разбавленной серной кислоты синтезируют ГАС под давлением более 2,5 атм. АКК с массовой долей азотной кислоты 7-8,5% направляют в реактор, где в присутствии платинового катализатора гидрируют водородом. Образующуюся при этом смесь чистого оксида азота (II) и водорода смешивают с основным потоком концентрированного оксида азота (II). Продукт гидрирования с массовой долей азотной кислоты до 0,45% направляют в смеситель для разбавления концентрированной серной кислоты. Отходящие газы из каскада реакторов синтеза ГАС направляют в рекуперативно-экологическую установку.
Недостатком данного способа является отсутствие контроля за взрывобезопасностью синтез-газа (NO+Н2), получаемого в смесителе после его разбавления газообразными продуктами из реактора гидрирования АКК, тем более, что нижняя граница взрывобезопасности определяется не только составом газовой смеси, но и давлением.
Известен способ получения ГАС [Патент РФ 2259940 МПК С01В 21/14, 2005], включающий приготовление реакционной смеси аммиака, кислорода и водяного пара, каталитическое окисление аммиака, смешение полученного нитрозного газа с водородом, стабилизацию нитрозного газа путем гидрирования кислорода на серебряно-марганцевом катализаторе, его концентрирование конденсацией паров воды, очистку концентрированного нитрозного газа от оксида азота (IV), смешение его с водородом, смесью серной кислоты и воды, и синтез ГАС. Конденсацию содержащихся в нитрозном газе паров воды осуществляют в выпарной установке под вакуумом с подачей в греющую камеру установки нитрозного газа, предварительно охлажденного до температуры выше 100°С, и продукционного раствора с массовой долей ГАС 24%, после чего нагретый до 80-90°С раствор ГАС подают в испарительную часть выпарной установки для упаривания до 40%.
Образующийся при концентрировании нитрозного газа АКК с массовой долей азотной кислоты более 1% подвергают жидкофазному гидрированию в присутствии платинового катализатора, образующийся при этом оксид азота (II) в смеси с водородом направляют на синтез ГАС, а продукт гидрирования с массовой долей азотной кислоты 0,45% направляют на разбавление концентрированной серной кислоты.
Недостатком данного способа является отсутствие контроля за взрывобезопасностью синтез-газа (NO+Н2) на выходе из смесителя и после смешения этого потока с синтез-газом, получаемым после гидрирования азотной кислоты.
Известен способ получения ГАС [Патент РФ 2279401 МПК С01В 21/14, 2006], включающий приготовление реакционной смеси аммиака, кислорода и водяного пара, каталитическое окисление аммиака, стабилизацию состава нитрозного газа путем гидрирования на серебряно-марганцевом катализаторе, концентрирование нитрозного газа за счет конденсации водяных паров, смешение концентрированного нитрозного газа с водородом, смесью серной кислоты, катализата после каталитического гидрирования азотной кислоты, каталитическое гидрирование азотной кислоты и синтез ГАС. Каталитическое окисление аммиака осуществляют под давлением более 3 атм., концентрирование нитрозного газа осуществляют в колонне дистилляции с подачей нитрозного газа в кипятильник колонны дистилляции, где АКК концентрируют до массовой доли азотной кислоты до 8% за счет тепла конденсации водяных паров при концентрировании нитрозного газа, тепло образовавшегося при этом газообразного дистиллята используют для концентрирования ГАС до массовой доли 38%, а сам дистиллят, а также часть образующегося при концентрировании ГАС вторичного пара, в виде конденсатов используют для разбавления серной кислоты, АКК с массовой долей азотной кислоты до 8% подвергают каталитическому гидрированию.
Недостатком этого способа является отсутствие контроля за взрывобезопасностью синтез-газа, подаваемого на стадию получения ГАС.
Наиболее близким решением поставленной технической задачи (прототипом) является способ получения ГАС [Патент ФРГ 19842538 МПК С01В 21/14, 2000]. Процесс получения ГАС включает следующие основные стадии:
1) приготовление реакционной смеси из аммиака, кислорода и водяного пара;
2) каталитическое окисление аммиака;
3) смешивание полученного нитрозного газа с водородом;
4) стабилизация состава нитрозного газа путем гидрирования;
5) двухступенчатое концентрирование путем конденсации водяных паров;
6) очистка нитрозного газа из второй стадии путем конденсации оксида азота (IV) в воде до разбавленной азотной кислоты;
7) смешивание очищенного нитрозного газа с водородом;
8) смешивание серой кислоты, воды и АКК первой стадии концентрирования оксида азота (II);
9) синтез ГАС.
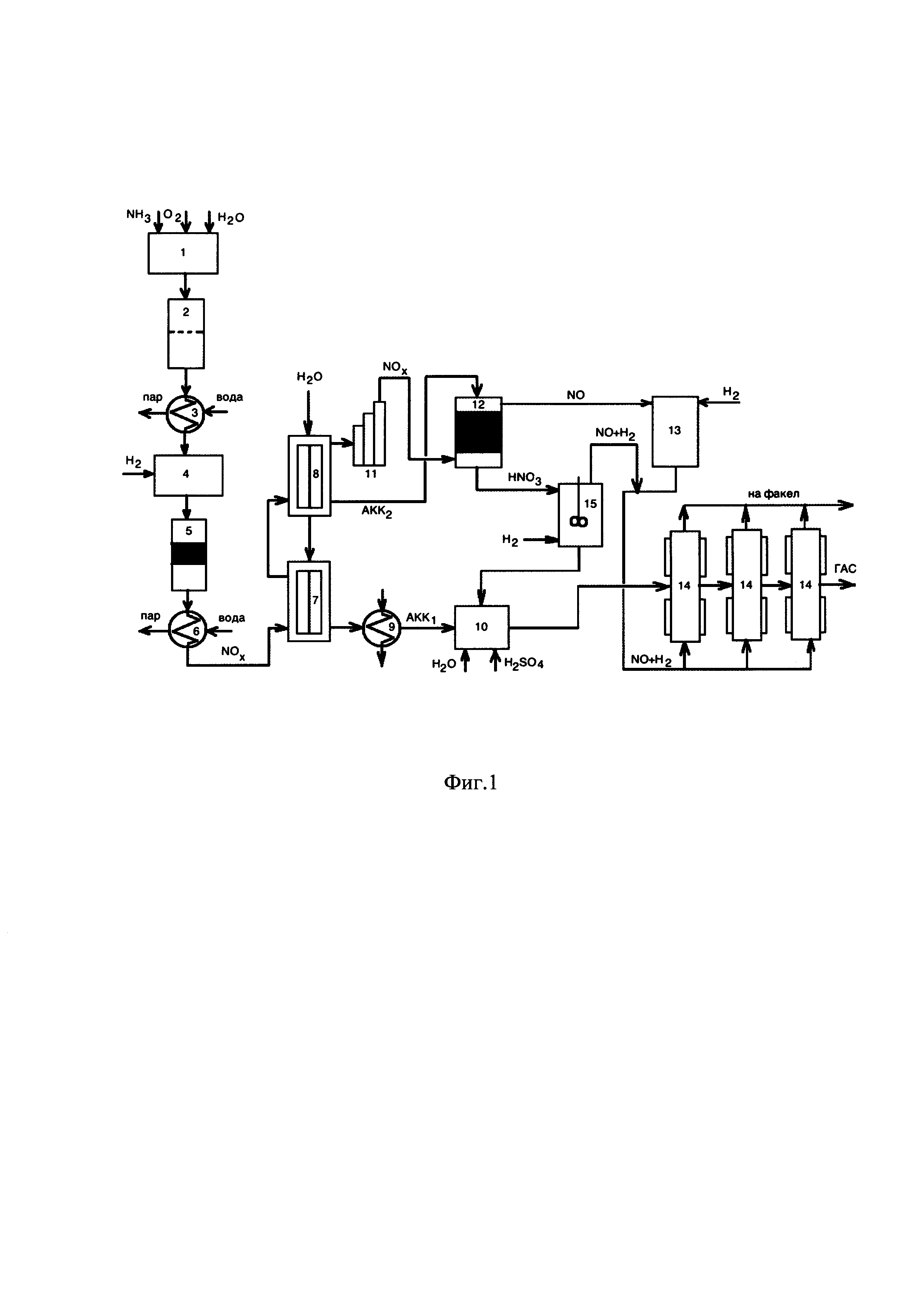
Процесс проводят в соответствии с принципиальной технологической схемой, приведенной на фиг. 1. В смесителе (1) готовят реакционную смесь из аммиака, кислорода и водяного пара. Смесь направляют в реактор (2), где аммиак окисляется кислородом на платинородиевом катализаторе при температуре 800-950°С и повышенном давлении с получением нитрозного газа. Образовавшийся нитрозный газ охлаждается в нижней части реактора (2) и в теплообменнике (3) до температуры 260-280°С, смешивается в смесителе (4) с водородом и направляется в реактор (5) для стабилизации состава. В реакторе (5) избыточный кислород на серебряно-марганцевом катализаторе при температуре 400-450°С гидрируется до воды. Степень гидрирования кислорода достигает 90%. Тепло реакций окисления аммиака и гидрирования кислорода с помощью теплообменников (3) и (6) используется для производства пара.
Не содержащий кислорода нитрозный газ охлаждают до температуры 140-160°С и подают в конденсатор (7) первой ступени, где 70-80% конденсата с содержанием азотной кислоты до 0,45% масс. (АКК1) выделяется при температуре 90-95°С. Затем нитрозный газ подают в конденсатор (8) второй ступени, где выделяется 20-30% конденсата с содержанием азотной кислоты 2-4% масс. (АКК2). Конденсат первой ступени с содержанием азотной кислоты до 0,45% масс. (АКК1) направляют через холодильник (9) в смеситель (10) для производства 19-25%-ного раствора серной кислоты, которая необходима для синтеза ГАС.
Концентрированная смесь оксидов азота из конденсатора (8) через компрессор (11) направляется в абсорбер (12), в который подают азотнокислый конденсат второй ступени (АКК2), и в котором смесь оксидов азота освобождается от оставшихся количеств оксида азота (IV). Полученный оксид азота (II) направляют в смеситель (13) для смешивания с водородом. Полученную в смесителе (13) смесь направляют в каскад реакторов (14), где синтезируют ГАС в среде разбавленной серой кислоты гидрированием оксида азота (II) водородом при температуре 30-70°С, давлении 1-4 атм., объемном соотношении оксид азота (II) : водород, равном 1:(1,5-1,9) в присутствии мелкодисперсного катализатора «платина на графите».
Конденсат второй ступени, содержащий азотную кислоту, после абсорбера (12) направляется в реактор (15), где азотная кислота гидрируется при температуре 85-90°С и повышенном давлении водородом на катализаторе «платина на графите». Процесс гидрирования протекает в соответствии с уравнением реакции:
2HNO3+3Н2=2NO+4H2O
Водород подают в реактор (15) в таком количестве, что состав газовой смеси на выходе из реактора (15) соответствует составу газовой смеси, направляемой из смесителя (13) на стадию синтеза ГАС. Газовая смесь - чистый оксид азота (11) и водород, - смешивается с основным потоком смеси NO+Н2 и направляется на стадию синтеза ГАС.
Недостатками данного способа являются: 1) Отсутствие контроля за составом синтез-газа (NO+Н2), как на выходе синтез-газа из реактора (15) после гидрирования азотной кислоты при температуре 85-90°С водородом на платиновом катализаторе, так и на линиях синтез-газа после смесителя (13) и после объединения потоков синтез-газа перед подачей его в каскад реакторов (14) синтеза ГАС. Отсутствие этого контроля может привести к возникновению взрывоопасной ситуации при работе с синтез-газом. Известно, что нижняя граница взрывоопасной области определяется давлением синтез-газа и содержанием водорода в синтез-газе. При большом содержании водорода смесь NO+Н2 взрывобезопасна в более широком интервале давлений [Патент РФ 2690931 МПК С01В 21/14, 2018].
2) Гидрирование азотной кислоты при температуре 85-90°С на катализаторе «платина на графите» только в одной каталитической зоне (в одном реакторе (15)) не обеспечивает полноту протекания реакции.
3) Сложность управления процессом, которая обусловлена необходимостью коррекции количества водорода, подаваемого в реактор (15) в зависимости от состава газовой смеси, получаемой на выходе из этого же реактора.
Целью настоящего изобретения является устранение всех перечисленных выше недостатков.
Согласно изобретению поставленная цель достигается способом получения гидроксиламинсульфата путем приготовления смеси аммиака, кислорода и водяного пара; каталитическим окислением смеси на платинородиевом катализаторе при температуре 800-950°С и повышенном давлении с получением нитрозного газа; охлаждением нитрозного газа до температуры 260-280°С; стабилизации охлажденного нитрозного газа путем их смешивания с водородом и последующим гидрированием полученной смеси газов на серебряно-марганцевом катализаторе при температуре 400-450°С с получением стабилизированного нитрозного газа; охлаждением стабилизированного нитрозного газа до температуры 140-160°С; конденсацией водой охлажденного стабилизированного нитрозного газа в две стадии с получением:
- на первой стадии конденсации азотнокислого конденсата с концентрацией азотной кислоты менее 0,45% масс, охлаждением конденсата и его смешиванием с водой и серной кислотой для производства раствора серной кислоты с концентрацией 19-25% масс и использованием этого раствора на стадии синтеза гидроксиламинсульфата гидрированием оксида азота (II) водородом при температуре 30-70°С, давлении 1-4 атм., объемном соотношении оксид азота (II) : водород равном 1:(1,5-1,9) в присутствии мелкодисперсного катализатора «платина на графите» в нескольких каталитических зонах;
- на второй стадии конденсации азотнокислого конденсата с концентрацией азотной кислоты 2-4% масс, и концентрированной смеси оксидов азота (IV) и (II) с последующей абсорбцией оксида азота (IV) азотнокислым конденсатом второй стадии и получением оксида азота (II), который используют на стадии синтеза гидроксиламинсульфата, и азотной кислоты, которую гидрируют водородом при температуре 85-90°С и повышенном давлении в присутствии мелкодисперсного катализатора «платина на графите» с получением газовой смеси оксида азота (II) и водорода, которую направляют на стадию синтеза гидроксиламинсульфата, и жидкой фазы, которую направляют на стадию производства раствора серной кислоты с концентрацией 19-25% масс;
- регулированием состава газовой смеси оксида азота (II) и водорода на стадии синтеза гидроксиламинсульфата введением дополнительного количества водорода. Гидрирование азотной кислоты водородом проводят в двух реакционных зонах с вводом азотной кислоты в первую по ходу движения жидкостного потока реакционную зону и вывода жидкой фазы из второй по ходу движения жидкостного потока реакционной зоны, в избытке водорода, подаваемого в каждую реакционную зону при мольном отношении водород : азотная кислота равном (3-5):1 с получением в каждой реакционной зоне газовой смеси оксида азота (II) и водорода, объединением газовых смесей и вводом объединенной газовой смеси непосредственно в каталитические зоны на стадии синтеза гидроксиламинсульфата; оксид азота (II), получаемый на второй стадии конденсации, направляют непосредственно в каталитические зоны на стадию синтеза гидроксиламинсульфата, а введение дополнительного количества водорода осуществляют в объединенную газовую смесь.
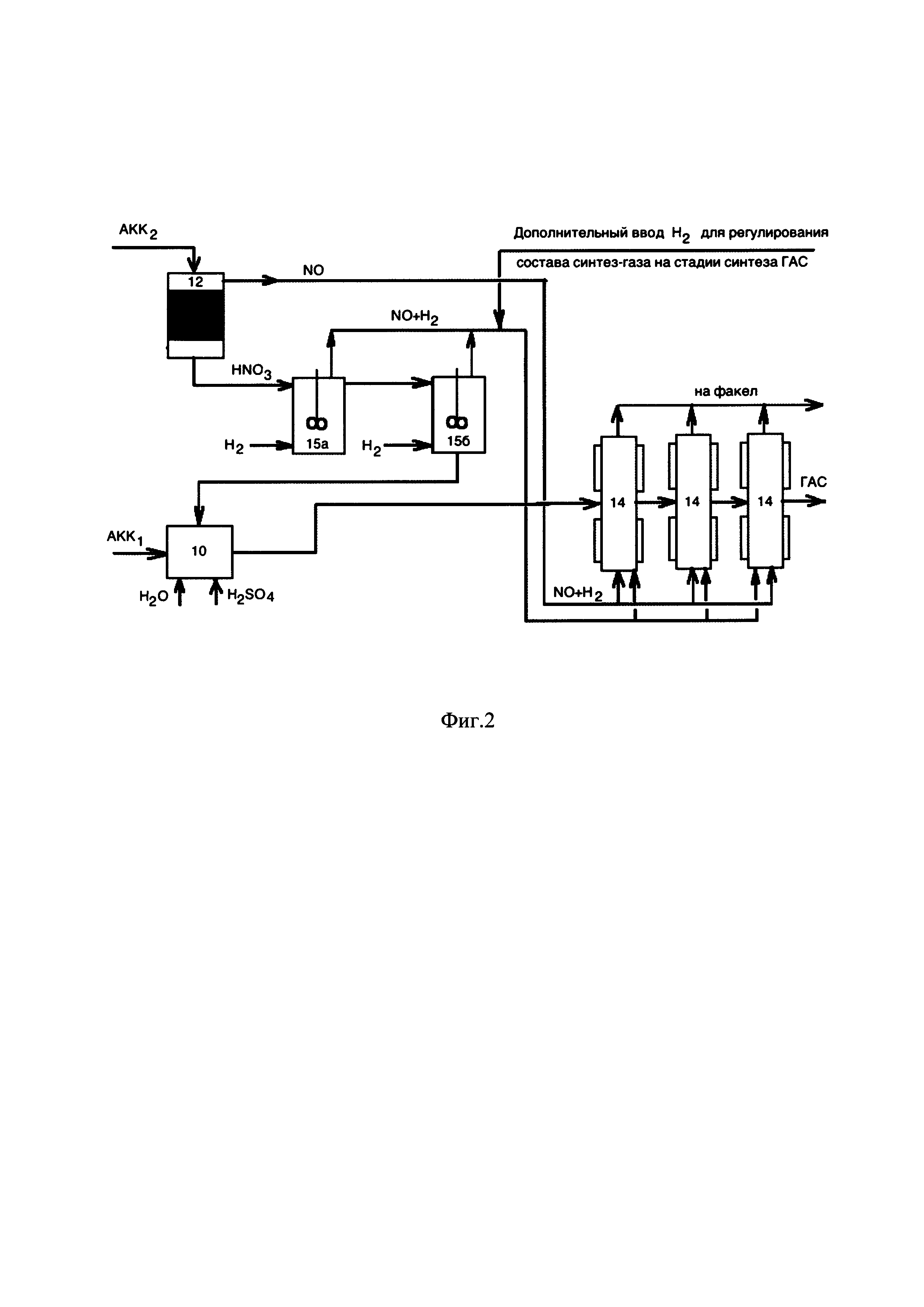
Процесс проводят в соответствии с принципиальными технологическими схемами, приведенными на фиг. 1 и 2. Основные отличия предлагаемого способа от прототипа касаются технологии переработки азотнокислого конденсата, получаемого после второй стадии конденсации.
Процесс проводят следующим образом (см. фиг. 1 и 2). В смесителе (1) готовят реакционную смесь из аммиака, кислорода и водяного пара. Смесь направляют в реактор (2), где аммиак окисляется кислородом на платинородиевом катализаторе при температуре 800-950°С и повышенном давлении с получением нитрозного газа. Образовавшийся нитрозный газ охлаждается в нижней части реактора (2) и в теплобменнике (3) до температуры 260-280°С, смешивается в смесителе (4) с водородом и направляется в реактор (5) для стабилизации состава. В реакторе (5) избыточный кислород на серебряно-марганцевом катализаторе при температуре 400-450°С гидрируется до воды. Степень гидрирования кислорода достигает 90%. Тепло реакций окисления аммиака и гидрирования кислорода с помощью теплообменников (3) и (6) используется для производства пара.
Не содержащий кислорода нитрозный газ охлаждают до температуры 140-160°С и подают в конденсатор (7) первой ступени где 70-80% конденсата с содержанием азотной кислоты до 0,45% масс. (АКК1) выделяется при температуре 90-95°С. Затем нитрозный газ подают в конденсатор (8) второй ступени, где выделяется 20-30% конденсата с содержанием азотной кислоты 2-4% масс. (АКК2). Конденсат первой ступени с содержанием азотной кислоты до 0,45% масс. (АКК1) направляют через холодильник (9) в смеситель (10) для производства 19-25%-ного раствора серной кислоты, которая необходима для синтеза ГАС.
Концентрированная смесь оксидов азота из конденсатора (8) через компрессор (11) направляется в абсорбер (12), в который подают азотнокислый конденсат второй ступени (АКК2) и в котором смесь оксидов азота освобождается от оставшихся количеств оксида азота (IV). Полученный оксид азота (II) направляют (см. фиг. 2) непосредственно в каскад реакторов (14), где синтезируют ГАС в среде разбавленной серой кислоты гидрированием оксида азота (II) водородом при температуре 30-70°С, давлении 1-4 атм., объемном соотношении оксид азота (II) : водород равном 1:(1,5-1,9) в присутствии мелкодисперсного катализатора «платина на графите».
Конденсат второй ступени АКК2, содержащий азотную кислоту, после абсорбера (12) направляют в первую по ходу движения реакционного потока реакционную зону (15а), где азотную кислоту гидрируют при температуре 85-90°С и повышенном давлении в присутствии катализатора «платина на графите» и мольном отношении водород : азотная кислота равном (3-5):1 с получением газовой смеси оксида азота (II) и водорода и жидкостного потока, который направляют во вторую по ходу движения жидкостного потока реакционную зону (15б), где его также гидрируют в тех же условиях, что и в первой реакционной зоне (15а). Полученные в реакционных зонах (15а) и (15б) газовые смеси оксида азота (II) и водорода объединяют и направляют непосредственно в каталитические зоны на стадии синтеза ГАС. Полученную в реакционной зоне (15б) жидкую фазу направляют в смеситель (10) для производства раствора серной кислоты с концентрацией 19-25% масс. Дополнительный ввод водорода для регулирования состава синтез-газа на стадии синтеза ГАС осуществляют в объединенную газовую смесь, полученную в реакционных зонах (15а) и (15б).
Преимуществами предлагаемого способа являются:
1) взрывобезопасные условия ведения процесса за счет раздельного ввода компонентов синтез газа в реакторы синтеза ГАС и проведение процесса гидрирования азотной кислоты в избытке водорода, что приводит к получению продуктовой газовой смеси с большим содержанием водорода, что является одним из условий взрывобезопасности процесса [Патент РФ 2690931 МПК С01В 21/14, 2018];
2) упрощение технологии процесса за счет исключения из технологической схемы смесителя (13), в котором существовала вероятность образования взрывоопасных смесей оксида азота (II) и водорода;
3) увеличение полноты протекания реакции гидрирования азотной кислоты за счет проведения процесса в двух реакционных зонах;
4) простота управления процессом за счет ввода требуемого дополнительного количества водорода непосредственно в объединенную газовую смесь, получаемую после стадии гидрирования азотной кислоты.
Способ иллюстрируется следующими примерами.
Пример 1 (сравнительный по прототипу). Процесс проводят в соответствии с технологической схемой, приведенной на фиг. 1, в условиях промышленного производства. В смесителе (1) готовят реакционную смесь аммиака, кислорода и водяного пара при мольном отношении аммиак : кислород равном 1,36:1 и содержанием аммиака в смеси 9%. Общая нагрузка по аммиаку на стадии окисления составляет 5700 кг/час. Смесь направляют в реактор (2), где аммиак окисляют кислородом на платинородиевом катализаторе при температуре 900°С с получением нитрозного газа. Образовавшийся нитрозный газ охлаждают в нижней части реактора (2) и в теплообменнике (3) до температуры 270°С, смешивают в смесителе (4) с водородом и направляют в реактор (5) для стабилизации состава. В реакторе (5) избыточный кислород на серебряно-марганцевом катализаторе при температуре 425°С гидрируют до воды. Степень гидрирования кислорода составляет 90%. Тепло реакций окисления аммиака и гидрирования кислорода с помощью теплообменников (3) и (6) используют для производства пара. Не содержащий кислорода нитрозный газ, охлажденный до температуры 150°С, направляют в конденсатор (7) первой ступени конденсации, где при температуре 92°С выделяют 72% конденсата (азотнокислый конденсат 1-ой ступени - АКК1) с содержанием азотной кислоты 0,42% масс. АКК1 с содержанием азотной кислоты 0,42% масс, направляют через холодильник (9) в смеситель (10) для производства 20%-ного раствора серной кислоты, необходимой для синтеза ГАС. Нитрозный газ после первой ступени конденсации подают в конденсатор (8) второй ступени, где выделяют 28% конденсата (азотнокислого конденсата 2-ой ступени - АКК2) с содержанием азотной кислоты 2,0% масс, и концентрированную смесь оксидов азота с помощью компрессора (11) направляют в абсорбер (12). В абсорбере (12) смесь оксидов азота освобождается от оставшегося количества оксида азота (IV) путем его абсорбции АКК2 и полученный оксид азота (II) направляют в смеситель (13) для смешивания с водородом. Полученную в смесителе (13) смесь газов направляют в каскад 6-ти реакторов (на фиг. 1 - три реактора каскада), где синтезируют ГАС в среде разбавленной серной кислоты гидрированием оксида азота (II) водородом при температуре 45°С, давлении 2 атм., объемном соотношении оксид азота (II) : водород равном 1:1,4 в присутствии мелкодисперсного катализатора «платина на графите». АКК2 содержащий азотную кислоту после абсорбера (12) направляют в реактор (15), где под давлением 3,6 атм., температуре 90°С и концентрации катализатора 50 г/л гидрируют водородом при объемной скорости по водороду 46,7 час-1. Водород подают в реактор (15) в таком количестве, что мольное отношение оксид азота (II) : водород на выходе из реактора (15) равно 1:1,4 и в точности соответствует соотношению оксид азота (II) : водород, используемому на стадии синтеза ГАС. Жидкую фазу после гидрирования в реакторе (15) с содержанием азотной кислоты 0,5% масс, в количестве 15,1 м3/час направляют в смеситель (10) для производства 20%-ного раствора серной кислоты, необходимой для синтеза ГАС. Получают ГАС в количестве 17630 кг/час. Основные технологические параметры ведения процесса по примеру 1 приведены в таблице.
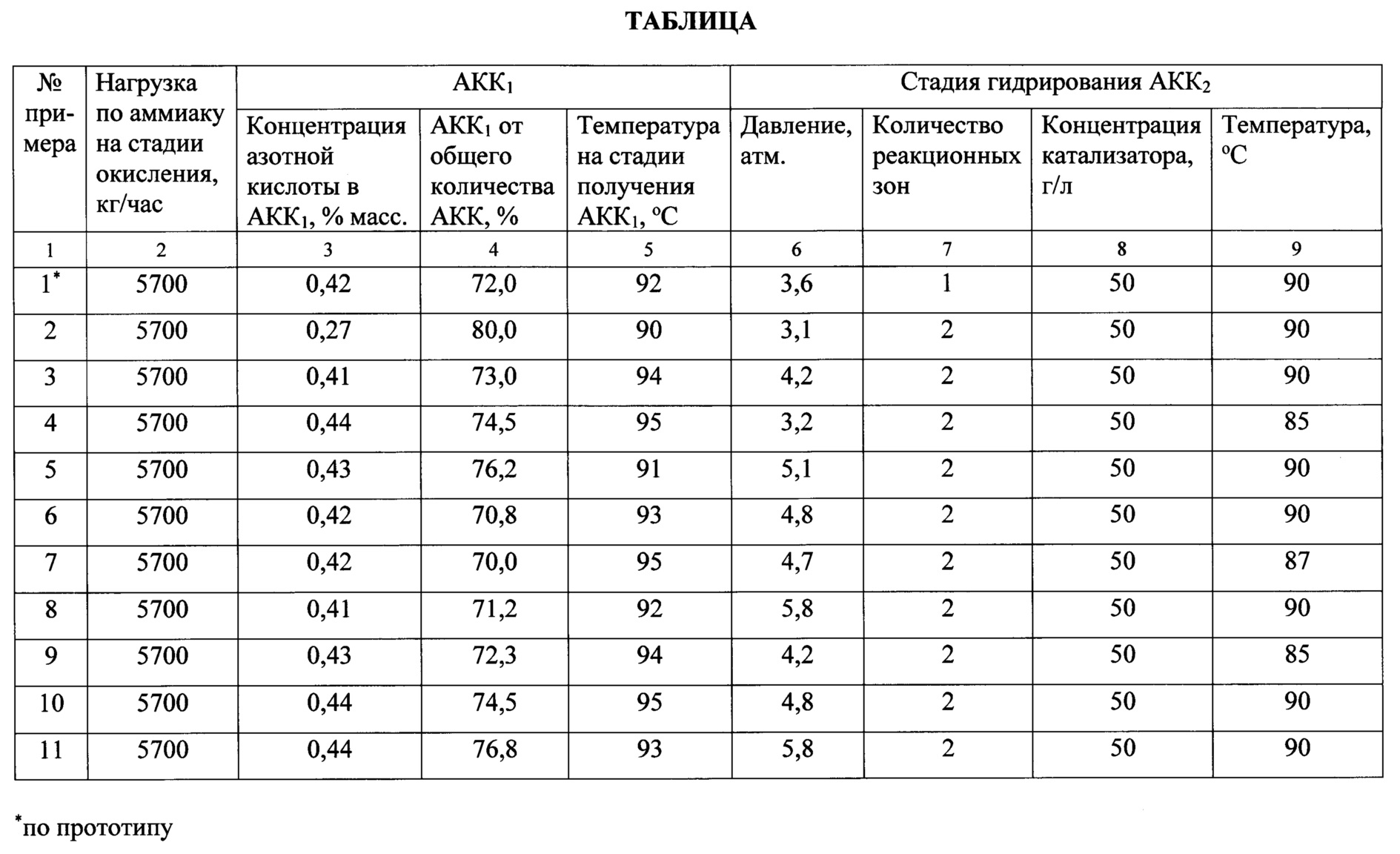
Пример 2. Процесс проводят в соответствии с технологической схемой, приведенной на фиг. 1 и 2, в условиях промышленного производства. В смесителе (1) готовят реакционную смесь аммиака, кислорода и водяного пара при мольном отношении аммиак : кислород равном 1,37:1 и содержанием аммиака 9%. Общая нагрузка по аммиаку на стадии окисления составляет 5700 кг/час. Смесь направляют в реактор (2), где аммиак окисляют кислородом на платинородиевом катализаторе при температуре 850°С с получением нитрозного газа. Образовавшийся нитрозный газ охлаждают в нижней части реактора (2) и в теплообменнике (3) до температуры 260°С, смешивают в смесителе (4) с водородом и направляют в реактор (5) для стабилизации состава. В реакторе (5) избыточный кислород на серебряно-марганцевом катализаторе при температуре 450°С гидрируют до воды. Степень гидрирования кислорода составляет 92%. Тепло реакций окисления аммиака и гидрирования кислорода с помощью теплообменников (3) и (6) используют для производства пара. Не содержащий кислорода нитрозный газ, охлажденный до температуры 140°С, подают в конденсатор (7) первой ступени конденсации, где при температуре 90°С выделяют 80% АКК1 с содержанием азотной кислоты 0,37% масс. АКК1 с содержанием азотной кислоты 0,37% масс, направляют через холодильник (9) в смеситель (10) для производства 22%-ного раствора серной кислоты, необходимой для синтеза ГАС. Нитрозный газ после первой ступени конденсации подают в конденсатор (8) второй ступени, где выделяют 20% АКК2 с содержанием азотной кислоты 2,0% масс, и концентрированную смесь оксидов азота, которую через компрессор (11) направляют в абсорбер (12). В абсорбере (12) смесь оксидов азота освобождается от оставшегося количества оксида азота (IV) с использованием в качестве абсорбента АКК2 и полученный оксид азота (II) непосредственно направляют в каскад из 6-ти реакторов (на фиг. 2 - три реактора), где синтезируют ГАС в среде разбавленной серной кислоты гидрированием оксида азота (II) водородом при температуре 51°С, давлении 1,5 атм., объемном соотношении оксид азота (II) : водород равном 1:1,6 в присутствии мелкодисперсного катализатора «платина на графите». АКК2, содержащий азотную кислоту, после абсорбера (12) направляют в первую по ходу движения жидкостного потока реакционную зону (15а), где его гидрируют при температуре 90°С и давлении 3,1 атм. в присутствии катализатора «платина на графите» в количестве 50 г/л при мольном отношении водород : азотная кислота равном 3:1 и объемной скорости по водороду 45,1 час-1 с получением газовой смеси оксида азота (II) и водорода и жидкостного потока, который направляют во вторую по ходу движения жидкостного потока реакционную зону (15б), где жидкостной поток гидрируют в тех же условиях, что и в реакционной зоне (15а). Жидкую фазу после гидрирования в реакционной зоне (15б) и содержащую 0,2% масс, азотной кислоты в количестве 15,7 м3/час направляют в смеситель (10) для производства 22%-ного раствора серной кислоты, необходимой для получения ГАС. Конверсия азотной кислоты 90,0%. Полученные в реакционных зонах (15а) и (15б) газовые смеси оксида азота (II) и водорода объединяют и направляют непосредственно в каталитические зоны на стадии синтеза ГАС. Дополнительный ввод водорода, необходимого для получения соотношения оксид азота (II) : водород равном 1:1,6 на стадии синтеза ГАС, осуществляют в объединенную газовую смесь, полученную в реакционных зонах (15а) и (15б). Получают ГАС в количестве 17892 кг/час (увеличение выхода ГАС по сравнению с прототипом составляет 1,49%). Основные технологические параметры ведения процесса по примеру 2 приведены в таблице.
Примеры 3-11. Процесс проводят также, как и в примере 2. Условия и результаты ведения процесса приведены в таблице.
Предлагаемый способ позволяет увеличить конверсию азотной кислоты на стадии гидрирования с 75% до 95,8% и увеличить выход ГАС до 1,85%.
Реферат
Изобретение относится к химической промышленности, а именно к способу получения гидроксиламинсульфата (ГАС), используемого в качестве одного из основных реагентов в производстве капролактама. Способ получения ГАС включает окисление аммиака с получением нитрозного газа, получением из него оксида азота (II) и азотнокислого конденсата, часть которого направляют на получение 19-25%-ной серной кислоты, а другую часть гидрируют в избытке водорода в двух реакционных зонах (15а) и (15б) при температуре 85-90°С и повышенном давлении в присутствии мелкодисперсного катализатора «платина на графите» с получением газовой смеси оксида азота (II) и водорода, которую направляют непосредственно на стадию синтеза ГАС (14), который получают гидрированием оксида азота (II) водородом при мольном отношении оксид азота (II) : водород, равном 1:(1,5-1,9), в среде 19-25 мас.%, серной кислоты в присутствии мелкодисперсного катализатора «платина на графите» при температуре 30-70°С и давлении 1-4 атм. Способ обеспечивает взрывобезопасное ведение процесса, увеличивает конверсию азотной кислоты на стадии гидрирования до 95%, упрощает технологию и управление за ходом процесса. 2 ил., 1 табл., 11 пр.

Комментарии