Аффинные лиганды, связывающие антитела - RU2440582C2
Код документа: RU2440582C2
Чертежи



Описание
Область техники, к которой относится изобретение
Настоящее изобретение относится к аффинным лигандам, ковалентно связанным с материалом твердого носителя, таким как полимерная матрица, и к их применению для очистки и/или выделения биологических молекул, таких как белки, в частности, антител, таких как моноклональные антитела. Аффинные лиганды содержат два различных домена или функциональных группы: (i) гидрофобный домен и (ii) катионный домен.
Уровень техники
Аффинная хроматография делает возможной селективную и обратимую адсорбцию биологических веществ, таких как моноклональные антитела, на комплементарном связывающем веществе, таком как аффинный лиганд, иммобилизованном на материале твердого носителя, помещенном в аффинную колонку.
Аффинные колонки часто содержат материал твердого носителя, обычно, пористую полимерную матрицу, к которой ковалентно присоединен соответствующий лиганд, непосредственно или посредством линкера. Образец, содержащий биологические вещества, имеющие сродство к лиганду, может приводиться в контакт с аффинным лигандом, ковалентно иммобилизованным на материале твердого носителя, при соответствующих условиях связывания, которые способствуют специфичному связыванию лиганда с биологическими веществами, имеющими сродство к лиганду. После этого колонка может промываться буфером для удаления несвязанного материала, и на следующей стадии биологические вещества, имеющие сродство к лиганду, могут элюироваться и получаться в очищенной или выделенной форме. Соответственно, лиганд должен предпочтительно демонстрировать характеристики специфичного и обратимого связывания с биологическим веществом, таким как антитело, которое является желаемым при очистке или выделении.
Антитела имеют одну или несколько копий Y-образной единицы, состоящей из четырех полипептидных цепей. Каждый Y содержит две идентичных копии "тяжелой" цепи и две идентичных копии "легкой цепи", названных так по их относительным молекулярным массам.
Антитела могут быть разделены на пять классов: IgG, IgM, IgA, IgD и IgE, на основе количества единиц Y и типа тяжелой цепи. Тяжелая цепь определяет подкласс каждого антитела. Тяжелые цепи IgG, IgM, IgA, IgD и IgE известны, как гамма, мю, альфа, дельта и эпсилон соответственно. Легкие цепи каждого антитела могут классифицироваться либо как тип каппа (κ), либо тип лямбда (λ) (описание молекулярной характеристики полипептида).
Для фармацевтических применений, наиболее часто используемое антитело представляет собой IgG, которое может расщепляться на три части, две области F(ab) и одну область Fc, посредством протеолитического фермента папаина, или на две части, одну область F(ab')2 и одну область Fc, посредством протеолитического фермента пепсина.
Области F(ab) содержат "ветви" антитела, которые являются критичными для связывания антигена. Область Fc содержит "хвост" антитела и играет роль при иммунной реакции, а также служит в качестве полезной "ручки" для манипуляций антителом во время некоторых иммунохимических процедур. Количество областей F(ab) на антителе соответствует его подклассу и определяет "валентность" антитела (в широком смысле - это количество "ветвей", с помощью которых антитело может связывать его антиген).
Термин "антитело" обозначает иммуноглобулин, либо природный, либо полученный синтетически, полностью или частично. Все его фрагменты и производные, которые сохраняют способность к специфичному связыванию, также включаются в термин. Типичные фрагменты представляют собой FC, FAB, тяжелую цепь и легкую цепь. Термин также охватывает любой полипептид, имеющий домен связывания, который является гомологичным или по большей части гомологичным, например, по меньшей мере, идентичным на 95%, если сравнивать аминокислотную последовательность с доменом связывания иммуноглобулина. Эти полипептиды могут быть получены из природных источников или получаться синтетически, частично или полностью. Антитело может быть моноклональным или поликлональным. Антитело может представлять собой член любого класса иммуноглобулинов, включая любой из классов, для человека: IgG, IgM, IgA, IgD и IgE. Производные класса IgG, однако, являются предпочтительными в одном из вариантов осуществления настоящего изобретения.
Термин "фрагмент антитела" относится к любому производному антитела, которое имеет менее чем полную длину. Предпочтительно, фрагмент антитела сохраняет, по меньшей мере, значительную часть способности к специфичному связыванию полноразмерного антитела. Примеры фрагментов антитела включают в себя, но, не ограничиваясь этим, Fab, Fab', F(ab')2, scFv, Fv, димерное антитело dsFv и фрагменты Fd. Фрагмент антитела может быть получен с помощью любых средств. Например, фрагмент антитела может быть получен ферментативно или химически посредством фрагментирования интактного антитела, или он может быть получен рекомбинантно из гена, кодирующего частичную последовательность антитела. Альтернативно, фрагмент антитела может быть получен синтетически, полностью или частично. Фрагмент антитела необязательно может представлять собой фрагмент антитела с одной цепью. Альтернативно, фрагмент может содержать множество цепей, которые связаны вместе, например, посредством дисульфидных связей. Фрагмент также необязательно может представлять собой мультимолекулярный комплекс. Функциональный фрагмент антитела будет, как правило, содержать, по меньшей мере, примерно 50 аминокислот, а более конкретно, будет содержать, по меньшей мере, примерно 200 аминокислот.
"Одноцепочечные Fv" (scFv) представляют собой рекомбинантные фрагменты антитела, состоящие только из вариабельной легкой цепи (VL) и вариабельной тяжелой цепи (VH), ковалентно связанных друг с другом посредством полипептидного линкера. Либо VL, либо VH могут представлять собой аминоконцевой домен. Полипептидный линкер может иметь переменную длину и состав, постольку, поскольку два вариабельных домена соединяются без серьезных стерических затруднений. Как правило, линкеры состоят в основном из цепей из остатков глицина и серина, с некоторым количеством остатков глутаминовой кислоты или лизина, включенными между ними для растворимости. "Димерные антитела" представляют собой димерные scFv. Компоненты димерных антител, как правило, имеют более короткие пептидные линкеры, чем большинство scFv, и они показывают предпочтение к ассоциации в виде димеров. Фрагмент "Fv" представляет собой фрагмент антитела, который состоит из одного домена VH и одного VL, удерживаемых вместе посредством нековалентных взаимодействий. Термин "dsFv" используется здесь для обозначения Fv с полученной посредством генной инженерии внутримолекулярной дисульфидной связью, для стабилизации пары VH-VL. Фрагмент "F(ab')2" представляет собой фрагмент антитела, по существу эквивалентный фрагменту, который получают из иммуноглобулинов (как правило, IgG) посредством расщепления с помощью фермента пепсина при pH 4,0-4,5. Фрагмент может быть получен рекомбинантно. Фрагмент "Fab'" представляет собой фрагмент антитела, по существу эквивалентный фрагменту, полученному посредством восстановления дисульфидного мостика или мостиков, соединяющих две части тяжелой цепи во фрагменте F(ab')2. Фрагмент Fab' может быть получен рекомбинантно. Фрагмент "Fab" представляет собой фрагмент антитела, по существу эквивалентный фрагменту, полученному посредством расщепления иммуноглобулинов (как правило, IgG) ферментом папаином. Фрагмент Fab может быть получен рекомбинантно. Сегмент тяжелой цепи фрагмента Fab представляет собой часть Fd. Область "Fc" представляет собой константную область конкретного класса антитела.
Связывание между антигенами и антителами зависит от водородных связей, гидрофобных связей, электростатических сил и сил Ван дер Ваальса. Они все представляют собой связи слабой, нековалентной природы, хотя некоторые взаимодействия между антигеном и антителом могут быть достаточно сильными. Соответственно, константа сродства связывания антитело-антиген может находиться в широких пределах, простирающихся от более низких, чем 105 моль-1, до больших, чем 1012 моль-1. Константы сродства зависят от температуры, pH и растворителя. Кроме сродства антитела к лиганду, общая стабильность комплекса антитело-лиганд определяется также валентностью антигена и антитела и структурным расположением взаимодействующих частей.
Точные константы сродства могут быть определены только для моноклональных антител, которые представляют собой генетически идентичные молекулы, распознающие один-единственный эпитоп на антигене, в то время как для поликлональных антител, широкое распределение сродства может вносить вклад в наблюдаемую константу сродства. В наблюдаемую константу сродства может также вносить вклад тот факт, что поликлональные антитела могут распознавать более одного-единственного эпитопа на одном и том же антигене. Поскольку антитела обычно прикрепляются более чем к одному домену связывания в молекуле, имеют место множественные, кооперативные связи между антителами и их антигенами; этот эффект называется авидностью. Поскольку моноклональные антитела взаимодействуют только с одним-единственным эпитопом на антигене, они более склонны к потере эпитопа во время химической обработки антигена, чем поликлональные антитела. Это может устраняться посредством объединения двух или более моноклональных антител к одному и тому же антигену.
Моноклональные антитела могут быть получены в результате слияния B-лимфоцитов с бессмертными культурами клеток, с получением гибридом. Гибридомы будут производить множество копий точно такого же антитела - главная особенность при разработке антител для терапевтических или диагностических применений.
В настоящее время, наиболее исследованный аффинный лиганд для очистки и выделения биологических молекул, таких как моноклональные антитела, представляет собой белок A. Белок A представляет собой широко используемый лиганд, однако лиганд может страдать несколькими недостатками, такими как проблемы, связанные с нестабильностью, с одновременным вымыванием из колонки, и необходимостью удалять его из конечного продукта или недостаточной смывкой с хроматографической смолы, и, кроме того, белок A является довольно дорогим.
Следовательно, имеется необходимость в новых, стабильных, недорогих лигандах для выделения антител, в частности моноклональных антител, или их аналогов, производных, фрагментов и предшественников, полученных либо из природных, либо из рекомбинантных источников.
Сущность изобретения
В одном из аспектов настоящего изобретения предусматривается материал твердого носителя, имеющий ковалентно иммобилизованный на нем аффинный лиганд, который содержит одну или несколько гидрофобных функциональных групп и одну или несколько катионных функциональных групп,
где, по меньшей мере, одна гидрофобная функциональная группа отделена от, по меньшей мере, одной катионной функциональной группы расстоянием между связями от 5 Å до 20 Å,
где указанный лиганд имеет молекулярную массу от 120 Да до 5000 Да.
В другом аспекте настоящего изобретения, предусматривается материал твердого носителя, имеющий ковалентно иммобилизованный на нем аффинный лиганд, который имеет одну или несколько гидрофобных функциональных групп и одну или несколько гетероароматических функциональных групп,
где, по меньшей мере, одна гидрофобная функциональная группа отделена от, по меньшей мере, одной гетероароматической функциональной группы расстоянием между связями от 5 Å до 20 Å, и
где указанный лиганд имеет молекулярную массу от 120 Да до 5000 Да.
В дополнительном аспекте настоящего изобретения, предусматривается способ выделения биологических молекул, таких как белки, например, антитела, в частности, моноклональные антитела или их производные, включающий стадии (i) предоставления материала твердого носителя, имеющего ковалентно иммобилизованный на нем аффинный лиганд, как определено здесь, (ii) предоставления образца, предположительно, содержащего антитело, имеющее сродство к указанному лиганду, (iii) приведения в контакт указанного лиганда с указанным образцом, предположительно, содержащим указанное антитело, (iv) селективного связывания указанного антитела, когда указанное антитело содержится в указанном образце, и (v) селективного выделения указанного антитела, когда указанное антитело содержится в указанном образце.
Краткое описание фигур
Фиг.1: анализ селективности смолы B2. 1 = супернатант от ферментирования, 2 = Прохождение растворителя через аффинный сорбент (цикл 1), 3 = элюирование (цикл 1), 4 = регенерация/смывка (цикл 1), 5 = промывка (цикл 2), 6 = элюирование (цикл 2), 7 = белка нет, 8 = эталонный образец mAb.
Фиг.2: анализ селективности смолы B3. 1 = супернатант от ферментирования, 2 = Прохождение растворителя через аффинный сорбент (цикл 1), 3 = элюирование (цикл 1), 4 = регенерация/смывка (цикл 1), 5 = промывка (цикл 2), 6 = элюирование (цикл 2), 7 = регенерация/смывка (цикл 2), 8 = эталонный образец mAb.
Фиг.3: анализ селективности смолы D1. 1 = эталонный образец mAb, 2 = супернатант от ферментирования, 3 = Прохождение растворителя через аффинный сорбент (цикл 1), 4 = элюирование (цикл 1), 5 = регенерация/смывка (цикл 1), 6 = промывка (цикл 2), 7 = элюирование (цикл 2), 8 = регенерация/смывка (цикл 2).
Фиг.4: анализ селективности смолы D2. 1 = эталонный образец mAb, 2 = супернатант от ферментирования, 3 = Прохождение растворителя через аффинный сорбент (цикл 1), 4 = элюирование (цикл 1), 5 = регенерация/смывка (цикл 1), 6 = промывка (цикл 2), 7 = элюирование (цикл 2), 8 = регенерация/смывка (цикл 2).
Подробное описание изобретения
Как описано выше, настоящее изобретение относится к новым материалам твердого носителя, имеющим ковалентно иммобилизованный на нем аффинный лиганд, где лиганд содержит конкретный набор функциональных групп. Такие материалы являются особенно полезными для очистки и выделения биологических молекул, таких как белки, например, антитела, в частности, моноклональные антитела или их производные.
Лиганды
Когда здесь используется, термин "лиганд" обозначает молекулу, которая может связывать целевое соединение, например, антитело, в частности, моноклональное антитело. Лиганды предпочтительно связываются со своими партнерами по связыванию, по меньшей мере, по существу специфически ("специфичное связывание").
"Специфичное связывание" относится к свойству лиганда: (1) связываться с партнером по связыванию, например, моноклональным антителом, (2) предпочтительно, таким образом, что относительная масса связанного партнера по связыванию, например, моноклонального антитела, по меньшей мере, в два раза, например, в 50 раз, например, в 100 раз, например, в 1000 раз, или более, больше, чем относительная масса других связанных частиц, иных, чем партнер по связыванию, например, моноклональное антитело. Под относительной массой связанного соединения подразумевается масса связанного соединения минус масса несвязанного соединения, деленная на общую массу партнера по связыванию, то есть
относительная масса связанного соединения = (масса связанного соединения - масса несвязанного соединения)/(масса связанного соединения + масса несвязанного соединения),
для соединения, являющегося партнером по связыванию, или других частиц.
Термин "партнер по связыванию" обозначает любую биологическую молекулу, которая связывается с конкретным лигандом, предпочтительно, по существу специфически. Партнер по связыванию может быть общим для одного или нескольких лигандов. Предпочтительные партнеры по связыванию представляют собой антитела, включая поликлональные антитела и моноклональные антитела. Дополнительными предпочтительными партнерами по связыванию являются фрагменты антител из моноклональных антител или поликлональных антител.
Лиганды в соответствии с настоящим изобретением включают в себя обогащенные или разделенные оптические изомеры по любому или по всем асимметричным атомам, как видно из настоящего описания или иллюстраций. Как рацемические, так и диастереомерные смеси, а также индивидуальные оптические изомеры могут выделяться или синтезироваться с тем, чтобы они по существу не содержали их энантиомерных или диастереомерных партнеров, и они находятся в рамках настоящего изобретения.
Эксперименты неожиданно показали, что определенные классы аффинных лигандов, в том числе такие, где лиганды содержат одну или несколько гидрофобных функциональных групп и одну или несколько катионных функциональных групп, селективно связываются с mAb. Другой обещающий класс аффинных лигандов представляет собой класс, где лиганды содержат одну или несколько гидрофобных функциональных групп и одну или несколько гетероароматических функциональных групп.
Кроме того, обнаружено, что, по меньшей мере, одна гидрофобная функциональная группа предпочтительно должна отделяться, по меньшей мере, от одной катионной функциональной группы расстоянием между связями от 5 Å до 30 Å, например, расстоянием между связями от 5 Å до 20 Å, таким как расстояние между связями от 5 до 19 Å, например, расстоянием между связями от 5 до 18 Å, таким как расстояние между связями от 5 до 17 Å, например, расстоянием между связями от 5 до 16 Å, таким как расстояние между связями от 5 до 15 Å, например, расстоянием между связями от 5 до 14 Å, таким как расстояние между связями от 5 до 13 Å, например, расстоянием между связями от 5 до 12 Å, таким как расстояние между связями от 5 до 11 Å, например, расстоянием между связями от 5 до 10 Å, таким как расстояние между связями от 6 до 14 Å, или таким как расстояние между связями от 7 до 20 Å, например, расстоянием между связями от 7 до 19 Å, таким как расстояние между связями от 7 до 18 Å, например, расстоянием между связями от 7 до 17 Å, таким как расстояние между связями от 7 до 16 Å, например, расстоянием между связями от 7 до 15 Å, таким как расстояние между связями от 7 до 14 Å, например, расстоянием между связями от 7 до 13 Å, таким как расстояние между связями от 7 до 12 Å, например, расстоянием между связями от 7 до 11 Å, таким как расстояние между связями от 7 до 10 Å, например, расстоянием между связями от 8 до 12 Å, или например, расстоянием между связями от 9 до 20 Å, таким как расстояние между связями от 9 до 18 Å, например, расстоянием между связями от 9 до 16 Å, таким как расстояние между связями от 9 до 14 Å, например, расстоянием между связями от 9 до 12 Å, таким как расстояние между связями от 9 до 11 Å, например, расстоянием между связями примерно 10 Å.
Расстояние между связями представляет собой самое короткое внутримолекулярное расстояние между ковалентно связанными химическими остатками вдоль химических связей. Оно вычисляется посредством сложения индивидуальных длин связей атом-атом вдоль кратчайшего внутримолекулярного пути. Типичные длины связей атом-атом равны от 1,2 Å до 1,4 Å.
Пространственное расстояние между, по меньшей мере, одной гидрофобной функциональной группой и, по меньшей мере, одной катионной функциональной группой лиганда предпочтительно меньше, чем 30 Å, например, меньше, чем 28 Å, например, меньше, чем 26 Å, например, меньше, чем 24 Å, например, меньше, чем 22 Å, например, меньше, чем 20 Å, например, меньше, чем 18 Å, например, примерно или меньше, чем 16 Å, например, меньше, чем 15 Å, например, примерно или меньше, чем 14 Å, например, меньше, чем 13 Å, например, примерно или меньше, чем 12 Å, например, меньше, чем 11 Å, например, примерно или меньше, чем 10 Å, например, примерно или меньше, чем 8 Å, например, примерно 6 Å, например, в пределах от 5 до 20 Å, такое как пространственное расстояние от 5 до 19 Å, например, пространственное расстояние от 5 до 18 Å, такое как пространственное расстояние от 5 до 17 Å, например, пространственное расстояние от 5 до 16 Å, такое как пространственное расстояние от 5 до 15 Å, например, пространственное расстояние от 5 до 14 Å, такое как пространственное расстояние от 5 до 13 Å, например, пространственное расстояние от 5 до 12 Å, такое как пространственное расстояние от 5 до 11 Å, например, пространственное расстояние от 5 до 10 Å, такое как пространственное расстояние от 7 до 20 Å, например, пространственное расстояние от 7 до 19 Å, такое как пространственное расстояние от 7 до 18 Å, например, пространственное расстояние от 7 до 17 Å, такое как пространственное расстояние от 7 до 16 Å, например, пространственное расстояние от 7 до 15 Å, такое как пространственное расстояние от 7 до 14 Å, например, пространственное расстояние от 7 до 13 Å, такое как пространственное расстояние от 7 до 12 Å, например, пространственное расстояние от 7 до 11 Å, такое как пространственное расстояние от 7 до 10 Å, например, пространственное расстояние от 9 до 20 Å, такое как пространственное расстояние от 9 до 18 Å, например, пространственное расстояние от 9 до 16 Å, такое как пространственное расстояние от 9 до 14 Å, например, пространственное расстояние от 9 до 12 Å, такое как пространственное расстояние от 9 до 11 Å.
Расстояния между связями и пространственные расстояния могут вычисляться или определяться специалистом в данной области в соответствии с состоянием технологий в данной области. Молекулярное моделирование также может использоваться для определения минимального расстояния между атомами различных функциональных групп лигандов. Молекулярное моделирование может осуществляться, например, с помощью Sybyl/Mendyl 5.4 (Tripos Associates, St. Louis, Mo.), с использованием компьютера Evans and Sutherland PS390 graphics, снабженного стереографическим устройством для просмотра. Структуры соответствующих лигандов могут создаваться посредством конструирования с помощью программы Concord или из библиотек, с последующей минимизацией энергии. Вычисления энергии могут производиться с помощью силового поля Sybyl/Mendyl и параметра Ван дер Ваальса 1,2 Å для водорода. Заряды могут вычисляться с использованием способа Гастайгнера-Хюккеля, который включает в себя сигма-связь и пи-связь.
Лиганд предпочтительно имеет молекулярную массу меньшую, чем 5000 Да, такую как меньшую, чем 4000 Да, например, меньше, чем 3500 Да, такую как меньшую, чем 3000 Да, например, меньше, чем 2500 Да, такую как меньшую, чем 2000 Да, такую как меньшую, чем 1800 Да, например, меньше, чем 1600 Да, такую как меньшую, чем 1500 Да, такую как меньшую, чем 1400 Да, например, меньше, чем 1300 Да, такую как меньшую, чем 1200 Да, такую как меньшую, чем 1100 Да, например, меньше, чем 1000 Да.
В дополнение к этому, лиганд предпочтительно имеет молекулярную массу, большую, чем 120 Да, такую как большую, чем 140 Да, например, большую, чем 160 Да, такую как большую, чем 180 Да, например, большую, чем 200 Да, такую как большую, чем 220 Да, например, молекулярную массу большую, чем 240 Да.
Для уменьшения уровня неспецифичного связывания с катионными группами, лиганд дополнительно может содержать одну или несколько анионных групп для компенсации некоторой части положительного заряда на лиганде. Анионные группы включают в себя, но, не ограничиваясь этим, карбоксилат, сульфонат, сульфат, фосфат и другие отрицательно заряженные ионизируемые группы, и могут, например, располагаться на боковых группах лиганда.
Функциональные группы лигандов
В одной из основных групп пригодных для использования лигандов, каждый лиганд содержит одну или несколько гидрофобных функциональных групп и одну или несколько катионных функциональных групп.
В другой основной группе пригодных для использования лигандов, каждый лиганд содержит одну или несколько гидрофобных функциональных групп и одну или несколько гетероароматических функциональных групп.
Как здесь используется, катионная функциональная группа представляет собой органическую группу, которая имеет положительный заряд в диапазоне pH 3-7. Первичные, вторичные и третичные амины представляют собой типичные примеры катионных групп. Гуанидин представляет собой дополнительный важный пример. Дополнительные примеры катионных функциональных групп приведены в разделе "Катионные функциональные группы" ниже.
Гидрофобная функциональная группа представляет собой органическую группу, способную связываться с поверхностью биологической молекулы, в основном, посредством гидрофобного взаимодействия. Гидрофобные функциональные группы отличаются тем, что они являются по существу неполярными и незаряженными при нормальных физиологических условиях. Гидрофобные остатки отталкиваются водным раствором так, что они стремятся занять внутренние положения в конформации лиганда, когда лиганд находится в водной среде. Также, гидрофобные остатки стремятся занять гидрофобные карманы или бороздки партнера по связыванию лиганда, когда лиганд ассоциируется с партнером по связыванию при нормальных физиологических условиях.
Когда он здесь используется, термин "нормальные физиологические условия" обозначает условия, которые являются типичными внутри живого организма или клетки. Хотя наблюдается, что некоторые органы или организмы создают экстремальные условия, окружающая среда внутри организма и внутри клетки обычно находится вблизи pH 7 (то есть, от pH 6,5 до pH 7,5), содержит воду в качестве преобладающего растворителя и существует при температуре выше 0°C и ниже 50°C. Будет понятно, что концентрация различных солей зависит от органа, организма, клетки или клеточного отдела, который упоминается.
Органические гидрофобные группы, как правило, имеют высокое содержание атомов углерода. Типичные примеры гидрофобных групп представляют сбой линейные и разветвленные алканы, циклические углеводороды, ароматические соединения и сочетания линейных и разветвленных алканов, циклических углеводородов и ароматических соединений. Также и замещенные варианты таких групп рассматриваются как гидрофобные, постольку, поскольку относительное содержание углерода выше определенного предела. Однако процент атомов углерода не является единственным параметром, который влияет на гидрофобность. Также положение и природа других атомов играет важную роль. Например, простой эфир, как правило, является более гидрофобным, чем спирт с таким же количеством атомов углерода и атомов кислорода, и сложный эфир является более гидрофобным, чем диол с таким же составом элементов. Когда один или несколько возможных атомов органической группы, иных, чем углерод, и иных, чем водород, находятся в первичных положениях, относительное количество атомов углерода должно быть выше для группы, которая должна быть гидрофобной, чем когда возможные атомы, иные, чем углерод, и иные, чем водород, находятся во вторичных, третичных или четвертичных положениях. Имея это в виду, авторы определяют гидрофобную группу как органические группы с 75% или более их атомов, иных, чем водород, являющимися атомами углерода, например, 80%, или более, предпочтительно, 85% или более их атомов, иных, чем водород, являются атомами углерода. Например, более низкое значение, 75%, применимо к простым эфирам и сложным эфирам, промежуточное значение, 80%, применимо к амидам и вторичным и третичным аминам, в то время как наивысшее значение, 85%, применимо к спиртам и первичным аминам. Примеры гидрофобных функциональных групп приведены ниже в разделе "Функциональные группы лиганда".
По меньшей мере, одна гидрофобная функциональная группа может содержать или состоять из одной или нескольких групп, выбранных из "алкила", "циклического алкила", "замещенного алкила", "арила", "замещенного арила", "алкенила", "замещенного алкенила", "алкинила", "замещенного алкинила", "аралкила", "замещенного аралкила", "гетероциклила", "замещенного гетероциклила", "гетероциклилалкила", "замещенного гетероциклилалкила", "алкиламиноалкила", "замещенного алкиламиноалкила", "диалкиламиноалкила", "замещенного диалкиламиноалкила", "гетероциклилоксиалкила", "замещенного гетероциклилоксиалкила", "ариламиноалкила", "замещенного ариламиноалкила", "гетероциклиламиноалкила", "замещеного гетероциклиламиноалкила", "алкиламиноалкокси", "замещенной алкиламиноалкокси", "диалкиламиноалкокси", "замещенной диалкиламиноалкокси", "гетероциклилокси" и "замещенной гетероциклилокси", как определено здесь ниже.
Гидрофобные функциональные группы, содержащие алифатические остатки
По меньшей мере, одна гидрофобная функциональная группа может содержать или состоять из необязательно замещенного алифатического остатка и/или необязательно замещенного ароматического остатка. Алифатические остатки, как правило, относятся к углеводородам, такие, например, как алкильные, алкиленовые и алкинильные остатки, которые могут быть замещенными или незамещенными.
"Алкил" как здесь используется, включает в себя алкильные группы с прямой цепью, такие как метил, этил, пропил, бутил, пентил, гексил, гептил, октил, нонил, децил, ундецил, додецил, и тому подобное. "Алкил" также включает в себя изомеры с разветвленной цепью алкильных групп с прямой цепью, включая, но, не ограничиваясь этим, следующие группы, которые приводятся в качестве примера: -CH(CH3)2, -CH(CH3)(CH2CH3), -CH(CH2CH3)2, -C(CH3)3, -C(CH2CH3)3, -CH2CH(CH3)2, -CH2CH(CH3)(CH2CH3), -CH2CH(CH2CH3)2, -CH2C(CH3)3, -CH2C(CH2CH3)3, -CH(CH3)CH(CH3)(CH2CH3), -CH2CH2CH(CH3)2, -CH2CH2CH(CH3)(CH2CH3), -CH2CH2CH(CH2CH3)2, -CH2CH2C(CH3)3, -CH2CH2C(CH2CH3)3, -CH(CH3)CH2CH(CH3)2, -CH(CH3)CH(CH3)CH(CH3)CH(CH3)2, -CH(CH2CH3)CH(CH3)CH(CH3)(CH2CH3) и другие.
Алифатический остаток может представлять собой необязательно замещенный линейный алифатический остаток или необязательно замещенный разветвленный алифатический остаток. Алифатический остаток также может представлять собой необязательно замещенный циклический алкил. "Циклический алкил" включает в себя группы, такие как циклопропил, циклобутил, циклопентил, циклогексил, циклогептил и циклооктил, и такие кольца, замещенные алкильными группами с прямой и разветвленной цепью, как определено выше, а также включает в себя полициклические алкильные группы, такие как, но, не ограничиваясь этим, адамантил, норборнил и бицикло[2.2.2]октил, и такие кольца, замещенные алкильными группами с прямой и разветвленной цепью, как определено выше. Таким образом, незамещенные алкильные группы включают в себя первичные алкильные группы, вторичные алкильные группы и третичные алкильные группы. Незамещенные алкильные группы могут быть связаны с одним или несколькими атомами углерода, атомами кислорода, атомами азота и/или атомами серы в лиганде.
Циклический алифатический остаток может, например, содержать или состоять из C5-C16 циклоалкильной группы. Более короткие цепи также могут иметь место, как правило, когда циклоалкил является замещенным арильным или гетероарильным остатком.
"Замещенный алкил" относится к незамещенной алкильной группе, как определено выше, в которой одна или несколько связей с атомами углерода или водорода заменяется связью с атомами, иными, чем водород, и иными, чем углерод, такими как, но, не ограничиваясь этим, атом галогена в галогенидах, такой как F, Cl, Br и I; и атом кислорода в группах, таких как гидроксильные группы, алкокси группы, арилокси группы и сложноэфирные группы; атом серы в группах, таких как тиольные группы, алкил- и арилсульфидные группы, сульфоновые группы, сульфонильные группы и сульфоксидные группы; атом азота в группах, таких как амины, амиды, алкиламины, диалкиламины, ариламины, алкилариламины, диариламины, N-оксиды, имиды, и энамины; атом кремния в группах, таких как в триалкилсилильные группы, диалкиларилсилильные группы, алкилдиарилсилильные группы и триарилсилильные группы; и другие гетероатомы в различных других группах.
Замещенные алкильные группы также включают в себя группы, в которых одна или несколько связей с атомами углерода или водорода заменяется связью с гетероатомом, таким как кислород в карбонильных, карбоксильных и сложноэфирных группах; азот в группах, таких как имины, оксимины, гидразоны и нитрилы. Замещенные алкильные группы, также включают в себя, среди прочего, алкильные группы, в которых одна или несколько связей с атомом углерода или водорода заменяются одной или несколькими связями с атомом галогена. Другие замещенные алкильные группы включают в себя такие группы, в которых одна или несколько связей с атомом углерода или водорода заменяется связью с атомом кислорода, так что замещенная алкильная группа включает в себя гидроксильную, алкокси, арилокси группу или гетероциклилокси группу. Другие алкильные группы включают в себя алкильные группы, которые имеют группу амина, алкиламина, диалкиламина, ариламина, (алкил)(арил)амина, диариламина, гетероциклиламина, (алкил)(гетероциклил)амина, (арил)(гетероциклил)амина или дигетероциклиламина.
В одном из вариантов осуществления, алифатическая функциональная группа является предпочтительно замещенной арильной группой, такой как (C6-C12)арильная группа, рассмотренная здесь ниже, которая может, в свою очередь, также быть замещенной, как также описано здесь. Пример замещенной арильной группы включает в себя "аралкильную группу", которая может быть замещенной или незамещенной.
Соответственно, "аралкил" относится к незамещенным алкильным группам, как определено выше, в которых связь с атомом водорода или углерода незамещенной алкильной группы заменяется связью с арильной группой, как определено выше. Например, метил (-CH3) представляет собой незамещенную алкильную группу. Если атом водорода метильной группы заменяется связью с фенильной группой, как если атом углерода метила связывается с атомом углерода бензола, тогда соединение представляет собой незамещенную аралкильную группу (то есть, бензильную группу). Таким образом, включаются, но, не ограничиваясь этим, такие группы как группа бензила, дифенилметила и 1-фенилэтил (-CH(C6H5)(CH3)), 2-фенилэтильная группа, 2-нафтилэтильная группа, и тому подобное.
"Замещенный аралкил" имеет такое же значение по отношению к незамещенным аралкильным группам, какое замещенные арильные группы имеют по отношению к незамещенным арильным группам. Однако замещенная аралкильная группа также включает в себя группы, в которых связь с атомом углерода или водорода алкильной части группы, заменяется связью с атомом, иным, чем атом углерода, или иным, чем атом водорода. Примеры замещенных аралкильных групп включают в себя, но, не ограничиваясь этим, -CH2C(=O)(C6H5) и -CH2(2-метилфенил), среди прочих.
В одном из вариантов осуществления, необязательно замещенный алифатический остаток содержит или состоит из C5-C20 алкильной группы. Более короткие цепи также могут иметь место, как правило, когда алкил является замещенным арильным или гетероарильным остатком. Дополнительные примеры алкильных групп, замещенных арилом или гетероарилом, включают в себя, например, линейную (C1-C10), разветвленную (C4-C10) или циклическую (C5-C10) группу, такую как метильная группа, этильная группа, пропильная группа, такая как н-пропильная группа и изопропильная группа, бутильную группу, такую как н-бутильная группа, изобутильная группа, трет-бутильная группа, н-амильная группа, пентильную группу, такую как неопентильная группа, циклопентильная группа, гексильную группу, такую как н-гексильная группа, циклогексильная группа, гептильную группу, октильную группу, такую как н-октильная группа, нонильную группу, такую как н-нонильная группа, децильную группу, такую как н-децильная группа, ундецильная группа, додецильная группа, ментильную группа, 2,3,4-триметил-3-пентильную группа, 2,4-диметил-3-пентильную группу, и тому подобное.
В одном из вариантов осуществления, C5-C20 алкильная группа может также быть замещенной, например, атомом галогена, алкокси группой, арилокси группой, алкилтио группой или арилтио группой. Примеры атома галогена представляют собой атом фтора, атом хлора, атом брома и атом йода. Примеры алкоксильной группы включают в себя, например, (C1-C4) алкокси группу, такую как метокси группа, этокси группа, н-пропокси группа, трет-бутокси группа или что-либо подобное. Примеры алкилтио группы включают в себя, например, группы, состоящие из (C1-C10)алкильной группы, как описано выше, и тио группы, и их конкретные примеры включают в себя, например, н-пропилтио группу, трет-бутилтио группу, или что-либо подобное. Примеры арилтио группы включают в себя, например, те группы, которые состоят из (C6-C12)арильной группы, как описано выше, и тио группы, и их конкретные примеры включают в себя, например, фенилтио группу, или что-либо подобное. Примеры арилокси группы, которая может присутствовать на арильных, гетероарильных и насыщенных углеводородных группах, например, включают в себя группы, которые состоят из (C6-C12)арильной группы, как описано выше, и окси группы, и их конкретные примеры включают в себя, например, фенокси группу, или что-либо подобное.
Алкильные группы, описанные здесь выше, могут содержать одну или несколько двойных связей углерод-углерод (алкенильные группы) или одну или несколько тройных связей углерод-углерод (алкинильные группы).
"Алкенил" относится к группам с прямой и разветвленной цепью и к циклическим группам, таким как те, которые описаны по отношению к незамещенным алкильным группам, как определено выше, за исключением того, что существует, по меньшей мере, одна двойная связь между двумя атомами углерода. Примеры включают в себя, но, не ограничиваясь этим, винил, -CH=C(H)(CH3), -CH=C(CH3)2, -C(CH3)=C(H)2, -C(CH3)=C(H)(CH3), -C(CH2CH3)=CH2, циклогексенил, циклопентенил, циклогексадиенил, бутадиенил, пентадиенил и гексадиенил, среди прочего.
"Замещенный алкенил" имеет такое же значение по отношению к незамещенным алкенильным группам, какое замещенные алкильные группы имеют по отношению к незамещенным алкильным группам. Замещенная алкенильная группа включает в себя алкенильные группы, в которых атом, иной, чем углерод, или иной, чем водород, связан с атомом углерода, связанным двойной связью с другим атомом углерода, и такие группы, в которых один из атомов, иных, чем углерод, или иных, чем водород, связывается с атомом углерода, не участвующим в двойной связи с другим атомом углерода.
"Алкинил" относится к группам с прямой и разветвленной цепью, таким как группы, которые описаны по отношению к алкильным группам, как определено выше, за исключением того, что, по меньшей мере, одна тройная связь существует между двумя атомами углерода. Примеры включают в себя, но, не ограничиваясь этим, -CC(H), -CC(CH3), -CC(CH2CH3), -C(H2)CC(H), -C(H)2CC(CH3), и -C(H)2CC(CH2CH3), среди прочего.
"Замещенный алкинил" имеет такое же значение по отношению к незамещенным алкинильным группам, какое замещенные алкильные группы имеют по отношению к незамещенным алкильным группам. Замещенная алкинильная группа включает в себя алкинильные группы, в которых атом, иной, чем атом углерода, или иной, чем атом водорода, связывается с атомом углерода, связанным тройной связью с другим атомом углерода, и группы, в которых атом, иной, чем углерод, или иной, чем водород, связывается с атомом углерода, не участвующим в тройной связи с другим атомом углерода.
Дополнительные примеры замещенных алкильных групп описаны здесь ниже.
"Алкиламиноалкил" относится к незамещенной алкильной группе, как определено выше, в которой атом углерод, или водородная связь заменяется связью с атомом азота, который связан с атомом водорода и незамещенной алкильной группой, как определено выше. Например, метил (-CH3) представляет собой незамещенную алкильную группу. Если атом водорода метильной группы заменяется связью с атомом азота, который связан с атомом водорода и этильной группой, тогда полученное соединение представляет собой -CH2-N(H)(CH2CH3), которое является незамещенной алкиламиноалкильной группой.
"Замещенный алкиламиноалкил" относится к незамещенной алкиламиноалкильной группе, как определено выше, за исключением случаев, когда одна или несколько связей с атомом углерода или водорода в одной или в обеих алкильных группах заменяются связью с атомом, иным, чем углерод, или иным, чем водород, как описано выше, по отношению к замещенным алкильным группам, за исключением того, что связь с атомом азота во всех алкиламиноалкильных группах сама по себе не квалифицирует все алкиламиноалкильные группы как замещенные. Однако замещенные алкиламиноалкильные группы включают в себя группы, в которых атом водорода, связанный с атомом азота группы, заменяется атомом, иным, чем углерод, и иным, чем водород.
"Диалкиламиноалкил" относится к незамещенной алкильной группе, как определено выше, в которой углеродная связь или водородная связь заменяется связью с атомом азота, который связывается с двумя другими одинаковыми или различными незамещенными алкильными группами, как определено выше.
"Замещенный диалкиламиноалкил" относится к незамещенной диалкиламиноалкильной группе, как определено выше, в которой одна или несколько связей с атомом углерода или водорода в одной или нескольких из алкильных групп, заменяется связью с атомом, иным, чем углерод, и иным, чем водород, как описано по отношению к замещенным алкильным группам. Связь с атомом азота во всех диалкиламиноалкильных группах сама по себе не квалифицирует все диалкиламиноалкильные группы как замещенные.
"Гетероциклилоксиалкил" относится к незамещенной алкильной группе, как определено выше, в которой углеродная связь или водородная связь заменяется связью с атомом кислорода, который связан с незамещенной гетероциклильной группой, как определено выше.
"Замещенный гетероциклилоксиалкил" относится к незамещенной гетероциклилоксиалкильной группе, как определено выше, в которой связь с группой углерода или водорода алкильной группы гетероциклилоксиалкильной группы связывается с атомом, иным, чем углерод, и иным, чем водород, как описано выше по отношению к замещенным алкильным группам, или в которых гетероциклильная группа гетероциклилоксиалкильной группы является замещенной гетероциклильной группой, как определено выше.
"Ариламиноалкил" относится к незамещенной алкильной группе, как определено выше, в которой углеродная связь или водородная связь заменяется связью с атомом азота, который связывается, по меньшей мере, с одной незамещенной арильной группой, как определено выше.
"Замещенный ариламиноалкил" относится к незамещенной ариламиноалкильной группе, как определено выше, за исключением случаев, когда либо алкильная группа ариламиноалкильной группы является замещенной алкильной группой, как определено выше, либо арильная группа ариламиноалкильной группы является замещенной арильной группой, за исключением того, что связи с атомом азота во всех ариламиноалкильных группах сами по себе не квалифицируют все ариламиноалкильные группы как замещенные. Однако замещенные ариламиноалкильные группы включают в себя группы, в которых водород, связанный с атомом азота группы, заменяется атомом, иным, чем углерод, и иным, чем водород.
"Гетероциклиламиноалкил" относится к незамещенной алкильной группе, как определено выше, в которой углеродная или водородная связь заменяется связью с атомом азота, который связан, по меньшей мере, с одной незамещенной гетероциклильной группой, как определено выше.
"Замещенный гетероциклиламиноалкил" относится к незамещенным гетероциклиламиноалкильным группам, как определено выше, в которых гетероциклильная группа является замещенной гетероциклильной группой, как определено выше, и/или алкильная группа является замещенной алкильной группой, как определено выше. Связи с атомом азота во всех гетероциклиламиноалкильных группах сами по себе не квалифицируют все гетероциклиламиноалкильные группы как замещенные. Однако замещенные гетероциклиламиноалкильные группы включают в себя группы, в которых водород, связанный с атомом азота группы, заменяется атомом, иным, чем углерод, и иным, чем водород.
"Алкиламиноалкокси" относится к незамещенной алкильной группе, как определено выше, в которой углеродная или водородная связь заменяется связью с атомом кислорода, который связывается с исходным соединением, и в которой другая углеродная или водородная связь незамещенной алкильной группы, связывается с атомом азота, который связывается с атомом водорода и незамещенной алкильной группой, как определено выше.
"Замещенная алкиламиноалкокси" относится к незамещенным алкиламиноалкокси группам, как определено выше, в которых связь с атомом углерода или водорода алкильной группы, связанным с атомом кислорода, который связан с исходным соединением, заменяется одной или несколькими связями с атомами, иными, чем углерод, и иными, чем водород, как обсуждается выше по отношению к замещенным алкильным группам, и/или если атом водорода, связанный с амино группой, связывается с атомом, иным, чем углерод, и иным, чем водород, и/или если алкильная группа, связанная с атомом азота амина, связывается с атомом, иным, чем углерод, и иным, чем водород, как описано выше по отношению к замещенным алкильным группам. Присутствие функциональной группы амина и алкокси во всех алкиламиноалкокси группах само по себе не квалифицирует все такие группы как замещенные алкиламиноалкокси группы.
"Незамещенная диалкиламиноалкокси" относится к незамещенной алкильной группе, как определено выше, в которой углеродная или водородная связь заменяется связью с атомом кислорода, который связан с исходным соединением, и в которой другая углеродная или водородная связь незамещенной алкильной группы связывается с атомом азота, который связывается с двумя другими одинаковыми или различными незамещенными алкильными группами, как определено выше.
"Замещенная диалкиламиноалкокси" относится к незамещенной диалкиламиноалкокси группе, как определено выше, в которой связь с атомом углерода или водорода алкильной группы, связанным с атомом кислорода, который связан с исходным соединением, заменяется одной или несколькими связями с атомами, иными, чем углерод, и иными, чем атом водорода, как обсуждается выше по отношению к замещенным алкильным группам, и/или если одна или несколько алкильных групп, связанных с азотом амина, связывается с атомом, иным, чем углерод, и иным, чем водород, как описано выше по отношению к замещенным алкильным группам. Присутствие функциональной группы амина и алкокси во всех диалкиламиноалкокси группах само по себе не квалифицирует все такие группы как замещенные диалкиламиноалкокси группы.
"Гетероциклилокси" относится к гидроксильной группе (-OH), в которой связь с атомом водорода заменяется связью с кольцевым атомом в остальном незамещенной гетероциклильной группы, как определено выше.
"Замещенная гетероциклилокси" относится к гидроксильной группе (-OH), в которой связь с атомом водорода заменяется связью с кольцевым атомом замещенной гетероциклильной группы, как определено выше.
Гидрофобные функциональные группы, содержащие ароматические остатки
Ароматические остатки могут представлять собой необязательно замещенные арильные или гетероарильные остатки. "Арил" включает в себя, но, не ограничиваясь этим, такие группы, как фенил, бифенил, антраценил, нафтенил, в качестве примера. Хотя "арил" включает в себя группы, содержащие конденсированные кольца, такие как нафталин, он не включает в себя арильные группы, которые имеют другие группы, такие как алкильные группы или группы галогенов, связанные с одним из членов кольца, поскольку арильные группы, такие как толил, рассматриваются здесь как замещенные арильные группы, как описано здесь ниже. Арильные группы могут быть связанными с одним или несколькими атомами углерода, атомами кислорода, атомами азота и/или атомами серы в лиганде.
"Замещенная арильная группа" имеет такое же значение по отношению к незамещенным арильным группам, какое замещенные алкильные группы имеют по отношению к незамещенным алкильным группам. Однако замещенная арильная группа также включает в себя арильные группы, в которых один из ароматических атомов углерода связан с одним из атомов, иных, чем углерод, или иных, чем водород, описанных выше, и также включает в себя арильные группы, в которых один или несколько ароматических атомов углерода арильной группы связываются с замещенной и/или незамещенной алкильной, алкенильной или алкинильной группой, как определено здесь. Они включают в себя расположение связей, при котором два атома углерода арильной группы связываются с двумя атомами алкильной, алкенильной или алкинильной группы, определяя слитую кольцевую систему (например, дигидронафтил или тетрагидронафтил).
Примеры арила и гетероарила включают в себя, например, (C6-C12)арильную группу, такую как фенильная группа, толильная группа, нафтильная группа, бифенильная группа или что-либо подобное, и (C4-C5)гетероарильную группу или пиридильную группу, или что-либо подобное.
Также, когда, по меньшей мере, одна гидрофобная функциональная группа содержит или состоит из необязательно замещенного ароматического остатка, ароматический остаток может выбираться из группы, состоящей из ароматических остатков, содержащих или состоящих из флуоренила, пирроила, фуранила, тиенила, тиофенила, тиазолила, изоиндолила, хинолинила, изохинолинила, оксазолила и пуринила. Дополнительные примеры включают в себя, но, не ограничиваясь этим, тетрагидротиофенил, S-окисленный тетрагидротиофенил, тетразолил, бензофуранил, тианафталенил, индоленил, бензимидазолил, пиперидинил, 4-пиперидонил, пирролидинил, 2-пирролидонил, пирролинил, тетрагидрофуранил, тетрагидрохинолинил, тетрагидроизохинолинил, декагидрохинолинил, октагидроизохинолинил, азоцинил, триазинил, 6H-1,2,5-тиадиазинил, 2H,6H-1,5,2-дитиазинил, тиантренил, пиранил, изобензофуранил, хроменил, ксантенил, феноксантиинил, 2H-пирролил, изотиазолил, изоксазолил, пиразинил, пиридазинил, индолизинил, изоиндолил, 3H-индолил, 1H-индазолил, 4H-хинолизинил, фталазинил, нафтиридинил, хиноксалинил, хиназолинил, циннолинил, птеридинил, 4aH-карбазолил, карбазолил, β-карболинил, фенантридинил, акридинил, пиримидинил, фенантролинил, феназинил, фенотиазинил, фуразанил, феноксазинил, изохроманил, хроманил, имидазолидинил, имидазолинил, пиразолидинил, пиразолинил, пиперазинил, индолинил, хинуклидинил, морфолинил, оксазолидинил, бензотриазолил, бензизоксазолил, оксиндолил, бензоксазолинил и изатиноил.
В качестве примера, а не ограничения, связанные через углерод гетероциклы могут связываться в положении 2, 3, 4, 5 или 6 пиридина, в положении 3, 4, 5 или 6 пиридазина, в положении 2, 4, 5 или 6 пиримидина, в положении 2, 3, 5 или 6 пиразина, в положении 2, 3, 4 или 5 фурана, тетрагидрофурана, тиофурана, тиофена, пиррола или тетрагидропиррола, в положении 2, 4 или 5 оксазола, имидазола или тиазола, в положении 3, 4 или 5 изоксазола, пиразола или изотиазола, в положении 2 или 3 азиридина, положении 2, 3 или 4 азетидина, в положении 2, 3, 4, 5, 6, 7 или 8 хинолина или в положении 1, 3, 4, 5, 6, 7 или 8 изохинолина. Еще чаще, связанные через атом углерода гетероциклы включают в себя 2-пиридил, 3-пиридил, 4-пиридил, 5-пиридил, 6-пиридил, 3-пиридазинил, 4-пиридазинил, 5-пиридазинил, 6-пиридазинил, 2-пиримидинил, 4-пиримидинил, 5-пиримидинил, 6-пиримидинил, 2-пиразинил, 3-пиразинил, 5-пиразинил, 6-пиразинил, 2-тиазолил, 4-тиазолил или 5-тиазолил.
В качестве примера, а не ограничения, связанные через атом азота гетероциклы связываются в положении 1 азиридина, азетидина, пиррола, пирролидина, 2-пирролина, 3-пирролина, имидазола, имидазолидина, 2-имидазолина, 3-имидазолина, пиразола, пиразолина, 2-пиразолина, 3-пиразолина, пиперидина, пиперазина, индола, индолина, 1H-индазола, в положении 2 изоиндола или изоиндолина, в положении 4 морфолина и в положении 9 карбазола или β-карболина. Как правило, гетероциклы, связанные через атом азота, включают в себя 1-азиридил, 1-азетедил, 1-пирролил, 1-имидазолил, 1-пиразолил и 1-пиперидинил.
Как будет ясно из того, что приведено выше, гетероароматическая группа может также выбираться из группы, состоящей из гетероароматических групп, содержащих или состоящих из необязательно замещенных, конденсированных гетероароматических соединений. Примеры включают в себя, например, индол, бензотиофен, бензотриазен и хинолин.
В одном из вариантов осуществления, ароматический остаток может быть замещенным одной или несколькими необязательно замещенными алифатическими группами, такими как необязательно замещенные алифатические группы, рассмотренные здесь, непосредственно выше, такими как линейная, разветвленная или циклическая (C1-C10)алкильная группа, например, метильная группа, этильная группа, изопропильная группа, н-бутильная группа, трет-бутильная группа, н-амильная группа, н-гексильная группа, и тому подобное.
Ароматический остаток может быть замещенным одним или несколькими гетероатомами или замещенным одной или несколькими ароматическими группами, или замещенным одной или несколькими гетероароматическими группами.
Также, ароматический остаток может, например, быть замещен замещенным алкилом или арилом, или гетероарилом, где ароматический остаток или алкил, или арил, или гетероарил является замещенным гетероатомом, выбранным из O, N, S и галогена, или замещенным одной или несколькими группами, выбранными из гидроксила, амино, тиола, галогена, карбонила, группы карбоновой кислоты, эфирной и сложноэфирной группы.
Арильные и гетероарильные группы также могут быть замещенными, например, атомом галогена, алкокси группой, арилокси группой, алкилтио группой или арилтио группой. Примеры атома галогена представляют собой атом фтора, атом хлора, атом брома и атом йода. Примеры алкоксильной группы включают в себя, например, (C1-C4)алкокси группу, такую как метокси группа, этокси группа, н-пропокси группа, трет-бутокси группа, или что-либо подобное. Примеры алкилтио группы включают в себя, например, группы, состоящие из (C1-C10)алкильной группы, как описано выше, и тио группы, и их конкретные примеры включают в себя, например, н-пропилтио группу, трет-бутилтио группу, или что-либо подобное. Примеры арилтио группы включают в себя, например, группы, которые состоят из (C6-C12)арильной группы, как описано выше, и тио группы, и их конкретные примеры включают в себя, например, фенилтио группу, или что-либо подобное. Примеры арилокси группы, которая может присутствовать на арильной, гетероарильной и насыщенной углеводородной группах, например, на группах, которые состоят из (C6-C12)арильной группы, как описано выше, и окси группы, и их конкретные примеры включают в себя, например, фенокси группу, или что-либо подобное.
Термин "гетероциклил", как здесь используется, относится как к ароматическим, так и к неароматическим кольцевым соединениям, включая моноциклические, бициклические и полициклические кольцевые соединения, такие как, но, не ограничиваясь этим, хинуклидил, содержащие 3 или более членов кольца, из которых один или несколько представляют собой гетероатом, такой как, но, не ограничиваясь этим, N, O и S. Хотя "гетероциклил" включает в себя конденсированные гетероциклические кольца, такие как бензимидазолил, он не включает в себя гетероциклильные группы, которые имеют другие группы, такие как алкильные группы или группы галогенов, связанные с членами кольца, когда соединения, такие как 2-метилбензимидазолил, являются замещенными гетероциклильными группами. Примеры гетероциклильных групп включают в себя, но, не ограничиваясь этим: ненасыщенные 3 - 8-членные кольца, содержащие 1-4 атома азота, такие как, но, не ограничиваясь этим, пирролил, пирролинил, имидазолил, пиразолил, пиридил, дигидропиридил, пиримидил, пиразинил, пиридазинил, триазолил (например, 4H-1,2,4-триазолил, 1H-1,2,3-триазолил, 2H-1,2,3-триазолил, и тому подобное), тетразолил, (например, 1H-тетразолил, 2H-тетразолил, и тому подобное); насыщенные 3-8-членные кольца, содержащие 1-4 атома азота, такие как, но, не ограничиваясь этим, пирролидинил, имидазолидинил, пиперидинил, пиперазинил; конденсированные ненасыщенные гетероциклические группы, содержащие 1-4 атома азота, такие как, но, не ограничиваясь этим, индолил, изоиндолил, индолинил, индолизинил, бензимидазолил, хинолил, изохинолил, индазолил, бензотриазолил; ненасыщенные 3-8-членные кольца, содержащие 1-2 атома кислорода и 1-3 атома азота, такие как, но, не ограничиваясь этим, оксазолил, изоксазолил, оксадиазолил (например, 1,2,4-оксадиазолил, 1,3,4-оксадиазолил, 1,2,5-оксадиазолил, и тому подобное); насыщенные 3-8-членные кольца, содержащие 1-2 атома кислорода и 1-3 атома азота, такие как, но, не ограничиваясь этим, морфолинил; ненасыщенные конденсированные гетероциклические группы, содержащие 1-2 атома кислорода и 1-3 атома азота, например, бензоксазолил, бензоксадиазолил, бензоксазинил (например, 2H-1,4-бензоксазинил, и тому подобное); ненасыщенные 3-8-членные кольца, содержащие 1-3 атома серы и 1-3 атома азота, такие как, но, не ограничиваясь этим, тиазолил, изотиазолил, тиадиазолил (например, 1,2,3-тиадиазолил, 1,2,4- тиадиазолил, 1,3,4-тиадиазолил, 1,2,5-тиадиазолил и т.п.); насыщенные 3-8-членные кольца, содержащие 1-2 атома серы и 1-3 атома азота, такие как, но, не ограничиваясь этим, тиазолодинил; насыщенные и ненасыщенные 3-8 членные кольца, содержащие 1-2 атома серы, такие как, но, не ограничиваясь этим, тиенил, дигидродитиинил, дигидродитионил, тетрагидротиофен, тетрагидротиопиран; ненасыщенные конденсированные гетероциклические кольца, содержащие 1-2 атома серы и 1-3 атома азота, такие как, но, не ограничиваясь этим, бензотиазолил, бензотиадиазолил, бензотиазинил (например, 2H-1,4-бензотиазинил, и тому подобное), дигидробензотиазинил (например, 2H-3,4-дигидробензотиазинил, и тому подобное), ненасыщенные 3-8 членные кольца, содержащие атомы кислорода, такие как, но, не ограничиваясь этим, фурил; ненасыщенные конденсированные гетероциклические кольца, содержащие 1-2 атома кислорода, такие как бензодиоксолил (например, 1,3-бензодиоксоил, и тому подобное); ненасыщенные 3-8-членные кольца, содержащие атом кислорода и 1-2 атома серы, такие как, но, не ограничиваясь этим, дигидрооксатиинил; насыщенные 3-8-членные кольца, содержащие 1-2 атома кислорода и 1-2 атома серы, такие как 1,4-оксатиан; ненасыщенные конденсированные кольца, содержащие 1-2 атома серы, такие как бензотиенил, бензодитиинил; и ненасыщенные конденсированные гетероциклические кольца, содержащие атом кислорода и 1-2 атома кислорода, такие как бензоксатиинил. Гетероциклильная группа также включает в себя группы, описанные выше, в которых один или несколько атомов S в кольце связаны двойной связью с одним или двумя атомами кислорода (сульфоксиды и сульфоны). Например, гетероциклильные группы включают в себя тетрагидротиофен, тетрагидротиофеноксид и тетрагидротиофен 1,1-диоксид. Предпочтительные гетероциклильные группы содержат 5 или 6 членов кольца. Более предпочтительные гетероциклильные группы включают в себя морфолин, пиперазин, пиперидин, пирролидин, имидазол, пиразол, 1,2,3-триазол, 1,2,4-триазол, тетразол, тиоморфолин, тиоморфолин, в которых атом S тиоморфолина связан с одним или несколькими атомами O, пирролом, гомопиперазином, оксазолидин-2-оном, пирролидин-2-оном, оксазолом, хинуклидином, тиазолом, изоксазолом, фураном и тетрагидрофураном.
"Замещенный гетероциклил" относится к незамещенной гетероциклильной группе, как определено выше, в которой один из членов кольца связан с атомом, иным, чем водорода, так как описано выше по отношению к замещенным алкильным группам и замещенным арильным группам. Примеры включают в себя, но, не ограничиваясь этим, 2-метилбензимидазолил, 5-метилбензимидазолил, 5-хлорбензтиазолил, 1-метилпиперазинил и 2-хлорпиридил, среди прочего.
"Гетероциклилалкил" относится к незамещенным алкильным группам, как определено выше, в которых связь с водородом или углеродом незамещенной алкильной группы заменяется связью с гетероциклильной группой, как определено выше. Например, метил (-CH3) представляет собой незамещенную алкильную группу. Если атом водорода метильной группы заменяется связью с гетероциклильной группой, например, если атом углерода метила связывается с атомом углерода 2 пиридина (один из атомов углерода, связанных с N пиридина) или атомами углерода 3 или 4 пиридина, тогда соединение представляет собой незамещенную гетероциклилалкильную группу.
"Замещенный гетероциклилалкил" имеет такое же значение по отношению к незамещенным гетероциклилалкильным группам, какое замещенные аралкильные группы имеют по отношению к незамещенным аралкильным группам. Однако замещенная гетероциклилалкильная группа также включает в себя группы, в которых атом, иной, чем водород, связывается с гетероатомом в гетероциклильной группе гетероциклилалкильной группы, таким как, но, не ограничиваясь этим, атом азота в пиперидиновом кольце пиперидинилалкильной группы.
В одном из конкретных вариантов осуществления, необязательно замещенный ароматический остаток может выбираться из группы, состоящей из ароматических и гетероароматических остатков, содержащих или состоящих из фенила, нафтила, флуоренила, пиридина, фурана, тиофена, индола, изоиндола, хинолина, изохинолина, оксазола, пирамидина и пурина.
Замещенные ароматические остатки могут также быть замещенными одной или несколькими алифатическими группами или замещенными одним или несколькими гетероатомами, или замещенными одной или несколькими ароматическими группами, или замещенными одной или несколькими гетероароматическими группами.
По меньшей мере, одна гидрофобная функциональная группа может также содержать или состоять из необязательно замещенного гетероароматического остатка, например, гетероароматического остатка, выбранного из группы, состоящей из гетероароматических остатков, содержащих или состоящих из фурана, пиррола и тиофена, или гетероароматического остатка, выбранного из группы, состоящей из гетероароматических остатков, содержащих или состоящих из конденсированных гетероароматических соединений, таких как слитое гетероароматическое соединение, выбранное из группы, состоящей из индола, бензотиофена, бензотриазена и хинолина.
В указанных выше вариантах осуществления, ароматический остаток может быть замещенным алкилом или арилом, или гетероарилом.
Также, ароматический остаток или алкил, или арил, или гетероарил может быть замещенным гетероатомом, выбранным из O, N, S и галогена, и/или ароматическим остатком, или алкилом или арилом, или гетероарил может быть замещенным одной или несколькими группами, выбранными из гидроксила, амино, тиола, галогена, карбонила, группы карбоновой кислоты, эфирной и сложноэфирной группы.
В одном из вариантов осуществления, лиганд содержит, по меньшей мере, один аминокислотный остаток, содержащий гидрофобную группу, например, гидрофобную группу, которая содержит или состоит из ароматической группы, или гидрофобную группу, которая содержит или состоит из алифатической группы.
Катионные функциональные группы
Катионные функциональные группы являются положительно заряженными либо благодаря постоянному положительному заряду, либо благодаря ассоциации с ионом H при нормальных физиологических условиях. Катионные функциональные группы притягиваются водным раствором таким образом, что стремятся занять поверхностные положения в конформации лиганда, когда лиганд находится в водной среде, при нормальных физиологических условиях. Катионные функциональные группы будут стремиться к анионным группам партнеров по связыванию лиганда, когда лиганд ассоциируется с партнером по связыванию при нормальных физиологических условиях.
Катионная функциональная группа предпочтительно выбирается из катионных групп, содержащих один или несколько положительно заряженных атомов азота, один или несколько атомов фосфора и/или один или несколько атомов серы.
Предпочтительные катионные группы содержат постоянный, положительно заряженный атом азота из групп, таких, например, как алкиламмоний, таких как триметиламмоний или триэтиламмоний, или диметиламмоний, или бензилдиметиламмоний, или гуанидиний, или положительно заряженный атом азота из положительно заряженных гетероциклов, таких как имидазолиний, пиперидиний и пирролидиний. Гуанидиний является особенно предпочтительным.
Другие предпочтительные катионные группы представляют собой моно- и дизамещенные амины, такие как моноалкиламины, диалкиламины, гетероциклические амины и ароматические амины, которые имеют частичный положительный заряд в водных растворах с pH в пределах от 3 до 8, в частности, в пределах от 3 до 7.
Положительно заряженный ион азота также может быть предоставлен аминокислотным остатком, таким как лизин, аргинин, гистидин, орнитин, цитруллин, диаминомасляная кислота, диаминопропионовая кислота, диаминопентановая кислота, диаминогексановая кислота, диаминопимелиновая кислота, гомоаргинин, гомоцитруллин, п-аминофенилаланин и 3-аминотирозин. Аргинин является особенно предпочтительным.
Боковая цепь аминокислоты может давать как одну или несколько гидрофобных функциональных групп, так и одну или несколько катионных функциональных групп. Обычно, когда аминокислоты обеспечивают обе указанных функциональных группы, по меньшей мере, одна гидрофобная функциональная группа и, по меньшей мере, одна катионная функциональная группа обеспечиваются различными аминокислотами лиганда. Кроме аминокислот, лиганд может содержать другие остатки лиганда, как описано здесь ниже более подробно.
Термин "аминокислота" в рамках настоящего изобретения используется в самом широком смысле и, как подразумевается, включает в себя существующие в природе L-аминокислоты или их остатки. Здесь используются обычно используемые одно- и трехбуквенные сокращения существующих в природе аминокислот (Lehninger, Biochemistry, 2d ed., pp.71-92, (Worth Publishers: New York, 1975). Термин также включает в себя D-аминокислоты (и их остатки), а также химически-модифицированные аминокислоты, такие как аналоги аминокислот, включая существующие в природе аминокислоты, которые обычно не включаются в белки, такие как норлейцин, а также химически-синтезированные соединения, имеющие свойства, известные в данной области как характерные для аминокислот.
Например, аналоги или миметики фенилаланина или пролина, которые делают возможным такое же конформационное ограничение лиганда, как природный Phe или Pro, включаются в определение аминокислоты. Такие аналоги и миметики упоминаются здесь как "функциональные эквиваленты" аминокислоты. Другие примеры аминокислот приведены Roberts and Vellaccio, the Peptides: Analysis, Synthesis, Biology, Eds. Gross and Meiehofer, Vol.5, p.341 (Academic Press, Inc.: N.Y. 1983).
Аминокислоты, как правило, связываются посредством амидных связей, но и другие связи, такие, например, как любая одна или несколько связей, выбранных из -NHN(R)CO-; -NHC(R)CO-; -NHC(RR')CO; -NHC(=CHR)CO-; -NHC6H4CO-; -NHCH2CHRCO-; -NHCHRCH2CO-; -COCH2-; -COS-; -CONR-; -COO-; -CSNH-; -CH2NH-; -CH2CH2-; -CH2S-; -CH2SO-; -CH2SO2; -CH(CH3)S-; -CH=CH-; -NHCO-; -NHCONH-; -CONHO-; -C(=CH2)CH2-; -PO2-NH-; -PO2-CH2-; -PO2-CH2N+-; -SO2NH-, также могут связывать аминокислотные остатки лигандов в соответствии с настоящим изобретением. R (и R') обозначает функциональную группу, такую, например, как гидрофобная функциональная группа или катионная группа, или другой структурный остаток, соединяющий указанные выше группы. Наиболее предпочтительная в настоящее время связь между "аминокислотами" представляет собой амидную связь.
Примеры аминокислот, которые в целом могут быть включены в состав лигандов в соответствии с настоящим изобретением, перечислены здесь ниже:
глицил; остатки аминополикарбоновых кислот, например, аспарагиновой кислоты, п-гидроксиаспарагиновой кислоты, глутаминовой кислоты, β-гидроксиглутаминовой кислоты, β-метиласпарагиновой кислоты, β-метилглутаминовой кислоты, β,β-диметиласпарагиновой кислоты, γ-гидроксиглутаминовой кислоты, β,γ-дигидроксиглутаминовой кислоты, β-фенилглутаминовой кислоты, γ-метиленглутаминовой кислоты, 3-аминоадипиновой кислоты, 2-аминопимелиновой кислоты, 2-аминосубериновой кислоты и 2-аминосебациновой кислоты; амиды аминокислот, такие как глутаминил и аспарагинил; полиамино- или многоосновные монокарбоновые кислоты, такие как аргинин, лизин, β-аминоаланин, γ-аминобутирин, орнитин, цитруллин, гомоаргинин, гомоцитруллин, остатки 5-гидрокси-2,6-диаминогексановой кислоты (обычно, гидроксилизин, включая аллогидроксилизин) и диаминомасляной кислоты; другие основные аминокислотные остатки, такие как гистидинил; остатки диаминодикарбоновых кислот, таких как α,α'-диаминоянтарная кислота, α,α'-диаминоглутаровая кислота, α,α'-диаминоадипиновая кислота, α,α'-диаминопимелиновая кислота, α,α'-диамино-β-гидроксипимелиновая кислота, α,α'-диаминосубериновая кислота, α,α'-диаминоазелаиновая кислота и остатки α,α'-диаминосебациновой кислоты; иминокислоты, такие как пролин, 4- или 3-гидрокси-2-пирролидин-карбоновая кислота (обычно, гидроксипролин, включая аллогидроксипролин), γ-метилпролин, пипеколиновая кислота, 5-гидроксипипеколиновая кислота, -N([CH2]nCOORPR)2, где n равно 1, 2, 3, 4, 5 или 6 и RPR представляет собой -H или защитную группу, и остатки азетидин-2-карбоновой кислоты; остатки моно- или диалкил (как правило, C1-C25 разветвленный или нормальный) аминокислоты, такие как аланин, валин, лейцин, аллилглицин, бутирин, норвалин, норлейцин, гептилин, α-метилсерин, α-амино-α-метил-γ-гидроксивалериановой кислоты, α-амино-α-метил-6-гидроксивалериановой кислоты, α-амино-α-метил-ε-гидроксикапроновой кислоты, изовалин, остатки α-метилглутаминовой кислоты, α-аминоизомасляной кислоты, α-аминодиэтилуксусной кислоты, α-аминодиизопропилуксусной кислоты, α-аминоди-н-пропилуксусной кислоты, α-аминодиизобутилуксусной кислоты, α-аминоди-н-бутилуксусной кислоты, α-аминоэтилизопропилуксусной кислоты, α-амино-н-пропилуксусной кислоты, α-аминодиизоамилуксусной кислоты, α-метиласпарагиновой кислоты, α-метилглутаминовой кислоты, 1-аминоциклопропан-1-карбоновой кислот; изолейцин, аллоизолейцин, трет-лейцин, β-метилтриптофан и остатки α-амино-α-этил-β-фенилпропионовой кислоты; β-фенилсеринил; остатки алифатических α-амино-β-гидрокси кислот, таких как серин, β-гидроксилейцин, β-гидроксинорлейцин, β-гидроксинорвалин, и остатки α-амино-α-гидроксистеариновой кислоты; α-амино, α-, γ-, δ- или ε-гидрокси кислот, такие как гомосерин, γ-гидроксинорвалин, δ-гидроксинорвалин, и остатки ε-гидроксинорлейцина; санавинила и саналинила; γ-гидроксиорнитинила; 2-гексозаминных кислот, таких как D-глюкозаминная кислота или D-остатки галактозаминных кислот; α-амино-β-тиолы, такие как пенициллинамин, β-тиолнорвалин или остатки β-тиолбутирина; другие содержащие серу аминокислотные остатки, включая цистеин; гомоцистин; β-фенилметионин; метионин; S-аллил-(L)-цистеин сульфоксид; 2-тиолгистидин; цистатионин; и простые тиоловые эфиры цистеина или гомоцистеина; фенилаланин, триптофан и аминокислоты, замещенные на кольце, такие как фенил- или циклогексиламино кислоты, α-аминофенилуксусная кислота, α-аминоциклогексилуксусная кислота и α-амино-β-циклогексилпропионовая кислота; аналоги и производные фенилаланина, содержащие арил, низший алкил (C1-C6), гидрокси, гуанидино, простой оксиалкиловый эфир, нитро, серу или галоген-замещенный фенил (например, тирозин, метилтирозин и o-хлор-, п-хлор-, 3,4-дихлор, o-, м- или п-метил-, 2,4,6-триметил-, 2-этокси-5-нитро, 2-гидрокси-5-нитро и п-нитро-фенилаланин); фурил-, тиенил-, пиридил-, пиримидинил-, пурин или нафтилаланины; и аналоги и производные триптофана, включая кинуренин, 3-гидроксикинуренин, 2-гидрокситриптофан и остатки 4-карбокситриптофана; α-амино-замещенные аминокислотные остатки, включая саркозин (N-метилглицин), N-бензилглицин, N-метилаланин, N-бензилаланин, N-метилфенилаланин, N-бензилфенилаланин, N-метилвалин и N-бензилвалин; и α-гидрокси и замещенные α-гидрокси аминокислотные остатки, включая серин, треонин, аллотреонин, фосфосерин и остатки фосфотреонина. Также представляют интерес гидрофобные аминокислоты, такие как моно- или диалкил- или ариламинокислоты, циклоалкиламинокислоты, и тому подобное.
Предпочтительные лиганды
Отмечаются выбранные остатки лигандов, как перечисленные ниже:
PPC: 4-Фенилпиперидин-4-карбоновая кислота
Dap: Диаминопропионовая кислота
L-Orn: L-орнитин
DPPAA: 2,4-Ди-трет-пентилфеноксиуксусная кислота
DMBA: 3,5-Диметоксибензойная кислота
TMPPA: 3-(3,4,5-триметоксифенил)пропионовая кислота
DBHPA: 3-(3,5-Ди-трет-бутил-4-гидроксифенил)пропионовая кислота
1H2NA: 1-Гидрокси-2-нафтойная кислота
DPPA: 3,3-Дифенилпропионовая кислота
SAA: Салициловая кислота
DBBA: 3,5-Ди-трет-бутилбензойная кислота
DPPBA: 4-(2,4-Ди-трет-пентилфенокси)масляная кислота
TEBA: 3,4,5-Триэтоксибензойная кислота
PCAA: α-Фенилциклопентануксусная кислота
MDCA: 3,4-(Метилендиокси)коричная кислота
Gly: Глицин
L-Phe: L-Фенилаланин
L-Arg: L-Аргинин
L-His: L-Гистидин
L-Trp: L-Триптофан
L-Pro: L-Пролин
L-Asn: L-Аспарагин
L-Lys: L-Лизин
L-Asp: L-Аспарагиновая кислота
D-Phe: D-Фенилаланин
D-Arg: D-Аргинин
D-Tyr: D-Тирозин
D-Ser: D-Серин
D-Trp: D-Триптофан
D-Pro: D-Пролин
D-Leu: D-Лейцин
Ahx: 6-Аминогексановая кислота
Aib: α-Аминоизомасляная кислота
DBHBA: 3,5-Ди-трет-бутил-4-гидроксибензойная кислота
INA: Изонипекотиновая кислота
Nle: L-Норлейцин
PPC: 4-Фенилпиперидин 4-карбоновая кислота
SAA: Салициловая кислота
3HBA: 3-Гидроксибензойная кислота
4HBA: 4-Гидроксибензойная кислота
В главном классе предпочтительных аффинных лигандов, каждый лиганд содержит одну или несколько гидрофобных функциональных групп и одну или несколько катионных функциональных групп, где, по меньшей мере, одна гидрофобная функциональная группа отделена, по меньшей мере, от одной катионной функциональной группы расстоянием между связями от 5 Å до 20 Å, и где указанный лиганд имеет молекулярную массу от 120 Да до 1500 Да.
В одном из предпочтительных вариантов осуществления, аффинный лиганд содержит или состоит из ковалентно связанных остатков X1-X2-X3, где необязательно X1, X2 и/или X3, в частности, X1и/или X3, ассоциируются с линкерным остатком, L.
Предпочтительно X1, X2, X3 и необязательный линкерный остаток предпочтительно представляют собой очень стабильные молекулы, которые могут выдержать многократное воздействие жестких химических условий (например, кислота в концентрации 1 M или основание в концентрации 1 M) и биологических условий (например, высокая активность протеазы). Подобным же образом, соответствующие связи между каждым Xl, X2, X3 и необязательным линкерным остатком являются очень стабильными и могут выдержать воздействие жестких химических и биологических условий.
Остаток X1 предпочтительно выбирается из группы, состоящей из Arg, Phe, PPC, DBHBA, SAA, DAP, DAB, (DBHBA)2-DAP, (MDCA)2-DAP, DPBBA, DBBA, PCAA, DPPAA, Trp, TMPPA, DBHPA, где каждый член необязательно дополнительно выбирается из выделенного и оптически активного остатка и рацемической смеси, содержащей оба оптически активных изомера этого же остатка. В одном из предпочтительных вариантов, X1 выбирается из группы, состоящей из L-Arg, D-Lys, D-Phe, D-Pro, INA, PPC, DBHBA, 3HBA, 4HBA и SAA.
Остаток X2 предпочтительно выбирается из группы, состоящей из Arg, Asn, Leu, Lys, Phe, Pro, PPC, DAP, DAB, His, Trp, Tyr, Ser, где каждый член необязательно дополнительно выбирается из выделенного и оптически активного остатка и рацемической смеси, содержащей оба оптически активных изомера этого же остатка. В одном из предпочтительных вариантов, X2 выбирается из группы, состоящей из L-Arg, L-Asn, D-Leu, D-Lys, D-Phe, D-Pro, L-Pro, AIB, AHX, INA, Nle и PPC.
Остаток X3 предпочтительно выбирается из группы, состоящей из Arg, Asn, Pro, PPC, Asp, Orn, (1H2NA)Dap, где каждый член необязательно дополнительно выбирается из выделенного и оптически активного остатка и рацемической смеси, содержащей оба оптически активных изомера этого же остатка. В частности, X3 предпочтительно выбирается из группы, состоящей из L-Arg, L-Asn, D-Lys, D-Phe, D-Pro, L-Pro и PPC.
Перспективный в настоящее время набор лигандов, имеющих сродство к антителу, такому как моноклональное антитело, представляет собой лиганды, содержащие или состоящие из одного или нескольких наборов (соответствующих X1-X2-X3):
D-Phe-(L)Arg-(L)Arg
L-Arg-D-Phe-(L)Arg
PPC-D-Pro-(L)Arg
PPC-D-Leu-PPC
INA-D-Phe-PPC
PPC-Aib-PPC
D-Phe-(L)Arg-(L)Arg
L-Arg-D-Phe-(L)Arg
L-Arg-(L)Arg-D-Phe
PPC-(L)Arg-D-Pro
D-Pro-PPC-(L)Arg
L-Arg-D-Pro-PPC
L-Arg-D-Lys-(L)Arg
L-Arg-(L)Arg-D-Lys
D-Lys-INA-(L)Arg
INA-(L)Arg-D-Lys
PPC-Ahx-PPC
PPC-Nle-PPC
SAA-(L)Arg-(L)Pro
SAA-(L)Pro-(L)Arg
DBHBA-(L)Arg-(L)Asn
DBHBA-(L)Asn-(L)Arg
3HBA-(L)Arg-(L)Pro
3HBA-(L)Pro-(L)Arg
4HBA-(L)Arg-(L)Pro
4HBA-(L)Pro-(L)Arg
В другом перспективном в настоящее время варианте осуществления, лиганд содержит или состоит из менее чем 5, например, менее чем 4 остатков, например, 3 остатков, выбранных из группы, состоящей из D-Leu; D-Lys; D-Phe; D-Pro; L-Arg; L-Asn; L-Pro; Ahx; Aib; DBHBA; INA; Nle; PPC; SAA; 3HBA и 4HBA. Таким образом, лиганд состоит из 3 остатков, X1-X2-X3, индивидуально выбранных из группы, состоящей из D-Leu; D-Lys; D-Phe; D-Pro; L-Arg; L-Asn; L-Pro; Ahx; Aib; DBHBA; INA; Nle; PPC; SAA; 3HBA и 4HBA.
Когда лиганд содержит или состоит из 3 остатков, X1-X2-X3,
X1 предпочтительно выбирается из группы, состоящей из D-Lys; D-Phe; D-Pro; L-Arg; DBHBA; INA; PPC; SAA; 3HBA и 4HBA,
X2 предпочтительно выбирается из группы, состоящей из D-Leu; D-Lys; D-Phe; D-Pro; L-Arg; L-Asn; L-Pro; Ahx; AIB; INA; Nle; PPC; и
X3 предпочтительно выбирается из группы, состоящей из D-Lys; D-Phe; D-Pro; L-Arg; L-Asn; L-Pro; PPC.
В дополнительном варианте осуществления, лиганд содержит или состоит из 3 ковалентно связанных остатков, X1-X2-X3,
где указанные ковалентно связанные остатки являются дополнительно ковалентно связанными с линкерным остатком L объекта L-PM, где PM представляет собой материал твердого носителя, предпочтительно, полимерную матрицу, необязательно, в поперечно сшитой форме и/или в форме шариков,
где X1представляет собой природную или неприродную аминокислоту в D- и/или L-конфигурации, или остаток карбоновой кислоты, содержащий необязательно замещенную ароматическую группу,
где X2 представляет собой природную или неприродную аминокислоту либо в D- и/или L-конфигурации, либо остаток карбоновой кислоты, содержащий необязательно замещенную ароматическую группу, при условии, что X2 не представляет собой остаток треонина, и
где X3 представляет собой природную или неприродную аминокислоту либо в D- и/или L-конфигурации, либо остаток карбоновой кислоты, содержащей необязательно замещенную ароматическую группу,
где, по меньшей мере, один из X1, X2 и X3 содержит катионную функциональную группу и где, по меньшей мере, один из X1, X2 и X3 содержит гидрофобную функциональную группу,
где X1 выбирается из L-Arg, D-Lys, D-Phe, D-Pro, INA, PPC, DBHBA, 3HBA, 4HBA и SAA;
где X2 выбирается из L-Arg, L-Asn, D-Leu, D-Lys, D-Phe, D-Pro, L-Pro, AIB, AHX, INA, NLE и PPC; и
где X3 выбирается из L-Arg, L-Asn, D-Lys, D-Phe, D-Pro, L-Pro и PPC.
Еще в одном перспективном варианте осуществления, лиганд содержит или состоит из 3 ковалентно связанных остатков, X1-X2-X3,
где указанные ковалентно связанные остатки ковалентно связанны с линкером L объекта L-PM,
где X1представляет собой природную или неприродную аминокислоту в D- и/или L-конфигурации, или остаток карбоновой кислоты, содержащей необязательно замещенную ароматическую группу,
где X2 представляет собой природную или неприродную аминокислоту либо в D- и/или L-конфигурации, либо остаток карбоновой кислоты, содержащей необязательно замещенную ароматическую группу, при условии, что X2 не представляет собой остаток треонина, и
где X3 представляет собой природную или неприродную аминокислоту либо в D- и/или L-конфигурации, либо остаток карбоновой кислоты, содержащей необязательно замещенную ароматическую группу,
где, по меньшей мере, один из X1, X2 и X3 содержит катионную функциональную группу, и
где, по меньшей мере, один из X1, X2 и X3 содержит гидрофобную функциональную группу,
где X1 выбирается из L-Arg, D-Lys, D-Phe, D-Pro, INA, PPC, DBHBA, 3HBA, 4HBA и SAA;
где X2 выбирается из L-Arg, L-Asn, D-Leu, D-Lys, D-Phe, D-Pro, L-Pro, AIB, AHX, INA, NLE и PPC; и
где X3 выбирается из L-Arg, L-Asn, D-Lys, D-Phe, D-Pro, L-Pro и PPC.
В одном из вариантов осуществления, линкерный остаток L, присоединенный к полимерной матрице, может отщепляться посредством кислот, оснований, температуры, света или посредством контакта с химическим реагентом. Как и раньше, линкер, присоединенный к полимерной матрице, может представлять собой линкер, выбранный из (3-формилиндол-1-ил)уксусной кислоты, 2,4-диметокси-4'-гидроксибензофенона, HMPA, HMPB, HMPPA, кислоты Ринка, амида Ринка, линкера Кнорра, линкера PAL, линкера DCHD, линкера Ванга и тритильного линкера. Лиганды, связанные с полимерной матрицей через отщепляемый линкер, могут использоваться для аналитических целей, например, для диагностических применений.
В одном из вариантов осуществления настоящего изобретения, X1, X2, и X3 выбираются из группы природных аминокислот и их стереоизомеров.
Обнаружено, что включение, по меньшей мере, одной аминокислоты, содержащей гуанидино или амино группу в боковой цепи, в частности, гуанидино группы, как правило, обеспечивают преимущественные свойства относительно емкости связывания. Следовательно, особенно важными аминокислотами для включения в лиганды являются аргинин, гомоаргинин, лизин, гомолизин и орнитин, в особенности, аргинин и гомоаргинин.
Особенно перспективный подкласс лигандов представляет собой такой, где лиганды содержат два аргининовых остатка. Следовательно, особенно благоприятными лигандами в этом варианте осуществления являются

H2N-(D)Phe-(L)Arg-(L)Arg-Gly-OH
и

H2N-(L)Arg-(D)Phe-(L)Arg-Gly-OH.
В дополнительном варианте осуществления, X1, X2 и X3 выбираются из группы природных и неприродных аминокислот.
Следовательно, для еще более перспективного подкласса лигандов
X1выбирается из группы, состоящей из Arg, Phe, PPC, DBHBA, SAA, DAP, DAB, (DBHBA)2-DAP, (MDCA)2-DAP, DPBBA, DBBA, PCAA, DPPAA, Trp, TMPPA и DBHPA,
X2 выбирается из группы, состоящей из Arg, Asn, Leu, Lys, Phe, Pro, PPC, DAP, DAB, His, Trp, Tyr и Ser,
X3 выбирается из группы, состоящей из Arg, Asn, Pro, PPC, Asp, Orn и (1H2NA)Dap.
Особенно благоприятными лигандами в этом подклассе являются:

HN-PPC-(D)Pro-(L)Arg-Gly-OH
и
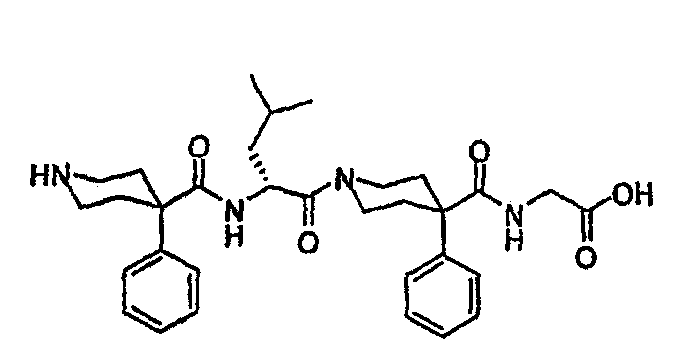
HN-PPC-(D)Leu-PPC-Gly-OH
Еще в одном подклассе лигандов каждый лиганд содержит одну или несколько замещенных или незамещенных фенильных или нафтильных групп и один или несколько первичных аминов или гуанидинов.
Особенно благоприятными лигандами в этом варианте осуществления являются:

DBBA-(L)His-(L)Arg-Gly-OH,
DBBA-His-Arg-Gly-OH,
DBBA-His-Arg-Arg-Gly-OH

DPPBA-(L)Phe-(L)Arg-Gly-OH,

PCAA-(L)Phe-(L)Arg-Gly-OH,

DPPBA-(L)Lys-(L)Arg-Gly-OH

SAA-(L)Arg-(L)Pro-Gly-OH

SAA-(L)Pro-(L)Arg-Gly-OH

DBHBA-(L)Arg-(L)Asn-Gly-OH

DBHBA-(L)Asn-(L)Arg-Gly-OH

DPPBA-(L)Trp-(L)Arg-Gly-OH

(MDCA)2-DAP-(L)Arg-(L)Orn-Gly-OH

(MDCA)2-DAP-(L)Arg-(L)Asp-Gly-OH

PPAA-(L)Phe-(L)Arg-Gly-OH
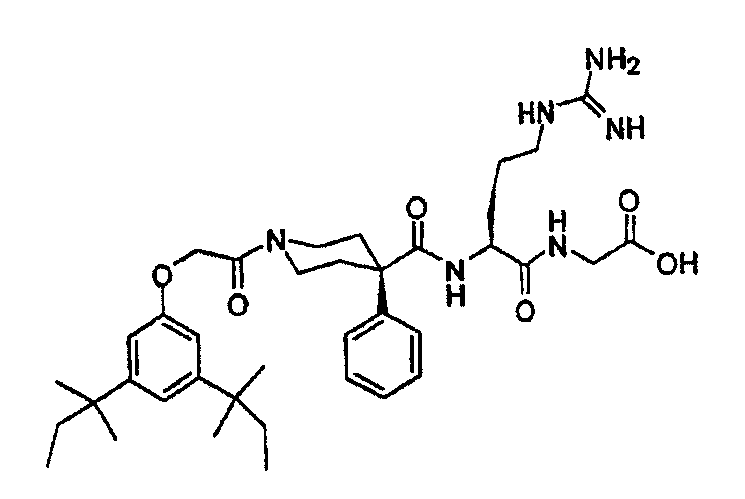
DPPAA-PPC-(L)Arg-Gly-OH

DBHBA-(D)Phe-(D)Arg-Gly-OH

DPPAA-(D)tyr-(D)Arg-Gly-OH
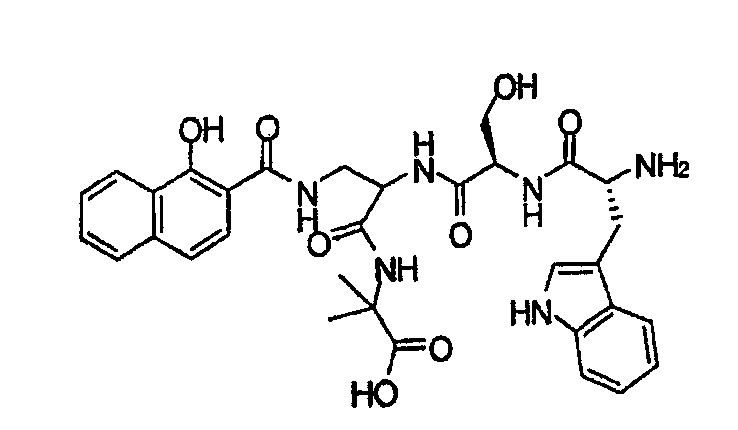
H2N-(D)Trp-(D)Ser-(1H2NA)DAP-Aib-OH,

H2N-(L)His-(D)Ser-(1H2NA)DAP-Aib-OH,

(DPPA)2-DAP-(L)Arg-(L)Orn-Gly-OH

(DBHBA)2-DAP-(L)Arg-(L)Arg-Gly-OH,
DBHBA-DAP-Arg-Gly-OH,
DBHBA-DAP-Arg-Arg-Gly-OH,
(DBHBA)2-DAP-Arg-Gly-OH,
(DBHBA)3-DAP-Arg-Arg-Gly-OH,
(DBHBA)3-DAP-Arg-Arg-Gly-OH,

TMPPA-(L)Trp-(L)Arg-Gly-OH
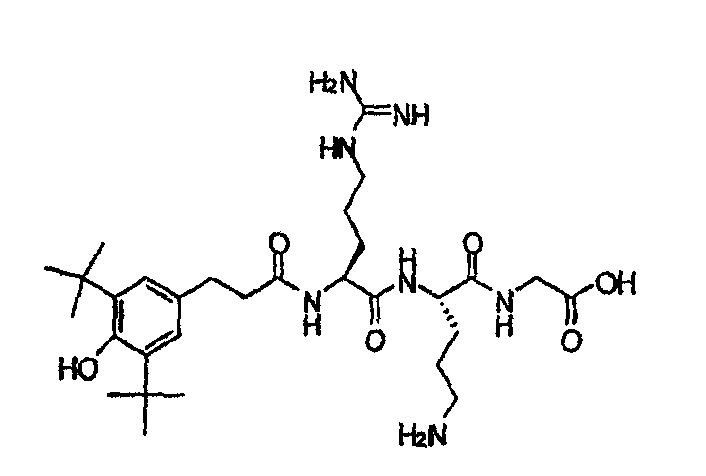
DBHPA-(L)Arg-(L)Orn-Gly-OH
Альтернативные аффинные лиганды
Другой перспективный в настоящее время класс аффинных лигандов представляет собой такой, где лиганды содержат одну или несколько гидрофобных групп и одну или несколько гетероароматических групп.
Следовательно, в другом главном классе предпочтительных аффинных лигандов, каждый лиганд содержит одну или несколько гидрофобных функциональных групп и одну или несколько гетероароматических функциональных групп, где, по меньшей мере, одна гидрофобная функциональная группа отделена, по меньшей мере, от одной гетероароматической функциональной группы расстоянием между связями от 5 Å до 20Å, и где указанный лиганд имеет молекулярную массу от 120 Да до 5000 Да,
Предпочтительно, аффинная смола, имеющая такой аффинный лиганд, иммобилизованный на ней, имеет емкость связывания, большую, чем 5 мг моноклонального антитела на мл аффинной смолы.
Термин "гетероароматическая функциональная группа (группы)" предназначается для охвата гетероароматических объектов, определенных выше как "гидрофобные функциональные группы, содержащие ароматические остатки" и "катионные функциональные группы".
Спецификации и предпочтения относительно длин кратчайших контурных связей, пространственных расстояний, молекулярной массы, и тому подобное, дополнительно, приведенные выше для главного класса аффиных лигандов, также применимы к этому классу аффинных лигандов, хотя необходимо понять, что "расстояния", упоминаемые здесь, относятся к расстояниям между гидрофобной функциональной группой (группами) и гетероароматической функциональной группой (группами).
Пример лиганда из этого класса представляет собой

(TEBA)2-DAP-(L)Trp-(L)Trp-Gly-OH.
Материал твердого носителя
Лиганды в соответствии с настоящим изобретением ковалентно иммобилизуются на материале твердого носителя, таком как полимерная смола, поверхность полимерного материала, стеклянная поверхность, и тому подобное, и могут использоваться для очистки и/или выделения антител, таких как моноклональные антитела.
Материал твердого носителя, как правило, содержит полимерную матрицу, например, поперечно-сшитую полимерную матрицу. Чаще всего, полимерная матрица представляет собой шарики, альтернативно, полимерная матрица приготавливается в виде монолитного узла. Предпочтительно, по меньшей мере, поверхность полимерной матрицы, представляющей собой шарики, содержит гидрофильные остатки.
Следовательно, материал твердого носителя, как правило, находится в форме смолы, монолита, фильтра, пластины, такой как микроматрица, волокна, сенсора, такого как консольный датчик, сенсора поверхностного плазмонного резонанса, или кварцевых кристаллических микровесов.
Смола представляет собой пористый твердый материал, используемый для разделения соединений в текучей среде. Смолы могут представлять собой поперечно сшитые полимеры, керамические материалы, такие как неорганические оксиды, например, оксид алюминия, оксид кремния. Смолы поставляются в виде частиц, таких как сферические частицы или нерегулярные частицы.
Лиганды характеризуются емкостью связывания, которая предпочтительно больше, чем 5 мг антитела на мл влажной смолы, например, больше, чем 6 мг антитела на мл смолы, например, больше, чем 7 мг антитела на мл смолы, например, больше, чем 8 мг антитела на мл смолы, например, больше, чем 9 мг антитела на мл смолы, например, больше, чем 10 мг антитела на мл смолы, например, больше, чем 12 мг антитела на мл смолы, например, больше, чем 14 мг антитела на мл смолы, например, больше, чем 16 мг антитела на мл смолы, например, больше, чем 18 мг антитела на мл смолы, например, больше, чем 20 мг антитела на мл смолы, например, больше, чем 22 мг антитела на мл смолы, например, больше, чем 24 мг антитела на мл смолы, например, больше, чем 26 мг антитела на мл смолы, например, больше, чем 28 мг антитела на мл смолы, например, больше, чем 30 мг антитела на мл смолы, например, больше, чем 35 мг антитела на мл смолы, например, больше, чем 40 мг антитела на мл смолы, например, больше, чем 45 мг антитела на мл смолы, например, больше, чем 50 мг антитела на мл смолы, например, например, самое большее, 500 мг антитела на мл смолы.
Выражение "емкость связывания" означает способность смолы к связыванию целевого соединения, такого, например, как антитело. Емкость связывания приводится в мг целевого соединения (например, антитела) на мл смолы (или другой формы материала в виде шариков) и может измеряться посредством прохождения раствора чистого целевого соединения при известной концентрации через смолу и измерения объема прохождения растворителя до появления целевого соединения. Затем емкость связывания вычисляется как объем прохождения, умноженный на концентрацию и деленный на объем слоя. Как здесь используется, емкость связывания обозначает способность смолы к связыванию антитела. Емкость связывания приводится в мг антитела на миллилитр смолы и может измеряться посредством прохождения водного буферного раствора (50 мМ Na-Фосфат, pH=7,0) чистого антитела с известной концентрацией и регистрации появления УФ поглощения (280 нм) раствора, покидающего смолу. Объем прохождения представляет собой объем раствора, который выходит из смолы в точке, где УФ поглощение достигает 5% от его конечного значения. Затем емкость связывания вычисляется как объем прохождения, умноженный на концентрацию антитела во вводимом растворе и деленный на объем слоя.
Когда лиганд присоединяется к поверхности по существу непористого материала, такого например, как и поверхность матрицы или поверхность сенсора, емкость связывания лиганда измеряется как масса белка, связанная на единицу площади поверхности. Лиганды отличаются емкостью связывания, которая предпочтительно больше, чем 1 нг антитела на см2, например, больше, чем 5 нг антитела на см2, например, больше, чем 10 нг антитела на см2, например, больше, чем 50 нг антитела на см2, например, больше, чем 100 нг антитела на см2.
Соответствующие примеры смол описываются здесь ниже более подробно.
Полимерные матрицы
Лиганд может присоединяться ковалентно к твердой подложке, такой как пористая, неорганическая матрица или полимерная матрица, необязательно, в поперечно сшитой форме и/или в форме шариков, или в монолитном пористом изделии. Предпочтительно, поры полимерной матрицы являются достаточно широкими для диффузии целевого белка через указанные поры и взаимодействия с лигандом на внутренней поверхности пор. Для моноклонального антитела с молярной массой приблизительно 150 кДа, предпочтительным является средний диаметр пор 50-200 нм, например, приблизительно 100 нм. Является доступным ряд коммерчески доступных пригодных для использования полимерных смол, например, Sepharose™, Fractogel™, CIMGEL™, Toyopearl.
Находящаяся в форме шариков и необязательно поперечно-сшитая полимерная матрица в одном из вариантов осуществления содержит множество гидрофильных остатков. Гидрофильные остатки могут представлять собой полимерные цепи, которые, когда поперечно сшиваются, образуют поперечно сшитую полимерную матрицу. Примеры включают в себя, например, полиэтиленгликолевые остатки, полиаминовые остатки, поливиниламиновые остатки, и полиольные остатки.
В некоторых вариантах осуществления, ядро и/или поверхность полимерной матрицы в форме шариков содержит полимерный материал, выбранный из группы, состоящей из поливинилов, полиакрилатов, полиакриламидов, полистиролов, сложных полиэфиров и полиамидов.
Полимерная матрица в форме шариков также может выбираться из группы, состоящей из PS, POEPS, POEPOP, SPOCC, PEGA, CLEAR, Expansin, Polyamide, Jandagel, PS-BDODMA, PS-HDODA, PS-TTEGDA, PS-TEGDA, GDMA-PMMA, PS-TRPGDA, ArgoGel, смол Argopore, ULTRAMINE, поперечно-сшитого LUPAMINE, PEGA высокой емкости, окиси кремния, Fractogel, Sephadex, Sepharose, стеклянных шариков, поперечно-сшитых полиакрилатов и производных указанных выше матриц; в частности, полимерная матрица выбирается из группы, состоящей из SPOCC, PEGA, HYDRA, POEPOP, PEG-полиакрилатных сополимеров, полиэфирно-полиаминовых сополимеров, и поперечно-сшитых полиэтилендиаминов.
Кроме указанных выше примеров, любой материал, способный к образованию полимерной матрицы, может, в принципе, использоваться при получении шариков по настоящему изобретению. Предпочтительно, материал ядра шарика является полимерным. В некоторых вариантах осуществления, ядро содержит или состоит из гидрофильного полимерного материала. В других вариантах осуществления, ядро содержит или состоит из гидрофобного полимерного материала. В некоторых вариантах осуществления, поверхность шариков содержит или состоит из такого же материала, как и ядро.
Смолы, пригодные для широкомасштабных применений, могут представлять собой одну из указанных выше или других коммерческих смол, таких как Sephadex™, Sepharose™, Fractogel™, CIMGEL™, Toyopearl, поперечно-сшитая агароза, и макропористый полистирол или полиакрилат. Матрица также может иметь в основном неорганическую природу, такую как макропористое стекло или минеральные глины, или сочетания смол и неорганики, таких как Ceramic HyperD™.
Полимерные шарики в соответствии с настоящим изобретением могут быть получены из разнообразных полимеризуемых мономеров, включая стиролы, акрилаты и ненасыщенные хлориды, сложные эфиры, ацетаты, амиды и спирты, включая, но, не ограничиваясь этим, полистирол (включая латексы полистирола высокой плотности, такие как бромированный полистирол), полиметилметакрилат и другие полиакриловые кислоты, полиакрилонитрил, полиакриламид, полиакролеин, полидиметилсилоксан, полибутадиен, полиизопрен, полиуретан, поливинилацетат, поливинилхлорид, поливинилпиридин, поливинилбензилхлорид, поливинилтолуол, поливинилиденхлорид и полидивинилбензол. В других вариантах осуществления, шарики получают из мономеров стирола или макромономеров на основе PEG. В предпочтительных вариантах осуществления, полимер выбирается из группы, состоящей из простых полиэфиров, поливинилов, полиакрилатов, полиметакрилатов, полиациламидов, полиуретанов, полиакриламидов, полистиролов, поликарбонатов, сложных полиэфиров, полиамидов и их сочетаний. В высшей степени предпочтительные поверхностные и сердцевинные остатки включают в себя остатки поперечно-сшитого PEG, полиаминовые остатки, поливиниламиновые остатки и полиольные остатки.
Предпочтительный гидрофобный полимер, который должен использоваться для получения шариков композиции по настоящему изобретению, представляет собой PS-DVB (полистирол, сшитый с помощью дивинилбензола). PS-DVB широко используется для твердофазного пептидного синтеза (SPPS), и совсем недавно продемонстрирована его полезность для получения конкретных органических молекул на полимерной подложке (Adams et al. (1998) J.Org.Chem. 63: 3706-3716). Когда они правильно приготовлены (Grøtli et al. (2000) J.Combi.Chem.2: 108-119), подложки из PS-DVB демонстрируют превосходные свойства для химического синтеза, такие как высокая нагрузка, разумное набухание в органических растворителях и физическая стабильность.
В одном из вариантов осуществления настоящего изобретения, лиганд ассоциируется с поверхностью сенсора или матричной пластины и используется для детектирования и/или количественного определения антител в биологическом образце.
Когда здесь он используется, термин "биологический образец" включает в себя природные образцы или образцы, полученные из промышленных процессов, например, рекомбинантных процессов, и включает в себя "физиологическую жидкость", то есть любое жидкое вещество, извлекаемое, экскретируемое или секретируемое из организма или ткани организма.
Физиологическая жидкость не должна обязательно содержать клетки. Физиологические жидкости, важные для настоящего изобретения, включают в себя, но, не ограничиваясь этим, целая кровь, сыворотку, мочу, плазму, спинномозговую жидкость, слезы, молоко, синовиальную жидкость и амниотическую жидкость.
В дополнительном варианте осуществления, множество лигандов присоединено к поверхности матричной пластины, и они располагаются в виде множества пятен, при этом каждое пятно представляет собой один лиганд. Такая функционализируемая матрица может использоваться для детектирования присутствия антител в растворе. Такая матрица может использоваться для диагностических применений с целью детектирования присутствия определенных антител в биологическом образце.
В дополнительном варианте осуществления, множество лигандов присоединено к поверхности связывания консольного сенсора для детектирования и необязательного количественного определения антител. Множество аффинных лигандов может быть присоединено к множеству консолей, при этом каждая консоль представляет один лиганд. Такая функционализованная матрица может использоваться для детектирования присутствия различных антител в растворе. Такой мультисенсор может использоваться для диагностических применений с целью детектирования присутствия определенного антитела в биологическом образце.
Линкеры
Указанный выше лиганд ковалентно иммобилизуется на материале твердого носителя, предположительно, через линкер. В предпочтительных вариантах осуществления, лиганд ковалентно присоединяется к линкеру, который ковалентно присоединяется к полимерной матрице. Общие методики для связывания аффинных лигандов с материалами твердых носителей можно найти в Hermanson, Krishna Mallia and Smith, Immobilized Affinity Ligand Techniques", Academic Press, 1992.
Линкеры используются для связывания лиганда с твердой подложкой, такой например, как полимерная матрица или неорганическая подложка. Предпочтительно, линкер формирует прочную и долговременную связь между лигандом и твердой подложкой. Это особенно важно, когда материал твердого носителя по настоящему изобретению должен использоваться для многократной очистки моноклональных антител или их фрагментов.
Однако в одном из вариантов осуществления настоящего изобретения, линкеры могут селективно отщепляться. Это может быть полезным, когда твердая подложка должна использоваться для аналитических целей.
Аминокислоты и полипептиды представляют собой примеры типичных линкеров. Другие возможные линкеры включают в себя углеводы и нуклеиновые кислоты.
В одном из вариантов осуществления, линкерный остаток L, присоединенный к полимерной матрице, может отщепляться посредством кислот, оснований, температуры, света или посредством контакта с химическим реагентом. В частности, линкер, присоединенный к полимерной матрице, может представлять собой (3-формилиндол-1-ил)уксусную кислоту, 2,4-диметокси-4'-гидроксибензофенон, HMPA, HMPB, HMPPA, кислоту Ринка, амид Ринка, линкер Кнорра, линкер PAL, линкер DCHD, линкер Ванга и тритильный линкер.
Лиганд может присоединяться к твердой подложке через линкер, имеющий длину, предпочтительно меньшую, чем 50 Å, такую как длина от 3 до 30 Å, например, длину от 3 до 20 Å, такую как длина от 3 до 10 Å.
Линкер может присоединяться к гидрофобной функциональной группе или к катионной функциональной группе, или к структурному остатку лиганда, соединяющему гидрофобную функциональную группу и катионную функциональную группу. В одном из вариантов осуществления, линкер присоединяется к катионной функциональной группе. Предпочтительно, однако, линкер присоединяется к аффинному лиганду через группу карбоновой кислоты или амино группу, в частности, через группу карбоновой кислоты.
Линкер также может содержать множество ковалентно связанных субъединиц, например, таких, что субъединицы выбираются из идентичных и неидентичных субъединиц линкеров. В одном из вариантов, линкер является гибким и содержит от 3 до, предпочтительно, менее чем 50 идентичных или неидентичных, ковалентно связанных субъединиц.
В предпочтительном варианте осуществления настоящего изобретения, линкер L выбирается из группы, состоящей из глицина, аланина, 3-аминопропионовой кислоты, 4-аминобутановой кислоты и HMBA.
Линкер также может выбираться из группы, состоящей из полидисперсного полиэтиленгликоля; монодисперсного полиэтиленгликоля, такого как триэтиленгликоль, тетраэтиленгликоль, пентаэтиленгликоль, гексаэтиленгликоль, гептаэтиленгликоль; аминокислот; дипептидов; трипептидов; тетрапептидов; пентапептидов; гексапептидов; гептапептидов; октапептидов; нонапептидов; декапептидов, полиаланинов; полиглицинов, полилизинов, полиаргинина, включая любое их сочетание.
Предпочтительные варианты осуществления
Один из предпочтительных вариантов осуществления относится к материалу твердого носителя, имеющего ковалентно иммобилизованный на нем аффинный лиганд, указанный лиганд содержит одну или несколько гидрофобных функциональных групп и одну или несколько катионных функциональных групп,
где, по меньшей мере, одна гидрофобная функциональная группа отделена, по меньшей мере, от одной катионной функциональной группы расстоянием между связями от 5 Å до 20 Å, где указанный лиганд имеет молекулярную массу от 120 Да до 1500 Да;
где лиганд содержит одну или несколько аминокислот, имеющих гуанидино группы в боковой цепи и одну или несколько аминокислот, имеющих замещенные фенильные или нафтильные группы в боковой цепи.
Имея в виду все указанное выше, обнаружено, что особенно интересные лиганды являются лигандами, выбранными из группы, состоящей из DBBA-(L)His-(L)Arg-Gly-OH и (DBHBA)2-DAP-(L)Arg-(L)Arg-Gly-OH.
Композиция
Настоящее изобретение также предусматривает материал твердого носителя, имеющий ковалентно иммобилизованное на нем множество различных аффинных лигандов. Такая композиция может использоваться для выделения различных антител из биологического образца.
Способ выделения антител
Другой аспект настоящего изобретения относится к способу выделения биологических молекул, таких как белки, например, антитела, в частности, моноклональные антитела, способ включает в себя стадии (i) предоставления материала твердого носителя, имеющего ковалентно иммобилизованный на нем аффинный лиганд, как определено здесь, (ii) предоставления образца, предположительно, содержащего антитело, имеющее сродство к указанному лиганду, (iii) приведения в контакт указанного лиганда с указанным образцом, предположительно, содержащим указанное антитело, (iv) селективного связывания указанного антитела, когда указанное антитело содержится в указанном образце, и (v) селективного выделения указанного антитела, когда указанное антитело содержится в указанном образце.
В одном из вариантов, способ включает в себя стадии создания лиганда, как определено здесь, присоединения указанного лиганда к твердой подложке, такой, например, как находящаяся в форме шариков и/или поперечно-сшитая полимерная матрица, создания образца, предположительно, содержащего антитело, имеющее сродство к указанному лиганду, приведения в контакт указанного лиганда с указанным образцом, предположительно, содержащим указанное антитело, селективного связывания указанного антитела, когда указанное антитело содержится в указанном образце, и селективного выделения указанного антитела, когда указанное антитело содержится в указанном образце.
Предпочтительно, емкость связывания лиганда больше, чем 5 мг антитела на мл смолы, или даже более, как дополнительно описано выше в разделе "Материал твердого носителя".
Необходимо понять, что манипуляции с материалом твердого носителя и процедура по существу следуют обычным методикам аффинной хроматографии.
ПРИМЕРЫ
Настоящее изобретение дополнительно иллюстрируется следующими далее неограничивающими примерами.
Примеры описывают, как большие библиотеки могут создаваться и исследоваться на их сродство к моноклональным антителам.
Материалы и методы
Все реагенты и растворители получают от коммерческих поставщиков и используют без дополнительной очистки. Все растворители, используемые здесь, имеют качество ВЭЖХ и хранятся над молекулярными ситами. Fmoc-защищенные аминокислоты и линкер HMBA получают от Bachem AG, Bubendorf, Switzerland. PPC и ACC покупают от Neosystem, Strasbourg, France. Sepharose™ покупают от Sterogene, и Fractogel™ покупают от Merck. Все лиганды синтезируют на смоле PEGA1900 (Versabeads™ A). 20-луночный многоколоночный пептидный синтезатор используют для синтеза комбинаторной библиотеки. Спектры1H ЯМР регистрируют в растворах CDCl3 с помощью спектрометра Varian Unity Inova 500 МГц. Химические сдвиги регистрируются в виде значений δ по отношению к тетраметилсилану. ESI-масс спектры регистрируют на масс-спектрометре Waters Global Ultima, и спектры MALDI-TOF регистрируют на масс-спектрометре Bruker Reflex III с использованием α-циано-4-гидроксициннамоновой кислоты в качестве матрицы. Аналитическое и препаративное разделение с помощью ВЭЖХ с обращенной фазой осуществляют на системе Waters HPLC, с использованием аналитических колонок Zorbax 300SB-C18 (4,5 × 50 мм), и Delta PAK C18 (25 × 300 мм), при скорости потока 1 см3мин-1 и 10 см3мин-1, соответственно. Детектирование осуществляют при 215 нм на детекторе с множеством длин волн (Waters 490E), для аналитических целей, и фотодиодный матричный детектор (Waters M991) используется для препаративного разделения. Используют систему растворителей, состоящую из A: 0,1% TFA в воде и B: 0,1% TFA в ацетонитриле/воде 90:10.
Мечение фрагмента Fc
Фрагмент Fc антитела очищают посредством диализа в бикарбонатном буфере (pH 8). Очищенный фрагмент Fc обрабатывают красителем Oregon Green (50 ×) в DMF и выдерживают в течение 1 часа при комнатной температуре. Реакцию останавливают посредством добавления гидроксиламина (1,5 M, pH 8,5). Меченый полипептид очищают посредством диализа в бикарбонатном буфере (pH 8).
Пример 1. Синтез лигандов
Твердофазный синтез следует схеме:

Все соединения синтезируются на амино-функциональной смоле на основе полиэтиленгликоля-акриламида, PEGA1900. Лиганды присоединяются к смоле, дериватизированной глицином, посредством основно-лабильного линкера п-гидроксиметилбензойной кислоты HMBA.
Добавляют структурный элемент (кислота/аминокислота; 3 экв), растворенный в DMF, и N-этилморфолин (4 экв), и TBTU (2,88 экв). Реакционную смесь выдерживают в течение 5 мин и добавляют к набухшей смоле в DMF в течение 2 часов. Смолу промывают DMF, EtOH-DMF и DCM.
Инкубирование синтезированных соединений в меченом фрагменте Fc
Шарики (10 мг) промывают водой (10 ×), бикарбонатным буфером (pH 8, 10 ×) и суспендируют в бикарбонатном буфере в течение 1 час. Затем к смоле добавляют меченый полипептид и выдерживают ее в течение ночи при комнатной температуре. Смолу промывают бикарбонатным буфером (pH 8) и водой.
Флуоресценцию на шариках регистрируют посредством использования флуоресцентного микроскопа и цифровой камеры. Ртутная лампа, снабженная фильтром испускания, обеспечивает возбуждение в видимом голубом диапазоне. Изображения шариков регистрируют в воде.
Приведенные ниже формулы иллюстрируют структурные элементы, которые используют для синтеза.
В таблице ниже перечислены лиганды и соответствующий видимый уровень флуоресценции, определяемый посредством простого взгляда на образцы и сравнения видимых интенсивностей цвета между образцами. По произвольной шкале от 0 до 3, где 0 указывает отсутствие флуоресценции и 3 показывает самый сильный уровень наблюдаемой флуоресценции.
Пример 2. Хроматографическая оценка лигандов (из Примера 1)
Приготовление хроматографической колонки
Новые смолы оценивают в режиме набивки. 1 мл каждой смолы набивают в хроматографическую колонку HR5 (GE Healthcare), применяя стандартные условия.
После набивки, колонка имеет высоту слоя 3,9 см и общий объем 0,76 мл.
Уравновешивание, загрузка, элюирование
Перед загрузкой матрицы моноклональным антителом, колонку уравновешивают 6 объемами колонки уравновешивающего буфера, содержащего 50 мМ Na-фосфата (pH 7,0; проводимость 9 мСим см-1). После уравновешивания раствор моноклонального антитела в уравновешивающем буфере (концентрация белка 1,14 мг/мл) загружают в колонку. После этого, колонку промывают 6 объемами колонки уравновешивающего буфера и элюируют 6 объемами колонки буфера для элюирования 1 (25 мМ ацетат натрия pH 5,5; проводимость 1,8 мСим см-1) и 6 объемами колонки буфера для элюирования 2 (25 мМ натрий ацетатный буфер pH 3,8; 0,5 мСим см-1). Колонку хранят в 20% этаноле. После этого матрицу регенерируют 40 мМ фосфорной кислоты и 20 мМ гидроксида натрия. Скорость потока для уравновешивания, загрузки и промывки равна 60 см/час, элюирование и регенерацию осуществляют при скорости потока 30 см/час.
Результаты для лиганда 55, связанного на Fractoqel
Результаты для лиганда 16, связанного на Fractoqel
Итоги и результаты
Связывание и элюирование mAb показаны для обоих лигандов, при использовании неоптимизированных условий работы. Для лиганда 55, только ограниченный материал находится при прохождении растворителя, в то время как ничего не детектируется при прохождении растворителя для лиганда 16.
Пример 3
Лиганды TMPPA-(L)Trp-(L)Arg-Gly-OH, DBHPA-(L)Arg-(L)Orn-Gly-OH, (DPPA)2-DAP-(L)Arg-(L)Orn-Gly-OH и (DBHBA)2-DAP-(L)Arg-(L)Arg-Gly-OH синтезируют на амино-активированной смоле Toyopearl (поставляется Tosoh). Емкость связывания каждой из полученных аффинных смол (B2, B3, D1 и D2 соответственно) по отношению к mAb оценивают посредством осуществления следующей последовательности стадий, два раза (цикл 1 и цикл 2):
1) прохождение водного раствора mAb (50 мМ Na-Фосфат, pH=7,0) через колонку, набитую смолой, в то же время, регистрация появления УФ поглощения пермеата и сбор образцов жидкости, покидающий колонку (Прохождение растворителя через аффинный сорбент),
2) прохождение водного буфера для элюирования (25 мМ ацетат pH=3,7) через колонку и сбор образцов жидкости, покидающей колонку (элюирование),
3) прохождение водного смывающего буфера (1 M уксусная кислота) через колонку и сбор образцов жидкости, покидающей колонку (регенерация/смывка).
Массу mAb, mi, i=1, 2, 3, затем определяют для каждого образца в каждом цикле.
"Емкость связывания" вычисляют как общую массу mAb, добавленного в колонку, m0, умноженную на объем буфера, добавленный в колонку в момент, где УФ поглощение достигает 5% от его конечного значения, V5%, деленную на общий объем используемого буфера, Vo, и деленную на объем влажной смолы, Vresin.

В таблице ниже приводятся результаты для B2, B3, D1 и D2 (Прохождение растворителя с аффинным сорбентом = m1/m0, элюирование = m2/m0и промывка = m3/m0)
Из таблицы ясно, что все исследуемые лиганды имеют емкости связывания, более высокие, чем 5 мг/мл.
Для определения селективности смол B2 и B3 по отношению к mAb эксперимент повторяют, но в этот раз на стадии 1 используют сырой супернатант от ферментирования. После эксперимента чистоту образцов определяют посредством SDS PAGE. Результаты показаны для B2, B3, D1 и D2 на фиг.1, 2, 3 и 4 соответственно.
Как видно из фиг.1-4, все четыре исследуемых лиганда показывают селективность по отношению к mAb, при этом B2 и D1 являются особенно селективными при данных условиях.
Реферат
Описан материал твердого носителя для выделения антител и их производных. На твердом носителе ковалентно иммобилизован аффинный лиганд, который содержит одну или несколько гидрофобных функциональных групп и одну или несколько катионных функциональных групп. По меньшей мере, одна гидрофобная функциональная группа отделена, по меньшей мере, от одной катионной функциональной группы расстоянием между связями от 5 Å до 20 Å. При этом лиганд имеет молекулярную массу не более 1000 Да, состоит из менее чем 5 остатков, обязательно содержащих структуру Х1-Х2-Х3. Указанная структура связана с твердым носителем линкером. Каждый из X1, Х2, Х3 выбирают из соответствующей группы соединений. Описаны также варианты твердого носителя со сходной структурой, но без линкера. Предложен также способ выделения антител или их производных на основе твердого носителя. Аффинная смола имеет емкость связывания более 5 мг моноклонального антитела на мл аффинной смолы и может найти применение в очистке антител и их производных. 4 н. и 9 з.п. ф-лы, 4 ил., 2 табл.
Формула
где, по меньшей мере, одна гидрофобная функциональная группа отделена, по меньшей мере, от одной катионной функциональной группы расстоянием между связями от 5 Å до 20 Å,
где указанный лиганд состоит из менее чем 5 остатков и имеет молекулярную массу не более 1000 Да; и
где лиганд содержит или состоит из ковалентно связанных остатков Х1-Х2-Х3, причем указанные ковалентно связанные остатки дополнительно ковалентно связаны с линкером L фрагмента L-PM, где L представляет собой линкер и РМ представляет собой материал твердого носителя,
где X1 выбран из L-Arg, D-Lys, D-Phe, D-Pro, INA, PPC, DBHBA, 3HBA, 4HBA и SAA;
где Х2 выбран из L-Arg, L-Asn, D-Leu, D-Lys, D-Phe, D-Pro, L-Pro, AIB, AHX, INA, NLE и РРС; и
где Х3 выбран из L-Arg, L-Asn, D-Lys, D-Phe, D-Pro, L-Pro и РРС,
где, по меньшей мере, один из X1, Х2 и Х3 содержит катионную функциональную группу, и
где, по меньшей мере, один из X1, X2 и Х3 содержит гидрофобную функциональную группу.
D-Phe-(L)Arg-(L)Arg,
L-Arg-D-Phe-(L)Arg,
PPC-D-Pro-(L)Arg,
PPC-D-Leu-PPC,
INA-D-Phe-PPC,
PPC-AIB-PPC,
L-Arg-(L)Arg-D-Phe,
PPC-(L)Arg-D-Pro,
D-Pro-PPC-(L)Arg,
L-Arg-D-Pro-PPC,
L-Arg-D-Lys-(L)Arg,
L-Arg-(L)Arg-D-Lys,
D-Lys-INA-(L)Arg,
INA-(L)Arg-D-Lys,
PPC-AHX-PPC,
PPC-Nle-PPC,
SAA-(L)Arg-(L)Pro,
SAA-(L)Pro-(L)Arg,
DBHBA-(L)Arg-(L)Asn,
DBHBA-(L)Asn-(L)Arg,
3HBA-(L)Arg-(L)Pro,
3HBA-(L)Pro-(L)Arg,
4HBA-(L)Arg-(L)Pro и
4HBA-(L)Pro-(L)Arg.
D-Phe-(L)Arg-(L)Arg-Gly,
L-Arg-D-Phe-(L)Arg-Gly,
PPC-D-Pro-(L)Arg-Gly,
PPC-D-Leu-PPC-Gly,
INA-D-Phe-PPC-Gly,
PPC-AIB-PPC-Gly,
L-Arg-(L)Arg-D-Phe-Gly,
PPC-(L)Arg-D-Pro-Gly,
D-Pro-PPC-(L)Arg-Gly,
L-Arg-D-Pro-PPC-Gly,
L-Arg-D-Lys-(L)Arg-Gly,
L-Arg-(L)Arg-D-Lys-Gly,
D-Lys-INA-(L)Arg-Gly,
INA-(L)Arg-D-Lys-Gly,
PPC-AHX-PPC-Gly,
PPC-Nle-PPC-Gly,
SAA-(L)Arg-(L)Pro-Gly,
SAA-(L)Pro-(L)Arg-Gly,
DBHBA-(L)Arg-(L)Asn-Gly,
DBHBA-(L)Asn-(L)Arg-Gly,
3HBA-(L)Arg-(L)Pro-Gly,
3HBA-(L)Pro-(L)Arg-Gly,
4HBA-(L)Arg-(L)Pro-Gly и
4HBA-(L)Pro-(L)Arg-Gly.
где, по меньшей мере, одна гидрофобная функциональная группа отделена, по меньшей мере, от одной катионной функциональной группы расстоянием между связями от 5 Å до 20 Å,
где указанный лиганд состоит из менее чем 5 остатков и имеет молекулярную массу не более 1000 Да; и
где лиганд содержит или состоит из ковалентно связанных остатков Х1-Х2-Х3, причем X1, Х2 и/или Х3 необязательно дополнительно связаны с остатком линкера L; и
где остаток X1 выбран из группы, состоящей из Arg, Phe, PPC, DBHBA, SAA, DAP, DAB, (DBHBA)2-DAP, (MDCA)2-DAP, DPBBA, DBBA, PCAA, DPPAA, Trp, TMPPA и DBHPA;
где остаток Х2 выбран из группы, состоящей из Arg, Asn, Leu, Lys, Phe, Pro, PPC, DAP, DAB, His, Trp, Tyr и Ser; и
где остаток Х3 выбран из группы, состоящей из Arg, Asn, Pro, PPC, Asp, Orn и (1H2NA)Dap.
H2N-(D)Phe-(L)Arg-(L)Arg-Gly-OH,
H2N-(L)Arg-(D)Phe-(L)Arg-Gly-OH,
HN-PPC-(D)Pro-(L)Arg-Gly-OH,
DBBA-(L)His-(L)Arg-Gly-OH,
DBBA-His-Arg-Gly-OH,
DBBA-His-Arg-Arg-Gly-OH,
DPPBA-(L)Phe-(L)Arg-Gly-OH,
PCAA-(L)Phe-(L)Arg-Gly-OH,
DPPBA-(L)Lys-(L)Arg-Gly-OH,
SAA-(L)Arg-(L)Pro-Gly-OH,
SAA-(L)Pro-(L)Arg-Gly-OH,
DBHBA-(L)Arg-(L)Asn-Gly-OH,
DBHBA-(L)Asn-(L)Arg-Gly-OH,
DPPBA-(L)Trp-(L)Arg-Gly-OH,
(MDCA)2-DAP-(L)Arg-(L)Orn-Gly-OH,
(MDCA)2-DAP-(L)Arg-(L)Asp-Gly-OH,
DPPAA-(L)Phe-(L)Arg-Gly-OH,
DPPAA-PPC-(L)Arg-Gly-OH,
DBHBA-(D)Phe-(D)Arg-Gly-OH,
DPPAA-(D)Tyr-(D)Arg-Gly-OH,
(DPPA)2-DAP-(L)Arg-(L)Orn-Gly-OH,
(DBHBA)2-DAP-(L)Arg-(L)Arg-Gly-OH,
DBHBA-DAP-Arg-Gly-OH,
DBHBA-DAP-Arg-Arg-Gly-OH,
(DBHBA)2-DAP-Arg-Gly-OH,
(DBHBA)2-DAP-Arg-Arg-Gly-OH,
TMPPA-(L)Trp-(L)Arg-Gly-OH и
DBHPA-(L)Arg-(L)Orn-Gly-OH.
где, по меньшей мере, одна гидрофобная функциональная группа отделена, по меньшей мере, от одной катионной функциональной группы расстоянием между связями от 5 Å до 20 Å,
где указанный лиганд состоит из 3 остатков, выбранных из группы, состоящей из D-Leu; D-Lys; D-Phe; D-Pro; L-Arg; L-Asn; L-Pro; Ahx; Aib; DBHBA; INA; Nle; PPC; SAA; 3НВА и 4НВА, и
имеет молекулярную массу не более 1000 Да.
D-Phe-(L)Arg-(L)Arg,
L-Arg-D-Phe-(L)Arg,
PPC-D-Pro-(L)Arg,
PPC-D-Leu-PPC,
INA-D-Phe-PPC,
PPC-AIB-PPC,
L-Arg-(L)Arg-D-Phe,
PPC-(L)Arg-D-Pro,
D-Pro-PPC-(L)Arg,
L-Arg-D-Pro-PPC,
L-Arg-D-Lys-(L)Arg,
L-Arg-(L)Arg-D-Lys,
D-Lys-INA-(L)Arg,
INA-(L)Arg-D-Lys,
PPC-AHX-PPC,
PPC-Nle-PPC,
SAA-(L)Arg-(L)Pro,
SAA-(L)Pro-(L)Arg,
DBHBA-(L)Arg-(L)Asn,
DBHBA-(L)Asn-(L)Arg,
3HBA-(L)Arg-(L)Pro,
3HBA-(L)Pro-(L)Arg,
4HBA-(L)Arg-(L)Pro и
4HBA-(L)Pro-(L)Arg.
D-Phe-(L)Arg-(L)Arg-Gly,
L-Arg-D-Phe-(L)Arg-Gly,
PPC-D-Pro-(L)Arg-Gly,
PPC-D-Leu-PPC-Gly,
INA-D-Phe-PPC-Gly,
PPC-AIB-PPC-Gly,
L-Arg-(L)Arg-D-Phe-Gly,
PPC-(L)Arg-D-Pro-Gly,
D-Pro-PPC-(L)Arg-Gly,
L-Arg-D-Pro-PPC-Gly,
L-Arg-D-Lys-(L)Arg-Gly,
L-Arg-(L)Arg-D-Lys-Gly,
D-Lys-INA-(L)Arg-Gly,
INA-(L)Arg-D-Lys-Gly,
PPC-AHX-PPC-Gly,
PPC-Nle-PPC-Gly,
SAA-(L)Arg-(L)Pro-Gly,
SAA-(L)Pro-(L)Arg-Gly,
DBHBA-(L)Arg-(L)Asn-Gly,
DBHBA-(L)Asn-(L)Arg-Gly,
3HBA-(L)Arg-(L)Pro-Gly,
3HBA-(L)Pro-(L)Arg-Gly,
4HBA-(L)Arg-(L)Pro-Gly и
4HBA-(L)Pro-(L)Arg-Gly.

Комментарии