Катализатор для получения серы по процессу клауса и способ его приготовления - RU2176156C2
Код документа: RU2176156C2
Чертежи

Описание
Изобретение относится к области неорганической химии, в частности к катализаторам на основе диоксида титана и способам их приготовления, и может быть использовано в газоперерабатывающей промышленности на установках Клауса.
Процесс Клауса предназначен для получения элементарной серы путем окисления сероводорода диоксидом серы по реакции:
2H2S + SO2 ---> 3/nSn + 2H2O (1)
В газах, поступающих на установки Клауса, наряду с сероводородом и диоксидом серы обычно содержатся
одноуглеродные сераорганические соединения - CS2 и COS.
Одним из требований, предъявляемых к катализаторам процесса Клауса, является их активность в реакциях гидролиза
сераорганических соединений:
CS2 + 2H2O ---> CO2 + 2H2S (2)
CS2 + H2O ---> COS + H2S
(3)
COS + H2O ---> CO2 + H2S (4)
В результате протекания реакций (2-4) образуется сероводород, который окисляется диоксидом серы по реакции
(1), что
приводит к повышению выхода целевого продукта - элементарной серы.
При низкой гидролизной активности катализатора сераорганические соединения (CS2 и COS), содержание которых в исходной газовой смеси составляет 0,5 - 2 об. %, проходят через всю цепочку аппаратов установок Клаус-Сульфрен и поступают с хвостовыми газами в печь термического обезвреживания, где сжигаются с образованием SO2. При высокой гидролизной активности катализатора CS2 и COS превращаются в сероводород, а затем в элементарную серу. Тем самым достигается повышение выхода целевого продукта и резко снижается выброс диоксида серы в окружающую среду.
В настоящее время на установках Клауса используются алюмооксидные и титаноксидные катализаторы. Алюмооксидные катализаторы быстро сульфатируются и теряют свою гидролизную активность. Титаноксидные катализаторы обладают значительно большей стабильностью каталитической активности в гидролизе CS2 и COS, чем оксид алюминия. Поэтому для повышения степени извлечения серы и снижения выбросов SO2 в атмосферу за счет гидролиза сераорганических соединений целесообразно использовать на установках Клауса титаноксидные катализаторы.
Известен титаноксидный катализатор процесса Клауса, полученный из ортотитановой и метатитановой кислот или оксигидроксида титана с добавками полиакриламида, полисахарида, угля, оксида алюминия или силиката натрия. Недостатком известного катализатора является низкая активность в реакциях гидролиза сераорганических соединений. Так, степень превращения CS2 и COS при 340oC и времени контакта 4 с не превышает 66% [1].
Известен катализатор для процесса Клауса, содержащий оксиды титана и алюминия (60: 40), полученный смешением и агломерацией активного глинозема и порошка диоксида титана. Недостатком известного катализатора является относительно невысокая активность в реакции гидролиза сераорганических соединений при малых временах контакта. Так, степень превращения CS2 при температуре 335oC и времени контакта 2,0 с составляет 62% [2].
Известен катализатор для процесса Клауса, содержащий оксиды титана и церия (40:60), полученный смешением гидроксидов металлов в присутствии азотной кислоты с последующей экструзией массы, сушкой и прокаливанием экструдатов. Недостатком известного катализатора является относительно невысокая активность в реакциях гидролиза сераорганических соединений при малых временах контакта. Так, степень превращения CS2 при температуре 340oC и времени контакта 0,5 и 1,0 с составляет 63 и 88% соответственно [3].
Известен катализатор для процесса Клауса, содержащий смесь оксидов титана, циркония и церия в соотношении 62,3:23,2:14,5. Катализатор получают раздельным осаждением оксигидроксидов титана, циркония и церия путем взаимодействия основных сульфатов титана, циркония и нитрата церия с щелочным агентом, их смешением, обработкой влажной катализаторной массы азотной кислотой при соотношении (оксигидроксиды металлов): (H2O):(HNO3) = 69:23:8 с последующими стадиями формовки, сушки и прокаливания. Полученный катализатор обеспечивает выход серы по реакции (1), близкий к термодинамически равновесному. Конверсия CS2 при температуре 340oC и времени контакта 0,5 и 1,0 с составляет 63 и 95% соответственно [4].
Недостатком известного катализатора является относительно невысокая активность в реакциях гидролиза сераорганических соединений при малых временах контакта.
Недостатками способа приготовления катализатора является раздельное получение трех осадков оксигидроксидов титана, циркония и церия, приводящее к осложнению технологии; введение в катализаторную массу азотной кислоты, в связи с чем требуется наличие дорогостоящей коррозионностойкой аппаратуры; выбросы в атмосферу значительных количеств оксидов азота, образующихся в результате разложения азотной кислоты при прокаливании катализатора.
Наиболее близким по технической сущности и достигаемому эффекту к предлагаемому техническому решению является катализатор, содержащий 65 - 98,5% диоксида титана и 1,5 - 35% сульфата кальция, стронция или бария (соединение щелочноземельного элемента).
Способ его приготовления заключается в получении оксигидроксида титана обработкой тетрахлорида титана водным раствором щелочного агента, отделении осадка, промывке водой (или без промывки), сушке при 110oC в течение 24 ч, перемешивании полученного порошка в течение 30 мин с водой и карбоксиметилцеллюлозой, экструзии этой смеси, сушке экструдата при 110oC в течение 8 ч, прокаливании при 450 - 500oC в течение 2 - 7 ч, пропитке продукта раствором сульфата аммония или серной кислоты, сушке в течение 4 ч при 110oC, последующей пропитке нитратом щелочноземельного элемента, сушке при 110oC в течение 4 - 12 ч и прокаливании при 450oC в течение 1 - 2 ч.
Полученный катализатор обеспечивает выход серы по реакции (1), близкий к термодинамически равновесному. Конверсия CS2 при температуре 260oC и времени контакта 1 с составляет 72%, при температуре 340oC и времени контакта 3с - 99% [5] - (прототип).
Недостатком известного катализатора является относительно невысокая активность в реакциях гидролиза сераорганических соединений при низких температурах и малых временах контакта.
Недостатками способа приготовления катализатора является многостадийность и сложность технологии, большие затраты энергии на многократные стадии сушки и прокаливания катализаторной массы, наличие выбросов в атмосферу оксидов азота (около 100 кг на 1 т катализатора).
Сравнение данных по активности в реакциях окисления сероводорода диоксидом серы и гидролиза сераорганических соединений показывает, что катализаторы, полученные по патентам [4] и [5], практически одинаковы. Выбор в качестве прототипа катализатора по патенту [5] обусловлен тем, что предлагаемый катализатор, также как и прототип, содержит оксидный компонент и соединение щелочноземельного элемента. Кроме того, производство катализатора по прототипу освоено в промышленности (катализатор CRS-31, фирма Рон-Пуленк), что позволяет использовать его для экспериментального определения каталитической активности прототипа и предлагаемого катализатора.
Технической задачей изобретений является создание катализатора для получения серы по процессу Клауса, обладающего повышенной активностью в реакциях гидролиза сераорганических соединений, а также способа его приготовления, позволяющего улучшить текстурные характеристики катализатора, повысить механическую прочность и устранить выбросы оксидов азота в атмосферу.
Задача изобретений решается путем создания катализатора, содержащего оксидный компонент и соединения
щелочноземельного элемента, который отличается тем, что в него
дополнительно введены соединения алюминия, в качестве соединения щелочноземельного элемента - соединения кальция, а в качестве оксидного
компонента он содержит твердый раствор диоксида титана и
пентаоксида ниобия при следующем содержании компонентов, мас.%:
Соединения кальция - 1,0 - 5,0
Соединения алюминия - 20,0
- 55,0
Твердый раствор диоксида титана и
пентаоксида ниобия - Остальное
Задача решается также тем, что содержание диоксида титана в твердом растворе составляет 90,0 - 99,0 мас.%, и
также тем, что он содержит в своем составе твердый
раствор диоксида титана и пентаоксида ниобия следующего состава:
Ti(Nb)xO(2+2,5x), где 0,006 ≤ x ≤ 0,
06.
Задача решается также тем, что в качестве соединений кальция катализатор содержит оксид и карбонат кальция.
Задача решается также тем, что в своем составе он содержит 0,5 - 2,5 мас. % оксида кальция, а в качестве соединений алюминия он содержит алюминат кальция или алюминат кальция и оксид алюминия.
Задача решается и тем, что катализатор
состоит из следующих компонентов, мас.%:
Оксид
кальция - 0,5 - 2,5
Карбонат кальция - 0,5 - 2,5
Алюминат кальция - 20,0 - 25,0
Твердый раствор диоксидов титана и
пентаоксида ниобия - Остальное
Задача решается и
тем, что катализатор состоит из следующих компонентов, мас.%:
Оксид кальция - 0,5 - 2,5
Карбонат кальция - 0,5 - 2,5
Алюминат кальция - 20,0 - 25,0
Оксид алюминия
- Не более 30,0
Твердый раствор диоксида титана и пентаоксида ниобия - Остальное
Задача решается созданием способа
приготовления катализатора для получения серы по процессу Клауса,
включающего обработку тетрахлорида титана водным раствором или суспензией щелочного агента, формование, сушку и прокаливание с
получением катализатора, который отличается тем, что совместно с
тетрахлоридом титана ведут обработку пентахлорида ниобия водным раствором или суспензией щелочного агента с получением оксигидроксидов
титана и ниобия, осадок оксигидроксидов титана и ниобия смешивают
с соединениями кальция и ведут процесс при условиях, обеспечивающих получение катализатора, содержащего соединения алюминия, в
качестве соединений щелочноземельного элемента - соединения кальция, а в
качестве оксидного компонента - твердый раствор диоксида титана и пентаоксида ниобия при следующем содержании компонентов,
мас.%:
Соединения кальция - 1,0 - 5,0
Соединения алюминия
- 20,0 - 55,0
Твердый раствор диоксида титана и пентаоксида ниобия - Остальное
Задача решается созданием
способа, в котором после обработки пентахлорида ниобия водным раствором или
суспензией щелочного агента с получением оксигидроксидов титана и ниобия осадок оксигидроксидов титана и ниобия смешивают
дополнительно с соединениями кальция и соединениями алюминия, в качестве
которых берут оксид кальция, карбонат кальция, оксигидроксид алюминия и алюминат кальция и ведут процесс при условиях,
обеспечивающих получение катализатора, содержащего соединения алюминия, в
качестве соединений щелочноземельного элемента - соединения кальция, а в качестве оксидного компонента - твердый раствор
диоксида титана и пентаоксида ниобия при следующем содержании компонентов,
мас.%:
Оксид кальция - 0,5 - 2,5
Карбонат кальция - 0,5 - 2,5
Алюминат кальция - 20,0 - 25,0
Твердый раствор диоксида титана и пентаоксида ниобия - Остальное
Задача решается также созданием способа, в котором после обработки пентахлорида ниобия водным раствором или суспензией
щелочного агента с получением оксигидроксидов титана и ниобия, осадок
оксигидроксидов титана и ниобия смешивают дополнительно с соединениями кальция и соединениями алюминия, в качестве которых берут
оксид кальция, карбонат кальция, оксигидроксид алюминия и алюминат
кальция и ведут процесс при условиях, обеспечивающих получение катализатора, содержащего соединения алюминия, в качестве соединений
щелочноземельного элемента - соединения кальция, а в качестве
оксидного компонента - твердый раствор диоксида титана и пентаоксида ниобия при следующем содержании компонентов, мас.%:
Оксид
кальция - 0,5 - 2,5
Карбонат кальция - 0,5 - 2,5
Алюминат кальция - 20,0 - 25,0
Оксид алюминия - До 30,0
Твердый раствор диоксида титана и пентаоксида ниобия
- Остальное
При этом количества тетрахлорида титана и
пентахлорида ниобия берут из расчета, чтобы соотношение оксидов титана и ниобия в твердом растворе было в пределах (90-99): (1-10) и
кроме того процесс ведут при условиях, обеспечивающих получение
катализатора, содержащего твердый раствор диоксида титана и пентаоксида ниобия следующего состава: Ti(Nb)xO(2+2,
5x), где 0,006 ≤ x ≤ 0,06.
Отличительными признаками способа приготовления катализатора являются:
- одновременное получение оксигидроксидов титана и
ниобия путем совместной обработки тетрахлорида титана и пентахлорида
ниобия водным раствором или суспензией щелочного агента;
- предварительное введение соединения кальция (оксид и карбонат
кальция) в полученный осадок оксигидроксидов титана и ниобия;
- смешение влажной массы оксигидроксидов титана и ниобия и соединений кальция с алюминатом кальция и оксигидратом алюминия;
- гидротермальная обработка просушенных экструдатов.
Указанные отличительные признаки позволяют получить катализатор, обладающий высокой активностью в реакциях гидролиза сераорганических соединений и окисления сероводорода диоксидом серы, высокой механической прочностью и относительно низкой насыпной массой.
Получение катализаторов осуществляют следующим образом.
В реактор заливают определенное количество водного раствора или суспензии щелочного агента и при перемешивании вводят рассчитанные количества тетрахлорида титана и пентахлорида ниобия, обеспечивающие нейтрализацию щелочного агента.
При взаимодействии тетрахлорида титана и пентахлорида ниобия со щелочным агентом образуется смесь оксигидроксидов титана и ниобия, выпадающая в осадок, и хлориды аммония, щелочного или щелочноземельного элемента, растворяющиеся в маточнике. Количества TiCl4 и NbCl5 берут из расчета, чтобы соотношение (TiO2):(Nb2O5) в твердом растворе было в пределах (90-99):(1-10).
Полученный осадок, содержащий оксигидроксиды титана и ниобия, отделяют фильтрацией и промывают водой для удаления хлоридов аммония, щелочного или щелочноземельного элемента. Промытый осадок оксигидроксидов титана и ниобия с влажностью 75 ± 5 мас.% смешивают в смесителе с карбонатом кальция и оксидом кальция из расчета, чтобы в готовом катализаторе их содержание было в пределах 1 - 5 мас.%, алюминатом кальция или алюминатом кальция и оксигидратом алюминия из расчета, чтобы в готовом продукте их содержание было в пределах 20 - 25 мас.% или 20 - 55 мас.% соответственно, а также 1,0 мас.% в расчете на готовый продукт пластификатора (поливиниловый спирт или карбоксиметилцеллюлоза), формуют в виде экструдатов, которые сушат при 110 - 120oC в течение 2 ч и подвергают гидротермальной обработке при температуре 85 - 95oC в течение 1 ч. Полученные экструдаты сушат при 110 - 120oC в течение 2 ч и прокаливают при 450oC в течение 4 ч.
При совместном осаждении оксигидроксидов титана и ниобия по описанному способу происходит равномерное распределение оксигидроксида ниобия в оксигидроксиде титана. Последующие стадии сушки и прокаливания приводят к формированию твердого раствора оксидов титана и ниобия, обладающего повышенной активностью в реакциях гидролиза сераорганических соединений.
Наличие 1 - 5 мас.% карбоната и оксида кальция в составе катализатора усиливает его основные свойства, что также повышает активность в реакциях гидролиза CS2 и COS.
Алюминат кальция относится к быстросхватывающимся цементам. Добавка его в катализаторную массу позволяет повысить механическую прочность катализатора, сформованного в виде экструдатов. Дополнительное упрочнение экструдатов происходит на стадиях гидротермальной обработки, сушки и прокаливания катализатора. Кроме того, введение алюмината кальция в катализаторную массу сопровождается улучшением пористой структуры катализатора за счет увеличения доли мезопор и макропор, приводящей к интенсификации массообменных процессов внутри гранул катализатора и, как следствие, к повышению скорости протекающих реакций.
Оксигидрат алюминия - AlO(OH), введенный в состав катализаторной массы, после прокаливания превращается в оксид алюминия: 2AlO(OH) ---> Al2O3 + H2O.
Оксид алюминия обладает высокой удельной поверхностью (200 - 250 м2/г) и поэтому повышает активность катализатора как в реакции Клауса (окисление сероводорода диоксидом серы), так и в реакциях гидролиза COS и CS2. Активность синтезированных образцов катализатора определяют в реакции гидролиза сероуглерода и в реакции Клауса на микроимпульсной установке с хроматографическим анализом продуктов. Для проведения испытаний определенное количество катализатора с размером зерна 0, 25 - 0,50 мм помещают в стальной микрореактор (длина 70 мм, диаметр 3 мм) и прогревают в токе гелия в течение 1 ч.
При определении активности катализаторов в реакции гидролиза сераорганических соединений в микрореактор помещают 0,05 см3 катализатора и микрошприцем вводят смесь жидкостей в мольном отношении CS2:H2O = 1:2.
При определении активности в реакции Клауса в микрореактор помещают 0,01 см3 катализатора и вводят смесь газов в мольном отношении H2S:SO2 = 2:1.
Время контакта реагентов с катализатором составляет 0,05 и 0,01 с, температура в зоне реакции 300oC и 220o C соответственно для реакций гидролиза сероуглерода и окисления сероводорода диоксидом серы. Активность катализаторов выражают в виде константы скорости реакции, рассчитанной по уравнению Хебгуда и Бассета /J. Phys. Chem., 1960, v. 64, p. 769/. Значение константы скорости реакции рассчитывают как среднее из пяти измерений.
Устойчивость катализаторов к сульфатации определяют путем сопоставления их активности в гидролизе CS2 до и после обработки газовой смесью, содержащей, об.%: SO2 25, пары воды 25 и воздух 50. Сульфатацию проводят в проточном стеклянном реакторе, в который загружают навеску катализатора, поднимают температуру до 400oC и подают газовую смесь со скоростью 10 см3/мин•г катализатора.
Изобретение иллюстрируется следующими примерами.
Пример 1. В реактор загружают 1386 мл 10%-ной суспензии гидроксида кальция и при перемешивании прибавляют 1,52 г пентахлорида ниобия и 176,3 г (101,9 см3) тетрахлорида титана. После прибавления TiCl4 перемешивание продолжают в течение 30 мин для завершения реакции нейтрализации (pH суспензии 6,8 ± 0,2). Полученный осадок отделяют фильтрацией и промывают водой для удаления хлорида кальция. Промытый осадок оксигидроксидов титана и ниобия смешивают с 2,5 г CaO, 2,5 г CaCO3, 20 г алюмината кальция и 1 г пластификатора (поливинилового спирта или карбоксиметилцеллюлозы в виде 10%-ного раствора). Катализаторную массу перемешивают в течение 30 мин, затем формуют экструзией. Полученные экструдаты сушат при 110 - 120oC в течение 2 ч, затем подвергают гидротермальной обработке в течение 1 ч, помещая их в воду, нагретую до 85 - 95oC, после чего сушат при 110 - 120oC в течение 2 ч и прокаливают при 450oC в течение 4 ч. Получают катализатор, содержащий мас.%: 2,5 CaCO3, 2,5 CaO, 20,0 алюмината кальция и 75,0 твердого раствора оксидов металлов состава TiNb0,006O2, 02 при массовом соотношении оксидов титана и ниобия, равном 99:1.
Пример 2. Катализатор готовят аналогично описанному в примере 1 с той разницей, что в реактор загружают 1307 мл 10%-ной суспензии гидроксида кальция, вводят при перемешивании 4,26 г пентахлорида ниобия и 163,6 г (94,6 см3) тетрахлорида титана, а осадок оксигидроксидов титана и ниобия смешивают с 1,5 г CaCO3 и 25 г алюмината кальция.
Получают катализатор, содержащий мас.%: 2,5 CaO, 1,5 CaCO3, 25,0 алюмината кальция и 71,0 твердого раствора оксидов металлов состава TiNb0,018O2,05 при массовом соотношении оксидов титана и ниобия, равном 97: 3.
Пример 3. Катализатор готовят аналогично описанному в примере 1 с той разницей, что в реактор загружают 1333 мл 10%-ного раствора гидроксида аммония и вводят при перемешивании 10, 35 г пентахлорида ниобия и 161,3 г (93,2 см3) тетрахлорида титана, а осадок оксигидроксидов титана и ниобия смешивают с 2,0 г CaO, 2,0 г CaCO3 и 23 г алюмината кальция.
Получают катализатор, содержащий мас.%: 2,0 CaO, 2,0 CaCO3, 23,0 алюмината кальция и 73,0 твердого раствора оксидов металлов состава TiNb0,04O2,10 при массовом соотношении оксидов титана и ниобия, равном 93:7.
Пример 4. Катализатор готовят аналогично описанному в примере 1 с той разницей, что в реактор загружают 1397 мл 10%-ной суспензии гидроксида кальция и вводят при перемешивании 15,63 г пентахлорида ниобия и 164, 6 г (95,2 см3) тетрахлорида титана, а осадок оксигидроксидов титана и ниобия смешивают с 0,5 г CaO, 0,5 г CaCO3 и 22 г алюмината кальция.
Получают катализатор, содержащий мас.%: 0,5 CaO, 0,5 CaCO3, 22,0 алюмината кальция и 77,0 твердого раствора оксидов металлов состава TiNb0,06O2,15 при массовом соотношении оксидов титана и ниобия, равном 90: 10.
Пример 5. Катализатор готовят аналогично описанному в примере 1 с той разницей, что в реактор загружают 1350 мл 10%-ной суспензии гидроксида кальция и вводят при перемешивании 9,66 г пентахлорида ниобия и 165,4 г (95,6 см3) тетрахлорида титана, а осадок оксигидроксидов титана и ниобия смешивают с 0,3 г CaO, 0,3 г CaCO3 и 25,0 г алюмината кальция.
Получают катализатор, содержащий мас.%: 0,3 CaO, 0,3 CaCO3, 25,0 алюмината кальция и 74,4 твердого раствора оксидов металлов состава TiNb0,04O2, 10 при массовом соотношении оксидов титана и ниобия, равном 93,6: 6,4.
Пример 6. Катализатор готовят аналогично описанному в примере 1 с той разницей, что в реактор загружают 1394 мл 10 %-ной суспензии гидроксида кальция и вводят при перемешивании 17,2 г пентахлорида ниобия и 162, 8 г (94,1 см3) тетрахлорида титана, а осадок оксигидроксидов титана и ниобия смешивают с 18,0 г алюмината кальция.
Получают катализатор, содержащий мас.%: 2,5 CaO, 2,5 CaCO3, 18,0 алюмината кальция и 77,0 твердого раствора оксидов металлов состава TiNb0,074O2,19 при массовом соотношении оксидов титана и ниобия, равном 89: 11.
Пример 7. Катализатор готовят аналогично описанному в примере 1 с той разницей, что в реактор загружают 1253 мл 10%-ной суспензии гидроксида кальция и вводят при перемешивании 4,14 г пентахлорида ниобия и 156,7 г (90,6 см3) тетрахлорида титана, а осадок оксигидроксидов титана и ниобия смешивают с 1,0 г CaO, 1,0 г CaCO3 и 30,0 г алюмината кальция.
Получают катализатор, содержащий мас.%: 1,0 CaO, 1,0 CaCO3, 30,0 алюмината кальция и 68,0 твердого раствора оксидов металлов состава TiNb0,018O2,05 при массовом соотношении оксидов титана и ниобия, равном 97: 3.
Пример 8. Катализатор готовят аналогично описанному в примере 1 с той разницей, что в реактор загружают 1270 мл 10%-ной суспензии гидроксида кальция и вводят при перемешивании 4,20 г пентахлорида ниобия и 158,9 г (91,8 см3) тетрахлорида титана, а осадок оксигидроксидов титана и ниобия смешивают с 3,0 г CaO, 3,0 г CaCO3 и 25,0 г алюмината кальция.
Получают катализатор, содержащий мас.%: 3,0 CaO, 3,0 CaCO3, 25,0 алюмината кальция и 69,0 твердого раствора оксидов металлов состава TiNb0,019O2,05 при массовом соотношении оксидов титана и ниобия, равном 97: 3.
Пример 9. Катализатор готовят аналогично описанному в примере 1 с той разницей, что в реактор загружают 1204 мл 10%-ной суспензии гидроксида кальция и вводят при перемешивании 0, 61 г пентахлорида ниобия и 153,7 г (88,8 см3) тетрахлорида титана, а осадок оксигидроксидов титана и ниобия смешивают с 30,0 г алюмината кальция.
Получают катализатор, содержащий мас.%: 2,5 CaO, 2,5 CaCO3, 30,0 алюмината кальция и 65,0 твердого раствора оксидов металлов состава TiNb0,003O2,007 при массовом соотношении оксидов титана и ниобия, равном 99,5:0,5.
Пример 10. Катализатор готовят аналогично описанному в примере 1 с той разницей, что в реактор загружают 1386 мл 10%-ной суспензии гидроксида кальция и вводят при перемешивании 1,50 г пентахлорида ниобия и 174,6 г (100,6 см3) тетрахлорида титана, а осадок оксигидроксидов титана и ниобия смешивают с 1,18 г оксигидрата алюминия.
Получают катализатор, содержащий мас.%: 2,5 CaO, 2,5 CaCO3, 20,0 алюмината кальция, 1,0 Al2O3 и 74,0 твердого раствора оксидов металлов состава TiNb0, 006O2,02 при массовом соотношении оксидов титана и ниобия, равном 99: 1.
Пример 11. Катализатор готовят аналогично описанному в примере 1 с той разницей, что в реактор загружают 1294 мл 10%-ной суспензии гидроксида кальция и вводят при перемешивании 1, 42 г пентахлорида ниобия и 164,6 г (95,1 см3) тетрахлорида титана, а осадок оксигидроксидов титана и ниобия смешивают с 5,88 г оксигидрата алюминия.
Получают катализатор, содержащий мас.%: 2,5 CaO, 2,5 CaCO3, 20,0 алюмината кальция, 5,0 Al2O3 и 70,0 твердого раствора оксидов металлов состава TiNb0,006O2,02 при массовом соотношении оксидов титана и ниобия, равном 99: 1.
Пример 12. Катализатор готовят аналогично описанному в примере 1 с той разницей, что в реактор загружают 1203 мл 10%-ной суспензии гидроксида кальция и вводят при перемешивании 1,50 г пентахлорида ниобия и 152,8 г (88,3 см3) тетрахлорида титана, а осадок оксигидроксидов титана и ниобия смешивают с 11,76 г оксигидрата алюминия.
Получают катализатор, содержащий мас.%: 2,5 CaO, 2,5 CaCO3, 20,0 алюмината кальция, 10,0 Al2O3 и 65,0 твердого раствора оксидов металлов состава TiNb0,006O2,02 при массовом соотношении оксидов титана и ниобия, равном 99: 1.
Пример 13. Катализатор готовят аналогично описанному в примере 1 с той разницей, что в реактор загружают 1017 мл 10%-ной суспензии гидроксида кальция и вводят при перемешивании 1,12 г пентахлорида ниобия и 129,3 г (74,7 см3) тетрахлорида титана, а осадок оксигидроксидов титана и ниобия смешивают с 23,53 г оксигидрата алюминия.
Получают катализатор, содержащий мас.%: 2,5 CaO, 2,5 CaCO3, 20,0 алюмината кальция, 20,0 Al2O3 и 55,0 твердого раствора оксидов металлов состава TiNb0,006O2,02 при массовом соотношении оксидов титана и ниобия, равном 99: 1.
Пример 14. Катализатор готовят аналогично описанному в примере 1 с той разницей, что в реактор загружают 924 мл 10%-ной суспензии гидроксида кальция и вводят при перемешивании 1,02 г пентахлорида ниобия и 117,6 г (68,0 см3) тетрахлорида титана, а осадок оксигидроксидов титана и ниобия смешивают с 29,4 г оксигидрата алюминия.
Получают катализатор, содержащий мас.%: 2, 5 CaO, 2,5 CaCO3, 20,0 алюмината кальция, 25,0 Al2O3 и 50,0 твердого раствора оксидов металлов состава TiNb0,006O2,02 при массовом соотношении оксидов титана и ниобия, равном 99: 1.
Пример 15. Катализатор готовят аналогично описанному в примере 1 с той разницей, что в реактор загружают 832 мл 10%-ной суспензии гидроксида кальция и вводят при перемешивании 0,91 г пентахлорида ниобия и 105,8 г (61,2 см3) тетрахлорида титана, а осадок оксигидроксидов титана и ниобия смешивают с 35,2 г оксигидрата алюминия.
Получают катализатор, содержащий мас.%: 2,5 CaO, 2,5 CaCO3, 20,0 алюмината кальция, 30,0 Al2O3 и 45,0 твердого раствора оксидов металлов состава TiNb0,006O2,02 при массовом соотношении оксидов титана и ниобия, равном 99: 1.
Пример 16. Катализатор готовят аналогично описанному в примере 1 с той разницей, что в реактор загружают 740 мл 10%-ной суспензии гидроксида кальция и вводят при перемешивании 0,81 г пентахлорида ниобия и 94,1 г (54,4 см3) тетрахлорида титана, а осадок оксигидроксидов титана и ниобия смешивают с 41,3 г оксигидрата алюминия.
Получают катализатор, содержащий мас.%: 2,5 CaO, 2,5 CaCO3, 20,0 алюмината кальция, 35,0 Al2O3 и 40, 0 твердого раствора оксидов металлов состава TiNb0,006O2,02 при массовом соотношении оксидов титана и ниобия, равном 99: 1.
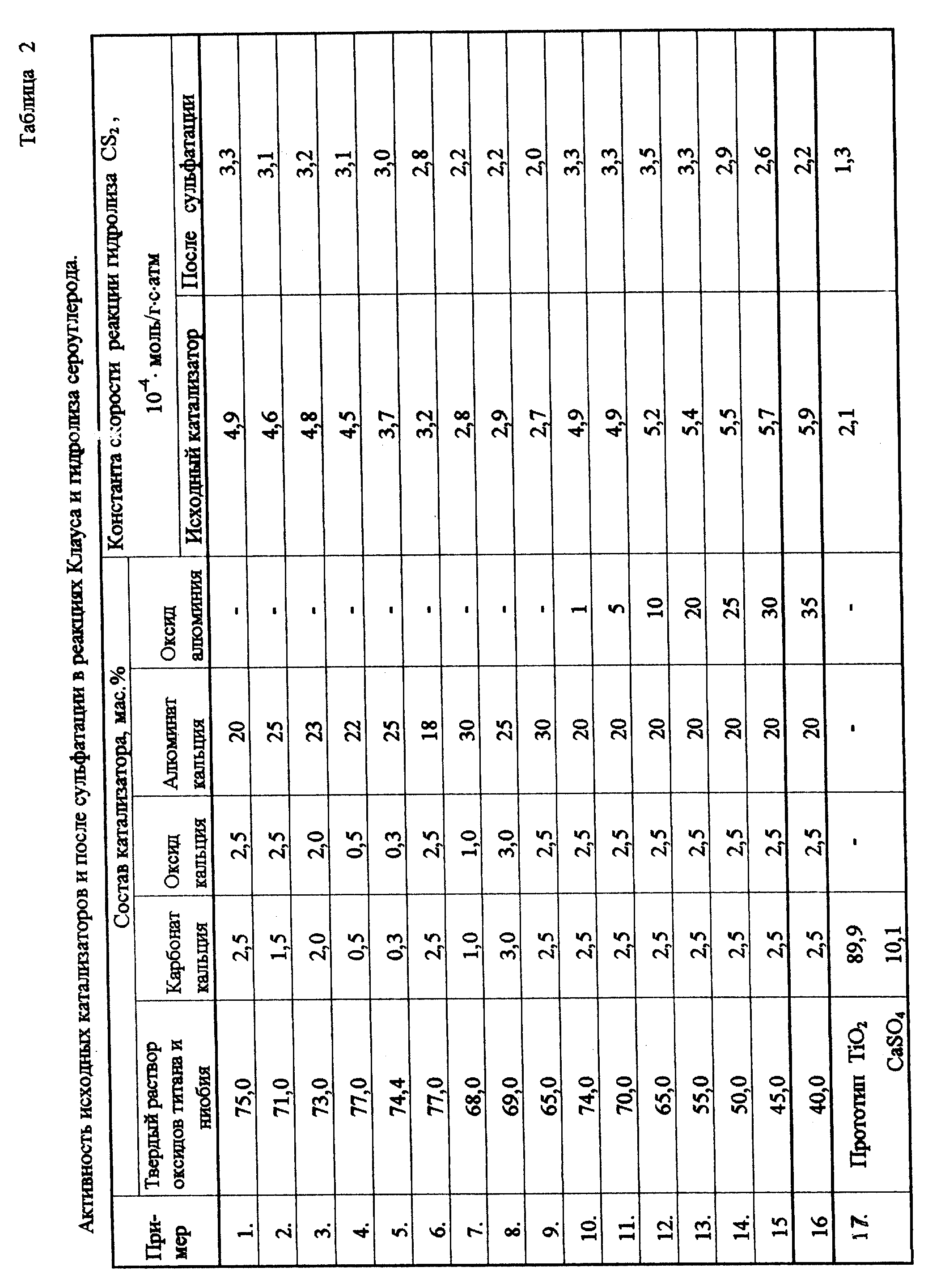
Приведенные в таблицах 1 и 2 данные по физико-химическим свойствам и активности катализаторов, приготовленных по описанному способу и прототипу (титаноксидный катализатор марки CRS-31 фирмы Рон-Пуленк, Франция) показывают, что образцы катализатора, полученные по предлагаемому способу, обладают значительно более высокой активностью в реакции гидролиза сероуглерода по сравнению с прототипом. Так, константа скорости реакции гидролиза сероуглерода на предлагаемом катализаторе в 2,1 - 2,8 раза выше по сравнению с известным катализатором: превращение сероуглерода при температуре 300oC и времени контакта 0,25 с в примерах 1 - 4 и 11 - 16 на предлагаемом катализаторе составляет 57 - 65 %, на катализаторе по прототипу - 38%. В примерах 5 - 9 активность катализаторов в реакции гидролиза сероуглерода несколько ниже в связи с тем, что в образцах, полученных в примерах 6 и 9, соотношение компонентов в твердом растворе (оксиды титана и ниобия) выходит за границы оптимума, в катализаторах, полученных в примерах 5 и 8, содержание CaO и CaCO3 выходит за границы оптимума.
Катализатор, полученный в примере 6 и содержащий в своем составе 18 мас. % алюмината кальция, обладает относительно более низкой механической прочностью, а катализатор, содержащий 30 мас.% алюмината кальция (примеры 7 и 9), по механической прочности не отличается от катализаторов с содержанием алюмината кальция 20 - 25 мас.%, которое является оптимальным.
Катализатор, полученный в примере 16 и содержащий 35 мас.% оксида алюминия, в реакции гидролиза сероуглерода проявляет активность, близкую к активности катализатора из примера 15, однако после сульфатации его активность снижается в большей мере, чем у прототипа.
Все образцы катализатора, приготовленные описанным способом, обладают более развитой поверхностью по сравнению с прототипом, что способствует повышению их активности в реакции Клауса, обеспечивая термодинамически равновесные выходы целевого продукта, а также высокой термостабильностью (после прокаливания катализаторов при температуре 600oC в течение 4 ч активность практически не снижается).
Приготовленные по описанному способу образцы катализаторной пасты обладают высокой пластичностью и при формовании получаются гладкие экструдаты.
Катализаторы, приготовленные по описанному способу, имеют относительно низкую насыпную массу (0,68 - 0,72 кг/л) и высокую механическую прочность: разрушающее усилие на раздавливание составляет 0,6 - 0,8 кг/мм2, для прототипа - 0,3 кг/мм2.
Предлагаемый способ приготовления катализатора по сравнению с прототипом позволяет упростить технологию промышленного производства, снизить его стоимость за счет сокращения количества технологических операций, в частности, сокращения числа и продолжительности стадий сушки и прокаливания, связанных с большими затратами энергии, а также исключить образование и выбросы оксидов азота в окружающую среду в связи с тем, что для приготовления катализатора не используются нитраты.
Использование предлагаемого катализатора в газоперерабатывающей промышленности позволит за счет высокой активности в реакции гидролиза CS2 и COS увеличить выход газовой серы и сократить выбросы диоксида серы в окружающую среду, поскольку при низкой активности катализатора часть CS2 и COS, не подвергшаяся гидролизу, поступает с хвостовыми газами установок Клаус-Сульфрен в печь термического обезвреживания, где сжигается с образованием диоксида серы и выбрасывается в атмосферу.
Изложенное выше обуславливает получение технического результата, включающего создание катализатора и способа его приготовления.
Технический результат изобретения заключается в более высокой активности предлагаемого катализатора в реакции гидролиза сераорганических соединений, более высокой механической прочности и относительно низкой насыпной массе по сравнению с прототипом, упрощении способа приготовления катализатора за счет резкого сокращения количества технологических операций и исключении выбросов оксидов азота в окружающую среду.
ЛИТЕРАТУРА
1. Патент Франции N 2481145, кл.
B 01 J 21/06, 1981.
2. Патент ФРГ N 2417092, кл. B 01 D 53/36, 1977.
3. Патент EP N 0272979, кл. B 01 J 23/10, 1988.
4. Патент Франции N 2598094, кл. В 01 D 53/36, 1987.
5. Патент СССР, N 1213976, кл. В 01 J 21/06, 1986.
Реферат
Изобретение относится к катализаторам для получения серы по процессу Клауса и способам его приготовления. Описывается катализатор для получения серы по процессу Клауса, содержащий оксидный компонент и соединения щелочноземельного элемента, который дополнительно содержит соединения алюминия, в качестве соединений щелочноземельного элемента он содержит соединения кальция, а в качестве оксидного компонента - твердый раствор диоксида титана и пентаоксида ниобия при следующем содержании компонентов, мас.%: соединения кальция 1,0-5,0, соединения алюминия 20,0-55,0, твердый раствор диоксида титана и пентаоксида ниобия остальное. Описывается также способ приготовления катализатора для получения серы по процессу Клауса, включающий обработку тетрахлорида титана водным раствором или суспензией щелочного агента, формование, сушку и прокаливание с получением катализатора, отличающийся тем, что совместно с тетрахлоридом титана ведут обработку пентахлорида ниобия водным раствором или суспензией щелочного агента с получение оксигидроксидов титана и ниобия, осадок оксигидроксидов титана и ниобия смешивают с соединениями кальция, и ведут процесс при условиях, обеспечивающих получение катализатора. Технический результат изобретения заключается в более высокой активности предлагаемого катализатора в гидролизе сераорганических соединений и механической прочности, более низкой насыпной массы по сравнению с прототипом, упрощении способа приготовления катализатора за счет сокращения количества технологических операций и исключении выбросов оксидов азота в окружающую среду. 2 с. и 11 з.п.ф-лы, 2 табл.
Формула
Соединения кальция - 1,0-5,0
Соединения алюминия - 20,0-55,0
Твердый раствор диоксида титана и пентаоксида ниобия - Остальное
2. Катализатор по п.1, отличающийся тем, что содержание диоксида титана в твердом растворе составляет 90,0-99,0 мас.%.
Оксид кальция - 0,5-2,5
Карбонат кальция - 0,5-2,5
Алюминат кальция - 20,0-25,0
Твердый раствор диоксида титана и пентаоксида ниобия - Остальное
8. Катализатор по п.1, отличающийся тем, что он состоит из следующих компонентов, мас.%:
Оксид кальция - 0,5-2,5
Карбонат кальция - 0,5-2,5
Алюминат кальция - 20,0-25,0
Оксид алюминия - Не более 30,0
Твердый раствор диоксида титана и пентаоксида ниобия - Остальное
9. Способ приготовления катализатора для получения серы по процессу Клауса, включающий обработку тетрахлорида титана водным раствором или суспензией щелочного агента, формование, сушку и прокаливание с получением катализатора, отличающийся тем, что совместно с тетрахлоридом титана ведут обработку пентахлорида ниобия водным раствором или суспензией щелочного агента с получением оксигидроксидов титана и ниобия, осадок оксигидроксидов титана и ниобия смешивают с соединениями кальция и ведут процесс при условиях, обеспечивающих получение катализатора, содержащего соединения алюминия, в качестве соединений щелочноземельного элемента - соединения кальция, а в качестве оксидного компонента - твердый раствор диоксида титана и пентаоксида ниобия при следующем содержании компонентов, мас.%:
Соединения кальция - 1,0-5,0
Соединения алюминия - 20,0-55,0
Твердый раствор диоксида титана и пентаоксида ниобия - Остальное
10. Способ по п.9, отличающийся тем, что после обработки пентахлорида ниобия водным раствором или суспензией щелочного агента с получением оксигидроксидов титана и ниобия осадок оксигидроксидов титана и ниобия смешивают дополнительно с соединениями кальция, в качестве которых берут оксид кальция и карбонат кальция, с соединением алюминия, в качестве которого берут алюминат кальция, и ведут процесс при условиях, обеспечивающих получение катализатора, содержащего соединения алюминия, в качестве соединений щелочноземельного элемента - соединения кальция, а в качестве оксидного компонента - твердый раствор диоксида титана и пентаоксида ниобия при следующем содержании компонентов, мас.%:
Оксид кальция - 0,5-2,5
Карбонат кальция - 0,5-2,5
Алюминат кальция - 20, 0-25,0
Твердый раствор диоксида титана и пентаоксида ниобия - Остальное
11. Способ по п.9, отличающийся тем, что после обработки пентахлорида ниобия водным раствором или суспензией щелочного агента с получением оксигидроксидов титана и ниобия осадок оксигидроксидов титана и ниобия смешивают дополнительно с соединениями кальция, в качестве которых берут оксид кальция и карбонат кальция, с соединениями алюминия, в качестве которых берут оксигидроксид алюминия и алюминат кальция, и ведут процесс при условиях, обеспечивающих получение катализатора, содержащего соединения алюминия, в качестве соединений щелочноземельного элемента - соединения кальция, а в качестве оксидного компонента - твердый раствор диоксида титана и пентаоксида ниобия при следующем содержании компонентов, мас.%:
Оксид кальция - 0,5-2,5
Карбонат кальция - 0,5-2, 5
Алюминат кальция - 20,0-25,0
Оксид алюминия - Не более 30,0
Твердый раствор диоксида титана и пентаоксида ниобия - Остальное
12. Способ по п.9, отличающийся тем, что количество тетрахлорида титана и пентахлорида ниобия берут из расчета, чтобы соотношение оксидов титана и ниобия в твердом растворе было в пределах (90-99):(1-10).

Комментарии