Каталитически активные вещества - RU2741805C1
Код документа: RU2741805C1
Чертежи




Описание
ПЕРЕКРЕСТНАЯ ССЫЛКА НА РОДСТВЕННЫЕ ЗАЯВКИ
В данной заявке испрашивается приоритет предварительной заявки США с серийным номером 62/609370, поданной 22 декабря 2017 г., содержание которой включается в данный документ посредством ссылки во всей ее полноте.
ПРЕДШЕСТВУЮЩИЙ УРОВЕНЬ ТЕХНИКИ
Биологические чипы находятся среди широкого спектра средств, используемых для выявления и анализа молекул, включая дезоксирибонуклеиновую кислоту (ДНК) и рибонуклеиновую кислоту (РНК). В данных применениях чипы сконструированы для включения зондов для нуклеотидных последовательностей, присутствующих в генах человека и других организмов. В некоторых применениях, например, индивидуальные зонды ДНК и РНК могут быть присоединены в определенных положениях в геометрической сетке (или случайно) на подложке чипа. Опытный образец, например, от человека или организма, может быть нанесен на сетку таким образом, что комплементарные фрагменты гибридизуются с зондами в индивидуальных сайтах на чипе. Данный чип может затем быть проверен посредством сканирования специфических частот света над данными сайтами для идентификации того, какие фрагменты присутствуют в образце, по флуоресценции сайтов, в которых гибридизуются фрагменты.
Биологические чипы могут использоваться для генетического секвенирования. В общем, генетическое секвенирование включает определение порядка нуклеотидов или нуклеиновых кислот по длине генетического материала, такого как фрагмент ДНК или РНК. Анализируются все более и более длинные последовательности пар оснований, и полученную в результате информацию о последовательности можно использовать в разных методах биоинформатики для приведения фрагментов в логическую связь таким образом, чтобы надежно определить последовательность значительной длины генетического материала, из которого происходят фрагменты. Разработали автоматизированную проверку характеризующих фрагментов на основе компьютера и использовали в картировании генома, идентификации генов и их функции, оценке рисков определенных состояний и болезненных состояний, и так далее. Помимо данных применений, биологические чипы могут использоваться для выявления и оценки широкого спектра молекул, семейств молекул, генетических уровней экспрессии, однонуклеотидных полиморфизмов и генотипирования.
ВВЕДЕНИЕ
В одном аспекте каталитически активное вещество содержит минеральную частицу сульфида меди(I); и молекула, функционализированная алкином, непосредственно связывается с поверхностью минеральной частицы сульфида меди(I).
В одном примере данного аспекта минеральная частица сульфида меди(I) выбрана из группы, состоящей из халькозина, джарлеита и дигенита.
В одном примере данного аспекта молекула, функционализированная алкином, представляет собой праймер, имеющий алкиновую функциональную группу, факультативно где данная алкиновая функциональная группа присоединяется к 5'-концу праймера.
В одном примере данного аспекта координационная связь связывает молекулу, функционализированную алкином, с поверхностью минеральной частицы сульфида меди(I).
Следует понимать, что любые характеристики данного аспекта каталитически активного вещества могут быть объединены друг с другом любым желательным способом и/или в любой конфигурации.
В другом аспекте способ включает проведение реакции минерала на основе сульфида меди(I) с молекулой, функционализированной алкином, с образованием каталитически активного вещества; и проведение реакции указанного каталитически активного вещества с молекулой, функционализированной азидом, для связывания каталитически активного вещества с молекулой, функционализированной азидом. В другом аспекте способ получения триазола включает проведение реакции молекулы, функционализированной алкином, с молекулой, функционализированной азидом, в присутствии минерала на основе сульфида меди(I).
В одном примере данного аспекта способ дополнительно включает отфильтровывание непрореагировавшего минерала на основе сульфида меди(I) от каталитически активного вещества перед проведением реакции каталитически активного вещества с молекулой, функционализированной азидом.
В одном примере данного аспекта перед проведением реакции минерала на основе сульфида меди(I) с молекулой, функционализированной алкином, указанный способ дополнительно включает добавление стехиометрического избытка минерала на основе сульфида меди(I) по отношению к молекуле, функционализированной алкином, к молекуле, функционализированной алкином.
В одном примере данного аспекта сульфид меди(I) имеет средний размер частиц, составляющий от примерно 500 нм до примерно 45 мкм.
В одном примере данного аспекта проведение реакции минерала на основе сульфида меди(I) с молекулой, функционализированной алкином, включает образование смеси минерала на основе сульфида меди(I), молекулы, функционализированной алкином, и растворителя, вещества, состоящего из молекул, функционализированных алкином, и поддержание данной смеси при температуре, которая выше точки замерзания растворителя и ниже точки кипения растворителя в течение периода времени вплоть до примерно 50 суток. В данном примере растворитель выбран из группы, состоящей из воды, натрий-карбонатного буфера, калий-фосфатного буфера и диметилсульфоксида; и рН данной смеси составляет от примерно 4 до примерно 12. Также в данном примере поддержание включает нагревание смеси до температуры, составляющей от примерно 30°С до примерно 60°С в течение периода времени, составляющего от примерно 30 минут до примерно 90 минут.
В одном примере данного аспекта перед проведением реакции молекулы, функционализированной алкином, или каталитически активного вещества с молекулой, функционализированной азидом, указанный способ дополнительно включает образование слоя из молекул, функционализированных азидом, на поверхности субстрата проточной ячейки, и где проводится реакция молекулы, функционализированной алкином, или каталитически активного вещества со слоем из молекул, функционализированных азидом, на поверхности субстрата проточной ячейки. В данном примере молекула, функционализированная алкином, или каталитически активное вещество присутствует в жидкой смеси, и при этом обеспечивают протекание указанной жидкой смеси по слою молекул, функционализированных азидом, на поверхности субстрата проточной ячейки. Также в данном примере, перед образованием слоя данный способ может дополнительно включать присоединение силана или производного силана к поверхности субстрата с образованием силанизированной поверхности.
В одном примере данного аспекта данный способ проводится без координации лиганда и без воздействия восстановителя.
Следует понимать, что любые характеристики этого аспекта данного способа могут быть объединены друг с другом любым желательным способом. Кроме того, следует понимать то, что любая комбинация характеристик этого аспекта данного способа и/или аспекта каталитически активного вещества может использоваться совместно, и/или что любые характеристики из одного из двух или обоих данных аспектов могут быть объединены с любым из примеров, раскрытых в данном документе.
В еще одном аспекте смесь для прививки содержит праймер, включающий алкиновую функциональную группу; растворитель; и минерал на основе сульфида меди(I).
В одном примере данного аспекта предусмотрена реакция алкиновой функциональной группы с поверхностью минерала на основе сульфида меди(I) с образованием в смеси для прививки каталитически активного вещества.
В одном примере данного аспекта смесь для прививки дополнительно содержит молекулу, функционализированную азидом, при этом предусмотрена реакция молекулы, функционализированной азидом, с молекулой, функционализированной алкином, что опосредуется минералом на основе сульфида меди(I). В одном примере молекула, функционализированная азидом, представляет собой полимер. В одном примере данный полимер находится на поверхности субстрата, факультативно, где субстрат представляет собой проточную ячейку.
В одном примере данного аспекта смесь для прививки включает стехиометрический избыток минерала на основе сульфида меди(I) по отношению к праймеру.
В одном примере данного аспекта смесь для прививки включает от примерно 1 мкМ до примерно 20 мкМ праймера; и от примерно 0,1 М до примерно 3 М минерала на основе сульфида меди(I).
В одном примере данного аспекта минерал на основе сульфида меди(I) выбран из группы, состоящей из халькозина, джарлеита и дигенита, и имеет средний размер частиц, составляющий от примерно 500 нм до примерно 45 мкм.
Следует понимать, что любые характеристики этого аспекта данной смеси для прививки могут быть объединены друг с другом любым желательным способом. Кроме того, следует понимать то, что любая комбинация характеристик либо из смеси для прививки и/или из спосба и/или из каталитически активного вещества может использоваться совместно, и/или что любые характеристики из любого или всех данных аспектов могут быть объединены с любыми характеристиками из примеров, раскрытых в данном документе.
В еще одном аспекте способ прививки праймера к поверхности проточной ячейки включает проведение реакции праймера, функционализированного алкином, в присутствии минерала на основе сульфида меди(I) с молекулой, функционализированной азидом, на поверхности проточной ячейки.
В одном примере данного аспекта минерал на основе сульфида меди(I) реагирует с праймером, функционализированным алкином, с образованием каталитически активного вещества, и данное каталитически активное вещество реагирует с молекулой, функционализированной азидом, со связыванием каталитически активного вещества с молекулой, функционализированной азидом, на поверхности проточной ячейки. В некоторых примерах перед проведением реакции минерала на основе сульфида меди(I) с праймером, функционализированным алкином, данный способ дополнительно включает добавление стехиометрического избытка минерала на основе сульфида меди(I) по отношению к праймеру, функционализированному алкином, к праймеру, функционализированному алкином. В некоторых примерах проведение реакции минерала на основе сульфида меди(I) с праймером, функционализированным алкином, включает образование смеси минерала на основе сульфида меди(I), праймера, функционализированного алкином, и растворителя праймера, функционализированного алкином, и поддержание данной смеси при температуре, которая выше точки замерзания растворителя и ниже точки кипения растворителя, в течение периода времени вплоть до примерно 50 суток. В некоторых из данных примеров растворитель выбран из группы, состоящей из воды, натрий-карбонатного буфера, калий-фосфатного буфера и диметилсульфоксида, и рН данной смеси составляет от примерно 4 до примерно 12. Также в некоторых из этих примеров поддержание включает нагревание смеси до температуры, составляющей от примерно 30°С до примерно 60°С в течение периода времени, составляющего от примерно 30 минут до примерно 90 минут.
В одном примере этого другого аспекта перед проведением реакции каталитически активного вещества с молекулой, функционализированной азидом, на поверхности проточной ячейки данный способ дополнительно включает образование слоя из молекул, функционализированных азидом, на поверхности проточной ячейки, и где каталитически активное вещество подвергается реакции со слоем из молекул, функционализированных азидом, на поверхности проточной ячейки. В данном примере каталитически активное вещество присутствует в жидкой смеси, и при этом обеспечивают протекание указанной жидкой смеси по слою молекул, функционализированных азидом, на поверхности проточной ячейки. В некоторых из данных примеров перед образованием слоя данный способ дополнительно включает присоединение силана или производного силана к поверхности проточной ячейки с образованием силанизированной поверхности. Также в некоторых из данных примеров слой из молекул, функционализированных азидом, представляет собой слой поли(N(5-азидоацетамидилпентил)акриламид-со-акриламида).
Пример этого другого аспекта дополнительно включает отфильтровывание непрореагировавшего минерала на основе сульфида меди(I) от каталитически активного вещества перед осуществлением реакции указанного каталитически активного вещества с молекулой, функционализированной азидом, на поверхности проточной ячейки.
Следует понимать то, что любые характеристики этого аспекта данного способа могут быть объединены друг с другом любым желательным образом. Кроме того, следует понимать то, что любая комбинация характеристик из данного способа и/или смеси для прививки, и/или другого способа, и/или из каталитически активного вещества может использоваться совместно, и/или, что любые характеристики из любого или всех данных аспектов могут быть объединены с любыми характеристиками примеров, раскрытых в данном документе.
КРАТКОЕ ОПИСАНИЕ ГРАФИЧЕСКИХ МАТЕРИАЛОВ
Характеристики примеров настоящего раскрытия станут очевидными посредством ссылки на следующее подробное описание и графические материалы, в которых подобные номера позиций соответствуют аналогичным, хотя, возможно, и не идентичным компонентам. Ради краткости, номера позиций или характеристики, имеющие описанную ранее функцию, могут быть или могут не быть описаны в связи с другими графическими материалами, на которых они появляются.
Фиг. 1 представляет собой структурную диаграмму, иллюстрирующую пример способа, раскрытого в данном документе;
Фиг. 2А-2Е представляют собой схематичные виды поперечных срезов, иллюстрирующие пример добавления поверхностной химии к структурированному субстрату с использованием первого примера смеси для прививки и Фиг. 2А, 2В и 2Е представляют собой схематичные виды поперечных срезов, иллюстрирующие пример добавления поверхностной химии к структурированному субстрату с использованием второго примера смеси для прививки;
Фиг. 3A-3D представляют собой схематичные виды поперечных срезов, иллюстрирующие пример добавления поверхностной химии к неструктурированному субстрату с использованием первого примера смеси для прививки, и Фиг. 3А, 3В и 3D представляют собой схематичные виды поперечных срезов, иллюстрирующие пример добавления поверхностной химии к неструктурированному субстрату с использованием второго примера смеси для прививки;
Фиг. 4 представляет собой график интенсивности флуоресценции (относительные единицы интенсивности, RFU) после анализа доступности поверхностного праймера (анализ CFR) для типичной проточной ячейки и сравнительных проточных ячеек;
Фиг. 5 представляет собой график интенсивности флуоресценции (относительные единицы интенсивности, RFU) после анализа доступности поверхностного праймера (анализ CFR) для разных типичных проточных ячеек, образованных из каталитически активных веществ, которые инкубировали в течение разных периодов времени; и
Фиг. 6А-6С представляют собой графики, показывающие результаты динамического рассеяния света для разных смесей, причем данные результаты иллюстрируют то, что смесь для прививки, раскрытая в данном документе, образует каталитически активные вещества.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Примеры способа, раскрытого в данном документе, включают образование каталитически активного вещества, которое содержит медь (Cu) в состоянии ее окисления +1. Минералы на основе сульфида меди(I) представляют собой моносульфиды меди, где 1,6≤Cu/S≤2. Примерами минералов на основе сульфида меди(I) являются халькозин (Cu2S) или джарлеит (Cu31S16), или дигенит (Cu9S5). В некоторых аспектах каталитически активное вещество образуется с использованием минерального сульфида меди(I), который функционирует как источник активных соединений меди (Cu+). В примерах, раскрытых в данном документе, минерал на основе сульфида меди(I) подвергается реакции с молекулой, функционализированной алкином, и молекулой, функционализированной азидом, с образованием триазола. В некоторых аспектах сульфид меди(I) реагирует с молекулой, функционализированной алкином, с образованием каталитически активного вещества, которое включает минеральную частицу сульфида меди(I) и молекулу, функционализированную алкином, непосредственно связанную с поверхностью минеральной частицы сульфида меди(I). Обнаружили то, что данная реакция может проводиться без координации соединений Cu2+ со стабилизирующим лигандом (например, для избегания осаждения) и без подвергания стабилизированных соединений Cu2+ воздействию восстановителя (например, аскорбата), с получением каталитически активных соединений меди. Избегание применения дополнительных реактивов для координации лиганда и восстановления Cu2+ является желательным, так как данные дополнительные реактивы могут увеличивать сложность и стоимость реакции, могут приводить к нежелательным побочным реакциям и могут включать нежелательные или токсичные реактивы. Без координации лиганда и восстановления типичный способ, раскрытый в данном документе, представляет собой упрощенный способ, который не включает дополнительные реактивы, помимо минерального сульфида меди(I) и молекулы, функционализированной алкином.
Кроме того, обнаружили, что гетерогенная реакция молекулы, функционализированной алкином, на поверхности минерала на основе сульфида меди(I) происходит в отсутствие света (т.е. не управляется светом), что отличается от квантовых точек Cu2S, стабилизированных полимером.
Кроме того, в некоторых примерах способа, раскрытого в данном документе, молекула, функционализированная алкином, представляет собой праймер, включающий алкиновую функциональную группу. В данных примерах каталитически активное вещество может использоваться в катализируемой медью(I) реакции цикпоприсоединения азид-алкин для связывания алкиновой функциональной группы праймера с молекулой, функционализированной азидом. Данная реакция цикпоприсоединения может происходить в присутствии водной среды и в присутствии кислорода без диспропорционирования активных соединений меди до Cu0 и Cu2+, отчасти из-за того, что активные соединения меди координируются в каталитически активном веществе с праймером и с серой.
Удаление медного катализатора оказалось сложным в других реакциях цикпоприсоединения азид-алкин, отчасти из-за тенденции активных соединений меди к диспропорционированию до Cu0 и Cu2+. Методики удаления, которые часто используются, включают ионообменные и жидкость-жидкостные методики экстракции. Другие методики для облегчения удаления медного катализатора включали включение в катализатор фторной метки, где фторная метка облегчает удаление меченого катализатора посредством методик твердофазной экстракции. В отличие от данных методик, которые включают сложные приборы и/или дополнительные вещества для облегчения удаления медного катализатора, некоторые примеры способа, раскрытого в данном документе, включают простые способы, такие как центрифугирование или фильтрование, для удаления непрореагировавшего минерального сульфида меди(I). Данные простые методики можно использовать, так как, в некоторых примерах, одна смесь для прививки (именуемая в данном документе как второй пример смеси для прививки) включает растворенный продукт реакции азид-алкин и нерастворенный, непрореагировавший минерал на основе сульфида меди(I), последний из которых может быть отделен центрифугированием или фильтрованием.
Следует понимать, что термины, использованные в данном документе, будут принимать их обычное в релевантной области значение, если не определено иначе. Несколько терминов, использованных в данном документе, и их значений излагаются ниже.
Формы единственного числа включают объекты ссылки во множественном числе, если контекст ясно не диктует иное.
Термины содержащий, включающий, вмещающий и разные формы данных терминов являются синонимичными друг другу, и подразумевается то, что они являются равным образом широкими.
Термины верхняя часть, дно, нижний, верхний, на и т.д. используются в данном документе для описания проточной ячейки и/или разных компонентов данной проточной ячейки. Следует понимать то, что подразумевается, что данные термины направления не подразумевают специфическую ориентацию, но используются для обозначения относительной ориентации между компонентами. Применение терминов направления не должно интерпретироваться как ограничивающее примеры, раскрытые в данном документе, какой(кими)-либо специфической(кими) ориентацией(ями).
Термин «алкил» в том виде, в котором он используется в данном документе, относится к прямой или разветвленной углеводородной цепи, которая является полностью насыщенной (т.е. не содержит двойных или тройных связей). Алкильная группа может иметь от 1 до 20 атомов углерода. Типичные алкильные группы включают метильную, этильную, пропильную, изопропильную, бутильную, изобутильную, третичную бутильную, пентильную, гексильную и тому подобные. В качестве примера обозначение «С1-4 алкил»указывает то, что в алкильной цепи имеется от одного до четырех атомов углерода, т.е. алкильная цепь выбирается из группы, состоящей из метила, этила, пропила, изо-пропила, н-бутила, изобутила, втор-бутила и трет-бутила.
Термин «алкенил» в том виде, в котором он используется в данном документе, относится к прямой или разветвленной углеводородной цепи, содержащей одну или более чем одну двойную связь. Алкенильная группа может иметь от 2 до 20 атомов углерода. Типичные алкенильные группы включают этенильную, пропенильную, бутенильную, пентенильную, гексенильную и тому подобные.
Термин «алкин» или «алкинил» в том виде, в котором он используется в данном документе, относится к прямой или разветвленной углеводородной цепи, содержащей одну или более чем одну тройную связь. Алкинильная группа может иметь от 2 до 20 атомов углерода. Молекула, функционализированная алкином, представляет собой любую молекулу, включающую алкиновую функциональную группу.
Термин «арил» в том виде, в котором он используется в данном документе, относится к ароматическому кольцу или кольцевой системе (т.е. два или более чем два конденсированных кольца, которые имеют два общих смежных атома углерода), содержащих только углерод в остове кольца. Когда арил представляет собой кольцевую систему, каждое кольцо в системе является ароматическим. Данная арильная группа может иметь от 6 до 18 атомов углерода. Примеры арильных групп включают фенильную, нафтильную, азуленильную и антраценильную.
Термин «присоединенный» в том виде, в котором он используется в данном документе, относится к состоянию двух предметов, которые присоединяются, пристегиваются, прилипают, соединяются или связываются друг с другом. Например, нуклеиновая кислота может быть присоединена к полимеру ковалентной или нековалентной связью. Ковалентная связь характеризуется обобщением пар электронов между атомами. В одном примере ковалентная связь может представлять собой координационную связь между сульфидом меди(I) и молекулой, функционализированной алкином. Нековалентная связь представляет собой физическую связь, которая не включает обобщение пар электронов, и она может включать, например, водородные связи, ионные связи, вандерваальсовы силы, гидрофильные взаимодействия и гидрофобные взаимодействия.
Термин «азид» или «азидо» функциональная группа относится к -N3. Молекула, функционализированная азидом, представляет собой любую молекулу, включающую азидную функциональную группу.
Термин «область связывания» в том виде, в котором он используется в данном документе, относится к области на подложке или субстрате, которая подлежит связыванию другим веществом, которое может представлять собой, в качестве примеров, слой спейсера, крышку, другой субстрат и т.д. или их комбинации (например, слой спейсера и крышку). Связь, которая образуется в области связывания, может представлять собой химическую связь (как описано выше) или механическую связь (например, с использованием застежки и т.д.).
Термин «карбоциклил» в том виде, в котором он используется в данном документе, означает неароматическое циклическое кольцо или кольцевую систему, содержащую только атомы углерода в остове кольцевой системы. Когда карбоциклил представляет собой кольцевую систему, два или более чем два кольца могут быть связаны друг с другом конденсированным, мостиковым или спиросоединенным способом. Карбоцикпилы могут иметь любую степень насыщения, при условии, что по меньшей мере одно кольцо в кольцевой системе не является ароматическим. Таким образом, карбоцикпилы включают циклоалкилы, циклоалкенилы и цикпоалкинилы. Карбоциклильная группа может иметь от 3 до 20 атомов углерода. Примеры карбоциклильных колец включают циклопропильное, циклобутильное, циклопентильное, циклогексильное, циклогексенильное, 2,3-дигидроинденовое, бицикло[2.2.2]октанильное, адамантильное и спиро[4.4]нонанильное.
Термин «цикпоалкилен» в том виде, в котором он используется в данном документе, означает полностью насыщенное карбоциклильное кольцо или кольцевую систему, которая присоединяется к остальной молекуле через две точки присоединения.
Термин «циклоалкенил» или «циклоалкен» в том виде, в котором он используется в данном документе, означает карбоциклильное кольцо или кольцевую систему, имеющую по меньшей мере одну двойную связь, где ни одно кольцо в кольцевой системе не является ароматическим. Примеры включают циклогексенил или циклогексен и норборненил или норборнен. Также термины «гетероциклоалкенил» или «гетероциклоалкен» в том виде, в котором они используются в данном документе, означают карбоциклильное кольцо или кольцевую систему с по меньшей мере одним гетероатомом в остове кольца, имеющее по меньшей мере одну двойную связь, где ни одно кольцо в кольцевой системе не является ароматическим.
Термин «циклоалкинил» или «цикпоалкин» в том виде, в котором он используется в данном документе, означает карбоциклильное кольцо или кольцевую систему, имеющую по меньшей мере одну тройную связь, где ни одно кольцо в кольцевой системе не является ароматическим. Примером является циклооктин. Другим примером является бициклононин. Также термин «гетероциклоалкинил» или «гетероцикпоалкин» в том виде, в котором он используется в данном документе, означает карбоциклильное кольцо или кольцевую систему с по меньшей мере одним гетероатомом в остове кольца, имеющую по меньшей мере одну тройную связь, где ни одно кольцо в кольцевой системе не является ароматическим.
Термин «нанесение» в том виде, в котором он используется в данном документе, относится к любой подходящей методике нанесения, которое может осуществляться вручную или автоматически и приводит к модификации свойств поверхности. В общем, нанесение может осуществляться с использованием методик нанесения осаждением из паровой фазы, методик покрытия, методик прививки или тому подобных. Такие конкретные примеры включают химическое осаждение из паровой фазы (CVD), покрытие распылением (например, ультразвуковое покрытие распылением), нанесение способом центрифугирования, покрытие окунанием или погружением, покрытие, наносимое ножевым устройством, нанесение в ванночке, проточное покрытие, аэрозольную печать, струйную печать или тому подобные.
Термин «впадина» в том виде, в котором он используется в данном документе, относится к дискретному вогнутому элементу в структурированном субстрате, имеющему отверстие на поверхности, которое полностью окружается промежуточной(ными) областью(тями) поверхности структурированного субстрата. Впадины могут иметь любую из целого ряда форм в их отверстии в поверхности, включая, в качестве примеров, круглую, эллиптическую, квадратную, полигональную, звездчатую (с любым числом вершин) и т.д. Поперечный срез впадины, взятый ортогонально относительно поверхности, может быть искривленным, квадратным, полигональным, гиперболическим, коническим, угловым и т.д. В качестве примера, впадина может представлять собой лунку. Термин «функционализированная впадина» в том виде, в котором он используется в данном документе, относится к дискретному вогнутому элементу, где присоединяются полимер и праймер(ры).
Подразумевается то, что термин «каждый», при использовании в связи с набором элементов, идентифицирует индивидуальный элемент в наборе, но не обязательно относится к каждому элементу в наборе. Исключения могут встречаться, если прямое раскрытие или контекст явно диктуют иное.
Подразумевается то, что термин «проточная ячейка» в том виде, в котором он используется в данном документе, означает сосуд, имеющий камеру (т.е. проточный канал), где может проводиться реакция, входное отверстие для доставки реактива(вов) в камеру и выходное отверстие для удаления реактива(вов) из камеры. В некоторых примерах данная камера обеспечивает выявление реакции, которая происходит в камере. Например, данная камера может включать одну или более чем одну прозрачную поверхность, обеспечивающую оптическое выявление чипов, оптически меченых молекул или тому подобного в камере.
Термин «проточный канал» в том виде, в котором он используется в данном документе, может представлять собой область, определенную между двумя связанными компонентами, которая может селективно получать жидкий образец. В некоторых примерах проточный канал может быть определен между структурированным субстратом и крышкой, и, таким образом, может находиться в жидкостной связи с одной или более чем одной впадиной, определенной в структурированном субстрате. В других примерах проточный канал может быть определен между неструктурированным субстратом и крышкой.
Термин «функционализированный слой» относится к слою, включающему молекулу, функционализированную азидом, имеющую связанную с ней молекулу, функционализированную алкином.
Термин «смесь для прививки» в том виде, в котором он используется в данном документе, относится к смеси или раствору, включающему компоненты поверхностной химии. Первый пример смеси для прививки, раскрытый в данном документе, включает сульфид меди(I) и молекулу, функционализированную алкином, и/или продукт реакции сульфида меди(I) и молекулы, функционализированной алкином (который именуется в данном документе как каталитически активное вещество). Этот первый пример смеси для прививки также может включать растворитель. Как описано в данном документе далее, первый пример смеси для прививки можно использовать для введения молекулы, функционализированной алкином, в уже образованный слой из молекул, функционализированных азидом. Второй пример смеси для прививки, раскрытый в данном документе, включает сульфид меди(I), молекулу, функционализированную алкином, и молекулу, функционализированную азидом, и/или каталитически активное вещество, и/или продукт реакции каталитически активного вещества и молекулы, функционализированной азидом. Данный второй пример смеси для прививки также может включать растворитель. Как описано в данном документе далее, второй пример смеси для прививки можно использовать для введения функционализированного слоя на субстрат проточной ячейки.
Термин «гетероарил» в том виде, в котором он используется в данном документе, относится к ароматическому кольцу или кольцевой системе (т.е. двум или более чем двум конденсированным кольцам, которые имеют два общих смежных атома), которая(рые) содержит(жат) один или более чем один гетероатом, то есть, элемент, отличный от углерода, включающий азот, кислород и серу в остове кольца, но не ограничиваясь ими. Когда гетероарил представляет собой кольцевую систему, каждое кольцо в данной системе является ароматическим. Данная гетероарильная группа может иметь 5-18 членов кольца.
Термин «гетероциклил» в том виде, в котором он используется в данном документе, означает неароматическое циклическое кольцо или кольцевую систему, содержащую по меньшей мере один гетероатом в остове кольца. Гетероциклилы могут соединяться друг с другом конденсированным, мостиковым или спиро-соединенным способом. Гетероциклилы могут иметь любую степень насыщенности, при условии, что по меньшей мере одно кольцо в кольцевой системе не является ароматическим. В данной кольцевой системе гетероатом(мы) может(гут) присутствовать либо в неароматическом, либо в ароматическом кольце. Гетероциклильная группа может иметь от 3 до 20 элементов кольца (т.е. число атомов, составляющих остов кольца, включающих атомы углерода и гетероатомы). В некоторых примерах гетероатом(мы) представляет(ют) собой О, N или S.
Термин «гидрокси» или «гидроксил» в том виде, в котором он используется в данном документе, относится к группе -ОН.
Термин «промежуточная область» в том виде, в котором он используется в данном документе, относится к области в субстрате или на поверхности, которая разделяет впадины. Например, промежуточная область может отделять один элемент чипа от другого элемента чипа. Два элемента, которые отделяются друг от друга, могут быть дискретными, т.е. не имеющими физического контакта друг с другом. В другом примере промежуточная область может отделять первую часть элемента от второй части элемента. Во многих примерах промежуточная область является непрерывной, тогда как элементы являются дискретными, например, как в случае целого ряда лунок, определенным на непрерывной в иных отношениях поверхности. Разделение, обеспечиваемое промежуточной областью, может быть частичным или полным разделением. Промежуточные области могут иметь поверхностное вещество, которое отличается от поверхностного вещества элементов, определенных в данной поверхности. Например, элементы чипа могут иметь количество или концентрацию покрывающего слоя и праймера(ров), которые превышают количество или концентрацию, присутствующие в промежуточных областях. В некоторых примерах покрывающий слой и праймер(ры) могут не присутствовать в промежуточных областях.
Термин «нуклеотид» в том виде, в котором он используется в данном документе, включает азотсодержащее гетероциклическое основание, сахар и одну или более чем одну фосфатную группу. Нуклеотиды представляют собой мономерные звенья последовательности нуклеиновой кислоты. В РНК сахар представляет собой рибозу, а в ДНК сахар представляет собой дезоксирибозу, т.е. сахар, не имеющий гидроксильной группы, которая присутствует в 2'-положении в рибозе. Азотсодержащее гетероциклическое основание (т.е. нуклеиновое основание) может представлять собой пуриновое основание или пиримидиновое основание. Пуриновые основания включают аденин (А) и гуанин (G), и их модифицированные производные или аналоги. Пиримидиновые основания включают цитозин (С), тимин (Т) и урацил (U), и их модифицированные производные или аналоги. Атом С-1 дезоксирибозы связывается с N-1 пиримидина или N-9 пурина.
Термин «субстрат проточной ячейки» или «субстрат» относится к подложке, на которую можно добавлять поверхностную химию. Термин «структурированный субстрат» относится к подложке, в которой или на которой определяются впадины. Термин «неструктурированный субстрат» относится к по существу плоской подложке. Данный субстрат может представлять собой кристаллическую пластину, панель, прямоугольный лист, штампованную плиту или иметь любую другую подходящую конфигурацию. Данный субстрат обычно является твердым и нерастворимым в водной жидкости. Данный субстрат может быть инертным в отношении химии, которая используется для модификации впадин. Например, субстрат может быть инертным в отношении химии, используемой для образования полимерного слоя, для присоединения праймера(ров) к полимерному слою и т.д. Примеры подходящих субстратов включают эпоксисилоксан, стекло и модифицированное или функционализированное стекло, пластмассы (включающие акрилы, полистирол и сополимеры стирола и других веществ, полипропилен, полиэтилен, полибутилен, полиуретаны, политетрафторэтилен (такой как TEFLON® от Chemours), циклические олефины/цикпо-олефиновые полимеры (СОР) (такие как ZEONOR® от Zeon), полиимиды и т.д.), нейлон, керамику/оксидную керамику, диоксид кремния, аморфный кварц или вещества на основе диоксида кремния, силикат алюминия, кремний и модифицированный кремний (например, р+ кремний с присадкой бора), нитрид кремния (Si3N4), оксид кремния (SiO2), пентоксид тантала (TaO5) или другой(гие) оксид(ды) тантала (ТаОх), оксид гафния (HaO2), углерод, металлы, виды неорганического стекла или тому подобные. Данный субстрат также может представлять собой стекло или диоксид кремния с покрывающим слоем оксида тантала или другой оксидной керамикой на поверхности.
Термин «плазменное травление» в том виде, в котором он используется в данном документе, относится к процессу удаления органического вещества из субстрата посредством кислородной плазмы. Продукты, которые возникают в результате плазменного травления, могут быть удалены вакуумным насосом/системой. Плазменное травление может активировать субстрат посредством введения реакционноспособных гидроксильных групп.
Подразумевается, что термин «полимерный слой», на который дается ссылка в данном документе, означает полутвердый материал, который является проницаемым для жидкостей и газов. Данный полимерный слой может представлять собой гидрогель, который может набухать при поглощении жидкости, и который может сокращаться при удалении жидкости посредством сушки. В примерах, раскрытых в данном документе, полимерный слой может включать молекулу, функционализированную азидом, которая может реагировать с алкиновой функциональной группой. В одном примере молекула, функционализированная азидом, и полимерный слой представляют собой поли(N(5-азидоацетамидилпентил)акриламид-со-акриламид) (PAZAM).
Термин «праймер» в том виде, в котором он используется в данном документе, определяется как последовательность одноцепочечной нуклеиновой кислоты (например, одноцепочечной ДНК или одноцепочечной РНК), которая служит в качестве исходной точки для синтеза ДНК или РНК. 5'-Конец праймера может быть модифицирован для обеспечения реакции связывания с молекулой, функционализированной азидом. Длиной данного праймера может быть любое число оснований, и он может включать целый ряд неприродных нуклеотидов. В одном примере праймер для секвенирования представляет собой короткую нить, составляющую от 20 до 40 оснований.
Термины «силан» и «производное силана» в том виде, в котором они используются в данном документе, относятся к органическому или неорганическому соединению, содержащему один или более чем один атом кремния. Примером неорганического силанового соединения является SiH4 или галогенированный SiH4, где атом водорода заменяется одним или более чем одним атомом галогена. Примером органического силанового соединения является X-RB-Si(ORC)3, в котором X представляет собой негидролизуемую органическую группу, такую как амино, винил, метакрилат, эпокси (


В некоторых примерах силан или производное силана включает ненасыщенную группировку, которая способна взаимодействовать с функциональной группой молекулы, функционализированной азидом. Термин «ненасыщенная группировка» в том виде, в котором он используется в данном документе, относится к химической группе, которая включает циклоалкены, циклоалкины, гетероциклоалкены, гетероциклоалкины или их факультативно замещенные варианты, включающие по меньшей мере одну двойную связь или одну тройную связь. Данные ненасыщенные группировки могут быть одновалентными или двухвалентными. Когда ненасыщенная группировка является одновалентной, термины «циклоалкен», «циклоалкин», «гетероциклоалкен» и «гетероциклоалкин» используются взаимозаменяемо с терминами «циклоалкенилы», «циклоалкинилы», «гетероциклоалкенилы» и «гетероциклоалкинилы» соответственно. Когда ненасыщенная группировка является двухвалентной, термины «циклоалкен», «циклоалкин», «гетероциклоалкен» и «гетероциклоалкин» используются взаимозаменяемо с терминами «цикпоалкенилен», «цикпоалкинилен», «гетероциклоалкенилен» и «гетероциклоалкинилен» соответственно.
Ненасыщенная группировка может быть ковалентно присоединена либо непосредственно к атомам кремния силана или производного силана, либо опосредованно присоединена через линкеры. Примеры подходящих линкеров включают факультативно замещенные алкилены (т.е. двухвалентные насыщенные алифатические радикалы (такие как этилен), рассматриваемые как происходящие из алкена посредством открытия двойной связи или из алкана посредством удаления двух атомов водорода от разных атомов углерода), замещенные полиэтиленгликоли или тому подобные.
Термин «спейсерный слой» в том виде, в котором он используется в данном документе, относится к веществу, которое связывает два компонента друг с другом. В некоторых примерах спейсерный слой может представлять собой вещество, поглощающее излучение, которое помогает связыванию, или он может быть приведен в контакт с веществом, поглощающим излучение, которое помогает связыванию.
Термин «поверхностная химия» в том виде, в котором он используется в данном документе, относится к химически и/или биологически активному(ным) компоненту(там), которые включаются в камеру проточной ячейки. Примеры поверхностной химии, раскрытой в данном документе, включают праймер, который может быть частью каталитически активного вещества, и который может присоединяться к молекуле, функционализированной азидом. В силу этого один пример поверхностной химии представляет собой функционализированный слой.
Пример способа 100 показан на Фиг. 1. Способ 100 включает проведение реакции минерала на основе сульфида меди(I) с молекулой, функционализированной алкином, с образованием каталитически активного вещества (как показано в номере позиции 102), и проведение реакции каталитически активного вещества с молекулой, функционализированной азидом, для связывания каталитически активного вещества с молекулой, функционализированной азидом (как показано в номере позиции 104).
Как упомянуто ранее, минерал на основе сульфида меди(I) может представлять собой любой минерал на основе сульфида меди(I), такой как халькозин (Cu2S) или джарлеит (Cu31S16), или дигенит (Cu9S5). Формой данного минерала является встречающаяся в природе форма минерала на основе сульфида меди(I). Минерал на основе сульфида меди(I), как таковой, не стабилизируется поверхностным полимером или другим стабилизирующим соединением, не подвергается обработкам поверхности и т.д. Минерал на основе сульфида меди(I) может иметь любой подходящий размер частиц. В одном примере минерал на основе сульфида меди(I) имеет средний размер частиц, меньший или равный 45 мкм. В другом примере минерал на основе сульфида меди(I) имеет средний размер частиц, составляющий от примерно 500 нм до примерно 45 мкм. В еще одном другом примере минерал на основе сульфида меди(I) имеет средний размер частиц, составляющий от примерно 1 мкм до примерно 40 мкм. В то время как было предложено несколько примеров, средний размер частиц минерала на основе сульфида меди(I) может быть больше или меньше.
В примерах, раскрытых в данном документе, можно использовать любую молекулу, функционализированную алкином. В одном примере молекула, функционализированная алкином, представляет собой праймер, такой как праймер для секвенирования, который включает алкиновую функциональную группу. Данный праймер может представлять собой любой прямой амплификационный праймер или обратный амплификационный праймер, который включает алкиновую функциональную группу. Конкретные примеры подходящих праймеров включают праймеры Р5 и/или Р7, которые используются на поверхности коммерческих проточных ячеек, продаваемых Illumina inc. для секвенирования на HISEQ™, HISEQX™, MiSEQ™, MiSEQX™, NEXTSEQ™, NOVASEQ™, GENOME ANALYZER™ и других приборных платформах.
Для образования каталитически активного вещества минерал на основе сульфида меди(I) и молекулу, функционализированную алкином, объединяют друг с другом и инкубируют в течение периода времени, обеспечивающего взаимодействие компонентов. Данные компоненты можно объединять в любом растворителе, в котором является растворимой молекула, функционализированная алкином. В некоторых примерах также может быть желательным выбор растворителя, который может растворять молекулу, функционализированную алкином, так как реакция каталитически активного вещества с молекулой, функционализированной азидом, также может происходить в растворителе. В одном примере данный растворитель представляет собой полярный растворитель. Примеры подходящих полярных растворителей выбраны из группы, состоящей из воды, натрий-карбонатного буфера (NaHCO3), калий-фосфатного буфера (KH2PO4), диметилсульфоксида (DMSO), диметилформамида (DMF), ацетона, ацетонитрила, бутанола, пропанола, этанола, метанола и их смесей. Считается, что можно использовать другие растворители, и в некоторых случаях каталитически активное вещество может быть нерастворимым или может быть частично растворимым в этих других растворителях.
Пример проведения реакции минерала на основе сульфида меди(I) с молекулой, функционализированной алкином, включает образование смеси (т.е. первого примера смеси для прививки) минерала на основе сульфида меди(I), молекулы, функционализированной алкином, и растворителя молекулы, функционализированной алкином, и поддержание первого примера смеси для прививки при температуре, которая выше точки замерзания растворителя и ниже точки кипения растворителя, в течение периода времени вплоть до примерно 50 суток. В то время как данная реакция может инициироваться сразу при объединении минерала на основе сульфида меди(I) и молекулы, функционализированной алкином, период инкубации может быть продлен для того, чтобы обеспечить то, что реакция является завершенной.
рН первого примера смеси для прививки может составлять от примерно 4 до примерно 12, в зависимости, отчасти, от использованного растворителя и от того, будет ли данный растворитель присутствовать на протяжении последующей реакции каталитически активного вещества с молекулой, функционализированной азодом. Для водных растворителей для подведения рН можно использовать подходящий буфер или сильную кислоту.
В одном примере для образования первого примера смеси для прививки молекулу, функционализированной алкином, можно добавлять к растворителю с образованием раствора, и затем в данный раствор можно добавлять минерал на основе сульфида меди(I). В другом примере для образования первого примера смеси для прививки в растворитель можно добавлять молекулу, функционализированной алкином, и минерал на основе сульфида меди(I). В еще одном другом примере для образования первого примера смеси для прививки растворитель можно добавлять к минералу на основе сульфида меди(I). Например, минерал на основе сульфида меди(I) может быть упакован в колонку, и раствор молекулы, функционализированной алкином, в данном растворителе может протекать через колонку с образованием каталитически активного вещества. В любом из данных примеров может был добавлен стехиометрический избыток минерала на основе сульфида меди(I) (по отношению к концентрации в растворе молекулы, функционализированной алкином). Количество использованного минерала на основе сульфида меди(I) также может частично зависеть от среднего размера частиц минерала на основе сульфида меди(I). Меньшие частицы минерала на основе сульфида меди(I) имеют большее отношение площади поверхности к объему, чем большие частицы минерала на основе сульфида меди(I), и, таким образом, можно использовать меньшие количества меньших частиц минерала на основе сульфида меди(I) по сравнению с количествами больших частиц минерала на основе сульфида меди(I).
Первый пример смеси для прививки может включать от примерно 1 мкМ до примерно 100 мкМ молекулы, функционализированной алкином, и от примерно 0,1 М до примерно 3 М частиц минерала на основе сульфида меди(I). Можно использовать любую концентрацию молекулы, функционализированной алкином, хотя верхний предел зависит от растворимости молекулы, функционализированной алкином, в использованном растворителе. Как описано ранее, можно использовать любую концентрацию минерала на основе сульфида меди(I), при условии, что она находится в стехиометрическом избытке по отношению к концетрации молекулы, функционализированной алкином.
В качестве конкретного примера первого примера смеси для прививки праймеры Р5 и Р7 (имеющие алкиновую функциональную группу, присоединенную к ним) и стехиометрический избыток частиц Cu2S смешивают в 0,5 М или 1 М натрий-карбонатном буфере при рН примерно 10. В качестве другого конкретного примера первого примера смеси для прививки праймеры Р5 и Р7 (имеющие алкиновую функциональную группу, присоединенную к ним) и стехиометрический избыток частиц Cu2S смешивают в деионизированной воде или диметилсульфоксиде. В качестве еще одного другого конкретного примера первого примера смеси для прививки праймеры Р5 и Р7 (имеющие алкиновую функциональную группу, присоединенную к ним) и стехиометрический избыток частиц Cu2S смешивают в 50 мМ калий-фосфатном буфере при рН примерно 8.
Некоторые примеры первого примера смеси для прививки, как таковые, включают праймер, включающий алкиновую функциональную группу, растворитель праймера и минерал на основе сульфида меди(I). В некоторых примерах первый пример смеси для прививки включает стехиометрический избыток минерала на основе сульфида меди(I) по отношению к праймеру. В одном примере первый пример смеси для прививки включает от примерно 1 мкМ до примерно 20 мкМ праймера и от примерно 0,1 М до примерно 3 М минерала на основе сульфида меди(I). Поскольку реакция между алкиновой функциональной группой и минералом на основе сульфида меди(I) может происходить по существу мгновенно, первый пример смеси для прививки может включать каталитически активное вещество, помимо любых непрореагировавших праймеров (или другой молекулы, функционализированной алкином), любого непрореагировавшего минерала на основе сульфида меди(I) и растворителя.
Как только данная смесь (первый пример смеси для прививки) приготовлена, первый пример смеси для прививки поддерживается при температуре, которая выше точки замерзания растворителя и ниже точки кипения растворителя, в течение периода инкубации вплоть до примерно 50 суток. В силу этого, температура, при которой поддерживается смесь, отчасти, зависит от растворителя, используемого для реакции. Обнаружили то, что каталитически активное вещество, образовавшееся в результате реакции, является стабильным и все еще каталитически активным при инкубации в течение вплоть до примерно 50 суток. Однако следует понимать то, что период инкубации может быть дольше, если, в конце данного периода, каталитически активное вещество остается стабильным и каталитически активным. В некоторых примерах поддержание первого примера смеси для прививки включает обеспечение нахождения данной смеси в течение периода инкубации без какого-либо дополнительного нагревания. В других примерах поддержание первого примера смеси для прививки включает нагревание данной смеси до желательной температуры. Например, поддержание первого примера смеси для прививки может включать нагревание первого примера смеси для прививки до температуры, составляющей от примерно 30°С до примерно 60°С в течение периода времени, составляющего от примерно 30 минут до примерно 90 минут.
Реакция с образованием каталитически активного вещества не управляется светом и, таким образом, может проводиться в темном контейнере или печи, или может происходить при окружающем освещении. Дополнительный свет не используется для управления данной реакцией.
Данный способ может включать смешивание минерала на основе сульфида меди(I) и молекулы, функционализированной алкином, во время проведения реакции. Например, первый пример смеси для прививки может перемешиваться время от времени или непрерывно по мере инкубирования. Как упомянуто в данном документе, способ также может включать пропускание раствора молекулы, функционализированной алкином, через колонку с минералом на основе сульфида меди(I).
В первом примере смеси для прививки и во время периода инкубации сульфид меди(I) реагирует с алкиновой функциональной группой молекулы, функционализированной алкином, с образованием каталитически активного вещества. Более конкретно, алкин молекулы, функционализированной алкином, может подвергаться гетерогенной реакции на поверхности сульфида меди(I). В силу этого алкин может подвергаться химическому изменению на поверхности контакта, например, на поверхности твердого катализатора на основе сульфида меди(I). В силу этого молекула, функционализированная алкином, непосредственно связывается с поверхностью твердой минеральной частицы сульфида меди(I). Образующееся вещество может находиться в виде кластеров, которые могут быть растворимыми в растворителе, используемом в данной реакции. В данных кластерах молекула, функционализированная алкином, может координироваться с Cu+ на поверхности твердого сульфида меди(I). Одиночный кластер включает одну частицу сульфида меди(I) с одной или более чем одной координированной с ней молекулой, функционализированной алкином. Одна частица сульфида меди(I) имеет много потенциальных сайтов связывания алкина, число которых зависит от размера данной частицы. Размер кластера, который образуется, определяется размером частицы сульфида меди(I) (который может определяться, например, динамическим рассеянием света (DLS)) и размером молекулы, функционализированной алкином, которая используется. В некоторых примерах данный кластер представляет собой нанокластер, который имеет размер, составляющий от примерно 1 нм до меньше, чем 1000 нм. В других примерах данный кластер имеет размер примерно 2 мкм или меньше и, таким образом, может представлять собой микрокластер или нанокластер.
При образовании данного вещества первый пример смеси для прививки представляет собой жидкую смесь, которая может включать растворитель, каталитически активное вещество (которое может быть растворено в растворителе) и любые непрореагировавшие минеральные частицы сульфида меди(I). Первый пример смеси для прививки затем можно хранить (например, вплоть до примерно 50 суток, если период инкубации короче), использовать также, как и в реакции с полимером, функционализированным азидом, или подвергать воздействию процесса, который удаляет непрореагировавшие минеральные частицы сульфида меди(I) до их применения в реакции с полимером, функционализированным азидом. В силу этого, не будучи показанным на Фиг. 1, один пример способа 100 может включать отфильтровывание непрореагировавшего минерала на основе сульфида меди(I) от каталитически активного вещества в первом примере смеси для прививки до проведения реакции каталитически активного вещества с молекулой, содержащей азид.
Для удаления непрореагировавших минеральных частиц сульфида меди(I) первый пример смеси для прививки можно отфильтровывать или осаждать. Фильтрование может осуществляться с использованием любого подходящего фильтра, который будет удалять любые непрореагировавшие минеральные частицы сульфида меди(I) из первого примера смеси для прививки. В одном примере используется 0,2 мкм фильтр. Размер фильтра может зависеть от среднего размера частиц минерала на основе сульфида меди(I), используемого в данном способе. Осаждение может осуществляться с использованием центрифугирования и затем удаления жидкости от осажденных частиц. После фильтрования или осаждения, или некоторого другого способа для отделения непрореагировавшего минерала на основе сульфида меди(I) от остатка первого примера смеси для прививки первый пример смеси для прививки представляет собой жидкую смесь, которая может включать растворитель и каталитически активное вещество, растворенное или диспергированное в растворителе. При отфильтровывании минеральных частиц непрореагировавшего сульфида меди(I) первый пример смеси для прививки может превращаться из черного до по существу бесцветного или иметь слегка прозрачный голубой цвет.
Хранящийся или не хранящийся и отфильтрованный или неотфильтрованный первый пример смеси для прививки можно затем объединять с молекулой, функционализированной азидом, для реакции каталитически активного вещества с молекулой, функционализированной азидом, для связывания каталитически активного вещества с молекулой, функционализированной азидом.
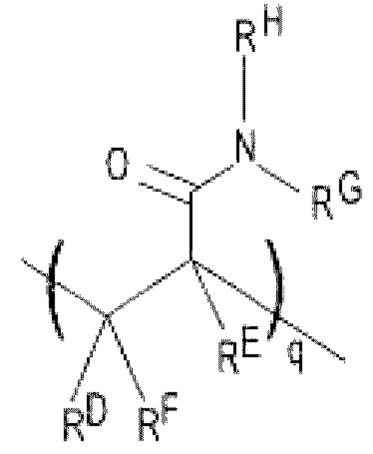
Молекула, функционализированная азидом, может представлять собой любую молекулу (например, мономер, полимер и т.д.), которая включает азидную функциональную группу для реакции с алкином каталитически активного вещества. Пример молекулы, функционализированной азидом, включает акриламидный полимер, такой как поли(N(5-азидоацетамидилпентил)акриламид-соакриламид - PAZAM. PAZAM и другие формы акриламидного сополимера обычно представлены повторяющимся звеном Формулы (I):

в которой:
RA выбран из группы, состоящей из азидо, факультативно замещенного амино, факультативно замещенного алкенила, факультативно замещенного гидразона, факультативно замещенного гидразина, карбоксила, гидрокси, факультативно замещенного тетразола, факультативно замещенного тетразина, нитрилоксида, нитрона итиола;
RB представляет собой Н или факультативно замещенный алкил;
RC, RD и RE независимо выбраны из группы, состоящей из Н и факультативно замещенного ал кила;
каждый из -(СН2)р- факультативно может быть замещенным;
р представляет собой целое число в интервале от 1 до 50;
n представляет собой целое число в интервале от 1 до 50000; и
m представляет собой целое число в интервале от 1 до 100000.
Обычный специалист в данной области поймет, что организация повторяющихся элементов «n» и «m» в Формуле (I) является репрезентативной, и мономерные субъединицы могут присутствовать в структуре полимера в любом порядке (например, в случайном, в виде блоков, упорядоченных структур или их комбинации).
Конкретные примеры PAZAM представлены:

в которой n представляет собой целое число в интервале 1-20000, и m представляет собой целое число в интервале 1-100000. Как и с Формулой (I), обычному специалисту в данной области будет известно, что субъединицы «n» и «m» представляют собой повторяющиеся элементы, которые присутствуют в случайном порядке по всей структуре полимера.
Молекулярная масса полимера Формулы (I) или PAZAM может варьировать от примерно 10 кДа до примерно 1500 кДа или в конкретном примере может составлять примерно 312 кДа.
В некоторых примерах полимер Формулы (I) или PAZAM представляет собой линейный полимер. В некоторых других примерах полимер Формулы (I) или PAZAM представляет собой слегка сшитый полимер.
В других примерах молекула, функционализированная азидом, может представлять собой вариацию Формулы (I). В одном примере акриламидное звено может быть заменено N,N-диметилакриламидом (


Следует понимать, что можно использовать другие молекулы, функционализированные азидом, при условии, что они включают азидную функциональную группу для реакции с молекулой, функционализированной алкином, например, посредством взаимодействия с каталитически активным веществом. Другие примеры подходящих молекул, функционализированных азидом, включают другие азидолизированные полиакриламидные полимеры или азидолизированную версию акриламида, не содержащего силан (SFA).
Каталитически активное вещество (из первого примера смеси для прививки) и молекулу, функционализированную азидом, можно смешивать друг с другом, и нанокпастеры сульфида меди(I) действуют как источник Cu+ для реакции циклоприсоединения азид-алкин между каталитически активным веществом и молекулой, функционализированной азидом. Данное циклоприсоединение образует азолы для связывания молекулы, функционализированной азидом, с каталитически активным веществом. В более конкретном примере данное циклоприсоединение образует азолы для связывания алкиновой группы праймера с азидной группой полимера. Как только алкин связывается с доступным поверхностным сайтом на частице сульфида меди(I), азид затем также связывается с данным поверхностным сайтом (посредством координации с Cu+), что образует переходное состояние для стадии образования связи C-N. Любой 1,2,3-триазольный продукт, который образуется, диссоциирует от частицы сульфида меди(I).
На протяжении реакции цикпоприсоединения азид-алкин может присутствовать жидкость из первого примера смеси для прививки.
В некоторых примерах способа 100, раскрытого в данном документе, реакция циклоприсоединения азид-алкин может происходить на поверхности проточной ячейки. В данных примерах молекула, функционализированная азидом, может представлять собой полимерный слой на субстрате проточной ячейки, и первый пример смеси для прививки может подвергаться воздействию данного полимерного слоя. В некоторых примерах до осуществления реакции каталитически активного вещества с молекулой, функционализированной азидом, способ 100 дополнительно включает образование слоя из молекул, функционализированных азидом, на поверхности проточной ячейки (например, на субстрате проточной ячейки), и каталитически активное вещество реагирует с данным слоем из молекул, функционализированных азидом, на поверхности проточной ячейки с образованием функционализированного слоя. Примеры данных способов будут дополнительно описаны со ссылкой на Фиг. 2А-Д и 3А-3Г.
В другом примере способа 100 используется второй пример смеси для прививки. В данном примере молекула, функционализированная алкином, может быть добавлена в растворитель с образованием раствора, и данный раствор может быть объединен с молекулой, функционализированной азидом. Затем в данный раствор, включающий молекулы, функционализированные и алкином, и азидом, может быть добавлен минерал на основе сульфида меди(I). В начале второй пример смеси для прививки включает растворитель, молекулу, функционализированную алкином, молекулу, функционализированную азидом, и минерал на основе сульфида меди(I). По мере прохождения реакции(ций), второй пример смеси для прививки может включать каталитически активное вещество, молекулу, функционализированную азидом, и любые из непрореагировавших молекулы, функционализированной алкином, и минерала на основе сульфида меди(I) или продукта реакции азид-алкин (т.е. продукта реакции каталитически активного вещества и молекулы, функционализированную азидом) и любой из других компонентов, которые не прореагировали.
Любые из веществ и/или количества/концентрации, изложенные для первого примера смеси для прививки, могут использоваться для образования второго примера смеси для прививки.
Как только приготовлен второй пример смеси для прививки, данный второй пример смеси для прививки поддерживается при температуре, которая выше точки замерзания растворителя и ниже точки кипения растворителя, в течение периода инкубации вплоть до примерно 50 суток. В силу этого, температура, при которой поддерживается данная смесь, отчасти зависит от растворителя, использованного для реакции. Обнаружили то, продукт реакции азид-алкин, образовавшийся в результате данных реакций, является стабильным и активным при инкубации в течение вплоть до примерно 50 суток. Однако следует понимать то, что период инкубации может быть дольше, если, в конце данного периода, продукт реакции азид-алкин остается стабильным и активным. В некоторых примерах поддержание второго примера смеси для прививки включает обеспечение нахождения данной смеси в течение периода инкубации без какого-либо дополнительного нагревания. В других примерах поддержание второго примера смеси для прививки включает нагревание данной смеси до желательной температуры. Например, поддержание второго примера смеси для прививки может включать нагревание второго примера смеси для прививки до температуры, составляющей от примерно 30°С до примерно 60°С в течение периода времени, составляющего от примерно 30 минут до примерно 90 минут.
Для удаления непрореагировавших минеральных частиц сульфида меди(I) второй пример смеси для прививки можно отфильтровывать или осаждать. Фильтрование может осуществляться с использованием любого подходящего фильтра, который будет удалять любые непрореагировавшие минеральные частицы сульфида меди(I) из второго примера смеси для прививки. В одном примере используется 0,2 мкм фильтр. Размер фильтра может зависеть от среднего размера частиц минерала на основе сульфида меди(I), используемого в данном способе. Осаждение может осуществляться с использованием центрифугирования и затем удаления жидкости из осажденных частиц. После фильтрования или осаждения, или некоторого другого способа для отделения непрореагировавшего минерала на основе сульфида меди(I) от остатка второго примера смеси для прививки второй пример смеси для прививки представляет собой жидкую смесь, которая может включать растворитель и продукт реакции азид-алкин, растворенный или диспергированный в растворителе.
В некоторых других примерах способа 100, раскрытого в данном документе, второй пример смеси для прививки можно использовать для образования функционализированного слоя на субстрате проточной ячейки или на поверхности подложки. В данных примерах второй пример смеси для прививки можно наносить на субстрат проточной ячейки/поверхность подложки, и функциональная группа продукта реакции азид-алкин может взаимодействовать с функциональной(ными) группой(ами) на поверхности проточной ячейки с присоединением продукта реакции азид-алкин к поверхности с образованием функционализированного слоя. Примеры данных способов будут дополнительно описаны со ссылкой на Фиг. 2А, 2В и 2Е, и 3А, 3В и 3D.
Следует понимать то, что на поверхность структурированного субстрата или неструктурированного субстрата можно добавлять поверхностную химию (например, функционализированный слой). Добавление поверхностной химии на структурированный субстрат будет описано со ссылкой на Фиг. 2А-2Е, и добавление поверхностной химии на неструктурированный субстрат будет описано со ссылкой на Фиг. 3A-2D.
Фиг. 2А представляет собой вид поперечного среза структурированного субстрата 12. Структурированный субстрат 12 может представлять собой структурированную кристаллическую пластину или структурированную штампованную плиту, или любой другой структурированный субстрат (например, панель, прямоугольный лист и т.д.). Можно использовать любой пример субстрата 12, описанного в данном документе. Структурированную кристаллическую пластину можно использовать для образования нескольких проточных ячеек, структурированную штампованную плиту можно использовать для образования одной проточной ячейки. В одном примере данный субстрат может иметь диаметр, составляющий от примерно 2 мм до примерно 300 мм, или представлять собой прямоугольный лист или панель, имеющие их наибольшее измерение вплоть до порядка 3 метров. В одном примере субстрат - кристаллическая пластина имеет диаметр, составляющий от примерно 200 мм до примерно 300 мм. В другом примере субстрат-штампованная плита имеет ширину, составляющую от примерно 0,1 мм до примерно 10 мм. В то время как были приведены примерные измерения, следует понимать то, что можно использовать субстраты с любыми подходящими измерениями.
Структурированный субстрат 12 включат впадины 14, определенные на или в экспонированном слое, или на поверхности субстрата 12, и промежуточные области 16, разделяющие смежные впадины 14. В примерах, раскрытых в данном документе, впадины 14 становятся функционализированными с использованием поверхностной химии (например, 20, 22), тогда как промежуточные области 16 можно использовать для связывания, но они не будут иметь праймера(ров) 22 (показанного на Фиг. 2Д), присутствующего(щих) на них.
Впадины 14 могут быть изготовлены в или на субстрате 12 с использованием целого ряда методик, включая, например, фотолитографию, наноимпринтную литографию, методики штамповки, методики тиснения, методики отливки, методики микротравления, методики печати и т.д. Как будет понятно специалистам в данной области, использованная методика будет зависеть от состава и формы субстрата 12.
Может рассматриваться много разных схем впадин 14, включая регулярные, повторяющиеся и нерегулярные структуры. В одном примере впадины 14 располагаются в гексагональной сетке для плотной упаковки и улучшенной плотности. Другие схемы могут включать, например, прямолинейные (т.е. прямоугольные) схемы, треугольные схемы и так далее. В некоторых примерах схема или структура может иметь х-у формат впадин 14, которые находятся в рядах и колонках. В некоторых других примерах схема или структура может представлять собой повторяющуюся организацию впадин 14 и/или промежуточных областей 16. В других примерах схема или структура может представлять собой случайную организацию впадин 14 и/или промежуточных областей 16. Структура может включать пятна, блоки, лунки, столбики, полоски, завитки, линии, треугольники, прямоугольники, круги, дуги, клетки, шотландские клетки, диагонали, стрелки, квадраты и/или штриховки перекрестными линиями.
Схема или структура может быть охарактеризована в отношении плотности впадин 14 (т.е. числа впадин 14) в определенной области. Например, впадины 14 могут присутствовать при плотности приблизительно 2 миллиона на мм2. Данная плотность может быть настроена до разных плотностей, включая, например, плотность по меньшей мере примерно 100 на мм2, примерно 1000 на мм2, примерно 0,1 миллиона на мм2, примерно 1 миллион на мм2, примерно 2 миллиона на мм2, примерно 5 миллионов на мм2, примерно 10 миллионов на мм2, примерно 50 миллионов на мм2 или больше. Альтернативно или дополнительно, плотность может быть настроена так, чтобы составлять не более чем примерно 50 миллионов на мм2, примерно 10 миллионов на мм2, примерно 5 миллионов на мм2, примерно 2 миллиона на мм2, примерно 1 миллион на мм2, примерно 0,1 миллиона на мм2, примерно 1000 на мм2, примерно 100 на мм2 или меньше. Кроме того, следует понимать то, что плотность впадин 14 на субстрате 12 может варьировать между одним из меньших значений и одним из больших значений, выбранных из интервалов, приведенных выше. В качестве примеров, чип высокой плотности может характеризоваться наличием впадин 14, разделенных меньше, чем примерно 100 нм, чип средней плотности может характеризоваться наличием впадин 14, разделенных от примерно 400 нм до примерно 1 мкм, и чип низкой плотности может характеризоваться наличием впадин 14, разделенных больше, чем примерно 1 мкм. В то время как были приведены типичные плотности, следует понимать, что можно использовать субстраты с любыми подходящими плотностями.
Схема или структура может также или альтернативно характеризоваться в показателях среднего шага, т.е. расстояния от центра впадины 14 до центра смежной промежуточной области 16 (расстояние от центра до центра). Данная структура может быть регулярной, таким образом, что коэффициент вариации около среднего шага является маленьким, или данная структура может быть нерегулярной, причем в данном случае коэффициент вариации может быть относительно большим. В любом случае средний шаг может составлять, например, по меньшей мере примерно 10 нм, примерно 0,1 мкм, примерно 0,5 мкм, примерно 1 мкм, примерно 5 мкм, примерно 10 мкм, примерно 100 мкм или больше. Альтернативно или дополнительно, средний шаг может составлять, например, самое большее примерно 100 мкм, примерно 10 мкм, примерно 5 мкм, примерно 1 мкм, примерно 0,5 мкм, примерно 0,1 мкм или меньше. Средний шаг для конкретной структуры сайтов 16 может составлять между одним из меньших значений и одним из больших значений, выбранных из интервалов, приведенных выше. В то время как были приведены типичные значения среднего шага, следует понимать, что можно использовать другие значения среднего шага.
В примере, показанном на Фиг. 2А-2Е, впадины 14 представляют собой лунки 14', и, таким образом, структурированный субстрат 12 включает совокупность лунок 14' на его поверхности. Лунки 14' могут представлять собой микролунки или нанолунки. Размер каждой лунки 14' может характеризоваться ее объемом, площадью отверстия лунки, глубиной и/или диаметром.
Каждая лунка 14' может иметь любой объем, который способен содержать жидкость. Можно выбрать минимальный или максимальный объем, например, для приспособления к производительности (например, мультиплексности), разрешению, составу аналита или реакционной способности аналита, ожидаемой для последующих применений проточной ячейки. Например, объем может составлять по меньшей мере примерно 1×10-3 мкм3, примерно 1×10-2 мкм3, примерно 0,1 мкм3, примерно 1 мкм3, примерно 10 мкм3, примерно 100 мкм3 или более. Альтернативно или дополнительно, объем может составлять самое большее примерно 1×104 мкм3, примерно 1×103 мкм3, примерно 100 мкм3, примерно 10 мкм3, примерно 1 мкм3, примерно 0,1 мкм3 или меньше. Следует понимать то, что функционализированный покрывающий слой может заполнять весь объем или часть объема лунки 14'. Объем покрывающего слоя в индивидуальной лунке 14' может составлять больше чем, меньше чем или между значениями, определенными выше.
Площадь, занимаемая каждым отверстием лунки на поверхности может быть выбрана на основе аналогичных критериев, что и критерии, изложенные выше для объема лунки. Например, площадь для каждого отверстия лунки на поверхности может составлять по меньшей мере примерно 1×10-3 мкм2, примерно 1×10-2 мкм2, примерно 0,1 мкм2, примерно 1 мкм2, примерно 10 мкм2, примерно 100 мкм2 или более. Альтернативно или дополнительно, площадь может составлять самое большее примерно 1×103 мкм2, примерно 100 мкм2, примерно 10 мкм2, примерно 1 мкм2, примерно 0,1 мкм2, примерно 1×10-2 мкм2 или меньше. Площадь, занимаемая каждым отверстием лунки может составлять больше чем, меньше чем или между значениями, определенными выше.
Глубина каждой лунки 14' может составлять по меньшей мере примерно 0,1 мкм, примерно 1 мкм, примерно 10 мкм, примерно 100 мкм или более. Альтернативно или дополнительно, глубина может составлять самое большее примерно 1×103 мкм, примерно 100 мкм, примерно 10 мкм, примерно 1 мкм, примерно 0,1 мкм или меньше. Глубина каждой лунки 14' может составлять больше чем, меньше чем или между значениями, определенными выше.
В некоторых случаях диаметр каждой лунки 14' может составлять по меньшей мере примерно 50 нм, примерно 0,1 мкм, примерно 0,5 мкм, примерно 1 мкм, примерно 10 мкм, примерно 100 мкм или больше. Альтернативно или дополнительно, данный диаметр может составлять самое большее примерно 1×103 мкм, примерно 100 мкм, примерно 10 мкм, примерно 1 мкм, примерно 0,5 мкм, примерно 0,1 мкм или меньше (например, примерно 50 нм). Диаметр каждой лунки 14' может быть больше чем, меньше чем или между значениями, определенными выше.
Структурированный субстрат 12 может подвергаться воздействию ряда процессов для того, чтобы добавить поверхностную химию 20, 22 во впадину(ны) 14.
В то время как это не показано, следует понимать, что структурированный субстрат 12 может подвергаться воздействию плазменного травления для того, чтобы очистить и активировать поверхность. Например, способ плазменного травления может удалять органическое вещество и вводить поверхностные гидроксильные или карбоксильные группы. Можно использовать другие подходящие способы очистки для очистки субстрата 12, отчасти в зависимости от типа субстрата 12. Например, химическую очистку можно осуществлять окислителями или каустическими растворами. Следует понимать то, что если азидная функциональная молекула может присоединяться к функциональным группам -ОН на поверхности, может не использоваться дополнительная подготовка поверхности субстрата.
Структурированный субстрат 12 (показанный на Фиг. 2А) может затем подвергаться воздействию процесса, который будет готовить поверхность 12 для нанесения азидной функциональной молекулы с образованием полимерного слоя 20 (Фиг. 2С) или для нанесения второго примера смеси для прививки с образованием функционализированного слоя 24 (Фиг. 2Е). В одном примере структурированный субстрат 12 может подвергаться воздействию силанизации, которая присоединяет силан или производное силана 18 (Фиг. 2В) к поверхности структурированного субстрата 12. Силанизация вводит силан или производное силана 18 по всей поверхности, включая впадину 14, 14' (например, на поверхности дна и вдоль боковых стенок), и на промежуточных областях 16.
Силанизация может осуществляться с использованием любого силана или производного силана 18. Выбор силана или производного силана 18 может зависеть, отчасти, от молекулы, функционализированной азидом, которую следует использовать для образования полимерного слоя 20 (показанного на Фиг. 2С) или которая используется во второй смеси для прививки, так как может быть желательным образование ковалентной связи между силаном или производным силана 18 и полимерным слоем 20 или молекулой, функционализированной азидом, во второй смеси для прививки. Способ, используемый для присоединения силана или производного силана 18 к субстрату 12 может варьировать, в зависимости от силана или производного силана 18, которые используются. В данном документе излагаются несколько примеров.
В одном примере силан или производное силана 18 представляет собой (3-аминопропил)триэтоксисилан (APTES) или (3-аминопропил)триметоксисилан (APTMS) (т.е., X-RB-Si(ORC)3, где X представляет собой амино, RB представляет собой -(СН2)3- и RC представляет собой этил или метил). В данном примере поверхность субстрата 12 может быть предобработана (3-аминопропил)триэтоксисиланом (APTES) или (3-аминопропил)триметоксисиланом (APTMS) для ковалентного связывания кремния с одним или более чем одним атомом кислорода на поверхности (без намерения сосредотачиваться на механизме, каждый кремний может связываться с одним, двумя или тремя атомами кислорода). Данная химически обработанная поверхность подвергается термической обработке с образованием монослоя с аминогруппами. Данные аминогруппы затем подвергаются реакции с Сульфо-HSAB с образованием азидопроизводного. Активация УФ (ультрафиолетовое излучение) при 21°C с использованием энергии от 1 Дж/см2 до 30 Дж/см2 генерирует активные нитреновые соединения, которые могут легко подвергаться целому ряду реакций вставки с использованием PAZAM (например, молекулы, функционализированной азидом).
Также можно использовать другие способы силанизации. Примеры подходящих способов силанизации включают осаждение паровой фазы, способ YES, нанесение покрытия центрифугированием или другие способы нанесения. Некоторые примеры способов и веществ, которые можно использовать для силанизации субстрата 12, описываются в данном документе, хотя следует понимать то, что можно использовать и другие способы и вещества.
В одном примере с использованием печи YES CVD структурированный субстрат 12 помещают в CVD (химическое осаждение из паровой фазы) печь. Камера может вентилироваться, и затем начинается цикл силанизации. Во время циклирования сосуд с силаном или производным силана может поддерживаться при подходящей температуре (например, примерно 120°С для норборненового силана), паровые линии для силана или производного силана поддерживаются при подходящей температуре (например, примерно 125°С для норборненового силана), и вакуумные линии следует поддерживать при подходящей температуре (например, примерно 145°С).
В другом примере силан или производное силана 18 (например, жидкий норбореновый силан) может быть внесено внутрь стеклянного сосуда и помещено внутрь стеклянного вакуумного десикатора со структурированным субстратом 12. Из данного десикатора затем может быть откачан воздух до давления, составляющего от примерно 20 Па до примерно 40 Па, и он может быть помещен внутрь печи при температуре, составляющей от примерно 60°С до примерно 125°С. Дают идти силанизации, и затем десикатор удаляют из печи, охлаждают и вентилируют на воздухе.
Осаждение из паровой фазы, способ YES и/или вакуумный десикатор можно использовать с целым рядом силанов или производных силана 18, таких как те силаны или производные силана 18, которые включают примеры ненасыщенных группировок, раскрытых в данном документе. В качестве примеров, данные способы можно использовать, когда силан или производное силана 18 включает циклоалкеновую ненасыщенную группировку, такую как норборнен, производное норборнена (например, (гетеро)норбонрен, включающий кислород или азот вместо одного из атомов углерода), трансцикпооктен, производные трансциклооктена, трансциклопентен, трансциклогептен, транс-цикпононен, бицикло[3.3.1]нон-1-ен, бицикпо[4.3.1]дец-1(9)-ен, бицикпо[4.2.1]нон-1(8)-ен и бицикло[4.2.1]нон-1-ен. Любой из данных цикпоалкенов может быть замещен, например, группой R, такой как водород, алкил, алкенил, алкинил, циклоалкил, цикпоалкенил, циклоалкинил, арил, гетероарил, гетероалициклил, аралкил или (гетероалициклил)алкил. Пример норборненового производного включает [(5-бицикло[2.2.1]гепт-2-енил)этил]триметоксисилан. В качестве других примеров данные способы можно использовать, когда силан или производное силана 18 включает цикпоалкиновую ненасыщенную группировку, такую как циклооктин, циклооктиновое производное или бициклононины (например, бицикпо[6.1.0]нон-4-ин или его производные, бицикпо[6.1.0]нон-2-ин или бицикпо[6.1.0]нон-3-ин). Данные цикпоалкины могут быть замещены любыми группами R, описанными в данном документе.
Как показано на Фиг. 2В, присоединение силана или производного силана 18 образует силанизированный структурированный субстрат, включающий силанизированные впадины и силанизированные промежуточные области.
В примере, показанном на Фиг. 2С, силанизированный структурированный субстрат может затем быть подвергнут воздействию процесса, который образует полимерный слой 20 на силанизированных впадинах и силанизированных промежуточных областях.
Как описано в данном документе, примеры молекулы, функционализированной азидом (используемой для образования полимера 20), включают PAZAM или любую другую молекулу, которую функционализируют для реакции со структурированной кристаллической пластиной 12, и наносимый(мые) впоследствии праймер(ры) 22 (как часть каталитически активного комплекса). Данная молекула, функционализированная азидом, может присутствовать в растворе. В одном примере данный раствор включает PAZAM в этаноле и водную смесь. Полимерный слой 20 может быть образован на поверхности силанизированной структурированной кристаллической пластины (т.е. на силанизированных впадинах и силанизированных промежуточных областях) с использованием любой подходящей методики. Молекула, функционализированная азидом, может быть нанесена на поверхность структурированного субстрата 12 с использованием нанесения покрытия центрифугированием или окунания, или нанесения покрытия погружением, или тока молекулы, функционализированной азидом, при положительном или отрицательном давлении, или другими подходящими методиками. Образующийся слой 20 показан на Фиг. 2С.
Присоединение полимерного слоя 20 к силанизированным впадинам и силанизированным промежуточным областям (т.е. 18) может осуществляться посредством ковалентного связывания. Ковалентное связывание полимерного слоя 20 с силанизированными впадинами является полезным для сохранения полимерного слоя 20 во впадинах 14, 14' на протяжении всего срока службы образованной в конечном счете проточной ячейки во время целого ряда применений. Следующее представляет собой некоторые примеры реакций, которые могут происходить между силаном или производным силана 18 и полимерным слоем 20.
При включении силаном или производным силана 18 норборнена или норборненового производного в качестве ненасыщенной группировки данный норборнен или норборненовое производное может подвергаться реакции 1,3-диполярного циклоприсоединения с азидом/азидогруппой PAZAM.
При включении силаном или производным силана 18 цикпооктина или циклооктинового производного в качестве ненасыщенной группировки данный циклооктин или цикпооктиновое производное может подвергаться стимулируемой деформацией реакции 1,3-циклоприсоединения азид-алкин (SPAAC) с азидом/азидо PAZAM.
При включении силаном или производным силана 18 бицикпононина в качестве ненасыщенной группировки данный бицикпононин может подвергаться аналогичному цикпоприсоединению алкина SPAAC с азидами к PAZAM из-за деформации в бицикпической кольцевой системе.
В то время как это не показано, следует понимать, что в некоторых примерах данного способа структурированный субстрат 12 может не подвергаться силанизации. Скорее структурированный субстрат 12 может быть подвергнут воздействию плазменного травления, и затем молекула, функционализированная азидом, может быть непосредственно нанесена в виде покрытия центрифугированием (или нанесена иным способом) на подвергнутый плазменному травлению структурированный субстрат 12 с образованием полимерного слоя 20. В данном примере плазменное травление может генерировать агент(ты), активирующий(щие) поверхность (например, группы -ОН), которые могут приклеить полимерный слой 20 к структурированному субстрату 12. В данных примерах полимерный слой 20 выбирают таким образом, что он реагирует с поверхностными группами, генерированными плазменным травлением.
После покрытия молекула, функционализированная азидом, также может подвергаться воздействию процесса отверждения с образованием полимерного слоя 20 по всему структурированному субстрату (т.е. на впадине(нах) и промежуточной(ных) области(тях)). В одном примере отверждение молекулы, функционализированной азидом, может происходить при температуре, составляющей от комнатной температуры (например, примерно 25°С) до примерно 60°С в течение периода времени, составляющего от примерно 5 минут до примерно 2 часов.
Силанизированный и покрытый структурированный субстрат (показанный на Фиг. 2С) может подвергаться процессу очистки. В данном процессе могут использоваться водная баня и обработка ультразвуком. Водная баня может поддерживаться при относительно низкой температуре, составляющей от примерно 22°С до примерно 45°С. В другом примере температура водной бани варьирует от примерно 25°С до примерно 30°С.
Силанизированный и покрытый структурированный субстрат затем подвергают полировке для удаления части(тей) полимерного слоя 20 от силанизированных промежуточных областей. Силанизированный, покрытый и отполированный структурированный субстрат показан на Фиг. 2D. Части силана или производного силана 18, которые являются смежными с промежуточными областями 16, могут быть или могут не быть удалены в результате полировки. Ввиду этого части силана или производного силана 18, которые являются смежными с промежуточными областями 16, показаны на Фиг. 2D и 2Е в полуразрезе, так как они могут по меньшей мере частично сохраняться после полировки, или они могут быть удалены после полировки. При полном удалении данных силанизированных частей следует понимать, что экспонируется подлежащий субстрат 12.
Способ полировки может осуществляться с использованием мягкой химической суспензии (включающей, например, абразив, буфер, хелатор, поверхностно-активное вещество и/или диспергент), которая может удалять тонкий полимерный слой 20 и, в некоторых случаях, по меньшей мере часть силана или производного силана 18 от промежуточных областей 16 без вредного влияния на подлежащий субстрат 12 в данных областях. В качестве альтернативы, полировка может осуществляться раствором, который не включает абразивные частицы.
Данную химическую суспензию можно использовать в химической механической полировочной системе для полировки поверхности силанизированного и покрытого структурированного субстрата, показанного на Фиг. 2С. Полировальная(ные) головка(ки)/подложка(ки) или другое(гие) полировальное(ные) средство(ва) способно(ны) стачивать полимерный слой 20 с промежуточных областей 16, оставляя полимерный слой 20 во впадинах 14, 14' и оставляя подлежащий субстрат 12 по меньшей мере частично интактным. В качестве примера, полировальная головка может представлять собой полировальную головку Strasbaugh ViPRR II.
Как упомянуто выше, полировка может осуществляться полировальной подложкой и раствором без какого-либо абразива. Например, полировальная подложка может использоваться с использованием раствора, не содержащего абразивных частиц (т.е раствора, который не включает абразивные частицы).
Полировка удаляет часть(ти) полимерного слоя 20 (и в некоторых случаях по меньшей мере часть силана или производного силана 18) от промежуточных областей 16 и оставляет часть(ти) полимерного слоя 20 в силанизированных впадинах, как показано на Фиг. 2D. Также как упомянуто выше, промежуточная(ные) область(ти) 16 может оставаться силанизированной после завершения полировки. Другими словами, силанизированные промежуточные области могут оставаться интактными после полировки. В качестве альтернативы (как показано частями в полуразрезе 18), силан или производное силана 18 может быть удалено из промежуточной(ных) области(тей) 16 в результате полировки.
В то время как это не показано, следует понимать, что силанизированный, покрытый и отполированный субстрат (показанный на Фиг. 2D) может подвергаться процессу очистки. В данном процессе могут использоваться водная баня и обработка ультразвуком. Водная баня может поддерживаться при относительно низкой температуре, составляющей от примерно 22°С до примерно 30°С. Силанизированный, покрытый и отполированный структурированный субстрат также может быть высушен центрифугированием или высушен посредством другой подходящей методики.
Силанизированный, покрытый и отполированный структурированный субстрат, показанный на Фиг. 2D, затем может подвергаться процессу прививки для того, чтобы привить праймер 22 к полимерному слою 20 во впадине(нах) 14, 14'. В данном примере прививка может осуществляться посредством покрытия окунанием, покрытия распылением, нанесения в ванночке или другим подходящим способом, который будет присоединять праймер(ры) 22 каталитически активного вещества к полимерному слою 20 в по меньшей мере некоторых из впадин 14, 14'. В каждой из данных типичных методик используется первый пример смеси для прививки, раскрытой в данном документе, которая включает каталитически активное(ные) вещество(ва). Данные вещества вводят и праймер(ры) 22 для прививки, и Cu+ катализатор для реакции циклоприсоединения азид-алкин.
Покрытие окунанием может включать погружение структурированного субстрата (имеющего полимерный слой 20 в его впадине(нах) 14, 14') в серии ванн с контролируемой температурой. Данные ванны также могут иметь контроль потока и/или быть покрыты атмосферой азота. Данные ванны могут включать первый пример смеси для прививки. Во всех разных ваннах праймер(ры) 22 будет(дут) присоединяться к полимерному слою 20 в по меньшей мере некоторой(рых) впадине(нах). В одном примере покрытый и отполированный структурированный субстрат будет вводиться в первую ванну, включающую первый пример смеси для прививки, где происходит реакция циклоприсоединения азид-алкин с присоединением праймера(ров) 22, и затем данный структурированный субстрат будет перемещен в дополнительные ванны для промывки. Структурированный субстрат может перемещаться из ванны в ванну роботом-манипулятором или вручную. При покрытии окунанием также может использоваться система сушки.
Покрытие распылением может осуществляться распылением первого примера смеси для прививки непосредственно на покрытый и отполированный структурированный субстрат. Субстрат, покрытый распылением, может инкубироваться в течение вплоть до примерно 60 минут при температуре, составляющей от примерно 0°С до примерно 70°С. После инкубации первый пример смеси для прививки может быть разведен и удален с использованием, например, прибора для нанесения покрытия центрифугированием.
Нанесение в ванночке может осуществляться способом бассейна и центрифугирования, и, таким образом, может осуществляться прибором для нанесения покрытия центрифугированием. Первый пример смеси для прививки может наноситься (вручную или посредством автоматизированного способа) на покрытый и отполированный структурированный субстрат. Нанесенный первый пример смеси для прививки может наноситься или распределяться по всей поверхности покрытого и отполированного структурированного субстрата. Структурированный субстрат, покрытый первым примером смеси для прививки, может инкубироваться в течение времени вплоть до примерно 90 минут при температуре, составляющей от примерно 0°С до примерно 90°С. После инкубации первый пример смеси для прививки может быть разбавлен и удален с использованием, например, прибора для нанесения покрытия центрифугированием.
Прививка праймеров 22 от каталитически активного(ных) вещества(ществ) на полимерный слой 20 образует функционализированный слой 24, как показано на Фиг. 2Е.
В другом примере данного способа полимер 20 не наносится отдельно от праймеров 22. Скорее, второй пример смеси для прививки, который включает продукт реакции азид-алкин, можно использовать для образования функционализированного слоя 24 в одном процессе.
Возвращаясь к Фиг. 2В, силанизированный структурированный субстрат может подвергаться полировке для удаления части(тей) силана или производного силана 18 от силанизированных промежуточных областей. Данный процесс оставляет силанизированные впадины 14, 14'.
Второй пример смеси для прививки можно затем наносить на силанизированный и отполированный структурированный субстрат. Нанесение второго примера смеси для прививки может осуществляться посредством покрытия окунанием, покрытия распылением, нанесения в ванночке или другим подходящим способом. Любая(бые) непрореагировавшая(шие) азидная(ные) функциональная(ные) группа(пы) продукта реакции азид-алкин реагирует(ют) с силаном или производным силана 18 по меньшей мере в некоторых впадинах 14, 14', как описано ранее в связи в Фиг. 2С. В одном примере продукт реакции азид-алкин включает PAZAM (например, полимер 20), присоединенный к алкину праймера 22, и любые непрореагировавшие азиды PAZAM способны реагировать с силаном или производным силана 18 для того, чтобы присоединить продукт реакции азид-алкин к структурированному субстрату 12. В отличие от первого примера смеси для прививки, который включает многие стадии для образования функционализированного слоя 24 (описанные на Фиг. 2С-2Е), применение второго примера смеси для прививки делает возможным образование функционализированного слоя 24 (например, слоя 20 с присоединенными праймерами 22) при одном нанесении (двигаясь от Фиг. 2В до Фиг. 2Е).
После покрытия продукт реакции азид-алкин также может подвергаться процессу отверждения с образованием функционализированного слоя 24 в области(тях) впадины(дин). В одном примере отверждение продукта реакции азид-алкин может происходить при температуре, составляющей от комнатной температуры (например, примерно 25°С) до примерно 60°С в течение периода времени, составляющего от примерно 5 минут до примерно 2 часов.
Нанесение поверхностной химии 20, 22 (т.е. образование функционализированного слоя 24) может осуществляться таким образом, что связывающая область структурированного субстрата 12 остается экспонированной. Связывающая область структурированного субстрата 12 обычно располагается на некоторой(рых) из промежуточной(ных) области(тей) 16 структурированного субстрата 12, где крышка будет связываться со структурированным субстратом 12. Когда структурированный субстрат представляет собой кристаллическую пластину, данная связывающая область может определять границы нескольких проточных ячеек, которые образуются из данной кристаллической пластины. Когда структурированный субстрат представляет собой штампованную плиту, данная связывающая область может определять наружные границы одной проточной ячейки, которая образуется.
В силу этого некоторые примеры способа 100 включают присоединение крышки к связывающей области структурированного субстрата 12 с образованием проточного канала, который находится в селективной жидкостной связи с(со) впадиной(нами) 14, 14'. Когда структурированный субстрат представляет собой кристаллическую пластину, разные области крышки могут по меньшей мере частично определять соответствующие проточные каналы, которые образуются с использованием кристаллической пластины. Когда структурированный субстрат 12 представляет собой формованную плиту, крышка может определять один или более чем один проточный канал, который образуется.
Крышка может быть из любого материала, который является прозрачным для возбуждающего света, который направляется к поверхностной химии 20, 22 во впадине(нах) 14, 14'. В качестве примеров, крышка может быть стеклянной (например, борсиликатной, из кварцевого стекла и т.д.), пластмассовой или тому подобное. Имеющийся в продаже пример подходящего борсиликатного стекла - D 263®, доступный у Schott North America, Inc. Имеющиеся в продаже примеры подходящих пластмассовых материалов, а именно: цикпоолефиновые полимеры - продукты ZEONOR®, доступные у Zeon Chemicals L.P.
Крышка может быть присоединена к связывающей области структурированного субстрата 12 с использованием любой подходящей методики, такой как лазерное связывание, диффузное связывание, анодное связывание, эвтектическое связывание, связывание на основе активации плазмы, пайка стеклокристаллическим припоем или другие способы, известные в данной области. В одном примере можно использовать спейсерный слой для связывания крышки со связывающей областью структурированного субстрата 12. Данный спейсерный слой может представлять собой любое вещество, которое будет склеивать по меньшей мере некоторые из промежуточных областей 16 (например, связывающую область) структурированного субстрата 12 и крышку друг с другом.
В одном примере спейсерный слой может представлять собой вещество, поглощающее излучение, которое потощает излучение при длине волны, которая пропускается крышкой и/или структурированным субстратом. Поглощенная энергия, в свою очередь, образует связь между спейсерным слоем и крышкой, и между спейсерным слоем и структурированным субстратом. Примером данного вещества, поглощающего излучение, является черный KAPTON® (полиимид, содержащий углеродную сажу) от DuPont (США), который поглощает при примерно 1064 нм. Следует понимать то, что полиимид мог бы использоваться без добавления углеродной сажи, за исключением того, что длина волны должна была бы быть изменена до длины волны, которая значительно поглощается природным полиимидным веществом (например, 480 нм). В качестве другого примера полиимид CEN JP может связываться при облучении светом при 532 нм. Когда спейсерный слой представляет собой вещество, поглощающее излучение, данный спейсерный слой может быть расположен на поверхности контакта между крышкой и структурированным субстратом, таким образом, что спейсерный слой контактирует с желательной связывающей областью. При приложении к поверхности контакта энергии лазера при подходящей длине волны (т.е. вещество, поглощающее излучение, облучается) может прилагаться сжатие (например, давление приблизительно 689,4 кПа). Энергия лазера может быть приложена к поверхности контакта как сверху, так и снизу для достижения подходящего связывания.
В другом примере спейсерный слой может включать вещество, поглощающее излучение, находящееся в контакте с ним. Данное вещество, поглощающее излучение, может наноситься на поверхность контакта между спейсерным слоем и крышкой, а также на поверхность контакта между спейсерным слоем и структурированным субстратом. В качестве примера, спейсерный слой может представлять собой полиимид, а отдельное вещество, поглощающее излучение, может представлять собой углеродную сажу. В данном примере отдельное вещество, поглощающее излучение, поглощает энергию лазера, что образует связи между спейсерным слоем и крышкой, и между спейсерным слоем и структурированным субстратом. В данном примере при приложении к поверхностям контакта энергии лазера при подходящей длине волны (т.е. вещество, поглощающее излучение, облучается) к соответствующим поверхностям контакта может прилагаться сжатие.
Когда структурированный субстрат 12 представляет собой кристаллическую пластину, спейсерный слой и боковые стенки (крышки или соединенные с крышкой) могут физически отделять один проточный канал от смежного проточного канала и могут располагаться на периферии кристаллических пластин. Когда структурированный субстрат 12 представляет собой формованную плиту, и проточная ячейка, которая образуется, должна включать один проточный канал или полосу, спейсерный слой и боковые стенки (крышки или соединенные с крышкой) могут быть расположены на периферии формованной плиты для определения проточного канала и запечатывания проточной ячейки. Когда структурированный субстрат 12 представляет собой формованную плиту, и проточная ячейка, которая образуется, должна включать многие изолированные проточные каналы (например, восемь или четыре проточных канала), спейсерный слой и боковые стенки (крышки или соединенные с крышкой) могут физически отделять один проточный канал/полосу от соседнего проточного канала/полосы и могут быть расположены на периферии формованной плиты. Однако следует понимать то, что спейсерный слой и боковые стенки могут располагаться в любой желательной области, в зависимости от применения.
Когда структурированный субстрат 12 представляет собой формованную плиту, связывание крышки образует проточную ячейку. Когда структурированный субстрат 12 представляет собой кристаллическую пластину, способ 100 может включать дополнительную обработку, такую как резка пластины на кристаллы, после связывания крышки. В одном примере крышка может быть связана со структурированным субстратом 12, и резка пластины на кристаллы образует индивидуальные проточные ячейки.
Как упомянуто выше, поверхностная химия 20, 22 (функционализированный слой 24) также может быть добавлена к неструктурированному субстрату 12', и данные примеры будут описаны со ссылкой на Фиг. 3А-3Г. С неструктурированным субстратом 12' непрерывная поверхность включала бы такую же поверхностную химию 20, 22, которая находится в лунках 14' Фиг. 2А-2Е. В качестве неструктурированного субстрата 12' может использоваться любой из субстратов, раскрытых в данном документе, за исключением того, что неструктурированный субстрат 12' не включает впадины 14 или промежуточные области 16. В данном типичном способе крышка 26 (показанная на Фиг. 3В) связывается с неструктурированным субстратом 12' на боковине с образованием проточного(ных) канала(лов) 30. Крышка 26 может состоять из любых материалов и находиться в любых конфигурациях, описанных в данном документе. Крышка 26 также может связываться с неструктурированным субстратом 12' посредством любой из методик, описанных в данном документе.
В примере, показанном на Фиг. 3В, крышка 26 включает верхнюю часть 27, интегрально образованную с боковой(выми) стенкой(ками) 29. Боковая(вые) стенка(ки) 29 связывает(ют)ся со связывающей областью неструктурированного субстрата 12' через спейсерный слой 28. Связывающая область может находиться на периферии неструктурированного субстрата 12' или в любых областях, где желательно образовать границу проточного канала 30. В других примерах спейсерный слой 28 может образовать боковую(вые) стенку(ки) и может быть присоединен к по меньшей мере существенно плоской крышке 26.
Крышка 26 (включающая боковую(вые) стенку(ки) 29) и неструктурированный субстрат 12' совместно определяют проточный канал 30. Проточный канал 30 может служить, например, для селективного введения жидкостей для того, чтобы образовать поверхностную химию 20, 22 и для селективного введения компонентов реакции или реактивов к поверхностной химии 20, 22 для того, чтобы инициировать установленные реакции в пределах проточного канала 30.
Перед образованием полимерного слоя 20 (показанного на Фиг. 3В) данный способ может включать подвергание неструктурированного субстрата 12' (посредством процесса протекания) процессу очистки и/или другому процессу (например, силанизации), который готовит экспонированную поверхность неструктурированного субстрата 12' для последующего нанесения молекулы, функционализированной азидом (с образованием слоя 20), или второго примера смеси для прививки (с образованием функционализированного слоя 24).
Силанизация неструктурированного субстрата 12' показана на Фиг. ЗВ. В данном примере силанизация присоединяет силан или производное силана 18 к экспонированным частям поверхности неструктурированной кристаллической пластины 12', которые присутствуют в проточном канале 30.
Силанизация может осуществляться с использованием любого силана или производного силана 18. Выбор силана или производного силана 18 может включать функциональную группу, которая может образовать ковалентную связь с азидом или с молекулой, функционализированной азидом (используемой для образования полимерного слоя 20, показанного на Фиг. 3С), или с азидом продукта реакции азид-алкин во втором примере смеси для прививки (используемой для образования функционализированного слоя 24, показанного на Фиг. 3Г). Способом, используемым для присоединения силана или производного силана 18 к субстрату 12', может быть процесс протекания.
Как показано на Фиг. 3С, в данном примере полимерный слой 20 затем образуется на силане или производном силана 18, или на другой химии, которая была нанесена для получения экспонированной поверхности неструктурированного субстрата 12' в пределах проточного канала 30.
Можно использовать любые из молекул, функционализированных азидом, описанных в данном документе. В данном примере образование полимерного слоя может осуществляться посредством процесса протекания. В процессе протекания молекула, функционализированная азидом, может вводиться в проточный(ные) канал(лы) 30 через соответствующий(щие) впускной(ные) порт(ты) и может отверждаться. Полимерный слой 20 будет формироваться на экспонированной поверхности неструктурированного субстрата 12', и полировка не происходит.
Как показано на Фиг. 3D, праймер 22 прививается к полимерному слою 20 в проточном канале 30 с использованием первого примера смеси для прививки, который включает каталитически активное(ные) вещество(ва). В данном примере прививка может осуществляться посредством процесса протекания. В данном процессе протекания первый пример смеси для прививки, описанный в данном документе, может вводиться в проточный(ные) канал(лы) 30 через соответствующий(щие) впускной(ные) порт(ты), может сохраняться в данном(ных) проточном(ных) канале(лах) в течение достаточного времени (т.е. периода инкубации) для прохождения реакции цикпоприсоединения азид-алкин, катализируемой медью(1), которая присоединяет праймер 22 к полимерному слою 20, с образованием функционализированного слоя 24. Первый пример смеси для прививки может затем удаляться из соответствующего(щих) выпускного(ных) порта(тов). После присоединения праймера дополнительная(ные) жидкость(ти) может(гут) направляться через проточный(ные) канал(лы) для промывки теперь функционализированного(ных) проточного(ных) канала(лов) 30. Образующаяся в данном примере проточная ячейка 10 показана на Фиг. 3D.
В другом примере данного способа полимер 20 не наносится отдельно от праймеров 22. Скорее для образования функционализированного слоя 24 в одном процессе может использоваться второй пример смеси для прививки, который включает продукт реакции азид-алкин.
В данном примере второй пример смеси для прививки можно затем наносить на силанизированный неструктурированный субстрат, показанный на Фиг. 3В. Нанесение второго примера смеси для прививки может осуществляться посредством проточного процесса. Любая(бые) непрореагировавшая(шие) азидная(ные) функциональная(ные) группа(пы) продукта реакции азид-алкин реагирует с силаном или производным силана 18, как описано в данном документе ранее. В одном примере продукт реакции азид-алкин включает PAZAM (например, полимер 20), присоединенный к алкину праймера 22, и любые непрореагировавшие азиды PAZAM способны реагировать с силаном или производным силана 18 для того, чтобы присоединять продукт реакции азид-алкин к неструктурированному субстрату 12. В отличие от первого примера смеси для прививки, который включает многочисленные стадии для образования функционализированного слоя 24 (описанные на Фиг. 3C-3D), применение второго примера смеси для прививки делает возможным образование функционализированного слоя 24 (например, слоя 20 с присоединенными праймерами 22) за одно нанесение (переходя от Фиг. 3В до Фиг. 3D). Также может осуществляться отверждение функционализированного слоя 24.
В то время как это не показано, следует понимать то, что структурированный субстрат 12 или неструктурированный субстрат 12' может включать впускной и выпускной порты, которые служат для жидкостного занятия других портов (не показанных) для направления жидкости(тей) в соответствующие проточные каналы (например, от картриджа с реактивами или другой системы хранения жидкости) и из проточных каналов (например, в систему удаления отходов).
В то время как это также не показано, следует понимать, что некоторые примеры проточных ячеек могут быть непосредственно прикреплены и, таким образом, находиться в физическом контакте с выявляющим прибором (не показан) через один или более чем один механизм крепления (например, адгезивное средство, сцепление, застежки и тому подобное). Выявляющий прибор может включать прибор CMOS (комплементарный металло-оксидный полупроводник) (который включает целый ряд собранных в стопку слоев, включающих например, кремниевый(вые) слой(слои), диэлектрический(кие) слой(слои), металл-диэлектрический(кие) слой(слои), металлический(кие) слой(слои) и т.д.) и оптические компоненты. Данные оптические компоненты могут быть организованы таким образом, что оптический сенсор выявляющего прибора является по меньшей мере существенно выровненным и, таким образом, является функционально ассоциированным с одним оптическим световодом выявляющего прибора и поверхностной химией 20, 22 в пределах одной впадины 14, 14' или в пределах проточного канала 30 проточной ячейки.
В то время как это также не показано, следует понимать, что вместо связывания с крышкой 26 функционализированный субстрат (с поверхностной химией 20, 22 на нем или в его впадине(нах) 14) может быть связан с другим функционализированным субстратом с поверхностной химией 20, 22 на нем в его впадине(нах). Две данные функционализированные поверхности могут находиться напротив друг друга и могут иметь проточный канал, определенный между ними. Можно использовать спейсерный слой и подходящий способ связывания для связывания друг с другом двух функционализированных субстратов.
Проточные ячейки, раскрытые в данном документе, можно использовать в целом ряде подходов секвенирования или технологий, включающих методики, часто именуемые секвенированием посредством синтеза (SBS), секвенированием на циклическом чипе, секвенированием посредством лигирования, пиросеквенированием и так далее. При использовании любой из данных методик и в примерах с использованием структурированного субстрата, поскольку функционализированный полимерный слой 20 и присоединенный(ные) праймер(ры) для секвенирования присутствует(ют) в функционализированных впадинах (т.е. 14, 14' с поверхностной химией на них), а не на промежуточных областях 16, амплификация будет ограничиваться функционализированными впадинами. В других примерах амплификация будет происходить по всему каналу проточной ячейки (например, каналу 30).
В качестве одного примера реакция секвенирования посредством синтеза (SBS) может идти на такой системе, как системы секвенаторов HISEQ™, HISEQXT™, MISEQ™, NOVASEQ™ или NEXTSEQ™ от Illumina (Сан Диего, СА). При SBS отслеживается удлинение нуклеиновой кислоты-праймера вдоль нуклеиновой кислоты-матрицы для определения последовательности нуклеотидов в матрице. Лежащим в основе химическим процессом может быть полимеризация (например, катализируемая ферментом-полимеразой) или лигирование (например, катализируемое ферментом-лигазой). В конкретном способе SBS на основе полимеразы флуоресцентно меченые нукпеотиды добавляются к праймеру 22 (посредством этого удлиняя праймер 22) зависимым от матрицы способом, таким образом, что выявление порядка и типа нуклеотидов, добавленных к праймеру 22, можно использовать для определения последовательности матрицы. Например, для инициации первого цикла SBS один или более чем один меченый нуклеотид, ДНК-полимеразу и т.д. можно доставлять в/через проточный канал 30 и т.д., который содержит набор праймеров 22. Функционализированные впадины (т.е. 14, 14' с поверхностной химией 20, 22 на них), где удлинение праймера вызывает включение меченого нукпеотида, могут быть выявлены посредством события визуализации. Во время события визуализации система освещения (не показана) может давать возбуждающий свет функционализированным впадинам (т.е. 14, 14' с поверхностной химией 20, 22 на них).
В некоторых примерах данные нукпеотиды могут дополнительно иметь свойство обратимой терминации, которое останавливает дальнейшее удлинение праймера сразу после добавления нуклеотида к праймеру 22. Например, нукпеотидный аналог, имеющий обратимую терминирующую группировку, может быть добавлен к праймеру 22 таким образом, что последующее удлинение не может происходить, пока не доставляется деблокирующий агент для удаления данной группировки. Таким образом, для примеров, в которых используется обратимая терминация, в проточный канал 30 может доставляться деблокирующий агент и т.д. (до или после выявления).
Между разными стадиями доставки жидкости может(гут) происходить промывка(ки). Цикл SBS затем может повторяться n раз для удлинения праймера 22 на n нуклеотидов, выявляя, посредством этого, последовательность длиной n.
В то время как было подробно описано SBS, следует понимать, что проточные ячейки, описанные в данном документе, могут использоваться с другими протоколами секвенирования, для генотипирования или в других химических и/или биологических приложениях.
Для дальнейшей иллюстрации настоящего раскрытия в данном документе приводятся примеры. Следует понимать то, что данные примеры приводятся для иллюстративных целей и не должны истолковываться как ограничивающие объем данного раскрытия.
НЕОГРАНИЧИВАЮЩИЕ РАБОЧИЕ ПРИМЕРЫ
Пример 1
Смесь 0,25 М частиц Cu2S и 10 мкМ алкин-Р5- и алкин-Р7-праймеров готовили в 0,5 М натрий-карбонатном буфере при рН 10. Данной смеси давали инкубироваться при температуре 60°С в течение периода времени примерно 1 час. Без фильтрования полосу/канал со структурированным субстратом, включающую PAZAM в лунках структурированного субстрата, подвергали воздействию 10 мкм смеси для прививки (именуемой Е1 и примеру первого примера смеси для прививки, раскрытого в данном документе).
Готовили три сравнительные смеси для прививки. В качестве двух сравнительных примеров готовили смеси для прививки из алкин-Р5- и алкин-Р7-праймеров, CuSO4 (в качестве катализатора) и N,N,N',N'',N''-пентаметилдиэтилентриамина, с аскорбатом (СЕ1) или без аскорбата (СЕ2). В качестве третьего сравнительного примера (СЕ3) готовили смеси для прививки из алкин-Р5- и алкин-Р7-праймеров. В каждой из данных сравнительных смесей для прививки растворителем был 0,5 М натрий-карбонатный буфер. Соответствующие полосы/каналы со структурированным субстратом, включающие PAZAM в лунках структурированного субстрата, подвергали воздействию 10 мкм каждой сравнительной смеси для прививки.
Проводили анализ CFR для сравнения прививки праймеров с использованием смеси для прививки с каталитически активными веществами, раскрытой в данном документе (Е1), и сравнительных смесей для прививки (СЕ1, СЕ2, СЕ3). Во время анализа CFR поверхности с привитыми праймерами подвергаются воздействию флуоресцентно меченых (Cal Fluor Red) комплементарных олигонуклеотидов в буферном растворе. Данные олигонуклеотиды связываются с праймерами, связанными с поверхностью, а избыток CFR отмывается. Поверхность затем сканируется на флуоресцентном детекторе для измерения интенсивности GFR на поверхности для предоставления количественной меры концентрации и здоровья праймеров на поверхности. После измерения олигонуклеотиды удаляются с использованием раствора слабого основания, и поверхности подвергаются повторному сканированию для подтверждения удаления всего CFR.
Результаты по интенсивности в показателях относительных единиц интенсивности для типичной проточной ячейки и сравнительных проточных ячеек показаны на Фиг. 4. Относительные интенсивности варьировали от примерно 0,182 до 0,209 для СЕ1 и варьировали от примерно 0,175 до 0,205 для типичной смеси для прививки с Cu2S (Е1). Как показано, типичная смесь для прививки Е1, включающая каталитически активные вещества, была такой же эффективной в прививке праймеров, как и сравнительная смесь для прививки СЕ1, которая включала медный катализатор, стабилизирующий лиганд и аскорбат. Типичная смесь для прививки Е1 также была значительно более эффективной в прививке праймеров, чем сравнительные примеры СЕ2 и CE3.
Типичную проточную ячейку Е1 и проточную ячейку СЕ1 сравнительного примера использовали для секвенирования генома PhiX и анализировали на процентную долю кластеров, проходящих фильтр (%), балл качества (Q30), интенсивность после одного цикла секвенирования, процентную долю выровненных и частоту ошибок (%). % прохождения фильтра (PF) представляет собой показатель, используемый для описания кластеров, которые проходят через порог чистоты и используются для дальнейшей обработки и анализа данных секвенирования. Более высокий % прохождения фильтра приводит к повышенному выходу непустых лунок подходящего качества для данных по секвенированию. Q30, процентная доля выровненных и частота ошибок представляют собой показатели качества. Более конкретно, Q30 представляет собой эквивалент вероятности неправильного распознавания основания в 1 из 1000 случаев. Это означает то, что точность распознавания основания (т.е. вероятность правильного распознавания основания) составляет 99,9%. Меньшая точность распознавания основания - 99% (Q20) будет иметь вероятность неправильного распознавания основания 1 из 100, означая то, что каждый считываемый фрагмент секвенирования из 100 пар оснований вероятно будет содержать ошибку. Когда качество секвенирования достигает Q30, фактически все считываемые фрагменты будут превосходными, имеющими ноль ошибок и двусмысленностей. Результаты показаны в Таблице 1.

Данные результаты показывают то, что праймеры, привитые с использованием первого примера смеси для прививки (Е1) с каталитически активным веществом, работают для секвенирования также хорошо или лучше.
Результаты в данном примере представляют собой средние значения для четырех плиток изображений полос/каналов, которые подвергались прививке и анализу.
Пример 2
Смеси 0,25 М частиц Cu2S и 10 мкМ алкин-Р5- и алкин-Р7-праймеров готовили в 0,5 М натрий-карбонатном буфере при рН 10. Готовили три смеси, и давали им инкубироваться при температуре 60°С в течение разных периодов времени, включая 15 минут, 30 минут и 60 минут. После фильтрования полосу/канал со структурированным субстратом, включающую PAZAM в лунках структурированного субстрата, подвергали воздействию 10 мкм каждой смеси для прививки (которые представляют собой примеры первого примера смеси для прививки, раскрытого в данном документе).
Результаты по интенсивности в показателях единиц относительной интенсивности относительно времени инкубации (или экстракции) для типичных проточных ячеек показаны на Фиг. 5. Относительные интенсивности флуоресценции для данных примеров варьировали от примерно 0,036 до примерно 0,152. Как показано, эффективность в прививке праймера возрастала с увеличением периодов инкубации. Это указывает на то, что образовались более каталитически активные вещества, когда смесям давали инкубироваться дольше.
Пример 3
Готовили разные смеси для иллюстрации того, что примеры, раскрытые в данном документе, генерируют каталитически активные вещества. Сравнительная смесь 1 включала сульфид меди(I) в воде, который не был отфильтрован до анализа. Другая сравнительная смесь 2 включала сульфид меди(I) в воде, который тогда отфильтровывали до анализа. Данный пример включал частицы Cu2S и алкин-Р5- и алкин-Р7-праймеры в воде. Каждой смеси, которую фильтровали перед анализом, давали инкубироваться при тмпературе 60°С в течение периода времени примерно 1 час.
На каждой смеси проводили динамическое светорассеяние. Результаты показаны на Фиг. 6А (сравнительная смесь 1), 6В (сравнительная смесь 2) и 6С (типичная смесь). Результаты на Фиг. 6А показывают то, что присутствуют частицы сульфида меди(I) микрометрового размера, и результаты Фиг. 6 В показывают то, что частицы сульфида меди(I) микрометрового размера удалялись во время фильтрования. Результаты Фиг. 6С показывают то, что каталитически активные вещества присутствовали после проведения фильтрования.
Дополнительные примечания
Следует понимать то, что все комбинации вышеописанных идей и дополнительных идей, обсуждаемых с большими подробностями ниже (при условии, что такие идеи не являются взаимоисключающими), рассматриваются как часть объекта изобретения, раскрытого в данном документе. В частности, все комбинации заявленных объектов изобретения в конце данного раскрытия рассматриваются как часть объекта изобретения, раскрытого в данном документе. Также следует понимать то, что терминология, прямо использованная в данном документе, которая также может появиться в любом раскрытии, включенном посредством ссылки, должна предоставлять наиболее согласующееся значение с конкретными идеями, раскрытыми в данном документе.
Ссылка во всем данном описании изобретения на «один пример», «другой пример», «пример» и так далее означает то, что конкретный элемент (например, свойство, структура и/или характеристика), описанный в связи сданным примером, включается в по меньшей мере один пример, описанный в данном документе, и может присутствовать или может не присутствовать в других примерах. Кроме того, следует понимать то, что описанные элементы для любого примера могут объединяться в разных примерах любым подходящим образом, если контекст явно не диктует иное.
Следует понимать то, что интервалы, приведенные в данном документе, включают заявленный интервал и любое значение или подинтервал в пределах заявленного интервала. Например, интервал от примерно 500 нм до примерно 45 мкм следует интерпретировать как включающий не только явным образом перечисленные границы от примерно 500 нм до примерно 45 мкм, но также включающий индивидуальные значения, такие как примерно 708 нм, примерно 945 нм, примерно 35 мкм и т.д., и подинтервалы, такие как от примерно 825 мм до примерно 29 мкм, от примерно 950 нм до примерно 40 мкм и т.д. Кроме того, при использовании для описания значения термина «примерно» и/или «по существу», подразумевается то, что они охватывают небольшие вариации (вплоть до плюс/минус 10%) от заявленного значения.
В то время как несколько примеров были подробно описаны, следует понимать то, что раскрытые примеры могут быть модифицированы. Следовательно, вышеописанное описание следует рассматривать как неограничивающее.
Реферат
Изобретение может быть использовано при секвенировании генома. Предложено каталитически активное вещество, содержащее минеральную частицу сульфида меди(I) и молекулу, функционализированную алкином, непосредственно связанную с поверхностью минеральной частицы сульфида меди(I). Способ получения триазола включает проведение реакции молекулы, функционализированной алкином, с молекулой, функционализированной азидом, в присутствии минерала на основе сульфида меди(I). Предложены также смесь для прививки праймера к поверхности проточной ячейки и способ прививки праймера к поверхности проточной ячейки. Изобретение позволяет упростить получение триазола за счет исключения координации соединений меди со стабилизирующим лигандом и восстановления Cu2+, исключения применения дополнительных реактивов. 4 н. и 11 з.п. ф-лы, 6 ил., 1 табл., 3 пр.

Комментарии