Тестирующее устройство, способ выполнения (био- и/или иммунно) химического теста (варианты), дозирующее устройство и набор - RU2108156C1
Код документа: RU2108156C1
Чертежи





Описание
Изобретение относится к тестирующему устройству, включающему пластину, содержащую множество ячеек.
Изобретение также относится к дозирующему устройству, пригодному для одновременного введения равных объемов реагента в различные ячейки тестирующего устройства. Кроме того, изобретение относится к способу выполнения (био- и/или иммуно) химического исследования с использованием тестирующего устройства и/или дозирующего устройства. В изобретении рассматривается набор, который включает тестирующее устройство и дозирующее.
Тестирующее устройство, включающее пластину, содержащую множество ячеек, известно уже много лет в форме так называемой пластины микротитратора. Известная пластина микротитратора имеет размер порядка 12,5 см • 8,0 см и содержит 96 ячеек. Диаметр каждой ячейки около 0,6 см и глубина каждой ячейки около 1 см, так что каждая ячейка содержит до 250 мл образца. Ячейки разделены барьерами шириной приблизительно 2,0 мм.
Известную пластину микротитратора используют, когда выполняют разнообразные био- и/или иммунохимические исследования. При испытаниях такого типа часто используют фотометрическое определение. Очень хорошо известным примером подобных испытаний является ELISA. В случае фотометрических определений дно ячейки должно быть равномерно покрыто слоем образца, который анализируют, чтобы получить достоверные результаты. Более того, этот слой должен иметь по меньшей мере такую толщину, при которой имеет место поглощение, которое возможно обнаружить. На практике это обычно означает, что используют образцы, которые имеют объем по меньшей мере 50 мкл.
В ВОИС-91/06859 описан способ испытания для обнаружения реакции или активации клеток, включая лимфоциты. Способ обнаружения иммунологической чувствительности предмета исследования включает введение клетки, активирующей субстанцию, что заставляет фермент клеток стать доступным для реакции и измерения ферментативной реакции, использующей субстрат, который генерирует обнаруживаемый продукт, и раскрывается набор для выполнения таких испытаний. Упоминается, что применение образца объемом 30 мкл является предпочтительным при использовании пластины микротитратора с ячейками диаметром 6 мм. Заявляется реакционный сосуд диаметр 6 мм и высотой 0,5-5,0 мм с предпочтительной высотой 1-2 мм. В цитированной работе сосуд предназначен для оптимизации физиологического контроля реакции, допуская адекватный обмен газов, таких как кислород и CO2, достаточно быстрое установление pH-равновесия, адекватную диффузию молекул и рассеяние тепла. Реакционный сосуд в упомянутой работе связан с соотношением реакционного объема и площадью поверхности реакционного образца. Упомянутый документ не раскрывает каких-либо проблем, которые могут возникнуть при ополаскивании малых объемов в таких процессах как ELISA и PEPSCAN.
Так как био- и/или иммунохимические исследования часто включают большое число испытаний на образцах (таких как кровь и сыворотка), которые должны быть получены от испытуемых людей и/или животных, существует необходимость использовать для исследований настолько малое количество образца, насколько возможно.
Однако образец можно разбавлять только до определенной степени, так как соединение, которое анализируют, также должно присутствовать в ячейке в некоторой минимальной концентрации, для того чтобы получить поглощение, которое можно определить. Это имеет место потому, что в соответствии с законом Ламберта-Бэра интенсивность света зависит от концентрации и коэффициента поглощения компонента, который анализируют, и также от расстояния, которое должен пройти свет через измеряемый образец. На практике это означает применение 12,5 мл реагентов на пластину микротитратора. В таком случае существует очевидная необходимость уменьшить количество используемого образца.
Другое частое применение распространенной пластины микротитратора заключается в синтезе пептидов. При таких синтезах можно синтезировать пептиды, содержащие различные аминокислотные последовательности. Это может быть осуществлено, например, для определения местоположения эпитопа белка для специфического антитела. Для этого отдельно синтезируют пептиды, содержащие аминокислотные последовательности, соответствующие фрагменту белка, который изучают. Синтез может быть выполнен таким образом, что каждый пептид частично содержит аминокислотную последовательность другого пептида. Возможно осуществить синтез даже так, что не совпадает только одна аминокислота. Возможно также получить ряд коротких сегментов, например, гексапептидов, которые совпадают за исключением одной аминокислоты. Затем осуществляют определение, чтобы установить, с каким пептидным антителом образуется связь. Пептиды, c которыми связывается антитело, содержат эпитоп.
В первую очередь, при осуществлении синтеза пептида в ячейку, в которой должен быть синтезирован пептид, добавляют аминокислоту, которую нужно присоединить, затем присоединяют нужную аминокислоту к растущей пептидной цепи, промывают ячейку, чтобы удалить непрореагировавшую аминокислоту, и процедуру повторяют со следующей аминокислотой.
Однако при таком способе возникают проблемы, связанные с промыванием ячеек, поэтому принимают способ синтеза пептидов, при котором используют маленькие полиэтиленовые прутки (rod) в качестве опоры для растущих пептидных цепей (Geysen, Н.M., Meloen R.Н. and Barteling S.J., Proc.NatI. Acad. Sci. USA, vol. 81 (july 1984), pp. 3998-4002). Здесь описан способ одновременного синтеза сотен пептидов на твердом носителе с адекватной чистотой для выполнения ELISA. Взаимодействие пептидов с антителами может быть установлено просто, без удаления пептидов с носителя. В результате становится возможным определить иммуногенный эпитоп с хорошим разрешением. Это способ называется PEPSCAN.
По этому способу растущим пептидным цепям дают возможность прилипать к полиэтиленовым пруткам (имеющим диаметр 4 мм и длину 40 мм), и реакции, требуемые для синтеза пептидов, затем осуществляют, используя концы прутков-носителей. С этой целью полиэтиленовые прутки сначала погружают в 6%-ный раствор акриловой кислоты в воде и подвергают действию γ-облучения. Для последующих реакций концы прутков затем приводят в контакт с тефлоновой пластиной, содержащей матрицу из ячеек, соответствующих местоположению прутков (известная пластина микротитратора). Обычные методы химии пептидов в твердой фазе могут быть использованы здесь, например, для присоединения метилового эфира Nα-трет-бутоксикарбонил-L-лизина к полиэтилену с полиакриловой кислотой через Nα- аминогруппу боковой цепи. (Erickson, B.W. and Merrifield, R.B. (1976) в the Proteins, Eds, Neurath, H. & Hill, R.L. (Academic, New York), vol. 2, pp.255- 527 и Meienhofer, J. (1973) в Hormonal Proteins and Peptides, Ed. Li, C.H., (Academic, New York), vol.2, pp.45-267). После удаления трет-бутоксикарбонильной группы может быть присоединен трет-бутоксикарбонил-L-аланин, причем образуется пептидоподобная прослойка (spacer). Нужные аминокислоты могут быть успешно присоединены и после последней желаемой реакции сочетания и после удаления защитной трет-бутоксикарбонильной группы концевая аминокислота может быть ацетилирована уксусным ангидридом в диметилформамиде и триэтаноламине. Все реакции сочетания, осуществленные с N, N-дициклогексилкарбодиимидом, могут осуществляться в диметилформамиде в присутствии N-гидроксибензотриазола. Любые защитные группы в боковых цепях аминокислот, использованных в синтезе пептида, также могут быть удалены. Прежде чем синтезированные пептиды проверяют далее, например, посредством ELISA, прутки могут быть промыты раствором фосфатно-солевого буфера.
Еще одно применение пептидного синтеза происходит, если одну или несколько аминокислот известного эпитопа заменяют для того, чтобы определить, какие другие последовательности способны функционировать в качестве эпитопа, и/или для того, чтобы определить, какие аминокислоты являются существенными для действия эпитопа (Geysen, Н.M., Weloen, R.Н. and Bartelinq, S.J., Proc. Natl. Acad. Sci. USA, vol. 82 (January 1985) pp. 178-182).
Поскольку такие способы часто включают большое число синтезов и, таким образом, применение больших количеств реагентов, которые сверх того, часто являются дорогостоящими, существует потребность, с точки зрения снижения стоимости, использовать настолько малое количество образца, насколько возможно. Следовательно, имеются возможности для поиска путей миниатюризации подобного пeптиднoгo синтеза.
Способ миниатюрного синтеза пептидов недавно описан в статье Fodor, S.P. A. et al. (15 February 1991) pp.767-773). Здесь для управления одновременными синтезами большого числа различных химических соединений используют свет. Синтез происходит на твердой основе, такой как стеклянная пластина. Основу аминируют путем обработки 0,1%-ным аминопропилтриэтоксисиланом в 98%-ном этаноле. Сюда затем вводят светочувствительную защитную группу, причем упомянутая группа исчезает при последующем облучении и образует реакционноспособное место, к которому может быть присоединен элемент структуры, такой как аминокислота. Шаблон, через который воздействуют светом или иной формой энергии (например, через маску), определяет, какие пространства активируются для химического присоединения. Всю поверхность приводят в контакт с элементом структуры, который присоединяют (причем упомянутый элемент структуры также содержит светочувствительную защитную группу). Реакция сочетания будет происходить только в местах, активированных светом на предыдущей стадии. Подложку затем экспонируют через другую маску, и следующий элемент структуры может быть введен в нужном месте. Рисунок маски и последовательность реагентов определяют последовательности образовавшихся пептидов. При таком подходе может быть достигнута высокая степень миниатюризации. Например, можно синтезировать 40000 различных пептидов на 1 см2.
Однако этот способ имеет ряд недостатков. Удаление защитной светочувствительной группы (в статье называют нитровератрилоксикарбонил) происходит при облучении в течение 20 мин ртутной лампой, имеющей мощность 12 мВт/см3. Это приведет в результате к очень длительному синтезу в случае синтеза более длинных пептидов. Кроме того, на каждой стадии присоединения должна использоваться другая маска, и для каждой серии пептидов должны использоваться различные комплекты масок.
Более того, на каждой стадии присоединения может быть добавлен только один структурный элемент, потому что различные пептиды, которые синтезируют, не разделяются пространственно. Очевидно, что так или иначе будет происходить смешение реагентов и, таким образом, нежелательные продукты также будут образовываться. Поэтому этот способ является очень трудоемким, особенно при синтезе пептидов, которые различаются не только по длине, но также и по последовательности.
Авторы статьи также указывают на проблему надежности синтеза. Могут иметь место пропуски как следствие неполного удаления защитной группы после облучения светом. Чистый выход сочетания составляет 85-95%. Кроме того, при смене масок может происходить некоторый перехлест различных участков синтеза вследствие дифракции света, внутреннего отражения и рассеяния. Следовательно, в участках, которые считаются темными, будут образовываться соединения, в результате могут иметь место вставки из определенной аминокислоты.
В заявке на патент Франции FR-A-2 383 442 (Institut Pasteur) дается решение проблемы миниатюризации. Решение предполагает осуществление миниатюрных реакций с помощью вспомогательных средств, таких как центрифугирование и дополнительное вместилище для текущей реакции. Объем микрокюветы, описанной в цитированной работе, может составлять порядка нескольких микролитров, однако микрокювета предназначена только для измерений образца, который уже претерпел реакционные стадии, требовавшие другого значительно большего вместилища. При изучении цитированной работы очевидно, что микрокювета не подходит для осуществления реакции. Демонстрируется более сложная конструкция, для которой требуются промежуточное вместилище и стадия центрифугирования для осуществления реакции, после чего реакционная смесь в осевшем виде перемещается в микрокювету. В частности, так как такая реакция, как PEPSCAN включает большое число реакционных стадий, влекущих за собой некоторое количество стадий промывания, способ, как он преподан в упомянутой работе, не подходит для осуществления миниатюрного PEPSCAN.
В основу изобретения, которое относится к тестирующему устройству, положена задача решить описанные выше проблемы миниатюризации и сделать его подходящим для применения при био- и/или иммунохимических исследований, таких как ELISA, и исследований, при которых применяют синтез пептидов, например, PEPSCAN, как описано выше.
Поставленная задача решается тем, что тестирующее устройство, которое включает пластину, содержащую множество ячеек, которые согласно изобретению имеют объем в пределах 0,1-20,0 мкл, при этом диаметр ячеек составляет 1,0-4,0 мм. Размеры ячеек будут выбираться в зависимости от цены и наличия образцов и реагентов, которые используются. Вообще предпочтительными будут ячейки, которые настолько малы, насколько возможно, и, следовательно, настоящее изобретение предпочтительно относится к тестирующему устройству, в котором ячейки имеют объем в пределах 0,1-5,0 мкл.
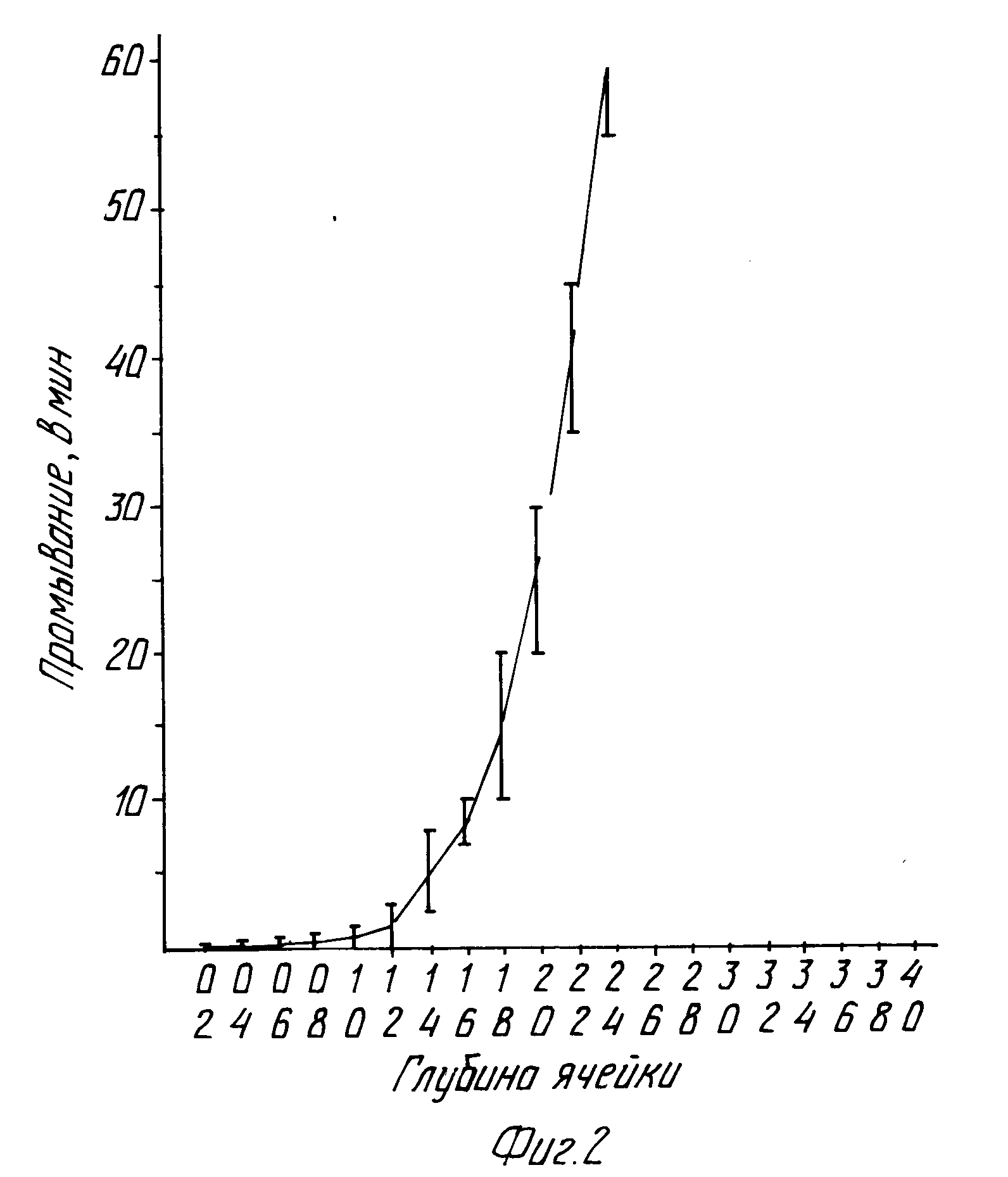
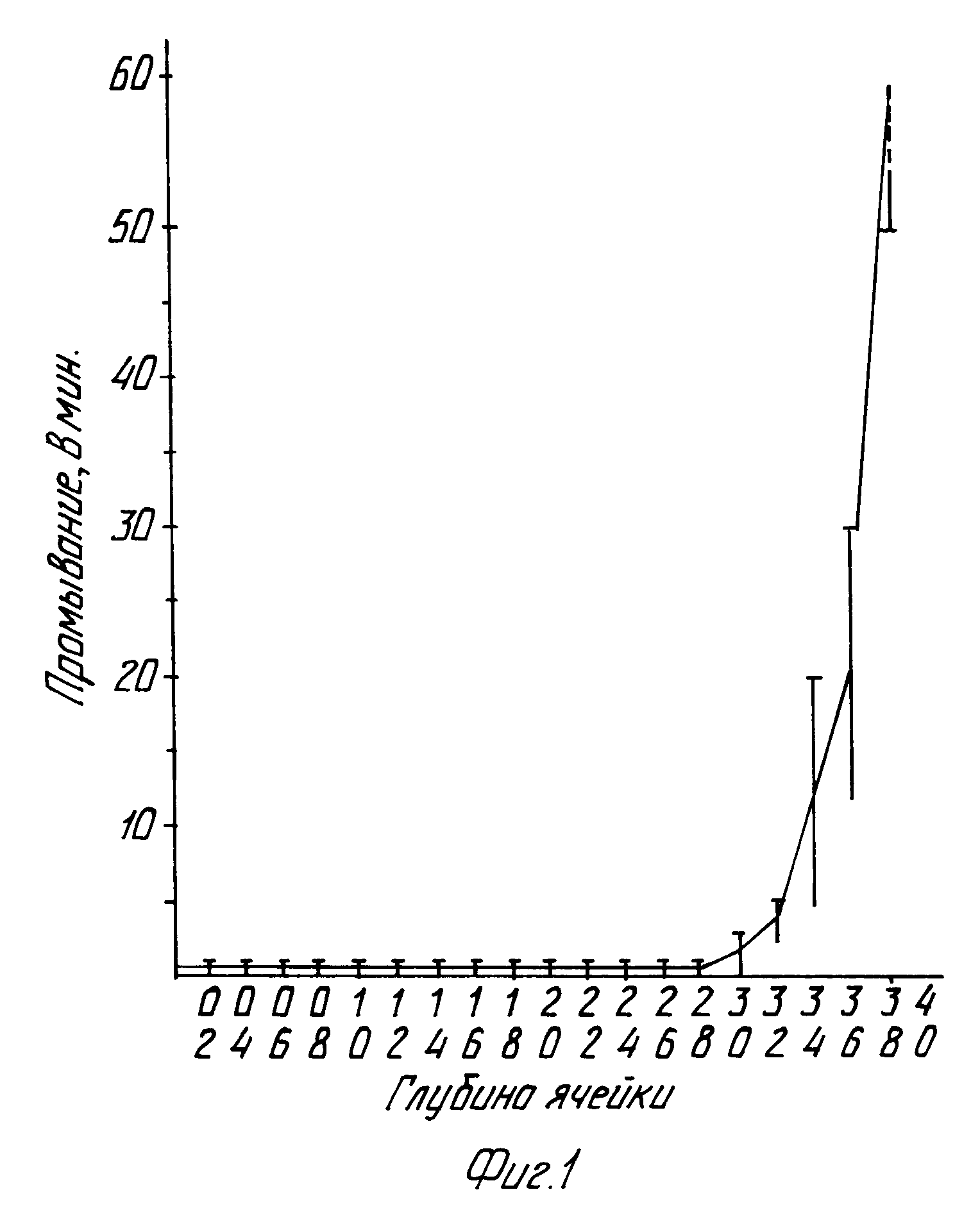
В полную противоположность ожиданиям найдено, что изготовление ячеек меньшего размера не оказывает вредного действия на возможность их эффективного промывания. Найдено, что времена промывания, необходимые для получения хорошего промывания, являются самыми короткими, если соотношение между глубиной ячеек и их диаметром составляет менее 1:1. Следовательно, тестирующее устройство, включающее пластину, содержащую множество ячеек, отличающееся тем, что ячейки имеют объем в пределах 0,1-20,0 мкл и диаметр ячеек составляет 1,0-4,0 мм и, кроме того, имеющее соотношение между глубиной ячеек и их диаметром менее 1:1, является очень подходящим. Предпочтительным является тестирующее устройство, соответствующее изобретению, в котором соотношение между глубиной ячеек и их диаметром составляет менее 2:3.
На фиг. 1 и 2 показаны результаты испытаний, в которых исследовалась возможность промывания в различных тестирующих устройствах. Тестирующие устройства имеют один и тот же диаметр ячеек (2 мм), но различную глубину. Возможность промывания исследуют на приборе для встряхивания при скоростях 47 и 40 соответственно. Глубину ячейки в мм откладывают против времени в минутах, необходимого для должным образом осуществленного промывания ячейки.
Изобретение предпочтительно нацелено на тестирующее устройство, в котором предпочтительными являются ячейки с диаметром 1,0-2,0 мм. Выбор размеров ячейки будет зависеть от желаемого специфического испытания, для которого используют тестирующее устройство: чем меньше диаметр, тем меньше требуемый объем образца.
В связи с требованием возможности хорошего промывания также предпочтительно, чтобы ячейки имели такую форму, при которой вертикальное сечение ячеек имеет по существу U-образную форму, причем переход между ножками и основанием U является плавным. Предпочтительно, чтобы в ячейке отсутствовали острые углы.
Некоторые подходящие формы ячеек показаны на фиг. 3.
U-образная форма, при которой угол между основанием и стенками является прямым, предпочтительна для фотометрических определений, при которых измерения выполняют снизу и сквозь пластину.
Тестирующее устройство, соответствующее изобретению, предпочтительно будет представлять собой пластину, содержащую ячейки, разделенные сплошными перегородками шириной от 1,0 до 5,0 мм, предпочтительно - с перегородками шириной от 1,0 до 2,0 мм. Перегородки должны быть достаточно широкими, чтобы предотвращать перетекание реагентов из одной ячейки в другую. Особенно перегородки должны быть достаточно широкими, когда в качестве растворителя применяют ДМФА, как это часто случается при синтезе пептидов. Это потому так, что известно, что ДМФА обладает способностью сильно растекаться.
Тестирующее устройство, соответствующее изобретению, в подходящем варианте осуществления изобретения будет включать в себя пластину, содержащую 5 - 20 ячеек на 1 см2, предпочтительно 10 - 15 ячеек на 1 см2.
Кроме того, в подходящем варианте осуществления изобретения тестирующее устройство будет включать материал, к которому способны прилипать пептиды, белки и другие биомолекулы, такие как молекулы гормонов и полисахаридов. Для тестирующих устройств, пригодных для исследований с синтезом пептидов, такой материал будет предпочтительно представлять собой материал, к которому способны прилипать пептиды и белки (например, полиэтилен или полистирол).
Другими подходящими примерами материалов, которые могут быть использованы в тестирующем устройстве, соответствующем изобретению, являются полипропилен и поликарбонат.
Выбор материала для тестирующего устройства будет также зависеть от реагентов, которые используют в таком тестирующем устройстве, и от метода определения. В случае, например, фотометрического анализа через дно тестирующего устройства по крайней мере дно ячеек должно быть изготовлено из прозрачного материала. В случае испытаний, при которых в качестве растворителя применяют ДМФА, нельзя использовать тестирующее устройство из полистирола, поскольку ДМФА слишком агрессивен.
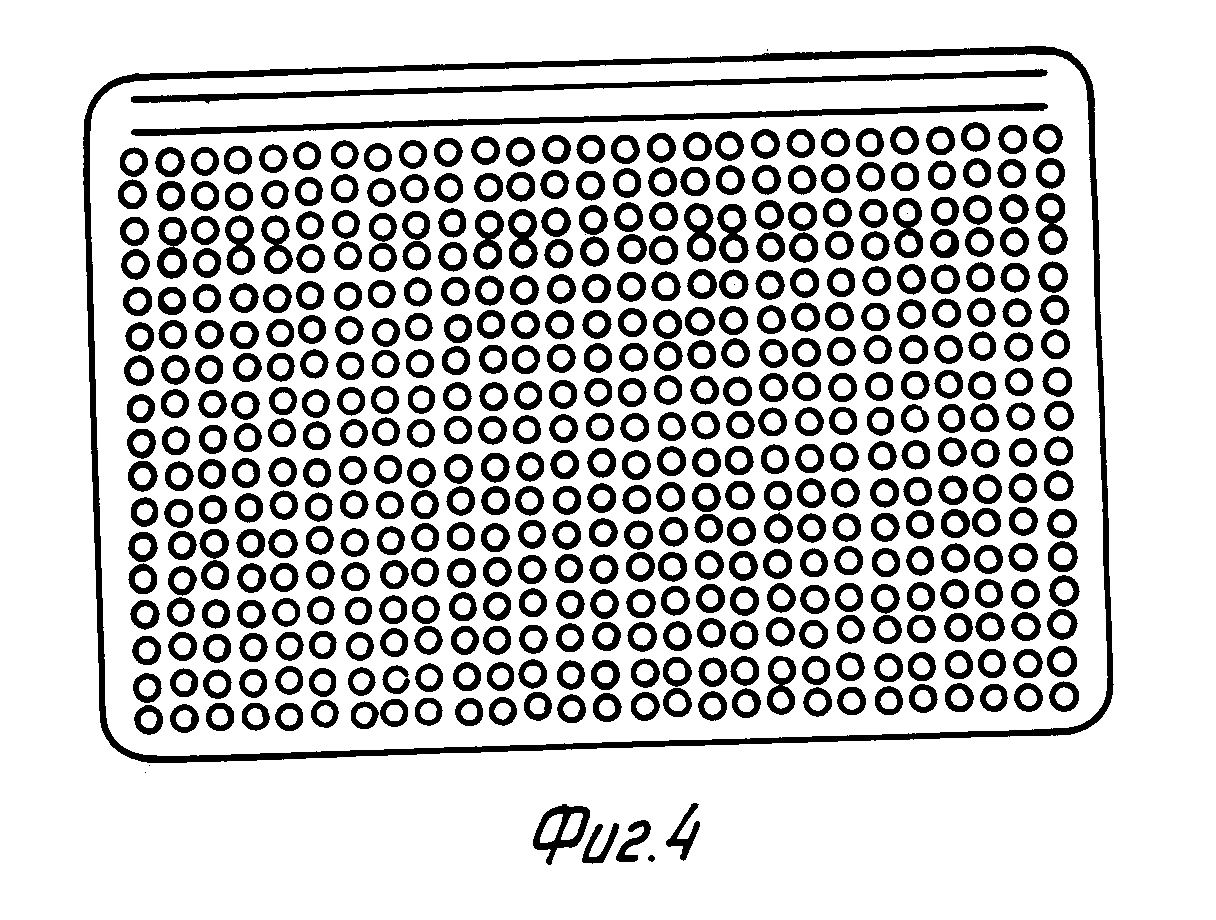
Предпочтительный вариант тестирующего устройства будет снабжаться средствами регистрации информации, например, полосковым кодом (bar code) или магнитной лентой. Тестирующее устройство может быть снабжено информацией, относящейся к испытанию, которое собираются осуществлять или которое осуществляют, например, такой, которая относится к реагентам или образцам, которые используют. Тестирующее устройство также может быть снабжено маркировкой, указывающей координацию ячеек в тестирующем устройстве.
На фиг. 4 показан один из вариантов осуществления тестирующего устройства, соответствующего изобретению, вид сверху; на фиг. 5 показан поперечный разрез тестирующего устройства.
Как упоминалось, изобретение также имеет своей задачей осуществить способ выполнения (био- и/или иммуно)химических исследований, при которых используют тестирующее устройство, соответствующее изобретению. Вообще тестирующее устройство, соответствующее изобретению, может быть использовано для тех же исследований, для которых используют известную пластину микротитратора. Теперь можно осуществлять существующие способы, используя намного меньшие количества образца и реагентов, и проводить так называемые мини-тесты. Существует возможность снизить количество образца в сто крат и использовать 2,5 мкл вместо 250 мкл образца на ячейку. Применение тестирующего устройства, соответствующего изобретению, теперь делает значительно привлекательнее массовый скрининг различных групп населения, поскольку значительно меньше требуется крови от донора, а также реактивов.
Другое большое преимущество миниатюризации методов за счет использования тестирующего устройства, соответствующего изобретению, заключается в отсутствии необходимости модифицировать существующие химические способы. В этом смысле большое преимущество имеется, например, в случае автоматизированных процессов, таких как PEPSCAN. Тестирующее устройство является особенно подходящим для применения при способах, в которых используют большое число образцов. Мини-ELISA и мини-PEPSCAN, в которых используют тестирующее устройство по изобретению, являются подходящими примерами способа, соответствующего изобретению. Преимущество мини-способа по изобретению состоит в том, что исследование может быть выполнено с образцом в количестве менее 20 мкл. Здесь без труда можно использовать количество образца менее 5 мкл.
Также в основу изобретения положена задача создать дозирующее устройство, пригодное для одновременного введения равных объемов реагента в различные ячейки дозирующего устройства, соответствующего изобретению. Это дозирующее устройство может применяться для того, чтобы максимально эффективно осуществить иммуно- и/или биохимические исследования, при которых применяют тестирующее устройство по изобретению. В связи с этим рассматривают необязательную автоматизацию некоторых методов, соответствующих изобретению.
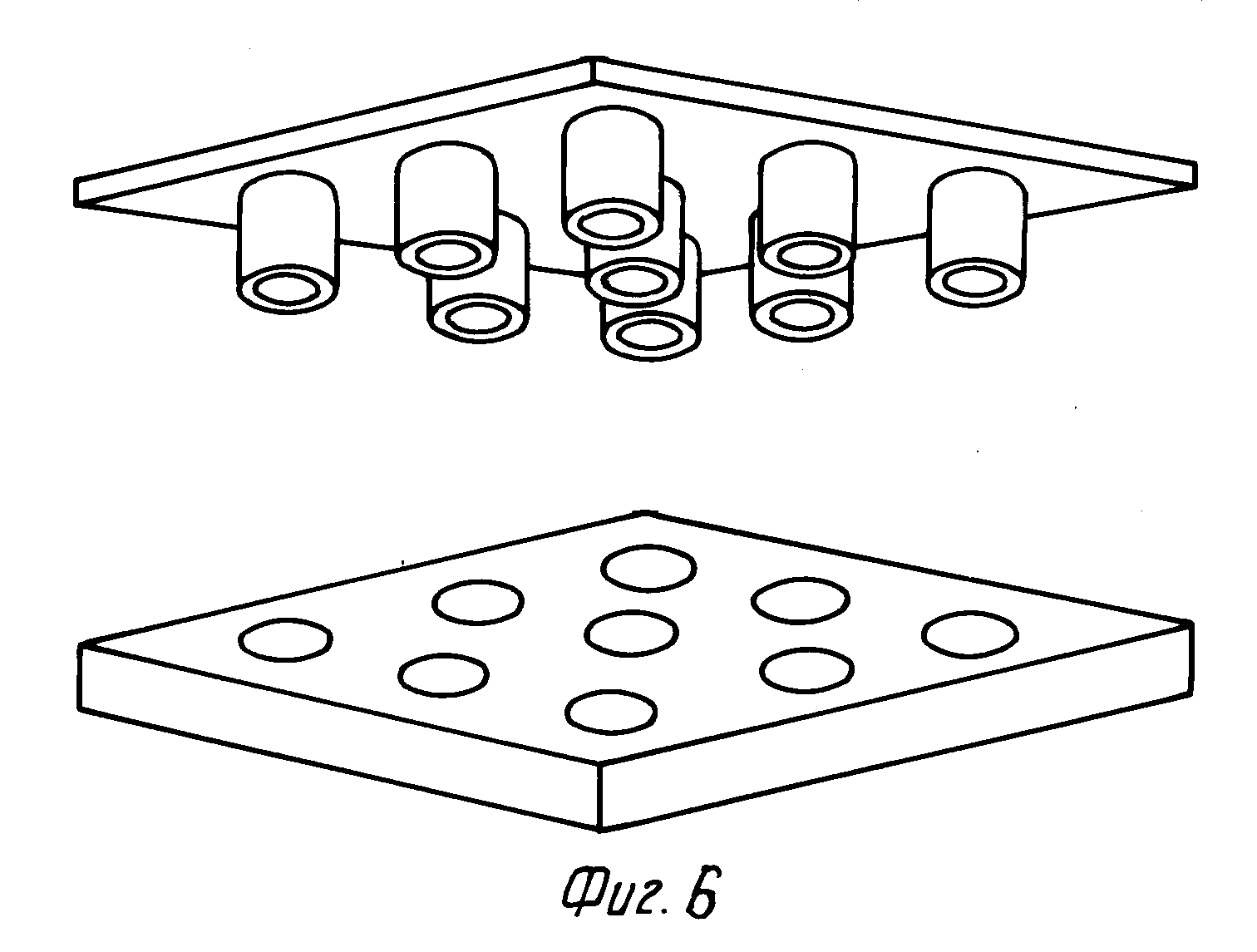
Если предварительно установленное одинаковое количество реагента должно быть введено одновременно в некоторое количество ячеек, то существует возможность использовать дозирующее устройство по изобретению, причем упомянутое устройство снабжают выступами, имеющими такие размер и взаимное расположение, чтобы отдельные выступы могли одновременно располагаться или выше ячеек тестирующего устройства, соответствующего изобретению, или в них. При дозирующем устройстве такого типа все ячейки могут быть одновременно снабжены равными объемами реагента, если положение выступов таково, что по существу соответствует расположению ячеек в тестирующем устройстве, соответствующем изобретению.
Один из вариантов дозирующего устройства и тестирующего устройства показан на фиг.6.
Если должны быть заполнены не все, а только некоторые ячейки тестирующего устройства, может быть использовано дозирующее устройство, которое имеет выступы, расположененные над выбранными ячейками.
На фиг.7 более темные ячейки представляют собой выбранные ячейки. Выступы на дозирующем устройстве располагаются таким образом, чтобы они могли одновременно расположиться над более темными ячейками или прямо в них.
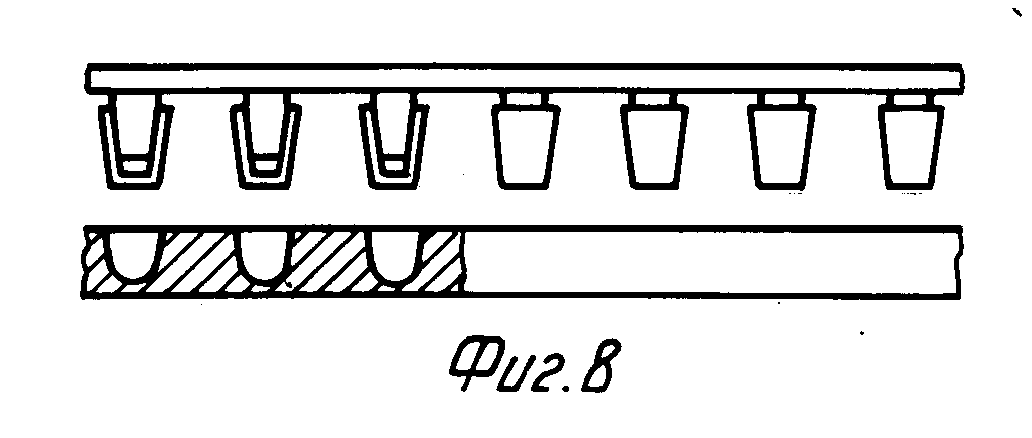
Для этого может быть успешно использовано дозирующее устройство, в котором выступы зафиксированы на опоре или могут быть зафиксированы в шаблоне, который соответствует рисунку ячеек, в которые должен быть введен реагент.
На фиг. 8 представлен пример варианта осуществления дозирующего устройства, в котором выступы могут быть зафиксированы на опоре.
Дозирующее устройство может включать выступы, которые фиксируются или могут быть зафиксированы на опоре по способу, эквивалентному щетинкам на щетке (фиг. 6 - 8).
Дозирующее устройство, в котором выступы фиксируются (фиг. 9) или могут быть зафиксированы (фиг. 10) у своих вершин к опоре, также является вариантом дозирующего устройства по изобретению, который весьма подходящий. Число выступов может быть меньшим или равным числу ячеек, образующих ряд в продольном направлении тестирующего устройства. Число выступов может быть меньшим или равным числу ячеек, образующих ряд в поперечном направлении тестирующего устройства. Число выступов будет зависеть от схемы расположения ячеек дозирующего устройства, в которые должен быть введен реагент.
Выступы дозирующего устройства, соответствующего изобретению, могут составлять единое целое с опорой или могут быть съемными. Выступы могут быть установлены на опоре таким образом, что будут образовывать рисунок, который соответствует схеме расположения ячеек, которые должны быть заполнены в тестирующем устройстве (фиг. 7).
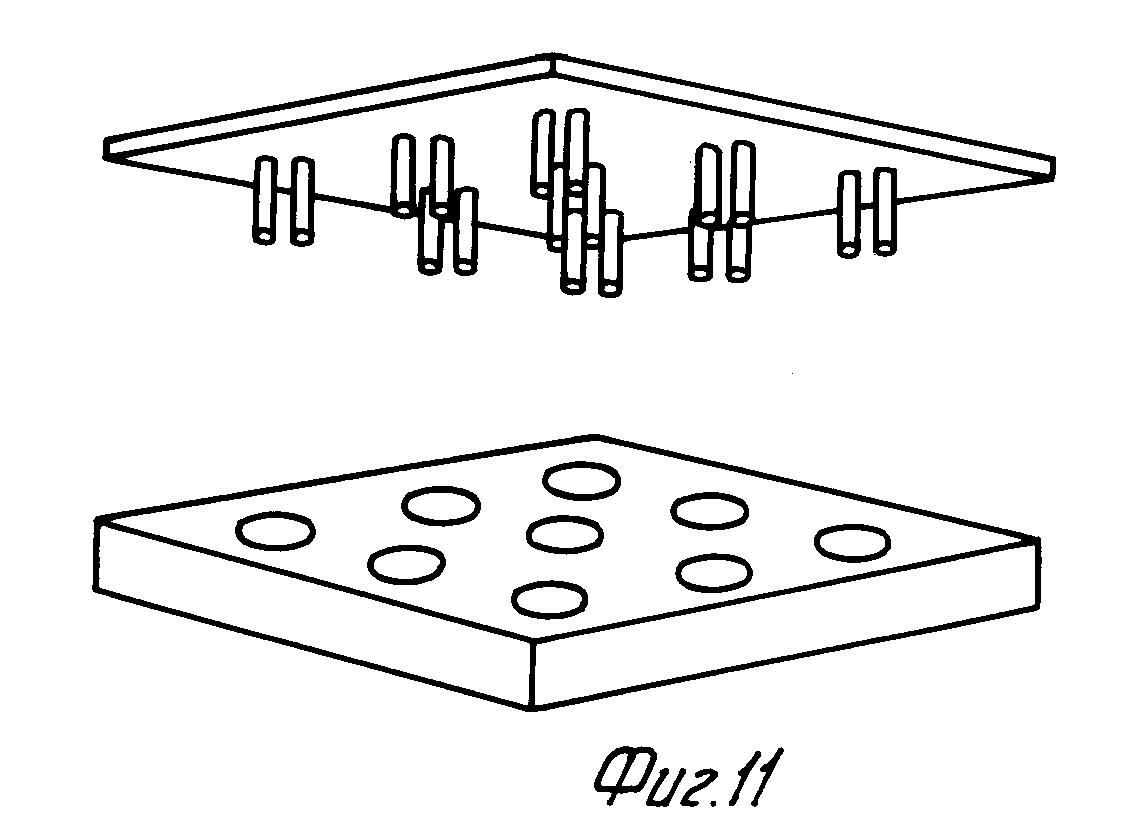
Также возможно использовать дозирующее устройство, в котором над или в ячейке могут быть установлены несколько выступов одновременно, если в ячейку требуется ввести одновременно несколько единиц реагентов.
На фиг. 11 показано дозирующее устройство, в котором два выступа могут быть установлены над каждой ячейкой либо прямо в них.
Таким образом, количество реагента, которое присутствует на выступе, может быть принято за стандарт, при этом могут использованы быть дозирующие устройства, имеющие группу выступов или в ячейке или над ней, зависящую от соотношения, в котором требуется вводить реагент в ячейки. Группа будет включать число выступов, которое соответствует числу требуемых единиц реагента.
В случае дозирующего устройства, соответствующего изобретению, выступы могут быть полными, но они также могут быть сплошными или закрытыми у дна. Последние две возможности являются предпочтительными при работе с очень малыми количествами образца и реагента, поскольку в таких случаях можно работать с каплями реагента.
Изобретение также имеет своей задачей осуществить способ выполнения (био- и/или иммуно) химического исследования с использованием дозирующего устройства,
соответствующего изобретению. При этом способе
выступы дозирующего устройства снабжают реагентом таким образом, что по существу равные объемы реагента присутствуют на отдельных выступах
дозирующего устройства или в них;
дозирующее устройство затем устанавливают над ячейками тестирующего устройства, соответствующего изобретению, либо прямо в ячейках, которые предназначены для
введения реагента, причем каждый отдельный выступ располагается в одно и то же время или в ячейке, или над ячейкой;
по существу равные объемы реагента вводят в отдельные ячейки тестирующего
устройства, которые предназначены для введения реагента.
Изобретение также относится к способу такого типа, при котором выступы дозирующего устройства одновременно снабжаются реагентом путем погружения выступов в реагент.
В изобретении также заявлен набор, который включает по меньшей мере тестирующее устройство и дозирующее устройство, соответствующие изобретению. Подобный набор может включать некоторое число дозирующих устройств в различных вариантах, описанных выше, и может также включать заменяемые выступы для таких дозирующих устройств.
Пример 1. Миниатюризованный синтез пептидов. Миниатюризованный синтез полной трипептидной сетки (8000 различных пептидов) осуществляют, используя дозирующие устройства, соответствующие изобретению. Тестирующее устройство, используемое в этом примере, напоминает по размеру кредитную карточку и сконструировано таким образом, что включает 455 ячеек диаметром 2 мм максимальным объемом 5 мкл каждая. Тестирующее устройство изготовляют из полиэтилена. Для того, чтобы этот твердый носитель сделать пригодным для пептидного синтеза, ячейки обрабатывают по способу Geysen et al. (1984), упомянутому ранее. Карбоксильные группы полиакриловой кислоты снабжаются NH2-группами через реакцию соединения с линкером трет-бутоксикарбонилгексаметилендиамином БОК-ГМДА в присутствии N, N-дициклогексилкарбодиимида и N-гидроксибекзотриазола (DDC/HOBT). Все подобные связывающие реакции осуществляют в диметилформиде (ДМФА).
После удаления трет-бутоксикарбонильной группы трифторуксусной кислотой (TFA) для присоединения смеси всех двадцати L-аминокислот используют тот же метод, который используют для присоединения линкера.
Общий объем, который используют в реакции присоединения, составляет 3 мкл для каждой ячейки. Подача пипеткой требуемых малых количеств достигается полностью автоматически с использованием управляемого компьютером автоматического держателя с пипеточным устройством (Hamilton Microlab 2200). Для этого составляют специальное программное обеспечение, позволяющее наполнять два тестирующих устройства, соответствующих изобретению, в 1 ч.
Время присоединения каждой аминокислоты составляет приблизительно 2-3 ч. Различие во времени соединения вызывается торможением реакции, когда реакционная смесь полностью испаряется.
Потом после удаления БОК-группы с TFA следующую аминокислоту присоединяют таким же образом, далее цикл повторяют дважды.
После последней реакции присоединения и после удаления БОК-группы концевую NH2-группу ацетилируют смесью ангидрида уксусной кислоты, ДМФА и триэтиламина в соотношении 2:5:1. Группы, защищающие боковые группы, удаляют в сильнокислой среде. В этом примере используют бор- трис-трифтор-уксусную кислоту (BTT) в TFA (30 мг/мл), реакцию осуществляют в течение 2 ч при комнатной температуре.
Общая
структура пептида имеет вид
Ac - A3 - A2 - A1 - X - носитель
где Ас означает ацетильную группу;
AX представляет собой отдельную
аминокислоту;
X - представляет собой смесь аминокислот.
Пример 2.Elisa. Прежде чем инкубировать пептиды с сывороткой, тестирующие устройства, соответствующие изобретению, промывают фосфатно-солевым буферным раствором (PBS, 3•10 мин), после чего тестирующие устройства предварительно покрывают в течение 1 ч при 37oC смесью 10%-ной лошадиной сыворотки, 10%-ного яичного альбумина и 1%-ного твина 80 в PBS (SuperQ), чтобы предотвратить неспецифическую абсорбцию антител. Тестирующие устройства, соответствующие изобретению, полностью погружают в жидкость.
Наполнение ячеек тестирующего устройства разбавленной сывороткой можно осуществить двумя способами. Если в распоряжении имеется только немного сыворотки, тестирующие устройства могут быть заполнены с использованием автоматического устройства, упомянутого в предыдущем примере, а когда сыворотки достаточно, тестирующие устройства могут быть погружены в сыворотку и затем вытерты, и все ячейки одновременно наполняются.
Инкубацию тестирующих устройств проводят в течение ночи при 4oC в воздушной атмосфере, насыщенной водой, после чего тестирующие устройства три раза промывают 0,05%-ным твином 80 в PBS, чтобы удалить антитела, которые остались несвязанными. Тестовые устройства, соответствующие изобретению, которые инкубированы с сывороткой, затем инкубируют в течение 1 ч при 37oC с соединяющимся с антителом ферментом пероксидазой (раствор в SuperQ 1/1000) путем погружения тестирующих устройств в раствор, содержащий упомянутый фермент. После этого тестирующие устройства промывают PBS, 3•10 мин. Присутствие второго антитела демонстрируют с субстратом жидкости ABTS (2,2'-азин-ди-3-этил-бензтиазолинсульфонат (6)). В этом примере также возможно применение двух вышеупомянутых способов наполнения ячеек, используя либо автомат, либо погружение устройств в субстрат.
Реферат
Изобретение относится к области микробиологического анализа. Тестирующее устройство представляет собой пластину, содержащую множество ячеек. Объем ячеек составляет от 0,1 до 20 мкл при их диаметре от 1,0 до 4,0 мм. Ячейки отделены друг от друга сплошными перегородками и выполнены из материала, способного сорбировать биохимические молекулы. При реализации способа пластину с ячейками используют известными способами микробиологического анализа. Предпочтительно использовать методы PEPSCAN или ELISA. Дозирующее устройство выполнено в виде пластины, на которой размещены выступы с возможностью одновременного помещения всех выступов в ячейки тестирующего устройства. На выступы помещают реагент, взаимодействующий с биохимическими молекулами в ячейках. 5 с. и 20 з.п. ф-лы, 11 ил.

Комментарии