Получение диоксида хлора - RU2519108C2
Код документа: RU2519108C2
Описание
Родственные заявки
Настоящая заявка притязает на приоритет заявки США с серийным номером 61/173,442, поданной 28 апреля 2009 года, которая включена в настоящий документ в ее полном объеме.
Область техники
Настоящее изобретение относится к получению диоксида хлора и, более конкретно, относится к усовершенствованному способу получения диоксида хлора, в котором проходящее преобразование хлорита в диоксид хлора имеет эффективность, ранее неизвестную для конкретных реагентов, с использованием системы из двух химических веществ, применяющей серную кислоту/хлорит натрия, и в которой прекурсоры могут оставаться в реакторе в течение длительного времени до разбавления без потери диоксида хлора путем реакции с водой для образования хлората, как сообщалось для случаев, когда в качестве донора протонов использовали соляную кислоту.
Описание уровня техники
Диоксид хлора является мощным окислителем и дезинфицирующим веществом. Применение диоксида хлора охватывает широкий спектр от дезинфекции пищевых продуктов и питьевой воды, обработки технологических вод, дезодорации, уничтожения речной дрейссены, уничтожения бактерий сибирской язвы, дезинфекции медицинских отходов, обработки сточных вод до интенсификации притока в нефтяные и нагнетательные скважины, беления целлюлозы и отбеливания тканей.
Диоксид хлора не доступен в продаже или может быть трудно доступен для каждого применения, где он может использоваться. В некоторых ситуациях регулирующие и экономические ограничения предполагают, что диоксид хлора нельзя транспортировать, и вместо этого он должен быть произведен на месте во время использования. Необходимости в его получении породила гамму способов, в которых прекурсоры из относительно небольшая группа объединяют разными путями. Их можно разбить на группы в зависимости от прекурсора и способа преобразования.
Два обычно незаменимых прекурсора, на которых построены многие способы получения диоксида хлора, это хлорат натрия, NaClO3, и хлорит натрия, NaClO2. Хлорат натрия из них двух стоит дешевле и как таковой стал предпочтительным прекурсором для бумажной промышленности, которая ежедневно использует диоксид хлора тоннами для беления и делигнификации целлюлозы, а также для таких применений как биологический контроль в конце мокрой части бумагоделательной машины. Снижение расходов на химические вещества оправдывает инвестиции в стойкое к коррозии, управляемое оператором оборудование из титана, подходящее для выполнения кислотного преобразования хлората. Существует коммерчески доступный маломасштабный способ с тремя химическими веществами для преобразования хлората согласно патенту США №6,790,427, который включен в настоящий документ в полном объеме путем ссылки. Этот способ предлагает сочетание концентрированной серной кислоты и патентованную смесь хлората натрия и перекиси водорода для преобразования хлората в диоксид хлора.
Другие известные способы получения используют хлорит натрия, несмотря на его более высокую стоимость, из-за относительной легкости преобразования. Способы преобразования могут быть охарактеризованы как таковые с одним веществом, двумя веществами и тремя веществами, где каждый имеет конкретное преимущество. Способ с одним химическим веществом включает электролитическое окисление аниона хлорита и. воздействие ультрафиолетовым светом. Существующие электролитические способы могут давать сотни фунтов диоксида хлора в сутки, тогда как ультрафиолетовые способы полезны тогда, когда достаточно нескольких фунтов в сутки.
Ввиду указанных недостатков существующего уровня техники было бы желательно создать усовершенствованный способ получения диоксида хлора с использованием двух химических веществ - прекурсоров, который может обеспечивать высокие скорости преобразования, может быть выполнен на месте при необходимости и может быть проведен масштабируемым образом, чтобы выполнять потребности крупных пользователей ClO2, таких как бумажные фабрики, и мелких пользователей, таких как частные предприятия по обработке воды.
Кроме того, известны многие способы с использованием кислоты и хлорита. Как известно, такие способы, где используется соляная кислота, обеспечивают не больше чем теоретические 80% преобразования используемого хлорита в диоксид хлора, при выходе на практике близком к 70%. В качестве кислоты при получении диоксида хлора из хлорита обычно используют разбавленную (9-15%, по массе) соляную кислоту. Концентрированную серную кислоты нельзя соединять непосредственно с хлоритом, поскольку они бурно реагируют и создают значительное количество теплоты, что приводит к улетучиванию полученного диоксида хлора и возможности повреждения используемого пластикового оборудования.
Поэтому было бы желательно иметь способ, в котором используется разбавленная серная кислота для получения диоксида хлора и который имеет повышенную эффективность преобразования по сравнению с известной для этого химического процесса при небольшом (или при отсутствии) преобразовании полученного диоксида хлора в хлорат даже при длительном времени выдержки в реакторе. Такое повышение эффективности преобразования даст очевидные экономические преимущества по сравнению с известными способами.
РАСКРЫТИЕ ИЗОБРЕТЕНИЯ
Настоящее изобретение предлагает усовершенствованный способ получения диоксида хлора с использованием двух химических веществ - прекурсоров. Описанные здесь варианты осуществления изобретения основаны на работе, которая описана в патенте США №7,407,642. Посредством дополнительных экспериментов авторы изобретения выявили, что использование серной кислоты в концентрациях, которые ранее считались небезопасными и невозможными, в действительности может быть реализовано безопасным образом для достижения более высоких выходов диоксида хлора. В частности, авторы изобретения установили, что серная кислота в концентрации выше 50% по массе может быть введена в реакцию с растворами хлорита натрия от 7,5 до 20% по массе. В одном варианте осуществления некоторый объем серной кислоты при 55-75% по массе соединяют в реакционной камере с некоторым объемом водного хлорита натрия при 7,5-20% по массе позволяют реагировать в течение заданного периода времени. В более конкретном варианте осуществления, некоторый объем серной кислоты 60-67% по массе реагирует с некоторым объемом хлорита натрия 7,5-15% по массе. Эти объемы могут быть в соотношениях от 0,1-10,0 до 10-0,1. В более конкретных вариантах осуществления соотношения объемов составляют 1-10:10-1, 1-5:5-1, 1-2:2-1, 1-1,5:1,5-1 или 1:1.
В одном иллюстративном варианте осуществления изобретения установлено, что при первоначальном разбавлении концентрированной серной кислоты водой до 55-75% кислоты по массе и последующем остывании горячего раствора кислоты полученную кислоту можно безопасно соединять непосредственно с хлоритом натрия, чтобы получить диоксид хлора в реакции, которая имеет эффективность приблизительно 80%. Это дает ряд неожиданных преимуществ над известными из уровня техники системами кислота-хлорит.
В одном иллюстративном варианте осуществления настоящее изобретение относится к использованию разбавленной серной кислоты при получении диоксида хлора, давая повышенные уровни преобразования, чем ожидались бы для этого химического состава при использовании в способах, известных из уровня техники. Кроме того, получение согласно настоящему изобретению дает ClO2 при небольшом (или при отсутствии) преобразования полученного диоксида хлора в хлорат даже при длительном времени выдержки в реакторе, как происходит при применении способов получения с двумя химическими веществами, включая соляную кислоту.
ПОДРОБНОЕ ОПИСАНИЕ
Предмет настоящего изобретения направлен на новые способы получения диоксида хлора. В одном варианте осуществления в способах настоящего изобретения могут использоваться раствор разбавленной серной кислоты и раствор хлорита натрия как единственные составляющие процесса получения.
Два иллюстративных способа химического преобразования хлорита включают два очень разных пути реакции с разной теоретической эффективностью преобразования. Один способ включает соединения хлорита с окислительным агентом, наиболее часто с водным или молекулярным хлором, и в другом способе используется простое подкисление для осуществления преобразования. Первый имеет теоретическую эффективность преобразования 100% (уравнения 3 и 4), тогда как теоретическая эффективность второго составляет 80% (уравнение 5). На практике фактическая максимальная эффективность составляет 95-98% и 65-75%, соответственно.



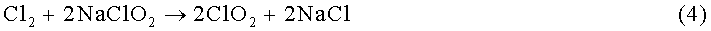
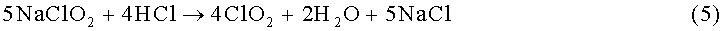
В многих способах получения диоксида хлора широко используется подготовка путем смешивания кислоты и хлорита из-за ее простоты и длительной химической устойчивости этих двух наиболее широко используемых прекурсоров, водного хлорита натрия и соляной кислоты. Типичная коммерчески доступная технология использует 7,5% хлорит натрия и 9% соляную кислоту (уравнение 5). Эти прекурсоры могут быть закачаны в реакционную камеру в надлежащих долях, и смеси позволяют оставаться в концентрированном контакте в течение периода времени, достаточно долгого для отведения времени реакции относительно медленного преобразования перед выпуском в разбавляющую воду, которая доводит раствор диоксида хлора то точки инжекции. Подача насоса при закачке регулируется до необходимого для изготовления требуемого количества диоксида хлора.
Соляная кислота почти универсально используется в качестве кислоты, поскольку считается что ион хлорида является катализатором этого преобразования. Недостаток этой реакции заключается в получении только четырех молекул диоксида хлора при пяти реагирующих ионах хлорита (уравнение 5), но положительные аспекты этого способа в смысле безопасности и надежности тем не менее делают его привлекательным и широко используемым.
Хотя вышеописанный способ имеет привлекательные преимущества, которые обеспечили ему широкое использование, существует фундаментальный недостаток, который должен быть принят во внимание. Преобразование хлорита в диоксид хлора прежде всего происходит с потерей 20% используемого хлорита из-за применяемого химического состава. Эта потеря считается приемлемой в свете легкости способа. При правильном получении эффективность преобразования должна составлять 80%; то есть, каждые пять ионов хлорита должны давать четыре молекулы диоксида хлора. Это обычно не так в реальной практике. Происходит конкурирующая реакция, которая снижает количество получаемого диоксида хлора.
Получение диоксида хлора из кислоты/хлорита происходит не мгновенно, а скорее требует, чтобы прекурсоры находились в концентрированном контакте в течение приблизительно 1-3 минут. Реагенты обычно выдерживают в реакционной камере в течение периода времени, необходимого для осуществления этого преобразования перед инжекцией в разбавляющую воду. Во время преобразования прекурсоров при очень высокой концентрации диоксида хлора, присутствующего в реакторе, диоксид хлора будет реагировать с водой, образуя хлорат и снижая фактический выход на величину, потерянную как хлорат (ссылка 1).

Поэтому реактор имеет размеры для конкретной подачи насоса при закачке, чтобы позволить выполнить полное преобразование при минимуме потери как хлората. Если подача насоса при закачке ниже предназначенных для реактора этих размеров, то прекурсоры и полученный диоксид хлора остаются в зоне реакции больше времени, и происходит большая потеря диоксида хлора при образовании хлората. Объем реактора тогда должен быть компромиссным между достаточно большим, чтобы позволить получить большой объем, и достаточно малым, чтобы ограничить потерю диоксида хлора при низкой подаче, или, если должен использоваться генератор, чтобы получать постоянное количество диоксида хлора, реактор будет иметь размеры для максимального преобразования при желательной подаче насоса.
В почти неизвестном и коммерчески доступном способе с кислотой/хлоритом серную кислоту используют в качестве донора протонов. Для этого есть несколько причин. Во-первых, по сообщениям химический состав с серной кислотой дает только 50% преобразования хлорита в диоксид хлора (уравнение 7). Хотя хлорид является побочным продуктом этой реакции, и можно было бы ожидать, что он явится катализатором преобразования и изменит химический состав на тот, который дает 80% преобразования, концентрация побочного продукта хлорида явно недостаточна для того, чтобы осуществлять значимый катализ в то короткое время, пока реагенты остаются в реакционной камере перед инжекцией в разбавляющую воду.

Другой причиной, по которой серная кислота обычно не используется в преобразовании хлорита, является трудность в работе с концентрированной серной кислотой, которая создает много теплоты при контакте раствора с водой и будет делать реакцию преобразования трудной в управлении и, возможно, вызывать тепловое повреждение производственного оборудования или даже взрывы. Однако авторы настоящего изобретения выяснили, что управляя используемыми соотношениями серной кислоты и хлорита натрия можно безопасно использовать серную кислоту для получения неожиданного выхода диоксида хлора. Авторы настоящего изобретения осознали, что, когда реакция управляемая, производимая теплоты фактически служит для запуска процесса в вышеупомянутом небольшом способами с тремя химическими веществами (кислота/перекись/хлорат) для стимулирования преобразования относительно инертного хлората в диоксид хлора. Единственное известное в Европе использование серной кислоты для преобразования выполняется с намерением удалить ион хлорида из конечного продукта.
Настоящее изобретение устанавливает четвертый новый химический состав кислоты/хлорита с использованием серной кислоты, который, как показывает анализ, дает 75-80% преобразования хлорита натрия в не содержащий хлора и хлорита диоксид хлора.
В настоящем изобретении раствор 7,5-20%, и все целочисленные значения в этом диапазоне, водного хлорита натрия соединяют с предварительно разбавленной и охлажденной 55-70% по массе, и все целочисленные значения в этом диапазоне, водной серной кислотой и позволяют оставаться в контакте на период времени от приблизительно 5 до приблизительно 300 секунд, хотя предпочтительно от приблизительно 30 секунд до приблизительно 60 секунд перед инжекцией в разбавляющую воду. Четырехступенчатой йодометрическое титрование (ссылка 2) показало, что продукт не содержит ионов хлора и хлорита при диапазоне преобразования от 75 до 80% от теоретического. Таким образом, этот способ дает более высокий выход высококачественного диоксида хлора, чем было описано ранее для преобразования хлорита серной кислотой.
В одном конкретном варианте осуществления объем 7,5-15% по массе (и все целочисленные значения в этом диапазоне) хлорида натрия соединяют с объемом 60-67% по массе (и все целочисленные значения в этом диапазоне) водной серной кислоты для получения диоксида хлора. В более конкретном варианте осуществления используется 64-66% по массе водной серной кислоты.
Путь, по которому может происходить это преобразование, заключается в том, что хлорит сначала преобразуется в хлористую кислоту, и затем в высоко концентрированной среде хлористая кислота преобразуется в диоксид хлора в порядке, аналогичном тому, который происходит при преобразовании соляной кислоты/хлорита, где 5 молекул хлористой кислоты дают 4 молекулы диоксида хлора, и одна молекула хлористой кислоты возвращается в хлорид (уравнение 9).
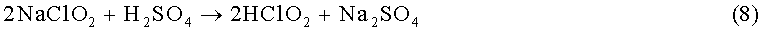

Примеры приведены в таблицах 1 и 2. Отношение титрования "В" (объем титранта, указывающий концентрацию иона хлорита) к титрованию "А" (объем титранта, указывающий концентрацию диоксид хлора) указано как колонка В:А. Идеальное преобразование должно давать отношение 4,0, поскольку каждая молекула диоксида хлора на этапе А титрования производит один анион хлорита, и каждый произведенный анион хлорита при подкислении на этапе В реагирует с объемом титранта в четыре раза больше, чем диоксид хлора.
В таблице также показано, что низкие выходы получают, если использовано недостаточно кислоты, но после достижения правильного отношения эффективность преобразования относительно нечувствительна к присутствию избытка серной кислоты, а также к времени выдержки в реакторе, где можно было бы ожидать, что длительное время выдержки приведет к потере диоксида хлора из-за реакции с водой с образованием хлората, как это происходит в генераторах соляная кислота/хлорит. Этот механизм распада явно не происходит в химическом составе для получения хлорита с серной кислотой. Пробы выдерживали в реакторе в течение периода времени до 15 минут без значительной потери диоксида хлора. В одной серии экспериментов эквивалентные объемы 7,5% хлорита натрия и 64,8% серной кислоты реагировали в течение 1,5 и 15 минут до разбавления. Анализ показал, что диоксид хлора, полученный в этих трех экспериментах, составил 37,8, 37,8 и 35,0 частей на миллион, соответственно, показав почти отсутствие потерь при увеличении времени выдержки на коэффициент 15. Это означает, что используемый реактор достаточно большой и поэтому может вмещать больше прекурсоров без потери продукта, позволяя масштабировать генератор на более высокую производительность чем обычные генераторы хлорит/соляная кислота.
Существует ряд способов измерения или количественного определения диоксида хлора в растворе. Принятая стандартная практика количественного определения диоксида хлора заключается в использовании четырехступенчатого йодометрического титрования. В таблице 3 показан выход, полученный в результате реакции растворов 7,5-10% хлорита натрия с серной кислотой разной концентрации, при которой преобразование хлорита в диоксид хлора превышает 85%, а в некоторых случаях превышает 100%. Хотя невозможно получить выход свыше 100%, сейчас не существует способов анализа для опровержения этого преобразования хлорита в диоксид хлора, приближающегося к 100%, с использованием этих концентраций хлорита натрия.
Использование диоксида хлора в качестве дезинфицирующего вещества и окислителя широко принято во всем мире. Настоящее изобретение предлагает способ, дающий значительные технологические и экономические преимущества над известными способами, чтобы сделать получение диоксида хлора более практичным для широкого диапазона применений.
В одном варианте осуществления предмет изобретения направлен на добавление охлажденной разбавленной серной кислоты к раствору хлорита натрия. В предпочтительном варианте осуществления соединения разбавленной серной кислоты с раствором хлорита натрия выполняют в реакционном сосуде с выпускным отверстием в поток очищаемой среды, так что реагенты не разбавляются, пока реакция не будет завершена.
Реферат
Изобретение может быть использовано в химической промышленности. Способ преобразования двух химических веществ для получения диоксида хлора включает реакцию 7,5-20% по массе водного раствора хлорита натрия с 55-75% по массе водной серной кислоты в реакционной камере. При этом обеспечивается реагирование водного раствора хлорита натрия и водной серной кислоты в течение приблизительно от 5 секунд до приблизительно 300 секунд с преобразованием 75% или больше ионов хлорита в растворе хлорита натрия в диоксид хлора. Изобретение позволяет повысить выход диоксида хлора при обеспечении безопасности процесса.3 н. и 19 з.п. ф-лы, 2 табл.
Формула
охлаждение разбавленной водной серной кислоты для удаления теплоты реакции перед началом реакции.
введение водного раствора хлорита натрия с концентрацией в диапазоне 7,5-20% по массе и водной серной кислоты с концентрацией в диапазоне 55-75% по массе по отдельности в реактор как единственных составляющих; и
реакцию водного хлорита натрия с водной серной кислотой для образования реакционной смеси путем преобразования от 75% до 85% ионов хлорита в диоксид хлора.
разбавление концентрированной серной кислоты водой для получения разбавленной водной серной кислоты 55-75% по массе; и
охлаждение разбавленной водной серной кислоты для удаления теплоты реакции перед началом реакции.
Документы, цитированные в отчёте о поиске
Способ получения диоксида хлора

Комментарии