Способ блокирования бактериального и вирусного фона - RU2763757C1
Код документа: RU2763757C1
Чертежи


Описание
ВВЕДЕНИЕ
Настоящее изобретение реализует способ блокирования бактериального и вирусного фона в воздушном пространстве. Дезинфицирующее действие по уничтожению бактерий и вирусов в воздухе осуществляется путем контролируемого высвобождения биоцидного компонента диоксида хлора, полученного в результате реакции хлорита натрия и соляной кислоты, из высокопористой матрицы сорбента аэрогеля.
КОМПОЗИЦИЯ, БЛОКИРУЮЩАЯ БАКТЕРИАЛЬНЫЙ И ВИРУСНЫЙ ФОН, СПОСОБ ЕЕ ПОЛУЧЕНИЯ И ПРИМЕНЕНИЕ В ДЕЗИНФЕКЦИИ ВОЗДУХА
Настоящее изобретение относится к области гигиены, а именно дезинфекции, стерилизации или дезодорации воздуха, и может быть использовано для химической очистки воздуха от патогенных микроорганизмов. Способ заключается в генерации дезинфицирующего компонента диоксида хлора внутри высокопористой матрицы аэрогеля и контролируемом высвобождении его из матрицы. Способ может быть использован для дезинфекции воздуха общественных пространств, таких как медицинские и образовательные учреждения и офисные помещения с большим скоплением людей.
Способ блокирования бактериального и вирусного фона - это способ уничтожения патогенных организмов в воздушном пространстве путем взаимодействия дезинфицирующего компонента с бактериальными и вирусными клетками с элиминацией их функций. Распространение патогенных микроорганизмов в воздухе происходит с перемешиванием и рециркуляцией воздушных масс.
Блокирование бактериального и вирусного фона, как правило, осуществляется с помощью распыления аэрозолей, содержащих дезинфицирующий компонент. В качестве дезинфицирующего компонента наиболее распространены хлорсодержащие дезинфектанты (KR patent №20150107687 А from 23.09.2015, US patent №20070243597 А1 from 18.10.2007). Основным компонентом хлорсодержащих дезинфектантов является молекулярный хлор, который в значительных концентрациях опасен для здоровья человека (ГН 2.2.5.3532-18). Кроме хлорсодержащих дезинфектантов используются аэрозоли на основе солей галогенидов пиридина (Patent № WO 2009151912 A1 from 21.05.2009), пероксида водорода (Andersen В.М., Rasch М., Hochlin K., Jensen F.-H., Wismar P., Fredriksen J.-E. Decontamination of rooms, medical equipment and ambulances using an aerosol of hydrogen peroxide disinfectant, Journal of Hospital Infection 2006; 62(2): 149-155), эфирных масел (Patent № CA 2549307 C from 24.11.2015), спиртов (Patent № EP 1683416 A1 from 26.07.2006) и озона (Patent № TWI 290838 B from 11.12.2007). Однако известно, что для безопасного для здоровья человека использования генераторов озона необходимо ограничение по времени и месту работы данных устройств в связи с высокой окисляющей способностью озона (Guo, С, Gao, Z., & Shen, J. Emission rates of indoor ozone emission devices: A literature review, Building and Environment 2019; 158: 302-318).
В качестве способа уничтожения патогенных микроорганизмов известно использование воздействия ультрафиолетового света в виде УФ-рециркуляторов (Umar М., Roddick F., Fan L. Moving from the traditional paradigm of pathogen inactivation to controlling antibiotic resistance in water - Role of ultraviolet irradiation, Science of the Total Environment 2019; 662: 923-939; Kowalski W.J., Bahnfleth W.P., Witham D.L., Severin B.F., Whittam T.S. Mathematical Modeling of Ultraviolet Germicidal Irradiation for Air Disinfection, Quantitative Microbiology 2000; 2: 249-270; Song K., Mohseni M., Taghipour F. Application of ultraviolet light-emitting diodes (UV-LEDs) for water disinfection: a review, Water Research 2016; 94: 341-349). Однако, ультрафиолетовое излучение способно ионизировать воздух, что также может привести к негативным последствиям для здоровья человека (Jiang, S.-Y., Ma, А., & Ramachandran, S. Negative Air Ions and Their Effects on Human Health and Air Quality Improvement, International Journal of Molecular Sciences 2018; 19(10): 2966.), поэтому УФ-рециркуляторы применяются с ограничениями по местоположению в пространстве дезинфекции и времени дезинфицирующего воздействия. В дополнение к данным недостаткам выделяют дороговизну подобного оборудования и неудобные габариты.
Кроме предложенных методов дезинфекции, доказана эффективность дезинфицирующего компонента диоксида хлора. Диоксид хлора является безопасным биоцидом при его контролируемом выделении в количестве, не превышающем ПДК (ГН 2.2.5.3532-18). Ранее обсуждался механизм воздействия диоксида хлора против вирусов. Механизм заключается в инактивации капсидных белков вирусов, а именно остатков аминокислот цистеина, тирозина и триптофана. Однако инактивации инфекционной вирусной РНК не происходит (Noss С.I., Hauchman F.S., Olivieri V.P. Chlorine dioxide reactivity with proteins, Water Res. 1986; 20(3): 351 356). Механизм антимикробной активности основан на денатурации определенных белков, в первую очередь остатков триптофана и тирозина (Ge, Y., Lei, Y., Lei, X., Gan, W., Shu, L., & Yang, X. Exploration of reaction rates of chlorine dioxide with tryptophan residue in oligopeptides and proteins, Journal of Environmental Sciences 2020; 93: 129-136). Деструкция белков в модельном штамме бактерий Е. Faecalis была исследована в работе (Ersoy, Z.G., Dinc, О., Cinar, В., Gedik, S.Т., & Dimoglo, A. Comparative evaluation of disinfection mechanism of sodium hypochlorite, chlorine dioxide and electroactivated water on Enterococcus faecalis, LWT 2019; 102: 205-213).
Реализация дезинфицирующего воздействия диоксида хлора осуществляется различными способами. Диоксид хлора обладает биоцидной активностью в газообразной форме и водном растворе (

В качестве сорбентов для контролируемого высвобождения диоксида хлора известны цеолиты (US patent №5567405 from 22.10.1996) и полимерные пленки (US patent №5360609 from 01.11.1994; Ray S., Jin Т., Fan X., Liu L., Yam K.L. Development of Chlorine Dioxide Releasing Film and Its Application in Decontaminating Fresh Produce, Journal of Food Science 2013; 78 (2): 276-284), а также системы, использующиеся в антибактериальных саше.
Таким образом, целью нашего изобретения является создание простого, дешевого и безопасного способа блокирования бактериального и вирусного фона, который будет отвечать следующим характеристикам: обладать эффективным воздействием, уничтожающим патогенные микроорганизмы, контролируемо высвобождать безопасное количество дезинфицирующего компонента, не иметь ограничений по времени воздействия.
Композиция, которая используется в настоящем решении, включает в себя диоксид хлора в качестве дезинфицирующего компонента и основу для реализации контролируемого высвобождения диоксида хлора. Предложено использование в качестве основы высокопористого материала аэрогеля диоксида титана в связи с высокоразвитой поверхностью, эффективными сорбционными способностями, предполагающими возможность контролируемого релиза диоксида хлора, доступным способом получения и способностью к простой видимой детекции сорбции компонентов и их релиза. Для проведения генерации и сорбции диоксида хлора была использована реакция хлорита натрия и соляной кислоты в условиях вакуума при 4°C с предварительным отжигом аэрогеля при 90°С в течение 2 часов в потоке воздуха 50 мл/мин для получения чистой не гидратированной поверхности. Дальнейшее высвобождение дезинфицирующего компонента диоксида хлора производится при комнатной температуре и нормальном давлении.
Нижеприведенные примеры иллюстрируют использование способа, предложенного в настоящем изобретении, и не должны рассматриваться как ограничивающие его полную сферу применения, охватываемую прилагаемой формулой изобретения.
ПРИМЕР 1. Синтез влажного геля диоксида титана
Синтез влажного геля диоксида титана, использующийся для производства основы для высвобождения диоксида хлора, производился по методике, предложенной в (Campbell L.K., Na В.K., Ko Е.I. Synthesis and characterization of titania aerogels, Chemistry of Materials 1992; 4: 1329-1333). Для реализации синтеза 15 г образца в реакционную емкость помещали 15 мл тетраизопропоксида титана, 37,5 мл метилового спирта в качестве растворителя и якорь магнитной мешалки, смесь перемешивали 10 мин. Отдельно готовили смесь 37,5 мл метилового спирта, 0,123 мл азотной кислоты для инициации гидролиза и 1,695 мл деионизованной воды и добавляли при перемешивании в реакционную емкость. Синтезированный влажный гель выдерживали в течение 24 часов под действием изопропилового спирта и производили замену растворителя трижды для получения высокопористой структуры. Влажный гель подвергали дальнейшей сверхкритической сушке в атмосфере углекислого газа для сохранения структуры и получения аэрогеля. Вид полученного геля приведен на рис. 1а.
ПРИМЕР 2. Сверхкритическая сушка влажного геля диоксида титана
Для устранения воды и замены растворителя, а также для предотвращения разрушения влажного геля, гель выдерживали под действием изопропилового спирта в течение 48 ч. После этого, гель помещали в автоклав для сверхкритической сушки. Процесс осуществлялся с предварительной экстракцией спирта жидким СО2, за счет чего система чистого жидкого СО2 может обеспечить экстинкцию мениска между жидкой и газовой фазами в достаточно мягких условиях (31°С и 73,7 бар). Вид полученного образца аэрогеля приведен на рис. 1b.
ПРИМЕР 3. Проверка морфологических характеристик полученных образов аэрогеля диоксида титана
Полученные образцы аэрогеля диоксида титана были проанализированы методами сканирующей электронной микроскопии (SEM), анализа сорбционных кривых азота, рентгеноструктурным анализом (XRD).
Результаты анализа сканирующей электронной микроскопией (SEM)
Метод сканирующей электронной микроскопии использовали для изучения морфологии полученных образцов аэрогеля. На рис. 2а представлено SEM изображение полученной структуры аэрогеля диоксида титана. Снимки отражают высокоразвитую поверхность, что указывает на продолжительный рост полимерных цепей в процессе поликонденсации. Высокая пористость указывает на эффективные сорбционные способности полученного материала.
Результаты анализа сорбционных кривых азота
Метод анализа сорбционных кривых азота был использован для количественного подтверждения морфологической структуры образцов аэрогеля диоксида титана. На рис. 26 изображены кривые сорбции-десорбции азота, полученные из модели Brunauer-Emmett-Teller (BET), и кривая распределения радиуса пор. Подсчет параметров морфологии образца таких, как удельная площадь поверхности, удельный объема пор и наиболее вероятный радиус пор показал сорбционную эффективность полученного материала. Количественные параметры морфологии представлены в табл. 1.

Результаты рентгеноструктурного анализа (XRD)
Метод рентгеноструктурного анализа был применен для понимания кристалличности структуры образца аэрогеля. На рис. 2с характерные плавные пики отвечают составу образца диоксида титана, однако кристаллической структуры не обнаружено. Таким образом, аэрогель диоксида титана обладает аморфной структурой.
ПРИМЕР 4. Генерация дезинфицирующего компонента диоксида хлора, изучение кинетики сорбционного и десорбционного процесса.
Генерацию диоксида хлора производили по реакции между 25% раствором хлорита натрия и 10% раствором соляной кислоты в отношении 5:4. Реакцию проводили в присутствии аэрогеля как основы для последующего высвобождения диоксида хлора в вакууме при 4°С. В качестве катализатора процесса генерации диоксида хлора используют цеолит.
Изучение кинетики сорбционного процесса
Изучение кинетики сорбционного процесса было произведено для понимания предельной емкости материала аэрогеля как основы для последующего высвобождения дезинфицирующего компонента. Построение сорбционных кривых производили при определении содержания диоксида хлора в каждой временной точке кривой методом йодометрического титрования (Kuen S.L., Ming J.Н. Disinfection effect of chlorine dioxide on air quality control in Armed Forces General Hospital of Taiwan, Nature and Science 2007; 5(4)) до достижения предельной емкости. Кривая сорбции диоксида хлора на основе из аэрогеля диоксида титана представлена на рис. 3а. Как видно из сорбционной кривой, максимальный рост сорбции наблюдается в первые 5 часов, после которых происходит полное заполнение поверхности аэрогеля молекулами диоксида хлора и достигается максимальная сорбционная емкость, которая составляет 3.78 ммоль/г.
Изучение кинетики десорбционного процесса
Изучение десорбционного процесса необходимо для понимания времени высвобождения дезинфицирующего компонента. Десорбционный процесс был проведен при трех температурах: 4, 25 и 36°С. Построение кривых производилось при определении содержания диоксида хлора в каждой временной точке кривой методом йодометрического титрования (Kuen S.L., Ming J.Н. Disinfection effect of chlorine dioxide on air quality control in Armed Forces General Hospital of Taiwan, Nature and Science 2007; 5(4)). Кривые десорбции диоксида хлора с поверхности аэрогеля диоксида титана при трех температурах показаны на рис. 3b. Как видно из кривых десорбции, кинетика десорбции при 4°С более замедленная, чем при 25 и 36°С, что объясняется большим движением молекул диоксида хлора при повышении температуры и их большей десорбционной способностью. При этом, в течение первого часа сорбционная емкость падает до 0,5 ммоль/г и затем достигается постоянная скорость десорбции 0,015 ммоль/г в сутки.
Тестирование десорбционных характеристик системы аэрогель-диоксид хлора
Тестирование десорбционных характеристик способа блокирования бактериального и вирусного фона: расстояния активного действия, времени активного действия и максимальной концентрации релиза диоксида хлора относительно его ПДК было проведено по следующей методике.
Была проверена десорбционная способность относительно расстояния активного действия диоксида хлора. Концентрация замерялась при помощи газоанализатора диоксида хлора. Измерение велось на расстоянии от 0,3 до 1 м в один момент времени в начале десорбционного процесса. Концентрация диоксида хлора, полученная в результате измерений на различном расстоянии от аэрогеля с диоксидом хлора, показана в табл. 2. Таким образом, расстояние активного действия для данного способа блокирования бактериального и вирусного фона составляет до 1 м.
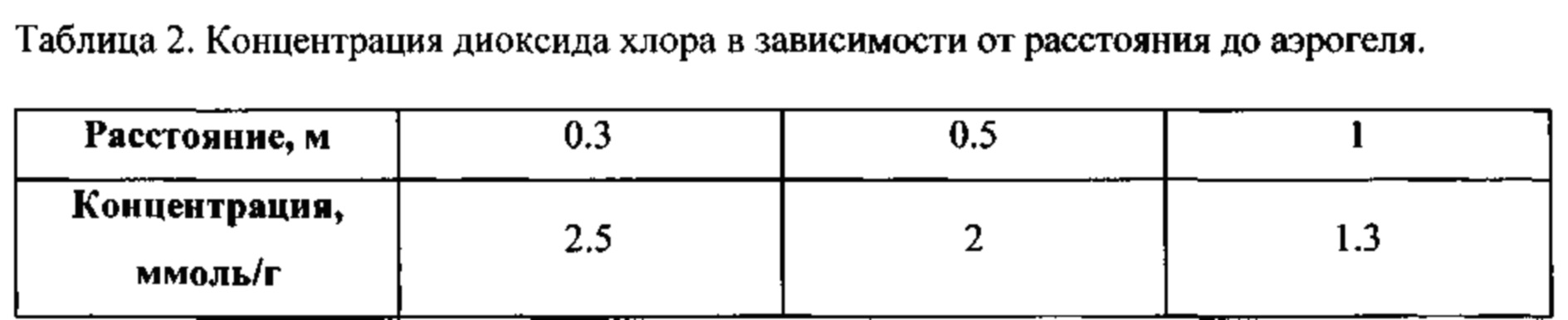
Кроме этого, была проверена сорбционная активность системы относительно времени активного высвобождения диоксида хлора. Концентрация диоксида хлора, десорбированного с поверхности аэрогеля диоксида титана, измеренная через сутки, 15 и 30 суток, представлена в табл. 3. Таким образом, время активного действия для данного способа блокирования бактериального и вирусного фона составляет не менее 30 дней.

Была проверена концентрация высвобождения диоксида хлора на расстоянии 0,3 м в первый час после начала десорбции. Результаты измерений и ПДК диоксида хлора в воздухе рабочей зоны приведены в табл. 4. Таким образом, данный пример демонстрирует основу для блокирования бактериального и вирусного фона с возможностью контролируемого релиза дезинфицирующего компонента диоксида хлора в количестве не более 3 ммоль/г в течение первого часа

ПРИМЕР 5. Тестирование биологической активности системы аэрогель-диоксид хлора
Способ блокирования бактериального фона
Способ блокирования бактериального фона был испытан на трех модельных штаммах грамотрицательных и грамположительных бактерий Escherichia coli АТСС 25922, Staphylococcus aureus АТСС 209Р, Pseudomonas aeruginosa (клинический полирезистентный штамм из НИИ эпидемиологии и микробиологии им. Пастера). В первые сутки бактериальные штаммы инкубировали в жидкой среде LB (Лурия-Бертани) в течение 24 часов при 37°С, 250 об/мин в орбитальном шейкере-инкубаторе «Biosan». Для культивирования Р. aeruginosa в питательные среды добавляли 200 мкг/мл натриевой соли ампициллина. На второй день 10 мкл каждой ночной бактериальной культуры высевали при разведении 10-8 на твердую среду LB и инкубировали с аэрогелями (концентрация диоксида хлора 3 ммоль/г) и без них в чашках Петри для подсчета колониеобразующих единиц (КОЕ). Были выбраны три временных точки инкубации с аэрогелями - 5 минут, 15 минут и 60 минут. В качестве контроля культуры инкубировали также без аэрогелей. После воздействия аэрогелей бактерии инкубировали при 37°С в течение 24 часов. На третьи сутки количество КОЕ (мл-1) рассчитывали путем подсчета колоний на чашках Петри. Каждый эксперимент по изучению биоцидной активности аэрогелей проводился трижды. Статистический анализ проводился в программном обеспечении GraphPad Prism 7.0. Результаты показали, что после 60 мин воздействия аэрогеля все три штамма погибают. Через 15 минут воздействия диоксида титана наблюдались колонии Е. coli и S. aureus. Через 5 мин действия аэрогеля количество всех трех штаммов уменьшалось на 1 lg. Исходя из данных, что после 15 минутного воздействия аэрогеля наблюдались только колонии Staphylococcus aureus АТСС 209Р, можно сделать вывод, что грамположительные бактерии менее восприимчивы к действию аэрогелей, чем грамотрицательные. Блокирование бактериального фона во временной экспозиции представлено в табл. 5 и на рис. 4.
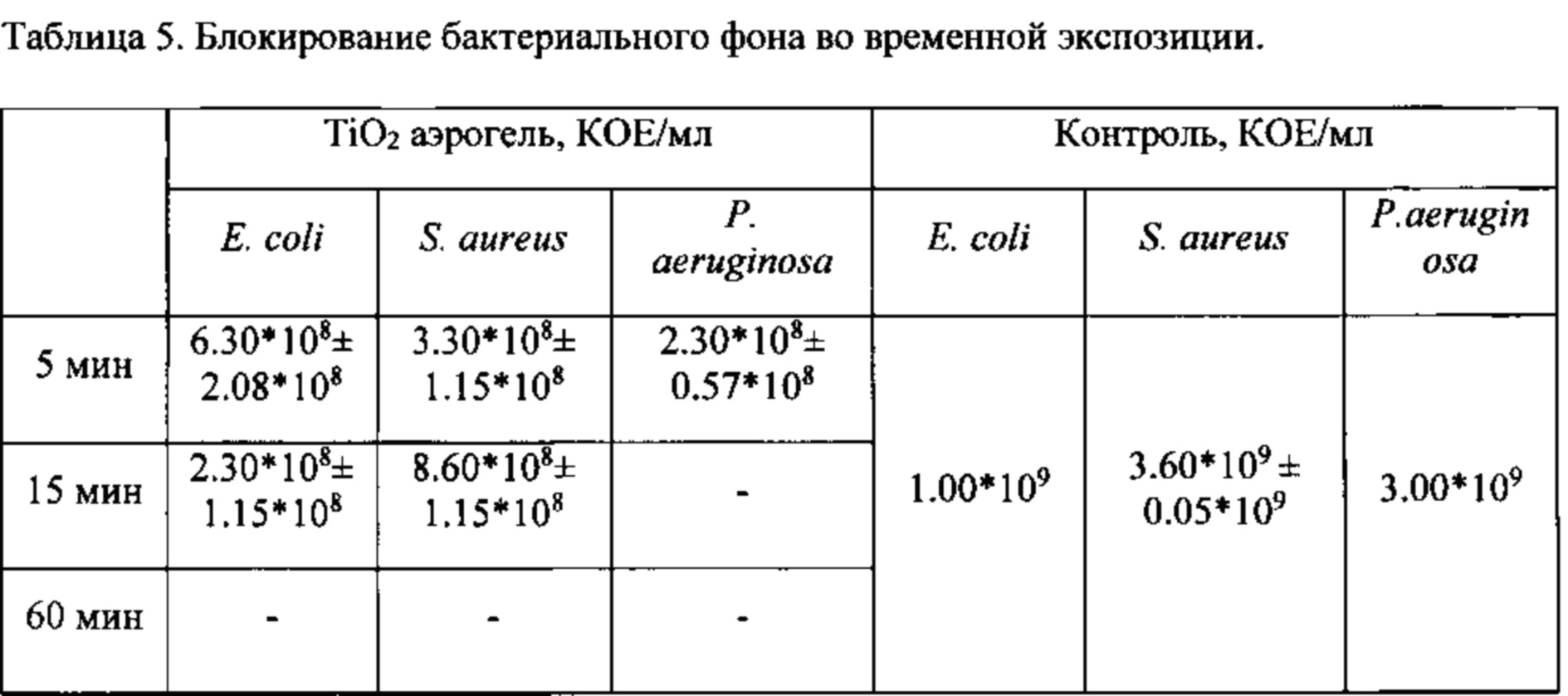
Таким образом, способ блокирования бактериального фона обеспечивает уничтожение более чем 80% бактерий в течение часа в активной области.
Способ блокирования вирусного фона
Способ блокирования вирусного фона был протестирован по следующей методике. Для культивирования вируса гриппа использовали культуру клеток MDCK, для культивирования аденовируса - линию Vero. Вирусы культивировали в клетках соответствующих линий в течение 72 часов и использовали в качестве исходного инфекционного материала. Вируссодержащий материал наносили в объеме 0.1 мл на поверхность стеклянной чашки Петри в двух параллельных образцах и высушивали на воздухе при комнатной температуре в течение 10 минут. Чашки Петри с нанесенными пробами помещали в стеклянный эксикатор с притертой крышкой. Активированный диоксидом хлора аэрогель (концентрация диоксида хлора 3 ммоль/г) помещали в эксикатор с пробами вирусов. Крышку закрывали и выдерживали экспериментальные образцы в течение 5 или 30 минут при комнатной температуре. Контрольные пробы вирусов обрабатывали таким же образом в отсутствие активированного аэрогеля. По истечении указанного срока крышку открывали, извлекали чашки Петри с нанесенными пробами и смывали отдельно каждую из проб 4 раза по 250 мкл среды для культур клеток. В полученных пробах определяли инфекционный титр вирусов, как описано ниже.
Клетки соответствующих линий рассевали в 96-луночный планшет в количестве 104 кл./лунку и объеме 100 мкл/лунку полной среды МЕМ (содержит 2 мМ L-глутамина, 250 мг/л гентамицина, 10% эмбриональной сыворотки крупного рогатого скота). Инкубацию проводили в течение суток в СО2-инкубаторе при 37°С в 5% атмосфере СО2 до формирования монослоя. Непосредственно перед экспериментом клетки промывали средой МЕМ, дальнейшие манипуляции проводили в бессывороточной среде. Для определения инфекционной активности вируса в культуре клеток из культуральной жидкости готовили серию десятикратных разведений от 10-1 до 10-7, вносили в лунки с монослоем клеток соответствующей линии и инкубировали в течение 72 часов в атмосфере 5% СО2 при 37°С. Титр вируса гриппа определяли по результатам реакции гемагглютинации, титр аденовируса - по наличию вирусспецифического ЦПД. Каждую из концентраций исследуемого препарата и препаратов сравнения испытывали в двух параллельных лунках. Противовирусную активность образцов оценивали по снижению титра вируса в опытных лунках планшетов по сравнению с контрольными (группа контроля вируса).
Для определения наличия вируса гриппа в культуральной жидкости проводили реакцию гемагглютинации. Для этого культуральную жидкость переносили в лунки планшета для иммунологических реакций, после чего добавляли равный объем 1% куриных эритроцитов в физиологическом растворе. Планшеты инкубировали при 20°С в течение 1 ч, после чего визуально проводили учет результатов. За титр вируса принимали наибольшее разведение вируссодержащего материала, при котором наблюдалась положительная реакция гемагглютинации. Положительным считают результат реакции, при котором эритроциты равномерно покрывали дно лунки. При отрицательной реакции эритроциты в виде маленького диска располагаются в центре анализируемой лунки планшета. Титр вируса в каждом из экспериментальных образцов определяли по методу Рида и Менча.
Результаты измерения инфекционного титра вирусов представляли в виде M±SE, где М - среднее значение, SE - ошибка эксперимента. Полученные данные сравнивали между собой с помощью U-критерия Манна-Уитни. Различия считали значимыми при р<0.05.
Данные по изучению влияния системы аэрогель-диоксид хлора на инфекционную активность респираторных вирусов человека суммированы в табл. 6.


Как следует из представленных данных, исходный титр вирусов в инфекционном материале составлял 5.5-6.5 lg ID50/0.2 мл в зависимости от вируса. Высушивание на воздухе (столбец «0» в табл. 1) приводило к потере инфекционности, что следует объяснить его инактивацией при высыхании частиц материала, негативно влияющем на биологические свойства вирионов.
Таким образом, способ блокирования вирусного фона обеспечивает уничтожение более чем 80% вирусов в течение 30 мин в активной области.
В приведенных примерах показано, что предлагаемый способ блокирования бактериального и вирусного фона позволяет уничтожать патогенные организмы более 80% в области активного действия системы, что является эффективным и безопасным дополнительным методом дезинфекции воздуха общественных пространств. Это обеспечивается благодаря окислительному воздействия диоксида хлора, контролируемо высвобожденному из высокопористого материала аэрогеля, на клетки патогенных микроорганизмов, разрушающее их и элиминирующее их функции. Из вышесказанного следует, что в качестве оптимального способа блокирования бактериального и вирусного фона в общественных пространствах предлагается система аэрогель-диоксид хлора с контролируемым релизом дезинфицирующего компонента. Предлагаемый способ безопасен, эффективен и прост.
Преимуществом данного способа является его универсальность и отсутствие ограничений по времени и месту действия, а также нахождения людей в пространстве дезинфекции. Способ блокирования бактериального и вирусного фона может быть использован в различных типах общественных пространств, включая медицинские и образовательные учреждения, офисы и предприятия. Предлагаемое решение уменьшает бактериальный и вирусный фон более чем на 80% в активной области действия и обеспечивает эффективную дезинфекцию воздуха общественных пространств.
Изображения:
Рис. 1 (а) Вид влажного геля диоксида титана, (b) вид аэрогеля диоксида титана.
Рис. 2 (a) SEM изображение, (b) анализ сорбционных кривых азота и кривая распределения размера пор и (с) XRD кривая аэрогеля диоксида титана.
Рис. 3 (а) Процесс сорбции диоксида хлора на поверхности аэрогелей диоксида титана при температуре 25°С, адсорбционной влажности 90%. Кривые кинетики адсорбции строили путем измерения количества ClO2 методом йодометрического титрования с двумя параллельными определениями и допустимым расхождением определения 0,05%. Процесс десорбции диоксида хлора с поверхности аэрогеля диоксида титана при (b) 4 (1), 25 (2), 36 (3) °С.
Рис. 4. Антибактериальная активность аэрогеля диоксида титана, активированного диоксидом хлора, по отношению к трем типичным патогенным штаммам бактерий, а именно Р. aeruginosa (1), S. aureus (2) и Е. coli (3). А, В, С, D, Е - изображения колониеобразующих единиц бактерий (КОЕ) различных штаммов до воздействия аэрогелей (а), после 5 мин (Б), 15 мин (в), 60 мин (г) воздействия, (Д) без воздействия. Результаты представляют собой среднее значение трех независимых экспериментов (по три повтора в каждом) ± стандартное отклонение.
Реферат
Изобретение относится к дезинфекции воздуха и может быть использовано для очистки воздуха от патогенных микроорганизмов. Основа для блокирования бактериального и вирусного фона представляет собой высокопористый сорбент - аэрогель диоксида титана с удельной площадью поверхности 583,1 м2/г, насыщенный дезинфицирующим компонентом в виде молекулярного диоксида хлора, с максимальной сорбционной емкостью аэрогеля по отношению к диоксиду хлора 3,78 ммоль/г. Предложены способы блокирования бактериального и вирусного фона с использованием указанной основы. Группа изобретений позволяет проводить дезинфекцию воздуха общественных пространств, таких как медицинские, образовательные и офисные помещения с большим скоплением людей, с контролируемым высвобождением безопасного количества децинфицирующего компонента без ограничения по времени воздействия. 4 н. и 1 з.п. ф-лы, 4 ил., 6 табл., 5 пр.

Комментарии