Синбиотическая смесь - RU2448720C2
Код документа: RU2448720C2
Чертежи





Описание
Область техники, к которой относится изобретение
Изобретение относится к препаратам, содержащим пробиотик и пребиотическую смесь, специально предназначенную для усиления эффективности и действенности пробиотика, и к пищевым продуктам, содержащим указанный препарат.
Предшествующий уровень техники
В кишечнике человека обитает множество видов бактерий, которые оказывают как положительное, так и отрицательное воздействие на физиологию кишечника, а также другие системные воздействия. Доминирующими группами бактерий, обнаруженными в кишечнике, являются бактероиды, бифидобактерии, эубактерии, клостридии и лактобациллы. Присутствующие бактерии проявляют неустойчивую активность в зависимости от доступности субстрата, окислительно-восстановительного потенциала, pH, давления O2 и локализации в толстом кишечнике. В большинстве случаев кишечные бактерии можно подразделить на виды, которые могут потенциально оказывать либо вредное, либо полезное воздействие на организм-хозяин. Патогенные воздействия (которые могут вызываться, например, клостридиями или бактероидами) включают диарею, инфекции, поражение печени, канцерогенез и гнилостные процессы в кишечнике. Полезные для здоровья воздействия могут быть обусловлены ингибированием роста вредных бактерий и колонизации ими кишечника, стимулированием иммунных функций, улучшением пищеварения и абсорбцией незаменимых нутриентов и синтезом витаминов. Крайне желательным является повышение количества и/или активности таких видов бактерий, как Bifidobacterium и Lactobacillus, которые способны оказывать полезное для здоровья действие.
В недавнем прошлом некоторые штаммы бактерий стали привлекать повышенный интерес в связи с тем, что при потреблении их человеком эти штаммы проявляют, как было установлено, ценные для его здоровья свойства. В частности, было установлено, что специфические штаммы рода Lactobacilli и Bifidobacteria способны заселять, по меньшей мере временно, слизистую оболочку кишечника, снижать прилипание патогенных бактерий к эпителию кишечника, оказывать иммуномодулирующий эффект и способствовать поддержанию хорошего самочувствия. Такие бактерии обычно называют пробиотиками.
С целью идентификации новых пробиотических штаммов было проведено большое число исследований. Например, EP 0199535, EP 0768375, WO 97/00078, EP 0577903 и WO 00/53200 раскрывают специфические штаммы лактобацилл и бифидобактерий и их полезное для здоровья действие.
Пробиотик можно определить как кормовую добавку жизнеспособных микроорганизмов, которая благотворно воздействует на животное-хозяина, улучшая его кишечный микробный баланс. Показано, что такими свойствами обладают некоторые штаммы лактобацилл и бифидобактерий, такие как, например, Lactobacillus paracasei CNCM I-2116, Lactobacillus rhamnosus ATCC 53103, Bifidobacterium lactis BB12®, Bifidobacterium longum ATCC BAA-999, Lactobacillus reuteri ATCC 55730 и Bifidobacterium breve M-16V®. Эти пробиотические лактобациллы и бифидобактерии традиционно добавляются в пищевые продукты для человека, например в ферментированные молочные продукты. Известно, что пробиотики в большинстве случаев оказывают профилактический и лечебный эффект на патогенные инфекции желудочно-кишечного тракта, такие как, например, инфекции, вызываемые видами Clostridia и Salmonella. В ЕР 904784 предлагается использовать комбинацию трех различных видов пробиотиков для лечения желудочно-кишечных расстройств. А совсем недавно было выдвинуто предположение, что некоторые пробиотические штаммы могут быть эффективными также в предупреждении и лечении инфекций верхних дыхательных путей (British Medical Journal 2001, 322: 1-5).
Что касается конкретно грудных детей, то считается, что желудочно-кишечный тракт ребенка незадолго до появления последнего на свет является стерильным. В процессе родов он контактирует с бактериями пищеварительного тракта и кожи матери и начинает заселяться ими. Существуют большие различия в составе микробиоты кишечника у грудных детей в зависимости от их кормления. Микрофлора фекалий грудных детей, вскармливаемых материнским молоком, содержит значительные популяции бифидобактерий с некоторым количеством лактобацилл, в то время как у грудных детей, вскармливаемых искусственными смесями, микробиота является более сложной по составу и включает обычно бифидобактерии, бактероиды, клостридии и стрептококки. После отнятия от груди у детей постепенно устанавливается микробиота кишечника, сходная с микробиотой кишечника взрослого человека.
Материнское молоко рекомендуется всем грудным детям. Однако в некоторых случаях грудное вскармливание является неадекватным или безуспешным по медицинским показаниям либо матери отказываются кормить грудью. Для таких ситуаций разработаны детские смеси.
В такие смеси для детского питания было предложено добавлять пробиотики, с тем чтобы обеспечить и стимулировать заселение кишечника в первую очередь "хорошими" бактериями (бифидобактериями и лактобациллами), а не вредными бактериями, такими как патогенные, например клостридии и др. В типичных случаях в указанные смеси добавляется минимум 107 KOE (колониеобразующих единиц)/г смеси, хотя в большинстве случаев предпочитается вводить повышенное количество, например до 1012 KOE/г смеси.
Другой подход к стимуляции количества и/или активности полезных бактерий в толстом кишечнике предусматривает добавление в пищевые продукты пребиотиков. Пребиотик - это неусвояемый пищевой ингредиент, который благотворно влияет на организм-хозяин, избирательно стимулируя рост и/или активность одного или ограниченного количества видов бактерий в толстом кишечнике и улучшая тем самым здоровье хозяина. Такие ингредиенты являются неусвояемыми в том смысле, что они не расщепляются в желудке или тонком кишечнике, а абсорбируются в них и проходят в целостном виде в толстый кишечник, где они избирательно сбраживаются полезными бактериями. Примеры пребиотиков включают некоторые олигосахариды, такие как фруктоолигосахариды (FOS) и галактоолигосахариды (GOS).
Известно, что женское молоко содержит повышенное количество неперевариваемых олигосахаридов по сравнению с молоком большинства видов животных. Фактически неперевариваемые олигосахариды представляют собой третий по количеству твердый компонент (после лактозы и липидов) женского молока: его концентрация составляет от 12 до 15 г/л в молозиве и от 5 до 8 г/л в зрелом молоке. Олигосахариды женского молока очень устойчивы к ферментативному гидролизу, что указывает на то, что эти олигосахариды могут выполнять жизненно важные функции, не связанные непосредственно с их энергетической ценностью.
По мере досконального изучения состава женского молока было предложено вводить в смеси для детского питания и пребиотики. Промышленностью выпускаются различные смеси для детского питания с добавлением пребиотиков, таких как смеси фруктоолигосахаридов с галактоолигосахаридами. Однако эти смеси лишь довольно приблизительно имитируют смесь олигосахаридов женского молока. В женском молоке обнаружено свыше 100 различных олигосахаридных компонентов, некоторые из которых не были обнаружены в молоке животных, например, в коровьем молоке указанные компоненты не были обнаружены вообще или были обнаружены только в малых количествах. Примерами тех классов олигосахаридов женского молока, которые присутствуют в коровьем молоке и молозиве только в очень малых количествах или не присутствуют вообще, могут служить сиалилированные и фукозилированные олигосахариды.
Смеси для детского питания, содержащие как пробиотики, так и пребиотики, были также предложены в ходе продолжающегося поиска по созданию таких смесей для детского питания, которые были бы максимально приближены по составу и эффективности к женскому молоку. Например, в WO 2005/000748 предлагается дополнять смесь для детского питания смесью из штамма Bifidobacterium breve, галактоолигосахаридов и фруктоолигосахаридов (инулин). Заявляется, что такая смесь, которая описывается как синбиотическая, регулирует популяцию Bifidobacterium в толстом кишечнике грудных детей, которым скармливается указанная дополненная смесь, делая ее более приближенной к популяции у вскармливаемого грудью ребенка, т.е. с пониженным содержанием Bifidobacterium catenulatum, Bifidobacterium pseudocatenulatum и Bifidobacterium adolescentis и повышенным содержанием Bifidobacterium infantis, Bifidobacterium breve и Bifidobacterium longum. Утверждается также, что эта смесь полезна для профилактики или лечения иммунного состояния.
Однако по-прежнему сохраняется потребность в препаратах, содержащих пробиотик и пребиотическую смесь, специально предназначенную для усиления эффективности и действенности пробиотика.
Сущность изобретения
Удивительным образом было установлено, что пребиотическая смесь, которая содержит от 5% до 70% масс. по меньшей мере одного N-ацетилированного олигосахарида, выбранного из группы, состоящей из GalNAcα1,3Galβ1,4Glc и Galβ1,6GalNAcα1,3Galβ1,4Glc; от 20% до 90% масс. по меньшей мере одного нейтрального олигосахарида, выбранного из группы, состоящей из Galβ1,6Gal,Galβ1,6Galβ1,4Glc Galβ1,6Galβ1,6Glc, Galβ1,3Galβ1,3Glc, Galβ1,3Galβ1,4Glc, Galβ1,6Galβ1,6Galβ1,4Glc, Galβ1,6Galβ1,3Galβ1,4Glc Galβ1,3Galβ1,6Galβ1,4Glc и Galβ1,3Galβ1,3Galβ1,4Glc, и от 5% до 50% масс. по меньшей мере одного сиалилированного олигосахарида, выбранного из группы, включающей NeuAcα2,3Galβ1,4Glc и NeuAcα2,6Galβ1,4Glc, является высокоэффективной в усилении благотворного для здоровья эффекта и действенности пробиотических бактерий, потребляемых вместе с пребиотической смесью.
Таким образом, в первом аспекте настоящее изобретение обеспечивает препарат, содержащий пробиотический бактериальный штамм и пребиотическую смесь, включающую от 5% до 70% масс. по меньшей мере одного N-ацетилированного олигосахарида, выбранного из группы, состоящей из GalNAcα1,3Galβ1,4Glc и Galβ1,6GalNAcα1,3Galβ1,4Glc; от 20% до 95% масс. по меньшей мере одного нейтрального олигосахарида, выбранного из группы, состоящей из Galβ1,6Gal, Galβ1,6Galβ1,4Glc Galβ1,6Galβ1,6Glc, Galβ1,3Galβ1,3Glc, Galβ1,3Galβ1,4Glc, Galβ1,6Galβ1,6Galβ1,4Glc, Galβ1,6Galβ1,3Galβ1,4Glc Galβ1,3Galβ1,6Galβ1,4Glc и Galβ1,3Galβ1,3Galβ1,4Glc, и от 2% до 50% масс. по меньшей мере одного сиалилированного олигосахарида, выбранного из группы, включающей NeuAcα2,3Galβ1,4Glc и NeuAcα2,6Galβ1,4Glc.
Во втором аспекте настоящее изобретение обеспечивает применение пробиотического бактериального штамма и пребиотической смеси, содержащей от 5% до 70% масс. по меньшей мере одного N-ацетилированного олигосахарида, выбранного из группы, состоящей из GalNAcα1,3Galβ1,4Glc и Galβ1,6GalNAcα1,3Galβ1,4Glc; от 20% до 95% масс. по меньшей мере одного нейтрального олигосахарида, выбранного из группы, состоящей из Galβ1,6Gal, Galβ1,6Galβ1,4Glc, Galβ1,6Galβ1,6Glc, Galβ1,3Galβ1,3Glc, Galβ1,3Galβ1,4Glc, Galβ1,6Galβ1,6Galβ1,4Glc, Galβ1,6Galβ1,3Galβ1,4Glc Galβ1,3Galβ1,6Galβ1,4Glc и Galβ1,3Galβ1,3Galβ1,4Glc, и от 2% до 50% масс. по меньшей мере одного сиалилированного олигосахарида, выбранного из группы, включающей NeuAcα2,3Galβ1,4Glc и NeuAcα2,6Galβ1,4Glc, в производстве лекарственного средства для профилактики и/или лечения патогенных инфекций желудочно-кишечного тракта.
В третьем аспекте настоящее изобретение обеспечивает применение пробиотического бактериального штамма и пребиотической смеси, содержащей от 5% до 70% масс. по меньшей мере одного N-ацетилированного олигосахарида, выбранного из группы, состоящей из GalNAcα1,3Galβ1,4Glc и Galβ1,6GalNAcα1,3Galβ1,4Glc; от 20% до 95% масс. по меньшей мере одного нейтрального олигосахарида, выбранного из группы, состоящей из Galβ1,6Gal, Galβ1,6Galβ1,4Glc Galβ1,6Galβ1,6Glc, Galβ1,3Galβ1,3Glc, Galβ1,3Galβ1,4Glc, Galβ1,6Galβ1,6Galβ1,4Glc, Galβ1,6Galβ1,3Galβ1,4Glc Galβ1,3Galβ1,6Galβ1,4Glc и Galβ1,3Galβ1,3Galβ1,4Glc, и от 2% до 50% масс. по меньшей мере одного сиалилированного олигосахарида, выбранного из группы, включающей NeuAcα2,3Galβ1,4Glc и NeuAcα2,6Galβ1,4Glc, в производстве лекарственного средства для профилактики или лечения иммунного состояния.
В четвертом аспекте настоящее изобретение обеспечивает применение пробиотического бактериального штамма и пребиотической смеси, содержащей от 5% до 70% масс. по меньшей мере одного N-ацетилированного олигосахарида, выбранного из группы, состоящей из GalNAcα1,3Galβ1,4Glc и Galβ1,6GalNAcα1,3Galβ1,4Glc; от 20% до 95% масс. по меньшей мере одного нейтрального олигосахарида, выбранного из группы, состоящей из Galβ1,6Gal, Galβ1,6Galβ1,4Glc Galβ1,6Galβ1,6Glc, Galβ1,3Galβ1,3Glc, Galβ1,3Galβ1,4Glc, Galβ1,6Galβ1,6Galβ1,4Glc, Galβ1,6Galβ1,3Galβ1,4Glc Galβ1,3Galβ1,6Galβ1,4Glc и Galβ1,3Galβ1,3Galβ1,4Glc, и от 2% до 50% масс. по меньшей мере одного сиалилированного олигосахарида, выбранного из группы, включающей NeuAcα2,3Galβ1,4Glc и NeuAcα2,6Galβ1,4Glc, в производстве лекарственного средства для профилактики или лечения инфекций верхних дыхательных путей.
В пятом аспекте изобретение обеспечивает способ предупреждения или лечения патогенных инфекций желудочно-кишечного тракта у субъекта, нуждающегося в этом, который предусматривает прием субъектом терапевтического количества препарата, содержащего пробиотический бактериальный штамм и пребиотическую смесь, включающую от 5% до 70% масс. по меньшей мере одного N-ацетилированного олигосахарида, выбранного из группы, состоящей из GalNAcα1,3Galβ1,4Glc и Galβ1,6GalNAcα1,3Galβ1,4Glc; от 20% до 95% масс. по меньшей мере одного нейтрального олигосахарида, выбранного из группы, состоящей из Galβ1,6Gal, Galβ1,6Galβ1,4Glc Galβ1,6Galβ1,6Glc, Galβ1,3Galβ1,3Glc, Galβ1,3Galβ1,4Glc, Galβ1,6Galβ1,6Galβ1,4Glc, Galβ1,6Galβ1,3Galβ1,4Glc Galβ1,3Galβ1,6Galβ1,4Glc и Galβ1,3Galβ1,3Galβ1,4Glc, и от 2% до 50% масс. по меньшей мере одного сиалилированного олигосахарида, выбранного из группы, включающей NeuAcα2,3Galβ1,4Glc и NeuAcα2,6Galβ1,4Glc.
В шестом аспекте изобретение обеспечивает способ предупреждения или лечения иммунного состояния у субъекта, нуждающегося в этом, который предусматривает прием субъектом терапевтического количества препарата, содержащего пробиотический бактериальный штамм и пребиотическую смесь, включающую от 5% до 70% масс. по меньшей мере одного N-ацетилированного олигосахарида, выбранного из группы, состоящей из GalNAcα1,3Galβ1,4Glc и Galβ1,6GalNAcα1,3Galβ1,4Glc; от 20% до 95% масс. по меньшей мере одного нейтрального олигосахарида, выбранного из группы, состоящей из Galβ1,6Gal, Galβ1,6Galβ1,4Glc Galβ1,6Galβ1,6Glc, Galβ1,3Galβ1,3Glc, Galβ1,3Galβ1,4Glc, Galβ1,6Galβ1,6Galβ1,4Glc, Galβ1,6Galβ1,3Galβ1,4Glc Galβ1,3Galβ1,6Galβ1,4Glc и Galβ1,3Galβ1,3Galβ1,4Glc, и от 2% до 50% масс. по меньшей мере одного сиалилированного олигосахарида, выбранного из группы, включающей NeuAcα2,3Galβ1,4Glc и NeuAcα2,6Galβ1,4Glc.
В седьмом аспекте изобретение обеспечивает способ предупреждения или лечения инфекции верхних дыхательных путей у субъекта, нуждающегося в этом, который предусматривает прием субъектом терапевтического количества препарата, содержащего пробиотический бактериальный штамм и пребиотическую смесь, включающую от 5% до 70% масс. по меньшей мере одного N-ацетилированного олигосахарида, выбранного из группы, состоящей из GalNAcα1,3Galβ1,4Glc и Galβ1,6GalNAcα1,3Galβ1,4Glc; от 20% до 95% масс. по меньшей мере одного нейтрального олигосахарида, выбранного из группы, состоящей из Galβ1,6Gal, Galβ1,6Galβ1,4Glc Galβ1,6Galβ1,6Glc, Galβ1,3Galβ1,3Glc, Galβ1,3Galβ1,4Glc, Galβ1,6Galβ1,6Galβ1,4Glc, Galβ1,6Galβ1,3Galβ1,4Glc Galβ1,3Galβ1,6Galβ1,4Glc и Galβ1,3Galβ1,3Galβ1,4Glc, и от 2% до 50% масс. по меньшей мере одного сиалилированного олигосахарида, выбранного из группы, включающей NeuAcα2,3Galβ1,4Glc и NeuAcα2,6Galβ1,4Glc.
Краткое описание фигур
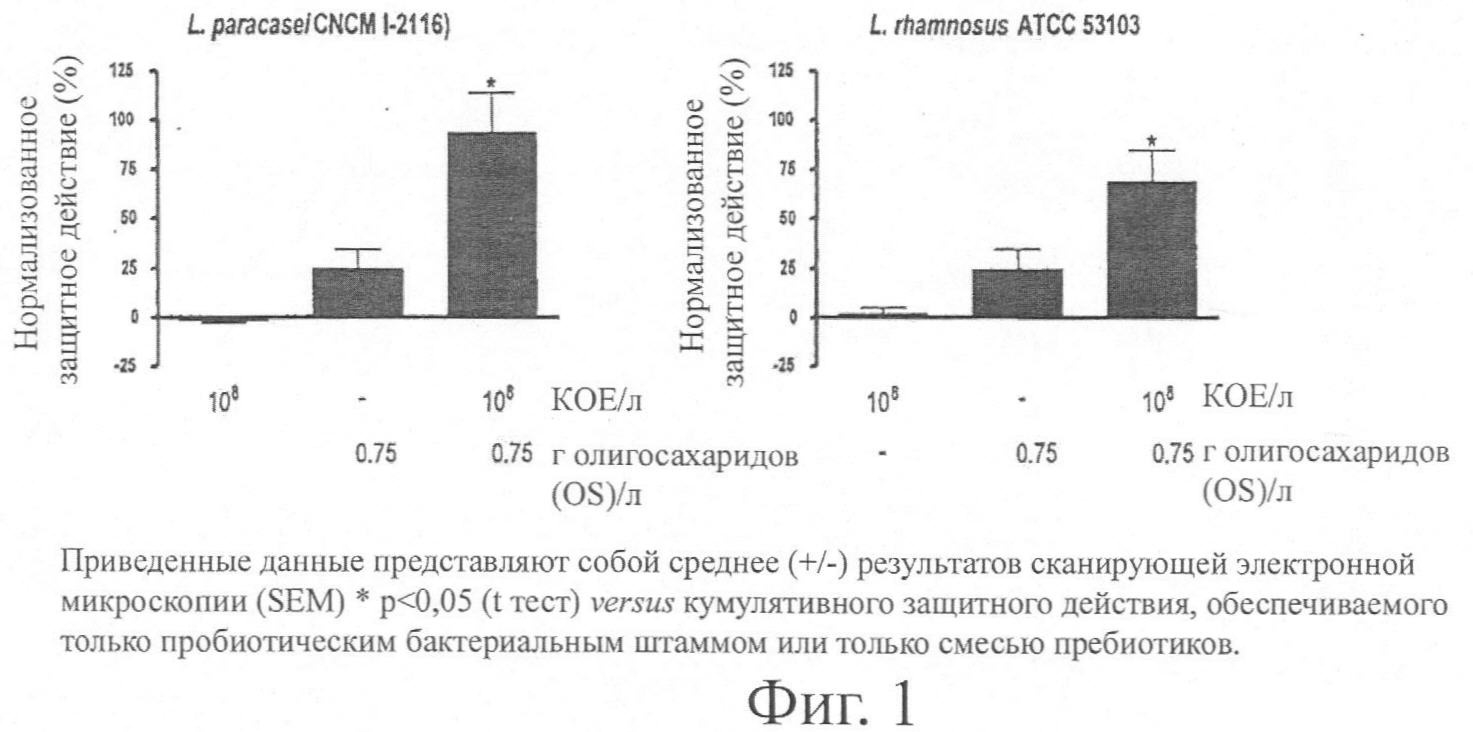
Фиг.1 показывает защитное действие препарата по изобретению от токсина А, продуцируемого Clostridium difficile, по сравнению с защитным действием, проявляемым отдельными компонентами препарата.
Фиг.2 показывает защитное действие от токсина А, продуцируемого Clostridium difficile, которое проявляют пробиотические бактериальные штаммы, указанные на фиг.1, в комбинации с различными пребиотиками, известными из уровня техники.
Фиг.3 сравнивает количество Bifidobacterium breve в тонком кишечнике гнотобионтных мышей, которым принудительно с помощью зонда была введена микробиота грудного ребенка и которым скармливался препарат по изобретению, с количеством Bifidobacterium breve у мышей, получавших компоненты препарата по отдельности.
Фиг.4 сравнивает количество Staphylococci в фекалиях гнотобионтных мышей, которым принудительно с помощью зонда была введена микробиота грудного ребенка и которым скармливался препарат по изобретению, с количеством Staphylococci у мышей, получавших компоненты препарата по отдельности.
Фиг.5 сравнивает количество Clostridium perfringens в тонком кишечнике гнотобионтных мышей, которым принудительно с помощью зонда была введена микробиота грудного ребенка и которым скармливался препарат по изобретению, с количеством Clostridium perfringens у таких же мышей, получавших компоненты препарата по отдельности.
Фиг.6 сравнивает относительную метаболическую активность резидента Bifidobacterium longum в период двух недель у безмикробных (стерильных) мышей, которым принудительно с помощью зонда была введена микробиота грудного ребенка и которым скармливался препарат по изобретению, с относительной метаболической активностью резидента Bifidobacterium longum у таких же мышей, получавших компоненты препарата по отдельности.
Подробное описание изобретения
В настоящем описании нижеприведенные термины даются в том определении, которое следует учитывать при чтении и толковании описания, примеров и формулы изобретения:
под "бифидогенной кишечной микробиотой" имеется в виду кишечная микробиота грудных детей, в которой доминируют бифидобактерии, такие как Bifidobacterium breve, Bifidobacterium infantis и Bifidobacterium longum, за исключением поддающихся оценке популяций таких видов, как бактероиды, клостридии и стрептококки, и которая в большинстве случаев сравнима с кишечной микробиотой вскармливаемых грудью младенцев;
"грудной ребенок" относится к ребенку в возрасте менее 12 месяцев;
"смесь для детского питания" означает пищевой продукт, предназначенный для полноценного питания грудных детей в течение первых от четырех до шести месяцев жизни или служащий добавкой к другим пищевым продуктам до достижения ребенком возраста 12 месяцев;
"N-ацетилированный олигосахарид" означает олигосахарид, содержащий N-ацетил-остаток;
NCC обозначает Nestlé Culture Collection (коллекцию культур фирмы Nestlé);
"нейтральный олигосахарид" означает олигосахарид, не имеющий заряда и не содержащий N-ацетил-остатка;
"пробиотические бактерии" означают препараты или компоненты микробных клеток, оказывающих благотворное действие на здоровье или самочувствие хозяина. (Salminen S., Ouwehand A., Benno Y. et al. "Probiotics: how should they be defined" Trend Food Sci. Technol. 1999: 10 107-10);
"пребиотик" означает неусвояемый пищевой ингредиент, который благотворно влияет на хозяина, избирательно стимулируя рост и/или активность одного вида или ограниченного числа видов бактерий в толстом кишечнике и улучшая тем самым здоровье хозяина. (Gibson and Roberfroid "Dietary Modulation of the Human Colonic Microbiota: Introducing the Concept of Prebiotics" J. Nutr. 125: 1401-1412);
"олигосахарид" означает углевод, имеющий степень полимеризации (DP) от 2 до 20 включительно, но не включающий лактозу, и
"сиалилированный олигосахарид" означает олигосахарид, содержащий остаток сиаловой кислоты с ассоциированным зарядом.
Предпочтительно пребиотическая смесь содержит от 10% до 70% масс. N-ацетилированных олигосахаридов, от 20% до 80% масс. нейтральных олигосахаридов и от 10% до 50% масс. сиалилированных олигосахаридов. Более предпочтительно пребиотическая смесь содержит от 15% до 40% масс. N-ацетилированных олигосахаридов, от 40% до 60% масс. нейтральных олигосахаридов и от 15% до 30% масс. сиалилированных олигосахаридов. Особенно предпочтительная пребиотическая смесь содержит от 30% масс. N-ацетилированных олигосахаридов, 50% масс. нейтральных олигосахаридов и 20% масс. сиалилированных олигосахаридов.
Альтернативно смесь может содержать от 5% до 20% масс. конкретного N-ацетилированного олигосахарида(ов), от 60% до 95% масс. конкретного нейтрального олигосахарида(ов) и от 2% до 30% масс. конкретного сиалилированного олигосахарида(ов).
Пребиотическая смесь изобретения может быть получена из молока одного или многих видов животных, т.е. из молока любого млекопитающего, в частности из молока коров, коз, буйволиц, кобыл, слоних, верблюдиц или овец.
Альтернативно пребиотическая смесь может быть получена путем закупки и смешивания отдельных компонентов. Например, синтезированные галактоолигосахариды, такие как Galβ1,6Galβ1,4Glc Galβ1,6Galβ1,6Glc, Galβ1,3Galβ1,4Glc, Galβ1,6Galβ1,6Galβ1,4Glc, Galβ1,6Galβ1,3Galβ1,4Glc и Galβ1,3Galβ1,6Galβ1,4Glc и их смеси реализуются на рынке под торговыми марками Vivinal® и Elix' или ®. Другими поставщиками олигосахаридов являются Dextra Laboratories, Sigma-Aldrich Chemie GmbH и Kyowa Hakko Co., Ltd. Альтернативно для получения нейтральных олигосахаридов могут использоваться специфические гликозилтрансферазы, такие как галактозилтрансферазы.
N-ацетилированные олигосахариды могут быть получены действием глюкозаминидазы и/или галактозаминидазы на N-ацетил-глюкозу и/или N-ацетил-галактозу. Равным образом, для этой цели могут использоваться N-ацетил-галактозил-трансферазы и/или N-ацетил-гликозил-трансферазы. N-ацетилированные олигосахариды могут быть получены также технологией ферментации с применением соответствующих ферментов (рекомбинантных или природных) и/или микробной ферментацией. В последнем случае микроорганизмы могут либо экспрессировать свои природные ферменты и субстраты, либо могут быть генетически модифицированы с целью продуцирования ими соответствующих субстратов и ферментов. Могут использоваться культуры одного вида микроорганизмов или смешанные культуры. Образование N-ацетилированных олигосахаридов может инициироваться акцепторными субстратами начиная с любой степени полимеризации (DP) от DP=1 и выше. Другим вариантом является химическая конверсия кето-гексоз (например, фруктозы), либо свободных, либо связанных с олигосахаридом (например, лактулозой), в N-ацетилгексозамин или в N-ацетилгексозамин-содержащий олигосахарид, как описано у Wrodnigg, T.M.; Stutz, A.E. (1999) в "Angew. Chem. Int." Ed. 38: 827-828.
Сиалилированные олигосахариды - 3'сиалил-лактоза и 6'сиалил-лактоза - могут быть выделены хроматографией или технологией фильтрации из природного источника, например из молока животных. Альтернативно они могут быть получены также биотехнологией с применением специфических сиалилтрансфераз либо технологией ферментации, основанной на применении ферментов (рекомбинантных или природных), либо микробной ферментацией. В последнем случае микроорганизмы могут либо экспрессировать свои природные ферменты и субстраты, либо могут быть генетически модифицированы с целью продуцирования ими соответствующих субстратов и ферментов. Могут использоваться культуры одного вида микроорганизмов или смешанные культуры. Образование сиалил-олигосахаридов может инициироваться акцепторными субстратами начиная с любой степени полимеризации (DP) от DP=1 и выше.
Бактериальный штамм может выбираться из любого штамма, удовлетворяющего определению пробиотика и сохраняющего эффективность в течение срока хранения продукта, в который предполагается включить препарат изобретения. Например, основным требованием к смесям для детского питания является сохранение ими стабильности и эффективности в течение до 36 месяцев. Разумеется, препарат изобретения может не вводиться в другой продукт, например в пищевой продукт, а потребляться в своем нативном виде или в смеси с подходящим носителем (эксципиентом) в форме порошка или капсулы либо прессоваться, например, в таблетки.
Пробиотический бактериальный штамм предпочтительно представляет собой штамм лактобацилл или бифидобактерий. Предпочтительно используются штаммы, которые продуцируют L(+)-молочную кислоту. Примерами предпочтительных видов Lactobacillus являются Lactobacillus rhamnosus, Lactobacillus paracasei и Lactobacillus reuteri. Особенно предпочтительными штаммами являются Lactobacillus rhamnosus ATCC 53103, Lactobacillus rhamnosus CGMCC 1.3724, Lactobacillus reuteri ATCC 55730 и Lactobacillus paracasei CNCM 1-2116. Примерами предпочтительных видов Bifidobacterium являются Bifidobacterium lactis, Bifidobacterium breve и Bifidobacterium longum. Особенно предпочтительными штаммами являются штамм В. lactis, реализуемый датской компанией Christian Hansen company of Denmark под торговой маркой Bb12, и штамм Bifidobacterium longum ATCC BAA-999, поставляемый японской фирмой Morinaga Milk Industry Co., Ltd. of Japan под торговой маркой ВВ536.
Препарат по изобретению способен обеспечивать от 102 до 1010 KOE пробиотических бактерий на каждый грамм пребиотической смеси.
В предпочтительном аспекте изобретения описанный выше препарат вводится в пищевой продукт. В контексте настоящего изобретения термин "пищевой продукт" означает любое потребляемое вещество. Следовательно, это может быть продукт, предназначенный для потребления человеком, в частности смесь для детского питания, молоко для прикорма и т.п. Однако потребление препарата не ограничивается грудными младенцами и детьми более старшего возраста. В частности, препарат изобретения может вводиться в сухое молоко или зерновые смеси.
Если препарат изобретения предназначен для введения в смесь для детского питания или другую питательную композицию на молочной основе, то указанный препарат может быть приготовлен любым пригодным способом, известным из уровня техники. Например, смесь для детского питания может быть приготовлена путем смешивания источника белка, любых углеводов, кроме лактозы, и источника жира в соответствующих соотношениях. При необходимости могут быть добавлены эмульгаторы. Одновременно могут добавляться витамины и минералы, однако обычно они добавляются позднее во избежание их расщепления при нагреве. Липофильные витамины, эмульгаторы и т.п. можно предварительно растворить в источнике жира перед смешиванием. Затем для получения жидкой смеси можно примешать воду, предпочтительно воду, подвергнутую обработке обратным осмосом.
После этого полученная жидкая смесь может подвергаться тепловой обработке для снижения бактериальной нагрузки. Например, жидкая смесь может подвергаться быстрому нагреву до температуры примерно от 80°C до 110°C в течение примерно от 5 секунд до 5 минут. Это может осуществляться путем прямой инжекции пара или пропусканием через теплообменник, например пластинчатый теплообменник.
Затем жидкая смесь может охлаждаться до температуры примерно от 60°C до 85°C, например, мгновенным охлаждением. После этого жидкая смесь может подвергаться гомогенизации, например, в две стадии при давлении примерно от 7 МПа до 40 МПа на первой стадии и примерно от 2 МПа до 14 МПа на второй стадии. Гомогенизированная смесь может охлаждаться далее до температуры, при которой можно добавлять чувствительные к нагреву компоненты, такие как витамины и минералы. Именно в этот момент удобно стандартизировать гомогенизированную смесь по pH и содержанию сухих веществ.
Гомогенизированная смесь подается в соответствующую сушильную установку, например в распылительную сушилку или сублимационную сушилку, и превращается в порошок. Порошок должен иметь влагосодержание ниже примерно 5% масс.
Препарат по изобретению может быть приготовлен заранее, а позднее добавлен непосредственно в питательную композицию сухим способом смешивания. Однако предпочтительнее добавлять в питательную композицию входящие в препарат компоненты по отдельности, поскольку в этом случае пребиотическая смесь будет добавляться предпочтительно в жидкую фазу прямо перед сушкой, а пробиотический бактериальный штамм будет добавляться предпочтительно в высушенную композицию сухим способом смешивания.
Выбранный пробиотический бактериальный штамм может культивироваться любым пригодным методом, известным из уровня техники, и его подготовка к добавлению в смесь для детского питания может проводиться, например, сублимационной или распылительной сушкой. Альтернативно бактериальные штаммы могут закупаться у специализирующихся на их производстве поставщиков, таких как Christian Hansen и Morinaga, в уже готовом виде и в такой форме, в которой их удобно вводить в пищевые продукты, такие как смесь для детского питания.
Если пребиотическая смесь получена из молока животных, например, как описано ниже, и предназначена для добавления в смесь для детского питания, то удобнее добавлять ее без предварительного удаления всей лактозы. Поскольку смесь для детского питания содержит углеводный компонент, который зачастую полностью или частично представлен лактозой, квалифицированному в данной области техники специалисту понятно, что количество углевода в смеси для детского питания необходимо отрегулировать с учетом количества дополнительного углевода, вносимого вместе с пребиотической смесью. Конечная концентрация препарата по изобретению в пищевом продукте или смеси для грудного ребенка или ребенка более старшего возраста предпочтительно составляет от 0,3% до 6,0%, более предпочтительно от 0,75% до 4,0% масс., в пересчете на сухое вещество. Это соответствует концентрации от 0,2 до 8 г/л, предпочтительно от 1 до 5 г/л восстановленной смеси. Однако указанные количества не следует рассматривать как предельные, а необходимо адаптировать их к той группе населения, для которой они предназначены, например, в случае новорожденных или грудных детей следует учитывать их массу тела и возраст или состояние здоровья. Предпочтительно смесь (или корм), содержащая смесь олигосахаридов по изобретению, скармливается малышу в каждое кормление.
Помимо препарата по изобретению, пищевой продукт, например смесь для детского питания, может содержать один или более других олигосахаридов, которые добавляются по отдельности до конечного содержания олигосахаридов 10 г/л восстановленной или жидкой детской смеси.
Хотя более предпочтительным является дополнение препаратом по изобретению пищевых продуктов целевого назначения, т.е. предназначенных для питания новорожденных или грудных детей, однако может быть полезным также дополнять указанным препаратом и пищевые продукты нецелевого назначения или предназначенные для взрослого населения. Например, смеси олигосахаридов по изобретению могут вводиться в продукты здорового питания и питательные продукты для людей старшего возраста. Такие пищевые продукты могут включать смеси для напитков на молочной основе, йогурты, ферментированные продукты на молочной основе и мороженое, а также продукты на зерновой основе наряду с другими.
Удивительным образом было установлено, что пребиотическая смесь в препаратах по изобретению синергистическим путем усиливает противопатогенные и иммуномодулирующие свойства пробиотика, что обеспечивает лечебный эффект, который значительно превосходит лечебный эффект смеси, например, такого же пробиотика только с одним из пребиотиков. Поэтому препараты изобретения и пищевые продукты, содержащие их, пригодны для предупреждения и лечения желудочно-кишечных инфекций, вызываемых патогенами, в частности бактериальными патогенами, а также инфекции верхних дыхательных путей, такие как воспаление среднего уха. Вот почему пищевые продукты, содержащие препараты по изобретению, особенно пригодны для восприимчивых групп населения, таких как грудные дети и лица пожилого возраста.
Кроме того, препараты изобретения пригодны для поддержания иммунной защиты организма, например, путем усиления ответной реакции на вакцины и снижения продолжительности и тяжести инфекций, а также для предупреждения и лечения состояний, связанных с нарушением функции иммунной системы у грудных детей и детей младшего возраста, такие как пищевая аллергия, экзема, аллергический ринит, атопический дерматит и другие атопические заболевания.
Другим преимуществом препаратов изобретения является то, что они способствуют приживаемости бифидогенной кишечной микробиоты у грудных детей, повышая относительную метаболическую активность различных видов бифидобактерий, которые доминируют в указанной кишечной микробиоте у грудных детей.
Сведения, подтверждающие возможность осуществления изобретения
Изобретение иллюстрируется нижеприведенными примерами.
Пример 1
200000 литров пермеата от ультрафильтрации молочной сыворотки предварительно концентрировали до общего содержания сухих веществ (TS) 22% (масс./масс.), пастеризовали при ~75°C в течение примерно 30 секунд, а затем концентрировали выпариванием при 60°C до достижения TS 59% (масс./масс.). Жидкость охлаждали в кристаллизаторе со скоростью 2°C/час в течение 24 часов для кристаллизации лактозы. Кристаллизованную лактозу промывали, а затем удаляли с помощью отжимных вальцов. Оставшуюся жидкость осветляли в декантаторе. 77000 литров осветленной жидкости с 17,7% TS повторно концентрировали выпариванием при 60°C до достижения TS 55% (масс./масс.) и подвергали стадии вторичной кристаллизации лактозы при тех же условиях, что и ранее. 29000 литров полученного при этом раствора с 20,5% TS подвергали деминерализации комбинированным методом электродиализа и ионного обмена с выходом 28 500 литров деминерализованного на 90% раствора с TS 17,3%. Этот раствор, который содержит около 1,5 г/л смеси, состоящей из примерно 30% масс. GalNAcα1,3Galβ1,4Glc и Galβ1,6GalNAcα1,3Galβ1,4Glc, 50% масс. Galβ1,6Galβ1,4Glc и Galβ1,3Galβ1,4Glc и 20% масс. NeuAcα2,3Galβ1,4Glc и NeuAcα2,6Galβ1,4Glc, в зависимости от исходного материала, можно либо добавлять прямо в пищевой продукт, например смесь для детского питания, либо подвергнуть последующему концентрированию способом, известным per se квалифицированным в данной области техники специалистам.
Например, лактозу, оставшуюся в растворе, можно подвергнуть гидролизу до глюкозы и галактозы, а эти моносахариды можно либо удалить нанофильтрацией, либо в случае необходимости подвергнуть галактозу по меньшей мере частичной полимеризации, например, воздействуя на нее β-галактозидазой с образованием галактоолигосахаридов, которые будут также задерживаться нанофильтрационной мембраной.
Пример 2
100 кг пребиотической смеси, полученной в примере 1 с TS 50%, нагревали до 60°C в стандартном танке и устанавливали pH смеси на уровне pH от 6 до 6,5. Затем на каждый грамм TS добавляли 4,5 мг Lactase F (Amano, Japan) и смесь выдерживали при 60°C в течение трех часов. После этого температуру повышали до 110°C в течение 11 секунд путем прямой инжекции пара с целью инактивирования фермента. Полученная жидкость содержала примерно 100 г/л смеси, состоящей из примерно 10% масс. GalNAcα1,3Galβ1,4Glc и Galβ1,6GalNAcα1,3Gaβ1,4Glc, 87% масс. Galβ1,6Galβ1,6Glc, Galβ1,6Galβ1,4Glc и Galβ1,3Galβ1,4Glc и 3% масс. NeuAcα2,3Galβ1,4Glc и NeuAcα2,6Galβ1,4Glc. Ее можно либо добавлять непосредственно в пищевой продукт, например смесь для детского питания, либо подвергнуть последующему концентрированию, как описано выше.
Пример 3
Пример композиции смеси для детского питания, содержащей препарат настоящего изобретения, дается ниже.
Пример 4
Для сравнительной оценки эффективности препаратов по изобретению с использованием двух различных штаммов пробиотических бактерий и эффективности смесей таких же пробиотических бактерий с другими пребиотиками по предупреждению патогенной инфекции проводили эксперименты in vitro. В качестве показательного токсина, продуцируемого патогенными бактериями, был выбран токсин А, продуцируемый Clostridium difficile.
Кишечные эпителиальные Т84 клетки, выращенные в монокультуре на планшетах Transwell (с двухкамерными лунками с мембраной между камерами), инкубировали (i) только с пробиотиком, (ii) только с пребиотиком или (iii) с комбинацией пробиотика с пребиотиком. После предварительной инкубации в течение 2 часов при 37°C, 5% CO2, Т84 клетки заражали токсином А, продуцируемым C.difficile, в концентрации 100 нг/мл. Трансэпителиальное электрическое сопротивление (TER), которое служит показателем для оценки защиты от действия токсина А, контролировали систематически с определенными интервалами в течение до 24 часов. Был рассчитан нормализованный балльный показатель защиты.
В качестве пробиотических бактериальных штаммов использовали L. paracasei (CNCM 1-2116) и L. rhamnosus (ATCC 53103), причем конечные концентрации обоих штаммов составляли 108 KOE/л.
В качестве пребиотиков использовали описанную выше пребиотическую смесь в количестве 1 г/л; фруктоолигосахариды (Raftilose P95, Orafti, Belgium); галактоолигосахариды (Vivinal GOS, DOMO, The Netherlands) и сиалиллактозу (Kyowa Hakko Kogyo, Japan) в количестве 10 г/л.
Результаты показаны на фиг.1 и 2. Фиг.1 сравнивает результаты, полученные только с пробиотиком, только с пребиотической смесью и препаратом изобретения для двух пробиотических штаммов. Фиг.2 сравнивает результаты, полученные с такими же пробиотическими штаммами, что и на фиг.1, и фруктоолигосахаридами (20 г/л), галактоолигосахаридами (20 г/л) и сиалиллактозой (10 г/л). Лактоза (Sigma) в количестве 20 г/л служила контролем.
Из фиг.1 можно видеть, что препарат изобретения обладает значительным синергистическим эффектом по отношению к токсину А, продуцируемому С. difficile, который сравним с синергистическим эффектом, обеспечиваемым отдельными компонентами (т.е. пребиотической смесью и пробиотическим штаммом) препарата. Из фиг.2 можно видеть, что сравнимый эффект не достигался, когда те же пробиотические бактериальные штаммы тестировались в комбинации только с фруктоолигосахаридами, только с галактоолигосахаридами или только с сиалиллактозой. Можно видеть также, что умеренная защита достигалась при использовании L. rhamnosus в комбинации с сиалиллактозой, но только при 10 г/л, а не при 1 г/л, как в случае препарата изобретения.
Пример 5
Для сравнительной оценки действия на кишечную микробиоту добавки только с пребиотической смесью, только с пробиотическим Bifidobacterium lactis и с препаратом по изобретению проводили эксперименты in vivo с введением модельного образца микробиоты грудного ребенка гнотобионтным животным.
Стерильным мышам принудительно с помощью зонда вводили модельный образец микробиоты грудного ребенка и отводили две недели на приживление указанной микробиоты. Затем мышей распределяли по четырем группам: в первой группе животные получали в составе рациона 3% масс. только пребиотической смеси; во второй - только пробиотический штамм Bifidobacterium lactis CNCM I-3446 (NCC 2818) в воде для питья; в третьей - корм с добавлением пребиотика и воду с добавлением пробиотика; четвертая группа служила контролем. Микробиоту фекалий контролировали в течение всего периода исследований (две недели), по окончании которых животных умерщвляли и исследовали дополнительно микробиоту тонкого кишечника.
Результаты показаны на фиг.3, 4 и 5. Из указанных фигур можно видеть, что препарат по изобретению синергистически стимулировал бифидогенную кишечную микробиоту, что явствует из результатов подсчета количества Bifidobacterium breve в тонком кишечнике (фиг.3) и пониженного количества Staphylococci и Clostridium perfringens в фекалиях (фиг.4 и 5), по сравнению с действием отдельных компонентов препарата.
Пример 6
Для сравнительной оценки действия на приживление и метаболическую активность Bifidobacterium longum в желудочно-кишечном тракте стерильных мышей добавки только с пребиотической смесью, только с пробиотическим штаммом Lactobacillus rhamnosus и с препаратом по изобретению проводили эксперименты in vivo.
Стерильным мышам принудительно с помощью зонда вводили модельный образец микробиоты грудного ребенка и контролировали приживление микробиоты во времени чашечным подсчетом и путем оценки уровней 16S гРНК, указывающей на метаболическую активность. 16S гРНК амплифицировали полимеразной цепной реакцией, продукты разделяли в геле с денатурирующим градиентом и проводили количественную оценку постоянных уровней 16S гРНК Е. Coli, служивших в качестве внутреннего стандарта. Проводили сравнительную оценку следующих рационов: контрольного рациона и контрольного питья (вода); контрольного рациона с добавлением 3% пребиотической смеси и воды; контрольного рациона и Lactobacillus rhamnosus CGMCC 1.3724 (NCC 4007) в воде для питья; контрольного рациона с добавлением 3% пребиотической смеси и Lactobacillus rhamnosus CGMCC 1.3724 в воде для питья.
Результаты показаны на фиг.6. Препарат по изобретению синергистическим путем стимулировал общую метаболическую активность резидента Bifidobacterium longum в процессе приживления микробиоты грудного ребенка у стерильных мышей. Количество резидента В. longum в микробиоте грудного ребенка спустя 14 суток было на одинаковом уровне в контрольной группе и в группах, получавших только пробиотик и только пребиотическую смесь, в то время как значительное повышение синергистическим путем относительной метаболической активности было отмечено в группе, получавшей препарат по изобретению (фиг.6D по сравнению с 6А, В, С).
Реферат
Изобретение относится к фармакологической промышленности, а именно к препарату, содержащему пребиотическую смесь и пробиотический бактериальный штамм. Препарат, содержащий пребиотическую смесь, включающую по меньшей мере один N-ацетилированный олигосахарид, выбранный из группы: GalNAcα1,3Galβ1,4Glc и Galβ1,6GalNAcα1,3Galβ1,4Glc; по меньшей мере один нейтральный олигосахарид, выбранный из группы: Galβ1,6Gal,Galβ1,6Galβ1,4Glc Galβ1,6Galβ1,6Glc, Galβ1,3Galβ1,3Glc, Galβ1,3Galβ1,4Glc, Galβ1,6Galβ1,6Galβ1,4Glc, Galβ1,6Galβ1,3Galβ1,4Glc, Galβ1,3Galβ1,6Galβ1,4Glc; и Galβ1,3Galβ1,3Galβ1,4Glc, и по меньшей мере один сиалилированный олигосахарид, выбранный из группы: NeuAcα2,3Galβ1,4Glc и NeuAcα2,6Galβ1,4Glc, и пробиотический бактериальный штамм, выбранный из штамма Lactobacillus или штамма Bifidobacterium, взятые в определенном количестве. Пищевой продукт, содержащий препарат. Применение препарата в производстве лечебной питательной композиции или лекарственного средства (варианты). Вышеописанный препарат обладает повышенной приживаемостью бифидогенной кишечной микробиоты у грудных детей, позволяет повысить относительную метаболическую активность различных видов бифидобактерий. 6 н. и 11 з.п. ф-лы, 6 ил., 1 табл., 6 пр.

Комментарии