Продукт источника железа в форме частиц и способ их получения - RU2491059C2
Код документа: RU2491059C2
Чертежи







Описание
По данной заявке испрашивается приоритет предварительной патентной заявки США № 61/114261, поданной 13 ноября 2008 г. и европейской патентной заявки EP08166052.4, которые включены в данный документ посредством ссылки.
Область техники изобретения
Настоящее изобретение относится к обогащенным железом продуктам питания и их применению для предотвращения возникновения дефицита железа или для уменьшения дефицита железа в организме человека.
Уровень техники изобретения
Дефицит железа является одним из наиболее частых заболеваний, вызванных нехваткой факторов питания, которое встречается в большинстве развивающихся стран, а также основным заболеванием, вызванным нехваткой факторов питания, в промышленно развитых странах. Обогащение железом некоторых продуктов питания является одним из способов предотвращения возникновения дефицита железа. Однако, для того чтобы обогащенные продукты питания были эффективны для уменьшения дефицита железа, добавленное железо должно быть в достаточной степени биологически доступно.
Подходящее обогащающее железом средство должно удовлетворять ряду требований. Во-первых, оно должно быть безвредным для человеческого организма. Кроме того, оно должно быть нерастворимым в воде в нейтральной или умеренно кислой среде, что является решающим фактором для способности к длительному хранению. Оно должно также иметь высокую абсорбционную способность в организме человека, то есть хорошую биодоступность (что означает хорошую растворимость в желудочно-кишечном тракте). Кроме того, оно должно иметь хорошую стабильность и поддающийся определению химический состав, а также быть продуцируемым воспроизводимым образом, то есть, оно должно иметь гарантированные постоянные и контролируемые свойства.
Биодоступность железа зависит от его химической формы, от чего зависит его растворимость, а также от присутствия пищевых компонентов, либо способствующих, либо препятствующих его абсорбции. Биодоступность тесно связана с сенсорными изменениями. Легко растворимые в воде источники железа, такие как сульфат железа, глюконат железа, лактат железа и двойная соль лимоннокислого железа и лимоннокислого аммония, обладают относительно высокой биодоступностью, однако они имеют недостатки, связанные с обесцвечиванием и изменением вкуса обогащенных ими продуктов, когда они вступают в реакцию с другими компонентами пищи. Фумарат железа, сукцинат железа и сахарат железа медленно растворяются в воде, но легко растворяются в разбавленных кислотах, таких как желудочный сок. Хотя может показаться, что они обладают преимуществами перед сульфатом железа с точки зрения их влияния на окисление жиров и обесцвечивание, их взаимодействие с пищей может уменьшать абсорбцию железа. Отсутствие какого-либо взаимодействия с пищей во время хранения плохо растворимых источников железа, таких как пирофосфат железа, ортофосфат железа и элементарное железо, делает их привлекательными обогащающими веществами с коммерческой точки зрения, и в настоящее время многие изделия из дробленого зерна содержат такие формы железа. Тем не менее, биодоступность этих источников железа всегда низкая.
Таким образом, обычные коммерчески доступные соединения железа оказываются либо достаточно растворимыми в воде, чтобы вызывать технические проблемы, либо так трудно растворимыми, что их абсорбционная способность в организме человека низка.
Были предприняты попытки создания стабильного биодоступного источника железа для обогащения пищи путем инкапсуляции его с инертным соединением, чтобы защитить его от окисления и свести к минимуму его органолептический эффект. Тем не менее, инкапсуляция некоторых солей железа с гидрогенизированным соевым маслом, моно- и диглицеридами или этилцеллюлозой, хотя и обеспечивает определенную защиту для соли железа, как оказалось, не подходит для обогащения некоторых продуктов питания (см. R.F. Hurrell et al. «Iron fortification of infant cereals: a proposal for the use of ferrous fumarate or ferrous succinate», Am. J. Clin. Nutr. 1989, vol.49, pp.1274).
В EP-A-1694312 раскрыты частицы моногидратированного сульфата железа, покрытые слоем альгината натрия. Для получения частиц, раствор альгината натрия распыляют по поверхности твердых частиц сульфата железа при перемешивании. Тонкий слой раствора альгината откладывается на частицах, что способствует образованию пленки альгината железа, покрывающей немодифицированное ядро из сульфата железа. При контакте с водой частицы медленно растворяются, высвобождая ядро из сульфата железа в среду. Соответственно, эти частицы можно включать в обезвоженные продукты питания, такие как мука пшеницы и других зерновых культур, но они не подходят для обогащения пищевых продуктов, содержащих воду, таких как йогурты или соки.
Кроме того, хелатообразователи показали свою эффективность в повышении биодоступности железа и солей железа. Сочетание железа и натриевой соли ЭДТА считается перспективным обогатителем железом. Связыванию ЭДТА железа способствует кислая среда желудка, но в более щелочной среде двенадцатиперстной кишки происходит частичный обмен железа на другие металлы. На основании некоторых исследований с привлечением животных и людей было высказано предположение, что железо диссоциирует из комплекса с ЭДТА в просвете кишечника, прежде чем всасывается, так что оно может транспортироваться с помощью строго регулируемого трансцеллюлярного DMT-1 метаболического пути. Сообщалось также, что сочетание железа и ЭДТА защищает железо от воздействия других ингибиторов абсорбции железа, таких как фитаты или полифенолы. Его потенциал как обогатителя железом был подтвержден в пяти расширенных испытаниях на обогащение продуктов, проведенных в развивающихся странах (L. Zhu et al. «Iron dissociates from the NaFeEDTA complex prior to or during intestinal absorption in rats», J. Agric. Food Chem. 2006, Vol.54, 7929-34). Некоторые органические кислоты с короткой цепью, такие как винная кислота, яблочная кислота, янтарная кислота и фумаровая кислота, демонстрируют возрастание биодоступности соединений железа вплоть до 40-кратного в анализах in vitro с использованием клеток CACO-2 (S. Salovaara et al., «Organic acids influence iron uptake in the human epithelial cell line Caco-2», J. Agric. Food Chem. 2002, Vol.50, p.6233). Предполагаемый механизм действия аналогичен таковому для ЭДТА. Хелатообразователь связывает катион железа, Fe (II) или Fe (III), и сохраняет его от осаждения из-за щелочного рН или любого другого соединения, которое захватывает и осаждает железо. Железо может затем диффундировать к энтероцитам, где оно может быть абсорбировано.
Хотя уже известны различные источники железа для обогащения продуктов питания, по-прежнему существует потребность в обогащающем железом средстве для продуктов питания, которое может быть использовано с водосодержащими продуктами питания и которое имеет хорошую механическую прочность, обеспечивая при этом высокую биодоступность в организме человека и хорошую стабильность обогащенных продуктов во время их хранения.
Сущность изобретения
Авторы изобретения обнаружили продукт, являющийся биодоступным источником железа с улучшенными физическими свойствами, который не растворяется в воде или в слабокислых средах, при добавлении которого к продуктам питания полученные обогащенные железом продукты питания не претерпевают изменения цвета и не становятся прогорклыми, даже если они имеют высокое содержание воды. В то же время, новый продукт источника железа достаточно растворим при рН среды желудка (который в пустом желудке может соответствовать даже 1), чтобы обеспечить хорошую биодоступность. Этот продукт источника железа прост в обращении, имеет хорошую механическую прочность и может систематически воспроизводиться.
Таким образом, один аспект настоящего изобретения относится к обогащенному железом продукту питания, содержащему продукт источника железа в форме твердых частиц, где частицы включают ядро, содержащее альгинат железа, и внешний слой, содержащий альгинат кальция.
Другой аспект настоящего изобретения относится к использованию вышеуказанного обогащенного железом продукта питания для предотвращения возникновения дефицита железа или для уменьшения дефицита железа в организме человека.
Подробное описание изобретения
Термины «биодоступность» и «биодоступный» относятся к степени, в которой питательное вещество или микроэлемент может абсорбироваться и использоваться организмом. Для целей изобретения соли железа, используемые для получения продукта источника железа в форме твердых частиц, применяемых в обогащенном железом продукте питания по настоящему изобретению, должны иметь хорошую биодоступность, что означает хорошую растворимость в желудочно-кишечном тракте. Соответственно, используемые в данном документе термины «биодоступная соль железа», «биодоступная водорастворимая соль железа» и «водорастворимая соль железа» означают любую соль железа, которая свободно растворяется в воде, такую как сульфат железа, глюконат железа, лактат железа и двойная соль лимоннокислого железа и лимоннокислого аммония, а также любую соль железа, которая медленно растворяется в воде, но легко растворяется в разбавленных кислотах, такую как фумарат железа, сукцинат железа и сахарат железа.
Водорастворимые альгинатные соли, такие как альгинат натрия, калия, магния или аммония, представляют собой природные линейные полисахариды из морских бурых водорослей, состоящие из двух типов мономеров, остатков бета-D-маннуроновой (M) и альфа-L-гулуроновой кислоты (G), расположенных нерегулярным образом и блоками вдоль цепи. Биополимер, несущий карбоксильные группы, способен образовывать комплексы с поливалентными ионами металлов.
Когда водорастворимая соль железа входит в контакт с водорастворимой альгинатной солью, происходит сшивание и огеливание карбоновых групп альгината в результате реакции с катионами железа, такими как Fe2+ или Fe3+.
Было установлено, что, когда ядро, содержащее альгинат железа, находится в контакте с водным раствором соли кальция, образуется частица (сформированная ядром, покрытым внешним слоем, содержащим альгинат кальция) в результате реакции альгинатной соли с катионами кальция. Этот внешний слой, будучи нерастворимым в воде или в слабых кислотах, устраняет контакт железа с окружающей средой при одновременном повышении механической прочности частицы. Данный продукт источника железа в форме твердых частиц подходит для обогащения водосодержащих продуктов питания.
В целом, продукт питания, который будет обогащен вышеупомянутым продуктом источника железа в форме твердых частиц, представляет собой продукт питания или напиток, в частности, продукт питания или напиток, который чувствителен к окислению, развитию неприятного вкуса или обесцвечиванию в присутствии свободного железа. В частности, продукт источника железа можно использовать для обогащения водосодержащих продуктов питания, таких как йогурт, молоко, бульоны, соусы, соки и другие напитки, а также обычно обогащаемых продуктов питания, таких как сыпучие продукты, мука пшеничная и других зерновых культур, а также полученных из них продуктов питания, таких как хлеб, макаронные изделия и выпечка. Дополнительными примерами продуктов питания, которые можно обогащать по изобретению, являются мясные эмульсии, такие как сосиски.
При формировании ядра, если количество соли железа выше, чем это необходимо для реакции со всеми мономерами альгинатной соли, соль железа будет захвачена образовавшимся гелем. Напротив, если количество водорастворимой альгинатной соли выше, чем это необходимо для реакции со всеми доступными поливалентными катионами, водорастворимая альгинатная соль также будет являться частью образовавшегося геля. Соответственно, в варианте осуществления первого аспекта настоящего изобретения ядро дополнительно содержит по меньшей мере одну биодоступную соль железа. В другом варианте осуществления этого же аспекта изобретения ядро дополнительно содержит по меньшей мере одну водорастворимую альгинатную соль, такую как альгинат натрия, калия, магния или аммония. Предпочтительно, водорастворимая альгинатная соль представляет собой альгинат натрия.
Растворимые в воде соли железа улучшают биодоступность железа и поэтому являются предпочтительными. Таким образом, предпочтительно, биодоступная соль железа является свободно растворимой в воде солью железа, такой как сульфат железа, глюконат железа, лактат железа и двойная соль лимоннокислого железа и лимоннокислого аммония, или медленно растворимой в воде, но легко растворимой в разбавленных кислотах, такой как фумарат железа, сукцинат железа и сахарат железа. Предпочтительно, биодоступную соль железа выбирают из сульфата железа и сахарата железа. Более предпочтительно, биодоступная соль железа представляет собой сахарат железа.
Кроме того, как упоминалось выше, хелатообразователи продемонстрировали свою эффективность в повышении биодоступности железа и солей железа.
Соответственно, в варианте осуществления первого аспекта настоящего изобретения ядро дополнительно содержит хелатообразователь. Предпочтительно, хелатообразователь выбирают из группы, состоящей из винной, яблочной, янтарной, фумаровой, лимонной, молочной и щавелевой кислот или их соли, ЭДТА и сахарозы. Более предпочтительно, хелатообразователь представляет собой сахарозу. Сочетание железа или соли железа и хелатообразователя при формировании ядра, содержащего альгинат железа, с внешним слоем, содержащим альгинат кальция, по настоящему изобретению улучшает биодоступность железа и в то же время способно изолировать его от окружающей среды за пределами желудочно-кишечного тракта, что позволяет избежать распада матрицы, содержащей железо, и появления неприятного привкуса, связанного с солями железа, используемыми для обогащения продуктов. Как упоминалось выше, сахарат железа включен в число водорастворимых солей железа, используемых по настоящему изобретению, хотя, строго говоря, это комплекс гидроксида железа и сахарозы. Использование сахарата железа в качестве соли железа включает преимущества хелатообразователя благодаря наличию сахарозы.
Указанный продукт источника железа получают следующим способом, включающим стадии: (i) образования ядра, содержащего альгинат железа, путем контактирования по меньшей мере одной биодоступной водорастворимой соли железа и по меньшей мере одной водорастворимой альгинатной соли, (ii) контактирования ядра и водного раствора соли кальция в концентрации, составляющей от 0,025 M до концентрации ниже точки насыщения раствора, и (iii) выделения полученных твердых частиц. Предпочтительно, по меньшей мере одна биодоступная соль железа, используемая для образования ядра, представляет собой сахарат железа. Кроме того, предпочтительно, по меньшей мере одна альгинатная соль, используемая для образования ядра, представляет собой альгинат натрия.
Ядро, используемое для получения частиц, может быть образовано отложением по меньшей мере одной водорастворимой альгинатной соли на поверхности частиц из по меньшей мере одной соли железа. Можно использовать любой метод, который делает возможным отложение альгинатной пленки на частицах соли железа. Предпочтительно, это осуществляется путем распыления раствора альгинатной соли через распылительное сопло на частицы соли железа, происходящего при перемешивании в обычном оборудовании для перемешивания твердых веществ. Для данного метода предназначено такое оборудование, как наклонные пластины или вращающиеся барабаны, которые могут быть снабжены или не снабжены вспомогательными лопастными мешалками для флюидизированного слоя, в которых поддерживается температура и в которых частицы продолжают двигаться вверх и вниз по воздушному потоку, пронизывающему слой частиц.
Продукт источника железа предпочтительно получают, (i) формируя ядро путем растворения или суспендирования по меньшей мере одной биодоступной соли железа в водном растворе по меньшей мере одной водорастворимой альгинатной соли для получения геля, (ii) медленно добавляя полученный гель в водный раствор соли кальция в концентрации, составляющей от 0,025 M до концентрации ниже точки насыщения раствора, при интенсивном перемешивании и (iii) фильтруя и промывая водой полученные твердые частицы.
Когда внутреннее ядро, содержащее альгинат железа, образуется путем растворения или суспендирования по меньшей мере одной соли железа в водном растворе по меньшей мере одной альгинатной соли, во всем ядре происходит перекрестная сшивка альгината катионами железа, что делает само ядро менее растворимым в воде и обладающим большей механической прочностью. Для формирования ядра необходима концентрация альгината натрия выше 0,6% масс./масс. (или эквивалентная концентрация в случае использования другой водорастворимой альгинатной соли). Таким образом, предпочтительно, по меньшей мере одна альгинатная соль представляет собой альгинат натрия и ее концентрация в водном растворе составляет по меньшей мере 0,6% масс./масс. Более низкие концентрации приводят к образованию вязких растворов, но не твердых частиц. Верхний предел концентрации используемой альгинатной соли определяется ее растворимостью в воде и вязкостью полученного раствора альгината.
Концентрацию соли железа, используемой в производстве ядра, можно выбирать по желанию. Более низкие концентрации железа приведут к образованию обедненных железом твердых частиц, в то время как более высокие концентрации приведут к образованию частиц с более высоким содержанием железа. Верхний предел концентрации используемой соли железа определяется ее растворимостью в воде. Полностью удовлетворительные результаты были достигнуты с использованием как железа, так и солей железа, в диапазоне концентраций вплоть до 1 M. Смешивание соли железа с водным раствором альгината проводят при интенсивном перемешивании, чтобы избежать слишком вязкой полученной смеси или образования осадка.
Когда впоследствии смесь в виде геля из железа и альгинатной соли медленно добавляют в раствор, содержащий соль кальция, для образования ядра с внешним слоем, содержащим альгинат кальция, получаются твердые частицы с особенно хорошей механической прочностью. Для образования таких частиц необходима минимальная концентрация кальция выше 0,025 M. Максимальная концентрация не является критической, при условии, что она соответствует концентрации ниже точки насыщения раствора. Любой специалист в данной области хорошо понимает, что точка насыщения раствора, то есть, точка максимальной концентрации, зависит от температуры жидкости, а также от химической природы участвующих веществ.
Концентрацию кальция в процессе приготовления можно использовать для регулирования конечной концентрации кальция в частицах. При добавлении ядра частицы из железа/альгината в раствор кальция можно использовать измельчающее оборудование для уменьшения размера частиц. В приведенных ниже примерах использовали лабораторный гомогенизатор для превращения твердых частиц в песочную пасту. В конечном итоге полученные частицы фильтруют и тщательно промывают водой для удаления любых свободных металлических катионов.
Вышеуказанный продукт источника железа должен иметь размер частиц достаточно небольшой, чтобы допускать хорошее смешивание и не вызывать их обособления при добавлении к обогащаемым продуктам питания, а также для того, чтобы оказывать наименьшее органолептическое воздействие на конечный обогащенный продукт питания. Таким образом, предпочтительный размер частиц по изобретению будет зависеть от обогащаемых продуктов питания.
Способ получения продукта источника железа, используемого для обогащения водосодержащих продуктов питания, позволяет контролировать размер полученных частиц с помощью измельчающего оборудования (чем более тонко измельчает оборудование, тем мельче будут частицы). В процессе производства могут образовываться макроскопические агрегаты частиц, например, агрегаты, имеющие размеры порядка 0,1-1 мм, хотя также получаются и более мелкие образования, соответствующие агрегатам из меньшего числа частиц или отдельным частицам. Таким образом, дополнительно можно проводить классификацию по размеру частиц путем скрининга готового продукта для отбрасывания грубых частиц. Процесс производства частиц позволяет получать очень мелкий порошок с едва заметными частицами. Предпочтительно, средний размер частиц продукта источника железа, который может находиться в форме частиц или некоторых небольших агрегатов частиц, находится в диапазоне от 5 до 20 мкм, хотя могут образовываться частицы даже меньшего размера.
Частицы, составляющие продукт источника железа, используемый для обогащения водосодержащих продуктов питания, характеризуются отличной нагрузочной способностью. Кроме того, они имеют хорошую стабильность при стандартных местных условиях хранения и использования. Таким образом, они незначительно влияют на внешний вид, вкус и поддержание качества обогащенных пищевых продуктов. Кроме того, они доказали свою безопасность для организма человека, то есть они не являются токсичными при пероральном введении, при этом их цитотоксичность даже меньше, чем у свободной соли железа, которую они содержат. Вследствие этого, данные частицы хорошо подходят для обогащения пищевых продуктов, так как они стабильны в течение длительного периода времени в пищевой матрице и способны высвобождать водорастворимый компонент железа при вхождении в желудочно-кишечный тракт.
Количество железа и кальция, содержащееся в частицах, можно определять, сначала солюбилизируя частицы и анализируя раствор методом атомной спектроскопии для количественной оценки. Высокое содержание железа в частицах делает возможным обогащение продуктов питания для обеспечения желаемой абсорбции железа организмом даже при добавлении небольшого количества обогащающего продукта.
Продукт источника железа, используемый для обогащения продуктов питания, можно добавлять в качестве обогащающего железом средства как к обезвоженным продуктам питания, таким как мука пшеничная и из других злаков, а также полученным из них продуктам питания, таким как хлеб, макаронные изделия и выпечка, так и к водосодержащим продуктам питания, таким как йогурт, молоко, бульоны, соусы, соки и другие напитки.
Исключительно высокая механическая прочность твердых частиц, наряду с нерастворимостью их в воде или в слабокислой среде, делает продукт источника железа особенно подходящим для обогащения продуктов питания, которые подвергаются агрессивным производственным процессам и/или агрессивным условиям, свойственным самим продуктам, таким как высокое содержание воды и кислая среда, что происходит в случае обогащения йогурта.
Возможное включение твердых частиц в пищевой носитель было протестировано с помощью йогурта. Йогурт популярен в большинстве групп населения с более высокой склонностью к дефициту железа. Поэтому обогащение йогуртов будет отличным способом борьбы с железодефицитной анемией. Неблагоприятные условия, которым частицы могут подвергаться в йогуртах, служат показателем способности частиц защищать окружающую среду от присутствия растворимого источника железа. Одной из проблем в случае продуктов с высоким содержанием жира, обогащенных железом в высокой концентрации, является окисление жира и развитие прогорклого привкуса. Это не только снижает популярность такого продукта у потребителя, но также уменьшает его питательную ценность.
Как указано в приведенных ниже примерах, обогащенный йогурт был получен с использованием продукта источника железа в форме частиц по настоящему изобретению. Частицы железа добавляли в молоко, а затем проводили пастеризацию, гомогенизацию и ферментацию путем добавления фермента. Результаты проведенных анализов показали, что частицы способны преодолевать трудности, связанные с обогащением йогурта (как связанные с процессом производства, так и со свойствами самого носителя), поскольку конечный продукт был как зрительно (никаких соответствующих изменений ни в цвете, ни во внешнем виде), так и органолептически (не отмечено прогорклого или металлического привкуса) сравним с необогащенным йогуртом. Кроме того, полученный обогащенный йогурт, содержащий продукт источника железа по настоящему изобретению, продемонстрировал хорошую стабильность при хранении. Следовательно, в случае менее проблемных носителей задача будет еще более упрощаться.
Соответственно, в предпочтительном варианте осуществления обогащенный железом продукт питания по изобретению представляет собой йогурт.
В другом предпочтительном варианте осуществления обогащенный железом продукт питания по изобретению представляет собой молоко.
В другом предпочтительном варианте осуществления обогащенный железом продукт питания по изобретению представляет собой напиток.
В другом предпочтительном варианте осуществления обогащенный железом продукт питания по изобретению представляет собой мясную эмульсию.
В следующем предпочтительном варианте осуществления обогащенный железом продукт питания по изобретению представляет собой сосиску.
Кроме того, настоящее изобретение охватывает все возможные сочетания конкретных и предпочтительных групп, описанных выше в данном документе.
Приведенные диапазоны, например, для температуры, времени, размеров и тому подобного, следует считать приблизительными, если прямо не указано иное.
Краткое описание чертежей
На фиг.1 представлено изменение массы тела в граммах у животных в контрольной группе (B) и у животных, принимающих частицы (C). Ось X представляет время в днях, а ось Y - вес в граммах.
На фиг.2 представлено изменение потребления пищи в граммах в сутки на одну клетку в контрольной группе (B) и в группе, принимающей частицы (C).
На фиг.3 представлено изменение потребления воды в граммах в сутки на одну клетку в контрольной группе (B) и в группе, принимающей частицы (C).
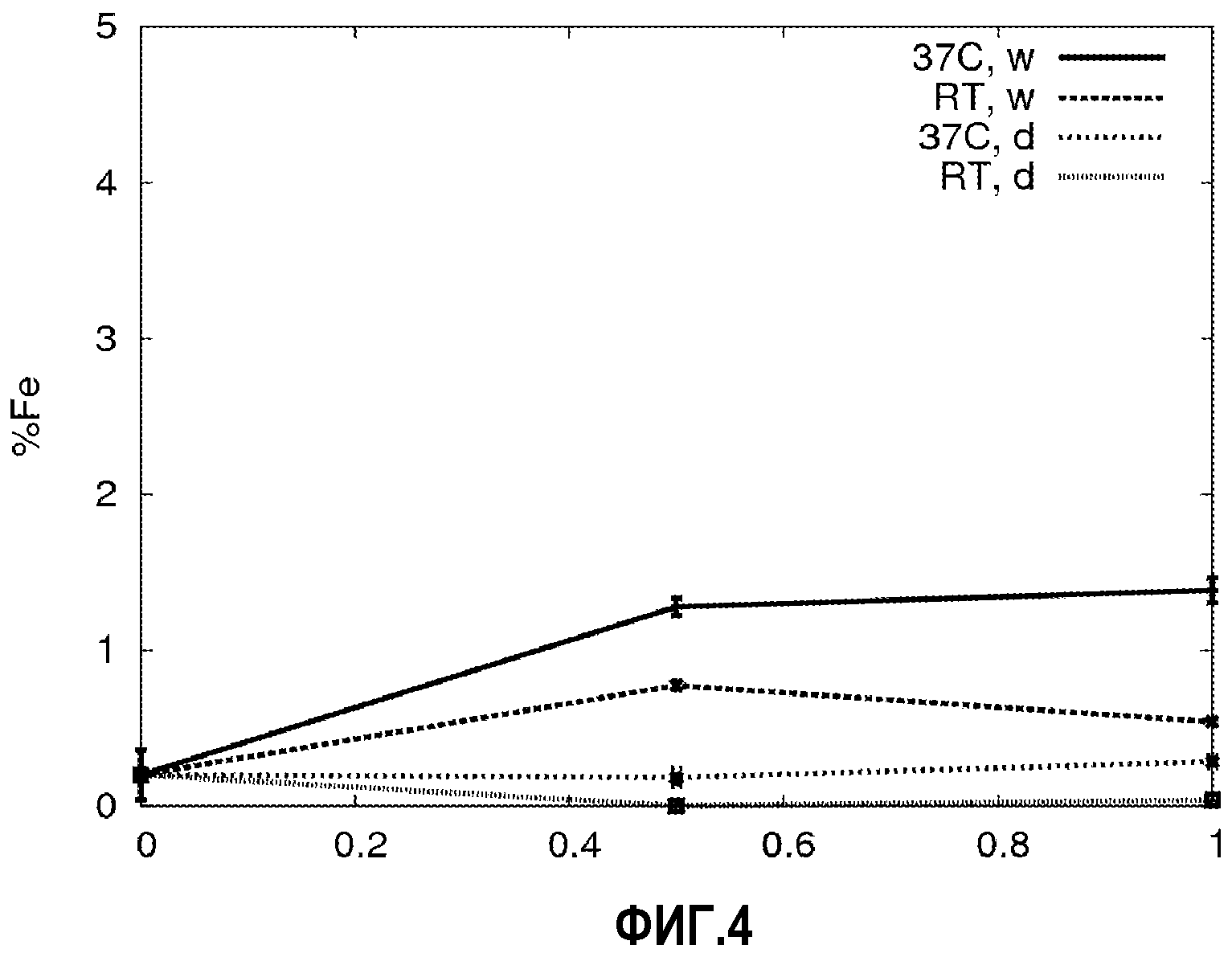
На фиг.4 представлено выраженное в процентах высвобождение железа (% Fe) при четырех различных условиях хранения, где RT = хранение при комнатной температуре, 37C = хранение при 37°C, w = хранение в водном растворе, d = хранение без растворителя. Ось X представляет время в месяцах.
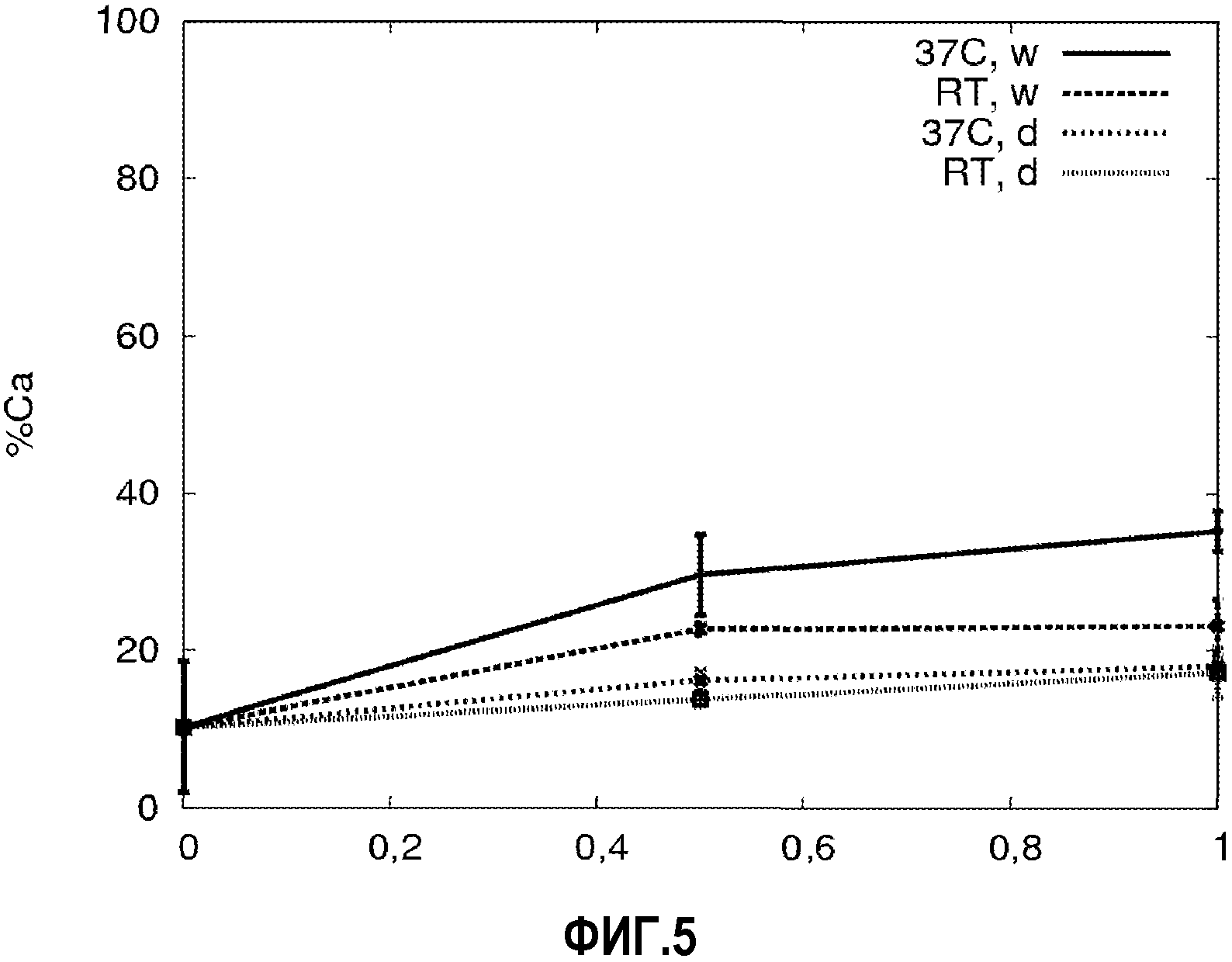
На фиг.5 представлено выраженное в процентах высвобождение кальция (% Ca) при четырех различных условиях хранения, указанных выше. Ось X представляет время в месяцах.
На фиг.6 представлено соотношение катионов металлов, высвобожденных в среду (%Fe/%Ca) через полмесяца и один месяц при четырех различных условиях хранения, указанных выше.
На фиг.7 схематически изображено высвобождение металлов из области, близкой к поверхности: (A) частиц, имеющих внутреннее ядро из альгината железа и внешний слой, содержащий альгинат кальция (представлено заштрихованной областью), и (B) частиц, в которых оба металла гомогенно распределены в альгинатной матрице.
На фиг.8 представлены периоды грудного вскармливания, индукции анемии и восстановления от анемии при тестировании животных в исследовании биодоступности in vivo.
На фиг.9 представлено увеличение веса в процессе восстановления от анемии. Время в днях указано на горизонтальной оси, а вес в граммах - на вертикальной оси. Группы: M = самцы, F = самки, - = отрицательный контроль, + = положительный контроль, c = частицы.
Дополнительные цели, преимущества и новые признаки изобретения будут частично изложены в описании и частично станут очевидными для специалиста в данной области после изучения описания, либо могут быть изучены при применении на практике изобретения. Следующие примеры и рисунки приводятся в качестве иллюстрации и не предназначены для ограничения настоящего изобретения.
Примеры
Пример 1
Способ получения твердых частиц с Fe/Ca
В растворе 1,5 г альгината натрия в 100 мл воды растворяли 7,98 г сахарата железа (примерно 35% Fe). Используя экстракционную воронку, смесь альгината натрия/сахарата железа добавляли по каплям в 300 мл 0,5М водного раствора CaCl2. В процессе добавления по каплям суспензию образовавшихся частиц перемешивали при помощи лабораторного гомогенизатора (Diax 900, Heidolph Instruments GmbH). Полученные твердые частицы отделяли фильтрацией в вакууме. Частицы суспендировали три раза в дистиллированной воде для удаления любой растворимой соли и фильтровали в вакууме. Получали 30 г влажных частиц (частицы 0).
Тот же процесс осуществляли с использованием либо хлорида железа, либо гептагидрата сульфата железа в качестве соли железа вместо сахарата железа. Следующие частицы были успешно получены с использованием любой из трех различных указанных солей железа, а также различных концентраций трех основных компонентов (то есть соли железа, альгинатной соли и соли кальция):
Частицы 1: сахарат железа (35% железа) 1M, CaCl2 0,1М, альгинат натрия 1,5%.
Частицы 2: сахарат железа (35% железа) 1M, CaCl2 0,1М, альгинат натрия 3,0%.
Частицы 3: сахарат железа (35% железа) 1M, CaCl2 1M, альгинат натрия 1,5%.
Частицы 4: сахарат железа (35% железа) 1M, CaCl2 1M, альгинат натрия 3,0%.
Частицы 5: FeSO4·7H2O 1M, CaCl2 0,1М, альгинат натрия 1,5%.
Частицы 6: FeSO4·7H2O 1M, CaCl2 0,1М, альгинат натрия 3,0%.
Частицы 7: FeSO4·7H2O 1M, CaCl2 1M, альгинат натрия 1,5%.
Частицы 8: FeSO4·7H2O 1M, CaCl2 1M, альгинат натрия 3,0%.
Частицы 9: FeSO4·7H2O 0,1M, CaCl2 0,1М, альгинат натрия 1,5%.
Частицы 10: FeSO4·7H2O 0,1M, CaCl2 0,1М, альгинат натрия 3,0%.
Частицы 11: FeSO4·7H2O 0,1M, CaCl2 1M, альгинат натрия 1,5%.
Частицы 12: FeSO4·7H2O 0,1M, CaCl2 1M, альгинат натрия 3,0%.
Частицы 13: FeCl4 0,1M, CaCl2 0,1М, альгинат натрия 1,5%.
Частицы 14: FeCl3 0,1M, CaCl2 1M, альгинат натрия 1,5%.
Полученные частицы имели цвет в зависимости от используемой соли железа. Низкое высвобождение катионов из частиц делает их безвкусными и суспендируемыми в воде.
Пример 2
Размеры частиц продукта источника железа
Для того чтобы оценить размер частиц, полученных в примере 1 (частиц 1-14), использовали оптический микроскоп, откалиброванный для измерения длины. Во всех случаях макроскопические агрегаты частиц были хорошо видны даже невооруженным глазом, и наиболее четко - при использовании микроскопа. Хотя эти агрегаты имели размеры порядка 0,1-1 мм, можно было наблюдать гораздо более мелкие образования, возможно, агрегаты меньшего количества частиц или отдельные частицы.
Небольшую, едва видимую часть образца частиц помещали на помеченное предметное стекло микроскопа. К частицам добавляли одну каплю воды. Суспензию слегка перемешивали с помощью металлического ножа и на каждое предметное стекло микроскопа помещали покровное стекло. Каждый образец изучали, используя оптический микроскоп (Nikon Eclipse E800, Nikon Corp., Tokyo, Japan) с 20× объективом и 10× окуляром. Для каждого образца выбирали область, в которой можно было наблюдать либо отдельные частицы, либо наименьшие кластеры частиц. Эту область фотографировали с помощью цифровой камеры (Soft Imaging Systems, Colorview II), подключенной к ПК, управляющему анализатором изображения (analySIS3.0, SoftImaging System Corp., Lakewood Co.). На каждое изображение накладывали калиброванную шкалу для определения размера.
Полученные изображения свидетельствовали о том, что размер частиц и некоторых из наименьших агрегатов, как правило, был близок к 20 мкм, в некоторых случаях уменьшался до менее чем 5 мкм. При помощи более грубого измельчающего оборудования можно получать частицы большего размера, хотя для обогащения продуктов питания, как правило, предпочтительны более мелкие частицы.
Пример 3
Характеристика твердых частиц
0,3 г влажных частиц расщепляли в микроволновой печи в концентрированной азотной кислоте. Концентрацию железа и кальция количественно определяли методом ICP-OES (оптической эмиссионной спектроскопии индуктивно-связанной плазмы).
Количество железа и кальция в частицах почти не зависело от партии анализируемых частиц. Две партии частиц были получены в соответствии с примером 1 (частицы 0). Концентрации железа и кальция, выраженные в процентах от веса (± стандартное отклонение), в двух партиях приведены ниже в таблице 1.
Для обеих партий не только были получены очень сходные результаты, но также наблюдалась превосходная нагрузочная способность частиц.
Пример 4
Цитотоксичность твердых частиц
Для проверки отсутствия токсичности у частиц по изобретению, содержащих соль железа, проводили тест in vitro. Тест включал инкубацию клеток клеточной линии HELA с веществами, цитотоксичность которых предстояло проверять, этот тест широко используется как способ проверки токсичности. Тестируемые соединения включали частицы, а также их основные составляющие в отдельности: соль железа, используемую в частицах (сахарат железа), и альгинат натрия. Также готовили отрицательный контроль, содержащий только ростовую среду для HELA, который использовали для контроля роста.
Тестируемые среды готовили в стерильных условиях. Частицы, полученные как в примере 1 (частицы 0; партия 2 примера 3), стерилизовали в автоклаве (20 мин, 110°C). Используя стерильный материал, 72 мг частиц (среды с частицами), 17 мг сахарата железа (среды с солью железа) и 18 мг альгината натрия (среды с альгинатом) в отдельности растворяли в 50 мл ростовой среды для HELA. Частицы были нерастворимы и оставались в виде суспензии. Разведения 1:1, 1:10 и 1:100 каждой из тестируемых сред получали, разводя следующие количества сред с частицами, солью железа или альгинатом свежей ростовой среды для HELA:
1:1 20 мкл + 0 мкл свежей среды для HELA
1:10 2 мкл + 18 мкл свежей среды для HELA
1:100 0,2 мкл + 19,8 мкл свежей среды для HELA
Растворы 1:1 частиц и соли железа имели практически одинаковую концентрацию железа (0,285 мг железа/мл и 0,297 мг железа/мл, соответственно). То же самое относится к их разведениям 1:10 и 1:100.
3500 клеток HeLa культивировали в 36 лунках двух 96-луночных планшетов: 9 контрольных лунок и 27 лунок для трех повторов 3 концентраций 3 продуктов. В каждую лунку добавляли среду до 100 мкл. Клетки инкубировали при 37°C в течение 24 час. 20 мкл каждой из тестируемых сред и 80 мкл свежей среды добавляли в каждую лунку. В контроли добавляли только 100 мкл свежей среды. Один из планшетов инкубировали в течение 24 час, а другой в течение 72 час. Жизнеспособность клеток определяли через 24 и 72 час инкубации при помощи EZ4U нерадиоактивного теста на клеточную пролиферацию и цитотоксичность (Biomedica Medizinproducte GmbH).
Результаты выражали в процентах от роста по отношению к контролю, то есть, как процент жизнеспособности, который рассчитывался как количество живых клеток в каждом из тестируемых растворов (частиц, сахарата железа или альгината натрия), разделенное на количество живых клеток в отрицательном контроле, и выражали в процентах. Результаты, приведенные ниже в таблице 2, свидетельствуют, что цитотоксичность инкапсулированного железа меньше, чем у свободного железа. Принимая во внимание, что сахарат железа является безопасной пищевой добавкой, таковой является и инкапсулированная форма. Никакой токсичности не наблюдалось также и для альгината натрия.
Пример 5
Острая токсичность частиц
Тест in vivo проводили для оценки отсутствия токсичности для крыс в дозе, 100-кратно превышающей ту, что предусмотрена для людей. Референтной дозой для людей считали две трети от RDI (рекомендуемой суточной дозы) для человека массой 70 кг (0,14 мг Fe/кг массы тела). Вследствие этого, дозу 14 мг Fe/кг массы тела использовали в данном исследовании острой токсичности на крысах.
Частицы железа, использованные в этом тесте, были изготовлены как в примере 1 (частицы 0; партия 2 примера 3). Поскольку частицы были предназначены для употребления в пищу животными, их изготавливали в стерильных условиях, чтобы избежать загрязнения частиц патогенными микроорганизмами.
Используемые животные описаны ниже:
- Вид и линия: крысы, Sprague-Dawley (SD), Crl:CD, предоставлены компанией Charles River Laboratories, Франция.
- Количество и тип животных: 12 нерожавших и не беременных самок крыс.
- Возраст (во время применения продукта): 2 недели.
- Вес (во время применения продукта): 172-193 г.
- Критерии включения: ±20% от среднего веса в начале исследования.
- Группы: Животных разделяли на две группы (контрольную и тестируемую), исходя из равномерного распределения веса животных в группах.
График исследования был следующим:
- День -5: Животные прибывают на объект. Начало карантина в карантинном помещении.
- День -3: Окончание карантина. Начинается период акклиматизации в определенном помещении.
- День 0: Введение контрольного или тестируемых растворов. Начало исследования.
- День 14: Окончание исследования. Эвтаназия с помощью пентобарбитала и некропсия.
Крысы проводили два дня в карантинном помещении и следующие три дня в определенном помещении для акклиматизации. Стандартные условия содержания были следующими: 20-24°C, 30-70% относительная влажность (RH) и более 15 смен воздуха в час. Температуру и влажность постоянно контролировали. Использовали световой цикл из 12 час флуоресцентного света и 12 час темноты. Животных (по два в клетке) обеспечивали пищей и водой (декальцинированной водопроводной водой, фильтрованной и облученной УФ-светом) без ограничений.
Введение частиц и контроля, а также наблюдения проводили, как описано ниже:
Вводимый объем: 2 мл/кг массы тела вводили однократно (день 0 исследования). Контрольная группа получала только транспортную среду (дистиллированная вода), а тестируемая группа получала 87 мг/мл суспензии частиц (14 мг/кг массы тела железа).
Интервал введения: Время, прошедшее между началом введения первому животному и окончанием введения последнему животному, составляло 45 минут.
Смертность и заболеваемость: Оба показателя проверяли в течение дня 0 через 5, 15, 30, 90 минут, 2, 4, 6 и 8 час после введения, и ежедневно до дня 14.
Масса тела: Регистрировали ежедневно со дня 3. В день 0 животных взвешивали перед введением.
Потребление пищи и воды: Регистрировали три раза в неделю (по понедельникам, средам и пятницам), начиная со дня 3.
Клинические симптомы: Проверяли через 5, 15, 30, 90 минут, 2, 4, 6 и 8 час после введения, и ежедневно в течение следующих 13 дней.
Все процедуры, используемые в настоящем исследовании, имели в основе и строго следовали следующим законодательным актам: Директиве Европейской комиссии 2003/63/EC от 25-го июня 2003 г., которая изменяет директиву 2001/83/EC и относится к медицинским продуктам для человека. Процедуры и оборудование для содержания животных находились в строгом согласовании с требованиями по защите животных, используемых в экспериментах:
- Директива Европейской комиссии 2003/63/EC
- Европейская директива 89/609/EEC
- Испанский Real Decreto 1201/2005
- Руководство FELASA
- Документ OECD ENV/JM/MONO (2000)7
Вышеуказанные параметры проверяли для каждой из крыс, и контрольную и экспериментальные группы сравнивали, используя критерий Стьюдента с альфа<0,05 (если применимо). Среди всех животных не наблюдали никакой спонтанной смертности. Ни у кого из животных не было обнаружено существенных клинических признаков, свидетельствующих о необходимости умерщвления, на протяжении 14-дневного периода наблюдения. Не было обнаружено существенной разницы ни в массе тела (см. таблицу 3 ниже, в которой средние значения были получены на основании результатов для 6 животных; фиг.1), ни в потреблении пищи и воды (см. таблицу 4 ниже, в которой средние значения были получены на основании результатов для 3 групп животных (3 клетки); фиг.2 и фиг.3, соответственно) между группами, принимающими добавку и не принимающими добавку. Значения в скобках соответствуют стандартному отклонению. Макроскопические посмертные наблюдения были аналогичными для групп, принимающих и не принимающих добавку.



Из вышеприведенных результатов можно сделать вывод, что, вследствие отсутствия смертности или любых относящихся к продукту клинических признаков, тестируемый продукт не вызывает острую токсичность и не токсичен при пероральном введении восьминедельным самкам крыс Sprague-Dawley в эквивалентной дозе железа, соответствующей 14 мг/кг массы тела.
Пример 6
Стабильность твердых частиц
Способность частиц противостоять высвобождению их полезной нагрузки в процессе хранения тестировали в различных условиях, близких к тем, которые можно найти в различных средах, в которые предстоит помещать частицы. Частицы были разделены на четыре группы, и каждая группа подвергалась различным условиям:
1. Хранение при комнатной температуре (RT), водный раствор
2. Хранение при комнатной температуре, твердые частицы
3. Хранение при 37°C, водный раствор
4. Хранение при 37°C, твердые частицы.
Два различных типа условий с точки зрения содержания воды были выбраны для моделирования двух диаметрально противоположных внешних условий, в которые, наиболее вероятно, будут помещены частицы: жидкие продукты питания или продукты питания с высоким содержанием воды, и сухие продукты питания или продукты питания с низким содержанием воды. Поскольку продукты питания или пищевые добавки, как правило, хранятся при комнатной или более низкой температуре, и поскольку чем выше температура, тем более агрессивна окружающая среда, эксперименты проводили при комнатной температуре. Также использовали более высокую температуру для экстраполяции на более длительное хранение при более низких температурах, а также для моделирования поведения частиц в более жестких условиях, чем те, с которыми они, вероятно, столкнутся.
Используемые частицы железа были изготовлены, как в примере 1 (частицы 0; партия 2 примера 3). Любые следы железа с пластикового или стеклянного материала, используемого в экспериментах, удаляли, оставляя его погруженным в течение ночи в 10% (об./об.) раствор концентрированной соляной кислоты или азотной кислоты и промывая 5-6 раз избытком воды категории mili-Q. Два образца и контроль были подготовлены для каждого анализа в стерильных условиях путем взвешивания примерно 120 мг частиц (за исключением контроля) и добавления 15 мл дистиллированной воды (за исключением экспериментов с «твердыми частицами»). Каждый образец хранился запечатанным при комнатной температуре или при 37°C в течение 0, 0,5 или 1 месяца. Через 0, 0,5 или 1 месяц к образцам с «твердыми частицами» добавляли 15 мл дистиллированной воды. Все анализируемые образцы затем фильтровали для удаления твердых частиц и высвободившиеся железо и кальций количественно определяли в супернатанте методом ICP-AOS.
Высвобождение железа и кальция из частиц использовали как индикатор стабильности частиц. Чем меньше высвобождается железа, тем лучше способность частиц сохранять полезную нагрузку в частицах и защищать окружающую среду от разрушения железом, а железо от захвата окружающей средой. Высвобождение железа (среднее значение из двух образцов) при четырех различных условиях хранения представлено ниже в таблице 6 (см. также фиг.4). Значения в скобках соответствуют стандартному отклонению.

Из данных по высвобождению нагруженного в частицы железа, приведенных выше, видно, что стабильность частиц превосходна. В наиболее жестких условиях высвобождается всего лишь менее чем 1,4% инкапсулированного железа. Сравнивая скорость высвобождения в различных условиях, можно увидеть, как присутствие воды и температура хранения влияет на стабильность частиц. Среди четырех групп тенденция совершенно очевидна. Повышение температуры (37°C вместо комнатной температуры, примерно 20-25°C) увеличивает скорость высвобождения, так же как и в случае контакта частиц с большим количеством воды. Из предыдущих результатов можно также заметить, что эффект от добавления воды к частицам или содержание их в среде с высокой активностью воды имеет более сильное влияние на скорость высвобождения железа, чем повышение температуры от комнатной температуры до 37°C. Хорошие скорости высвобождения, достигнутые при хранении частиц в водном растворе и при 37°C, даже улучшались, когда температура понижалась до более реалистических значений. При комнатной температуре максимальная скорость высвобождения составляет только 0,5410% ± 0,0050 спустя первый месяц. Показатели частиц становятся близки к превосходным, если их хранить также при комнатной температуре, но в условиях низкой активности воды: никакого высвобождения железа не обнаружено в течение первых двух недель (высвобождение железа было меньше 0,017%) и всего лишь 0,037% ± 0,011 полезной нагрузки было потеряно в окружающую среду через месяц хранения.
Результаты несколько отличались для количества высвободившегося кальция, как показано ниже в таблице 7 (см. также фиг.5). Значения в скобках соответствуют стандартному отклонению.

Доля кальция, высвободившегося в окружающую среду, более чем в десять раз превышает таковую для железа, свидетельствуя, что способность частиц удерживать металлы внутри гораздо выше для железа, чем для кальция. Высвобождение кальция означает, что, скорее всего, частицы изнашиваются со временем, но поскольку кальций является более доступным, чем железо, кальций первым высвобождается в окружающую среду. Если бы частицы были изготовлены с использованием только железа, то в окружающую среду высвобождалось бы железо, а не кальций.
Пример 7
Структура частиц
Получение частиц с использованием двух различных катионов металлов, железа и кальция, было выбрано с целью обеспечения частиц дополнительным слоем защиты по сравнению с тем, что образуется только благодаря альгинатному полимеру. Порядок, в котором катионы металлов добавляются в процессе получения частиц, также выбран специально, чтобы способствовать формированию внутреннего ядра, содержащего альгинат железа (то есть богатого железом), и внешнего слоя, содержащего альгинат кальция (то есть богатого кальцием). Это гарантирует, что если частицы изнашиваются во время их хранения или обработки, области, богатые кальцием, будут высвобождаться в окружающую среду, задерживая высвобождение железа из ядра, содержащего альгинат железа.
Как видно из данных, полученных в исследовании стабильности частиц, при всех тестируемых условиях доля высвободившегося кальция гораздо больше, чем доля железа (см. таблицы 6 и 7 и фиг.6). Этот факт полностью согласуется с предполагаемой структурой частиц, где внутренний слой содержит альгинат железа, а внешний слой содержит альгинат кальция. Высвобождение металлов из частиц обусловлено химической солюбилизацией их компонентов или физическим износом частиц. В обоих случаях в первую очередь высвобождение происходит из области, близкой к поверхности частиц. Поскольку частицы намного богаче железом, чем кальцием (7,93% Fe против 1,23% Ca), большая часть кальция должна быть расположена близко к поверхности частицы, тогда как большая часть железа должна быть расположена вдали от нее, как это изображено на фиг.7 (A). Если бы распределение обоих металлов в частицах было полностью однородным, как изображено на фиг.7 (B), можно было бы ожидать, что соотношение высвободившегося железа/кальция будет близко или равно таковому у частиц, и отношение высвободившийся % Fe/высвободившийся % Ca будет близко к 1. Наблюдаемое соотношение более чем в 23 раза меньше, чем соотношение, предсказанное на основании данной модели. Так что это подтверждает слоистую структуру частиц, имеющих внутреннюю область, богатую железом, и внешнюю оболочку, богатую кальцием.
Пример 8
Тесты на биодоступность - растворимость
Абсорбция Fe происходит в желудочно-кишечном тракте. Величина pH в желудке меняется в течение дня в зависимости от количества пищи, находящейся в нем. В целом, среда в желудке довольно кислая. На пустой желудок величина pH может достигать даже 1, возрастая примерно до 5 после полноценного приема пищи.
Так как полный анализ биодоступности на людях является очень сложным и трудоемким, биодоступность продукта источника железа по изобретению сначала оценивали, используя в качестве эталона растворимость в искусственной среде желудка.
Биодоступность частиц железа зависит от их способности высвобождать полезную нагрузку. Если частицы настолько стабильны, что они выдерживают среду желудочно-кишечного тракта, не высвобождая свое содержимое, биодоступность железа будет близка к нулю, поскольку частицы слишком велики, чтобы абсорбироваться в кишечнике. С другой стороны, если частицы дестабилизируются в процессе прохождения через желудочно-кишечный тракт, полезная нагрузка будет высвобождена в виде растворимой соли железа, которая будет абсорбирована в кишечнике, обеспечивая высокую биодоступность инкапсулированного железа. Эксперимент in vitro, проведенный для оценки высвобождения полезной нагрузки во время кислотного расщепления, имел целью выявление высвобождения железа из частиц при расщеплении соляной кислотой при pH=2, близком к значению pH в желудке.
В 10-мл пробирке Эппендорфа взвешивали 10 мг частиц с сахаратом железа, полученных как в примере 1 (частицы 1), а затем добавляли 9 мл воды. Пробирку Эппендорфа энергично встряхивали вручную для облегчения ресуспендирования частиц. Большинство частиц легко ресуспендировались, хотя некоторые крупные агрегаты частиц оставались на дне пробирки. Каплю суспензии помещали на предметное стекло микроскопа для осмотра. Частицы, а также некоторые более крупные агрегаты были видны при 100× увеличении. (Olympus CH-2, 10× окуляр, 10× объектив). В пробирку Эппендорфа добавляли 1 мл 0,1M HCl в воде и энергично встряхивали. Вторую каплю кислой суспензии также помещали на предметное стекло микроскопа и сравнивали с предыдущей каплей. Больших различий между двумя каплями не наблюдали. Через 30 минут кислотного расщепления, каплю с частицами помещали на предметное стекло микроскопа. Перед осмотром под микроскопом каплю 1M NaOH приводили в контакт с первой каплей и смесь рассматривали под микроскопом. Растворение частиц было почти мгновенным, поскольку NaOH диффундировал сквозь суспензию частиц.
Небольшой образец со свежими частицами помещали на чистое предметное стекло микроскопа. Каплю 1M NaOH помещали сверху на частицы. Не наблюдали никаких изменений в структуре частиц и частицы оставались стабильными в течение всего времени наблюдения (до тех пор, пока капля не испарялась, оставляя осадок NaOH с включенными частицами).
Эксперимент по высвобождению состоял из двух стадий. На первой стадии частицы суспендировали в кислой среде при примерном значении pH, равном 2. Это значение pH близко к значению pH в желудке. В таких условиях не наблюдали видимых изменений в структуре частиц, о чем свидетельствовали две микрофотографии, полученные при 100× увеличении. Такое отсутствие изменений при суспендировании частиц в дистиллированной воде или в 0,01 M HCl не удивительно, если принять во внимание химические вещества, ожидаемые в данных растворах. В дистиллированной воде частицы стабильны, образуя осадок альгината железа и альгината кальция. Взаимодействие железа и кальция с альгинатом является сильным из-за присутствия карбоксилатных групп (-COO-) в альгинатном полимере. Закисление суспензии ниже значения pKa альгиновой кислоты (pKa>4) преобразует карбоксилатные группы (-COO-) в карбоксильные группы (-COOH), которые имеют значительно более слабое взаимодействие с катионами. Это является важным событием, которое приводит к высвобождению полезной нагрузки частиц. Хотя непротонированная форма альгинатов (-COO-) относительно растворима в воде, протонированная форма нерастворима. Это объясняет отсутствие видимых изменений, поскольку полимерная матрица остается нерастворимой, хотя и отличающейся химически, что можно продемонстрировать на следующей схеме реакции:

Преобразовав альгинат в альгиновую кислоту, высвобождение металлов измеряют опосредованно, солюбилизируя альгиновую кислоту в щелочной среде. Если катионы высвободились, то оставшееся представляет собой растворимые хлориды железа и кальция и нерастворимую альгиновую кислоту. Подщелачивание среды, например, с помощью 1M NaOH, приведет к растворению осадка альгиновой кислоты. Это быстрое растворение объясняется преобразованием альгиновой кислоты обратно в альгинат натрия. Железо и кальций присутствуют в слишком низкой концентрации, чтобы образовывать осадок с альгинатом натрия, который в форме альгината является растворимым.
С другой стороны, если катионы все еще связаны с альгинатной матрицей, подщелачивание преобразует альгиновую кислоту обратно в альгинат, который нерастворим, когда связан железа и кальция. Таким образом, подщелачивание частиц, проведенное для нерасщепленных частиц, должно оставлять их без изменений, поскольку карбоксильные группы, присутствующие в частицах, уже находятся в форме карбоксилата (-COO-) и сильно взаимодействуют с обоими катионами, железа и кальция. Небольшую часть нерасщепленных частиц, суспендированных в 1M NaOH, также фотографировали под микроскопом, изображение оставалось неизменным с течением времени, что, как ожидалось, выявило, что частицы стабильны, если они не расщеплены и хранятся в 1M NaOH.
Непрямое высвобождение металлов, наблюдаемое с помощью этого эксперимента, показывает, что после попадания в желудок кислый pH преобразует нерастворимые частицы в нерастворимую альгиновую кислоту и растворимые соли кальция и железа. Поскольку растворимые соли железа обладают высокой биодоступностью, ожидаемая биодоступность этих частиц также высока. Вследствие этого, данные частицы хорошо подходят для обогащения пищевых продуктов, поскольку они стабильны в течение длительного периода времени в пищевой матрице и способны высвобождать металлы при вхождении в желудочно-кишечный тракт.
Пример 9
Биодоступность - тест in vivo
Данное исследование биодоступности направлено на сравнение биодоступности микроинкапсулированного железа с таковой у сульфата железа. Сульфат железа был выбран в качестве положительного контроля, поскольку он не только широко используется для стандартных исследований биодоступности железа, но он также обладает высокой биодоступностью.
Исследование было разработано для оценки возможности восполнять недостаток железа у анемичных крыс при помощи трех различных источников железа:
- Отрицательная контрольная группа: базовая диета, обедненная железом, без добавления железа
- Положительная контрольная группа: базовая диета, обедненная железом, с обогащением 10 ppm железа из растворимого сульфата железа
- Тестируемая группа: базовая диета, обедненная железом, с обогащением 10 ppm железа из микрочастиц железа (инкапсулированный сахарат железа).
Три диеты были составлены на основе рекомендованной AIN-93G диеты для экспериментов на грызунах без добавления железа (по сообщениям, содержащей 2-6 ppm Fe). Базовую диету использовали в качестве отрицательного контроля. Положительную контрольную диету готовили, дополняя базовую диету 10 ppm Fe с помощью 50 мг/кг FeSO4·7H2O. Тестируемую диету готовили, дополняя базовую диету 10 ppm Fe с помощью 125 мг/кг микроинкапсулированного железа 7,93% масс./масс. Fe в микрочастицах в форме сахарата железа). Диеты и дистиллированную воду предоставляли без ограничений на протяжении всего исследования.
Использовали 40 крыс линии Sprague Dawley (20 самцов, 20 самок) из 4 различных пометов. Крысы были отлучены от матери в возрасте 21 дня (день 0, начало исследования) и случайным образом рассажены в клетки из нержавеющей стали. В каждой клетке размещали по два животных одного пола. Животных содержали в контролируемых условиях (20-22°C, 30-50% RH, световой цикл: 08:00 ч-20:00 ч).
Анемию индуцировали в трех группах животных, которых кормили базовой диетой без железа в течение первых 22 дней (самки) или 23 дней (самцы) исследования, как показано на фиг.8. После периода индукции анемии диеты в трех группах были изменены на
- Отрицательный контроль: 3 клетки с самцами и 3 клетки с самками (6+6 животных). Эта группа продолжала получать базовую диету без добавления железа.
- Положительный контроль: 3 клетки с самцами и 3 клетки с самками (6+6 животных). Эта группа получала базовую диету, обогащенную 10 ppm Fe в форме сульфата железа
- Тестируемая группа: 4 клетки с самцами и 4 клетки с самками (8+8 животных). Эта группа получала базовую диету, обогащенную 10 ppm Fe в форме микроинкапсулированного железа (инкапсулированный сахарат железа).
Животным давали возможность восстановиться от анемии в течение 2 недель (14 дней). По истечении этого периода их анестезировали вдыханием изофлурана (индукционная доза: 3%, поддерживающая доза: 1,5-2%) и подвергали эвтаназии удалением крови через внутрисердечный прокол. Животных периодически взвешивали на протяжении всего эксперимента. Количество потребляемой пищи также измеряли.
Изменение массы тела во время восстановительного периода представлено в таблицах 8 и 9 (см. также фиг.9).


Результаты продемонстрировали четкое различие между тремя различными группами, с гораздо большим и сходным увеличением массы тела в группах с применением обогащения пищи, при этом группа, употребляющая базовую диету, сильно отставала от других двух групп. Статистически не существовало никаких существенных различий между двумя группами с применением обогащения пищи в период восстановления от анемии. С другой стороны, показатели массы тела в любой из двух групп с применением обогащения пищи (положительном контроле и тестируемой группе) были значительно выше, чем масса тела у отрицательного контроля.
Та же картина наблюдается и при изучении эффективности питания. Эффективность питания определяется как:
и относится к тому, как пища преобразуется в ткани тела. Рассчитанные значения эффективности питания для трех групп в период восстановления от анемии представлены в таблице 10. Значения в скобках соответствуют стандартному отклонению.
Среди групп самцов и самок различия являются значительными только между отрицательным контролем и любой из групп с применением пищевых добавок, но не между группами с применением пищевых добавок. Таким образом, можно сделать вывод, что различия между сульфатом железа и микрочастицами железа статистически не значимы, но они являются статистически значимыми между отрицательным контролем и микрочастицами железа. Вследствие этого, биодоступность микроинкапсулированного железа должна быть такой же, как у сульфата железа, но без многих недостатков растворимой соли железа.
Пример 10
Обогащенный йогурт
Изучали включение продукта источника железа в форме частиц по настоящему изобретению в йогурт, выступающий в роли пищевого носителя. Тестирование частиц путем включения их в йогурт было выбрано по следующим причинам:
- Йогурт имеет кислый pH, который является достаточно агрессивным для разрушения продуктов источника железа в форме частиц, уже раскрытых в предшествующем уровне техники. Это вызовет высвобождение содержимого частиц и порчу йогурта.
- Йогурт имеет высокое содержание воды, также агрессивной среды для других уже известных продуктов источника железа. Содержание воды вместе с ее кислотностью облегчает солюбилизацию железа, что делает обогащение им более трудной задачей.
- Железо ускоряет окисление жиров, что усиливает прогорклый вкус пищи. В йогурте около 3% его содержимого может составлять жир, что означает большое количество субстрата для окисления в случае, если он находится в прямом контакте с компонентом железа в обогащающем средстве.
Обогащенный йогурт готовили с использованием частиц, полученных как в примере 1 (частицы 0; партия 1 примера 3). Вторую партию йогурта готовили без добавления частиц железа и использовали в качестве контроля. Йогурт готовили следующим способом:
1. Кондиционированием и стандартизацией 25 л молока путем добавления сухого молока при перемешивании до его полного растворения, что в конечном итоге соответствовало 2,5-3% жирности.
2. Добавлением и диспергированием 50 г частиц железа при непрерывном перемешивании (за исключением контрольного йогурта).
3. Пастеризацией в течение 90 секунд при 95°C.
4. Гомогенизацией при 180 кг/см2.
5. Внесением фермента при 45°C.
6. Ферментацией при 44°C в течение 4 часов до тех пор, пока pH йогурта не достигнет значения 4,7-4,8.
7. Консервированием йогуртов при 4,5°C на срок вплоть до 1,5 месяцев.
Одной из целей производства обогащенного йогурта было оценить отсутствие металлического привкуса и визуально сравнить обогащенный продукт с контрольным йогуртом. Была проведена дегустация йогурта группой из пяти неподготовленных мужчин, ни один из которых не был в состоянии обнаружить даже небольшой металлический привкус в обогащенном йогурте, хотя анализ йогуртов выявил в них содержание 42,5±4,1 ppm железа. Также проводили визуальное сравнение обогащенного и контрольного йогуртов, и можно было обнаружить лишь немного более темный цвет обогащенного йогурта. Небольшое окрашивание могло происходить из-за использования очень темной соли железа, и его можно было заметить, только если помещать йогурты рядом.
Пример 11
Стабильность частиц в йогурте
Йогурты, произведенные с продуктом источника железа в форме частиц по настоящему изобретению, и контрольные йогурты (без добавления частиц железа) проверяли на окисление липидов, делая условия хранения более жесткими, чем обычно. Йогурты анализировали в срок, составляющий 150% от их срока годности, на полмесяца позже, чем их установленный срок хранения в один месяц. После этого продолжительного хранения уровень прогорклости оценивали методом газовой хроматографии. Гексанал является обычно используемым маркером прогорклости, так как он представляет собой один из продуктов окисления липидов. Способность человека к обнаружению следов гексанала достаточно высока, он способен ощущать прогорклость, если уровень гексанала выше примерно на 10 ppm (частей на миллион, мг/кг носителей). Чтобы достичь цели, заключающейся в том, чтобы прогорклость не ощущалась или уровни гексанала были значительно ниже порога обнаружения человеком, для анализа йогуртов использовали GC/MS (газовую хроматографию/масс-спектрометрию). Этот метод способен количественно определять следы гексанала вплоть до 50 ppb (частей на миллиард, нг/кг), почти на три порядка ниже порога обнаружения у людей.
Йогурты готовили как в примере 10. Затем в поисках следов гексанала проводили анализ йогуртов методом GC/MS.
Оба проанализированных образца имели уровни гексанала ниже 50 ppb, значительно ниже порога прогорклости, который близок к 10 ppm (частей на миллион, нг/г). Таким образом, частицы являются хорошим способом изолировать жир в йогурте от растворимого источника железа и избежать его окисления.
Пример 12
Обогащенный мясной продукт и стабильность
Возможное включение микрочастиц в пищевой носитель тестировали, используя сосиски из мяса индейки и мясную эмульсию, такую как франкфуртская сосиска. Наличие железа в этих образцах может привести к окислению жиров, если железо высвобождается из микрочастиц.
Для приготовления обогащенных железом франкфуртских сосисок использовали следующий список ингредиентов и относительные количества: филе свинины (40%); бекон (20%); смесь добавок, специй и ароматизаторов (paymfurt ST-1800, Carinsa Group; 3,4%); растительный белок (paymprotein ST-91, Carinsa Group; 3%); соль (1,5%); вода/лед (27,3%); аромат дыма (0,2%) и картофельный крахмал (5%).
Микрочастицы железа (1 г/конечный кг) добавляли вместе с paymfurt ST-1800.
Способ приготовления франкфуртских сосисок был следующим:
1. Порубить все ингредиенты, измельчить мясо до состояния однородной массы. Использовать лед для предотвращения нагрева мяса.
2. Заполнить эмульсией контейнеры (пластиковые пакеты).
3. Варить в бойлере при 75°C в течение 45 минут.
4. Упаковать в вакууме и хранить при 4°C.
Для приготовления обогащенных железом сосисок из мяса индейки использовали следующий список ингредиентов и относительные количества: грудка индейки (69%); вода (24%); смесь добавок и ароматизаторов (Carinsa formula CMA-1251#1; 6%); кукурузный крахмал (1%). Микрочастицы железа (1 г/конечный кг) добавляли вместе с Carinsa formula CMA-1251#1.
Для приготовления сосисок использовали следующий способ:
1. Приготовить рассол, смешивая воду с кукурузным крахмалом и Carinsa formula CMA-1251 #1.
2. Порубить мясо.
3. Смешать в вакууме рубленое мясо с рассолом и вымачивать его в течение 24 ч.
4. Приготовить однородную массу, измельчая часть мяса до образования однородной массы.
5. Заполнить мясом контейнеры (пластиковые пакеты).
6. Варить в бойлере при 75°C до тех пор, пока внутренняя температура не достигнет 72°C.
7. Упаковать в вакууме и хранить при 4°C.
Количество железа в образцах измеряли методом ICP-OES (оптической эмиссионной спектроскопии индуктивно-связанной плазмы) после расщепления образцов в концентрированной HNO3 в микроволновой печи. Результаты количественного определения, выраженные в ppm (частей на миллион, мг/кг), представлены в таблице 11. Значения в скобках соответствуют стандартному отклонению в процентах.
Способность микрочастиц не участвовать в окислении жиров тестировали, подсчитывая количество гексанала, присутствующего в образцах. Гексанал является обычно используемым маркером окисления жиров, так как он представляет собой один из основных продуктов окисления жиров. Его концентрацию определяли в начале и в конце срока хранения сосисок (день 0 и день 60), и проводили сравнение между образцами, обогащенными железом (>100 ppm Fe), и образцами без добавления железа (~10 ppm Fe). Образцы хранили в холодильнике в течение их срока годности и замораживали при -80°C до проведения анализа. Гексанал количественно определяли методом HS-GC-MS (газовой хроматографии в свободном пространстве над продуктом - масс-спектрометрии). Результаты, выраженные в ppm гексанала (мг/кг), представлены в таблице 12. Значения в скобках соответствуют стандартному отклонению в процентах.
Сравнение этих результатов в день 0 показывает, что хотя количество гексанала может казаться более высоким в образцах железа, статистически количество гексанала не может рассматриваться как отличающееся. Следовательно, микрочастицы эффективно предотвращают окисление жира в присутствии железа во время наиболее агрессивных стадий производства сосисок, а именно, их варки. То же самое относится и к результатам на конец срока годности, после хранения образцов в течение 2 месяцев. Разница в результатах между образцами, обогащенными железом, и теми, в которые железо не добавляли, статистически не значима. Более того, если одни и те же образцы сравнивали в начале и в конце срока годности, разница также не была значима. Таким образом, можно сделать вывод, что присутствие железа в форме микрочастиц железа существенно не влияет на скорость окисления жиров в исследуемых образцах мяса.
Пример 13
Устойчивость микрочастиц к гомогенизации
Одной из ключевых стадий в производстве многих продуктов питания, в частности молочных продуктов, является стадия гомогенизации, при которой жидкость или суспензия подвергается высоким напряжениям сдвига. В результате, частицы в суспензии, такие как жировые шарики, разрушаются, делая суспензию более гомогенной. Это напряжение сдвига может также являться причиной разрушения микрочастиц, высвобождения их содержимого (железа) в супернатант и, вследствие этого, делать защиту бесполезной.
Чтобы проверить, в какой степени гомогенизация микрочастиц высвобождает их содержимое в супернатант, готовили 7,9 л суспензии с 10,38 ppm микроинкапсулированного Fe, используя 7,9 л деионизованной воды и 1,025 г микрочастиц. Образец тщательно перемешивали и непрерывно подавали в одноступенчатый гомогенизатор, установленный на величину давления от 20 МПа до 100 МПа. 100 мл образца собирали после доведения давления до желаемого значения и после стабилизации системы. Выбранными значениями давления были: 20 МПа, 35 МПа, 50 МПа и 100 МПа. После гомогенизации каждый образец оставляли на 8 дней без перемешивания в закрытом резервуаре. Непосредственно перед анализом образцы подвергали микрофильтрации (фильтр 0,45 мкм). Концентрированную HNO3 добавляли к каждому микрофильтрованному образцу до конечной концентрации 0,5% (об./об.) для стабилизации железа в суспензии. Железо в подкисленном супернатанте количественно определяли методом ICP-OES.
Количество железа в супернатанте и соответствующее количество железа, высвобожденное из микрочастиц при различных значениях давления гомогенизации, приведены ниже в таблице 13. Образец, обозначенный как гомогенизированный при 0 МПа, не был гомогенизирован, а образец, обозначенный как 20 (контрольная проба), был гомогенизирован при 20 МПа, но содержал только деионизованную воду.
Как видно из предыдущих результатов, стабильность микрочастиц при гомогенизации превосходна. Даже при использовании высоких давлений лишь очень малая часть от общего количества железа высвобождается из микрочастиц.
Пример 14
Получение и стабильность обогащенного молока
Тестировали включение продукта источника железа в форме частиц по настоящему изобретению в молоко как в пищевой носитель. Тестирование частиц путем включения их в молоко было выбрано по следующим причинам:
- Молоко является жидким продуктом питания, что облегчает высвобождение в случае других уже известных продуктов источника железа. Это делает обогащение цельного молока более сложной задачей, в отличие от обезжиренного молока, поскольку наличие железа приводит к окислению жиров, присутствующих в молоке, оставляя прогорклый вкус.
- Будучи жидкостью, молоко не может быть с легкостью обогащено твердыми пищевыми продуктами, поскольку они будут иметь тенденцию к оседанию на дно контейнера.
Цельное коровье молоко, предоставленное местным фермером, хранили в холодильнике (4°C до обработки). 35 г влажных микрочастиц (75% влажности) диспергировали в 600 мл дистиллированной воды. 50 л молока обрабатывали без добавления железа и 50 л молока смешивали с 600 мл суспензии микрочастиц. В оба типа молока добавляли 1 г/л E-339. Сначала для 50 л молока без добавления железа, а затем для 50 л молока с добавлением микрочастиц железа: (a) молоко постепенно нагревали и когда температура достигала 75°C, его гомогенизировали с использованием двухступенчатого гомогенизатора (18 МПа для первой стадии, 4 МПа для второй); (b) когда молоко достигало температуры 90°C, его оставляли при данной температуре на 1 мин; (c) молоко обрабатывали при сверхвысокой температуре (UHT) в течение 15 секунд при 135°C; и (d) молоко охлаждали до комнатной температуры и разливали в нестерильные стеклянные бутылки емкостью 0,5 л.
После разлива по бутылкам оба типа молока тестировали и никакого металлического привкуса не смогли обнаружить. Для предотвращения микробиологической порчи молока его автоклавировали при 121°C в течение 15 мин. После охлаждения молоко хранили при 4°C. В конце срока хранения (1 месяц) количественно определяли наличие гексанала в молоке.
В начале и в конце срока годности визуально проверяли внешний вид молока. Никаких следов осадка не наблюдалось, однако можно было заметить немного более темный цвет обогащенного молока. После производства молока проверяли его вкус и запах. Ни в одном из типов молока не ощущалось никакого металлического или прогорклого запаха или вкуса. Фактически никакой разницы во вкусе или запахе не было найдено между обогащенным железом и необогащенным молоком. Отсутствие прогорклого запаха или вкуса полностью согласуется с определенной концентрацией гексанала в обоих типах молока в конце срока годности: гексанал нельзя было обнаружить в образцах, следовательно, если он и присутствовал, то в концентрации ниже 10 мкг/л.
Пример 15
Производство микрочастиц с использованием ацетата кальция
Высокая концентрация кальция, используемая для получения микрочастиц, может приводить к коррозии, если используемой солью является хлорид кальция. Причина в том, что анионы хлорида очень агрессивны в отношении стали, материала, обычно используемого в промышленных емкостях, трубах и мешалках. Для того чтобы избежать этих проблем и пользуясь тем, что анионы хлорида не играют никакой роли в процессе производства микрочастиц, партия микрочастиц была получена с использованием другой соли кальция, в частности ацетата кальция.
В отличие от хлорида кальция, который превосходно растворим в воде, ацетат кальция менее растворим, так что начальная концентрация кальция в 5М не может быть достигнута. Вместо этого использовали более низкую концентрацию (1,8М).
Способ, используемый для получения микрочастиц, практически не отличался от того, который использовали для получения частиц с хлоридом кальция:
В растворе 1,5 г альгината натрия в 100 мл воды растворяли 16 г сахарата железа (примерно 35% Fe). Используя экстракционную воронку, смесь альгината натрия/сахарата железа добавляли по каплям в 70 мл 1,8M раствора Ca(AcO)2. В процессе добавления по каплям суспензию образовавшихся частиц перемешивали при помощи лабораторного гомогенизатора (Diax 900, Heidolph Instruments GmbH). Полученные твердые частицы отделяли фильтрацией в вакууме. Частицы суспендировали три раза в дистиллированной воде для удаления любой растворимой соли и фильтровали в вакууме. Получали 35,6 г влажных частиц.
Содержание Fe и Ca измеряли способом из примера 3. Стабильность частиц определяли, измеряя высвобождение Fe и Ca в день 0 способом из примера 6. % влажности и % сухого остатка измеряли следующим способом:
1. Взвесить стеклянный химический стакан (веспустой).
2. Отвесить примерно 1 г микрочастиц в стакан. Снова взвесить стакан (весвлажный).
3. Поместить стакан в сушильный шкаф при 110-120°C на два часа.
4. Оставить стакан с сухими микрочастицами охлаждаться до комнатной температуры в течение 30 мин.
5. Снова взвесить стакан с микрочастицами (вессухой).
6. Повторить цикл сушки/охлаждения/взвешивания до тех пор, пока вес не останется постоянным.
7. Рассчитать содержание влаги как:

Полученные результаты
- содержание Fe: 15,0% Fe (масс./масс.) во влажных микрочастицах, 45,4% Fe (масс./масс.) в сухих микрочастицах
- содержание Ca: 0,6% Ca (масс./масс.) во влажных микрочастицах, 1,9% Ca (масс./масс.) в сухих микрочастицах
- влажность: 66,9% влажности (33,1% сухого остатка)
- высвобождение Fe и Ca: 0,2% высвобожденного Fe и 8,2% высвобожденного Ca.
Пример 16
Термостойкость
Далее пригодность микрочастиц для продуктов питания тестировали, проверяя, влияет ли высокая температура, используемая при приготовлении или стерилизации пищи, на их способность удерживать полезную нагрузку (железо) внутри микрочастиц.
По 1 г микрочастиц отвешивали в каждый из двух взвешенных стеклянных химических стаканов. В сушильном шкафу при температуре 125°C один из образцов держали в течение 30 мин, а другой оставался в сушильном шкафу в течение 180 мин. Затем частицы охлаждали до комнатной температуры и каждый стакан снова взвешивали. 40 мг сухих микрочастиц суспендировали в 100 мл деионизованной воды и суспензию перемешивали вручную. 1 мл каждой суспензии разводили до 10 мл, добавляя 9 мл деионизованной воды. Образцы фильтровали для удаления твердых частиц из суспензии. Затем добавляли 50 мкл концентрированной азотной кислоты в каждый образец для стабилизации железа в суспензии, и образцы подвергали ICP-OES для количественного определения высвобожденного железа и кальция.
Суспензия микрочастиц непосредственно перед фильтрацией имела общую концентрацию 11 ppm Fe. Супернатант после фильтрации содержал только железо, высвобожденное из микрочастиц, которое количественно определяли методом ICP-OES, получив следующие результаты:
30 мин, 125°C: 0,04 ppm Fe
180 мин, 125°C: 0,03 ppm Fe.
В обоих случаях менее 1% железа, присутствующего в микрочастицах, высвобождалось из них в результате нагревания микрочастиц. Вследствие этого, микрочастицы можно считать стабильными даже после обработок, гораздо более агрессивных, чем те, которым обычно подвергают продукты питания (3 ч при 125°C).
Реферат
Изобретение относится к обогащенному железом продукту питания, содержащему продукт источника железа в форме твердых частиц, где частицы включают ядро, содержащее альгинат железа, и внешний слой, содержащий альгинат кальция, где частицы получены способом, включающим следующие стадии: (i) образование ядра, содержащего альгинат железа, путем контактирования биодоступной водорастворимой соли железа и одной водорастворимой альгинатной соли, (ii) контактирование ядра с водным раствором соли кальция, в концентрации, составляющей от 0,025 М до концентрации ниже точки насыщения раствора, и (iii) выделение полученного твердого продукта. Твердые частицы пригодны для обогащения железом продуктов питания и характеризуются улучшенной нагрузочной способностью, а также обладают хорошей стабильностью при стандартных условиях хранения и использования. Обогащенный железом продукт питания применяется для профилактики или лечения железодефицитных состояний у человека. 4 н. и 7 з.п. ф-лы, 9 ил., 13 табл., 16 пр.
Формула
(i) образование ядра, содержащего альгинат железа, путем контактирования, по меньшей мере, одной биодоступной водорастворимой соли железа и, по меньшей мере, одной водорастворимой альгинатной соли,
(ii) контактирование ядра с водным раствором соли кальция в концентрации, составляющей от 0,025 М до концентрации ниже точки насыщения раствора, и
(iii) выделение полученного твердого продукта.
(i) ядро формируют путем растворения или суспендирования, по меньшей мере, одной биодоступной соли железа в водном растворе, по меньшей мере, одной альгинатной соли для получения геля,
(ii) полученный гель медленно добавляют к водному раствору соли кальция в концентрации, составляющей от 0,025 М до концентрации ниже точки насыщения раствора, при интенсивном перемешивании,
(iii) полученные твердые частицы фильтруют и промывают водой.

Комментарии