Использование алкоксилированных неионогенных поверхностно-активных веществ в качестве добавки в водных составах для чистки мембран - RU2636661C2
Код документа: RU2636661C2
Чертежи








Описание
Целью настоящего изобретения является использование разветвленных алкоксилированных неионогенных поверхностно-активных веществ (ПАВ) в качестве добавки к водному составу для чистки мембран, в котором поверхностно-активное вещество имеет значение гидрофильно-липофильного баланса HLBd от 9 до 12,5 и среднюю степень разветвленности Bs≥1,5.
Во многих промышленных применениях, связанных с очисткой воды, например, таких как очистка сточных вод или опреснение морской воды, используются мембраны для отделения воды от соли и/или других примесей. Широко применяемые мембранные процессы включают в себя микрофильтрацию, ультрафильтрацию, нанофильтрацию, обратный осмос, электролиз и диализ. Микрофильтрация и ультрафильтрация широко используются в технологических процессах при производстве продуктов питания и напитков (микрофильтрация пива, концентрация сыворотки), в биотехнологии и фармацевтической промышленности (производство антибиотиков, очистка белков), при очистке воды и очистке сточных вод, в микроэлектронике и других отраслях промышленности. Нанофильтрация и мембраны обратного осмоса используются в основном для целей очистки воды (т.е. опреснения воды). Производительность мембраны определяется размером пор и материалом поверхности мембраны. Типичными материалами мембраны являются полисульфон, полиэфирсульфон, полиамид, полиакрилонитрил, поливинилидендифторид и полиимид. Механизм разделения во время процесса очистки задуман как процесс фильтрации, в котором увеличение приложенного давления увеличивает скорость потока. Тем не менее, мембраны могут быть загрязнены вследствие адсорбции или осаждения некоторых веществ, присутствующих в процессе разделения, что приводит к закупориванию пор мембран солью и/или другими примесями. Такое засорение вызывает снижение производительности мембраны в процессе разделения. Загрязнение в основном происходит из трех источников, а именно частиц питательной воды, накопления слабо растворимых минералов и роста микроорганизмов. Все эти условия требуют частой очистки. Процессы очистки, используемые до сих пор, состоят в применении чистящего раствора поверхностно-активных веществ с очень кислым, нейтральным или очень щелочным рН (интенсивная очистка) и/или в приложении обратного давления на мембрану (усиленная химическая промывка обратным потоком). В чистящих растворах в основном используются анионные поверхностно-активные вещества (LAS), поскольку до сих пор не известны эффективные неионогенные поверхностно-активные вещества, которые бы не закупоривали мембраны. Концентрация поверхностно-активного вещества в используемых чистящих растворах, если применяются, находится в пределах от 100 частей на миллион до 1000 частей на миллион, и ограничена из-за вспенивания анионного ПАВ. Неионогенные поверхностно-активные вещества, как правило, имеют тенденцию к проявлению сродства к мембранам или демонстрируют плохую эффективность очистки мембраны. Они с трудом смываются впоследствии и, как правило, сами закупоривают поры мембраны (Руководство для пользователя - Owners manual ECH2O Tec. Watermakers, 1000-BHL-2, page 9; DOW Filmtec, Form No. 609-01010-498QRP; Hydranautics Technical Application Bulletin No 109, February 22nd, 2002, Revision B, page 3; K. Yamagiwa, H. Kobayashi, A. Ohkawa, M. Onodura, J. Chem. Eng Jp 26, Nol, 13, 1993). Ионные поверхностно-активные вещества, таким образом, используются чаще, но имеют тот недостаток, что они образуют пену во время процесса очистки мембраны.
Патент WO 03/022752 включает в себя смеси, содержащие ферменты и поверхностно-активные вещества, используемые в способе для снижения биопленки в водной системе, причем указанная система является системой фильтрации с поперечным потоком или системой обратного осмоса. Используемые поверхностно-активные вещества могут быть неионогенными, анионными, амфотерными, катионными или их комбинацией.
Патент ЕР 2164939 В1 относится к жидкому моющему составу, содержащему этоксилат спирта Гербе согласно формулы R1-(OC2H4)N-OH, где R1представляет собой С9-С20 алкильную группу и n составляет от 2 до 10. Жидкий моющий состав для стирки текстильных изделий содержит компоненты, которые не влияют на процесс фильтрации в мембранной фильтровальной установке, используемой для очистки сточных вод процесса стирки текстильных изделий.
Патент WO 2005/118760 А1 описывает пастообразный чистящий или моющий состав для стирки текстильных изделий, подходящий для использования при очистке сточных вод процесса стирки, и содержащий алкоксилаты жирных спиртов. Указанные алкоксилаты жирных спиртов имеют общую формулу R-(ЕО)х-(РО)у, в которой R может быть разветвленной С8-С22 алкильной цепью и сумма x и y составляет по меньшей мере 5.
Патент US 2009/0200234 описывает способ удаления загрязнения с мембраны с применением кислотного раствора с активным кислородом, а затем корректирующего щелочного раствора. Кислый раствор с активным кислородом содержит пероксидное соединение и поверхностно-активное вещество, которое может быть неионогенным, анионным, катионным, амфотерным, цвиттерионным или их смесью.
Патент DE 19726287 А1 описывает состав средства, используемого в способе очистки тканей в промышленном масштабе, в котором состав средства содержит линейные и/или разветвленные этоксилированные и/или пропоксилированные C8-C18 жирные спирты. Накопленные в ходе процесса сточные воды обрабатывают с помощью мембранной фильтровальной установки.
Патент WO 02/46351 А1 включает в себя моющее или чистящее средство, содержащее этоксилированный разветвленный или неразветвленный С10-С20жирный спирт, в котором средняя степень этоксилирования имеет значение от 5 до 20. Накопленные в ходе процесса сточные воды обрабатывают с помощью мембранной фильтровальной установки.
Патент DE 4445070 А1 описывает способ удаления биопленки или предотвращения образования шлама на поверхностях водоносной системы посредством добавления в систему фермента и гликолевого компонента.
Гликолевый компонент имеет следующую формулу: R2(O-R1)n-OR3, где n представляет собой целое число меньше 10, R1 представляет собой алкильный остаток с 2 или 3 атомами углерода, и R2 и R3 в каждом случае независимо друг от друга представляют собой водород, алкильную группу, содержащую от 1 до 6 атомов углерода, или арильную группу.
Таким образом, целью настоящего изобретения является поиск неионогенных поверхностно-активных веществ, которые не будут осаждаться на мембранах и закупоривать поры, при этом отличаясь низким пенообразованием, и демонстрируют хорошую и быструю эффективность очистки в водных растворах, используемых для очистки мембран.
Неожиданно было обнаружено, что алкоксилированные неионогенные поверхностно-активные вещества, представленные в формуле (I), и имеющие значение HLBd от 9 до 12,5, и среднюю степень разветвленности ≥1,5, предпочтительно≥2, при использовании в качестве добавки к водным составам для чистки мембран, обеспечивают превосходные результаты с точки зрения эффективности очистки, и скорость очистки мембраны, и в то же время имеют пониженное сродство с поверхностью мембраны и низкий профиль ценообразования.
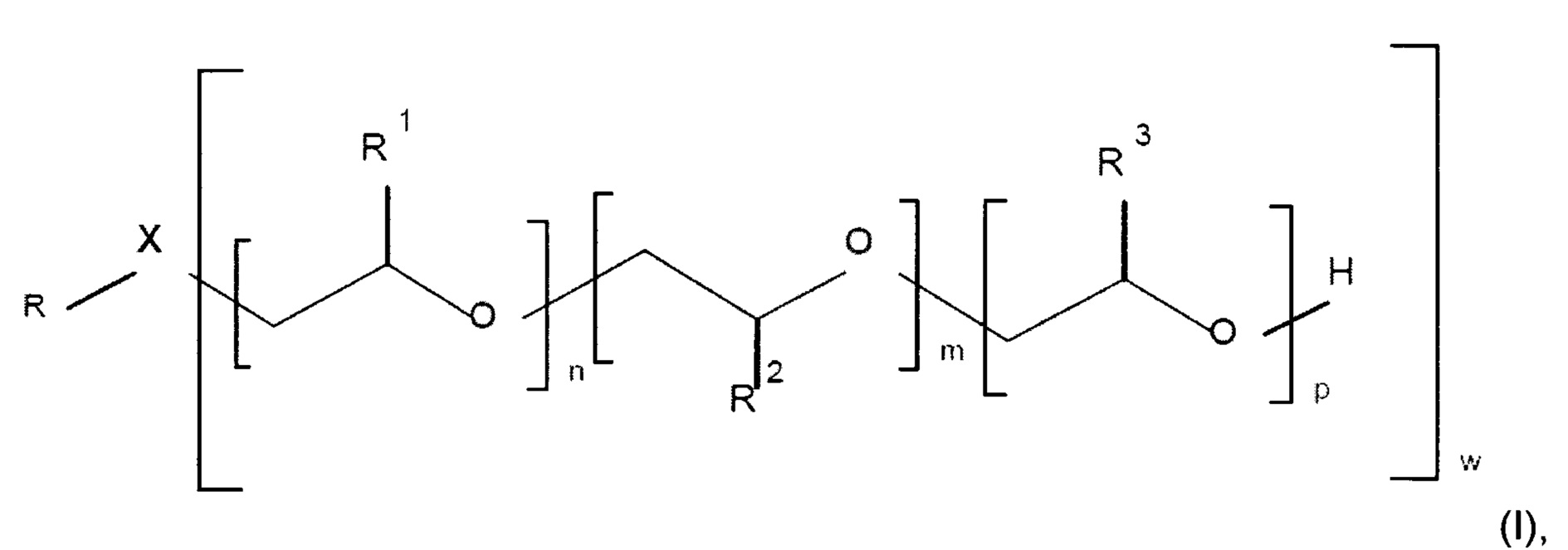
Указанные неионогенные поверхностно-активные вещества имеют следующую формулу (I):

R представляет собой линейную или разветвленную C8-C18углеводородную цепь,
X представляет собой О или N,
R1, R2 и R3 независимо друг от друга представляют собой водород, метил, этил, пропил, изопропил или их смесь, и предпочтительно n имеет значение от 1 до 8, наиболее предпочтительно n имеет значение от 1 до 6.
Предпочтительно m имеет значение от 1 до 8, наиболее предпочтительно m имеет значение от 2 до 6.
Предпочтительно р имеет значение от 0 до 8, наиболее предпочтительно р имеет значение от 1 до 6.
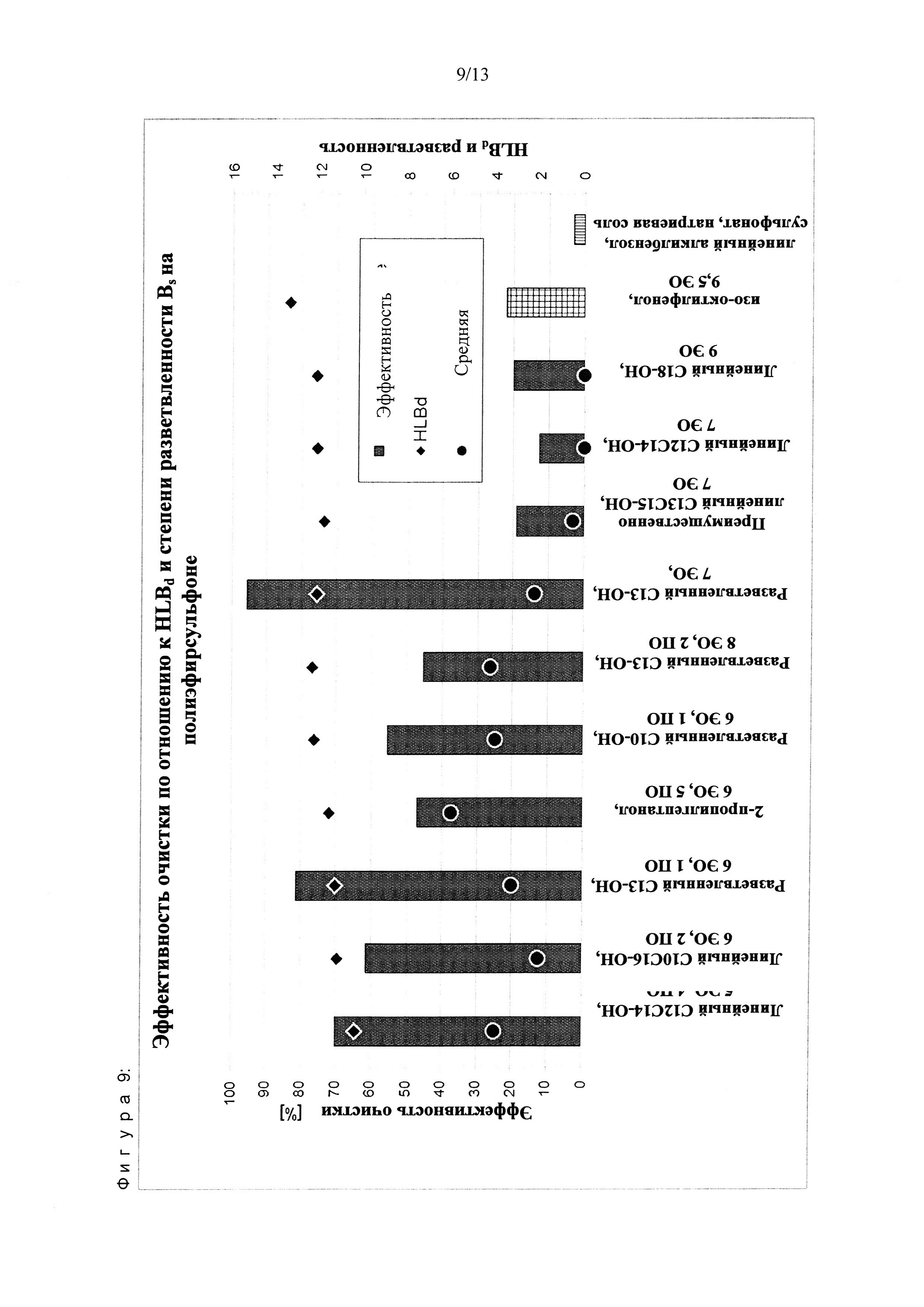
Предпочтительно поверхностно-активные вещества, используемые в соответствии с изобретением, имеют расчетную величину HLBd от 9 до 12,5 и среднюю степень разветвленности Bs≥1,5, предпочтательно Bs≥2.
Средняя степень разветвленности
Степень разветвленности жирных спиртов определяется как число атомов углерода в алифатическом углеводороде (3° атома углерода), которые связаны с тремя дополнительными атомами углерода, плюс два раза число атомов углерода (4° атома углерода), которые связаны с четырьмя дополнительными атомами углерода. Средняя степень разветвленности Bh вычисляется как сумма всех степеней разветвленности отдельных алифатических углеводородных молекул, разделенная на общее число отдельных алифатических углеводородных молекул.
Bh=n*С(3°)+2*m*С(4°)
Степень разветвленности в алкиленокси цепи определяется как число атомов углерода (3° атома углерода), которые связаны с тремя дополнительными атомами, отличными от водорода, плюс два раза число атомов углерода (4° атома углерода), которые связаны с четырьмя дополнительными атомами, отличными от водорода. Средняя степень разветвленности Ва вычисляется как сумма всех степеней разветвленности отдельных алкиленокси молекул, разделенная на общее число отдельных алкиленокси молекул.
Ва=р*С(3°)+2*q*C(4°)
В качестве еще одного определения, фрагмент третичного амина (NR3) имеет степень разветвленности 1 (BN=1).
Средняя степень разветвленности поверхностно-активных веществ Bsпредставляет собой сумму средней степени разветвленности углеводородной части Bh и разветвленности, полученной от количества алкиленокси групп Ва и, если присутствует, разветвленности фрагмента третичного амина BN:
Bs=Bh+Ва+BN
Степень разветвленности может быть определена, например, посредством использования методов ядерно-магнитного резонанса ЯМР С13, таких как COSY, DEPT, INADEQUATE, с последующим количественным анализом с использованием релаксационных реагентов. Также могут быть использованы другие методы ЯМР и методы газовой хроматографии-масс-спектрометрии (ГХМС).
Поверхностно-активные вещества, используемые в настоящем изобретении, имеет среднюю степень разветвленности Bs≥1,5, предпочтительно Bs≥2.
Предпочтительно неионогенные поверхностно-активные вещества, используемые в соответствии с настоящим изобретением, являются этоксилированными и/или пропоксилированными.
В одном варианте осуществления настоящего изобретения, в соответствии с формулой (I), R представляет собой метил, R представляет собой водород, R3представляет собой водород или метил.
В другом варианте осуществления настоящего изобретения, в
соответствии с формулой (I), R1 представляет собой водород, R2 представляет собой метил, R3 представляет собой водород или метил.
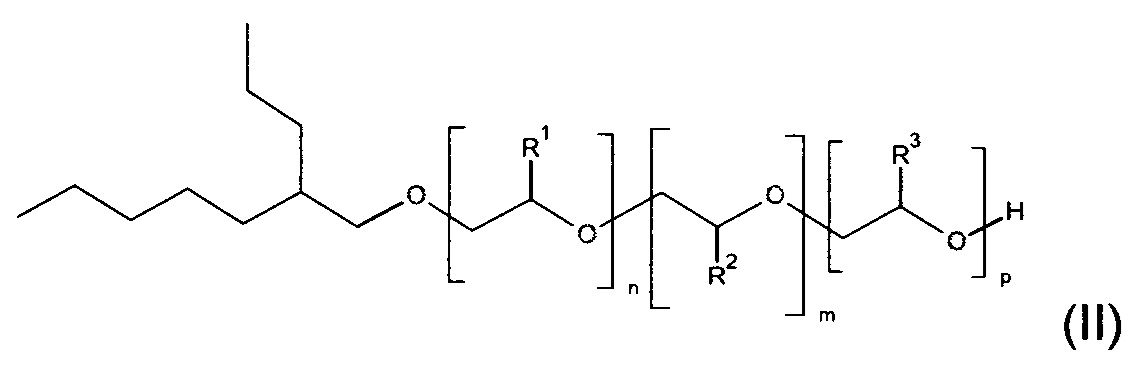
Предпочтительные алкоксилированные поверхностно-активные вещества, используемые в составе для чистки мембран, имеют Формулу (II) и включают в себя 2-пропилгептил смешанные этоксилированные и пропоксилированные жирные спирты, в которых в соответствии с формулой (I), R обозначает 2-пропилгептил и X представляет собой О

Предпочтительно n имеет значение от 1 до 6.
Предпочтительно m имеет значение от 1 до 6.
Предпочтительно р имеет значение от 0 до 6, наиболее предпочтительно р имеет значение от 1 до 6.
Кроме того, предпочтительные алкоксилированные поверхностно-активные вещества, используемые в составе для чистки мембран, включают в себя разветвленные алкоксилаты жирных спиртов, в которых поверхностно-активное вещество имеет следующую формулу:
Формула (III),
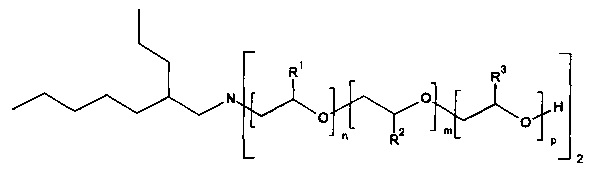
в которой в соответствии с формулой (I), R обозначает 2-пропилгептил и X представляет собой N.
Предпочтительно n имеет значение от 1 до 6.
Предпочтительно m имеет значение от 1 до 6.
Предпочтительно р имеет значение от 0 до 6, наиболее предпочтительно р имеет значение от 1 до 6.
Другие предпочтительные алкоксилированные поверхностно-активные вещества, используемые в составе для чистки мембран, включают в себя разветвленные алкоксилаты жирных спиртов в соответствии с формулой (I), в которой
- R представляет собой разветвленную алкильную цепь, содержащую 13 атомов углерода,
- X представляет собой О.
Как известно в данной области техники, расчетная величина HLB поверхностно-активного вещества является измерением степени, в которой это вещество является гидрофильным или липофильным, как определено с помощью уравнения Гриффина (W.C. Griffin, J. Soc. Cosmet. Chem. 1, 311 (1950); 5, 249 (1954) - see also H. Mollet et al. "Formulation Technology", 1st ed. Wiley-VCH Verlags GmbH, Weinheim 2001, pages 70-73).
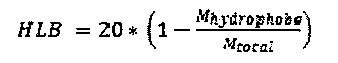
где Mhydrophobe является средней молекулярной массой гидрофобной части и Mtotal является общей средней молекулярной массой молекулы поверхностно-активного вещества. Таким образом, расчетное значение HLB, по существу, является заменой для соотношения гидрофильных этиленоксидных групп и гидрофобной алкильной и/или арильной группы в поверхностно-активном веществе. Уравнение Гриффина первоначально является действительным только для этоксилатов, а не для алкоксилатов. Поскольку пропиленокси группы в неионогенном поверхностно-активном веществе не являются ни чисто гидрофобными, ни чисто гидрофильными, мы определили значение HLBd алкоксилатов как таковое:
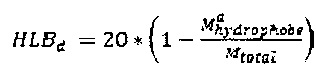
где

Поверхностно-активное вещество, используемое в настоящем изобретении, имеет расчетное значение HLBd в диапазоне от 9 до 12,5.
Алкоксилаты спиртов были синтезированы, как описано в патенте ЕР 1675811, алкоксилаты с узким диапазоном в соответствии с описанием в патенте US 2005/0215452 А1, алкоксилаты аминов в соответствии с описанием в патенте US 2011/0177945 А1.
Тридецилэтоксилаты были изготовлены в соответствии с патентом ЕР 1675811. Тридецилспирт (изотридеканол N от компании BASF SE, полученный в результате оксосинтеза додецена, который получают в результате тримеризации бутена) этоксилируют в щелочных условиях (КОН) в соответствующие этоксилаты. Эти тридецилэтоксилаты имеют отличные экологические характеристики (см. Kaluza, U. and К. Taeger. 1996. Einfluss der chemischen Struktur auf okotoxikologische Eigenschaften von Alkanol-Ethoxylaten (Влияние химической структуры на экотоксикологические свойства алканолэтоксилатов). Tenside Surfactants Detergents, 33, 46-51).
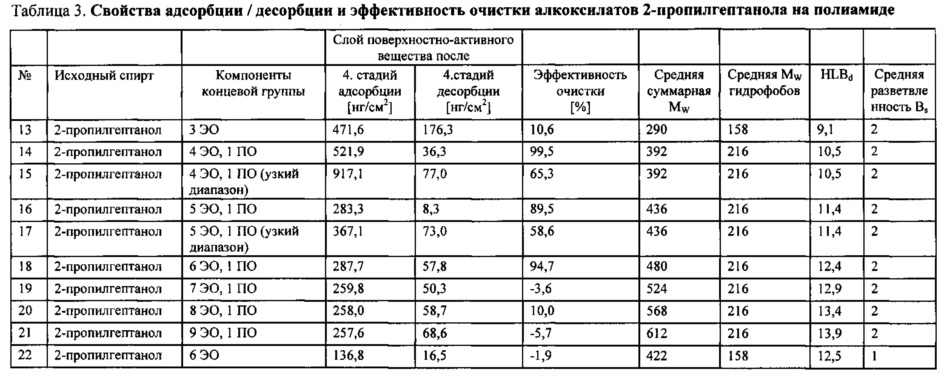
2-пропилгептанолэтоксилаты были изготовлены соответственно, при этом используемый технический сорт 2-пропилгептанола состоит из от 70 до 99 вес. % 2-пропилгептанола и от 1 до 30 вес. % 2-пропил-4-метилгексанола и/или 2-пропил-5-метилгексанола. Поверхностно-активное вещество на основе 2-пропилгептиламина было получено из описаного выше 2-пропилгептанола.
Предпочтительные алкоксилированные поверхностно-активные вещества, используемые в составах для чистки мембран, включают в себя 2-пропилгептил смешанные этоксилированные и пропоксилированные жирные спирты, в которых число заместителей этиленоксида имеет среднюю величину 6, а число заместителей пропиленоксида имеет среднюю величину, равную 1 или 5.
В другом варианте осуществления настоящего изобретения, разветвленное неионогенное поверхностно-активное вещество, используемое в качестве добавки в составах для чистки мембран, имеет величину HLBd от 10 до 12,5 и является этоксилированным разветвленным тридеканолом, содержащим от 5 до 7 этиленоксидных групп.
В предпочтительном варианте осуществления, концентрация поверхностно-активных веществ согласно изобретению в используемом составе для чистки мембран составляет 100 частей на миллион до 10 вес. %, предпочтительно 1000 частей на миллион до 5 вес. %.
Водные составы для чистки мембран могут содержать дополнительные соединения, такие как ионные поверхностно-активные вещества, выбранные из группы, состоящей из анионных, катионных, амфотерных, цвиттерионных поверхностно-активных веществ и/или их смесей, присутствующих в составе в концентрации от 0 вес. % до 20 вес. %, предпочтительно от 3 вес. % до 15 вес. %, еще более предпочтительно от 5 вес. % до 12 вес %.
Другими соединениями, которые могут присутствовать в составе для чистки мембран, являются дезинфицирующие средства, кислоты, основания, структурообразователи, хелатирующие агенты, ферменты, ферментные стабилизаторы, биоциды, гидротропы, загустители, окислительные агенты, восстанавливающие агенты.
Ионные поверхностно-активные вещества
Примерами анионных поверхностно-активных веществ являются: карбоксилаты, сульфонаты, сложные метиловые эфиры жирных сульфокислот, сульфаты, фосфаты. Примерами катионных поверхностно-активных веществ являются: четвертичные аммониевые соединения. Примерами цвиттерионных поверхностно-активных веществ являются: бетаины или аминоксиды.
"Карбоксилат" представляет собой соединение, которое содержит, по меньшей мере, одну карбоксилатную группу в молекуле. Примерами карбоксилатов, которые могут быть использованы в соответствии с настоящим изобретением, являются мыла, такие как стеараты, олеаты, кокоаты щелочных металлов или аммония и эфиркарбоксилаты.
"Сульфонат" представляет собой соединение, которое содержит, по меньшей мере, одну сульфонатную группу в молекуле. Примерами сульфонатов, которые могут быть использованы в соответствии с настоящим изобретением, являются алкилбензолсульфонаты, алкилсульфонаты, сульфированные масла, олефинсульфонаты, ароматические сульфонаты.
"Сложный метиловый эфир жирных сульфокислот" представляет собой соединение, имеющее следующую общую формулу (I):

в которой R имеет от 6 до 20 атомов углерода; предпочтительно от 10 до 18 и особенно предпочтительно от 14 до 16 атомов углерода.
"Сульфат" представляет собой соединение, которое содержит, по меньшей мере, одну SO4-группу в молекуле. Примерами сульфатов, которые могут быть использованы в соответствии с настоящим изобретением, являются сульфаты спиртов жирных кислот, такие как сульфат жирного спирта кокосового масла (CAS 97375-27-4), сульфаты других спиртов, сульфаты простых эфиров жирных спиртов кокосового масла, сульфаты простых эфиров других спиртов.
"Фосфат" представляет собой соединение, которое содержит, по меньшей мере, одну PO4-группу. Примерами фосфатов, которые могут быть использованы в соответствии с настоящим изобретением, являются фосфаты простых алкиловых эфиров, фосфаты, моно- и диалкиловые фосфаты.
При получении химического состава по настоящему изобретению анионные поверхностно-активные вещества предпочтительно добавляют в виде солей. Приемлемыми солями являются, например, соли щелочных металлов, такие как натриевые, калиевые и литиевые соли, и аммониевые соли, такие как моно(гидроксиэтил)аммониевые, ди(гидроксиэтил)аммониевые и три(гидроксиэтил)аммониевые соли.
Одной группой катионных поверхностно-активных веществ являются четвертичные аммониевые соединения.
"Четвертичные аммониевые соединения" представляет собой соединение, которое содержит, по меньшей мере, одну R4N+-группу в каждой молекуле. Примерами противоионов, которые могут быть использованы в четвертичных аммониевых соединениях, являются галогены, метосульфаты, сульфаты и карбонаты кокосового жира, жира сальных желез или цетил/олеилтриметиламмония.
Особенно подходящими катионными поверхностно-активными веществами являются эстеркваты, особенно моно-, ди- и триалканоламины, этерифицированные С8-С22-карбоновой кислотой, а затем кватернизированные алкилирующими агентами, имидазолиниумкваты, особенно соли 1-алкилимидазолиниума.
Бетаин является поверхностно-активным веществом, которое содержит, по меньшей мере, одно катионное и, по меньшей мере, одно анионное звено в каждой молекуле. Примером бетаинов, которые могут быть использованы в соответствии с изобретением, является кокамидопропилбетаин.
Аминоксид является поверхностно-активным веществом, которое содержит, по меньшей мере, одно N-O звено, примером аминоксида является алкил диметил аминоксид.
Адъюванты
Биоцидами могут быть: окисляющие агенты, галогены, такие как хлор и йод и веществ, которые их высвобождают, спирты, такие как этанол, 1-пропанол и 2-пропанол, альдегиды, такие как формальдегид, глутаровый альдегид, глиоксаль, фенолы, этиленоксид, хлоргексидин и мецетрония метилсульфат.
Преимущество использования биоцидов состоит в том, что рост патогенных микроорганизмов вряд ли возможен. Патогенными микроорганизмами могут быть: бактерии, споры, грибы и вирусы.
Кислоты являются соединениями, которые могут быть преимущественно использованы для растворения или недопущения образования накипи. Неограничивающими примерами кислот являются муравьиная кислота, уксусная кислота, лимонная кислота, соляная кислота, серная кислота и сульфоновые кислоты, как метансульфокислота.
Основы являются соединениями, которые могут быть использованы для регулирования предпочтительного диапазона рН для комплексообразующих агентов. Примерами основ, которые могут быть использованы в соответствии с настоящим изобретением, являются: NaOH, КОН и аминоэтанол.
Восстанавливающие агенты являются соединениями, которые могут быть использованы для удаления остатков окислителей, примером является гидросульфит натрия.
В качестве неорганических структурообразователей особенно полезными являются следующие:
- кристаллические и аморфные алюмосиликаты, имеющие ионообменные свойства, такие как цеолиты: различные типы цеолитов являются полезными, особенно тип А, X, В, Р, MAP и HS в своей Na-модификации или в модификациях, в которых Na частично замещен другими катионами, такими как Li, К, Са, Mg или аммоний;
- кристаллические силикаты, такие как дисиликаты и силикаты слоистой структуры, например, δ- и β-Na2Si2O5. Силикаты могут быть использованы в качестве солей щелочных металлов,солей щелочноземельных металлов или аммониевых солей, предпочтительными являются Na-, Li- и Mg-силикаты;
- аморфные силикаты, такие как метасиликат натрия и аморфный дисиликат;
- карбонаты и гидрокарбонаты: Они могут быть использованы в качестве солей щелочных металлов, солей щелочноземельных металлов или аммониевых солей. Предпочтительными являются Na-, Li- и Mg-карбонаты и - гидрокарбонат, особенно карбонат натрия и/или гидрокарбонат натрия;
- полифосфаты, такие как трифосфат пентанатрия, триполифосфат натрия;
- фосфонаты,
Полезными в качестве олигомерных и полимерных совместных структурообразователей являются:
Олигомерные и полимерные карбоновые кислоты, такие как гомополимеры акриловой кислоты и аспарагиновой кислоты, олигомалеиновая кислота, сополимеры малеиновой кислоты и акриловой кислоты, метакриловая кислота или С2-С22-олефины, например изобутен или длинноцепочечные α-олефины, винил-C1-C8-простой алкиловый эфир, винилацетат, винилпропионат, сложный эфир (мет)акриловой кислоты C1-C8 спиртов и стирола. Предпочтительными являются гомополимеры акриловой кислоты и сополимеры акриловой кислоты с малеиновой кислотой. Олигомерные и полимерные карбоновые кислоты предпочтительно используются в виде кислот или солей натрия.
Хелатирующие агенты представляют собой соединения, которые могут связывать катионы. Они могут быть использованы для снижения жесткости воды и хелатирования тяжелых металлов. Примерами хелатирующих агентов являются: NTA, EDTA, MGDA, DTPA, DTPMP, IDS, HEDP, β-ADA, GLDA, лимонная кислота, оксоянтарная кислота и бутантетракарбоновая кислота. Преимущество в использовании этих соединений состоит в том, что многие соединения, которые служат в качестве чистящих средств, являются более активными в мягкой воде. В дополнение к этому, образование накипи может быть снижено или даже предотвращено.
Полезными ферментами являются, например, протеазы, липазы, амилазы, целлюлазы, маннаназы, оксидазы и пероксидазы, полисахаридазы.
Гидротропы являются соединениями, которые повышают растворимость поверхностно-активного вещества/поверхностно-активных веществ в химическом составе. Примером является кумолсульфонат.
Загустители являются соединениями, которые повышают вязкость химического состава. Неограничивающими примерами загустителей являются: полиакрилаты и гидрофобно-модифицированные полиакрилаты, полиуретаны, ксантановые камеди, бентониты. Преимущество использования загустителей состоит в том, что жидкости, имеющие высокую вязкость, имеют более длительное время пребывания на поверхности, подлежащей обработке, в тех случаях, когда эта поверхность является наклонной или даже вертикальной. Это приводит к увеличению времени взаимодействия.
Мембраны
Типичными материалами мембраны являются полисульфон, полиэфирсульфон, полиамид, полиакрилонитрил, поливинилидендифторид, полиимид.
Мембрана состоит из полимера, выбранного из группы, состоящей из сложного полиэфира, полисульфона, поликарбоната, полипропилена, полиамида (ПА) и полиэфирсульфона (ПЭС).
Полиолефины, такие как полипропилен, могут быть полимерами, образованными из, по меньшей мере, одного олефинового мономера или, по меньшей мере, одного олефинового мономера и малеинового мономера. Примерами полиолефинов являются полиэтилен низкой плотности (ПЭНП), полиэтилен высокой плотности (ПЭВП), полипропилен (ГШ), биаксиально ориентированный полипропилен (БОПП), полибутадиен, политетрафторэтилен (тефлон - ПТФЭ), хлорированный полиэтилен и сополимер изопропилена-малеинового ангидрида.
Полиамиды могут быть полимерами, образованными из, по меньшей мере, одного мономера, имеющего амидную группу или аминогруппу, а также карбокси-группу или, по меньшей мере, одного мономера, имеющего две аминогруппы и, по меньшей мере, одного мономера, имеющего две карбоксильные группы. Примером мономера, имеющего амидную группу, является капролактам. Примером диамина является 1,6-диаминогексан. Примерами дикарбоновых кислот являются адипиновая кислота, терефталевая кислота, изофталевая кислота и 1,4-нафталиндикарбоновая кислота. Примерами полиамидов являются полигексаметиленадипамид и поликапрол актам.
Сложные полиэфиры могут быть полимерами, образованными из, по меньшей мере, одного мономера, имеющего гидроксигруппу, а также карбоксигруппу или, по меньшей мере, одного мономера, имеющего две гидроксигруппы и, по меньшей мере, одного мономера, имеющего две карбоксигруппы или лактоновую группу. Примером мономера, имеющего гидроксильную, а также карбоксильную группы, является адипиновая кислота. Примером диола является этиленгликоль. Примером мономера, имеющего лактоновую группу, является капролактон.
Примерами дикарбоновых кислот являются терефталевая кислота, изофталевая кислота и 1,4-нафталиндикарбоновая кислота. Примером сложного полиэфира является полиэтилентерефталат (ПЭТ). Так называемые алкидные смолы также рассматриваются как принадлежащие к полиэфирным полимерам.
Примерами поликарбонатов являются полихроматические карбонаты) и поли(алифатические карбонаты).
Поли(алифатические карбонаты) могут быть образованы из диоксида углерода и, по меньшей мере, одного эпоксида.
Примерами полимеров на основе сульфона являются полиарилсульфон, полиэфирсульфон (ПЭС), полифенилсульфон (ПФС) и полисульфон (ПС). Полисульфон (ПС) представляет собой полимер, образованный из 4,4-дихлордифенил сульфона и бисфенола А.
Еще одной целью настоящего изобретения является создание способа для удаления загрязнения с мембраны. Типичный способ очистки мембраны состоит из следующих стадий: (Hydranautics Technical Service Bulletin October 2011 TSB 107.21)
Предварительная промывка водой
Циркуляция с чистящим раствором
Вымачивание
Нагнетание насосом с большим расходом
Промывка
Способ согласно изобретению включает в себя стадии:
i) предварительной промывки мембраны водой,
ii) циркуляция на мембране водного состава для чистки мембраны, содержащего неионогенное поверхностно-активное вещество, в котором ПАВ имеет величину HLBd от 9 до 12,5 и среднюю степень разветвленности Bs≥1,5 и, в котором ПАВ имеет следующую формулу:

где - R представляет собой линейную или разветвленную C8-C18 углеводородную цепь,
- X представляет собой О или N,
- R1, R2 и R3 независимо друг от друга представляют собой водород, метил, этил, пропил, изопропил или их смесь,
- n имеет значение от 1 до 8,
- m имеет значение от 1 до 8,
- p имеет значение от 0 до 8.
iii) вымачивание мембраны составом для чистки мембран,
iv) необязательно нагнетание насосом с большим расходом,
v) промывка составом для чистки мембраны.
Весь способ может быть повторен с различными чистящими растворами, в зависимости от засорения отложениями, предпочтительно дважды и до пяти раз. Каждая чистка занимает до 12 часов, в зависимости от количества и типа засорения отложениями.
Примеры:
Подготовка полиамидной тонкослойной пленки (ПА-слой)
Свежеочищенные плоские носители на основе оксида кремния (кремниевые пластины 15×20 мм, GESIM, Германия или QCM-D кристаллы с SiO2-покрытием, Q-Sense, Швеция) или предметные стекла (24×24 мм, Menzel-Glaser, Braunschweig, Германия) были окислены в смеси водного раствора аммиака (Acros Organics, Geel, Бельгия) и перекиси водорода (Merck, Darmstadt, Германия), прежде чем они были подвергнуты гидрофобизации с гексаметилдисилазаном (ABCR, Karlsruhe, Германия). Впоследствии тонкослойные пленки из полиамида иммобилизовали с нанесением покрытия методом центрифугирования из растворов РА-12

Подготовка полиэфирсульфоновой тонкослойной пленки (ПЭС-слой)
Свежеочищенные плоские носители на основе оксида кремния (кремниевые пластины 15×20 мм, GESIM, Германия или QCM-D кристаллы с SiO2-покрытием, Q-Sense, Швеция) или предметные стекла (24×24 мм, Menzel-Glaser, Braunschweig, Германия) были окислены в смеси водного раствора аммиака (Acros Organics, Geel, Бельгия) и перекиси водорода (Merck, Darmstadt, Германия), прежде чем они были подвергнуты гидрофобизации с гексаметилдисилазаном (ABCR, Karlsruhe, Германия). Впоследствии тонкослойные пленки из полиэфирсульфона иммобилизовали с нанесением покрытия методом центрифугирования из растворов ПЭС (Ultrason PES Type E 6020 P, BASF SE, Германия). Растворы 0,3% Ultrason PES растворили в дихлорметане (Acros Organics, Германия), а затем нанесли покрытие методом центрифугирования при 4000 оборотах в минуту в течение 30 сек. (RC 5 Suess Microtec, Garching, Германия). Тонкослойные пленки Ultrason имели толщину 30±2 нм (эллипсометрия, SE 400, Sentech, Берлин, Германия).
Адсорбция поверхностно-активного вещества (чистящего средства) n-осредством пьезоквариевого микровзвешивания (ОСМ)
Адсорбцию поверхностно-активных веществ на поли(амидной) и поли(эфирсульфоновой) тонкослойной пленке анализировали при постоянной температуре (23°C) с помощью пьезокварцевого микровзвешивания QCM-E4 (Q-Sense АВ, Gothenburg, Швеция). QCM-кристаллы с полимерным покрытием набухали в деионизированной воде для достижения стабильного исходного состояния, а затем инкубировались с различными поверхностно-активными веществами, растворенными в деионизированной воде (0,025% активной). Стабильность/десорбцию полученного слоя одного компонента оценивали посредством промывки деионизированной водой. Сдвиги частоты и рассеивания, вызываемые адсорбцией/десорбцией компонентов, использовали для определения изменений в поверхностной концентрации поверхностно-активных веществ.
Подготовка (морских) слоев загрязнения на основе BSA /альгината/ гуминовой кислоты (ПА)
Слои загрязнения сформировали непосредственно путем нанесения на субстрат тонкослойной ПА пленки, подготовленный на носителях на основе оксида кремния, раствора 0,25% альгината (AG; средняя вязкость, Sigma-Aldrich), 200 частей на миллион альбумина бычьей сыворотки (BSA; Sigma-Aldrich) и 20 частей на миллион гуминовой кислоты (НА; Sigma-Aldrich). После 10 минут адсорбции, избыток жидкости удалили, осторожно переворачивая пластины, с последующей стадией сушки при 60°C в течение 5 минут. Молекулярные слои загрязнения стабилизировали посредством их погружения в раствор концентрированного CaCl2 (Merck) (8% [вес/объем]) в течение 10 сек. с последующей дополнительной стадией сушки при комнатной температуре. После промывки при помощи MilliQ, этот тип слоев был использован для всех последующих экспериментов очистки. Перед началом экспериментов очистки, все молекулярные слои загрязнения погружали в MilliQ в течение 1 минуты и сушили при комнатной температуре. Полученную толщину слоя анализировали с помощью эллипсометрии.
Подготовка (молочных) слоев загрязнения на основе лакталъбумина/казеина (ПЭС)
Слои загрязнения подготовили посредством погружения субстратов тонкослойной ПЭС пленки в избыточный объем 0,1% [вес/вес] α-лактальбумина (LA, Sigma-Aldrich) и 1% казеина (СА, растворимый в щелочи, Merck), растворенных в MilliQ. Субстраты извлекли и адсорбцию жидкого слоя, остающегося на верхней поверхности, осуществляли при 60°C в течение 2 минут. После этого избыток жидкости удалили и субстраты сушили при 60°C в течение 30 минут. Для стабилизации слоев, высушенные субстраты погрузили в раствор концентрированного CaCl2 (8% [вес/вес]) в течение 10 сек. с последующей дополнительной стадией сушки при комнатной температуре. Этот тип слоев был использован для всех последующих экспериментов очистки. Перед началом экспериментов очистки, все молекулярные слои загрязнения погружали в жесткую воду (16° dH, рН 8) в течение 1 минуты и сушили при комнатной температуре. Полученную толщину слоя анализировали с помощью эллипсометрии.
Оценка эффективности очистки
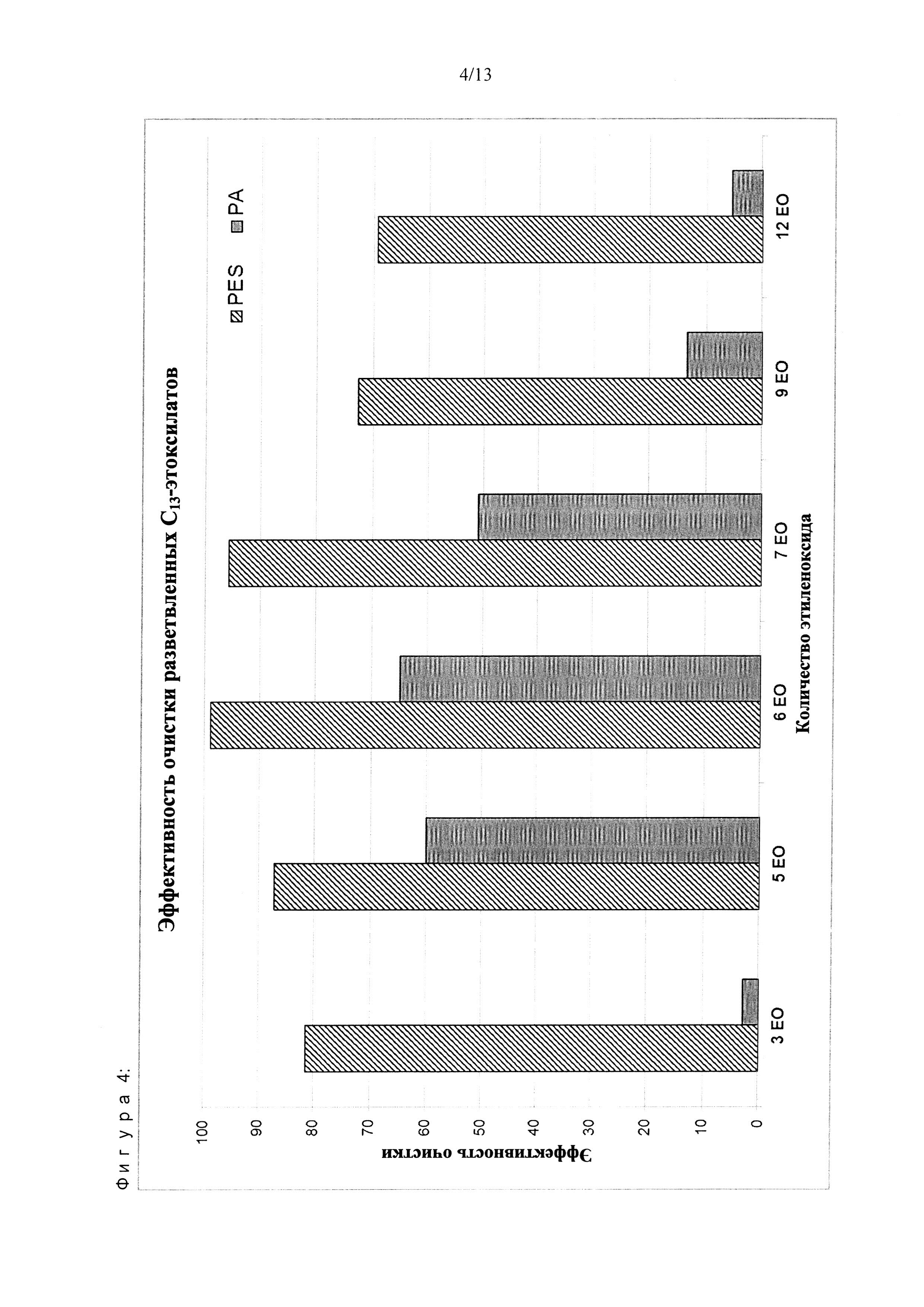
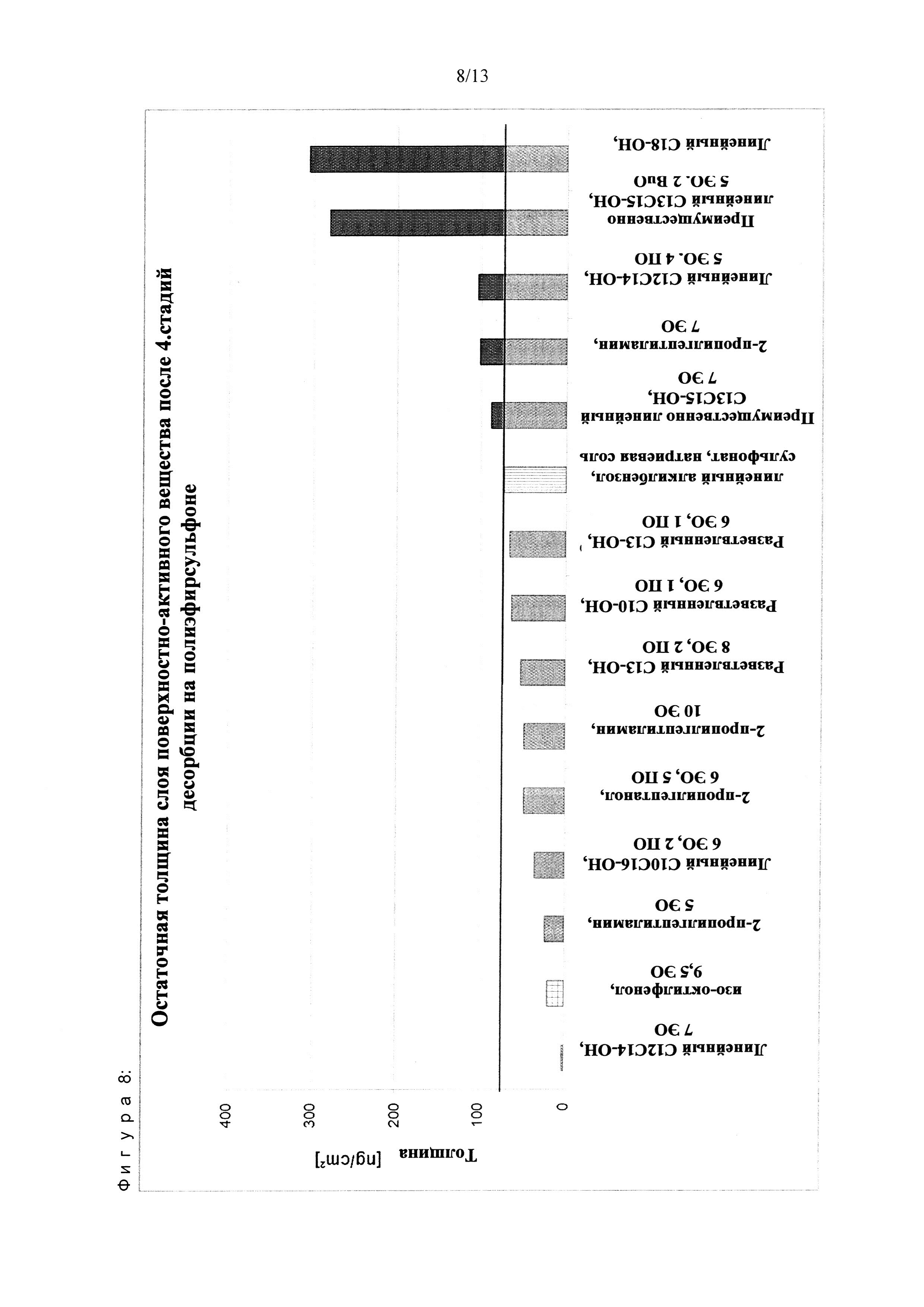
Избранные условия очистки (щелочной рН) и агенты (ПАВ) были испытаны на предмет их способности уменьшать толщину многокомпонентных слоев загрязнения. Если не указано иное, все вещества были растворены в деионизированной воде (рН 12) с активной концентрацией 0,025%) для очистки слоев BSA/AG/HA на ПА-поверхностях (фиг. 3-8, 10 и таб. 7, 10, 11). Для очистки слоев LA/CA (молочных белков) на ПЭС-поверхностях была использована активная концентрация 0,025% при рН 8 в жесткой воде (16° dH) (фиг. 9, 10). Модели слоев биологического загрязнения были погружены в водные растворы, содержащие избранные агенты, в течение 10 минут при комнатной температуре с последующей промывкой в деионизированной воде и сушкой при комнатной температуре. Остаточная толщина слоя была определена методом эллипсометрии. Эффективность очистки была рассчитана в соответствии с формулой эффективности очистки = [1-(остаточная толщина слоя/первоначальная толщина слоя)]*100%.
Определение толщины слоя методом эллипсометрии
Толщина слоя определялась с помощью микрофокусного эллипсометра Sentech SE-400 от компании SENTECH Instruments GmbH, Германия с длиной волны λ=632,8 нм. Угол падения был установлен на 65, 70 и 75°. При дальнейших измерениях толщины многослойная модель была применена для расчета толщины слоев загрязнения и лежащей под ними полиамидной тонкослойной пленки. Показатели преломления были следующими: n(Si)=3.858; n(SiO2)=1.4571; N(полиамид или Полиэфирсульфон)=1,50 и n(слой загрязнения)=1,47. Все данные представлены в виде средних значений.
2. Слои бактериального загрязнения
Бактериальный штамм и условия роста
Для получения слоев бактериального загрязнения в данном исследовании использовали морские бактерии Cobetia marina (DSMZ4741). Штамм был приобретен из коллекций культур DSMZ, Германия. Морскую соль и пептон (SSP, все ингредиенты были приобретены у Sigma-Aldrich) (морской соли 20 г; пептона 18 г; деионизированной воды 1000 мл, рН 7,8) использовали в качестве среды для выращивания. Исходную культуру поддерживали на скошенном агаре с морской солью - пептоном (SSPA, все ингредиенты были приобретены у Sigma-Aldrich) (морской соли 20 г; пептона 18 г; агара 30 г; деионизированной воды 1000 мл, рН 7,8). Перед экспериментами, культуру выращивали в среде SSP на ротационном шейкере при 180 оборотах в минуту при 28°C в течение 20-22 часов, чтобы получить клетки в фазе логарифмического роста.
Подготовка слоев бактериального загрязнения
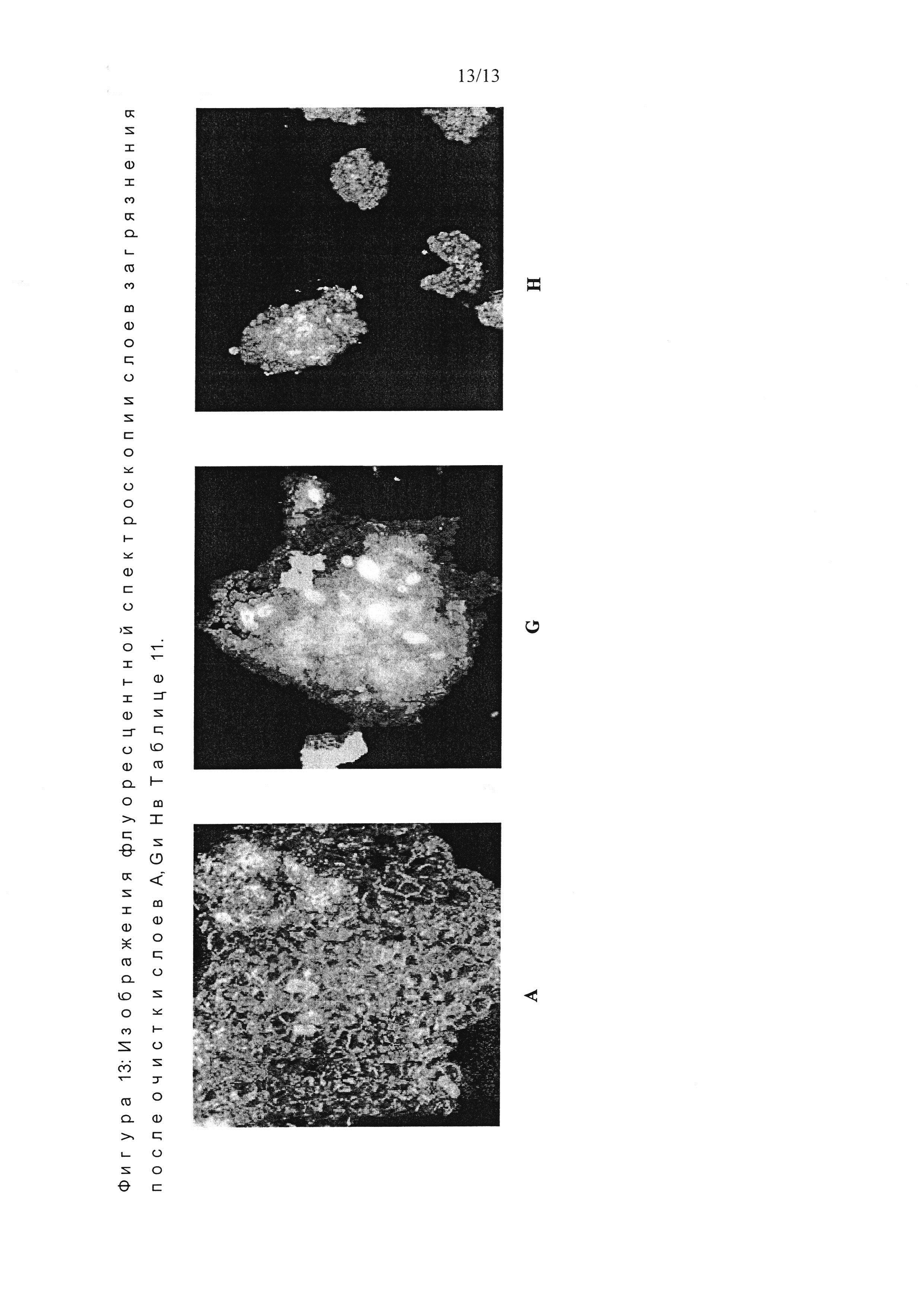
Субстраты полиамидной тонкослойной пленки, приготовленные на предметных стеклах, выдерживали в течение 24 часов в искусственной морской воде (морской соли 20 г, деионизированной воды 1000 мл, рН 7,8) перед их переносом в суспензии бактериальных клеток. Свежевыращенную (в фазе логарифмического роста) бактериальную суспензию получили с оптической плотностью 0,2 при длине волны 600 нм (DU 800, Beckman Coulter, Krefeld, Германия). Кондиционированные реплицированные стекла (четыре для каждого анализа) поместили в отдельные отсеки квадратных чашек Петри и добавили 5 мл бактериальной суспензии, таким образом полностью погрузив в нее стекла. Стекла поместили в инкубатор при 28°C на ротационном шейкере (90 оборотов в минуту). После 1 часа инкубации, стекла перенесли в новые квадратные чашки Петри, содержащие 5 мл свежей среды SSP. Стекла инкубировали в течение еще 4 часов при 28°C на ротационном шейкере (90 оборотов в минуту), чтобы прикрепленные бактерии быстро размножились на поверхности стекол. В конце инкубации стекла аккуратно промыли в искусственной морской воде, чтобы удалить любые неприкрепленные клетки (фиг. 11-13).
Эксперименты по очистке слоев бактериального загрязнения
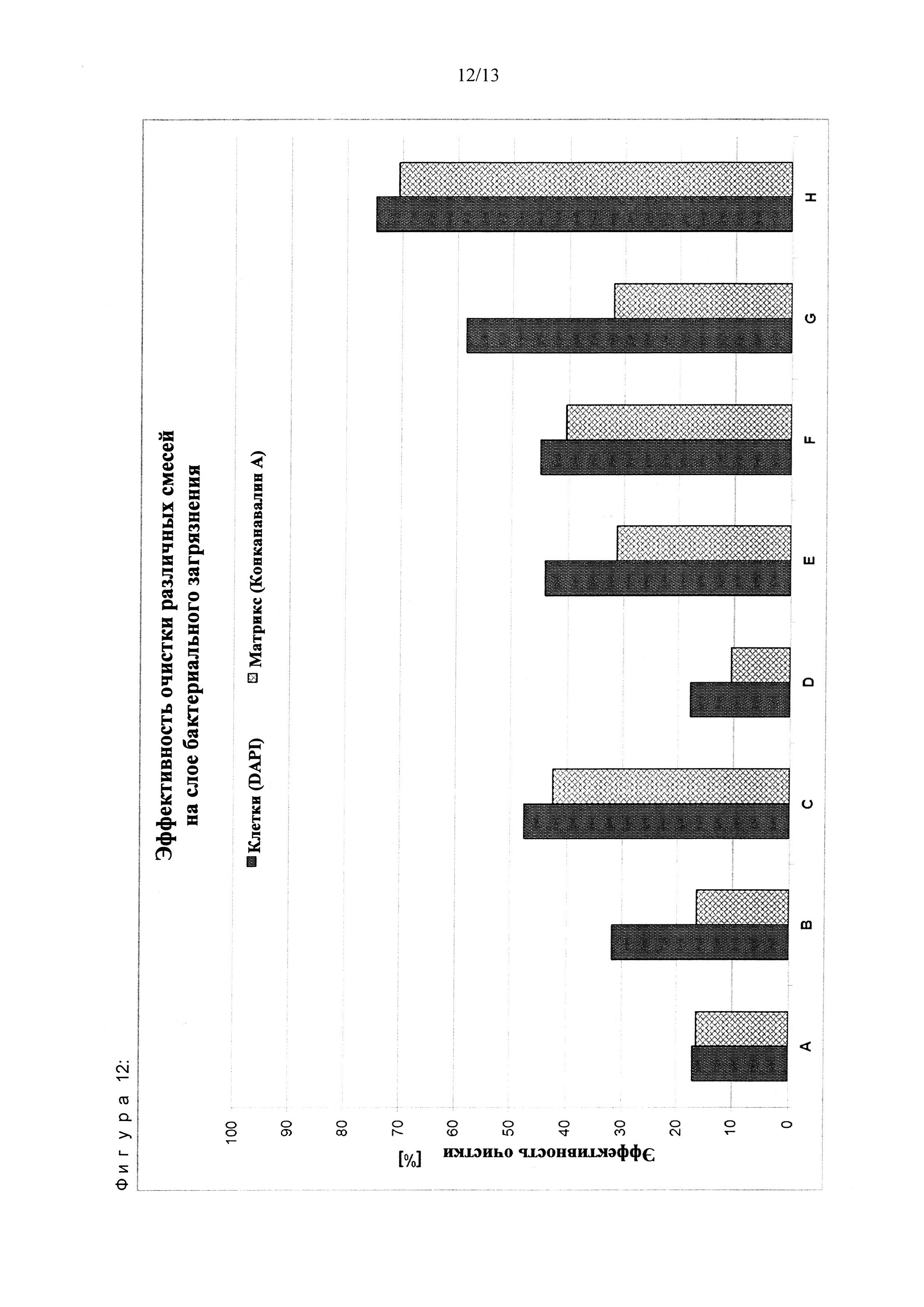
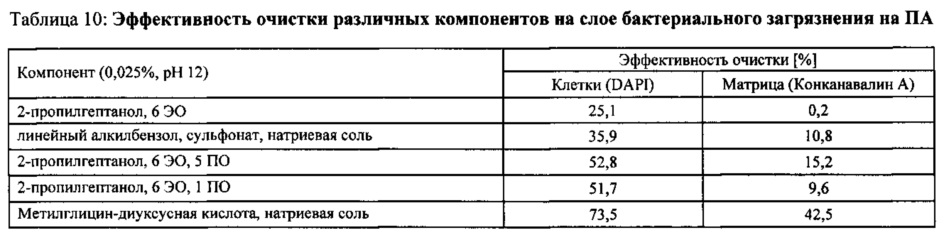
Как и в экспериментах с использованием многокомпонентных молекулярных слоев загрязнения, выбранные условия для очистки (рН 12) и агенты были испытаны на предмет их способности удалять бактериальные клетки и внеклеточный полимерный матрикс (EPS-матрикс). Дополнительно оценивали потенциальные возможности очистки для протеазы субтилизина (субтилизин А типа VIII из Bacillus licheniformis, 12 ед/мг, Sigma-Aldrich) и метилглицин-диуксусной кислоты, натриевой соли (Trilon® М жидкий, BASF SE), применяемых отдельно или в сочетании с поверхностно-активным веществом 2-пропилгептанолом, 6 ЭО, 1 ПО (Lutensol® XL 60, BASF SE). С этой целью фермент (100 мкг/мл) и/или хелатирующий агент (активная концентрация 0,2%) и/или поверхностно-активное вещество (активная концентрация 0,025%) растворили в 10 мМ буфера NaH2PO4 (Sigma-Aldrich, рН 8,1). Слои бактериального загрязнения погружали в соответствующий чистящий раствор в течение 10 минут при комнатной температуре с последующей промывкой деионизированной водой. После этого, их сразу же подвергали фиксации.
Фиксация и окрашивание
Для проведения флуоресцентной микроскопии/спектроскопии и атомно-силовой микроскопии, слои бактериального загрязнения фиксировали посредством переноса соответствующих предметных стекол в квадратные чашки Петри, содержащие 4% пара-формальдегида (Sigma-Aldrich). После инкубации в течение 15 минут, слои промывали деионизированной водой и сушили азотом.
Для флуоресцентного окрашивания, стела поместили в специально изготовленные инкубационные камеры во избежание окрашивания обратной стороны. Для окрашивания EPS-матрикса Конканавалин А, конъюгированный Alexa 488 (Molecular Probes, распределяемый Invitrogen, Нидерланды), растворенный в 0,1 М буферного раствора бикарбоната натрия (Sigma-Aldrich) (рН 8,3), добавляли в течение 1 часа в темноте (25 мкг/см2). После инкубации раствор удалили и образцы дважды промыли фосфатно-солевым буферным раствором (PBS, Sigma-Aldrich). Для окрашивания бактериальных клеток раствор DAPI (растворенный в PBS) наносили на образцы, окрашенные Конканавалином А, в течение 5 минут в темноте (25 мкг/см). После удаления раствора слои дважды промывали деионизированной водой. Образцы извлекли из инкубационных камер и высушили азотом.
Для сканирующей электронной микроскопии выполнили альтернативную процедуру фиксации с целью обеспечения оптимизированной визуализации EPS-матрикса. Таким образом, образцы промыли в буфере PBS и фиксировали в 0,1 М какодилатном буфере с рН 7,3, содержащем 2% параформальдегида, 2% глутарового альдегида и 0,2% рутения красного, в течение 1 часа при комнатной температуре. После промывки в течение 30 минут в 0,1 М какодилатном буфере, содержащем 7,5% сахарозы и 0,1% рутения красного, последовала постфиксация в 0,1 М какодилатного буфера, содержащего 1% тетраоксида осмия и 0,05% рутения красного (все реагенты от Sigma, Германия; OSO4 от Roth, Германия). Затем образцы промыли деионизованной водой и высушили в критической точке (BAL-ТЕС CPD 030, Bal-Tec, Liechtenstein), выполнили напыление золотом (с использованием установки для напыления Sputtercoater, BAL-TEC) и визуализировали с помощью сканирующего электронного микроскопа FEI XL 30.
Морфологический анализ слоев бактериального загрязнения
После фиксации морфологию слоев бактериального загрязнения анализировали с помощью микроскопии. Флуоресцентно окрашенные образцы оценивали с помощью флуоресцентной микроскопии (DMIRE2, Leica, Bensheim, Германия) с использованием 100х объектива масляной иммерсии. Таким образом, флуоресценцию DAPI контролировали с длиной волны возбуждения 360 нм и длиной волны эмиссии 460 нм, при этом для Конканавалина А, конъюгированного Alexa 488, использовали длину волны возбуждения 492 нм и длину волны эмиссии 520 нм. Оба изображения были объединены, чтобы сформировать изображение наложения.
Для анализа морфологии слоя бактериального загрязнения с более высоким разрешением, были использованы атомно-силовая микроскопия (АСМ) и сканирующая электронная микроскопия (СЭМ). АСМ проводили на образцах, высушенных на воздухе, с использованием системы JPK Nanowizard AFM (JPK Instruments, Германия), установленной на инвертированном оптическом микроскопе Axiovert Observer D.l (Zeiss, Германия). Используемые кантилеверы АСМ имели номинальную жесткость пружины 60 мН/м (SNL, Bruker). Коэффициенты усиления обратной связи были оптимизированы, чтобы получить топограммы с наилучшим разрешением. Топограммы были записаны с линейной скоростью 1,5 Гц в контактном режиме постоянной силы, поддерживая силу контакта »200 пН на протяжении всего процесса измерения. Измерения СЭМ были выполнены на покрытых золотом образцах с использованием электронного микроскопа XL30 ESEM (FEI, Нидерланды) в режиме высокого вакуума с подачей напряжения 5-10 кВ.
Количественная оценка эффективности очистки с помощью флуоресцентной спектроскопии
Флуоресцентно окрашенные образцы поместили в специально изготовленный держатель предметных стекол. Флуоресценцию DAPI и Конканавалина А, конъюгированного Alexa 488, измеряли с помощью планшет-ридера (многолуночного планшет-ридера SPECTROFluor от TECAN Genios, программное обеспечение Magellan, Crailsheim, Германия) с режимом верхнего считывания с использованием трех вспышек. Метод планшет-ридера был запрограммирован для имитации 6-луночных плоскодонных планшетов, обеспечивая в результате общее количество 16 точек измерения по каждому предметному стеклу. Среднее количество этих точек было использовано для определения относительной бактериальной биомассы и EPS-матрикса, прикрепленных к поверхности после извлечения заготовки. В качестве заготовки было использовано предметное стекло с полиамидным покрытием, которое подвергалось воздействию в тех же условиях, но в отсутствие бактерий. Для оценки эффективности очистки интенсивность флуоресценции конкретных образцов сравнивали с необработанными стеклами, таким образом представляя изначально нанесенную биопленку.
Определение динамического угла контакта
Динамический угол контакта измеряли с помощью высокоскоростного видеоизмерительного прибора для определения угла контакта типа ОСАН 200 компании Dataphysics Instruments 5 GmbH, Raiffeisenstr. 34, Fildersstadt, на предметных стеклах с покрытием, нанесенным методом центрифугирования.
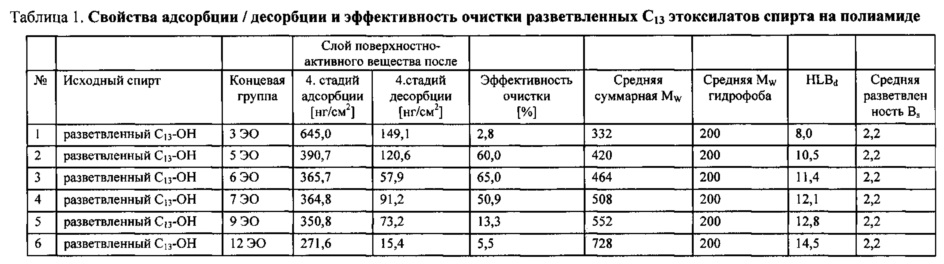
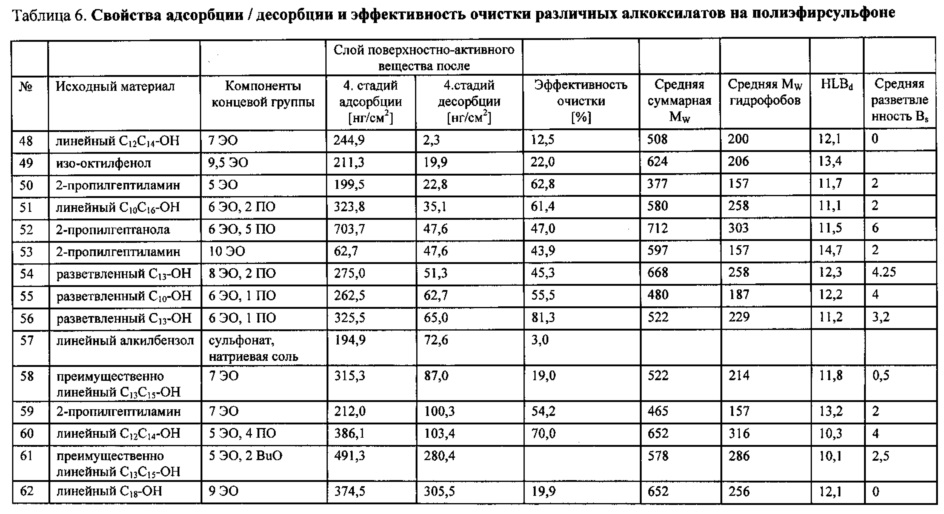
Поверхностно-активные вещества в соответствии с изобретением, указанные в Таблицах 1-6, используются в водном растворе с концентрацией 0,2 г/л.
Угол контакта постоянно определялся (60 раз в секунду) при 23°C в течение 10 секунд после нанесения (фиг. 1, 2 и таб. 8, 9). В этих условиях угол контакта воды без добавления поверхностно-активного вещества остается примерно на уровне 65°. Угол контакта на ПА водных растворов разветвленных тридецилэтоксилатов падает от 10° до 33°. Угол контакта на ПЭС водных растворов разветвленных тридецилэтоксилатов падает от 17° до 37°. Предпочтительным является угол контакта через 10 секунд ниже 30°.







Реферат
Целью настоящего изобретения является использование разветвленного алкоксилированного неионогенного поверхностно-активного вещества в качестве добавки к водному составу для чистки мембран. Описан водный состав для чистки мембран, содержащий алкоксилированное неионогенное поверхностно-активное вещество, имеющее следующую формулу:где R представляет собой линейную или разветвленную С-Суглеводородную цепь, X представляет собой О или N, R, Rи Rнезависимо друг от друга представляют собой водород, метил, этил, пропил, изопропил или их смесь, n имеет значение от 1 до 8, m имеет значение от 1 до 8, p имеет значение от 0 до 8, причем если X означает О, то w означает число 1, а если X означает N, то w означает число 2, поверхностно-активное вещество, имеющее величину HLBот 9 до 12,5 и среднюю степень разветвленности B≥1,5. Технический результат – эффективная очистка в водных растворах, используемых для очистки мембран. 2 н. и 13 з.п. ф-лы, 13 ил., 11 табл.
Формула


Комментарии