Бактериоцин, способ его получения, штамм micrococcus varians, нуклеотидный фрагмент, сигнальный пептид - RU2172324C2
Код документа: RU2172324C2
Чертежи











Описание
Изобретение относится к бактериоцину, к штамму, который продуцирует упомянутый бактериоцин, к способу получения бактериоцина и к применению такого бактериоцина и/или штамма, продуцирующего упомянутый бактериоцин, в производстве пищевых продуктов и косметики.
Бактериоцины выделены из многочисленных грам-положительных и грам-отрицательных бактерий. Бактериоцины представляют собой молекулы, по своей природе напоминающие белок, которые обладают бактерицидным эффектом, и по этой причине бактериоцин вызывает антагонистическую реакцию между бактерией, его продуцирующей, и другими, одним или более видами бактерий. Кроме того, спектр ингибирования бактериоцина зачастую ограничен видами, близкими к тому штамму, который его продуцирует.
Бактериоцины были, в частности, обнаружены в молочнокислых бактериях. Например, в патенте ЕР 0643136 (Societe des produits Nestle) описывается идентификация двух бактериоцинов из Streptococcus thermophilus. Сходным образом был выделен бактериоцин из Lactobacillus lactis (Арр. and Env. Microbiol., 1992, 58, 279-284; J. of Biol. Chem., 1993, 268, 16361-16368).
Однако к настоящему времени не известен бактериоцин, полученный из Micrococcus varians. Micrococcus varians в настоящее время широко применяется в производстве пищевых продуктов, в частности при ферментации мяса с целью получения деликатесных продуктов, таких как салями и другие колбасы. В этой связи очень важно иметь доступный продуцирующий бактериоцин штамм этой бактерии для того, чтобы бороться против патогенов.
Настоящее изобретение направлено на решение этой проблемы.
Описываемый в настоящем изобретении бактериоцин представляет собой бактериоцин из Micrococcus varians, при этом упомянутый бактериоцин представляет собой аминокислотную последовательность SEQ ID No: 1 или любую аминокислотную последовательность, отличающуюся от последовательности SEQ ID No: 1 одним замещением, одной делецией и/или одной вставкой от 1 до 4 аминокислот.
Кроме того, любой нуклеотидный фрагмент, кодирующий указанный бактериоцин, в частности, нуклеотидный фрагмент, представленный последовательностью SEQ ID No: 2, также входит в рамки настоящего изобретения.
Описываемый в настоящем изобретении штамм относится также к штамму Micrococcus varians, который продуцирует указанный бактериоцин, в частности к штаммам CNCM I- 1586 и CNCM I-1587 Micrococcus varians.
По способу получения бактериоцина в соответствии с настоящим изобретением штамм Micrococcus varians, который продуцирует бактериоцин, в частности, штамм CNCM I-1586 или штамм CNCM I-1587, культивируют в подходящей для роста микроорганизма среде с соблюдением благоприятных условий, позволяющих получить культуральную среду, содержащую от 107 до 1011 организмов нужного штамма на миллилитр, после чего культуральную среду центрифугируют, а экстракт супернатанта, содержащий бактериоцин, используют для дальнейших стадий получения препарата. И, наконец, в настоящем изобретении описывается применение бактериоцина из Micrococcus varians, которое включает применение его нуклеотидной последовательности, равно, как и сигнальной последовательности, экстракта супернатанта, содержащего бактериоцин, а также штамма Micrococcus varians, который продуцирует бактериоцин, в производстве пищевых продуктов, косметики и фармацевтических продуктов для использования в области дерматологии и в гигиене полости рта.
В приведенном ниже описании изобретения бактериоцин обозначается термином "вариации".
В рамках настоящего изобретения условная единица (уе) определяется как величина, обратная наибольшему разбавлению, при котором образец все еще проявляет бактерицидный эффект в тесте, который каждому специалисту в данной области известен как "агаровый тест".
В рамках настоящего изобретения термин "фрагмент" или "фрагмент ДНК" следует понимать как фрагмент одноцепочечной или двухцепочечной ДНК, который частично или полностью является кодирующим и который может быть синтезирован, реплицирован in vitro с помощью, например, известного метода полимеразно-цепьевой реакции, или реплицирован in vivo в бактерии, например, типа Escherichia coli.
В рамках настоящего изобретения термин "гомологичный фрагмент" следует понимать как любой фрагмент, который отличается от фрагментов настоящего изобретения земещением, делецией или вставкой небольшого числа оснований. В контексте настоящего изобретения два фрагмента ДНК, которые кодируют один и тот же полипептид, в связи с дегенерацией генетического кода будут рассматриваться как гомологичные. В качестве гомологичного фрагмента рассматривается также фрагмент, который проявляет более 80% гомологии с фрагментом настоящего изобретения. В последнем случае гомология определяется по соотношению между количеством оснований в гомологичном фрагменте и их количеством в фрагменте настоящего изобретения.
И, наконец, в рамках настоящего изобретения термин "фрагмент, который гибридизируется" следует понимать как любой фрагмент, который способен к гибридизации с фрагментами настоящего изобретения по методу Саузерн-Блоттинга (Sambrook et al. Molecular Cloning, A Laboratory Manual, Cold Spring Harbor Laboratory Press, U.S.A., 1989, chapter 9.31 to 9.58). Предпочтительно гибридизация выполняется в условиях, достаточно строгих, для того, чтобы избежать неспецифической гибридизации или гибридизации, которая оказывается относительно нестабильной.
Протеиноподобный фактор, в настоящем случае бактериоцин, обладающий мощным бактерицидным эффектом, был выделен из штаммов CNCM I-1586 и CNCM I-1587. Бактериоцин, который был выделен из Micrococcus varians и который, следовательно, представлен аминокислотной последовательностью SEQ ID No: 1, приведенной в перечне последовательностей ниже, был назван вариацином.
В связи со свойствами вариацина, настоящее изобретение относится к любому бактериоцину, который имеет аминокислотную последовательность, отличающуюся от SEQ ID No: 1 одним замещением, одной делецией и/или одной вставкой от 1 до 4 аминокислот. Таким образом, упомянутый бактериоцин, который имеет аминокислотную последовательность, отличающуюся от последовательности SEQ ID No: 1 одним замещением, одной делецией и/или одной вставкой от 1 до 4 аминокислот, может иметь более широкий спектр ингибирования для бактериального рода или для бактериальных штаммов, чем, например, упомянутый вариации.
Представляется также возможным провести селекцию хромосомного нуклеотидного фрагмента, кодирующего вариации настоящего изобретения, из двух штаммов CNCM I-1586 и CNCM I-1587. Оба упомянутых фрагмента описываются последовательностью SEQ ID No: 2, приведенной ниже в списке последовательностей.
Интерес настоящего изобретения представляет также любой нуклеотидный фрагмент, кодирующий вариацин настоящего изобретения, в частности, нуклеотидные фрагменты, которые являются гомологичными к последовательности SEQ ID No: 2 или гибридизируются с ней.
В частности, настоящее изобретение относится к нуклеотидам с 88 по 153 в последовательности SEQ ID No: 2, которые кодируют сигнальный пептид вариацина, к нуклеотидам от 154 до 228 в последовательности SEQ ID No: 2, кодирующим секретируемый вариацин настоящего изобретения, и/или к нуклеотидам с 88 по 228 в последовательности SEQ ID No: 2, кодирующим бактериоцин, слитый с сигнальным пептидом.
Фрагмент, кодирующий секретируемый вариацин, может быть использован для экспрессии вариацина настоящего изобретения в тех или иных микроорганизмах, отличных от Micrococcus varians. В этом случае нуклеотиды от 154 до 228 в последовательности SEQ ID No: 2 могут быть клонированы в вектор экспрессии справа от промотора или от сигнальной последовательности и слева от терминатора, учитывая рамку считывания, и затем упомянутый вектор может быть введен в растение, бактерию или дрожжи с тем, чтобы увеличить спектр ингибирования, включив в него, например, определенные бактерии.
Можно добиться использования сигнальной последовательности настоящего изобретения путем слияния участка с 88 по 153 нуклеотидов в последовательности SEQ ID No: 2 с интересующим геном, учитывая рамку считывания, и затем клонирования его целиком в вектор экспрессии Micrococcus varians так, чтобы позволить белку, кодируемому упомянутым интересующим геном, экспрессироваться и секретироваться, например, в Micrococcus varians.
Нуклеотиды с 88 по 228 в последовательности SEQ ID No: 2 могут быть клонированы в вектор экспрессии Micrococcus varians и введены затем в другой штамм Micrococcus varians, так что последний указанный штамм начинает продуцировать вариацин настоящего изобретения.
Кроме того, штамм Micrococcus varians, который содержит либо интегрированный в свой геном, либо через участие вектора экспрессии фрагмент ДНК, кодирующий вариации настоящего изобретения, является частью настоящего изобретения. В частности, штаммы Micrococcus varians, депонированные 7 июня 1995 г. в соответствии с Будапештским договором, в Национальной коллекции культур микроорганизмов. Институт Пастера, Париж, Франция (Collection National de Cultures de Microorganimes, Institut Pasteur, 25 Rue du Docteur Roux, F-75724 PARIS CEDEX 15, France), где они получили депозитные номера CNCM I-1586 и CNCM I-1587, являются частью настоящего изобретения.
Бактерии Micrococcus varians представляют собой грам-положительные и положительные на каталазу аэробные бактерии, являющиеся постоянно иммобилизованными. Они имеют сферическую форму и встречаются в виде тетрад, хаотично сгруппированных.
Колонии Micrococcus varians на ВН1 среде (с сердечно-мозговой вытяжкой) окрашены в желтый цвет. Оптимальная температура для роста указанных штаммов составляет 25-37oC.
Штаммы CNCM I-1586 и CNCM I-1587, охватываемые настоящим изобретением, метаболизируют и глюкозу, и фруктозу. А штамм CNCM 1-1587 метаболизирует также сахарозу и фуранозу.
Кроме того, штамм CNCM I-1586 несет две плазмиды с размерами 4 и 12 т.п. н. , тогда как штамм CNCM I-1587 имеет единственную плазмиду размером 7 т.п. н.
Культуральные супернатанты штаммов CNCM I-1586 и CNCM I-1587 демонстрируют сравнительно широкий спектр ингибирования роста других бактерий, среди которых можно упомянуть, например, следующие: Lactococcus lactis, Lactobacillus helveticus, Lactobacillus delbrueckii subsp. bulg-aricus, Lactobacillus delbrueckii subsp. lactis, Lactobacillus delbrueckii subsp. delbrueckii, Lactobacillus acidophilus, Lactobacillus johnsonii, Lactobacillus plantarum, Lactobacillus sake, Lactobacillus curvatus, Leuconostoc carnosum, Leuconostoc mesenteroides subsp. mesenteroldes, Streptococcus thermophilus, Listeria monocytogenes, Enterococcus faecalis subsp. faecalis, споры и вегетативные клетки Bacillus subtilis, Bac. illus cereus. Bacillus polyinyxa. Bacillus circulans. Bacillus pumulus и Bacillus liqueniformis и Clostridia.
Предпочтительно, по способу получения вариацина, штамм Micrococcus varians, продуцирующий вариацин, культивируют в среде и в условиях, благоприятных для его роста, с тем чтобы получать культуральную среду, содержащую от 107 до 1010 организмов упомянутого штамма на миллилитр, после чего полученную культуру центрифугируют, а экстракт супернатанта, содержащий описываемый бактериоцин, подвергают дальнейшей обработке.
Для получения указанного экстракта штамм Micrococcus varians настоящего изобретения, продуцирующий вариацин, в частности штамм CNCM I- 1586 или штамм CNCM I-1587, может культивироваться в той среде и с соблюдением тех условий, которые благоприятны для роста Micrococcus varians. В этом случае культивирование может осуществляться в BHI среде при температуре 25-37oC в аэробных условиях на качалке, до получения нужной концентрации организмов, например, от 107 до 1011 на миллилитр среды. Полученную стандартную культуру затем центрифугируют при 4000 - 6000 g, а экстракт супернатанта, содержащий описываемый бактериоцин, собирают.
Настоящее изобретение относится также к использованию вариацина, в частности, в форме экстракта, или к использованию штамма Micrococcus varions, который продуцирует упомянутый бактериоцин, для производства пищевых и косметических продуктов.
Культура одного из упомянутых штаммов Micrococcus varians настоящего изобретения может быть, в частности, использована при ферментации фарша для приготовления салями, а также для борьбы с заражением, например, клостридиями.
Вариацин в виде неочищенного экстракта или в очищенном виде может использоваться при добавлении к закваске, которую получают при использовании бактерий, устойчивых к упомянутому вариацину, в процессе приготовления сыров, таких, как сыры типа моццарелла, для того, чтобы избежать появления в сырах глазков, продуцируемых Bacillus poymyxa, споры которого выживают в процессе ферментации, и типа вахерина для того, чтобы бороться с загрязнениями, вызванными, например, Listeria monocytogenes.
Вариацин в грубом экстракте или в очищенной форме, или один из двух продуцирующих его штаммов может использоваться как добавка или агент, активные против патогенных бактерий, для получения десертных муссов, таких, как пастеризованные кремы, с тем, чтобы препятствовать росту спор таких микроорганизмов, как Clostridia и Bacillus cereus, или росту таких бактериальных штаммов, как Listeria.
Кроме того, вариацин в грубом экстракте или в очищенном виде или один из двух вышеуказанных штаммов могут использоваться как добавка или как агент, активные против патогенных бактерий, для изготовления косметических продуктов таких, как увлажняющие кремы или дезодоранты с тем, чтобы бороться с патогенными бактериями, загрязняющими в данном случае кожу.
Вариацин настоящего изобретения более подробно описывается ниже с помощью различных микробиологических, биохимических и генетических данных, которые иллюстрируют его свойства. Приведенные проценты являются весовыми процентами.
Единица бактериальной активности - "агаровый тест".
В контексте настоящего изобретения бактерицидная активность определяется в терминах условных единиц.
Супернатант стандартной культуры Micrococcus varlans настоящего изобретения, приготовленный в условиях, описанных например, в примере 1, имеет в типичном случае активность 640 уе/мл. Аналогично концентрат упомянутого супернатанта, который получают в условиях, описанных, например, в примере 2, имеет обычно активность 24000 уе/мл.
Упомянутый агаровый тест используют для определения наличия у образца при данном значении разбавления бактерицидной активности.
Для проведения этого теста 15 мл MRS агаровой среды, содержащей индикаторный штамм в концентрации 105-106 КОЕ/мл, наносят на чашку Петри. Штамм, чувствительный к вариацину, в настоящем случае, Lactobacillus bulgaricus (YL 5) или штамм Lactobacillus helveticus (N2), используется как индикаторный штамм.
В культуральной среде делают отверстия диаметром 5 мм. Исследуемые образцы супернатанта или концентрата супернатанта вливают в указанные отверстия в количестве 50 Midi на отверстие. Чашки ставят на предварительную инкубацию при 4oC в течение 2 часов и затем инкубируют в течение ночи при температуре 30oC или 37oC, в зависимости от вида индикаторного штамма. После окончания роста индикаторного штамма становятся видимыми ореолы ингибирования. Величина разбавления, при котором образец больше не проявляет бактерицидной активности, представляет собой значение разбавления, начиная с которого ореол ингибирования уже больше не просматривается.
Инактивация ферментами
Упомянутый агаровый тест используется для определения того, инактивируется ли вариацин, выделенный в соответствии с настоящим
изобретением, в присутствии протеолитического фермента или в присутствии
каталазы.
Для того, чтобы провести такой тест, со скоростью 5 мг/мл к концентрату культурального супернатанта, описанному в примере 2, добавляют фермент. Создают условия для действия фермента при температуре инкубации в течение 60 минут перед помещением образца в агаровую лунку.
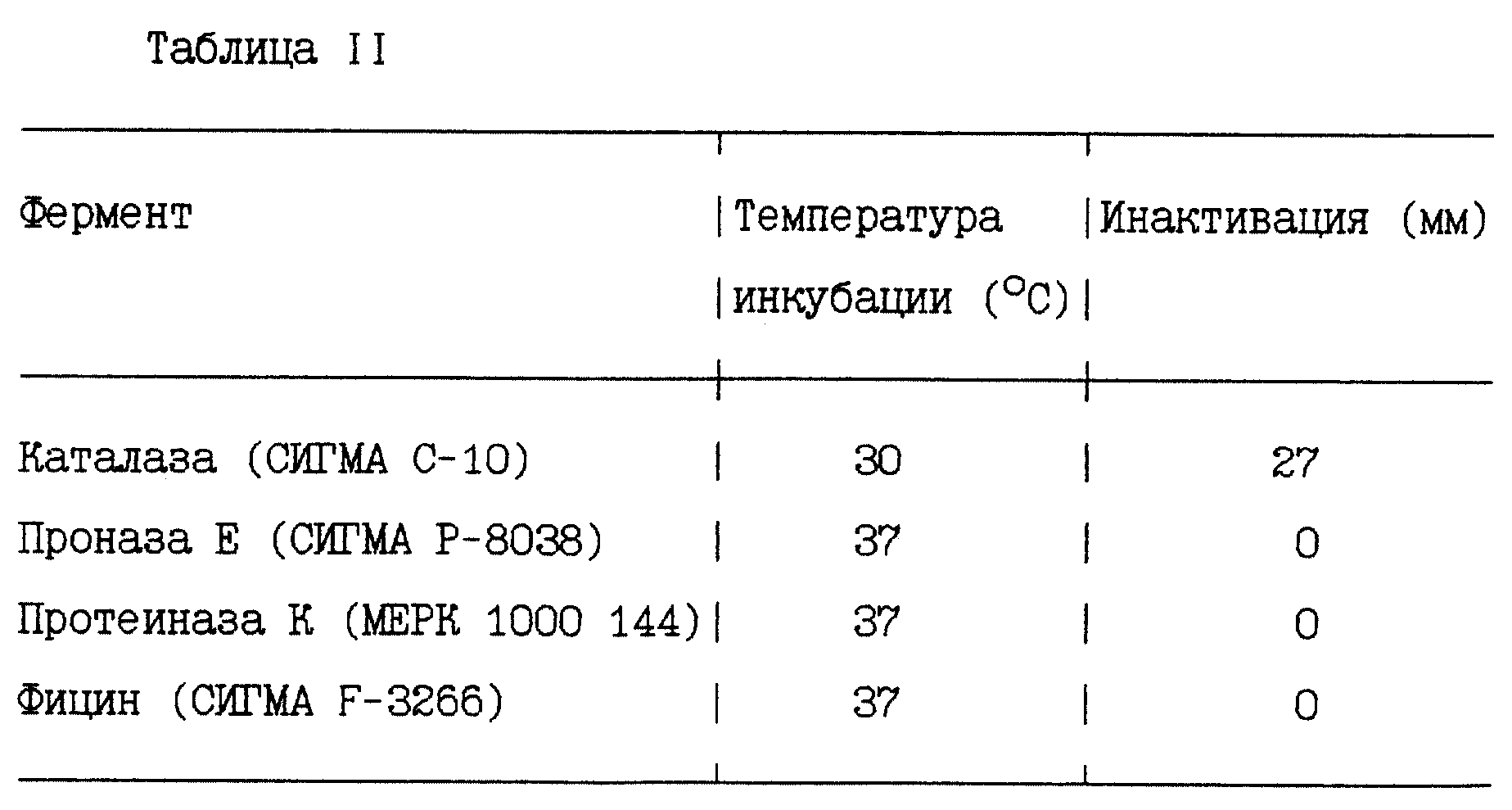
Параллельно готовят контроль с использованием того же концентрата при pH 7 и без добавления фермента. Контрольный образец инкубируют при температуре 37oC в течение 60 минут перед помещением его в агаровую лунку для тестирования с целью сравнения ореола ингибирования, полученного в присутствии фермента, с ореолом ингибирования в контроле. Диаметр контрольного ореола ингибирования составляет 27 мм.
В табл. 1 приведены результаты, полученные с ферментами, которые исследовали с использованием индикаторного штамма Lactobacillus helveticus (N2). В указанной таблице, как и в табл. II, фермент обозначается по его типу, названию поставщика и номера в каталоге поставщика. Число О указывает на отсутствие ореола ингибирования, другими словами, что бактерицидный эффект бактериоцина подавляется инкубированием последнего с ферментом. Число 27 указывает на то, что имеется ореол ингибирования размером 27 мм, соответствующий бактерицидной активности вариацина.
В табл. II приведены результаты, которые были получены для ферментов, исследованных с использованием индикаторного штамма Lactobacillus bulgaricus (YL 5).
Результаты, приведенные в табл. I и II, показывают, что все протеолитические ферменты подавляют бактерицидную активность вариацина. Они свидетельствуют о том, что вариацин по своей природе представляет белковоподобное вещество и что эта протеиноподобная часть участвует в осуществлении бактерицидной активности.
Факт отсутствия, по результатам исследований, воздействия каталазы на бактерицидную активность вариацина указывает на то, что ингибирование роста двух индикаторных штаммов происходит не вследствие антибактериальной активности H2O2, сходной с активностью бактериоцинов, поскольку H2O2 подверглась бы деградации каталазой.
Спектр ингибирования культурального супернатанта, содержащего вариацин
Был применен агаровый тест для того,
чтобы определить, является ли
антибактериальная активность культурального супернатанта, содержащего вариацин настоящего изобретения, ингибирующей активностью в отношении роста различных штаммов спор и
бактерий. Таким образом был
определен спектр ингибирования супернатанта.
Для проведения указанных тестов 15 мл стандартной среды, содержащей 15 мкл инокулята исследуемой культуры, которая была получена в ходе ночного культивирования накануне, наносят на чашки Петри с таким расчетом, чтобы получить бактериальную концентрацию в диапазоне 105-106 на 1 мл стандартной среды. При этом под стандартной средой понимается среда, благоприятная для роста исследуемого штамма. Если исследуемый штамм происходит из спор, их рост осуществляют в покрывающей среде в количестве 105 -106 спор на 1 мл среды.
В каждой чашке Петри делают отверстия диаметром по 5 мм. По методу, приведенному в примере 1, в каждую из них вносят образцы культурального супернатанта по 50 мкл. Чашки ставят на предварительную инкубацию при температуре 4oC в течение 2 часов и затем инкубируют при температуре, благоприятной для роста исследуемого штамма в условиях теста в течение времени, необходимого для того, чтобы покрыть чашку видимым бактериальным газоном.
Эффект или степень ингибирования оценивается по диаметру наблюдаемого ореола ингибирования. Ингибирование оценивается как очень сильное (++++), если упомянутый ореол имеет диаметр 18-28 мм, сильное (+++), если ореол имеет диаметр 10-17 мм, среднее (++), если диаметр составляет 5-9 мм, слабое (+), если диаметр равен 1-4 мм, и нулевое (-), если ореол ингибирования не обнаруживается.
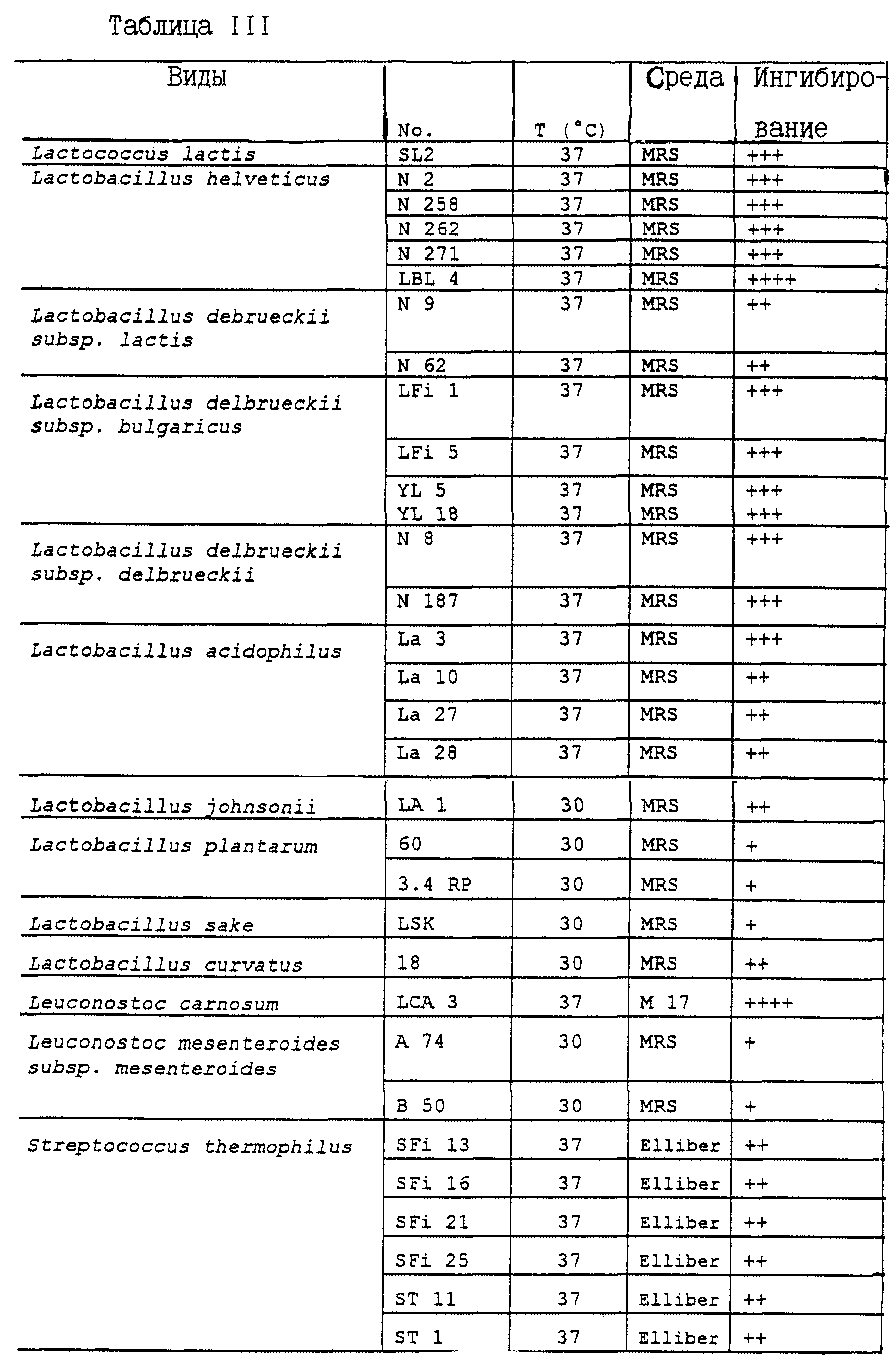
Указанным способом были исследованы 32 штамма различных видов и подвидов молочнокислых бактерий, и ни один из них не проявил устойчивость к супернатанту. В табл. III приведены более подробные результаты проведенного исследования. В ней, как и в последующих таблицах, обозначение штамма или его номер относятся к номерам, присвоенным данному штамму в Коллекции микроорганизмов Нестле в Швейцарии (Nestle Collection; Адрес: NESTEC S.A. Centre de Recherche, Vers-chez-les-Blanc, CH-lOOO Lausanne 26, Switzerland). Указанная в таблице температура означает температуру инкубации в рамках теста. А указанная среда означает стандартную среду, благоприятную для роста исследуемого штамма.
Из данных табл. III видно, что спектр ингибирования супернатантом достаточно широк, поскольку уровень ингибирования имеет примерно одинаковую степень выраженности у различных исследованных видов.
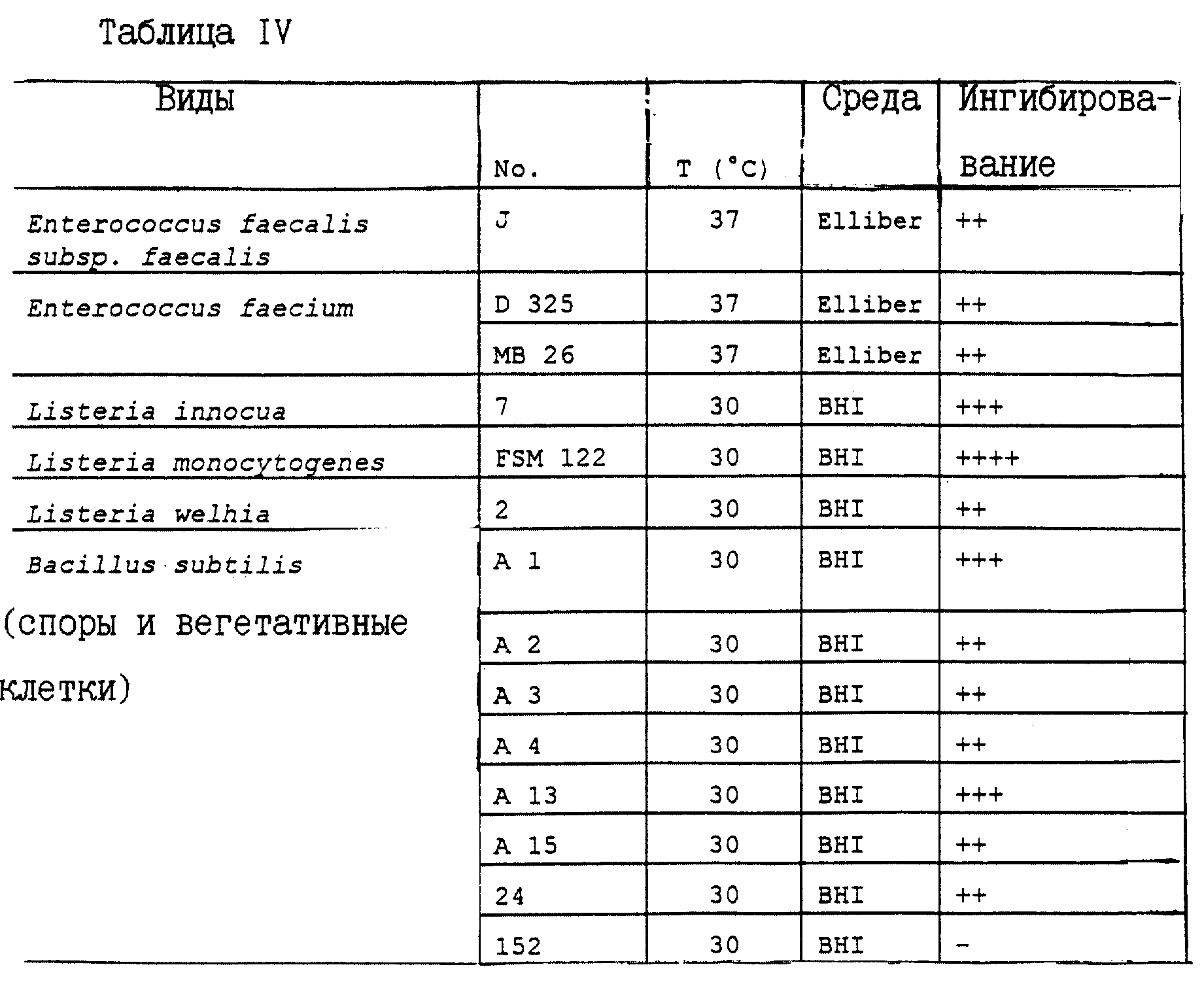
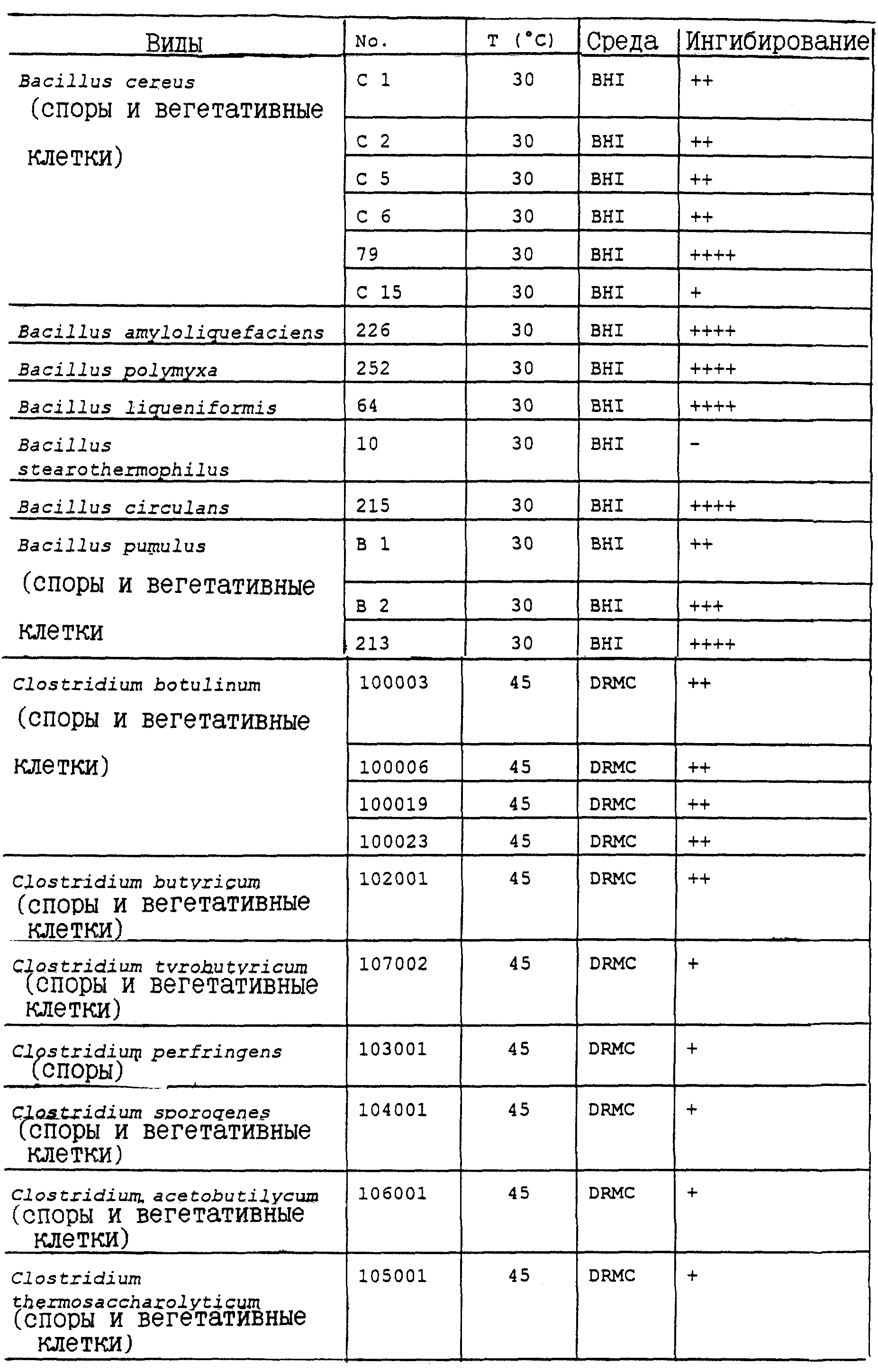
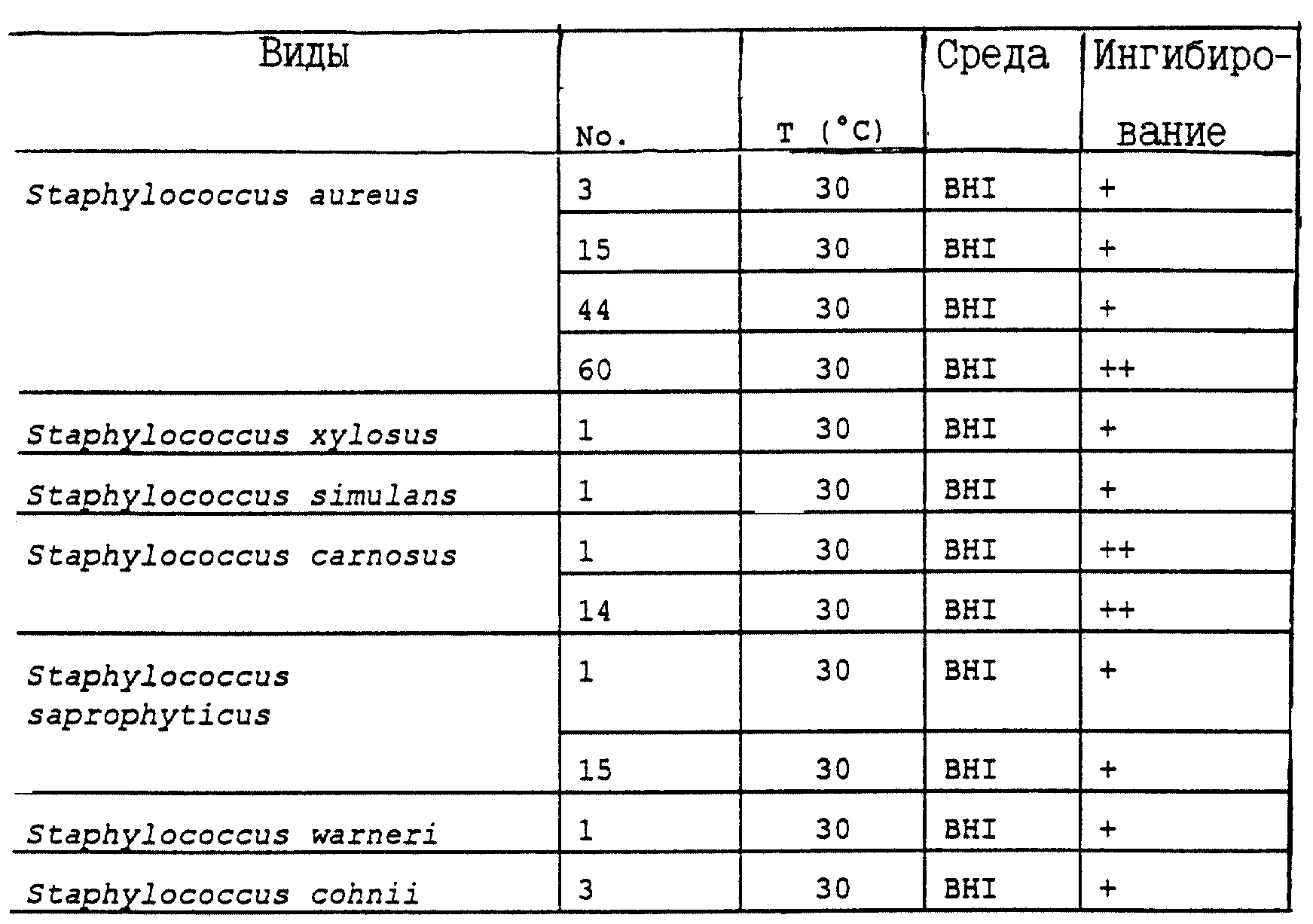
Спектр ингибирования культурального супернатанта, продуцирующего вариации настоящего изобретения также рассматривается как широкий, поскольку он не ограничивается видами молочнокислых бактерий, а включает, как видно из представленных в табл. IV результатов, также другие виды грам-положительных бактерий, в частности, нежелательные или патогенные бактерии, такие, как Listeria innocua, Listeria welhia, Listeria monocytogenes и споры, например. Bacilli, как видно из табл. IV.
Приведенные в табл. IV результаты позволяют предположить возможность использования описываемого супернатанта или очищенного вариацина как добавку при изготовлении пищевых продуктов, которая будет выполнять роль агента, активного против патогенных бактерий, в частности, против Clostridia, в мясных продуктах, против Listeria monocytogenes в сырах, против Bacillus cereus и Listeria в десертных муссах, или против Bacilli в свежих паштетах или соусах для свежих паштетов, от которых произошли указанные штаммы бактерий.
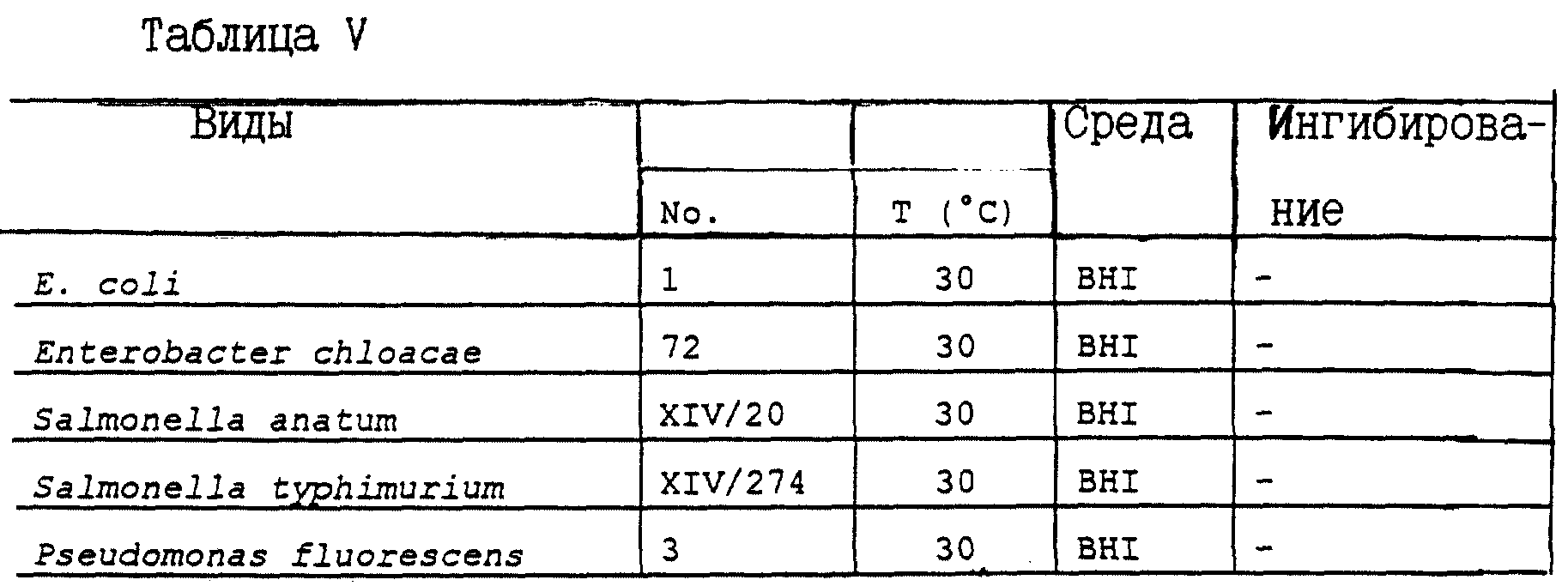
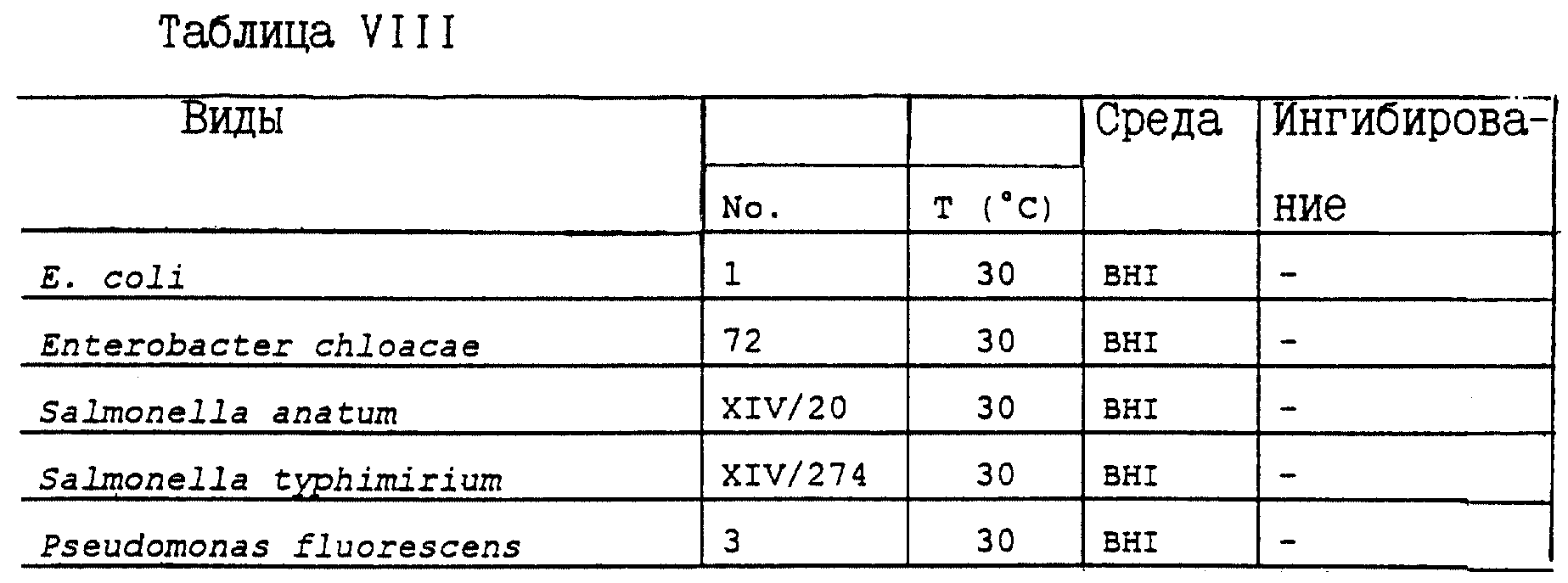
И, наконец, как можно видеть из результатов, приведенных в табл. V, вариации не оказывает какого-либо ингибирующего эффекта на рост грам-отрицательных бактерий.
Спектр ингибирования концентрата супернатанта, содержащего вариацин
Процедура совпадает с
описанным выше методом, за исключением того, что определяют ингибирующий эффект концентрата супернатанта, полученного по методу примера 2, на рост различных штаммов спор и бактерий.
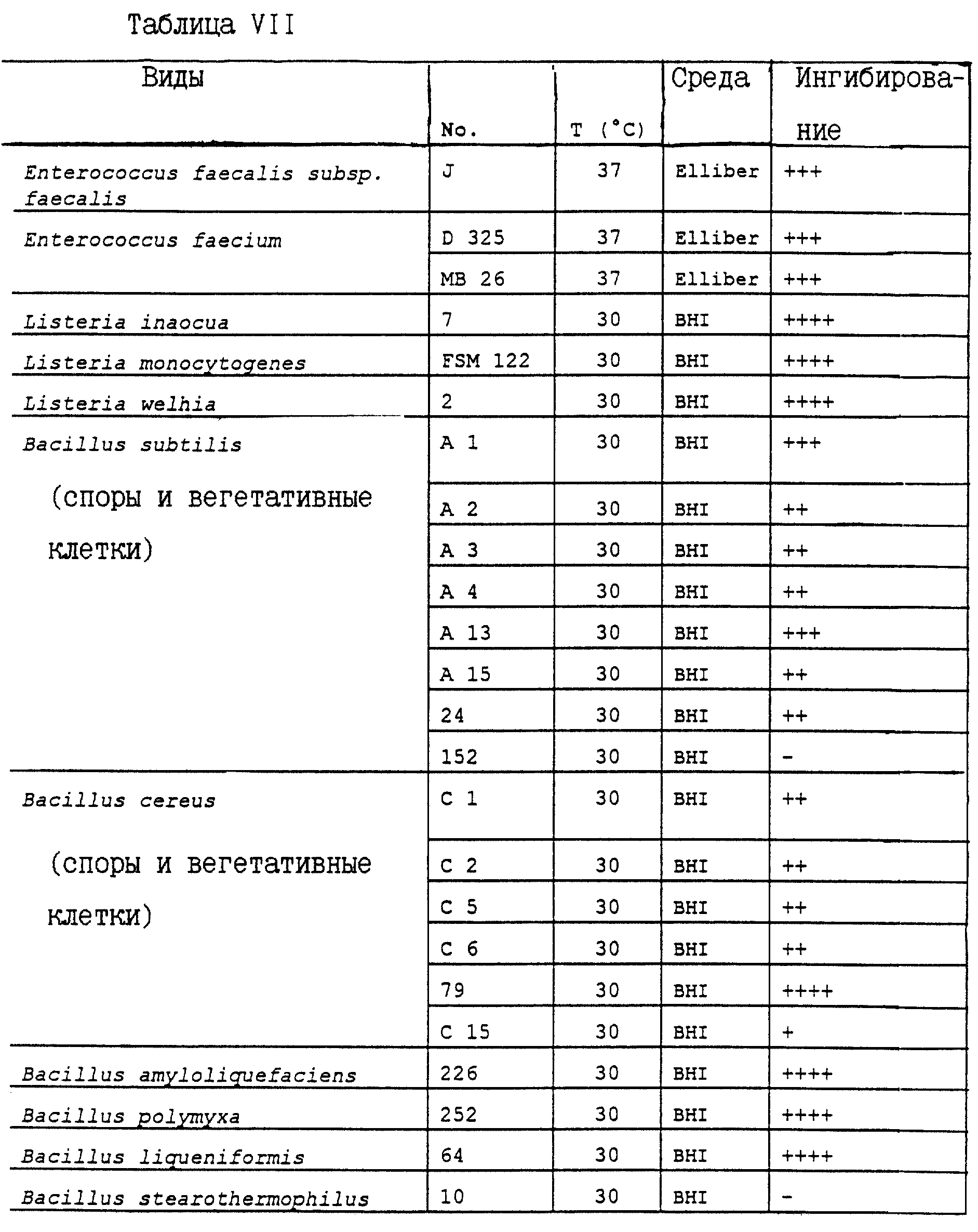
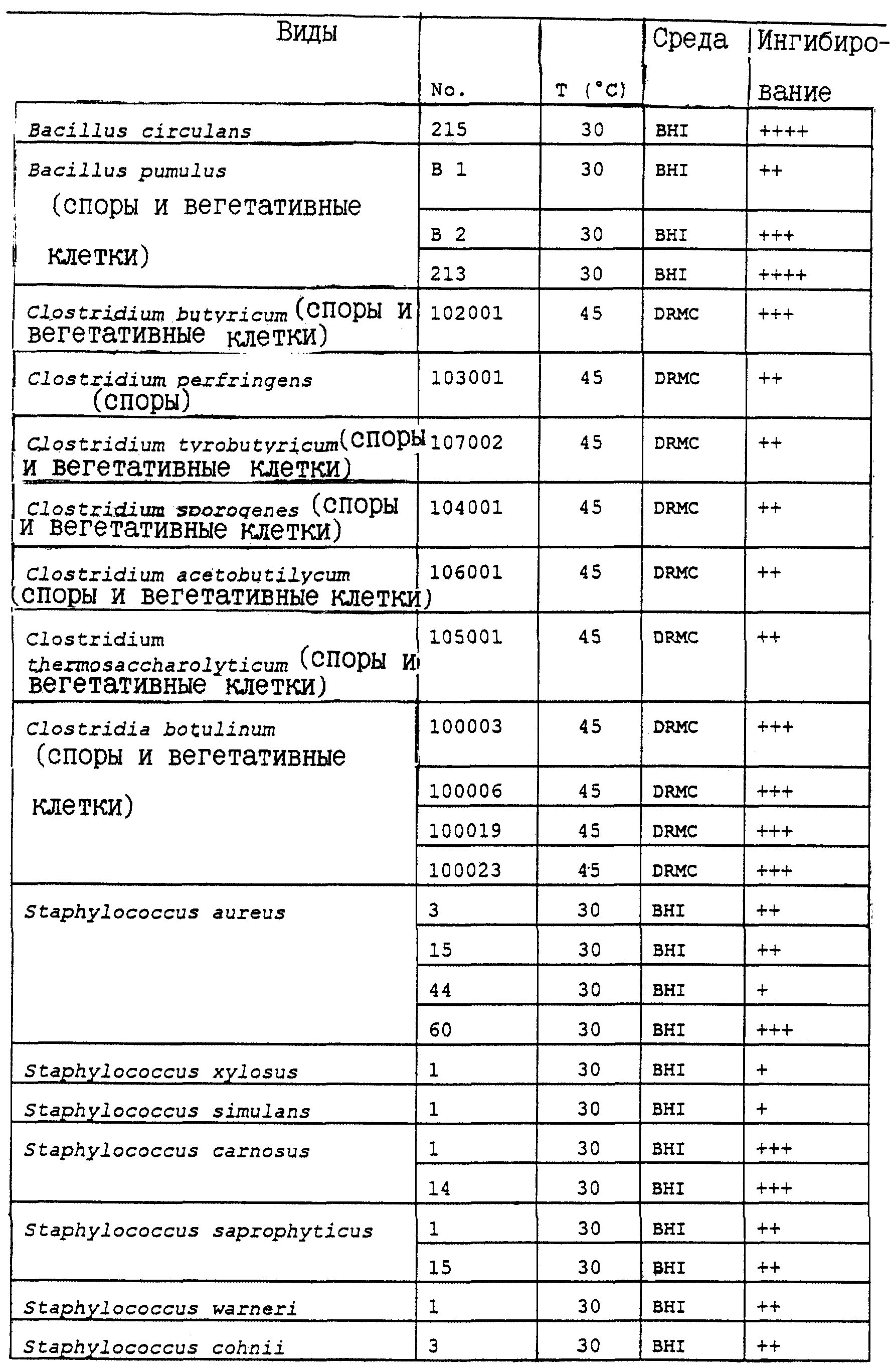
Исследуют те же виды и подвиды, что и ранее. Результаты тестов приведены в табл. VI, VII и VIII. Указанное обозначение штамма или его номер соответствуют номеру, присвоенному данному штамму в Коллекции микроорганизмов Нестле, Швейцария (Nestle, Адрес: NESTEC S.A. Centre de Recherche, Verz-chez-les-Blanc, CH-lOOO Lausanne 26, Switzerland). Указанная температура относится к температуре инкубации, поддерживаемой в ходе тестирования. Указанная в таблицах среда относится к стандартной среде, благоприятной для роста исследуемого штамма.
Результаты, приведенные в табл. VI, VII и VIII, свидетельствуют о повышенной эффективности концентрата супернатанта по сравнению с супернатантом при ингибировании роста многих исследованных штаммов. При этом спектр ингибирования отмечается для тех же видов и подвидов, но характеризуется большим уровнем ингибирования.
Приведенные данные позволяют предположить целесообразность получения, по методу примера 2, концентрата супернатанта, содержащего вариацин, и его применения для борьбы против патогенных бактерий при приготовлении, например, пищевых продуктов и косметики.
Устойчивость к pH
Для определения того, является ли вариацин, выделенный по способу настоящего изобретения, pH-зависимым, применяют также агаровый тест.
В этом случае на агар наносят индикаторный штамм с соблюдением всех условий, описанных в разделе "агаровый тест". В качестве индикаторного штамма используют Lactobacillus helveticus (N2).
pH экстракта концентрата культурального супернатанта, описанного в примере 2, доводят до значения от 2 до 10 с по мощью 2н NaOH и/или 2н HCL, экстракт инкубируют при температуре 37oC в течение 60 минут, после чего значение pH вновь доводят до 6-7, и затем в агаровую лунку вносят образец экстракта для проведения агарового теста.
Параллельно проводят исследование контроля с использованием того же концентрата супернатанта при pH 7, который инкубируют при температуре 37oC в течение 60 минут и затем контрольный образец вносят в агаровую лунку с тем, чтобы сравнить зоны ингибирования исследуемых образцов и контроля. Диаметр зоны подавления контроля составляет 27 мм.
В табл. IX, а также в табл. X и XI число 27 указывает на наличие зоны ингибирования размером 27 мм, что свидетельствует о полной бактерицидной активности вариацина.
Приведенные в табл. IX результаты показывают, что бактерицидная активность бактериоцина не подавляется. Поэтому можно сделать вывод о том, что бактерицидная активность вариацина не зависит от pH.
Устойчивость к нагреванию
Для определения того, является ли вариацин, выделенный по способу
настоящего изобретения, температурозависимым, применяют также агаровый тест.
В этом случае на агаре выращивают индикаторный штамм, с соблюдением всех условий, описанных в разделе "агаровый тест". В качестве индикаторного штамма используют Lactobacillus helveticus (N2).
Экстракт концентрата культурального супернатанта, описанного в примере 2, доведенный до pH 7, инкубируют при температуре 100oC в течение периода времени от 15 до 60 минут, после чего значение pH доводят до 6-7 и затем в агаровую лунку вносят образец экстракта для проведения агарового теста.
Параллельно проводят исследование контроля с использованием того же концентрата супернатанта при pH 7, который также инкубируют при температуре 37oC в течение 60 минут и затем в агаровую лунку вносят контрольный образец. Проведенные процедуры позволяют провести сравнение зон подавления исследуемых образцов с зоной контроля. Диаметр зоны ингибирования контроля составляет 27 мм.
Приведенные в табл. X данные указывают на то, что активность вариацина не зависит от температуры. Так, бактерицидная активность вариацина не подавляется даже после 60-минутной инкубации при температуре 100oC.
Устойчивость вариацина к нагреванию является весьма важной его биохимической характеристикой, которая имеет значение для использования его при получении пищевых продуктов и косметики. Так, вариации можно использовать в виде грубого экстракта или в очищенном виде при получении, например, пастеризованных пищевых продуктов, с тем, чтобы предохранить их от прорастания спор, в частности Bacilli, которые являются термотолерантными.
Устойчивость к нагреванию и pH
Активность вариацина исследуют, кроме того, при сочетании воздействия двух факторов: pH и температуры.
В этом случае на агаре выращивают индикаторный штамм, с соблюдением всех условий, описанных в разделе "агаровый тест". В качестве индикаторного штамма используют Lactobacillus helveticus (N2).
Экстракт концентрата культурального супернатанта, описанного в примере 2, доведенный до pH 4 или 7 с помощью 2н HCl и/или 2н NaOH, инкубируют при температуре 115oC в течение 20 минут, после чего значение pH доводят вновь до значения 6-7 и вносят в агаровую лунку образец экстракта для проведения агарового теста.
Параллельно проводят исследование контроля, имеющего pH 7, который инкубируют при температуре 37oC в течение 20 минут и затем в агаровую лунку вносят контрольный образец, с тем, чтобы сравнить зоны ингибирования исследуемых образцов с зоной контроля. Диаметр зоны ингибирования контроля составляет 27 мм.
Приведенные в табл. XI результаты показывают, что бактерицидная активность вариацина не подавляется при pH 4 или 7 в случае сочетания pH-фактора с повышением температуры.
Очистка
вариацина
В 4 л BHI среды инокулируют культуру Micrococcus varians, которая продуцирует вариацин настоящего изобретения. Указанную стандартную культуру инкубируют при температуре
30oC в течение ночи в аэробных условиях при качании, после чего ее центрифугируют при 5000 g, а супернатант собирают в приемный сосуд, в который добавляют 72 г смолы XAD-7 (Амберлит
(R)).
Смесь перемешивают при температуре 25oC в течение 30 минут для облегчения адгезии молекул вариацина со смолой и затем все вместе переносят в сосуд из спекшегося стекла, после чего под вакуумом отфильтровывают супернатант.
Смолу последовательно промывают в 3 буферах, содержащих 20 мМ цитрата натрия, pH 4 и изопропанол. При этом первый буфер содержит 10% изопропанола, второй буфер содержит 15% изопропанола и третий буфер содержит 20% изопропанола.
Смолу переносят на колонку, после чего проводят элюцию вариацина с помощью 700 мл буфера, содержащего 20 мМ цитрата натрия, pH 4 и 25% изопропанола. Постоянно осуществляют мониторинг бактерицидной активности с помощью описанного выше агарового теста.
Смешивают активные фракции и выпаривают изопропанол. Подготавливают 5 мл S-Ресурсную (S-Resourse) колонку для ВЭЖХ [Фармация (Pharmacia)], уравновешивая ее 20 мМ натрий-цитратным буфером. Упаренную смесь активных фракций наносят на колонку, после чего проводят элюцию содержимого колонки NaCI-буфером в градиенте от 100 до 400 мМ.
Собирают фракции и с помощью агарового теста проверяют бактерицидную активность очищенного таким образом вариацина.
Секвенирование вариацина N-терминальный участок вариацина, выделенного из штаммов CNCM I-1586 и CNCM I-1587 и затем очищенного, секвенируют с использованием автоматизированного секвенатора Эпплайд Байосистемз 4774 (Applied Biosystems 4774).
В результате анализа было выявлено, что пептидная последовательность из 5 аминокислот идентична таковой на N-конце последовательности SEQID No: 1, приведенной ниже в перечне последовательностей.
Не представилось возможным в ходе секвенирования продемонстрировать наличие пептида, состоящего более чем из 5 аминокислот.
Кроме того, вариацин, выделенный из штаммов CNCM I-1586 и CNCM I-1587 и впоследствии очищенный, гидролизуют под действием 6н HCl в течение 10 минут. При этом были получены 3 пептида, которые анализируют обычным способом с использованием ВЭЖХ. Оказалось возможным провести секвенирование только одного из трех выделенных пептидов, поскольку два других, по всей видимости, включают модификации пептидов.
Последовательность выделенного таким образом пептида оказалась идентичной участку, включающему аминокислоты с 19 по 22 в последовательности SEQ ID No: 1, приведенной ниже в списке последовательностей.
И, наконец, фракция, содержащая вариацин, выделенный и впоследствии очищенный из штаммов CNCM I-1586 и CNCM I-1587, исследуют методом масс-спектрометрии, в результате чего был определен молекулярный вес вариацина, равный 2659 дальтон.
Гомология
Между последовательностями лактицина 481 из Lactococcus lactis и вариацина настоящего изобретения наблюдалась гомология. Гомология касается, в частности,
последовательностей
N-концевых участков обоих бактериоцинов. Так, последовательность от 1 до 5 аминокислоты на N-концевом участке вариацина идентична участку от 3 до 7 аминокислоты в
последовательности SEQ ID No: 8
лактицина 481, который будет описан ниже в перечне последовательностей. Тем не менее описанное явление относится только лишь к области частичной гомологии, но не
идентичности.
Кроме того, как было показано с помощью масс-спектро-метрического анализа, секретируемый лактицин имеет молекулярный вес, равный 2900 дальтон, тогда как молекулярный вес секретируемого вариацина, как уже упоминалось, составляет 2659 дальтон.
В случае инокулирования по методу, описанному ранее в тесте на определение спектра ингибирования, в присутствии экстракта вариацина, штамма Lactococcus lactis, продуцирующего лактицин 481, видно, что рост упомянутого штамма ингибируется. Штамм Lactococcus lactis, продуцирующий лактицин 481, обладает иммунитетом к своему собственному бактериоцину-лактицину 481, однако, он не иммунен к вариацину, продуцируемому одним из двух штаммов Micrococcus varians настоящего изобретения. Таким образом, результаты, полученные с использованием вышеописанного теста на определение спектра ингибирования, подтверждают представление о том, что оба указанных бактериоцина различаются.
Приведенные выше генетические данные показывают, что, несмотря на то, что лактицин 481 и вариации проявляют гомологию последовательностей, их последовательности не идентичны. Биохимические и микробиологические данные подтверждают представление о том, что лактицин 481 и вариации являются двумя различными бактериоцинами.
Секвенирование гена
вариацина
Дегенеративную нуклеотидную последовательность SEQ ID No: 4, которая
описана ниже в перечне последовательностей и которая соответствует С-концевому участку пептида в
секвенированном ранее вариацине, конструируют известным способом. Затем смесь последовательностей SEQ
ID No: 4 радиоактивно облучают при участии полинуклеотидкиназы из Т4.
Традиционным способом получают препарат хромосомной ДНК из штаммов CNCM I-1586 и CNCM I-1587. Упомянутый препарат ДНК подвергают перевариванию ферментами SalI, SacI, Sphi и BamHI в соответствии с рекомендациями, данными в инструкции поставщика. После этого на агарозный гель наносят 2 мкг продукта переваривания. Находящуюся в геле ДНК промывают 250 мМ HCl, после чего продукт перемещения переносят в щелочной среде из геля на мембрану "Зетапроба" (Биорад) ["Zetaprobe" (Biorad)]. После этого мембраны "Зетапроба" подвергают предварительной гибридизации при температуре около 55oC при последующем снижении указанной температуры на 5oC каждые 2 часа до температуры 40oC в среде, содержащей 6 х SSC раствор хлорида и цитрата натрия, 1% ДСН (SDS) и 0, 25% снятого молока. Указанную мембрану далее гибридизируют с дегенеративной радиоактивной пробой, представляющей собой последовательность SEQ ID No: 4 в описанной ранее гибридизационной среде и при тех же температурных условиях. После этого смесь оставляют для инкубации при температуре 40oC в течение 4 часов, затем мембрану промывают при температуре 40oC в 6 х SSC. И наконец, ее наносят на пленку для ауторадиографии при - 80oC в течение 16 часов.
Результаты гибридизации демонстрируют наличие множества полос миграции: SalI полоса размером 7 т.п.н., SacI полоса размером 1,4 т.п.н., BamHI полоса размером 1,8 т.п.н. и SphI полоса размером более 15 т.п.н.
Затем 5 мкг геномной ДНК из штамма CNCM I-1586 расщепляют рестрикционным ферментом BamHI и отделяют фрагмент размером 1,6-2 т.п.н. хроматографией в геле агарозы с последующей элюцией той части геля, которая включает нужный фрагмент. Элюированный фрагмент ДНК лигируют с вектором рК19 (Gene, 56 (1987) 309-312), который был перед этим переварен BamHI и затем обрабатывают фосфатазой из кишечника теленка [Берингер Маннгейм (Boehringer Mannheim), часть N 713032].
Затем традиционным способом проводят трансформацию Escherichia coli, штамм BZ 234 [Коллекция Биоцентрум, (Blocentrum collection), Базельский Университет, Швейцария] , который является компетентным, средой для лигирования. Клоны, содержащие вставку, идентифицируют на агаровой среде, содержащей 50 мкг/мл канамицина, 60 нг/мл IPTG (изопропилтиогалактозида) (Берингер Маннгейм, N 724815) и 300 нг/мл Х-гал (5-бром-4-хлор-3- индолил-β-D-галактозида) (Берингер Маннгейм, часть N 651745), которую инкубируют при температуре 37oC в течение 16 часов.
Белые колонии, которые обычно содержат вставку, вносят на 96-гнездное микротитрационное плато. При этом каждую белую колонию помещают в одно гнездо плато, которое содержит, кроме того, 150 мкл LB среды с добавлением 50 мкг/мл канамицина и инкубируют при температуре 37oC в течение 20 часов для продуцирования мини-культур.
Готовят также праймеры противоположной ориентации, поскольку ориентация гена в векторе рК19 не известна. В этом случае указанные праймеры получают за счет лигирования нуклеотидного фрагмента, описываемого последовательностью SEQ ID No: 5, частично кодирующего лактицин 481, с одной или другой универсальной пробой pUC векторов, которые представляют собой соответственно последовательность SEQ ID No: 6 или последовательность SEQ ID No: 7.
1 мкл содержимого из каждой ячейки смешивают со 100 пмолями одного из указанных праймеров, 6 мкл 2 мМ дНТФ и 2,5 мкл Taq буфера (Р.Н. Stehelin & Cie AG, кат. No TP05b), после чего на всю полученную смесь наносят каплю Дина-вакс (Финнзимес Ой, 02201 Эспоо, Финляндия) (Dyna-wax, Finnzymes Оу, 02201 Espoo) и нагревают при температуре 98oC в течение 10 минут для лизиса бактерий; затем проводят полимеразно-цепьевую реакцию (ПЦР).
Далее осуществляют гель-электрофорез, в ходе которого позитивные клоны дают полосу размером 800 п.н.
С помощью описанного способа отбирают позитивные клоны и затем экстрагируют из этих клонов плазмидную ДНК; после этого дидезоксинуклеотидным методом секвенируют фрагмент ДНК, клонированный в вектор рК 19, с использованием набора для секвенирования [Фармация Биотех (Pharmacia Biotech), часть No. 27-1682-01] и универсальных праймеров, после которых на основании данных, характеризующих полученную последовательность, используют специфичные праймеры.
В результате проведенного исследования получают нуклеотидную последовательность SEQ ID No: 2, приведенную ниже в перечне последовательностей. Упомянутая нуклеотидная последовательность кодирует последовательность SEQ ID No: 1, которая соответствует аминокислотной последовательности вариацина до созревания.
Приведенные ниже примеры служат целям иллюстрации способа получения и использования бактериоцина в соответствии с настоящим изобретением. Если нет других оговорок, указанные в примерах проценты означают весовые проценты.
Пример 1
В BHI среду инокулируют культуру,
содержащую штамм Micrococcus varians. Проводят
инкубацию в течение ночи при температуре 30oC при качании в аэробных условиях, что приводит к получению культуры, содержащей 108
организмов выращиваемого штамма на 1 мл среды.
Полученную таким образом стандартную культуру центрифугируют. А стандартный супернатант собирают.
Пример 2
На основе 750 мл
вышеупомянутого супернатанта, полученного по
методу примера 1, готовят концентрат супернатанта, к которому добавляют 15 г смолы XAD-7 (Амберлит (R)). Смесь перемешивают при температуре 4oC
в течение 60 минут и затем фильтруют через
фильтр No. 604 (Schleicher & Schuell, Германия). Затем для удаления всех неадсорбированных белков фильтр промывают 1% цитратом натрия. Смолу отделяют
и переносят в приемный сосуд, содержащий
цитрат натрия и перемешивают всю полученную смесь в течение 2 минут. После этого смолу вместе с цитратом натрия переносят на колонку и элюируют цитрат натрия
50% ацетонитрилом и 0,1% ТФУ
(Трифторуксусная кислота). Элюат выпаривают, а остаток ресуспендируют в 50 мМ фосфатном буфере при pH 6,8.
Пример 3
При культивировании на ВН1
среде в течение ночи при
температуре 30oC при качании в аэробных условиях получают 10 л культуры штамма Micrococcus varians. Затем непосредственно к культуре добавляют 200 г смолы XAD-7
(Амберлит) и все несильно
перемешивают при температуре 4oC в течение 1 часа. После этого смесь фильтруют через фильтр No. 604 (Schlelcher & Schuell, Германия), а смолу, оставшуюся на
фильтре, промывают 10 л
50 мМ раствора уксусной кислоты, pH 5,2, для удаления бактерий. После этого к смоле добавляют 450 мл раствора, содержащего 100% этанол и 20 мМ ацетат аммония, и фильтруют всю
полученную смесь для
удаления смолы; затем фильтрат лиофилизуют с получением порошка, содержащего вариации настоящего изобретения, который может быть далее использован в пищевой промышленности.
С помощью описанного ранее агарового теста определяют бактерицидную активность полученного порошка, который предварительно развели водой. Указанный порошок проявляет активность не менее 105 уе/г порошка.
И, наконец, вышеупомянутый порошок добавляют в дозе 0,5 г/кг к получаемой традиционным способом мясной пене. В результате мясная пена содержит 50 ye
бактериоцина в расчете
на 1 г пены, и этого количества достаточно для полного ингибирования развития в ней патогенных бактерий, в частности Clostridia
Пример 4
Данный пример
относится к получению
увлажняющего крема для ухода за кожей, который содержит порошок, описанный в примере 3, в дозе 0,05 г/кг, который представляет собой вариацин, способный при активности 5 уе/г
ингибировать развитие на
коже нежелательных бактерий, таких как Staphylococcus aureus и Streptococcus pyogenes.
Для приготовления указанной среды смешивают компоненты липидной фазы А и нагревают при температуре 75oC. Готовят липидную фазу Б и также нагревают при температуре 75oC медленно, при помешивании, добавляют липидную фазу А, затем все содержимое, также при медленном помешивании, охлаждают до температуры окружающей среды, что соответствует примерно 25oC. Медленно, при этой же температуре, в порядке, указанном ниже, добавляют составляющие смеси В.
Жидкая фаза A - %
G"U-6 стеарат, глицерат и ПЭГ-20-цетиловый эфир (ПЭГ-полиэтиленгликоль) - 15
Жидкий парафин - 5
Масло из проростков пшеницы,
стабилизированное
0,1% фенилинданом (антиоксидантом) и 1% соевым фосфолипидом (см. EP94109355.1) - 3
Масло из сладкого миндаля - 2
Цетиловый спирт - 1
Изостеарил изостеарат
- 2
2-Октилдодецил миристат - 1
Ланолиновый воск - 1
Водная фаза Б - %
Meтилизотиазолин - 0,1
Деминерализованная вода - 59,6
Плацентарный белок
человека
- 2
В Добавки - %
Пропиленгликоль и экстракт календулы - 2
50%-ный растворимый коллаген в деминерализованной воде - 5,8
Парфюмерная отдушка - 0,3
2,5%
порошок бактериоцина, полученный по методу примера 3, в деминерализованной воде - 0,2
Пример 5
Описанный в примере 3 порошок бактериоцина добавляют в количестве 0,5 г/кг к
средству
для полоскания ротовой полости. Указанное средство приобретает в результате этого способность ингибировать развитие патогенных бактерий, в частности Streptococcus sorbinus. Streptococcus
sanguis,
Streptococcus mutans и Actinomyces viscosus в ротовой полости.
Пример 6
Раствор, включающий порошок бактериоцина, полученный по методу примера 3, разбавляют водой до
1%-ной
концентрации и разбрызгивают на пищевые продукты, которые подлежат стерилизации для предупреждения вторичной контаминации в процессе упаковки.
Реферат
Изобретение относится к биотехнологии и касается бактериоцина из Micrococcus varians, нуклеотидного фрагмента, кодирующего бактериоцин, штаммов Micrococcus varians CNCM 1-1586 и CNCM 1-1587, продуцирующих указанный бактериоцин, а также способа получения бактериоцина и его применения для получения пищевых продуктов и косметики в качестве агента, активного против патогенов. Бактериоцин настоящего изобретения обладает мощным бактерицидным эффектом, а также имеет более широкий спектр ингибирования различных бактериальных штаммов. 6 с. и 8 з.п. ф-лы, 11 табл.

Комментарии