Применение lactobacillus для лечения вирусных инфекций - RU2440123C2
Код документа: RU2440123C2
Чертежи











Описание
Область техники, к которой относится изобретение
Настоящее изобретение относится к применению по меньшей мере одного штамма пробиотических бактерий, выбранных из Lactobacillus, для производства фармацевтической композиции для лечения и/или предотвращения вирусной инфекции.
Уровень техники
Пробиотические бактерии представляют собой живые микроорганизмы, которые при применении в адекватных количествах, оказывают полезное воздействие на реципиента. Наиболее часто используемыми бактериями в пробиотических продуктах являются Lactobacilli и bifidobacteria. Эти бактерии в целом безопасны, как и пробиотики на основе этих организмом. Отсутствие патогенности распространяется на все возрастные группы и для индивидуумов с ослабленным иммунитетом. При приеме различных пробиотических бактерий были показаны благоприятные клинические воздействия при различных физиологических или патологических случаях. Самые ярко выраженные побочные эффекты выражались в диарее, вызванной терапией антибиотиками или ротавирусной инфекцией. Также есть исследования, в которых были показаны положительные клинические эффекты при воспалительных заболеваниях кишечника, атопическом дерматите и гиперхолестеринемии после приема пробиотических бактерий. Механизм действия пробиотических бактерий в отношении этих клинических улучшений не ясен. Исследования in vitro в отношении человека, а также in vivo и in vitro в отношении животных показали, что различные виды lactobacilli воздействуют по-разному на врожденную и приобретенную иммунную систему. В основном, клинические исследования показали стимуляцию врожденной клеточной иммунной системы и усиление гуморальных иммунных реакций на спонтанные инфекции и системную или пероральную иммунизацию. Что касается влияния на врожденную иммунную систему, то были сообщения об усиленной фагоцитарной активности полиморфнонуклеарных клеток (PMN) и усиление противоопухолевой активности NK-клеток (натуральных киллеров). Сведения о клинических исследованиях, в которых продемонстрированы воздействие на специфическую клеточную иммунную систему после приема пробиотических бактерий, отсутствуют.
В соответствии с настоящим изобретением было детально исследовано воздействие на врожденную и приобретенную иммунную систему ежедневного приема lactobacilli или грамотрицательных бактерий P.Lundensi. Интересно, что наблюдали активацию специфической клеточной иммунной системы у субъектов, получающих L.plantarum, и такие признаки у субъектов, получающих L.paracasei. Кроме того, у субъектов, получающих различные виды lactobacilli, наблюдали усиливающие иммунитет воздействия на врожденную иммунную систему, такие как увеличение популяции NKT клеток и усиление фагоцитарной активности. При этом введение грамотрицательных бактерий P.lundensis не оказало влияния на различные иммунные параметры, измеренные в ходе экспериментов, описанных здесь.
Усиливающийся интерес к пробиотикам, как альтернативным средствам, возник с развитием устойчивости к антибиотикам и расстройств при различном лечении инфекций. Возникла потребность в пробиотических функциональных пищевых продуктах для целвого решения проблем простуды. Это явно следует из большого количества случая простудных инфекций каждый год. Обычно, для уменьшения числа случаев простуды, применяли пищевые продукты с высоким содержанием витамина С. На рынке представлен широкий ряд таких продуктов, влияющих на иммунную систему.
Цель настоящей заявки заключается в исследовании, может ли пробиотический функциональный пищевой продукт после регулярного введения воздействовать на симптомы простуды подобным способом и, таким образом, может ли быть альтернативным решением для этой проблемы общества.
Краткое описание изобретения
Объектом настоящего изобретения является применение по меньшей мере одного штамма пробиотических бактерий, выбранных из Lactobacillus, для производства фармацевтической композиции для лечения и/или предотвращения вирусной инфекции.
Другим объектом по настоящему изобретению является способ лечения и/или предотвращения вирусной инфекции, в котором по меньшей мере один штамм пробиотических бактерий, выбранный из Lactobacillus, вводится индивидууму.
Краткое описание фигур
На фигуре 1 показано количество добровольцев, сообщающих о любых незначительных неблагоприятных желудочно-кишечных воздействиях во время исследования.
На фигуре 2 показано начальное количество (день 0) различных лимфоцитов на мл крови (среднее значение±(SEM (стандартная ошибка среднего))).
На фигуре 3 показано начальное (день 0) процентное содержание или GMFI (среднее значение±(SEM)) лимфоцитов, положительных к различным активаторам клеток и маркерам памяти.
Фигура 4. Субъектов в произвольном порядке разделили на девять различных исследуемых групп. Исследование начинали с двухнедельного периода вымывания. После этого проводили активный период исследования. В течение этого периода субъекты потребляли одну дозу исследуемого продукта в сутки в течение 14 (группы L.plantarumHeal19, L.fermentum, L.paracasei, L.gasseri, L.rhamnosus, P.Lundensis) или 35 дней (группы L.plantarum 299v и плацебо). Каждая доза содержала 1010 колониеобразующих единиц (КОЕ) (группы lactobacilli) или 109 КОЕ бактерии (группа P.lundensis).
Фигура 5. Процентное содержание лимфоцитов, экспрессирующих фенотипы активации CD8CD25, CD8HLA-DR, CD4CD25 и CD4HLA-DR, анализировали проточной цитометрией. Показано среднее для группы (±SEM) по отдельным соотношениям день 14/день 0 и день 35/день 0 (только для групп L.plantarum и плацебо).
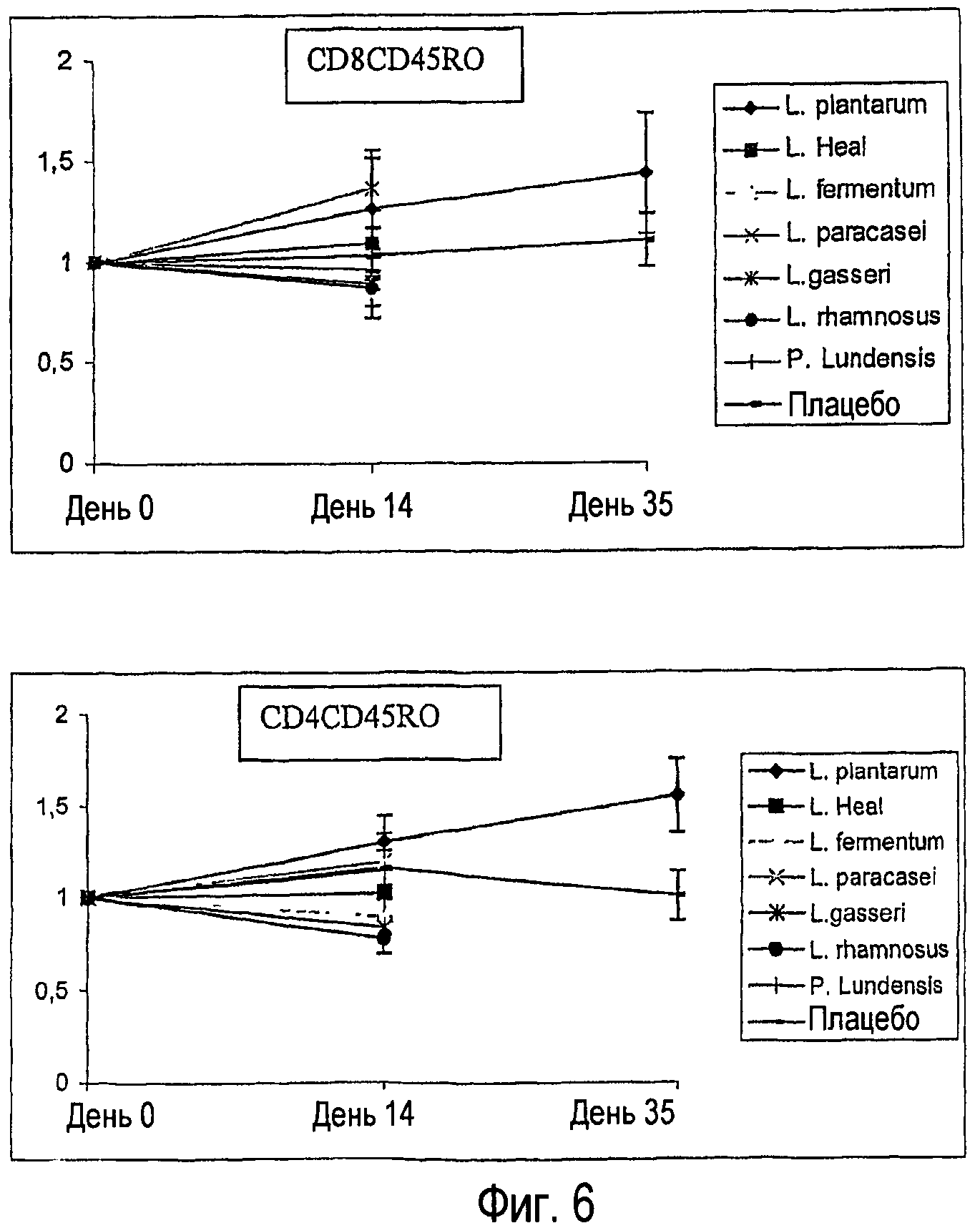
Фигура 6. Процентное содержание лимфоцитов, экспрессирующих фенотипы памяти CD8CD45RO и CD4CD45RO, анализировали проточной цитометрией. Показано среднее для группы (±SEM) по отдельным соотношениям день 14/день 0 и день 35/день 0 (только для групп L.plantarum и плацебо).
Фигура 7. Процентное содержание положительных лимфоцитов по маркерам NKT- клеток (CD56CD16CD3), анализировали проточной цитометрией. Расчеты для группы проводили по отдельным соотношениям (день 14/день 0).
Фигура 8. Фагоцитарная активность нейтрофилов анализировали, инкубируя клетки цельной крови с FITC-меченными E.coli или S.aureus. Отношение между средними значениями флуоресценции, полученными в 14 день и 0 день, определяли индивидуально, и групповые вычисления показаны на этой фигуре.
На фигуре 9 показано отношение лимфоцитов, эксперессирующих фенотипы активации CD4CD25 в эксперименте 2.
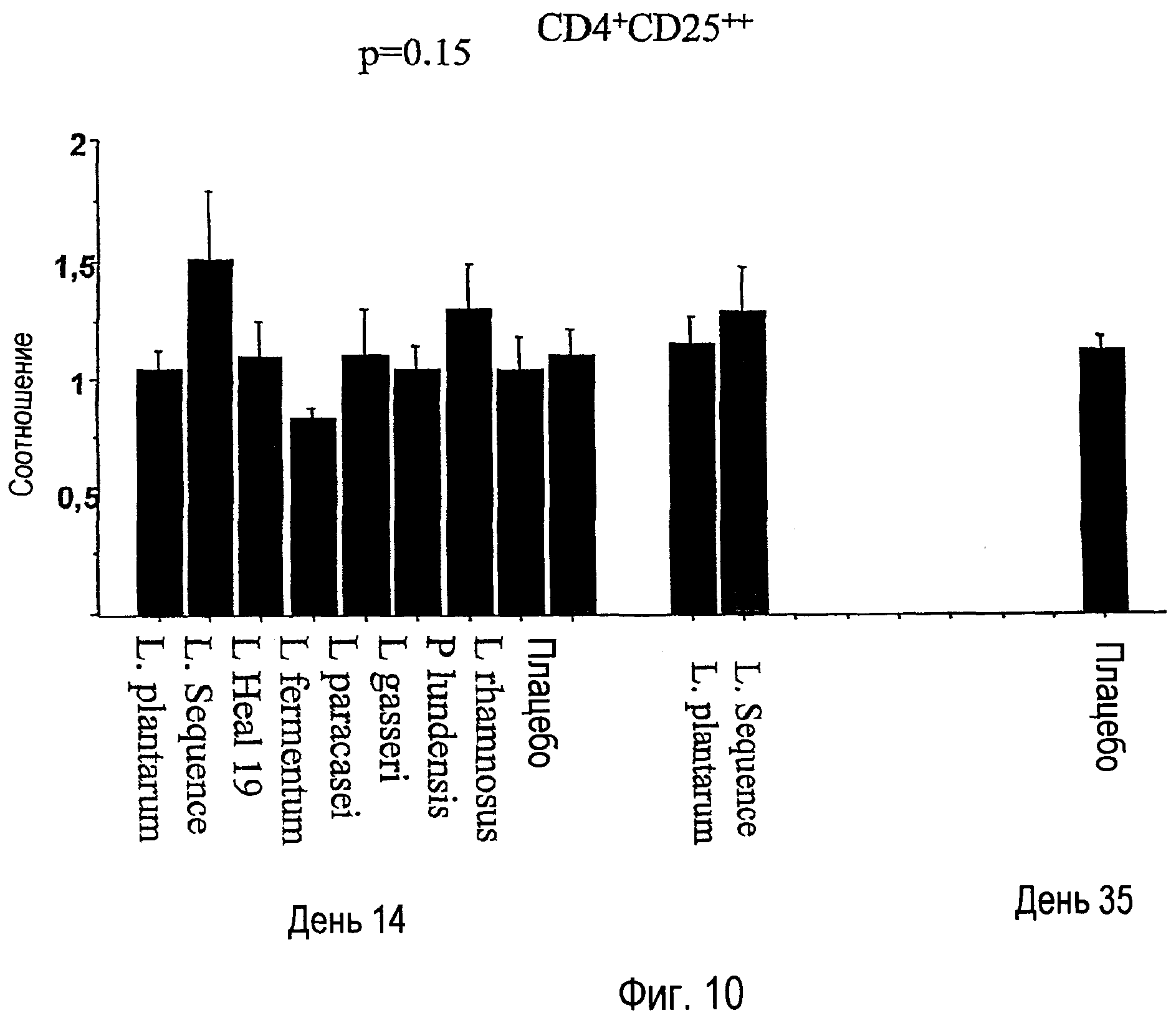
На фигуре 10 показано отношение лимфоцитов, эксперессирующих фенотипы активации CD4+CD25++ в эксперименте 2.
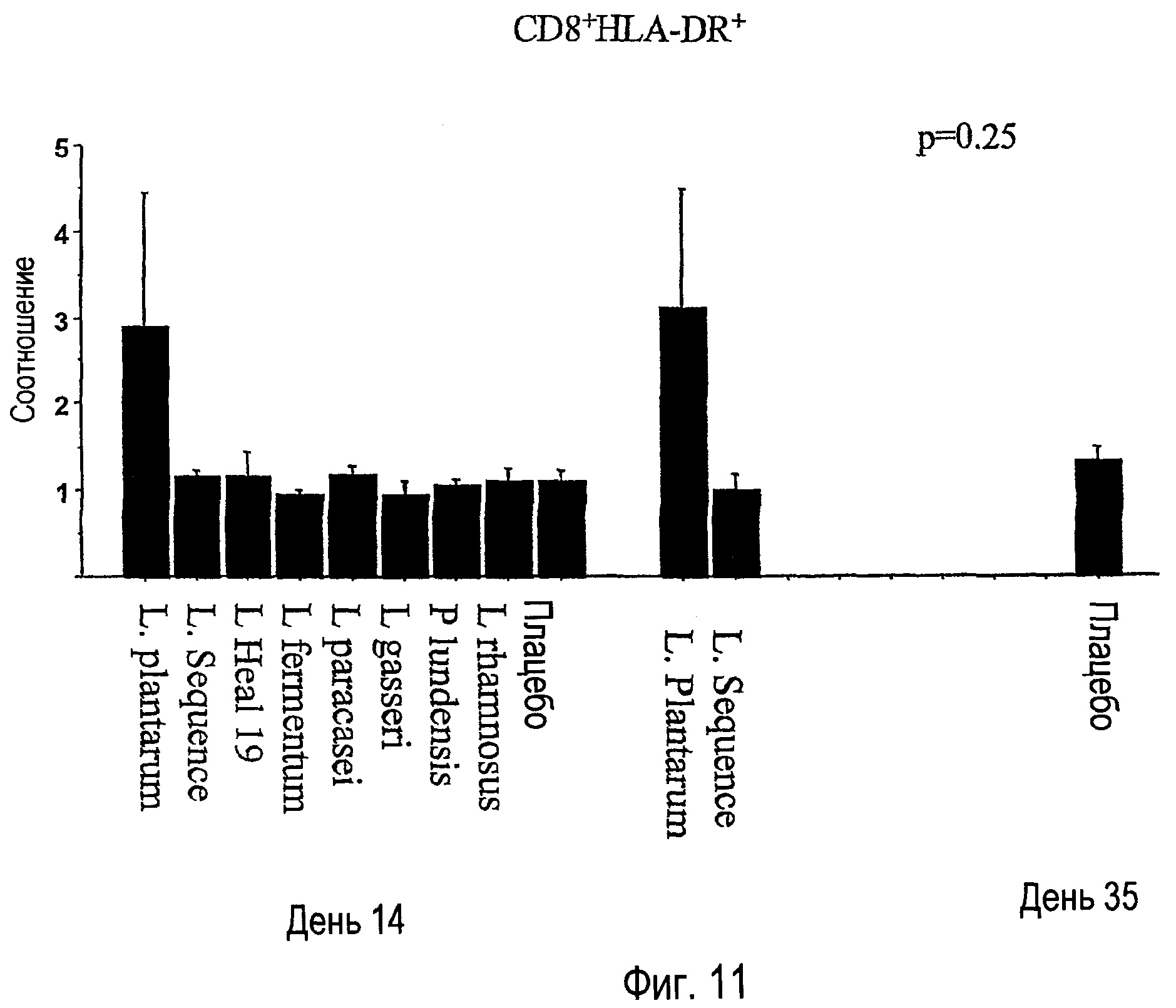
На фигуре 11 показано отношение лимфоцитов, эксперессирующих фенотипы активации CD8+HLA-DR+ в эксперименте 2.
На фигуре 12 показано отношение лимфоцитов, эксперессирующих фенотипы активации CD8+CD25+ в эксперименте 2.
На фигуре 13 показано отношение лимфоцитов, эксперессирующих фенотипы активации CD4CD45RO в эксперименте 2.
Подробное описание изобретение
Lactobacillus, используемые по изобретению, могут быть без ограничения выбраны из группы, состоящей из Lactobacillusplantarum, Lactobacillus rhamnsosus, Lactobacillus fermentum, Lactobacillus paracasei и Lactobacillus gasseri.
Lactobacillus plantarum, используемые по изобретению, могут быть без ограничения выбраны из группы, состоящей из Lactobacillus plantarum 299, DSM 6595, Lactobacillus plantarum 299v, DSM 9843, Lactobacillus plantarum HEAL 9, DSM 15312, Lactobacillus plantarum HEAL 19, DSM 15313 и Lactobacillus plantarum HEAL 99, DSM 15316.
Lactobacillus paracasei, используемые по изобретению, могут быть без ограничения выбраны из группы, состоящей из Lactobacillus paracasei 8700:2, DSM 13434 и Lactobacillus paracasei 02A, DSM13432.
Lactobacillus gasseri, используемые по изобретению, могут быть без ограничения выбраны из группы, состоящей из Lactobacillus gasseri VPG44, DSM 16737.
Естественно, другие пробиотические штаммы бактерий, отличные от конкретно раскрытых здесь, могут быть использованы по настоящему изобретению и включены в объем притязаний изобретения в той мере, пока они обеспечивают требуемое воздействие, то есть оказывают профилактическое действие на вирусную инфекцию или облегчает вирусную инфекцию.
В одном варианте выполнения изобретения в фармацевтической композиции использованы по меньшей мере два штамма пробиотических бактерий. Указанные по меньшей мере два штамма могут вводиться последовательно или одновременно. Таким образом, штаммы могут быть введены в смеси в одной композиции или они могут быть введены последовательно в разных композициях.
Изобретение обеспечивает возможность лечения вирусных инфекций. Вирусные инфекции представляют собой таковые, вызванные вирусом, без ограничения выбранным из группы, состоящей из вируса простого герпеса I, вируса простого герпеса II, вируса опоясывающего герпеса, вируса простуды, риновируса, аденовируса, вируса парагриппа, респираторно-синцитиального вируса, энтеровируса и коронавируса. Любая другая вирусная инфекция, конкретно не указанная здесь, на которую оказывают воздействие пробиотические бактерии, также включена в объем притязаний настоящего изобретения. Известно, что существует множество различных вирусов и их форм, которые вызывают простуду. Все такие вирусы включены в объем притязаний по настоящему изобретению.
В настоящем описании термин "лечение и/или предотвращение" включает профилактическое введение индивидууму, то есть введение пробиотических бактерий было начато до развития заболевания или вирусной инфекции для предотвращения заболевания/инфекция, а также лечение уже развитых у индивидуума заболевания/инфекции. В последнем случае ожидается, например, облегчение симптомов или улучшение общего состояния пациента, или более быстрого выздоровления пациента от заболевания/инфекции. Таким образом, индивидуум может представлять собой человека с риском развития инфекции или пациентом с уже развитой инфекцией.
В варианте выполнения изобретения каждый указанный(ы) штамм(ы) присутствует в фармацевтической композиции в количестве без ограничения от 1×106 до приблизительно 1×1014 КОЕ, предпочтительно от приблизительно 1×108 до приблизительно 1×1012 и более предпочтительно от приблизительно 1×109 до приблизительно 1×1011.
Фармацевтическая композиция по изобретению может представлять собой препарат в жидкой или твердой форме.
В случае если фармацевтическая композиция представляет собой твердый препарат, она может быть приготовлена в форме таблетки, сосательной таблетки, леденца, жевательной таблетки, жевательной резинки, капсулы, саше, порошка, гранул, частиц с покрытием, таблетки с покрытием, таблетки с кишечнорастворимым покрытием, капсулы с кишечнорастворимым покрытием, рассасываемых полоски или пленки.
В случае, если фармацевтическая композиция представляет собой жидкий препарат, она может быть приготовлена в форме перорального раствора, суспензии, эмульсии или сиропов. Указанная композиция может дополнительно включать носитель без ограничения независимо выбранный из группы, состоящей из овсяной муки, молочнокислых ферментированных пищевых продуктов, устойчивого крахмала, диетических волокон, углеводов, белков, и гликозилированных белков.
В варианте выполнения изобретения указанная фармацевтическая композиция представляет собой медицинский пищевой продукт, функциональный пищевой продукт, диетическую добавку, питательный продукт или пищевой препарат.
Фармацевтическая композиция по изобретению, применяемая по изобретению или полученная по изобретению, может также включать другие вещества, такие как инертный носитель или фармацевтические приемлемые вспомогательные компоненты, носители, консерванты и т.д., которые известны специалистам в данной области.
Термин "фармацевтическая композиция" не обязательно относится к фармацевтической композиции в ее обычном понимании, но также может относиться к пищевой композиции, диетической добавке, функциональному пищевому продукту, медицинскому пищевому продукту или питательному продукту до тех пор, пока оказывается требуемое воздействие, то есть лечение или предотвращение вирусных инфекций. Указанная пищевая композиция может быть выбрана из группы, состоящей из напитков, йогуртов, соков, мороженого, хлеба, бисквитов, продуктов из дробленого зерна, батончиков для здорового образа жизни, пастообразных продуктов и питательных продуктов. Пищевая композиция может дополнительно включать носитель, где указанный носитель представляет собой выбранный из группы, состоящей из овсяной муки, молочнокислых ферментированных пищевых продуктов, устойчивого крахмала, диетических волокон, углеводов, белков и гликозилированных белков.
Таким образом, преимущества применения композиции по изобретению заключается в возможности профилактического приема, то есть до развития вирусной инфекции. Используемая фармацевтическая композиция не обязательно представляет собой фармацевтическую композицию в ее обычном понимании, и может также представлять собой диетическую добавку или функциональный пищевой продукт, что является очень удобным для нормального здорового индивидуума для профилактического потребления композиции по изобретению.
Примеры
Пример 1
Субъекты и параметры исследований
Для слепого плацебо-контролируемого исследования были отобраны пятьдесят семь практически здоровых добровольцев в возрасте 18-55 лет (средний возраст, 26 лет). Субъектов в произвольном порядке разделили на восемь групп, получавших одно из следующих грамположительных бактерий, L.plantarum 299v (n=7), L.Plantarum Heal 19 (n=7), L.fermentum 35D (n=7), L.paracasei 8700:2 (n=7), L.gasseri VPG44 (n=7), L.rhamnosus 271 (n=7), или грамотрицательных бактерий, P.lundensis (n=7) или плацебо (n=10). Доза бактерий составляла 1010 бактерий/день для lactobacilli и 109 бактерий/день для P.lundensis. Контрольной группе давали сухое обезжиренное молоко (1 г). В зависимости от группы, продолжительность исследования составляла 6 или 9 недель, состоящих из двухнедельного период вымывания, 2 или 5 недель активного периода исследования и 2 недель периода последующего наблюдения (фиг.4). Каждому субъекту был выдан список продуктов, содержащих пробиотические продукты, которые не должны потребляться во время всего периода исследования. Образцы периферической крови отбирали у субъектов венопункцией два или три раза на 0 день, 14 день и 35 день. Дневник, в котором каждый субъект отмечал неблагоприятные эффекты, состояние здоровья и подтверждал прием исследуемого продукта, хранили в течение исследования.
Проточная цитометрия
Фенотипический анализ лимфоцитов в цельной крови выполняли проточной цитометрией. Следующие моноклональные антитела для человека были использованы в качестве поверхностных маркеров для различных клеточных популяций: CD3 FITC (SK7), CD4 APC (SK3), CD8 PerCP (SKl), CD19 PerCP (SJ25C1), CD56 PE (MY31), CD16 PE (B73.1), и CD5 FITC (L17F12). Следующие моноклональные антитела для человека были использованы для определения различной активации и маркеров: CD25 FITC (2A3), PE HLA-DR (L243), CD45RO PE (UCHL-I), CD38 PE (HB7), CD27 PE (L128), и CD11b PE (D12). Все антитела были закуплены у Becton-Dickinson (Erembodegum, Belgium). Цельная кровь (100 мкл) инкубировали с антителами (10 мкл/антитело) в течение 30 минут при 4°C в темноте. Затем добавляли 2 мл раствора для лизиса FACS (Becton-Dickinson) и инкубировали в течение 15 минут при 20°C в темноте. Клетки промывали добавлением 3 мл FACSFlow и центрифугировали при 300×g в течение 5 мин. Промытые клетки ресуспендировали в 200 мкл FACSFlow и анализировали на FacsCalibur (Becton-Dickinson) с программным обеспечением CellQuest.
Исследование фагоцитоза
Фагоцитарную активность гранулоцитов и моноцитов количественно оценивали с использованием PHAGOTEST® (Orpegen Pharma, Heidelberg, Germany) в соответствии с инструкцией изготовителя с некоторыми изменениями. Кратко, 20×106E.Coli, меченные FITC, или S.aureus, меченные FITC, добавляли к предварительно охлажденной цельной крови (100 мкл). Клетки крови и бактерии инкубировали при 37°C для анализа 10 FacsCalibur с программным обеспечением CellQuest.
Расчеты
Изменения различных иммунных параметров индивидуумов определяли расчетом отношения между отдельными значениями, полученными в 14 день и 0 день, или значениями, полученными в 35 день и 0 день. Эти отношения использовали для всех групп расчетов и статистических вычислений.
Статистические вычисления
Все статистические исследования были выполнены, используя Stat-view. Критерий U Манна-Уитна использовался при сравнивании различных групп.
Результаты
Клинические наблюдения
Пятьдесят четыре из пятидесяти семи добровольцев прошли полное исследование. Два индивидуума были исключены вследствие инфекции и терапии антибиотиками (один в группе плацебо и один в группе, получающей P.lundensis). Один индивидуум был исключен на 16 день вследствие беременности (группа плацебо). Во время приема исследуемых продуктов сообщали только об умеренных неблагоприятных желудочно-кишечных побочных эффектах (фиг.1).
Активация Т-клеткок при приеме lactobacilli
Наблюдали значительные единичные отклонения значений при исходных данных (день 0) в отношении маркеров активации на CD4+ и CD8+ Т-клеток. Исходные данные о процентном содержании клеток, экспрессирующих различные клеточные поверхностные маркеры, показаны на фиг.2. Между различными группами в этой точке времени не было никакого значительного отличия. Поскольку наблюдали очень большие единичные отклонения в пределах значения, то проводили сравнение соотношения значений в 14 день и 35 день к значениям в день 0 для каждого индивидуума. Все вычисления и сравнения выполняли при этих значениях соотношений (день 14/день 0 и день 35/день 0). После 14 дней приема исследуемого продукта, содержащего L.plantarum 299v, наблюдали приблизительно двукратное увеличение экспрессии маркера активации CD25 на CD8+ Т-клетках (p=0,01) (фиг.5). Также наблюдали сильный, хотя незначительный (p=0,12), показатель повышенной регуляции HLA-DR на CD8+ клетках после приема L.plantarum 299v. Кроме того, также наблюдали тенденцию к активации CD4+ Т-клеток после приема L.Plantarum 299v. Прием других видов lactobacilli, включенных в это исследование, а также грамотрицательных бактерий P.lundensis не активировал ни CD8+, ни CD4+ Т-клетки. Однако наблюдали тенденцию увеличения экспрессии HLA-DR на CD4+ Т-клетках (р=0,18) при приеме L.paracasei.
Прием lactobacilli вызывает фенотип памяти CD4+ Т-клеток
Средние геометрические значения флуоресцентной интенсивности (GMFI) экспрессии CD45RO на CD4+ и CD8+ Т-клетках сравнивали между группами, получающими различные исследуемые продукты. Как отмечалось выше, для сравнения использовали расчеты для групп, основанные на отдельных соотношениях значений (день 14/день 0 и день 35/день 0). После 35 дней приема исследуемого продукта, содержащего L.Plantarum 299v, CD45RO GMFI на CD4+ Т-клетках значительно увеличились (p=0,03). Также наблюдали тенденцию к увеличению экспрессии CD45RO на CD8+ Т-клетках после приема L.plantarum (фиг.6). Кроме того, прием L.paracasei, как представляется, оказывает положительные эффект на усиление регуляции CD45RO на CD8+ Т-клетках (p=0,10) (фиг.6).
Влияние на различные группы клеток после приема исследуемого продукта
Прием L.paracasei вызвал увеличение процентного содержания лимфоцитов, идентифицируемых как NKT-клетки (р=0,06) (фиг.7). Относительное увеличение/уменьшение по сравнению с 0 днем не могли быть обнаружены в отношении других групп клеток, таких как CD4+ Т-клетки, CD8+ Т-клетки, B-клетки, B-1-клетки (CD19+CD5+), NK-клетки, гранулоциты и моноциты.
Фагоцитарная активность
Гранулоциты и моноциты идентифицировали по диаграмме FSC-SSC. Тестировали свойства этих клеток к фагоцитозу FITC-меченных грамположительных или грамотрицательных бактерий. Как показано на фиг.8, гранулоциты от добровольцев, получавших L.plantarum 299v (p=0,064), L.plantarumHeal19 (p=0,064), L.fermentum (p=0,064) или L.paracasei (p=0,05) были более эффективны, чем лейкоциты от добровольцев, получавших плацебо, при фагоцитозе грамотрицательных бактерий E.coli. Однако не было обнаружено какого-либо отличия между группами при фагоцитозе грамположительных бактерий S.aureus. Не были обнаружены какие-либо различия фагоцитарной активности моноцитов (данные не показаны).
Обсуждение
Основной задачей иммунной системы заключается в быстрой и резкой реакции на микроорганизмы, таким образом предотвращая и излечивая инфекцию. При уничтожении микроорганизмов используются мощные механизмы, которые также оказывают вред нашим собственным тканям. Поэтому необходимо отсутствие реакции на наши собственные ткани и на безвредные вещества, присутствующие в среде. Поэтому иммунная система развивается и обеспечивает толерантность как к компонентам нашего собственного тела, так и к пищевым продуктам и белками, попадающими при дыхании. Если она дает сбой, то может возникнуть множество заболеваний. Способ достижения специфической иммунной переносимости является основной задачей иммунной системы.
Центральную роль во всех иммунных реакциях принадлежит Т-клеткам-хелперам. Если Т-клетка-хелпер активируется ее специфическим антигеном, она становится активируемой, делится, созревает и вырабатывает ряд цитокинов, которые управляют действием других типов клеток в иммунной системе, таких как цитотоксические Т-клетки и B-клетки. Активация Т-клеток-хелперов необходима для получения большой части типов иммунных реакций, включая выработку антител. Наоборот, при отсутствии активации Т-клеток-хелперов, отсутствует большая часть типов иммунных реакций.
Существует несколько механизмов, обеспечивающих активацию Т-клеток-хелперов и поддержания толерантности. Один из механизмов заключается в устранении в тимусе Т-клеток, распознающих и реагирующих с тканями. Однако это устранение не является полным, кроме того, мы должны также развивать специфическую иммунную толерантность к экзогенным антигенам. В противном случае, мы резко реагировали бы на любой тип веществ, которые попадают внутрь, что привело бы к общему воспалению и потратило впустую иммунные ресурсы.
Регуляторная Т-клетка представляет собой тот тип клетки, который является центральным для поддержания толерантности. Этот тип клетки может быть распознан некоторыми маркерами, такими как поверхностная экспрессия CD4 и CD25, захват внутриклеточного CTLA-4 и транскрипция ядерного белка Foxp3. Регуляторные Т-клетки способны предотвращать активацию других Т-клеток при встрече с безопасными веществами и, следовательно, предотвращать любые типы нежелательных иммунных реакций.
В настоящем контексте символ "+" в сочетании каким-либо маркером, такое как CD4+ и CD25+, означает, что маркер экспрессируется на Т-клетке. Например CD4+CD25+ Т-клетки представляет собой Т-клетки, которые экспрессируют как CD4 маркер, так и CD25 маркер на поверхности. Однако это указывает, что маркер присутствует, но не дает сведений о количестве маркера, который экспрессируется. В настоящем описании символ "++" в сочетании с маркером, такое как CD4++ или CD25 ++, означает, что в данном случае экспрессируется большое количество маркера. Регуляторные Т-клетки представляю собой клетки с большим количеством CD25 на поверхности, то есть CD4+CD25++ клетки. С другой стороны, CD4+CD25+ Т-клетки представляют собой только активируемые Т-клетки. Иногда символы "+" и "++" не используются, например, только CD4CD25, это означает что клетки активируемые, такие как CD4+CD25+ клетки. Таким образом, CD4CD25 тоже самое, что CD4+CD25+. При упоминании о регуляторных Т-клетках, они всегда написаны как CD4+CD25++ клетки.
Это слепое плацебо-контролируемое исследование уникально в том, что оно представляет собой первое исследование, в котором сравниваются влияние приема различных грамположительных lactobacilli или грамотрицательных бактерий P.lundensis на ряд иммунных параметров. Интересно, что прием P.lundensis не оказал влияния ни на один из измеренных параметров. Напротив, прием lactobacilli оказал влияние на различные компоненты как специфической, так и врожденной иммунной системы. Новые сведения, полученные при этом исследовании, заключались в том, что прием L.plantarum оказал явный положительный эффект на активацию и индукцию клеток памяти в группах Т-клеток. Наблюдали значительное усиление регуляции IL-2 рецептора α цепи (CD25) и сильную тенденцию к усилению регуляции HLA-DR на цитотоксических Т-клетках. Тенденция к усилению регуляции этих маркеров активации также наблюдали в отношении Т-хелперов после приема L.plantarum. Экспрессия маркеров активации показывает, что Т-клетки начинают пролиферировать в ответ на антигенспецифические или неспецифические воздействия и что эти клетки быстрее проявляют их эффекторные функции, по сравнению с Т-клетками в покое. Механизмы против L.plantarum вызвали активацию Т-клеток, могут осуществляться посредством антигенпрезентирующих клеток, которые активируются toll-подобными рецепторами, связывающимися с микробными соединениями. Активация антигенпрезентирующих клеток делает их более эффективными в представлении антигена к Т-клеткам. Кроме того, как хелперные, так и цитотоксические Т-клетки показали различные экспрессии toll-подобных рецепторов, которые вероятно делают эти клетки чувствительными к неспецифической активации микробными компонентами и продуктами.
По аналогии с Т-хелперными клетками, экспрессия CD45RO также, вероятно, метит популяции клеток памяти среди цитотоксических Т-клеток. Было обнаружено значительное увеличение экспрессии этого клеточного маркера памяти на Т-хелперах и тенденция к усилению регуляции на цитотоксических Т-клетках во время приема L.plantarum в течение 35 дней. Кроме того, прием L.paracasei также показал тенденцию к усилению регуляции CD45RO на цитотоксических Т-клетках. Что касается наивных Т-клеток, то CD45RO+ Т-клетки могут секретировать широкий спектр цитокинов. Кроме того, CD45RO+ Т-клетки могут пролиферировать и продуцировать IL-2 при стимуляции комплекса CD3-TCR в близких к оптимальным условиях, тогда как наивные Т-клетки требуют сильной стимуляции CD3-TCR для выполнения этих функций. Формирование Т-клеток памяти важно для индукции эффективного иммунного ответа после инфекции и прививки.
На врожденную клеточную иммунную систему также воздействовали введением пробиотических бактерий. Было продемонстрировано, что популяция натуральных киллерных T (NKT) клеток увеличилась после приема L.paracasei. NKT-клетки составляют субпопуляцию лимфоцитов, которая совместно экспрессируют маркер CD56 NK-клеткок и рецепторный комплекс маркер CD3-Т-клетки. Исследования как на людях, так и на мышах показали, что NKT-клетки играют центральную роль в регуляции аутоиммунных заболеваний, таких как рассеянный склероз, диабет типа I и системная волчанка. NKT-клетки также проявляют эффекторные функции против клеток, инфицированных опухолью и вирусами. Таким образом, NKT клетки являются плейотропными по своим свойствам. Другие клинические исследования, оценивающие иммунологические эффекты пробиотических бактерий, показали, что прием L.rhamnosus HN001 и Bifidobacterium lactis HN019 усиливает противоопухолевую активность NK-клеток (включая NKT) K562 клеток. В этом исследовании также был подтверждено наблюдение, что фагоцитарная активность полиморфнонуклеарных клеток увеличивается после приема различных lactobacilli. В результате наблюдаемых воздействий на различные иммунные параметры в настоящем исследовании можно предположить, что совместная активация цитотоксических Т-клеток и увеличение NKT клеток направлены на усиление иммунной защиты против вирусных инфекций и/или опухолей. Полученные in vitro результаты о том, что lactobacilli стимулирует одноядерные клетки секретировать IL-12 и IL-18, поддерживают теорию, что прием этих бактерий стимулирует активность, опосредованную клетками.
В соответствии с настоящим изобретением были сделаны выводы, что прием L.plantarum и L.paracasei оказывает сильный эффект на специфическую и врожденную клеточную иммунную систему. Однако усиление иммунной функции, показанное здесь, в настоящее время трудно коррелировать с доказанными преимуществами для здоровья людей. Для конкретного применения этих результатов необходимы дополнительные клинические исследования на индивидуумах с, например, вирусными инфекциями или опухолями. В таких исследованиях, особенно интересно было бы сравнить эффекты введения L.plantarum и L.paracasei по отдельности или в комбинации.
Пример 2
Цель этого примера заключалась в том, чтобы исследовать воздействие на иммунную систему, при введении одинаковых видов lactobacilli в течение более длительного периода времени, по сравнению с последовательным введением нескольких видов lactobacilli (различных видов).
Добровольцам давали порошок с высушенными замораживанием бактериями в течение 14 или 35 дней. В качестве грамположительных бактерий использовали пробиотические бактерии Lactobacillus plantarum 299v, отдельно или в комбинации с L.rhamnosus, L.fermentum, L.paracasei и L.gasseri. В качестве грамотрицательных бактерий использовали Psedomonas lundensis.
Были исследованы следующие группы:
1) Lactobacillus plantarum 35 дней
2) L.plantarum 7 дн, L.rhamnosus 7 дн, L.fermentum 7 дн, L.paracasei 7 дн, L.gasseri 7 дн. Всего 35 дней. (Последовательно)
3) смесь L.plantarum, L.rhamnosus, L.fermentum, L.paracasei, L. gasseri. Всего 14 дней
4) L.rhamnosus 14 дней
5) L.fermentum 14 дней
6) L.paracasei 14 дней
7) L.gasseri 14 дней
8) Pseudomonas lundensis 14 дней
Контрольная группа 1) Плацебо 35 дней
Контрольная группа 2) Плацебо 14 дней
Пробы крови отбирали на 0, 14 и 35 день. Содержание Т-хелперов (CD4+) экспрессирующих большие количества CD25 определяли в каждой группе поточной цитометрией, как было указано в примере 1.
Результаты
На 14 день наблюдали пограничное состояние увеличения CD4+CD25++ Т-клеток, у индивидуумов, потребляющих последовательно пять различных штаммов lactobacilli.
Обсуждение
Было показано, что Т-клетки-хелперы (CD4+) экспрессирующие c высокой плотностью CD25 молекулы (CD4+CD25++) являются важными для предотвращения аутоиммунных заболеваний, аллергий и воспалительных заболеваний кишечника. Обнаружено, что эти клетки количество этих клеток увеличивается после последовательного приема различных lactobacilli, что показывает, что прием этих бактерий может быть полезен для индивидуумов, с риском развития вышеупомянутых заболеваний.
Эксперимент 3
Цель настоящего исследования заключается в том, чтобы исследовать влияние приема молочнокислых бактерий в высушенной замораживанием форме/функциональном пищевом продукте в течение по меньшей мере 3 месяцев на тяжесть симптомов и случаев и продолжительности простуды.
Важно, что это исследование выполняется in vivo на людях, поскольку ни изучения in vitro, ни исследования на животных, не отразили бы степень эффективности при введении людям. Свойство этих бактерий не изменяться в кишечном тракте, при введении сразу после культивирования было показано раннее в исследованиях.
Таким образом, цель заключается в том, чтобы исследовать может ли прием смеси Lactobacillus plantarum 299v (DSM 9843) и Lactobacillus paracasei 8700:2 (DSM 13434) (1×109 КОЕ/дн) уменьшить риск простуды.
Исследование проводят в течение 90 дней и 500 индивидуумов приняли участие в исследовании. 250 индивидуумов получали активный продукт и 250 индивидуумов получали плацебо.
Исследование двойное слепое рандомизированное и плацебо-контролируемое с двумя параллелями.
Критерии исключения: Известное отсутствие толерантности или аллергии на любой компонент, включенный в препарат; лечение аллергии лекарственными препаратами; лечение тяжелых желудочно-кишечных нарушений; беременность или кормление грудью; прививка против гриппа в течение последних 12 месяцев; и курящие.
Потребляемые пробиотики: лиофилизированный Lactobacillus plantarum 299v и Lactobacillus paracasei 8700; 2. В качестве криопротектантов добавляли сахарозу, мальтодекстрин и гидролизованный желатин. Суточная доза составляла 1 г лиофилизированных Lactobacilli (приблизительно 1×109 КОЕ/день). Дозу принимали за завтраком.
Продукты были изготовлены, упакованы и маркированы Probi AB, Lund, Sweden. Качество продукта было также проверено Probi AB. На каждом саше указываются: название исследования, срок годности, условия хранения, изготовитель, имя изготовителя и ее/его номера телефона. В дополнение к указанной выше информации, номер, назначенный субъекту, проставляется на вторичной упаковке. Подробная инструкция по растворению и приему вкладывается во вторичную упаковку. Продукт поставляется в форме саше.
С 14 дня до 104 дня субъекты не должны потреблять продукты, содержащие пробиотические бактерии. Субъекту выдается список пробиотических продуктов, которые не должны потребляться во время исследования.
Фекальные образцы сдаются в 1 день (до приема исследуемого продукта), 15 день (после приема) и 104 (после приема). Образцы должны быть собраны в две пробирки не позднее, чем за 18 часов до сдачи для анализа и во время этого периода должны храниться в холодильнике. Образцы анализируются в отношении lactobacilli.
Пробы крови отбираются на 1 и 15 дни. Образцы анализируются в отношении CD4+ и CD8+.
В свете экспериментов 1 и 2 ожидается наблюдение улучшенной защиты против простуды у индивидуумов, потребляющих пробиотическую смесь, по сравнению с группой плацебо.
Реферат
Предложено применение по меньшей мере одного штамма пробиотических бактерий, выбранных из Lactobacillus plantarum 299, DSM 6595, Lactobacillus plantarum 299v, DSM 9843, Lactobacillus plantarum HEAL 9, DSM 15312, Lactobacillus plantarum HEAL 19, DSM 15313, Lactobacillus plantarum HEAL 99, DSM 15316, Lactobacillus paracasei 8700:2, DSM 13434 и Lactobacillus paracasei 02A, DSM 13432, для производства композиции для лечения и/или предотвращения вирусной инфекции, вызванной вирусом простуды и соответствующий способ лечения и/или предотвращения. Показано усиление иммунной защиты против вирусной инфекции, что способствует снижению эпизодов простуды по сравнению с контролем. Количество дней, в течение которых ощущались симптомы простуды, также было снижено в группе, принимавшей пробиотик. 2 н. и 14 з.п. ф-лы, 13 ил.

Комментарии