Новые пестицидные протеины и штаммы - RU2196824C2
Код документа: RU2196824C2
Чертежи











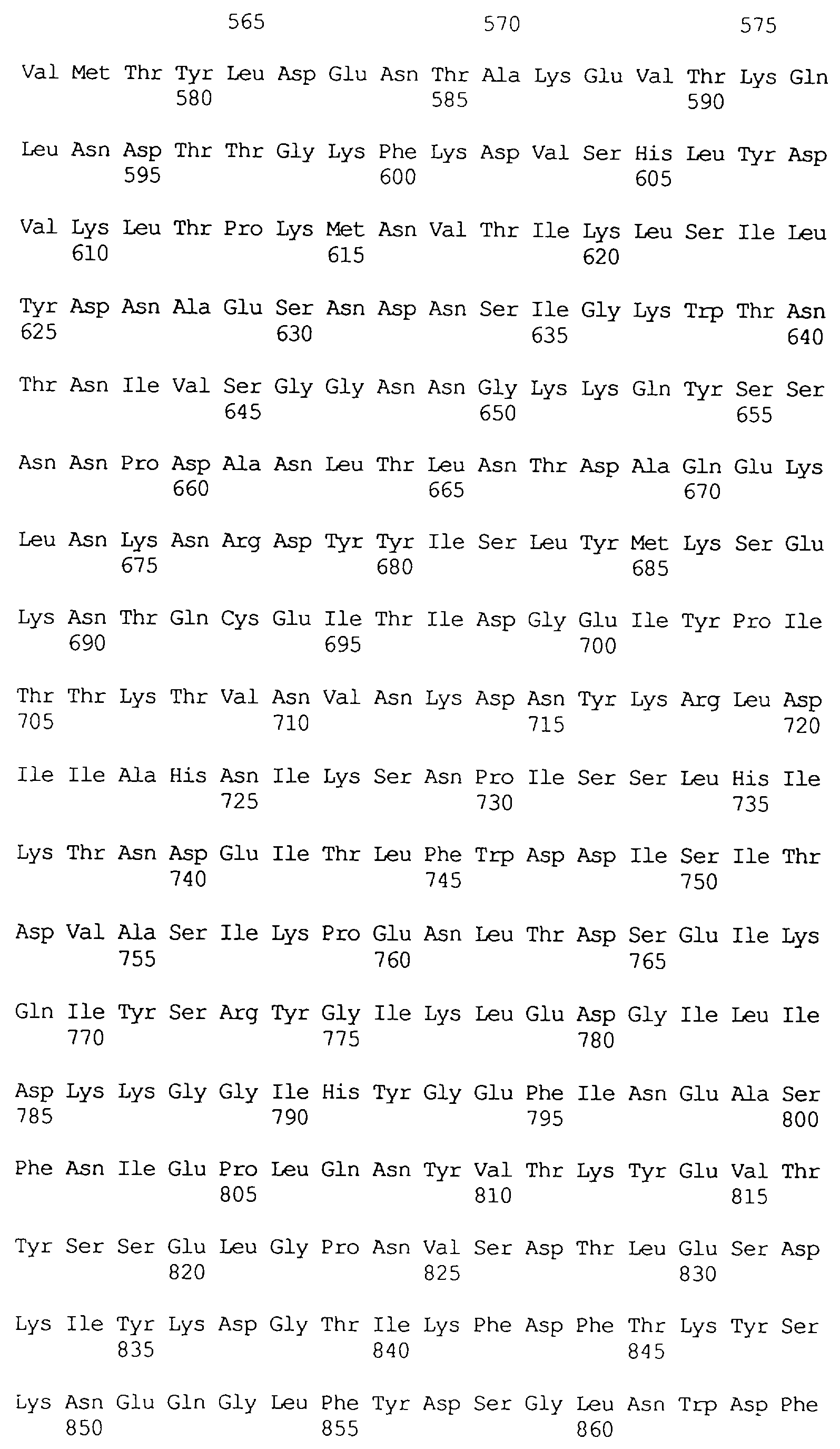




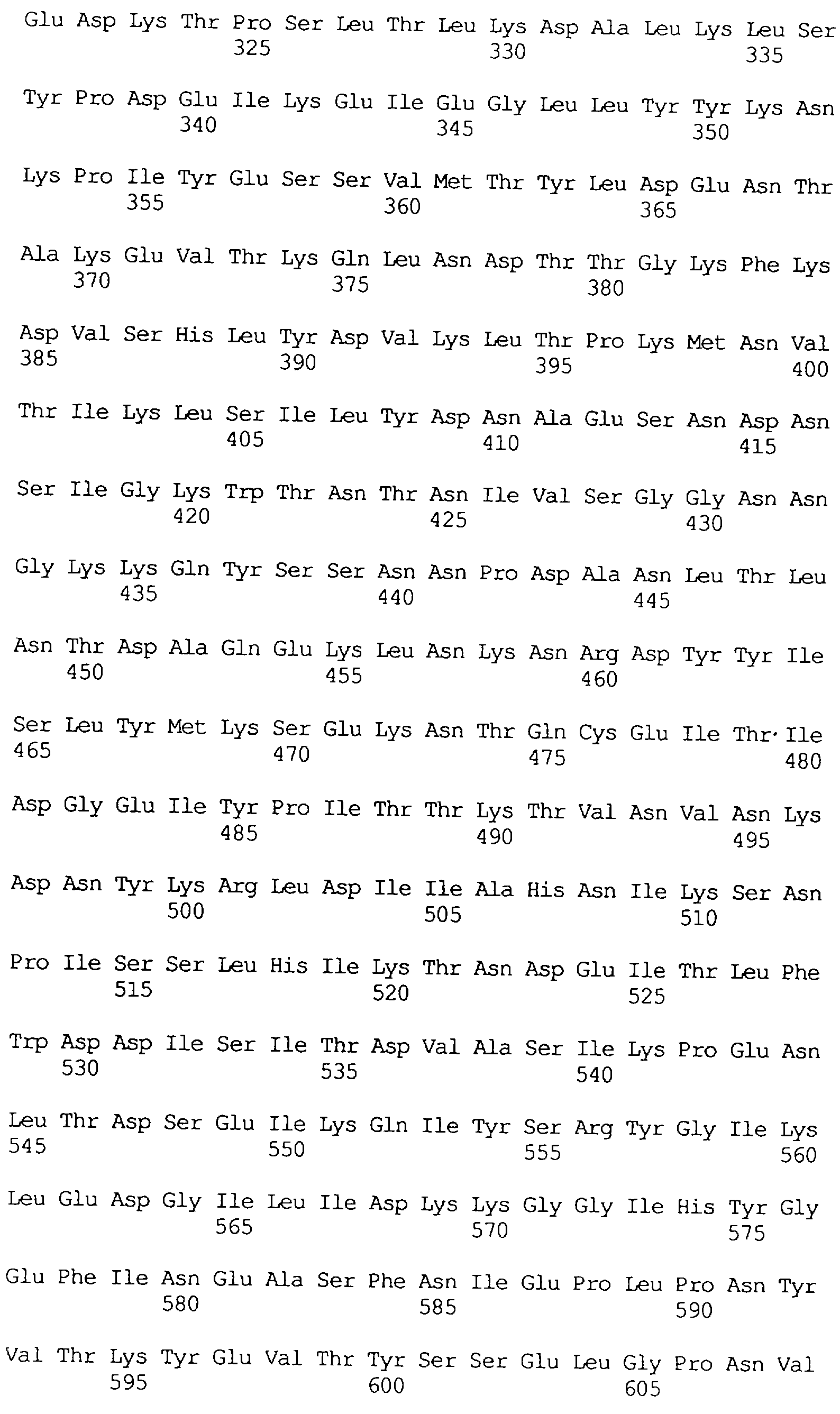














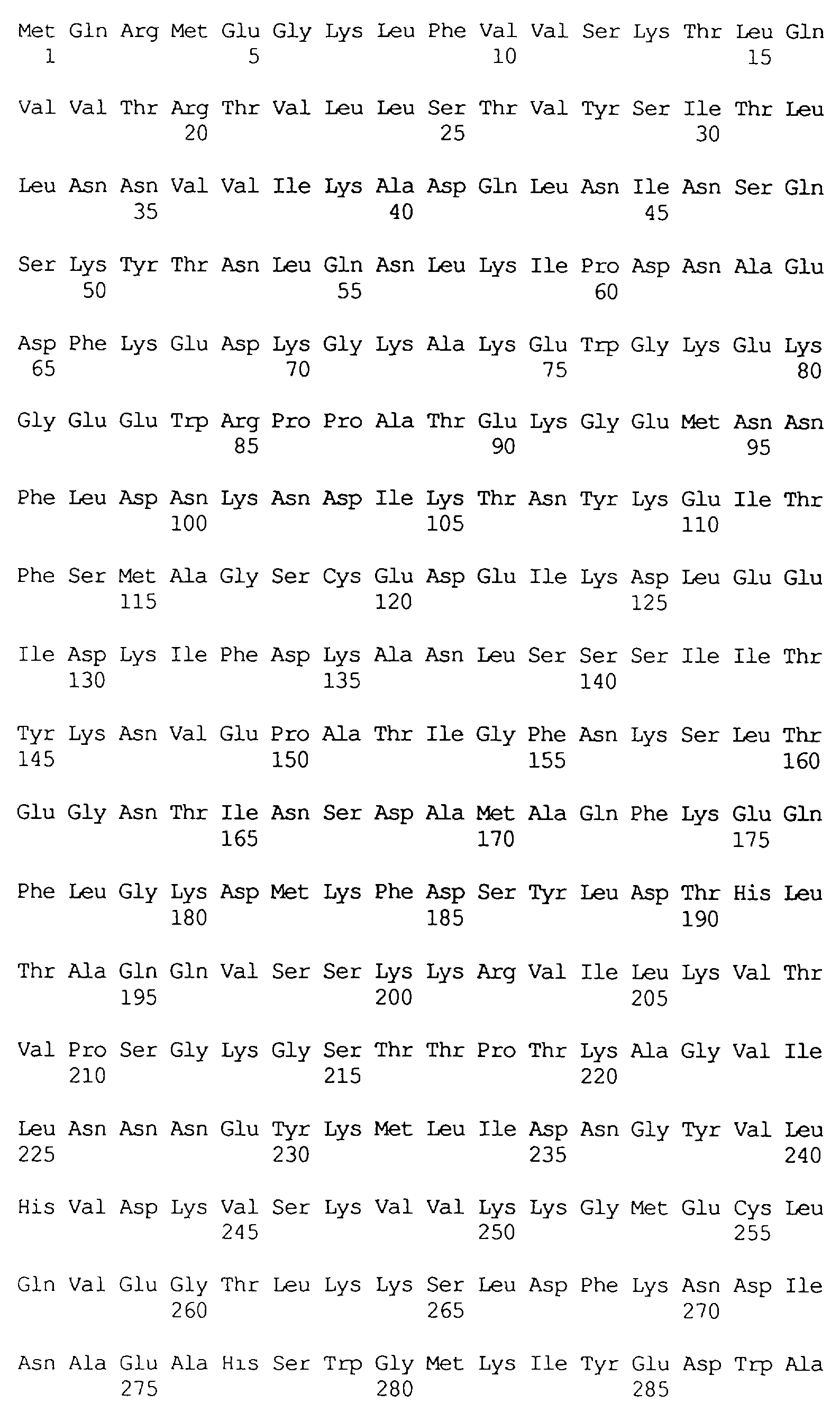

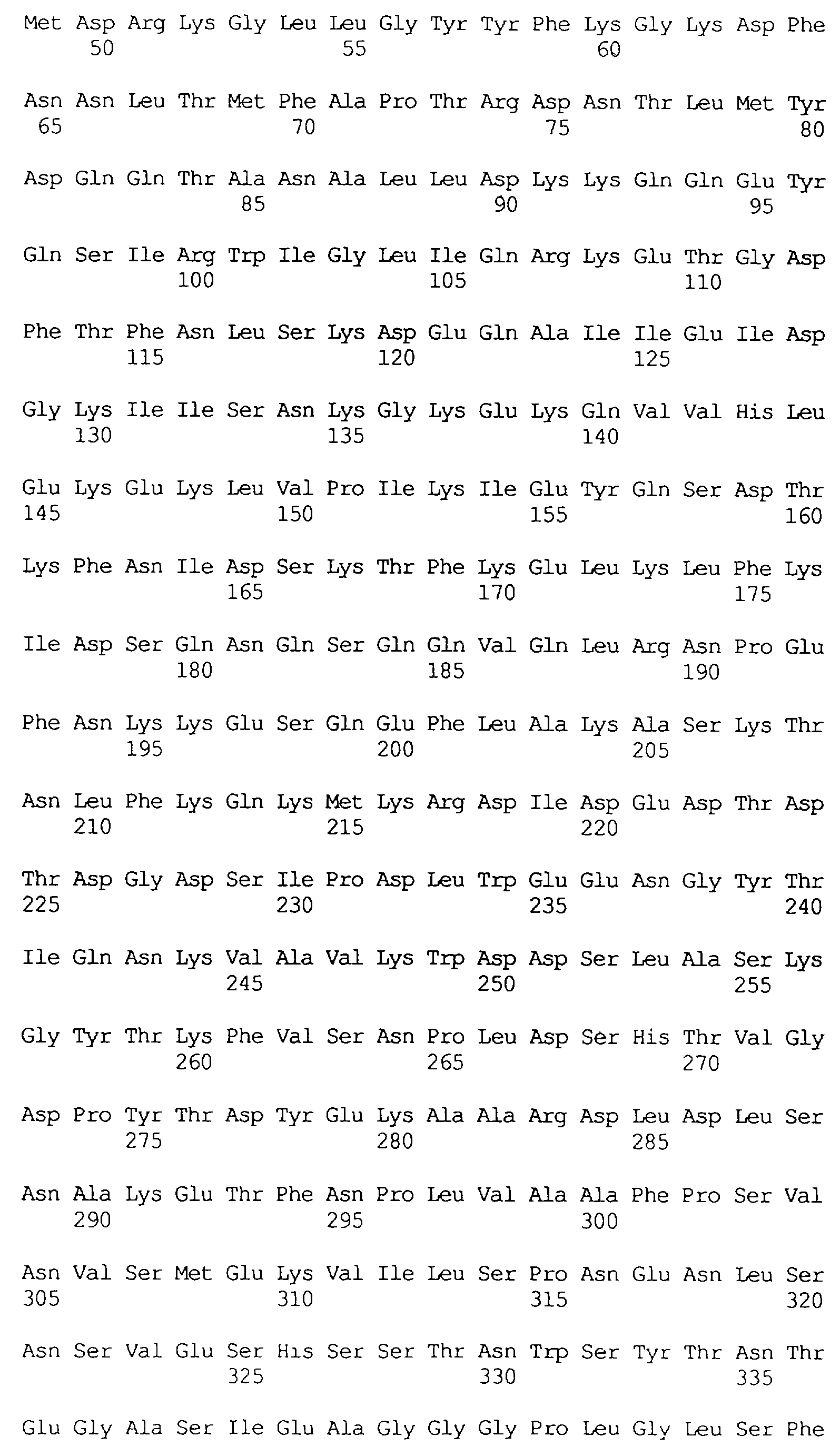



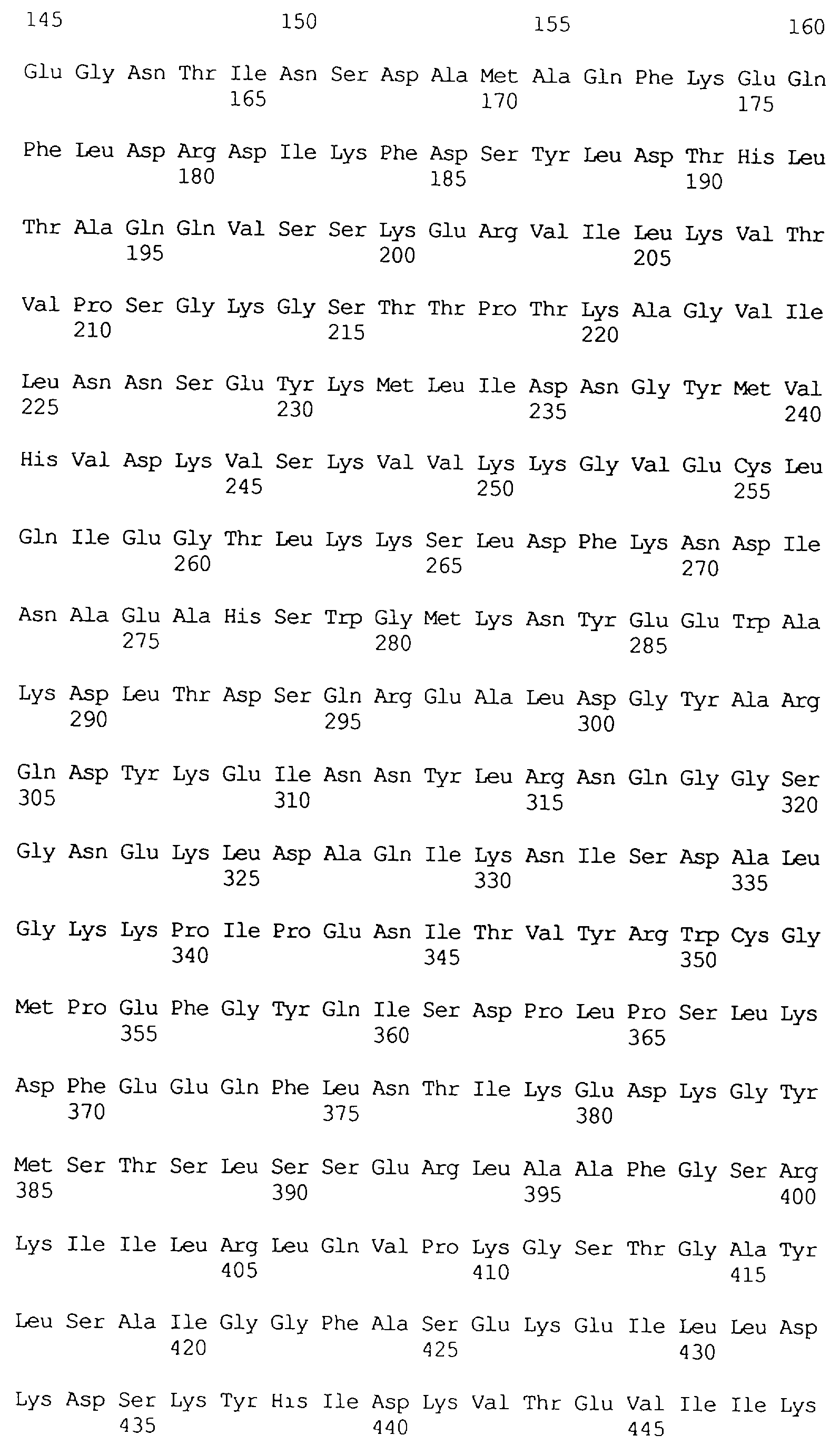
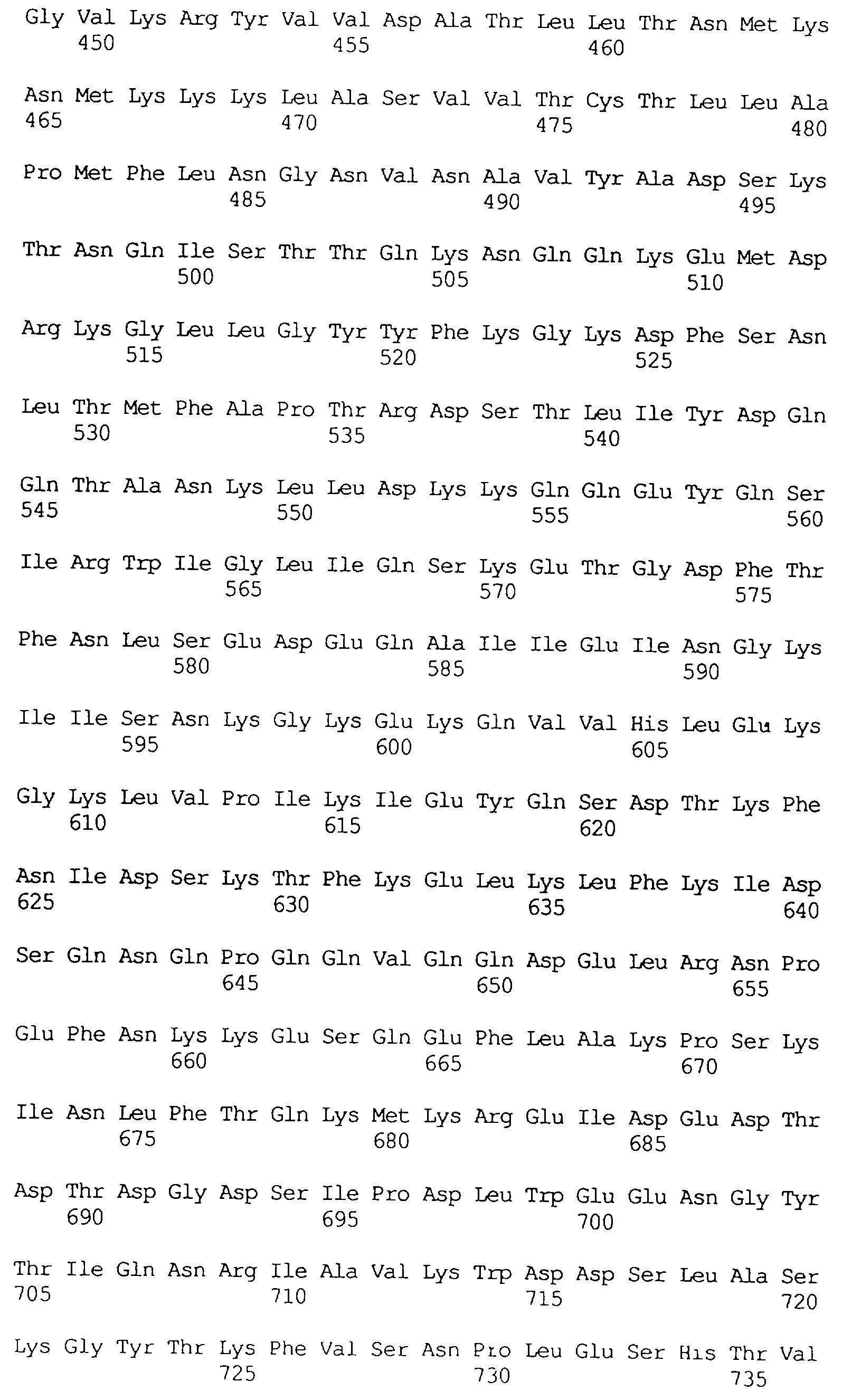
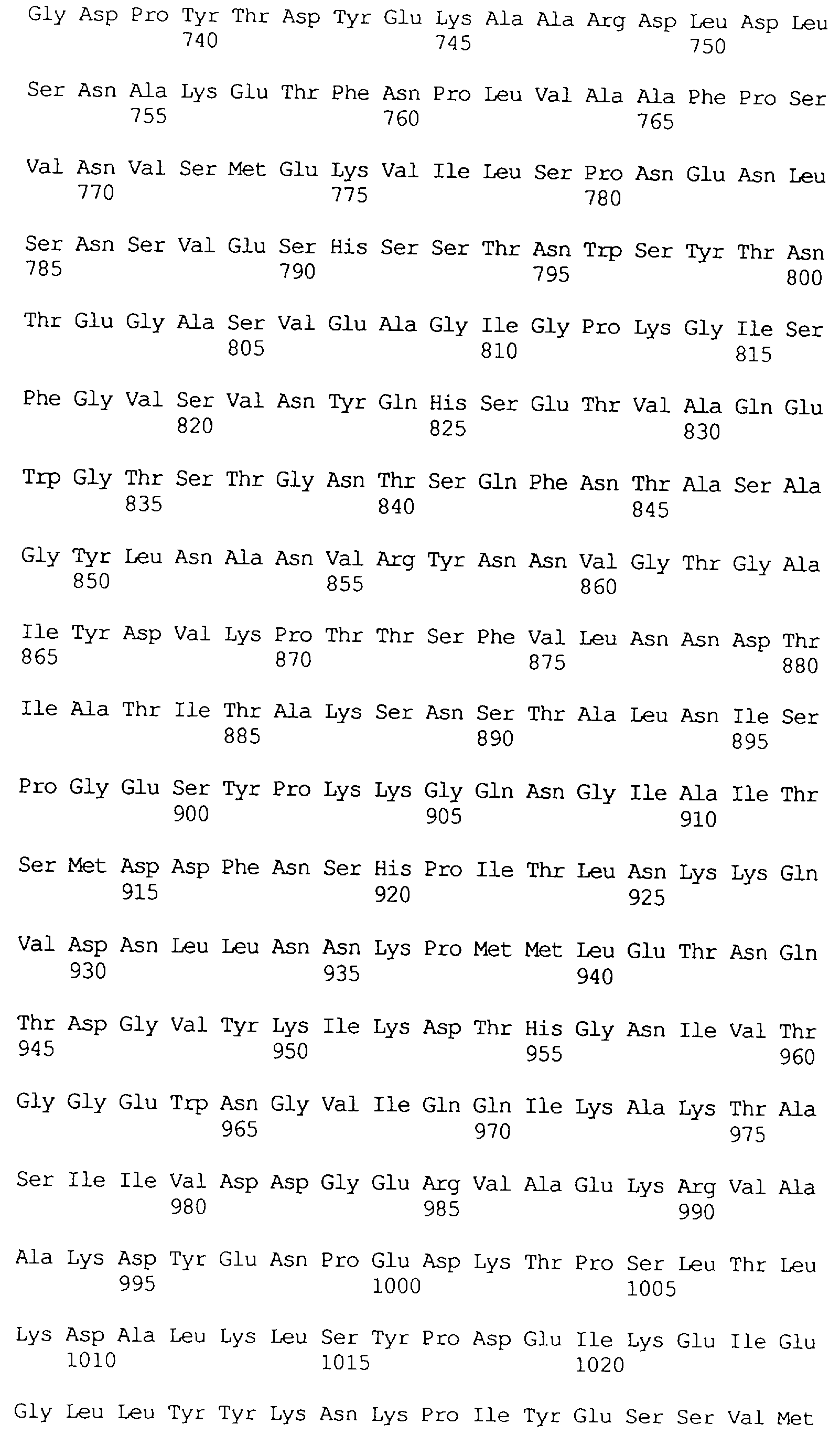
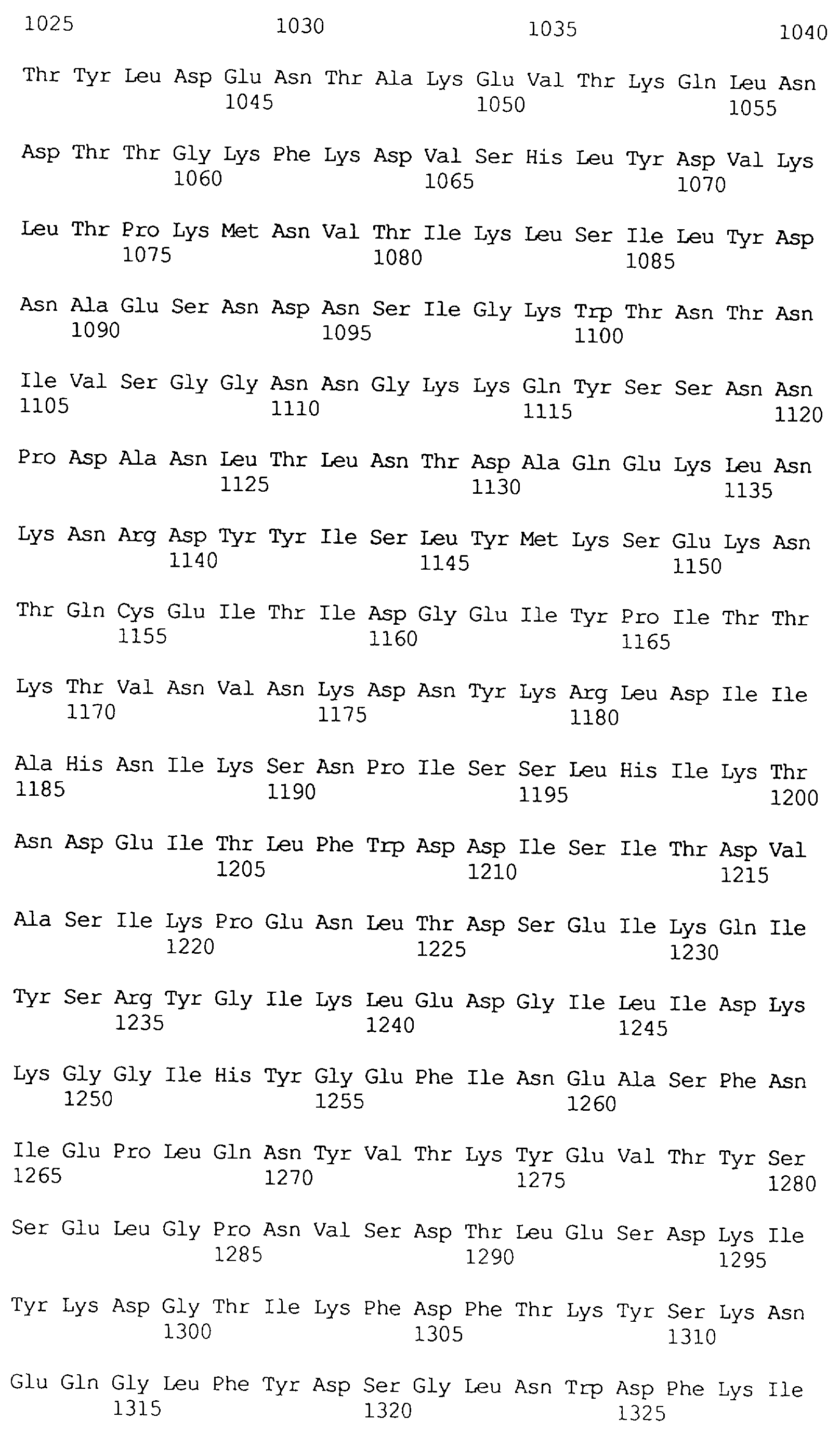















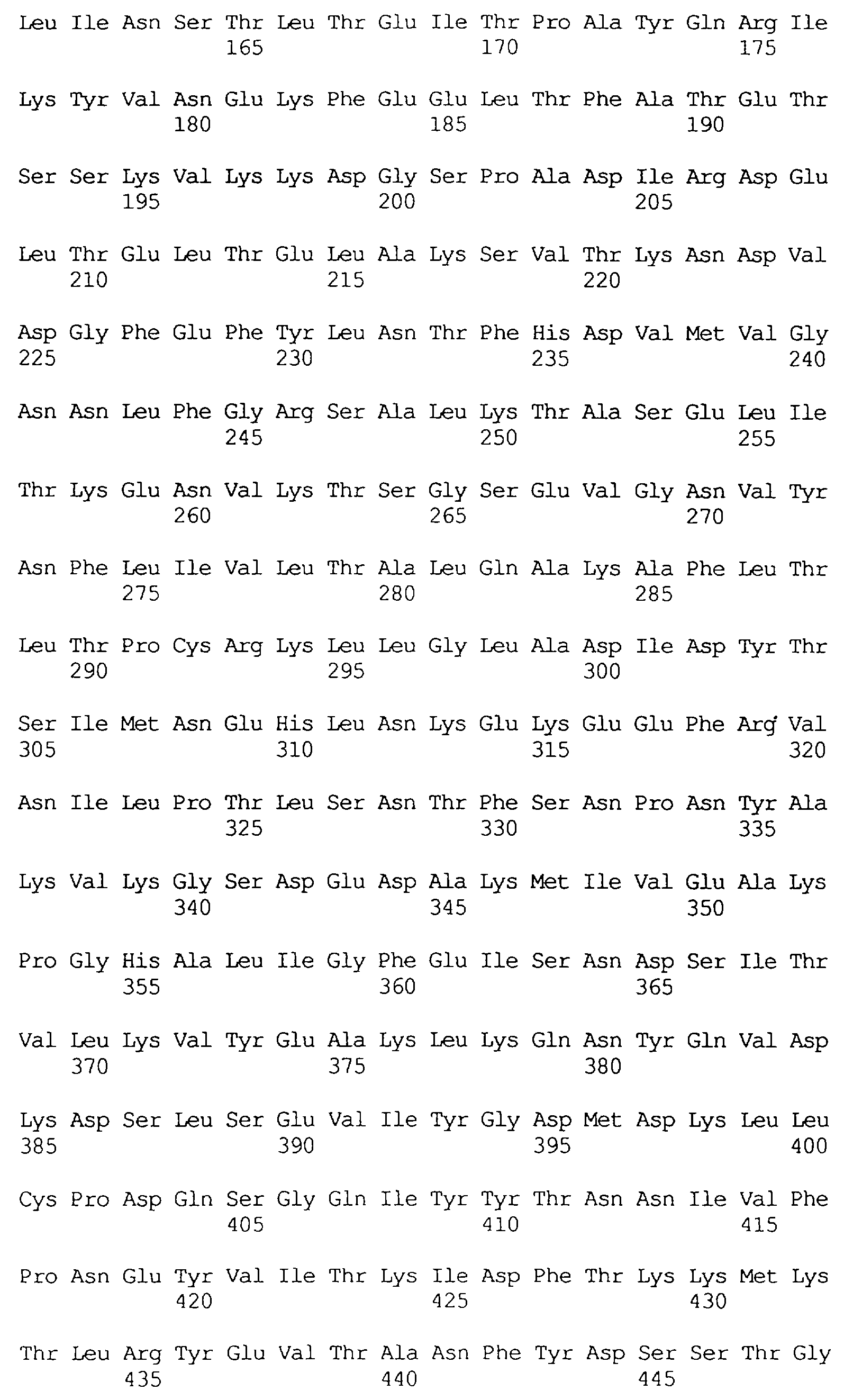



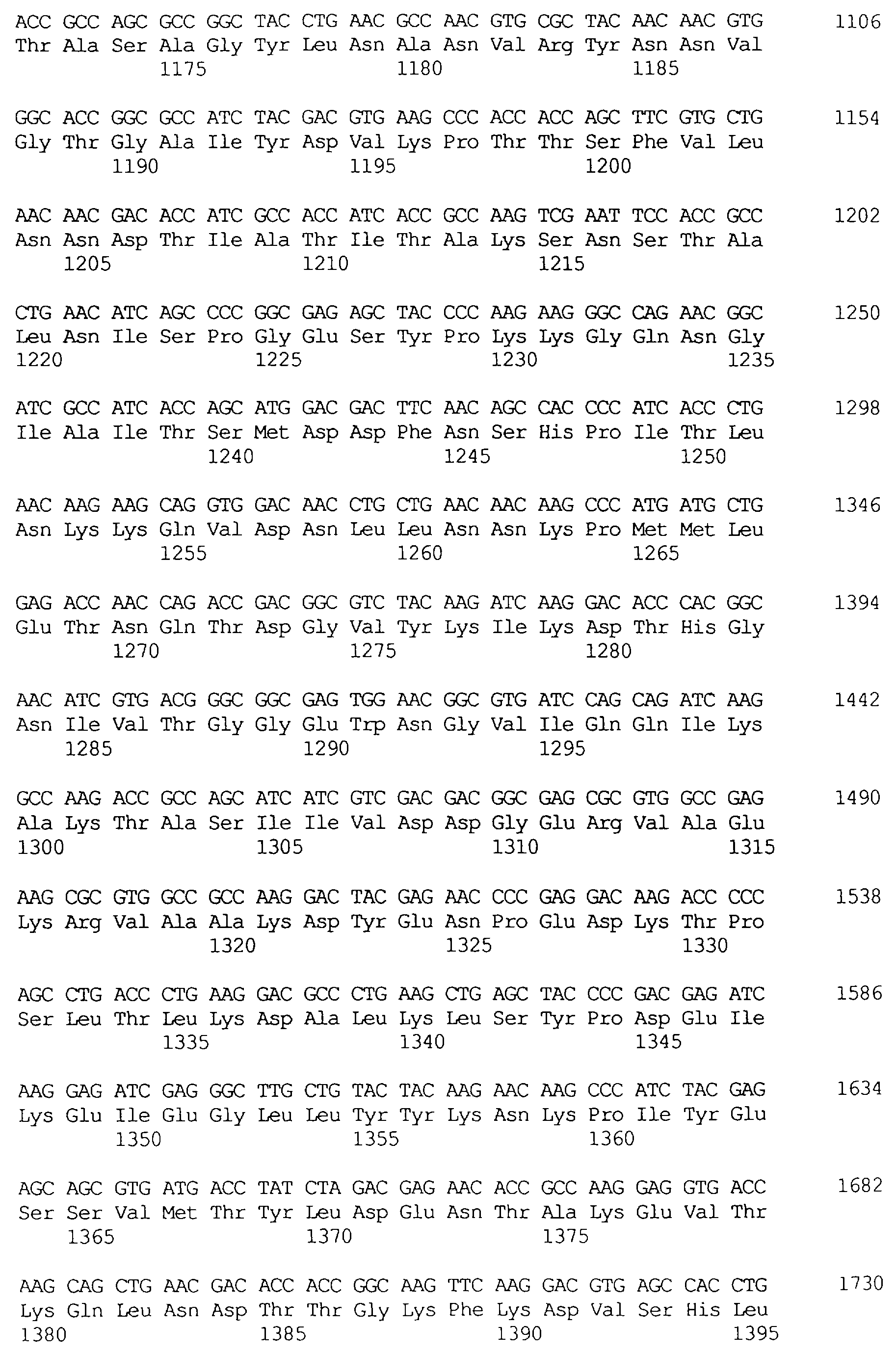

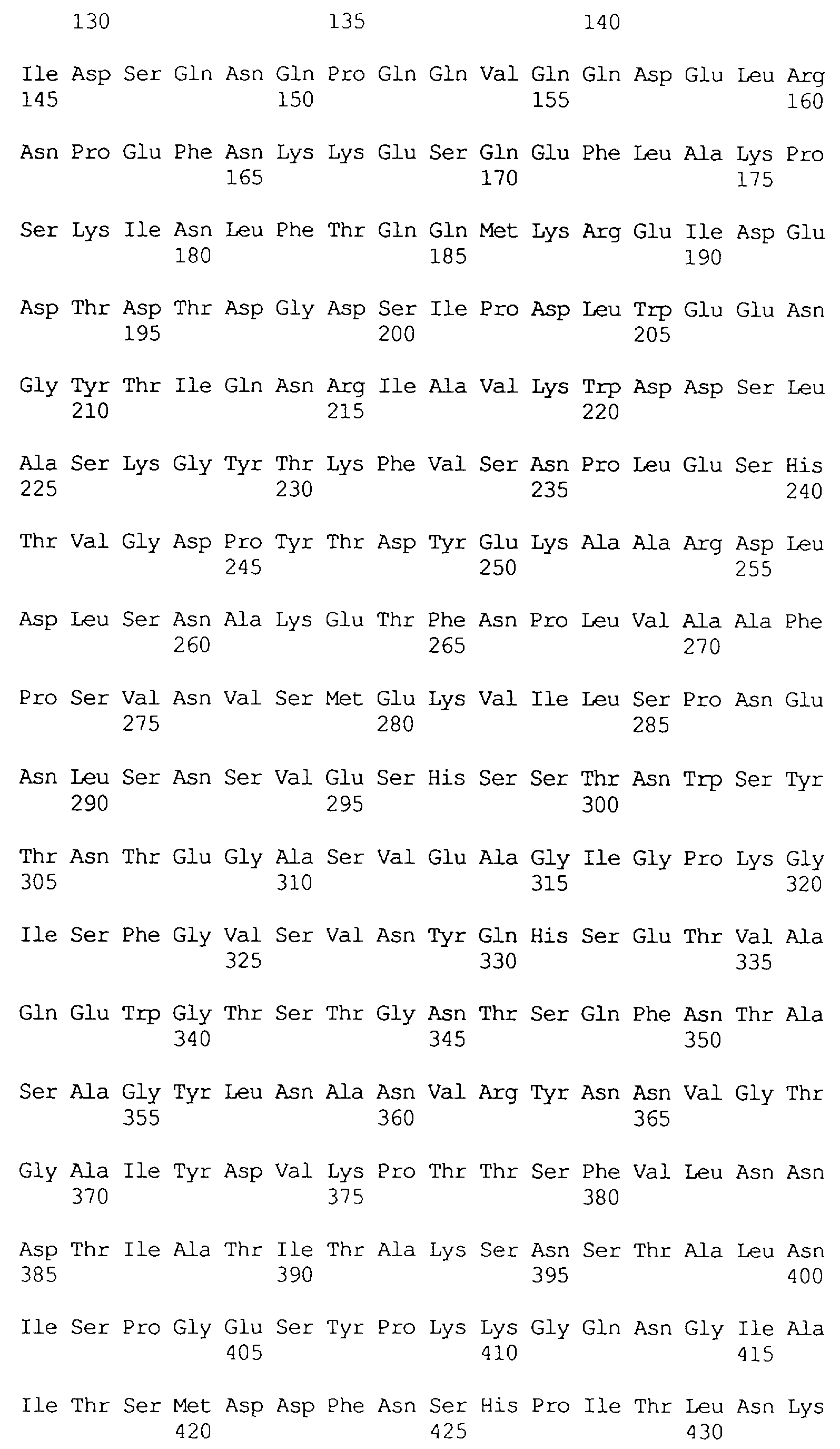




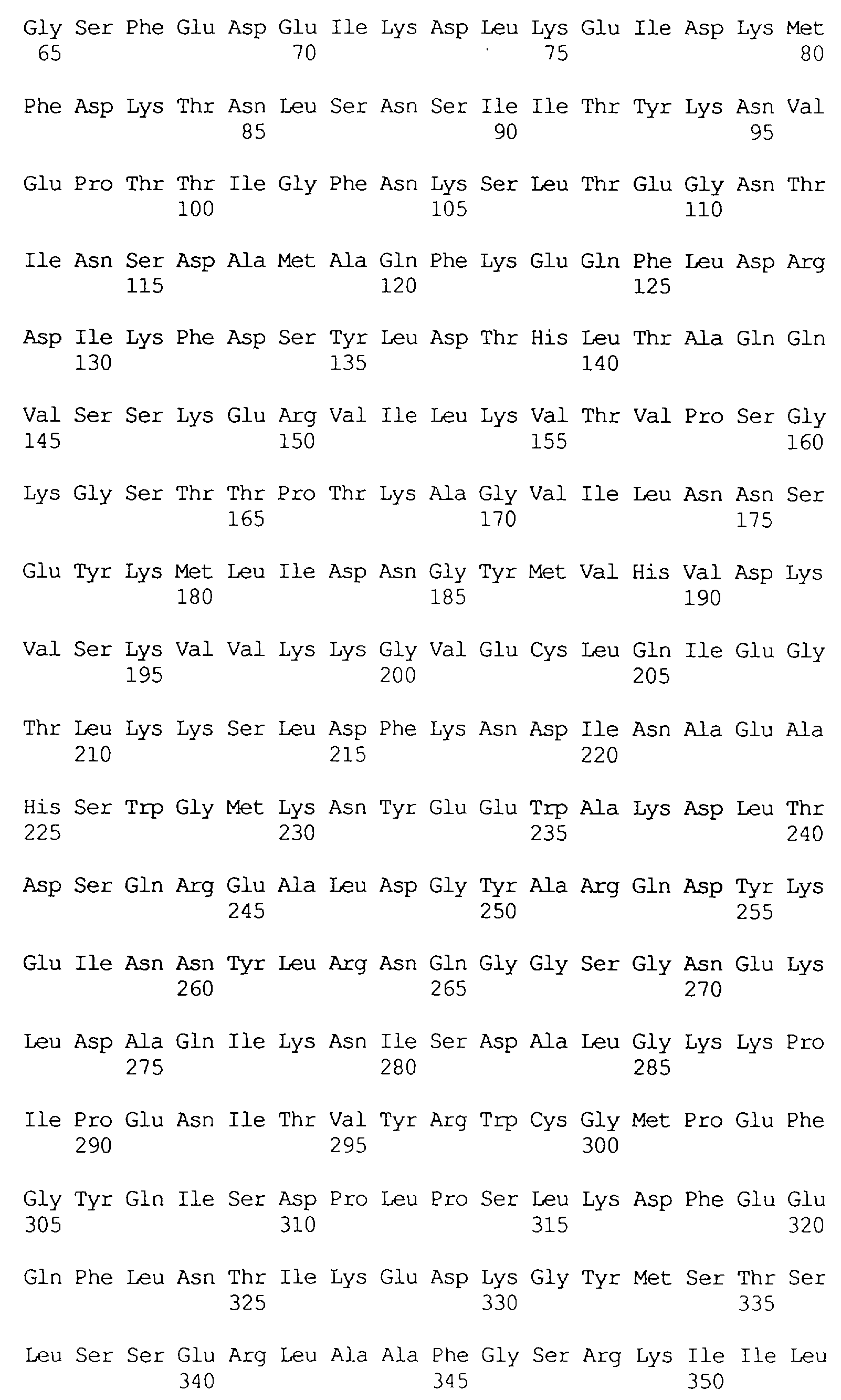











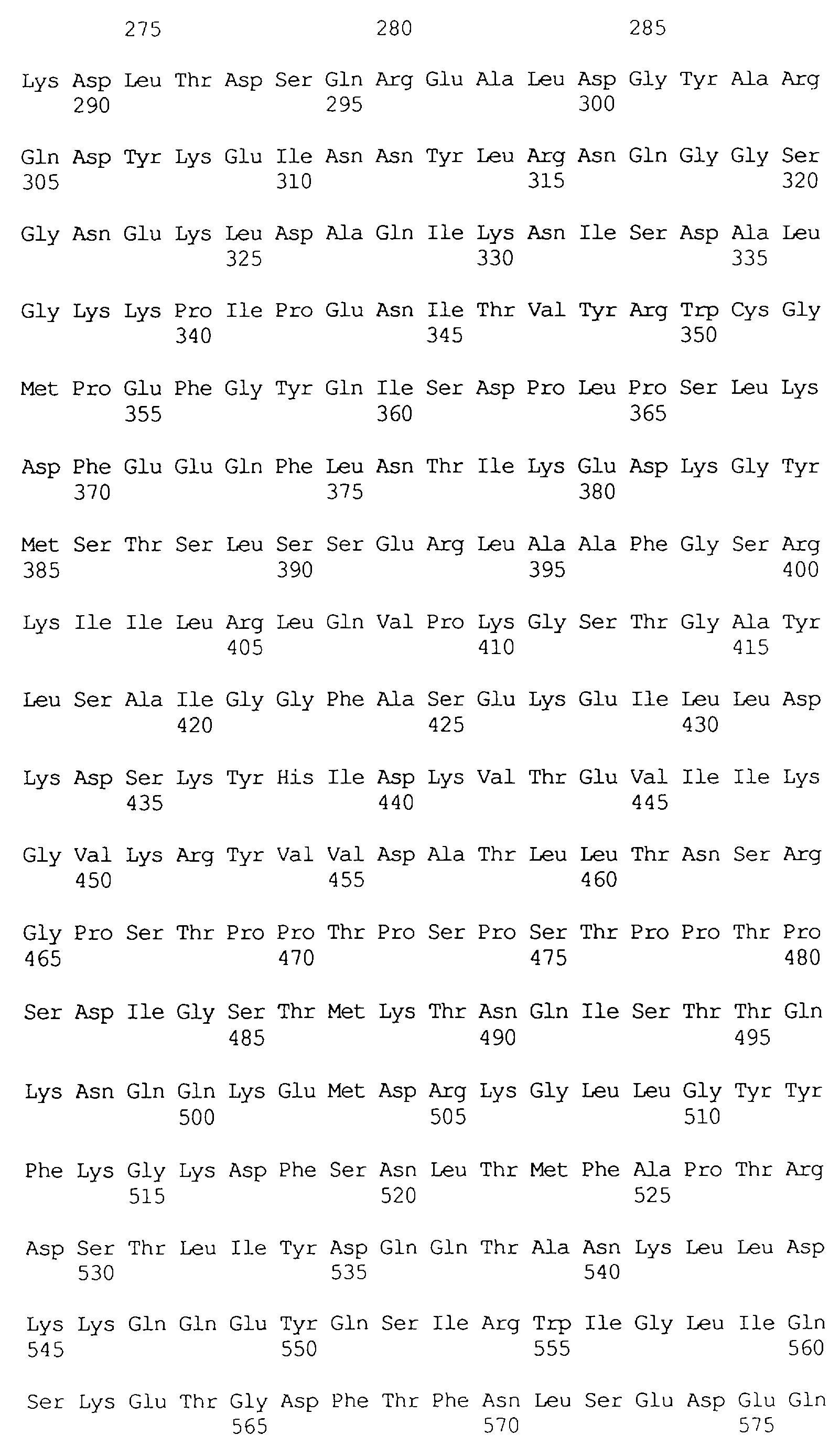
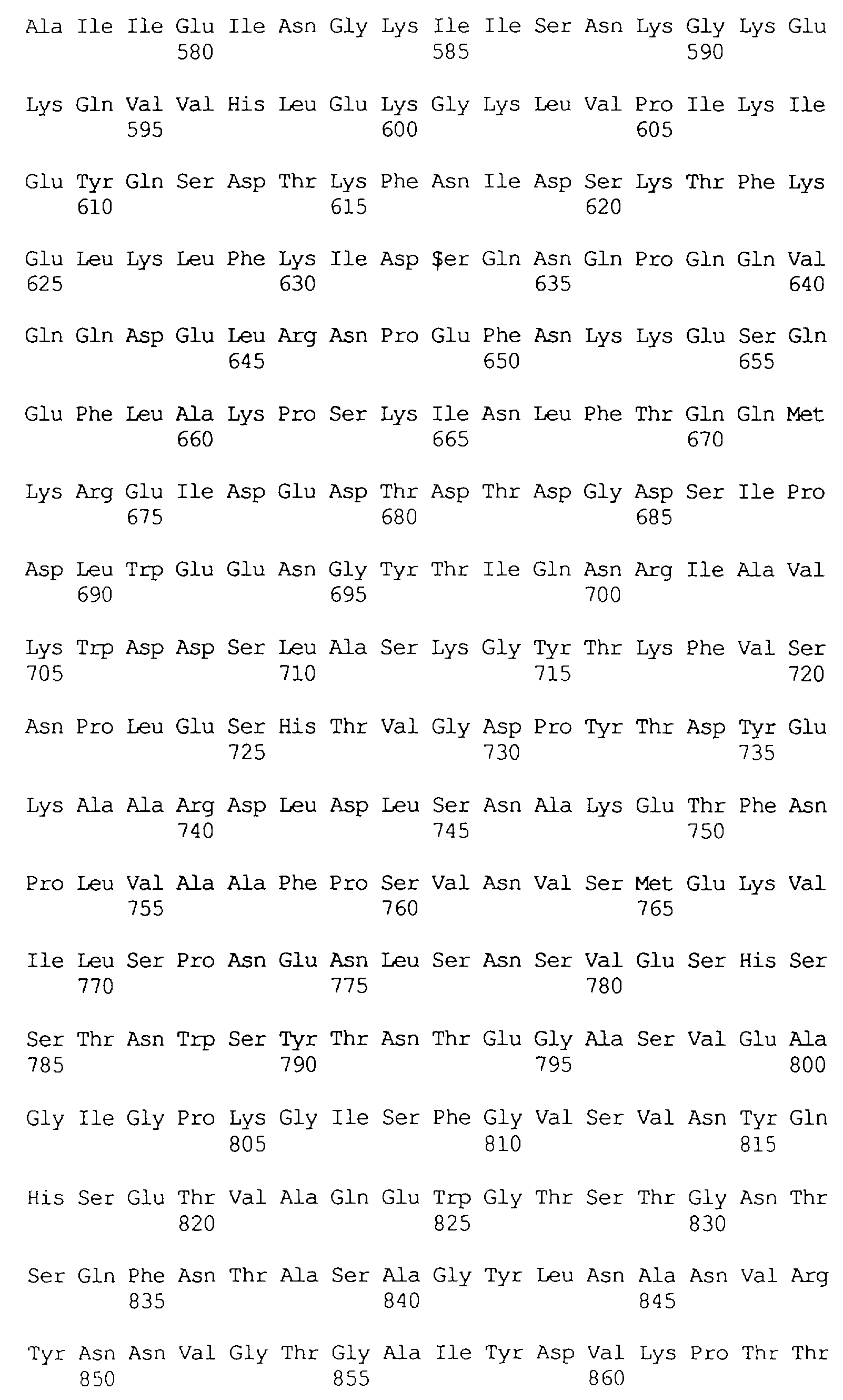
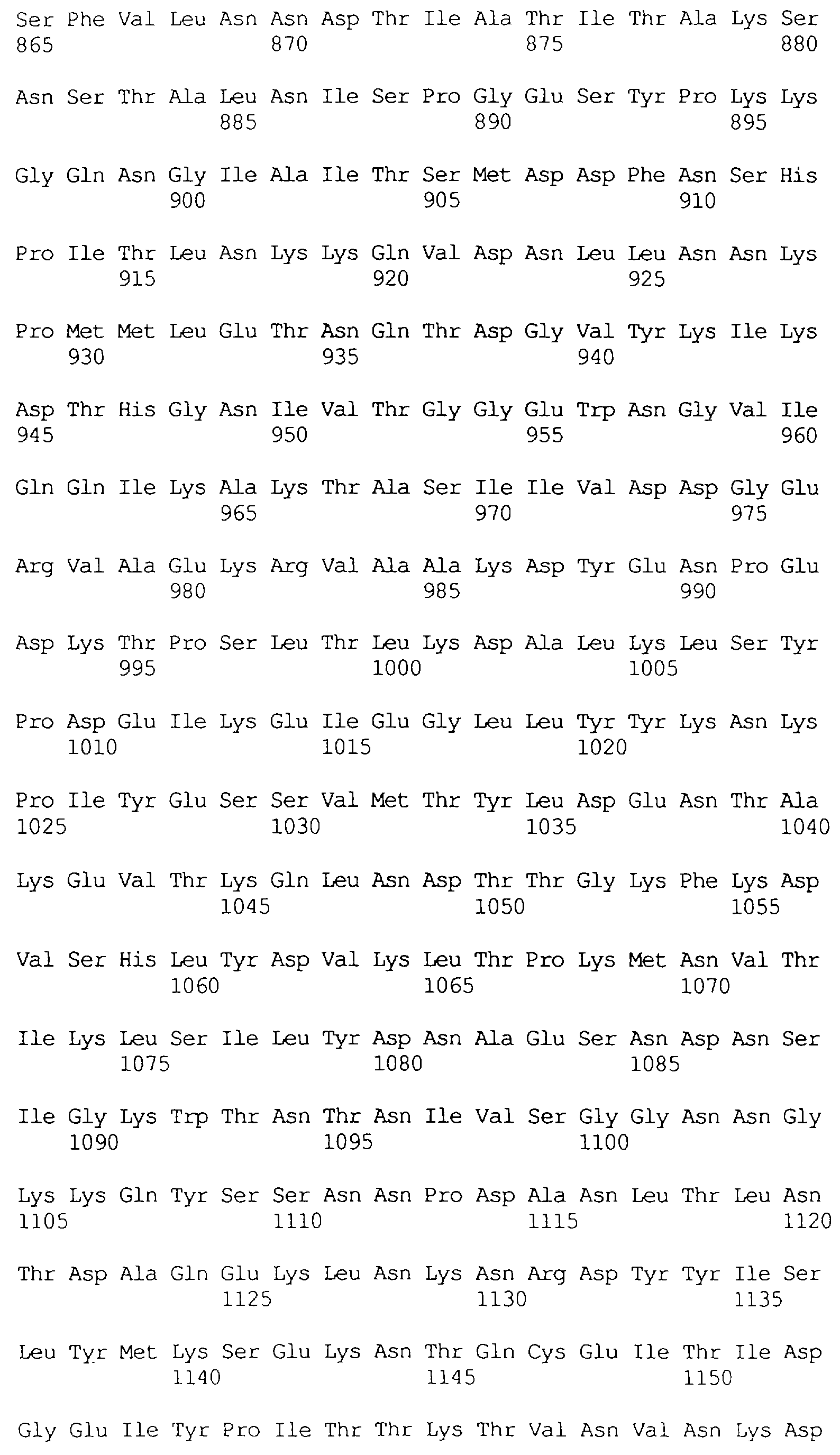



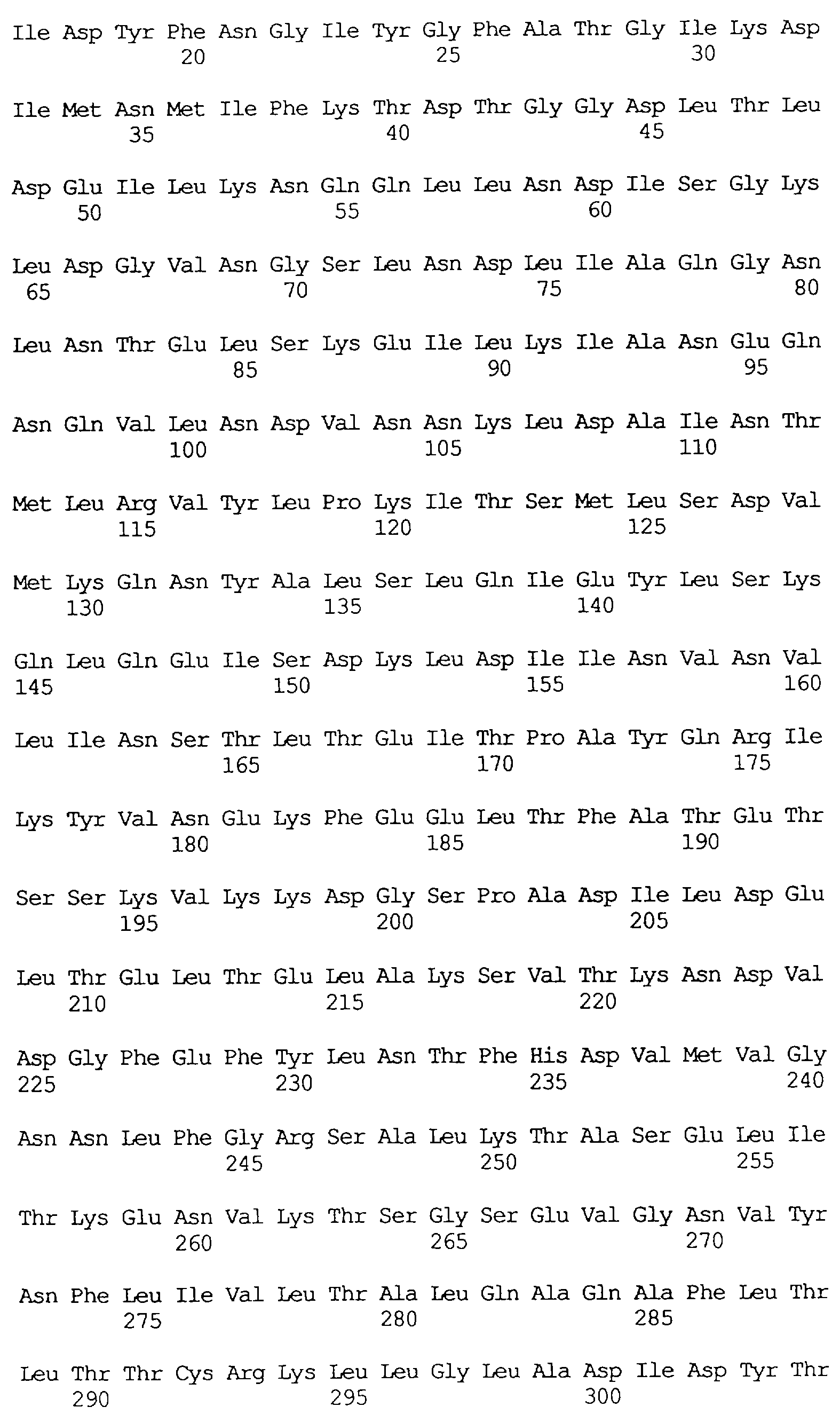
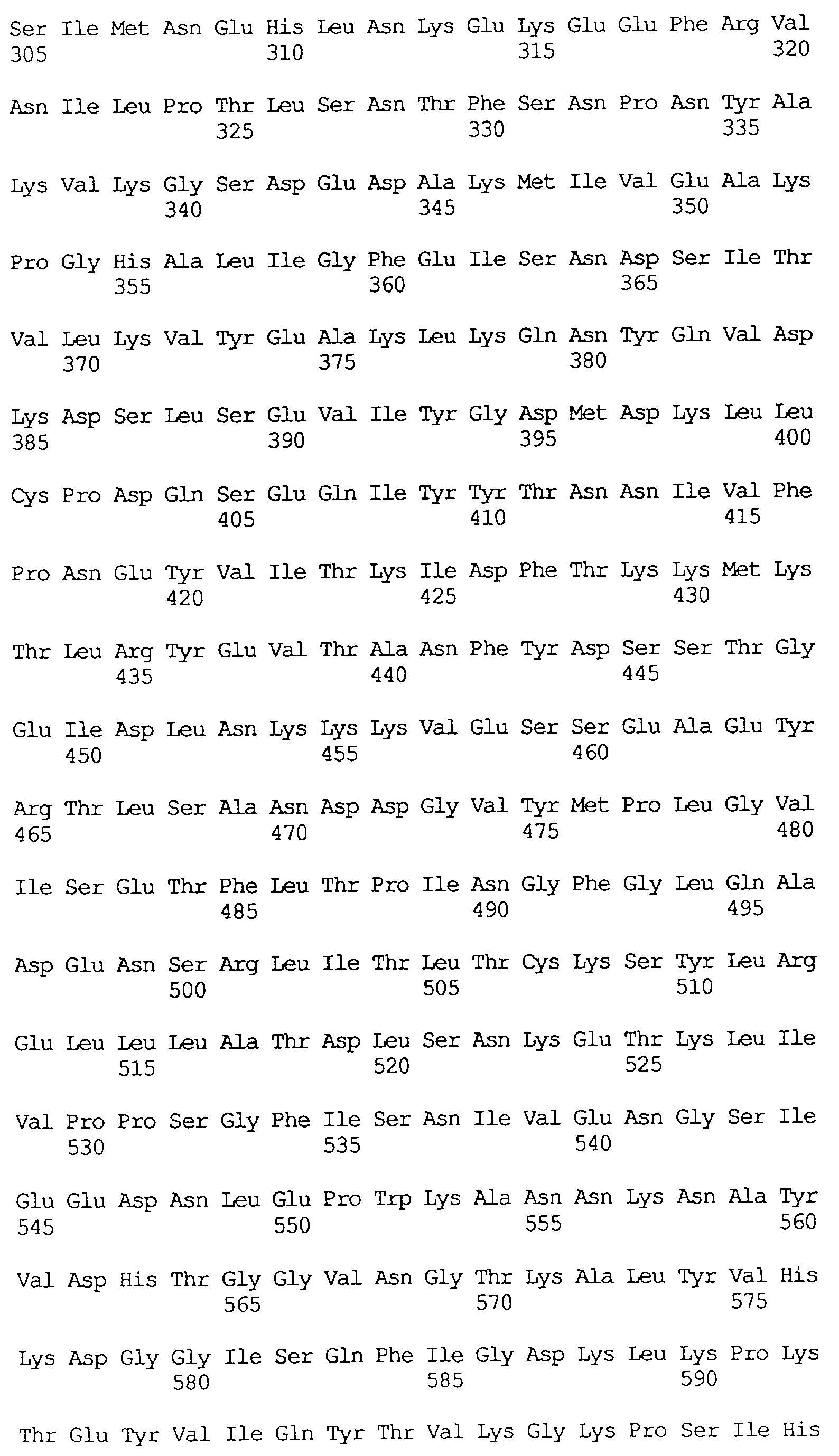





























Описание
Изобретение относится к способам и композициям для борьбы с вредителями растений и другими вредителями. В частности оно относится к новым протеинам с пестицидной активностью, которые могут быть выделены из Bacillus на стадии вегетативного роста. Изобретение относится также к штаммам Bacillus, протеинам и генам, кодирующим протеины. Способы и композиции, также предлагаемые согласно настоящему изобретению, могут быть использованы в различных системах для борьбы с вредителями растений и другими вредителями.
Насекомые-вредители являются основным фактором потери урожая экономически важных сельскохозяйственных культур во всем мире. Для борьбы или полного уничтожения важных с сельскохозяйственной точки зрения вредителей используют широкий спектр химических пестицидов. Тем не менее существенный интерес представляет разработка эффективных альтернативных пестицидов.
Микробиологические пестициды играют важную роль в качестве альтернативы химическому методу борьбы с вредителями. Наиболее широко применяемый микробиологический продукт основан на использовании бактерии Bacillus thuringiensis (Bt). Bt представляет собой грамположительную спорообразующую бактерию рода Bacillus, которая во время споруляции продуцирует инсектицидный кристаллический протеин (ИКП).
Известны многочисленные разновидности Bt, которые продуцируют более 25 различных, но родственных ИКП. Большинство ИКП, продуцируемых Bt, токсичны для личинок определенных видов насекомых из отрядов Lepidoptera (Чешуекрылых), Diptera (Двукрылых) и Coleoptera (Жесткокрылых). Обычно при поедании ИКП чувствительным к нему насекомым кристалл растворяется и превращается с помощью протеаз кишечника насекомого в токсичное производное. Ни один из ИКП, активных в отношении личинок жуков, таких как колорадский жук (Leptinotarsa decemlineata) или большой мучной хрущак (Tenebrio molitor), не проявил существенной эффективности в отношении представителей рода Diabrotica, в частности Diabrotica virgifera virgifera - блошки длинноусой западной (БДЗ) - или Diabrotica longicornis barberi - блошки длинноусой северной.
Bacillus cereus (Bc) во многом схож с Bt. Основным характерным отличием является отсутствие у Вс параспорального кристалла. Вс является широко распространенной бактерией, обычно присутствующей в почве и выделяемой из различных пищевых и лекарственных продуктов. Этот организм принимает участие в порче пищи.
Хотя Bt очень полезна для борьбы с насекомыми-вредителями, необходимо расширять количество потенциальных агентов, предназначенных для биологической борьбы.
Настоящее изобретение относится, таким образом, к композициям и способам борьбы с вредителями растений. В частности оно относится к новым пестицидным протеинам, которые продуцируются штаммами Bacillus на стадии вегетативного роста. Эти протеины могут найти применение в качестве пестицидных агентов.
Настоящее изобретение относится прежде всего к практически очищенному штамму Bacillus, который продуцирует протеин с пестицидной активностью на стадии вегетативного роста, причем этот штамм Bacillus не является В. sphaericus SSII-1. Предпочтительным является штамм Bacillus cereus, имеющий регистрационный номер NRRL В-21058 и Bacillus thuringiensis, имеющий регистрационный номер NRRL В-21060. Также предпочтительным является штамм, выбранный из группы штаммов, имеющих регистрационные номера NRRL В-21224, NRRL В-21225, NRRL В-21226, NRRL В-21227, NRRL В-21228, NRRL В-21229, NRRL В-21230 и NRRL B-21439.
Кроме того, изобретение относится к специфичному в отношении насекомых протеину, который может быть выделен в фазе вегетативного роста из Bacillus spp. и предпочтительно из штамма Bacillus thuringiensis и В. cereus, и к его компонентам, причем этот протеин не является токсичным для комаров из В. sphaericus SSII-1. Специфичный в отношении насекомых протеин по изобретению предпочтительно является токсичным для насекомых из отрядов Coleoptera или Lepidoptera и имеет молекулярную массу приблизительно 30 кДа или более, предпочтительно от приблизительно 60 до приблизительно 100 кДа и более предпочтительно приблизительно 80 кДа.
В частности специфичный в отношении насекомых протеин по изобретению обладает таким спектром инсектицидной активности, который включает активность в отношении видов Agrotis и/или Spodoptera и предпочтительно активность в отношении совки ипсилон [Agrotis ipsilon; СИ], и/или совки травяной [Spodoptera frugiperda], и/или совки малой [Spodoptera exigua], и/или табачной листовертки, и/или совки хлопковой [Helicoverpa zea].
Специфичный в отношении насекомых протеин по изобретению предпочтительно может быть выделен, например, из штамма Bacillus cereus, имеющего регистрационный номер NRRL В-21058, или из Bacillus thuringiensis, имеющего регистрационный номер NRRL B-21060.
Специфичный в отношении насекомых протеин по изобретению предпочтительно может быть выделен из штамма Bacillus spp., выбранного из группы штаммов, имеющих регистрационные номера NRRL В-21224, NRRL В-21225, NRRL B-21226, NRRL B-21227, NRRL B-21228, NRRL B-21229, NRRL В-21230 и NRRL B-21439.
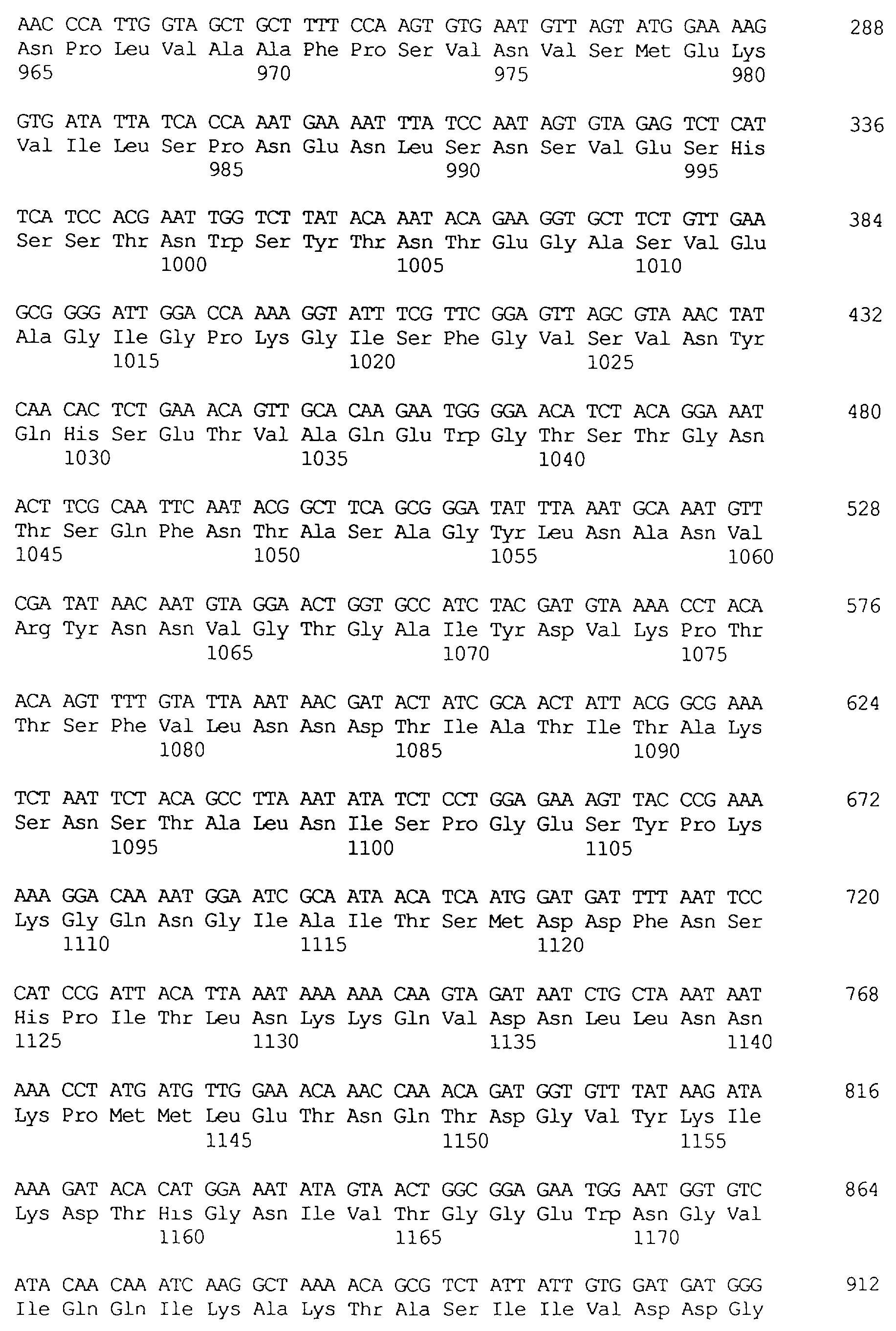
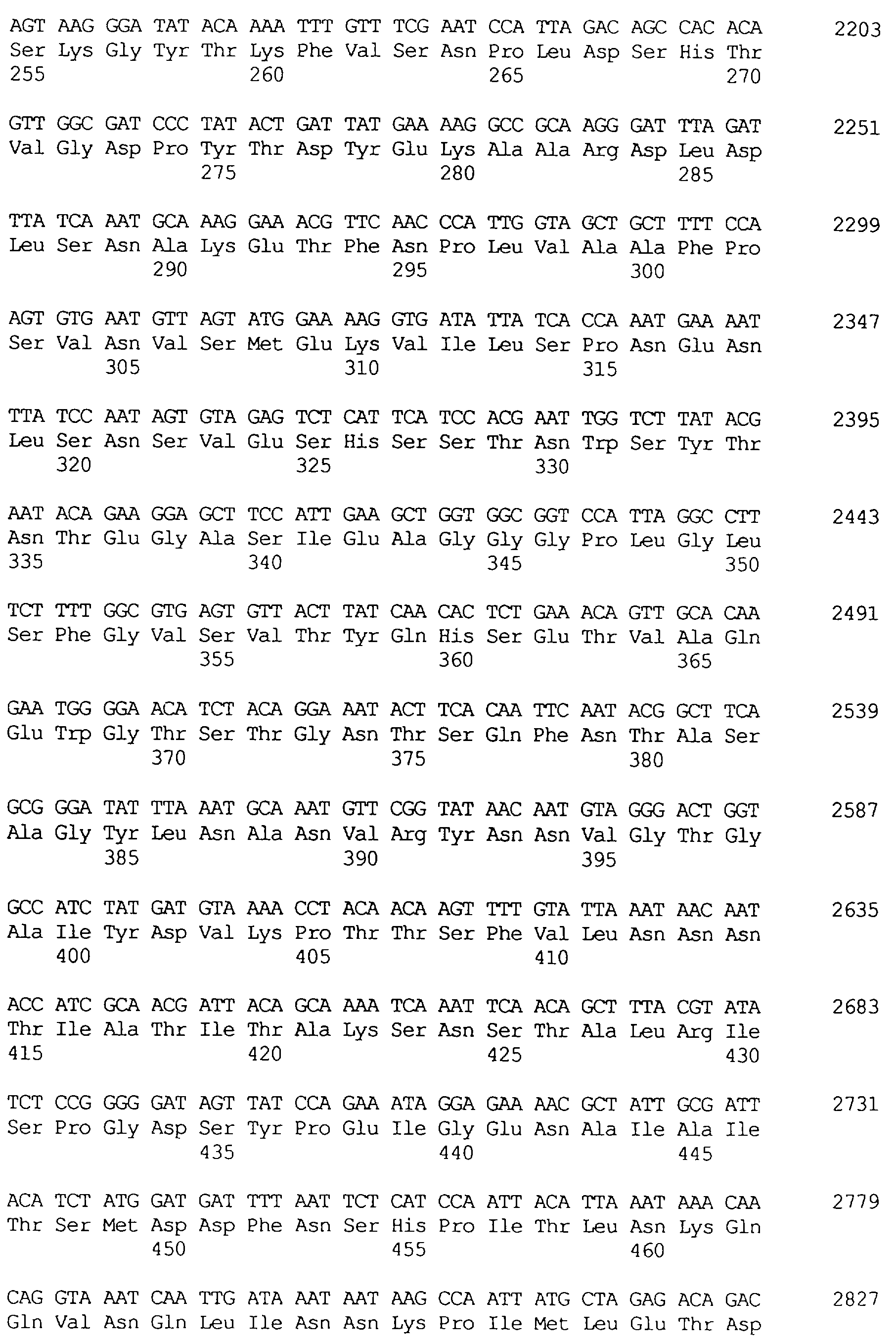
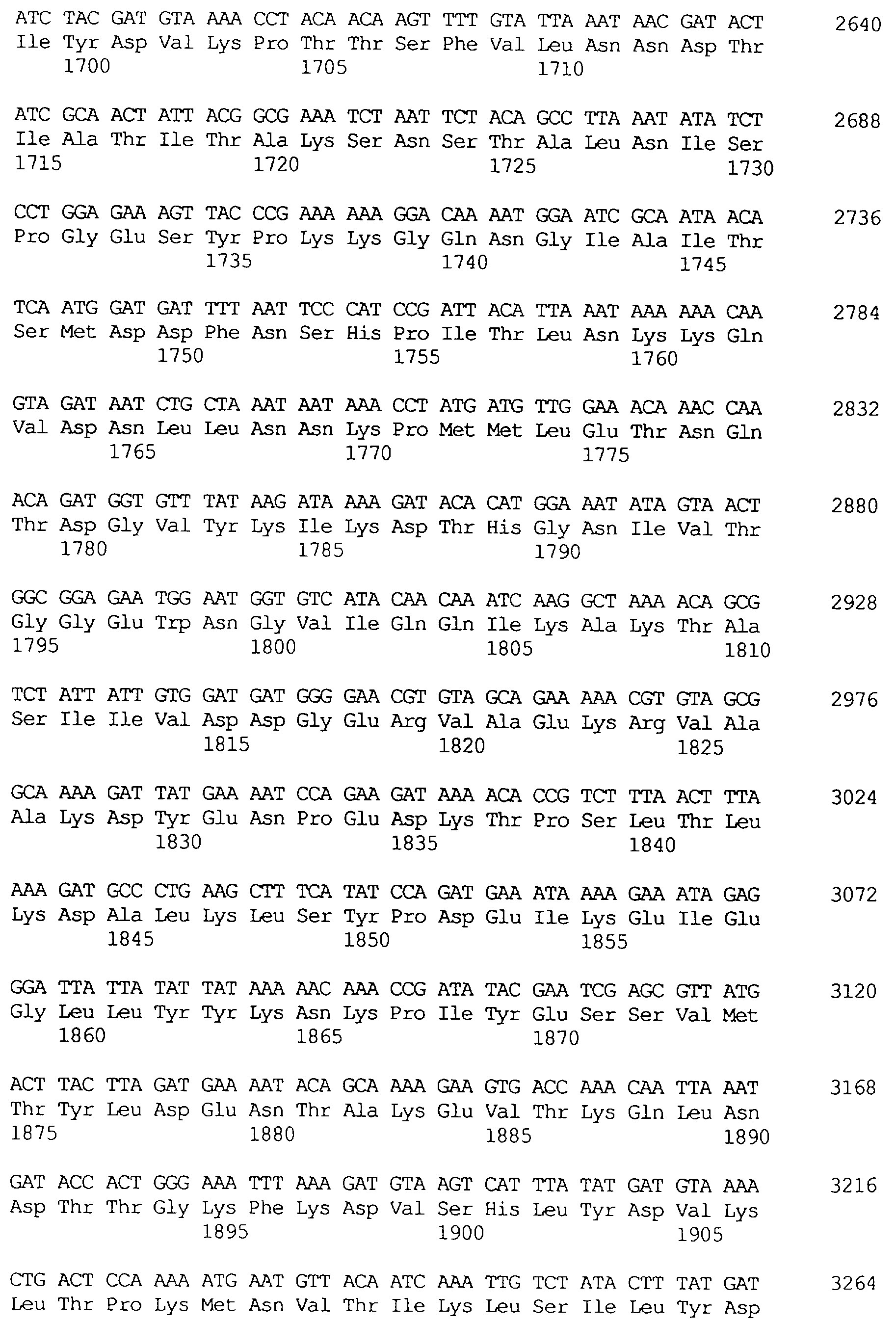
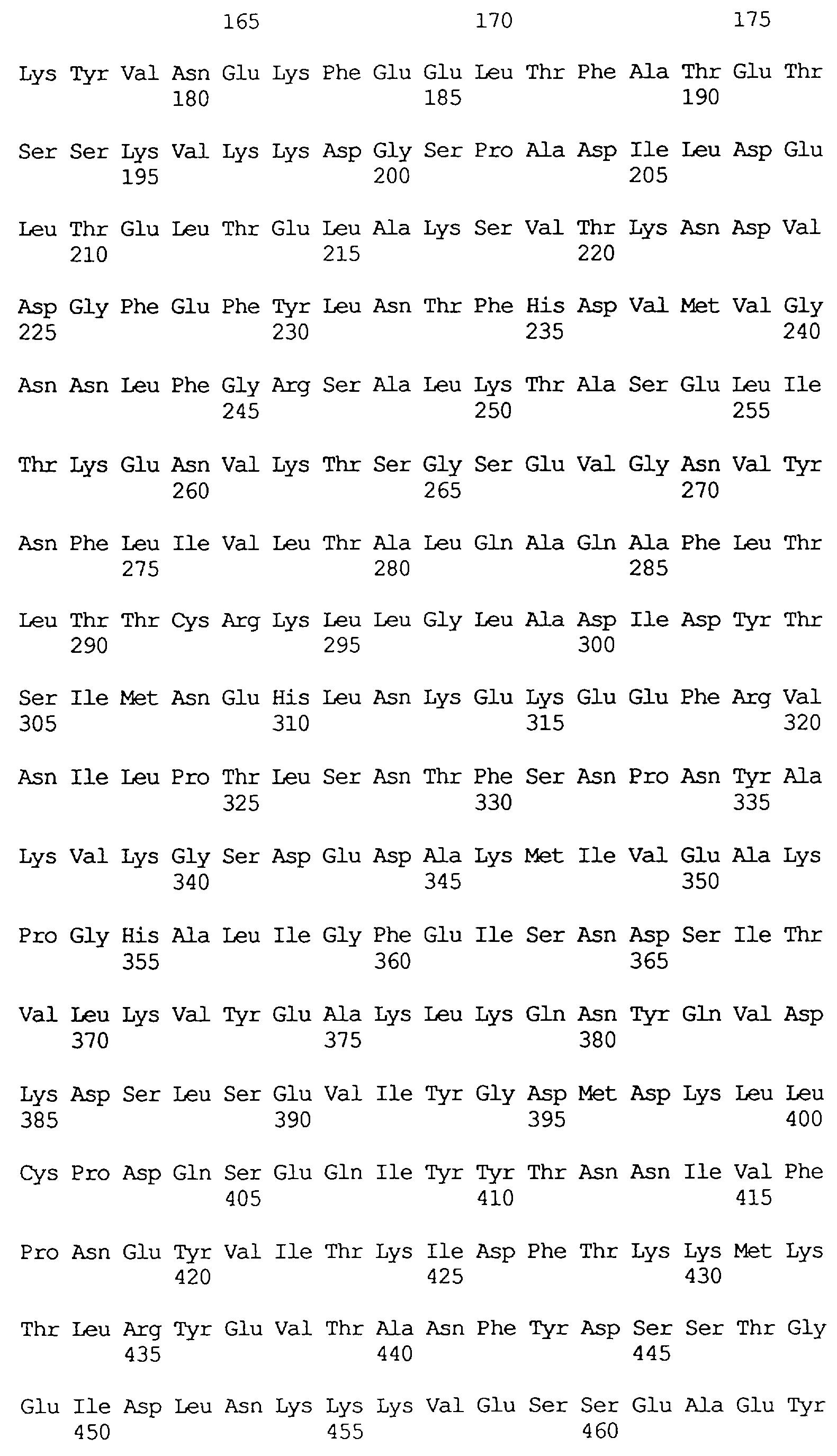
В частности в объем настоящего изобретения включен специфичный в отношении насекомых протеин, который имеет аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO: 5 и SEQ ID NO: 7, включая любые протеины, которые структурно и/или функционально являются его гомологами.
Кроме того, предпочтительным является специфичный в отношении насекомых протеин, когда этот протеин имеет последовательность, выбранную из группы, состоящей из SEQ ID NO: 20, SEQ ID NO: 21, SEQ ID NO: 29, SEQ ID NO: 32 и SEQ ID NO: 2, включая любые протеины, которые структурно и/или функционально являются его гомологами.
Особенно предпочтительным является специфичный в отношении насекомых протеин, когда этот протеин имеет последовательность, выбранную из группы, состоящей из SEQ ID NO: 29 и SEQ ID NO: 32, включая любые протеины, которые структурно и/или функционально являются его гомологами.
Кроме того, предпочтительный вариант осуществления изобретения включает специфичный в отношении насекомых протеин по изобретению, в котором последовательности, представляющие собой сигнал секреции, были удалены или инактивированы.
В объем настоящего изобретения, кроме того, включены вспомогательные протеины, которые усиливают специфичную в отношении насекомых активность протеина, специфичного в отношении насекомых. Эти вспомогательные протеины предпочтительно имеют молекулярную массу приблизительно 50 кДа и могут быть выделены, например, из штамма Bacillus cereus во время фазы вегетативного роста и особенно предпочтительно из штамма Bacillus cereus AB78.
В предпочтительном варианте осуществления изобретение относится к вспомогательному протеину, в котором последовательности, представляющие собой сигнал секреции, были удалены или инактивированы.
Кроме того, настоящее изобретение относится к обладающим пестицидной активностью многомерным протеинам, которые содержат более одной полипептидной цепи и в которых по крайней мере одна из полипептидных цепей представляет собой специфичный в отношении насекомых протеин по изобретению, а по крайней мере одна из полипептидных цепей представляет собой вспомогательный протеин по изобретению, который активирует или усиливает пестицидную активность специфичного в отношении насекомых протеина.
Многомерные протеины по изобретению, обладающие пестицидной активностью, предпочтительно имеют молекулярную массу от приблизительно 50 кДа до приблизительно 200 кДа.
В объем изобретения включен, в частности, обладающий пестицидной активностью многомерный протеин, который содержит специфичный в отношении насекомых протеин по изобретению и вспомогательный протеин по изобретению, который активирует или усиливает пестицидную активность специфичного в отношении насекомых протеина.
Кроме того, настоящее изобретение относится к слитым протеинам, содержащим несколько протеиновых доменов, включающих по крайней мере специфичный в отношении насекомых протеин по изобретению и/или вспомогательный протеин по изобретению, образующихся посредством генетических слияний, которые при трансляции рибосомами продуцируют слитый протеин, сочетающий в себе по крайней мере свойства специфичного в отношении насекомых протеина по изобретению и/или вспомогательного протеина по изобретению и необязательно других компонентов, применяемых при слиянии.
Один из вариантов осуществления изобретения относится к слитому протеину, содержащему рибонуклеазный S-протеин, специфичный в отношении насекомых протеин по изобретению и вспомогательный протеин по изобретению.
Кроме того, еще один вариант осуществления изобретения относится к слитому протеину, содержащему специфичный в отношении насекомых протеин по изобретению и вспомогательный протеин по изобретению, причем либо специфичный в отношении насекомых протеин, либо вспомогательный протеин находятся на N-конце слитого протеина.
Предпочтительным является слитый протеин, который содержит специфичный в отношении насекомых протеин, представленный в SEQ ID NO: 5, и вспомогательный протеин, представленный в SEQ ID NO: 2, что приводит к образованию протеина, представленному в SEQ ID NO: 23, включая любые протеины, которые структурно и/или функционально являются его гомологами.
Также предпочтительным является слитый протеин, содержащий специфичный в отношении насекомых протеин, представленный в SEQ ID NO:35, и вспомогательный протеин, представленный в SEQ ID NO: 27, что приводит к образованию протеина, представленного в SEQ ID NO: 50, включая любые протеины, которые структурно и/или функционально являются его гомологами.
Кроме того, изобретение относится к слитому протеину, содержащему специфичный в отношении насекомых протеин по изобретению и/или вспомогательный протеин по изобретению, слитый с сигнальной последовательностью, предпочтительно с секретирующей сигнальной последовательностью или с последовательностью, обеспечивающей целенаправленную доставку, которая направляет трансгенный продукт к определенной органелле или компартменту клетки, причем сигнальная последовательность является гетерологичной по происхождению по отношению к протеину-реципиенту.
Особенно предпочтительным по изобретению является слитый протеин, когда этот протеин имеет последовательность, представленную в SEQ ID NO: 43 или в SEQ ID NO: 46, включая любые протеины, которые структурно и/или функционально являются его гомологами.
В контексте настоящего изобретения такое понятие, как "практически гомологичная последовательность", обозначает близкое структурное сходство между последовательностями аминокислот. Например, практически гомологичные протеины могут быть гомологичными на 40%, предпочтительно на 50% и наиболее предпочтительно гомологичными на 60% или 80% или более. Гомология также включает сходство, когда отсутствуют одна или несколько субпоследовательностей аминокислот или когда включены субпоследовательности с дополнительными аминокислотами.
Еще один предмет изобретения относится к молекуле ДНК, содержащей нуклеотидную последовательность, которая кодирует специфичный в отношении насекомых протеин, который может быть выделен в фазе вегетативного роста из Bacillus spp., и его компоненты, причем этот протеин не является токсичным для комаров из В. sphaericus SSII-1. В частности настоящее изобретение относится к молекуле ДНК, содержащей нуклеотидную последовательность, которая кодирует специфичный в отношении насекомых протеин, причем спектр его инсектицидной активности включает активность в отношении видов Agrotis и/или Spodoptera и предпочтительно активность в отношении совки ипсилон [Agrotis ipsilon; СИ], и/или совки травяной ISpodoptera frugiperda], и/или совки малой [Spodoptera exigua], и/или табачной листовертки, и/или совки хлопковой [Helicoverpa zea] .
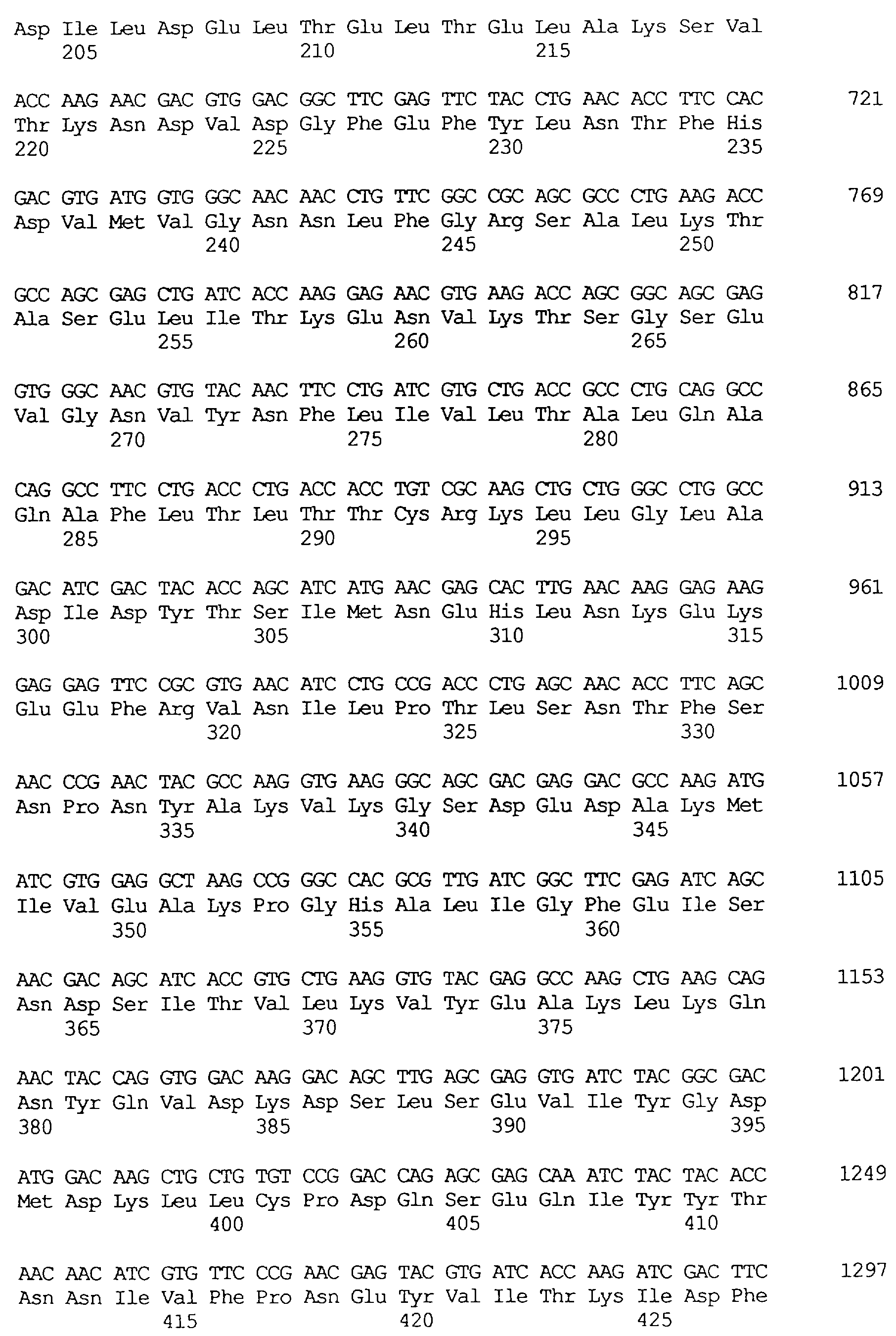
Предпочтительной является молекула ДНК, когда эта молекула содержит нуклеотидную последовательность, представленную в SEQ ID NO: 4 или SEQ ID NO: 6, включая любые молекулы ДНК, которые являются ее структурными и/или функциональными гомологами.
Также предпочтительной является молекула ДНК, когда эта молекула содержит нуклеотидную последовательность, представленную в SEQ ID NO: 19, SEQ ID NO: 28, SEQ ID NO: 31 или SEQ ID NO: 1, включая любые молекулы ДНК, которые являются ее структурными и/или функциональными гомологами.
Кроме того, изобретение относится к молекуле ДНК, содержащей нуклеотидную последовательность, которая кодирует вспомогательный протеин по изобретению, усиливающий специфичную в отношении насекомых активность протеина, специфичного в отношении насекомых.
Предпочтительной является молекула ДНК, когда эта молекула содержит нуклеотидную последовательность, представленную в SEQ ID NO: 19, включая любые молекулы ДНК, которые являются ее структурными и/или функциональными гомологами.
Еще один вариант осуществления изобретения относится к молекуле ДНК, содержащей нуклеотидную последовательность, кодирующую специфичный в отношении насекомых протеин, который может быть выделен в фазе вегетативного роста из Bacillus spp. , и его компоненты, когда этот протеин не является токсичным для комаров из В. sphaericus SSII-1, причем эта нуклеотидная последовательность оптимизирована для экспрессии в микроорганизме или в растении.
Предпочтительной является молекула ДНК, когда эта молекула содержит нуклеотидную последовательность, представленную в SEQ ID NO: 17 или SEQ ID NO: 18, включая любые молекулы ДНК, которые являются ее структурными и/или функциональными гомологами.
Также предпочтительной является молекула ДНК, когда эта молекула содержит нуклеотидную последовательность, представленную в SEQ ID NO: 24, SEQ ID NO: 26, SEQ ID NO: 27 или SEQ ID NO: 30, включая любые молекулы ДНК, которые являются ее структурными и/или функциональными гомологами.
Кроме того, изобретение относится к молекуле ДНК, которая содержит нуклеотидную последовательность, кодирующую обладающий пестицидной активностью многомерный протеин, который содержит более одной полипептидной цепи и в котором по крайней мере одна из полипептидных цепей представляет собой специфичный в отношении насекомых протеин по изобретению, а по крайней мере одна из полипептидных цепей представляет собой вспомогательный протеин по изобретению, который активирует или усиливает пестицидную активность специфичного в отношении насекомых протеина.
Предпочтительной является молекула ДНК, которая содержит нуклеотидную последовательность, кодирующую специфичный в отношении насекомых протеин по изобретению и вспомогательный протеин по изобретению, который активирует или усиливает пестицидную активность специфичного в отношении насекомых протеина.
Особенно предпочтительной является молекула ДНК, когда эта молекула содержит нуклеотидную последовательность, представленную в SEQ ID NO: 1 или SEQ ID NO: 19, включая любые нуклеотидные последовательности, которые являются ее структурными и/или функциональными гомологами.
Еще один вариант осуществления изобретения относится к молекуле ДНК, которая содержит нуклеотидную последовательность, кодирующую слитый протеин, который содержит несколько протеиновых доменов, включающих по крайней мере специфичный в отношении насекомых протеин по изобретению и/или вспомогательный протеин по изобретению, образуемый посредством генетических слияний, и которая при трансляции на рибосомах продуцирует слитый протеин, который по крайней мере сочетает в себе свойства специфичного в отношении насекомых протеина по изобретению и/или вспомогательного протеина по изобретению и необязательно других компонентов, применяемых при слиянии.
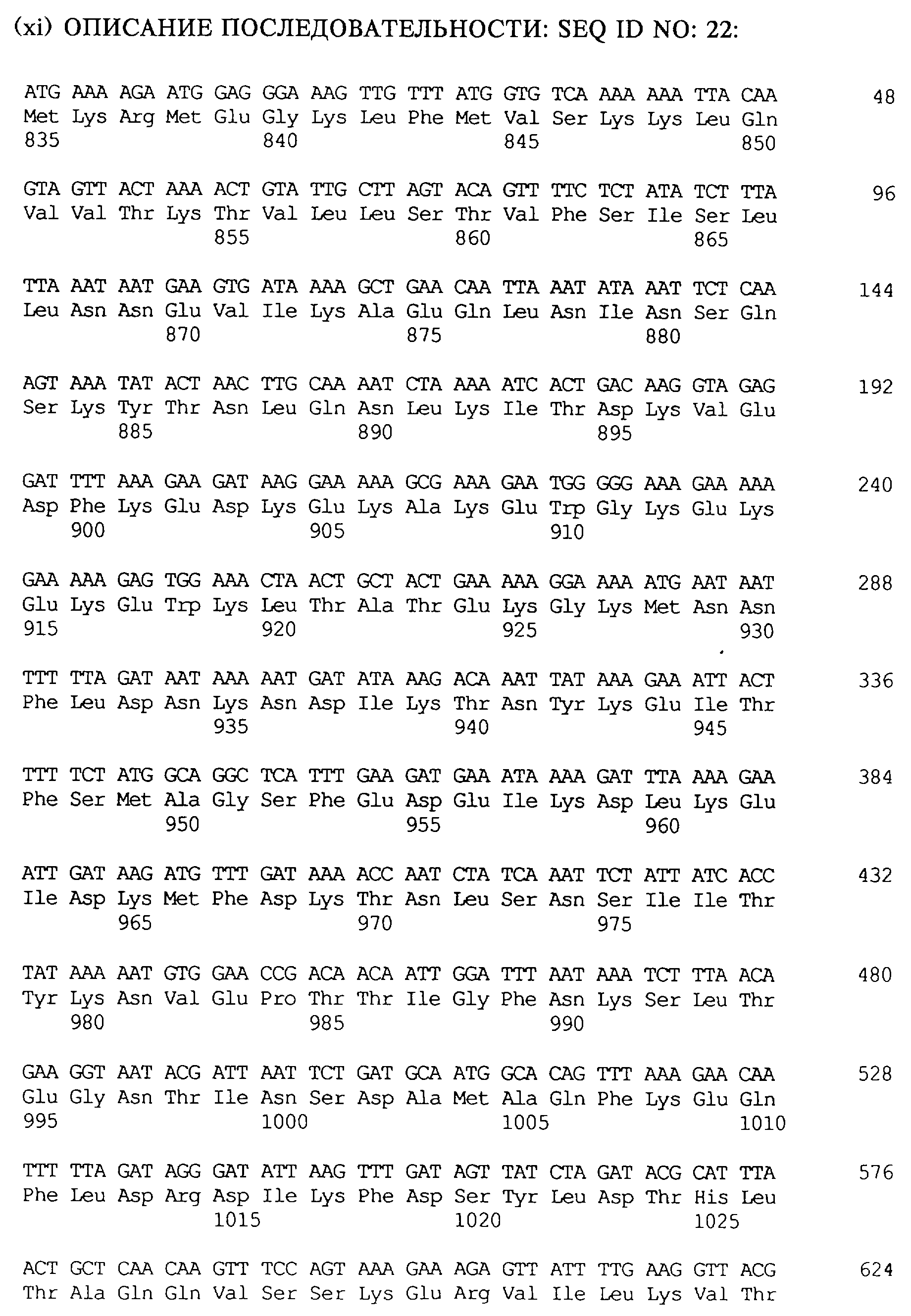
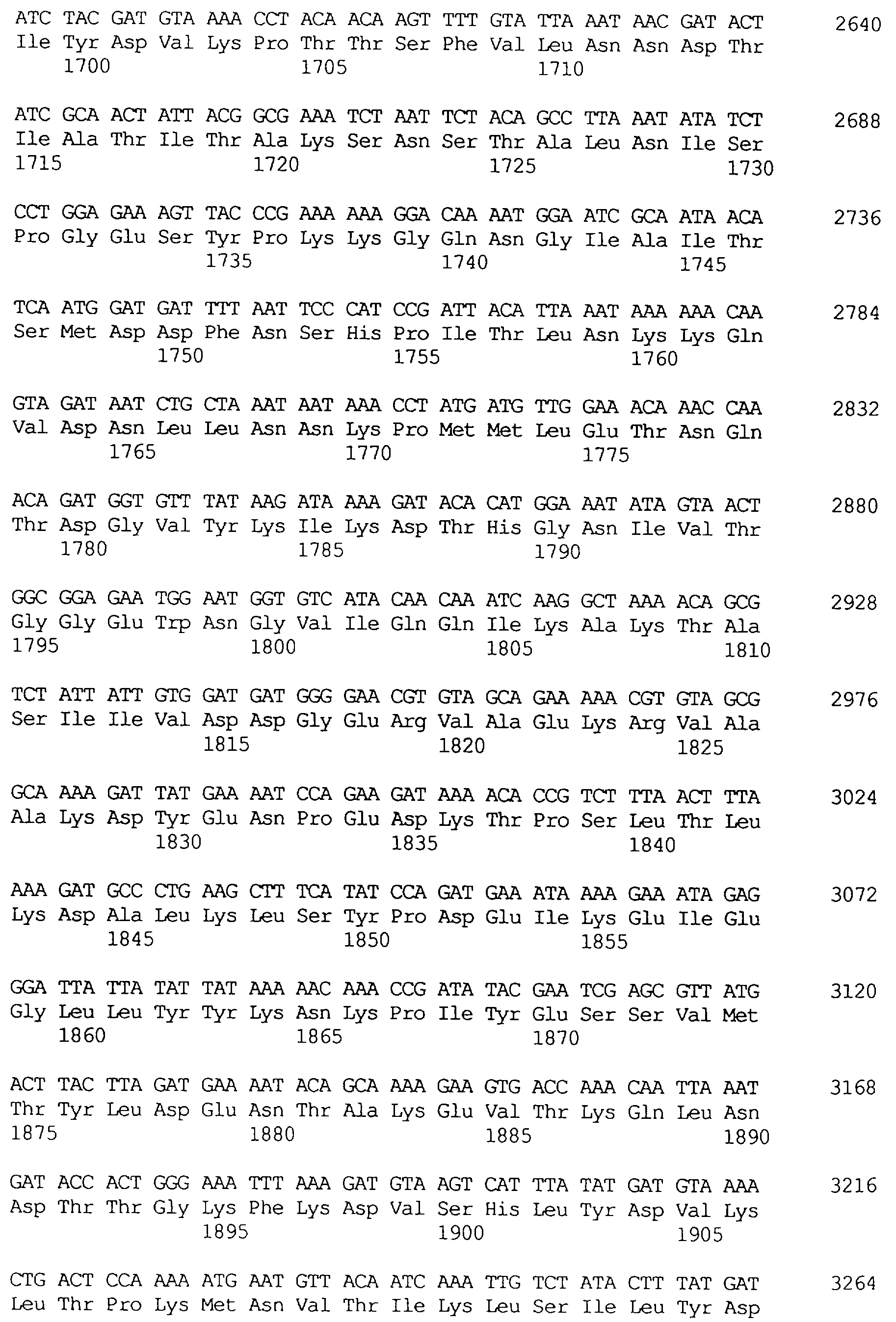
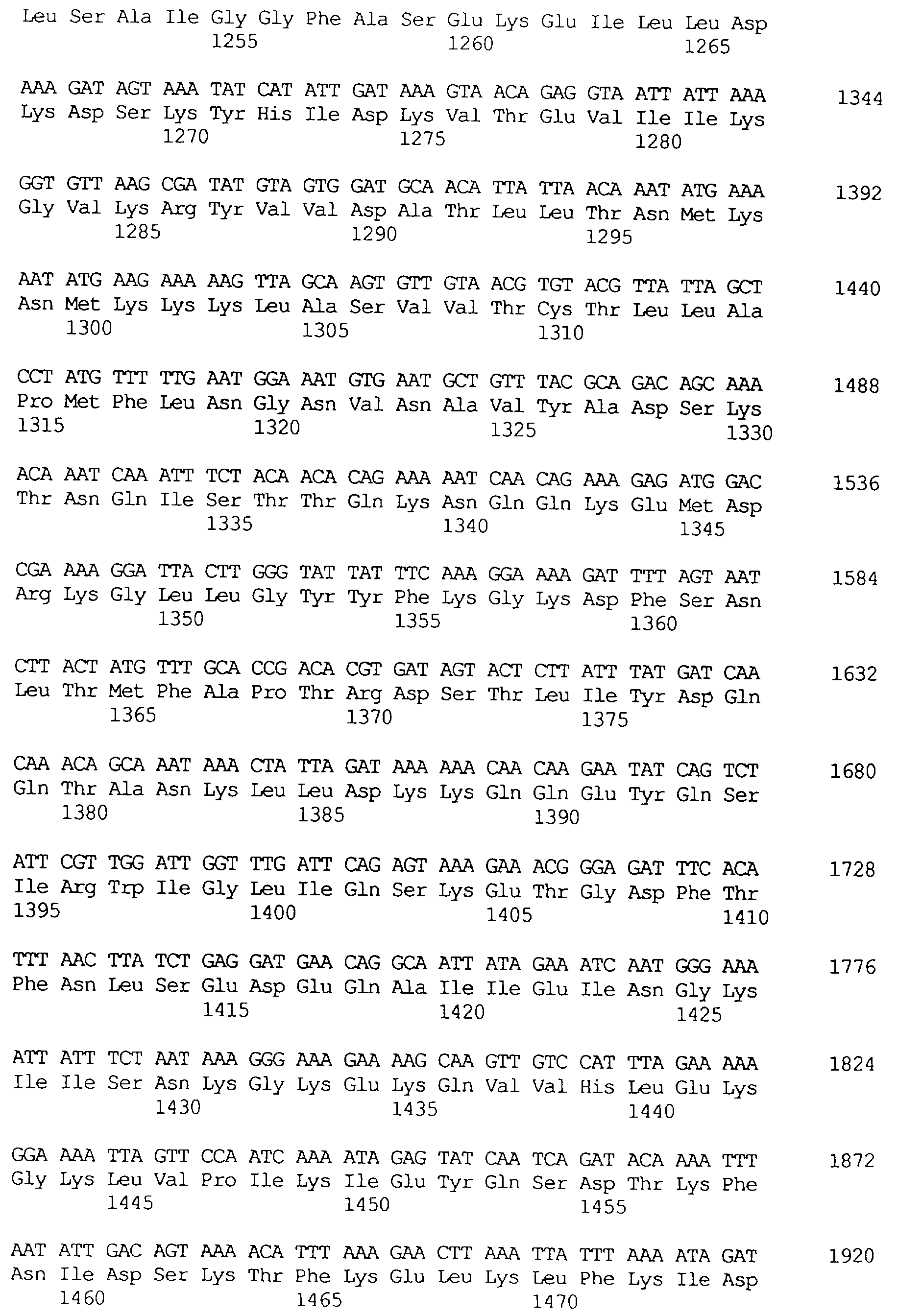
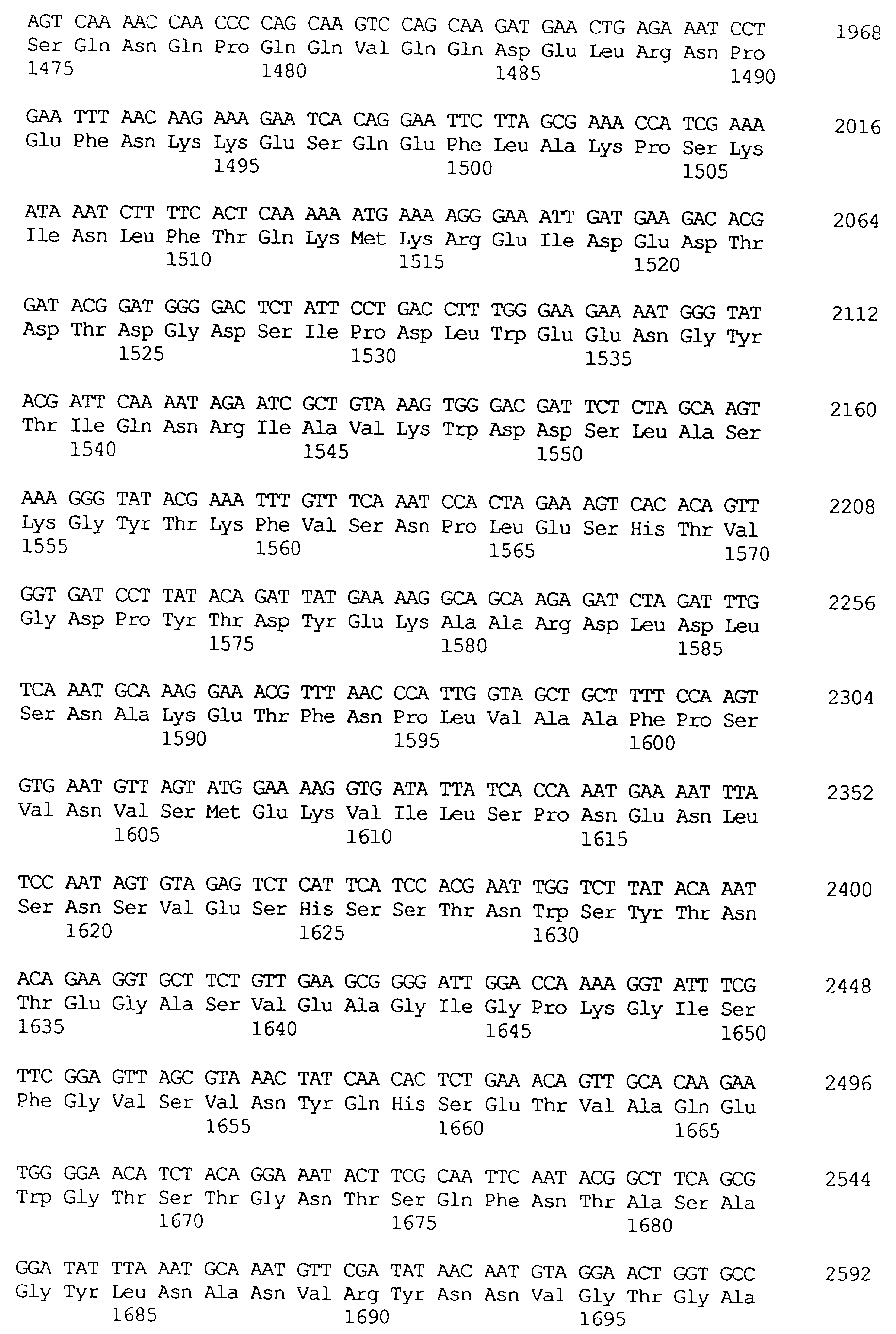
Предпочтительной по изобретению является молекула ДНК, которая содержит нуклеотидную последовательность, кодирующую слитый протеин, содержащий специфичный в отношении насекомых протеин по изобретению и вспомогательный протеин по изобретению, причем либо специфичный в отношении насекомых протеин, либо вспомогательный протеин находятся на N-конце слитого протеина. Особенно предпочтительной является молекула ДНК, когда эта молекула содержит нуклеотидную последовательность, представленную в SEQ ID NO: 22, включая любые молекулы ДНК, которые являются ее структурными и/или функциональными гомологами.
Кроме того, изобретение относится к молекуле ДНК, которая содержит нуклеотидную последовательность, кодирующую слитый протеин, содержащий специфичный в отношении насекомых протеин по изобретению и/или вспомогательный протеин по изобретению, слитый с сигнальной последовательностью, предпочтительно с секретирующей сигнальной последовательностью или с последовательностью, обеспечивающей целенаправленную доставку, которая направляет трансгенный продукт к конкретной органелле или компартменту клетки, причем сигнальная последовательность является гетерологичной по происхождению по отношению к ДНК-реципиенту.
В объем настоящего изобретения, кроме того, включена молекула ДНК, которая содержит нуклеотидную последовательность, кодирующую слитый протеин или многомерный протеин по изобретению, и которая оптимизирована для экспрессии в микроорганизме или в растении.
Предпочтительной является оптимизированная молекула ДНК, причем эта молекула содержит нуклеотидную последовательность, представленную в SEQ ID NO: 42, SEQ ID NO: 45 или SEQ ID NO:49, включая любые молекулы ДНК, которые являются ее структурными и/или функциональными гомологами.
Кроме того, изобретение относится к оптимизированной молекуле ДНК, в которой последовательности, кодирующие сигнал секреции, удалены с ее 5'- конца, и прежде всего к оптимизированной молекуле ДНК, когда эта молекула содержит нуклеотидную последовательность, представленную в SEQ ID NO: 35 или SEQ ID NO: 39, включая любые молекулы ДНК, которые являются ее структурными и/или функциональными гомологами.
В контексте настоящего изобретения такое понятие, как "практически гомологичная последовательность", обозначает близкое структурное сходство между последовательностями нуклеотидов. Например, практически гомологичные молекулы ДНК могут быть гомологичными на 60%, предпочтительно на 80% и наиболее предпочтительно гомологичными на 90% или 95% или более. Гомология также включает сходство, когда одна или несколько субпоследовательностей нуклеотидов или аминокислот отсутствуют или когда включены субпоследовательности с дополнительными нуклеотидами или аминокислотами.
Настоящее изобретение также включает молекулы ДНК, которые гибридизируются в умеренно строгих условиях с молекулой ДНК по изобретению, как она определена выше в настоящем описании, и предпочтительно с олигонуклеотидным зондом, который получают из этой молекулы и который включает смежную часть кодирующей последовательности для специфичного в отношении насекомых протеина длиной по крайней мере 10 нуклеотидов, причем эти молекулы имеют специфичную в отношении насекомых активность, и эти молекулы ДНК также кодируют специфичные в отношении насекомых протеины.
Предпочтительными являются молекулы ДНК, когда гибридизация происходит при 65oС в буфере, содержащем 7%-ный ДСН (додецилсульфат натрия) и 0,5М фосфат натрия.
Особенно предпочтительной является молекула ДНК, которая содержит нуклеотидную последовательность, кодирующую специфичный в отношении
насекомых протеин по изобретению, и которую получают способом, включающим:
(а) получение молекулы ДНК, содержащей нуклеотидную последовательность, кодирующую специфичный в отношении насекомых
протеин;
(б) гибридизацию этой молекулы ДНК с олигонуклеотидным зондом, получаемым из молекулы ДНК, содержащей нуклеотидную последовательность, представленную в SEQ ID NO: 28, SEQ ID NO: 30
или SEQ ID NO: 31; и
(в) выделение гибридизующейся ДНК.
Изобретение, кроме того, относится к специфичному в отношении насекомых протеину, когда этот протеин кодируется молекулой ДНК по изобретению.
Также в объем настоящего изобретения включена кассета экспрессии, содержащая молекулу ДНК по изобретению, функционально связанную с обеспечивающими экспрессию последовательностями, включающими регуляторные сигналы транскрипции и трансляции, необходимые для экспрессии объединенных конструкций ДНК в организме-хозяине, предпочтительно в микроорганизме или растении, и необязательно дополнительные регуляторные последовательности.
Изобретение, кроме того, относится к векторной молекуле, содержащей кассету экспрессии по изобретению.
Кассета экспрессии и/или веторная молекула по изобретению предпочтительно представляет собой часть генома растения.
Еще один вариант осуществления изобретения относится к организму-хозяину, предпочтительно к организму-хозяину, выбранному из группы, состоящей из клеток растений и насекомых, бактерий, дрожжей, бакуловирусов, простейших, нематод и водорослей, и содержащему молекулу ДНК по изобретению, кассету экспрессии, содержащую эту молекулу ДНК, или векторную молекулу, содержащую эту кассету экспрессии, предпочтительно стабильно включенную в геном организма-хозяина.
Изобретение, кроме того, относится к трансгенному растению и предпочтительно к растению кукурузы, включая его части, а также потомство и семенной материал, содержащему молекулу ДНК по изобретению, кассету экспрессии, содержащую эту молекулу ДНК, или векторную молекулу, содержащую эту кассету экспрессии, предпочтительно стабильно включенную в геном растения.
Предпочтительным является трансгенное растение, включая его части, а также потомство и семенной материал, стабильно трансформированные молекулой ДНК по изобретению, кассетой экспрессии, содержащей эту молекулу ДНК, или векторной молекулой, содержащей эту кассету экспрессии.
Также предпочтительным является трансгенное растение, включая его части, а также потомство и семенной материал, экспрессирующие специфичный в отношении насекомых протеин по изобретению.
Кроме того, изобретение относится к трансгенному растению, предпочтительно к растению кукурузы по изобретению, как оно определено выше в настоящем описании, которое дополнительно экспрессирует второй, отличный от первого, пригодный для борьбы с насекомыми ингредиент, предпочтительно δ-эндотоксин Bt. Это растение предпочтительно представляет собой гибридное растение.
Следует отметить, что в объем настоящего изобретения включены части трансгенного растения, в том числе клетки растения, протопласты, ткани, каллюс, эмбрионы, а также цветки, стебли, плоды, листья, корни, имеющие происхождение от трансгенных растений или их потомства, предварительно трансформированного молекулой ДНК по изобретению и, следовательно, состоящего, по крайней мере частично, из трансгенных клеток, которые являются предметом настоящего изобретения.
Кроме того, изобретение относится к растительному материалу для размножения растения по изобретению, который обрабатывают защитным покрытием для семенного материала.
Кроме того, изобретение включает микроорганизм, трансформированный молекулой ДНК по изобретению, кассетой экспресии, содержащей эту молекулу ДНК, или вектороной молекулой, содержащей кассету экспресии, причем этот микроорганизм предпочтительно представляет собой микроорганизм, который размножается на растениях, и более предпочтительно представляет собой бактерию, образующую колонии на корнях.
Еще один вариант осуществления изобретения относится к инкапсулированному специфичному в отношении насекомых протеину, который содержит микроорганизм, включающий специфичный в отношении насекомых протеин по изобретению.
Изобретение также относится к инсектицидной композиции, содержащей организм-хозяин по изобретению, предпочтительно очищенный штамм Bacillus, в количестве, обладающем инсектицидной активностью, вместе с пригодным носителем.
Кроме того, изобретение включает инсектицидную композицию, содержащую выделенную молекулу протеина по изобретению индивидуально либо в сочетании с организмом-хозяином по изобретению и/или инкапсулированный специфичный в отношении насекомых протеин по изобретению в количестве, обладающем инсектицидной активностью, вместе с пригодным носителем.
Изобретение относится также к способу получения очищенного специфичного в отношении насекомых протеина по изобретению, причем этот способ включает нанесение раствора, содержащего специфичный в отношении насекомых протеин, на NAD-колонку и элюирование связанного протеина.
Изобретение относится также к способу выявления
инсектицидной активности специфичного в отношении насекомых протеина по изобретению, включающему:
выращивание штамма Bacillus в культуре;
получение супернатанта из этой культуры;
кормление личинки насекомого пищей с добавлением супернатанта; и
определение смертности.
Еще один предмет настоящего изобретения относится к способу выделения
специфичного в отношении насекомых протеина по изобретению, включающему:
выращивание штамма Bacillus в культуре;
получение супернатанта из этой культуры; и
выделение
специфичного в отношении насекомых протеина из супернатанта.
В объем изобретения также включен способ выделения молекулы ДНК, содержащей нуклеотидную последовательность, кодирующую
специфичный в отношении насекомых протеин, обладающий инсектицидной активностью протеинов по изобретению, причем этот способ включает:
получение молекулы ДНК, содержащей нуклеотидную
последовательность, кодирующую специфичный в отношении насекомых протеин;
гибридизацию этой молекулы ДНК с ДНК, полученной из видов р. Bacillus; и
выделение этой гибридизующейся
ДНК.
Кроме того, изобретение относится к способу расширения спектра насекомых-мишеней в результате использования специфичного в отношении насекомых протеина по изобретению в сочетании по крайней мере еще с одним, вторым инсектицидным протеином, отличным от специфичного в отношении насекомых протеина по изобретению, и предпочтительно с инсектицидным протеином, выбранным из группы, состоящей из δ-эндотоксинов Bt, ингибиторов протеаз, лектинов, α-амилаз и пероксидаз.
Предпочтительным является способ расширения спектра насекомых-мишеней для растения путем экспрессии в этом растении специфичного в отношении насекомых протеина по изобретению в сочетании по крайней мере еще с одним, вторым инсектицидным протеином, отличным от специфичного в отношении насекомых протеина по изобретению, и предпочтительно с инсектицидным протеином, выбранным из группы, состоящей из δ-эндотоксинов Bt, ингибиторов протеаз, лектинов, α-амилаз и пероксидаз.
Изобретение также относится к способу защиты растений от повреждений, вызываемых насекомым-вредителем, предпочтительно видами Spodoptera и/или Agrotis и более предпочтительно насекомым-вредителем, выбранным из группы, состоящей из совки ипсилон [Agrotis ipsilon; СИ], совки травяной [Spodoptera frugiperda] , совки малой [Spodoptera exigua], табачной листовертки и совки хлопковой [Helicoverpa zea], причем этот способ включает обработку растения или места произрастания этого растения инсектицидной композицией или токсичным протеином по изобретению.
Изобретение также относится к способу защиты растений от повреждений, вызываемых насекомым-вредителем, предпочтительно видами Spodoptera и/или Agrotis и более предпочтительно насекомым-вредителем, выбранным из группы, состоящей из совки ипсилон [Agrotis ipsilon; СИ], совки травяной [Spodoptera frugiperda] , совки малой [Spodoptera exigua], табачной листовертки и совки хлопковой [Helicoverpa zea], причем этот способ включает выращивание трансгенного растения, экспрессирующего специфичный в отношении насекомых протеин по изобретению, в ареале, где может встречаться это насекомое-вредитель.
Изобретение также включает способ получения организма-хозяина, который содержит стабильно интегрированную в его геном молекулу ДНК по изобретению и предпочтительно экспрессирует специфичный в отношении насекомых протеин по изобретению, причем этот способ включает трансформацию организма-хозяина молекулой ДНК по изобретению, кассетой экспрессии, содержащей эту молекулу ДНК, или вектороной молекулой, содержащей кассету экспрессии.
Еще один предмет изобретения относится к способу получения трансгенного растения или клетки растения, которая содержит стабильно интегрированную в геном растения молекулу ДНК по изобретению и предпочтительно экспрессирует специфичный в отношении насекомых протеин по изобретению, причем этот способ включает трансформацию растения и клетки растения соответственно молекулой ДНК по изобретению, кассетой экспрессии, содержащей эту молекулу ДНК, или векторной молекулой, содержащей кассету экспрессии.
Изобретение также относится к способу получения инсектицидной композиции, включающему смешение выделенного штамма Bacillus, и/или организма-хозяина, и/или выделенной молекулы протеина, и/или инкапсулированного протеина по изобретению в количестве, обладающем инсектицидной активностью, с пригодным носителем.
В изобретении также предлагается способ получения трансгенного потомства трансгенного родительского растения, содержащего стабильно включенную в геном растения молекулу ДНК, содержащую нуклеотидную последовательность, кодирующую специфичный в отношении насекомых протеин по изобретению, причем этот способ включает трансформацию родительского растения молекулой ДНК по изобретению, кассетой экспрессии, содержащей молекулу ДНК, или векторной молекулой, содержащей кассету экспрессии, и передачу признака пестицидной активности потомству этого трансгенного родительского растения с использованием известных методов селекции растений.
Изобретение также относится к олигонуклеотидному зонду, способному к специфической гибридизации с нуклеотидной последовательностью, кодирующей специфичный в отношении насекомых протеин, выделяемый на стадии вегетативного роста Bacillus spp., и его компоненты, где этот протеин не является токсичным для комаров из В. sphaericus SSII-1, причем этот зонд включает смежную часть кодирующей последовательности для специфичного в отношении насекомых протеина длиной по крайней мере 10 нуклеотидов, и к применению олигонуклеотидного зонда для скрининга любого штамма Bacillus или других организмов для определения того, присутствует ли в нем специфичный в отношении насекомых протеин в естественных условиях или включает ли определенный трансформированный организм этот ген.
Согласно настоящему изобретению предполагается, что протеины, обладающие пестицидной активностью, продуцируются во время вегетативного роста штаммов Bacillus. Принимая во внимание, что такой класс существует, в объем настоящего изобретения включены все вегетативные инсектицидные протеины, обозначаемые в настоящем описании как VIP, за исключением токсина для комаров из В. sphaericus.
Указанные VIP присутствуют в небольшом количестве после споруляции, и они практически экспрессируются во время фазы логарифмического роста перед стационарной фазой. Согласно настоящему изобретению вегетативный рост определяется как период времени до начала споруляции. Гены, кодирующие такие VIP, могут быть выделены, клонированы в различные средства доставки и использованы для трансформации с целью использования в программах регуляции численности вредителей.
Согласно настоящему изобретению под понятие "вредители" подпадают, но не ограничены ими, насекомые, грибы, бактерии, нематоды, растительноядные клещи, иксодовые клещи, паразиты-простейшие, паразитирующие на животных печеночные двуустки и т.п.. Насекомые-вредители включают насекомых, выбранных из отрядов Coleoptera (Жесткокрылые), Diptera (Двукрылые), Hymenoptera (Перепончатокрылые), Lepidoptera (Чешуекрылые), Mallophaga (Пухоеды), Homoptera (Равнокрылые), Hemiptera (Полужесткокрылые), Orthoptera (Прямокрылые), Thysanoptera (Трипсы), Dennaptera (Уховертки), Isoptera (Термиты), Anoplura (Вши), Siphonaptera (Блохи), Trichoptera (Ручейники) и др., в частности насекомые из отрядов Coleoptera и Lepidoptera.
В таблицах 1-10 представлен список вредителей основных сельскохозяйственных культур и вредителей, имеющих медицинское и ветеринарное значение. Указанные вредители включены в объем настоящего изобретения.
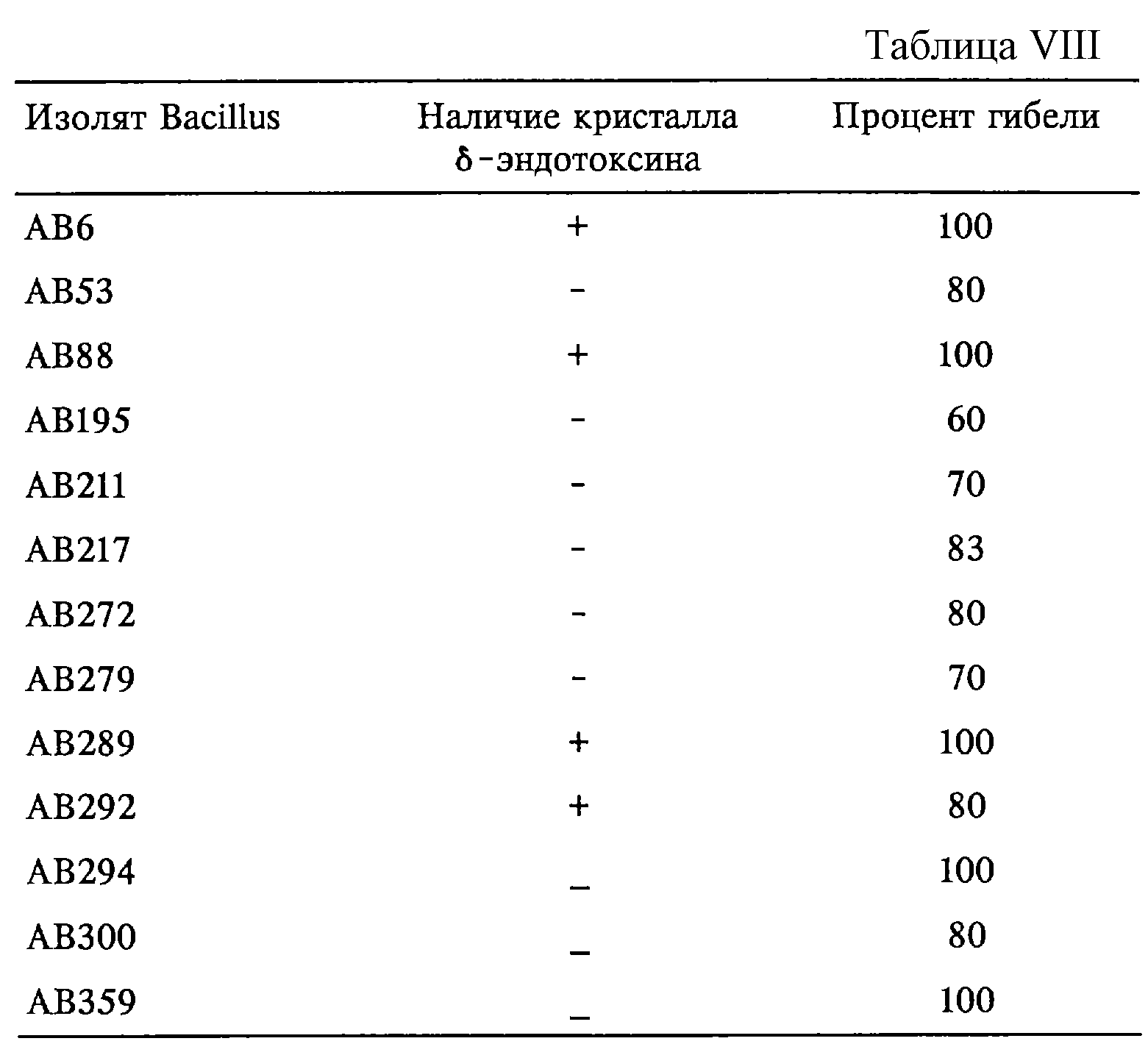
Было установлено, что протеины, обладающие пестицидной активностью, могут быть выделены из Bacillus во время фазы вегетативного роста и из других штаммов, которые могут быть выделены с помощью стандартных методик, а их активность может быть определена в отношении конкретных вредителей растений и других вредителей. Обычно штаммы Bacillus могут быть выделены из любых образцов, взятых из окружающей среды, включая почву, растение, насекомого, зерновую элеваторную пыль, других материалов и т.д., с помощью методов, известных в данной области техники. См., например, у Travers и др. (1987) Appl. Environ. Microbiol. 53: 1263-1266; Saleh и др. (1969) Can. J. Microbiol. 15: 1101-1104; DeLucca и др. (1981) Can J. Microbiol. 27: 865-870; и у Norris и др. (1981) в "The genera Bacillus and Sporolactobacillus", у Starr и др. (ред.) в The Prokaryotes: A Handbook on Habitats, Isolation, and Identification of Bacteria, том II, Springer-Veriog, Berlin-Heidelberg. После выделения штаммы могут быть исследованы на пестицидную активность во время вегетативного роста. Таким образом могут быть выявлены новые пестицидные протеины и штаммы.
Те микроорганизмы рода Bacillus, которые используются в настоящем изобретении, включают Bacillus cereus и Bacillus thuringiensis, а также виды Bacillus, перечисленные в таблице 11.
Группировка дана согласно Parry J.M. и др., (1983) Color Atlas of Bacillus species, Wolfe Medical Publications, Лондон.
В соответствии с настоящим изобретением из Bacillus могут быть выделены обладающие пестицидной активностью протеины, продуцируемые во время вегетативного роста. В одном из вариантов осуществления изобретения могут быть выделены инсектицидные протеины, продуцируемые во время вегетативного роста. Методы выделения протеинов известны в данной области техники. Обычно протеины могут быть очищены с помощью стандартной хроматографии, включающей гель-фильтрацию, ионообменную и иммуноаффинную хроматографии, жидкостную хроматографию высокого разрешения (ЖХВР), такую как жидкостная хроматография высокого разрешения с обращенной фазой, ионообменная жидкостная хроматография высокого разрешения, гель-фильтрирующая жидкостная хроматография высокого разрешения, хроматофокусирование высокого разрешения и хроматография с гидрофобным взаимодействием, и т.д., с помощью электрофоретического разделения, такого как одномерный гель-электрофорез, двумерный гель-электрофорез и т.д. Такие методы известны в данной области техники. См., например, в Current Protocols in Molecular Biology, т.т. 1 и 2, Ausubel и др. (ред.), John Wiley & Sons, NY (1988). Кроме того, могут быть получены антитела против практически чистых препаратов протеина. См., например, у Radka и др. (1983) в J. Immunol. 128: 2804; и у Radka и др. (1984) в Immunogenetics 19: 63. Для очистки протеина, обладающего пестицидными свойствами, могут быть использованы любые комбинации методов. После выбора протокола пестицидную активность определяют после каждой стадии очистки.
Такие стадии очистки приводят к получению практически очищенных фракций протеина. Под понятиями "практически очищенный" или "практически чистый" понимают протеин, который практически не содержит любых компонентов, обычно связанных с протеином в его естественном состоянии. Оценку "практически чистых" препаратов протеина можно проводить по отсутствию выявляемых полос другого протеина при электрофорезе в полиакриамидном геле с додецилсульфатом натрия (ДСН-ПААГ), что определяется визуально или денсиометрическим сканированием. В другом варианте уровень очистки может характеризовать отсутствие в очищенном препарате других последовательностей с концевой аминогруппой или остатков с концевым атомом азота. Чистота может быть проверена с помощью повторной хроматографии "чистых" препаратов, показывающей отсутствие других пиков при ионообменной хроматографии, хроматографии с обращенной фазой или капиллярном электорофорезе. Понятия "практически чистый" или "практически очищенный" не означают, что исключаются искусственные или синтетические смеси протеинов с другими соединениями. Эти понятия также не означают, что исключается присутствие малых количеств примесей, которые не влияют на биологическую активность протеина и которые могут присутствовать, например, вследствие неполной очистки.
После выделения очищенного протеина этот протеин или полипептиды, из которых он состоит, могут быть охарактеризованы и секвенированы с помощью стандартных методов, известных в данной области техники. Например, очищенный протеин или полипептиды, из которых он состоит, могут быть разделены на фрагменты с помощью бромистого цианогена или с помощью протеаз, таких как папаин, химотрипсин, трипсин, лизил-С-эндопептидаза и т.д. (Oike и др.. (1982) J. Biol. Chem. 257:9751-9758; Liu и др., (1983) Int. J. Pept. Protein Res. 21: 209-215). Полученные пептиды разделяют предпочтительно с помощью ЖХВР или с помощью разделения гелей и электроблоттинга на PVDF-мембранах и определяют последовательность аминокислот. Для осуществления этого пептиды предпочтительно анализируют с помощью автоматических секвенаторов. Известно, что можно определить N-концевые, С-концевые или внутренние последовательности аминокислот. На основе аминокислотной последовательности очищенного протеина может быть синтезирована нуклеотидная последовательность, которая может быть использована в качестве зонда с целью выделения гена, кодирующего пестицидный протеин.
Известно, что протеины с пестицидной активностью могут представлять собой олигомеры и могут различаться по молекулярной массе, количеству протомеров, по составу пептидов, активности в отношении определенных вредителей и другим характеристикам. Однако с помощью способов, приведенных в данном описании, могут быть выделены и охарактеризованы протеины, активные в отношении различных вредителей.
Известно, что после выделения и определения характеристик очищенного протеина он может быть видоизменен различными способами, включающими аминокислотные замещения, делении, усечения и инсерции. Способы осуществления таких операций широко известны в данной области техники. Например, варианты аминокислотной последовательности пестицидных протеинов могут быть получены с помощью мутаций в ДНК. Такие варианты будут обладать требуемой пестицидной активностью. Очевидно, что мутации, которые будут сделаны в ДНК, кодирующей данный вариант, не должны вызывать расположение последовательности вне рамки считывания и предпочтительно не должны создавать комплементарных областей, которые могут вызывать образование вторичной структуры мРНК. См. публикацию заявки на европейский патент 75444.
Таким образом, в объем настоящего изобретения включены протеины, обладающие пестицидной активностью, а также их компоненты и фрагменты. Это означает, что может быть получено сочетание промоторов, полипептидов или фрагментов протеинов, которое обеспечивает сохранение пестицидной активности. Эти фрагменты включают усеченные последовательности, а также N-концевые, С-концевые, внутренние аминокислотные последовательности протеинов и последовательности с внутренними делениями.
Можно предположить, что большинство делений, инсерций и замещений последовательности протеина не приведет к радикальным изменениям характеристик пестицидного протеина. Однако, хотя сложно заранее точно предсказать воздействие замещения, делении или инсерций, для специалиста в данной области техники должно быть очевидно, что их воздействие может быть оценено с помощью традиционных методов скрининга.
Протеины или другие компоненты полипептидов по настоящему изобретению могут быть использованы отдельно или в комбинации. Это означает, что для борьбы с различными насекомыми-вредителями может применяться несколько протеинов.
Некоторые протеины представляют собой одиночные полипептидные цепи, в то время как многие протеины состоят из более чем одной полипептидной цепи, т. е. представляют собой олигомеры. Кроме того, некоторые VIP обладают пестицидной активностью в виде олигомеров. В этих случаях применяют дополнительные протомеры для усиления пестицидной активности или для активации пестицидных протеинов. Такие протомеры, которые усиливают или активируют пестицидный протеин, называются вспомогательными протеинами. Вспомогательные протеины активируют или усиливают пестицидный протеин путем взаимодействия с пестицидным протеином, образуя олигомерный протеин с повышенной пестицидной активностью по сравнению с таковой, наблюдаемой в отсутствие вспомогательного протеина.
Вспомогательные протеины активируют или усиливают активность пестицидных протеинов, таких, как протеин VIP1 из штамма АВ78. Примером таких вспомогательных протеинов, которые не ограничены этим примером, является протеин VIP2 из АВ78. Как указано в экспериментальном разделе данного описания, вспомогательные протеины могут активировать большое количество пестицидных протеинов. Так, в одном из вариантов осуществления изобретения растение, обозначенное как "родитель 1", может быть трансформировано вспомогательным протеином. Этот "родитель 1" может быть скрещен с рядом родительских растений 2, трансформированных одним или несколькими пестицидными протеинами, пестицидные активности которых активируются вспомогательным протеином.
Среди пестицидных протеинов по изобретению неожиданно был выявлен новый класс специфичных для насекомых протеинов, подпадающих под объем настоящего изобретения. Эти протеины, которые обозначены в настоящем описании как VIP3, могут быть получены из штаммов Bacillus spp., предпочтительно из штаммов Bacillus thuringiensis и наиболее предпочтительно из штаммов Bacillus thuringiensis AB88 и АВ424. Эти VIP в основном присутствуют в супернатантах культур Bacillus, составляя по крайней мере 75% от общего количества в штамме AB88. Для протеинов VIP3, кроме того, характерен уникальный спектр инсектицидной активности, который включает активность в отношении видов Agrotis и/или Spodoptera и прежде всего в отношении совки ипсилон (СИ), и/или совки травяной, и/или совки малой, и/или табачной листовертки, и/или совки хлопковой.
Совка ипсилон является важным сельскохозяйственным насекомым-вредителем, обладающим высокой устойчивостью к δ-эндотоксинам. Как описано у Macintosh и др. (1990) в J. Invertebr. Pathol. 56, 258-266, δ-эндотоксины CryIA(b) и CryIA(c) обладают инсектицидными свойствами в отношении СИ, причем значения LC50 составляют более 80 мкг/мл и 18 мкг/мл питательной среды соответственно. Инсектицидные протеины VIP3A по изобретению обеспечивают гибель более чем на 50%, когда количество добавленного протеина по крайней мере в 10-500, предпочтительно в 50-350 и более предпочтительно в 200-300 раз ниже количества протеинов CrylA, необходимых для достижения такой же 50%-ной гибели. Особенно предпочтительными по изобретению являются протеины VIP3A, которые обеспечивают 100%-ную гибель при добавлении протеина в количестве, по крайней мере в 260 раз ниже того количества протеинов CrylA, которое необходимо для достижения такой же 50%-ной гибели.
Инсектицидные протеины VIP3 по изобретению в основном присутствуют в супернатантах культур и, следовательно, могут быть классифицированы как секретируемые протеины. Они предпочтительно содержат в N-концевой последовательности ряд положительно заряженных остатков, за которыми расположена гидрофобная коровая область, и не подвергаются N-концевому процессингу во время экспорта.
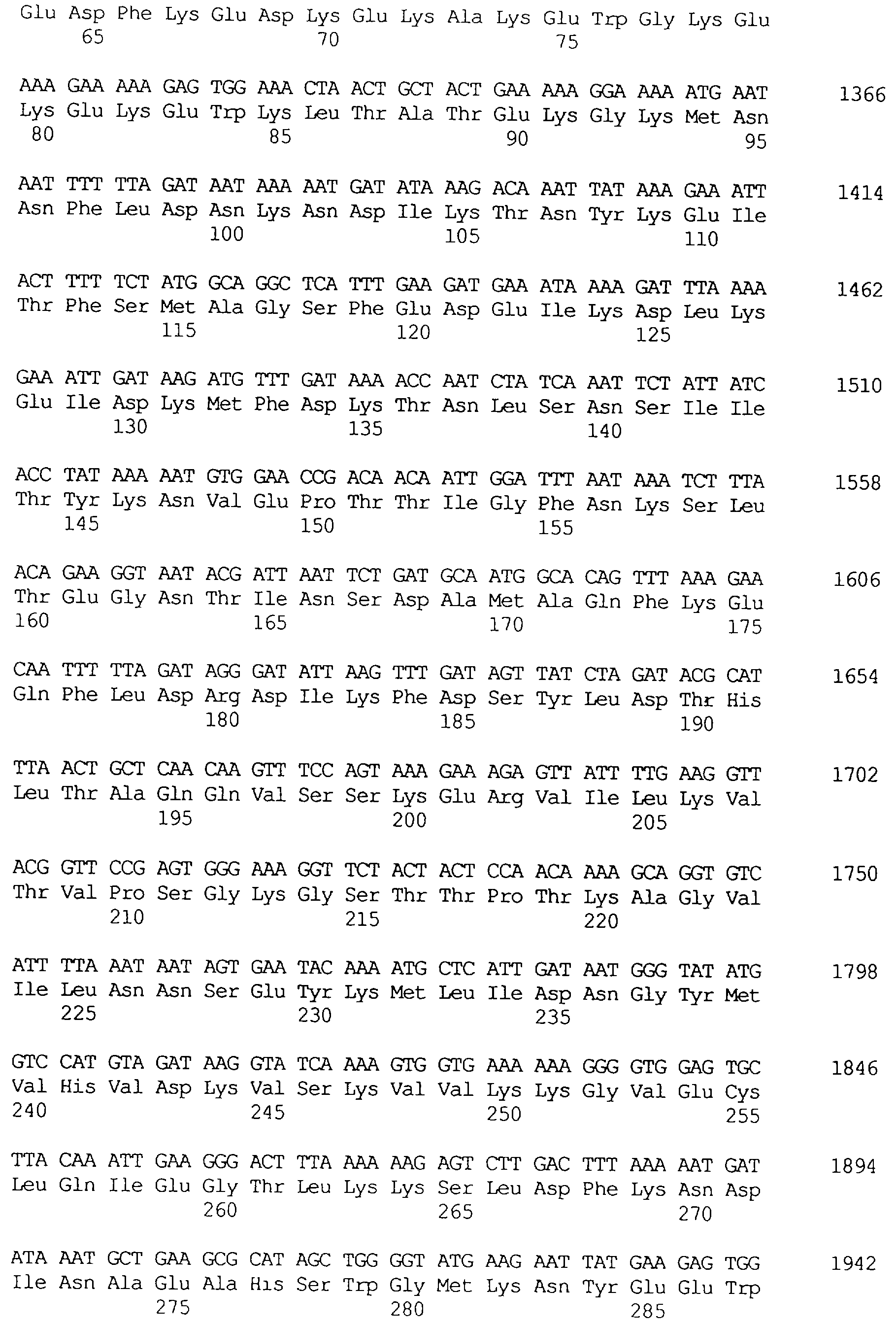
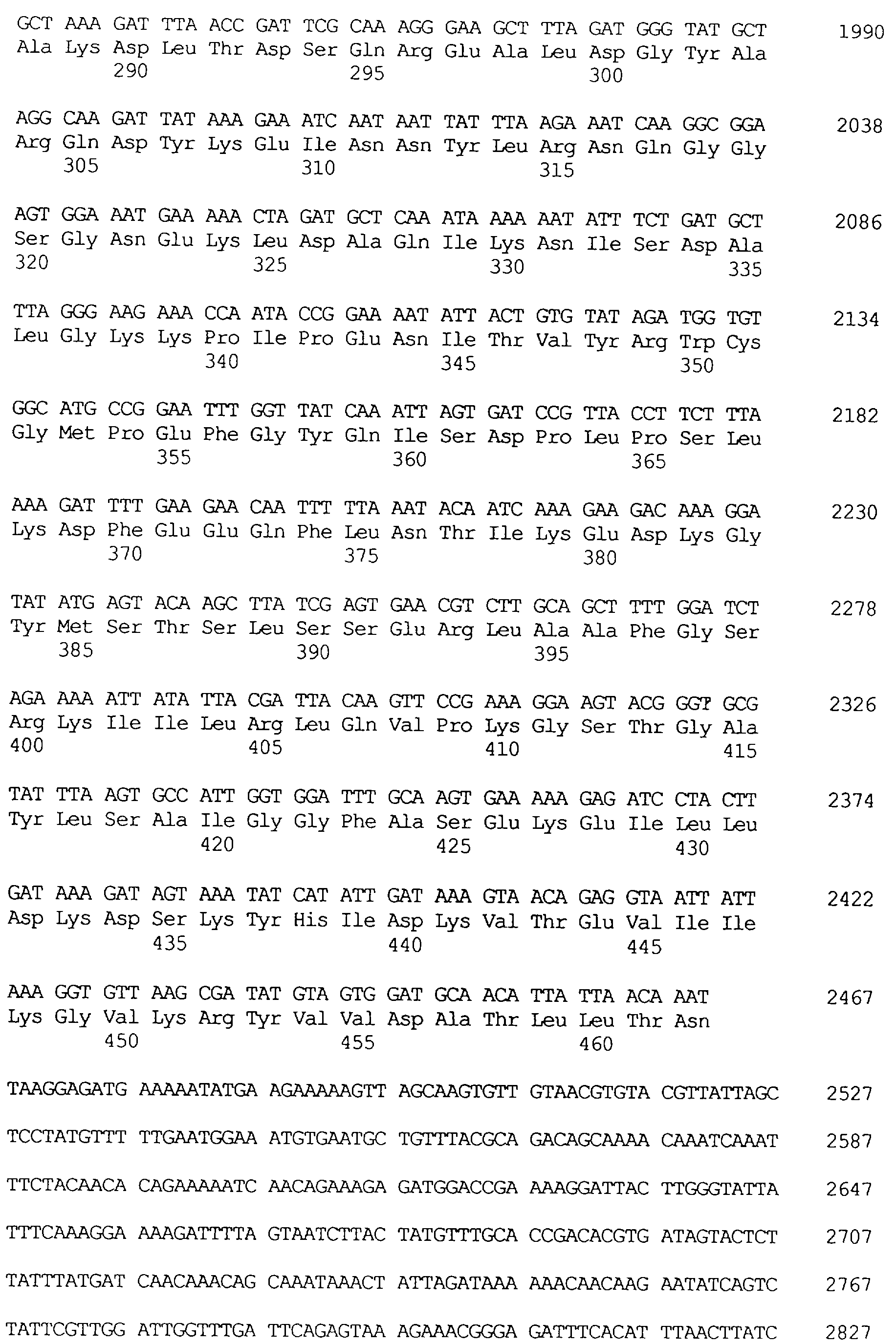
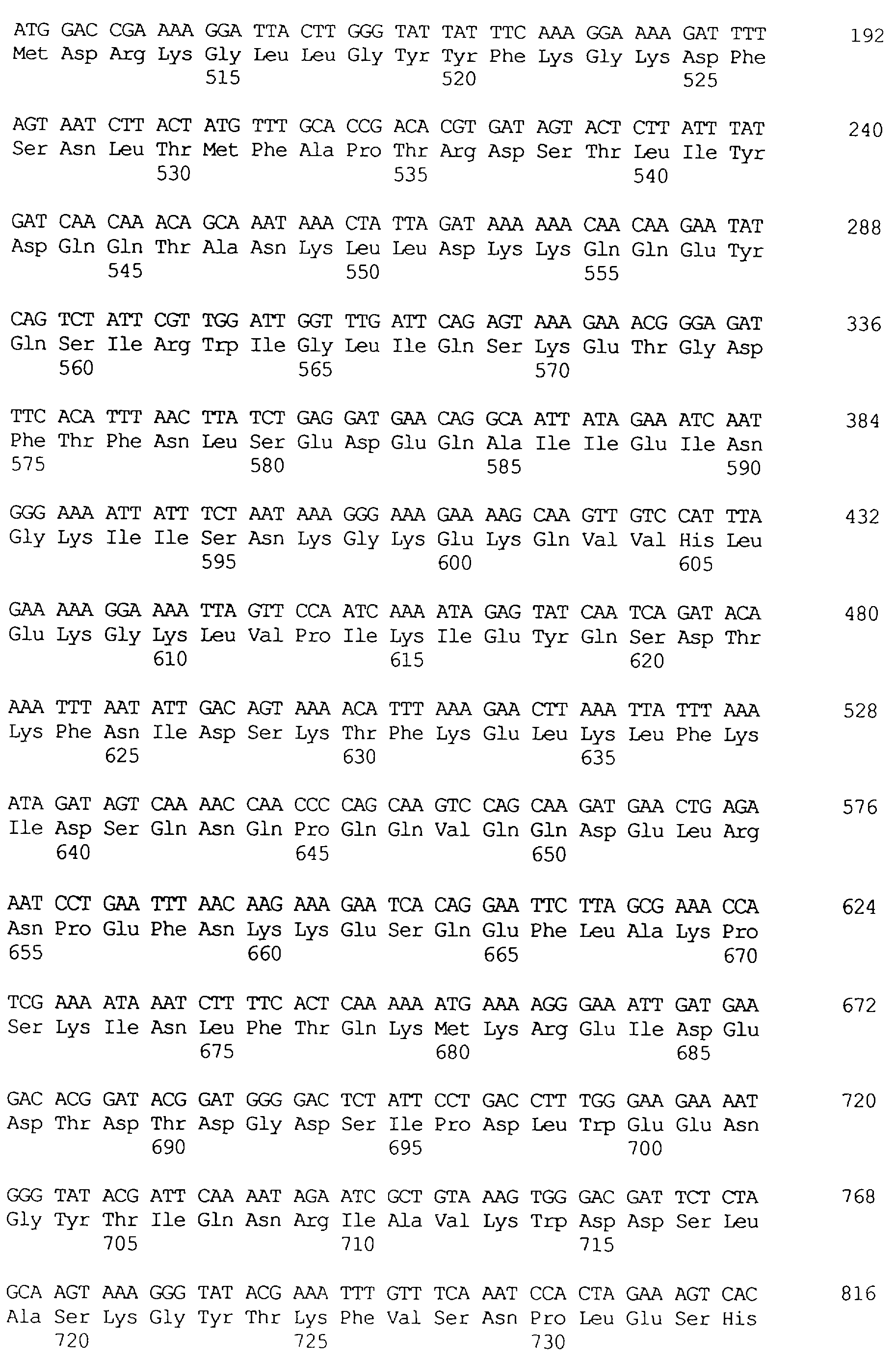
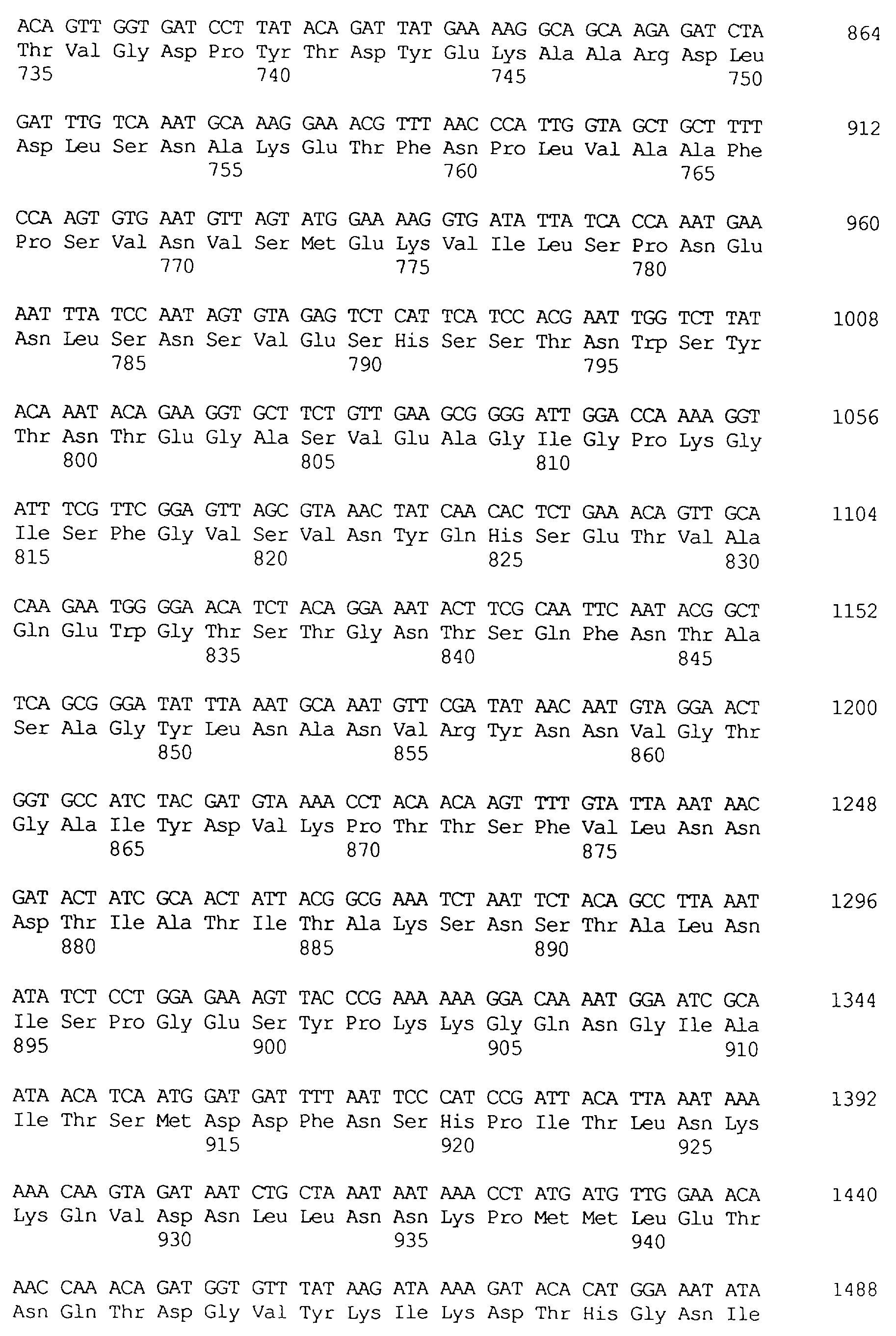
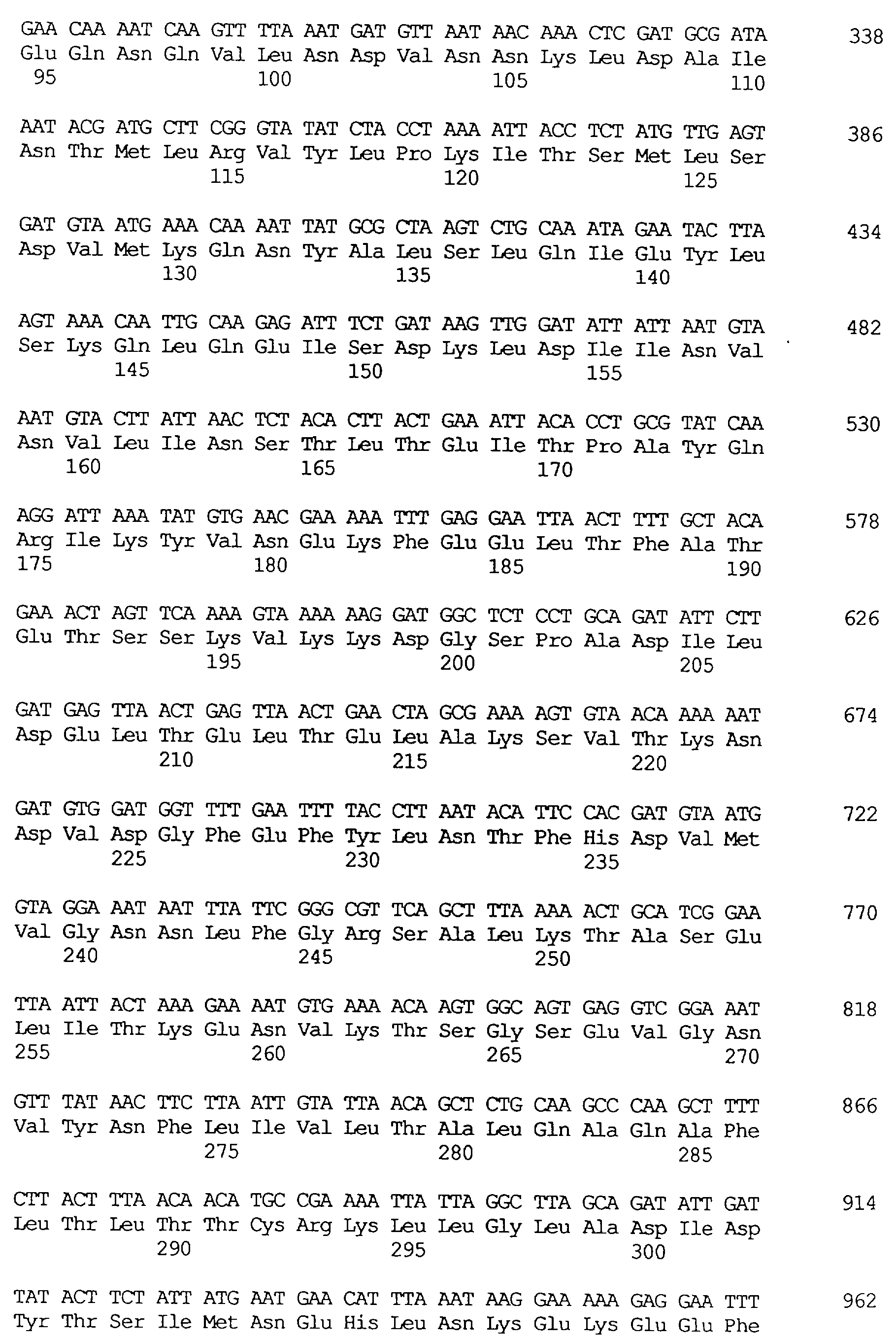
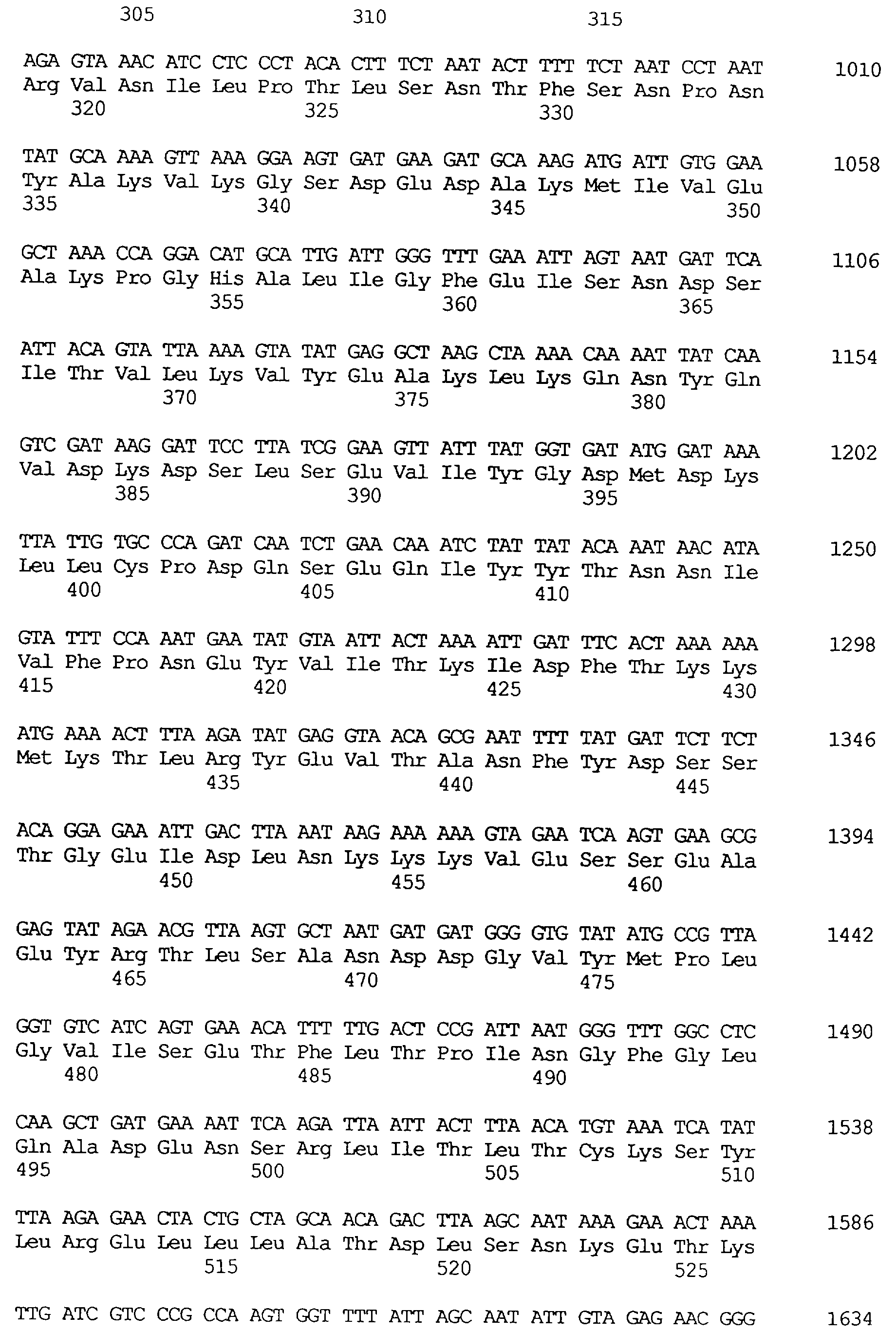
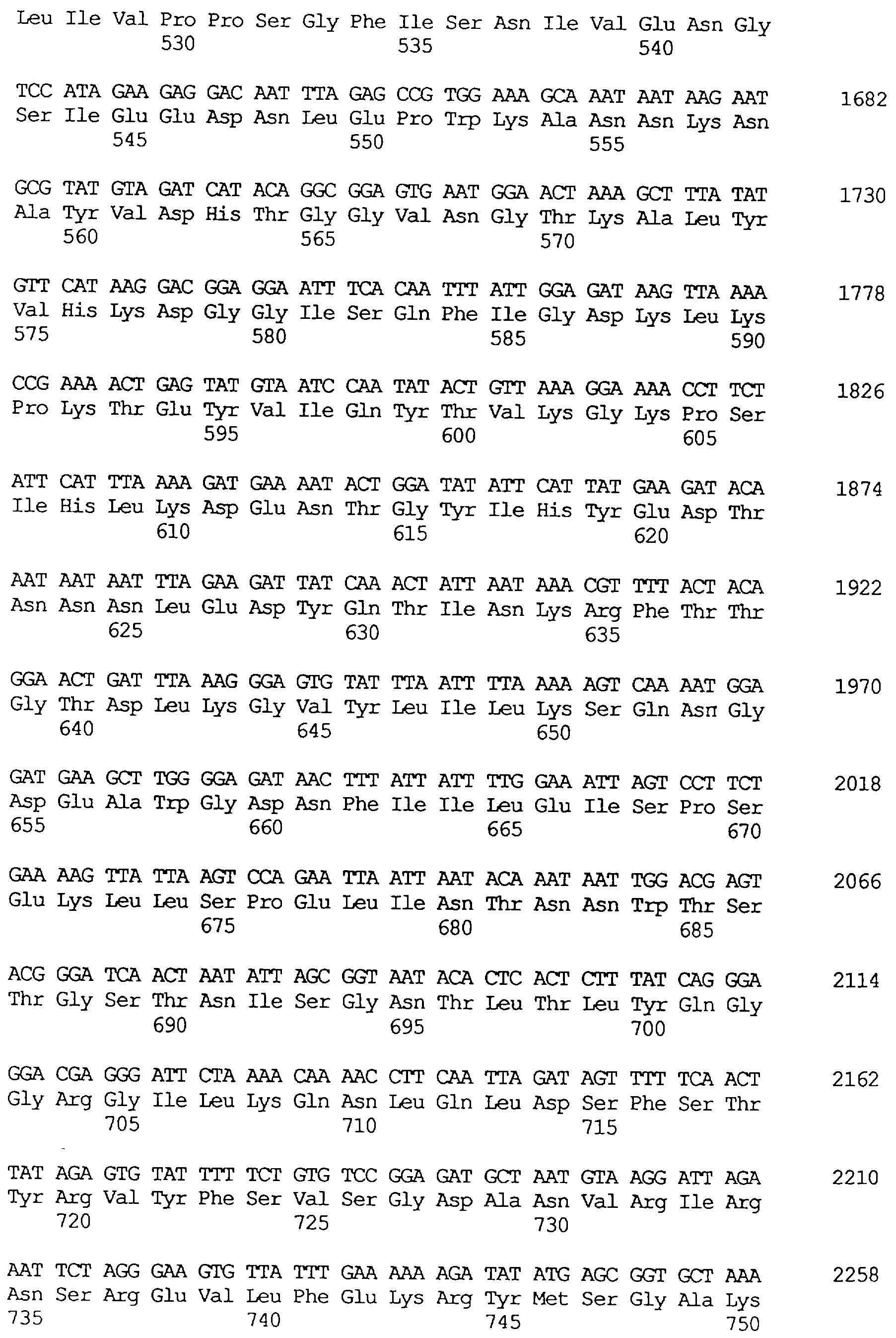
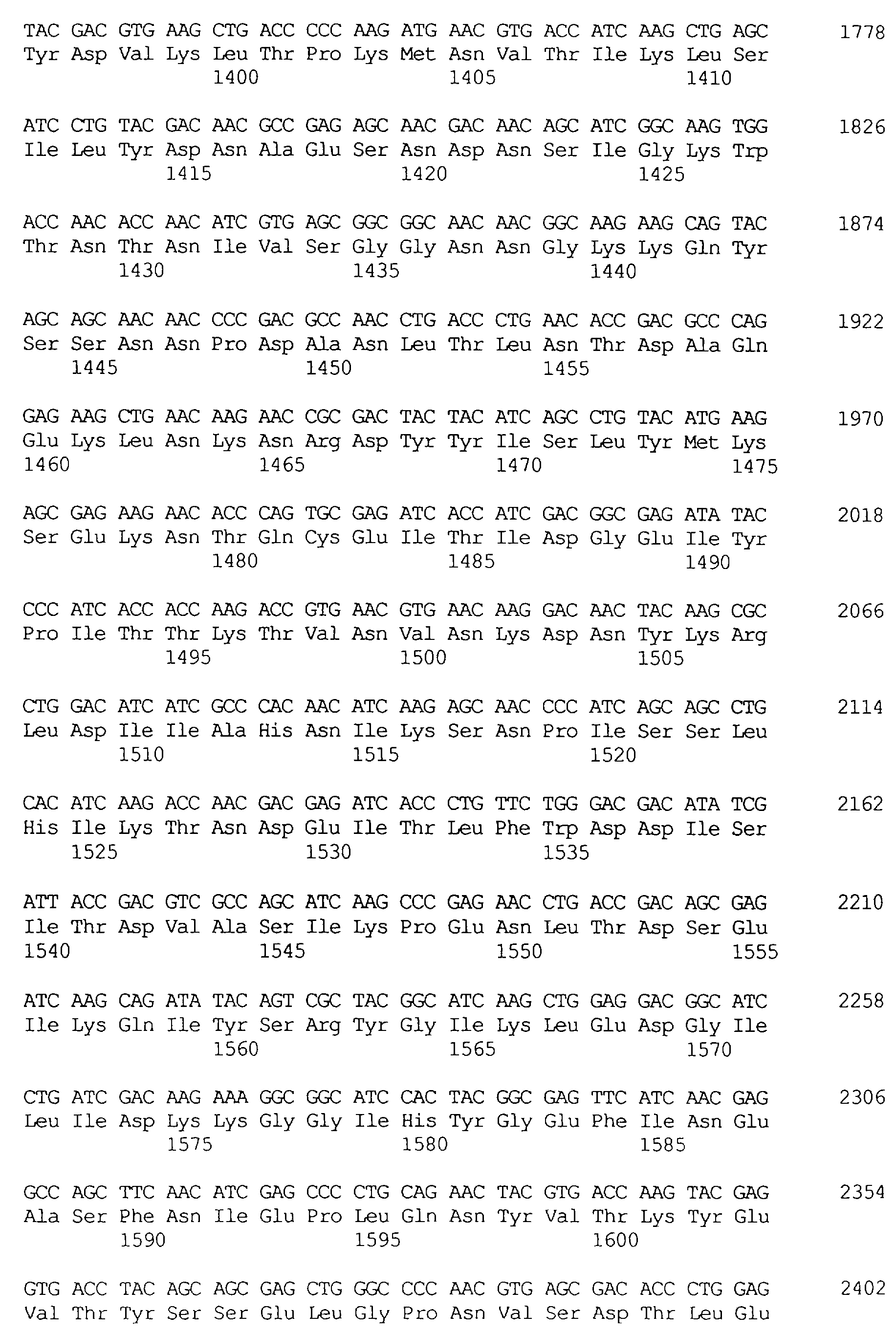
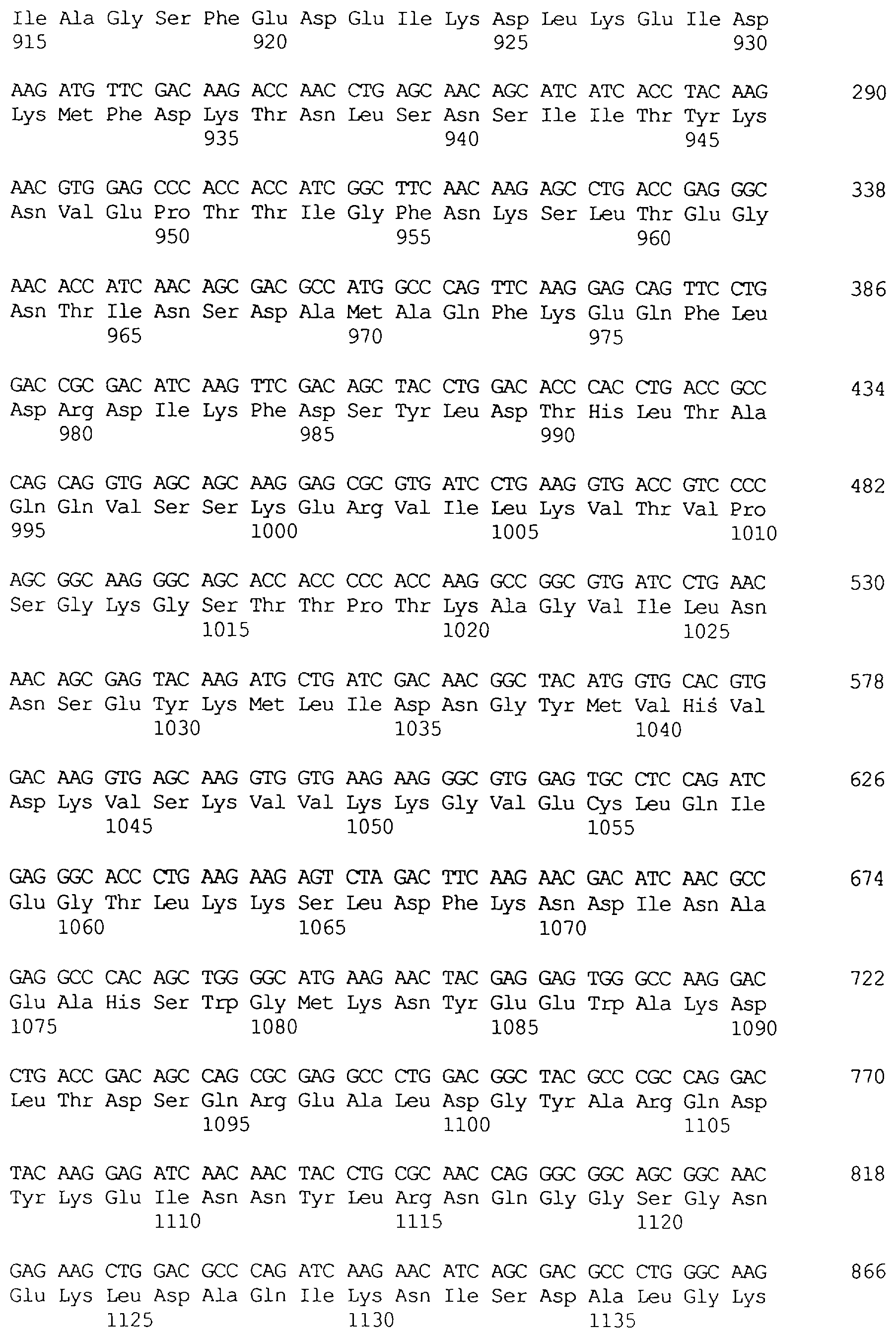
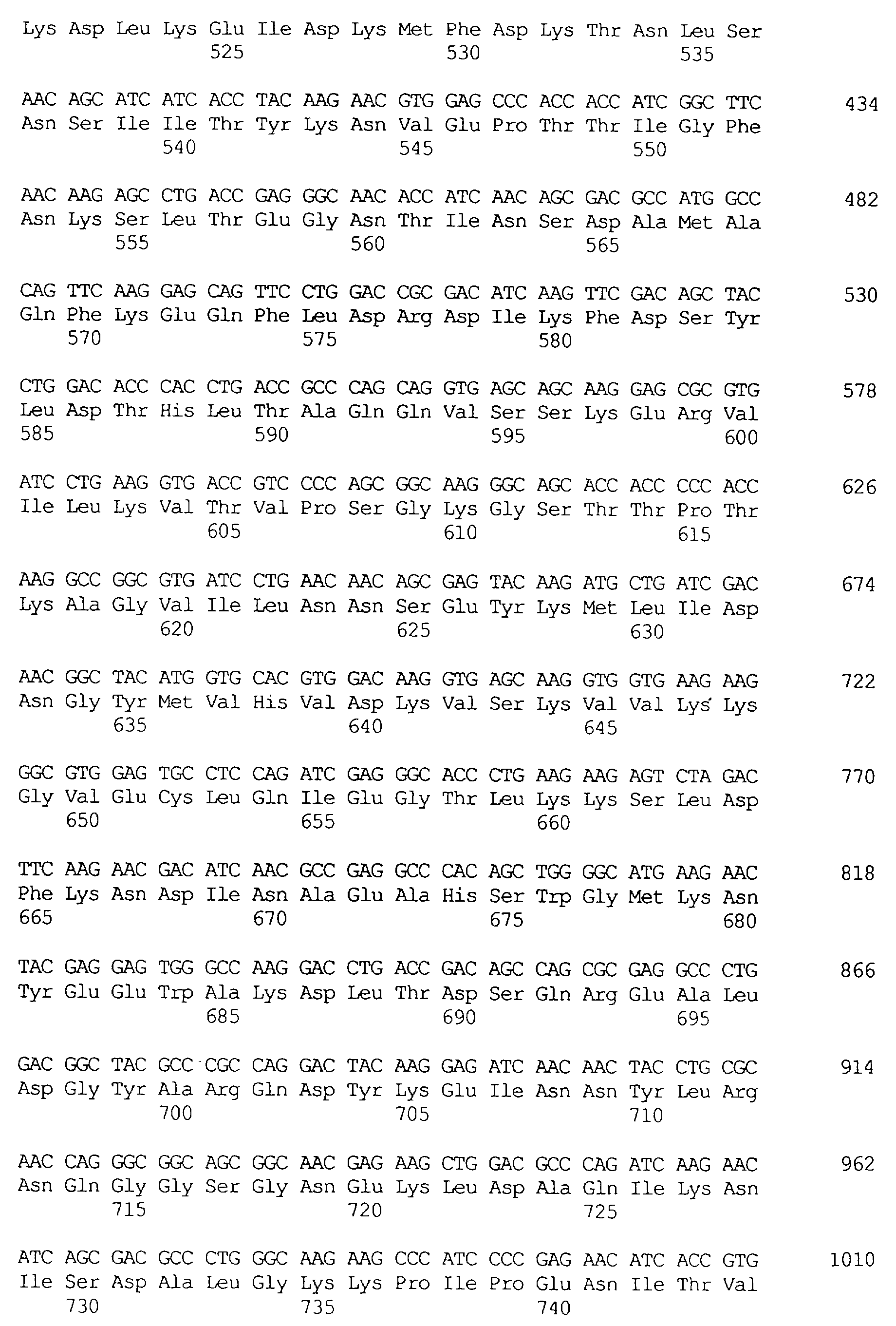
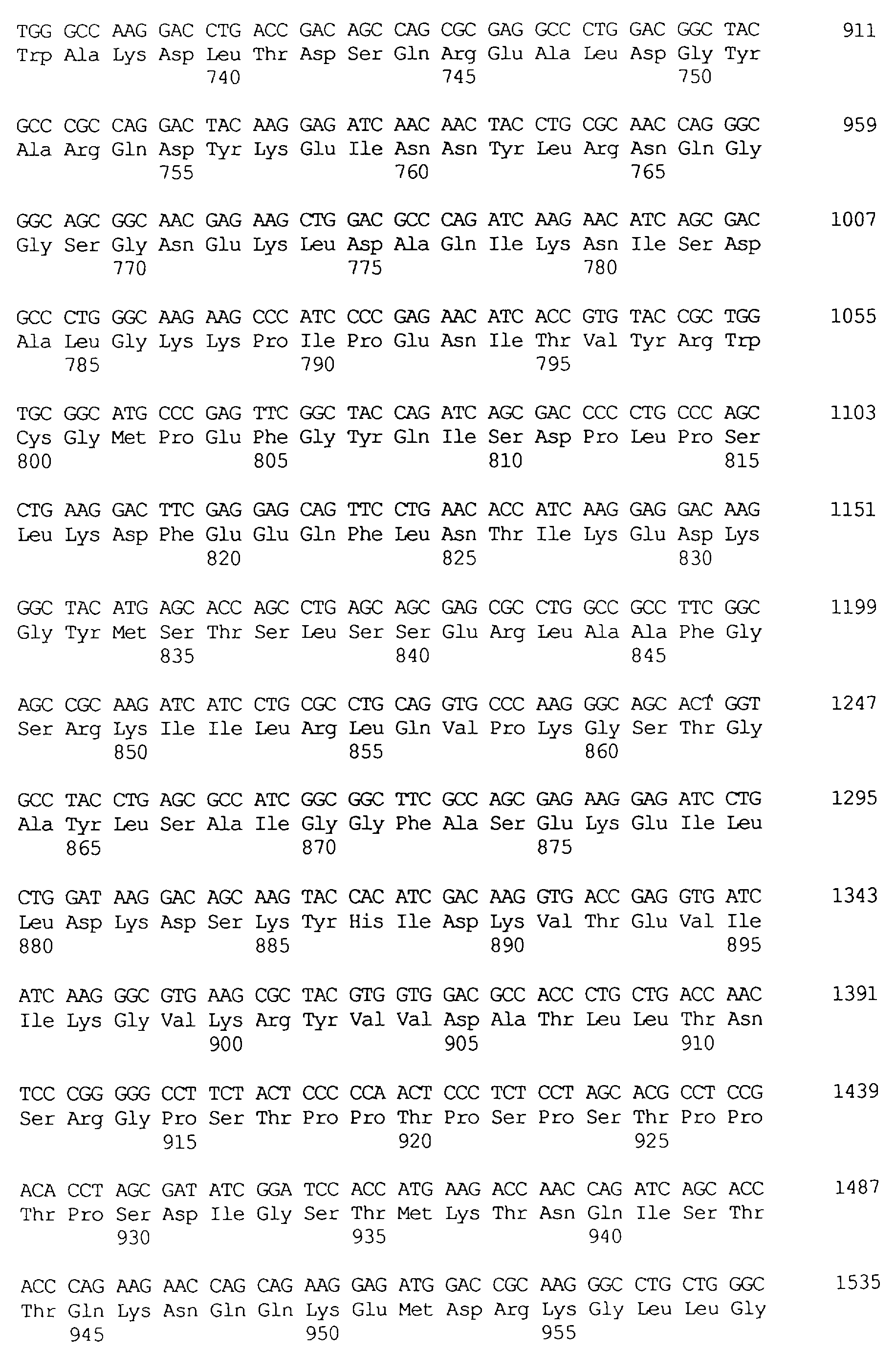
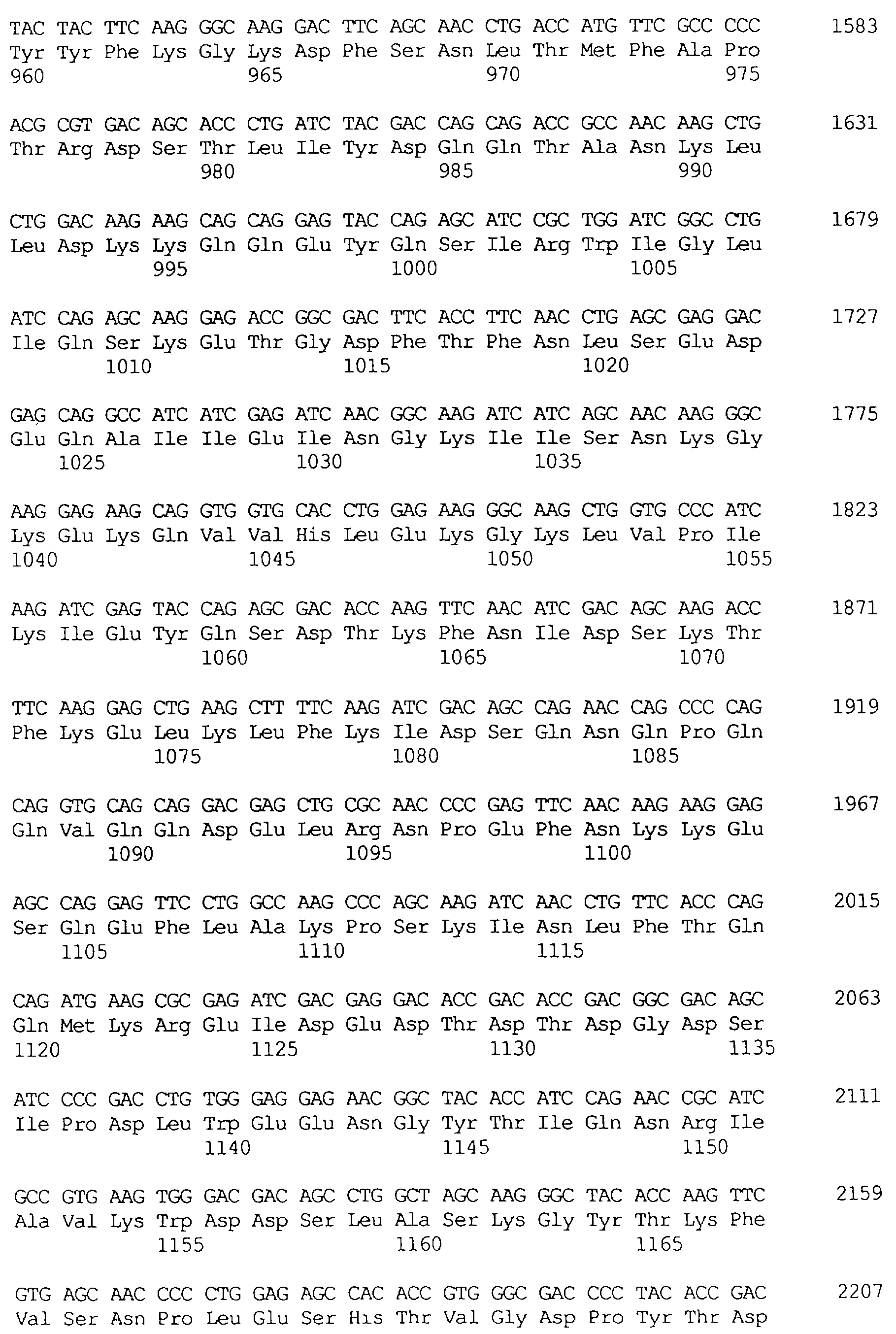
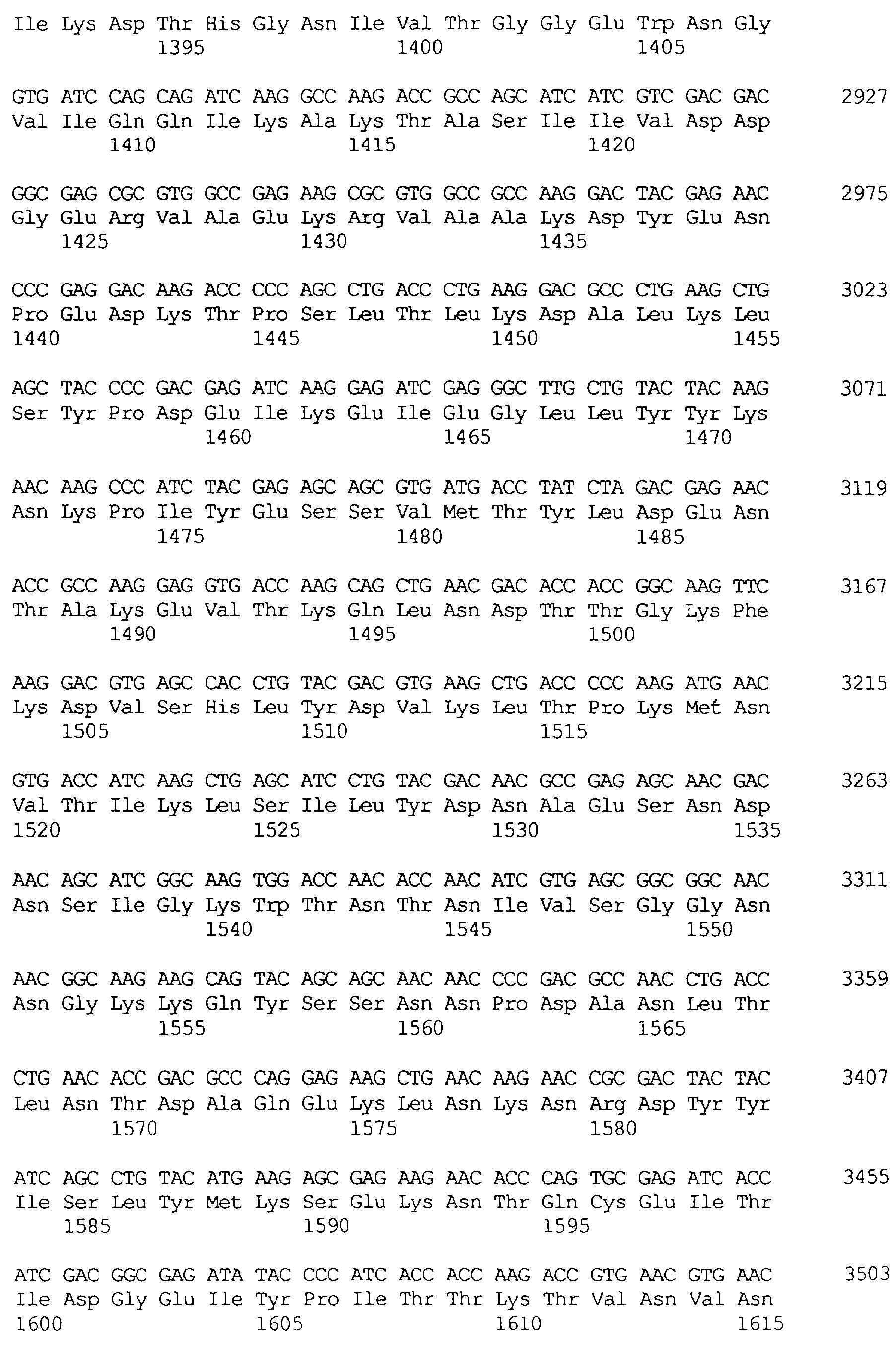
Протеины VIP3, равно как и другие протеины с пестипидной активностью, которые, как указано, включены в настоящее изобретение, могут быть обнаружены на стадиях роста до споруляпии, что является еще одним их выраженным отличием от других протеинов, которые принадлежат к семейству δ-эндотоксинов. Предпочтительно экспрессия специфичных в отношении насекомых протеинов начинается в течение средней логарифмической фазы и продолжается во время споруляпии. Благодаря специфической схеме экспрессии в сочетании с высокой стабильностью протеинов VIP3 большие количества протеинов VIP3 могут быть обнаружены в супернатантах культур во время споруляпии. Особенно предпочтительными являются протеины VIP3, представленные в SEQ ID NO: 29 и SEQ ID NO: 32, и соответствующие молекулы ДНК, содержащие нуклеотидные последовательности, кодирующие эти протеины, и прежде всего такие молекулы ДНК, которые содержат нуклеотидные последовательности, представленные в SEQ ID NO: 28, SEQ ID NO: 30 и SEQ ID NO: 31.
Протеины с пестипидной активностью по изобретению могут применяться в сочетании с эндотоксинами Bt или с другими инсектицидными протеинами для расширения спектра насекомых-мишеней. Кроме того, применение VIP по настоящему изобретению в сочетании с δ-эндотоксинами Bt или с другими инсектицидными ингредиентами иной природы имеет особое значение для предотвращения и/или преодоления устойчивости насекомых. Другие инсектицидные ингредиенты включают ингибиторы протеаз (как серинового, так и цистеинового типов), лектины, α-амилазу и пероксидазу. В предпочтительном варианте осуществления изобретения экспрессия VIP в трансгенном растении сопровождается экспрессией одного или нескольких δ-эндотоксинов Bt. Такая совместная экспрессия более чем одного инсектицидного ингредиента в одном и том же трансгенном растении может быть достигнута с помощью методов генной инженерии, позволяющих сконструировать растение, содержащее и экспрессирующее все необходимые гены. В другом варианте для экспрессии VIP методами генной инженерии может быть сконструировано растение - родитель 1. Для экспрессии δ-эндотоксина Bt может быть сконструировано методами генной инженерии второе растение - родитель 2. При скрещивании родителя 1 с родителем 2 получают потомство растений, которое экспрессирует все гены, интродуцированные в родителей 1 и 2. Особенно предпочтительными δ-эндотоксинами Bt являются таковые, описанные в европейской заявке ЕР-А 0618976, включенной в настоящее описание в качестве ссылки.
Как известно, значительное количество цитотоксичных протеинов, хотя и не все из них, обладают бинарным действием. Обычно бинарные токсины состоят из двух протеиновых доменов: первого, называемого А-доменом, и второго, называемого В-доменом (см. в Sourcebook of Bacterial Protein Toxins, J.E. Alouf и J. H. Freer (ред.) (1991) Academic Press). А-домен обладает потенциальной цитотоксичной активностью. В-домен связывается с рецептором внешней поверхности клетки перед поглощением. Обычно цитотоксичный А-домен эскортируют в цитоплазму транслокационным доменом. Часто А- и В-домены представляют собой отдельные полипептиды или протомеры, которые связаны с помощью взаимодействия протеин-протеин или с помощью дисульфидного мостика. Однако токсин может представлять собой одиночный полипептид, который протеолитическим путем превращается внутри клетки в два домена, как это происходит в случае экзотоксина A Pseudomonas. В целом бинарные токсины имеют три важных домена: цитотоксичный А-домен, связывающийся с рецептором В-домен и транслокационный домен. Часто А- и В-домены связываются посредством взаимодействия протеин-протеин.
Связывающиеся с рецепторами домены по настоящему изобретению пригодны для доставки любого протеина, токсина, фермента, фактора транскрипции, нуклеиновой кислоты, химического или любого другого фактора в насекомых-мишеней, имеющих рецептор, распознаваемый связывающимся с рецептором доменом бинарных токсинов, описанных в настоящем изобретении. Аналогично этому, поскольку бинарные токсины имеют транслокационные домены, которые проникают через фосфолипидный двойной слой мембран и эскортируют цитотоксины через эти мембраны, такие транслокационные домены могут быть пригодны при эскортировании любых протеинов, токсинов, ферментов, фактора транскрипции, нуклеиновой кислоты, химического или любого другого фактора через фосфолипидный двойной слой, такой, как плазматическая мембрана или мембрана пузырьков. Транслокационный домен может сам перфорировать мембраны, обладая, таким образом, токсичными или инсектицидными свойствами. Кроме того, все бинарные токсины имеют цитотоксичные домены; такой цитотоксичный домен может быть пригоден в качестве вызывающего гибель протеина либо индивидуально сам по себе, либо при его доставке к любой клетке(ам)-мишени(ням) с помощью каких-либо средств.
И, наконец, поскольку бинарные токсины, состоящие из двух полипептидов, часто образуют комплекс, то полагают, что существуют области взаимодействия протеин-протеин внутри компонентов бинарных токсинов по изобретению. Эти домены взаимодействия протеин-протеин Moгут быть пригодны для образования ассоциации между любой комбинацией токсинов, ферментов, факторов транскрипции, нуклеиновых кислот, антител, связывающих клетку фрагментов или любых других химических соединений, факторов, протеинов или доменов протеина.
Токсины, ферменты, факторы транскрипции, антитела, связывающиеся с клеткой фрагменты или другие домены протеинов могут быть слиты с пестицидными или вспомогательными протеинами посредством генетических слияний с продуцированием гибридов, которые при трансляции с помощью рибосом будут продуцировать слитый протеин, сочетающий свойства VIP и другого компонента, используемого при слиянии. Кроме того, если домен протеина, слитый с VIP, обладает сродством к другому протеину, нуклеиновой кислоте, углеводу, липиду или другому химическому соединению или фактору, то может быть образован комплекс, состоящий из трех компонентов. Этот комплекс будет иметь свойства всех этих компонентов. Аналогичный подход может быть использован для получения комплексов, состоящих из четырех или более компонентов. Такие комплексы пригодны в качестве инсектицидных токсинов, фармацевтических средств, лабораторных реактивов и диагностических реагентов и т.д. Примерами областей, в которых такие комплексы применяются в настоящее время, являются слитые токсины для интенсивной раковой терапии, реагенты для метода ELISA и для иммуноблоттинга.
Один из методов по изменению пестицидных или вспомогательных протеинов состоит в слиянии 15-той аминокислоты "S-tag" с протеином без разрушения домена(ов), связывающегося(ихся) с клеткой насекомых, транслокационных доменов или доменов протеина, осуществляющих связь протеин-протеин. S-tag имеет высокую степень сродства (Кd=10-9М) с рибонуклеазным S-протеином, который, будучи связанным с S-tag, образует активную рибонуклеазу (см. у F.M. Richards и H.W. Wyckoff (1971) в "The Enzymes", том IV (Boyer P.D. ред.), с. 647-806, Academic Press, New York). Слияние может быть осуществлено таким образом, чтобы разрушить или удалить цитотоксичную активность пестицидного или вспомогательного протеина, тем самым замещая цитотоксичную активность VIP новой цитотоксичной рибонуклеазной активностью. Окончательный токсин будет содержать S-протеин, пестицидный протеин и вспомогательный протеин, где либо пестицидный протеин либо вспомогательный протеин получают в результате трансляционных слияний с S-tag. Аналогичные подходы могут применяться для слияния других потенциальных цитотоксинов с пестицидными или вспомогательными протеинами, включающими (но не ограниченных ими) рибосом-инактивирующие протеины, гормоны насекомых, рецепторы гормонов, факторы транскрипции, протеазы, фосфатазы, экзотоксин A Pseudomonas или любой другой протеин или химический фактор, который является летальным, будучи доставленным в клетки. Аналогично этому в клетки могут быть доставлены протеины, которые не являются летальными, но могут изменять биохимию или физиологию клетки.
Спектр токсичности по отношению к различным видам может быть изменен путем слияния доменов, которые обладают способностью распознавать рецепторы на поверхности клетки других видов, с пестицидными или вспомогательными протеинами. Такие домены могут включать (но не ограничены ими) антитела, трансферрин, гормоны или пептидные последовательности, выделенные из селектируемых библиотек проявляющего сродство фага. Кроме того, для изменения спектра токсичности могут применяться пептидные последовательности, которые связаны с питательными веществами, витаминами, гормонами или другими химическими соединениями, которые транспортируются в клетку. Аналогично этому для изменения спектра активности VIP1 и VIP2 может применяться любой другой протеин или химичесое соединение, которое связывается с рецептором поверхности клетки или с мембраной и которое может быть поглощено.
Пестицидные протеины по настоящему изобретению представляют собой такие протеины, которые обладают срецифичной пестицидной активностью. Такие протеины могут иметь разную молекулярную массу, включая компоненты полипептидов, имеющих молекулярную массу 30 кДа или выше, предпочтительно 50 кДа или выше.
Вспомогательные протеины по настоящему изобретению могут иметь различную молекулярную массу, их молекулярная масса составляет по крайней мере приблизительно 15 кДа или более, предпочтительно приблизительно 20 кДа или выше; более предпочтительно приблизительно 30 кДа или более. Сами вспомогательные протеины могут содержать компоненты полипептидов.
В одном из вариантов пестицидный протеин и вспомогательный протеин могут быть составляющими многомерного пестицидного протеина. Такой пестицидный протеин, включающий вспомогательные протеины в качестве одного или более составляющих его полипептидов, может иметь различную молекулярную массу, которая может составлять по крайней мере от 50 кДа до по крайней мере 200 кДа, предпочтительно примерно от 100 кДа до 150 кДа.
Вспомогательный протеин может быть использован в комбинации с пестицидными протеинами по изобретению для повышения активности или активации пестицидного протеина. Для определения того, будет ли вспомогательный протеин влиять на активность, пестицидный протеин может быть экспрессирован индивидульно и в комбинации со вспомогательным протеином, а соответствующие активности сравнены с точки зрения увеличения пестицидной активности при внесении в пищу.
Может оказаться целесообразным проводить скрининг штаммов на потенциальную пестицидную активность путем исследования активности одного штамма и в комбинации со вспомогательным протеином. В некоторых случаях вспомогательный протеин в сочетании с нативными протеинами штаммов проявляет пестицидную активность, которая не выявляется в отсутствие вспомогательного протеина.
Вспомогательный протеин может быть модифицирован, как описано выше, с помощью различных способов, известных в данной области техники. Следовательно, в контексте настоящего изобретения под понятие "вегетативный инсектицидный протеин" (VIP) подпадают такие производимые во время вегетативного роста протеины, которые по отдельности или в комбинации могут быть использованы как средства, обладающие пестипидной активностью. Это понятие включает пестицидные протеины, вспомогательные протеины и такие протеины, которые проявляют активность только в присутствии вспомогательного протеина, или полипетидные компоненты этих протеинов.
Предполагается, что существуют альтернативные способы, пригодные для получения нуклеотидных и аминокислотных последовательностей указанных протеинов. Например, для получения нуклеотидной последовательности, кодирующей пестицидный протеин, из библиотеки генов могут быть выделены космидные клоны, которые экспрессируют этот пестицидный протеин. Из более крупных активных космидных клонов могут быть созданы более мелкие субклоны и исследована их активность. Таким образом, клоны, экспрессирующие активный пестицидный протеин, могут быть секвенированы с целью определить нуклеотидную последовательность гена. Затем может быть установлена аминокислотная последовательность протеина. Общепринятые методы молекулярной биологии описаны, например, в Molecular Cloning, A Laboratory Manual, второе издание, тома 1-3, Sambrook и др. (ред.). Cold Spring Harbor Laboratory Press, Cold Spring Harbor, NY (1989), и приведенные в этой публикации ссылки.
Настоящее изобретение также включает нуклеотидные последовательности организмов, отличных от Bacillus, причем нуклеотидные последовательности могут быть выделены путем гибридизации с нуклеотидными последовательностями Bacillus по изобретению. Может быть исследована пестицидная активность протеинов, кодируемых такими нуклеотидными последовательностями. Изобретение также включает протеины, кодируемые нуклеотидными последовательностями. Кроме того, в объем изобретения включены протеины, полученные из организмов, отличных от Bacillus, в которых протеин перекрестно реагирует с антителами, продуцируемыми против протеинов по изобретению. В этом случае выделенные протеины также могут быть исследованы на пестицидную активность с помощью методов, представленных в настоящем описании, и других методов, хорошо известных в данной области техники.
После выделения нуклеотидных последовательностей, кодирующих пестицидные протеины по изобретению, с ними можно манипулировать и применять для экспрессии данного протеина в различных хозяевах, включающих разнообразные организмы, в том числе микроорганизмы и растения.
Пестицидные гены по изобретению можно оптимизировать для увеличения экспрессии в растениях. См. , например, ЕР-А 0618976; ЕР-А 0359472; ЕР-А 0385962; WO 91/16432; у Perlak и др. (1991), Ргос. Natl. Acad. Sci. USA, 88: 3324-3328; и у Murray и др. (1989), Nucleic Acids Research, 17: 477-498. Таким способом могут быть синтезированы гены с использованием предпочтительных для растения кодонов. Это означает, что предпочтительным кодоном для определенного хозяина является кодон, который наиболее часто кодирует определенную аминокислоту в указанном хозяине. Например, предпочтительный для кукурузы кодон для конкретной аминокислоты может быть установлен на основе известных последовательностей генов кукурузы. Наиболее часто встречающиеся кодоны у кукурузы для 28 генов растений кукурузы представлены у Murray и др. (1989), Nucleic Acids Research, 17: 477-498, причем описание этого исследования включено в настоящее изобретение в качестве ссылки. На основе данных о встречаемости кодонов, кодирующих определенную аминокислоту у конкретного хозяина, также могут быть созданы синтетические гены.
Таким образом, нуклеотидные последовательности могут быть оптимизированы для экспрессии в любом растении. Было установлено, что вся или любая часть последовательности гена может быть оптимизирована или получена путем синтеза. Это означает, что также могут применяться синтетические или частично оптимизированные последовательности.
Аналогичным образом нуклеотидные последовательности могут быть оптимизированы для экспрессии в любом микроорганизме. Данные о предпочтительных наиболее часто встречающихся кодонах у Bacillus представлены, например, в патенте США 5024837 и у Johansen и др. (1988), Gene, 65: 293-304.
Методологии конструирования растительных кассет экспрессии, а также для интродукции чужеродной ДНК в растения известны в данной области техники и описаны. Такие кассеты экспрессии могут включать промоторы, терминаторы, энхансеры, лидерные последовательности, интроны и другие регуляторные последовательности, функционально сцепленные с последовательностью, кодирующей пестицидный протеин. Кроме того, подразумевается, что в кассетах экспрессии могут применяться промоторы или терминаторы генов VIP.
Обычно для интродукции чужеродной ДНК в растения в качестве векторов используют Ti-плазмиду, а также непосредственное поглощение ДНК, липосомы, электропорацию, микроинъекцию и, кроме того, используют микроснаряды. Такие способы известны в данной области техники и опубликованы. См., например, у Guerche и др. (1987), Plant Science, 52: 111-116; у Neuhause и др.(1987), Theor. Appl. Genet., 75: 30-36; у Klein и др. (1987), Nature, 327: 70-73; у Howell и др. (1980), Science, 208: 1265; у Horsch и др. (1985), Science 227: 1229-1231; у DeBlock и др. (1989). Plant Physiology, 91: 694-701; в Methods for Plant Molecular Biology (Weissbach и Weissbach, ред.) Academic Press, Inc. (1988); и в Methods in Plant Molecular Biology (Schuler и Zielinski, ред.) Academic Press, Inc. (1989). См. также заявку на патент США 08/008374, которая включена в настоящее описание в качестве ссылки. См. также европейские заявки ЕР-А 0193259 и ЕР-А 0451878. Очевидно, что метод трансформации будет зависеть от растительной клетки, которая должна быть трансформирована.
Далее предполагается, что компоненты кассеты экспрессии могут быть модифицированы с целью усиления экспрессии. Например, могут быть использованы усеченные последовательности, нуклеотидные замещения или другие модификации. См. , например, у Perlak и др., (1991) Proc. Natl. Acad. Sci.USA, 88: 3324-3328; у Murray и др., (1989) Nucleic Acid Research, 17: 477-498; и в международную заявку WO 91/16432.
Конструкция также может включать другие необходимые регуляторы, такие как терминаторы (Guerineau и др.,
(1991) Mol. Gen. Genet., 226; 141-144; Proudfoot, (1991) Cell, 64: 671-674; Sanfacon и др., (1991) Genes Dev., 5: 141-149; Mogen и др., (1990) Plant Cell, 2: 1261-1272; Munroe и др., (1990) Gene, 91:
151-158; Ballas и др., (1989) Nucleic Acids Res., 17: 7891-7903; Joshi и др., (1987) Nucleic Acid Res., 15: 9627-9639), трансляционные консенсусные последовательности растений (Joshi C.P., (1987)
Nucleic Acids Research, 15: 6643-6653), интроны (Luehrsen и Walbot, (1991), Mol. Gen. Genet, 225: 81-93) и т.п., функционально связанные с нуклеотидной последовательностью. Может
оказаться
целесообразным включение 5'-лидерных последовательностей в конструкцию кассеты экспрессии. Такие лидерные последовательности могут способствовать усилению трансляции. Лидеры трансляции известны в
данной области техники и включают:
лидерные последовательности пикорнавирусов, например, EMCV-лидер (5'-некодирующая область энцефаломиокардита) (Elroy -Stein О., Fuerst T.R. и Moss В..
(1989) PNAS USA. 86:6126-6130);
лидерные последовательности потивирусов, например, TEV-лидер (вирус гравировки табачной) (Allison и др., (1986); MDMV-лидер (вирус мозаичной карликовости
кукурузы); Virology, 154:9-20);
связывающий протеин тяжелой цепи человеческого иммуноглобулина (BiP) (Macejak D.G. и Sarnow P., (1991) Nature, 353:90-94);
нетранслируемую лидерную
последовательность мРНК из покровного протеина вируса мозаики люцерны (AMV RNA 4) (Jobling S.A. и Gehrke L., (1987) Nature, 325: 622-625);
лидерную последовательность вируса мозаики табака
(TMV) (Galliе D.R. и др., (1989), Molecular Biology of RNA, с. 237-256); и
лидерную последовательность вируса хлорозной мозаики кукурузы (MCMV) (Lommel S.A. и др., (1991) Virology, 81:
382-385; см. также у Della-Cioppa и др., (1987) Plant Physiology, 84:956-968).
В кассете экспрессии может быть использован терминатор из растений. См., например, у Rosenberg и др., (1987) Gene, 56: 125, у Guerineau и др., (1991) Mol. Gen. Genet. , 226: 141-144; у Proudfoot, (1991) Cell, 64: 671-674; у Sanfacon и др., (1991) Genes Dev., 5: 141-149; у Mogen и др., (1990) Plant Cell, 2: 1261-1271; у Munroe и др., (1990) Gene, 91: 151-158; у Ballas и др. , (1989) Nucleic Acid Res., 17: 7891-7903; у Joshi и др., (1987) Nucleic Acid Res., 15: 9627-9639.
Для тканеспецифичной экспрессии нуклеотидные последовательности по изобретению могут быть функционально связаны со специфичными для ткани промоторами. См. , например, европейскую заявку ЕР-А 0618976, включенную в настоящее описание в качестве ссылки.
Кроме того, настоящее изобретение включает трансгенные растения, в частности трансгенные фертильные растения, трансформированные с помощью вышеописанных способов, и их бесполое и/или половое потомство, включающее и, кроме того, предпочтительно экспрессирующее пестицидный протеин по изобретению. Особенно предпочтительными являются гибридные растения.
Трансгенное растение по изобретению может представлять собой двудольное или однодольное растение. Предпочтительными являются однодольные растения семейства Graminaceae (злаки), включающие растения родов Lolium, Zea, Triticum, Triticale, Sorghum, Saccharum, Bromus, Oryzae, Avena, Hordeum, Secale и Setaria.
Особенно предпочтительными являются трансгенные растения кукурузы, пшеницы, ячменя, сорго, ржи, овса, дернообразующих злаков и риса.
Среди двудольных растений особенно предпочтительными по изобретению являются соя, хлопчатник, табак, сахарная свекла, масличный рапс и подсолнечник.
Следует отметить, что понятие "потомство" включает потомство трансгенных растений, полученное как "бесполым", так и "половым" путем. Под это понятие также подпадают все мутанты и все разновидности, которые получают с помощью известных способов, таких как, например, гибридизация клеток или селекция мутантов, и которые проявляют характерные свойства исходного трансформированного растения, наряду со всеми продуктами скрещивания и гибридизации трансформированного растительного материала.
Еще один предмет изобретения относится к материалу для размножения трансгенных растений.
Под материалом для размножения трансгенных растений в контексте настоящего изобретения понимают любой растительный материал, который может быть размножен половым или бесполым путем in vivo или in vitro. Особенно предпочтительными согласно настоящему изобретению являются протопласты, клетки, каллюсы, ткани, органы, семена, эмбрионы, пыльца, яйцеклетки, зиготы, а также любой другой материал для размножения, получаемый из трансгенных растений.
Части растений, такие как, например, цветки, стебли, плоды, листья, корни, образующиеся у трансгенных растений или у их потомства, ранее трансформированных с помощью способа по изобретению и, следовательно, состоящие по крайней мере частично из трансгенных клеток, также являются предметом настоящего изобретения.
До поступления в продажу в качестве коммерческого продукта материала для размножения растений (плодов, клубней, зерна, семян) и прежде всего семенного материала его обычно обрабатывают защитным покрытием, содержащим гербициды, инсектициды, фунгициды, бактерициды, нематоциды, моллюскициды или смеси, состоящие из нескольких этих препаратов, при необходимости вместе с другими дополнительными носителями, поверхностно-активными веществами или способствующими нанесению адьювантами, обычно применямыми в области изготовления препаративных форм для обеспечения защиты от повреждения, вызванного бактериями, грибами или насекомыми-вредителями.
Для обработки семенного материала защитное покрытие может быть нанесено на семенной материал либо путем пропитки клубней или зерен жидким составом, либо путем нанесения на них покрытия из сложной влажной или сухой композиции. Кроме того, в особых случаях возможно использование других способов обработки растений, например путем направленной обработки почек или плодов.
Семенной материал для растения по изобретению содержит молекулу ДНК, содержащую нуклеотидную последовательность, кодирующую пестицидный протеин по изобретению, и может быть обработан покрытием, защищающим семенной материал и содержащим соединение, предназначенное для обработки семенного материала, такое как, например, каптан, карбоксин, тирам (TMTD®), металаксил (Apron®), пиримифос-метил (Actellic®) и другие соединения, которые обычно применяют для обработки семян. Предпочтительными по изобретению являются защищающие семенной материал покрытия, содержащие инсектицидную композицию по изобретению индивидуально или в сочетании с одним из защищающих семенной материал покрытий, обычно применяемым для обработки семян.
Таким образом, еще один предмет настоящего изобретения относится к материалу для размножения растений, предназначенному для получения культурных растений, и прежде всего к семенному материалу растения, который обрабатывают защищающим семенной материал покрытием, как это указано выше.
Было установлено, что гены, кодирующие пестицидные протеины, могут быть использованы для трансформации патогенных для насекомых организмов. К таким организмам относятся бакуловирусы, грибы, простейшие, бактерии и нематоды.
Штаммы Bacillus по изобретению могут применяться для защиты сельскохозяйственных культур и продуктов от вредителей. В альтернативном варианте ген, кодирующий пестицид, может быть интродуцирован с помощью пригодного для этой цели вектора в микроорганизм-хозяин, и этот хозяин может быть помещен в окружающую среду растений или животных. Могут быть отобраны микроорганизмы-хозяева, для которых известна способность заселять "фитосферу" (филлоплан, филлосферу, ризосферу и/или ризоплан) одного или нескольких представляющих интерес культурных растений. Отбирают такие микроорганизмы, которые способны успешно конкурировать в определенной среде с микроорганизмами дикого типа, обеспечивать стабильное поддержание и экспрессию гена, обладающего способностью к экспрессии полипептидного пестицида, и при необходимости обеспечивать улучшенную защиту пестицида от разложения и инактивации в окружающей среде.
Такие микроорганизмы включают бактерии, водоросли и грибы. Особенный интерес представляют такие микроорганизмы, как бактерии, например, Pseudomonas, Erwinia, Serratia, Klebsiella, Xanthomonas, Streptomyces, Rhizobium, Rhodopseudomonas, Methylius, Agrobacterium, Acetobacter, Lactobacillus, Arthrobacter, Azotobacter, Leuconostoc и Alcaligenes; грибы, прежде всего дрожжевые грибы, например, Saccharomyces, Cryptococcus, Kluyveromyces, Sporobolomyces, Rhodotorula и Aureobasidium. Особый интерес представляют такие виды бактерий фитосферы, как Pseudomonas syringae, Pseudomonas fluorescens, Serratia marcescens, Acetobacter xylinum, Agrobacteria, Rhodopseudomonas spheroides, Xanthomonas campestris, Rhizobium melioti, Alcaligenes entrophus, Clavibacter xyli и Azotobacter vinlandii; а также такие виды дрожжевых грибов фитосферы, как Rhodotorula rubra, R. glutinis, R. marina, R. aurantiaca, Cryptococcus albidus, C. diffluens, C. laurentii, Saсcharomyces rosei, S. pretoriensis, S. cerevisiae, Sporobolomyces rosues, S. odorus, Kluyveromyces veronae и Aureobasidium pollulans. Особый интерес представляют пигментированные микроорганизмы.
Для интродукции гена, экспрессирующего пестицидный протеин, в реципиентный микроорганизм в условиях, обеспечивающих стабильное поддержание и экспрессию гена, существует большое количество способов. Например, могут быть сконструированы кассеты экспрессии, влючающие представляющие интерес конструкции ДНК, функционально связанные с регуляторными сигналами транскрипции и трансляции для экспрессии конструкций ДНК и последовательности ДНК, гомологичной последовательности, в организме-хозяине, посредством чего достигается интеграция, и/или система репликации, которая функционирует в хозяине, посредством чего достигается интеграция или стабильное поддержание.
Регуляторные сигналы транскрипции и трансляции включают, но не ограничены ими, промотор, сайт инициации транскрипции, операторы, активаторы, энхансеры, другие регуляторные элементы, сайты связывания рибосом, инициирующий кодон, сигналы окончания транскрипции и т.п. См., например, патент США 5039523; патент США 4853331; опубликованную европейскую заявку ЕРО 0480762 А2; Sambrook и др., см. выше; Molecular Cloning, a Laboratory Manual, Maniatis и др. (ред.) Cold Spring Harbor Laboratory, Cold Spring Harbor, NY (1982); Advanced Bacterial Genetics, Davis и др. (ред.) Cold Spring Harbor Laboratory, Cold Spring Harbor, NY (1980); и указанные в этих публикациях ссылки.
Соответствующие клетки-хозяева, в которых содержащие пестицид клетки могут быть обработаны для пролонгирования активности токсина в клетке, с последующим внесением обработанной клетки в среду, окружающую вредителя(лей)-мишень(и), могут включать как клетки прокариот, так и эукариот, но обычно ограничены такими клетками, которые не продуцируют веществ, токсичных для высших организмов, таких как млекопитающие. Однако могут применяться также организмы, образующие токсичные для высших организмов вещества, если токсины нестабильны либо если уровень их выделения достаточно низок, что позволяет исключить любую возможность интоксикации хозяина-млекопитающего. В качестве хозяев особый интерес представляют прокариоты и низшие эукариоты, такие как грибы. Примеры прокариот, как грамотрицательных, так и грамположительных, включают Enterobacteriaceae, такие как Escherichia, Erwinia, Shigella, Salmonella и Proteus; Bacillaceae; Rhizobiceae, такие как Rhizobium; Spirillaceae, такие как фотобактерия, Zymomonas, Serratia, Aeromonas, Vibrio, Desulfоvibrio, Spirillum; Lactobacillaceae; Pseudomonadaceae, такие как Pseudomonas и Acetobacter; Azotobacteraceae и Nitrobacteraceae. Среди эукариот можно назвать грибы, такие как Phycomycetes и Ascomycetes, которые включают дрожжевые грибы, такие как Saccharomyces и Schizosaccharromyces; и дрожжевые грибы из класса Basidiomycetes, такие как Rhodotorula, Aureobasidium, Sporobolomyces и т.п.
При выборе хозяина для целей производства особый интерес представляют такие характеристики, как легкость интродукции гена протеина в хозяина, пригодность систем экспрессии, эффективность экспрессии, стабильность протеина в хозяине и наличие вспомогательных генетических возможностей. Характеристики, представляющие интерес для выбора используемой пестицидной микрокапсулы, включают защитные качества для пестицида, такие как толстые клеточные стенки, пигментация и внутриклеточная упаковка или образование включенных тел; сродство к листу; отсутствие токсичности для млекопитающих; привлекательность для вредителей при питании; способность легко вызывать гибель и поглощаться без повреждения токсина; и т.п. Другие важные условия включают простоту изготовления и применения, экономичность, стабильность при хранении и т.п.
Организмы-хозяева, представляющие особенный интерес, включают дрожжи, такие как Rhodotorula sp., Aureobasidium sp., Saccharomyces sp. и Sporobolomyces sp. ; организмы, обитающие на поверхности листа (филлоплан), такие как Pseudomonas sp., Erwinia sp. и Flavobacterium sp.; или другие организмы, такие как Escherichia, Lactobacillus sp., Bacillus sp. и т.п. Конкретные виды включают Pseudomonas aeurginosa, Pseudomonas fluorescens, Saccharomyces cerevisiae, Bacillus thuringiensis, Escherichia coli, Bacillus subtilis и т. п.
Гены VIP могут быть интродуцированы в микроорганизмы, которые размножаются на растениях (эпифиты), с целью доставить VIP-протеины к потенциальным вредителям-мишеням. Эпифиты могут представлять собой, например, грамположительные или грамотрицательные бактерии.
Бактерии, образующие колонии на корнях, например, могут быть выделены из представляющего интерес растения с помощью методов, известных в данной области техники. В частности из корней растений может быть выделен штамм Bacillus cereus, который образует колонии на корнях (например, см. у J. Handelsman, S. Raffel, E. Mester, L. Wunderlich и С. Grau в Appl. Environ. Microbiol. 56: 713-718 (1990)). VIP1 и/или VIP2 и/или VIP3 могут быть интродуцированы в Bacillus cereus, образующий колонии на корнях, с помощью стандартных методов, известных в данной области техники.
В частности VIP1 и/или VIP2, имеющие происхождение из штамма Bacillus cereus AB78, с помощью конъюгации с использованием стандартных методов (J. Gonzalez, В. Brown и В. Carlton, Proc. Natl. Acad. Sci. 79: 6951-6955 (1982)) могут быть интродуцированы в штамм Bacillus cereus, образующий колонии на корнях растений.
Кроме того, VIP1, и/или VIP2, и/или VIP3 либо другие VIP по изобретению с помощью электротрансформации могут быть интродуцированы в вид Bacillus, образующий колонии на корнях растений. В частности VIP могут быть клонированы в бифункциональном векторе, например, в рНТ3101 (D. Lereclus и др., FEMS Microbiol. Letts., 60: 211-218 (1989)), как описано в примере 10. Бифункциональный вектор рНТ3101, содержащий кодирующую последовательность для определенного VIP, затем с помощью электропорации (D. Lereclus и др., FEMS Microbiol. Letts., 60: 211-218 (1989)) может быть трансформирован в вид Bacillus, образующий колонии на корнях растений.
Системы экспрессии могут быть сконструированы таким образом, чтобы VIP-протеины секретировались вне цитоплазмы грамотрицательных бактерий, например, E.coli. Преимуществами секреции VIP-протеинов является то, что это (1) позволяет избежать потенциальных токсических воздействий VIP-протеинов, экспрессируемых внутри цитоплазмы, (2) способствует увеличению уровней экспрессируемых VIP-протеинов и (3) может способствовать эффективной очистке VIP-протеина.
Могут быть созданы VIP-протеины, обладающие способностью секретироваться, например, в Е.coli, путем слияния соответствующего сигнального пептида Е.coli с N-концом сигнального пептида VIP или путем замены сигнального пептида VIP на сигнальный пептид Е.coli. Сигнальные пептиды, распознаваемые Е. coli, могут быть выбраны среди протеинов, для которых уже известна способность секретироваться в Е.coli, например, таковым является протеин OmpA (J. Ghrayeb, H. Kimura, M. Takahara, Y. Masui и М. Inouye, EMBO J., 3: 2437-2442 (1984)). OmpA представляет собой основной протеин внешней мембраны Е. coli, и следовательно, его сигнальный пептид, как полагают, может быть эффективен для процесса транслокации. Кроме того, сигнальный пептид OmpA не нуждается в модификации перед процессингом, что необходимо для других сигнальных пептидов, например сигнального пептида липопротеина (G. Duffaud, P. March и Inouye, Methods in Enzymology, 153: 492 (1987)).
В частности уникальные сайты рестрикции BamHI могут быть интродуцированы на содержащие концевую аминогруппу и концевую карбоксильную группу концы последовательностей, кодирующих VIP, с использованием стандартных методов, известных в данной области техники. Эти BamHI-фрагменты могут быть клонированы в рамке считывания в векторе pIN-III-ompAl, А2 или A3 (J. Ghrayeb, H. Kimura, М. Takahara, Y. Masui и М. Inouye, EMBO J., 3: 2437-2442 (1984)), при этом получают слитый ген ompA:VIP, который секретируется в периплазматическое пространство. Другие сайты рестрикции в полилинкере pIN-III-ompAl могут быть удалены с помощью стандартных методов, известных в данной области техники, так что аминоконцевая аминокислота последовательности, кодирующей VIP, расположена непосредственно после сайта отщепления сигнального пептида оmрА. При этом последовательность, секретирующая VIP в Е. coli, должна быть идентична нативной последовательности VIP.
Если нативный сигнальный пептид VIP не требуется для соответствующей укладки зрелого протеина, то такие сигнальные последовательности могут быть удалены и замещены сигнальной последовательностью оmрА. Уникальные сайгы рестрикции BamHI могут быть интродуцированы на N-концы последовательностей, кодирующих пропротеин, непосредственно за последовательностью, кодирующей сигнальный пептид, последовательностями, кодирующими VIP, и на С-концы последовательностей, кодирующих VIP. Затем эти BamHI-фрагменты могут быть клонированы в векторах pIN-III-ompA, как описано выше.
Общие способы применения штаммов по изобретению в качестве пестицидов для борьбы с вредителями или для создания других организмов в качестве пестицидных агентов известны в данной области техники. См., например, патент США 5039523 и европейскую заявку ЕР 0480762 А2.
VIP в бактериальном хозяине могут быть подвергнуты ферментации, а полученные бактерии могут быть обработаны и применяться для микробиологического опрыскивания тем же образом, каким штаммы Bacillus thuringiensis используют для инсектицидных обработок. В случае VIP, которые секретируются из Bacillus, сигнал секреции удаляют или в нем получают мутации с использованием методов, известных в данной области техники. Такие мутации и/или делеции препятствуют секреции VIP-протеина(ов) в ростовую среду во время процесса ферментации. VIP сохраняют внутри клетки и клетки затем обрабатывают с получением инкапсулированных VIP. Для этой цели может использоваться любой пригодный микроорганизм. Для экспрессии эндотоксинов Bacillus thuringiensis в виде инкапсулированных протеинов применяли Pseudomonas, а образовавшиеся клетки обрабатывали и наносили путем опрыскивания как инсектициды (Н. Gaertner и др., 1993, Advanced Engineered Pesticides, ред. L. Kim).
Таким же образом применяют различные штаммы Bacillus thuringiensis. Такие штаммы Bt продуцируют протеин(ы) эндотоксина, а также VIP. В другом варианте такие штаммы могут продуцировать только VIP. Было подтверждено, что штамм Bacillus subtilis с дефицитом споруляции обладает способностью продуцировать высокие уровни эндотоксина CryIIIA из Bacillus thuringiensis (Agaisse Н. и Lereclus D., "Expression in Bacillus subtilis of the Bacillus thuringiensis CryIIIA toxin gene is not dependent on sporulation-specific sigma factor and is increased in a spoOA mutant", J. Bacteriol., 176: 4734-4741 (1994)). Аналогичный spoOA-мутант может быть получен в Bacillus thuringiensis и использован для получения инкапсулированного VIP, который не секретируется в среду, но сохраняется внутри клетки.
С целью поддерживать VIP в клетке Bacillus сигнальный пептид может быть изменен ("обезоружен") таким образом, чтобы он не мог более функционировать в качестве сигнала секреции. В частности предполагаемый сигнальный пептид VIP1 состоит из первых 31 аминокислот протеина с предполагаемым консенсусным сайтом расщепления Ala-X-Ala на С-концевой части этой последовательности (G. von Heijne, J. Mol. Biol. 184:99-105 (1989)), а предполагаемый сигнальный пептид VIP2 состоит из первых 40 аминокислот протеина с предполагаемым сайтом расщепления после А1а40. В сайтах расщепления как в VIP1, так и в VIP2 мутации можно получить способами, известными в данной области техники, с той целью, чтобы заменить сайт расщепления консенсусной последовательности на альтернативные аминокислоты, которые не распознаются сигнальными пептидазами.
Альтернативно этому сигнальные пептиды VIP1, VIP2 и/или других VIP по изобретению могут быть удалены из последовательности, что тем самым делает эти секретируемые протеины не распознаваемыми для Bacillus. В частности стартовый кодон метионина может быть встроен впереди последовательности пропротеина VIP1, начинаясь на Asp32, или последовательности предшественника протеина VIP2, начинаясь на Glu41, с использованием методов, известных в данной области техники.
Гены VIP могут быть интродуцированы в микроорганизмы, которые размножаются на растениях (эпифиты), с целью доставить VIP-протеины к потенциальным вредителям-мишеням. Эпифиты могут представлять собой, например, грамположительные или грамотрицательные бактерии.
Штаммы Bacillus по изобретению или микроорганизмы, которые генетически были изменены таким образом, чтобы они содержали пестицидный ген и протеин, могут применяться для защиты сельскохозяйственных культур и продуктов от вредителей. В одном из вариантов изобретения целые, т.е. неповрежденные клетки токсин (пестицид)-продуцирующего организма обрабатывают реагентами, которые пролонгируют активность токсина, образующегося в клетке, когда клетка внесена в среду, окружающую вредителя(лей)-мишень(и).
В другом варианте пестициды получают путем интродукции гетерологичного гена в клетку-хозяин. Экспрессия гетерологичного гена приводит, прямо или косвенно, к внутриклеточному производству и поддерживанию пестицида. Затем эти клетки обрабатывают в условиях, позволяющих пролонгировать активность токсина, образующегося в клетке, когда клетка внесена в среду, окружающую вредителя(лей)-мишень(и). Образовавшийся продукт сохраняет токсичность токсина. Эти естественные инкапсулированные пестициды могут быть затем приготовлены в соответствии со стандартными методами для обработки естественного окружения вредителя-мишени, например почвы, воды или листьев растений. См., например, европейскую заявку ЕРА 0192319 и указанные в ней ссылки.
Действующие вещества по изобретению при обработке обычно используют в виде композиций, и ими можно обрабатывать возделываемую посевную площадь или растения, подлежащие обработке, одновременно или поочередно с другими соединениями. Эти соединения могут представлять собой как удобрения, так и доноры микроэлементов либо другие препараты, влияющие на рост растения. Они могут также представлять собой определенные гербициды, инсектициды, фунгициды, бактеридиды, нематоциды, моллюскициды или смеси из нескольких этих препаратов, при необходимости совместно с приемлемыми для сельского хозяйства носителями, поверхностно-активными веществами или способствующими нанесению адъювантами, обычно применяемыми в области изготовления препаративных форм. Соответствующие носители и адъюванты могут быть твердыми или жидкими и представляют собой вещества, обычно применяемые в технологии приготовления препаративных форм, например натуральные или регенерированные минеральные вещества, растворители, диспергирующие агенты, смачивающе агенты, вещества, повышающие клейкость, связующие вещества или удобрения.
Предпочтительные способы обработки действующим веществом по изобретению или агрохимической композиций по изобретению, которая содержит по крайней мере один из специфичных в отношении насекомых протеинов, полученный из бактериальных штаммов по изобретению, включают обработку листьев, покрытие семян или внесение в почву. Количество обработок и норма расхода при обработке зависят от интенсивности заражения соответствующим вредителем.
Настоящее изобретение, кроме того, относится к инсектицидной композиции, содержащей в качестве действующего вещества по крайней мере один из новых специфичных в отношении насекомых протеинов по изобретению и/или рекомбинатнтный микроорганизм, содержащий по крайней мере одну молекулу ДНК, которая содержит нуклеотидную последовательность, кодирующую новые специфичные в отношении насекомых протеины в рекомбинантной форме, и прежде всего рекомбинантный штамм Bacillus spp., такой как Bacillus cereus или Bacillus thuringiensis, включающий по крайней мере одну молекулу ДНК, которая содержит нуклеотидную последовательность, кодирующую новые специфичные в отношении насекомых протеины в рекомбинантной форме, или ее производное либо ее мутант вместе с приемлемым для сельского хозяйства адъювантом, таким как носитель, растворитель, поверхностно-активное вещество или способствующий нанесению адъювант. Композиция также может содержать дополнительное биологически активное соединение. Это соединение может представлять собой как удобрение, так и донор микроэлементов или другие препараты, влияющие на рост растения.
Оно также может представлять собой определенный гербицид, инсектицид, фунгицид, бактерицид, нематоцид, моллюскицид или смеси из нескольких этих препаратов, при необходимости вместе с дополнительными приемлемыми для сельского хозяйства носителями, поверхностно-активными веществами или способствющими нанесению адъювантами, обычно применяемыми в области приготовления препаративных форм. Соответствующие носители и адъюванты могут быть твердыми или жидкими и представляют собой вещества, обычно применяемые в технологии приготовления препаративных форм, например натуральные или регенерированные минеральные вещества, растворители, диспергирующие агенты, смачивающие агенты, вещества, повышающие клейкость, связующие вещества или удобрения.
Композиция может содержать от 0,1 до 99 мас.% действующего вещества, от 1 до 99,9 мас.% твердого или жидкого адъюванта и от 0 до 25 мас.% поверхностно-активного вещества. Обработка действующим веществом, включающим по крайней мере один из новых специфичных в отношении насекомых протеинов по изобретению или рекомбинантный микроорганизм, содержащий по крайней мере одну молекулу ДНК, которая содержит нуклеотидную последовательность, кодирующую новые специфичные в отношении насекомых протеины в рекомбинантной форме, и прежде всего рекомбинантный штамм Bacillus spp., такой как штамм Bacillus cereus или Bacillus thuringiensis, включающий по крайней мере одну молекулу ДНК, которая содержит нуклеотидную последовательность, кодирующую новые специфичные для насекомых протеины в рекомбинантной форме, или ее производное либо ее мутант, или композицией, содержащей это действующее вещество, может быть осуществлена без потери активности при применении на подлежащих защите растениях или сельскохозяйственных культурах совместно с некоторыми другими инсектицидами или химическими веществами (1993 Crop Protection Chemicals Reference, Chemical and Pharmaceutical Press, Canada). Это действующее вещество совместимо с большинством других материалов, обычно применяемых в сельском хозяйстве для опрыскивания, но не должно применяться в сильно щелочных растворах для опрыскивания. Его можно применять в виде дуста, суспензии, смачивающегося порошка или в виде любой другой препаративной формы, пригодной для сельскохозяйственной обработки.
Кроме того, изобретение относится к способам борьбы или подавления насекомых-вредителей путем обработки действующим веществом, включающим по крайней мере один из новых специфичных в отношении насекомых протеинов по изобретению или рекомбинантный микроорганизм, содержащий по крайней мере одну молекулу ДНК, которая содержит нуклеотидную последовательность, кодирующую новые специфичные в отношении насекомых протеины в рекомбинантной форме, или композицией, содержащей это действующее вещество, (а) окружающей среды, в которой насекомое-вредитель может обитать, (б) растения или части растения для защиты растения или его части от повреждения, вызываемого насекомым-вредителем или (в) семенного материала для защиты растения, которое развивается из семенного материала, от повреждения, вызываемого насекомым-вредителем.
Предпочтительным способом обработки в области защиты растений является обработка листьев растений (листовая обработка) с периодичностью и нормой расхода, зависящими от растения, подлежащего защите, и риска поражения предполагаемым вредителем. Однако действующее вещество также может проникать в растение через корни (системное действие) при насыщении местообитания растения жидкой композицией либо, если действующее вещество применяют в твердой форме, в место произрастания растений, например в почву, в том числе в виде гранул (почвенная обработка). В случае культур риса-падди обработку такими гранулами можно проводить в определенных количествах на затопленных рисовых полях.
Композиции по изобретению также пригодны для защиты от насекомых-вредителей материала для размножения растения, например семенного материала, такого как плоды, клубни или зерна, либо черенков растения. Материал для размножения может быть обработан композицией до посадки, например семенной материал можно протравливать перед посевом. Действующее вещество по изобретению также может быть нанесено на зерна (покрытие) либо путем пропитки зерен жидкой композицией, либо путем покрытия их твердой композицией. Композицией также может быть обработано место посадки при высаживании материала для размножения, например, борозды при посеве семян. Изобретение также относится к этим способам обработки материала для размножения растений и к обработанному таким образом материалу для размножения растений.
Обработку композициями по изобретению, содержащими в качестве действующего вещества рекомбинантный микроорганизм, содержащий по крайней мере один из новых генов токсина в рекомбинантной форме, и прежде всего рекомбинантный штамм Bacillus spp. , такой как штамм Bacillus cereus или Bacillus thuringiensis, включающий по крайней мере одну молекулу ДНК, которая содержит нуклеотидную последовательность, кодирующую новые специфичные в отношении насекомых протеины в рекомбинантной форме, или ее производное либо ее мутант, можно проводить с помощью любого известного способа, применяемого для обработки семян или почвы штаммами бактерий. См. , например, патент США 4863866. Штаммы эффективны для биологической борьбы даже при использовании неживого микроорганизма. Однако предпочтительной является обработка живым микроорганизмом.
Подлежащие защите культурные растения-мишени, подпадающие под объем настоящего изобретения, включают, например, следующие виды растений: зерновые (пшеница, ячмень, рожь, овес, рис, сорго и родственные культуры), свекольные (сахарная свекла и кормовая свекла), кормовые травы (ежа сборная, овсяница и т. п. ), косточковые, семечковые, ягодные культуры (яблони, груши, сливы, персики, миндаль, вишни, земляника, малина и ежевика), бобовые растения (бобы, чечевица, горох, соя), масличные культуры (рапс, горчица, мак, маслины, подсолнечниковые, кокосы, клещевина, какао-бобы, арахис), огуречные растения (огурец, тыква, дыня), волокнистые растения (хлопчатник, лен, конопля, джут), цитрусовые культуры (апельсины, лимоны, грейпфрут, мандарины), овощные культуры (шпинат, салат, спаржа, капустные и другие представители сем. Brassicae, луки, томаты, картофель, перец), лавровые (авокадо, морковь, коричное дерево, камфорный лавр), лиственные и хвойные деревья (например, липа, тис, дуб, ольховые, тополевые, береза, пихтовые, лиственничные, сосновые) или такие растения, как кукуруза, табак, орех, кофе, сахарный тростник, чай, виноград, хмель, бананы и природные каучуконосы, а также декоративные (включая цветочные) культуры.
Рекомбинантный штамм Bacillus spp., такой как штамм Bacillus cereus или Bacillus thuringiensis, включающий по крайней мере одну молекулу ДНК, которая содержит нуклеотидную последовательность, кодирующую новые специфичные в отношении насекомых протеины в рекомбинантной форме, обычно применяют в виде инсектицидных композиций, и ими можно обрабатывать возделываемую посевную площадь или растение, подлежащее обработке, одновременно или последовательно с другими биологически активными соединениями. Эти соединения могут представлять собой как удобрения или доноры микроэлементов, так и другие препараты, оказывающие влияние на рост растения. Они также могут представлять собой определенные гербициды, инсектициды, фунгициды, бактерициды, нематоциды, моллюскициды или смеси, состоящие из нескольких этих препаратов, при необходимости вместе с другими носителями, поверхностно-активными веществами или способствующими нанесению адъювантами, обычно применямыми в области приготовления препаративных форм.
Действующее вещество по изобретению также может применяться в немодифицированной форме или вместе с любым пригодным, применяемым в сельском хозяйстве носителем. Такие носители представляют собой адъюванты, обычно применяемые в области приготовления сельскохозяйственных препаративных форм, которые, следовательно, можно обычным способом приготавливать в виде эмульсионных концентратов, покрывающих паст, готовых к применению разбрызгиваемых или разбавляемых растворов, разбавленных эмульсий, смачивающихся порошков, растворимых порошков, дустов, гранул, а также в виде инкапсулированных препаративных форм, например, в полимерных веществах. Способы обработки, такие как опрыскивание, обработка в виде туманов, опыливание, опудривание или полив, равно как и тип композиций выбирают в соответствии с поставленными целями и существующими конкретными условиями. Предпочтительные нормы расхода обычно составляют от 50 г до 5 кг действующего вещества (д.в.) на гектар (1 "га" приблизительно равен 2471 акру), предпочтительно от приблизительно 100 г до приблизительно 2 кг д.в./га. Наиболее часто используемые нормы расхода составляют от приблизительно 200 г до до приблизительно 1 кг д.в./га и от 200 до 500 г д.в./га.
Для протравливания семян предпочтительные нормы расхода составляют от 0,5 г до 1000 г д.в. на 100 кг семян, предпочтительно от 3 г до 100 г д.в. на 100 кг семян или от 10 г до 50 г д.в. на 100 кг семян.
Соответствующие носители и адъюванты могут быть твердыми или жидкими и представляют собой вещества, обычно применяемые в технологии приготовления препаративных форм, например, они могут быть натуральными или регенерированными минеральными веществами, растворителями, диспергирующими агентами, смачивающими агентами, повышающими клейкость агентами, связующими веществами или удобрениями. Препаративные формы, т.е. инсектицидные композиции, препараты или смеси, содержащие в качестве действующего вещества рекомбинантный штамм Bacillus spp. , такой как штамм Bacillus cereus или Bacillus thuringiensis, включающий по крайней мере одну молекулу ДНК, которая содержит нуклеотидную последовательность, кодирующую новые специфичные в отношении насекомых протеины в рекомбинантной форме, или его комбинации с другими действующими веществами и при необходимости твердый или жидкий адъювант, получают обычными способом, например путем гомогенного смешения и/или измельчения действующих веществ с наполнителями, например с разбавителями, твердыми носителями и в некоторых случаях с поверхносто-активными веществами (детергентами).
Пригодными растворителями являются: ароматические углеводороды, предпочтительно фракции с 8-12 атомами углерода, например, ксилоловые смеси или замещенные нафталины, фталаты, такие как дибутилфталат или диоктилфталат, алифатические углеводороды, такие как циклогексан или парафины, спирты и гликоли и их простые и сложные эфиры, такие как этанол, монометиловый или моноэтиловый эфиры этиленгликоля, кетоны, такие как циклогексанон, высокополярные растворители, такие как N-метил-2-пирролидон, диметилсульфоксид или диметилформамид, а также растительные масла или эпоксидированные растительные масла, такие как эпоксидированное кокосовое масло или соевое масло; или вода.
Твердые носители, применяемые, например, для дустов и диспергируемых порошков, обычно представляют собой природные минеральные наполнители, такие как кальцит, тальк, каолин, монтмориллонит или аттапульгит. С целью улучшить физические свойства также можно добавлять высокодисперсную кремниевую кислоту или высокодисперсные адсорбирующие полимеры. Пригодными гранулированными адсорбционными носителями являются таковые пористого типа, например пемза, битый кирпич, сепиолит или бентонит; а пригодными несорбирующим носителями являются такие материалы, как кальцит или песок. Кроме того, может применяться большое число предварительно гранулированных материалов неорганического или органического происхождения, например, особенно предпочтительны доломит или растертые в порошок растительные остатки.
В зависимости от природы используемых в композиции действующих веществ пригодными поверхностно-активными соединениями являются неионогенные, катионогенные и/или анионогенные поверхностно-активные вещества, обеспечивающие хорошие эмульгирующие, диспергирующие и смачивающие свойства. Под понятие "поверхностно-активные вещества" также подпадают смеси поверхностно-активных веществ. Пригодные неионогенные поверхностно-активные вещества могут представлять собой как водорастворимые мыла, так и водорастворимые синтетические поверхностно-активные вещества.
Пригодными мылами являются соли щелочных металлов, соли щелочноземельных металлов или незамещенные либо замещенные соли аммония и высших жирных кислот (C10-C22), например натриевые или калиевые соли олеиновой или стеариновой кислоты, или смесей природных жирных кислот, которые могут быть получены, например, из кокосового или таллового масла. Кроме того, пригодными поверхностно-активными веществами также являются метилтауриновые соли жирных кислот, а также модифицированные или немодифицированные фосфолипиды.
Более часто, однако, применяют так называемые синтетические поверхностно-активные вещества, прежде всего жирные сульфонаты, жирные сульфаты, сульфированные производные бензимидазола или алкиларилсульфонаты. Жирные сульфонаты или сульфаты обычно применяют в виде солей щелочных металлов, солей щелочно- земельных металлов или незамещенных либо замещенных аммонийных солей, и они обычно содержат C8-С22алкильный радикал, который также включает алкильный фрагмент ацильных радикалов, например, в виде натриевой или кальциевой соли лигносульфоновой кислоты, додецилсульфата или смеси сульфатов жирных спиртов, полученных из природных жирных кислот. Эти соединения также включают соли эфиров серной кислоты и соли сульфоновых кислот аддуктов жирного спирта/этиленоксида. Сульфированные производные бензимидазола предпочтительно содержат 2 группы сульфоновой кислоты и один радикал жирной кислоты, содержащий приблизительно от 8 от 22 атомов углерода. Примерами алкиларилсульфонатов являются натриевые, кальциевые или триэтаноламиновые соли додецилбензолсульфоновой кислоты, дибутилнафталинсульфоновой кислоты или продукта конденсации нафталинсульфоновой кислоты/формальдегида. Также пригодными являются соответствующие фосфаты, например соли эфира фосфорной кислоты и аддукта пара-нонилфенола с 4-14 моль этиленоксида.
Неионогенные поверхностно-активные вещества предпочтительно представляют собой производные полигликолевого эфира и алифатических или циклоалифатических спиртов или насыщенных либо ненасыщенных жирных кислот и алкилфенолов, и эти производные содержат 3-30 гликольэфирных групп и 8-20 атомов углерода в (алифатическом) углеводородном фрагменте и 6-18 атомов углерода в алкильном фрагменте алкилфенолов.
Кроме того, пригодными неионогенными поверхностно-активными веществами являются водорастворимые аддукты полиэтиленоксида и полипропиленгликоля, этилендиаминпропиленгликоля и алкилпропиленгликоля, содержащие 1-10 атомов углерода в алкильной цепи, причем аддукты содержат 20-250 групп этиленгликолевого эфира и 10-100 групп пропиленгликолевого эфира. Эти соединения обычно содержат 1-5 фрагментов этиленгликоля на фрагмент пропиленгликоля. Характерными примерами неионогенных поверхностно-активных веществ являются нонилфенолполиэтоксиэтанолы, простые эфиры касторового масла и полигликоля, аддукты полипропилен/полиэтиленоксида, трибутилфеноксиполиэтоксиэтанол, полиэтиленгликоль и октилфеноксиэтоксиэтанол. Эфиры жирных кислот и полиоксиэтиленсорбитана, такие как триолеат полиоксиэтиленсорбитана, также являются пригодными неионогенными поверхностно-активными веществами.
Катионогенные поверхностно-активные вещества предпочтительно представляют собой соли четвертичного аммония, которые имеют в качестве N-заместителя по крайней мере один С8-С22алкильный радикал и, кроме того, в качестве дополнительных заместителей незамещенные либо галогенированные низшие алкильные, бензильные или гидрокси-(низший)алкильные радикалы. Предпочтительны соли в виде галогенидов, метилсульфатов или этилсульфатов, например хлорид стеарилтриметиламмония или бромид бензилди(2-хлорэтил)этиламмония.
Поверхностно-активные вещества, обычно применяемые в области приготовления препаративных форм, описаны, например, в "McCutcheon's Detergents and Emulsifiers Annual", MC Publishing Corp. Ridgewood, N.J., 1979; и у Dr. Helmut Stache, "Tensid Taschenbuch" (Handbook of Surfactants), Carl Hanser Verlag, Munich/Vienna.
Другой особенно предпочтительной характеристикой инсектицидной композиции по настоящему изобретению является персистентность действующего вещества при обработке растений и почвы. Возможные причины потери активности включают инактивацию под действием ультрафиолетового излучения, температуры, выделений из листьев и рН. Например, при высоком значении рН, в частности в присутствии восстановителя, кристаллы δ-эндотоксина растворяются и, таким образом, становятся более чувствительными к протеолитической инактивации. Высокое значение рН листа также может иметь важное значение, в частности, когда рН листовой поверхности находится в диапазоне 8-10. Препаративная форма инсектицидной композиции по настоящему изобретению позволяет решить эти проблемы либо путем включения добавок, помогающих предотвратить потерю действующего вещества, либо путем инкапсулирования материала таким образом, чтобы защитить действующее вещество от инактивации. Инкапсулирование может быть осуществлено либо химическим путем (McGuire и Shasha, J. Econ. Entomol. 85:1425-1433, 1992), либо биологическим путем (Barnes и Cummings, 1986; ЕР-А 0192319). Химическое инкапсулирование включает процесс, при котором действующее вещество покрывают полимером, в то время как биологическое инкапсулирование включает экспрессию генов δ-эндотоксина в микроорганизме. Для биологического инкапсулирования в качестве действующего вещества в композиции применяют интактный микроорганизм, содержащий по крайней мере одну молекулу ДНК, которая содержит нуклеотидную последовательность, кодирующую новые специфичные в отношении насекомых протеины в рекомбинантной форме. Добавление агентов, защищающих от УФ, может эффективно снизить отрицательное воздействие облучения УФ-лучами. Инактивацию вследствие нагрева также можно контролировать путем включения соответствующей добавки.
Предпочтительными по настоящему изобретению являются препаративные формы, содержащие в качестве действующего вещества живые микроорганизмы в виде вегетативной клетки либо более предпочтительно в виде спор, если это возможно. Соответствующие препаративные формы могут состоять, например, из полимерных гелей, которые сшивают с многовалентными катионами, и они также включают эти микроорганизмы. Это описано, например, у D.R. Fravel и др., Phytopathology, том. 75, 7, 774-777, 1985, при использовании в качестве полимерного материала альгината. Из этой публикации также известно, что совместно могут быть использованы носители. Такие препаративные формы, как правило, получают путем смешения растворов из встречающихся в естественных условиях или синтетических гелеобразующих полимеров, например альгинатов, и водных солевых растворов ионов поливалентных металлов с образованием форм в виде отдельных капель, при этом микроорганизмы могут быть суспендированы в одном из двух или в обоих реакционных растворах. Гелеобразование начинается со смешения в капельной форме. Возможна последующая сушка этих частиц геля. Этот процесс называют ионотропным гелеобразованием. В зависимости от степени высушивания получают компактные и твердые частицы полимеров, которые структурно сшиты многозарядными катионами и содержат в основном однородно распределенные микроорганизмы и носитель. Размер частиц может достигать 5 мм.
Композиции, которые основаны на частично сшитых полисахаридах и которые в дополнение к микроорганизмам могут включать, например, тонкодиперсную кремниевую кислоту в качестве носителя, где сшивание происходит посредством ионов Ca++, описаны в европейской заявке ЕР-А1-0097571. Композиции имеют активность в водном растворе не более 0,3. У W.J. Cornick и др. в обзорной статье [New Directions in Biological Control: Alternatives for Suppressing Agricultural Pests and Diseases, с. 345-372, Alan R. Uss, Inc. (1990)] описаны различные системы препаративных форм, гранулы с вермикулитом в качестве носителя и компактные альгинатные гранулы, полученные способом указанного выше ионотропного гелеобразования. Такие композиции также описаны у D. R. Fravel в Pesticide Formulations and Applications Systems: 11-й том, ASTM STP 1112 American Society for Testing and Materials, Philadelphia, 1992, с. 173-179, и они могут быть использованы для приготовления препаративной формы рекомбинантных микроорганизмов по изобретению.
Инсектицидные композиции по изобретению обычно содержат от приблизительно 0,1 до приблизительно 99%, предпочтительно от приблизительно 0,1 до приблизительно 95% и наиболее предпочтительно от приблизительно 3 до приблизительно 90% действующего вещества, от приблизительно 1 до приблизительно 95%, предпочтительно от приблизительно 1 до приблизительно 99% и наиболее предпочтительно от приблизительно 5 до приблизительно 95% твердого или жидкого адъюванта и от приблизительно 0 до приблизительно 25%, предпочтительно от приблизительно 0,1 до приблизительно 25% и наиболее предпочтительно от приблизительно 0,1 до приблизительно 20% поверхностно-активного вещества.
В предпочтительном варианте осуществления инсектицидные композиции по изобретению обычно содержат от 0,1 до 99%, предпочтительно от 0,1 до 95% рекомбинантного штамма Bacillus spp., такого как штамм Bacillus cereus или Bacillus thuringiensis, включающего по крайней мере одну молекулу ДНК, которая содержит нуклеотидную последовательность, кодирующую новые специфичные в отношении насекомых протеины в рекомбинантной форме, или его комбинации с другими действующими веществами, от 1 до 99,9% твердого или жидкого адъюванта и от 0 до 25%, предпочтительно от 0,1 до 20% поверхностно-активного вещества.
Хотя коммерческие продукты предпочтительно изготавливают в виде концентратов, конечный потребитель обычно должен применять разбавленные композиции с существенно более низкой концентрацией. Инсектицидные композиции также могут содержать дополнительные ингредиенты, такие как стабилизаторы, пеногасители, регуляторы вязкости, связующие вещества, повышающие клейкость агенты, а также удобрения или другие активные ингредиенты для достижения определенных эффектов.
В одном из примеров осуществления изобретения был выделен микроорганизм Bacillus cereus, обладающий способностью вызывать гибель Diabrotica virgifera virgifera и Diabrotica longicornis barberi. Новый штамм B.cereus AB78 был помещен в Agricultural Research Service, Patent Culture Collection (NRRL), Nothern Regional Research Center (коллекция культур для целей патентования Службы сельскохозяйственных исследований США (NRRL), Северный региональный исследовательский центр), 1815 North University Street, Peoria, IL 61604, USA, и получил регистрационный NRRL B-21058.
Фракция протеина из штамма B.cereus была практически чистой. Эта чистота протеина была подтверждена с помощью электрофореза в ДСН-ПААГ и на основе его биологической активности. Протеин, имеющий молекулярную массу приблизительно от 60 до приблизительно 100 кДа, в частности приблизительно от 70 до приблизительно 90 кДа, и прежде всего приблизительно 80 кДа, обозначен в настоящем описании как VIP.
Аминоконцевое секвенирование показало, что N-концевая аминокислотная последовательность должна представлять собой: NH2 -Lys-Arg-Glu-Ile-Asp-Glu-Asp-Thr-Asp-Thr-Asx-Gly-Asp-Ser-Ile-Pro-(последовательность SEQ ID NO: 8), где Asx обозначает либо Asp, либо Asn. Полная аминокислотная последовательность представлена в SEQ ID NO: 7. Последовательность ДНК, которая кодирует аминокислотную последовательность SEQ ID NO: 7, представлена в SEQ ID NO: 6.
Был получен олигонуклеотидный зонд для области гена,
кодирующей аминокислоты 3-9 NH2-конца. Зонд синтезировали на основе наиболее часто встречающегося кодона гена δ-эндотоксина Bacillus thuringensis (Bt). Нуклеотидная
последовательность олигонуклеотидного зонда, используемого для Саузерн-гибридизаций, была следующей:
5'-GAA ATT GAT САА GAT ACN GAT-3' (SEQ ID NO: 9). где N обозначает любое основание.
Кроме того, ДНК-зонд для гена VIP1 Bс AB78, представленный в настоящем описании, позволяет осуществлять отбор любого штамма Bacillus или других организмов с целью определить, присутствует ли в нем ген VIP1 (или родственный ему ген) в естественном состоянии, или трансформированный специальным образом организм включает ген VIP1.
Таким образом, выше представлено общее описание изобретения, сущность которого более подробно поясняется на приведенных ниже примерах, иллюстрирующих настоящее изобретение, и их не следует рассматривать как ограничивающие его объем, если нет специального указания.
Была разработана стандартная номенклатура на основе идентичности последовательностей протеинов, включенных в объем настоящего изобретения. Названия генов и протеинов, используемые в подробных примерах, и их взаимосвязь с названиями, которые использовались в первичной заявке [заявка на патент США 314594/08], представлены в табл.I.
Экспериментальная часть
Примеры композиций
Действующее вещество, применяемое в приведенных ниже примерах препаративных форм, представляет собой штамм Bacillus cereus, имеющий
регистрационнй номер NRRL В-21058; штаммы Bacillus thuringiensis, имеющие регистрационные номера NRRL В-21060. NRRL B-21224, NRRL B-21225, NRRL В-21226, NRRL В-21227 и NRRL B-21439; и штаммы Bacillus
spp., имеющие регистрационные номера NRRL В-21228, NRRL В-21229 и NRRL B-21230. Все указанные выше штаммы представляют собой природные изоляты, содержащие специфичные в отношении насекомых протеины по
изобретению.
В альтернативном варианте выделенные специфичные в отношении насекомых протеины применяют в качестве действующего вещества по отдельности или в комбинации с перечисленными выше штаммами Bacillus.
А1. Смачиващиеся порошки см табл. II
Споры тщательно смешивают с адъювантами и смесь тщательно размалывают в пригодной для этой цели
мельнице, получая смачивающиеся порошки, которые могут быть разбавлены водой для получения суспензий требуемых концентраций.
А2. Эмульсионные концентраты
Споры Bacillus
thuringiensis - 10%
Полиэтиленгликолевый эфир октилфенола (4-5 моль этиленоксида) - 3%
Додецилбензолсульфонат кальция - 3%
Полиэтиленгликолевый эфир касторового масла (36
моль этиленоксида) - 4%
Циклогексанон - 30%
Смесь ксилолов - 50%
Эмульсии любой требуемой концентрации могут быть получены из этого концентрата разбавлением водой.
A3. Дусты см. табл. III.
Готовые к применению дусты получают смешением действующего вещества с носителями и измельчением смеси в пригодной для этой цели мельнице.
А4. Экструдированный гранулят
Споры Bacillus thuringiensis - 10%
Лигносульфонат натрия - 2%
Карбоксиметилцеллюлоза - 1%
Каолин - 87%
Действующее
вещество или их комбинацию смешивают и измельчают совместно с адъювантами и смесь далее увлажняют водой. Смесь экструдируют, гранулируют и сушат в потоке воздуха.
А5. Гранулы с
покрытием
Споры Bacillus thuringiensis - 3%
Полиэтиленгликоль (мол. масса 200) - 3%
Каолин - 94%
Действующее вещество или их комбинацию равномерно подают в
смеситель к каолину, увлажненному полиэтиленгликолем. Таким путем получают беспылевые гранулы с покрытием.
А6. Суспензионный концентрат
Споры Bacillus thuringiensis - 40%
Этиленгликоль - 10%
Полиэтиленгликолевый эфир нонилфенола (15 моль этиленоксида) - 6%
Лигносульфонат натрия - 10%
Карбоксиметилцеллюлоза - 1%
37%-ный водный
раствор формальдегида - 0,2%
Силиконовое масло в виде 75%-ного водного раствора - 0,8%
Вода - 32%
Действующее вещество или их комбинацию смешивают до гомогенности с
адъювантами, получая суспензионный концентрат, из которого путем разбавления водой могут быть получены суспензии любой требуемой концентрации.
Пример 1. Выделение и характеристика
АВ78
Штамм Bacillus cereus AB78 выделяли в лабораторных условиях как контаминант на чашках в среде Т3 (на литр: 3 г триптона, 2 г триптозы, 1,5 г дрожжевого экстракта, 0,05М фосфат натрия (рН
6,8) и 0,005 г MnCl2; Travers R. S. , 1983). Во время фазы логарифмического роста штамм АБ78 проявлял выраженную активность в отношении блошки длинноусой западной. Была также подтверждена
антибиотическая активность в отношении грамположительных Bacillus spp. (таблица 12).
Морфологические характеристики штамма АВ78 были следующими.
Вегетативные палочки прямые, 3,1-5,0 мм длиной и 0,5-2,0 мм шириной. Клетки с закругленными концами, одиночные, собранные в короткие цепочки. Из каждой клетки образуется одиночная субтерминальная, цилиндрически-овальная эндоспора. Параспоральный кристалл не образуется. Колонии непрозрачные, складчато-морщинистые, долевидные и плоские. Не продуцирует пигментов. Клетки подвижные. Имеются жгутики.
Характеристики роста АВ78 были следующими. Факультативный анаэроб с оптимальной температурой для роста 21-30oС. Может расти при 15, 20, 25, 30 и 37oС. Не может расти при температуре свыше 40oС. Растет в среде с 5-7%-ным NaCl.
В таблице 13 представлен биохимический профиль штамма АВ78.
Пример 2. Бактериальная культура
Субкультуру штамма Bc AB78 использовали для инокуляции в среду, известную как ТВ-бульон следующего состава:
Триптон - 12 г/л
Дрожжевой экстракт - 24 г/л
Глицерин - 4
мл/л
КН2РO4 - 2,1 г/л
К2НРO4 - 14,7 г/л
РН 7,4
Фосфат калия добавляли к автоклавированному бульону после охлаждения.
Колбы инкубировали при 30oС на роторном вибраторе при 250 об/мин в течение 24-36 часов, что соответствует началу средней логарифмической фазы.
Вышеописанную методику легко можно адаптировать для применения в ферментаторах больших размеров с использованием способов, хорошо известных в данной области техники.
В процессе вегетативного роста, обычно в течение 24-36 часов после начала культивирования, что соответствует началу средней логарифмической фазы, бактерии штамма АВ78 отделяли с помощью центрифугирования от супернатанта культуры. Супернатант культуры, содержащий активный протеин, использовали для определения биологической активности.
Пример 3. Определение биологической активности в отношении насекомых
Активность
штамма B.cereus AB78 в отношении различных насекомых исследовали по описанной ниже методике.
В отношении блошки длинноусой западной, северной и южной (Diabrotica virgifera virgifera, D.longcornis barberi и D.undecempunctata howardi соответственно): из супернатанта культуры AB78, выращенной в течение 24-36 часов, готовили растворы, смешивали с искусственной питательной жидкой средой (Marrone и др. , (1985) J. of Economic Entomology, 78: 290-293) и давали возможность отвердеть. Отвердевшую среду нарезали и помещали в чашки. Новорожденных личинок помещали на питательную среду и выдерживали при 30oС. Учет гибели проводили через 6 дней.
Определение биологической активности клона E.coli: Клетки E.coli выращивали в течение ночи при 37oС в бульоне, содержащем 100 мкг/мл ампициллина. 10 мл культуры обрабатывали ультразвуком трижды по 20 с каждый раз. Добавляли 500 мкл обработанной ультразвуком культуры к жидкой питательной среде для блошки длинноусой западной.
В отношении колорадского жука (Leptinotarsa decemlineata): из супернатанта культуры AB78, выращенной в течение 24-36 часов, готовили растворы в Тритоне Х-100 (до получения конечной концентрации 0,1% ТХ-100). Кусочки картофельного листа размером 5 см2 погружали в эти растворы, сушили на воздухе и помещали на увлажненную фильтровальную бумагу в пластиковые чашки. Новорожденных личинок помещали на кусочки листьев и выдерживали при 30oС. Учет гибели проводили через 3-5 дней.
В отношении большого мучного хрущака (Tenebrio molitor): из супернатанта культуры АВ78, выращенной в течение 24-36 часов, готовили растворы, смешивали с жидкой искусственной питательной средой (фирма Bioserv F9240) и давали возможность отвердеть. Отвердевшую среду нарезали и помещали в пластиковые чашки. Новорожденных личинок помещали на питательную среду и выдерживалии при 30oС. Учет гибели проводили через 6-8 дней.
В отношении кукурузного мотылька, совки ипсилон, коробочного червя хлопчатника, табачного бражника и совки малой (Ostrinia nubilalis, Agrotis ipsilon, Heliothis virescens, Manduca sexta и Spodoptera exigua соответственно): из супернатанта культуры АБ78, выращенной в течение 24-36 часов, готовили растворы в ТХ-100 (до получения конечной концентрации 0,1% ТХ-100). С помощью пипетки наносили 100 мкл на поверхность площадью 18 см2 отвердевшей искусственной питательной среды (фирма Bioserv F9240) и давали возможность высохнуть на воздухе. Затем новорожденных гусениц помещали на поверхность питательной среды и выдерживали при 30oС. Учет гибели проводили через 3-6 дней.
В отношении комара обыкновенного (Culex pipiens): из супернатанта культуры АВ78, выращенной в течение 24-36 часов, готовили растворы. С помощью пипетки 100 мкл в 10 мл воды вносили в пластиковую чашку объемом 30 мл. Личинок третьего возраста помещали на воду и выдерживали при комнатной температуре. Учет гибели проводили через 24-48 часов. Спектр энтомологической активности штамма АВ78 представлен в таблице 14.
Подтверждено, что спектр инсектицидной активности впервые описанного штамма B.cereus AB78 существенно отличается от такового известных активных в отношении жесткокрылых δ-эндотоксинов из Bt. В частности AB78 проявил более избирательную активность в отношении жуков по сравнению с известными активными в отношении жесткокрылых штаммами Bt, прежде всего он показал специфическую активность в отношении Diabrotica spp. В частности он оказался наиболее активным в отношении D.virgifera virgifera и D.longicornis barberi, но не в отношении D.undecimpunctata howardi.
Определяли биологическую активность в течение вегетативного роста нескольких штаммов Bacillus в отношении блошки длинноусой западной (таблица 15). Результаты свидетельствуют о том, что уникальная активность AB78 в отношении блошки длинноусой западной не является общим явлением.
Специфическая активность AB78 в отношении блошки длинноусой западной представлена в таблице 16.
На основе этих данных было установлено, что значение LC50 составляет 6,2 мкл супернатанта культуры на мл питательной среды блошки длинноусой западной.
Также определяли биологическую активность дебриса, и было установлено, что он не обладает активностью в отношении БДЗ. Таким образом, наличие активности только в супернатанте свидетельствует о том, что VIP представляет собой экзотоксин.
Пример 4. Выделение и очистка из АВ78 протеинов, активных в отношении блошек длинноусых
Среду для культивирования, лишенную клеток и дебриса,
насыщали до 70%, добавляя твердый сульфат аммония (472 г/л). Растворение осуществляли при комнатной температуре с последующим охлаждением в ледяной бане и центрифугированием при 10000•g в
течение тридцати минут до получения в пробирке для центрифугирования осажденных протеинов. Супернатант удаляли и осадок в пробирке для центрифугирования растворяли в 1/10 от первоначального объема 20
мМ Трис-НСl-буфера с рН 7,5. Растворенный осадок в пробирке для центрифугирования обессоливали либо путем диализа в 20 мМ Трис-HCl-буфере с рН 7,5, либо пропуская через обессоливающую колонку.
Обессоленный продукт титровали до рН 3,5, используя 20 мМ натрийцитратный буфер, рН 2,5. После 30-минутной инкубации при комнатной температуре раствор центрифугировали при 3000•g в течение 10 минут. На этой стадии супернатант содержал наибольшее количество активного протеина.
После нейтрализации до рН 7,0 супернатант наносили на колонку для анионообменной хроматографии типа Mono-Q, уравновешенную с помощью 20 мМ Трис, рН 7,5, при скорости потока 300 мл/мин. Хроматографирование проводили с использованием ступенчатого и линейного градиента 400 мМ NaCl в 20 мМ Трис, рН 7,5.
Определение биологической активности фракций колонки и анализ с помощью ДСН-ПААГ применяли для выявления активных фракций. Анализ с помощью ДСН-ПААГ выявил биологически активный протеин, имеющий компоненты с молекулярной массой, находящейся в диапазоне приблизительно 80 кДа и 50 кДа.
Пример 5. Анализ последовательности протеина,
активного в отношении блошек длинноусых
Компонент с молекулярной массой 80 кДа, выделенный с помощью ДСН-ПААГ, переносили на PVDF-мембрану и подвергали аминоконцевому секвенированию с
использованием повторных циклов Эдмана в импульсно-жидкостном секвенаторе типа ABI 470. Перенос осуществляли в 10 мМ CAPS-буфере с метанолом (10%), рН 11,0, следующим образом.
Проводили инкубацию геля после электрофореза в транспортном буфере в течение пяти минут. Слегка смачивали 100%-ным МеОН первичную PVDF-мембрану для блоттинга типа ProBlott, затем уравновешивали в транспортном буфере. Создавали сэндвич между вспененной губкой и квадратиками из фильтровальной бумаги с конфигурацией катод-гель-мембрана-анод.
Перенос осуществляли в течение 1 часа при постоянном напряжении 70 вольт.
После переноса мембрану промывали водой и окрашивали в течение двух минут 0,25%-ным кумассином синим (Coomassie Blue R-250) в 50%-ном МеОН.
Обесцвечивание осуществляли путем нескольких промывок смесью 50% МеОН, 40% воды и 10% уксусной кислоты.
После обесцвечивания мембрану сушили на воздухе перед вырезанием полос для анализа последовательности. Для получения максимальной эффективности и выхода использовали блотт-картридж и соответствующие циклы. Для идентификации и количественной оценки производных РТН-аминокислот в каждом последовательном цикле анализ данных проводили с использованием модели 610 программного обеспечения для анализа последовательности.
Было установлено, что N-концевая последовательность представляет собой NH2-Lys-Arg-Glu-Ile-Asp-Glu-Asp-Thr-Asp-Thr-Asx-Gly-Asp-Ser-Ile-Pro-(SEQ ID NO: 8), где Asx обозначает Asp или Asn. Полная аминокислотная последовательность для компонента с молекулярной массой 80 кДа представлена в последовательности SEQ ID NO: 7. Последовательность ДНК, которая кодирует SEQ ID NO: 7, представлена в последовательности SEQ ID NO: 8.
Пример 6. Строение ДНК-зонда
Получали олигонуклеотидный зонд для области гена, кодирующей аминокислоты 3-9 N-концевой последовательности (пример 5). Зонд
синтезировали на основе наиболее часто встречающегося кодона гена 6-эндотоксина Bacillus thuringensis (Bt). Нуклеотидную последовательность 5'-GAA ATT GAT CAA GAT ACN GAT-3' (SEQ ID NO: 9)
использовали в качестве зонда в Саузерн-гибридизациях. Олигонуклеотид синтезировали с использованием стандартных способов и оборудования.
Пример 7. Определение изоэлектрической точки
протеина, активного в отношении блошек длинноусых
Очищенный протеин после пятой стадий процесса очистки анализировали на изоэлектрическом фокусирующем геле с рI 3-9, используя систему для
электрофореза типа Phastgel (фирма Pharmacia). Процесс разделения, равно как и процесс окрашивания серебром, осуществляли с использованием стандартных для этого устройства методов. Значение рI
составило приблизительно 4,9.
Пример 8. Данные о АВ78, полученные на основе ПЦР
Для подтверждения того, что штамм B.cereus AB78 не содержал любых генов инсектицидного
кристаллического протеина B.thuringiensis или B.sphaericus, применяли ПЦР-анализ (см., например, заявку на патент США 08/008006; и Carozzi и др., (1991) Appl. Environ. Microbiol. 57 (11): 3057-3061,
включенные в настоящее описание в
качестве ссылок) (таблица 17).
Пример 9. Космидное клонирование обшей ДНК из штамма B.cereus AB78 Ген VIP1A(a) клонировали из общей ДНК, полученной из штамма AB78, следующим образом.
Выделение ДНК штамма AB78 осуществляют следующим образом.
1. Выращивают бактерии в 10 мл L-бульона в течение ночи (применяют стерильную центрифужную пробирку объемом 50 мл).
2. Добавляют 25 мл свежего L-бульона и ампициллин (30 мкг/мл).
3. Выращивают клетки при встряхивании в течение 2-6 часов при 30oС.
4. Вращают клетки в полипропиленовой пробирке с оранжевой крышкой объемом 50 мл в клинической центрифуге с верхним расположением пробирок типа IEC при 3/4 скорости.
5. Ресуспендуют клеточный дебрис в 10 мл TES (TES = 50 мМ Трис, рН 8,0, 100 мМ ЭДТК, 15 мМ NaCl).
6. Добавляют 30 мг лизоцима и инкубируют в течение 2 ч при 37oС.
7. Добаляют 200 мкл 20%-ного ДСП и 400 мкл маточного раствора протеиназы К (20 мг/мл). Инкубируют при 37oС.
8. Добавляют 200 мкл свежей протеиназы К. Инкубируют 1 час при 55oС. Добавляют 5 мл TES до получения 15 мл конечного объема.
9. Дважды экстрагируют фенолом (10 мл фенола, центрифугируют при комнатной температуре при 3/4 скорости в клинической центрифуге с верхним расположением пробирок типа IEC). Переносят супернатант (верхнюю фазу) в чистую пробирку, используя пипетку с широким отверстием.
10. Экстрагируют один раз смесью 1: 1 (объем/объем) фенол: хлороформ/изоамиловый спирт (соотношение 24:1).
11. Осаждают ДНК равным объемом холодного изопропанола; центрифугируют до получения в пробирке для центрифугирования осадка ДНК.
12. Ресуспендируют полученный в пробирке для центрифугирования осадок в 5 мл ТЕ.
13. Осаждают ДНК с помощью 0,5 мл 3М NaOAc, pH 5,2, и 11 мл 95%-ного этанола. Выдерживают в течение 2 часов при -20oС.
14. Извлекают ДНК из пробирки с помощью пластиковой петельки, переносят в микроцентрифужную пробирку, вращают, отбирают пипеткой избыток этанола, сушат в вакууме.
15. Ресуспендируют в 0,5 мл ТЕ. Инкубируют 90 минут при 65oС для облегчения возвращения ДНК в раствор.
16. Определяют концентрацию, используя стандартные методы.
Космидное клонирование АБ78
Все процедуры, если не указано
иное, выполняли в соответствии с Stratagene Protocol, Supercos 1 Instruction Manual, Cat. 251301. Обычно используют следующие стадии:
А. Частичное разложение ДНК АВ78 рестриктазой SAU ЗА.
Б. Получение ДНК-вектора.
В. Лигирование и упаковка ДНК.
Г. Формирование космидной библиотеки.
1. Начинают разведение культуры клеток НВ101 путем посева 50 мл выдержанной в течение ночи культуры в 5 мл ТВ с 0,2%-ной мальтозой. Икубируют в течение 3,5 ч при 37oС.
2. Центрифугируют клетки и ресуспендируют в 0,5 мл 10 мМ MgSO4.
3. Объединяют вместе:
100 л клеток
100 л растворенной упаковочной смеси
100 л 10 мМ MgSO4
30 л ТВ
4. Адсорбируют при комнатной температуре в течение 30 минут без встряхивания.
5. Добавляют 1 мл ТВ и осторожно смешивают. Инкубируют в течение 30 минут при 37oС.
6. Высевают 200 л на L-amp-чашки. Инкубируют в течение ночи при 37oС.
Случайным образом отбирали по крайней мере 400 космидных клонов и подвергали скринингу на активность в отношении блошки длинноусой западной, как описано в примере 3. ДНК из 5 активных клонов и 5 неактивных клонов использовали в Саузерн-гибридизациях. Результаты показали, что гибридизация с использованием вышеописанного олигонуклеотидного зонда коррелировала с активностью в отношении блошки длинноусой западной (таблица 18).
Космидные клоны Р3-12 и Р5-4 были помещены в Agricultural Research Service Patent Culture Collection (NRRL) и получили регистрационные номера NRRL В-21061 и NRRL В-21059 соответственно.
Пример 10. Выявление области длиной 6
т.п.н. активной в отношении блошки длинноусой западной
ДНК из космидного клона Р3-12 частично расщепляли с помощью рестриктазы Sau3A и лигировали с вектором pUC19 E.coli, а затем
трансформировали в E. coli. ДНК-зонд, специфичный в отношении протеина VIP1A(a) с молекулярной массой 80 кДа, синтезировали с помощью ПЦР-амплификации части ДНК клона Р3-12. Олигонуклеотиды МК113 и
МК117, которые гибридизуются с частями VIP-lA(a), синтезировали с использованием неполной аминокислотной последовательности протеина с молекулярной массой 80 кДа. Субклоны плазмиды идентифицировали с
помощью гибридизации колоний с зондом, полученным в результате ПЦР, и исследовали биологическую активность в отношении блошки длинноусой западной. Один из этих клонов, а именно PL2, гибридизовался с
фрагментом, образованным в результате ПЦР, и обладал активностью в отношении блошки длинноусой западной в исследовании, проведенном по описанной выше методике.
Фрагмент длиной 6 т.п.н., полученный из PL2 с помощью рестриктазы ClaI, клонировали в сайте SmaI бифункционального вектора рНТ 3101 E.coli-Bacillus (Lereclus D. и др., 1989, FEMS Microbiology Letters, 60: 211-218), получая pCIB6201. Эта конструкция в любой ориентации придает активность в отношении блошки длинноусой западной как штаммам Bacillus, так и штаммам E.coli. pCIB6022 содержит тот же самый ClaI-фрагмент длиной 6 т.п.н. в pBluescript SK(+) (фирма Stratagene), образует протеин, эквивалентный VIP-1А(а) (как подтверждено методом Вестерн-блоттинга), а также обладает активностью в отношении блошки длинноусой западной.
Нуклеотидную последовательность рС1Р6022 определеляли с помощью метода дидезокси-терминации Sanger и др., Ргос. Natl. Acad. ScL, USA, 74: 5463-5467 (1977), с использованием наборов PRISM Ready Reaction Dye Deoxy Terminator Cycle Sequencing Kits и набора PRISM Sequenase® Terminator Double-Stranded DNA Sequencing Kit и анализировали на автоматическом секвенаторе типа АВ1 373. Последовательность представлена в SEQ ID NO: 1. Фрагмент длиной 6 т.п. н. кодирует как VIP1A(a), так и VIP2A(a), что установлено с помощью открытых рамок считывания, описанных в SEQ ID NO: 1. Последовательность, кодирующая VIP2A(a), кроме того, представлена в SEQ ID NO: 4. Взаимосвязь между VIP1A(a) и VIP2A(a) внутри фрагмента длиной 6 т.п.н., созданного в рСIВ6022, представлена в таблице 19. рСIВ6022 депонирован в Agricultural Research Service, Patent Culture Collection (NRRL), Northern Regional Research Center, 1815, North University Street, Peoria, Illinois, 61604, USA, под регистрационным номером NRRL B-21222.
Пример 11. Определение функций VIP1A(a)-области ДНК
Для подтверждения того, что открытая рамка
считывания (ОРС) гена VIP1A(a) необходима для проявления инсектицидной активности, в гене создавали трансляционнную мутацию "сдвига рамки". Рестриктаза Bg1II распознает уникальный сайт, локализованный
в кодирующей области VIP1A(a) длиной 857 пар оснований. рСIВ6201 расщепляли с помощью BglII и одноцепочечные концы заполняли с помощью ДНК-полимеразы (фрагмент Кленова) и дНТФ. Плазмиду повторно
дотировали и трансформировали в Е.соli. Образовавшаяся плазмида рСIВ6203 содержит четыре нуклеотидные инсерпии в области, кодирующей VIP1A(a). pCIB6203 не обладает инсектицидной активностью в
отношении БДЗ, что подтверждает то, что VIP1A(a) является основным компонентом, обусловливающим активность в отношении блошки длинноусой западной.
Для дальнейшего определения области, необходимой для кодирования VIP1A(a), конструировали области субклонов VIP1A(a) и VIP2A(a) (вспомогательный протеин) и определяли их способность к комплементации мутации в pCIB6203. pCIB6203 содержит фрагмент XbaI-EcoRV длиной 3,7 т.п.н. в pBluescript SK(+) (фирма Stratagene). Вестерн-блоттинг показал, что рСIВ6023 продуцирует протеин VIP1A(a) такого же размера и в таком же количестве, что и клоны PL2 и рСIВ6022. рСIВ6023 содержал полный ген, кодирующий протеин 80 кДа. рСIВ6023 депонировали в Agricultural Research Service, Patent Culture Collection, (NRRL), Nothern Regional Research Center, 1815 North University Street, Peoria, Illinois 61604, USA, под регистрационным номером NRRL B-21223N. pCIB6206 содержал XbaI-ClaI-фрагмент длиной 4,3 т.п.н. из рСIВ6022 в pBluescript SK(+) (фирма Stratagene). pCIB6206 депонировали в Agricultural Research Service, Patent Culture Collection, (NRRL), Northern Regional Research Center, 1815 North University Street, Peoria, Illinois 61604, USA, под регистрационным номером NRRL B-21321.
pCIB6023, pCIB6206 и рСIВ6203 не проявляли выраженной активности в отношении блошки длинноусой западной, когда их исследовали по отдельности. Однако смесь клеток, содержащих pCIB6203 (VIP1A(a) -мутированный плюс VIP2A(a)), и клеток, содержащих pCIB6023 (только VIP1A(a)), проявляла высокую активность в отношении блошки длинноусой западной. Аналогично этому смесь клеток, содержащих pCIB6206, и клеток, содержащих pCIB6203, проявляла высокую активность в отношении блошки длинноусой западной.
Для дальнейшего определения пределов активности VIP2A(a) конструировали рСIВ6024, которая полностью содержит VIP2A(a), но лишена большей части кодирующей области VIP1A(a). pCIB6024 конструировали путем гель-фильтрации рестрикционного ClaI- SeaI-фрагмента длиной 2,2 т.п.н. из рСIВ6022, заполняя одноцепочечные концы с помощью ДНК-полимеразы (фрагмент Кленова) и дНТФ, и лигирования этого фрагмента с вектором pBluescript SK(+) (фирма Stratagene), расщепленного ферментом EcoRV. Клетки, содержащие pCIB6024, не проявляли активности в отношении блошки длинноусой западной. Однако смесь клеток, содержащих pCIB6024, и клеток, содержащих pCIB6023, проявляла высокую активность в отношении блошки длинноусой западной (см. таблицу 19).
Таким образом, pCIB6023 и pCIB6206 должны продуцировать функционально активный продукт гена VIP1A(a), в то время как pCIB6203 и pCIB6024 должны продуцировать функционирующий продукт гена VIP2A(a). Эти результаты позволяют предположить, что для получения максимальной активности в отношении блошки длинноусой западной необходим(ы) продукт(ы) гена из области VIP2A(a) в сочетании с VIP1A(a) (см. таблицу 19).
Прямоугольные области обозначают протяженность VIP1A(a) и VIP2A(a). Светлый прямоугольник обозначает часть VIP1, кодирующую протеин 80 кДа, обнаруженный у Bacillus. Темный прямоугольник обозначает N-концевой пропептид VIP1A(a), предсказанный на основе анализа последовательности ДНК. Помеченный пунктиром прямоугольник обозначает кодирующую область VIP2A(a). Большая буква "X" обозначает местоположение интродуцированной в VIP1A(a) мутации "сдвига рамки считывания". Стрелки показывают конструкции, транскрибируемые промотором бета-галактозидазы.
Пример 12. Образование антител против
АВ78
Вызывали образование антител у двух крыс линии Lewis, давая обеим возможность двигаться, с последующим использованием этих клеток для образования линии клеток гибридомы, а также для
образования достаточного количества сыворотки для ограниченного скрининга библиотеки геномной ДНК. Другим фактором было очень ограниченное количество доступного антигена, а также тот факт, что он мог
быть получен только путем очистки с помощью электрофореза в ПААГ и последующего электроблоттинга на нитроцеллюлозе.
Вследствие ограниченной доступности антигена на нитроцеллюлозе последнюю эмульгировали в ДМСО и инъецировали в подушечки на лапках задних ног животных с той целью, чтобы вызвать продуцирование В-клеток в вышележащих подколенных лимфатических узлах. Из первой порции крови получали сыворотку, обладающую сильной реакцией, что было подтверждено с помощью Вестерн-блоттинга. Последующие несколько инъекций и кровопусканий позволили получить достаточное количество сыворотки, чтобы осуществить весь требуемый скрининг.
Затем, используя одну из крыс, создавали гибридомы. Подколенные лимфатические узлы вырезали, измельчали и полученные клетки сливали с мышиной миеломой P3•63Ag8.653. Последующий скриниг клеток осуществляли по описанной ниже методике. Сначала отбирали четыре лунки, которые давали наиболее сильную реакцию на эмульгированный антиген, чтобы ограничить получение клонов с ослабленной реакцией на антиген. Дополнительные 10 лунок выбирали для увеличения количества и криоконсервации.
Методика
эмульгирования АВ78 на нитропеллюлозе в ДМСО для скрининга с помощью твердофазного иммуноферментного анализа (ELISA)
После электроблоттинга на нитроцеллюлозу образцов АВ78, прошедших
электрофорез в ПААГ, используют способный к реверсии штамм Ponceau S для визуализации всех перенесенных протеинов. Определяли полосу, соответствующую ранее идентифицированному и прошедшему N-концевое
секвенирование токсину АВ78, и вырезали из нитроцеллюлозы. Каждая полоса имеет размер примерно 1•5 мм, что позволяет снизить до минимума количество эмульгируемой нитроцеллюлозы. Отдельную
полосу помещают в микроцентрифужную пробирку с 250 мкл ДМСО и измельчают с помощью пластикового пестика (фирма Konte, Vineland, NJ). С целью способствовать эмульгированию смесь с ДМСО выдерживают в
течение 2-3 минут при 37-45oС. После нагревания может потребоваться дополнительное измельчение; однако вся нитроцеллюлоза должна быть эмульгирована. Когда образец АВ78 проэмульгирован, его
помещают на лед. В препарате, предназначенном для титрационного микропланшета, покрытого эмульгированным антигеном, образец должен быть растворен в забуференном боратом физиологическом растворе (ЗБФР)
в следующих соотношениях: 1: 5, 1:10, 1:15, 1:20, 1:30, 1:50, 1:100 и 0. Адсорбируемый антиген должен быть приготовлен непосредственно перед использованием.
Протокол ELISA:
1. Наносят покрытие из АВ78/ДМСО в ЗБФР. Инкубируют в течение ночи при 4oС.
2. Трижды промывают планшет однократным буфером для промывки ELISA.
3. Блокируют (1% БСА и 0,05%-ный Твин 20 в ЗФР (забуференный фосфатом физиологический раствор)) в течение 30 минут при комнатной температуре.
4. Трижды промывают планшет однократным буфером для промывки ELISA.
5. Добавляют крысиную сыворотку. Инкубируют в течение 1,5 ч при 37oС.
6. Трижды промывают планшет однократным буфером для промывки ELISA.
7. Добавляют козлиное антикрысиное антитело в концентрации 2 мкг/мл в растворителе ELISA. Инкубируют 1 час при 37oС.
8. Трижды промывают планшет однократным буфером для промывки ELISA.
9. Добавляют кроличью антикозлиную щелочную фосфатазу в концентрации 2 мкг/мл в растворителе ELISA. Инкубируют 1 час при 37o С.
10. Трижды промывают планшет однократным буфером для промывки ELISA.
11. Добавляют субстрат. Инкубируют 30 минут при комнатной температур
12. Прекращают
процесс с помощью 3Н NaOH через 30 минут.
Получение антисыворотки против VIР2А(а)
Частично очищенный супернатант культуры штамма АВ78 разделяли с помощью непродолжительного
электрофореза в ДСН-ПААГ (фирма Novex), следуя инструкциям производителя. Разделенные протеины подвергали электрофорезу на нитроцеллюлозе (S& S 21640), как описано у Towbin и др. (1979).
Нитроцеллюлозу окрашивали с помощью Ponceau S и выявляли полосу соответствующую VIP2A(a). Полосу VIP2A(a) вырезали и эмульгировали в ДМСО непосредственно перед инъекцией. Первоначально кролика
иммунизировали эмульгированным VIP2A(a), смешанным в соотношении приблизительно 1:1 с полным адъювантом Фрейнда, путем внутримышечной инъекции в четыре разных места. Последующие иммунизации проводили
с четырехнедельными интервалами, и они были идентичны первой, за исключением того, что использовали неполный адъювант Фрейнда. Первую сыворотку собирали после иммунизации, вызывающей ответную реакцию
на протеин VIP2A(a). Анализ на основе Вестрен-блоттинга супернатанта культурь АВ78 с использованием этой антисыворотки показал наличие протеина VIP2A(a), имеющего в основном полную длину.
Пример 13. Усиление инсектицидной активности неактивных штаммов Bt с помощью клонов VIP AB78
Добавление рСIВ6203 вместе с супернатантом 24-часовой культуры (начало средней
логарифмической фазы) из штамма Bt GC91 вызывает 100%-ную гибель Diabrotica virgifera virgifera. Ни рСIВ6203, ни GC91 по отдельности не проявляют активности в отношении Diabrotica virgifera virgifera.
Полученные результаты представлены ниже.
Исследуемый материал - Процент гибели Diabrotica
рСIВ6203 - 0
GC91 - 16
рСIВ6203 + GC91 - 100
Контроль
- 0
Пример 14. Выделение и биологическая активность штамма B.cereus AB81 Второй штамм B.cereus, обозначенный как AB81, выделяли из образцов элеваторной зерновой пыли с помощью стандартных
методик. Субкультуру AB81 выращивали и готовили к определению биологической активности, как описано в примере 2. Биологическую активность оценивали по описанной в примере 3 методике. Были получены
следующие результаты.
Виды исследуемых насекомых - Процент гибели
Ostrinia nubilalis - 0
Agrotis ipsilon - 0
Diabrotica virgifera virgifera - 55
Пример 15. Выделение и биологическая активность штамма B.thuringiensis АВ6
Штамм B. thuringiensis, обозначенный как АВ6, выделяли из образцов элеваторной зерновой пыли стандартными методами,
известными в данной области техники. Субкультуру АВ6 выращивали и готовили к определению биологической активности, как описано в примере 2. Половину образца автоклавировали в течение 15 минут с той
целью, чтобы установить присутствие β-экзотоксина.
Биологическую активность оценивали по описанной в примере 3 методике. Были получены следующие результаты.
Виды исследуемых насекомых - Процент смертности
Ostrinia nubilalis - 0
Agrotis ipsilon - 100
Agrotis ipsilon (автоклавированный образец) - 0
Diabrotica virgifera
virgifera - 0
Снижение инсектицидной активности супернатанта культуры при автоклавировании до незначительных уровней свидетельствует о том, что активный ингредиент не является β
-экзотоксином.
Штамм АВ6 был депонирован в Agricultural Research Service, Patent Culture Collection (NRRL), Nothern Regional Research Center, 1815 North University Street, Peoria, Illinois 61604, USA, под регистрационным номером NRRL B-21060.
Пример 16. Выделение и биологическая характеристика штамма B.thuringiensis AB88
Штамм Bt, обозначенный как AB88,
выделяли из образцов элеваторной зерновой пыли с помощью стандартных методов. Субкультуру AB88 выращивали и готовили для исследования биологической активности, как описано в примере 2. Половину
образца автоклавировали в течение 15 минут с той целью, чтобы установить присутствие β-экзотоксина. Биологическую активность в отношении различных видов насекомых оценивали по описанной в
примере 3 методике. Были получены результаты, представленные в табл. IV.
Снижение инсектицидной активности супернатанта культуры при автоклавировании до незначительных уровней свидетельствет о том, что активный ингредиент не является β-экзотоксином.
Кристаллы дельта-эндотоксина очищали из штамма АВ88 при помощи стандартных методов. Никакой активности чистых кристаллов не обнаружили при изучении биологической активности в отношении Agrotis ipsilon.
Пример 17. Очистка VIP из штамма АВ88
Бактериальную жидкую культуру
выращивали в течение ночи (12 ч) при 30oС в ТВ-среде. Клетки центрифугировали при 5000•g в течение 20 минут и собирали супернатант. Протеины, присутствующие в супернатанте, осаждали
сульфатом аммония (70% насыщения), центрифугировали (при 5000•g в течение 15 минут) и собирали осадок в пробирке после центрифугирования. Осадок в пробирке после центрифугирования
ресуспендировали в начальном объеме 20 мМ Трис, рН 7,5, и подвергали диализу в течение ночи с использованием этого же самого буфера при 4oС. Диализат из АВ88 оказался более мутным, чем
соответствующий материал из АВ78. Диализат титровали до рН 4,5, используя 20 мМ натрий -цитратный буфер (рН 2,5) и после 30-минутной выдержки при комнатной температуре раствор центрифугировали при
3000•g в течение 10 мин. Осадок протеина в пробирке после центрифугирования повторно растворяли в 20 мМ бис-трис-пропане, рН 9,0.
Протеины штамма АВ88 после осветления разделяли с помощью нескольких различных методов, включающих изоэлектрическое фокусирование (фирма Rotofor, BioRad, Hercules, CA), осаждение при рН 4,5, ионообменную хроматографию, гель-фильтрацию и ультрафильтрацию.
Протеины разделяли на анионообменной колонке типа Poros HQ/N (фирма PerSeptive, Biosystems, Cambridge, Ma) с использованием линейного градиента от 0 до 500 мМ NaCl в 20 мМ бис-трис-пропане, рН 9,0, со скоростью потока 4 мл/мин. Инсектицидный протеин элюировали при 250 мМ NaCl.
Протеин, активный в отношении кукурузного мотылька (КМ), полученный
путем осаждения диализата при рН 4,5, сохранялся в осадке в пробирке после центрифугирования. После осуществления препаративного изоэлектрического фокусирования (ИЭФ) диализата с использованием
амфотерных электролитов с рН 3-10 инсектицидная активность в отношении КМ была обнаружена во всех фракциях с рН 7 или выше. Анализ этих фракций с помощью электрофореза в ДСН-ПААГ выявил полосы
протеина с молекулярной массой ~60 кДа и ~80 кДа. Полосы с 60 кДа и 80 кДа разделяли с помощью анионообменной ЖХВР на колонке типа Poros-Q (фирма PerSeptive Biosystems, Cambridge, MA). N-концевую
последовательность получали из двух фракций, содержащих протеины со слегка различной молекулярной массой, но приблизительно равной 60 кДа. Полученные последовательности оказались сходными между собой
и с некоторыми δ-эндотоксинами:
анионобменная фракция 23 (меньшая): xEPFVSAxxxQxx (SEQ ID NO: 10)
анионобменная фракция 28 (большая): xEYENVEPFVSAx (SEQ ID NO: 11)
Когда активный в отношении KM осадок в пробирке после центрифугирования с рН 4,5 далее разделяли с помощью анионнообменной хроматографии на колонке типа Poros-Q, активность была обнаружена только во
фракциях с основной полосой ~60 кДа.
Активный в отношении совки-ипсилон протеин также сохранился в осадке в пробирке после центрифугирования, когда рН диализата АБ88 снижали до 4,5. При препаративном ИЭФ с использованием амфотерных электролитов с рН 3-10 активность не была обнаружена в КМ-активных фракциях ИЭФ; вместо этого она оказалась наиболее высокой во фракции с рН 4,5-5,0. Ее основные компоненты имеют молекулярные массы ~35 и ~80 кДа.
Осадок в пробирке после центрифугирования с рН 4,5 отделяли с помощью анионобменной ЖХВР с целью получения фракций, содержащих только продукт с молекулярной массой 35 кДа, и фракций, содержащих полосы как 35 кДа, так и 80 кДа.
Пример 18. Характеристика VIP штамма АВ88
Фракции, содержащие
вегетативные протеины, активные в отношении различных чешуекрылых, готовили по описанной в примере 17 методике. Фракции с инсектицидной активностью разделяли с помощью электрофореза в 8-16%-ных
ДСН-полиакрилаидных гелях и переносили на PVDF-мембраны [LeGendre и др., (1989) A Practical Guide to Protein and Peptide Purification for Microsequencing, ред. Matsudaria P.T. (Academic Press Inc.,
New York)]. Биологический анализ фракций показал, что различные VIP ответственны за активность в отношении разных видов чешуекрылых.
Активность в отношении Agrotis ipsilon определяется протеином 80 кДа и/или 35 кДа, взятых либо по отдельности, либо в комбинации. Эти протеины не похожи на любые δ-эндотоксины из Bt, что было установлено по отсутствию последовательности, гомологичной известным последовательностям δ-эндотоксина Bt. В основном (по крайней мере на 75%) в супернатантах культур АВ88 присутствует инсектицидный протеин VIP3A(a) из штамма АВ88.
Кроме того, эти протеины не обнаружены в кристаллах δ-эндотоксина штамма АВ88. N-концевые последовательности основных протеинов δ-эндотоксина сравнивали с N-концевыми последовательности 80 кДа и 35 кДа VIP и не обнаружили гомологии последовательностей. N-концевая последовательность инсектицидного протеина VIP3A(a) несет определенное количество положительно заряженных остатков (от Asn2 до Asn7), за которыми расположена гидрофобная внутренняя область (от Thr8 до Ilе34). В отличие от большинства известных секретируемых протеинов инсектицидный протеин VIP3A(a) из штамма АВ88 не подвергается N-концевому процессингу во время экспорта. В табл. V приведены обобщенные результаты.
Активность в отношении Ostrinia nubilalis определяется VIP с молекулярной массой 60 кДа, а активность в отношении Spodoptera frugiperda определяется VIP неизвестного размера.
Штамм Bacillus thuringiensis AB88 был депонирован в Agricultural Research Service, Patent Culture Collection (NRRL), Northern Regional Research Center, 1815 North University Street, Peoria, Illinois 61604, USA, под регистрационным номером NRRL B-21225.
Пример 18А. Выделение и биологическая активность штамма Bacillus thuringiensis AB424
Штамм В.thuringiensis, обозначенный как AB424, выделяли из образца покрытой мхом
сосновой шишки стандартными методами, известными в данной области техники. Субкультуру AB424 выращивали и готовили к определению биологической активности, как описано в примере 2. Биологическую
активность оценивали по описанной в примере 3 методике. Были получены следующие результаты.
Исследованные виды насекомых - Процент гибели
Ostrinia nubilalis - 100
Agrotis ipsilon - 100
Diabrotica virgifera virgifera - 0
Штамм AB424 был депонирован в Agricultural Research Service, Patent Culture Collection (NRRL), Northern Regional Research
Center, 1815 North University Street, Peoria, Illinois 61604, USA, под регистрационным номером NRRL B-21439.
Пример 18Б. Клонирование генов VIР3А(а) и VIP3A(b). которые кодируют
протеины, активные в отношении совки ипсилон
Общую ДНК из изолятов АВ88 и AB424 выделяли [Ausubel и др., (1988) Current Protocols in Molecular Biology (John Wiley & Sons, NY)] и
расщепляли рестиктазами XbaI [библиотека ДНК разделенных на фракции по размерам от 4,0 до 5,0 т. п. н. XbаI-фрагментов штамма В. thuringiensis AB88] и EcoRI [библиотека ДНК разделенных на фракции по
размерам от 4,5 до 6,0 т.п.н. EcoRI-фрагментов штамма В. thuringiensis AB424] соответственно и лигировали с предварительно линеаризированным этими же ферментами и дефосфорилированным вектором
pBluescript, а затем трансформировали в штамм Е.coli DH5α. Рекомбинантные клоны продвергали блоттингу на нитроцеллюлозных фильтрах, которые затем зондировали меченным Р32
олигонуклеотидом, состоящим из 33 оснований, который соответствует 11-ти N-концевым аминокислотам протеина 80 кДа, активного в отношении Agrotis ipsilon (совки ипсилон). Гибридизацию осуществляли при
42oС в 2•SSC/0,l% ДСН (1•SSC=0,15М NaCl/0,15M цитрат натрия, рН 7,4) в течение 5 минут и дважды при 50oС в 1•SSC/0,l% ДСН в течение 10 минут. Четыре из 400
рекомбинатных клонов оказались позитивными. Изучение биологической активности рекомбинантов, позитивных в отношении насекомых, показало, что их токсичность в отношении гусениц совки ипсилон сравнима с
таковой супернатантов АВ88 или АВ424.
Плазмида рСIВ7104 содержит XbaI-фрагмент длиной 4,5 т.п.н. ДНК штамма АВ88. С целью определить кодирующую область инсектицидного протеина конструировали субклоны.
Конструировали плазмиду рСIВ7105 для Е.coli путем клонирования XbaI-AccI-фрагмента длиной 3,5 т.п.н. плазмиды рСIВ7104 в pBluescript.
Плазмида рСIВ7106 содержала EcoRI-фрагмент длиной 5,0 т.п.н. ДНК штамма АВ424. Этот фрагмент затем расщепляли рестриктазой HincII с той целью, чтобы встроить EcoRI-HincII-вставку длиной 2,8 т.п.н. (рСIВ7107), которая также кодировала функционально активный инсектицидный протеин.
Нуклеотидную последовательность рСIВ7104, т. е. позитивного рекомбинантного клона из АВ88, и рСIВ7107, т.е. позитивного рекомбинантного клона из АВ424, определяли с помощью метода дидезокси-терминации Sanger и др., Ргос. Natl. Acad. Sci., USA, 74: 5463-5467 (1977) с использованием наборов PRISM Ready Reaction Dye Deoxy Terminator Cycle Sequencing Kits и набора PRISM Sequenase® Terminator Double-Stranded DNA Sequencing Kit, а затем анализировали на автоматическом секвенаторе типа АВ1 373.
Клон рСIВ7104 содержит ген VIP3A(a), кодирующая область которого представлена в SEQ ID NO: 28, а последовательность кодируемого протеина представлена в SEQ ID NO: 29. Синтетическая версия кодирующей области, сконструированная таким образом, чтобы она обладала высокой экспрессией в кукурузе, представлена в SEQ ID NO: 30. На основе аминокислотной последовательности, приведенной в SEQ ID NO: 29, может быть сконструировано любое количество синтетических генов.
Клон рСIВ7107 содержит ген VIP3A(b), кодирующая область которого представлена в SEQ ID NO: 31, а последовательность кодируемого протеина представлена в SEQ ID NO: 32. pCIB7104 и рСIВ7107 были депонированы в Agricultural Research Service под регистрационными номерами NRRL В-21422 и NRRL В-21423 соответственно.
Ген VIP3A(a) содержит открытую рамку считывания (ОРС), которая проходит от нуклеотида 732 до 3105. Эта ОРС кодирует пептид длиной в 791 аминокислоту, соответствующий молекулярной массе 88500 Да. Последовательность Шайна-Дальгарно (SD) (сайт связывания рибосом) локализована за 6 оснований до первого метионина, и эта последовательность свидетельствует о сильной SD у Bacillus.
Ген VIP3A(b) на 98% идентичен гену VIP3A(a).
Когда блот общей ДНК, выделенной из клеток штамма В. thuringiensis АВ88, зондировали фрагментом длиной 33 основания, который охватывает N-концевую область инсектицидного протеина VIP3A, в переварах различных рестриктаз могли наблюдать отдельные полосы. Этот результат был подтвержден с использованием более крупных зондов, охватывающих кодирующую область гена. Поиск в базе данных GenBank показал отсутствие гомологии с известными протеинами.
Пример 18В. Экспрессия инсектидидных протеинов VIP3A
С использованием Вестрен-блоттинга анализировали зависимость экспрессии инсектицидного протеина VIP3A(a) от времени. Были взяты
образцы из культур В. thuringiensis AB88 в процессе их роста и споруляции. Инсектицидный протеин VIP3A (а) может быть обнаружен в супернатантах культур AB88 во время фазы логарифмического роста, а
именно через 15 ч после начала культивирования. Он достигал своего максимального уровня в начале стационарной фазы и сохранялся на высоких уровнях во время и после споруляции. Аналогичные результаты
получали при использовании супернатантов культур Bacillus cereus AB424. Уровни инсектицидного протеина VIP3A(a) отражали экспрессию гена VIP3A(a), как это было установлено с помощью Назерн-блоттинга.
Начало споруляции определяли с помощью непосредственных микроскопических исследований и путем анализа присутствия δ-эндотоксинов в дебрисе. Протеины типа Сrу-1 могли быть выявлены на поздней
стационарной фазе, во время и после споруляции.
Пример 18Г. Выявление новых VIP3 -подобных генов путем гибридизации
Для выявления Bacillus, содержащих гены, родственные
VIP3A(a) из изолята АВ88, коллекцию изолятов Bacillus подвергали скринингу путем гибридизации. Культуры 463 штаммов Bacillus выращивали в лунках микротитровальных планшетов до споруляции. Для переноса
культур на чашки диаметром 150 мм, содержащей L-агар, использовали приспособление для нанесения колоний с 96 наконечниками. Инокулированные чашки выдерживали при 30oС в течение 10 часов, а
затем при 4oС в течение ночи. Колонии блоттировали на найлоновые фильтры и зондировали HindIII-фрагментом длиной 1,2 т.п.н., имеющим происхождение из VIP3A(a). Гибридизацию осуществляли в
течение ночи при 62oС, используя условия гибридизации, предложенные Maniatis и др. в Molecular Cloning: A Laboratory Manual (1982). Фильтры промывали с помощью 2•SSC/0,l% ДСН при
62oС и экспонировали на рентгеновской пленке.
Из 463 штаммов Bacillus, подвергнутых скринингу, 60 содержали VIP3-подобные гены, которые могут быть выявлены при гибридизации. Дополнительное изучение характеристик некоторых из них (АВ6 и АВ426) показало, что их супернатанты содержали инсектицидный протеин, активный в отношении БДЗ, аналогичный протеину VIP3, активному в отношении совки ипсилон.
Пример 18Д.
Характеристика штамма В. thuringiensis M2194. содержащего критический VIP3-подобный ген
Путем гибридизации колоний по
описанной в примере 18В методике было установлено, что штамм В. thuringiensis, обозначенный как M2194, содержит VIР3-подобный(ые) ген(ы). VIР3-подобный ген штамма M2194 считают критическим, поскольку
его экспрессия не может быть обнаружена во время фаз бактериального роста ни с помощью метода иммунноблоттинга с использованием поликлональных антител против протеина VIP3A(a), выделенного из АВ88, ни
с помощью биологического анализа, как описано в примере 3.
Получали кроличью антисыворотку против очищенного инсектицидного протеина VIP3A(a). Протеин, связанный с нитроцеллюлозой (50 мкг), растворяли в ДМСО и эмульгировали с помощью полного адъюванта Фрейнда (фирма Difco). Двум кроликам каждый месяц делали подкожные инъекции в течение трех месяцев. У них брали кровь через 10 дней после второй и третьей инъекций и получали сыворотку из образца крови [Harlow и др. (1988) в Antibodies: A Laboratory Manual (Cold Spring Harbor Lab. Press, Plainview, NY)].
VIР3-подобный ген штамма М2194 клонировали в pKS, следуя протоколу, описанному в примере 9, создавая таким образом pCIB7108. E.coli, содержащая рСIВ7108, которая включает ген VIP3 из штамма М2194, обладает активностью в отношении совки ипсилон, что свидетельствует о том, что ген кодирует функционально активный протеин, обладающий инсектицидной активностью. Плазмида pCIB7108 была депонирована в Agricultural Research Service, Patent Culture Collection (NRRL) под регистрационным номером NRRL B-21438.
Пример 18Е. Инсектицидная активность протеинов VIP3A
Спектр
активности инсектицидных протеинов VIP3A оценивали качественно в биологических опытах, в которых рекомбинатный штамм E.coli, несущий гены VIP*А, включали в пищу личинок. В этих опытах клетки, несущие
гены VIP3A(a) и VIP3A(b), проявили инсектицидную активность в отношении Agrotis ipsilon, Spodoptera frugiperda, Spodoptera exigua, Heliothis virescens и Helicoverpa zea. В аналогичных
экспериментальных условиях бактериальные экстракты, содержащие протеины VIP3A, не проявили активности в отношении Ostrinia nubilalis. (см. табл. VI и VII).
Пример 19. Выделение и биологическая активность других Bacillus spp.
Были выделены другие виды Bacillus, которые продуцируют во время вегетативного роста протеины, обладающие инсектицидной активностью. Эти штаммы выделяли из образцов, взятых из окружающей среды, с помощью стандартных методов. Изоляты готовили для определения биологической активности и оценивали, как описано в примерах 2 и 3 соответственно. Изоляты, которые продуцировали инсектицидные протеины во время вегетативного роста, обладающие активностью в отношении Agrotis ipsilon в опытах по определению биологической активности, представлены в табл. VIII. Не обнаружено корреляции между наличием кристаллов δ-эндотоксина и производством вегетативного инсектипидного протеина.
Изоляты АВ289, АВ294 и АВ359 были депонированы в Agricultural Research Service, Patent Culture Collection (NRRL), Northern Regional Research Center, 1815 North University Street, Peoria II 61604, USA, под регистрационными номерами NRRL B-21227, NRRL B-21229 и NRRL В-21226 соответственно.
Изоляты Bacillus, продуцирующие во время вегетативного роста протеины, обладающие инсектицидной активностью в отношении Diabrotica virgifera vireifera. ппиведены в табл. IX.
Изоляты АВ59 и АВ256 были депонированы в Agricultural Research Service, Patent Culture Collection (NRRL), Northern Regional Research Center, 1815 North University Street, Peoria Illinois 61604, USA, под регистационными номерами NRRL B-21228 и NRRL В-21230 соответственно.
Пример 20. Выделение новых
VIР1/VIР2-подобных генов путем гибридизации
Для выявления штаммов, содержащих гены, родственные тем, которые были обнаружены в области VIP1A(a)/VIP2A(a) штамма АВ78, коллекцию штаммов
Bacillus подвергали скринингу путем гибридизации. Независимые культуры 463 штаммов Bacillus выращивали в лунках 96-луночных микротитровальных планшетов (всего использовали пять планшетов) до
споруляпии культуры. Из всех изученных штаммов 288 были классифицированы как Bacillus thuringiensis, a 175 были классифицированы как другие виды Bacillus на основе наличия или отсутствия кристаллов
δ-эндотоксина. Для каждого микротитровального планшета для переноса приблизительно 10 мкл культуры спор на две чашки диаметром 155 мм, содержащие L-агар, использовали приспособление для
нанесения колоний с 96 наконечниками. Инокулированные чашки выращивали при 30oС в течение 4-8 часов, а затем охлаждали до 4oС. Колонии переносили на найлоновые фильтры и
лизировали клетки с помощью стандартных методов, известных в данной области техники. Фильтраты гибридизировали с ДНК-зондом, полученным из фрагментов ДНК, содержащих последовательности ДНК как
VIP1A(a), так и VIP2A(a). Гибридизацию осуществляли в течение ночи при 62oС, используя условия гибридизации, предложенные Church и Gilbert (Church G.M. и W. Gilbert., PNAS, 81: 1991-1995
(1984)). Фильтры промывали с помощью 2•SSC, содержащего 0,1% ДСН, при 65oС и экспонировали на рентгеновской пленке.
Из 463 штаммов Bacillus, подвергнутых скринингу, выделили 55 штаммов, которые гибридизируются с VIP1A(a)/VIP2A(а)-зондом. Из 22 этих штаммов выделяли ДНК и анализировали методом Саузерн-блоттинга, используя в качестве ДНК-зондов VIP1A(a)/VIP2A(a). Эти штаммы группировали в 8 классов на основе картины их Саузерн-блоттинга. Каждый класс отличался по картине Саузерн-блоттинга от АВ78. Один класс имел картину, идентичную таковой для гомологов VIP1A(a)/VIP2A(a) из Bacillus thuringiensis var. tenebrionis (см. ниже). Активность каждого из 22 штаммов определяли в отношении блошки длинноусой западной (БДЗ). Было обнаружено, что три штамма АВ433, АВ434 и АВ435 проявляют активность в отношении БДЗ. Анализ методом Вестерн-блоттинга с использованием антисывортки против VIP2A(a) выявил, что штаммы АВ6, АВ433, АВ434, АВ435, АВ444 и АВ445 продуцируют протеин(ы), эквивалентные по размеру VIP2A(a).
Среди этих выявленных штаммов особо следует отметить штамм Bacillus thuringiensis АВ6 (NRRL В-21060), который продуцирует VIP, активный в отношении совки ипсилон (Agrotis ipsilon), как описано в примере 15. Анализ методом Вестерн-блоттинга с использованием поликлональной антисывортки против VIP2A(a) и поликлональной антисывортки против VIP1A(a) позволяет сделать предположение, что АВ6 продуцирует протеины, аналогичные VIP2A(a) и VIP1A(a). Таким образом, АВ6 может содержать VIP, аналогичные VIP1A(a) и VIP2A(a), но отличающиеся по спектру инсектицидной активности.
Пример 21. Клонирование гомолога VIP1A(a)/VIP2A(a) из Bacillus thuringiensis var. tenebrionis
Несколько ранее
охарактеризованных штаммов Bacillus исследовали методом Саузерн-блоттинга на наличие ДНК, сходной с VIP1A(a)/VIP2A(a). ДНК из штаммов Bacillus AB78, АВ88, GC91, HD-1 и АТСС 10876 анализировали на
присутствие VIP1A(a)/VIP2A(а)-подобных последовательностей. ДНК из штаммов Bt GC91 и HD-1 и штамма Вс АТСС 10876 не гибридизуются с ДНК VIP2A(a)/VIP1A(a), что свидетельствует о том, что они лишены
последовательностей ДНК, аналогичных генам VIP1A(a)/VIP2A(a). Аналогично этому ДНК из инсектидного штамма АВ88 (пример 16) не гибридизовалась с VIP1A(a)/VIP2A(а)-областью ДНК, позволяя предположить,
что активность VIP, продуцируемого этим штаммом, не является результатом гомологии с VIP1A(a)/VIP2A(a). В противоположность этому Bacillus thuringiensis var. tenebrionis (Btt) содержал
последовательности, которые гибридизовались с VIP1A(a)/VIP2A(а)-областью. Дальнейший анализ подтвердил, что Btt содержит VIP1A(а)/VIP2A(а)-подобные последовательности.
С целью охарактеризовать в штамме Btt гомологи VIP2A(a) и VIP1A(а) клонировали гены, кодирующие эти протеины. Анализ методом Саузерн-блоттинга показал, что фрагмент длиной 9,5 т.п.н., полученный с помощью обработки рестриктазой EcoRI, вероятно содержит области, кодирующие гомологи. Геномную ДНК ращепляли EcoRI и с помощью гель-фильтрации очищали фрагменты длиной приблизительно 9,5 т.п.н. Эту ДНК лигировали с вектором pBluescript SK(+), расщепленным рестриктазой EcoRI, и трансформировали в Е.coli с той целью, чтобы создать плазмидную библиотеку. Приблизительно 10000 колоний подвергали скринингу путем гибридизации колоний на наличие последовательностей, гомологичных VIP2A(а). Были выявлены 28 позитивных колоний. Все 28 колоний являются идентичными и содержат гомологи VIP1A(a)/VIP2A(a). Клон рСIВ7100 был депонирован в Agricultural Research Service, Patent Culture Collection (NRRL), Northern Regional Research Center, 1815 North University Street, Peoria Illinois 61604, USA, под регистрационным номером NRRL B-21322. Из рСIВ7100 конструировали несколько субклонов. XbaI-фрагмент из рСIВ7100 длиной 3,8 т.п. н. клонировали в pBluescript SK(+), получая рСIВ7101. HindIII-фрагмент длиной 1,8 т.п.н. и HindIII-фрагмент длиной 1,4 т.п.н. из рСIВ7100 клонировали в pBluescript SK(+), получая рСIВ7102 и рСIВ7103 соответственно. Субклоны рСIВ7101, рСIВ7102 и рСIВ7103 были депонированы в Agricultural Research Service, Patent Culture Collection (NRRL), Northern Regional Research Center, 1815 North University Street, Peoria Illinois 61604, USA, под регистрацинным номерами В-21323, В-2134 и В-2135 соответственно.
Последовательность ДНК из области рСIВ7100, содержащей гомологи VIP2A(a)/VIP1A(a), определяли с помощью метода терминации дидезокси-цепи (Sanger и др. , Proc. Natl. Acad. ScL, USA, 74:5463-5467 (1977)). Реакции проводили с использованием наборов PRISM Ready Reaction Dye Deoxy Terminator Cycle Sequencing Kits и набора PRISM Sequenase® Terminator Double-Stranded DNA Sequencing Kit и анализировали на автоматическом секвенаторе типа АВ1 373. В качестве праймеров для определения последовательности ДНК в определенных областях использовали имеющиеся в продаже олигонуклеотиды. Последовательность ДНК этой области приведена в SEQ ID NO: 19.
Область длиной 4 т.п.н., приведенная в SEQ ID NO: 19, содержит две открытые рамки считывания (ОРС), которые кодируют протеины с высокой степенью гомологии к протеинам VIP1A(a) и VIP2A(a) из штамма АВ78. Аминокислотная последовательность гомолога VIP2A(a), обозначенного на основе стандартной номенклатуры как VIP2A(b), обнаружена на SEQ ID NO: 20, а аминокислотная последовательность гомолога VIP1A(a), обозначенного на основе стандартной номенклатуры как VIP1A(b), обнаружена на SEQ ID NO: 21. Аминокислоты протеина VIP2A(b) на 91% идентичны таковым VIP2A(a) из АВ78. Сравнительный анализ аминокислотных последовательностей двух протеинов VIP2 представлен в таблице 20. Аминокислоты протеина VIP1A(b) на 77% идентичны таковым VIP1A(a) из АВ78. Сравнительный анализ аминокислотных последовательностей двух протеинов VIP1 представлен в таблице 21. Сравнительный анализ, представленный в таблице 21, показывает сходство между VIP1A(b) и VIP1A(a) из АВ78. Этот сравнительный анализ первичной структуры свидетельствует о том, что аминоконцевые области двух протеинов VIP1 имеют более высокую идентичность аминокислот в аминоконцевой области, чем в карбоксиконцевой области. Так, аминоконцевые две трети (до аминокислоты 618 последовательности VIP1A(b), представленной в таблице 21) двух протеинов идентичны на 91%, в то время как карбоксиконцевые трети (от аминокислоты 619 до 833 VIP1A(b)) идентичны только на 35%.
Анализ методом Вестерн-блоттинга показал, что Bacillus thuringiensis var. tenebrionis (Btt) продуцирует как VIP1A(а)-подобные, так и VIP2A(а)-подобные протеины. Однако эти протеины не проявляют активности в отношении блошки длинноусой западной. Определение биологической активности в отношении блошки длинноусой западной осуществляли, используя либо 24-часовой супернатант культуры Btt, либо клон E.coli pCIB7100 (который содержит полную область гомологов VIP1A(a)/VIP2A(a)). В каждом случае не обнаружено активности в отношении блошки длинноусой западной.
Учитывая сходство между протеинами VIP2 из Btt и АВ78, изучали способность VIP2A(b) из Btt замещать VIP2A(a) из АВ78. Клетки, содержащие рСIВ6206, которые продуцируют VIP1A(a) из АВ78, но не протеин VIP2A(a), смешивали с супернатантом культуры Btt и определяли активность в отношении блошки длинноусой западной. В то время как ни супернатант культуры Btt, ни клетки, содержащие рСIВ6206, не обладали активностью в отношении БДЗ, смесь Btt и рСIВ6206 проявила высокую активность в отношении БДЗ. Кроме того, дополнительные биологические испытания показали, что клон Btt рСIВ7100, который содержит Вtt-гены VIP1A(b)/VIP2A(b) в E.coli, также проявляет активность в отношении БДЗ при смешении с рСIВ6206. Таким образом, протеин VIP2A(b), продуцируемый Btt, функционально эквивалентен протеину VIP2A(a), продуцируемому АВ78.
Таким образом, подтверждена способность выявлять новые штаммы с инсектицидной активностью с использованием в качестве зондов гибридизации ДНК VIP. Кроме того, штаммы Bacillus, которые содержат VIP1A(a)/VIP2A(a)-подобные последовательности, продуцируют VIP1A(a)/VIP2A(a)-подобный протеин, обладая при этом токсичностью по отношению к различным насекомым-вредителям. Аналогичные способы позволяют выявить существенно больше представителей семейства VIP1/VIP2. Кроме того, применение аналогичных методов позволяет выявить гомологи других разновидностей VIP (например, VIP из штамма АВ88).
Пример 22. Слияние протеинов VIP для создания отдельного полипептида
Протеины VIP могут встречаться в природе в виде
отдельных полипептидов или в виде двух или нескольких взаимодействующих полипептидов. Когда активный VIP состоит из двух или нескольких цепей взаимодействующих протеинов, то эти цепи протеина могут
быть получены в виде отдельной полипептидной цепи из гена, образовавшегося в результате слияния двух или нескольких кодирующих областей VIP. Гены, кодирующие две цепи, сливают, соединяя кодирующие
области генов с той целью, чтобы получить отдельную открытую рамку считывания, кодирующую оба полипептида VIP. Сложные полипептиды могут быть слиты для того, чтобы получить меньший по размеру
полипептид в виде NH2-концевого слитого протеина, или они могут быть слиты для того, чтобы получить более крупные полипептиды в виде NН2-концевого слитого протеина. Между этими
двумя полипептидными доменами необязательно может быть использована линкерная область. Такие линкеры хорошо известны в данной области техники. Такой линкер необязательно может быть сконструирован
таким образом, чтобы он содержал сайты протеазного расщепления, так что, когда отдельный слитый полипептид переваривается насекомым-мишенью, он расщепляется в линкерной области, высвобождая два
полипептидных компонента молекулы активного VIP.
VIP1A(a) и VIP2A(a) из штамма B.cereus AB78 гибридизируют с целью создать отдельный полипептид, сливая их кодирующие области. Образовавшаяся ДНК содержит последовательность, представленную в SEQ ID NO: 22, которая кодирует протеин, представленный в SEQ ID NO: 23. Аналогичным образом могут быть получены другие слитые протеины.
Слияние генов, кодирующих VIP1A(a) и VIP2A(a), осуществляют с использованием стандартных методов молекулярной биологии. Подлежащие делеции нуклеотиды между кодирующими областями VIP1A(a) и VIP2A(a) удаляют, используя известные методы мутагенеза, или в другом варианте кодирующие области сливают, используя методы ПЦР.
Слитые полипептиды VIP могут быть экспрессированы в других организмах с использованием синтетического гена или частично синтетического гена, оптимизированного для экспрессии в альтернативном хозяине. Например, для экспрессии слитого указанного выше полипептида VIP в кукурузе создают синтетический ген, используя для каждой аминокислоты предпочтительные для кукурузы кодоны, см. , например, европейскую заявку ЕР-А 0618976, включенную в настоящее описание в качестве ссылки. Синететические последовательности ДНК, созданные этими методами, представлены в SEQ ID NO: 17 (оптимизированная для кукурузы версия кодирующей последовательности VIP1A(a) с молекулярной массой 100 кДа), в SEQ ID NO: 18 (оптимизированная для кукурузы версия кодирующей последовательности VIP1A(a) с молекулярной массой 80 кДа) и в SEQ ID NO: 24 (оптимизированная для кукурузы версия кодирующей последовательности VIP2A(a)).
Синтетические гены VIP1 или VIP2, оптимизированные для экспрессии в кукурузе, могут быть слиты с использованием методов ПЦР или же могут быть созданы синтетические гены для слияния в определенном сайте рестрикции. Альтернативно этому может быть создан синтетический слитый ген с той целью, чтобы кодировать отдельный полипептид, содержащий домены как VIP1, так и VIP2.
Добавление пептидного линкера между доменами VIP1 и VIP2 слитого протеина может быть осуществлено с помощью ПЦР-мутагенеза, с помощью синтетической линкерной ДНК, кодирующей линкерный полипептид, или с помощью других методов, известных в данной области техники.
Слитые полипептиды VIP могут состоять из одного или нескольких связывающих доменов. Если при слиянии используют более одного связывающего домена, то, применяя такой гибрид, можно бороться со многими вредителями-мишенями. Другие связывающие домены могут быть получены с использованием всех либо части других VIP; эндотоксинов Bacillus thuringiensis либо их части; или других протеинов, способных связываться с вредителем-мишенью, либо соответствующих связывающих доменов, имеющих происхождение из таких связывающих протеинов.
Одним из примеров гибридной конструкции, содержащей оптимизированную для кукурузы последовательность ДНК, кодирующую гибридную отдельную полипептидную цепь, имеющую VIP2A(a) на N-конце и VIP1A(a) на С-конце, является рСIВ5531. Последовательность ДНК, кодирующую линкер, имеющий пептидную последовательность PSTPPTPSPSTPPTPS (SEQ ID NO:47), встраивали между двумя кодирующими областями. Последовательность, кодирующая этот линкер и соответствующие сайты клонирования, представляет собой 5'-CCC GGG CCT TCT ACT CCC ССА ACT CCC TCT CCT AGC ACG ССТ CCG АСА CCT AGC GAT АТС GGA ТСС-3' (SEQ ID NO: 48). Синтезировали олигонуклеотиды, представляющие собой верхнюю и нижнюю нити, и клонировали в векторе pUC после гибридизации и фосфорилирования с использованием стандартных методов. Терминирующий кодон в VIP2A(a) удаляли с использованием ПЦР и замещали на сайт SmaI с помощью сайта рестрикции BglII. Трансляционное слияние осуществляли путем лигирования фрагмента BamHI/PstI гена VIP2A(a) из рСIВ5522 (см. пример 24), ПЦР-фрагмента, содержащего Pstl-концевой фрагмент гена VIP2A(a) (идентичный таковому, примененному при конструировании рСIВ5522), синтетического линкера, имеющего концы, которые могут быть слиты с дефосфорилированным сайтом на 5'-конце и с BamHI на 3'-конце, и модифицированного синтетического гена VIP1A(a) из описанной ниже рСIВ5526 (см. SEQ ID NO: 35). Гибрид получали с помощью лигирования четырех компонентов, что приводит к образованию плазмиды, содержащей ген VIP2A(a) без кодона терминации трансляции с линкером и кодирующую область VIP1A(a) без сигнала секреции Bacillus. Последовательность ДНК этой конструкции, представленная в SEQ ID NO: 49, кодирует слитый протеин, представленный в SEQ ID NO: 50. Отдельный полипептидный гибрид, в котором VIP1A(a) представляет собой N-конец, a VIP2A(a) представляет собой С-конец, может быть создана аналогичным образом. Кроме того, либо один, либо оба гена могут быть связаны в трансляционном гибриде, содержащем или не содержащем линкер, либо на 5'-, либо на 3'-конце с другими молекулами типа генов, кодирующих токсины, или репортерных генов.
Пример 23. Обеспечение доставки VIP2 в органеллы растений
Известно, что в растениях имеются различные механизмы
доставки генных продуктов, а последовательности, контролирующие функции этих механизмов, охарактеризованы в некоторых деталях. Например, обеспечение доставки генных продуктов в хлоропласт
контролируется сигнальной последовательностью, обнаруженной на конце с аминогруппой различных протеинов. Этот сигнал отщепляется в процессе импорта в хлоропласт, давая зрелый протеин (см., например, у
Comai и др. , J. Biol. Chem. 263: 15104-15109 (1988)). Эти сигнальные последовательности могут быть слиты с продуктами гетерологичных генов, таких как VIP2, для осуществления импорта этих продуктов в
хлоропласт (van den Broeck и др. Nature 313: 358-363 (1985)). ДНК, кодирующая соответствующие сигнальные последовательности, может быть выделена из 5'-конца кДНК, кодирующих протеин RUBISCO, протеин
CAB, фермент EPSP-синтазу, протеин GS2 и многие другие протеины, которые, как известно, локализованы в хлоропласте.
Другие генные продукты локализованы в других органеллах, таких как митохондрия и пероксисома (см., например, у Unger и др.. Plant Molec. Biol. 13: 411-418 (1989)). кДНК, кодирующие эти продукты, могут также быть подвергнуты обработке, чтобы обеспечивать эффективные доставки продуктов гетерологичных генов, таких как VIP2, в эти органеллы. Примерами таких последовательностей являются кодируемые в ядре АТФазы и специфичные в отношении митохондрий изоформы аспартатаминотрансферазы. Аналогично этому обеспечение доставки к клеточным протеиновым тельцам описано у Rogers и др. (Ргос. Natl. Acad. Sci. USA 82:6512-6516 (1985)).
Путем слияния соответствующих обеспечивающих доставку последовательностей, описанных выше, с представляющими интерес кодирующими последовательностями, такими как VIP2, трансгенный продукт можно направлять к любой органелле или компартменту клетки. Для обеспечения доставки в хлоропласт, например сигнальную последовательность хлоропласта из гена RUBISCO, гена CAB, гена EPSP-синтазы или гена GS2 сливают в рамке считывания с аминоконцевым кодоном ATG трансгена. Выбранная сигнальная последовательность должна включать известный сайт расщепления, а при конструировании гибрида следует принимать во внимание любые аминокислоты, расположенные после сайта расщепления, которые необходимо отщепить. В некоторых случаях это требование может быть реализовано путем добавления небольшого количества аминокислот между сайтом расщепления и инициирующим кодоном ATG или в альтернативном варианте путем замещения некоторых аминокислот в кодирующей последовательности. Гибриды, сконструированные для импорта в хлоропласт, могут быть оценены с точки зрения эффективности поглощения хлоропластом путем трансляции in vitro транскрибируемых in vitro конструкций с последующим поглощением в хлоропласт in vitro с использованием методов, описанных у Barlett и др., под ред. Edelmann и др. , Methods in Chloroplast Molecular Biology, Elsevier. с. 1081-1091 (1982); Wasmann и др. , Mol. Gen. Genet. 205: 446-453 (1986). Эти методы конструирования хорошо известны в данной области техники и равным образом применимы как для митохондрий, так и для пероксисом.
Описанные выше механизмы, обеспечивающие доставку в клетку, могут быть применены не только в сочетании с родственными им промоторами, но также и в сочетании с гетерологичными промоторами, чтобы достичь конкретной цели, а именно доставки в клетку в условиях регуляции транскрипции промотором, имеющим схему экспрессии, отличную от таковой, свойственной промотору, от которого происходит обеспечивающий доставку сигнал.
Последовательность ДНК, кодирующая сигнал секреции, присутствует в нативном гене VIP2 Bacillus. Этот сигнал отсутствует в зрелом протеине, имеющем N-концевую последовательность LKITDKVEDF (аминокислотные остатки с 57 по 66 последовательности SEQ ID NO: 2). VIP2 можно сконструировать таким образом, чтобы он секретировался из растительной клетки или чтобы была обеспечена его доставка в субклеточные органеллы, такие как эндоплазматический ретикулюм, вакуоль, митохондрия или пластиды, в том числе хлоропласты. Гибридные протеины, созданные путем слияния сигнального пептида секреции с геном-маркером, успешно доставляли протеин в область секреции (см. Itimaga G. и др., The Plant Cell, 1: 381-390 (1989), Denecke и др.. The Plant Cell, 2: 51-59 (1990)). Были выявлены аминоконцевые последовательности, ответственные за обеспечение доставки в эндоплазматический ретикулюм, апопласт и за внеклеточную секрецию из алейронных клеток (Koehler & Но, Plant Cell 2:769-783 (1990)).
Чтобы сохранить протеин в эндоплазматическом ретикулюме или в вакуоли, необходимо наличие дополнительных сигналов. Для сохранения протеина в эндоплазматическом ретикулюме требуется наличие пептидной последовательности KDEL/HDEL на его карбоксильном конце (см. обзор Pelham, Annual Review Cell BioL, 5: 1-23 (1989). Также были охарактеризованы сигналы для сохранения протеинов в вакуоли. Сигналы, обеспечивающие доставку в вакуоль, могут присутствовать либо на аминоконцевом участке (Holwerda и др.. The Plant Cell, 4: 307-318 (1992), Nakamura и др., Plant PhysioL, 101: 1-5 (1993)), либо на карбоксиконцевом участке, либо во внутренней последовательности протеина, подлежащего доставке (Tague и др., The Plant Cell, 4: 307-318 (1992), Saalbach и др. , The Plant Cell, 3: 695-708 (1991)). Кроме того, аминоконцевые последовательности вместе с карбоксиконцевыми последовательностями ответственны за доставку генных продуктов в вакуоль (Shinshi и др., Plant Molec. Biol. 14: 357-368 (1990)). Аналогично этому протеины могут быть доставлены в митохондрии или пластиды с использованием специфичных гибридов сигнального пептида с карбоксильным концом (Heijne и др., Eur. J. Biochem., 180: 535-545 (1989), Archer и Keegstra, Plant Molecular Biology, 23: 1105-1115 (1993)).
Чтобы обеспечить доставку VIP2 либо для секреции, либо в различные субклеточные органеллы, может быть создана оптимизированная для кукурузы последовательность ДНК, кодирующая известный(ные) сигнальный(ные) пептид(ы) либо на 5'-, либо на 3'-конце гена, в зависимости от требований. Чтобы секретировать VIP2 из клетки, последовательность ДНК, кодирующая эукариотический сигнальный пептид секреции MGWSWIFLFLLSGAAGVHCL (SEQ ID NO: 25 из заявки РСТ W095/00497 или любая другая известная из литературы (например, Itirriaga и др.. The Plant Cell, 1: 381-390 (1989), Denecke и др.. The Plant Cell, 2: 51-59 (1990)), может быть добавлена на 5'-конце либо полной последовательности гена VIP2, либо укороченной последовательности с той целью, чтобы кодировать зрелый протеин или ген, укороченный до нуклеотида 286, или кодировать протеин, который должен начинаться от аминокислотного остатка 94 (метионин). Чтобы обеспечить сохранение доставленного VIP2 в эндоплазматическом ректикулюме, в дополнение к сигналу секреции на 3'-конце гена должна быть добавлена последовательность ДНК, кодирующая сигнальный пептид KDEL/HDEL эндоплазматического ретикулюма. Для обеспечения доставки в вакуоль может быть сконструирована последовательность ДНК, кодирующая сигнальный пептид SSSSFADSNPIRVTDRAAST (SEQ ID NO: 3; Holwerda и др. The Plant Cell, 4: 307-318 (1992)) и примыкающая к сигналу секреции, или последовательность, кодирующая сигнальный пептид с концевой карбоксильной группой и описанная у Dombrowski и др. The Plant Cell, 5: 587-596 (1993), или же ее функциональный вариант может быть встроен на 3'-конце гена. Аналогично этому может быть сконструирован VIP2 для обеспечения доставки либо в митохондрии, либо в пластиды, в том числе в хлоропласты, путем встраивания в последовательность VIP2 последовательностей, которые, как известно, могут кодировать необходимые сигналы, обеспечивающие доставку. Бактериальный сигнал секреции, присутствующий в VIP2, может быть сохранен или удален из окончательной конструкции.
Одним из примеров конструкции, которая содержит эукариотический сигнал секреции, слитый с кодирующей последовательностью VIP, является рСIВ5528. Синтезировали олигонуклеотиды, соответствующие как верхней, так и нижней нити последовательностей, кодирующих сигнальный пептид секреции SEQ ID NO: 25, и имеющие последовательность 5'-GGАТССАСС ATG GGC ТGG AGС TGG АТС ТТС СТG ТТС СТG СТG АGС GGС GСС GСG GGС GТG САС ТGС СТGСАG-3' (SEQ ID NO: 41). После гибридизации 5'-конец сигнала секреции напоминал "липкие концы", соответствующие сайтам рестрикции BamHI и PstI. Олигонуклеотид гибридизировали, фосфорилировали и лигировали в рСIВ5527 (конструкция, описанная в примере 23А), которую расщепляли BamHI/PstI с использованием стандартных методов. Полученная оптимизированная для кукурузы кодирующая последовательность представлена в SEQ ID NO: 42, она кодирует протеин, описанный в SEQ ID NO: 43. Этот кодируемый ею протеин содержит эукариотический сигнал секреции эукариот вместо сигнала секреции, присущего Bacillus.
Одним из примеров конструкции, которая содержит сигнал, обеспечивающий доставку в вакуоль и слитый с кодирующей последовательностью VIP, является рСIВ5533. Синтезировали олигонуклеотиды, соответствующие как верхней, так и нижней нити последовательностей, кодирующих пептид SEQ ID NO: 3, обеспечивающий доставку к вакуоли, и имеющих последовательность 5'-ССG СGG GСG ТОС ACT GСС ТСА GСА GСА GСА GСТ ТСG CCG АСА GСА АСС ССА ТСС GСG ТGА ССG АСС GСG ССG ССА GСА ССС ТGСАG-3' (SEQ ID NO: 44). После гибридизации 5'-конец сигнала, обеспечивающего доставку в вакуоль, напоминал "липкие концы", соответствующие сайтам рестрикции SacII и PstI. Олигонуклеотид гибридизировали, фосфорилировали и лигировали в рСIВ5528 (конструкция, описанная выше), которую расщепляли SacII/PstI с использованием стандартных методов. Полученная оптимизированная для кукурузы последовательность представлена в SEQ ID NO: 45, кодирующей протеин, описанный в SEQ ID NO: 46. Этот кодируемый протеин в дополнение к эукариотическому сигналу секреции содержит пептид, обеспечивающий доставку в вакуоль.
Аналогичными способами может быть создан ген VIP1 для секреции или обеспечения доставки в субклеточные органеллы.
Пример 23А. Удаление сигнала секреции, присущего Bacillus из VIP1A(a) и VIР2А(а)
VIP1A(a) и VIP2A(a) секретируются
во время роста штамма АВ78. Природа пептидных последовательностей, которые действуют как сигналы секреции, описана в литературе (Simonen и Palva, Microbiological reviews, с. 109-137 (1993)).
Руководствуясь информацией, приведенной в вышеуказанной публикации, выявляли предполагаемый сигнал секреции в обоих генах. В VIP1A(a) этот сигнал состоит из аминокислот 1-33 (см. SEQ ID NO: 5).
Процессинг сигнала секреции, по-видимому, происходит после серина на аминокислоте 33. Было выявлено, что в VIP2A(a) сигнал секреции состоит из аминокислот 1-49 (см. SEQ ID NO: 2). Анализ N-концевого
пептида секретируемого зрелого протеина VIP2A(a) выявил N-концевую последовательность LKITDKVEDFKEDK. Было установлено, что эта последовательность начинается с аминокислоты 57 в SEQ ID NO: 2. Гены,
кодирующие эти протеины, модифицировали путем удаления сигналов секреции, присущих Bacillus.
Конструировали кодирующую область оптимизированного для кукурузы гена VIP1A(a), которая имела последовательности, кодирующие первые 33 аминокислоты, т.е. сигнал секреции, удаленный с 5'-конца этого гена. Эту модификацию получали с помощью ПЦР, используя прямой праймер, который содержит последовательность 5'-GGA ТСС АСС ATG AAG АСС AAC CAG АТС AGC-3' (SEQ ID NO: 33) и который гибридизируется с оптимизированным для кукурузы геном (SEQ ID NO: 26) за нуклеотидом в положении 100, и добавляли сайт рестрикции BamHI и эукариотический трансляционный инициирующий консенсусный сайт, включающий стартовый кодон. Обратный праймер, содержащий последовательность 5'-AAG CTT CAG CTC CTT G-3' (SEQ ID NO: 34), гибридизируется с комплементарной нитью за нуклеотидом в положении 507. Получали продукт амплификации длиной 527 пар оснований, содержащий сайты рестрикции BamHI на 5'-конце и HindIII на 3'-конце. Продукт амплификации клонировали в Т-векторе (описанном в примере 24, см. ниже) и секвенировали для гарантии правильности последовательности ДНК. Затем с помощью расщепления рестриктазами получали BamHI/HindIII- фрагмент и применяли для замещения BamHI/HindIII-фрагмента, оптимизированного для кукурузы гена VIP1A(a), клонированного в кассете промотора, предпочтительного для корня. Полученную конструкцию обозначали как рСIВ5526. Оптимизированная для кукурузы кодирующая область VIP1A(a) с удаленным сигналом секреции Bacillus представлена в SEQ ID NO: 35, а кодируемый протеин представлен в SEQ ID NO: 36.
Ген, кодирующий форму VIP2A(a), которая образуется после процессинга, т. е. кодирующую область с удаленным сигналом секреции, конструировали с использованием методики, аналогичной описанной выше для конструирования формы VIP1A(a), которая образуется после процессинга. Модификацию получали с помощью ПЦР, используя прямой праймер 5'-GGA TCC ACC ATG СТG CAG ААС СТG AAG АТС AC-3' (SEQ ID NO: 37). Этот праймер гибридизируется с оптимизированным для кукурузы геном VIP2A(a) (SEQ ID NO: 27) за нуклеотидом в положении 150. Молчащую мутацию получали в нуклеотиде в положении 15 этого праймера, получая сайт рестрикции Pstl. Обратный праймер имеет последовательность 5'-AAG СТТ ССА СТС СТТ СТС-3' (SEQ ID NO: 38). Получали продукт длиной 259 пар оснований, содержащий сайт рестрикции HindIII на 3'-конце. Продукт амплификации клонировали в Т-векторе, секвенировали и лигировали с ращепленной BamHI/HindIII, предпочтительной для корня кассетой промоторов, содержащей оптимизированный для кукурузы VIP2A(a). Полученную конструкцию обозначали как рСIВ5527. Оптимизированная для кукурузы кодирующая область VIP2A(a) с удаленным сигналом секреции, присущим Bacillus, представлена в SEQ ID NO: 39, а кодируемый протеин представлен в SEQ ID NO: 40.
Пример 24. Конструирование и клонирование оптимизированных для кукурузы генов
VIP1A(a) и VIР2А(а)
Конструирование: Оптимизированные для кукурузы гены конструировали путем обратной трансляции нативных последовательностей протеинов VIP1A(a) и VIP2A(a), используя кодоны,
которые в основном применяют для кукурузы (Murray и др. , Nucleic Acid Research, 17: 477-498 (1989)). Для облегчения клонирования последовательность ДНК, кроме того, модифицировали, включая уникальные
сайты рестрикции с интервалами через каждые 200-360 нуклеотидов. Конструировали VIP1A(a) при клонировании в виде 11 таких фрагментов, a VIP2A(a) клонировали в виде 5 фрагментов. После клонирования
индивидуальных фрагментов соседние фрагменты объединяли, используя сайты рестрикции, общие для обоих фрагментов, получая полный ген. Для клонирования каждого фрагмента конструировали олигонуклеотиды
(50-85 нуклеотидов), представляющие собой как верхнюю, так и нижнюю нить ДНК. Верхний олигонуклеотид из первой олигонуклеотидной пары конструировали таким образом, чтобы он имел однонитевую область
длиной 15 пар оснований на 3'-конце, которая гомологична аналогичной однонитевой области нижней нити следующей олигонуклеотидной пары, с целью направлять ориентацию и последовательность различных
олигонуклеотидных пар внутри данного фрагмента. Также конструировали олигонуклеотиды таким образом, чтобы, когда все олигонуклеотиды, представляющие фрагмент, гибридизируются, концы имели однонитевые
области, соответствующие конкретному сайту рестрикции, который должен быть образован. Строение каждого олигомера оценивали на стабильность вторичных структур, таких как петли из двухцепочечных
участков одноцепочечных молекул, используя программу OLIGO фирмы NBI Inc. При необходимости нуклеотиды изменяли, чтобы уменьшить стабильность вторичной структуры без изменения аминокислотной
последовательности протеина. Растительную консенсусную последовательность сайта связывания рибосом растений TAAACAATG (Joshi и др., Nucleic Acid Res., 15: 6643-6653 (1987)) или эукариотическую
консенсусную последовательность сайта связывания рибосом CCACCATG (Kozak, Nucleic Acid Research, 12: 857-872 (1984)) встраивали за трансляционным стартовым кодон гена.
Клонирование: Олигонуклеотиды синтезировали по методу фирмы IDT Inc. и использовали в виде лиофилизированных порошков. Их ресуспендировали в концентрации 200 мкМ. К 30 мкл каждого олигонуклеотида добавляли формамид до конечной концентрации 25-50% и образец кипятили в течение 2 минут перед разделением на предварительно приготовленном геле из 10%-ного полиакрил-амид/мочевина, полученном от фирмы Novex. После электрофореза олигонуклеотид определяли с помощью УФ-экранирования, помещая гель на пластинку для ТСХ, содержащую флуоресцентный индикатор, и экспонируя ее УФ-лучами. Область, содержащую ДНК правильного размера, вырезали и экстрагировали от полиакриламидного геля путем инкубации в течение ночи измельченного фрагмента геля в буфере, содержащем 0,4 М LiC1, 0,1 мМ ЭДТК. ДНК отделяли от остатка геля путем центрифугирования через фильтр типа Millipore UFMC. Экстрагированную ДНК подвергали осаждению этанолом, добавляя 2 объема абсолютного спирта. После центрифугирования осадок ресуспендировали в dH2O в концентрации 2,5 мкМ. Фрагменты клонировали либо путем гибридизации олигомеров и лигирования с соответствующим вектором, либо путем амплификации гибридизованного фрагмента, используя в качестве матрицы эквимолярную смесь всех олигомеров для конкретного фрагмента и специфичные для конца ПЦР-праймеры.
Клонирование путем гибридизации и лигирование: Гомологичные двунитевые олигонуклеотидные пары получали путем смешения 5 мкл верхнего и нижнего олигонуклеотида каждой олигонуклеотидной пары с буфером, содержащим однократный полинуклеотидкиназный (ПНК) буфер (70 мМ Трис-НС1 (рН 7,6), 10 мМ MgCl2, 5 мМ дитиотриитол (ДТТ)), 50 мМ КС1 и 5%-ный формамид в конечном объеме 50 мкл. Олигонуклеотиды кипятили в течение 10 минут и медленно охлаждали до 37oС или до комнатной температуры. Для анализа на 4%-ной агарозе в буферной системе ТАЕ (Metaphore®; фирма FMC) использовали 10 мкл олигонуклеотидов. Каждую гибридизованную олигонуклеотидную пару обрабатывали киназой путем добавления АТФ до конечной концентрации 1 мМ, БСА до конечной концентрации 100 мг/мл и 200 единиц полинуклеотидкиназы и 1 мкл десятикратного ПНК-буфера в объеме 10 мкл. После гибридизации и фосфорилирования реакционную смесь инкубировали при 37oС от 2 до 12 часов (в течение ночи). 10 мкл каждой олигонуклеотидной пары для конкретного фрагмента смешивали в конечном объеме 50 мкл. Олигонуклеотидные пары гибридизировали путем выдержки при 80oС в течение 10 минут и медленного охлаждения до 37oС. 2 мкл олигонуклеотидов смешивали с приблизительно 100 нг соответствующего вектора и лигировали, используя буфер, содержащий 50 мМ Трис-НСl (рН 7,8), 10 мМ MgCl2, 10 мМ ДТТ, 1 мМ АТФ. Реакционную смесь инкубировали при комнатной температуре от 2 до 12 часов (в течение ночи) и трансформировали в штамм E.coli DH5α, высеянный на L-чашки, содержащие ампициллин в концентрации 100 мкг/мл, используя стандартные методы. Позитивные клоны подвергали дальнейшему изучению и определяли с помощью ПЦР-микроскрининга, описанного подробно в европейской заявке ЕР-А 0618976, используя в качестве праймеров универсальные праймеры "Reverse" и "MIS-20". Позитивные клоны выявляли путем расщепления соответствующими ферментами с последующим секвенированием. Рекомбинанты, имеющие ожидаемую последовательность ДНК, затем отбирали для дальнейшей работы.
ПЦР-амплификация и клонирование в Т-векторе: ПЦР-амплификацию осуществляли, используя в качестве матрицы смесь всех олигомеров, которые представляют собой верхнюю и нижнюю нить определенного фрагмента (конечная концентрация каждого 5 мМ), специфические концевые праймеры для конкретного фрагмента (конечная концентрация 2 мкМ), 200 мкМ каждого дАТФ, дТТФ, дЦТФ и дГТФ, 10 мМ Трис-НСl (рН 8,3), 50 мМ КС1, 1,5 мМ MgCl2, 0,01% желатина и 5 единиц Taq-полимеразы в конечном объеме реакционной смеси 50 мкл. Реакцию амплификации осуществляли в термоциклере модели 9600 фирмы Perkin Elmer путем инкубации при 95oС в течение 1 минуты (1 цикл), далее 20 циклов при 95oС в течение 45 секунд, при 50oС в течение 45 секунд и при 72oС в течение 30 секунд. В заключение реакционную смесь инкубировали в течение 5 минут при 72oС перед анализом продуктов. 10 мкл реакционной смеси анализировали на 2,5%-ном агарозном геле типа Nusieve (фирма FMC) в системе ТАЕ-буфера. Фрагмент правильного размера выделяли из геля и применяли для клонирования в ПЦР-векторе клонирования или в Т-векторе. Т-векторная конструкция описана у Marchuk и др. , Nucleic Acid Research, 19: 1154 (1991). В качестве родительского вектора применяли pBluescript SK(+) (Stratagene®, CA). Трансформацию и идентификацию нужного клона осуществляли по описанной выше методике.
Фрагменты 1, 3, 4, 5, 6, 8 и 9 VIP1A(a) и фрагменты 2 и 4 VIP2A(a) получали путем клонирования продуктов ПЦР-амплификации; в то время как фрагменты 2, 7, 10 и 11 VIP1A(a) и фрагменты 1, 3 и 5 VIP2A(a) получали путем гибридизации/лигирования.
Когда получали фрагменты нужной последовательности, полный ген объединяли путем клонирования вместе с соседними фрагментами. Полный ген повторно секвенировали и определяли его активность в отношении БДЗ перед введением его в векторы экспрессии растений, содержащие предпочтительный для корня промотор (описанный в заявке на патент США 08/017209, включенной в настоящее описание в качестве ссылки) и промотор актина риса.
Одним из таких растительных векторов экспрессии является рСIВ5521. Оптимизированную для кукурузы кодирующую область VIP1A(a) (SEQ ID NO:26) клонировали в растительном векторе экспрессии, содержащем на 5'-конце гена предпочтительный для корня промотор, с интроном 9 РЕР-карбоксилазы, за которым на 3'-конце расположен 35S-терминатор. Плазмида также содержит последовательность, обеспечивающую устойчивость к ампициллину из плазмиды pUC19. Второй вектор экспрессии растения представляет собой рСIВ5522, который содержит оптимизированную для кукурузы кодирующую область VIP2A(a) (SEQ ID NO: 27), слитую на 5'-конце гена с предпочтительным для корня промотором, с интроном 9 РЕР-карбоксилазы, за которым на 3'-конце расположен 35S-терминатор.
Пример 25. NAD-аффинная хроматография
Использовали метод очистки, основанный на сродстве VIP2 к субстрату NAD. Супернатант, описанный в
примере 4, после обработки натрий-нитратным буфером с рН 3,5 в течение ночи подвергали диализу в 20 мМ Трис, рН 7,5. Нейтрализованный супернатант добавляли к равному объему промытой NAD агарозы и
инкубировали при осторожном встряхивании при 4o С в течение ночи. Смолу и раствор протеина добавляли в 10-миллилитровую полипропиленовую колонку одноразового использования и давали
протекать раствору протеина. Колонку промывали 20 мМ Трис, рН 7,5 (5 объемов колонки), затем промывали 20 мМ Трис, рН 7,5 (2-5 объемов колонки), 100 мМ NaCl, а затем 20 мМ Трис, рН 7,5 (2-5 объемов
колонки). Протеины VIP элюировали 20 мМ Трис, рН 7,5, дополненным 5 мМ NAD. Элюент собирали в объеме, составляющем приблизительно 3 объема колонки, и концентрировали в Centricon-10. Выход обычно
составлял 7-15 мкг протеина на 1 мл смолы.
Когда очищенные протеины анализировали с помощью электрофореза в ДСН-ПААГ с последующим окрашиванием серебром, проявлялись два полипептида, один с Mr приблизительно 80000, а другой с Мг приблизительно 45000. N-концевое секвенирование показало, что протеин с Мг 80000 соответствовал форме VIP1A(a), полученной в результате протеолитического расщепления, а протеин с Mw 45000 соответствовал форме VIP2A(a), полученной в результате протеолитического расщепления. Совместная очистка VIP1A(a) с VIP2A(a) свидетельствует о том, что два протеина, вероятно, образуют комплекс и имеют области связывания протеин-протеин. Очищенные таким образом протеины VIP1A(a) и VIP2A(a) обладали биологической активностью в отношении блошки динноусой западной.
Пример 26. Экспрессия оптимизированных для кукурузы VIP1A(a) и VIР2А(а)
Штаммы E.coli, содержащие различные плазмиды, включающие гены VIP, анализировали в отношении
экспрессии VIP. Штаммы E.coli, содержащие индивидуальные плазмиды, выращивали в течение ночи в L-бульоне и экспрессируемый протеин экстрагировали из культуры, как описано выше в примере 3. Экспрессию
протеина анализировали с помощью Вестерн-блоттинга, используя антитела, полученные с помощью стандартных методов, известных в данной области техники и аналогичных таковым, описанным выше в примере 12.
Кроме того, инсектицидную активность экспрессируемых протеинов оценивали в отношении блошки длинноусой западной в соответствии с методом из приведенного выше примера 3. Результаты анализа экспрессии в
E.coli представлены в табл. X.
ДНК из этих плазмид применяли для временной экспрессии VIP в системе экспрессии протопласта кукурузы. Протопласты выделяли из 6 суспензионных культур кукурузы линии 2717 путем разложения клеточных стенок с использованием целлюлазы Cellulase RS и мацеразы Macerase RIO в соответствующем буфере. Протопласты получали путем фильтрования и центрифугирования. Протопласты трансформировали стандартным методом прямого переноса гена, используя приблизительно 75 мкг ДНК плазмиды и ПЭГ-40. Обработанные протопласты инкубировали в течение ночи в темноте при комнатной температуре. Анализ экспрессии VIP осуществляли на эксплантатах протопластов с помощью Вестерн-блоттинга. Инсектипидную активность в отношении блошки длинноусой западной определяли аналогично методике, описанной выше для экспрессии в E.coli. Результаты анализа экспрессии в протопласте кукурузы приведены в табл. XI.
Данные об экспрессии, полученные как для E.coli, так и для протопластов кукурузы, свидетельствуют о том, что оптимизированные для кукурузы гены VIP1A(a) и VIP2A(a) продуцируют такой же протеин, что и нативные гены VIP1A(a) и VIP2A(a) соответственно и что протеины, кодируемые оптимизированными для кукурузы генами, функционально эквивалентны протеинам, кодируемым нативными генами.
Все публикации и заявки на патент, упомянутые в настоящем описании изобретения, характеризуют уровень техники для специалистов в данной области техники, для которых предназначено настоящее изобретение. Все публикации и заявки на патент включены в настоящее описание в качестве ссылки в той степени, в какой каждая отдельная публикация или описание патента, взятые конкретно и по отдельности, должны были бы быть включены в качестве ссылки.
В Agricultural Research Service, Patent Culture Collection (NRRL), Northern Regional Research Center, 1815 North University Street, Peoria Illinois 61604, USA, были депонированы штаммы, представленные в табл. XII.
Хотя вышеприведенное изобретение описано и проиллюстрировано достаточно подробно на примерах с целью облегчения понимания его сущности, очевидно, что на практике в рамках прилагаемой формулы изобретения могут быть внесены определенные изменения и модификации. То
Реферат
Изобретение может быть использовано в селекции растений. Трансгенное растение получают введением в его геном молекулы ДНК, кодирующей инсектицидный протеин, который секретируется на вегетативной стадии роста Bacillus spp. Трансформация может также включать использование последовательностей ДНК, кодирующих вспомогательные и/или слитые протеины. Секреция инсектицидных протеинов во время вегетативной стадии роста штаммов Bacillus обеспечивает защиту растения от повреждения насекомыми-вредителями. 3 с. и 43 з.п. ф-лы, 33 табл.
Формула
28.09.1994 по пп. 1-6, 7 (кроме NRRL B - 21439), 8-10, 12-22, 24, 25, 27, 28, 30, 31, 32 (в отношении Seq ID Nos. 17 и 18), 33 ( в отношении Seq ID No: 24), 35, 36, 38 (в отношении Seq ID Nos. 1, 4 и 6), 39-46, (в отношении Seq ID Nos. 1, 4 и 6);
05.06.1995 по пп. 7 (в отношении NRRL B - 21439), 11 (в отношении Seq ID Nos. 29 и 32), 26, 29, 32 (в отношении Seq ID Nos. 26 и 35), 33 (в отношении Seq ID Nos. 27, 39, 42 и 45), 34 (в отношении Seq ID No: 30), 37, 38 (в отношении Seq ID Nos. 28, 30 и 31), 46 (в отношении Seq ID Nos. 28, 30 и 31);
27.09.1995 по пп. 11 (в отношении Seq ID No: 52), 23, 34 (в отношении Seq ID No: 51), 38 (в отношении Seq ID No: 51), 46 (в отношении Seq ID No: 51).

Комментарии