Способ синтеза альфа-аминоалкиленфосфоновой кислоты - RU2674022C2
Код документа: RU2674022C2
Описание
Область техники, к которой относится изобретение
[0001] Настоящее изобретение относится к способу синтеза альфа-аминоалкиленфосфоновой кислоты или ее сложных фосфонатных эфиров.
Уровень техники
[0002] Соединения альфа-аминофосфоновой кислоты хорошо известны из уровня техники и нашли широкое промышленное применение для ряда областей применения, в том числе обработки воды, замедления процесса образования накипи, моющих присадок, комплексообразователей, вспомогательных веществ, применяемых при бурении в ходе добычи нефти с морских промыслов, ионообмена при прививке на смолах и в качестве фармацевтических компонентов. Хорошо известно, что в таких областях применения предпочтительно необходимы аминоалкиленфосфоновые кислоты, в которых основная часть заместителей по азоту представляет собой группы алкиленфосфоновой кислоты.
[0003] Существует несколько способов получения альфа-аминоалкиленфосфоновой кислоты, такие как, например, помимо прочих, раскрытые в патентах GB 1142294, GB 1230121, US 3288846, JP 57075990, US 3832393, ЕР 1681294, ЕР 1681295 и ЕР 0638577 и в патентных заявках WO 96/40698, JP 2007022956 и WO 2009/130322.
[0004] В патенте US 3796749 раскрыт способ получения практически чистых аминометиленфосфоновых кислот с высоким выходом, предусматривающий осуществление реакции N-замещенных альфа-аминомоно- или поликарбоновых кислот, или их солей с щелочными металлами, с фосфорной кислотой в присутствии водопоглощающих средств при температуре от приблизительно 90°С до приблизительно 160°С. Подходящими водопоглощающими средствами являются ангидриды кислоты, которые при объединении с водой превращаются в соответствующие кислоты. Такими средствами, например, являются ангидриды низших алкановых кислот, такие как ангидрид уксусной кислоты, ангидрид пропионовой кислоты или ангидриды неорганических кислот, такие как пентаоксид фосфора и т.п.
[0005] В патенте US 3816517 раскрыт способ получения практически чистых аминометиленфосфоновых кислот с высоким выходом путем осуществления реакции N-замещенных альфа-аминомоно- или поликарбоновых кислот, или их солей с щелочными металлами, с фосфорной кислотой и/или тригалогенидом фосфора, предпочтительно трихлоридом фосфора, в присутствии или отсутствии инертных разбавителей. Если не применяют фосфорную кислоту, а лишь трихлорид фосфора, то к трихлориду фосфора добавляют некоторое количество воды с получением фосфорной кислоты так, чтобы в реакционной смеси присутствовала смесь трихлорида фосфора и фосфорной кислоты. Реакцию также можно проводить только с фосфорной кислотой. В целом, фосфорную кислоту и/или тригалогенид фосфора добавляют к альфа-аминометиленкарбоновой кислоте.
[0006] В патенте IN 192483 раскрыт способ получения этилендиаминтетра-(метиленфосфоновой кислоты) путем осуществления реакции этилендиаминотетра-(уксусной кислоты) с трихлоридом фосфора и фосфористой кислотой.
[0007] В патенте US 3451937 заявлен моющий состав, фактически состоящий из (А) водорастворимого органического моющего средства и (В) зтангидрокситрифосфоновой кислоты или ее соли. В столбце 4, строках 60-75 раскрыта реакция фосфоноуксусной кислоты (2 моля) с тетрафосфорным гексаоксидом (1 моль), с атомным отношением С:Р реакционной системы, составляющим 4:6, при этом получают высокий выход этан-1-гидрокси-1,1,2-трифосфоновой кислоты.
[0008] В патентной заявке ЕР 2112156 раскрыт способ получения аминоалкиленфосфоновой кислоты, включающий стадии добавления тетрафосфорного гексаоксида в водную реакционную среду, содержащую, гомогенную кислоту Бренстеда, в результате чего тетрафосфорный гексаоксид будет практически качественно гидролизироваться до фосфористой кислоты, в результате чего уровень свободной воды в реакционной среде, после завершения гидролиза тетрафосфорного гексаоксида, будет находиться в диапазоне от 0 до 40% по весу. На следующей стадии в реакционную среду добавляют амин, формальдегид и дополнительную кислоту Бренстеда, после чего реакцию завершают с получением, таким образом, аминоалкиленфосфоновой кислоты. В варианте такого способа амин можно добавлять до или на стадии гидролиза тетрафосфорного гексаоксида.
[0009] Таким образом, как и ожидалось, область техники изобилует и включает способы получения таких соединений. Известное из уровня техники получение альфа-аминоалкиленфосфоновых кислот основано на превращении фосфористой кислоты, полученной в результате гидролиза трихлорида фосфора, или на превращении фосфористой кислоты посредством добавления хлористоводородной кислоты, при этом хлористоводородную кислоту можно, частично или полностью, добавлять в форме солянокислого амина.
[0010] Современная технология, основанная на гидролизе трихлорида фосфора, обладает хорошо известными недостатками: от наличия хлористоводородной кислоты до потерь трихлорида фосфора вследствие летучести и уноса хлористоводородной кислотой. Кроме того, очень важен контроль температуры реакции для ограничения потерь трихлорида фосфора (температура кипения 76°С) и для избегания образования низших оксидов фосфора, что создает проблемы безопасности.
[0011] Дополнительные способы получения аминометиленфосфоновых кислот, при которых осуществляют реакцию аминов с альдегидом или кетоном и соединением трехвалентного фосфора, такого как фосфористая кислота, сложные эфиры фосфористой кислоты или трехгалоидный фосфор, в целом, характеризуются довольно низкими выходами, которые обычно не превышают приблизительно 55%-60%. Такие низкие выходы обусловлены образованием побочных продуктов, а также конечных продуктов с различными степенями замещения алкиленфосфоновой кислоты. Таким образом, разделение и очистка становятся затруднительной и проблематичной задачей.
[0012] Следовательно, существует необходимость в получении соединений альфа-аминоалкиленфосфоновой кислоты с помощью новых в технологическом плане, но экономически приемлемых способов, наиболее согласующихся с существующими потребностями.
[0013] Исходя из вышеприведенного, абсолютно неожиданно, что карбоксильная группа альфа-аминоалкиленкарбоновой кислоты может быть заменена группой фосфоновой кислоты посредством реакции альфа-аминоалкиленкарбоновой кислоты с тетрафосфорным гексаоксидом. С другой стороны, как, например, раскрыто в патенте US 3451937, карбоксильная группа совершенно иным образом вступает в реакцию с тетрафосфорным гексаоксидом.
Цели изобретения
[0014] Целью настоящего изобретения является создание нового и эффективного синтеза альфа-аминоалкиленфосфоновой кислоты или ее сложных фосфонатных эфиров, который лишен недостатков известных из уровня техники способов. Другой целью настоящего изобретения является создание способа одностадийного синтеза, с помощью которого можно селективно получать соединения более высокого качества с высокой чистотой и высоким выходом. Еще одной целью настоящего изобретения является синтез соединений фосфоновой кислоты за более короткий срок и с меньшей затратой энергии.
Краткое описание изобретения
[0015] Настоящее изобретение раскрывает способ синтеза альфа-аминоалкиленфосфоновой кислоты или ее сложного эфира, включающий стадии:
-а) получения реакционной смеси путем смешивания соединения, содержащего один или несколько ангидридных фрагментов Р-О-Р, причем указанные фрагменты содержат один атом Р со степенью окисления (+III) и другой атом Р со степенью окисления (+III) или (+V), альфа-аминоалкиленкарбоновой кислоты и кислотного катализатора, где
указанное соединение, содержащее один или несколько ангидридных фрагментов Р-О-Р, выбирают из группы, состоящей из:
- тетрафосфорного гексаоксида, тетраэтилпирофосфита, соединения, полученного в результате объединения одного или нескольких соединений, содержащих один или несколько фрагментов Р-ОН, с одним или несколькими соединениями, содержащими один или несколько ангидридных фрагментов Р-О-Р, где атом Р в одном или нескольких соединениях имеет степень окисления (+III), и где соединения с одним или несколькими фрагментами Р-ОН поддаются таутомеризации по фрагменту >Р(=O)Н; и
- соединения, полученного в результате объединения одного или нескольких соединений с 2 или более фрагментами Р-О-Р и воды, где фрагменты Р-О-Р имеют один атом Р со степенью окисления (+III) и один атом Р со степенью окисления (+IIII) или (+V);
и где
указанная реакционная смесь характеризуется эквивалентным отношением альфа-аминоалкиленкарбоновой кислоты к ангидридным фрагментам Р-О-Р, составляющим по меньшей мере 0,2, и
- b) выделения из указанной реакционной смеси полученного соединения альфа-аминоалкиленфосфоновой кислоты или ее сложного эфира.
[0016] В предпочтительных вариантах осуществления настоящего изобретения раскрывают один или несколько из следующих признаков:
- реакционную смесь получают путем постепенного добавления соединения, содержащего ангидридный фрагмент Р-О-Р с одним атомом Р со степенью окисления (+III) и другим атомом Р со степенью окисления (+III) или (+V), к смеси, содержащей альфа-аминоалканкарбоновую кислоту и кислотный катализатор;
- реакционную смесь получают путем постепенного добавления смеси, содержащей альфа-аминоалканкарбоновую кислоту и кислотный катализатор, к соединению, содержащему ангидридный фрагмент Р-О-Р с одним атомом Р со степенью окисления (+III) и другим атомом Р со степенью окисления (+III) или (+V);
- способ синтеза альфа-аминоалкиленфосфоновой кислоты или ее сложного эфира включает дополнительные стадии:
- добавления воды к реакционной смеси после завершения превращения альфа-аминоалкиленкарбоновой кислоты в альфа-аминоалкиленфосфоновую кислоту;
- доведения реакционной смеси, содержащей добавленную воду, до температуры, составляющей от 20°С до 100°С, и
- выдерживания реакционной смеси, содержащей добавленную воду, при указанной температуре в течение по меньшей мере 10 минут;
- соединение, содержащее ангидридный фрагмент Р-О-Р, выбирают из группы, состоящий из тетрафосфорного гексаоксида, тетраэтилпирофосфита, и при этом содержащие ангидридный фрагмент Р-О-Р соединения получают в результате объединения фосфористой кислоты и тетрафосфорного гексаоксида, фосфористой кислоты и тетрафосфорного декаоксида, диметилфосфита и тетрафосфорного декаоксида, а также тетрафосфорного гексаоксида и воды;
- соединение, содержащее ангидридный фрагмент Р-О-Р, представляет собой тетрафосфорный гексаоксид;
- соединение, содержащее фрагмент альфа-аминоалкиленкарбоновой кислоты, имеет общую формулу:
R1-N(R2)-CR3R4-CO2M,
где R1 может представлять собой замещенный атом С или замещенный атом S; R2 может представлять собой атом Н, замещенный атом С или замещенный атом S; R3 и R4 независимо могут представлять собой атом Н или замещенный атом С; М может представлять собой атом Н или щелочной или щелочно-земельный металл;
- соединение, содержащее фрагмент альфа-аминоалкиленкарбоновой кислоты, выбирают из
a) соединения, где атом N обладает низкой основностью в результате замещения по атому N электроноакцепторными группами или группами, которые могут частично делокализовывать неподеленную пару у N;
b) полиамина, у которого присутствуют по меньшей мере два атома N, и каждый атом N отделен по меньшей мере двумя атомами углерода от следующего соседнего атома N;
c) соединения, у которого атом N имеет в качестве заместителей алкильные группы;
- соединение, содержащее фрагмент альфа-аминоалкиленкарбоновой кислоты, выбирают из
а) нитрилтрехуксусной кислоты, этилендиаминтетрауксусной кислоты, диэтилентриаминпентауксусной кислоты, N-бензилиминодиуксусной кислоты, N-метилиминодиуксусной кислоты, иминодиуксусной кислоты, N,N-бис(карбоксиметил)-1-глутаминовой кислоты, тринатрия-N,N-бис(карбоксиметил)-аланина, N-цианометилаланина, N,N-бис(цианометил)-глицина, 4-морфолинуксусной кислоты, пироглутаминовой кислоты, N-ацетил глицина, N,N-бис(карбоксиметил)-6-аминокапроновой кислоты, N-фенилглицина, N-тозилглицина, моногидрата транс-1,2-циклогексилдиаминотетрауксусной кислоты, N-фосфонометилиминодиуксусной кислоты, иминодиуксусной кислоты, привитой на смолу, такую как, например, подкисленная Amberlite IRC748i;
b) 1,4,7,10-тетраазадодекан-1,4,7,10-тетрауксусной кислоты, моногидрата транс-1,2-циклогексилдиаминотетрауксусной кислоты;
c) N,N'-диметилглицина;
- кислотный катализатор представляет собой гомогенный катализатор на основе кислоты Бренстеда, предпочтительно выбранный из группы, состоящей из метансульфоновой кислоты, трифторметансульфоновой кислоты, уксусной кислоты, трифторуксусной кислоты, п-толуолсульфоновой кислоты, хлористоводородной кислоты, фосфористой кислоты, фосфорной кислоты и их смесей;
- кислотный катализатор представляет собой гетерогенный катализатор на основе кислоты Бренстеда, выбранный из группы, состоящей из:
(i) комбинаций твердых кислотных оксидов металлов как таковых или на подложке из материала-носителя;
(ii) катионообменных смол, выбранных из группы, включающей сополимеры стирола, этилвинилбензола и дивинилбензола, функционализированных таким образом, что обеспечивается прививка фрагментов SO3H на ароматическую группу и перфорированные смолы, несущие группы карбоновой и/или сульфоновой кислоты;
(iii) органических сульфоновых, карбоновых и фосфоновых кислот Бренстеда, (которые являются практически несмешиваемыми в реакционной среде при температуре реакции);
(iv) кислотного катализатора, полученного:
- в результате взаимодействия твердой подложки, содержащей неподеленную пару электронов, на которую осаждается органическая кислота Бренстеда; или
- в результате взаимодействия твердой подложки, содержащей неподеленную пару электронов, на которую осаждается соединение, содержащее Льюисовские кислотные центры; или
- из гетерогенных твердых веществ, функционализированных посредством химической прививки группы кислоты Бренстеда или ее предшественника; и
(v) гетерогенных гетеропол и кислот общей формулы HxPMyOz, где Р выбран из фосфора и кремния, а M выбран из вольфрама и молибдена и их комбинаций.
- кислотный катализатор представляет собой катализатор на основе кислоты Льюиса, выбранный из группы, состоящей из LiN(CF3SO2)2, Mg(OCF3SO2)2, Al(OCF3SO2)3, Bi(OCF3SO2)3, Sc(OCF3SO2)3;
- реакционная смесь содержит разбавитель, выбранный из группы, состоящей из 1,4-диоксана, толуола, этилацетата, сульфолана, ацетонитрила, 1-этил-3-метил-имидазолий-бис(трифторметилсульфонил)имида или их смесей;
- эквивалентное отношение альфа-аминоалкиленкарбоновой кислоты к ангидридному фрагменту Р-О-Р составляет от 0,2 до 4,5, предпочтительно от 0,3 до 3,0, более предпочтительно от 0,3 до 2,5 и наиболее предпочтительно от 0,5 до 1,5;
- отношение эквивалентов альфа-аминоалкиленкарбоновой кислоты к молям тетрафосфорного гексаоксида составляет от 1,0 до 12,0, предпочтительно от 1,0 до 10,0, более предпочтительно от 1,5 до 8,0 и наиболее предпочтительно от 2,0 до 6,0;
- отношение молей кислотного катализатора к эквивалентам альфа-аминоалкиленкарбоновой кислоты составляет от 0,01 до 11,0, предпочтительно от 0,01 до 10,0, более предпочтительно от 0,1 до 9,0, еще более предпочтительно от 1,0 до 7,0 и наиболее предпочтительно от 2,0 до 5,0;
- соединение, содержащее ангидридный фрагмент Р-О-Р, смешивают со смесью альфа-аминоалкиленкарбоновой кислоты и кислотного катализатора при температуре, составляющей от 20°С до 120°С, предпочтительно от 20°С до 80°С;
- реакционную смесь после завершения смешивания выдерживают при температуре, составляющей от 20°С до 100°С, предпочтительно от 40°С до 90°С и более предпочтительно от 50°С до 80°, в течение периода времени, составляющего от 10 минут до 72 часов;
- реакционную смесь после завершения добавления соединения, содержащего ангидридный фрагмент Р-О-Р, выдерживают при температуре, составляющей от 20°С до 100°С, предпочтительно от 40°С до 90°С и более предпочтительно от 50°С до 80°, в течение периода времени, составляющего от 10 минут до 72 часов;
- полученная альфа-аминоалкиленфосфоновая кислота выбрана из группы, состоящей из аминометилфосфоновой кислоты, (N,N-диметиламино)метилфосфоновой кислоты, фталимидометилфосфоновой кислоты, N-фениламинометилфосфоновой кислоты, N-тозиламинометилфосфоновой кислоты, N-фосфонометилглицина, фосфонометилиминодиуксусной кислоты, 4-морфолинметилфосфоновой кислоты, 4-амино-4-фосфономасляной кислоты, 5-фосфоно-2-пирролидона, N,N-бис(фосфонометил)-6-аминокапроновой кислоты, N,N-бис(фосфонометил)-4-амино-4-фосфономасляной кислоты, N,N-бис(фосфонометил)-4-аминоглутаминовой кислоты, N,N-бис(фосфонометил)-1-аминоэтилфосфоновой кислоты, имино(бисметиленфосфоновой кислоты), N-метилимино(бисметиленфосфоновой кислоты), N-бензилимино(бисметиленфосфоновой кислоты), аминотрисметиленфосфоновой кислоты, этилендиаминотетра-(метиленфосфоновой кислоты), транс-1,2-циклогексилдиаминотетраметиленфосфоновой кислоты, 1,4,7,10-тетраазадодекан-1,4,7,10-тетраметиленфосфоновой кислоты, N-метилиминодифосфоновой кислоты;
- монооксид углерода, образовавшийся в результате реакции соединения, содержащего ангидридный фрагмент Р-О-Р, и альфа-аминоалкиленкарбоновой кислоты, выделяют и применяют повторно;
- альфа-аминоалкиленфосфоновую кислоту или ее сложные эфиры, полученные с помощью способа по настоящему изобретению, применяют в качестве ингибитора образования накипи, диспергирующего средства, комплексообразователя, моющей присадки, вспомогательного вещества, применяемого при бурении в ходе добычи нефти с морских промыслов, фармацевтического компонента, для ионообмена при прививке на органической или неорганической подложке, в качестве лигандов для иммобилизации гомогенных металлических катализаторов и в качестве гетерогенных кислотных катализаторов.
Подробное описание изобретения
[0017] Настоящее изобретение предлагает эффективный и экономичный способ синтеза альфа-аминоалкиленфосфоновой кислоты, или ее сложных фосфонатных эфиров, с высокой селективностью и высоким выходом, при этом сложные фосфонатные эфиры содержат одну или несколько замещенных или незамещенных гидрокарбильных групп, которые могут быть разветвленными или неразветвленными, насыщенными или ненасыщенными и могут содержать одно или несколько колец. Подходящие гидрокарбилы включают алкильные, алкенильные, алкинильные и арильные фрагменты. Они также включают алкильные, алкенильные, алкинильные и арильные фрагменты, замещенные другими алифатическими или циклическими гидрокарбильными группами, такими как алкарильная, алкенарильная и алкинарильная.
[0018] Замещенный гидрокарбил определяют как гидрокарбил, в котором по меньшей мере один атом водорода был замещен атомом, отличным от водорода, таким как атом галогена, атом кислорода с образованием, например, простого эфира или сложного эфира, атом азота с образованием амидной или нитрильной группы или атом серы с образованием, например, тиоэфирной группы. Сложные фосфонатные эфиры, в целом, получают с применением содержащего ангидридный фрагмент Р-О-Р соединения, замещенного соответствующими гидрокарбильными заместителями.
[0019] Настоящий способ включает группировку, благодаря чему осуществляют реакцию соединения, содержащего ангидридный фрагмент Р-О-Р с одним атомом Р со степенью окисления (+III) и другим атомом Р со степенью окисления (+III) или (+V), и альфа-аминоалкиленкарбоновой кислоты в присутствии кислотного катализатора и необязательного разбавителя.
[0020] Несмотря на то, что соединение, содержащее ангидридный фрагмент Р-О-Р, предпочтительно выбрано из группы, состоящей из тетрафосфорного гексаоксида и частично гидролизированных соединений тетрафосфорного гексаоксида, полученных в результате реакции 1 моля тетрафосфорного гексаоксида с 1, 2, 3, 4 и 5 молями воды, соответственно, понятно, что в контексте настоящего изобретения можно применять все соединения, содержащие по меньшей мере один ангидридный фрагмент Р-О-Р, где один атом Р имеет степень окисления (+III), а другой атом Р имеет степень окисления (+III) или (+V).
[0021] Подходящие содержащие ангидридный фрагмент Р-О-Р соединения могут либо содержать ангидридный фрагмент Р-О-Р в собственно соединении (например, P4O6 или пирофосфиты (RO)2P-O-P(OR)2), либо могут быть получены in situ посредством объединения реагентов, которые будут образовывать необходимый ангидридный фрагмент Р-О-Р, при объединении до реакции с альфа-аминоалкиленкарбоновой кислотой.
[0022] Подходящими комбинациями реагентов являются а) соединения, содержащие по меньшей мере один фрагмент Р-ОН (также поддающийся таутомеризации фрагмент >Р(=O)Н в >P(LP)OH (где LP представляет собой неподеленную пару электронов)), как это возможно для диметилфосфита (MeO)2Р(=O)Н), а также соединения, содержащие по меньшей мере один ангидридный фрагмент Р-О-Р, например, P2O5 или P4O6; и b) продукты частичного гидролиза соединения, содержащего ангидридные фрагменты Р-О-Р. В случае а) обязательным является то, чтобы по меньшей мере в одном из используемых соединений атом Р имел степень окисления (+III), в то время как в случае b) чтобы фрагменты Р-О-Р содержали один атом Р со степенью окисления (+III) и другой атом Р со степенью окисления (+III) или (+V) с целью образования соединения, содержащего ангидридный фрагмент Р-О-Р с одним атомом Р со степенью окисления (+III) и другим атомом Р со степенью окисления (+III) или (+V).
[0023] Содержащие ангидридный фрагмент Р-О-Р соединения, где ангидридный фрагмент Р-О-Р уже присутствует, представляют собой оксиды фосфора с формулой P4On с n=6-9, пирофосфиты с общей формулой (RO)2P-O-P(OR)2, где R представляет собой алкильную или арильную группу, пирофосфористую кислоту (H4P2O5) и изогипофосфорную кислоту (Н(НО)Р(O)-O-Р(O)(ОН)2).
[0024] Комбинации, описанные в а), получают посредством осуществления реакции, например, оксидов фосфора с формулой P4On с n=6-10; алкил-замещенных пирофосфитов, пирофосфористой кислоты, изогипофосфорной кислоты, метафосфорной кислоты или полифосфорной кислоты с фосфористой кислотой, фосфорной кислотой, моно- или дизамещенными фосфитами с формулой (RO)PO2H2 или (RO)2POH, где R представляет собой алкильную или арильную группу, фосфатными сложными эфирами (RO)PO3H2 или (RO)2PO2H, фосфоновыми кислотами или их сложным моноэфиром RPO3H2 или RPO2H(OR), при условии, что такие комбинации будут приводить к получению соединения, содержащего ангидридный фрагмент Р-О-Р с одним атомом Р со степенью окисления (+III) и другим атомом Р со степенью окисления (+III) или (+V).
[0025] Наиболее предпочтительными являются тетрафосфорный гексаоксид, тетраэтилпирофосфит и комбинации из фосфористой кислоты и тетрафосфорного гексаоксида, из фосфористой кислоты и тетрафосфорного декаоксида, из диметилфосфита и тетрафосфорного декаоксида и из тетрафосфорного гексаоксида и воды.
[0026] Количество 'реакционно-способных' атомов Р(+III), которые могут быть превращены в фосфоновые кислоты, согласно настоящему изобретению определяют по количеству атомов Р(+III) и количеству ангидридных фрагментов Р-О-Р. Если ангидридных фрагментов Р-О-Р больше, чем атомов Р(+III), то все атомы Р(+III) превращаются в фосфоновые кислоты. Если ангидридных фрагментов Р-О-Р меньше, чем атомов Р(+III), то только часть атомов Р(+III), эквивалентная количеству ангидридных фрагментов Р-О-Р, превращается в фосфоновые кислоты.
[0027] Тетрафосфорный гексаоксид, предпочтительно применяемый в объеме настоящего изобретения, может быть представлен практически чистым соединением, содержащим по меньшей мере 85%, предпочтительно более 90%, более предпочтительно по меньшей мере 95% и в одном конкретном варианте осуществления по меньшей мере 97% P4O6. Несмотря на то, что тетрафосфорный гексаоксид, подходящий для применения в контексте настоящего изобретения, может быть получен по любой известной технологии, в предпочтительных вариантах осуществления его получают согласно способу, описанному в патентных заявках WO 2009/068636 и/или WO 2010/055056 в разделе под названием "Способ получения P4O6 с улучшенным выходом" ("Process for the manufacture of P4O6 with improved yield"). Более подробно, проводят реакцию кислорода или смеси кислорода и инертного газа, а также газообразного или жидкого фосфора фактически в стехиометрических количествах в реакционном блоке при температуре в диапазоне от 1600 K до 2000 K с отводом тепла, образующегося при экзотермической реакции фосфора и кислорода, при поддержании предпочтительного времени пребывания от 0,5 секунды до 60 секунд с последующим гашением продукта реакции при температуре ниже 700 K и очисткой неочищенного продукта реакции посредством перегонки. Полученный таким образом тетрафосфорный гексаоксид представляет собой чистый продукт, обычно содержащий по меньшей мере 97% оксида. Полученный таким образом P4O6 обычно представлен в виде жидкого материала с высокой степенью чистоты, содержащего, в частности, низкие уровни элементарного фосфора, Р4, предпочтительно ниже 1000 ppm в пересчете на P4O6, составляющий 100%. Предпочтительное время пребывания составляет от 5 секунд до 30 секунд, более предпочтительно от 8 секунд до 30 секунд. Продукт реакции в одном предпочтительном варианте осуществления может быть охлажден до температуры ниже 350 K.
[0028] Предполагают, что P4O6, участвующий в реакции при температуре от 24°С (t° плавления) до 120°С, обязательно должен быть жидким или газообразным, несмотря на это, теоретически, для получения реакционной среды можно применять твердые вещества.
[0029] С целью удобства и оперативного знания, тетрафосфорный гексаоксид, представленный P4O6, является высокочистым и содержит очень низкие уровни примесей, в частности, элементарного фосфора, Р4, на уровне ниже 1000 ppm, обычно ниже 500 ppm и предпочтительно не более 200 ppm в пересчете на Р4O6, составляющий 100%.
[0030] Соединение, содержащее фрагмент альфа-аминоалкиленкарбоновой кислоты, применяемое в настоящем изобретении, может быть молекулой, полимером, смолой или органической молекулой или полимером, привитым на неорганический материал, и может быть представлено общей формулой:
R1-N(R2)-CR3R4-CO2M,
где R1 может представлять собой замещенный атом С или замещенный атом S; R2 может представлять собой атом Н, замещенный атом С или замещенный атом S; R3 и R4 независимо могут представлять собой атом Н или замещенный атом С; М может представлять собой атом Н или щелочной или щелочно-земельный металл.
[0031] Предпочтительно, соединение, содержащее фрагмент альфа-аминокарбоновой кислоты, может быть выбрано из:
a) соединения, где атом N обладает низкой основностью в результате замещения по атому N электроноакцепторными группами или группами, которые могут частично делокализовывать неподеленную пару у N; под низкой основностью в настоящем изобретении понимают альфа-аминоалкиленкарбоновую кислоту, в которой аминогруппа характеризуется pKb приблизительно 3,0 или более предпочтительно pKb 3,3 или более;
b) полиамина, у которого присутствуют по меньшей мере два атома N, и каждый атом N отделен по меньшей мере двумя атомами углерода от следующего соседнего атома N;
c) соединения, у которого атом N имеет в качестве заместителей алкильные группы.
[0032] Наиболее предпочтительными являются:
а) нитрилтрехуксусная кислота, этилендиаминтетрауксусная кислота, диэтилентриаминпентауксусная кислота, N-бензилиминодиуксусная кислота, N-метилиминодиуксусная кислота, иминодиуксусная кислота, N,N-бис(карбоксиметил)-1-глутаминовая кислота, тринатрия-N,N-бис(карбоксиметил)-аланин, N-цианометилаланин, N,N-бис(цианометил)-глицин, 4-морфолинуксусная кислота, пироглутаминовая кислота, N-ацетилглицин, N,N-бис(карбоксиметил)-6-аминокапроновая кислота, N-фенилглицин, N-тозилглицин, моногидрат транс-1,2-циклогексилдиаминотетрауксусной кислоты, N-фосфонометилиминодиуксусная кислота, иминодиуксусная кислота, привитая на смолу, такую как, например, подкисленная Amberlite IRC748i;
b) 1,4,7,10-тетраазадодекан-1,4,7,10-тетрауксусная кислота, моногидрат транс-1,2-циклогексилдиаминотетрауксусной кислоты;
c) N,N'-диметилглицин.
[0033] В способе по настоящему изобретению отдельные молекулы представляющих интерес альфа-аминоалкиленкарбоновых кислот могут включать, среди прочих, N,N-диметилглицин, N-фталоглицин, N-фенилглицин, N-тозилглицин, N-цианометилглицин, N,N-бисцианометилглицин, 4-морфолинуксусную кислоту, пироглутаминовую кислоту, N-ацетилглицин, N,N-бис(карбоксиметил)-6-аминокапроновую кислоту, N,N-бис(карбоксиметил)-1-глутаминовую кислоту, N-цианометилаланин, тринатрия N,N-бис(карбоксиметил)-аланин, иминодиуксусную кислоту, N-метил-иминодиуксусную кислоту, N-бензилиминодиуксусную кислоту, нитрилтрехуксусную кислоту, этилендиаминотетрауксусную кислоту, диэтилентриаминпентауксусную кислоту, N,N-бис(карбоксиметил)глицин, монокарбоксиметилсаркозин и смолы и полимеры, содержащие по меньшей мере один фрагмент альфа-аминоалкиленкарбоновой кислоты.
[0034] Применение нейтрализованных или частично нейтрализованных соединений, содержащих фрагмент альфа-аминокарбоновой кислоты, нуждается в дополнительном вспомогательном веществе с pKa, ниже чем соответствующее значение у группы альфа-аминокарбоновой кислоты, которую добавляют на начальном этапе реакции в количестве, по меньшей мере достаточном для превращения всех функциональных групп нейтрализованных или частично нейтрализованных карбоновых кислот в соответствующие функциональные группы свободных карбоновых кислот.
[0035] Кислотный катализатор, применяемый в объеме настоящего изобретения, предпочтительно представляет собой гомогенный катализатор на основе кислоты Бренстеда необязательно в присутствии растворителя, или гетерогенный катализатор на основе кислоты Бренстеда в присутствии растворителя, или катализатор на основе кислоты Льюиса в присутствии растворителя, или растворителя, являющегося катализатором на основе кислоты Бренстэда.
[0036] Гомогенный катализатор на основе кислоты Бренстеда предпочтительно выбирают из группы, состоящей из метансульфоновой кислоты, фторметансульфоновой кислоты, трихлорметансульфоновой кислоты, трифторметансульфоновой кислоты, уксусной кислоты, трифторуксусной кислоты, трет-бутилсульфоновой кислоты, п-толуолсульфоновой кислоты, нафталинсульфоновой кислоты, 2,4,6-триметилбензолсульфоновой кислоты, перфтор- или перхлорсульфоновых кислот, перфтор- или перхлоркарбоновых кислот, хлористоводородной кислоты, бромистоводородной кислоты, йодистоводородной кислоты, фосфористой кислоты, фосфорной кислоты и их смесей.
[0037] В конкретном варианте осуществления настоящего изобретения катализатор на основе кислоты Бренстеда ведет себя как катализатор и как растворитель.
[0038] Гетерогенный катализатор на основе кислоты Бренстеда предпочтительно выбирают из группы из:
(i) комбинаций твердых кислотных оксидов металлов как таковых или на подложке из материала-носителя;
(ii) катионообменных смол, выбранных из группы, включающей сополимеры стирола, этилвинилбензола и дивинилбензола, функционализированных таким образом, что обеспечивается прививка фрагментов SO3H на ароматическую группу и перфорированные смолы, несущие группы карбоновой и/или сульфоновой кислоты;
(iii) органических сульфоновых, карбоновых и фосфоновых кислот Бренстеда, (которые являются практически несмешиваемыми в реакционной среде при температуре реакции);
(iv) кислотного катализатора, полученного:
- в результате взаимодействия твердой подложки, содержащей неподеленную пару электронов, на которую осаждается органическая кислота Бренстеда; или
- в результате взаимодействия твердой подложки, содержащей неподеленную пару электронов, на которую осаждается соединение, содержащее Льюисовские кислотные центры; или
- из гетерогенных твердых веществ, функционализированных посредством химической прививки группы кислоты Бренстеда или ее предшественника; и
(v) гетерогенных гетерополикислот общей формулы HxPMyOz, где Р выбран из фосфора и кремния, а М выбран из вольфрама и молибдена и их комбинаций.
[0039] Гетерогенный катализатор на основе кислоты Бренстеда для применения в способе настоящего изобретения предпочтительно выбирают из группы, состоящей из макромолекулярных полимерных смол, имеющих непрерывную открытопористую структуру и содержащих фрагменты сульфоновой, карбоновой и/или фосфоновой кислоты.
[0040] Гетерогенный катализатор на основе кислоты Бренстеда является практически нерастворимым или несмешиваемым в реакционной среде. Катализатор может формировать, в реакционных условиях, в частности при температуре реакции, вторую жидкую фазу и может быть выделен в конце реакции с помощью традиционных методик, таких как фильтрация или разделение фаз.
[0041] Гомогенные катализаторы на основе кислоты могут оставлять осадок в конечном продукте реакции. Тем не менее, известны методики выделения кислотного катализатора из реакционной среды, такие как ионообмен, нанофильтрация или электродиализ, которые можно применять для устранения или уменьшения таких проблем. Альтернативно, конечный продукт можно отделить, например, осаждением с применением вспомогательного растворителя, а катализатор на основе кислоты Бренстеда выделить и повторно применять после удаления вспомогательного растворителя.
[0042] Кислота Льюиса, будучи включенной в растворитель, обычно является гомогенной или гетерогенной кислотой Льюиса.
[0043] Растворители на основе кислоты Бренстеда можно заменить кислотами Льюиса, растворенными или суспендированными в органическом растворителе.
[0044] Предпочтительные гомогенные кислоты Льюиса могут быть выбраны из солей металлов с общей формулой:
MXn,
где М представляет собой элемент основной группы или переходный металл, такой как Li, В, Mg, Al, Bi, Fe, Zn, La, Sc, Yb или Pd; X в MXn, как правило, представляет собой анион кислоты или производное кислоты, такие как Cl, OTf или NTf2, где Tf представляет собой CF3SO2, и n равняется степени окисления М, которая может составлять от 1 до 5. Например, возможными комбинациями являются LiNTf2, Mg(OTf)2, MgCl2, ZnCl2, PdCl2, Fe(OTf)3, Al(OTf)3, AlCl3, Bi(OTf)3, BiCl3, Sc(OTf)3, Ln(OTf)3, Yb(OTf)3. Предпочтительно применяют комбинации жесткого металла или металла на границе между жестким и мягким согласно принципа HSAB (жестких и мягких кислот и оснований), такого как Li, Mg, Al, Sc, Zn, Bi, и слабо координирующих анионов, таких как OTf или NTf2. Примерами таких предпочтительных комбинаций являются: LiNTf2, Mg(OTf)2, Al(OTf)3, Bi(OTf)3. Предпочтительные гетерогенные кислоты Льюиса могут быть представлены веществами из дискретно выбранных подклассов, образованными при взаимодействии/связывании гомогенных кислот Льюиса, например, комплексных соединений металлов, солей металлов или металлорганических веществ, с полимерными органическими или неорганическими главными цепями. Пример такого подкласса представляет собой полистироловую матрицу со связанными группами Sc(OTf)2. Такой катализатор может быть получен, например, посредством взаимодействия смолы на основе полистиролсульфоновой кислоты, например, Amberlyst 15, с Sc(OTf)3. Число эквивалентов функциональных групп кислоты Льюиса может быть определено в данном случае различными способами, например, посредством кислотно-основного определения непрореагировавших групп сульфоновой кислоты, посредством количественного определения высвобожденной трифторметансульфоновой кислоты, а также посредством измерения с применением ICP количества Sc в смоле.
[0045] Типичными примерами подходящих органических растворителей являются анизол; хлорсодержащие или фторсодержащие углеводороды, такие как хлорбензол, фторбензол, тетрахлорэтан, тетрахлорэтилен, дихлорэтан, дихлорметан; полярные растворители, такие как диглим, глим, дифенилоксид, производные полиалкиленгликоля с защищенными ОН-группами, такими как OR***, где R*** представляет собой низшую алкильную или ацильную группу; алифатические углеводороды, такие как гексан, гептан, циклогексан; ациклические эфиры, такие как дибутиловый эфир, диэтиловый эфир, диизопропиловый эфир, дипентиловый эфир и бутилметиловый эфир; циклические эфиры, такие как тетрагидрофуран, диоксан и тетрагидропиран; смешанные циклические/ациклические эфиры, такие как циклопентилметиловый эфир; циклические и ациклические сульфоны, такие как сульфолан; ароматические растворители, такие как толуол, бензол, ксилол; органические ацетаты, такие как этилацетат; органические нитрилы, такие как ацетонитрил, бензонитрил; жидкости на основе кремния, такие как полиметилфенилсилоксан или его смеси; нереакционно-способные ионогенные жидкости, такие как 1-н-бутил-имидазолий-трифторметансульфонат и 1-этил-3-метил-имидазолий-бис(трифторметилсульфонил)имид; или их смеси.
[0046] Способ по настоящему изобретению начинают путем смешивания альфа-аминоалкиленкарбоновой кислоты, необязательных разбавителей и кислотного катализатора.
Необязательно, альфа-аминоалкиленкарбоновую кислоту или смесь альфа-аминоалкиленкарбоновой кислоты и необязательных разбавителей охлаждают до температуры ниже температуры окружающей среды, предпочтительно до температуры ниже приблизительно 10°С перед добавлением кислотного катализатора, предпочтительно катализатора на основе кислоты Бренстеда.
[0047] Способ по настоящему изобретению включает стадию получения реакционной смеси путем постепенного перемешивания соединения, содержащего ангидридный фрагмент Р-О-Р с одним атомом Р со степенью окисления (+III) и другим атомом Р со степенью окисления (+III) или (+V), предпочтительно тетрафосфорный гексаоксид, и смеси, содержащей аминоалканкарбоновую кислоту, кислотный катализатор, предпочтительно катализатор на основе кислоты Бренстеда или растворитель, являющийся катализатором на основе кислоты Бренстеда, и необязательно разбавитель, придерживаясь соответствующей температуры (предпочтительно составляющей от приблизительно 20°С до приблизительно 120°С), и выдерживания данной реакционной смеси при соответствующей температуре (предпочтительно при температуре, составляющей от приблизительно 20°С до приблизительно 100°С) в течение соответствующего периода, предпочтительно в течение по меньшей мере 10 минут, после завершения процесса перемешивания.
[0048] В конкретном варианте осуществления настоящего изобретения способ включает стадию получения реакционной смеси путем постепенного добавления соединения, содержащего ангидридный фрагмент Р-О-Р с одним атомом Р со степенью окисления (+III) и другим атомом Р со степенью окисления (+III) или (+V), предпочтительно тетрафосфорный гексаоксид, к смеси, содержащей аминоалканкарбоновую кислоту, кислотный катализатор, предпочтительно катализатор на основе кислоты Бренстеда или растворитель, являющийся катализатором на основе кислоты Бренстеда, и необязательно разбавитель, придерживаясь соответствующей температуры (предпочтительно составляющей от приблизительно 20°С до приблизительно 120°С), и выдерживания данной реакционной смеси при соответствующей температуре (предпочтительно при температуре, составляющей от приблизительно 20°С до приблизительно 100°С) в течение соответствующего периода, предпочтительно в течение по меньшей мере 10 минут, после завершения процесса перемешивания.
[0049] В другом варианте осуществления настоящего изобретения способ включает стадию получения реакционной смеси путем постепенного добавления смеси, содержащей аминоалканкарбоновую кислоту, кислотный катализатор, предпочтительно катализатор на основе кислоты Бренстеда или растворитель, являющийся катализатором на основе кислоты Бренстеда, и необязательно разбавителя, придерживаясь соответствующей температуры (предпочтительно составляющей от приблизительно 20°С до приблизительно 120°С), к соединению, содержащему ангидридный фрагмент Р-О-Р с одним атомом Р со степенью окисления (+III) и другим атомом Р со степенью окисления (+III) или (+V), предпочтительно тетрафосфорному гексаоксиду, и выдерживания данной реакционной смеси при соответствующей температуре (предпочтительно при температуре, составляющей от приблизительно 20°С до приблизительно 100°С) в течение соответствующего периода, предпочтительно в течение по меньшей мере 10 минут, после завершения процесса перемешивания.
[0050] Отношение молей кислотного катализатора к эквивалентам альфа-аминоалкиленкарбоновой кислоты составляет от приблизительно 0,01 до приблизительно 11,0, предпочтительно от приблизительно 0,1 до приблизительно 9,0, более предпочтительно от приблизительно 1,0 до приблизительно 7.0 и наиболее предпочтительно от приблизительно 2 до приблизительно 5.
[0051] В соответствии с настоящим изобретением смесь альфа-аминоалкиленкарбоновой кислоты и кислотного катализатора, необязательно содержащую разбавитель(разбавители), затем доводят до температуры, составляющей от приблизительно 20°С до приблизительно 120°С и предпочтительно от приблизительно 20°С до приблизительно 80°С.
[0052] К смеси, придерживаясь температуры, составляющей от приблизительно 20°С до приблизительно 120°С и предпочтительно от приблизительно 20°С до приблизительно 80°С, медленно при помешивании добавляют соединение, содержащее ангидридный фрагмент Р-О-Р, таким образом, чтобы температура реакционной смеси не превышала предварительно установленное значение максимальной температуры.
[0053] В способе по настоящему изобретению эквивалентное отношение альфа-аминоалкиленкарбоновой кислоты к ангидридному фрагменту Р-О-Р составляет от приблизительно 0,2 до приблизительно 4,5, предпочтительно от приблизительно 0,3 до приблизительно 3,0 и более предпочтительно от приблизительно 0,5 до приблизительно 1,5.
[0054] Отношение эквивалентов альфа-аминоалкиленкарбоновой кислоты к молям тетрафосфорного гексаоксида составляет от приблизительно 1,0 до приблизительно 12,0, предпочтительно от приблизительно 1,5 до приблизительно 8,0 и более предпочтительно от приблизительно 2,0 до приблизительно 6,0.
[0055] После завершения процесса перемешивания соединения, содержащего ангидридный фрагмент Р-О-Р, и альфа-аминоалкиленкарбоновой кислоты реакционную смесь сохраняют при температуре процесса перемешивания или нагревают или охлаждают до температуры, составляющей от приблизительно 20°С до приблизительно 100°С, предпочтительно от приблизительно 40°С до приблизительно 90°С и более предпочтительно от приблизительно 50°С до приблизительно 80°С и выдерживают при такой температуре в течение периода времени, составляющего от приблизительно 10 минут до приблизительно 72 часов, предпочтительно от приблизительно 30 минут до приблизительно 48 часов, более предпочтительно от приблизительно 1 часа до приблизительно 24 часов и наиболее предпочтительно от приблизительно 2 часов до приблизительно 10 часов для содействия превращению альфа-аминоалкиленкарбоновой кислоты в альфа-аминоалкиленфосфоновую кислоту (т.е. замены группы карбоновой кислоты на группу фосфоновой кислоты).
[0056] В ходе реакции соединения, содержащего ангидридный фрагмент Р-О-Р, с альфа-аминоалкиленкарбоновой кислотой, монооксид углерода и фрагмент Р-С образуются в эквимолярных отношениях. В ходе превращения соединения, содержащего фрагмент альфа-аминокарбоновой кислоты, один эквивалент СО будет образовываться на каждый превращенный эквивалент фрагмента альфа-аминокарбоновой кислоты. СО будет покидать реакционную смесь в виде газа с очень высокой степенью чистоты. Этот газообразный СО можно использовать во многих областях применения, таких как, например, топливо, в сочетании с водородом для получения метанола и углеводородов в ходе синтеза Фишера-Тропша, для реакций гидроформилирования, для карбонилирования спиртов, например, карбонилирования метанола до уксусной кислоты или превращения метилацетата в уксусный ангидрид.
[0057] После завершения превращения альфа-аминоалкиленкарбоновой кислоты в альфа-аминоалкиленфосфоновую кислоту, ее дегидратированные формы или их сложные фосфонатные эфиры в реакционную смесь необязательно добавляют воду для превращения дегидратированных форм альфа-аминоалкиленфосфоновой кислоты или их сложных фосфонатных эфиров в альфа-аминоалкиленфосфоновую кислоту или ее сложные фосфонатные эфиры и для гидролиза непрореагировавших ангидридных фрагментов Р-О-Р, при наличии таковых.
[0058] Предпочтительно, воду в реакционную смесь добавляют после ее охлаждения до комнатной температуры. Альтернативно, реакционную смесь можно охладить путем добавления воды. Такой гидролиз проводят при температуре, составляющей от комнатной температуры до приблизительно 100°С, в течение периода, составляющего от приблизительно 10 минут до приблизительно 48 часов и предпочтительно от приблизительно 1 часа до приблизительно 24 часов.
[0059] Непрореагировавшие ангидридные фрагменты Р-О-Р могут быть результатом неполного превращения или нестехиометрического количества соединений, содержащих ангидридную группу Р-О-Р, составляющих реакционную смесь.
[0060] В случае практически полного превращения и стехиометрической загрузки реактивов добавление воды и, следовательно, стадию гидролиза, можно опустить.
[0061] Выход в результате превращения альфа-аминоалкиленкарбоновой кислоты в альфа-аминоалкиленфосфоновую кислоту, в соответствии со способом по настоящему изобретению, предпочтительно составляет по меньшей мере приблизительно 50%, преимущественно по меньшей мере приблизительно 80%, еще более преимущественно по меньшей мере приблизительно 95%.
Примеры
[0062] Настоящее изобретение будет подробно описано в приведенных далее примерах, которые иллюстрируют настоящее изобретение. Они предназначены только для иллюстрации настоящего изобретения, но не предназначены для ограничения объема настоящего изобретения.
Пример 1.
[0063] В круглодонной колбе, оснащенной механической мешалкой, термометром и холодильником, 7,26 г (60 ммоль) 4-морфолинуксусной кислоты перемешивали с 22 мл (249 ммолями) трифторметансульфоновой кислоты. К смеси, придерживаясь комнатной температуры, медленно при помешивании добавляли 5,50 г (25 ммоль) тетрафосфорного гексаоксида. После завершения добавления тетрафосфорного гексаоксида реакционную смесь нагревали до 70°С и помешивали в течение 7 часов при 70°С. В ходе добавления тетрафосфорного гексаоксида и последующего 7-часового периода прохождения реакции наблюдали образование монооксида углерода. Затем к реакционной смеси добавляли 20 мл воды. Полученный таким образом раствор анализировали с помощью1H-NMR и31P-NMR спектроскопии. Выявляли 94,7 вес. % 4-морфолинометилфосфоновой кислоты.
Пример 2.
[0064] В круглодонной колбе, оснащенной механической мешалкой, термометром и холодильником, 15,7 г (82 ммоля) нитрилацетилацетоуксусной кислоты перемешивали с 49,8 мл (767 ммолями) метансульфоновой кислоты. Смесь нагревали до 75°С и медленно при помешивании добавляли 13,4 г (61 ммоль) тетрафосфорного гексаоксида. После завершения добавления тетрафосфорного гексаоксида реакционную смесь помешивали в течение 30 минут при 75°С. В ходе добавления тетрафосфорного гексаоксида и последующего 30-минутного периода прохождения реакции наблюдали образование монооксида углерода. Затем к реакционной смеси добавляли 20 мл воды. Полученный таким образом раствор анализировали с помощью31P-NMR спектроскопии. Выявляли 95,6 вес. % аминотрисметиленфосфоновой кислоты.
Пример 3.
[0065] В круглодонной колбе, оснащенной механической мешалкой, термометром и холодильником, 10,00 г (65,4 ммоля) N,N-бисцианометилглицина перемешивали с 50 мл ацетонитрила и 12,7 мл (196 ммолями) метансульфоновой кислоты. К смеси, придерживаясь комнатной температуры, медленно при помешивании добавляли 3,60 г (16,3 ммоля) тетрафосфорного гексаоксида. После завершения добавления тетрафосфорного гексаоксида реакционную смесь помешивали в течение 5 часов при 40°С, а затем в течение 16 часов при температуре окружающей среды. Ацетонитрил затем отгоняли, а остаток растворяли в 50 мл воды. Раствор, содержащий остаток и воду, нагревали до 90°С и помешивали в течение 7 часов при 90°С. Полученный таким образом раствор охлаждали до температуры окружающей среды, при которой образовывалось 12,67 г осадка. Осадок выделяли посредством фильтрации. Твердое вещество и фильтрат анализировали с помощью1H-NMR и31P-NMR спектроскопии. Твердое вещество на 97,3 вес. % состояло из N,N-фосфонометилиминодиуксусной кислоты.
Пример 4.
[0066] Amberlite IRC 748 представляет собой катион-обменную смолу, состоящую из макропористой стиролдивинилбензольной матрицы с привитыми фрагментами иминодиуксусной кислоты.
[0067] В колонку помещали 23,4 г Amberlite IRC 748i (в Na+ форме) и медленно пропускали через колонку 0,1 М водный раствор HCl.
Несколько раз проверяли pH фильтрата до тех пор, пока не наблюдали pH, равный 2 (через примерно 200 мл). Колонку опустошали, а гранулы промывали 100 мл 1,4-диоксана и 200 мл простого диэтилового эфира. Затем гранулы сушили в печи в течение 4 часов при 50°С и в осушителе над Р205 в течение ночи.
[0068] В круглодонной колбе, оснащенной механической мешалкой, термометром и холодильником, 2,00 г (21,6 ммоля функциональных групп COOH) протонированной формы подкисленной Amberlite IRC748i (подготовленной, как описано выше) перемешивали с 5,6 мл метансульфоновой кислоты. После этого реакционную смесь нагревали до 85°С и добавляли 1,19 г (5,4 ммоля) P4O6. Реакционную смесь помешивали в течение 6 часов при 85°С. В ходе добавления и во время реакции наблюдали образование CO. После этого реакционную смесь охлаждали до 25°С и медленно добавляли 30 мл H2O. Гранулы отфильтровывали, и дважды промывали 100 мл H2O, и выдерживали в осушителе над P2O5 в течение ночи. Гранулы анализировали с помощью FTIR-спектроскопии. Полосы, соответствовавшие функциональным группам СООН, полностью исчезали, в то же время появлялись новые полосы в областях, характерных для растягивания Р=O групп у фосфонатов.
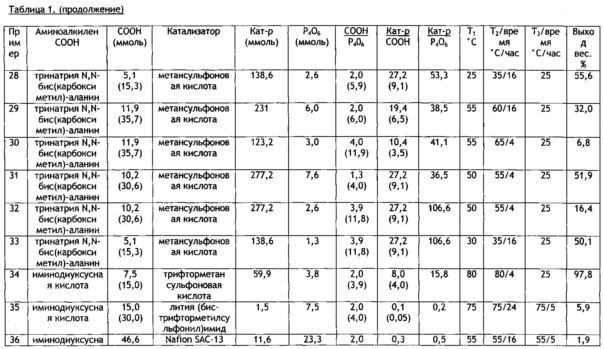
[0069] В таблице 1 изложен ряд примеров по настоящему изобретению.
В данной таблице:
в столбце 1: указан идентификационный номер примера;
в столбце 2: указан тип альфа-аминоалкиленкарбоновой кислоты, вводимой в реакцию с тетрафосфорным гексаоксидом;
в столбце 3: указано количество ммолей альфа-аминоалкиленкарбоновой кислоты с приведенным в скобках количеством миллиэквивалентов карбоновой кислоты;
в столбце 4: указан тип катализатора;
в столбце 5: указано количество ммолей катализатора;
в столбце 6: указано количество ммолей тетрафосфорного гексаоксида или реакционно-способных атомов 'P(+III)';
в столбце 7: указано отношение ммолей альфа-аминоалкиленкарбоновой кислоты к ммолям тетрафосфорного гексаоксида или реакционно-способных атомов 'Р(+III)' с указанным в скобках отношением миллиэквивалентов карбоновой кислоты в виде α-аминоалкиленкарбоновой кислоты к ммолям тетрафосфорного гексаоксида или реакционно-способных атомов 'Р(+III)';
в столбце 8: указано отношение ммолей катализатора к ммолям альфа-аминоалкиленкарбоновой кислоты с указанным в скобках отношением ммолей катализатора к миллиэквивалентам карбоновой кислоты в виде альфа-аминоалкиленкарбоновой кислоты;
в столбце 9: указано отношение ммолей катализатора к ммолям тетрафосфорного гексаоксида или реакционно-способных атомов 'Р(+III)'
в столбце 10: указана температура (°С) смеси, содержащей α-аминоалкиленкарбоновую кислоту и катализатор, к которой добавляют тетрафосфорный гексаоксид или реакционно-способные атомы 'P(+III)'; данную температуру поддерживали в ходе всего добавления тетрафосфорного гексаоксида или реакционно-способных атомов 'Р(+III)';
в столбце 11: указаны температурные (°С) и временные (часы) условия для реакционной
смеси после завершения добавления тетрафосфорного гексаоксида или реакционно-способных атомов 'Р(+III)';
в столбце 12: указаны температурные (°С) и временные (часы) условия для реакционной
смеси, содержавшей воду, для гидролиза дегидратированных форм α-аминоалкиленфосфоновой кислоты или их сложных фосфонатных эфиров и непрореагировавшего тетрафосфорного гексаоксида или реакционно-способных атомов 'Р(+III)';
в столбце 13: указан выход реакции в вес. % по результатам измерения с помощью1H-NMR и31P-NMR спектроскопии.
[0070] Альфа-аминоалкиленфосфоновыми кислотами, полученными в примерах из таблицы 1, являются:
пример 5: (N,N-диметиламино)метилфосфоновая кислота;
пример 6 и 7: 4-морфолинометилфосфоновая кислота;
пример 8-10: N,N-бис(фосфонометил)-6-амино-капроновая кислота;
пример 11: фталимидометилфосфоновая кислота;
пример 12: N-фениламинометилфосфоновая кислота;
пример 36: N-тозиламинометилфосфоновая кислота;
пример 14: аминометилфосфоновая кислота;
пример 15-18: 5-фосфоно-2-пирролидон и 4-амино-4-фосфономасляная кислота;
пример 19: этилендиаминтетраметиленфосфоновая кислота;
пример 20: диэтилентриаминопентаметиленфосфоновая кислота;
пример 21-26: N,N-бис(фосфонометил)-4-амино-4-фосфономасляная кислота;
пример 27: N-бензилиминобисметиленфосфоновая кислота;
пример 28-33: N,N-бис(фосфонометил)-1-аминоэтилфосфоновая кислота;
пример 34-36: имино(бисметиленфосфоновая кислота);
пример 37: N-метилимино(бисметиленфосфоновая кислота);
пример 38-41: N-фосфонометилглицин;
пример 42-46: фосфонометилиминодиуксусная кислота;
пример 47-58, и 63, и 65-67: аминотрисметиленфосфоновая кислота;
пример 59: N-фосфонометилглицин;
пример 60: привитые группы иминодифосфоновой кислоты на макропористой стиролдивинилбензоловой матрице;
пример 61: транс-1,2-циклогексилдиаминотетраметиленфосфоновая кислота;
пример 62: 1,4,7,10-тетраазадодекан-1,4,7,10-тетраметиленфосфоновая кислота;
пример 64: N-метил-иминодифосфоновая кислота.















Реферат
Изобретение относится к способу синтеза альфа-аминоалкиленфосфоновой кислоты или ее сложного эфира, применяемых, например, для обработки воды, замедления процесса образования накипи, моющих присадок, комплексообразователей. Способ включает следующие стадии: а) получение реакционной смеси путем смешивания соединения, содержащего один или несколько ангидридных фрагментов Р-О-Р, причем указанные фрагменты содержат один атом Р со степенью окисления (+III) и другой атом Р со степенью окисления (+III) или (+V), альфа-аминоалкиленкарбоновой кислоты и кислотного катализатора, где указанное соединение, содержащее один или несколько ангидридных фрагментов Р-О-Р, которые содержат один атом Р в степени окисления (+III) и другой атом Р в степени окисления (+III) или (+V), выбирают из группы, состоящей из: тетрафосфорного гексаоксида, PO, PO, РО, тетрафосфорного декаоксида, тетраэтилпирофосфита, диметилфосфита и их комбинаций, и где указанная альфа-аминоалкиленкарбоновая кислота выбрана из группы, состоящей из: нитрилтрехуксусной кислоты, этилендиаминтетрауксусной кислоты, диэтилентриаминпентауксусной кислоты, N-бензилиминодиуксусной кислоты, N-метилиминодиуксусной кислоты, иминодиуксусной кислоты, N,N-бис(карбоксиметил)-1-глутаминовой кислоты, тринатрия-N,N-бис(карбоксиметил)-аланина, N-цианометилаланина, N,N-бис(цианометил)-глицина, 4-морфолинуксусной кислоты, пироглутаминовой кислоты, N-ацетилглицина, N,N-бис(карбоксиметил)-6-аминокапроновой кислоты, N-фенилглицина, N-тозилглицина, моногидрата транс-1,2-циклогексилдиаминотетрауксусной кислоты, N-фосфонометилиминодиуксусной кислоты, иминодиуксусной кислоты, привитой на смолу, такую как, например, подкисленная Amberlite IRC748i, 1,4,7,10-тетраазадодекан-1,4,7,10-тетрауксусной кислоты, моногидрата транс-1,2-циклогексилдиаминотетрауксусной кислоты и N,N'-диметилглицина; b) добавление воды в реакционную смесь после завершения превращения альфа-аминоалкиленкарбоновой кислоты в альфа-аминоалкиленфосфоновую кислоту, и с) выделение из указанной реакционной смеси полученного соединения альфа-аминоалкиленфосфоновой кислоты или ее сложного эфира. Предлагаемый способ позволяет получить целевой продукт с высокой селективностью, чистотой и выходом. 30 з.п. ф-лы, 1 табл., 4 пр.

Комментарии