Способ синтеза аминоалкиленфосфоновой кислоты - RU2694047C2
Код документа: RU2694047C2
Описание
Область техники, к которой относится изобретение
[0001] Настоящее изобретение относится к способу синтеза соединений, содержащих фрагменты альфа-аминоалкиленфосфоновой кислоты, или их сложных фосфонатных эфиров.
Уровень техники
[0002] Соединения аминоалкиленфосфоновой кислоты хорошо известны из уровня техники и нашли широкое промышленное применение для ряда областей применения, в том числе в качестве фитотоксиканта, средства для обработки воды, замедления процесса образования накипи, моющих присадок, комплексообразователей, вспомогательных веществ, применяемых при бурении в ходе добычи нефти с морских промыслов и в качестве фармацевтических компонентов. Хорошо известно, что в таких областях применения предпочтительно необходимы аминоалкиленфосфоновые кислоты, в которых основная часть заместителей по азоту представляет собой группы алкиленфосфоновой кислоты.
[0003] В патенте ЕР 0595598 раскрывают способ получения N-(фосфонометил)иминоацетоуксусной кислоты, при котором осуществляют реакцию растворов солей щелочного металла и иминоацетоуксусной кислоты с формальдегидом с целью образования соли щелочного металла и гидроксиметилиминоацетоуксусной кислоты, которая затем может реагировать с источником фосфора, таким как фосфористая кислота, с получением N-фосфонометил-иминоацетоуксусной кислоты с хорошим выходом.
[0004] В патенте RO 101476 раскрывают способ получения диалкил-N,N,-бис-(2-гидроксиэтил)-аминометилфосфоната из диэтиламина, параформальдегида и диалкилфосфита в виде 23-24 вес. % раствора в толуоле в присутствии катализатора на основе ледяной уксусной кислоты.
[0005] В патентной заявке WO 94/22880 раскрывают способ получения аминометанфосфоновой кислоты, включающий а) осуществление реакции соединения формулы, R-CH2-NH-CO-NH-CH2-R', где R и R', представляет собой галоген, гидроксил, группы С1-С4алкокси, арилокси и С1-C4алкилового сложного эфира, с фосфонирующим средством, выбранным из трихлорида фосфора, фосфористой кислоты и диалкилфосфита, а затем b) проведение гидролиза продукта со стадии а) с образованием аминометанфосфоновой кислоты. Смесь фосфонирующих средств может применяться при необходимости. Предпочтительные фосфонирующие средства представляют собой трихлорид фосфора, диалкил-хлорфосфинат или смесь трихлорида фосфора и спирта. Безводный растворитель может применяться с фосфонирующим средством.
[0006] В патенте ЕР 0537786 раскрывают способ получения N-ациламинометилфосфоновой кислоты из N-метилоламидного соединения и тригалогенида фосфора. Исходные соединения смешивают и нагревают в апротонном растворителе в присутствии воды при 0,25-2,5 кратном молярном количестве относительно тригалогенида фосфора при температуре 60-160°С. N-метилоламидное соединение представляет собой соединение, выбранное из группы, состоящей из N-метилол-низший-алкиламидов и N-метилолариламидов. Тригалогенид фосфора предпочтительно представляет собой трихлорид фосфора. Апротонный растворитель выбирают из числа углеводородов, галогенированных углеводородов, эфиров, полиэфиров, нитрилов и ароматических нитросоединений. Смешивание могут осуществлять при температуре 60°С. Одним из наиболее важных требований в способе является добавление предварительно определенного количества воды к смеси исходных соединений (N-метилоламида и тригалогенида фосфора) при инициации реакции.
[0007] В патенте ЕР 480307 раскрывают способ получения ациламинометанфосфоновых кислот, которые представляют собой полезные промежуточные соединения для получения гербицида N-(фосфонометил)глицина и его солей. Ациламинометанфосфоновые кислоты формулы R1-CO-NH-CH2-PO3H2, в которой R1 представляет собой Н, С1-С6-алкил, бензил или необязательно замещенный фенил, могут быть получены промышленным способом, который включает осуществление реакции соединения формулы R1-CO-NH-CH2-OH с P2O3 и его гидролиз водой. При необходимости может применяться растворитель, такой как уксусная кислота, ацетонитрил, тетрагидрофуран и диоксан. Молярное отношение N-гидроксиметилацетамида к P2O3 предпочтительно составляет 2:1. Компоненты смешивают в температурном диапазоне от 5°С до 60°С; последовательность добавления компонентов не имеет решающего значения. После этого реакционную смесь нагревают до температуры, составляющей от 60°С до 200°С. После завершения реакции обеспечивают охлаждение смеси и ее обрабатывают водой. Для ускорения гидролиза может быть целесообразным повышение температуры, например, до температуры флегмы.
[0008] В патентной заявке ЕР 2112156 раскрыт способ получения аминоалкиленфосфоновой кислоты, включающий стадии добавления гексаоксида тетрафосфора в водную реакционную среду, содержащую, гомогенную кислоту Бренстеда, в результате чего гексаоксид тетрафосфора будет практически качественно гидролизоваться до фосфористой кислоты, в результате чего уровень свободной воды в реакционной среде, после завершения гидролиза гексаоксида тетрафосфора, будет находиться в диапазоне от 0 до 40% по весу. На последующей стадии амин, формальдегид и дополнительную кислоту Бренстеда добавляют в реакционную среду, после чего реакцию завершают с получением таким образом аминоалкиленфосфоновой кислоты. В варианте данного способа амин можно добавлять перед или во время стадии гидролиза гексаоксида тетрафосфора.
[0009] В патенте DE 4026026 раскрывают способ получения ациламинометанфосфоновой кислоты формулы R2-CO-NH-CH2-P(O)(OH)R1, где R1 представляет собой гидрокси, С1-С4алкил или фенил, а R2 представляет собой С1-С6алкил, бензил или фенил, которая может быть замещена одним или несколькими остатками, выбранными из группы, состоящей из С1-С4алкила, С1-С4алкокси и галогена. Такие молекулы представляют собой полезные промежуточные продукты при получении биологически активных соединений. Они могут быть получены посредством осуществления реакции соединения формулы R2-CO-NH-CH2-OH с соединениями формулы H-P(O)(OH)R1 в присутствии по меньшей мере эквимолярных количеств, в отношении соединения формулы R2-CO-NH-CH2-OH, уксусного ангидрида.
[0010] В патенте US 4422982 раскрывают способ получения N-(фосфонометил)глицина, который включает стадии (а) осуществления реакции формальдегида с формамидом при pH 9-10 с образованием N-(гидроксиметил)формамида, (b) осуществления реакции N-(гидроксиметил)формамида с триэтилфосфитом при молярном отношении 1/1, при температуре примерно 120°С-125°С в течение периода времени в диапазоне от 2 до 3 часов с образованием диэтил-N-(формил)аминометилфосфоната и этанола, (с) осуществления реакции диэтил-N-(формил)аминометилфосфоната с метилхлорацетатом в присутствии отнимающего протон основания (предпочтительно гидрида натрия) и подходящего растворителя (предпочтительно тетрагидрофурана) с образованием N-(диэтилфосфонометил)-N-(формил)глицинметилового сложного эфира и (d) осуществления реакции N-(диэтилфосфонометил)-N-(формил)глицинметилового сложного эфира с хлористоводородной кислотой с образованием N-(фосфонометил) глицина.
[0011] В патенте US 4804499 раскрывают способ получения N-замещенной аминометилфосфоновой кислоты, включающий осуществление реакции соединения на основе 2,5-дикетопиперазина с фосфористой кислотой и формальдегидом в кислой среде.
[0012] В патенте US 4400330 раскрывают способ получения N-фосфонометилглицина, который включает стадии первого осуществления реакции 2,5-дикетопиперазина с параформальдегидом в ледяной уксусной кислоте, затем добавления галоген-замещенного фосфорсодержащего соединения, все в присутствии растворителя на основе низкомолекулярной карбоновой кислоты, с образованием промежуточного соединения N,N'-бисфосфонометил-2,5-дикетопиперазина.
[0013] Синтез (2S*,3aS*,7aS*)-октагидроиндол-2-фосфоновой кислоты, исходя из цис-октагидроиндол-2-она, раскрыт в Arizpe et al., Eur. J. Org. Chem. 2011, 3074-3081. Затем осуществляют реакцию 2-метокси-октагидроиндола, полученного в результате реакции неустойчивого промежуточного соединения 2-гидрокси-октагидроиндола и метанола, с триметилфосфитом в присутствии диэтилового эфира трифторида бора с образованием октагидроиндол-2-фосфоновой кислоты при обработке 33% раствором бромоводорода в уксусной кислоте.
[0014] Процедура синтеза DL-диэтилпирролидин-2-фосфоната и непосредственное превращение пептидов, содержащих карбокси-концевой пролин, в соответствующие фосфоно-аналоги, содержащие фосфо-концевой 2-фосфонопирролидин, описана в Pagani et al., Int. J. Peptide Protein Res. 34, 1989, 33-36. Как сообщается, процедура включает обработку при комнатной температуре эфирного раствора карбиноламидов триэтилфосфитом в присутствии этилэфирата трифторида бора. Карбиноламиды получают из соответствующих карбокси-активированных N-защищенных аминокислот и пептидов посредством окислительного декарбоксилирования.
[0015] Синтез полученного из дипептида диарил-изоиндолин-1-ил-фосфоната описан в Van der Veken et al., J. Med. Chem. 2007, 50, 5568-5570. В данном синтезе промежуточная стадия заключается в воздействии на циклический гемиаминаль по модифицированному протоколу Birum-Oleksyszyn с применением либо трифенилфосфита, либо трис(4-ацетамидофенил)фосфата и катализатора на основе кислоты Льюиса с образованием дифенил- или бис(4-ацетамидофенил)изоиндолин-1-ил-фосфоната.
[0016] Об уреидоалкилировании соединений фосфора (III) сообщается в Petersen et al., Liebigs Ann. Chem. 766, 58-72 (1972). На страницах 65 и 72 описана реакция диэтилфосфита и 2-оксо-1,3,5,5-тетраметил-4-гидрокси-гексагидропиримидина с образованием диэтилового сложного эфира 2-оксо-1,3,5,5-тетраметил-гексагидро-4-пиримидил-фосфоновой кислоты. В данном случае реакционную смесь нагревают до температуры приблизительно 90°С-95°С при перемешивании и поддерживают при данной температуре в течение периода времени приблизительно 2 часа. Затем воду и избыток диэтилфосфита отгоняют под вакуумом.
[0017] Об обработке N-гидроксиметилированных лактамов 2,4-диамино-L-бутановой кислоты, L-орнитина и L-лизина трихлоридом фосфора с получением фосфоновых кислот и метилдихлорфосфином с получением метилфосфиновых кислот сообщается в Natchev, Phosphorus and Sulfur, 1988, Vol. 37, 143-148. Гидроксиметильные производные и трихлорид фосфора перемешивают в течение 1 часа при комнатной температуре и в течение еще 15 минут при температуре приблизительно 50°С-60°С. Получаемые в результате продукты реакции растворяют в тетрахлорметане и добавляют холодную уксусную кислоту с образованием производных фосфиновой кислоты. Смесь после отстаивания в течение 24 часов при комнатной температуре декантируют и полученную в результате массу перекристаллизовывают из воды.
Цели изобретения
[0018] Целью настоящего изобретения является обеспечение нового и эффективного синтеза аминоалкиленфосфоновой кислоты или ее сложных фосфонатных эфиров, который лишен недостатков известных из уровня техники способов. В частности, другой целью настоящего изобретения является обеспечение одностадийного синтеза, с помощью которого можно селективно получать соединения более высокого качества с высокой чистотой и высоким выходом. Другой целью настоящего изобретения является синтез соединений фосфоновой кислоты за более короткий срок и с меньшей затратой энергии.
Краткое описание изобретения
[0019] Настоящее изобретение раскрывает способ синтеза аминоалкиленфосфоновой кислоты ее фосфонатных сложных эфиров, включающий следующие стадии:
а) образования в присутствии альдегида или кетона и кислотного катализатора реакционной смеси посредством смешивания соединения (а.1.), содержащего по меньшей мере один фрагмент HNR1R2, или его соли с соединением (а.2.), содержащим один или несколько ангидридных фрагментов Р-О-Р, причем указанные фрагменты содержат один атом Р в степени окисления (+III) и один атом Р в степени окисления (+III) или (+V), где соотношение молей альдегида или кетона и фрагментов N-H составляет 1 или более, и где соотношение фрагментов N-H и ангидридных фрагментов Р-О-Р составляет 0,3 или более,
и где
соединение (а.1.), содержащее HNR1R2, характеризуется тем, что
(а.1.1) R1 и R2 независимо выбраны из группы, состоящей из водорода, С1С6алкила, С1-С6алкенила, С1-С6алкинила, С1-С6ацила, необязательно содержащего этиленненасыщенную двойную связь, и (мет)акрилоильного C1-С6-фрагмента, причем С1-С6-часть указанных фрагментов имеет нормальную, разветвленную или циклизированную цепь и необязательно замещена одним или несколькими фрагментами, выбранными из группы, состоящей из С1-С4углеводорода, арила и аралкила, и необязательно содержит один или несколько гетероатомов, выбранных из группы, состоящей из кислорода, азота и серы, и необязательно содержит один или несколько карбонильных фрагментов, или
(а.1.2) R1 и R2 образуют кольцевую структуру, где N-H включены в указанное кольцо, и где указанное кольцо необязательно замещено одним или несколькими фрагментами, выбранными из группы, состоящей из С1-С4углеводорода, арила и аралкила, и необязательно содержит один или несколько гетероатомов, выбранных из группы, состоящей из кислорода, азота и серы, и необязательно содержит один или несколько карбонильных фрагментов, или
(а.1.3.) R1 и R2 образуют часть полимера, где по меньшей мере один >NH включен в полимерную цепь, или где по меньшей мере один HNR1 представляет собой повторяющийся фрагмент-заместитель в полимерной цепи, содержащей полимеризованные фрагменты R2, необязательно сополимеризованные с другими полимеризуемыми мономерами, характеризующуюся тем, что R1 и R2 независимо выбраны из группы, состоящей из водорода, С1-С6алкила, С1-С6алкенила, С1-С6алкинила, С1-С6ацила, необязательно содержащего этиленненасыщенную двойную связь, и (мет)акрилоильного С1-С6-фрагмента, причем С1-С6-часть указанных фрагментов имеет нормальную, разветвленную или циклизированную цепь и необязательно замещена одним или несколькими фрагментами, выбранными из группы, состоящей из С1-С4углеводорода, арила и аралкила, и необязательно содержит один или несколько гетероатомов, выбранных из группы, состоящей из кислорода, азота и серы, и необязательно содержит один или несколько карбонильных фрагментов,
и где
соединения (а.2.), содержащие ангидридные фрагменты Р-О-Р, выбраны из группы, состоящей из:
- гексаоксида тетрафосфора, тетраэтилпирофосфита и соединений (а.2.), содержащих ангидридные фрагменты Р-О-Р, полученных в результате объединения одного или нескольких соединений, содержащих:
(а.2.1) один или несколько фрагментов Р-ОН с одним или несколькими соединениями, содержащими один или несколько ангидридных фрагментов Р-О-Р или один или несколько фрагментов Р-Х, где атом Р в одном или нескольких соединениях находится в степени окисления (+III);
(а.2.2) один или несколько фрагментов Р-Х и воду, где атом Р в соединении, содержащем фрагмент Р-Х, находится в степени окисления (+III);
(а.2.3) два или более фрагментов Р-О-Р и воду, где соединение, содержащее фрагмент Р-О-Р, содержит атом Р в степени окисления (+III) и атом Р в степени окисления (+III) или (+V);
где соединения, содержащие один или несколько фрагментов Р-ОН, доступны при таутомеризации фрагмента >Р(=O)Н,
где X представляет собой галогенид, выбранный из группы, состоящей из хлора, брома и йода, и
где уровень галогена в соединении, содержащем ангидридный фрагмент Р-О-Р, составляет 1000 ppm или менее, предпочтительно 500 ppm или менее и более предпочтительно 200 ppm или менее,
и
b) извлечения получаемого в результате соединения, содержащего фрагмент аминоалкиленфосфоновой кислоты или одного из ее фосфонатных сложных эфиров.
[0020] В конкретных вариантах осуществления настоящего изобретения раскрывают один или несколько из следующих признаков:
- соотношение фрагментов N-H и фрагментов Р-О-Р находится в диапазоне от 0,3 до 2,0 и предпочтительно от 0,5 до 1,5;
- реакцию на стадии а) проводят при температуре в диапазоне от 20°С до 120°С, предпочтительно от 40°С до 100°С, в течение периода времени в диапазоне от 30 минут до 24 часов, предпочтительно от 1 часа до 20 часов;
- способ по настоящему изобретению включает дополнительные стадии:
- добавления воды в реакционную смесь после завершения превращения соединения, содержащего фрагмент HNR1R2, в соединение, содержащее фрагмент аминоалкиленфосфоновой кислоты;
- доведения реакционной смеси, содержащей добавленную воду, до температуры в диапазоне от 20°С до 150°С; и
- выдерживания реакционной смеси, содержащей добавленную воду, при указанной температуре в течение по меньшей мере 10 минут;
- соединение, содержащее ангидридный фрагмент Р-О-Р, выбрано из группы, состоящей из гексаоксида тетрафосфора, тетраэтилпирофосфита и соединения, содержащего ангидридный фрагмент Р-О-Р, полученного в результате объединения фосфористой кислоты и гексаоксида тетрафосфора, фосфористой кислоты и декаоксида тетрафосфора, фосфористой кислоты и трихлорида фосфора, диметилфосфита и декаоксида тетрафосфора, трихлорида фосфора и воды, а также гексаоксида тетрафосфора и воды;
- соединение, содержащее ангидридные фрагменты Р-О-Р, представляет собой гексаоксид тетрафосфора;
- фрагмент R альдегида с общей формулой R-CO-H выбран из группы, состоящей из водорода, алифатического фрагмента, аралифатического фрагмента, ароматического фрагмента и гетероциклического фрагмента, где общее число атомов углерода и гетероатомов находится в диапазоне от 1 до 11;
- R' и R'' кетона с общей формулой R'-CO-R'' независимо выбраны из группы, состоящей из алифатического фрагмента, аралифатического фрагмента и ароматического углеводородного фрагмента, где общее число атомов углерода находится в диапазоне от 1 до 12;
- альдегид представляет собой формальдегид;
- кислотный катализатор представляет собой гомогенный катализатор на основе кислоты Бренстеда, предпочтительно выбранный из группы, состоящей из метансульфоновой кислоты, трифторметансульфоновой кислоты, трифторуксусной кислоты, п-толуолсульфоновой кислоты, хлористоводородной кислоты, фосфористой кислоты, фосфорной кислоты и их смесей;
- кислотный катализатор представляет собой гетерогенную кислоту Бренстеда, предпочтительно выбранную из группы, состоящей из:
(i) комбинаций твердых кислотных оксидов металлов как таковых или на подложке из материала-носителя;
(ii) катионообменных смол, выбранных из группы, включающей сополимеры стирола, этилвинилбензола и дивинилбензола, функционализированные таким образом, что обеспечивается прививка фрагментов SO3H на ароматическую группу, и перфорированные смолы, несущие группы карбоновой и/или сульфоновой кислоты;
(iii) органических сульфоновых, карбоновых и фосфоновых кислот Бренстеда, которые являются практически несмешиваемыми в реакционной среде при температуре реакции;
(iv) кислотного катализатора, полученного:
- в результате взаимодействия твердой подложки, содержащей неподеленную пару электронов, на которую осаждена органическая кислота Бренстеда; или
- в результате взаимодействия твердой подложки, содержащей неподеленную пару электронов, на которую осаждено соединение, содержащее льюисовский кислотный центр; или
- из гетерогенных твердых веществ, функционализированных посредством химической прививки группы кислоты Бренстеда или ее предшественника; и
(v) гетерогенных гетерополикислот общей формулы HxPMyOz, где Р выбран из фосфора и кремния, а М выбран из вольфрама и молибдена, а также их комбинаций;
- кислотный катализатор представляет собой гомогенную кислоту Льюиса, предпочтительно выбранную из группы, состоящей из LiN(CF3SO2)2, Mg(OCF3SO2)2, Al(OCF3SO2)3, Bi(OCF3SO2)3, Sc(OCF3SO2)3;
- кислотный катализатор представляет собой гетерогенную кислоту Льюиса, полученную в результате взаимодействия гомогенного катализатора на основе кислоты Льюиса и органического или неорганического полимерного соединения;
- стадия а) включает растворитель, выбранный из группы, состоящей из 1,4-диоксана, толуола, этилацетата, ацетонитрила, уксусной кислоты, сульфолана, 1-этил-3-метил-имидазолий-бис(трифторметилсульфонил)имида или их смеси;
- способ по настоящему изобретению включает стадии:
- а) образования реакционной смеси посредством смешивания соединения, содержащего по меньшей мере один фрагмент HNR1R2, с альдегидом или кетоном и кислотным катализатором необязательно в присутствии растворителя с образованием соединения, содержащего по меньшей мере один аминоалкилольный фрагмент;
- b) добавления соединения, содержащего по меньшей мере один ангидридный фрагмент Р-О-Р, содержащий один атом Р в степени окисления (+III) и один атом Р в степени окисления (+III) или (+V), в реакционную смесь со стадии а), содержащую по меньшей мере один аминоалкилольный фрагмент, с образованием соединения, содержащего фрагмент аминоалкиленфосфоновой кислоты;
- с) добавления воды в реакционную смесь со стадии b);
- d) извлечения получаемого в результате соединения, содержащего фрагмент аминоалкиленфосфоновой кислоты или одного из ее фосфонатных сложных эфиров;
- гидролиз после завершения образования соединения, содержащего фрагмент аминоалкиленфосфоновой кислоты, проводят при pH в диапазоне от 4,0 до 7,0;
- гидролиз после завершения образования соединения, содержащего фрагмент аминоалкиленфосфоновой кислоты проводят при температуре в диапазоне от 20°С до 150°С, предпочтительно от 40°С до 100°С, в течение периода времени в диапазоне от 10 минут до 72 часов и предпочтительно от 1 часа до 10 часов;
- соединение, содержащее фрагмент аминоалкиленфосфоновой кислоты, или его фосфонатные сложные эфиры, получаемые в результате осуществления способа по настоящему изобретению, применяют в качестве фитотоксиканта, ингибитора образования накипи, диспергирующего средства и/или комплексообразователя.
Подробное описание изобретения
[0021] Настоящее изобретение предусматривает эффективный и экономичный способ синтеза аминоалкиленфосфоновой кислоты или ее фосфонатных сложных эфиров с высокой селективностью и высоким выходом.
[0022] Фосфонатные сложные эфиры по настоящему изобретению содержат одну или несколько замещенных или незамещенных гидрокарбильных групп, которые могут быть разветвленными или неразветвленными, насыщенными или ненасыщенными и могут содержать одно или несколько колец. Подходящие гидрокарбилы включают алкильные, алкенильные, алкинильные и арильные фрагменты. Они также включают алкильные, алкенильные, алкинильные и арильные фрагменты, замещенные другими алифатическими или циклическими гидрокарбильными группами, как например, алкарил, алкенарил и алкинарил.
[0023] Замещенный гидрокарбил определяют как гидрокарбил, в котором по меньшей мере один атом водорода был замещен атомом, отличным от водорода, как например, атомом галогена (F, Cl, Br и I), атомом кислорода с образованием, например, простого эфира или сложного эфира, атомом азота с образованием амидной или нитрильной группы или атомом серы с образованием, например, тиоэфирной группы.
[0024] Фосфонатные сложные эфиры, в целом, получают с применением соединения, содержащего ангидридный фрагмент Р-О-Р, замещенного соответствующими гидрокарбильными заместителями.
[0025] Способ по настоящему изобретению включает группировку, благодаря чему осуществляют реакцию соединения, содержащего ангидридный фрагмент Р-О-Р с одним атомом Р со степенью окисления (+III) и другим атомом Р со степенью окисления (+III) или (+V), аммиака или первичного или вторичного амина и альдегида или кетона в присутствии кислотного катализатора и необязательно растворителя.
[0026] Несмотря на то, что соединение, содержащее ангидридный фрагмент Р-О-Р, предпочтительно выбрано из группы, состоящей из гексаоксида тетрафосфора и частично гидролизованных соединений гексаоксида тетрафосфора, полученных в результате реакции 1 моля гексаоксида тетрафосфора с 1, 2, 3, 4 и 5 молями воды, соответственно, понятно, что в контексте настоящего изобретения можно применять все соединения, содержащие по меньшей мере одну ангидридную группу Р-О-Р, где один атом Р имеет степень окисления (+III), а другой атом Р имеет степень окисления (+III) или (+V).
[0027] Подходящие соединения, содержащие ангидридный фрагмент Р-О-Р, могут либо содержать ангидридный фрагмент Р-О-Р в самом соединении (например, P4O6 или пирофосфиты (RO)2P-O-P(OR)2), либо могут быть получены in situ посредством объединения реагентов, которые будут образовывать необходимый ангидридный фрагмент Р-О-Р, при объединении до реакции с аминоалкилолом.
[0028] Подходящие комбинации реагентов представляют собой:
a) соединения, содержащие по меньшей мере один фрагмент Р-ОН (также доступны при таутомеризации фрагмента >Р(=O)Н в >P(LP)OH (где LP представляет собой неподеленную пару электронов), такой как, например, что и в случае для диметилфосфита (MeO)2Р(=O)Н), а также соединения, содержащие по меньшей мере один ангидридный фрагмент Р-О-Р, например, P2O5 или P4O6;
b) соединения, содержащие по меньшей мере один фрагмент Р-ОН, и соединения, содержащие по меньшей мере один фрагмент Р-Х (X=Cl, I, Br);
c) соединения, содержащие по меньшей мере один фрагмент Р-Х и H2O;
d) соединения, содержащие ангидридные фрагменты Р-О-Р и H2O, для частичного гидролиза.
[0029] В случае а) и b) обязательным является то, что по меньшей мере в одном из используемых соединений атом Р находится в степени окисления (+III), тогда как в случае с) необходимо, чтобы атом Р находился в степени окисления (+III), а в случае d), чтобы фрагменты Р-О-Р содержали атом Р в степени окисления (+III) и другой атом Р в степени окисления (+III) или (+V) с целью образования соединения, содержащего ангидридный фрагмент Р-О-Р, содержащий атом Р в степени окисления (+III) и другой атом Р в степени окисления (+III) или (+V).
[0030] Содержащие ангидридный фрагмент Р-О-Р соединения, где ангидридный фрагмент Р-О-Р уже присутствует, представляют собой оксиды фосфора с формулой P4On, где n=6-9, пирофосфиты с общей формулой (RO)2P-O-P(OR)2, где R представляет собой алкильную или арильную группу, пирофосфористую кислоту (H4P2O5) и изогипофосфорную кислоту (Н)(НО)Р(O)-O-Р(O)(OH)2.
[0031] Комбинации, описанные в а), получают посредством осуществления реакции, например, оксидов фосфора с формулой P4On, где n=6-10, алкил-замещенных пирофосфитов, пирофосфористой кислоты, изогипофосфорной кислоты, метафосфорной кислоты или полифосфорной кислоты с фосфористой кислотой, фосфорной кислотой, моно- или дизамещенными фосфитами с формулой (RO)PO2H2 или (RO)2POH, где R представляет собой алкильную или арильную группу, фосфатными сложными эфирами (RO)PO3H2 или (RO)2PO2H, фосфоновыми кислотами RPO3H2 или их сложным моноэфиром RPO2H(или), при условии, что такие комбинации будут приводит к соединениям, содержащим ангидридный фрагмент Р-О-Р, содержащий один атом Р в степени окисления (+III) и другой атом Р в степени окисления (+III) или (+V).
[0032] Комбинации, описанные в b), получают посредством объединения PCl3, PBr3, POCl3 или моно- или дихлорфосфитов типа (RO)2PCl и (RO)PCl2 с фосфористой кислотой, фосфорной кислотой или моно- или дизамещенными фосфитами с формулой (RO)PO2H2 или (RO)2POH, при условии, что такие комбинации будут приводить к соединениям, содержащим ангидридный фрагмент Р-О-Р, содержащий один атом Р в степени окисления (+III) и другой атом Р в степени окисления (+III) или (+V).
[0033] Комбинации, описанные в с), получают посредством объединения PCl3, PBr3 или моно- или дихлорфосфитов типа (RO)2PCl и (RO)PCl2 с H2O.
[0034] С целью получения содержащих ангидридный фрагмент Р-О-Р соединений, не содержащих функциональные группы Р-Х, оставшиеся функциональные группы Р-Х гидролизуют. Оставшиеся ангидридные фрагменты Р-О-Р также могут быть гидролизованы, поскольку необходимый ангидридный фрагмент Р-О-Р, где один атом Р находится в степени окисления (+III) и другой атом Р находится в степени окисления (+III) или (+V), остается.
[0035] Наиболее предпочтительными являются гексаоксид тетрафосфора, тетраэтилпирофосфит и комбинации фосфористой кислоты и гексаоксида тетрафосфора, фосфористой кислоты и декаоксида тетрафосфора, фосфористой кислоты и трихлорида фосфора, диметилфосфита и декаоксида тетрафосфора, трихлорида фосфора и воды, а также гексаоксида тетрафосфора и воды.
[0036] Количество 'реакционноспособных' атомов Р(+III), которые могут быть превращены в фосфоновые кислоты, согласно настоящему изобретению определяют по количеству атомов Р(+III) и количеству ангидридных фрагментов Р-О-Р. Если ангидридных фрагментов Р-О-Р больше, чем атомов Р(+III), то все атомы Р(+III) превращаются в фосфоновые кислоты. Если ангидридных фрагментов Р-О-Р меньше, чем атомов Р(+III), то только часть атомов Р(+III), равная количеству ангидридных фрагментов Р-О-Р, превращается в фосфоновые кислоты.
[0037] Если применяют галогенсодержащие исходные вещества, например, PCl3, POCl3 или PBr3, уровень галогена в соединении, содержащем ангидрид Р-О-Р, следует поддерживать ниже 1000 ppm, обычно ниже 500 ppm, предпочтительно ниже 200 ppm в пересчете на вещество с Р-О-Р, составляющее 100%. Следовательно, все избыточные функциональные группы Р-Х гидролизуют перед реакциями с субстратом посредством добавления одной молекулы H2O на избыток функциональной группы Р-Х. Образованный Н-Х удаляют посредством, например, продувки сухим инертным газом, таким как азот или гелий, через раствор.
[0038] Гексаоксид тетрафосфора, предпочтительно применяемый в объеме настоящего изобретения, может быть представлен практически чистым соединением, содержащим по меньшей мере 85%, предпочтительно более 90%, более предпочтительно по меньшей мере 95% и в одном конкретном осуществлении по меньшей мере 97% P4O6. Несмотря на то, что гексаоксид тетрафосфора, подходящий для применения в контексте настоящего изобретения, может быть получен по любой известной технологии, в предпочтительных вариантах осуществления его получают согласно способу, описанному в патентных заявках WO 2009/068636 и/или WO 2010/055056 в разделе под названием "Способ получения P4O6 с улучшенным выходом" ("Process for the manufacture of P4O6 with improved yield"). Более подробно, проводят реакцию кислорода или смеси кислорода и инертного газа, а также газообразного или жидкого фосфора фактически в стехиометрических количествах в реакционном блоке при температуре в диапазоне от 1600 K до 2000 K с отводом тепла, образующегося при экзотермической реакции фосфора и кислорода, при поддержании предпочтительного времени пребывания от 0,5 секунды до 60 секунд с последующим гашением продукта реакции при температуре ниже 700 K и очисткой неочищенного продукта реакции посредством перегонки. Полученный таким образом гексаоксид тетрафосфора представляет собой чистый продукт, обычно содержащий по меньшей мере 97% оксида. Полученный таким образом P4O6 обычно представлен в виде жидкого материала с высокой степенью чистоты, содержащего, в частности, низкие уровни элементарного фосфора, Р4, предпочтительно ниже 1000 ppm в пересчете на P4O6, составляющий 100%. Предпочтительное время пребывания составляет от 5 секунд до 30 секунд, более предпочтительно от 8 секунд до 30 секунд. Продукт реакции в одном предпочтительном варианте осуществления может быть охлажден до температуры ниже 350 K.
[0039] Предполагается, что P4O6, участвующий в реакции при температуре от 24°С (t° плавления) до 120°С, обязательно должен быть жидким или газообразным, несмотря на это, твердые вещества можно, теоретически, применять для получения реакционной среды.
[0040] С целью удобства и оперативного знания, гексаоксид тетрафосфора, представленный P4O6, является высокочистым и содержит очень низкие уровни примесей, в частности, элементарного фосфора, Р4, при уровне ниже 1000 ppm, обычно ниже 500 ppm и предпочтительно не более 200 ppm в пересчете на P4O6, составляющий 100%.
[0041] В настоящем изобретении известно, что применение терминологии "соединение, содержащее ангидридный фрагмент Р-О-Р," подразумевает "соединение, содержащее ангидридный фрагмент Р-О-Р, где один атом Р находится в степени окисления (+III), а другой атом Р находится в степени окисления (+III) или (+V).
[0042] Соединение, содержащее HNP^R2, применяемое в настоящем изобретении, может представлять собой низкомолекулярную органическую молекулу или образовывать часть полимера, где низкомолекулярная органическая молекула или полимер могут быть привиты на неорганическом материале.
[0043] Что касается соединения, содержащего HNR1R2, которое представляет собой низкомолекулярную органическую молекулу, оно дополнительно характеризуется тем, что
R1 и R2 независимо выбраны из водорода, С1-С6алкила, С1-С6алкенила, C1-С6алкинила, С1-С6ацила, необязательно содержащего этиленненасыщенную двойную связь, и (мет)акрилоильного С1-С6-фрагмента, причем С1-С6-часть указанных фрагментов имеет нормальную, разветвленную или циклизированную цепь и необязательно замещена одним или несколькими фрагментами, выбранными из группы, состоящей из С1-С4углеводорода, арила и аралкила, и необязательно содержит один или несколько гетероатомов, выбранных из группы, состоящей из кислорода, азота и серы, и необязательно содержит один или несколько карбонильных фрагментов.
[0044] R1 и R2 могут образовывать кольцевую структуру, где N-H включены в указанное кольцо, и где указанное кольцо необязательно замещено одним или несколькими фрагментами, выбранными из группы, состоящей из С1-С4углеводорода, арила и аралкила, и необязательно содержит один или несколько гетероатомов, выбранных из группы, состоящей из кислорода, азота и серы, и необязательно содержит один или несколько карбонильных фрагментов.
[0045] Для соединения, содержащего HNR1R2, которое образует часть полимера, по меньшей мере один >N-H включен в полимерную цепь, или по меньшей мере один -NHR1 представляет собой повторяющийся фрагмент-заместитель в полимерной цепи, содержащей полимеризованные фрагменты R2, необязательно сополимеризованные с другими полимеризуемыми мономерами.
[0046] Соединение, содержащее HNR1R2, которое образует часть полимера, дополнительно характеризуется тем, что R1 и R2 независимо выбраны из группы, состоящей из:
водорода, С1-С6алкила, С1-С6алкенила, С1-С6алкинила, С1-С6ацила, содержащего по меньшей мере 1 этиленненасыщенную двойную связь, и (мет)акрилоильного С1-С6-фрагмента, причем С1-С6-часть указанных фрагментов имеет нормальную, разветвленную или циклизированную цепь и необязательно замещена одним или несколькими фрагментами, выбранными из группы, состоящей из С1-С4углеводорода, арила и аралкила, и необязательно содержит один или несколько гетероатомов, выбранных из группы, состоящей из кислорода, азота и серы, и необязательно содержит один или несколько карбонильных фрагментов.
[0047] Альдегид с общей формулой R-CO-H, подлежащий применению в способе по настоящему изобретению, выбран из соединений, в которых R представляет собой водород, алифатический, аралифатический, ароматический или гетероциклический фрагмент, и в которых общее число атомов углерода и гетероатомов предпочтительно предполагается составляющим значение от 1 до 11. Алифатические фрагменты, в частности, представляют собой алкильные фрагменты, предпочтительно таковые с 1-6 атомами углерода, примерами которых являются метил, этил, пропил, бутил. Алифатические фрагменты также могут быть разветвленными, примерами которых является изобутил. Ароматические фрагменты представляют собой, например, фенил или α- или β-нафтил, а гетероциклические фрагменты представляют собой, например, фурфурил. Альдегид может также содержать один или несколько заместителей, таких как, например, алкоксигруппа.
[0048] Примерами альдегидов с насыщенными алифатическими фрагментами являются формальдегид, ацетальдегид и бутиральдегид. Примеры альдегидов с замещенными насыщенными алифатическими фрагментами представляют собой метоксиацетальдегид и 3-метоксипропиональдегид. Примеры альдегидов с аралифатическими фрагментами представляют собой фенилацетальдегид и фенилпропиональдегид. Примеры альдегидов с ароматическими или гетероциклическими фрагментами представляют собой бензальдегид, фурфураль и 4-метоксифурфураль.
[0049] Кетон с общей формулой R'-CO-R'', подлежащий применению в способе по настоящему изобретению, представляет собой симметричное или асимметричное соединение с R' и R'', независимо выбранными из алифатических, аралифатических, циклических или ароматических углеводородных фрагментов при условии, что общее число атомов углерода предпочтительно составляет от 1 до 12. Алифатические фрагменты представляют собой таковые с неразветвленной или разветвленной цепью и предпочтительно насыщенные алкильные фрагменты, такие как, например, метил, этил, пропил и изобутил. Аралифатические фрагменты представляют собой, например, бензил или фенетил, а ароматические фрагменты представляют собой, например, α- или β-нафтил и предпочтительно фенил. Кетоны могут также содержать один или несколько заместителей, таких как, например, алкоксигруппа.
[0050] Примеры кетонов с насыщенными алифатическими фрагментами представляют собой ацетон, метилэтилкетон, метилизобутилкетон; примеры кетонов с замещенными алифатическими фрагментами представляют собой метоксиацетон. Пример кетонов с аралифатическими фрагментами представляет собой бензилацетон; примеры кетонов с циклическими фрагментами представляют собой циклогексанон и циклопентанон, при этом примеры кетонов с ароматическими фрагментами представляют собой ацетофенон и 4-метокси-ацетофенон.
[0051] Формальдегид применяют с особым предпочтением в форме альдегида.
Формальдегид, известный как оксиметилен, характеризующийся формулой CH2O, получают и реализуют в виде водных растворов, содержащих различные, часто незначительные, например, 0,3-3%, количества метанола, и они, как правило, представляют собой 37% растворы на основе формальдегида, несмотря на то, что могут применяться различные концентрации. Формальдегидные растворы находятся в виде смеси олигомеров. Такие предшественники формальдегида могут, например, быть представлены параформальдегидом, находящейся в твердом состоянии смесью линейных поли(оксиметиленгликолей) обычно с достаточно короткой, n=8-100, длиной цепи, и циклическим тримером формальдегида, называемым выражением 1,3,5-триоксан. Концентрации жидкого формальдегида выше приблизительно 37% требуют хранения при температуре выше комнатной температуры во избежание осаждения формальдегидных полимеров. Температура, необходимая для поддержания прозрачного раствора и во избежание разделения твердого полимера, повышается от комнатной температуры по мере того, как концентрация раствора повышается выше приблизительно 37%.
[0052] Несмотря на то, что формальдегид предпочтительно добавляют в виде 37% по весу раствора в воде, известного как формалин, его также можно добавлять в виде водного раствора с концентрацией формальдегида, отличной от 37% по весу, либо в виде твердого вещества, такого как, например, параформальдегид или 1,3,5-триоксан.
[0053] Когда формальдегид применяют в виде водного раствора, само собой разумеется, что сначала необходимо выделить промежуточное соединение аминоалкилол перед его добавлением в реакцию с соединением, содержащим ангидридный фрагмент Р-О-Р, при условии, что стадия выделения аминоалкилола может быть исключена для данных случаев, когда количества воды, присутствующие в водном растворе формальдегида, соответствуют таковым, необходимым для преобразования сначала соединения, содержащего ангидридный фрагмент Р-О-Р, в модифицированное соединение, содержащее ангидридный фрагмент Р-О-Р, посредством частичного гидролиза указанного первого соединения, содержащего ангидридный фрагмент Р-О-Р, после чего будут осуществлять реакцию указанного модифицированного соединения, содержащего ангидридный фрагмент Р-О-Р, с аминоалкилолом с образованием аминоалкиленфосфоновой кислоты.
[0054] Кислотный катализатор, применяемый в объеме настоящего изобретения, предпочтительно представляет собой гомогенный катализатор на основе кислоты Бренстеда необязательно в присутствии растворителя, или гетерогенный катализатор на основе кислоты Бренстеда в присутствии растворителя, или катализатор на основе кислоты Льюиса в присутствии растворителя.
[0055] Гомогенная кислота Бренстеда предпочтительно выбрана из группы, состоящей из метансульфоновой кислоты, фторметансульфоновой кислоты, трихлорметансульфоновой кислоты, трифторметансульфоновой кислоты, трифторуксусной кислоты, трет-бутилсульфоновой кислоты, п-толуолсульфоновой кислоты, нафталинсульфоновой кислоты, 2,4,6-триметилбензолсульфоновой кислоты, перфтор- или перхлор-алкилсульфоновых кислот, перфтор- или перхлор-алкилкарбоновых кислот, хлористоводородной кислоты, бромистоводородной кислоты, йодистоводородной кислоты, фосфористой кислоты, фосфорной кислоты и их смесей. Гомогенная кислота Бренстеда предпочтительно представляет собой метансульфоновую кислоту.
[0056] Гетерогенная кислота Бренстеда предпочтительно выбрана из группы, состоящей из:
(i) комбинаций твердых кислотных оксидов металлов как таковых или на подложке из материала-носителя;
(ii) катионообменных смол, выбранных из группы, включающей сополимеры стирола, этилвинилбензола и дивинилбензола, функционализированные таким образом, что обеспечивается прививка фрагментов SO3H на ароматическую группу, и перфорированные смолы, несущие группы карбоновой и/или сульфоновой кислоты;
(iii) органических сульфоновых, карбоновых и фосфоновых кислот Бренстеда, которые являются практически несмешиваемыми в реакционной среде при температуре реакции;
(iv) кислотного катализатора, полученного:
- в результате взаимодействия твердой подложки, содержащей неподеленную пару электронов, на которую осаждена органическая кислота Бренстеда; или
- в результате взаимодействия твердой подложки, содержащей неподеленную пару электронов, на которую осаждено соединение, содержащее льюисовский кислотный центр; или
- из гетерогенных твердых веществ, функционализированных посредством химической прививки группы кислоты Бренстеда или ее предшественника; и
(v) гетерогенных гетерополикислот общей формулы HxPMyOz, где Р выбран из фосфора и кремния, а М выбран из вольфрама, а также молибдена и их комбинаций.
[0057] Предпочтительные гомогенные кислоты Льюиса могут быть выбраны из солей металла, характеризующихся общей формулой,
MXn,
где М представляет собой элемент основной группы или переходный металл, такой как Li, В, Mg, Al, Bi, Fe, Zn, La, Sc, Yb или Pd; X в MXn, как правило, представляет собой анион кислоты или производное кислоты типа Cl, OTf или NTf2, где Tf представляет собой CF3SO2, и n равняется степени окисления М, которая может составлять от 1 до 5. Например, возможны комбинации LiNTf2, Mg(OTf)2, MgCl2, ZnCl2, PdCl2, Fe(OTf)3, Al(OTf)3, AlCl3, Bi(OTf)3, BiCl3, Sc(OTf)3, Ln(OTf)3, Yb(OTf)3. Предпочтительно применяют комбинации жесткого металла или металла на границе между жестким и мягким согласно принципа HSAB (жестких и мягких кислот и оснований), такого как Li, Mg, Al, Sc, Zn, Bi, и слабо координирующих анионов, таких как OTf или NTf2. Примеры таких предпочтительных комбинаций представляют собой LiNTf2, Mg(OTf)2, Al(OTf)3, Bi(OTf)3.
[0058] Предпочтительные гетерогенные кислоты Льюиса могут быть представлены веществами из дискретно выбранных подклассов, образованными при взаимодействии/связывании гомогенных кислот Льюиса, например, комплексных соединений металлов, солей металлов или металлорганических веществ, с органическими или неорганическими остовами полимеров. Пример такого подкласса представляет собой полистироловую матрицу со связанными группами Sc(OTf)2. Такой катализатор может быть получен, например, посредством взаимодействия смолы на основе полистиролсульфоновой кислоты, например, Amberlyst 15, с Sc(OTf)3. Число эквивалентов функциональных групп кислоты Льюиса может быть определено в данном случае различными способами, например, посредством кислотно-основного определения непрореагировавших групп сульфоновой кислоты, посредством количественного определения высвобожденной трифторметансульфоновой кислоты, а также посредством измерения с применением ICP количества Sc в смоле.
[0059] Типичными примерами подходящих органических растворителей, подлежащих применению в способе по настоящему изобретению, являются анизол; уксусная кислота; хлорированные и фторированные углеводороды, такие как фторбензол, хлорбензол, тетрахлорэтан, тетрахлорэтилен, дихлорэтан, дихлорметан; полярные растворители, такие как диглим, глим, дифенилоксид, производные полиалкиленгликоля с защищенными OH-группами, такими как OR***, где R*** представляет собой низшую алкильную или ацильную группу; алифатические углеводороды, такие как гексан, гептан, циклогексан; ациклические эфиры, такие как дибутиловый эфир, диэтиловый эфир, диизопропиловый эфир, дипентиловый эфир и бутилметиловый эфир; циклические эфиры, такие как тетрагидрофуран, диоксан и тетрагидропиран; смешанные циклические/ациклические эфиры, такие как циклопентилметиловый эфир; циклические и ациклические сульфоны, такие как сульфолан; ароматические растворители, такие как толуол, бензол, ксилол; органические ацетаты, такие как этилацетат; органические нитрилы, такие как ацетонитрил, бензонитрил; жидкости на основе кремния, такие как полиметилфенилсилоксан; не являющиеся реакционноспособными ионные жидкости, такие как 1-н-бутил-имидазолий-трифторметансульфонат и 1-этил-3-метил-имидазолий-бис(трифторметилсульфонил)имид.
В конкретном варианте осуществления настоящего изобретения кислотный катализатор выступает в качестве катализатора и в качестве растворителя.
[0060] Способ по настоящему изобретению начинают со смешивания соединения, содержащего HNR1R2, соединения, содержащего ангидридный фрагмент Р-О-Р, предпочтительно гексаоксида тетрафосфора, и альдегида или кетона, предпочтительно формальдегида, в присутствии кислотного катализатора и необязательно растворителя,
- соотношение эквивалентов фрагментов >N-H и молей альдегида или кетона находится в диапазоне от 0,9 до 1,5 и предпочтительно от 1,1 до 1,4;
- соотношение эквивалентов фрагментов >N-H и ангидридных фрагментов Р-О-Р находится в диапазоне от 0,3 до 2,0 и предпочтительно от 0,5 до 1,5.
[0061] В контексте настоящего изобретения способ может включать стадии образования реакционной смеси посредством попеременного постепенного добавления альдегида или кетона, предпочтительно формальдегида, и соединения, содержащего ангидридный фрагмент Р-О-Р, предпочтительно гексаоксида тетрафосфора, порциями к соединению, содержащему HNR1R2, в присутствии кислотного катализатора и необязательно растворителя.
[0062] В конкретном варианте осуществления настоящего изобретения способ включает стадии образования реакционной смеси посредством смешивания соединения, содержащего HNR1R2, и соединения, содержащего ангидридный фрагмент Р-О-Р, предпочтительно гексаоксида тетрафосфора, в присутствии кислотного катализатора и необязательно растворителя; затем альдегид или кетон, предпочтительно формальдегид, постепенно добавляют в реакционную смесь (пример 19).
Как правило, реакцию проводят при температуре в диапазоне от 20°С до 120°С и предпочтительно от 50°С до 110°С в течение периода времени в диапазоне от 30 минут до 24 часов.
[0063] В контексте настоящего изобретения способ может включать стадии образования реакционной смеси посредством смешивания альдегида или кетона, предпочтительно формальдегида, и соединения, содержащего HNR1R2, в присутствии кислотного катализатора и необязательно растворителя; затем соединение, содержащее ангидридный фрагмент Р-О-Р, предпочтительно гексаоксид тетрафосфора, постепенно добавляют в реакционную смесь (примеры 12 и 13, примеры 14-18 и пример 20).
[0064] В контексте настоящего изобретения способ может включать стадии образования реакционной смеси посредством смешивания альдегида или кетона, предпочтительно формальдегида, и соединения, содержащего HNR1R2, в присутствии кислотного катализатора и необязательно растворителя; выделения, необязательно очистки соединения, содержащего аминоалкилольный фрагмент, а затем постепенного добавления соединения, содержащего ангидридный фрагмент Р-О-Р, предпочтительно гексаоксида тетрафосфора, к соединению, содержащему аминоалкилольный фрагмент, в присутствии кислотного катализатора и необязательно растворителя (примеры 1-11).
[0065] Как правило, добавление альдегида или кетона, предпочтительно формальдегида, в реакционную смесь проводят при температуре в диапазоне от приблизительно 20°С до приблизительно 120°С и предпочтительно от приблизительно 40°С до 100°С и после завершения добавления альдегида или кетона реакционную смесь поддерживают при данной температуре в течение периода времени в диапазоне от приблизительно 10 минут до приблизительно 24 часов и предпочтительно от приблизительно 1 часа до приблизительно 20 часов.
[0066] Как правило, добавление соединения, содержащего ангидридный фрагмент Р-О-Р, предпочтительно гексаоксида тетрафосфора, в реакционную смесь проводят при температуре в диапазоне от приблизительно 20°С до приблизительно 120°С и предпочтительно от приблизительно 40°С до 100°С и после завершения добавления гексаоксида тетрафосфора реакционную смесь поддерживают при данной температуре в течение периода времени в диапазоне от приблизительно 10 минут до приблизительно 24 часов и предпочтительно от приблизительно 1 часа до приблизительно 20 часов.
[0067] После завершения превращения соединения, содержащего HNR1R2, в соединение, содержащее фрагмент аминоалкиленфосфоновой кислоты, в реакционную смесь необязательно добавляют воду с целью гидролиза непрореагировавших ангидридных фрагментов Р-О-Р, если они присутствуют, и необязательно превращения соединения, содержащего фрагмент аминоалкиленфосфоновой кислоты, или его дегидратированных форм, или их фосфонатных сложных эфиров в их гидролизованную форму, такую как в примерах 14-17, где N-фосфонометил-2,5-оксазолидиндион гидролизуют в N-(фосфонометил)глицин с образованием диоксида углерода, или в примере 11, где N,N'-бис(фосфонометил)мочевину гидролизуют в аминометилфосфоновую кислоту с образованием диоксида углерода.
[0068] Гидролиз осуществляют при температуре в диапазоне от приблизительно 20°С до приблизительно 150°С, предпочтительно от приблизительно 40°С до приблизительно 100°С, в течение периода в диапазоне от приблизительно 10 минут до приблизительно 72 часов и предпочтительно от приблизительно 1 часа до приблизительно 10 часов.
[0069] Непрореагировавшие ангидридные фрагменты Р-О-Р могут быть результатом неполного превращения или добавления избытка соединений, содержащих ангидридную группу Р-О-Р, составляющих реакционную смесь.
[0070] В случае практически полного превращения и стехиометрической загрузки реактивов добавление воды и, следовательно, стадию гидролиза, можно опустить.
[0071] Гидролиз предпочтительно проводят по отношению к реакционной смеси, поддерживаемой при pH в диапазоне от 4 до 7, что в общем достигается посредством добавления гидроксидов щелочных металлов, предпочтительно гидроксида натрия или калия.
Примеры
[0072] Следующие иллюстративные примеры предназначены для иллюстрации, но не предназначены для ограничения объема настоящего изобретения.
Пример 1
[0073] В круглодонной колбе, оснащенной механической мешалкой, термометром и конденсатором, смешивали 3,56 г (40 ммоль) N-гидроксиметилацетамида с 10 мл ацетонитрила. Медленно добавляли 2,20 г (10 ммоль) P4O6. Затем реакционную смесь нагревали до 80°С в течение 1 часа. Затем добавляли 0,15 г (1 ммоль) трифторметансульфоновой кислоты и продолжали перемешивание в течение 2 часов при 80°С. Все летучие вещества удаляли под вакуумом и остаток растворяли в 5 мл H2O и 10 мл раствора NaOH (50% вес/вес в H2O) и нагревали до 100°С в течение 2 часов. Полученный раствор анализировали с помощью31Р-ЯМР спектроскопии. Аминометилфосфоновую кислоту выявляли в концентрации 15,5% вес/вес.
Пример 2
[0074] С использованием оборудования из примера 1 1,77 г (10 ммоль) N-гидроксиметилфталимида смешивали с 8,5 мл метансульфоновой кислоты при 60°С в атмосфере N2. Медленно добавляли 0,285 г (2,5 ммоля) P4O6. Затем реакционную смесь нагревали при 85°С в течение ночи. Затем добавляли 3 мл воды и смесь нагревали в течение 1 часа при 80°С. Раствор разбавляли водой и доводили до pH 5,4 посредством добавления гидроксида натрия. Смесь анализировали с помощью1Н- и31Р-ЯМР спектроскопии. N-фталимидометилфосфоновую кислоту выявляли в концентрации 11,5% вес/вес.
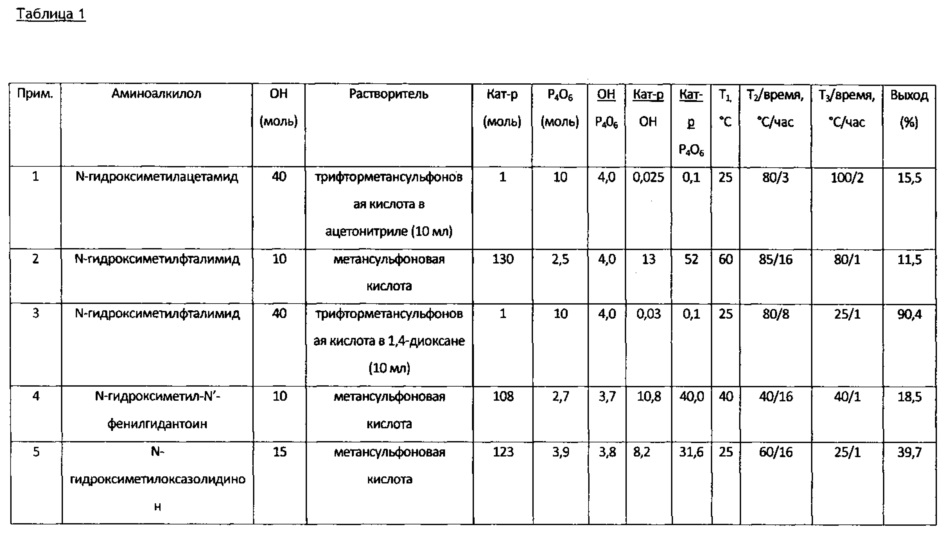
[0075] В таблице 1 изложен ряд примеров, полученных согласно способу по настоящему изобретению, а также с использованием оборудования и способа из примера 1 и примера 2.
В данной таблице:
в столбце 1: указан идентификационный номер примера;
в столбце 2: указан тип соединения, содержащего аминоалкилольный фрагмент, добавляемого в реакцию с гексаоксидом тетрафосфора;
в столбце 3: указано количество ммолей соединения, содержащего аминоалкилольный фрагмент, с приведенным в скобках количеством миллиэквивалентов аминоалкилола;
в столбце 4: указан тип применяемых кислотного катализатора и растворителя;
в столбце 5: указано количество ммолей кислотного катализатора;
в столбце 6: указано количество ммолей гексаоксида тетрафосфора;
в столбце 7: указано отношение ммолей соединения, содержащего аминоалкилольный фрагмент, к ммолям гексаоксида тетрафосфора с приведенным в скобках отношением миллиэквивалентов аминоалкилола к ммолям гексаоксида тетрафосфора;
в столбце 8: указано отношение ммолей кислотного катализатора к ммолям соединения, содержащего аминоалкилольный фрагмент, с приведенным в скобках отношением ммолей кислотного катализатора к миллиэквивалентам аминоалкилольных фрагментов;
в столбце 9: указано отношение ммолей кислотного катализатора к ммолям гексаоксида тетрафосфора;
в столбце 10: указана температура (°С), при которой проводят смешивание соединения, содержащего фрагмент HNR1R2, альдегида и соединения, содержащего ангидридный фрагмент Р-О-Р, в присутствии растворителя;
в столбце 11: указаны температурные (°С) и временные (часы) условия для реакционной смеси сразу после того, как все компоненты были добавлены;
в столбце 12: указаны температурные (°С) и временные (часы) условия для гидролиза;
в столбце 13: указан выход реакции в % по весу, как измерено с помощью1Н-ЯМР и31Р-ЯМР спектроскопии.
[0076] Соединением, содержащим фрагмент аминометиленфосфоновой кислоты, полученным в примерах из таблицы 1, является:
пример 1: аминометилфосфоновая кислота;
примеры 2 и 3: N-фталимидометилфосфоновая кислота;
пример 4: N-фосфонометил, N'-фенилгидантоин;
пример 5: N-фосфонометилоксазолидинон;
примеры 6-10: N-фосфонометилпирролидинон;
пример 11: N,N'-бис(фосфонометил)мочевина, дополнительно гидролизованная в аминометилфосфоновую кислоту.
Пример 12
[0077] С использованием оборудования из примера 1 1 эквивалент гидрохлорида метилового сложного эфира глицина смешивали с 1,5 эквивалента параформальдегида в 18,5 эквивалента метансульфоновой кислоты при 50°С в течение 1 часа, а затем при 75°С в течение 25 минут в атмосфере N2. Температуру регулировали до 25°С перед медленным добавлением 0,25 эквивалента P4O6 при поддержании температуры реакционной среды ниже 35°С. После этого реакционную смесь нагревали до 60°С в течение 1 часа. Затем добавляли 30 эквивалентов воды и смесь нагревали при 110°С в течение 30 минут. Раствор разбавляли водой и доводили до pH 5,4. Смесь анализировали с помощью31Р-ЯМР спектроскопии. N-(фосфонометил)глицин выявляли в концентрации 5,2 мольных %.
Пример 13
[0078] С использованием оборудования из примера 1 0,8 эквивалента N-(2-аминоэтил)этан-1,2-диамина смешивали с 5,35 эквивалента параформальдегида в ацетонитриле, содержащем 5 эквивалентов трифторуксусной кислоты. Смесь перемешивали в течение 40 минут при 65°С в атмосфере N2. Реакционную среду охлаждали до 35°С и медленно добавляли 1,0 эквивалент P4O6 при поддержании температуры ниже 35°С. После этого реакционную смесь нагревали до 60°С в течение 20 минут. Затем добавляли избыток воды и смесь нагревали при 85°С в течение 15 минут. Раствор разбавляли водой и доводили до pH 5,4. Смесь анализировали с помощью31Р-ЯМР спектроскопии. Диэтилентриамин-пента(метиленфосфоновую кислоту) выявляли в концентрации 10 мольных %.
Пример 14
[0079] С использованием оборудования из примера 1 0,30 г (9,9 ммоля) параформальдегида смешивали с 8 мл трифторуксусной кислоты. Затем реакционную смесь нагревали до 50°С и добавляли 1,00 г (9,9 ммоля) 2,5-оксазолидиндиона. После этого реакционную смесь перемешивали в течение 1 часа при 50°С. Медленно добавляли 0,55 г (2,5 ммоля) P4O6 и продолжали перемешивание в течение 24 часов при 50°С. Добавляли 10 мл H2O и продолжали перемешивание в течение 72 часов при 50°С. Полученный раствор анализировали с помощью1Н- и31Р-ЯМР спектроскопии. N-(фосфонометил)глицин выявляли в концентрации 42,5% вес/вес.
Пример 15
[0080] С использованием оборудования из примера 1 1,00 г (9,9 ммоля) 2,5-оксазолидиндиона смешивали с 8 мл трифторуксусной кислоты. Затем добавляли 0,30 г (9,9 ммоля) параформальдегида. После этого реакционную смесь перемешивали в течение 24 часов при температуре окружающей среды. Затем температуру повышали до 50°С и медленно добавляли 0,55 г (2,5 ммоля) P4O6. Продолжали перемешивание в течение 24 часов при 50°С. Добавляли 10 мл H2O и продолжали перемешивание в течение 72 часов при 50°С. Полученный раствор анализировали с помощью1Н- и31Р-ЯМР спектроскопии. N-(фосфонометил)глицин выявляли в концентрации 44,7% вес/вес.
Пример 16
[0081] С использованием оборудования из примера 1 1,00 г (9,9 ммоля) 2,5-оксазолидиндиона смешивали с 8 мл трифторуксусной кислоты. Затем добавляли 0,30 г (9,9 ммоля) параформальдегида. После этого реакционную смесь перемешивали в течение 1 часа при температуре окружающей среды. Медленно добавляли 0,55 г (2,5 ммоля) P4O6. Продолжали перемешивание в течение 24 часов при 60°С. Добавляли 10 мл H2O и продолжали перемешивание в течение 8 часов при 60°С. Полученный раствор анализировали с помощью1Н- и31Р-ЯМР спектроскопии. N-(фосфонометил)глицин выявляли в концентрации 34,9% вес/вес.
Пример 17
[0082] С использованием оборудования из примера 1 1,00 г (9,9 ммоля) 2,5-оксазолидиндиона смешивали с 8 мл толуола. Затем добавляли 0,30 г (9,9 ммоля) параформальдегида. После этого реакционную смесь перемешивали в течение 3 часов при 80°С. Медленно добавляли 1 мл метансульфоновой кислоты и 0,55 г (2,5 ммоля) P4O6. Продолжали перемешивание в течение 5 часов при 60°С. Добавляли 10 мл H2O и продолжали перемешивание в течение 8 часов при 60°С. Водный раствор анализировали с помощью1Н- и31Р-ЯМР спектроскопии. N-(фосфонометил)глицин выявляли в концентрации 5,6% вес/вес.
Пример 18
[0083] С использованием оборудования из примера 1 7,36 г (245,2 ммоля) параформальдегида смешивали с 64 мл метансульфоновой кислоты. Затем реакционную смесь нагревали до 40°С и медленно добавляли 3,69 г (61,5 ммоля) этилендиамина. После этого реакционную смесь нагревали до 50°С и медленно добавляли 13,55 г (61,6 ммоля) P4O6. Реакционную смесь нагревали до 85°С в течение 1 часа. При температуре окружающей среды добавляли 35 мл H2O и полученный раствор, а также твердое вещество анализировали с помощью31Р-ЯМР спектроскопии. Этилендиамин-тетраметиленфосфоновую кислоту выявляли в концентрации 36,6% вес/вес.
Пример 19
[0084] С использованием оборудования из примера 1 11,08 г (184,4 ммоля) этилендиамин смешивали с 64 мл метансульфоновой кислоты. Затем реакционную смесь нагревали до 70°С и медленно добавляли 40,64 г (184,7 ммоля) P4O6. После этого реакционную смесь нагревали до 105°С и 60,4 г (735,5 ммоля), добавляли раствор параформальдегида (36,6% вес/вес в H2O) в течение 30 минут. Реакционную смесь нагревали до 105°С в течение 1 часа. При температуре окружающей среды добавляли 25 мл H2O и полученный раствор, а также твердое вещество анализировали с помощью31Р-ЯМР спектроскопии. Этилендиамин-тетраметиленфосфоновую кислоту выявляли в концентрации 57,5% вес/вес.
Пример 20
[0085] С использованием оборудования из примера 1 7,36 г (245,2 ммоля) параформальдегида смешивали с 64 мл метансульфоновой кислоты. Затем реакционную смесь нагревали до 40°С и медленно добавляли 3,69 г (61,5 ммоля) этилендиамина. После этого реакционную смесь нагревали до 55°С и медленно добавляли 13,55 г (61,6 ммоля) P4O6. Реакционную смесь нагревали до 80°С в течение 3 часов. При температуре окружающей среды добавляли 35 мл H2O и полученный раствор, а также твердое вещество анализировали с помощью31Р-ЯМР спектроскопии. Этилендиамин-тетраметиленфосфоновую кислоту выявляли в концентрации 31,9% вес/вес.
Пример 21
[0086] С использованием оборудования из примера 1 4,24 г (40,0 ммоля) бензальдегида, 3,48 (40,0 ммоля) морфолина и 0,12 г (0,8 ммоля) трифторметансульфоновой кислоты смешивали с 10 мл 1,4-диоксана. Затем реакционную смесь перемешивали в течение 48 часов при температуре окружающей среды. Затем медленно добавляли 2,20 г (10,0 ммоля) P4O6 с последующим добавлением 0,48 г (3,2 ммоля) трифторметансульфоновой кислоты. Реакционную смесь нагревали до 80°С в течение 1 часа. При температуре окружающей среды добавляли 20 мл H2O; полученный раствор испаряли до сухого состояния и твердое вещество анализировали с помощью1Н- и31Р-ЯМР спектроскопии. 4-Морфолинил-фенилметил-фосфоновую кислоту выявляли в концентрации 72,9% вес/вес.
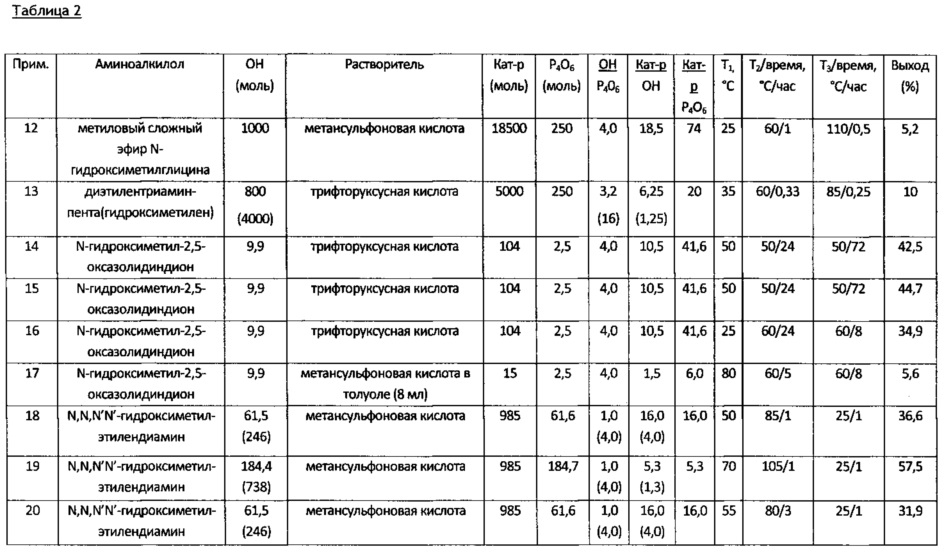
[0087] В таблице 2 приведены примеры 12-21, полученные согласно настоящему изобретению. В данной таблице соответствующие колонки имеют значения, соответствующие колонкам из таблицы 1.
[0088] В таблице 2,
- в примере 12 описан синтез метилового сложного эфира N-(гидроксиметил)глицина в результате реакции метилового сложного эфира глицина и формальдегида с последующим образованием N-(фосфонометил)глицина посредством реакции с гексаоксидом тетрафосфора;
- в примере 13 описан синтез N,N',N',N'',N''-гидроксиметил-(2-аминоэтил)этан-1,2-диамина с последующим образованием N,N',N',N'',N''-фосфонометил-(2-аминоэтил)этан-1,2-диамина посредством реакции с гексаоксидом тетрафосфора;
- в примерах с 14 по 17 описан синтез N-гидроксиметил-2,5-оксазолидиндиона в результате реакции 2,5-оксазолидиндиона и формальдегида с последующим образованием N-(фосфонометил)глицина посредством реакции с гексаоксидом тетрафосфора;
- в примерах с 18 по 20 описан синтез этилендиамин-тетраметиленфосфоновой кислоты в результате реакции этилендиамина, формальдегида и гексаоксида тетрафосфора в присутствии кислотного катализатора, где в
примерах 18 и 20 сначала осуществляют реакцию формальдегида и этилендиамина с образованием N,N,N',N'-тетракис(гидроксиметил)этандиамина с последующей реакцией с гексаоксидом тетрафосфора, и где в
примере 19 сначала осуществляют реакцию этилендиамина и гексаоксида тетрафосфора с последующим добавлением формальдегида;
- в примере 21 описан синтез 4-морфолинил-фенилметанола в результате реакции морфолина и бензальдегида в присутствии кислотного катализатора с последующим образованием 4-морфолинил-фенил-метилфосфоновой кислоты посредством реакции с гексаоксидом тетрафосфора.


Реферат
Настоящее изобретение относится к способу синтеза аминоалкиленфосфоновой кислоты или ее фосфонатных сложных эфиров и может использоваться в химической промышленности. Предложенный способ включает стадии: а) образования в присутствии альдегида и кислотного катализатора реакционной смеси посредством смешивания соединения (a.1.), содержащего по меньшей мере один фрагмент HNRR, или его соли с соединением (a.2.), содержащим один или несколько ангидридных фрагментов P-O-P, причем фрагменты содержат один атом P в степени окисления (+III) и один атом P в степени окисления (+III) или (+V), где отношение молей альдегида к фрагментам N-H составляет 1 или более, и где соотношение фрагментов N-H к ангидридным фрагментам P-O-P составляет 0,3 или более, и где альдегид имеет общую формулу R-CO-H, где R выбран из группы, состоящей из водорода, алифатического фрагмента, аралифатического фрагмента, ароматического фрагмента и гетероциклического фрагмента, где общее число атомов углерода и гетероатомов составляет от 1 до 11, соединение (a.1.) характеризуется тем, что (a.1.1) Rи Rнезависимо выбраны из водорода, C-Cалкила, C-Cалкенила, C-Cалкинила, C-Cацила, необязательно содержащего этиленненасыщенную двойную связь, и (мет)акрилоильного C-C-фрагмента, причем C-C-часть указанных фрагментов имеет нормальную, разветвленную или циклизированную цепь и необязательно замещена одним или несколькими фрагментами, выбранными из C-Cуглеводорода, арила и аралкила, и необязательно содержит один или несколько гетероатомов, выбранных из кислорода, азота и серы, и необязательно содержит один или несколько карбонильных фрагментов, или (a.1.2) Rи Rобразуют кольцевую структуру, где N-H включены в указанное кольцо, и где указанное кольцо необязательно замещено одним или несколькими фрагментами, выбранными из C-Cуглеводорода, арила и аралкила, и необязательно содержит один или несколько гетероатомов, выбранных из кислорода, азота и серы, и необязательно содержит один или несколько карбонильных фрагментов, и где соединения (a.2.), содержащие ангидридные фрагменты P-O-P, которые содержат один атом P в степени окисления (+III) и другой атом P в степени окисления (+III) или (+V), выбраны из гексаоксида тетрафосфора, PO, PO, PO, тетраэтилпирофосфита и их комбинаций, b) добавления воды в реакционную смесь и c) извлечения получаемого в результате соединения, содержащего фрагмент аминоалкиленфосфоновой кислоты или одного из ее фосфонатных сложных эфиров. Предложен новый эффективный способ получения аминоалкиленфосфоновой кислоты и ее фосфонатных сложных эфиров. 18 з.п. ф-лы, 21 пр., 2 табл.
Формула
Документы, цитированные в отчёте о поиске
Способ получения соединений аминополиалкиленфосфоновой кислоты

Комментарии