Инсектоакарицидная композиция - RU2055476C1
Код документа: RU2055476C1
Чертежи





















Описание
Изобретение относится к инсекто-акарицидной композиции и к ее использованию в обработке вредных насекомых.
Ненасыщенные амиды, имеющие цепь из метиленовых звеньев с числом атомов углерода 1-10, возможно имеющие как минимум один атом кислорода или дополнительную метиленовую группу, как известно, являются пестицидами или инсектицидами, имеющими различные концевые группы, перечень которых включает в себя фенильную группу, возможно, содержащую заместители (Европейские заявки NN 228222, 194764, 225011, заявка Японии N 57-212150, Meisters and Wailes: Aust. J. Chem, 1966, 19, 1215, Vig. et. al: J. And Chem. Soс. 1974, 51, (9), 817), или пиридильную группу, возможно содержащую заместители (Европейская заявка N 269457), или конденсированную лициклическую систему (Европейские заявки NN 143593, 228853), дигалоиндвинильную группу или возможно содержащую заместители: этинильную группу (Европейская заявка N 228222).
Отсутствует информация о каких-либо промежуточных циклоалкильных группах, связывающих диеновый фрагмент с концевой группой.
Н. О. Нuisman et. al. Rev. trav. Chim. 77, 97-102, (1958) сообщают о группе 5-(2,6, 6-триметилциклогексил)2,4-пентадиенамидов как об инсектицидах.
Обнаружено, что новые ненасыщенные амиды, содержащие 1,2-циклопропильное ядро, соседствующее с диеновым фрагментом и связывающее последний с концевой группой, выбранной из числа возможно замещенных моноциклических ароматических систем или возможно замещенных конденсированных бициклических системах, дигалоидвинильных групп или возможно замещенных этинильных групп, обладают интересными пестицидными свойствами.
Предлагается инсектоакарицидная композиция,
содержащая в качесте активного компонента
формулы (1):
QQ1CR2 CR3CR4 CR5C(=X)NHR1, (1) где Q фенил, возможно замещенный 1-3
заместителями, выбранными из галогена,
С1-С4-алкокси, галоген-С1-С4-алкила, галоген-С1-С4-алкокси, однократно С2-С4-алкенилом, бензилом, нафтилом,
возможно замещенным галогеном, пиридилом, дигалоидвинилом, три-С1-С4-алкилсилилом;
Q1 обозначает циклопропильное ядро,
возможно замещенные С1-С4-алкилом;
R2, R3, R4 и R5 обозначают одинаковые или разные группы, причем как минимум одна из них
представляет собой водород, а остальные
независимо друг от друга представляют собой группы, выбранные из галогена С1-С4-алкила; Х обозначает атом кислорода;
R1 С1-8-алкил возможно
замещенный С1-С4-алкилом или диоксаланилом либо С2-С5-алкенил.
Соединения, отвечающие формуле (I), можно использовать для борьбы с вредителями, такими как членистоногие, например, насекомые-вредители и клещи-паразиты, и паразитические черви, например, нематоды.
Таким образом, настоящее изобретение предлагает способ борьбы с членистоногими и/или паразитическими червями, который включает в себя воздействие на членистоногое и/или на паразитического червя, или на их окружение, соединения, отвечающего формуле (I), в количестве, обеспечивающем эффективность воздействия.
Изобрретение предлагает также способ борьбы и/или ликвидации вызванных членистоногими и/или паразитическими червями инвазий животных (включая людей) и/или растений (включая деревья) и/или хранящихся продуктов, который включает в себя воздействие на животное или очаг заражения эффективного количества соединения, отвечающего формуле (I).
Соединения, отвечающие формуле (I), и композиции на их основе представляют особую ценность для защиты полевых культур, кормовых растений, плантационных культур, тепличных культур, плодовых деревьев и виноградников, декоративных растений и плантационных и лесных деревьев, например, зерновых (таких как, например, кукуруза, пшеница рис, сорго), хлопка, табака, овощей и овощных культур салатного назначения (таких как, например, бобы, капуста, салат, латук, лук репчатый, помидоры и перец), полевых культур (таких как, например, картофель, сахарная свекла, арахис, соя, масличные семена рапса), сахарного тросника, пастбищ и кормовых культур (таких как, например, кукуруза, сорго, люцерна), плантационных культур (таких как, например, чай, кофе, какао, бананы, масличная пальма, кокосы, каучуконосы, пряности), плодовых деревьев и садов (например, костяники, односемянки, цитрусовых, киви, авокадо, манго, маслин и орехов), виноградников, декоративных растений, цветов и кустарников в оранжереях и в садах и парках, лесных деревьев (как лиственных, так и вечнозеленых) в лесах, на плантациях и в питомниках.
Эти композиции представляют также ценность для защиты лесоматериалов (растущих, срубленных, переработанных, хранящихся или оструктуренных) от нападения пильщиков (например, Wrocerus) или жуков (например, жуков-короедов, платиподидов, ликтидов, бострицидов жуков-дровосеков, анобиидов).
Другой областью их применения является защита хранящихся продуктов, таких как, например, зерно, фрукты, орехи, пряности и табак, в цельном и размолотом виде и в виде составных продуктов, от нападения моли, жуков и клещей. Они защищают также хранящиеся продукты животного происхождения, такие как, например, шкуры, волосы, шерсть и перья в натуральном или переработанном виде (например, ковровые или текстильные изделия) от нападения моли и жуков; а также хранящиеся мясо и рыбу от нападения жуков, клещей и мух.
Композиции на основе соединений, отвечающих общей формуле (I), представляют особую ценность для борьбы с членистоногими или паразитическими червями, которые являются вредными для человека и домашних животных, или размножаются в них, или действуют как переносчики заболеваний человека и домашних животных, названными выше, более конкретно, для борьбы с клещами, вшами, блохами, мелкими двукрылыми насекомыми, кусающимися насекомыми.
Соединения, отвечающие формуле (I), можно использовать для этих целей, применяя их в разбавленном виде, в форме дезинфицирующего раствора, разбрызгиваемого раствора, тумана, лака, пены, дуста, порошка, водной суспензии, пасты, геля, крема, шампуня, жира, горючего твердого вещества, парообразующего мата, горючей спирали, отравленной приманки, кормовой добавки, смачивающегося порошка, гранул, аэрозоля, эмульгируемого концентрата масляных суспензий, масляных растворов, упаковок под давлением, пропитанных изделий, выливаемого на поверхность препарата или в других стандартных формах, хорошо известных специалистам в данной области. Концентрированные дезинфицирующие растворы не применяют per se, но разбавляют водой и погружают животных в дезинфицирующую ванну, содержащую дезинфицирующий промывочный раствор. Разбрызгиваемые растворы можно применять вручную или с помощью дуговой штанги опрыскивателя. Обрабатываемые животное, почву, растение или поверхность можно насытить разбрызгиваемым раствором, применяя большие объемы, или покрыть их поверхности разбрызгиваемым раствором, применяя малые или сверхмалые объемы. Водяные суспензии можно применять так же, как разбрызгиваемые растворы или дезинфицирующие расторы. Пылевидные препараты (дусты) можно наносить с помощью машины для внесения порошкообразных препаратов или, в случае обработки животных, помещать в перфорированные мешки, прикрепленные к деревьям.
Пасты, шампуни и жировые препараты можно применять мануально или распределять по поверхности инертного материала, такого, об который животные трутся и переносят таким образом препарат себе на шкуры. Выливаемые на поверхность препараты распределяют в виде порции жидкости небольшого объема на спине животного таким образом, чтобы вся жидкость или большая ее часть осталась на животном.
Соединения, отвечающие формуле (I), можно формулировать или в виде, готовом для непосредственного применения для животных, растений или поверхностей, или в виде, требующем разбавления перед употреблением, но обе формы содержат оединение, отвечающее формуле (I), в смеси одним или несколькими носителями или разбавителями. Носители могут быть жидкими, твердыми или газообразными, или содержать смеси таких веществ, а соединение формулы (I) может присутствовать в концентрации 0, 025-99% массовых/объемных, в зависимости от того, требует ли данная форма дальнейшего разбавления или нет, предпочтительно 0,1-70 мас.
Пылевидные препараты, порошкообразные препараты и гранулированные препараты, а также другие твердые формы, содержащие соединение формулы (I) в смеси с порошкообразным твердым инертным носителем, например, с подходящими глинами, каолином, бентонитом, аттальпугитом, активированным углем, тальком, слюдой, мелом, гипсом, трикальцийфосфатом, порошкообразной пробкой, силикатом магния, носителями растительного происхождения, крахмалом и диатомитовыми почвами. Такие твердые формы, как правило, готовят пропиткой твердых разбавителей растворами соединения формулы (I) в летучих растворителях, выпариванием растворителя и, если желательно, размалыванием полученных продуктов с получением порошка, или, если желательно, гранулированием, прессованием или капсулированием продуктов.
Разбрызгиваемые растворы, содержащие соединение формулы (I), могут включать в себя раствор в органическом растворителе (например, в нижеперечисленных растворителях), или эмульсию в воде (дезинфицирующий моющий раствор или разбрызгиваемый моющий раствор), приготовляемую на месте использования из эмульгируемого концентрата, который можно также использовать для дезинфекции. Концентрат предпочтительно содержит смесь активного ингредиента с органическим растворителем (или органический растворитель отсутствует), и один или несколько эмульгаторов. Количество растворителя, присутствующего в смеси, может меняться в широких пределах, но предпочтительно составляет 0-90% массовых/объемных композиций, растворитель может быть выбран из числа нижеследующих: керосин, кетоны, спирты, ксилол, ароматические углеводороды и другие растворители, известные в данной области техники. Концентрация эмульгаторов может меняться в широких пределах, но предпочтительно составляет 5-25% массовых/объемных, и эмульгаторы обычно представляют собой неионные поверхностно-активные вещества, включая полиоксиалкиленовые сложные эфиры и анионные поверхностно-активные вещества, включая лаурилсульфат натрия, сульфаты простых эфиров жирных спиртов, натриевые и кальциевые соли алкиларилсульфонатов и алкилсульфосукцинатов, катионные эмульгаторы, амфотерные эмульгаторы.
Парообразующие маты, как правило, представляют собой смесь хлопка и целлюлозы, спрессованные в щитки размером приблизительно 35х22х3 мм, обработанные концентратом (до 0,3 мл), одержащим активиный ингредиент в органичеком растворителе, и возможно антиоксидант, краситель и ароматический компонент. Инсектицид испаряют, используя источник тепла, например, электрический нагреватель матов.
Горючие твердые вещества, как правило, содержат порошок древесины и связывающего вещества, смешанные с активным ингредиентом и сформованным в виде полосок (обычно спиралевидных). Могут быть также добавлены краситель и фунгицид.
Смачивающиеся порошки содержат инертный твердый носитель, один или несколько поверхностно-активных агентов, и возможно стабилизаторы и/или антиоксиданты.
Эмульгируемые концентраты содержат эмульгирующие агенты и часто органический растворитель, такой как, например, керосин, кетоны, спирты, ксилолы, ароматические углеводороды, и другие растворители, известные в данной области техники.
Смачивающиеся порошки и эмульгируемые концентраты, как правило, разбавляются, например водой перед использованием.
Лаки содержат раствор активного ингредиента в органическом растворителе вместе со смолой и возможно пластификатор.
Дезинфицирующие моющие растворы можно приготовлять не только из эмульгируемых концентратов, но также из смачивающихся порошков, мыльных дезинфицирующих растворов и водных суспензий, содержащих соединение формулы (I) в смеси с диспергирующим агентом одним или несколькими поверхностно-активными агентами.
Водные суспензии соединения формулы (I) могут содержать суспензию в воде вместе с суспендирующим, стабилизирующим или каким-либо другим агентом. Суспензии или растворы можно применять per se или в разбавленном виде известным способом.
Жировые препараты (или мази) можно приготовить из растительных масел, синтетических сложных эфиров жирных кислот или из жира с инертной основой, такой как, например, мягкий парафин. Соединение формулы (I) предпочтительно равномерно распределяют в растворе или суспензии. Жировые препараты можно также приготовить из эмульгируемых концентратов, разбавляя их мазевой основой.
Пасты и шампуни также представляют собой полужидкие препараты, в которых соединение формулы (I), может находиться в виде однородной дисперсии в подходящей основе, такой как, например, мягкий или жидкий парафин, или изготовлены на нежировой основе с глицерином, растительным клеем или подходящим мылом. Как и жировые препараты, шампуни и пасты обычно применяют без дальнейшего разбавления и поэтому они должны содержать соответствующий процент соединения формулы (I), требуемый для обработки.
Аэрозольные разбрызгиваемые растворы можно приготовить в виде простого раствора активного ингредиента в аэрозольном пропелленте и сорастворителе, таких как, например, галоидалкилы и вышеуказанные растворители соответственно. Выливаемые на поверхность препараты можно приготовить в виде раствора или суспензии соединения формулы (I) в жидкой среде. Птицу-хозяина или млекопитающее-хозяина можно также защитить от инвазии клещевыми эктопаразитами с помощью ношения ими соответствующим образом профилированных пластмассовых изделий, пропитанных соединением формулы (I). Такие изделия включают пропитанные хомуты, бирки, повязки, пластинки и ленты, закрепленные на соответствующих участках тела. Подходящим материалом для этих изделий является поливинилхлорид (ПВХ).
Концентрация соединения формулы (I), применяемая к животному или к участкам, находящимся на открытом воздухе, меняется в зависимости от выбранного соединения, интервала между обработками, природы препарата (его вида), и предлагаемой инвазии, но, как правило 0,001-20,0% массовых/объемных, и предпочтительно от 0,01-10% соединения можно присутствовать в применяемом препарате. Количество соединения, наносимое на животное, меняется в зависимости от способа применения, размера животного, концентрации соединения в применяемом препарате, способа разбавления препарата и вида препарата, но, как правило, лежит в интервале 0,0001%-0,5% по массе, исключая неразбавленные препараты, например, выливаемые на поверхность, которые, как правило, наносятся в концентрации 0,1-20% предпочтительно 0, 1-10% Количество соединения, применяемого для хранящихся продуктов, как правило, лежит в интервале 0,1-20 ррm. Разбрызгиваемые в пространстве растворы можно применять так, чтобы создать среднюю начальную концентрацию соединения формулы (I), от 0,001 до 1 мг на кубический метр обрабатываемого пространства.
Композиция соединений формулы (I) используется также для защиты и обработки растений, в этом случае применяют такое количество активного ингредиента, которое эффективно по отношению к насекомым, клещевым паразитам и нематодам. Интенсивность применения меняется в зависимости от выбранного соединения, вида препарата, способа применения, вида растения, плотности посадки растения и вероятного заражения, а также от других подобных факторов, но, как правило, обычная норма для сельскохозяйственных культур лежит в интервале от 0,001 до 3 кг/га, предпочтительно в интервале 0,01-1 кг/га. Обычно применяемые в сельском хозяйстве препараты содержат от 0,0001% до 50% соединения формулы (I), обычно 0,1-15% по массе соединения формулы (I).
Пылевидные, жировые, пастообразные и аэрозольные препараты обычно применяют произвольным способом, как это описано выше, и в применняемом препарате может содержаться 0,001-20% массовых/объемных соединения формулы (I).
Найдено, что композиции соединений формулы (I) обладают активностью по отношению к обыкновенной мухе комнатной (Musca domestica). Кроме того, определенные соединения формулы (I) обладают активностью по отношению к другим членистоногим-вредителям, включая Myzus persical, Fetranychus urticae. Plutella xylostella, Culex spp. Tribolium costasieum, Sitophilus granarius, Periplaneta americana и Blattella germanica. Композиции изобретения таким образом полезны при борьбе с членистоногими, например, с насекомыми и клещами, в любой области, где они являются вредителями, например, в сельском хозяйстве, в живодноводстве, в народном здравоохранении и в быту.
Соединения I можно сочетать с одним или несколькими другими ингредиентами, обладающми пестицидной активностью (например, пиретроидами, карбаматами и органофосфатами) и/или с аттрактантами, репеллентами, бактериоцидами, фунгицидами, нематоцидами, гельминтоцидами и им подобными. Найдено, что активность заявляемых соединений можно увеличить добавлением синергиста или потенциирующего средства, например одного из синергистов класса ингибиторов оксидаз, такого как, например, пиперониблутоксид; второго соединения формулы I или пиретроидного пестицидного соединения. Когда в композиции присутствует синергист ингибитор оксидазы, отношение синергиста к соединению формулы (I) лежит в интервале от 25:1 до 1:25, например, около 10:1.
Стабилизаторы для предотвращения какого-либо химического разрушения, которому могут подвергаться заявляемые соединения, включают, например антиоксиданты (такие как, например, токоферолы, бутилоксианизол и бутилокситолуол) и органические или неорганические основания, например, триалкиламины, например, триэтиламин.
Примеры композиций.
1. Эмульгируемый концентрат Соединение формулы (I) 10,00
Алкилфенолэтоксилатх 7,50 Алкиларилсульфонатх 2,50 Ароматический растворитель С8
-С13 80,00

2. Эмульгируемый концентрат Соединение формулы (I) 10,00 Алкилфенолэтоксилатх 2,50 Алкиларилсульфонатх 2,50 Растворитель класса кетонов 64, 00 Ароматический растворитель С8-С13 18,00 Антиоксидант 3,00

3. Смачиваемый порошок Соединение формулы (I) 5,00 Ароматический раствори- тель С8-С13 7,00
Ароматический раство- ритель С18 28,00 Китайская глина 10,00 Алкиларилсульфонатх 1,00
Нафталинсульфоновая кислотах 3,00 Диатомовая земля 46, 00

4. Дуст Соединение формулы (I) 0,50 Тальк 99,50


6. Эмульсионный концентрат Соединение формулы (I) 5,00
Ароматический раство- ритель С8-С13 32,00 Цетиловый спирт 3,00
Моноолеат полиоксиэти- ленглицеринах 0,75
Сложные эфирых полио- ксиэтиленсорбитнах 0,25 Силиконовый раствор 0,1 Вода 58,9

7. Суспензионный концентрат Соединение формулы (I) 10,00 Алкиларилэтоксилатх 3,00 Силиконовый раствор 0,1 Алкандиол 5,0 Мелкодисперсный кизельгур 0,50 Ксантановая смола 0,20 Вода 80,0 Буферный агент 1,2

8. Микроэмульсия Соединение формулы (I) 10,00 Моноолеат полиоксиэти- ленглицеринах 10,00 Алкандиол 4,00 Вода 76,00

9. Диспергируемые в воде гранулы Соединение формулы (I) 70,00 Поливинилпирролидин 2,50 Алкиларилэтоксилат 1,25 Алкиларилсульфонат 1,25 Китайская глина 25,00

10. Гранулы Соединение формулы (I) 2,00 Алкилфенолэтоксилатх 5,00 Алкиларилсульфонатх 3,00 Ароматический раство- ритель С8 -С13 20,00 Гранулы из кизельгура 70,00

11. Аэрозоль (упаковка под давлением) Соединение формулы (I) 0,3 Пиперонилбутоксид 1,5 Насыщенный углеводо- родный растворитель С8-13 58, 2 Бутан 40,0

12. Аэрозоль (упаковка под давлением) Соединение формулы (I) 0,3 Насыщенный углеводородный растворитель С8-С13 10,0 Моноолеат сорбитах 1,0 Вода 40,0 Бутан 48,7


14. Лак Соединение формулы (I) 2,50 Смола 5,00 Антиоксидант 0,50 Высокоароматический уайт-спирит 92,00
15. Разбрызгиваемый раствор (готовый к употреблению) Соединение формулы (I) 0,10 Антиоксидант 0,10 Керосин без запаха 99,8

16. Разбрызгиваемый раствор, содержащий потенцирующее средство (готовый к употреблению) Соединение формулы (I) 0,10 Пиперонилблутоксид 0,50 Антиоксидант 0,10 Керосин без запаха 99,30

17. Микрокапсулированный состав Соединение формулы (I) 10,0
Ароматический раство- ритель С8-13 10,0 Ароматический диизоцианат 4, 5 Алкилфенолэтоксилатх 6,0 Алкилдиамин 1,0 Диэтилентриамин 1,0 Концентрированная соляная кислота 2,2 Ксантановая смола 0,2 Толкоизмельченная дву- окись кремния 0,5 Вода 64,6

х поверхностно-активное вещество;
реагируют с образованием полимочевинных стенок микрокапсулы.
Антиоксидант может представлять собой любое из нижеперечисленных соединений или их
сочетание:
Бутилированный окситолуол
Бутилированный оксианизол
Витамин С
(аскорбиновая кислота)
Получение соединений общей формулы I.
Общие синтетические способы и методики.
Разнообразные соединения были синтезированы и охарактеризованы в соответствии с нижеследующими экспериментальными методиками.
1Н ЯМР-спектры были получены на спектрометре Bruker АМ-250 для раствора в дейтеpохлоpофоpте с использованием тетраметилсилана в качестве внутреннего стандарта; результаты приведены в виде м.д. от количества ТМС, числа протонов, числа пиков, константы спин-спинового взаимодействия I, Гц.
За протеканием реакции удобно также следить с помощью алюминиевых пластинок, предварительно покрытых слоями силикагеля толщиной 0,25 мм, содержащими флюоресцентный индикатор, проявляемых в подходящем растворителе или в смеси растворителей. Температура дана в градусах Цельсия.
Обычно обработку реакционной смеси проводили следующим образом.
Реакционную смесь разделяли между органическим растворителем и водой. Фазы отделяют друг от друга, и органическую фазу промывают как минимум эквивалентным объемом разбавленного водного раствора основания, а затем насыщенным рассолом. Затем органическую фазу сушили над осушителем, обычно над сульфатом магния, и фильтровали. Удаляли летучие растворители, и полученный продукт подвергали соответствующей очистке, после чего использовали в следующей стадии синтеза или анализировали как конечный продукт.
Исходный альдегид, коричную кислоту и амин получали от Aldrich, BDH, Fluorochem, Fluka и Lancaster Synthesis, исключая следующие исходные соединения, получение которых описано ниже.
а) 4-Трифторметоксибензойную кислоту (5 г) (от Fluorochem) в этаноле (100 мл) обрабатывали концентрированной серной кислотой (1 мл). После нескольких часов кипячения с обратным холодильником смесь концентрировали в вакууме, и остаток обрабатывали обычным путем с получением этил-4-трифторметоксибензоата (5 г).
ЯМР1Н: 8,90 2H
[дублет (д)] 7,22 (2Н, д), 4,37 [2Н, квартет (к)] 1,40 3H [триплет (Т)]
Указанный сложный эфир (5 г) в
дихлометане (40 мл) в атмосфере азота при -20о обрабатывали
диизобутилалюминийгидридом 43 мл). После 18 ч при 25о добавляли разбавленную соляную кислоту, и смесь обрабатывали
обычным путем, получая 4-трифторметоксибензиловый спирт, ЯМР1
Н: 7,24 (2Н, д), 7,15 (2Н, д), 4,52 [2H, синглет (с)] 3,37 (3Н, с).
Указанный спирт окисляли, используя условия Swern, a (оксалилхлорид, 2,05 мл; диметилсульфоксид, 3,33 мл, триэтиламин, 14,8 мл), в дихлорметане, получая 4-трифторметоксибензальдегид (4 г).
ЯМР1Н: 10,04 (2Н, с), 7,98 (2Н, д), 7,35 (2Н, д).
b) 4-бром-2-фтортолуол (от Fluorochem) в ледяной уксусной кислоте (88 мл) и уксусным ангидриде (89,7 г), охлаждали до -10о. По каплям добавляли серную кислоту (11,7 г), поддерживая температуру реакции ниже -5о. Триоксид хрома (14,7 г) добавляли порциями при 0оС, смесь выливали в лед (300 г) и обрабатывали обычным путем, получая диацетоксиметил-2-фтор-4-бром-бензол.
Указанный диацетат в этаноле (30 мл) и воде (30 мл) обрабатывали концентрированной серной кислотой (3 мл). После нескольких часов кипячения с обратным холодильником раствор концентрировали, и остаток обрабатывали обычным путем, получая 2-фтор-4-бромбензальдегид (4,89 г).
ЯМР1Н: 10,3
(1Н, с), 7,5 [3Н, мультиплет (м)]
d) К суспензии 4-хлор-3-трифторметиланилина
(от Fluorochem) (15,9 г) в воде (16 мл) добавляли концентрированную соляную кислоту (18 мл). Добавляли лед (30
г) и смесь охлаждали до 0о и обрабатывали раствором нитрида натрия (5,6 г) в
воде (8 мл). Через 15 мин смесь делали нейтральной по конго-рот добавлением раствора ацетата натрия (8 г) в
воде (10 мл). Раствор формальдоксима, приготовленный из гидрохлорида формальдоксима (от
Lancaster) (9,9 г) и ацетата натрия (от BDH), в воде (57 мл), при 10оС обрабатывали сульфатом меди
(2 г) (от BDH) и сульфитом натрия (0,34 г) и затем раствором ацетата натрия (55 г) в воде
(60 мл). Ранее приготовленную смесь (содержащую производное анилина) добавляли по каплям при 10-15о
. После 1 ч при 15о добавляли соляную кислоту (77 мл) и смесь обрабатывали
обычным путем. Очистка дистилляцией (80о, 0,5 мм рт.ст.) давала 4-хлоp-3-трифторметилбензальдегид (1,5
г).
е) К нафтойной кислоте (50 г) (от Аldrich) в ледяной уксусной кислоте при нагревании с обратным холодильником добавляли несколько капель брома (от ВDH), а затем йод (0,5 г) (от BDH). В течение 1 ч по каплям добавляли бром (15 мл). Смесь охлаждали до 25о и перемешивали при этой температуре в течение 18 ч. Образовавшийся белый осадок отфильтровывали, растворяли в горячей воде и обрабатывали концентрированной соляной кислотой. Осадок отфильтровывали и сушили над пятиокисью фосфора (от ВDH), получая 5-бром-2-нафтойную кислоту (перекристаллизация из этанола) (28 г). Температура плавления 261-2о.
ЯМР1H: (DMCl3), 8,60 (1H, c), 8,00 (5Н, м), 7,40 (1Н, м).
Вышеуказанную кислоту (34 г) в этаноле (240 мл) обрабатывали концентрированной серной кислотой (0,5 мл) при нагревании с обратным холодильником в течение 6 ч. Дальнейшая обработка реакционной смеси, осуществленная обычным путем, давала этил-5-бром-2-нафтоат (23 г). Температура плавления: 52-54о .
ЯМР1H: 8,68 (1Н, с), 7,80-8,35 (4Р, м), 7,43 [1Н, двойной дублет (дд)] 4,50 (2Н, к), 1,48 (3Н, т).
П р и м е р 1. (±)-(2

(i) 4-Бромбензальдегид (9,25 г) растворяли в сухом дихлорметане (250 мл) при 25оС в атмосфере азота. Карбометоксиметоксиметилентрифенилфосфоран (17,4 г) (от Lancaster) добавляли к раствору и полученный раствор перемешивали при 25оС в течение 18 ч. Растворитель удаляли в вакууме. Остаток промывали гексаном и отфильтровывали. После удаления гексана в вакууме получали этиловый эфир 4-бромкоричной кислоты (12,12 г).
ЯМР1H: 7,35 (5Н, м), 6,38 (1Н, д), 4,1 (2Н, к), 1,35 (3Н, т).
(ii) Этиловый эфир 4-бромкоричной кислоты (12,12 г) растворяли в сухом дихлорметане (50 мл) в атмосфере азота и охлаждали до -20оС. По каплям добавляли диизобутилалюминийгидрид (100 мл 1М раствора в дихлорметане) (от Aldrich). Раствору давали нагреться до 25оС, затем перемешивали в течение 18 ч, затем разделяли раствор между простым эфиром и разбавленной соляной кислотой. Органическую фазу промывали насыщенным раствором бикарбоната натрия, рассолом, сушили над сульфатом магния и концентрировали в вакууме, получая 3-(4-бромфенил)пропен-2-1-ол (8,9 г).
ЯМР1Н: 7,28 (2Н, д), 7,05 (2Н, д), 6,45 (1Н, д), 6,25 (1Н, т), 4,25 (2Н, д), 2,0 (1Н, с).
(iii) Вышеуказанный спирт (1,07 г) суспендировали в гексане (50 мл) при комнатной температуре и охлажлали до -20о в атмосфере азота. Диэтилцинк (от Aldrich) (22,7 мл 1,1 М раствора в гексане) добавляли по каплям, затем добавляли дийодметан (от Aldrich) (4,1 мл). Давали смеси медленно нагреться до 25оС, затем перемешивали в течение 18 ч. Добавляли насыщенный раствор хлорида аммония и экстрагировали смесь простым эфиром. Совмещенные эфирные экстракты промывали насыщенным раствором тиосульфата натрия сушили над сульфатом магния и удаляли растворители в вакууме. Хроматографическая очистка (силикагель, простой эфир/гексан) давала (±)-
ЯМР1Н: 7,38 (2Н, д), 6,95 (2Н, д), 3,65 (2Н, д), 1,8 (1Н, м), 1,55 (1Н, с), 1,44 (1Н, м), 0, 95 (2Н, м).
(iv) Оксалилхлорид (от Aldrich) (0,22 мл) растворяли в дихлорметане (3 мл) и охлаждали до -70оС в атмосфере азота. По каплям добавляли раствор диметилсульфоксида (от ВDH) (0,36 мл) в дихлорметане (1 мл). Через 5 мин добавляли вышеуказанный спирт (0,53 г) в дихлорметане (4 мл) и перемешивали суспензию при -70оС в течение 30 мин. Добавляли триэтиламин (от Aldrich) (1,6 мл) и давали смеси нагреться в течение 1 ч до 0о . Дальнейшая обработка полученной смеси, осуществленная обычным путем, давала (±)-

ЯМР1Н: 9,4 (1Н, д), 7,33 (2Н, д), 6, 9 (2Н, д), 2,54 (1Н, м), 2,20 (1Н, м), 1,0-1,9 (2Н, м).
(v) Раствор диизопропиламида лития в сухом тетрагидрофуране, приготовленный из н-бутиллития (от Aldrich) (1,6 мл) и диизопропиламина (от Aldrich) (0,4 мл), обрабатывали при -60оС в атмосфере азота раствором триэтил-4-фосфонокротоната (0,58 г) в тетрагидрофуране. Через 2 ч при -60о добавляли вышеуказанный альдегид (0,52 г). После 18 ч при 25оС смесь разделяли между простым эфиром и водой, эфирную фракцию обрабатывали так, как это описано выше. Хроматографическая очистка (силикагель, простой эфир/гексан) давала (± )-этил-5-[транс-2-(4-бромфенил)-циклопропил]пента-2,4-диеноат (0,36 г).
ЯМР1Н: 7,4 (2Н, м), 7,26 (1Н, дд), 6,93 (2Н, д), 6, 28 (1Н, дд), 5,80 (1Н, д), 5,76 (1Н, дд), 4,20 (2Н, к), 2,05 (1Н, м), 1,75 (1Н, м), 1,35 (2Н, м), 1,30 (3Н, т).
(vi) Вышеуказанный сложный эфир (0,18 г) в сухом толуоле добавляли при -10оС к комплексу, приготовленному из триметилалюминия (от Aldrich) (0,62 мл 2М раствора в толуоле) и 1,2-диметилпропиламина (от Aldrich) (0,55 г в сухом толуоле). Полученную смесь нагревали с обратным холодильником в течение 3 ч. обрабатывали 2 N соляной кислотой и отделяли органический слой, который далее обрабатывали так, как это описано выше. Хроматографическая очистка (силикагель, эфир/гексан) давал соединение, указанное в заглавии примера 1, в количестве 0,096 г. Тонкослойная хроматография (силикагель, этилацетат:гексан, 3:7) Rf 0,25, т.пл. 141,9-143,2о С.
Соединения 2-17, 63, 64, 99 и 100,
полученные аналогичным путем с использованием соответствующих альдегида, реагента Виттига и амина, приведены ниже:
Cоединение Название
соединения
2 (±)-(2


3 (±)-(2



4 (±)-(2


5 (±)-(2



6 (±)-(2




7 (±)-(2



8 (±)-(2




9 (±)-(2




10 (±)-(2



11 (±)-(2



12 (±)-(2



13 (±)-(2



14 (±)-(2



15 (±)-(2



16 (±)-(2



17 (±)-(2



63 (±)-(2



64 (±)-(2



99 (±)-(2



100 (±)-(2



П р и м е р 2. (±)-(2



(i) Раствор m-трифторметилкоричной кислоты (10,4 г) в этаноле (120 мл) нагревали с обратным холодильником в присутствии серной кислоты (6 мл) в течение 8 ч. После удаления растворителя в вакууме и обработки, осуществленной обычным путем, получали этиловый эфир m-трифторметилкоричной кислоты (12,1 г).
ЯМР1Н: 7,58 (4Н, м), 6,4 (1Н, д), 4,25 (2Н, к), 1,3 (3Н, т).
(ii-vi) Данное соединение превращали в конечный продукт по аналогии со стадиями (ii)-(vi) примера 1, только вместо 1,2-диметилпропиламина использовали изобутиламин.
Соединение Название соединения
19 (±)-(2



20 (±)-(2



21 (±)-(2

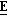

22 (±)-(2



23 (±)-(2



24 (±)-(2
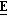



25 (±)-(2




26 (±)-(2



27 (±)-(2
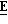


28 (±)-(2



29 (±)-(2



30 (±)-(2



31 (±)-(2


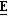

32 (±)-(2



33 (±)-(2

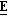

34 (±)-(2




35 (±)-(2




36 (±)-(2



37 (±)-(2



38 (±)-(2



(39) (±)-(2



40 (±)-(2



41 (±)-(2
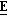


42 (±)-(2



43 (±)-(2



95 (±)-(2



96 (±)-(2



97 (±)-(2
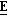


98 (±)-(2



П р и м е р 3. (±)-(2

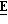

(i) К раствору цис/транс (3: 1) этил-2-формилциклопропилкарбоксилата (1,42 г) (от Aldrich) в дихлорметане в атмосфере азота добавляли при комнатной температуре трифенилфосфин (от Aldrich) (12 г) и четырехбромистый углерод (6,6 г) (от Aldrich). Раствор перемешивали при комнатной температуре в течение трех часов перед его разделением между простым эфиром и водой. После обработки, осуществленной обычным способом, трифенилфосфиноксид удаляли фильтрованием, после чего хроматографическим путем выделяли этил-2-(2,2-дибромэтенил)циклопропилкарбоксилат (2,9 г).
ЯМР1Н: 5,92 (1Н, д), 4,16 (2Н, к, 2,44-0,95 (4Н, м), 1,26 (3Н, т).
(ii) Вышеуказанный сложный эфир (1,8 г) в дихлорметане охлаждали дл -20оС и по каплям добавляли диизобутилалюминийгидрид (12 мл 1М раствора в гексане). Раствор нагревали до 0о и выдерживали при этой температуре перед добавлением 2 N соляной кислоты с последующей обработкой полученной смеси, которую осуществляли обычным путем. В результате получали 2-(2,2-дибромэтенил)-1-оксиметилциклопропан (1,58 г).
ЯМР1Н: 6,0 5,7 (1Н, д), 3,44 (2Н, д), 2,52 (1Н, с), 1,8-1,0 (2Н, м) 0,8 (2Н,
м)
(iii) В вышеуказанный спирт (1,58 г) окисляли, используя условия (Swern'a (оксалилхлорид, 0,6 мл. диметилсульфоксид, 1,0 мл; триэтиламин, 4 мл) в дихлорметане с получением 2-(2,
2-дибромэтенил)циклопропилметаналь, который непосредственно использовали в следующей стадии.
ЯМР1Н: 9,6 9,43 (1Н, д), 5,80 (1Н, д), 2,46-1,82 (2Н, м), 1,82-1,0 (2Н, м).
(iv) Раствор диизопропиламина лития, полученного из н-бутиллития (2,3 мл 1,6 М раствор в гексане) и диизопропиламина (0,55 мл) в сухом тетрагидрофуране, обрабатывали при -60оС триэтилфосфонокротонатом (0,85 г) в ТГФ в атмосфере азота. После выдерживания в течение 2 ч при -60оС к раствору добавляли указанный альдегид. После выдерживания в течение 18 ч при 25оС, смесь разделяли между простым эфиром и водой и обрабатывали обычным путем. Хроматографической очисткой (силикагель, простой эфир/гексан) получали (±)-(2


ЯМР1Н: 7,24 (1Н, дд), 6,28 (1Н, дд), 5,87 (1Н, д), 5,80 (1Н, д), 5,67 (1Н, дд), 4,20 (2Н, к), 1,75 (2Н, м), 1,30 (3Н, т), 1,15 (м).
(v) К раствору вышеуказанного сложного эфира (1,233 г) в этаноле (5 мл) и воде (2 мл) добавляли гидроокись калия (0,25 г). Полученный раствор перемешивали в течение 18 ч перед удалением этанола в вакууме. После добавления разбавленной 2 N соляной кислоты производили экстракцию простым сложным эфиром, сушили над сульфатом магния и концентрировали в вакууме, получая (±)-(2


ЯМР (СD3OD): 7,30 (1Н, дд), 6,45 (1Н, дд), 6,15 (1Н, д), 5,88 (1Н, Д), 5,00 (1Н, с), 1, 92 (2Н, м), 1,28 (2Н, м).
(vi) Вышеуказанную кислоту (0,32 г) растворяли в дихлорметане (5 мл) и добавляли триэтиламин (0,14 мл). Добавляли фенил-N-фенил-фосфоамидохлоридат (от Lancaster). Через 30 минут выдерживали при комнатной температуре добавляли 1,2-диметилпропиламин (0,087 г) и триэтиламин (0,14 мл). Раствор перемешивали в течение 18 часов при комнатной температуре перед обработкой, которую осуществляли обычным путем. Хроматографической очисткой (силикагель, простой эфир/гексан) получали соединение, название которого указано в заглавии примера 3.
П р и м е р 4. (± )-(2



Этерификацию коричной кислоты (7,4 г) проводили обычным путем (этанол, 120 мл; концентрированная серная кислота, 6 мл) с получением этилового эфира коричной кислоты (8,5 г). ЯМР1 Н: 7,55 (1Н, д), 7,15 (5Н, м), 6,2 (1Н, д), 4,05 (2Н, к), 1,15 (3Н, т). Указанный эфир (3,52 г) обрабатывали диизобутилалюминийгидридом (40 мл 1М раствора в гексане) в дихлорметане (40 мл) обычным путем, получая 3-фенил-пропен-2-1-ол (2,8 г).
ЯМР1Н: 7,2 (5Н, м), 6,55 (1Н, д), 6,35 (1Н, т), 4,25 (2Н, д), 1,97 (1Н, с).
Вышеуказанный спирт (2,05 г) в пиридине (1,6 мл) перемешивали с уксусным ангидридом (1,8 г) при 25оС в течение 3 ч перед разделением смеси между простым эфиром и разбавленной соляной кислотой. Последующей обработкой, осуществленной обычным путем, получали 3-фенил-пропенил-2-ацетат. (2,2 г). ЯМР1Н: 7,15 (5Н м), 6,52 (1H, д), 6,22 (1H, т), 4,57 (2H,д)2,00 (3Н, с). Вышеуказанный ацетат (1,65 г) растворяли в диглиме (от ех Aldrich) и добавляли хлордифторацетат натрия (от ех Huorochem) (8,4 г) при 25оС в атмосфере азота. Раствор нагревали до 180оС и выдерживали при этой температуре в течение получаса. После охлаждения до 40оС добавляли следующую порцию хлордифторацетата натрия (6,2 г) и снова нагревали смесь до 180оС, выдерживая при этой температуре еще полчаса. Смесь охлаждали и разбавляли гексаном. Органическую фазу промывали водой, сушили над сульфатом магния и удаляли растворитель в вакууме. Хроматографической очисткой (силикагель; простой эфир/гексан) получали транс-2,2-дихлор-3-фенилциклопропилметилацетат (1,56 г). ЯМР1Н: 7,30 (5Н, м), 4,37 (1Н, дд), 4,26 (1Н, дд), 2,67 (1Н, дд), 2,29 1Н [тройной дублет (тд)] 2,13 (3Н, с).
Вышеуказанный ацетат (1,56 г) перемешивали в течение 18 ч в водном метаноле (10 мл) с углекислым калием (2,94 г). Дальнейшей обработкой, осуществленной обычным путем, получали 2, 2-дифтор-3-фенилциклопропилметанол. (1,08 г ЯМР1H: 7,30 (5Н, м), 3,94 (2Н, м), 2,63 (1Н, м), 2,24 (1Н, м), 1,67 (1Н, с). Вышеуказанный спирт (0,55 г) перемешивали в дихлорметане (6 мл) при 25оС и добавляли пиридиндихромат (2 г) (от Aldrich) и молекулярные сита 3



П р и м е р 5. (±)-(2



3-(4-Бромфенил)пропен-2-1-ол (2,13 г) (см. пример 1) реагировал с уксусным ангидридом обычным путем с образованием 3-(4-бромфенил)пропенил-2-ацетата (2,25 г). ЯМР1Н: 7,35 (2Н, д), 7,08 (2Н, д), 6,52 (1Н, д), 6,10 (1Н, дт), 4,65 (2Н, д), 2,1 (3Н, с). Вышеуказанный ацетат (2,25 г) реагировал обычным путем с хлордифторацетатом натрия с образованием транс-2,2-дифтор-3-(4-бромфенил)циклопропилметилацетата (2,39 г). ЯМР1Н: 7,48 (2Н, д), 7, 1 (2Н, д), 4,30 (2Н, м), 2,62 (1Н, дд), 2, 23 (2Н, м), 2,12 (3Н, с).
Вышеуказанный ацетат (2,39 г) реагировал обычным путем с углекислым калием (2,36 г) с образованием 2, 2-дифтор-3-(4-бромфенил)циклопропилметанола (1,93 г). ЯМР1Н: 7,3 (2Н, д), 7,0 (2Н, д), 3,8 (2Н, м), 3,18 (1Н, с), 2,55 (1Н, м), 2,1 (1Н, м). Вышеуказанный спирт (1,93 г) превращали в целевое соединение способом, аналогичным описанному в стадиях (iii) (vi) примера 3.
(±)-(2



П р и м е р 6. (±)-(2



(i) Бутин-4-он (0,31 г) нагревали при 60оС в течение одного часа с трибутилоловогидридом (от Aldrich) (1,6 г) и азобисизобутиронитрилом (0,01 г) (от Aldrich). Охлаждением и дистилляцией (Кugelrohr 150о, 1 мм рт.ст.) получали 4-трибутилоловобутен-3-1-ол (1,17 г) в виде смеси 1:1 транс:цис изомеров олефина (ссылка) J. K. Stille, Ang. Chem. int. Ed. Engl. 1986, 25, 508). ЯМР1Н: 5,95 (2Н, м), 3,60 (2Н, м), 2,3 (2Н, м), 0,9-2,0 (21Н, м).
(ii) Бис-ацетонитрилпалладийдихлорид (0,01 г) растворяли в сухом диметилдформамиде (10 мл) при 25оС в атмосфере аргона. Добавляли 3-трифторметилиодбензол (1,03 г) (от Fluorochem) в ДМФА, после чего добавляли вышеуказанный спирт (1,17 г). После выдерживания в течение 72 ч раствор разделяли между простым эфиром и 10%-ным раствором гидроокиси аммония и затем обрабатывали обычным путем.
Хроматографической очисткой (силикагель, простой эфир/гексан) получали 4-(3-трифторметилфенил)бутен-3-1-ол (0,67 г) в виде смеси: 1:1 цис:транс изомеров олефина (ссылка i. K. Stille and l. B. L. Groh, i, Am. Chem. Soc. 109, 1987, 815). ЯМР1H: 7,5 (4Н, м), 6,55 (1Н, д), 6,32 (1Н, дт), 3,78 (2Н, м), 2,55 (2Н, м), 1,50 (1Н, с).
(iii-vi). Вышеуказанный спирт превращали в целевое соединение по аналогии со стадиями (iii)-(vi) примера 1.
П р и м е р 7. (±)-(


(i). Этилпропионат (0,98 г) (от Lancaster) и трибутилоловогидрид (3,01 г) с азобисизобутиронитрилом (0,01 г) нагревали при 60оС в течение 18 ч. Охлаждением и хроматографической очисткой (силикагель, простой эфир гексан) получали (Z)-этил-3-трибутилоловопропеноат (1, 9 г) (ссылка i. K. Stille et al. i. Amer. Chem. Soc. 109, 1987, 815), ЯМР1Н: 7,14 (1Н, д), 6,73 (1Н, д), 4,22 (2Н, к), 1,38 (18Н, м), 0,9 (12Н, м).
(ii) Вышеуказанный сложный эфир (0,78 г) растворяли в дихлорметане (4 мл) и охлаждали до -20оС в атмосфере азота. По каплям добавляли диизобутилалюминийгидрид (4 мл 1М раствора в гексане). После 18 ч выдерживания при 25оС аккуратно добавляли разбавленную соляную кислоту, после чего обрабатывали смесь обычным путем, получая 3-трибутилолово-пропен-2-1-ол (0,75 г). ЯМР1Н: 6,72 (1Н, дт), 6,10 (1Н, д), 4,15 (2Н, дд), 1,40 (18Н. м), 0,90 (9Н, м).
(iii-v) Вышеуказанный спирт (0,75 г) превращали в (±)-цис-2-(3-трифторметилфенил)-1-формилциклопропан (0,2 г) способом, аналогичным стадии (ii) примера 6 и стадиям (iii) и ( iv ) примера1. ЯМР1Н: 8,95 (1Н, д), 7,50 (4Н, м), 1,0-2, 5 (4Н, м).
(vi) Вышеуказанный альдегид (0,2 г) перемешивали в дихлорметане (5 мл) с карбоэтоксиметилентрифенилфосфораном в атмосфере азота в течение 18 ч при 25оС; после концентрирования в вакууме остаток промывали гексаном, и после удаления гексана в вакууме получали (+)-(Е)-этил-3-[цис-2-(3-трифторметилфенил)циклопропан] пропен-2-оат (0,18 г). ЯМР1Н: 7, 43 (4Н, м), 6,18 (1Н, дд), 5,94 (1Н, д), 4.06 (2Н, к), 2,62 (1Н, м), 2,09 (1Н, м), 1,55 (1Н, м), 1,34 (1Н, м), 1,22 (3Н, т).
(vii). Вышеуказанный эфир превращали в целевое соединение по аналогии со стадией (vi) примера 1.
П р и м е р 8. (±)-(2



Вышеуказанный спирт (1,35 г) окисляли, используя способ Swern'a (оксалилхлорид, 0, 54 мл; диметилсульфоксид, 0,86 мл; триэтиламин, 3,8 мл), в дихлорметане, получая цис-2-(3-трифторметилфенил)-1-(1-пропен-3-аллил)циклопропан (1,3 г). ЯМР1Н: 9,21 (4Н, д), 7,50 (4Н, м), 6, 28 (1Н, дд), 5,98 (1Н, дд), 2,79 (1Н, м), 2,12 (1Н, м), 1,68 (1Н, м), 1,42 (1Н, м).
Вышеуказанный альдегид (1,3 г) реагировал с карбоэтоксиметилентрифенилфосфораном (1,74 г) по аналогии с примером 7 (vi) с образованием (±)-(2

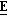
(±)-(2



П р и м е р 9. (±)-(2


К раствору изопропилциклогексиламида лития, получен из 12,5 мл 1,6М раствора н-бутиллития и изопропилциклогексиламина (3,3 мл) (от Aldrich) в ТГФ, добавляли при -60оС этилтриметилсилилацетат (3,6 мл) (от Fluka). После 30 мин выдерживания при -60оС добавляли 4-хлорацетофенон (от Aldrich) (1,55 г). После 18 ч выдерживания при 25оС смесь разделяли между простым эфиром и водой и обрабатывали обычным путем. Хроматографической очисткой (силикагель, простой эфир/гексан) получали этил-3-(4-хлорфенил)-бутен-2-оат (1,22 г) в виде смеси Е:Z изомеров олефина состава 1:1. ЯМР1Н: 7,2 (4Н, м), 5,0 (1Н, м), 4,12 (2Н, м), 1,90 (3Н, с), 1,25 (3Н, м). Вышеуказанный сложный эфир (1,44 г) растворяли в дихлорметане (13 мл) и охлаждали до -20оС. По каплям добавляли диизобутилалюминийхлоргидрид (12,8 мл 1М раствора в гексане). После выдерживания в течение 18 ч при 25оС аккуратно добавляли разбавленную соляную кислоту и обрабатывали полученную смесь обычным путем, получая 3-(4-хлорфенил)бутен-2-1-ол. ЯМР1Н: 7,18 (4Н, с), 5,85 (1Н, т), 4,25 (2Н, д), 3,05 (1Н, с), 2,05 (3Н, с). Вышеуказанный спирт превращали в целевое соединение способом, аналогичным стадиям (iii)-(vi) примера 1.
П р и м е р 10. (±)-(2



Этиловый эфир 3-трифторметилкоричной кислоты (0,98 г) (пример 2) в тетрагидрофуране в атмосфере азота обрабатывали илидом, полученным из изопопилтрифенилфосфониййодида (2,12 г) и н-бутиллития (2,8 мл). После 20 ч выдерживания при 80оС смесь обрабатывали обычным путем. Хроматографической очисткой (силикагель; простой эфир/гексан) получали (±)-н-бутил-[транс-3-(3-трифторметилфенил)- 2,2-диметилциклопропил] -формат (0,78 г). ЯМР1Н: 7, 22 (4Н, м), 4,20 (2Н, м), 2,72 (1Н, м), 2,00 (1Н, м), 1,40 (7Н, м), 0,89 (6Н, м).
Вышеуказанный сложный эфир (0,78 г) растворяли в дихлорметане (12 мл) в атмосфере азота и охлаждали до -20оС. По каплям добавляли диихобутилалюминийгидрид (7,4 мл) и перемешивали раствор при 25оС в течение 18 ч. Аккуратно добавляли разбавленную соляную кислоту, после чего обрабатывали полученную смесь обычным путем, получая (± )-транс-3-(3-трифторметилфенил)-2,2-диметилциклопропил метанол (0,31 г). ЯМР1Н: 7,5 (4Н, м), 3,65 (2Н, д), 2,55 1Н (широкий (ш) с), 1,62 (1Н, д), 1,14 (1Н, м), 1,15 (3Н, с), 0,90 (3Н, с).
Вышеуказанный спирт превращали в целевое соединение способом, аналогичным стадиям (ii)-(vi) примера 1.
(±)-(2



П р и м е р 11. (±)-(2

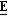

4-Хлорбензальдегид (6,8 г) (от Aldrich) в дихлорметане (250 мл) реагировал с карбоэтоксиметилентрифенилфосфораном (17,5 г) (от Lancaster) при 25оС в течение 18 ч. Проводили концентрирование в вакууме, затем обильно промывали остаток гексаном. Собранные гексановые промывки концентрировали, получая (Е)-этил-3-(4-хлорфенил)-2-метилпропен-2-оат. (11,6 г). ЯМР1Н: 7,35 (4Н, м), 4,25 (2Н, к), 2,05 (3Н, с), 1,31 (3Н, т). Вышеуказанный сложный эфир 11,6 г) растворяли в дихлорметане (100 мл) и охлаждали до -20оС. По каплям добавляли диизобутилалюминийгидрид (100 мл). После 18 часов выдерживания при 25о аккуратно добавляли разбавленную соляную кислоту. Полученную смесь обрабатывали обычным путем, получая (Е)-3-(4-хлорфенил)-2-метилпропен-2-1-ол (8,6 г). ЯМР1Н: 7,34 (2Н, д), 7,22 (2Н, д), 6,49 (1Н, с), 4,18 (1Н, с), 1,90 (3Н, с), 1,66 (1Н, с).
Вышеуказанный спирт обрабатывали диэтилцинком (45,5 мл) и дийодметаном (8,1 мл) в гексане обычным способом, получая (± )-[транс-2-(4-хлорфенил)-1-метилциклопропил]метанол (1,94 г).
ЯМР1Н: 8,94 (1Н, с), 7,30 (2Н, д), 7,06 (2Н, д), 2,68 (1Н, дд), 2,24 (1Н, дд), 1,46 (1Н, дд), 0,98 (3Н, д). Данный продукт был превращен в целевое соединение способом, аналогичным стадиям (iv)-(vi) примера 3.
П р и м е р 12. (-)

3-(3,4-Дихлорфенил)пропен-2-1-ол (1,0 г) (получен по аналогии со стадией (i) примера 2 и стадией (ii) примера 1) окисляли, используя способ Swern'a (оксалилхлорид, 0,5 мл; диметилсульфоксид, 0,7 мл; триэтиламин, 3,4 мл), получая 3-(3, 4-дихлор-фенил)-пропен-2-аль (0,9 г). ЯМР1Н: 9,76 (1Н, д), 7,53 (3Н, м), 7,41 (1Н, д), 6,68 (2Н, дд).
Вышеуказанный альдегид (0,66 г) перемешивали в этаноле (5 мл) с триэтилортоформатом (0,6 мл) (от Aldrich) и нитратом аммония (от Aldrich) (0,01 г) в течение 3,5 ч при 25оС. Концентрированием в вакууме и обработкой обычным путем получали Е-1-(3, 4-дихлорфенил)-3,3-диэтоксибутен-1 (0,97 г). ЯМР1H: 7,32 (3Н, м), 6,79 (1Н, д), 6,19 (1Н, дд), 5,08 (1Н, д), 3,69 (4Н, м), 1,29 (6Н, м).
Вышеуказанную ацеталь (0,67 г) растворяли в бензоле (25 мл) и обрабатывали (+)-L-диизопропилтартратом (0,7 г) (от Aldrich) и п-толуолсульфокислотой (0,01 г) (от Aldrich). Смесь нагревали при 80оС в течение 6 ч, используя прибор Дина-Старка. Раствор охлаждали и обрабатывали обычным путем, получая (-)-4,5-дикарбоизопропокси-2-[(Е)-2-(3,4-дихлорфенил)этенил] -1,3-диоксолан (0,92 г). ЯМР1Н: 7,50 (1Н, д), 7,40 (1Н, д), 7,25 (1Н, дд), 6,74 (1Н, д), 6,25 (1Н, дд), 5,81 (1Н, д), 5,14 (2Н, м), 4,77 (1Н, д), 4,69 (1Н, д), 1,33 (12Н, м).
Вышеуказанная ацеталь (0,9 г) реагировала с диэтилцинком (11 мл) и дийодметаном (1,8 мл) в гексане обычным путем, давая (-(-4,5-дикарбоизопропокси-2-[транс-(2R, 3R)-2-(3,4-дихлорфенил)циклопропил-1] -1,3-диоксолан (0,8 г). [αD-96,1о(с, 0,96, этанол). ЯМР1Н: 7,21 (1Н, д), 7,13 (1Н, д), 6,85 (1Н, дд), 5,05 (1Н, д), 5,02 (2Н, м), 4,65 (1Н, д), 4,52 (1Н. д), 2,08 (1Н, м), 1,47 (1Н, м), 1,21 (12Н, м), 1,14 (1Н, м), 0,92 (1Н, м).
Вышеуказанную ацеталь (0,8 г) нагревали при 70оС в течение 12 ч в тетрагидрофуране (5 мл) в присутствии разбавленной соляной кислоты (3
мл). Обработкой смеси
обычным путем получали (-)-[транс-(2R, 3S)-2-(3,4-дихлорфенил)циклопропил]-метаналь (0,23 г)
ЯМР1Н: 9,39 (1Н, д), 7,39 (2Н, м), 6,94 (1Н, дд), 2,56 (1Н, м),
2,09 (1Н, м), 1,65 (2Н,
м).
Диизопропиламид лития, полученный из н-бутиллития (0,6 мл) в диизопропиламина (0,14 мл), обрабатывали при -60оС в среде тетрагидрофурана триэтил-4-фосфонокротонатом (0, 21 г) в тетрагидрофуране; обработку проводили в атмосфере азота. После 2 ч обработки при -60оС добавляли вышеуказанный альдегид. После выдерживания в течение 18 ч при 25оС добавляли воду и обрабатывали смесь обычным путем. Хроматографической очисткой (силикагель, гексан/простой эфир) получали (-)-(2Е, 4Е)-этил-5-[транс-(2R, 3S))-2-(3, 4-дихлорфенил)циклопропил] пента-2, 4-диеноат (0,16 г). [ αD-304,7о (сО.9, этанол). ЯМР1: 7,28 (3Н, м), 6,88 (1Н, дд), 6,18 (1Н, дд), 5,84 (1Н, дд), 5,78 (1Н, д), 4,10 (2Н, к), 1,90 (2Н, м), 1,20 (5Н, м). Вышеуказанный эфир превращали в целевое соединение способом, аналогичным стадии (vi) примера 1.
(+)-N-изобутил-5-[(1R, 2S)-транс-2-(3, 4-дихлорфенил)циклопропил]пента-2, 4-диенамид (соединение 57) получали аналогичным способом, используя (-)-D-диизопропилтартат (от Aldrich).
П р и м е р 13. (±)-(2



2, 6-Дихлоризоникотиновую кислоту (4,0 г) (приготовленную согласно M. M. Robinson, i. Amer, Chem. Soc. 80, 5481, 1958) растворяли в этаноле (20 мл) и концентрированной серной кислоте (1 мл). После 6 часов нагревания при 80оС раствор охлаждали, концентрировали в вакууме и остаток обрабатывали обычным путем, получая этил 2,6-дихлоризоникотинат (3,7 г).
ЯМР1 Н: 7,84 (2Н, с), 4,48 (2Н, к), 1,48 (3Н, т).
Вышеуказанный сложный эфир растворяли в дихлорметане (60 мл) и охлаждали до -20оС в атмосфере азота. По каплям добавляли диизобутилалюминийгидрид (38 мл). После выдерживания в течение 2 ч при 0оС к смеси добавляли разбавленную соляную кислоту, и полученную смесь далее обрабатывали обычным путем, получая 2, 6-дихлор-4-оксиметилпиридин. ЯМР1Н: 7,64 (2Н, с), 4,98 (2Н, с). Вышеуказанный спирт (1,2 г) окисляли в условиях Swern'a (оксалилхлорид, 0,33 мл; диметилсульфоксид, 0,54 мл; триэтиламин, 2, 35 мл), получая (2, 6-дихлор-4-пиридил)метаналь (1,2 г).
ЯМР1Н: 10,02 (1Н, с), 7,68 (2Н, с). Вышеуказанный альдегид (1,2 г) растворяли в дихлорметане (40 мл) и добавляли карбоэтоксиметилентрифенилфосфоран (2,4 г). После 18 ч выдерживания при 25оС раствор концентрировали в вакууме и остаток промывали гексаном. Собранные гексановые промывки концентрировали в вакууме, получая этил-3(2,6-дихлор-4-пиридил)пропаноат (1,2 г). ЯМР1Н: 7,50 (2Н, д), 2,28 (2Н, с), 6,52 (2Н, д), 4,29 (2Н, к), 1,32 (3Н, т).
Вышеуказанный сложный эфир (0, 25 г) добавляли при 25оС в атмосфере азота в диметилсульфоксиде (4 мл) к илиду, полученному из триметилсульфоксониййодида (0,24 г) и гидрида натрия (0,44 г 60%-ной дисперсии в минеральном масле). После выдерживания в течение 18 ч при 25оС к смеси аккуратно добавляли воду, и полученную смесь обрабатывали обычным путем. Хроматографической очисткой (простой эфир/гексан, силикагель) получали (±)-этил[транс-2-(2,6-дихлор-4-пиридил)циклопропил] формиат (0,12 г). ЯМР1Н: 6,93 (2Н, с), 4,16 (2Н, к), 2,42 (1Н, тд), 1,99 (1Н, тд), 1,69 (1Н, тд), 1,30 (2Н, м), 1,25 (3Н, т).
Вышеуказанный сложный эфир (0,34 г) растворяли в дихлорметане (7 мл) в атмосфере азота и охлаждали до -20оС. По каплям добавляли диизобутилалюминийгидрид (2,9 мл). Через 0,5 ч добавляли метанол (0,5 мл), и затем 2М гидроокись натрия (5 мл). Полученную смесь далее обрабатывали обычным путем. ЯМР1Н: 6,98 (2Н, с), 3,64 (2Н, м), 3,30 (1Н, шс), 0,9-2,0 (4Н, м). Полученный выше спирт (0,21 г) окисляли, используя условия Swern'a (оксалилхлорид, 0,1 мл; диметилсульфоксид, 0,15 мл; триэтиламин, 0,66 мл), получая (±)-транс-2-(2, 6-дихлор-4-пиридил циклопропил метаналь (0,2 г). ЯМР1Н: 9,44 (1Н, д), 6,96 (2Н, с), 1,0-2,6 (4Н, м).
Раствор диизопропиламида лития в тетрагидрофуране (2 мл), полученный из н-бутиллития (0,7 мл) и диизопропиламина (0,16 мл), обрабатывали при -60оС триэтил-4-фосфоно-3-метилкротонатом (0,26 г). После выдерживания смеси в течение 2 ч при -60о к ней добавляли вышеуказанный альдегид (0,2 г). После выдерживания в течение 25оС к полученной смеси добавляли воду, после чего проводили обработку обычным путем. Хроматографической очисткой (силикагель, простой эфир/гексан) получали (+)-(2Е, 4Е)-этил-3-метил-5-[транс-2-(2,6-дихлор-4-пиридил) циклопропил]пента-2,4-диеноат (0,18 г). ЯМР1Н: 6,92 (2Н, с), 6,22 (1Н, д), 5,75 (2Н, м), 4,13 (2Н, к), 2,24 (3Н, с), 1,94 (2Н, м), 1,41 (1Н, м), 1,28 (1Н, м), 1,22 (3Н, т). Вышеуказанный сложный эфир превращали в целевое соединение по аналогии со стадией (vi) примера 1.
П р и м е р 14. (±)-(2

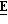

Вышеуказанный аминотолуол (24 г) перемешивали в концентрированной бромистоводородной кислоте (230 мл) при 0оС. Добавляли раствор нитрита натрия (9,8 г) (от BDH) в воде (35 мл), поддерживая температуру реакции между 0 и 5оС. Смесь выливали в раствор бромида меди (37 г) (от BDH) в воде (230 мл) и бромистоводородной кислоте при 50о. После выдерживания в течение 2 ч при 50оС и 18 ч при 25оС смеси добавляли воду и полученную смесь обрабатывали обычным путем. После очистки дистилляцией (100оС, 0,5 мм рт.ст.) получали 3,4-дибромтолуол (12,7 г). ЯМР1Н: 7,53 (2Н, м), 6,95 (1Н, мд), 23,30 (3Н, с). Раствор вышеуказанного производного толуола (5 г) в ледяной уксусной кислоте (20 мл) (от BDH) и уксусным ангидриде (32,6 г) охлаждали до -10оС. По каплям добавляли серную кислоту (7,8 г), поддерживая температуру реакции ниже -5оС. Порциями добавляли триоксид хрома (от ВDН) (6 г), поддерживая температуру реакции между -5 и 0оС. После выдерживания в течение 15 мин при 0оС смесь выливали на лед (150 г) и далее обрабатывали обычным путем, получая диацетоксиметил-3,4-дибромбензол. ЯМР1Н: 7,53 (2Н, м), 6,95 (1Н, дд), 2,50 (6Н, с).
Вышеуказанный диацетат растворяли в смеси вода (15 мл) этанол (15 мл) и добавляли концентрированную серную кислоту (1,5 мл). После кипячении с обратным холодильником в течение 1 ч раствор обрабатывали обычным путем, получая 3,4-дибромбензальдегид, (2,25 г), ЯМР1Н: 10,04 (1Н, с), 7,53 (2Н, м), 6,95 (1Н, дд). Вышеуказанный альдегид (2,25 г) растворяли в дихлорметане (25 мл) и добавляли карбоэтоксиметилентрифенилфосфонар (2,96 ). После выдерживания в течение 18 ч при 25оС раствор концентрировали в вакууме и остаток промывали гексаном. Собранные гексановые отмывки концентрировали в вакууме, получая этил-3-(3,4-дибромфенил)пропеоат (2,4 г). ЯМР1Н: 70,7 (2Н, м), 7,50 (1Н, д), 7,15 (1Н, дд), 6, 32 (1Н, д), 4,26 (2Н, к), 1,33 (3Н, т).
Вышеуказанный сложный эфир (2,4 г) растворяли в дихлорметане (25 мл) в атмосфере азота и охлаждали раствор до -20оС, после чего по каплям добавляли диизобутилалюминийгидрид (14,5 мл). После выдерживания в течение 18 ч при 25оСМ аккуратно добавляли к смеси разбавленную соляную кислоту, и полученную смесь обрабатывали обычным путем, получая 3-(3,4-дибромфенил)пропен-2-1ол. (2,04 г). ЯМР1Н: 7,53 (2Н, м), 7,13 (1Н, дд), 6,56 (1Н, д), 6,20 (1Н, дт), 4,30 (2Н, д), 1,98 (1Н, с).
Вышеуказанный спирт (2 г) обрабатывали в гексане диэтилцинком (35 мл) и дийодметилом (15,52 мл) обычным способом, получая (±)-[транс-2-(3,4-дибромфенил)циклопропил] метанол (1,3 г). ЯМР1H: 7,40 (1Н, д), 7,30 (1Н, д), 6,76 (1Н, дд), 3,53 (2Н, д), 2,30 (1Н, с), 1,68 (1Н, м), 1,33 (1Н, м), 0,87 (2Н, м).
Вышеуказанный спирт превращали в целевое соединение по аналогии со стадиями (iv) (vi) примера 1.
(i) (±)-(2Е, 4Е) N-изобутил-3-метил-5-[транс-2-(3,4-дибромфенил)циклопропил] пента-2,4-диенами д (соединение 60) и (ii) (+)-(2Е, 4Е) N-(2-метилбутенил-2-3-метил-5-[транс-2-(3,4-дибромфенил)циклопропил] пента-2, 4-ди(соединение 93) получали аналогичным способом, используя триэтил-3-метилфосфонокротонат и (i) изобутиламин и (ii) 2-метилпропенил-2-амин соответственно.
П р и м е р 15. (±)-(2



Вышеуказанный аминонитрил (18,7 г) в концентрированной бромистоводородной кислоте (190 мл) обрабатывали при 0оС раствором нитрита натрия (7,6 г) в воде (30 мл). Полученную смесь выливали в раствор бромида меди (28,7 г) в воде (180 мл) и буромистоводородной кислоте (30 мл) при 50оС. После 2 ч выдерживания при 50оС и 18 ч выдерживания при 25оС смесь разбавляли водой и далее обрабатывали обычным путем, получая 3,5-дихлор-4-бромбензонитрил (9,2 г).
ЯМР1Н: 7,63 (2Н, с). Вышеуказанный нитрил (5 г) в простом эфире (100 мл) в атмосфере азота обрабатывали диизобутилалюминийгидридом (22 мл 1М раствора в толуоле). После выдерживания в течение 18 ч при 25о к смеси добавляли 1,4-диоксан (150 мл) и воду (10 мл) и затем разбавленную соляную кислоту (250 мл). После 30 мин выдерживания при 25оС полученную соляную кислоту (250 мл). После 30 мин выдерживания при 25оС полученную смесь обрабатывали обычным путем, получая 3,5-дихлор-4-бромбензальдегид (4,52 г). ЯМР1Н: 9,89 (1Н, с), 7,85 (2Н, с).
Вышеуказанный альдегид превращали в целевое соединение по аналогии с примером 1.
(±)-(2



П р и м е р 16. (±)-(2



Вышеуказанный сложный эфир (3,32 г) в дихлорметане (10 мл) обрабатывали в атмосфере азота при 20оС диизобутилалюминийгидридом (21 мл). После выдерживания в течение 1 ч при 0оС добавляли разбавленную соляную кислоту, и полученную смесь обрабатывали обычным путем, получая 4-(2,2-дибромэтенил)бензиловый эфир (3,18 г). ЯМР1Н: 7,50 (2Н, д), 7,41 (1Н, с), 7,20 (2Н, д), 4,33 (2Н, с), 3,65 (1Н, с).
Вышеуказанный спирт (3,18 г) окисляли, используя условия Swern'a (оксалилхлорид, 0,96 мл; диметилсульфоксид, 1,56 мл; триэтиламин, 6,9 мл), в среде дихлорметана, получая 4-(2,2-дибромэтенил)бензальдегид (2,04 г). ЯМР1Н: 10,94 (1Н, с). 7,86 (2Н, д), 7,61 (2Н, д), 7,45 (1Н, с). Вышеуказанный альдегид превращали в (±)-(2


П р и м е р 17. (±)-(2



(±)-Транс-2-[4-(2,2-дибромэтенил)фенил] циклопропилметанол (1,43 г) (получен так же, как в примере 16) обрабатывали в сухом тетрагидрофуране в атмосфере азота при -40оС н-бутиллитием (8,1 мл). После выдерживания смеси в течение 4 ч при 25оС добавляли воду, и полученную таким образом смесь обрабатывали обычным способом. Хроматографической очисткой (силикагель, простой эфир/гексан) получали (±)-транс-2-(4-этенилфенил)циклопропанметанол (0,62 г). ЯМР1H: 7,41 (2Н, д), 6,90 (2Н, д), 3,30 (2Н, д), 2,95 (1Н, с), 2,59 (1Н, с), 1,85 (1Н, м), 1,34 (1Н, м), 0,90 (2Н, м). Вышеуказанный спирт превращали в целевое соединение по аналогии с примером 1.
П р и м е р 18. (±)-(2






П р и м е р 19. (±)-(2



Вышеуказанный сложный эфир (4 г) растворяли в дихлорметане (30 г) и охлаждали до -20оС в атмосфере азота. По каплям добавляли диизобутилалюминийгидрид (26 мл). После выдерживания в течение 18 ч при 25оС добавляли к смеси разбавленную соляную кислоту, и полученную таким образом смесь обрабатывали обычным путем, получая (±)-(2Z)-3-[транс-2-(3,4-дихлорфенил)циклопропил] -2-фторпропен-2-1-ол (3,3 г). ЯМР1Н: 7,32 (1Н, д), 7,17 (1Н, д), 6,90 (1Н, дд), 4,10 (2Н, дд), 3,60 (1Н, т), 1,90 (2Н, м), 1,20 (2Н, м). Вышеуказанный спирт (3,3 г) окисляли, используя условия Swern'a (оксалилхлорид, 1,2 мл; диметилсульфоксид, 2,0 мл; триэтиламин, 8,8 мл), в среде дихлорметана, получая (±)-(2Z)-3-[транс-2-(3,4-дихлорфенил)циклопропил] -2-фторпропен-2-аль (3,25 г). ЯМР1Н: 9,20 (1Н, д), 7,39 (1Н, д), 7,22 (1Н, д), 6,95 (1Н, дд), 5,60 (1Н, дд), 2,20 (2Н, м), 1,50 (2Н, м).
Вышеуказанный альдегид (0,5 г) растворяли в дихлорметане (5 мл) в атмосфере азота и обрабатывали при 25оС карбоэтоксиметилентрифенилфосфораном (0,67 г). После выдерживания при 25оС в течение 18 ч раствор концентрировали в вакууме и остаток промывали гексаном. Собранные гексановые промывки концентрировали в вакууме, получая (±)-(2Е, 4Z)-этил-4-фтор-5-[транс-2-(3,4-дихлорфенил)циклопропил] пента-2,4-диеноат (0,58 г). ЯМР1Н: 7,30 (1Н, д), 7,00 (3Н, м), 6,05 (1Н, д), 5, 90 (1Н, м), 4,20 (2Н, к), 2,00 (2Н, м), 1,30 (3Н, т), 1,30 (2Н, м). Вышеуказанный сложный эфир превращали в целевое соединение по аналогии со стадией (vi) примера 1.
П р и м е р 20. (±)-(2
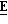
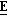

Вышеуказанный спирт (2,0 г) окисляли, используя условия Swern'a (оксалилхлорид, 0,7 мл; диметилсульфоксид, 61 мл; триэтиламин, 5,1 мл), в среде дихлорметана, получая (+)-(3Z)-3-фтор-4-[транс-2-(3,4-дихлорфенил)циклопропил] бутен-3-2-он (1,5 г). ЯМР1Н: 7,30 (1Н, д), 7,10 (2Н, д), 6,95 (1Н, дд), 5,70 (1Н, дд), 2,32 (3Н, д), 2,10 (2Н, м), 1.43 (2Н, м).
Хлорацетилхлорид (от Aldrich) (50 г) добавляли по каплям при перемешивании к изобутиламину (от Aldrich) (70 мл) в среде сухого простого эфира (250 мл) при 0оС. Когда смесь нагрелась до комнатной температуры, ее обрабатывали обычным способом, получив N-изобутил-2-хлорацетамид. Последнее соединение (20 г) нагревали в течение 3 ч при 120оС с триэтилфосфитом (23 г). Смесь подвергли дистилляции в вакууме, получив в результате N-изобутил-дифенилфосфоноацетамид (22,5 г). Темп. кип. 140-142,5оС при 0,1 мм рт.ст.). Раствор диизопропиламида лития в тетрагидрофуране, полученный из н-бутиллития (2,3 мл) и диизопропиламина (0,51 мл), в атмосфере азота при -70о обрабатывали диэтил-N-изобутилфосфоноацетамидом (0,46 г) в сухом тетрагидрофуране. После 2 ч выдерживания смеси при 25оС к ней добавили вышеуказанный кетон (0,5 г). После выдерживания полученной смеси при 25оС в течение 18 ч добавили воду, смесь обработали обычным способом. После хроматографической очистки (силикагель, простой эфир/гексан) получили целевое соединение (0,24 г).
(±)-(2Z, 4E) N-(2-Метилпропенил-2)-3-метил-4-фтор-5-[транс-2-(3,4-дихлорфенил) циклопропил] пента-2/4-диенамид (соединение 94) получали аналогичным способом, используя 2-метилпропенил-2-амин вместо изобутиламина.
П р и м е р 21. (±)-(2



П р и м е р 22. (±)-(2



Вышеуказанный сложный эфир (4 г) в сухом простом эфире обрабатывали при 0оС в атмосфере азота литийалюминийгидридом (0,9 г). После 1 ч выдерживания при 0о и 18 ч выдерживания при 25оС аккуратно добавляли воду и полученную смесь обрабатывали обычным путем, получая 4-бензилбензиловый спирт (2,52 г). ЯМР1Н: 7,21 (9Н, м), 4, 53 (2Н, с), 3,95 (2Н, с), 2,10 (1Н, шс).
Вышеуказанный спирт (2,52 г) окисляли, используя условия Swern'a (оксалилхлорид, 1,2 мл; диметилсульфоксид, 1,8 мл; триэтиламин, 8,8 мл), в среде дихлометана, получая 4-бензилбензальдегид (1,38 г). ЯМР 1Н: 9,93 (1Н, с), 7,78 (2Н, д), 7,33 (2Н, д), 7,20 (5Н, с), 4,04 (2Н, с). Вышеуказанный альдегид превращали в целевое соединение по аналогии с примером 15.
(±)-(2



П р и м е р 23. (±)-(2



Раствор диизопропиламида линия, приготовленного из н-бутиллития (6,25 мл) и диизопропиламина (1,4 мл) в ТГФ (10 мл) при -70оС в атмосфере азота обрабатывали вышеуказанным фосфокротонатом (2,82 г). После 2 ч выдерживания при -70оС добавляли (± )-транс-2-(3,4-дихлорфенил)циклопропилметаналь (2,15 г). После 18 ч выдерживания при 25оС добавляли воду, и полученную смесь обрабатывали обычным способом. После очистки хроматографированием (силикагель, простой эфир/гексан) получали (±)-(2


(±)-(2Z, 4E) N-(2-метилпропенил)-2-фтор-3-метил-5-[транс-2-(3,4-дихлорфенил)циклопропил] пента-2/4-диенамид (соединение 78) получали аналогичным способом, используя 2-метилпропенил-2-амин вместо изобутиламина.
П р и м е р 24. (±)-(2

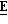

Следующие
соединения были приготовлены, аналогично. Соединение, номер Название соединения
80 (±)-(2



81 (±)-(2
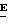


82 (±)-(2
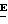



83 (±)-(2



84 (±)-(2



85 (±)-(2



86 (±)-(2




87 (±)-(2

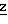


88 (±)-(2



101 (±)-(2




102 (±)-(2




103 (±)-(2

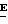

104 (± )-(2



105 (± )-(2




92 (±)-(2




109 (±)-(2
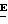



110 (±)-(2

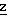
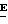

111 (±)-(2




112 (±)-(2




113 (±)-(2



114 (±)-(2




115 (±)-(2




116 (±)-(2




117 (±)-(2




118 (±)-(2



П р и м е р 25. (±)-(2



(±)-(2Е, 4Е) N-Изобутил-3-метил-5-[r-1-хлор-с-2-(3,4-дихлорфенил)циклопропил] пента-2, 4-ди енам(соединение 90) и (±)-(2Z, 4E) N-изобутил-3-метил-[r-1-хлор-с-2-(3,4-дихлорфенил)циклопропил] пента-2,4-диен амид(соединение 91) получали аналогичным способом, используя триэтил-4-фосфано-3-метилкротонат и изобутиламин вместо триэтил-4-фосфонокротоната и 1,2-диметилпропиламина.
П р и м е р 26. (±)-(2



Обработкой вышеуказанного сложного эфира (1,8 г) диизобутилалюминийгидридом (12,6 мл 1М раствора в гексане) в среде дихлорметана получали, после обработки реакционной смеси обычным способом, (±)-3-[транс-2-(3,4-дихлорфенил)циклопропил]пропен-2-1-ол (1,33 г).
Вышеуказанный спирт (1,33 г) окисляли в условиях Sewrn'a (оксалилхлорид, 0,7 мл; диметилсульфоксид, 1,15 мл; триэтиламин, 3,8 мл) в среде дихлорметана, получая (±)-3-[транс-2-(3,4-дихлорфенил)циклопропил]пропен-2-1-аль, который непосредственно использовали в следующей стадии.
К диметилметанфосфонату (15,2 г, 0,1 моль) в тетрагидрофуране (200 мл) добавляли при -70оС н-бутиллитий (62,5 мл, 0,1 моль). Через 30 мин добавляли изобутилизотиоцианат, (5,8 г, 0,05 моль) в тетрагидрофуране (50 мл). Смесь оставляли на ночь при комнатной температуре, затем выливали на смесь лед-вода и экстрагировали простым эфиром. Раствор в простом эфире промывали рассолом, сушили и удаляли растворитель, получая N-изобутил-2-(диэтоксифосфонил)ацетотиоамид.
N-изобутил-2-(диэтоксифосфорил)ацетотиоамид (0,7 г) в тетрагидрофуране (5 мл) добавляли при -70о к диизопропиламиду лития (5,4 ммолей) в тетрагидрофуране (15 мл). Смеси давали нагреться до -20оС, затем охлаждали ее до -40оС.
Полученный ране (±)-3-[транс-2-(3,4-дихлорфенил)циклопропил]пропен-2-аль в тетрагидрофуране (5 мл) добавляли к вышеуказанной смеси. Смесь оставляли на ночь при комнатной температуре, а затем обрабатывали ее обычным путем. Сырой продукт очищали колоночной хроматографией (силикагель, гексан:простой эфир 7:3), получая целевое соединение.
(±)-(2



(±)-(2



Табл. 2. Данные ЯМР1H.
Табл. 3: Физико-химические характеристики, полученных
соединений
Биологические данные
Нижеследующие примеры иллюстрируют пестицидную активность композиций на основе соединений формулы (I):
Пример А тесты с опрыскиванием
Активность заявляемых соединений тестировали, растворяя соединения в ацетоне (5% ) и затем разводя этот раствор смесью вода: "Synperonic" (94,5% 0,5% ) с получением водной эмульсии. Затем
полученный
раствор использовали для обработки следующих насекомых, для которых наблюдалась активность при следующих дозах опрыскивания:
Musca domestica
20 самок Musca помещали в
картонный
цилиндр, оба донышка которого были закрыты марлей. Раствором, содержащим соединение, опрыскивали насекомых и определяли смертность через 48 часов при 25оС.
Следующие
соединения оказались активными при 1000 ррm или менее:
1, 2, 3, 5, 6, 7, 8, 10, 11, 14, 15, 19, 20, 21, 36, 37, 38, 39, 40, 41, 96, 48, 55, 57, 65, 66, 78.
Следующие
соединения оказались активными при 200 ррm или менее:
4, 9, 13, 16, 17, 100, 30, 31, 32, 33, 34, 35, 42, 95, 97, 56, 59, 60, 61, 62, 63, 64, 67, 68, 69, 70, 71, 72, 73, 74, 77, 93,
94, 79, 80,
81, 82, 83, 84, 85, 86, 89, 90, 92, 87.
Plutella xylostella
Листья китайской капусты, зараженные 8 личинками Plutella второй возрастной стадии, опрыскивали
раствором,
содержащим соединение. Смертность определяли через 2 дня при 25оС: Следующие соединения оказались активными при 1000 ррm или менее: 12, 22, 25, 26, 45, 46, 47, 48, 51, 52, 53,
54, 58, 65,
76. Следующие соединения оказались активными при 200 рр или менее: 1, 2, 3, 4, 5, 6, 7, 9, 11, 13, 14, 15, 18, 19, 20, 21, 23, 24, 27, 28, 29, 30, 31, 32, 34, 36, 41, 42, 95, 44, 50, 57,
61, 66.
Следующие соединения оказались активными при 40 ррm или менее: 8, 10, 16, 17, 33, 35, 37, 38, 39, 40, 97, 55, 56, 59, 60, 62, 63, 64, 67, 68, 69, 70, 71, 72, 73, 74, 77, 78, 93, 79, 80, 81,
90, 92,
87.
Tetranychus urticae
Зараженные листья фасоли обыкновенной опрыскивали раствором, содержащим соединение. Смертность определяли через 2 дня при 25оС:
Следующие соединения оказались активными при 1000 ррm или менее:
8, 12, 13, 16, 17, 18, 21, 26, 28, 31, 33, 34, 37, 54, 56, 57, 59, 60, 61, 63, 67, 69, 70, 77, 78, 93, 80, 82, 83, 84,
85, 92,
87.
Spodoptera littoralis
Незараженные листья опрыскивали тестируемым раствором, содержащим соединение, и давали листьям высохнуть. Затем листья были заражены 10
новорожденными личинками. Смертность определяли через 3 дня.
Следующие соединения оказались активными при 1000 ррm или менее:
1, 5, 6, 7, 13, 14, 15, 100, 18, 20, 21, 29, 34,
36, 37, 38, 40, 41, 42, 95, 44, 46, 49, 50, 51, 53, 55, 63, 65, 66, 67, 91.
Следующие соединения оказались активными при 200 ррm или менее:
3, 4, 8, 9, 10, 11, 16, 17, 19,
30,
31, 32, 33, 35, 39, 96, 97, 56, 57, 59, 60, 61, 62, 64, 68, 69, 70, 71, 72, 73, 74, 77, 78, 93, 94, 79, 80, 81, 82, 83, 84, 86, 85, 89, 90, 92, 87.
Myzus persical
10
взрослых Myzus помещали на лист китайской капусты. Через 24 часа лист опрыскивали раствором, содержащим соединение. Смертность определяли через 2 дня при 25оС.
Следующие
соединения оказались активными при 1000 ррm или менее:
8, 9, 13, 18, 19, 20, 22, 24, 30, 31, 34, 35, 95, 44, 50, 59, 60, 61, 66, 72, 75, 77 78, 93, 94, 82, 83, 84, 85, 86, 92, 87.
Diabrotica undecimpunctata
Личинки второй возрастной стадии и их пищу опрыскивали на фильтровальной бумаге раствором, содержащим соединение. Активность определяли через 2 дня.
Следующие соединения оказались активными при 1000 ррm или менее:
3, 6, 9, 11, 12, 13, 14, 17, 28, 29, 30, 31, 32, 33, 35, 37, 39, 95, 96, 97, 44, 54, 55, 56. 59, 61, 62, 63, 67,
69, 71, 72, 74, 77, 78, 94, 80, 81, 82, 83, 86, 92.
Следующие соединения оказались активными при 200 ррm или менее:
10, 16, 68, 73, 79, 84, 85, 89.
Пример В
тесты с локальным применением
Blatella germanica
На самцов B. germanica локально воздействовали 0,5 мкл раствора соединения в бутаноле (с или без пиперонилбутоксида).
Смертность определяли через 6 дней.
Следующие соединения оказались активными при 10 мкг или менее (+ пиперонилбутоксид):
10, 11, 13, 15, 16, 17, 30, 35, 36, 37,
39, 40, 41,
42, 55, 56, 57, 59, 60, 61,62, 63 64, 67, 68, 69, 70, 71, 72, 73, 74, 77, 78, 94, 79, 80, 81, 82,83, 84, 85, 86, 92, 87
Следующие соединения оказались активными при 10 мкг или
менее (без
пиперонилбутоксида)
1, 8, 9, 20, 21, 30, 31, 32, 33, 34, 95
Далее приводятся данные значений процента поражения насекомых для соединений 1-100 (см. табл. 1).
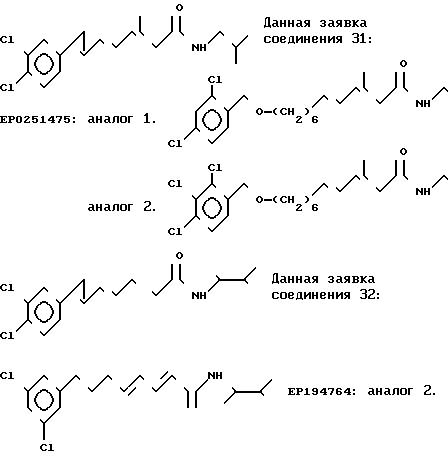
Далее приводятся данные сравнения активности соединений 31 и 32 данного изобретения с ранее известными аналогами.
Сравнительные данные:
Соединение 31 настоящего
изобретения и
аналог этого соединения из заявки на Евр. пат. N 0251475 (структуры соединения см. ниже) сравнивали при испытании против Musca domestica. Аналогично, соединение 32 настоящего
изобретения сравнивали с
аналогом этого соединения из заявки на Евр. пат. N 194764.
(i) Непосредственное применение к комнатной мухе (Musca domestica)
Соединения были
непосредственно применены в
растворе целлозольва без добавок или в сочетании с синергистом (3 или 6 мкг пиперонилбутоксида); смертности за 2 дня приведен ниже в табл. А.
Непосредственное (топическое) применение
к комнатной мухе (Musca domestica)
(2) (Применение опрыскиванием пути комнатной мухи (Musca domestica)
Соединения разбрызгивали в эмульсии
ацетон:вода:смачиватели (5:94:5);
смертности за 2 дня приведен ниже в табл.
Применение опрыскиванием пути комнатной мухи (Musca domestica)
Структура соединений/ испытанных в
сравнении

Реферат
Использование: сельское хозяйство, химическое средство защиты растений. Сущность изобретения: инсектоакарицидная композиция, включающая соединение формулы 1, где Q-фенил, незамещенный или замещеный 1-3 группами,выбранными из группы галоген,C1-C4-алкокси, галоген-C1-C4-алкил, либо Q-фенил, галоген-C1-C4алкокси, замещенный однократно алкенилом C2-C4, нафтил, незамещенный или замещенный галогеном; пиридил; дигалоидвинил; Q1-циклопропил, незамещенный или замещенный C1- C4-алкилом или фтором R2 R3 R4 R5- одинаковы или различны и по крайней мере один представляет водород, а другой независимо друг от друга галоген, C1-C4 -алкил, X-кислород, R1-C-C8 -алкил, возможно замещенный циклопропилом или диоксаланилом; C2-C5-алкенил в количестве 0,1-70%, целевые добавки - остальное. Структура формулы 1.

Формула

где Q - фенил, незамещенный или замещенный 1 - 3 группами, выбранными из группы галоген, С1-С4-алкокси, галоген-С1-С4-алкил, галоген-С1-С4- алкокси, либо Q - фенил, однократно замещенный алкенилом С2-С4, нафтил, незамещенный или замещенный галогеном, пиридил, дигалоидвинил;
Q′ -циклопропил, незамещенный или замещенный С1-С4 -алкилом или фтором;
R2-R5 - одинаковы или различны и по крайней мере один из них представляет водород, а другие независимо друг от друга - галоген, С1-С4-алкил;
Х - кислород;
R1 - С1-С8-алкил, возможно замещенный циклопропилом или диоксаланилом, С2-С5-алкенил,
в количестве 0,1 - 70,0 мас.%, целевые добавки - остальное.

Комментарии