Противомикробная композиция и ее применение для консервирования пищевых продуктов - RU2665094C2
Код документа: RU2665094C2
Чертежи







Описание
ОБЛАСТЬ ТЕХНИКИ
Настоящее изобретение относится к противомикробным композициям, которые могут быть использованы в консервировании пищевых продуктов. Композиции согласно настоящему изобретению основаны на лактопероксидазной системе и содержат помимо лактопероксидазы также глюкозооксидазу, тиоцианат и необязательно глюкозу. Настоящее изобретение также относится к применению таких композиций в консервирования пищевых продуктов, способах консервирования пищевых продуктов и пищевых продуктов, содержащих эти композиции.
УРОВЕНЬ ТЕХНИКИ
Порча продуктов является следствием различных природных процессов, которые неизбежно возникают с течением времени при хранении пищевых продуктов. Порча продуктов, как правило, характеризуется ухудшением органолептического восприятия или качества пищевого продукта, часто в большей или меньшей степени связана с риском для здоровья потребителя. Порче продуктов способствуют как внутренние, так и внешние факторы, влияющие на широкий спектр физико-химических процессов и свойств пищевых продуктов. Источником одного из основных результатов порчи продуктов является микробная контаминация пищевых продуктов, такая как контаминация бактериями, вирусами и плесенями или дрожжами. Наряду с тем, что общие гигиенические меры предосторожности могут помочь в продлении срока годности пищевого продукта, часто одно или несколько мер консервирования пищевых продуктов должны быть приняты для того, чтобы гарантировать оптимальное качество и безопасность пищевых продуктов.
В данной области техники известно большое разнообразие способов для сохранения продуктов питания и, следовательно, увеличения сроков хранения. Вообще говоря, среди таких методов сохранения различают как физические, так и химические методы и их комбинации. Известные методики консервирования пищевых продуктов включают термические процедуры, такие как стерилизация или пастеризация, холодные обработки, такие как охлаждение или замораживание, облучение, уменьшение активности воды, например, посредством высушивания или загущения (например, посредством добавления соли или сахара), копчение, вакуумные технологии хранения или хранение в контролируемой/модифицированной атмосфере, посредством кислотной (например, заквашиванием) или щелочной (например, вымачиванием в щелочи) обработки, уменьшением окислительно-восстановительного потенциала (например, антиоксидантами), или добавлением различных искусственных или природных пищевых добавок, выполняющих функцию консерванта или имеющих противомикробные эффекты. Многие методы консервирования пищевых продуктов имеют ряд недостатков, среди которых стоимость для достижения эффективного сохранения является одним из них. Например, физические методы консервации, такие как охлаждение или замораживание, часто требует довольно экстенсивного (и дорогого) холодильного оборудования, которое может быть даже не везде доступно. Также термические обработки требуют значительных затрат энергии, в то время как методы облучения могут представить сами по себе повышенный риск для безопасности и здоровья, помимо того, они дороги. Химические методы консервирования иногда обеспечивают более дешевую альтернативу для многих физических методов консервирования, так как многие компоненты для консервирования являются легко доступными. Однако хорошо известно, что добавка извне многих пищевых консервантов может оказать сильное воздействие на органолептические свойства обрабатываемого пищевого продукта. В то время как, например, добавление соли или сахара, если они добавлялись в больших количествах, может драматически повлиять на вкус пищевого продукта, также незначительные изменения во вкусе, во внешнем виде или запахе пищевых продуктов посредством различных добавок (т.е. консервантов), имеющих менее доминирующие органолептические эффекты, тем не менее могут быть нежелательными. Кроме того, общественное признание искусственных консервантов стремительно сокращается в том смысле, что многие люди в настоящее время предпочитают продукты питания с меньшим или без каких-либо ингредиентов ненатурального происхождения.
Лактопероксидаза (LP) представляет собой основный гликопротеин, который содержит гемовую группу. Как и в целом пероксидазы, LP катализирует реакцию, в которой пероксид водорода восстанавливается, а соответствующий донор электронов окисляется. LP встречается в природе в нескольких биологических жидкостях или выделениях, таких как секреты слизистой оболочки желез: молочных, слюнных и других желез. LP также может быть найдена в существенных количествах, например, в коровьем молоке. Сама по себе LP не обладает антибактериальным эффектом, но в сочетании с определенными субстратами, тиоцианатом (SCN-) и перекисью водорода (H2O2), образует мощную противомикробную систему, в совокупности называемую лактопероксидазной системой (LPS).
Хорошо известно, что пероксид водорода образует комплекс с LP; этот комплекс окисляет тиоцианат (SCN-) до сульфата, двуокиси углерода, аммиака и воды через неустойчивый промежуточный продукт окисления, который является ингибитором для некоторых бактерий, однако убивает другие бактерии, включая некоторые патогены (то есть проявляет бактерицидный эффект). Многие грамположительные бактерии, такие как Lactococcus sp и Lactobacillus sp ингибируются, то время как многие грамотрицательные бактерии, такие как Escherichia coli, Pseudomonas sp, Salmonella sp убиваются. По всей видимости, что противомикробные эффекты обусловливаются оксикислотами тиоцианата, например OSCN-.
В молоке LPS может быть "активирована" добавлением пероксида водорода или соответствующего источника пероксида водорода, возможно, с добавлением тиоцианата, хотя последний также эндогенно присутствует в молоке. Применение LPS для сохранения молока, следовательно, существенно зависит от действия LP, которая эндогенно присутствует в молоке, к которому добавляются один или несколько дополнительных компонентов LPS. GB 1468405, например описывает добавление глюкозы и глюкозооксидазы, которые совместно приводят к образованию пероксида водорода, к молоку для того, чтобы активировать LPS и, следовательно, продлить срок хранения молока.
Было установлено, однако, что например, добавление глюкозооксидазы может привести к искажению вкуса. Также удлинение срока годности пищевых продуктов может не быть полностью удовлетворительным посредством использования LPS, как известно в настоящее время. Таким образом, существует потребность в данной области техники для дальнейшего улучшения LPS, в особенности для использования в пищевой промышленности, которая не ограничивается молочными продуктами, с тем чтобы гарантировать оптимальную возможность сохранения, таким образом, обеспечения качества пищевых продуктов и безопасности, с отсутствием или минимальным эффектом на вкус или другие свойства, например на другие органолептические свойства, в то же время существенно удлиняя срок годности.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
Нежелательная пролиферация микробов в продуктах питания приводит сначала к ухудшению, а затем к порче вследствие разложения. Именно поэтому срок годности продукта не обязательно означает его свежесть, и не может быть определен посредством оценки времени исключительно до порчи. В равной степени важно учитывать постепенное ухудшение во внешнем виде, запахе, текстуре и вкусе, что происходит задолго до порчи. Изобретатели неожиданно обнаружили, что эти и вышеописанные цели могут быть достигнуты посредством применения к пищевым продуктам композиции, имеющей определенные концентрации компонентов LPS. Соответственно, в первом аспекте, настоящее изобретение относится к композиции, содержащей
(i) 1125-31875 Ед/100 г глюкозоксидазы (GOD), предпочтительно 1500-25500 Ед/100 г GOD;
(ii) 30000-1562500 Ед/100 г лактопероксидазы (LP), предпочтительно 40000-1250000 Ед/100 г LP;
(iii) 1,275-6,25 мас. % тиоцианата (SCN), предпочтительно 1,7-5,0 мас. % SCN; и
(iv) 0-37,5 мас. % глюкозы, предпочтительно 0-30 мас. % глюкозы.
Неожиданно было обнаружено, что композиции, имеющие эти концентрации, а также эти соотношения компонентов LPS при нанесении на пищевые продукты не только приводят к значительным улучшениям, касающимся времени хранения различных пищевых продуктов, но делает это без причинения существенного отклонения вкуса, текстуры, внешнего вида и/или других органолептических свойств. Кроме того, хорошо определенные композиции, как описанные в настоящем изобретении, допускают единообразное применение и результаты с минимальной изменчивостью эффективности. Кроме того, компоненты LPS являются естественными компонентами, такими, что добавление LPS-композиций, как описанные в данном документе, не влечет за собой добавку к пищевым продуктам искусственных консервантов. Композиции по настоящему изобретению являются эффективными как для удлинения срока годности пищевых продуктов, так и для сохранения своей свежести на более длительный период. В этом контексте эти композиции способны действовать как бактериостатические, так и как бактерицидные, хотя действие не ограничивается бактериальными контаминациями, но также включает в себя другие микроорганизмы, такие как дрожжи и плесень.
В одном варианте осуществления композиция содержит 0,075-2,125 мас. % GOD, предпочтительно 0,1-1,7 мас. % GOD и 0,03-1,57 мас. % LP, предпочтительно 0,04-1,25 мас. % LP.
В другом варианте осуществления композиция содержит по меньшей мере 0,5 мас. % глюкозы.
В другом варианте осуществления композиция представляет собой сухую композицию, предпочтительно порошок.
В другом варианте осуществления композиция представляет собой пищевую композицию.
В другом аспекте настоящее изобретение относится к композиции, как описанной в настоящем изобретении, в качестве пищевого консерванта.
В одном варианте осуществления указанный пищевой продукт выбирается из молочных продуктов, фруктовых и овощных соков, соусов, заправок, паст, (жидких) яичных продуктов, сыров и салатов.
В дополнительном аспекте настоящее изобретение относится к пищевому продукту, содержащему композицию, как описано в настоящем изобретении, где указанный пищевой продукт выбирается из молочных продуктов, фруктовых и овощных соков, соусов, заправок, паст, (жидких) яичных продуктов, сыров и салатов.
В одном варианте осуществления указанный пищевой продукт содержит 50-400 м.д. композиции, как описано в настоящем изобретении, предпочтительно 250-350 м.д., наиболее предпочтительно 300 м.д.
В другом аспекте, настоящее изобретение относится к пищевому продукту, с добавкой на 100 г указанного пищевого продукта:
(i) 0,056-12,75 Ед GOD, предпочтительно 0,45-7,65 Ед GOD;
(ii) 1,5-625 Ед LP, предпочтительно 12-375 Ед LP;
(iii) 0,063-2,5 мг SCN-, предпочтительно 0,51-1,5 мг SCN; и
(iv) 0-15 мг глюкозы, предпочтительно 0-9 мг глюкозы.
В одном варианте осуществления указанный пищевой продукт добавлял на 100 г указанного пищевого продукта 0,0037-0,85 мг GOD, предпочтительно 0,03-0,51 мг GOD и 0,0015-0,625 мг LP, предпочтительно 0,012-0,375 мг LP.
В другом аспекте настоящее изобретение относится к способу сохранения пищевого продукта, включающий добавление 50-400 м.д., предпочтительно 250-350 м.д., наиболее предпочтительно 300 м.д. композиции, как описано в настоящем изобретении, в пищевой продукт или компонент пищевого продукта.
В одном из вариантов осуществления указанный способ включает добавление 50-400 м.д., предпочтительно 250-350 м.д., наиболее предпочтительно 300 м.д. композиции, как описано в настоящем изобретении, в пищевой продукт или компонент пищевого продукта и подвергание этого пищевого продукта или указанного компонента термической обработке после от 1 до 12 часов, предпочтительно от 4 до 8 часов.
В одном варианте осуществления указанная термическая обработка представляет собой пастеризацию.
В одном варианте осуществления указанный пищевой продукт выбирается из молочных продуктов, фруктовых и овощных соков, соусов, заправок, паст, (жидких) яичных продуктов, сыров и салатов.
Изобретатели неожиданно обнаружили, что композиции согласно настоящему изобретению действуют синергически с термической обработкой в реализации противомикробного действия, такого как, например, бактерицидного и/или бактериостатического эффектов. Применение термической обработки через от 1 до 12 часов обработки с помощью композиции, как определено в настоящем описании, является особенно предпочтительным и увеличивает синергетический эффект между композицией в соответствии с изобретением и термической обработкой.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
Фиг. 1: Количество клеток (log КОЕ/мл) L. monocytogenes, инокулированных в молоке, и хранящихся при 7°C в соответствии с вариантом осуществления настоящего изобретения.
Фиг. 2: Количество клеток (log КОЕ/мл) в L. brevis, инокулированных в молоке, и хранящихся при 7°C в соответствии с различными вариантами осуществления настоящего изобретения (LPS1, LPS2, LPS3 и LPS4 друг на 300 м.д.).
Фиг. 3: Количество клеток (log КОЕ/мл) штамма Е. coli O157:Н7, инокулированных в молоке и хранящихся при 7°C в соответствии с вариантом осуществления настоящего изобретения.
Фиг. 4: Рост молочнокислых бактерий в заправках (с или без LPS) при 22°C.
Фиг. 5: Процесс изменения pH в заправках (с или без LPS) в соответствии с вариантом осуществления настоящего изобретения.
Фиг. 6: Влияние LPS на процесс изменения количества клеток (log КОЕ/мл) Salmonella spp., инокулированных в цельную яичную массу, хранившуюся 8 ч при 7°C, а затем пастеризованную при 55°C в соответствии с вариантом осуществления настоящего изобретения.
Фиг. 7: Общее количество аэробных психротропных клеток (инкубация при 22°C) (log КОЕ/мл) в молоке, хранящемся в течение 8 ч при 7°C, в зависимости от добавления LPS перед пастеризацией (72°C в течение 15 с) в соответствии с вариантом осуществления настоящего изобретения.
Фиг. 8: Общее количество аэробных психротропных клеток (инкубация при 22°C) (log КОЕ/мл) в молоке, хранящемся в течение 8 ч при 7°C, в зависимости от добавления LPS перед пастеризацией (72°C в течение 15 с) в соответствии с вариантом осуществления настоящего изобретения.
Фиг. 9: Общее количество аэробных психротропных клеток (инкубация при 22°C) (log КОЕ/мл) в сыром молоке, в которое LPS добавляли в соответствии с вариантом осуществления настоящего изобретения. После добавления молоко хранилось в течение 4 часов при 7°C, после чего его пастеризовали (72°C длительностью 15 с). Молоко далее хранилось при 12°C в течение 7 дней.
Фиг. 10: Общее количество аэробных психротропных клеток (инкубация при 22°C) (log КОЕ/мл) в сыром молоке, в которое LPS добавляли в соответствии с вариантом осуществления настоящего изобретения. После добавления молоко хранили в течение 4 часов при 7°C, после чего его пастеризовали (72°C длительностью 15 с). Молоко далее хранилось при 12°C в течение 7 дней.
Фиг. 11: Количество клеток молочнокислых бактерий (log КОЕ/мл) в сыром молоке, в которое LPS добавляли при различных концентрациях в соответствии с вариантом осуществления настоящего изобретения. После добавления молоко хранили в течение 8 ч при 7°C, после чего его пастеризовали (72°C длительностью 15 с). Молоко далее хранилось при 12°C в течение 7 дней.
Фиг. 12: Количество клеток аэробных психротропных бактерий (log КОЕ/мл) в сыром молоке, в которое LPS добавляли при различных концентрациях в соответствии с вариантом осуществления настоящего изобретения. После добавления молоко хранили в течение 8 ч при 7°C, после чего его пастеризовали (72°C длительностью 15 с). Молоко далее хранилось при 12°C в течение 7 дней.
Фиг. 13: Влияние LPS на процесс изменения количества клеток (log КОЕ/мл) Salmonella spp., инокулированных в цельную яичную массу, хранящуюся 8 ч при 7°C, а затем пастеризованную при температуре 55°C.
Фиг. 14: Влияние LPS на процесс изменения общего количества аэробных психротропных клеток (log КОЕ/мл; инкубации при 22°C) в салате с сурими, икокулированном молочнокислыми бактериями, хранящемся при 7°C.
Фиг. 15: Влияние LPS на процесс изменения общего количества анаэробных психротропных клеток (log КОЕ/мл; инкубации при 22°C) в салате с сурими, инокулированном молочнокислыми бактериями, хранящемся при 7°C.
Фиг. 16: Влияние LPS на процесс изменения количества клеток (log КОЕ/мл) молочнокислых бактерий (инкубации при 22°C) в салате с сурими, инокулированном молочнокислыми бактериями, хранящемся при 7°C.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Как используется в настоящем описании, формы единственного числа включают в себя как единственное, так и множественное число определяемых объектов, если контекст явно не диктует иное.
Термины "содержащий", "содержит" и "состоящий из", используемые в настоящем описании, являются синонимами "включающий", "включает" или "содержащий", "заключает в себе" и являются охватывающими или неограничивающими терминами и не исключает дополнительных, неперечисленных членов, элементов или этапов способа. Следует иметь в виду, что термины "содержащий", "содержит" и "состоит из", как используется в настоящем описании, включают термины "состоящий из"; "состоит" и "состоит из", а также термины "состоящий по существу из», "состоит по существу" и "по существу состоит из".
Перечисление числовых диапазонов конечными точками включает все числа и части, включенные в категорию в пределах соответствующих диапазонов, а также перечисленные конечные точки.
Термины "около" или "приблизительно", используемые в настоящем описании при ссылке на измеряемую величину, такие как параметр, величина, временная длительность и т.п., предназначены для охвата вариации +/-20% или менее, предпочтительно +/-10% или менее, более предпочтительно +/-5% или менее, и еще более предпочтительно +/-1% или менее от указанного значения, поскольку такие изменения являются подходящими для выполнения в раскрываемом изобретении. Следует понимать, что значение, к которому модификатор "около" или "приблизительно" относится, само также конкретно и предпочтительно, раскрывается.
В то время как термины "один или несколько" или "по меньшей мере один", такие как, один или более или, по меньшей мере один член(ы) группы членов, определяется по существу, посредством дополнительной экземплификации, термин охватывает, в частности ссылки на любой из указанных членов, или любые два или более из указанных членов, таких как, например, любой ≥3 ≥4, ≥5, ≥6 или ≥7 и т.д. указанных членов, и вплоть до всех указанных членов.
Все ссылки, приведенные в настоящем описании, включены в настоящем описании посредством ссылки в полном объеме. В частности, идеи всех ссылок в данном описании конкретно упоминается посредством ссылки.
Если не указано иное, все термины, используемые в раскрытии изобретения, включая технические и научные термины, имеют значение, которое обычно понимается специалистом с обычной квалификацией в данной области техники, к которой это изобретение принадлежит. Посредством дальнейших указаний, терминологические определения включены для лучшей оценки идей настоящего изобретения.
В следующих пассажах, различные аспекты настоящего изобретения будут определены более детально. Каждый аспект, так определяется, может быть объединен с любым другим аспектом или аспектами, если четко не указано противоположное. В частности, любой признак, указанный как предпочтительный или преимущественный, может быть объединен с любым другим признаком или признаками, указанными как предпочтительные или преимущественные.
Ссылка в данном описании на «один вариант осуществления» или «вариант осуществления» означает, что конкретный признак, структура или характеристика, описанные в связи с вариантом осуществления, включены, по меньшей мере в один вариант осуществления настоящего изобретения. Таким образом, появление выражений «в одном варианте осуществления» или «в варианте осуществления» в различных местах по всему данному описанию не обязательно относятся к одному и тому же варианту осуществления, но может относиться. Кроме того, конкретные признаки, структуры или характеристики могут быть объединены любым подходящим способом, как это было бы очевидно специалисту в данной области техники из этого описания, в одном или нескольких вариантах. Кроме того, в то время как некоторые варианты осуществления, описанные в настоящем описании, включают некоторые, но не другие отличительные признаки, включенные в других вариантах, комбинации признаков различных вариантах предназначены находиться в пределах объема изобретения, и образуют различные варианты, как должно быть понятно специалистам в данной области техники. Например, в прилагаемой формуле изобретения, любой из заявленных вариантов осуществления изобретения может быть использован в любой комбинации.
В нижеследующем подробном описании изобретения сделаны ссылки на сопроводительные чертежи, которые образуют часть описания и на которых показаны в качестве иллюстрации только конкретные варианты осуществления, в которых изобретение может быть осуществлено. Следует понимать, что другие варианты осуществления могут быть использованы и структурные или логические изменения могут быть сделаны без отступления от сущности и объема настоящего изобретения. Следующее подробное описание, следовательно, не должно восприниматься в ограничительном смысле, а объем настоящего изобретения определяется прилагаемой формулой изобретения.
Согласно одному аспекту, настоящее изобретение относится к композиции, такой как противомикробная композиция или пищевой консервант, содержащие, состоящие из по существу из или состоящие из:
(i) 1125-31875 Ед/100 г глюкозоксидазы (GOD), предпочтительно 1500-25500 Ед/100 г GOD;
(ii) 30000-1562500 Ед/100 г лактопероксидазы (LP), предпочтительно 40000-1250000 Ед/100 г LP;
(iii) 1,275-6,25 мас. % тиоцианата (SCN), предпочтительно 1,7-5,0 мас. % SCN; и
(iv) 0-37,5 мас. % глюкозы, предпочтительно 0-30 мас. % глюкозы.
В одном варианте осуществления эта композиция содержит от 0,075 до 2,125, предпочтительно, от 0,1 до 1,7 мас. % GOD. В другом варианте осуществления эта композиция содержит от 0,03 до 1,57 мас. % LP, предпочтительно от 0,04 до 1,25 мас. % LP. В предпочтительном варианте осуществления, эта композиция содержит 0,075-2,125 мас. % GOD, предпочтительно 0,1-1,7 мас. % GOD и 0,03-1,57 мас. % LP, предпочтительно 0,04-1,25 мас. % LP.
Согласно другому аспекту настоящее изобретение относится к композиции, такой как противомикробная композиция или пищевой консервант, содержащие, состоящие из по существу из или состоящие из:
(i) 0,075-2,125 мас. % глюкозооксидазы (GOD), предпочтительно 0,1-1,7 мас. % GOD;
(ii) 0,03-1,57 мас. % лактопероксидазы (LP), предпочтительно 0,04-1,25 LP;
(iii) 1,275-6,25 мас. % тиоцианата (SCN), предпочтительно 1,7-5,0 мас. % SCN; и
(iv) 0-37,5 мас. % глюкозы, предпочтительно 0-30 мас. % глюкозы.
Особенно предпочтительные композиции, как описано выше, подробно описаны ниже и содержат:
- 0,5-1,0 мас. %, предпочтительно 0,75 мас. % GOD; 1,0-1,5 мас. %, предпочтительно 1,25 мас. % LP; 3-7 мас. %, предпочтительно 5 мас. % SCN; 25-35 мас. %, предпочтительно 30 мас. % глюкозы; или
- 0,5-1,0 мас. %, предпочтительно 0,75 мас. % GOD; 1,0-1,5 мас. %, предпочтительно 1,25 мас. % LP; 1,4-2 мас. %, предпочтительно 1,7 мас. % SCN; 15-25 мас. %, предпочтительно 20 мас. % глюкозы; или
- 1,4-2 мас. %, предпочтительно 1,7 мас. % GOD; 0,03-0,05 мас. %, предпочтительно 0,04 мас. % LP; 1,4-2 мас. %, предпочтительно 1,7 мас. % SCN; менее 1 мас. %, предпочтительно 0 мас. % глюкозы.
В одном из вариантов осуществления композиции, описанные в настоящем описании, содержат по меньшей мере 0,05 мас. % глюкозы, предпочтительно по меньшей мере 0,1 мас. % глюкозы, такие как, например, 0,05, 0,1, 0,2, 0,3, 0,4, 0,5, 1, 2, 3, 4, 5, 7, 10, 15, 20, 25, 30 или 35 мас. % глюкозы. В одном из вариантов осуществления композиции, как описано в настоящем изобретении, содержат от 0,05 до 37,5 мас. % глюкозы, предпочтительно от 0,1 до 35 мас. % глюкозы.
Глюкозооксидаза (β-D-глюкоза : кислород 1-оксидоредуктаза; GOD) представляет собой оксидоредуктазу, которая катализирует окисление глюкозы, в особенности бета-D-глюкозы, до пероксида водорода и D-глюконо-δ-лактона. Учитывая вышеизложенное, когда речь идет о глюкозе в данном документе, хотя и не исключительно, предпочтительно имеется в виду β-D-глюкоза. Как используется в настоящем описании, термин глюкозооксидаза относится к функциональной глюкозооксидазе, димеру и включающей необходимый окислительно-восстановительный кофактор (например FAD), другими словами, к глюкозооксидазе, имеющей детектируемую каталитическую активность. GOD может быть получена из различных микробных и не микробных источников, среди которых выделенная из Penecillium sp., Aspergillus sp. (в частности, Aspergillus niger) и Saccharomyces sp. или полученная рекомбинантными технологиями. В предпочтительном варианте осуществления GOD получают из Aspergillus niger, предпочтительно получают ферментативно. Предпочтительно GOD обладает активностью между 10000 и 20000 Ед/г, более предпочтительно 15000 Ед/г или около 15000 Ед/г. Как определено в настоящем описании, одна единица GOD - это количество фермента (мг), которое окисляет один мкмоль β-D-глюкозы в минуту, что измеряется как разница поглощения при 500 нм при 37°C и pH 7. В предпочтительном варианте осуществления активность GOD, как описано в настоящем изобретении, составляет от 10 до 20 Ед/мг GOD, наиболее предпочтительно 15 Ед/мг GOD или около 15 Ед/мг GOD. В одном варианте осуществления GOD может быть получена от Amano Enzyme Inc.
Лактопероксидаза (пероксид водорода оксидоредуктаза; LP) является членом семейства ферментов гем-содержащих пероксидаз и катализирует окисление ряда органических и неорганических субстратов перекисью водорода. Как используется в настоящем описании, термин лактопероксидаза относится к функциональной лактопероксидазе, включающей необходимый гем в качестве кофактора, т.е. лактопероксидазе, обладающей детектируемой каталитической активностью. LP может быть получена из различных микробных и не микробных источников, среди которых, выделенная из коровьего молока, или полученная рекомбинантными методиками. Предпочтительно, LP обладает активностью между 500000 и 1500000 Ед/г, более предпочтительно 1000000 Ед/г или около 1000000 Ед/г. Как определено в настоящем описании, одна единица LP соответствует начальному увеличению поглощению (А412), за минуту, вызванному окислением ABTS (2,2'-азинобис(3-этилбензотиазолин-6-сульфоновой кислоты)) при pH 5,0 и 37°C, выраженному на мг образца лактопероксидазы. В предпочтительном варианте осуществления активность LP, как описано в настоящем документе, находится в диапазоне от 500 до 1500 Ед/мг LP, наиболее предпочтительно 1000 Ед/мг LP или около 1000 Ед/мг LP. В одном варианте осуществления LP может быть получена от Amano Enzyme Inc.
Тиоцианат, также известный как роданид или SCN-, представляет собой сопряженное основание тиоциановой кислоты. Тиоцианат представляет собой анион. Композиции согласно настоящему изобретению могут содержать тиоцианат-анион, но могут также содержать тиоцианатные соли, предпочтительно тиоцианат калия или тиоцианата натрия, наиболее предпочтительно тиоцианат натрия. В предпочтительном варианте осуществления композиции, как описано в настоящем изобретении, включают тиоцианатную соль. Концентрации или количества тиоцианата, как определяется в настоящем описании, предпочтительно относятся к концентрации или количеству тиоцианатной соли, предпочтительно натриевой соли тиоцианата.
Следует понимать, что когда речь идет о мас. %, его следует рассматривать, как концентрацию, определяемую как количество компонента в граммах на 100 грамм композиции, содержащей такой компонент (т.е. масса/масса %). Кроме того, когда речь идет о м.д. (частей на миллион), они вычисляется на основе массы. Например, 100 м.д. равны 0,01 мас. % или 100 мг/кг.
Как используется в настоящем описании, композиция, состоящая по существу из LPS-компонентов GOD, LP, SCN- и, возможно, глюкозы, как описано выше, относится к композиции, которая не содержит дополнительных активных ингредиентов. В частности, такая композиция не содержит дополнительных ферментов или субстратов, которые катализируют, приводит к, генерирует или способствует образованию OSCN-. Такая композиция также не содержит дополнительных противомикробных ингредиентов или по меньшей мере не содержит дополнительные ингредиенты, которые функционируют в качестве противомикробных компонентов в концентрации, в которой они присутствуют в композиции. Примеры таких ингредиентов включают, но не ограничиваются этим, ионы галогенов, таких как, например, иодид или бромид, лактоферрин, лизоцим, пероксидазы, и другие пероксидазы, отличные от LP (например, миелопероксидаза), оксидоредуктазы, отличные от GOD, которые приводят к образованию пероксида водорода (например, галактозооксидаза), антибиотики и др.
В одном варианте осуществления настоящее изобретение относится к композиции, как описано в настоящем изобретении, дополнительно содержащей одно или несколько (инертных) вспомогательных веществ или (инертных) наполнителей или носителей. Как используется в настоящем описании, термин инертный в контексте других компонентов относится к компонентам, которые не обладают противомикробным действием компонентов LPS и не влияют иным образом в композициях, как описано в настоящем изобретении. Вспомогательные вещества или наполнители, таким образом, являются нейтральными по отношению к противомикробному действию композиций, как описано в настоящем изобретении. В предпочтительном варианте осуществления композиции, как описанные в настоящем описании, дополнительно содержат сахарозу.
Композиции, как описано в настоящем изобретении, по существу являются противомикробными композициями. Что касается противомикробного действия композиций, как описано выше, следует понимать, что такое действие может включать как предотвращение, так и задержку микробного размножения (т.е. способствует микробному стазу), а также в качестве альтернативы или в дополнение к уничтожению микроорганизмов. Противомикробное действие может приводить микроорганизмы к неспособности к размножению, абсорбируя питательные вещества и поглощая метаболиты. Посредством примера, противомикробное действие, как указано в настоящем описании, может быть бактериостатическое и/или бактерицидное. Следует понимать, что, когда речь идет о качестве пищевого консерванта, как описано в настоящем изобретении, такой пищевой консервант, следует рассматривать в качестве противомикробной композиции.
Соответственно, в одном варианте осуществления настоящее изобретение относится к бактериостатической и/или бактерицидной композиции, содержащей, состоящей по существу из, или состоящей из:
(i) 1125-31875 Ед/100 г глюкозоксидазы (GOD), предпочтительно 1500-25500 Ед/100 г GOD;
(ii) 30000-1562500 Ед/100 г лактопероксидазы (LP), предпочтительно 40000-1250000 Ед/100 г LP;
(iii) 1,275-6,25 мас. % тиоцианата (SCN), предпочтительно 1,7-5,0 мас. % SCN; и
(iv) 0-37,5 мас. % глюкозы, предпочтительно 0-30 мас. % глюкозы.
В одном варианте осуществления эта композиция содержит от 0,075 до 2,125, предпочтительно, от 0,1 до 1,7 мас. % GOD. В другом варианте осуществления эта композиция содержит от 0,03 до 1,57 мас. % LP, предпочтительно между 0,04 и 1,25 мас. % LP. В предпочтительном варианте осуществления, эта композиция содержит 0,075-2,125 мас. % GOD, предпочтительно 0,1-1,7 мас. % GOD, и 0,03-1,57 мас. % LP, предпочтительно 0,04-1,25 мас. % LP.
Согласно другому варианту осуществления настоящее изобретение относится к бактериостатической и/или бактерицидной композиции, содержащей, по существу состоящей из, или состоящей из:
(i) 0,075-2,125 мас. % глюкозооксидазы (GOD), предпочтительно 0,1-1,7 мас. % GOD;
(ii) 0,03-1,57 мас. % лактопероксидазы (LP), предпочтительно 0,04-1,25 LP;
(iii) 1,275-6,25 мас. % тиоцианата (SCN), предпочтительно 1,7-5,0 мас. % SCN; и
(iv) 0-37,5 мас. % глюкозы, предпочтительно 0-30 мас. % глюкозы.
Противомикробное действие композиций, описанных в данном документе, направлено на разнообразные бактерии, как грамположительные, так и грамотрицательные бактерии, вирусы, дрожжи и плесени. В предпочтительном варианте осуществления противомикробное действие композиций, описанных в настоящем описании, направлено на бактерии, как грамположительные, так и грамотрицательные бактерии. Соответственно, в одном аспекте изобретение относится к применению композиций, как описано выше, для уничтожения и/или ингибирования роста и/или размножения видов микроорганизмов, как определено ниже.
Посредством примера, и без ограничения, композиции, описанные в данном документе, являются эффективными против следующих бактерий: Acinetobacter species, Aeromonas hydrophila, Bacillus brevis, Bacillus cereus, Bacillus megaterium, Bacillus subtilis, Burkholderia cepacia, Campylobacter jejuni, Capnocytophaga ochracea, Corynebacterium xerosis, Enterobacter cloacae, Escherichia coli, Haemophilus influenzae, Helicobacter Pylori, Klebsiella oxytoca, Klebsiella pneumoniae, Legionella, Listeria monocytogenes, Micrococcus, luteus, Mycobacterium smegmatis, Mycobacterium abscessus, Neisseria species, Pseudomonas aeruginosa, Pseudomonas pyocyanea, Salmonella species, Selenomonas sputigena, Shigella sonnei, Staphylococcus aerogenes, Staphylococcus aureus, Streptococcus agalactiae, Streptococcus faecalis, Streptococcus mutans, Wolinella recta, Xanthomonas campestris, Yersinia enterocolitica.
Посредством примера, и без ограничения, композиции, как описано в настоящем изобретении, эффективны против следующих вирусов: вируса простого герпеса, вируса иммунодефицита, респираторного синцитиального вируса, эховируса 11, вируса гриппа.
Посредством примера, и без ограничения, композиции, как описано в настоящем изобретении, являются эффективными против следующих дрожжей и плесени: Candida albicans, Aspergillus niger, Colletotrichum musae, Colletotrichum gloeosporioide, Botryodiplodia theobromae, Fusarium monoliforme, Fusarium oxysporum, Rhodotula rubra, Byssochlamys fulva, Sclerotinia.
Противомикробное действие, как описано в настоящем изобретении, например, бактериостатические или бактерицидные эффекты, а также способность композиций консервировать пищу, как описано в настоящем изобретении, могут быть определены непосредственно или опосредованно с помощью методик, известных в данной области техники. Посредством примера, может быть выполнено определение количества микроорганизмов на чашках Петри, в котором процесс изменения микробов можно наблюдать во времени (например, колониеобразующих единиц (КОЕ) микроорганизмов на количество пищевого продукта). Противомикробная активность, как описано в настоящем изобретении, может также быть количественно измерена косвенно посредством измерения образования (концентрации или процесса изменения концентрации) эффективного противомикробного продукта гипотиоцианата (OSCN-), который образуется под действием LPS. Концентрация OSCN- может непосредственно коррелировать с противомикробным действием. OSCN- может быть измерена с помощью методик, известных в данной области техники, таких как колориметрические анализы (например, Nbs-анализа, основанного на окислении окрашенной (5,5) дитиобис-2-нитробензойной кислоты (Nbs) до бесцветной (Nbs)2, посредством OSCN- ионов).
В одном варианте осуществления настоящее изобретение относится к композициям и их применению, как описано в настоящем изобретении, в которых указанная композиция предотвращает, задерживает, и/или ингибирует размножение микробов и/или их рост, предпочтительно размножение и/или рост микроорганизмов, как описано в настоящем изобретении в другом месте. В одном из вариантов осуществления композиции, как описано в настоящем изобретении, предотвращают, задерживают или ингибируют рост микроорганизмов по меньшей мере на 10%, предпочтительно по меньшей мере на 20%, 30%, 40%, 50%, 60%, 70%, 80%, 90%, 100% или больше, например, более предпочтительно на 200%, 300%, 400%, 500% или больше, по сравнению с размножением и/или ростом в отсутствии композиции, как определено в настоящем описании. Как используется в настоящем описании, предотвращение, задержка или ингибирование роста микроорганизмов на определенный процент относится к увеличению времени достижения конкретной концентрации микроорганизмов (например, КОЕ/мл или КОЕ/г). Например, задержка в 10% означает, что это занимает на 10% времени больше для достижения конкретной концентрации микроорганизмов. Этот вариант относится, например, к эффектам ингибирования роста микроорганизма, таким как бактериостатические эффекты композиций, как описано в настоящем изобретении.
В другом варианте осуществления настоящее изобретение относится к композициям и их применению, как описано в настоящем изобретении, в которых указанная композиция убивает микроорганизмы, предпочтительно микроорганизмы, какие описаны в настоящем изобретении в другом месте. В одном из вариантов осуществления композиции, как описано в настоящем изобретении, убивают по меньшей мере 10%, предпочтительно, по меньшей мере, 20%, 30% или 40%, более, предпочтительно по меньшей мере 50%, 60% или 70%, наиболее предпочтительно по меньшей мере 80% или 90%, например, 95, 96, 97, 98, 99% или более. Этот вариант осуществления относится, например, к бактерицидным эффектам, таким как бактерицидные эффекты композиций, как описано в настоящем изобретении.
В одном варианте осуществления настоящее изобретение относится к композиции, как описано в настоящем изобретении, в которой соотношение между LP и GOD (оба выражены в единицах) составляет от 1:1 до 1000:1, предпочтительно между 1,5:1 и 850:1, например, между 2:1 и 700:1, между 5:1 и 300:1 или между 10:1 и 100:1, более предпочтительно между 20:1 и 75:1, еще более предпочтительно между 25:1 и 50:1, такие как 30:1, 35:1, 40:1 или 45:1.
В другом варианте осуществления настоящее изобретение относится к композиции, как описано в настоящем изобретении, в которой отношение между GOD и LP (оба выражены в мг) составляет от 1:30 до 100:1, предпочтительно от 1:20 до 70:1, например, между 1:10 и 50:1, между 1:5 и 20:1, между 1:3 и 10:1 или между 1:2 и 5:1, более предпочтительно от 1:1 до 3:1, еще более предпочтительно между 1,35:1 и 2,5:1, например, 1,4:1, 1,6:1, 1,8:1, 2,0:1, 2,2:1 или 2,4:1.
В другом варианте осуществления настоящее изобретение относится к композиции, как описано в настоящем изобретении, в которой соотношение между GOD (выраженной в единицах) и SCN- (выраженной в г) составляет между 100:1 и 30000:1, предпочтительно между 180:1 и 25000:1, например, между 200:1 и 20000:1, между 400:1 и 15000:1 или между 600:1 и 10000:1, более предпочтительно между 800:1 и 6000:1, еще более предпочтительно между 900:1 и 5100:1, например, 1000:1, 2000:1, 3000:1, 4000:1 или 5000:1.
В другом варианте осуществления настоящее изобретение относится к композиции, как описано в настоящем изобретении, в которой соотношение между LP (выраженной в единицах) и SCN- (выраженной в г) находится между 5000:1 и 1250000:1, предпочтительно между 4800:1 и 1225500:1, например, между 5000:1 и 1000000:1, между 10000:1 и 750000:1, или между 15000:1 и 500000:1, более предпочтительно между 20000:1 и 300000:1, еще более предпочтительно между 23000:1 и 250000:1, например 25000:1, 50000:1, 100000:1, 150000:1 или 200000:1.
В предпочтительном варианте осуществления настоящее изобретение относится к композиции, как описано в настоящем изобретении, в которой соотношение между LP и GOD (оба выражены в единицах) составляет от 25:1 до 50:1, а соотношение между LP (выраженный в единицах) и SCN- (выраженный в г) находится между 23000:1 и 250000:1.
Композиции, как описано в настоящем изобретении, могут быть составлены тем или иным способом, такими как сухие композиции, жидкие композиции, частично жидкие композиции или гелевые композиции. В одном варианте осуществления композиция готовится в виде жидкой композиции, предпочтительно водной композиции. Жидкие композиции могут быть получены посредством растворения отдельных компонентов в жидкости. В другом варианте осуществления композиция готовится в виде геля. Гели могут быть получены посредством добавления соответствующих гелеобразователей к жидкой композиции, также известными в данной области техники, и не будут обсуждаться далее. В предпочтительном варианте осуществления композиция готовится в виде сухой композиции, предпочтительно гранулята, порошка или таблетки, наиболее предпочтительно в виде порошка. Методы приготовления композиций таких, как грануляты, порошки или таблетки, хорошо известны в данной области техники и не будут описываться далее. Композиции, как описано в настоящем изобретении, также могут быть приготовлены в виде сухой композиции, которая может быть предварительно разбавлена в концентрированный раствор, причем концентрированный раствор затем может быть добавлен к пищевому продукту. Специалисту в данной области техники понятно, как сделать предварительно разбавленный концентрированный раствор для того, чтобы прийти к конечной концентрации каждого из компонентов LPS, как описано в настоящем изобретении, в пищевом продукте.
В одном аспекте настоящее изобретение относится к применению композиции, как описано в настоящем изобретении (такой как противомикробная композиция, например, бактериостатическая или бактерицидная композиция), в качестве пищевого консерванта. В еще одном аспекте настоящее изобретение относится к композициям, как определено в настоящем описании, в качестве противомикробных композиций, таких как бактериостатические и/или бактерицидные композиции.
Как используется в настоящем описании, термин пищевой консервант относится к композиции, которая увеличивает срок годности при хранении или срок хранения (который относится, например, к сроку годности) пищевого продукта, и имеет общее значение, известное в данной области техники. В одном варианте осуществления настоящее изобретение относится к композиции, как описано в настоящем изобретении, которое способно удлинить срок годности или срок хранения пищевого продукта по меньшей мере на 10%, предпочтительно по меньшей мере на 20%, 30%, 40%, 50%, 60%, 70%, 80%, 90%, 100% или больше, например, более предпочтительно на 200%, 300%, 400%, 500% или больше, по сравнению со сроком годности или сроком хранения пищевого продукта без добавления композиции, как определено в настоящем описании. Пищевые консерванты, как описано в настоящем изобретении, таким образом, предотвращают, ингибируют и/или замедляют порчу пищевого продукта или разложение, предпочтительно бактериальную порчу посредством предотвращения, задержки и/или ингибирования роста микроорганизмов и/или размножения, как определено в настоящем описании в другом месте, и/или уничтожение, как определено в данном документе в другом месте, микроорганизмов, предпочтительно микроорганизмов, какие определены в настоящем описании в другом месте.
Как используется в настоящем описании, термин пищевой продукт может относиться к любому типу пищевого продукта, как к человеческой пищи, так и пищи для животных. Предпочтительно, пищевой продукт относится к человеческой пище. Следует понимать, что пищевой продукт, о котором говорится в настоящем описании, относится к продукту, который предназначен для потребления, т.е. перорального поступления. Посредством дальнейших указаний, как используется в настоящем описании, к пищевому продукту не относится, например, средства гигиены полости рта, такие как зубные пасты, дезинфицирующие средства для ротовой полости, продукты для гигиены зубов, такие как продукты против зубного камня.
В одном из вариантов осуществления композиции, как описанные в настоящем описании, являются пищевыми композициями. Как используется в настоящем описании, пищевая композиция представляет собой композицию, которая пригодна для потребления, т.е. для перорального поступления, желательно при соответствующем разбавлении, например, при нанесении на пищевой продукт.
В одном аспекте настоящее изобретение относится к пищевому продукту, содержащему композицию, такую как противомикробную композицию или пищевой консервант, как описано в настоящем изобретении. В другом аспекте настоящее изобретение относится к пищевому продукту, к которому добавляется композиция, такая как противомикробная композиция или пищевой консервант, как описано в настоящем изобретении. Следует понимать, что все компоненты композиций, описанных в данном документе, экзогенно наносятся на такие пищевые продукты (в отличие от продуктов питания эндогенно содержащих один или несколько компонентов из описанных в настоящем описании композиций, к котором добавляли экзогенно остаток компонентов).
Пищевые продукты, как описано в настоящем изобретении, могут быть твердыми, гелеобразными, жидкими или частично жидкими пищевыми продуктами. В одном варианте осуществления пищевой продукт, содержащий композицию, как описано в настоящем изобретении, является пищевым продуктом, который по меньшей мере частично жидкий. Как используется в настоящем описании, термин по меньшей мере частично жидкий относится к пищевому продукту, который при температуре окружающей среды и давлении является текучим. Специалисту в данной области техники будет понятно, что вязкость таких продуктов может измениться и, следовательно, определять текучесть пищевого продукта. Частично жидкие пищевые продукты включают в себя, например, также жидкие пищевые продукты, в которых твердые пищевые продукты диспергированы. В другом варианте осуществления пищевой продукт, содержащий композицию, как описано в настоящем изобретении, является твердым или полутвердым пищевым продуктом. В одном варианте осуществления пищевым продуктом является сыр (который может быть мягким или твердым сыром или может быть молодым сыром, т.е. полутвердым сыром). В предпочтительном варианте осуществления пищевой продукт, как описано в настоящем изобретении, выбирается из молочных продуктов, фруктовых и овощных соков, соусов, заправок, паст, (жидких) яичных продуктов, сыров и салатов (таких как, например, салаты на основе майонеза, содержащие овощи, мясо, морепродукты и т.д.). Специалисту в данной области техники будет понятно, что когда пищевой продукт является жидким или полужидким или, возможно, гелеобразным, композиции, как описаны в настоящем описании, могут быть добавлены к пищевой массе, в том случае, когда пищевой продукт является твердыми или, возможно, гелеобразными (в зависимости от консистенции) композициями, описанными в настоящем описании, могут быть добавлены на поверхность пищевого продукта (например, погружением пищевого продукта в жидкую композицию, содержащую LPS, в которой концентрация выбраны так, что конечная концентрация каждого из компонентов LPS на грамм пищевого продукта соответствуют тому, как описано в настоящем изобретении).
Следует понимать, что композиции, как описано в настоящем изобретении, могут также быть добавлены к одному или более компонентам составного пищевого продукта.
В одном варианте осуществления пищевой продукт, как описано в настоящем изобретении, содержит от 50 до 400 м.д. композиции, как описано в настоящем изобретении, такие как, например 50, 75, 100, 125, 150, 175, 200, 225, 250, 275, 300, 325, 350, 375 или 400 м.д. В еще одном варианте осуществления пищевой продукт, как описано в настоящем изобретении, содержит от 50 до 150 м.д. композиции, как описано в настоящем изобретении. В еще одном варианте осуществления пищевой продукт, как описано в настоящем изобретении, содержит от 100 до 200 м.д. композиции, как описано в настоящем изобретении. В еще одном варианте осуществления пищевой продукт, как описано в настоящем изобретении, содержит от 200 до 300 м.д. композиции, как описано в настоящем изобретении. В еще одном варианте осуществления пищевой продукт, как описано в настоящем изобретении, содержит от 300 до 400 м.д. композиции, как описано в настоящем изобретении. В еще одном варианте осуществления пищевой продукт, как описано в настоящем изобретении, содержит от 150 до 250 м.д. композиции, как описано в настоящем изобретении. В еще одном варианте осуществления пищевой продукт, как описано в настоящем изобретении, содержит от 250 до 350 м.д. композиции, как описано в настоящем изобретении. В еще одном варианте осуществления пищевой продукт, как описано в настоящем изобретении, содержит от 250 до 300 м.д. композиции, как описано в настоящем изобретении. В еще одном варианте осуществления пищевой продукт, как описано в настоящем изобретении, содержит от 300 до 350 м.д. композиции, как описано в настоящем изобретении. В другом варианте осуществления пищевой продукт, как описано в настоящем изобретении, содержит от 50 до 100 м.д., от 75 до 125 м.д., от 100 до 150 м.д., от 125 до 175 м.д., от 150 до 200 м.д., от 175 до 225 м.д., от 200 до 250 м.д., от 225 до 275 м.д., от 250 до 300 м.д., от 275 до 325 м.д., от 300 до 350 м.д., от 325 до 375 м.д. или от 350 до 400 м.д. композиции, как описано в настоящем изобретении.
В еще одном аспекте настоящее изобретение относится к пищевому продукту, как описано в настоящем изобретении, содержащему на 100 г пищевого продукта:
(i) 0,056-12,75 Ед GOD, предпочтительно 0,45-7,65 Ед GOD;
(ii) 1,5-625 Ед LP, предпочтительно 12-375 Ед LP;
(iii) 0,063-2,5 мг SCN, предпочтительно 0,51-1,5 мг SCN; и
(iv) 0-15 мг глюкозы, предпочтительно 0-9 мг глюкозы.
В одном из вариантов осуществления этот пищевой продукт содержит на 100 г между 0,0037 и 0,85, предпочтительно между 0,03 и 0,51 мг GOD. В другом варианте осуществления этот пищевой продукт содержит на 100 г между 0,0015 и 0,625 мг LP, предпочтительно между 0,012 и 0,375 мг LP. В предпочтительном варианте осуществления этот пищевой продукт содержит на 100 г 0,0037-0,85 мг GOD, предпочтительно 0,03-0,51 мг GOD и 0,0015-0,625 мг LP, предпочтительно 0,012-0,375 мг LP.
В другом аспекте настоящее изобретение относится к пищевому продукту, как описано в настоящем изобретении, содержащем на 100 г пищевого продукта:
(i) 0,0037-0,85 мг GOD, предпочтительно 0,03-0,51 мг GOD;
(ii) 0,0015-0,625 мг LP, предпочтительно 0,012-0,375 мг LP;
(iii) 0,063-2,5 мг SCN, предпочтительно 0,51-1,5 мг SCN; и
(iv) 0-15 мг глюкозы, предпочтительно 0-9 мг глюкозы.
В другом аспекте настоящее изобретение относится к способу для сохранения пищевого продукта, или одного или нескольких компонентом пищевого продукта, включающий добавление к композиции, как описано в настоящем изобретении, чтобы указанный пищевой продукт или один или несколько из указанных компонентов пищевого продукта. В другом аспекте настоящее изобретение относится к способу для продления срока годности или срока хранения пищевого продукта, включающий добавление композиции, как описано в настоящем изобретении, к указанному пищевому продукту или одному или нескольким компонентом указанного пищевого продукта. В дополнительном аспекте настоящее изобретение относится к способу предотвращения порчи пищевого продукта, в особенности бактериологической порчи пищевого продукта, включающему добавление композиции, как описано в настоящем изобретении, к указанному пищевому продукту или одному или нескольким компонентам указанного пищевого продукта. В другом аспекте настоящее изобретение относится к способу для по меньшей мере частичного ингибирования, предотвращения и/или задержки роста микроорганизмов в пищевом продукте, включающий добавление композиции, как описано в настоящем изобретении, к указанному пищевому продукту или одному или нескольким компонентам указанного пищевого продукта. В еще одном аспекте настоящее изобретение относится к способу для уничтожения по меньшей мере частично микроорганизмов в пищевом продукте, включающий добавление композиции, как описано в настоящем изобретении, к указанному пищевому продукту или одному или нескольким компонентом указанного пищевого продукта. Сроки и условия, определенные в этих аспектах, соответствуют тому, что описано в настоящем документе в другом месте. В вариантах осуществления способы, описанные в указанных выше аспектах, уменьшают количество микроорганизмов, предпочтительно жизнеспособных микроорганизмов, предпочтительно одного или нескольких микроорганизмов, как описано в настоящем изобретении в другом месте. В одном варианте осуществления в соответствии с методами, которые описаны выше, погибает микроорганизмов по меньшей мере 10%, предпочтительно по меньшей мере 20%, 30% или 40%, более предпочтительно по меньшей мере 50%, 60% или 70%, наиболее предпочтительно по меньшей мере 80% или 90%, например, 95, 96, 97, 98 или 99%, предпочтительно один или несколько микроорганизмов, как описано в настоящем изобретении в другом месте.
В одном варианте осуществления настоящее изобретение относится к любому из способов, описанных в данном документе, включающий добавление к пищевому продукту композицию, как описано в настоящем изобретении, до конечной концентрации от 50 до 400 м.д. указанной композиции, такие как, например 50, 75, 100, 125, 150, 175, 200, 225, 250, 275, 300, 325, 350, 375 или 400 м.д. В еще одном варианте осуществления пищевой продукт, как описано в настоящем изобретении, содержит от 50 до 150 м.д. композиции, как описано в настоящем изобретении. В еще одном варианте осуществления пищевой продукт, как описано в настоящем изобретении, содержит от 100 до 200 м.д. композиции, как описано в настоящем изобретении. В еще одном варианте осуществления пищевой продукт, как описано в настоящем изобретении, содержит от 200 до 300 м.д. композиции, как описано в настоящем изобретении. В еще одном варианте осуществления пищевой продукт, как описано в настоящем изобретении, содержит от 300 до 400 м.д. композиции, как описано в настоящем изобретении. В еще одном варианте осуществления пищевой продукт, как описано в настоящем изобретении, содержит от 150 до 250 м.д. композиции, как описано в настоящем изобретении. В еще одном варианте осуществления пищевой продукт, как описано в настоящем изобретении, содержит от 250 до 350 м.д. композиции, как описано в настоящем изобретении. В еще одном варианте осуществления пищевой продукт, как описано в настоящем изобретении, содержит от 250 до 300 м.д. композиции, как описано в настоящем изобретении. В еще одном варианте осуществления пищевой продукт, как описано в настоящем изобретении, содержит от 300 до 350 м.д. композиции, как описано в настоящем изобретении. В другом варианте осуществления пищевой продукт, как описано в настоящем изобретении, содержит от 50 до 100 м.д., от 75 до 125 м.д., от 100 до 150 м.д., от 125 до 175 м.д., от 150 до 200 м.д., от 175 до 225 м.д., от 200 до 250 м.д., от 225 до 275 м.д., от 250 до 300 м.д., до 275 до 325 м.д., от 300 до 350 м.д., от 325 до 375 м.д. или от 350 до 400 м.д. от композиции, как описано в настоящем изобретении. Пищевой продукт для применения в способах, как описано в настоящем документе, описывается подробно в настоящем изобретении в другом месте.
В одном варианте осуществления настоящее изобретение относится к способу, как описано в настоящем изобретении, в котором пищевой продукт контактирует с композицией, как описано в настоящем документе, в течение от 1 до 12 часов, например, в течение 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11 или 12 часов, предпочтительно в течение от 4 до 8 часов, например в течение 4,0, 4,5, 5,0, 5,5, 6,0, 6,5, 7,0, 7,5 или 8,0 часов. В другом варианте осуществления настоящее изобретение относится к способу, как описано в настоящем изобретении, в котором пищевой продукт контактирует с композицией, как описано в настоящем изобретении, при температуре между 5 и 45°C, предпочтительно между 5 и 35°C, например, между 5-30°C, 5-25°C, 5-20°C, 5-15°C, 5-10°C, 10-35°C, 10-30°C, 10-25°C, 10-20°C, 10-15°C, 15-35°C, 15-30°C, 15-25°C, 15-20°C, 20-35°C, 20-30°C, 20-25°C, 25-35°C или 30-35°C. В другом варианте осуществления настоящее изобретение относится к способу, как описано в настоящем изобретении, в котором пищевой продукт контактирует с композицией, как описано в настоящем изобретении, при температуре между 5 и 45°C, предпочтительно между 5 и 35°C, например, между 5-30°C, 5-25°C, 5-20°C, 5-15°C, 5-10°C, 10-35°C, 10-30°C, 10-25°C, 10-20°C, 10-15°C, 15-35°C, 15-30°C, 15-25°C, 15-20°C, 20-35°C, 20-30°C, 20-25°C 25-35°C или 30-35°C в течение от 1 до 12 часов, например, в течение 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11 или 12 часов, предпочтительно в течение между 4 и 8 часами, например в течение 4,0, 4,5, 5,0, 5,5, 6,0, 6,5, 7,0, 7,5 или 8,0 часов.
В одном варианте осуществления настоящее изобретение относится к любому способу, как описано в настоящем изобретении, дополнительно включающему стадию подвергания пищевого продукта или одного или нескольких компонентов пищевого продукта термической обработке после нанесения композиции, как описано в настоящем изобретении.
В предпочтительном варианте осуществления указанный пищевой продукт или указанные один или несколько компонентов указанного пищевого продукта подвергают термической обработке между 1 и 12 часами после нанесения композиции, как описано в настоящем изобретении, например, через 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11 или 12 часов. В предпочтительном варианте осуществления указанный пищевой продукт или указанные один или несколько компонентов указанного пищевого продукта подвергают термической обработке между 4 до 8 часами после нанесения композиции, как описано в настоящем изобретении, например, через 4,0, 4,5, 5,0, 5,5, 6,0, 6,5, 7,0, 7,5 или 8,0 часов. Соответственно, пищевой продукт контактируют с композицией, как описано в настоящем документе, в течение между 1 до 12 часов, например, в течение 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11 или 12 часов, предпочтительно в течение между 4 и 8 часами, например в течение 4,0, 4,5, 5,0, 5,5, 6,0, 6,5, 7,0, 7,5 или 8,0 часов.
Как используется в настоящем описании, термин термическая обработка относится к подверганию пищевого продукта, или одного или нескольких компонентов пищевого продукта, к увеличенной температуре для того, чтобы получить ингибирование роста микроорганизмов и/или противомикробные эффекты, например, термическая обработка приводит к задержке или ингибированию роста микроорганизмов или размножения и/или убивает микроорганизмы. В предпочтительном варианте осуществления термическая обработка представляет собой пастеризацию или включает пастеризацию. Пастеризация хорошо известна в данной области техники. Посредством дальнейших указаний, как используется в настоящем описании, пастеризация относится к процессу нагревания пищевого продукта, который может быть или, как правило, представляет собой жидкость, до определенной температуры в течение предварительно заданного периода времени, как правило, с последующим немедленным охлаждением пищевого продукта. Обычно пастеризации приводит к предупреждению или замедлению порчи продуктов за счет снижения количества жизнеспособных микроорганизмов. Часто, пастеризация не убивает все микроорганизмы, присутствующие в пищевом продукте.
Специалисту в данной области техники будет понятно, что условия пастеризации могут зависеть от типа пищевого продукта, и что обычно существует обратная зависимость между временем обработки и температурой, то есть более высокие температуры требуют более короткое время или более длительное время требует более низких температур, чтобы достичь аналогичных противомикробных эффектов. Посредством примера, и без ограничения, молочные продукты, например, могут быть пастеризованы при температуре 71-74°C в течение около 15-30 с, в результате чего происходит уменьшение жизнеспособных микроорганизмов по меньшей мере на три логарифмические единицы (т.е. уменьшение на 99,9% или больше). Яичные продукты, предпочтительно жидкие яичные продукты, можно, например, пастеризовать при температуре между 60 и 69°C в течение вариабельного времени.
Согласно этому варианту осуществления обработка пищевого продукта или одного или нескольких компонентов пищевого продукта композицией, как описано в настоящем изобретении, перед термической обработкой, предпочтительно пастеризацией, приводит к увеличению противомикробных эффектов, таких как, например, увеличенные антибактериальные, такие как ингибирование роста микроорганизма и/или противомикробные эффекты, то есть срок годности пищевого продукта увеличивается и/или количество жизнеспособных микроорганизмов уменьшается.
Соответственно, в одном варианте осуществления настоящее изобретение относится к любому из способов, описанных в данном документе, дополнительно включающему стадию подвергания пищевого продукта или одного или нескольких компонентов пищевого продукта термической обработке после нанесения композиции, как описано в настоящем изобретении, в котором больше микроорганизмов погибают в результате комбинированной обработки по сравнению с любой единственной обработкой. Было обнаружено, что композиции, как описано в настоящем изобретении, работают синергически с термической обработкой для получения противомикробных эффектов, в частности, предпочтительно антибактериальных эффектов, таких как бактериостатические или бактерицидные эффекты.
В одном варианте осуществления настоящее изобретение относится к комбинированной обработке пищевого продукта, или одного или нескольких компонентов пищевого продукта, композицией, как описано в настоящем изобретении, в соответствии с любым из способов, как описано в настоящем изобретении, и последующей термической обработкой, предпочтительно через 1-12 часов, более предпочтительно через 4-8 часов, чтобы уменьшить количество жизнеспособных микроорганизмов, предпочтительно одного или нескольких микроорганизмов, как описано в настоящем изобретении в другом месте, в результате чего уменьшение составило по меньшей мере четыре логарифмические единицы (т.е. по меньшей мере 10000-кратное уменьшение, или снижение на 99,99%), предпочтительно по меньшей мере пять логарифмических единиц, более предпочтительно по меньшей мере шесть логарифмических единиц или больше.
В другом варианте осуществления настоящее изобретение относится к комбинированной обработке пищевого продукта или одного или нескольких компонентов пищевого продукта композицией, как описано в настоящем изобретении, в соответствии с любым из способов, как описано в настоящем изобретении, и последующей термической обработкой, предпочтительно через 1-12 часов, более предпочтительно через 4-8 часов, чтобы уменьшить количество жизнеспособных микроорганизмов, предпочтительно одного или нескольких микроорганизмов, как описано в настоящем изобретении в другом месте, в результате чего происходит по меньшей мере двукратное уменьшение жизнеспособных микроорганизмов по сравнению только с термической обработкой (предпочтительно при стандартных условиях, которые известны в данной области техники), предпочтительно по меньшей мере трехкратное уменьшение, более предпочтительно по меньшей мере пятикратное уменьшение, еще более предпочтительно по меньшей мере десятикратное уменьшение, наиболее предпочтительно по меньшей мере на стократное уменьшение.
В другом варианте осуществления настоящее изобретение относится к комбинированной обработке пищевого продукта или одного или нескольких компонентов пищевого продукта композицией, как описано в настоящем изобретении, в соответствий с любым из способов, как описано в настоящем изобретении, и последующей термической обработкой, предпочтительно через 1-12 часов, более предпочтительно через 4-8 часов, чтобы уменьшить количество жизнеспособных микроорганизмов, предпочтительно одного или нескольких микроорганизмов, как описано в настоящем изобретении в другом месте, в результате чего происходит по меньшей мере двукратное увеличение сокращения жизнеспособных микроорганизмов по сравнению с обработкой только композицией, как описано в настоящем изобретении, предпочтительно по меньшей мере трехкратное увеличение, более предпочтительно по меньшей мере пятикратное увеличение, еще более предпочтительно по меньшей мере десятикратное увеличение, наиболее предпочтительно по меньшей мере стократное увеличение.
В другом варианте осуществления настоящее изобретение относится к комбинированной обработке пищевого продукта или одного или нескольких компонентов пищевого продукта композицией, как описано в настоящем изобретении в соответствии с любым из способов, как описано в настоящем изобретении, и последующей термической обработкой (предпочтительно пастеризацией), предпочтительно через 1-12 часов, более предпочтительно через 4-8 часов, в котором указанная термическая обработка уменьшается во времени, по меньшей мере на 10%, например от 10 до 50%, предпочтительно по меньшей мере на 20%, например, на 20, 30, 40, 50% или более, по сравнению со стандартной термической обработкой, которая известна в данной области техники. Было обнаружено, что в соответствии с этим вариантом осуществления по меньшей мере такие же, если не лучше, противомикробные эффекты могут быть получены, по сравнению с только термической обработкой. Например, по меньшей мере такие же или аналогичные количества микроорганизмов могут быть убиты или количества жизнеспособных микроорганизмов, предпочтительно одного или нескольких микроорганизмов, как описано в настоящем изобретении в другом месте, могут быть уменьшены по меньшей мере на таком же или подобном уровне.
В другом варианте осуществления настоящее изобретение относится к комбинированной обработке пищевого продукта или одного или нескольких компонентов пищевого продукта композицией, как описано в настоящем изобретении в соответствии с любым из способов, как описано в настоящем изобретении, и последующей термической обработкой (предпочтительно пастеризацией), предпочтительно через 1-12 часов, более предпочтительно через 4-8 часов, в котором температура указанной термической обработки уменьшается по меньшей мере на 2,5%, например от 2,5 до 25%, предпочтительно по меньшей мере на 5%, например, на 5, 10, 15, 20 или 25% или более, по сравнению со стандартной термической обработкой, какая известна в данной области техники. Было обнаружено, что в соответствии с этим вариантом осуществления по меньшей мере такие же, если не лучше, противомикробные эффекты могут быть получены, по сравнению с только термической обработкой. Например, по меньшей мере такие же или аналогичные количества микроорганизмов могут быть убиты или количества жизнеспособных микроорганизмов, предпочтительно одного или нескольких микроорганизмов, как описано в настоящем изобретении в другом месте, могут быть уменьшены по меньшей мере на таком же или подобной уровне.
Известно в данной области техники, что термическая обработка пищевого продукта может влиять на вкусовые характеристики указанного пищевого продукта. Соответственно, комбинированное применение композиций, как описано в настоящем изобретении, с термической обработкой позволяет использовать более короткое время термической обработки и/или более низкую температуру термической обработки, такие что воздействие на вкусовые характеристики могут быть уменьшены. Также более короткое время или более низкая температура являются более экономически эффективными.
Аспекты и варианты осуществления изобретения дополнительно поддерживается следующими неограничивающими примерами.
ПРИМЕРЫ
ПРИМЕР 1: Антилистериозная активность LPS в молоке
Экспериментальный дизайн
Оценивали антилистериозный эффект лактопероксидазной системы согласно варианту осуществления настоящего изобретения на основании провокационных испытаний при постоянной температуре (7°C). Провокационные испытания проводились в соответствии с ‘Technical guidance document on shelf-life studies for Listeria monocytogenes in ready-to-eat foods’ (EU CRL Listeria, november 2008) с помощью лаборатории, аккредитованной BELAC (accreditation certificate n° 059-TEST). Испытания были выполнены в ультрапастеризованном молоке, которое в асептических условиях разделяли на меньшие порции и инокулировали коктейлем штаммов L. monocytogenes (LMG 23194, LFMFP 392 и LFMFP 491) до уровня инокуляции приблизительно 50 КОЕ/мл. Продукт LPS добавляли в молоко в различных концентрациях (0, 100 и 300 м.д.). Образцы анализировали на день 0 (перед и после инокуляцией) и в разные дни во время хранения при 7°C. Провокационные испытания проводились в три раза.
Используемый продукт LPS в этом и следующих примерах, если не указано иное, содержит:
GOD: 0,75 мас. % (активность 15 Ед/мг)
LP: 1,25 мас. % (активность 1000 Ед/мг)
NaSCN: 5 мас. %
Глюкоза: 30 мас. %
Результаты
pH продукта составляло 6,66. После добавления продукта LPS наблюдалось небольшое увеличение до 6,74. Активность воды составляла 0,996. Перед инокуляцией все 9 образцов показали отсутствие L. monocytogenes в 25 мл. В таблице 1 приведены количества клеток (log КОЕ/мл) L. monocytogenes для различных тестируемых условий. Среднее значение и стандартное отклонение количества этих клеток показаны как функция времени на Фиг. 1.
Результаты показывают, что в контрольных образцах (=0 м.д.) L. monocytogenes начали расти немедленно и достигли приблизительно 7 логарифмических единиц КОЕ/мл через 8 дней. Добавление 100 м.д. продукта LPS удлинил лаг-фазу L. monocytogenes на 16 дней. Впоследствии L. monocytogenes начали расти при несколько более меньшей скорости роста, чем в контроле. В образцах, содержащих 300 м.д. продукта LPS, количество клеток было стабильным в течение первых 16 дней инкубации, а затем произошла инактивации. В последний день анализа (день 28), отсутствие L. monocytogenes в 25 мл обнаруживалось в течение двух из трех повторах.

Проведенные провокационные испытания доказывают антилистериозный эффект продукта LPS в ультрапастеризованном молоке, хранящемся при 7°C. Промежуточные концентрации дают задержку роста (более длительную лаг-фазу и более меньшую скорость роста), а самая высокая концентрация индуцировала инактивацию целевого микроорганизма.
ПРИМЕР 2: Противомикробная активность LPS в полуобезжиренном молоке, инокулированном Lactobacillus brevis
Lactobacillus brevis является очень хорошо известным микроорганизмом, ответственным за бактериальную порчу молока и многих других продуктов питания. Полуобезжиренное молоко инокулировали Lactobacillus brevis в провокационном испытании в соответствии с нижеприведенном протоколом.
Экспериментальный дизайн
МАТЕРИАЛЫ
- Lactobacillus brevis АТСС 8287 / Disc Oxoid NLB145
- Полуобезжиренное ультрапастеризованное молоко
- Инкубатор 12°C
- Инкубатор 30°C
- Вортекс
- Стерильные чашки Петри (9 см);
- Стерильные наконечники пипеток 100 мкл:
- Стерильные наконечники пипеток 1000 мкл:
- Бутылка со стерильным агаром MRS (Man, Rogosa and Sharpe) (готов к использованию)
- Стерильные пробирки с PPS (раствор натрия хлорида и пептона или триптона) (10 мл)
МЕТОД
Приготовление питательной среды
- Инокулировать 5 мл полуобезжиренного молока с одного диска Lactobacilus brevis;
- Перемешать инокулированное молоко встряхиванием
- Инкубировать в течение ночи при 30°C (от 20 ч до 24 ч). Получали маточный раствор с 107-108 КОЕ/мл.
- Разбавление уровня Lactobacillus brevis в растворе хлорида натрия и триптона:
- Разбавить молоко в 100 раз (от 108 до 106), добавив два раза от 1 мл до 9 мл PPS. «Раствор 1» получали с уровнем 106 КОЕ/мл Lactobacillus brevis.
- Добавить 2 мл раствора 1 в 8 мл PPS. В "Растворе 2" получали уровень Lactobacilus brevis 2*105 КОЕ/мл,
Приготовление контрольного раствора:
- Инокулировать 99,7 мл полуобезжиренного ультрапастеризованного молока 0,3 мл «Раствора 2», чтобы достичь уровня Lactobacilus brevis 6*102 КОЕ/мл ("Раствор 3").
- Инкубировать "Раствор 3" при 12°C и анализировать ежедневно.
Приготовление раствора LPS:
- Добавить 3 г LPS в 100 мл реципиента, довести объем до 100 мл деминерализованной водой и перемешать.
- Инкубировать раствор LPS при около 20°C в течение 15 минут;
- Инокулировать 98,7 мл полуобезжиренного ультрапастеризованного молока 0,3 мл "Раствора 2", чтобы достичь уровня Lactobacilus brevis 6*102 КОЕ/мл (инокулированное молоко)
- Добавить 1 мл раствора LPS к инокулированному молоку для достижения уровня Lactobacilus brevis 6*102 КОЕ/мл и концентрации LPS 300 м.д. (Раствор 4).
- Инкубировать "Раствор 4" при 12°C и анализировать ежедневно.
Бактериологический анализ:
Приготовление MRS-агара:
- Поместить бутылки с MRS-агаром в водяную баню при 95°C;
- Позволить MRS-агару расплавиться в течение 60 минут;
- Позволить MRS-агару остыть до приблизительно 47°C, при этом оставаясь жидким.
Приготовление чашек Петри:
- Удалить "раствор 4" и "раствор 3" из инкубатора при 12°C.
- В соответствии с уровнем концентрации Lactobacilus brevis, разбавить "раствор 4" и "раствор 3" во столько раз, сколько необходимо, каждый раз добавляя по 1 мл концентрированного раствора в 9 мл раствора хлорида натрия и триптона.
- Добавить 1 мл раствора с требуемой концентрацией в чашку Петри, используя пипетки с стерильными наконечниками пипеток.
- Налить полученный жидкий MRS-агар, как описано выше, в чашке Петри и заполнить на две трети объема чашки Петри.
- Осторожно встряхнуть чашки Петри и подождать 10 минут.
- Налить второй слой жидкого MRS-агара в чашку Петри (для создания «анаэробной» зоны между 2 слоями в MRS-агаре).
- Инкубировать чашки Петри при 30°C вверх дном в течение 72 часов.
Подсчет колоний бактерий в чашках Петри (КОЕ)
- Колонии Lactobacillus brevis - белые, круглые/овальные;
- Подсчитать количество колоний на чашке Петри, и определить количество колоний по отношению к используемому разбавлению.
- Сравнить результаты, полученные в контроле и растворе LPS.
РЕЗУЛЬТАТЫ
Использовались следующие типы продуктов LPS:
- LPS1: 0,75 мас. % GOD; 1,25 мас. % LP; 5 мас. % SCN; 30 мас. % глюкозы
- LPS2: 0,75 мас. % GOD; 1,25 мас. % LP; 1,7 мас. % SCN; 20 мас. % глюкозы
- LPS3:1,7 мас. % GOD; 0,04 мас. % LP; 1,7 мас. % SCN; 0 мас. % глюкозы
- LPS4: 0,1 мас. % GOD; 1,25 мас. % LP; 3,5 мас. % SCN; 20 мас. % глюкозы
Таблица 2 и Фиг. 2 показывают результаты провокационных испытаний в полуобезжиренном молоке, включающем 300 м.д. трех продуктов LPS, приведенных выше, и инокулированных в течение указанного количества дней с L. brevis. Контрольный образец не содержал какой-либо LPS.

Результаты показывают, что в контрольных образцах (=0 м.д.) L. brevis начали расти немедленно и достигли приблизительно 7 log КОЕ/мл через 6 дней. Добавление 300 м.д. продуктов LPS2 и LPS3 удлинило лаг-фазу L. brevis. Впоследствии L. brevis начали расти с меньшей скоростью роста, чем в контроле. Добавление 300 м.д. продуктов LPS4 привело к первоначальному уменьшению L. brevis. Впоследствии L. brevis начали расти с меньшей скоростью роста, чем в контроле. Добавление 300 м.д. LPS1 привело к даже стабильному уменьшению количества L. brevis в течение долгого времени.
Проведенные провокационные испытания доказали антибактериальное действие продукта LPS в ультрапастеризованном молоке, хранящемся при 7°C для различных продуктов LPS. В любом случае, задержка в росте бактерий наблюдается для различных концентраций компонентов LPS вплоть до поддерживаемого подавления роста бактерий.
ПРИМЕР 3: Противомикробная активность LPS на полуобезжиренном молоке, инокулированном Escherichia coli O157:Н7
Экспериментальный дизайн
Полуобезжиренное молоко инокулировали коктейлем штаммов Escherichia coli O157:Н7, (463 LFMFP, LFMFP 474 и LMG 21756) на уровне 50 КОЕ/мл. LPS добавляли в различных концентрациях (0 м.д. (= контроль), 100 м.д., 300 м.д.). Молоко разделяли на порции и хранили при 12°C. Анализы проводили в день 0, день 3, день 4, день 5, день 6 и день 7. Эксперимент проводили в три раза.
Результаты
Таблица 3 и Фиг. 3 представляют количество клеток Escherichia coli O157:Н7 в молоке в течение инкубации при 12°C. LPS четко подавляет рост смеси Escherichia coli O157:Н7, инокулированных в молоке. При 300 м.д., никакого роста патогена не наблюдалось через 7 дней.

ПРИМЕР 4: Оценка противомикробного эффекта LPS по отношению к молочнокислым бактериям
Экспериментальный дизайн
Эмульгированные соусы (тип заправки) были приготовлены с pH 4,0 и 2% соли. Перед приготовлением эмульсии добавили противомикробный компонент в двух различных концентрациях (100 и 300 м.д.). Эти продукты инокулировали коктейлем из трех молочнокислых бактерий (Lactobacillus brevis, Lactobacillus fructivorans и Lactobacillus plantarum). Соусы хранили при 22°C и через регулярные интервалы времени контролировали рост микроорганизмов, вызывающих порчу, по сравнению с ростом в контроле.
Результаты
Уровень инокуляции смеси молочнокислых бактерий был приблизительно 2,2 log КОЕ/г. Начальное значение pH заправки составляло 4,07±0,04 и активность воды 0,9611±0,001. Концентрация соли составляла 2,14%±0,04 (определено аналитически).
Результаты показывают четкое противомикробное действие по отношению к молочнокислым бактериям (Фиг. 4). В контроле (=0 м.д.) молочнокислые бактерии немедленно росли и максимальное количество клеток было достигнуто через 9 дней инкубации при 22°C. Поэтому анализы были остановлены после дня 16. Остальные временные точки элемента контроля были заменены дополнительными анализами, касающимися заправки с LPS (день 30). В заправках с 100 м.д., также в заправках с 300 м.д. LPS было замечено начальное снижение количества клеток даже ниже предела обнаружения для самой высокой концентрации продукта. При промежуточной концентрации (100 м.д.) была замечена задержка роста и количество клеток не достигало 4 log КОЕ/г в течение всего срока годности (30 дней). Это остается значительно ниже критерия для молочнокислых бактерий в этих продуктах в конце срока годности. Для наивысшей концентрации количество клеток остается ниже предела обнаружения в течение 26 дней при 22°C. На 30 день было обнаружено чуть больше количество клеток. Так как не было никаких оставшихся дополнительных дней анализов, эта тенденция не могла быть подтверждена.
Фиг. 5 показывает процесс изменения pH для различных заправок. Это доказывает, что pH является относительно стабильным также в заправках с противомикробным продуктом. Уменьшение pH в контроле в день 16 вызвано большим числом клеток молочнокислых бактерий.
Результаты показывают, что LPS имеет четкое противомикробное действие в отношении молочнокислых бактерий в средах с pH 4,0 и хранящихся при 22°C. Кроме того наблюдался концентрационный эффект продуктов: чем выше концентрация, тем выше эффективность.
ПРИМЕР 5: Противомикробная активность LPS в цельной яичной массе, инокулированной Salmonella spp.
Экспериментальный дизайн
Цельную яичную массу разделяли на более мелкие порции и инокулировали коктейлем штаммов сальмонелл (LMG 10395 и LMG 10396) на уровне 9000 КОЕ/мл. LPS добавляли в концентрации 300 м.д. Через 8 часов при 7°C цельную яичную массу пастеризовали в течение 1 мин, 3 мин и 5 мин при 55°C и охлаждали в бане с ледяной водой. Образцы немедленно анализировали.
- LPS: 0 м.д. (= контроль), 300 м.д.
- Цельная яичная масса
- сначала хранили 8 ч/7°, затем пастеризовали: 55°C в течение 1 мин, 3 мин, 5 мин.
- Salmonella enteritidis (LMG 10395), и Salmonella typhymurium (LMG 10396).
Результаты
Таблица 4 и Фиг. 6 показывают, что в яичных образцах, куда добавляли LPS, разрушение Salmonella spp. было более эффективным, чем в яичных образцах без LPS.

Эти результаты ясно показывают дополнительный эффект пастеризации, когда LPS добавляли за 8 часов при 7°C перед пастеризацией. Сочетание LPS и пастеризации существенно увеличивало эффект пастеризации цельной яичной массы.
ПРИМЕР 6: Противомикробная активность LPS, добавленной в сырое молоко перед пастеризацией (15 с/72°C)
Экспериментальный дизайн
Сырое молоко разделяли на меньшие порции и добавляли LPS в концентрации 300 м.д. Через 8 часов при 7°C сырое молоко пастеризовали в течение 15 с при 72°C и охлаждали в ледяной воде. Образцы хранили при 12°C. Анализ проводили на день 0, день 1, день 2 и день 3.
- LPS: 0 м.д. (= контроль), 300 м.д.
- сырое молоко
- сначала хранили 8 ч/7°C, затем пастеризовали: 72°C в течение 15 с.
- 3 дня при 12°C
Результаты
Таблица 5 и Фиг. 7 подытоживают общее количество аэробных психротропных клеток (инкубация при 22°C) (log КОЕ/мл) для различных тестируемых условий при 12°C. Результаты показывают, что рост бактерий в контрольных образцах (без LPS) начинается снова на день 3. В образцах с LPS (300 м.д.) бактерии инактивировались через 2 дня при 12°C и дальнейшего роста не наблюдалось.

Таблица 6 и Фиг. 8 подытоживает общее количество аэробных психотропных клеток (инкубация при 22°C) (log КОЕ/мл) для различных тестируемых условий при 12°C.
Результаты показывают, что рост бактерий в контрольных образцах (без LPS) начинается снова на день 3. В образцах с LPS (300 м.д.) бактерии инактивировались через 3 дня при 12°C.

Таблица 7 подытоживают общее количество клеток (log КОЕ/мл) молочнокислых бактерий для различных тестируемых условий при 12°C. Результаты показывают, что никакого роста молочнокислых бактерий не наблюдалось в контрольных образцах (без LPS) через 3 дня. В образцах с LPS (300 м.д.) молочнокислые бактерии полностью инактивировались посредством пастеризации. Никакого дополнительного роста не наблюдалось в течение 3 дней при 12°C.

Таблица 8 подытоживает количество дрожжевых клеток (log КОЕ/мл) для различных тестируемых условий при 12°C. Результаты показывают, что дрожжи полностью инактивировались посредством пастеризации. Никакого дополнительного роста не наблюдалось в течение 3 дней при 12°C.

Таблица 9 подытоживает количество плесневых клеток (log КОЕ/мл) для различных тестируемых условий при 12°C. Результаты показывают, что плесени полностью инактивировались посредством пастеризации. Никакого дополнительного роста не наблюдалось в течение 3 дней при 12°C.

LPS показали, что являются эффективной в молоке после пастеризации 15 с/72°C для предотвращения разрастания микроорганизмов, выживших после пастеризации после хранения в течение 3 дней при 12°C.
ПРИМЕР 7: Противомикробная активность LPS, добавленной в сырое молоко перед пастеризацией (15 с/72°C)
Экспериментальный дизайн 1
Свежее сырое молоко разделяли на меньшие порции и добавляли LPS в различных концентрациях (0 м.д., 300 м.д.). Через 8 часов при 7°C сырое молоко пастеризовали в течение 15 с при 72°C и охлаждали в ледяной воде. Образцы хранили при 12°C. Бактериологический анализ проводили на день 0, день 1, день 2, день 3, день 5 и день 7.
- LPS: 0 м.д. (= контроль), 300 м.д.
- Свежее сырое молоко
- Сначала хранили 8 ч/7°C, затем пастеризовали: 72°C в течение 15 с.
- 7 Дней при 12°C
Результаты
Таблица 10 подытоживает общее количество аэробных психротропных клеток (инкубация при 22°C) (log КОЕ/мл) для различных тестируемых условий при 12°C. Результаты показывают, что рост бактерий в контрольных образцах (без LPS) начинался снова на 2 день и достигал приблизительно 7 log КОЕ/мл для контрольных образцов через 7 дней при 12°C. В образцах, в которые добавляли 300 м.д. LPS бактерии начинали расти через 2 дня и достигали только log 4 КОЕ/мл через 7 дней при 12°C.

Таблица 11 подытоживает общее количество анаэробных психротропных клеток (инкубация при 22°C) (log КОЕ/мл) для различных тестируемых условий при 12°C. Результаты показывают, что рост бактерий в контрольных образцах (без LPS) начинался снова на день 3 и достигал приблизительно 7 log КОЕ/мл для контрольных образцов через 7 дней при 12°C. В образцах, в которые добавляли 300 м.д. LPS, рост бактерий начинался снова на через 7 дней при 12°C.

Таблица 12 подытоживает количество клеток (log КОЕ/мл) молочнокислых бактерий для различных тестируемых условий при 12°C. Результаты показывают, что рост бактерий в контрольных образцах (без LPS) начинался снова через 3 дня и достигал приблизительно 7 log КОЕ/мл через 7 дней при 12°C. В образцах, в которых добавляли 300 м.д. LPS, рост молочнокислых бактерий начинался снова через 7 дней при 12°C.


Таблица 13 подытоживает количество клеток дрожжей (log КОЕ/мл) для различных тестируемых условий при 12°C. Результаты показывают, что дрожжи полностью инактивировались посредством пастеризации. Никакого дополнительного роста не наблюдалось в течение 7 дней при 12°C.

Таблица 14 подытоживает количество плесневых клеток (log КОЕ/мл) для различных тестируемых условий при 12°C. Результаты показывают, что плесени полностью инактивировались посредством пастеризации. Никакого дополнительного роста не наблюдалось в течение 7 дней при 12°C.


Результаты показывают, что добавление 300 м.д. LPS перед пастеризацией и с промежуточным хранением 8 ч при 7°C, действительно пролонгировали срок годности при 12°C в пастеризованном молоке значительно.
Экспериментальный дизайн 2
Свежее сырое молоко разделяли на меньшие порции и LPS добавляли в концентрации 300 м.д. Через 4 часа при 7°C сырое молоко пастеризовали в течение 15 с при 72°C и охлаждали в ледяной воде. Образцы хранили при 12°C. Бактериологический анализ проводили на день 0, день 1, день 2, день 3, день 5 и день 7.
- LPS: 0 м.д., 300 м.д.
- Свежее сырое молоко
- Сначала хранили 4 ч/7°C, затем пастеризовали: 72°C в течение 15 с.
- 7 Дней в 12°C
Результаты
Таблица 15 и Фиг. 9 подытоживают общее количество анаэробных психротропных клеток (инкубация при 22°C) (log КОЕ/мл) для различных тестируемых условий при 12°C. Результаты показывают, что рост бактерий в контрольных образцах (без LPS) начинался снова на день 2 и достигал приблизительно 7 log КОЕ/мл через 7 дней при 12°C, В образцах, в которые добавляли 300 м.д. LPS, рост бактерий начинался снова на день 2 и достигал лишь приблизительно 4 log КОЕ/мл через 7 дней при 12°C.

Таблица 16 и Фиг. 10 подытоживают общее количество анаэробных психротропных клеток (инкубация при 22°C) (log КОЕ/мл) для различных тестируемых условий при 12°C. Результаты показывают, что рост бактерий в контрольных образцах (без LPS) начинается снова на день 2 и достигал приблизительно 7 log КОЕ/мл через 7 дней при 12°C. В образцах, в которые добавляли 300 м.д. LPS, никакого роста бактерий не наблюдалось через 7 дней при 12°C.


Таблица 17 подытоживает количество клеток (log КОЕ/мл) молочнокислых бактерий для различных тестируемых условий при 12°C. Результаты показывают, что рост бактерий в контрольных образцах (без LPS) начинался снова на день 2 и достигал приблизительно 6,5 log КОЕ/мл через 7 дней при 12°C. В образцах, в которые добавляли 300 м.д. LPS молочнокислые бактерии начинали расти снова через 7 дней при 12°C.

Таблица 18 подытоживает количество клеток дрожжей (log КОЕ/мл) для различных тестируемых условий при 12°C. Результаты показывают, что дрожжи полностью инактивировались посредством пастеризации. Никакого дополнительного роста не наблюдалось в течение 7 дней при 12°C.


Таблица 19 подытоживает количество плесневых клеток (log КОЕ/мл) для различных тестируемых условий при 12°C. Результаты показывают, что плесени полностью инактивировались посредством пастеризации. Никакого дополнительного роста не наблюдалось в течение 7 дней при 12°C.

Результаты показывают, что время ожидания 4 часа при 7°C между добавлением 300 м.д. LPS и пастеризацией является достаточным, чтобы достичь существенного увеличения срока годности пастеризованного молока.
ПРИМЕР 8: Противомикробная активность LPS, добавленной в сырое молоко перед пастеризацией (15 с/72°C) - сравнение концентрации LPS.
Экспериментальный дизайн
Свежее сырое молоко разделяли на меньшие порции и LPS добавляли в различных концентрациях (0 м.д., 100 м.д., 200 м.д. и 300 м.д.). Через 8 часов при 7°C сырое молоко пастеризовали в течение 15 с при 72°C и охлаждали в ледяной воде. Образцы хранили при 12°C. Бактериологический анализ проводили на день 0, день 1, день 2, день 3, день 5 и день 7.
- LPS: 0 м.д. (= контроль), 100 м.д., 200 м.д. и 300 м.д.
- Свежее сырое молоко
- Сначала хранили 8 ч/7°C, затем пастеризовали: 72°C в течение 15 с.
- 7 Дней при 12°C
Результаты
Таблица 20 и Фиг. 11 подытоживают количество клеток (log КОЕ/мл) молочнокислых бактерий для различных тестируемых условий при 12°C. Таблица 21 и Фиг. 12 подытоживают общее количество клеток аэробных психротропных бактерий (log КОЕ/мл) для различных тестируемых условий при 12°C. Результаты показывают, что рост молочнокислых бактерий в контрольных образцах (без LPS) начинался снова на день 3 и достигал приблизительно 7 log КОЕ/мл через 7 дней при 12°C. В образцах с 100 м.д. LPS и в образцах с LPS 200 м.д. рост бактерий начинался снова на день 5 и достигал приблизительно log 6 КОЕ/мл для LPS 100 м.д. и приблизительно log 8 КОЕ/мл для LPS 200 м.д. через 7 дней при 12°C. В образцах, в которые добавляли 300 м.д. LPS, рост молочнокислых бактерий начинался снова через 7 дней при 12°C. Аналогичная тенденция может быть замечена для аэробных психротропных бактерий, т.е. меньшее снижение количества клеток в контрольном образце, а также более быстрый бактериальный рост после пастеризации и более высокие конечные количества бактериальных клеток в контрольном образце по сравнению с образцами, обработанными LPS.



Результаты иллюстрируют, что добавление 300 м.д. LPS перед пастеризацией и с промежуточным хранением 8 ч при 7°C действительно значительно продлевало срок годности пастеризованного молока при 12°C. Меньшее добавленное количество LPS (100-200 м.д.) приводило к промежуточному эффекту на этот срок годности.
ПРИМЕР 9: Противомикробная активность LPS, добавленного в сырое молоко перед пастеризацией (при различных температурах)
Экспериментальный дизайн
Свежее сырое молоко разделяли на меньшие порции и LPS добавляли в концентрации 300 м.д. Через 6 часов при 7°C сырое молоко пастеризовали в течение 15 с при различных температурах в диапазоне от 54°C до 72°C и охлаждали в ледяной воде. Чтобы отделить эффект от предварительной LPS-инкубации от эффекта последующей термической обработки, и таким образом исследовать синергические эффекты обработки LPS и термической обработки, общее количество бактерий после обработки LPS и перед термической обработкой доводили (нормировали) к 6,4 log (КОЕ)/мл. Бактериологический анализ проводили немедленно после пастеризации.
- LPS: 0 м.д. (= контроль) и 300 м.д.
- Свежее сырое молоко
- Сначала хранили 8 ч/7°C, затем пастеризовали: 72°C в течение 15 с
- 7 Дней в 12°C
Композиция LPS:
- GOD: 0,75 мас. %
- LP: 1,25 мас. %
- SCN: 5 мас. %
- Глюкоза: 30 мас. %
Результаты
Таблица 22 подытоживает общее число клеток (log КОЕ/мл) в молоке немедленно после пастеризации при различных температурах, в которой сравнивается обработка LPS (300 м.д.) и контроль (0 м.д.).


Из таблицы 22 видно, что независимо от температуры пастеризации, общее количество клеток в образцах, обработанных LPS, было ниже, чем общее количество клеток в контрольных образцах, в то время как такое же количество бактерий (6,4 log КОЕ/мл) подвергали термической обработке. Эти результаты ясно показывают влияние предварительной обработки LPS на последующую термическую обработку, так как термическая обработка после предварительной обработки LPS приводит к более низкому количеству клеток по сравнению с термической обработкой того же количества исходных бактерий (6,4 log КОЕ/мл) без предварительной обработки LPS. Следовательно, обработка LPS и термическая обработка синергически влияют на выживание микробов.
ПРИМЕР 10: Противомикробная активность LPS в цельной яичной массе, инокулированной Salmonella spp.
Экспериментальный дизайн
Цельную яичную массу разделяли на более мелкие порции и инокулировали коктейлем штаммов сальмонелл (LMG 10395 и LMG 10396) на уровне 7500 КОЕ/мл. Следующие композиции LPS были добавлены при концентрации 300 м.д.
- LPS1: 0,75 мас. % GOD; 1,25 мас. % LP; 5 мас. % SCN; 30 мас. % глюкозы
- LPS2: 0,75 мас. % GOD; 1,25 мас. % LP; 1,7 мас. % SCN; 20 мас. % глюкозы
- LPS3:1,7 мас. % GOD; 0,04 мас. % LP; 1,7 мас. % SCN; 0 мас. % глюкозы
Через 8 часов при 7°C цельную яичную массу пастеризовали в течение 1 мин, 3 мин и 5 мин при 55°C и охлаждали в ледяной воде. Образцы анализировали немедленно после термической обработки.
- LPS1: 0 м.д. (= контроль), 300 м.д.
- LPS2: 0 м.д. (= контроль), 300 м.д.
- LPS3: 0 м.д. (= контроль), 300 м.д.
- цельная яичная масса
- сначала хранили 8 ч/7°C, затем пастеризовали: 55°C в течение 1 мин, 3 мин, 5 мин.
- Salmonella enteritidis (LMG 10395), и Salmonella typhymurium (LMG 10396).
Результаты
Таблица 23 и Фиг. 13 подытоживают количество клеток (log КОЕ/мл) молочнокислых бактерий для различных тестируемых условий. Результаты показывают, что в образцах яиц, в которые добавляли LPS, ингибирование Salmonella spp. было более эффективным, чем в образцах яиц без LPS.
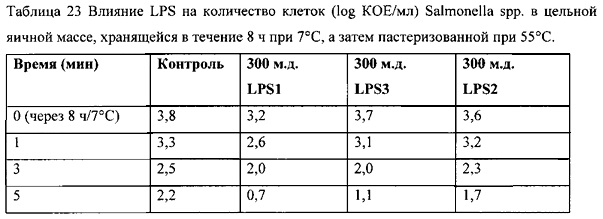
Результаты показывают, что LPS увеличила термоинактивацию Salmonella spp. в жидком цельном яйце, когда применялась перед пастеризацией. Эффект наиболее выражен с LPS1 и после пастеризации 5 минут при 55°C по сравнению с более коротким временем пастеризации при той же температуре.
ПРИМЕР 11: Противомикробная активность LPS в салате с сурими
Экспериментальный дизайн
Домашний салат с сурими разделяли на более мелкие порции и инокулировали коктейлем из молочнокислых бактерий на уровне инокуляции 1000 КОЕ/г. LPS добавляли к салату с сурими при различных концентрациях (0 м.д., 150 м.д., 300 м.д.), и салат с сурими хранили при 7°C в течение 6 недель на воздухе. Образцы анализировали на день 0, неделю 1, неделю 2, неделю 3, неделю 4, неделю 5 и неделю 6.
- LPS: 0 м.д. (= контроль), 150 м.д., 300 м.д.
- домашний салат с сурими
- молочнокислые бактерии: Lactobacillus plantarum (FF595, выделенные из салата с лососем)
Lactobacillus brevis (FF662, выделенные из мясного салата)
Lactococcus lactis ssp lactis 2 (FF649, выделенные их салата из яиц с чесноком)
- 7°C (6 недель)
Результаты
Таблица 24-26 и Фиг. 14-16 подытоживают соответственно общее количество аэробных психротропных клеток (инкубация при 22°C) (log КОЕ/г), общее количество анаэробных психротропных клеток (инкубация при 22°C) (log КОЕ/г) и количество клеток (log КОЕ/г) молочнокислых бактерий (инкубация при 22°C) для различных тестируемых условий. Результаты показывают, что рост в контроле (0 м.д.) начинался немедленно и достигал приблизительно 7 log КОЕ/г через 5 недель. В образцах с 150 м.д. LPS наблюдался более ограниченный рост бактерий (приблизительно 4,5 log КОЕ/г), в то время как в образцах с 300 м.д. LPS наблюдалась инактивации бактерий в процессе хранения.




Результаты ясно демонстрируют потенциал LPS ингибировать рост молочнокислых бактерий в салатах на основе соуса. 150 м.д. LPS предотвращало разрастание молочнокислых бактерий, а 300 м.д. LPS даже ингибировало молочнокислые бактерии при хранении при 7°C.
ПРИМЕР 12: Проба на вкус питьевого йогурта с и без LPS
Экспериментальный дизайн
В определении идентичности двух элементов из трех питьевой йогурт (60% воды, 40% йогурта (обезжиренный натуральный йогурт) и 1% соли) с 300 м.д. LPS сравнивали с питьевым йогуртом без LPS (контроль). Раствор LPS добавляли в питьевой йогурт, то же самое количество стерильной воды было добавлено в контроль. Оба образца хранились при 10°C в течение 3 недель. Образцы тестировали на вкус в день 0 (1 час после смешивания), неделю 2 и неделю 3.
Результаты
День 0: Панель состояла из 10 человек. Из этих 10 человек только 3 человека сделали правильное различие между двумя продуктами. Не было отмечено никаких существенных сенсорных различий. Члены группы нашли все образцы приемлемыми, и не было никакого существенного предпочтения.
Неделя 2: Группа состояла из 11 человек. Из этих 11 человек 8 человек сделали правильное различие между двумя продуктами, уровень значимости составил 0,01. Два члена панели отдавали предпочтение образцу с LPS.
Неделя 3: Группа состояла из 14 человек. Из этих 14 человек 9 человек сделали правильное различие между двумя продуктами, уровень значимости составил 0,05. Четыре члена панели отдавали предпочтение образцу с LPS.
Эти результаты показывают, что с течением времени, как правило, больше людей имеют тенденцию различать продукты с или без LPS. В то время как не было никакого предпочтения для продуктов с или без LPS в день 0, после двух недель, и даже в большей степени после трех недель, все большее количество людей отдавали предпочтение продукции с LPS.
ПРИМЕР 13: Проба на вкус молодого полуобезжиренного сыра с и без LPS
Экспериментальный дизайн
В определении идентичности двух элементов из трех молодой полуобезжиренный сыр с 300 м.д. LPS сравнивали с молодым полуобезжиренным сыром без LPS (контроль). Раствор LPS добавляли в молодой полуобезжиренный сыр, такое же количество стерильной воды было добавлено к контролю. Оба образца хранились при 10°C в течение 14 дней. Образцы тестировались на вкус в день 0 (2 часа после смешивания), день 7 и день 14.
Результаты
День 0: Панель состояла из 15 человек. Из этих 15 человек 7 человек сделали правильное различие между двумя продуктами. Члены группы нашли все образцы приемлемыми и не было никакого существенного предпочтения.
День 7: Панель состояла из 15 человек. Из этих 15 человек 6 человек сделали правильное различие между двумя продуктами. Один из членов группы отдал предпочтение образцу, содержащему LPS.
День 14: Панель состояла из 15 человек. Из этих 15 человек 6 человек сделали правильное различие между двумя продуктами. Два члена панели отдавали предпочтение образцу, содержащему LPS.
Эти результаты показывают, что в то время как никакого предпочтения не было дано для продуктов с или без LPS в день 0, через две недели, и даже в большей степени через три недели, все большее количество людей отдавали предпочтение продукции с LPS.
ПРИМЕР 14: Органолептическая оценка цельной яичной массы, обработанной различными композициями LPS
Экспериментальный дизайн
Органолептическая оценка (определение идентичности двух элементов из трех; ISO-4120: 2004) проводили с пастеризованной цельной яичной массой, которую обрабатывали тремя различными композициями LPS (каждая по 300 м.д.). Цвет и запах анализировали и сравнивали с необработанными образцами (blanco).
- LPS1: 2,5 мас. % GOD / 1,25 мас. % LP / 7,5 мас. % SCN и 30 мас. % глюкозы (не в соответствии с настоящим изобретением)
- LPS2: 0,75 мас. % GOD / 1,25 мас. % LP / 1,7 мас. % SCN и 20% глюкозы (в соответствии с настоящим изобретением)
- LPS3:1,7 мас. % GOD / 0,06 мас. % LP / 1,7 мас. % SCN и 0 мас. % глюкозы (в соответствии с настоящим изобретением)
Образцы хранили при 10°C до 14 дней и оценивали периодически в течение этого периода.
Результаты
День 0: панель из 10 человек; 2 человека правильно различили между продуктами, по разному обработанными; никаких существенных органолептических различий не были отмечены между продуктами, по разному обработанными.
День 7: панель из 10 человек:
- Бланко в сравнении с LPS1: 10 человек правильно различили Бланко и LPS1; LPS1 воспринимался как имеющий палевый цвет и сильный окислительный запах по сравнению с Бланко.
- Бланко в сравнении с LPS2: 3 человека правильно различили Бланко и LPS2; никаких существенных различий найдено не было; все органолептические характеристики были признаны приемлемыми.
- Бланко в сравнении с LPS3: 2 человека правильно различили Бланко и LPS2; никаких существенных различий найдено не было; все органолептические характеристики были признаны приемлемыми.
День 14: панель из 10 человек:
- Бланко в сравнении с LPS1: такие же результаты, как в день 7, но более выраженные; LPS1 был найден совершенно неприемлемым.
- Бланко в сравнении с LPS2: 4 человек правильно различили Бланко и LPS2, 2 человека отдали предпочтение образцу, обработанному LPS2, все органолептические характеристики были признаны приемлемыми.
- Бланко в сравнении с LPS3: такие же результаты, как в день 7.
Эти результаты показывают, что композиции LPS, не соответствующие настоящему изобретению, такие как композиции LPS, имеющие более высокие концентрации GOD или SCN, негативно влияют на органолептические характеристики с течением времени, до такой степени, что обработанные пищевые продукты воспринимается, как имеющие неприемлемые органолептические характеристики.
ПРИМЕР 15: Определение активности LP
Реагенты
Натрий цитратный буфер, 50 мМ, pH 5,0
Хлорид натрия 0,9 мас./об. %
Пероксид водорода 0,3 об./об. %
Раствор субстрата: 1 мМ ABTS (в 100 мкл 0,3 об./об. % пероксида водорода с добавлением натрий цитратного буфера до 100 мл)
Методика
Растворить 25 мг LP (Amano) в 10 мл 0,9 мас./об. % NaCl; разбавить 100 мкл 0,9 мас./об. % NaCl до 100 мл; добавить 100 мкл к 2 мл предварительно нагретого (37°C) раствора субстрата в кювету (d=10 мм). Измерить оптическую плотность через 30 с (Abs30) и через 90 с (Abs90).
Рассчитать активность (Ед/мг):
Активность LP (Ед/мг) = ((Abs90 - Abs30) × разбавление × 25)/(2,1×0,1×2,5 × масса в мг) = 47619 × (Abs90 - Abs30)/Macca в мг
ПРИМЕР 16: Определение активности GOD
Реагенты
A. Раствор аминоантипирина (4 мг/мл в деионизированной воде)
B. Раствор Тритона Х-100 (50 мг/мл в деионизированной воде)
C. Раствор фенола (50 мг/мл в деионизированном растворе)
D. Раствор пероксидазы (пурпурогаллиновое число пероксидазы 250 (LP, Amano) в 10 мл деионизированной воды)
E. фосфатный буфер 0,1 М (KH2PO4-NaOH, pH 7,0)
F. Фенольный буферный раствор (0,1 М KH2PO4, содержащий 3 мл раствора фенола и 3 мл раствора Тритона Х-100 на 100 мл конечного раствора, и доведенного до pH 7,0 с помощью NaOH)
G. Раствор субстрата (2,5 г D-глюкозы/25 мл в деионизированной воде)
H. Раствор фермента приблизительно 50 мг GOD ((Amano) в 0,1 М фосфатного буфера Е (такого что, значение ΔOD/мин составляет 0,030 +/- 0,005.
Методика
Смешать 2,0 мл F + 0,5 мл G + 0,5 мл D + 0,1 мл А и предварительно нагреть до 37°C в кювете (d=10 мм)
Добавить 0,1 мл Н, перемешать и выдерживать при 37°C или добавить 0,1 мл Е для бланко
Измерить поглощение через 2 и 5 минут при 500 нм
Рассчитать активность (Ед/мг)
Активность GOD (Ед/мг) = ((А5-А2)-(Ab5-Ab2)/3)×(1/(12,88×1/2))×3,2×(Dm/0,1)×1,339, где
А5 и А2 = поглощение GOD-содержащей реакции через 5 и 2 минуты соответственно
Ab5 и Ab2 = поглощение бланко реакции через 5 и 2 минуты соответственно
Dm = кратность разведения раствора Н (раствор фермента)
Реферат
Настоящее изобретение относится к противомикробным композициям, которые могут быть использованы для консервирования пищевых продуктов. Композиция для консервирования пищевого продукта содержит активные ингредиенты: 1125-31875 Ед глюкозооксидазы (GOD) на 100 г композиции, 30000-1562500 Ед лактопероксидазы (LP) на 100 г композиции, 1,275-6,25 мас. % тиоцианата (SCN), 0-37,5 мас. % глюкозы и наполнители. Настоящее изобретение также относится к применению такой композиции в качестве консерванта для пищевого продукта и к пищевым продуктам, содержащим такую композицию. Предложен также способ сохранения пищевого продукта, включающий добавление 50-400 м.д. вышеуказанной композиции к пищевому продукту или компоненту пищевого продукта. Изобретение позволяет получить композицию, обеспечивающую высокое противомикробное действие без неблагоприятного воздействия на органолептические свойства пищевого продукта при хранении. 4 н. и 11 з.п. ф-лы, 16 ил., 26 табл., 16 пр.

Комментарии