Инсектицид, акарицид и нематоцид, содержащие в качестве активного компонента производное 3-триазолилфенилсульфида - RU2394819C2
Код документа: RU2394819C2
Описание
Изобретение относится к новым производным 3-триазолилфенилсульфида и инсектицидам, акарицидам и нематоцидам для сельскохозяйственного и садоводческого применения, содержащим их в качестве активного компонента.
Известно, что производные 3-триазолилфенилсульфида в качестве инсектицидов, акарицидов и нематоцидов уже были впервые описаны в патенте 1. Как впервые указано в документе, группа соединений имеет высокую эффективность против клещей, когда непосредственно распыляется над растениями. Однако в документе не описывается обработка грунта. Группа соединений, впервые описанная в документе, имеет недостаточное проникновение в грунт и инфильтрацию в растения при обработке грунта. По этой причине, в некоторых случаях невозможно достичь достаточного действия из-за неравномерного распыления химикатов, транспирации, фотолиза, стекания химикатов под действием дождя и т.д.
В настоящее время известно незначительное количество акарицидов, имеющих практическую активность для обработки грунта. Химикаты, которые могут применяться для обработки грунта, являются выгодными для фермеров в связи с повышенной безопасностью, меньшими трудозатратами и т.д. Поэтому, требуется развитие акарицидов, обладающих активностью при обработке грунта.
Патент 1: JP-A-2000-198768
В этих обстоятельствах, целью настоящего изобретения является решение вышеупомянутых проблем традиционных инсектицидов, акарицидов и нематоцидов и предоставление инсектицидов, акарицидов и нематоцидов, превосходных по безопасности, пестицидным действиям, остаточной эффективности и т.д.
Авторы настоящего изобретения синтезировали различные производные 3-триазолилфенилсульфида и исследовали их физиологические активности с целью усовершенствования инсектицидов, акарицидов и нематоцидов, имеющих вышеупомянутые предпочтительные характеристики. В результате авторы нашли, что следующие новые производные 3-триазолилфенилсульфида по настоящему изобретению (в дальнейшем иногда определяемые как соединения по настоящему изобретению) демонстрируют превосходное действие на различных сельскохозяйственных и садовых паразитах, в особенности клещах, представленных клещиком паутинным двупятнистым, клещиком паутинным Канзавы и клещиком красным цитрусовым, паразитных чешуекрылых, представленных капустной молью, огневкой стеблевой азиатской и походных червях, паразитных полужесткокрылых, представленных коричневым рисовым дельфацидом, зеленой рисовой цикадкой и хлопковой тлей, паразитных жесткокрылых, представленных долгоносиком лучистой фасоли, и на нематодах, представленных южной нематодой корневых наростов; и имеют активность при обработке грунта, с которой становится возможным безопасное и трудосберегающее применение. Настоящее изобретение выполнено на основании этих открытий.
Таким образом, содержание настоящего изобретения представлено ниже.
(1) Производное 3-триазолилфенилсульфида, представленное формулой [I]:

где R представляет собой циклопропилметильную группу или трифторэтильную группу;
n представляет собой целое число от 0 до 1;
A1 И A3 выбраны из групп Группы I и Группы II, при условии, что по меньшей мере одна из них выбрана из групп Группы II;
B2 представляет собой атом водорода, атом галогена или метильную группу; и
B4 представляет собой атом галогена, цианогруппу, нитрогруппу или C1-C6-алкильную группу (которая может быть моно- или поли-замещена атомами галогена);
при условии, что, когда A3 представляет собой NH2, B2 представляет собой атом галогена или метильную группу.
(Группа I)
атом водорода, атом галогена, C1-C6-алкильная группа (которая может быть моно- или поли-замещена атомами галогена, гидроксильными группами, цианогруппами, C2-C7-алкоксикарбонильными группами или C1-C6-алкоксигруппами), C3-C8-циклоалкильная группа (которая может быть моно- или поли-замещена алкильными группами, атомами галогена, цианогруппами или C1-C6-алкоксигруппами), C2-C6-алкенильная группа (которая может быть моно- или поли-замещена атомами галогена или цианогруппами), C2-C6-алкинильная группа (которая может быть моно- или поли-замещена атомами галогена или цианогруппами), C1-C6-алкоксигруппа (которая может быть моно- или поли-замещена атомами галогена, цианогруппами, C2-C5-алкоксикарбонильными группами или C1-C3-алкоксигруппами), C1-C6-алкилтиотиогруппа (которая может быть моно- или поли-замещена атомами галогена, C1-C3-алкоксигруппами, C3-C8-циклоалкильными группами, которые могут быть замещены атомами галогена или цианогруппами), C1-C6-алкилсульфинильная группа (которая может быть моно- или поли-замещена атомами галогена, C1-C3-алкоксигруппами, C3-C8-циклоалкильными группами, которые могут быть замещены атомами галогена или цианогруппами), C1-C6-алкилсульфонильная группа (которая может быть моно- или поли-замещена атомами галогена, C1-C3-алкоксигруппами или C3-C8-циклоалкильными группами, которые могут быть замещены атомами галогена), C2-C6-алкинилтио группа (которая может быть моно- или поли-замещена атомами галогена, C1-C3-алкоксигруппами или цианогруппами), C2-C6-алкинилсульфинильная группа (которая может быть моно- или поли-замещена атомами галогена, C1-C3-алкоксигруппами или цианогруппами), C1-C7-ацильная группа и C2-C5-галогеналкилкарбонильная группа.
(Группа II)
нитротиогруппа, цианогруппа, -N=CR1R2 группа, -N=C(NR2'R3')NR2R3-группа, -N(SO2R2)R3-группа, -N(OR3)R3'-группа, -C(=O)OR2-группа, -C(=Q)NR2R3-группа, -SO2NR2R3-группа, -NR2R3-группа, -N(COR2)R3-группа и -N(COOR2)R3-группа;
где R1 представляет собой атом водорода, C1-C6-алкильную группу (которая может быть моно- или поли-замещена атомами галогена, гидроксильными группами, цианогруппами, C2-C7-алкоксикарбонильными группами или C1-C6-алкоксигруппами), C3-C6-алкенильную группу (которая может быть моно- или поли-замещена атомами галогена или цианогруппами), C3-C6-алкинильную группу (которая может быть моно- или поли-замещена атомами галогена или цианогруппами), C3-C6-циклоалкильную группу (которая может быть моно- или поли-замещена атомами галогена, гидроксильными группами, цианогруппами, C2-C7-алкоксикарбонильными группами или C1-C6-алкоксигруппами), арилалкильную группу (которая может быть моно- или поли-замещена атомами галогена, цианогруппами, C1-C6-алкильными группами, C1-C6-галогеналкильными группами, C2-C7-алкоксикарбонильными группами или C1-C6-алкоксигруппами), гетероарилалкильную группу (которая может быть моно- или поли-замещена атомами галогена, цианогруппами, C1-C6-алкильными группами, C1-C6-галогеналкильными группами, C2-C7-алкоксикарбонильными группами или C1-C6-алкоксигруппами), арильную группу (которая может быть моно- или поли-замещена атомами галогена, цианогруппами, C1-C6-алкильными группами, C1-C6-галогеналкильными группами, C2-C7-алкоксикарбонильными группами, C1-C6-алкоксигруппами или гидроксильными группами), гетероарильную группу (которая может быть моно- или поли-замещена атомами галогена, цианогруппами, C1-C6-алкильными группами, C1-C6-галогеналкильными группами, C2-C7-алкоксикарбонильными группами или C1-C6-алкоксигруппами), C1-C6-алкоксигруппу, C1-C6-алкилтиогруппу, аминогруппу, C1-C6-моноалкиламиногруппу или C2-C12-диалкиламиногруппу;
где каждый из R2 и R2' представляет собой атом водорода, C1-C6-алкильную группу (которая может быть моно- или поли-замещена атомами галогена, гидроксильными группами, цианогруппами, C2-C7-алкоксикарбонильными группами или C1-C6-алкоксигруппами), C3-C6-алкенильную группу (которая может быть моно- или поли-замещена атомами галогена или цианогруппами), C3-C6-алкинильную группу (которая может быть моно- или поли-замещена атомами галогена или цианогруппами), C3-C6-циклоалкильную группу (которая может быть моно- или поли-замещена атомами галогена, гидроксильными группами, цианогруппами, C2-C7-алкоксикарбонильными группами или C1-C6-алкоксигруппами), аминогруппу, C1-C6-моноалкиламиногруппу, C2-C12-диалкиламиногруппу, арилалкильную группу (которая может быть моно- или поли-замещена атомами галогена, цианогруппами, C1-C6-алкильными группами, C1-C6-галогеналкильными группами, C2-C7-алкоксикарбонильными группами или C1-C6-алкоксигруппами), гетероарилалкильную группу (которая может быть моно- или поли-замещена атомами галогена, цианогруппами, C1-C6-алкильными группами, C1-C6-галогеналкильными группами, C2-C7-алкоксикарбонильными группами или C1-C6-алкоксигруппами), арильную группу (которая может быть моно- или поли-замещена атомами галогена, цианогруппами, C1-C6-алкильными группами, C1-C6-галогеналкильными группами, C2-C7-алкоксикарбонильными группами или C1-C6-алкоксигруппами) или гетероарильную группу (которая может быть моно- или поли-замещена атомами галогена, цианогруппами, C1-C6-алкильными группами, C1-C6-галогеналкильными группами, C2-C7-алкоксикарбонильными группами или C1-C6-алкоксигруппами);
где каждый из R3 и R3' представляет собой атом водорода, C1-C6-алкильную группу (которая может быть моно- или поли-замещена атомами галогена, гидроксильными группами, цианогруппами, C2-C7-алкоксикарбонильными группами или C1-C6-алкоксигруппами), C3-C6-алкенильную группу (которая может быть моно- или поли-замещена атомами галогена или цианогруппами), C3-C6-алкинильную группу (которая может быть моно- или поли-замещена атомами галогена или цианогруппами) или C3-C6-циклоалкильную группу (которая может быть моно- или поли-замещена атомами галогена, гидроксильными группами, цианогруппами, C2-C7-алкоксикарбонильными группами или C1-C6-алкоксигруппами);
а Q представляет собой атом кислорода или атом серы;
при условии, что R1 И R2 в -N=CR1R2-группе, вместе с атомом углерода, к которому они присоединены, могут образовывать 5-6-членный цикл,
R2 и R3, или R2' и R3' в -N=C(NR2'R3')NR2R3-группе, совместно с атомом азота, к которому они присоединены, могут образовывать 5-6-членный цикл, и R2 и R3 в -NR2R3-группе, вместе с атомом азота, к которому они присоединены, могут образовывать 5-6-членный цикл.
(2) Производное 3-триазолилфенилсульфида согласно пункту (1) выше, где R представляет собой трифторэтильную группу;
n представляет собой целое число от 0 до 1;
A1 представляет собой C1-C6-алкильную группу (которая может быть моно- или поли-замещена атомами галогена или цианогруппами), C1-C6-алкилтиогруппу (которая может быть моно- или поли-замещена атомами галогена) или C1-C6-алкилсульфинильную группу (которая может быть моно- или поли-замещена атомами галогена или C1-C3-алкоксигруппами);
A3 представляет собой -NR2R3-группу или -N(COR2)R3-группу;
где каждый из R2 и R3, которые являются независимыми друг от друга, представляют собой атом водорода, C1-C6-алкиламино группу, C1-C6-алкильную группу (которая может быть моно- или поли-замещена атомами галогена или цианогруппами) или C3-C6-алкинильную группу (которая может быть моно- или поли-замещена атомами галогена или цианогруппами), при условии, что R2 и R3 не являются одновременно атомами водорода;
B2 представляет собой атом водорода, атом галогена или метильную группу; и
B4 представляет собой цианогруппу или C1-C6-алкильную группу (которая может быть моно- или поли-замещена атомами галогена).
(3) Производное 3-триазолилфенилсульфида согласно пункту (1) выше, где R представляет собой трифторэтильную группу; n представляет собой целое число от 0 до 1;
А1 представляет собой C1-C6-алкильную группу (которая может быть моно- или поли-замещена атомами галогена или цианогруппами), C1-C6-алкилтиогруппу (которая может быть моно- или поли-замещена атомами галогена) или C1-C6-алкилсульфинильную группу (которая может быть моно- или поли-замещена атомами галогена или C1-C3-алкоксигруппами);
A3 представляет собой аминогруппу;
B2 представляет собой атом галогена или метильную группу; и B4 представляет собой цианогруппу или C1-C6-алкильную группу (которая может быть моно- или поли-замещена атомами галогена).
(4) Производное 3-триазолилфенилсульфида согласно пункту (2) выше, где А1 представляет собой изопропильную группу, трет-бутильную группу, дифторметильную группу, трифторметильную группу, трифторметилтиогруппу, 2,2,2-трифторэтилтиогруппу, 1,1,2,2-тетрафторэтилтиогруппу, пентафторэтилтиогруппу, трифторметилсульфинильную группу, 2,2,2-трифторэтилсульфинильную группу или пентафторэтилсульфинильную группу; и A3 представляет собой метиламиногруппу, этиламиногруппу, пропиламиногруппу, цианометиламиногруппу, пропаргиламиногруппу, ацетиламиногруппу, пропиониламиногруппу, трифторацетиламиногруппу или дифторацетиламиногруппу.
(5) Производное 3-триазолилфенилсульфида согласно пункту выше (3), где A1 представляет собой изопропильную группу, трет-бутильную группу, дифторметильную группу, трифторметильную группу, трифторметилтио группу, 2,2,2-трифторэтилтио группу, 1,1,2,2-тетрафторэтилтио группу, пентафторэтилтио группу, трифторметилсульфинильную группу, 2,2,2-трифторэтилсульфинильную группу или пентафторэтилсульфинильную группу; и
A3 представляет собой аминогруппу.
(6) Производное 3-триазолилфенилсульфида согласно пункту (2) выше, где A1 представляет собой трифторметильную группу, трифторметилтио группу или 2,2,2-трифторэтилсульфинильную группу и
A3 представляет собой метиламиногруппу или трифторацетиламиногруппу.
(7) Производное 3-триазолилфенилсульфида согласно пункту (2) выше, где A1 представляет собой трифторметильную группу, трифторметилтио группу или 2,2,2-трифторэтилсульфинильную группу; и
A3 представляет собой аминогруппу.
(8) Производное анилина, представленное формулой [I-a], которое является промежуточным соединением для получения производного 3-триазолилфенилсульфида, как определено в любом из вышеупомянутых пунктов (1)-(7):

где B2 представляет собой атом галогена или метильную группу, и B4 представляет собой C1-C6-алкильную группу.
(9) Производное анилина согласно пункту (8), где B4 представляет собой метильную группу.
(10) Инсектицид, акарицид или нематоцид для сельскохозяйственного и садоводческого применения, содержащий в качестве активного компонента производное 3-триазолилфенилсульфида, как определено в любом из вышеупомянутых пунктов (1)-(7).
Соединения по настоящему изобретению проявляют превосходные пестицидные действия против широкого диапазона паразитов, включая полужесткокрылых паразитов, чешуекрылых паразитов, жесткокрылых паразитов, двукрылых паразитов, перепончатокрылых паразитов, прямокрылых паразитов, паразитов рода Isoptera, паразитов рода Thysanoptera, клещей и нематод, паразитирующих на растениях, и они также способны контролировать паразитов, которые имеют приобретенную устойчивость к традиционным пестицидам.
В частности, соединения по настоящему изобретению проявляют превосходное действие на различных паразитах, в особенности на сельскохозяйственных и садовых паразитах, включая клещей, представленных клещиком паутинным двупятнистым, клещиком паутинным Канзавы и клещиком красным цитрусовым, чешуекрылых паразитов, представленных капустной молью, огневкой стеблевой азиатской и походными червями, полужесткокрылых паразитов, представленных коричневым рисовым дельфацидом, зеленой рисовой цикадкой и хлопковой тлей, жесткокрылых паразитов, представленных долгоносиком лучистой фасоли, и нематод, представленных южной нематодой корневых наростов; и они обладают превосходным системным действием. Согласно этому они могут применяться для безопасного и трудосберегающего применения при обработке грунта.
Символы и термины, используемые в этом описании, будут определены ниже.
Атом галогена обозначает атом фтора, атом хлора, атом брома или атом иода.
Обозначение C1-C6-, и т.д., обозначает, что последующий заместитель имеет, в этом варианте, от 1 до 6 атомов углерода.
«C1-C6-алкильная группа» обозначает, если не оговорено особо, линейную или разветвленную алкильную группу, имеющую от 1 до 6 атомов углерода, такую как метильная, этильная, н-пропильная, изопропильная, н-бутильная, втор-бутильная, изобутильная, трет-бутильная, н-пентильная, 1-метилбутильная, 2-метилбутильная, 3-метилбутильная, 1-этилпропильная, 1,1-диметилпропильная, 1,2-диметилпропильная, неопентильная, н-гексильная, 1-метилпентильная, 2-метилпентильная, 3-метилпентильная, 4-метилпентильная, 1-этилбутильная, 2-этилбутильная, 1,1-диметилбутильная, 1,2-диметилбутильная, 1,3-диметилбутильная, 2,2-диметилбутильная, 2,3-диметилбутильная, 3,3-диметилбутильная, 1,1,2-триметилпропильная, 1,2,2-триметилпропильная, 1-этил-1-метилпропильная или 1-этил-2-метилпропильная группа.
«C3-C6-циклоалкильная группа» обозначает, если не оговорено особо, циклоалкильную группу, имеющую от 3 до 6 атомов углерода, такую как циклопропильная, циклобутильная, циклопентильная или циклогексильная группа.
«C2-C6-алкенильная группа» обозначает, если не оговорено особо, линейную или разветвленную алкенильную группу, имеющую от 2 до 6 атомов углерода, такую как винильная, 1-пропенильная, изопропенильная, 2-пропенильная, 1-бутенильная,
1-метил-1-пропенильная, 2-бутенильная, 1-метил-2-пропенильная, 3-бутенильная, 2-метил-1-пропенильная, 2-метил-2-пропенильная, 1,3-бутадиенильная, 1-пентенильная, 1-этил-2-пропенильная,
2-пентенильная, 1-метил-1-бутенильная, 3-пентенильная,
1-метил-2-бутенильная, 4-пентенильная, 1-метил-3-бутенильная,
3-метил-1-бутенильная, 1,2-диметил-2-пропенильная,
1,1-диметил-2-пропенильная, 2-метил-2-бутенильная,
3-метил-2-бутенильная, 1,2-диметил-1-пропенильная,
2-метил-3-бутенильная, 3-метил-3-бутенильная,
1,3-пентадиенильная, 1-винил-2-пропенильная, 1-гексенильная,
1-пропил-2-пропенильная, 2-гексенильная, 1-метил-1-пентенильная, 1-этил-2-бутенильная, 3-гексенильная, 4-гексенильная,
5-гексенильная, 1-метил-4-пентенильная, 1-этил-3-бутенильная,
1-(изобутил)винильная, 1-этил-1-метил-2-пропенильная,
1-этил-2-метил-2-пропенильная, 1-(изопропил)-2-пропенильная,
2-метил-2-пентенильная, 3-метил-3-пентенильная,
4-метил-3-пентенильная, 1,3-диметил-2-бутенильная,
1,1-диметил-3-бутенильная, 3-метил-4-пентенильная,
4-метил-4-пентенильная, 1,2-диметил-3-бутенильная,
1,3-диметил-3-бутенильная, 1,1,2-триметил-2-пропенильная,
1,5-гексадиенильная, 1-винил-3-бутенильная или
2,4-гексадиенильная группа.
«C3-C6-алкинильная группа» обозначает, если не оговорено особо, линейную или разветвленную алкинильную группу, имеющую от 2 до 6 атомов углерода, такую как этинильная, 1-пропинильная,
2-пропинильная, 1-бутинильная, 1-метил-2-пропинильная,
2-бутинильная, 3-бутинильная, 1-пентинильная,
1-этил-2-пропинильная, 2-пентинильная, 3-пентинильная,
1-метил-2-бутинильная, 4-пентинильная, 1-метил-3-бутинильная,
2-метил-3-бутинильная, 1-гексинильная,
1-(н-пропил)-2-пропинильная, 2-гексинильная,
1-этил-2-бутинильная, 3-гексинильная, 1-метил-2-пентинильная,
1-метил-3-пентинильная, 4-метил-1-пентинильная,
3-метил-1-пентинильная, 5-гексинильная, 1-этил-3-бутинильная,
1-этил-1-метил-2-пропинильная, 1-(изопропил)-2-пропинильная, 1,1-диметил-2-бутинильная или 2,2-диметил-3-бутинильная группа.
«C1-C6-галогеналкильная группа» обозначает, если не оговорено особо, C1-C4-линейную или разветвленную алкильную группу, замещенную 1-9 идентичными или различными атомами галогена, такие как фторметильная, хлорметильная, бромметильная, дифторметильная, дихлорметильная, трифторметильная, трихлорметильная, хлордифторметильная, бромдифторметильная,
2-фторэтильная, 1-хлорэтильная, 2-хлорэтильная, 1-бромэтильная, 2-бромэтильная, 2,2-дифторэтильная, 1,2-дихлорэтильная, 2,2-дихлорэтильная, 2,2,2-трифторэтильная, 2,2,2-трихлорэтильная,
1,1,2,2-тетрафторэтильная, пентафторэтильная, 2-бром-2-хлорэтильная, 2-хлор-1,1,2,2-тетрафторэтильная, 1-хлор-1,2,2,2-тетрафторэтильная, 1-хлорпропильная, 2-хлорпропильная, 3-хлорпропильная, 2-бромпропильная, 3-бромпропильная, 2-бром-1-метилэтильная, 3-иодпропильная, 2,3-дихлорпропильная, 2,3-дибромпропильная, 3,3,3-трифторпропильная, 3,3,3-трихлорпропильная, 3-бром-3,3-дифторпропильная, 3,3-дихлор-3-фторпропильная, 2,2,3,3-тетрафторпропильная, 1-бром-3,3,3-трифторпропильная, 2,2,3,3,3-пентафторпропильная, 2,2,2-трифтор-1-трифторметилэтильная, гептафторпропильная, 1,2,2,2-тетрафтор-1-трифторметилэтильная, 2,3-дихлор-1,1,2,3,3-пентафторпропильная, 2-хлорбутильная, 3-хлорбутильная, 4-хлорбутильная, 2-хлор-1,1-диметилэтильная, 4-бромбутильная, 3-бром-2-метилпропильная, 2-бром-1,1-диметилэтильная, 2,2-дихлор-1,1-диметилэтильная, 2-хлор-1-хлорметил-2-метилэтильная, 4,4,4-трифторбутильная, 3,3,3-трифтор-1-метилпропильная, 3,3,3-трифтор-2-метилпропильная, 2,3,4-трихлорбутильная, 2,2,2-трихлор-1,1-диметилэтильная, 4-хлор-4,4-дифторбутильная, 4,4-дихлор-4-фторбутильная, 4-бром-4,4-дифторбутильная, 2,4-дибром-4,4-дифторбутильная, 3,4-дихлор-3,4,4-трифторбутильная, 3,3-дихлор-4,4,4-трифторбутильная, 4-бром-3,3,4,4-тетрафторбутильная, 4-бром-3-хлор-3,4,4-трифторбутильная, 2,2,3,3,4,4-гексафторбутильная, 2,2,3,4,4,4-гексафторбутильная, 2,2,2-трифтор-1-метил-1-трифторметилэтильная, 3,3,3-трифтор-2-трифторметилпропильная, 2,2,3,3,4,4,4-гептафторбутильная, 2,3,3,3-тетрафтор-2-трифторметилпропильная, 1,1,2,2,3,3,4,4-октафторбутильная, нонафторбутильная или 4-хлор-1,1,2,2,3,3,4,4-октафторбутильная группа.
«C1-C6-алкоксигруппа» обозначает (алкил)-O-группу, где алкильный фрагмент определен выше, такую как метокси, этокси, н-пропокси, изопропокси, н-бутокси, изобутокси, трет-бутокси, пентилокси, изопентилокси или гексилокси-группа.
«C1-C6-алкокси-C1-C6-алкильная группа» обозначает алкильную группу, имеющую от 1 до 6 атомов углерода, замещенную алкокси группой, имеющей от 1 до 6 атомов углерода, где алкильный фрагмент и алкоксильный фрагмент определены выше, такую как метоксиметильная, этоксиметильная, изопропоксиметильная, н-бутоксиметильная, изобутоксиметильная, пентилоксиметильная, метоксиэтильная, н-бутоксиэтильная или изобутоксиэтильная группа.
«C1-C6-алкилтио группа» обозначает (алкил)-S-группу, имеющую от 1 до 6 атомов углерода, где алкильный фрагмент определен выше, такую как метилтио, этилтио, н-пропилтио или изопропилтио.
«C1-C6-алкилсульфинильная группа» обозначает (алкил)-SO-группу, имеющую от 1 до 6 атомов углерода, где алкильный фрагмент определен выше, такую как метилсульфинил, этилсульфинил, н-пропилсульфинил или изопропилсульфинил.
«C1-C6-алкилсульфонильная группа» обозначает (алкил)-SO2-группу, имеющую от 1 до 6 атомов углерода, где алкильный фрагмент определен выше, такую как метилсульфонил, этилсульфонил, н-пропилсульфонил или изопропилсульфонил.
«C1-C7-ацильная группа» обозначает формильную группу или (алкил)-C(=O)-группу, имеющую от 1 до 6 атомов углерода, где алкильный фрагмент определен выше, такую как ацетил или пропионил.
«C2-C7-алкоксикарбонильная группа» обозначает (алкил)-O-C(=O)-группу, имеющую от 1 до 6 атомов углерода, где алкильный фрагмент определен выше, такую как метоксикарбонил, этоксикарбонил, н-пропоксикарбонил или изопропоксикарбонил.
«C1-C4-галогеналкилкарбонильная группа» обозначает (галогеналкил)-C(=O)-группу, имеющую от 1 до 4 атомов углерода, где галогеналкильный фрагмент определен выше, такую как хлорацетил, трифторацетил, пентафторпропионил или дифторметилтио.
«C1-C6-моноалкиламиногруппа» обозначает аминогруппу, моно-замещенную алкильную группу, где алкильный фрагмент определен выше, такую как метиламино, этиламино или н-пропиламино.
«C2-C12-диалкиламиногруппа» обозначает аминогруппу, дизамещенную алкильными группами, где алкильные фрагменты определены выше, такую как диметиламино, диэтиламино или N-этил-N-метиламино.
«Арильная группа» обозначает ароматическую углеводородную группу, такой как фенил или нафтил.
«Арилалкильная группа» обозначает (арил)-(алкильную) группу, где арильный и алкильный фрагменты определены выше, такую как бензил, фенэтил или нафтилметил.
«Гетероарильная группа» обозначает ароматическую гетероциклическую группу, такую как тиенил, пиридил или бензотиазолил.
«Гетероарилалкильная группа» обозначает (гетероарил)-(алкильную) группу, где гетероарильный и алкильный фрагменты определены выше, такую как тиенилметил или пиридилметил.
Предпочтительные соединения вышеупомянутой формулы [I] представляют собой соединения, где R представляет собой 2,2,2-трифторэтильную группу и n равно 0 или 1.
Более предпочтительные соединения представляют собой соединения, где R представляет собой 2,2,2-трифторэтильную группу, B2 представляет собой атом галогена, B4 представляет собой алкильную группу или галогеналкильную группу, и n равен 0 или 1.
Конкретные примеры соединений по настоящему изобретению, представленные формулой [I], даны здесь в таблицах 1-6. Однако соединения по настоящему изобретению не ограничены этими соединениями. Далее, эти соединения включают в себя соединения, имеющие оптические изомеры. Номера соединений относятся к последующему описанию.
Сокращения в таблицах в этом описании обозначают нижеследующие соответствующие группы.
Например, Ph-4-Cl обозначает 4-хлорфенил, и 3-Py-6-Cl обозначает 6-хлор-3-пиридил.






Соединения по настоящему изобретению, представленные формулой [I], могут быть получены в соответствии со следующими способами получения. Однако их получение не ограничено этими способами.
<Способ получения 1>
Соединение по настоящему изобретению формулы [I-1] может быть получено способом, представленным на следующей схеме:

где L1 представляет собой атом галогена, алкилсульфонилокси группу, фенилсульфонилокси группу или SO2M, M представляет собой щелочной металл или щелочноземельный металл, щелочной металл представляет собой предпочтительно натрий или калий, и A1, A3, B2, B4 и R определены выше.
Таким образом, производное 3-триазолилфенилсульфида формулы [I-1], которое представляет собой соединение по настоящему изобретению, может быть получено взаимодействием соединения формулы [II] с соединением формулы [III] в растворителе в присутствии основания или в присутствии радикального инициатора.
Количество используемого соединения формулы [III] выбирают из диапазона от 1 до 5 молей на 1 моль соединения формулы [I], и предпочтительно от 1,2 до 2,0 молей.
Используемый в этой реакции растворитель может, например, представлять собой простой эфир, такой как диэтиловый эфир, тетрагидрофуран или диоксан, ароматический углеводород, такой как бензол, толуол, ксилол или хлорбензол, галогенированный углеводород, такой как дихлорметан, хлороформ или дихлорэтан, апротонный полярный растворитель, такой как ацетонитрил, N,N-диметилформамид, N,N-диметилацетамид, N-метил-2-пирролидон, диметилсульфоксид или сульфолан, спирт, такой как метанол, этанол или изопропиловый спирт, нитрил, такой как ацетонитрил или пропионитрил, сложный эфир, такой как этилацетат или этилпропионат, алифатический углеводород, такой как пентан, гексан, циклогексан или гептан, пиридин, такой как пиридин или пиколин, или воду, или смесь этих растворителей.
Основание, используемое в этой реакции, может, например, представлять собой неорганическое основание, такое как гидроксид щелочного металла, такой как гидроксид натрия или гидроксид калия, гидроксид щелочноземельного металла, такой как гидроксид кальция или гидроксид магния, карбонат щелочного металла, такой как карбонат натрия или карбонат калия, или бикарбонат щелочного металла, такой как бикарбонат натрия или бикарбонат калия, гидрид металла, такой как гидрид натрия или гидрид калия, спиртовую соль металла, такую как метоксид натрия, этоксид натрия или трет-бутоксид калия, или органическое основание, такое как триэтиламин, N,N-диметиланилин, пиридин, 4-N,N-диметиламинопиридин или 1,8-диазабицикло[5.4.0]-7-ундецен.
Количество используемого основания выбирают из диапазона от 0 до 5 молей на 1 моль соединения формулы [II], и предпочтительно от 0 до 1,2 молей.
Радикальный инициатор, используемый в этой реакции, может, например, представляет собой серную кислоту, соль сульфита или аддукт сульфита, такой как ронгалит (формальдегид-сульфоксилат натрия). Основание и радикальный инициатор могут применяться вместе.
В случае, когда используется радикальный инициатор, его количество выбирают из диапазона от 0,01 до 5 молей на 1 моль соединения [II], и предпочтительно от 0,05 до 1,2 молей.
Температура реакции может быть выбрана из диапазона от -30°C до температуры кипения реакционной смеси, и предпочтительно в пределах диапазона от 0°C до 150°C. Время реакции варьирует в зависимости от температуры реакции, реагирующего субстрата, загрузки реакции и т.д. и составляет обычно от 10 минут до 20 часов.
<Способ получения 2>
Соединение по настоящему изобретению формулы [I-1] может также быть получено с применением соединения формулы [IV], которое представляет собой окисленный димер соединения формулы [II], используемый в качестве исходного вещества в способе получения 1:

где L2 представляет собой атом галогена или сульфинатную соль, а A1, A3, B2, B4 и R определены выше.
Таким образом, целевое производное 3-триазолилфенилсульфида формулы [I-1] может быть получено взаимодействием соединения формулы [IV] с соединением формулы [V] в растворителе в присутствии радикального инициатора.
Количество соединения формулы [V], используемого в этой реакции, можно выбрать из диапазона от 1 до 5 молей на 1 моль соединения формулы [IV], и предпочтительно от 1,2 до 2,0 молей.
Растворитель, используемый в этой реакции, может, например, представлять собой простой эфир, такой как диэтиловый эфир, тетрагидрофуран или диоксан, ароматический углеводород, такой как бензол, толуол, ксилол или хлорбензол, апротонный полярный растворитель, такой как N,N-диметилформамид, N,N-диметилацетамид, N-метил-2-пирролидон, диметилсульфоксид или сульфолан, нитрил, такой как ацетонитрил или пропионитрил, сложный эфир, такой как этилацетат или этилпропионат, алифатический углеводород, такой как пентан, гексан, циклогексан или гептан, пиридин, такой как пиридин или пиколин, или вода, или смесь этих растворителей.
Радикальный инициатор может, например, представлять собой серную кислоту, сульфитную соль или сульфитный аддукт, такой как ронгалит (формальдегидсульфоксилат натрия).
В случае, когда применяют радикальный инициатор, его количество может быть выбрано из диапазона от 0,01 до 5 молей на 1 моль соединения [II], и предпочтительно от 0,05 до 1,2 молей.
Температуру реакции выбирают из диапазона от -30°C до температуры кипения реакционной смеси, и предпочтительно в пределах диапазона от 0°C до 150°C. Время реакции варьирует в зависимости от температуры реакции, реагирующего субстрата, загрузки реакции и т.д. и составляет обычно от 10 минут до 20 часов.
<Способ получения 3>
Соединение формулы [I-2], которое представляет собой соединение по настоящему изобретению, может быть получено способом, представленным на следующей схеме:
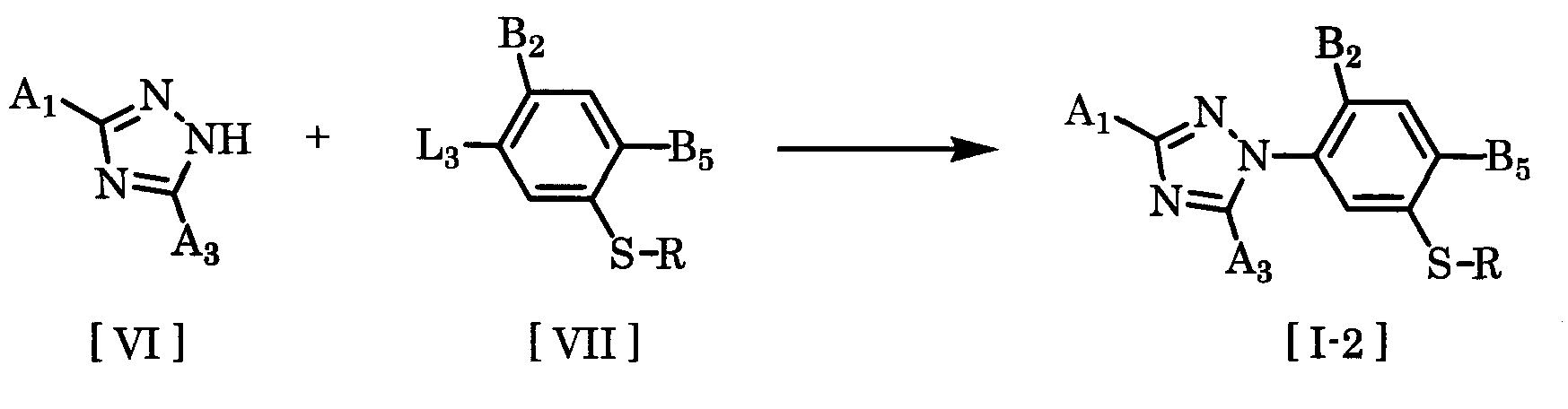
где B5 представляет собой электроноакцепторную группу, A1, A3, B2 и R определены выше, L3 представляет собой уходящую группу, такую как атом галогена, алкилсульфонилокси группу или фенилсульфонилокси группу, и электроноакцепторная группа представляет собой цианогруппу, нитрогруппу или подобные.
Таким образом, соединение по настоящему изобретению формулы [I-2] может быть получено взаимодействием соединения формулы [VI] с соединением формулы [VII] в растворителе в присутствии основания.
Количество соединения формулы [VII] может быть выбрано из диапазона от 1 до 5 молей на 1 моль соединения формулы [VI], и предпочтительно от 1,0 до 1,2 молей.
Растворитель, используемый в этой реакции, не ограничен тем, что он не ингибируют реакцию, и он может, например, представлять собой ароматический углеводород, такой как бензол, толуол или ксилол, простой эфир, такой как диэтиловый эфир, тетрагидрофуран, 1,2-диметоксиэтан или диоксан, кетон, такой как ацетон или метилэтилкетон, нитрил, такой как ацетонитрил или пропионитрил, апротонный полярный растворитель, такой как диметилсульфоксид, N,N-диметилформамид или N,N-диметилацетамид, алифатический углеводород, такой как пентан, гексан, циклогексан или гептан или пиридин, такой как пиридин или пиколин, или смесь этих растворителей.
Основание, используемое в этой реакции, может, например, представлять собой неорганическое основание, такое как гидроксид щелочного металла, такой как гидроксид натрия или гидроксид калия, гидроксид щелочноземельного металла, такой как гидроксид кальция или гидроксид магния, карбонат щелочного металла, такой как карбонат натрия или карбонат калия, или бикарбонат щелочного металла, такой как бикарбонат натрия или бикарбонат калия, гидрид металла, такой как гидрид натрия или гидрид калия, спиртовую соль металла, такую как метоксид натрия, этоксид натрия или трет-бутоксид калия, или органическое основание, такое как триэтиламин, N,N-диметиланилин, пиридин, 4-N,N-диметиламинопиридин или 1,8-диазабицикло[5.4.0]-7-ундецен.
Количество используемого основания выбирают из диапазона от 1 до 5 молей на 1 моль соединения формулы [II], и предпочтительно от 1,1 до 1,2 молей.
Температура реакции может быть выбрана из диапазона от -70°C до температуры кипения реакционной смеси, и предпочтительно в пределах диапазона от -20°C до 150°C. Время реакции варьирует в зависимости от температуры реакции, реагирующего субстрата, загрузки реакции и т.д. и составляет обычно от 10 минут до 20 часов.
<Способ получения 4>
Соединение формулы [I-2], которое представляет собой соединение по настоящему изобретению, может также быть получено следующей реакцией замещения:

где A1, A3, B2, B5 и R определены выше, а L4представляет собой атом галогена, алкилсульфонилокси группу, фенилсульфонилокси группу, алкилсульфонильную группу, фенилсульфонильную группу или нитрогруппу.
Таким образом, производное 3-триазолилфенилсульфида формулы [I-2], которое представляет собой соединение по настоящему изобретению, может быть получено взаимодействием соединения формулы [IX] с соединением формулы [X] в растворителе в присутствии основания или оксида меди (I).
Растворитель, используемый в этой реакции, может, например, представлять собой простой эфир, такой как диэтиловый эфир, тетрагидрофуран или диоксан, ароматический углеводород, такой как бензол, толуол, ксилол или хлорбензол, апротонный полярный растворитель, такой как N,N-диметилформамид, N,N-диметилацетамид, N-метил-2-пирролидон, диметилсульфоксид или сульфолан, спирт, такой как метанол, этанол или метилцеллозольв, алифатический углеводород, такой как пентан, гексан, циклогексан или гептан, пиридин, такой как пиридин или пиколин, или воду, или смесь этих растворителей.
Основание, используемое в этой реакции, может, например, представлять собой неорганическое основание, такое как гидроксид щелочного металла, такой как гидроксид натрия или гидроксид калия, гидроксид щелочноземельного металла, такой как гидроксид кальция или гидроксид магния, карбонат щелочного металла, такой как карбонат натрия или карбонат калия, или бикарбонат щелочного металла, такой как бикарбонат натрия или бикарбонат калия, гидрид металла, такой как гидрид натрия или гидрид калия, спиртовую соль металла, такую как метоксид натрия, этоксид натрия или трет-бутоксид калия, или органическое основание, такое как триэтиламин, N,N-диметиланилин, пиридин, 4-N,N-диметиламинопиридин или 1,8-диазабицикло[5.4.0]-7-ундецен.
Количество основания или используемого оксида меди (I) выбирают из диапазона от 1 до 5 молей на 1 моль соединения формулы [IX], и предпочтительно от 1,0 до 1,2 молей.
Температура реакции может быть выбрана из диапазона от -70°C до температуры кипения реакционной смеси, и предпочтительно в пределах диапазона от 0°C до 150°C. Время реакции варьирует в зависимости от температуры реакции, реагирующего субстрата, загрузки реакции и т.д. и составляет обычно от 10 минут до 20 часов.
<Способ получения 5>
Соединение формулы [I], которое представляет собой соединение по настоящему изобретению, может быть получено способом, представленным на следующей схеме:

где A1, A3, B2, B4, R и n определены выше.
Таким образом, соединение по настоящему изобретению, представленное формулой [I], может быть получено взаимодействием соединения формулы [VI] с соединением формулы [VIII] и безводной солью меди в растворителе в присутствии органического основания.
Количество используемого соединения формулы [VIII] выбирают из диапазона от 1 до 5 молей на 1 моль соединения формулы [VI], и предпочтительно от 1,0 до 2,0 молей.
Растворитель, используемый в этой реакции, не ограничен тем, что он не ингибирует реакцию, и он может, например, представлять собой галогенированный алкан, такой как хлороформ или дихлорметан, ароматический углеводород, такой как бензол, толуол или ксилол, простой эфир, такой как диэтиловый эфир, тетрагидрофуран, 1,2-диметоксиэтан или диоксан, кетон, такой как ацетон или метилэтилкетон, нитрил, такой как ацетонитрил или пропионитрил, апротонный полярный растворитель, такой как N,N-диметилформамид или N,N-диметилацетамид, алифатический углеводород, такой как пентан, гексан, циклогексан или гептан, или пиридин, такой как пиридин или пиколин, или смесь этих растворителей.
Безводная соль меди, используемая в этой реакции может, например, представлять собой безводный ацетат меди. Количество используемой безводной соли меди выбирают из диапазона от 1 до 5 молей на 1 моль соединения формулы [VI], и предпочтительно от 1,2 до 2,2 молей.
Органическое основание, используемое в этой реакции, может, например, представлять собой триэтиламин, N,N-диметиланилин, пиридин, 4-N,N-диметиламинопиридин или 1,8-диазабицикло[5.4.0]-7-ундецен.
Количество используемого органического основания выбирают из диапазона от 1 до 5 молей на 1 моль соединения формулы [VI], и предпочтительно от 1,2 до 4,4 молей.
Температура реакции может быть выбрана из диапазона от 0°C до температуры кипения реакционной смеси, и предпочтительно в пределах диапазона от 10°C до 30°C.
Время реакции варьирует в зависимости от температуры реакции, реагирующего субстрата, загрузки реакции и т.д. и составляет обычно от 8 до 48 часов.
<Способ получения 6>
Соединение формулы [I-1], которое представляет собой соединение по настоящему изобретению, может также быть получено способом, представленным на следующей схеме:

где A1, A3, B2, B4, R и M определены выше.
Таким образом, целевое производное 3-триазолилфенилсульфида формулы [I-1] может быть получено путем конвертирования в растворителе соединения формулы [XI] в диазониевую соль традиционным способом (способом с использованием минеральной кислоты (такой как соляная кислота или серная кислота) и соли нитрита или алкилнитрита) и взаимодействия диазониевой соли с солью меркаптана формулы [XII] или дисульфида формулы [XIII].
Количество соединения формулы [XII] или соединения формулы [XIII], используемых в этой реакции, выбирают из диапазона от 1 до 5 молей на 1 моль соединения формулы [XI], и предпочтительно от 1,0 до 2,0 молей.
Растворитель, используемый в этой реакции может, например, представлять собой простой эфир, такой как диэтиловый эфир, тетрагидрофуран или диоксан, ароматический углеводород, такой как бензол, толуол, ксилол или хлорбензол, галогенированный углеводород, такой как дихлорметан, хлороформ или дихлорэтан, апротонный полярный растворитель, такой как ацетонитрил, N,N-диметилформамид, N,N-диметилацетамид, N-метил-2-пирролидон, диметилсульфоксид или сульфолан, спирт, такой как метанол, этанол или изопропиловый спирт, нитрил, такой как ацетонитрил или пропионитрил, сложный эфир, такой как этилацетат или этилпропионат, алифатический углеводород, такой как пентан, гексан, циклогексан или гептан, пиридин, такой как пиридин или пиколин, или воду, или смесь этих растворителей.
Температура реакции может быть выбрана из диапазона от -30°C до температуры кипения реакционной смеси, и предпочтительно в пределах диапазона от -10°C до 100°C.
Время реакции варьирует в зависимости от температуры реакции, реагирующего субстрата, загрузки реакции и т.д. и составляет обычно от 10 минут до 20 часов.
<Способ получения 7>
Соединение формулы [I], которое представляет собой соединение по настоящему изобретению, может также быть получено способом, представленным на следующей схеме:

где L3, A1, A3, B2, B4, R и n определены выше, Y1 представляет собой алкоксигруппу или алкилтио группу, L5 представляет собой уходящую группу, такую как атом галогена, ацилокси группу, алкилсульфонилокси группу или фенилсульфонилокси группу, и R1' представляет собой алкильную группу.
[Стадия 1]
Таким образом, соединение по настоящему изобретению формулы [I] может быть получено взаимодействием соединения формулы [XIV] с соединением формулы [XV-1] или [XV-2] в растворителе в присутствии основания.
Количество соединения формулы [XV-1] или [XV-2], используемого в этой реакции, находится в пределах диапазона от 1 моль до большого избытка на 1 моль соединения формулы [XIV], и предпочтительно от 1,2 до 2,0 молей.
Растворитель, используемый в этой реакции, может, например, представлять собой простой эфир, такой как диэтиловый эфир, тетрагидрофуран или диоксан, ароматический углеводород, такой как бензол, толуол, ксилол или хлорбензол, галогенированный углеводород, такой как дихлорметан, хлороформ или дихлорэтан, апротонный полярный растворитель, такой как ацетонитрил, N,N-диметилформамид, N,N-диметилацетамид, N-метил-2-пирролидон, диметилсульфоксид или сульфолан, спирт, такой как метанол, этанол или изопропиловый спирт, нитрил, такой как ацетонитрил или пропионитрил, сложный эфир, такой как этилацетат или этилпропионат, алифатический углеводород, такой как пентан, гексан, циклогексан или гептан, пиридин, такой как пиридин или пиколин, или воду, или смесь этих растворителей.
Основание, используемое в этой реакции, может, например, представляет собой неорганическое основание, такое как гидроксид щелочного металла, такой как гидроксид натрия или гидроксид калия, гидроксид щелочноземельного металла, такой как гидроксид кальция или гидроксид магния, карбонат щелочного металла, такой как карбонат натрия или карбонат калия, или бикарбонат щелочного металла, такой как бикарбонат натрия или бикарбонат калия, гидрид металла, такой как гидрид натрия или гидрид калия, спиртовую соль металла, такую как метоксид натрия, этоксид натрия или трет-бутоксид калия, или органическое основание, такое как триэтиламин, N,N-диметиланилин, пиридин, 4-N,N-диметиламинопиридин или 1,8-диазабицикло[5.4.0]-7-ундецен.
Количество используемого основания выбирают из диапазона от 2 до 5 молей на 1 моль соединения формулы [XIV], и предпочтительно от 2,2 до 3,0 молей.
Температура реакции может быть выбрана из диапазона от 0°C до температуры кипения реакционной смеси, и предпочтительно в пределах диапазона от 10°C до 150°C. Время реакции варьирует в зависимости от температуры реакции, реагирующего субстрата, загрузки реакции и т.д. и составляет обычно от 3 до 12 часов.
В другом способе, целевое производное 3-триазолилфенилсульфида формулы [I] может быть получено взаимодействием соединения формулы [XIV] с водным аммиаком, что приводит к соединению формулы [XIV-1] (Стадия 2-1), и взаимодействия этого соединения с соединением формулы [XV-3] или [XV-4] в растворителе в присутствии основания или в присутствии кислотного катализатора (Стадия 2-2).
(Стадия 2-1)
Количество водного аммиака, используемого на этой стадии, выбирают из диапазона от 1 до 10 молей на 1 моль соединения формулы [XIV], и предпочтительно от 2,0 до 5,0 молей.
Растворитель, используемый на этой стадии, может, например, представлять собой простой эфир, такой как диэтиловый эфир, тетрагидрофуран или диоксан, ароматический углеводород, такой как бензол, толуол, ксилол или хлорбензол, галогенированный углеводород, такой как дихлорметан, хлороформ или дихлорэтан, апротонный полярный растворитель, такой как ацетонитрил, N,N-диметилформамид, N,N-диметилацетамид, N-метил-2-пирролидон, диметилсульфоксид или сульфолан, спирт, такой как метанол, этанол или изопропиловый спирт, нитрил, такой как ацетонитрил или пропионитрил, сложный эфир, такой как этилацетат или этилпропионат, алифатический углеводород, такой как пентан, гексан, циклогексан или гептан, пиридин, такой как пиридин или пиколин, или воду, или смесь этих растворителей.
Температура реакции может быть выбрана из диапазона от -30°C до температуры кипения реакционной смеси, и предпочтительно в пределах диапазона от -10°C до 100°C.
Время реакции варьирует в зависимости от температуры реакции, реагирующего субстрата, загрузки реакции и т.д. и составляет обычно от 10 минут до 20 часов.
(Стадия 2-2)
Далее, количество соединения формулы [XV-3] или соединения формулы [XV-4], используемых на этой стадии, находится в пределах диапазона от 1 моль до большого избытка на 1 моль соединения формулы [XIV-1], и предпочтительно от 1,0 до 2,0 молей.
Кислотный катализатор, используемый на этой стадии, может, например, представлять собой сульфоновую кислоту, такую как метансульфоновая кислота или пара-толуолсульфоновая кислота, неорганическую кислоту, такую как соляная кислота или серная кислота, или карбоновую кислоту, такую как уксусная кислота или трифторуксусная кислота.
Количество используемого кислотного катализатора выбирают из диапазона от 0,01 моль до большого избытка на 1 моль соединения формулы [XIV-1], и предпочтительно от 0,05 до 1,0 молей.
Растворитель, используемый на этой стадии, может быть тем же растворителем, как определено выше для стадии 1.
Основание, используемое в этой реакции, может, например, представлять собой неорганическое основание, такое как гидроксид щелочного металла, такой как гидроксид натрия или гидроксид калия, гидроксид щелочноземельного металла, такой как гидроксид кальция или гидроксид магния, карбонат щелочного металла, такой как карбонат натрия или карбонат калия, или бикарбонат щелочного металла, такой как бикарбонат натрия или бикарбонат калия, гидрид металла, такой как гидрид натрия или гидрид калия, спиртовую соль металла, такую как метоксид натрия, этоксид натрия или трет-бутоксид калия, или органическое основание, такое как триэтиламин, N,N-диметиланилин, пиридин, 4-N,N-диметиламинопиридин или 1,8-диазабицикло[5.4.0]-7-ундецен.
Количество используемого основания выбирают из диапазона от 1 моль до большого избытка на 1 моль соединения формулы [XIV-1], и предпочтительно от 1,0 до 1,5 молей.
Температура реакции может быть выбрана из диапазона от -30°C до температуры кипения реакционной смеси, и предпочтительно в пределах диапазона от -10°C до 100°C.
Время реакции варьирует в зависимости от температуры реакции, реагирующего субстрата, загрузки реакции и т.д. и составляет обычно от 10 минут до 20 часов.
<Способ получения 8>

где Y2 представляет собой атом галогена, алкоксигруппу или алкилтио группу, которые могут быть замещены галогеном, и R1', A1, A3, B2, B4, R и n определены выше.
(Стадия 3)
Соединение по настоящему изобретению формулы [I] может быть получено взаимодействием с соединением формулы [XVIII] соединения формулы [XVII-1], полученного из соединения формулы [XVI-1] и хлорангидрида кислоты, ангидрида кислоты или подобных.
Количество соединения формулы [XVII-1] выбирают из диапазона от 1,0 до 5,0 молей на 1 моль соединения формулы [XVIII], и предпочтительно от 1,0 до 1,5 молей.
Растворитель, используемый на этой стадии, может, например, представлять собой простой эфир, такой как диэтиловый эфир, тетрагидрофуран или диоксан, ароматический углеводород, такой как бензол, толуол, ксилол или хлорбензол, апротонный полярный растворитель, такой как ацетонитрил, N,N-диметилформамид, N,N-диметилацетамид, N-метил-2-пирролидон, диметилсульфоксид или сульфолан, спирт, такой как метанол, этанол или изопропиловый спирт, галогенированный углеводород, такой как хлористый метилен, хлороформ или дихлорэтан, алифатический углеводород, такой как пентан, гексан, циклогексан или гептан, кетон, такой как ацетон, метилэтилкетон или циклогексанон, или воду.
Температура реакции может быть выбрана из диапазона от -30°C до температуры кипения реакционной смеси, и предпочтительно в пределах диапазона от -10°C до 100°C.
Время реакции варьирует в зависимости от температуры реакции, реагирующего субстрата, загрузки реакции и т.д. и составляет обычно от 10 минут до 20 часов.
(Стадия 4)
Далее, целевое производное 3-триазолилфенилсульфида формулы [I-3] может быть получено взаимодействием соединения формулы [XVII-2], полученного из соединения формулы [XVI-2] и дисульфида углерода, алкилгалогенида или подобных, с соединением формулы [XVIII].
Количество соединения формулы [XVII-2] выбирают из диапазона от 1,0 до 10 молей на 1 моль соединения формулы [XVIII], и предпочтительно от 1,0 до 1,5 молей.
Растворитель, используемый на этой стадии, может быть тем же растворителем, как определено выше для стадии 3.
Температура реакции может быть выбрана из диапазона от -30°C до температуры кипения реакционной смеси, и предпочтительно в пределах диапазона от -10°C до 100°C.
Время реакции варьирует в зависимости от температуры реакции, реагирующего субстрата, загрузки реакции и т.д. и составляет обычно от 10 минут до 20 часов.
<Способ получения 9>
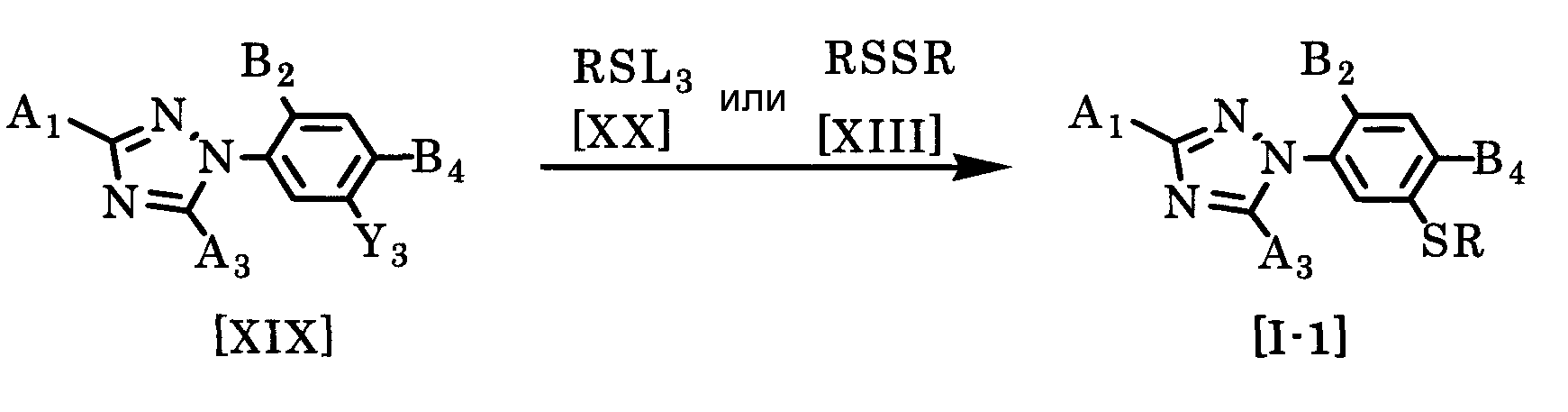
где Y3 представляет собой атом водорода или атом галогена, а L3, A1, A3, B2, B4 и R определены выше.
Соединение по настоящему изобретению формулы [I-1] может быть получено взаимодействием соединения формулы [XIX] с металлом или органическом соединением металла, затем реакцией с соединением формулы [XX] или [XIII].
Количество используемого соединения формулы [XX] или [XIII] выбирают из диапазона от 1 до 5 молей на 1 моль соединения формулы [XIX], и предпочтительно от 1,0 до 2,0 молей.
Растворитель, используемый в этой реакции, может, например, представлять собой простой эфир, такой как диэтиловый эфир, тетрагидрофуран или диоксан, ароматический углеводород, такой как бензол, толуол, ксилол или хлорбензол, алифатический углеводород, такой как пентан, гексан, циклогексан или гептан, или пиридин, такой как пиридин или пиколин, или смесь этих растворителей.
Металл, используемый в этой реакции, может, например, представлять собой щелочной металл, такой как литий, или щелочноземельный металл, такой как магний, и его используемое количество выбирают из диапазона от 1 до 3 молей на 1 моль соединения формулы [XIX], и предпочтительно от 1,0 до 1,1 молей.
Органическое соединение металла, используемое в этой реакции, может, например, представлять собой алкиллитий, такой как н-бутиллитий, и его используемое количество выбирают из диапазона от 1 до 3 молей на 1 моль соединения формулы [XIX], и предпочтительно от 1,0 до 1,1 молей.
Температура реакции может быть выбрана из диапазона от -90°C до температуры кипения реакционной смеси, и предпочтительно в пределах диапазона от -78°C до 70°C.
Время реакции варьирует в зависимости от температуры реакции, реагирующего субстрата, загрузки реакции и т.д. и составляет обычно от 10 минут до 20 часов.
<Способ получения 10>

где A1, A3, В2, B4 и R определены выше.
Соединение по настоящему изобретению формулы [I-4] может быть получено взаимодействием соединения формулы [I-1] с окисляющим реагентом в присутствии или в отсутствие катализатора.
Окисляющий реагент может, например, представлять собой пероксид водорода, мета-хлорпербензойную кислоту, перииодат натрия, OXONE (торговая марка, производимая E.I. du Pont; содержит калий гидропероксосульфат), N-хлорсукцинимид, N-бромсукцинимид, трет-бутилгипохлорит или гипохлорит натрия.
Количество используемого окисляющего реагента выбирают из диапазона от 1 до 6 молей на 1 моль соединения формулы [I-1], и предпочтительно от 1,0 до 1,2 молей.
Катализатор, используемый в этой реакции, может, например, представлять собой вольфрамат натрия.
Количество используемого катализатора выбирают из диапазона от 0 до 1 моль на 1 моль соединения формулы [I-1], и предпочтительно от 0,01 до 0,1 моль.
Растворитель, используемый в этой реакции, может, например, представлять собой простой эфир, такой как диэтиловый эфир, тетрагидрофуран или диоксан, ароматический углеводород, такой как бензол, толуол, ксилол или хлорбензол, апротонный полярный растворитель, такой как ацетонитрил, N,N-диметилформамид, N,N-диметилацетамид, N-метил-2-пирролидон, диметилсульфоксид или сульфолан, спирт, такой как метанол, этанол или изопропиловый спирт, галогенированный углеводород, такой как хлористый метилен, хлороформ или дихлорэтан, алифатический углеводород, такой как пентан, гексан, циклогексан или гептан, кетон, такой как ацетон, метилэтилкетон или циклогексанон, уксусную кислоту, или воду, или смесь этих растворителей.
Температура реакции может быть выбрана из диапазона от -30°C до температуры кипения реакционной смеси, и предпочтительно в пределах диапазона от -10°C до 100°C.
Время реакции варьирует в зависимости от температуры реакции, реагирующего субстрата, загрузки реакции и т.д. и составляет обычно от 10 минут до 20 часов.
<Способ получения 11>
Соединение по настоящему изобретению формулы [I] может быть получено из производного 3-триазолилфенилсульфида путем конвертирования функциональной группы, как правило, известным методом:

где A1, A3, B2, B4, n и R определены выше, и L6 представляет собой атом водорода, атом галогена, метилтио группу, метилсульфинильную группу, метилсульфонильную группу, пара-толуолсульфонильную группу или подобные.
(Стадия A)
Соединение по настоящему изобретению формулы [I] может быть получено взаимодействием соединения по настоящему изобретению формулы [I-3] с электрофильным рeагентом в присутствии или в отсутствие растворителя, в присутствии или в отсутствие основания, в присутствии или в отсутствие кислоты и в присутствии или в отсутствие дегидрагирующего конденсирующего реагента.
Электрофил, используемый на этой стадии, может, например, представлять собой галогенированный алкан, галогенированный алкен, галогенированный алкин, фенилалкилгалогенид, гетероциклилалкилгалогенид, ацилгалогенид, ангидрид кислоты, бензойную кислоту, бензоилгалогенид, гетероциклическую карбоновую кислоту, гетероциклический карбоксигалогенид, алифатический карбоксигалогенид, изоцианат, спирт, арилгалогенид, гетероциклический галогенид, сульфонилгалогенид или сульфоновый ангидрид, или кетон, или тиокетон.
Галогенированный алкан, используемый на этой стадии, может, например, представлять собой метилиодид, этилиодид или пропилиодид.
Галогенированный алкен, используемый на этой стадии, может, например, представлять собой аллилбромид или 1,1,3-трихлорпропен.
Галогенированный алкин, используемый на этой стадии, может, например, представляет собой пропаргилбромид или 4-хлор-2-бутин.
Фенилалкилгалогенид, используемый на этой стадии, может, например, представлять собой бензилбромид, 4-метоксибензилхлорид или 4-хлорбензилбромид.
Гетероциклический алкилгалогенид, используемый на этой стадии, может, например, представлять собой 2-хлор-5-хлорметилпиридин.
Ацилгалогенид, используемый на этой стадии, может, например, представлять собой ацетилхлорид, пропионилхлорид, дифторацетилхлорид, трифторацетилхлорид, метилхлороформиат, этилхлороформиат или N,N-диметилкарбамоилхлорид.
Ангидрид кислоты, используемый на этой стадии, может, например, представлять собой уксусный ангидрид, трифторуксусный ангидрид или хлордифторуксусный ангидрид.
Изоцианат, используемый на этой стадии, может, например, представлять собой метилизоцианат, этилизоцианат или хлорсульфонилизоцианат.
Арилгалогенид, используемый на этой стадии, может, например, представлять собой 3,5-дихлор-4-фторбензотрифторид.
Гетероциклический галогенид, используемый на этой стадии, может, например, представлять собой 2,3-дихлор-5-трифторметилпиридин.
Сульфонилгалогенид, используемый на этой стадии, может, например, представлять собой трифторметансульфонилфторид, трифторметансульфонилхлорид или дифторметансульфонилхлорид.
Сульфоновый ангидрид, используемый на этой стадии, может, например, представлять собой трифторметансульфоновый ангидрид.
Кетон, используемый на этой стадии, может, например, представлять собой ацетон или 4-гидрокси-3-метоксибензальдегид.
Бензоилгалогенид, используемый на этой стадии, может, например, представлять собой бензоилхлорид.
Гетероциклическая карбоновая кислота, используемая на этой стадии, может, например, представлять собой 3-пиридинкарбоновую кислоту или тиофенкарбоновую кислоту.
Гетероциклический карбоксигалогенид, используемый на этой стадии, может, например, представлять собой 3-пиридинкарбонилхлорид или тиофенкарбонилхлорид.
Алифатический карбоксигалогенид, используемый на этой стадии, может, например, представлять собой ацетилхлорид или пропионилхлорид.
Спирт, используемый на этой стадии, может, например, представлять собой метанол, этанол или бензиловый спирт.
Количество используемого электрофила выбирают из диапазона от 1 до 100 молей на 1 моль соединения формулы [I-3], предпочтительно от 1 до 10 молей и более предпочтительно от 1 до 3 молей.
В случае, когда на этой стадии используется основание, используемое основание, может, например, представлять собой неорганическое основание, такое как гидроксид щелочного металла, такой как гидроксид натрия или гидроксид калия, гидроксид щелочноземельного металла, такой как гидроксид кальция или гидроксид магния, карбонат щелочного металла, такой как карбонат натрия или карбонат калия, или бикарбонат щелочного металла, такой как бикарбонат натрия или бикарбонат калия, гидрид металла, такой как гидрид натрия или гидрид калия, спиртовую соль металла, такую как метоксид натрия, этоксид натрия или трет-бутоксид калия, или органическое основание, такое как триэтиламин, N,N-диметиланилин, пиридин, 4-N,N-диметиламинопиридин или 1,8-диазабицикло[5.4.0]-7-ундецен.
В случае, когда используется основание, количество используемого основания выбирают из диапазона от 0,01 до 3 молей на 1 моль соединения формулы [I-3], и предпочтительно от 0,1 до 2 молей, более предпочтительно от 0,1 до 1,2 молей.
В случае, когда на этой стадии применяют кислоту, используемая кислота представляет собой кислоту Льюиса, такую как сульфоновая кислота, такую как метансульфоновая кислота или пара-толуолсульфокислота, неорганическую кислоту, такую как соляная кислота, бромоводородная кислота или серная кислота, или карбоновую кислоту, такую как уксусная кислота или трифторуксусная кислота.
В случае, когда используется кислота, количество используемой кислоты выбирают из диапазона от 0,001 до 5 молей на 1 моль соединения формулы [I-3], и предпочтительно от 0,01 до 2 молей, более предпочтительно от 0,03 до 1,0 молей.
Растворитель, используемый на этой стадии, может, например, представлять собой простой эфир, такой как диэтиловый эфир, тетрагидрофуран или диоксан, ароматический углеводород, такой как бензол, толуол, ксилол или хлорбензол, апротонный полярный растворитель, такой как ацетонитрил, N,N-диметилформамид, N,N-диметилацетамид, N-метил-2-пирролидон, диметилсульфоксид или сульфолан, спирт, такой как метанол, этанол или изопропиловый спирт, галогенированный углеводород, такой как хлористый метилен, хлороформ или дихлорэтан, алифатический углеводород, такой как пентан, гексан, циклогексан или гептан, или кетон, такой как ацетон, метилэтилкетон или циклогексанон, или смесь этих растворителей.
В случае, когда на этой стадии применяют дегидрагирующий конденсирующий реагент, используемый дегидрагирующий конденсирующий реагент может представлять собой карбодиимид, такой как дициклогексилкарбодиимид.
В случае, когда применяют дегидрагирующий конденсирующий реагент, количество используемого дегидрагирующего конденсирующего реагента выбирают из диапазона от 1 до 3 молей на 1 моль соединения формулы [I-3], и предпочтительно от 1,0 до 1,2 молей.
Температура реакции может быть выбрана из диапазона от -20°C до температуры кипения реакционной смеси, и предпочтительно в пределах диапазона от 0°C до 80°C.
Время реакции варьирует в зависимости от температуры реакции, реагирующего субстрата, загрузки реакции и т.д. и составляет обычно от 15 минут до 24 часов.
(Стадия B)
Соединение по настоящему изобретению формулы [I] может быть получено взаимодействием соединения формулы [I-5] с соединением формулы [I-7] в присутствии или в отсутствие основания в присутствии растворителя.
В случае, когда в этом способе используется основание, основание, используемое в этой реакции, может, например, представлять собой неорганическое основание, такое как гидроксид щелочного металла, такой как гидроксид натрия или гидроксид калия, гидроксид щелочноземельного металла, такой как гидроксид кальция или гидроксид магния, карбонат щелочного металла, такой как карбонат натрия или карбонат калия, или бикарбонат щелочного металла, такой как бикарбонат натрия или бикарбонат калия, гидрид металла, такой как гидрид натрия или гидрид калия, спиртовую соль металла, такую как метоксид натрия, этоксид натрия или трет-бутоксид калия, или органическое основание, такое как триэтиламин, N,N-диметиланилин, пиридин, 4-N,N-диметиламинопиридин или 1,8-диазабицикло[5.4.0]-7-ундецен.
В случае, когда используется основание, количество используемого основания выбирают из диапазона от 1 до 10 молей на 1 моль соединения формулы [I-5], и предпочтительно от 1 до 3 молей, более предпочтительно от 1,0 до 1,2 молей.
Растворитель, используемый на этой стадии, может, например, представлять собой простой эфир, такой как диэтиловый эфир, тетрагидрофуран или диоксан, ароматический углеводород, такой как бензол, толуол, ксилол или хлорбензол, апротонный полярный растворитель, такой как ацетонитрил, N,N-диметилформамид, N,N-диметилацетамид, N-метил-2-пирролидон, диметилсульфоксид или сульфолан, спирт, такой как метанол, этанол или изопропиловый спирт, галогенированный углеводород, такой как хлористый метилен, хлороформ или дихлорэтан, алифатический углеводород, такой как пентан, гексан, циклогексан или гептан, или кетон, такой как ацетон, метилэтилкетон или циклогексанон, или воду, и смесь этих растворителей также может применяться.
Температура реакции может быть выбрана из диапазона от -20°C до температуры кипения реакционной смеси, и предпочтительно в пределах диапазона от -10°C до 150°C.
Время реакции варьирует в зависимости от температуры реакции, реагирующего субстрата, загрузки реакции и т.д. и составляет обычно от 15 минут до 12 часов.
(Стадия C)
Соединение по настоящему изобретению, представленное формулой [I], может быть получено взаимодействием соединения формулы [I-6] с амином, карбоновой кислотой или спиртом в присутствии или в отсутствие растворителя.
Амин, используемый на этой стадии, может, например, представлять собой метиламин, этиламин, диметиламин, пропиламин, изопропиламин, гидразин или метилгидразин.
Карбоновая кислота, используемая на этой стадии, может, например, представлять собой уксусную кислоту, пропионовую кислоту, метоксиуксусную кислоту или бензойную кислоту.
Спирт, используемый на этой стадии, может, например, представлять собой метанол, этанол, пропанол, аллиловый спирт, пропаргиловый спирт или циклопропанол.
Амин, карбоновую кислоту или спирт применяли в количестве от 1 моль до 100 молей, предпочтительно от 1 моль до 30 молей, более предпочтительно от 1 моль до 3 молей амина, карбоновой кислоты или спирта на 1 моль соединения, представленного формулой [I-6].
Растворитель, используемый в этой реакции может, например, представлять собой простой эфир, такой как диэтиловый эфир, тетрагидрофуран или диоксан, ароматический углеводород, такой как бензол, толуол, ксилол или хлорбензол, апротонный полярный растворитель, такой как ацетонитрил, N,N-диметилформамид, N,N-диметилацетамид, N-метил-2-пирролидон, диметилсульфоксид или сульфолан, спирт, такой как метанол, этанол или изопропиловый спирт, галогенированный углеводород, такой как хлористый метилен, хлороформ или дихлорэтан, алифатический углеводород, такой как пентан, гексан, циклогексан или гептан, или кетон, такой как ацетон, метилэтилкетон или циклогексанон, или смесь этих растворителей.
Температура реакции может быть выбрана из диапазона от -20°C до температуры кипения реакционной смеси, и предпочтительно в пределах диапазона от -10°C до 150°C.
Время реакции варьирует в зависимости от температуры реакции, реагирующего субстрата, загрузки реакции и т.д. и составляет обычно от 30 минут до 24 часов.
Далее будет описан детально синтез промежуточных соединений при получении соединений по настоящему изобретению.
<Способ 1 получения промежуточного соединения >
Синтез реакционных промежуточных соединений [II] и [IV].
Соединения формулы [II] и [IV] могут быть синтезированы, как описано ниже. Нет необходимости подчеркивать, что они взаимопревращаемы через реакцию окисления-восстановления. В особенности, соединение формулы [II] может быть в некоторых случаях легко окислено атмосферным кислородом в соединение формулы [IV]:

где R2' представляет собой метильную группу или трифторметильную группу, и Y2, A1, A3, B2 и B4 определены выше.
(Стадия 5)
Таким образом, целевое соединение, представленное формулой [II] или [IV], может быть получено, как описано ниже. Соединение формулы [XXI] окисляют окисляющим реагентом в метилсульфоксид, затем реакцией Пуммерера с уксусным ангидридом или трифторуксусным ангидридом переводят в ацилоксиметилсульфид, представленный формулой [XXII], и затем конечное соединение гидролизуют.
Окисляющий реагент может, например, представлять собой пероксид водорода, мета-хлорпербензойную кислоту, перииодат натрия, OXONE (торговая марка, производимая E.I. du Pont; содержит гидропероксосульфат калия), N-хлорсукцинимид, N-бромсукцинимид, трет-бутилгипохлорит или гипохлорит натрия.
Количество используемого окисляющего реагента выбирают из диапазона от 1 до 3 молей на 1 моль соединения формулы [XXI], и предпочтительно от 1,0 до 1,2 молей.
Используемые уксусный ангидрид или трифторуксусный ангидрид могут применяться как растворитель для реакции, в количестве от 1 моль или более, на 1 моль соединения формулы [XXI], и их количество предпочтительно составляет от 1,0 до 3,0 молей.
Температура реакции каждой реакции может быть выбрана из диапазона от -10°C до температуры кипения реакционной смеси, и предпочтительно в пределах диапазона от 0°C до 50°C.
Время реакции варьирует в зависимости от температуры реакции, реагирующего субстрата, загрузки реакции и т.д. и составляет обычно от 5 минут до 12 часов.
(Стадия 6)
Соединение, представленное формулой [II], может быть получено путем реакции соединения формулы [XIX] с металлом или органометаллическим соединением в растворителе, а затем реагирования с элементарной серой.
Растворитель, используемый на этой стадии, может, например, представлять собой простой эфир, такой как диэтиловый эфир, тетрагидрофуран или диоксан, ароматический углеводород, такой как бензол, толуол, ксилол или хлорбензол, алифатический углеводород, такой как пентан, гексан, циклогексан или гептан, или пиридин, такой как пиридин или пиколин, или смесь этих растворителей.
Металл, используемый на этой стадии, может, например, представлять собой литий или магний.
Количество используемого металла выбирают из диапазона от 1 до 3 молей на 1 моль соединения формулы [XIX], и предпочтительно от 1,0 до 1,2 молей.
Органометаллическое соединение, используемое на этой стадии, может, например, представлять собой н-бутиллитий.
Количество используемого органометаллического соединения может быть выбрано из диапазона от 1 до 3 молей на 1 моль соединения формулы [XIX], и предпочтительно от 1,0 до 1,2 молей.
Количество используемой серы выбирают из диапазона от 1 до 5 молей на 1 моль соединения формулы [XIX], и предпочтительно от 1,0 до 2,0 молей.
Температура реакции каждой реакции может быть выбрана из диапазона от -60°C до температуры кипения реакционной смеси, и предпочтительно в пределах диапазона от -60°C до комнатной температуры.
Время реакции варьирует в зависимости от температуры реакции, реагирующего субстрата, загрузки реакции и т.д. и составляет обычно от 30 минут до 12 часов.
(Стадия 7)
Соединение, представленное формулой [II], может быть получено, как описано ниже. Соединение, представленное формулой [XI], конвертируют в диазониевую соль тем же способом, как описано выше в способе получения 6. Затем диазониевую соль вводят в реакцию с ксантогенатом или тиоцианатом, затем подвергают щелочному гидролизу.
Количество используемых ксантогената или тиоцианата выбирают из диапазона от 1 до 3 молей на 1 моль соединения формулы [XI], и предпочтительно от 1,0 до 1,5 молей.
Температура реакции каждой реакции может быть выбрана из диапазона от -70°C до температуры кипения реакционной смеси, и предпочтительно от -20°C до 100°C.
Время реакции варьирует в зависимости от температуры реакции, реагирующего субстрата, загрузки реакции и т.д. и составляет обычно от 10 минут до 20 часов.
(Стадия 8)
Синтетическое промежуточное соединение, представленное формулой [II], может быть получено взаимодействием соединения формулы [XXIII] с хлорсульфоновой кислотой с образованием сульфонилхлорида формулы [XXIV], и восстановления его алюмогидридом лития, цинком с кислотой, оловом с кислотой или красным фосфором с иодом.
Количество хлорсульфоновой кислоты, используемой на этой стадии, выбирают из диапазона от 2 до 5 молей на 1 моль соединения формулы [XXIII], и предпочтительно от 2,2 до 3,0 молей.
Кислота может, например, представлять собой соляную кислоту или серную кислоту.
Количество используемой хлорсульфоновой кислоты выбирают из диапазона от 2 до 10 молей на 1 моль соединения формулы [XXIII], и предпочтительно от 2,2 до 3,5 молей.
Количество алюмогидрида лития, цинка и кислоты, олова и кислоты, или красного фосфора и иода, выбирают из диапазона от 1 до 5 молей на 1 моль соединения формулы [XXIII], и предпочтительно от 1,5 до 2,0 молей.
(Стадия 9)
Соединение, представленное формулой [IV], может быть получено взаимодействием соединения формулы [XXIII] с дихлоридом дисеры в присутствии или в отсутствие катализатора. Далее, соединение, представленное формулой [II], может быть получено путем восстановления традиционным способом соединения, представленного формулой [IV].
Количество используемого дихлорида дисеры выбирают из диапазона от 1 до 5 молей на 1 моль соединения формулы [XXIII], и предпочтительно от 1,1 до 1,5 молей.
Катализатор, используемый на этой стадии, может, например, представлять собой кислотный катализатор Льюиса, такой как хлорид алюминия, хлорид олова(II) или хлорид олова(IV).
Количество используемого катализатора выбирают из диапазона от 1 до 5 молей на 1 моль соединения формулы [XXIII], и предпочтительно от 1,1 до 2,0 молей.
Растворитель, используемый на этой стадии, может, например, представлять собой галогенированный углеводород, такой как хлористый метилен, хлороформ или дихлорэтан, или ароматический углеводород, такой как хлорбензол или дихлорбензол.
Температура реакции может быть выбрана из диапазона от -30°C до температуры кипения реакции, и предпочтительно в пределах диапазона от -10°C до 100°C.
Время реакции варьирует в зависимости от температуры реакции, реагирующего субстрата и загрузки реакции и составляет обычно от 1 до 20 часов.
<Способ 2 получения промежуточного соединения >
Далее, синтетическое промежуточное соединение формулы [II-1] может быть получено путем реакции замещения из соединения формулы [IX], где B5 представляет собой электроноакцепторную группу:

где L4, A1, A3, B2 и B5 определены выше.
Таким образом, целевое производное 3-триазолилфенилтиола, представленное формулой [II-1], может быть получено взаимодействием соединения формулы [IX] с соединением формулы [XXV] в растворителе в присутствии основания, с последующей нейтрализацией действием минеральной кислоты или подобным.
Количество используемого соединения формулы [XXV] выбирают из диапазона от 1 до 3 молей на 1 моль соединения формулы [IX], и предпочтительно от 1,0 до 1,5 молей.
Растворитель, используемый на этой стадии, может, например, представлять собой простой эфир, такой как диэтиловый эфир, тетрагидрофуран или диоксан, ароматический углеводород, такой как бензол, толуол, ксилол или хлорбензол, апротонный полярный растворитель, такой как N,N-диметилформамид, N,N-диметилацетамид, N-метил-2-пирролидон, диметилсульфоксид или сульфолан, спирт, такой как метанол, этанол или изопропиловый спирт, галогенированный углеводород, такой как хлористый метилен, хлороформ или дихлорэтан, алифатический углеводород, такой как пентан, гексан, циклогексан или гептан, кетон, такой как ацетон, метилэтилкетон или циклогексанон, или воду.
Основание, используемое на этой стадии, может, например, представлять собой неорганическое основание, такое как гидроксид щелочного металла, такой как гидроксид натрия или гидроксид калия, гидроксид щелочноземельного металла, такой как гидроксид кальция или гидроксид магния, карбонат щелочного металла, такой как карбонат натрия или карбонат калия, или бикарбонат щелочного металла, такой как бикарбонат натрия или бикарбонат калия, гидрид металла, такой как гидрид натрия или гидрид калия, спиртовую соль металла, такую как метоксид натрия, этоксид натрия или трет-бутоксид калия, или органическое основание, такое как триэтиламин, N,N-диметиланилин, пиридин, 4-N,N-диметиламинопиридин или 1,8-диазабицикло[5.4.0]-7-ундецен.
Количество используемого основания выбирают из диапазона от 1 до 5 молей на 1 моль соединения формулы [IX], и предпочтительно от 1,0 до 1,2 молей.
Минеральная кислота может, например, представлять собой соляную кислоту или серную кислоту.
Количество используемой минеральной кислоты выбирают из диапазона от 1 до 5 молей на 1 моль соединения формулы [IX], и предпочтительно от 1,0 до 2,0 молей.
Температура реакции может быть выбрана из диапазона от -30°C до температуры кипения реакционной смеси, и предпочтительно в пределах диапазона от -20°C до 100°C. Время реакции варьирует в зависимости от температуры реакции, реагирующего субстрата, загрузки реакции и т.д. и составляет обычно от 10 минут до 20 часов.
<Способ 3 получения промежуточного соединения >
Синтез промежуточного соединения [VI]

где A1, A3, R', Y1, L3 и L5 определены выше.
(Стадия 10)
Синтетическое промежуточное соединение, представленное формулой [VI], может быть получено тем же способом, как в способе получения 8, путем конвертирования соединения формулы [XVI] в соединение формулы [XVII], и реакции последнего соединения с гидразин гидратом формулы [XXVI].
Количество используемого гидразин гидрата [XXVI] выбирают из диапазона от 1 до 5 молей на 1 моль соединения формулы [XVII], и предпочтительно от 1,0 до 2,0 молей.
(Стадия 11)
Далее, синтетическое промежуточное соединение, представленное формулой [VI], может быть получено тем же способом, как в способе получения 7, взаимодействием соединения формулы [XXVII] с соединением формулы [XV-1] или с соединением формулы [XV-2].
Количество используемого соединения, представленного формулой [XV-1] или [XV-2], составляло от 1 моль до большого избытка на 1 моль соединения формулы [XXVII], и предпочтительно от 1,0 до 2,0 молей.
Температура реакции может быть выбрана из диапазона от -70°C до температуры кипения реакционной смеси, и предпочтительно в пределах диапазона от -20°C до 100°C.
Время реакции варьирует в зависимости от температуры реакции, реагирующего субстрата, загрузки реакции и т.д. и составляет обычно от 10 минут до 20 часов.
(Стадия 12)
Синтетическое промежуточное соединение, представленное формулой [VI], может быть получено взаимодействием соединения, представленного формулой [XXVII], с водным аммиаком, что приводит к амидразону, представленному формулой [XXVII-2], и введения в реакцию этого продукта реакции с соединением, представленным формулой [XV-3] или [XV-4].
Количество используемого водного аммиака выбирают из диапазона от 1 до 10 молей на 1 моль соединения представленное формулой [XXVII], и предпочтительно от 2,0 до 5,0 молей.
Количество соединения, представленное формулой [XV-3] или [XV-4], составляет от 1 моль до большого избытка на 1 моль соединения, представленного формулой [XXVII-2], и предпочтительно от 1,0 до 2,0 молей.
Температура реакции может быть выбрана из диапазона от -70°C до температуры кипения реакционной смеси, и предпочтительно в пределах диапазона от -20°C до 100°C. Время реакции варьирует в зависимости от температуры реакции, реагирующего субстрата, загрузки реакции, и т.д. и составляет обычно от 10 минут до 20 часов.
<Способ 4 получения промежуточного соединения >
Синтез промежуточного соединения [XIV]

где L3, L5, A1, B2, B4, R и n определены выше.
(Стадия 13)
Целевое соединение, представленное формулой [XIV], может быть получено взаимодействием производного фенилгидразина, представленного формулой [XVIII], с соединением, представленным формулой [XXVIII], в растворителе, в присутствии основания для реакции ацилирования, что приводит к соединению, представленному формулой [XXIX], с последующей обработкой соединения, представленного формулой [XXIX], галогенирующим агентом.
Количество используемого соединения формулы [XXVIII] выбирают из диапазона от 1 до 5 молей на 1 моль соединения формулы [XVIII], и предпочтительно от 1,0 до 1,1 молей.
Растворитель, используемый на этой стадии, может, например, представлять собой простой эфир, такой как диэтиловый эфир, тетрагидрофуран или диоксан, ароматический углеводород, такой как бензол, толуол, ксилол или хлорбензол, галогенированный углеводород, такой как дихлорметан, хлороформ или дихлорэтан, апротонный полярный растворитель, такой как N,N-диметилформамид, N,N-диметилацетамид, N-метил-2-пирролидон, диметилсульфоксид или сульфолан, спирт, такой как метанол, этанол или изопропиловый спирт, нитрил, такой как ацетонитрил или пропионитрил, сложный эфир, такой как этилацетат или этилпропионат, алифатический углеводород, такой как пентан, гексан, циклогексан или гептан, пиридин, такой как пиридин или пиколин, или воду, или смесь этих растворителей.
Основание, используемое на этой стадии, может, например, представлять собой неорганическое основание, такое как гидроксид щелочного металла, такой как гидроксид натрия или гидроксид калия, гидроксид щелочноземельного металла, такой как гидроксид кальция или гидроксид магния, карбонат щелочного металла, такой как карбонат натрия или карбонат калия, или бикарбонат щелочного металла, такой как бикарбонат натрия или бикарбонат калия, гидрид металла, такой как гидрид натрия или гидрид калия, спиртовую соль металла, такую как метоксид натрия, этоксид натрия или трет-бутоксид калия, или органическое основание, такое как триэтиламин, N,N-диметиланилин, пиридин, 4-N,N-диметиламинопиридин или 1,8-диазабицикло[5.4.0]-7-ундецен.
Количество используемого основания составляет от 1 моль до большого избытка на 1 моль соединения формулы [XVIII], и предпочтительно от 1,0 до 1,2 молей.
Галогенирующий агент может, например, представлять собой трихлорид фосфора, трибромид фосфора, тионилхлорид, оксохлорид фосфора, пентахлорид фосфора, трифенилфосфин/четыреххлористый углерод или трифенилфосфин/черырехбромистый углерод.
Количество используемого галогенирующего агента составляло от 1 моль до большого избытка на 1 моль соединения формулы [XXIX], и предпочтительно от 1,0 до 1,5 молей.
Температура реакции может быть выбрана из диапазона от -70°C до температуры кипения реакционной смеси, и предпочтительно в пределах диапазона от -20°C до 150°C.
Время реакции варьирует в зависимости от температуры реакции, реагирующего субстрата, загрузки реакции и т.д. и составляет обычно от 10 минут до 20 часов.
(Стадия 14)
Целевое соединение, представленное формулой [XIV], может быть иначе получено взаимодействием производного фенилгидразина, представленного формулой [XVIII], с соединением альдегида, представленным формулой [XXX], в растворителе в присутствии или в отсутствие кислотного катализатора, что приводит к производному фенилгидразона, представленному формулой [XXXI], с последующей обработкой его галогенирующим агентом.
Количество используемого соединения формулы [XXX] выбирают из диапазона от 1 до 5 молей на 1 моль соединения формулы [XVIII], и предпочтительно от 1,0 до 1,2 молей.
Растворитель, используемый на этой стадии, не ограничен теми, что не ингибируют реакцию, и он может, например, представлять собой ароматический углеводород, такой как бензол, толуол или ксилол, простой эфир, такой как диэтиловый эфир, тетрагидрофуран, 1,2-диметоксиэтан или диоксан, кетон, такой как ацетон или метилэтилкетон, нитрил, такой как ацетонитрил или пропионитрил, апротонный полярный растворитель, такой как диметилсульфоксид, N,N-диметилформамид или N,N-диметилацетамид, алифатический углеводород, такой как пентан, гексан, циклогексан или гептан, или пиридин, такой как пиридин или пиколин, или смесь этих растворителей.
Кислотный катализатор, используемый на этой стадии, может, например, представлять собой кислоту Льюиса, такую как сульфоновая кислота, такую как пара-толуолсульфокислота, или тетрахлорид титана.
В случае, когда применяли кислотный катализатор, его используемое количество выбирают из диапазона от 1 до 5 молей на 1 моль соединения формулы [XVIII], и предпочтительно от 1,0 до 1,2 молей.
Галогенирующий агент, используемый на этой стадии, может, например, представлять собой хлор, N-хлорсукцинимид, N-бромсукцинимид или трет-бутилгипохлорит.
Количество используемого галогенирующего агента выбирают из диапазона от 1 до 5 молей на 1 моль соединения формулы [XXXI], и предпочтительно от 1,0 до 1,1 молей.
Температура реакции может быть выбрана из диапазона от -70°C до температуры кипения реакционной смеси, и предпочтительно в пределах диапазона от -20°C до 150°C.
Время реакции варьирует в зависимости от температуры реакции, реагирующего субстрата, загрузки реакции и т.д. и обычно составляет от 10 минут до 20 часов.
Фенилгидразин формулы [XVIII] может быть синтезирован из соответствующего анилина по традиционному способу, как впервые описано в Comprehensive Organic Functional Group Transformations, vol. 2, p. 769.

где B2, B4 и R определены выше, а Ac представляет собой ацетильную группу.
3-Тиопроизводное анилина, представленное формулой [XXXVI], может быть получено путем конвертирования ацетанилида, представленного формулой [XXXII], в дисульфид, представленный формулой [XXXIV], или тиол, представленный формулой [XXXV], тем же способом, как и в способе 1 получения промежуточного соединения, с последующей обработкой, как впервые описано в вышеупомянутом способе получения 1 или 2.
Фенилгидразин, представленный формулой [XVIII-1], может быть получен путем реакции соединения, представленного формулой [XXXVI], с нитритом в присутствии минеральной кислоты, что приводит к образованию соли диазония, и восстановлении ее цинковым порошком, сульфитом, хлоридом олова или подобными. Минеральная кислота может, например, представлять собой соляную кислоту или серную кислоту.
Количество используемой минеральной кислоты выбирают из диапазона от 2 до 10 молей на 1 моль соединения [XXXVI], и предпочтительно от 3 до 5 молей. Количество используемого нитрита выбирают из диапазона от 1,0 до 5,0 молей на 1 моль соединения [XXXVI], и предпочтительно от 1,0 до 1,2 молей.
Температура реакции каждой реакции может быть выбрана из диапазона от -20°C до 50°C, и предпочтительно от -5°C до 20°C.
Время реакции варьирует в зависимости от температуры реакции, реагирующего субстрата, загрузки реакции и т.д. и составляет обычно от 30 минут до 5 часов.
Соединение формулы [I-5] может быть получено следующим способом:

где A1, A3, B2, B4, n и R определены выше, L7представляет собой атом галогена, а W представляет собой метилтио группу или пара-толилтио группу.
Соединение формулы [I-5a] может быть получено путем диазотирования соединения формулы [I-3] традиционным способом, с последующей реакцией с хлоридом меди(I) или бромидом меди(I).
Количество используемых хлорида меди(I) или бромида меди(I) составляло от 1 до 5 молей на 1 моль соединения формулы [I-3], предпочтительно от 1 до 2 молей.
Используемый растворитель может, например, представлять собой карбоновую кислоту, такую как уксусная кислота; минеральную кислоту, такую как соляная кислота, бромоводородная кислота или серная кислота; или воду, или смесь этих растворителей.
Температура реакции может быть выбрана из диапазона от -70°C до температуры кипения реакционной смеси, и предпочтительно в пределах диапазона от -20°C до 100°C.
Время реакции варьирует в зависимости от температуры реакции, реагирующего субстрата, загрузки реакции и т.д. и составляет обычно от 10 минут до 20 часов.
Соединение формулы [I-5a] может также быть получено по реакции при одновременном присутствии эфира нитрита, такого как трет-бутилнитрит или изоамилнитрит, с хлоридом меди(II) или бромидом меди(II) в растворителе. Количество используемого эфира нитрита составляло от 1 до 5 молей на 1 моль соединения формулы [I-3], предпочтительно от 1 до 2 молей.
Количество используемых хлорида меди(II) или бромида меди(II) составляло от 1 до 5 молей на 1 моль соединения формулы [I-3], предпочтительно от 1 до 2 молей.
Количество используемых хлорида меди(II) или бромида меди(II) составляло от 1 до 5 молей на 1 моль соединения формулы [I-3], предпочтительно от 1 до 2 молей.
Используемый растворитель может, например, представлять собой простой эфир, такой как диэтиловый эфир, тетрагидрофуран или диоксан, нитрил, такой как ацетонитрил, или апротонный полярный растворитель, такой как N,N-диметилформамид, N,N-диметилацетамид, N-метил-2-пирролидон, диметилсульфоксид или сульфолан, или смесь этих растворителей.
Температура реакции может быть выбрана из диапазона от -70°C до температуры кипения реакционной смеси, и предпочтительно в пределах диапазона от -20°C до 100°C. Время реакции варьирует в зависимости от температуры реакции, реагирующего субстрата, загрузки реакции и т.д. и составляет обычно от 10 минут до 20 часов.
Соединение формулы [I-5b] может быть получено взаимодействием в растворителе соединения формулы [I-5a] с метилмеркаптаном или 4-метилбензолтиолом в присутствии основания. Основание, используемое в этой реакции, может, например, представлять собой неорганическое основание, такое как гидроксид щелочного металла, такой как гидроксид натрия или гидроксид калия, гидроксид щелочноземельного металла, такой как гидроксид кальция или гидроксид магния, карбонат щелочного металла, такой как карбонат натрия или карбонат калия, или бикарбонат щелочного металла, такой как бикарбонат натрия или бикарбонат калия, гидрид металла, такой как гидрид натрия или гидрид калия, спиртовую соль металла, такую как метоксид натрия, этоксид натрия или трет-бутоксид калия, или органическое основание, такое как триэтиламин, N,N-диметиланилин, пиридин, 4-N,N-диметиламинопиридин или 1,8-диазабицикло[5.4.0]-7-ундецен.
Растворитель, используемый на этой стадии, может, например, представлять собой простой эфир, такой как диэтиловый эфир, тетрагидрофуран или диоксан, ароматический углеводород, такой как бензол, толуол, ксилол или хлорбензол, апротонный полярный растворитель, такой как N,N-диметилформамид, N,N-диметилацетамид, N-метил-2-пирролидон, диметилсульфоксид или сульфолан, спирт, такой как метанол, этанол или изопропиловый спирт, галогенированный углеводород, такой как хлористый метилен, хлороформ или дихлорэтан, алифатический углеводород, такой как пентан, гексан, циклогексан или гептан, кетон, такой как ацетон, метилэтилкетон или циклогексанон, или воду.
Соединения формулы [I-5c] или [I-5d] могут быть получены взаимодействием соединения формулы [I-5b] с окисляющим реагентом, таким как пероксид водорода, мета-хлорпербензойная кислота, перииодат натрия, OXONE (торговая марка, производимая E.I. du Pont, содержит гидропероксосульфат калия), N-хлорсукцинимид, N-бромсукцинимид, трет-бутилгипохлорит или гипохлорит натрия.
Количество используемого окисляющего реагента, в случае получения соединения [I-5c], составляет от 0,5 до 1,5 молей, предпочтительно от 0,8 до 1,2 молей на 1 моль соединения формулы [I-5b]. Далее, в случае получения соединения [I-5d], оно составляет от 2 до 10 молей, предпочтительно от 2 молей до 4 молей, на 1 моль соединения формулы [I-5b].
Используемый растворитель, температура реакции и время реакции определены выше для способа получения 10.
Далее, соединение формулы [I-5d] может также быть получено взаимодействием соединения, представленного формулой [I-5a], с солью метансульфиновой кислоты или солью пара-толуолсульфиновой кислоты.
Используемое количество соли метансульфиновой кислоты или соли пара-толуолсульфиновой кислоты составляло от 1 до 10 молей, предпочтительно от 1 до 5 молей, более предпочтительно от 1 до 3 молей на 1 моль соединения формулы [I-5a].
Используемый растворитель может, например, представлять собой нитрил, такой как ацетонитрил, или апротонный полярный растворитель, такой как диметилсульфоксид, N,N-диметилформамид или N,N-диметилацетамид.
Температура реакции может быть выбрана из диапазона от -0°C до температуры кипения реакционной смеси, и предпочтительно в пределах диапазона от 10°C до 100°C.
Время реакции варьирует в зависимости от температуры реакции, реагирующего субстрата, загрузки реакции и т.д. и составляет обычно от 1 до 24 часов.
Соединение формулы [I-5e] может быть получено взаимодействием соединения формулы [I-3] с эфиром нитрита, таким как трет-бутилнитрит или изоамилнитрит.
Количество используемого эфира нитрита, составляло от 1 до 5 молей на 1 моль соединения формулы [I-3], и предпочтительно от 1 до 2 молей.
Используемый растворитель может, например, представлять собой простой эфир, такой как диэтиловый эфир, тетрагидрофуран или диоксан, нитрил, такой как ацетонитрил, или апротонный полярный растворитель, такой как N,N-диметилформамид, N,N-диметилацетамид, N-метил-2-пирролидон, диметилсульфоксид или сульфолан, или смесь этих растворителей.
Температура реакции может быть выбрана из диапазона от -70°C до температуры кипения реакционной смеси, и предпочтительно в пределах диапазона от -20°C до 100°C. Время реакции варьирует в зависимости от температуры реакции, реагирующего субстрата, загрузки реакции и т.д. и составляет обычно от 10 минут до 20 часов.

где A1, A3, B2, B4, n и R определены выше.
Соединение, представленное формулой [I-6], может быть получено известным способом, взаимодействием соединения, представленного формулой [I-3], с оксалилхлоридом или фосгеном, в присутствии растворителя.
Количество используемых оксалилхлорида или фосгена, соответственно, выбирают из диапазона от 1 моль до того же количества, как количество растворителя для реакции на 1 моль соединения, представленного формулой [I-3], и предпочтительно от 1,1 до 3 молей.
Используемый растворитель может, например, представлять собой простой эфир, такой как диэтиловый эфир, тетрагидрофуран или диоксан, ароматический углеводород, такой как бензол, толуол, ксилол или хлорбензол, галогенированный углеводород, такой как дихлорметан, хлороформ или дихлорэтан, алифатический углеводород, такой как пентан, гексан, циклогексан или гептан, или смесь этих растворителей.
Когда соединение по настоящему изобретению применяют в качестве активного компонента пестицида, оно может применяться само по себе. Однако оно может быть рецептурировано в различных рецептурах, таких как эмульгируемый концентрат, суспензия, пудра, гранулы, таблетки, смачиваемый порошок, водорастворимый концентрат, раствор, текучая суспензия, вододиспергируемые гранулы, аэрозоль, паста, масляная рецептура, концентрированная эмульсия в воде и дымообразующий агент в комбинации с различными носителями, сурфактантами и другими вспомогательными средствами, которые обычно применяются для рецептурирования в сельскохозяйственных вспомогательных веществах. Они смешиваются обычно в таких соотношениях, что активный компонент составляет от 0,1 до 90 мас.% и сельскохозяйственные вспомогательные вещества составляют от 10 до 99,9 мас.%.
Носители, используемые для такой рецептуры, могут быть классифицированы на твердые носители и жидкие носители. Твердые носители включают в себя, например, животные и растительные порошки, такие как крахмал, активированный углерод, порошок соевых бобов, мука пшеницы, древесная мука, рыбная мука и порошковое молоко, и минеральные порошки, такие как тальк, каолин, бентонит, карбонат кальция, цеолит, диатомит, белый углерод, глина, окись алюминия, сульфат аммония и мочевина. Жидкие носители включают в себя, например, воду; спирты, такие как изопропиловый спирт и этиленгликоль; кетоны, такие как циклогексанон и метилэтилкетон; простые эфиры, такие как диоксан и тетрагидрофуран, алифатические углеводороды, такие как керосин и дизельное топливо; ароматические углеводороды, такие как ксилол, триметилбензол, тетраметилбензол, метилнафталин и растворитель лигроин; галогенированные углеводороды, такие как хлорбензол; амиды кислот, такие как диметилацетамид; сложные эфиры, такие как сложные эфиры глицерина и жирных кислот; нитрилы, такие как ацетонитрил; и серу-содержащие соединения, такие как диметилсульфоксид.
Поверхностно-активные вещества включают в себя, например, металлические соли алкилбензолсульфоновых кислот, металлические соли динафтилметандисульфоновых кислот, соли алкилсульфатов, алкиларилсульфонатов, сульфонатов лигнина, полиоксиэтиленгликолевых эфиров, полиоксиэтиленовых алкиларильных эфиров, и моноалкилатов полиоксиэтиленсорбита.
Другие вспомогательные вещества включают в себя, например, связующие агенты и загустители, такие как карбоксиметилцеллюлоза, гуммиарабик, аргинат натрия, гуаровую смолу, трагакантовую камедь, и поливиниловый спирт, пеноподавляющие агенты, такие как металлическое мыло, улучшители физических свойств, такие как жирные кислоты, алкилфосфатные соли, силикон, парафин и окрашивающие агенты.
Когда эти рецептуры применяются практически, они могут быть применены непосредственно или после разбавления с разбавителем, таким как вода, до предварительно определенной концентрации. Различные рецептуры, содержащие соединения по настоящему изобретению, с разбавлением или без, могут применяться традиционными способами, т.е. способами нанесения (такими как распыление, затуманивание, атомизация, образование дыма, гранульное нанесение, нанесение в воду на рисовом поле и предпосевное нанесение), обработкой грунта (такой как смешение или орошение), поверхностным нанесением (таким как окрашивание, припыливание и покрытие), маканием, отравленными приманками или дымообразованием. Далее, вышеописанные активные компоненты могут быть включены в питание крупного рогатого скота, для предотвращения инвазии или роста паразитов, в особенности паразитных насекомых, после того, как они попадают в экскременты. Иначе, они могут также применяться в малом объеме при высокой концентрации, когда активный компонент может содержаться в концентрации до 100%. Если необходимо, соответственно выбирается соотношение активного компонента, и оно составляет по существу от 0,1 до 20% (по массе) в случае пудры или гранул, и от 1 до 80% (по массе) в случае эмульгируемого концентрата или смачиваемого порошка.
Пестициды по настоящему изобретению применяются, когда они разбавлены с разбавителем, обычно при концентрации активного компонента от 0,1 до 5000 м.д. Когда они применяются непосредственно, доза на единицу области составляет от 0,1 до 5000 г на 1 га в расчете на соединение, которое служит активным компонентом. Однако доза не ограничена таким особым диапазоном.
Соединения по настоящему изобретению являются достаточно эффективными, когда применяются отдельно. Однако они могут применяться, если необходимо, в комбинации или в смеси с удобрениями или другими агрохимикалиями, такими как инсектициды, акарициды, нематоциды, фунгициды, антивирусные агенты, аттрактанты, гербициды и регуляторы роста растений, и такое комбинированное применение может иногда достигать улучшенного эффекта.
Типичные примеры инсектицидов, фунгицидов, акарицидов и подобных, которые могут применяться в комбинации с соединениями по настоящему изобретению, будут даны ниже.
Органофосфорные соединения и карбаматные инсектициды: фентион, фенитротион, диазинон, хлорпирифос, оксидепрофос, вамидотион, фентоат (фентоат), диметоат, формотион, малатион, трихлорфон, тиометон, фосмет, дихлорвос, ацефат, EPBP, метил-паратион, оксидиметон-метил, этион, диоксабензофос, цианофос (цианофос), изоксатион, пиридафентион, фосалон, метидатион, сулпрофос (сулпрофос), хлорфенвинфос, тетрахлорвинфос, диметилвинфос, пропaфос, изофенфос, дисулфотон, профенoфос, пираклофос, монокротофос, aзинфос-метил, альдикарб, метомил, тиодикарб, карбофуран, карбосулфан, бенфуракарб, фуратиокарб, пропоксур, фенобкарб, метолкарб, изопрокарб, карбарил (карбaрил), пиримикарб, этиофенкарб, дихлофентион, пиримифос-метил, хинальфос, хлорпирифос-метил, протиофос, наледь, EPN, XMC, бендиокарб, оксамил, аланикарб, хлорэтоксифос, и т.д.
Пиретроидные инсектициды: перметрин, циперметрин, дельтаметрин, фенвалерат, фенпропатрин, пиретрин, аллетрин, тетраметрин, ресметрин, диметрин, пропартрин, фенотрин, протрин, флувалинат, цифлутрин, цихалотрин, флуцитринат, этофенпрокс, циклопротрин, тралометрин, силафлуофен, тефлутрин, бифентрин, акринатрин, и т.д.
Инсектициды ацилмочевинного типа и другие: дифлубензурон, хлорфлуазурон, гексафлумурон, трифлумурон, тефлубензурон, флуфеноксурон, флуциклоксурон, бупрофезин, пирипросифен, луфенурон, сиромазин, метопрен, эндосулфан, диафентиурон, имидаклоприд, ацетамиприд, нитенпирам, клотианидин, динотефуран, тиаметоксам, тиаклоприд, пиметрозин, фипронил, пиридалил, никотин-сульфат, ротенон, метальдегид, машинное масло, микробные пестициды, такие как BT и энтомопатогенные вирусы, феноксикарб, картап, тиоциклам, бенсультар, тебуфенозид, хлорфенапир, эмамектин-бензоат, ацетаприд, нитенпирам, олеат натрия, рапсовое масло, и т.д.
Нематоциды: фенамифос, фостиазат, этопрофос, метилизотиоцианат, 1,3-дихлопропен, DCIP, и т.д.
Акарициды: хлорбензилат, фенизобромолат, дикофол, амитраз, пропаргит, бензомат, гесатиазокс, фенбутатин оксид, полинактин, хинометионат, хлорфенсон, тетрадифон, авермектин, милбемектин, слофентезин, пиридабен, фенпироксимат, тебуфенпирад, пиримидифен, фенотиокарб, диенохлор, этоксазол, бифеназат, ацехиноцил, галфенпрокс, спиродиклофен и т.д.
Фунгициды: тиофанат-метил, беномил, карбендазол, тиабендазол, фолпет, тиурам, дирам, зинеб, манеб, поликарбамат, ипробенфос, эдифенфос, фталид, пробеназол, изопротиолан, хлорталонил, каптан, полиоксин, бластицидин-S, касугамицин, стрептомицин, валидамицин, трициклазол, пирохилон, феназиноксид, мепронил, флутоланил, пенцицирон, ипродион, ксимексазол, металаксил, трифлумизол, трифорин, триaдимефон, битертанол, фенаримол, пропиконазол, цимоксанил, прохлораз, пефуразоат, гексаконазол, миклобутанил, дикломезин, теклофталам, пропинеб, дитианон, фосэтил, винклозолин, процимидон, оксадиксил, гуазатин, пропамокарб-гидрохлорид, флуазинам, оксолиновая кислота, гидроксиизоксазол, мепанипирим.
Соединения по настоящему изобретению проявляют превосходную пестицидную активность против паразитов, такие как полужесткокрылые паразиты, чешуекрылые паразиты, жесткокрылые паразиты, двукрылые паразиты, перепончатокрылые паразиты, прямокрылые паразиты, паразиты рода Isoptera, паразиты рода Thysanoptera, клещи и нематоды, паразитирующие на растениях. Следующие паразитные насекомые могут быть упомянуты в качестве таких паразитов.
Полужесткокрылые паразиты: клопы (HETEROPTERA), такие как соевый клоп (Riptortus clavatus), южный зеленый вонючий клоп (Nezaraviridula), клопики луговые (Lygus sp.), черепашковый клоп (Blissus leucopterus) и грушевые кружевницы (Stephanitis nashi); цикадки (Deltocephalinae), такие как зеленая рисовая цикадка (Nephotettix cincticeps) и цикадки (Empoasca sp., Erythroneura sp., Circulifer sp.); дельфациды, такие как коричневый рисовый дельфацид (Nilaparvata lugens), белобокий дельфацид (Sogatella furcifera) и малый коричневый дельфацид (Laodelphax striatellus); листоблошки, такие как Psyllids (Psylla sp.); белокрылки, такие как топольные белокрылки (Bemisiatabaci) и оранжерейные белокрылки (Trialeurodes vaporariorum); тли, такие как рапсовая вошь (Viteus vitifolii), зеленая персиковая тля (Myzus persicae), зеленая яблочная тля (Aphispomi), хлопковая тля (Aphis gossypii), Aphis fabae, турнепсовая тля (Rhopalosiphum psedobrassicas), тепличная помидорная тля (Aulacorthum solani) и тля злаковая обыкновенная (Schizaphis graminum); мучнистые червецы или щитовки, такие как комстоковский мучнистый клоп (Pseudococcus comstocki), красная восковая щитовка (Ceroplastes rubens), щитовка Сан Хосе (Comstockaspis perniciosa) и стрелолистная щитовка (Unaspis yanоnensis) и клопы-хищнецы (Rhodinius sp.).
Чешуекрылых паразитов: листовертки, такие как азиатская чайная листовертка (Homona magnanima), сетчатая листовертка (Adoxophyes orana), листовертки (Sparganothis pilleriana), листовертка восточная персиковая (Grapholitha molesta), точильщик соевых стручков (Leguminivora glycinivorella), плодожорка яблонная (Laspeyresia pomonella), Eucosma sp. и Lobesia botrana; Cochylidae, такие как виноградная плодожорка (Eupoecillia ambiguella); мешочницы, такие как Bambalina sp.; моль настоящая, такие как моль амбарная (Nemapogon granellus) и платяная моль (Tinea translucens); моль-крошка, такая как Lyonetid prunifoliella; моли-пестрянки, такие как яблочные моли-минеры узкокрылые (Phyllonorycter rigoniella); род Phyllocnistidae, такие как цитрусовые моли-минеры узкокрылые (Phyllocnistis citrella); моли, такие как серебристая моль (Plutella xylostella) и Prays citri; стеклянницы, такие как виноградная стеклянница (Pаrаnthrene regalis) и Synanthedon sp.; выемчатокрылые моли, такие как розовый коробочный червь хлопчатника (Pectinophora gossypiella), стеблевая нематода картофеля (Phthorimaea operculella) и Stomopteryx sp.; род Carposinidae, такие как персиковая моль (Carposina niponensis); бабочки-мокрицы, такие как азиатская моль (Monemaflavescens); огневки, такие как Огневка стеблевая азиатская (Chilo suppressalis), рисовые листовертки (Cnaphalocrocis medinalis), Ostrinia nubilalis, азиатский зерновой бурильщик (Qstrinia furnacalis), огневка капустная (Hellula undalis), моль большая восковая (Galleria mellonella), Elasmopalpus lignosellus и Loxostege sticticalis; бели, такие как обычный капустный червь (Pieris rapae); пяденицы, такие как полынная пяденица (Ascotis selenaria); коконопряды, такие как коконопряд (Malacosoma neustria); бражники, такие как Manducasexta; волнянки, такие как чайная волнянка (Euprоctis pseudoconspersa) и шелкопряд непарный (Lymantria dispar); медведницы, такие как американская белая бабочка (Hyphantria cunea); и совки, такие как табачная листовертка (Heliothis virescens), совка хлопковая (Helicoverpazea), свекольный походный червь (Spodoptera exigua), коробочный хлопковый червь (Helicoverpa armigera), обычная озимая совка (Spodoptera litura), капустный походный червь (Mamestra brassicae), черная озимая совка (Agrotis ipsiron), рисовый походный червь (Pseudaletia sepаrаta) и совка капустная (Trichoplusiani).
Жесткокрылые паразиты: майские жуки, такие как медный майский жук (Anomala cuprea), хрущик японский (Popillia japonica), соевый жук (Anomala rufocuprea) и Eutheolarugiceps; жуки-щелкуны, такие как проволочник (Agriotes sp.) и Conodeus sp.; божьи коровки, такие как божья коровка двадцати восьми пятен (Epilachna vigintioctopunctata) и жук мексиканского боба (Epilachna varivestis); чернотелки, такие как хрущак каштановый (Tribolium castaneum); длиннорогие жуки, такие как белопятный длиннорогий жук (Anoplophora malasiaca) и сосновый пилильщик (Моnоchamus alternatus); зерновки, такие как зерновка фасолевая (Acanthoscelides obtectus) и долгоносик лучистой фасоли (Callosobruchus chinensis); листоеды, такие как колорадский жук (Leptinotarsa decemlineata), червь кукурузного корня (Diаbrotica sp.), рисовый листоед (Oulema oryzae), свекольная блоха (Chaetocnema concinna), Phaedon cochlearias, Oulema melanopus и Dicladispa armigera; род Apionidae, такие как Apion godmani; долгоносики, такие как долгоносик рисовый водяной (Lissorhoptrus oryzophilus) и долконосик хлопчатника (Anthonomus grandis); род Rhynchophoridae, такие как кукурузный долгоносик (Sitophilus zeamais); жуки-короеды; кожееды; и хлебные точильщики.
Двукрылые паразиты: рисовые долгоножки (Tipraano), рисовые мошки (Tanytarsus oryzae), галлицы (Orseolia oryzae), муха средиземноморская плодовая (Ceratitis capitata), рисовые моли-минеры узкокрылые (Hydrellia griseola), вишневая дрозофила (Drosophila suzukii), мушка шведская (Oscinellafrit), личинки рисовых побегов (Chlorops oryzae), минер фасоли (Ophiomyia phaseoli), бобовые моли-минеры узкокрылые (Liriomyza trifolii), шпинатные моли-минеры узкокрылые (Pegomya hyoscyami), бородавочная личинка (Hylemia platura), сорговая мушка (Atherigona soccata), настоящие мухи (Musca domestica), желудочные оводы (Gastrophilus sp.), жигалка осенняя (Stomоxys sp.), москит желтой лихорадки (Aedes aegypti), домашний москит (Culex pipiens), малярийный москит (Anopheles slnensis) и Culex tritaeniorhynchus.
Перепончатокрылые паразиты: злаковые пилильщики (Cephus sp.); эвритомиды (Harmolita sp.); капустный пилильщик (Athalia sp.), шершни (Vespa sp.) и огненные муравьи.
Прямокрылые паразиты: прусак (Blatella germanica); американский таракан (Periplaneta americana); медведка африканская (Gryllotalpa africana); перелетная саранча (Locusta migratoria migratoriodes) и Melanoplus sanguinipes.
Паразиты рода Isoptera: термиты (Reticulitermes speratus) и тайваньский подземный термит (Coptotermes formosanus).
Паразиты рода Thysanopetra: желтые чайные трипсы (Scirtothrips dorsalis); дынные трипсы (Thrips palmi); оранжерейные трипсы (Heliothrips haemorrholidalis); западные цветочные трипсы (Frankliniella occidentalis) и рисовые шиповидные трипсы (Haplothrips aculeatus).
Клещи: клещик паутинный двупятнистый (Теtrаnychus urticae); клещик паутинный Канзавы (Теtrаnychus kanzawai); клещик красный цитрусовый (Panоnychus citri); Европейский красный клещ (Panоnychus ulmi), желтый паутинный клещик (Eotеtrаnychus carpini); Техасский цитрусовый клещ (Eotеtrаnychus banksi); красный цитрусовый клещ (Phyllocoptruta oleivora); широкий клещ (Polyphagotarsonemus latus); ложные паутинные клещи (Brevipalpussp.); корневой клещик (Rhizoglyphus robini) и плесневый клещ (Tyrophagus putrescentiae).
Нематоды, паразитирующие на растениях: нематода корневых наростов (Meloidogyne sp.); корневая нематода (Pratylenchus sp.); цистовая нематода соевого боба (Heterodera glycines); золотистая нематода (Globodera rostochiensis); банановая свищевая нематода (Radopholus similis); нематода земляничных клубней (Aphelenchoides fragariae); нематода побегов белого риса (Aphelenchoides besseyi) и сосновая нематода (Bursaphelenchus xylophilus).
Другие паразиты, животные-вредители, антисанитарные насекомые: брюхоногие (Gastropoda), такие как яблочные улитки (Pomaceacanaliculata), слизни (Incilaria sp.) и гигантская ахатина (Achatina fulica); равноногие (Isopoda), такие как мокрицы (Armadillidium sp.), равноногие ракообразные и сороконожки; книжная вошь, такая как Liposcelis sp.; чешуйницы, такие как Ctenolepisma sp.; блохи, такие как Pulex sp. и Ctenocephalides sp.; мехоеды, такие как Trichodectes sp.; постельные клопы, такие как Cimex sp.; клещи, паразитирующие на животных, такие как Boophilus microplus и Haemaphysalis longicornis и Epidermoptidae.
Далее, соединения по настоящему изобретению эффективны также против паразитных насекомых, которые проявляют устойчивость к органофосфорным соединениям, карбаматным соединениям, синтетическим пиретроидным соединениям, ацилмочевинным соединениям или традиционным инсектицидам.
ПРИМЕРЫ
Получение, рецептурирование и применение соединений по настоящему изобретению будут ниже описаны в деталях со ссылками на примеры. Также будет описано получение промежуточных соединений синтеза соединений по настоящему изобретению.
ПРИМЕР 1
Получение [5-(5-амино-3-трифторметил-1,2,4-триазолил)-4-хлор-2-метилфенил]2,2,2-трифторэтилсульфида (Соединение №7 по настоящему изобретению)
(1) Синтез 5-ацетилтио-2-хлор-4-метилацетанилида.
55 г 2-хлор-4-метилацетанилида добавляли к 100 мл хлорсульфоновой кислоты при температуре от 5 до 10°C. 65 г 60% дымящей серной кислоты добавляли к жидкой смеси при температуре от 10 до 15°C, и конечную смесь перемешивали при комнатной температуре в течение 1 часа и далее перемешивали при 90°C в течение 18 часов. Затем конечную реакционную смесь охлаждали до комнатной температуры, выливали в ледяную воду, добавляли толуол, отфильтровывали нерастворимые вещества, и конечный органический слой промывали водой и высушивали над безводным сульфатом магния. Растворитель отгоняли при пониженном давлении, смесь полученного остатка, 31 г красного фосфора, 1 г иода и 200 мл уксусной кислоты кипятили с нагреванием в течение 1 часа, и полученную реакционную смесь охлаждали до комнатной температуры. Затем отфильтровывали нерастворимые вещества, жидкость концентрировали при пониженном давлении, добавляли воду, и проводили экстракцию этилацетатом. Органический слой промывали водой и высушивали над безводным сульфатом магния, растворитель отгоняли при пониженном давлении, и остаток очищали хроматографией на силикагелевой колонке для получения 14 г 5-ацетилтио-2-хлор-4-метилацетанилида.
(2) Синтез 2-хлор-4-метил-5-меркаптоанилина.
14 г 5-ацетилтио-2-хлор-4-метилацетанилида растворяли в 150 мл этанола, и добавляли 22 г 50% водного раствора гидроксида натрия, затем нагревали до кипения в течение 4 часов. Полученную реакционную смесь концентрировали при пониженном давлении, добавляли воду, смесь нейтрализовали разбавленной соляной кислотой и затем экстрагировали этилацетатом. Органический слой промывали водой и высушивали над безводным сульфатом магния, растворитель отгоняли при пониженном давлении, что дало 9,4 г 2-хлор-4-метил-5-меркаптоанилина.
(3) Синтез 2-хлор-4-метил-5-(2,2,2-трифторэтилтио)анилина.
Смесь 9,4 г 2-хлор-4-метил-5-меркаптоанилина, 20 г 2,2,2-трифторэтилиодида, 13 г карбоната калия и 200 мл N,N-диметилформамида перемешивали при комнатной температуре в течение 16 часов. Реакционную смесь концентрировали при пониженном давлении, добавляли воду, и смесь экстрагировали толуолом. Органический слой промывали водой, высушивали над безводным сульфатом магния и растворитель отгоняли при пониженном давлении, что дало 13,5 г 2-хлор-4-метил-5-(2,2,2-трифторэтилтио)анилина.
Данные1Н-ЯМР (CDCl3/TMS, величина δ (м.д.)): 2,32 (3H, с), 3,33 (2H, кв.), 3,96 (2H, с), 6,94 (1H, с), 7,11 (1H, с)
(4) Синтез 2-хлор-4-метил-5-(2,2,2-трифторэтилтио)фенилгидразина.
13,5 г 2-хлор-4-метил-5-(2,2,2-трифторэтилтио)анилина добавляли по каплям к 30 мл концентрированной соляной кислоты при комнатной температуре, и к этой смеси добавляли по каплям водный раствор, содержащий 3,8 г нитрита натрия при температуре от 0 до 5°C, смесь перемешивали в течение 1 часа для получения соли диазония. 36 г дигидрата хлорида олова растворяли в 250 мл 6N соляной кислоты, и к этому полученному раствору по каплям добавляли вышеописанный водный раствор соли диазония при температуре от 0 до 5°C, далее раствор перемешивали при комнатной температуре в течение 2 часов. Добавляли толуол, раствор нейтрализовали водным раствором гидроксида натрия, нерастворимые вещества отфильтровывали, и органический слой промывали водой и высушивали над безводным сульфатом магния. Растворитель отгоняли при пониженном давлении, что дало 12,1 г 2-хлор-4-метил-5-(2,2,2-трифторэтилтио) фенилгидразина.
(5) Синтез {2-хлор-4-метил-5-(2,2,2-трифторэтилтио)фенил}гидразона трифторацетальдегида
Смесь 4,1 г 2-хлор-4-метил-5-(2,2,2-трифторэтилтио)-фенилгидразина, 2,3 г полуэтилацеталя трифторацетальдегида, 0,1 г моногидрата пара-толуолсульфоновой кислоты и 50 мл этанола кипятили с нагреванием в течение 6 часов. Полученную реакционную смесь концентрировали при пониженном давлении, добавляли воду, и смесь экстрагировали толуолом. Органический слой промывали водой, высушивали над безводным сульфатом магния и растворитель отгоняли при пониженном давлении, что дало 3,6 г {2-хлор-4-метил-5-(2,2,2-трифторэтилтио)фенил}гидразона трифторацетальдегида.
(6) Синтез N-{2-хлор-4-метил-5-(2,2,2-трифторэтилтио)фенил}-трифторацетогидразоноил бромида.
3,6 г (10,3 ммоль) {2-хлор-4-метил-5-(2,2,2-трифторэтилтио)фенил}гидразона трифторацетальдегида растворяли в 30 мл N,N-диметилформамида, добавляли 2,0 г N-бромсукцинимида при комнатной температуре, затем смесь перемешивали при комнатной температуре в течение 2 часов. Конечную реакционную смесь выливали в воду и экстрагировали толуолом, органический слой промывали водой и высушивали над безводным сульфатом магния. Растворитель отгоняли при пониженном давлении, что дало 4,1 г N-{2-хлор-4-метил-5-(2,2,2-трифторэтилтио)фенил}-трифторацетогидразоноил бромида.
(7) Синтез [5-(5-амино-3-трифторметил-1,2,4-триазолил)-4-хлор-2-метилфенил]2,2,2-трифторэтилсульфида.
3,5 г триэтиламина добавляли при комнатной температуре к смеси 4,1 г N-{2-хлор-4-метил-5-(2,2,2-трифторэтилтио)фенил}-трифторацетогидразоноил бромида, 4,4 г гидроиодида S-метилизотиомочевины и 100 мл тетрагидрофурана, и смесь перемешивали при 50°C в течение 3 часов. Реакционную смесь концентрировали при пониженном давлении, к полученному остатку добавляли ксилол и затем нагревали до кипения в течение 2 часов. Реакционную смесь охлаждали до комнатной температуры, затем промывали водой, и органический слой высушивали над безводным сульфатом магния. Растворитель отгоняли при пониженном давлении, и полученные неочищенные кристаллы перекристаллизовывали из этанола, что дало 2,0 г [5-(5-амино-3-трифторметил-1,2,4-триазолил)-4-хлор-2-метилфенил]-2,2,2-трифторэтилсульфида в виде слегка серых кристаллов (температура плавления 193-194°C).
ПРИМЕР 2
Получение [5-(5-амино-3-трифторметил-1,2,4-триазолил)-4-хлор-2-метилфенил]-2,2,2-трифторэтилсульфоксида (Соединение №8 по настоящему изобретению).
1,3 г [5-(5-амино-3-трифторметил-1,2,4-триазолил)-4-хлор-2-метилфенил]-2,2,2-трифторэтилсульфид растворяли в 80 мл этилацетата, и добавляли 0,9 г мета-хлорпербензойной кислоты (чистота 75%) при охлаждении льдом. Смесь перемешивали при охлаждении льдом в течение 2 часов, промывали водным раствором тиосульфата натрия, затем промывали водным раствором бикарбоната натрия и затем высушивали над безводным сульфатом магния. Растворитель отгоняли при пониженном давлении, полученные кристаллы промывали четыреххлористым углеродом, что дало 1,2 г [5-(5-амино-3-трифторметил-1,2,4-триазолил)-4-хлор-2-метилфенил]2,2,2-трифторэтилсульфоксида в виде белых кристаллов (температура плавления 235-237°C).
ПРИМЕР 3
Получение [5-(3-нитро-1,2,4-триазолил)-2-дифторметилфенил]-2,2,2-трифторэтилсульфида (Соединение №11 по настоящему изобретению).
(1) Синтез 4-(3-нитро-1,2,4-триазолил)-2-фторбензальдегида
10 мл раствора в N,N-диметилформамиде 3,4 г 3-нитро-1,2,4-триазола добавляли по каплям к суспензии (60%) 1,2 г гидрида натрия в 50 мл N,N-диметилформамида при охлаждении льдом. После того как заканчивалось выделение водорода, добавляли 4,3 г 2,4-дифторбензальдегида, затем перемешивали при 70°C в течение 3 часов. Смесь концентрировали при пониженном давлении, добавляли 200 мл воды и экстрагировали этилацетатом. Слой этилацетата промывали водой и высушивали над безводным сульфатом магния. Растворитель отгоняли при пониженном давлении, и полученные неочищенные кристаллы промывали диизопропиловым эфиром, что дало 1,6 г 4-(3-нитро-1,2,4-триазолил)-2-фторбензальдегида.
(2) Синтез 4-(3-нитро-1,2,4-триазолил)-2-(2,2,2-трифторэтилтио)бензальдегида.
0,8 г 2,2,2-трифторэтилмеркаптана добавляли по каплям при охлаждении льдом к смеси 1,6 г 4-(3-нитро-1,2,4-триазолил)-2-фторбензальдегида, 1,3 г карбоната калия и 50 мл N,N-диметилформамида, затем смесь перемешивали при температуре от 0 до 10°C в течение 4 часов. Смесь концентрировали при пониженном давлении, добавляли 200 мл воды и экстрагировали этилацетатом. Органический слой промывали водой и высушивали над безводным сульфатом магния. Растворитель отгоняли при пониженном давлении, что дало 1,8 г 4-(3-нитро-1,2,4-триазолил)-2-(2,2,2-трифторэтилтио)бензальдегида.
(3) Синтез [5-(3-нитро-1,2,4-триазолил)-2-дифторметилфенил]-2,2,2-трифторэтилсульфида.
2,6 г диэтиламинотрифторида серы добавляли при охлаждении льдом к смеси 1,8 г 4-(3-нитро-1,2,4-триазолил)-2-(2,2,2-трифторэтилтио)бензальдегида с 20 мл хлористого метилена, затем нагревали до кипения в течение 6 часов. После охлаждения смеси до комнатной температуры, выливали в ледяную воду, и органический слой промывали водным раствором бикарбоната натрия, водой и затем высушивали над безводным сульфатом магния. Растворитель отгоняли при пониженном давлении и остаток очищали хроматографией на силикагелевой колонке, что дало [5-(3-нитро-1,2,4-триазолил)-2-дифторметилфенил]-2,2,2-трифторэтилсульфида в виде слабо-желтых кристаллов (температура плавления 74-76°C).
ПРИМЕР 4
Получение [5-(5-амино-3-трифторметил-1,2,4-триазолил)-4-фтор-2-метилфенил]-2,2,2-трифторэтилсульфида (Соединение №1 по настоящему изобретению)
(1) Синтез 5-ацетилтио-2-фтор-4-метилацетанилида.
150 г 2-фтор-4-метилацетанилида добавляли к 500 г хлорсульфоновой кислоты при 50°C или менее, затем перемешивали в течение 1 часа. Реакционную смесь выливали в смесь ледяной воды с этилацетатом, органический слой промывали водой, высушивали над безводным сульфатом магния и растворитель отгоняли при пониженном давлении, что дало твердый остаток. Полученный твердый остаток растворяли в 350 мл уксусной кислоты, полученный раствор добавляли по каплям к смеси 84 г красного фосфора, 1 г йода и 300 мл уксусной кислоты при нагревании до кипения в течение 1 час, затем нагревали до кипения в течение 2 часов. Реакционную смесь охлаждали до комнатной температуры, нерастворимые вещества отфильтровывали, и жидкость концентрировали при пониженном давлении, выливали в воду, и смесь экстрагировали этилацетатом. Органический слой промывали водой, высушивали над безводным сульфатом магния и растворитель отгоняли при пониженном давлении, что дало 211 г 5-ацетилтио-2-фтор-4-метилацетанилида.
(2) Синтез 2-фтор-4-метил-5-меркаптоанилина.
211 г 5-ацетилтио-2-фтор-4-метилацетанилида растворяли в 500 мл этанола, и к этому раствору добавляли по каплям раствор, содержащий 200 г гидроксида калия и 500 мл воды в течение 30 минут, затем нагревали до кипения в течение 5 часов. Затем реакционную смесь охлаждали до комнатной температуры, нейтрализовали разбавленной соляной кислотой, концентрировали при пониженном давлении и экстрагировали этилацетатом. Органический слой высушивали над безводным сульфатом магния и растворитель отгоняли при пониженном давлении, что дало 129 г 2-фтор-4-метил-5-меркаптоанилина.
(3) Синтез 2-фтор-4-метил-5-(2,2,2-трифторэтилтио)анилина.
К 1000 мл раствора в N,N-диметилформамиде 129 г 2-фтор-4-метил-5-меркаптоанилина добавляли 250 г 2,2,2-трифторэтилиодида и 125 г карбоната калия, далее добавляли 10 г ронгалита и затем перемешивали при комнатной температуре в течение 8 часов. Реакционную смесь выливали в воду, смесь экстрагировали этилацетатом, органический слой высушивали над безводным сульфатом магния и растворитель отгоняли при пониженном давлении, что дало 182 г 2-фтор-4-метил-5-(2,2,2-трифторэтилтио)анилина.
Данные1Н-ЯМР (CDCl3/TMS, величина δ (м.д.)): 2,36 (3H, с), 3,30 (2H, кв.), 3,64 (2H, с), 6,86 (1H, д), 6,98 (1H, д).
(4) Синтез 2-фтор-4-метил-5-(2,2,2-трифторэтилтио)фенилгидразина
53 г нитрита натрия добавляли к 300 мл концентрированной серной кислоты при 50°C или менее, и добавляли по каплям 300 мл уксусной кислоты при 50°C или менее. К полученной смеси добавляли по каплям раствор в 100 мл уксусной кислоты 182 г 2-фтор-4-метил-5-(2,2,2-трифторэтилтио)анилина в течение 2 часов при 20°C или менее, затем перемешивали при 20°C в течение 3 часов. Реакционную смесь добавляли по каплям при 5°C или менее к жидкой смеси 390 г дигидрата хлорида олова(II) и 1000 мл 6N соляной кислоты, затем перемешивали в течение 30 минут. К этой реакционной смеси добавляли толуол, и реакционную смесь нейтрализовали 10% водным раствором гидроксида натрия. Нерастворимые вещества отфильтровывали, органический слой высушивали над безводным сульфатом магния и концентрировали при пониженном давлении, что дало 177 г 2-фтор-4-метил-5-(2,2,2-трифторэтилтио)фенилгидразина.
(5) Синтез {2-фтор-4-метил-5-(2,2,2-трифторэтилтио)фенил}-гидразона трифторацетальдегида.
Смесь 3,1 г 2-фтор-4-метил-5-(2,2,2-трифторэтилтио)-фенилгидразина, 1,9 г полуэтилацеталя трифторацетальдегида, 0,5 г метансульфоновой кислоты и 100 мл этанола кипятили с нагреванием в течение 5 часов. Затем реакционную смесь охлаждали до комнатной температуры, концентрировали при пониженном давлении, экстрагировали этилацетатом и органический слой высушивали над безводным сульфатом магния. Растворитель отгоняли при пониженном давлении, что дало 3,7 г {2-фтор-4-метил-5-(2,2,2-трифторэтилтио)фенил}гидразона трифторацетальдегида.
(6) Синтез N-{2-фтор-4-метил-5-(2,2,2-трифторэтилтио)фенил}-трифторацетогидразоноил бромида
3,7 г {2-фтор-4-метил-5-(2,2,2-трифторэтилтио)фенил}гидразон трифторацетальдегида растворяли в 50 мл N,N-диметилформамида, при комнатной температуре добавляли 2,0 г N-бромсукцинимида, затем перемешивали при комнатной температуре в течение 30 минут. Реакционную смесь выливали в воду, экстрагировали этилацетатом и органический слой высушивали над безводным сульфатом магния. Растворитель отгоняли при пониженном давлении, что дало 4,4 г N-{2-фтор-4-метил-5-(2,2,2-трифторэтилтио)фенил}-трифторацетогидразоноил бромида.
(7) [5-(5-амино-3-трифторметил-1,2,4-триазолил)-4-фтор-2-метилфенил]2,2,2-трифторэтилсульфид
К 100 мл тетрагидрофурана добавляли 4,5 г гидроиодида S-метилизотиомочевины, 4,4 г N-{2-фтор-4-метил-5-(2,2,2-трифторэтилтио)фенил}трифторацетогидразоноил бромида и 3,5 г триэтиламина, затем нагревали до кипения в течение 8 часов. Затем реакционную смесь охлаждали до комнатной температуры, концентрировали при пониженном давлении, экстрагировали этилацетатом, органический слой промывали водой и высушивали над безводным сульфатом магния. Растворитель отгоняли при пониженном давлении, и полученное твердое вещество очищали колоночной хроматографией (элюент: этилацетат:гексан=4:1), что дало 2,9 г [5-(5-амино-3-трифторметил-1,2,4-триазолил)-4-фтор-2-метилфенил]-2,2,2-трифторэтилсульфида в виде слабо-желтых кристаллов (температура плавления 171-173°C).
ПРИМЕР 5
Получение [5-(5-амино-3-трифторметил-1,2,4-триазолил)-4-фтор-2-метилфенил]2,2,2-трифторэтилсульфоксида. (Соединение №2 по настоящему изобретению)
1,9 г [5-(5-амино-3-трифторметил-1,2,4-триазолил)-4-фтор-2-метилфенил]-2,2,2-трифторэтилсульфида растворяли в 100 мл хлороформа, и при 0°C добавляли 1,0 г мета-хлорпербензойной кислоты, затем перемешивали при комнатной температуре в течение 1 часа. Растворитель отгоняли при пониженном давлении, и полученный остаток очищали колоночной хроматографией (элюент этилацетат:гексан:триэтиламин=50:50:1), что дало 1,8 г [5-(5-амино-3-трифторметил-1,2,4-триазолил)-4-фтор-2-метилфенил]-2,2,2-трифторэтилсульфоксида в виде слабо-желтых кристаллов (температура плавления 236-238°C).
ПРИМЕР 6
Получение [5-(5-трифторацетиламино-3-трифторметил-1,2,4-триазолил)-4-фтор-2-метилфенил]-2,2,2-трифторэтилсульфида. (Соединение №5 по настоящему изобретению)
1,1 г [5-(5-амино-3-трифторметил-1,2,4-триазолил)-4-фтор-2-метилфенил]-2,2,2-трифторэтилсульфида добавляли к 50 мл трифторуксусного ангидрида, затем перемешивали при комнатной температуре в течение 12 часов. Растворитель отгоняли при пониженном давлении, полученное твердое вещество очищали колоночной хроматографией (элюент этилацетат:гексан=2:1), что дало 1,1 г [5-(5-трифторацетиламино-3-трифторметил-1,2,4-триазолил)-4-фтор-2-метилфенил]-2,2,2-трифторэтилсульфида в виде слабо-желтых кристаллов (температура плавления 122-125°C).
ПРИМЕР 7
Получение [5-(5-амино-3-трифторметил-1,2,4-триазолил)-4-фтор-2-метилфенил]2,2,2-трифторэтилсульфоксида. (Соединение №6 по настоящему изобретению)
0,8 г [5-(5-трифторацетиламино-3-трифторметил-1,2,4-триазолил)-4-фтор-2-метилфенил]-2,2,2-трифторэтилсульфида растворяли в 50 мл хлороформа, и при 0°C добавляли 0,3 г мета-хлорпербензойной кислоты, затем перемешивали при комнатной температуре в течение 1 часа. Растворитель отгоняли при пониженном давлении, и полученное твердое вещество очищали колоночной хроматографией (элюент этилацетат:гексан=1:1), что дало 0,6 г [5-(5-трифторацетиламино-3-трифторметил-1,2,4-триазолил)-4-фтор-2-метилфенил]-2,2,2-трифторэтилсульфоксида в виде бледно-желтого порошка (температура плавления 233-237°C).
Структурные формулы и физические свойства соединений [I] по настоящему изобретению, синтезированных согласно вышеописанным примерам, включая вышеописанные примеры, показаны в таблицах 7-10, обозначения символов в таблицах определены выше.
Номера соединений относятся к последующему описанию.
Данные1Н-ЯМР (CDCl3/TMS, величины δ(м.д.)) для соединений №№ 49, 59, 101, 128, 158, 184, 185, 193, 195 и 209 будут показаны ниже.
Соединение №49: 2,56 (3H, с), 3,40 (2H, кв.), 5,29 (2H, с), 7,21 (1Н, д), 7,67 (1Н, д)
Соединение №59: 1,22-1,28 (3H, м), 2,55 (3H, с), 3,40 (2H, кв.), 3,46-3,55 (2H, м), 4,12 (1Н, т), 7,20 (1Н, д), 7,63 (1Н, д)
Соединение №101: 2,54 (3H, с), 3,07 (3H, д), 3,3,9 (2H, кв.), 4,25 (1Н, с), 7,17 (1Н, д), 7,61 (1Н, д)
Соединение №128: 1,32 (6H, т), 2,50 (3H, с), 3,25 (4H, кв.), 3,44 (2H, кв.), 7,19 (1Н, с), 7,75 (1Н, с)
Соединение №158: 1,98 (3H, с), 2,56 (3H, с), 3,05 (3H, с), 3,36 (2H, кв.), 3,85 (2H, кв.), 7,16 (1Н, д), 7,61 (1Н, д)
Соединение №184: 2,29 (1Н, д), 2,53 (3H, с), 3,39 (2H, кв.), 3,82 (2H, кв.), 4,20 (2H, дд), 4,34 (1Н, с), 7,16 (1Н, д), 7,61 (1Н, д)
Соединение №185: 2,29 (1Н, т), 2,47 (3H, с), 3,42-3,57 (2H, m), 3,83 (2H, кв.), 4,22 (2H, д), 4,40 (1Н, с), 7,22 (1Н, с), 8,12 (1Н, с)
Соединение №193: 2,30 (1Н, т), 2,55 (3H, с), 3,40 (2H, кв.), 4,24 (2H, кв.), 4,40 (1Н, с), 7,20 (1Н, д), 7,63 (1Н, д)
Соединение №195: 1,22-1,39 (1Н, м), 1,48-1,57 (1Н, м), 2,06-2,14 (1Н, м), 2,52 (3H, с), 3,07 (1Н, дд), 3,29 (1Н, дд), 3,42, (2H, т), 4,75 (2H, с), 7,16 (1Н, д), 7,65 (1Н, д)
Соединение №209: 2,61 (3H, с), 3,42 (2H, кв.), 7,31 (1Н, д), 7,74 (1Н, д)
Далее будет показан пример получения промежуточного соединения.
<Пример 1 получения промежуточного соединения>
(1) Синтез 5-ацетилтио-2,4-диметилацетанилида.
78 г 2-фтор-4-метилацетанилида добавляли к 168 г хлорсульфоновой кислоты при 40°C или менее, затем перемешивали при 70°C в течение 2 часов. Реакционную смесь выливали в смесь ледяной воды с этилацетатом, органический слой промывали водой, высушивали над безводным сульфатом магния и растворитель отгоняли при пониженном давлении, что дало твердый остаток. Полученный твердый остаток растворяли в 200 мл уксусной кислоты, полученный раствор добавляли по каплям к жидкой смеси 72 г красного фосфора, 1 г иода и 300 мл уксусной кислоты при нагревании до кипения в течение 1 часа, затем кипятили с нагреванием в течение 4 часов. Нерастворимые вещества отфильтровывали, уксусную кислоту отгоняли при пониженном давлении, добавляли воду, и остаток экстрагировали этилацетатом. Органический слой промывали водой и высушивали над безводным сульфатом магния. Растворитель отгоняли при пониженном давлении, что дало 42 г 5-ацетилтио-2,4-диметилацетанилида.
(2) Синтез 2-фтор-4-метил-5-меркаптоанилина.
42 г 5-ацетилтио-2-фтор-4-метилацетанилида добавляли к 5% водному раствору гидроксида калия, затем нагревали до кипения в течение 18 часов. Затем реакционную смесь охлаждали до комнатной температуры, доводили pH до 7 действием разбавленной соляной кислоты и экстрагировали этилацетатом. Органический слой высушивали над безводным сульфатом магния и растворитель отгоняли при пониженном давлении, что дало 25 г 2,4-диметил-5-меркаптоанилина.
(3) Синтез 2,4-диметил-5-(2,2,2-трифторэтилтио)анилина.
К раствору 20 г 2,4-диметил-5-меркаптоанилина в 150 мл N,N-диметилформамида, добавляли 41 г 2,2,2-трифторэтилиодида и 24 г карбоната калия, и далее добавляли 4 г ронгалита, затем перемешивали при комнатной температуре в течение 24 часов. Реакционную смесь выливали в воду и экстрагировали этилацетатом. Органический слой высушивали над безводным сульфатом магния, и растворитель отгоняли при пониженном давлении, полученный остаток очищали хроматографией на силикагелевой колонке (элюент гексан:этилацетат=5:1), что дало 29 г 2,4-диметил-5-(2,2,2-трифторэтилтио)анилина.
Данные1Н-ЯМР (CDCl3/TMS, величина δ (м.д.)): 2,13 (3H, с), 3,34 (3H, с), 3,32 (2H, кв.), 3,52 (2H, с), 6,84 (1Н, с), 6,91 (1Н, с).
Далее способы рецептурирования будут описаны детально со ссылкой на типичные примеры рецептурирования. Однако необходимо понимать, что типы и соотношения соединений и вспомогательных веществ не ограничены этими особыми примерами и могут варьировать в пределах широких диапазонов. В следующем описании, "часть(и)" обозначает "часть(и) по массе".
ПРИМЕР РЕЦЕПТУРЫ 1: Эмульгируемый концентрат
Для получения эмульгируемого концентрата растворяли, до единообразного вида смеси, соединение №6 (30 частей), циклогексанон (20 частей), полиоксиэтиленовый алкил-арильный эфир (11 частей), кальций алкилбензолсульфонат (4 части) и метилнафталин (35 частей).
ПРИМЕР РЕЦЕПТУРЫ 2: Смачиваемый порошок
Для получения смачиваемого порошка смешивали до единообразного вида смеси и растирали соединение №2 (10 частей), натриевую соль нафталинсульфоновой кислоты, конденсат формалина (0,5 части), полиоксиэтиленовый алкиларильный эфир (0,5 части), диатомит (24 части) и глину (65 частей).
ПРИМЕР РЕЦЕПТУРЫ 3: Пудра
Для получения пудры смешивали до единообразного вида смеси и растирали соединение №6 (2 части), диатомит (5 частей) и глину (93 части).
ПРИМЕР РЕЦЕПТУРЫ 4: Гранулы
Для получения гранул смешивали до единообразного вида смеси и растирали соединение №2 (5 частей), О-лаурилсульфат натрия (2 части), лигнинсульфонат натрия (5 частей), карбоксиметилцеллюлозу (2 части) и глину (86 частей). К этой смеси (100 частей) добавляли воду (20 частей) и смесь вымешивали, с образованием гранул с номерами сит 14-32 с применением гранулятора экструзионного типа и высушивали до получения гранулированной рецептуры.
Далее действия пестицидов, содержащих соединения по настоящему изобретению в качестве активных компонентов, будут описаны со ссылкой на примеры тестирования. Сравнительные соединения а и b представляли собой соединения [VI-208] и [VI-226], впервые описанные в JP-A-2000-198768:

ПРИМЕР ТЕСТИРОВАНИЯ 1. Акарицидный тест на клещиках паутинных двупятнистых (путем макания)
Смачиваемые порошки получали согласно примеру рецептуры 2 и разбавляли водой до концентрации активного компонента в 500 м.д. Проростки соевого боба, которые были привиты с имаго клещика паутинного двупятнистого, обмакивали в полученные растворы и высушивали на воздухе. Обработанные проростки помещали в термостатическую камеру при 25°C на 13 дней, и подсчитывали число уцелевших клещей для вычисления акарицидной величины с применением уравнения 2, тест проводили по системе одной серии. Результаты этого теста показаны в таблицах 11 и 12.
ПРИМЕР ТЕСТИРОВАНИЯ 2. Акарицидный тест на клещике паутинном двупятнистом (путем смачивания грунта)
Смачиваемые порошки получали согласно примеру рецептуры 2 и разбавляли водой до концентрации активного компонента в 100 м.д. 100 г грунта в горшках с проростками соевого боба, которые были привиты с имаго клещика паутинного двупятнистого, смачивали 5 мл полученных растворов. Обработанные проростки помещали в термопластическую камеру при 25°C на 13 дней, и подсчитывали число уцелевших клещей для вычисления акарицидной величины с применением уравнения 2, результаты этого теста показаны в таблицах 13 и 14.
ПРИМЕР ТЕСТИРОВАНИЯ 3. Инсектицидный тест на коричневом дельфациде.
Смачиваемые порошки получали согласно примеру рецептуры 2 и разбавляли водой до концентрации активного компонента в 500 м.д. Проростки риса погружали в полученные растворы и помещали в пластиковые чашки емкостью 60 мл. Десять личинок четвертой возрастной стадии коричневого дельфацида помещали в чашку, чашку закрывали и помещали в термостатическую камеру при 25°C на 6 дней, и уцелевших подсчитывали для вычисления инсектицидной величины по уравнению 1, тест проводили по системе одной серии. Результаты этого теста показаны в таблицах 15 и 16.
ПРИМЕР ТЕСТИРОВАНИЯ. Антигельминтный тест на южной нематоде корневых наростов.
Соединения по настоящему изобретению (5 частей) и в качестве поверхностно-активного вещества Tween 20 (торговая марка для монолаурата полиоксиэтиленсорбита) (1 часть) растворяли в N,N-диметилформамиде (94 частей) для получения 5% эмульгируемых концентратов соединений по настоящему изобретению. Добавляли дистиллированную воду к эмульгируемым концентратам для получения разбавленных растворов, имеющих концентрацию соединений по настоящему изобретению 20 м.д. Смешивали 0,5 мл разбавленных растворов и 0,5 мл водной суспензии, содержащей 100 личинок второй стадии южной нематоды корневых наростов, и смесь помещали в термостатическую камеру при 25°C на 5 дней, уцелевших подсчитывали для вычисления антигельминтной величины по уравнению 3. Тест проводили по системе двух серий. Результаты этого теста показаны в таблицах 17 и 18.
Уравнение 1
Величина инсектицидного действия (%) =
Число уцелевших в обработанной области × 100
10
Уравнение 2:
Величина акарицидного действия (%)=
число взрослых клещей в обработанной области на момент осмотра) × 100
число взрослых клещей в контрольной области на момент осмотра
Уравнение 3
ПРОМЫШЛЕННАЯ ПРИМЕНИМОСТЬ
Производные 3-триазолилфенилсульфида по настоящему изобретению проявляют выдающуюся эффективность на различных сельскохозяйственных и садовых паразитах, в особенности на клещах, чешуекрылых паразитах, полужесткокрылых паразитах, жесткокрылых паразитах и нематодах, и они могут широко применяться в качестве инсектицидов, акарицидов и нематоцидов, имеющих такую активность при обработке грунта, при которой становится возможным безопасное и трудосберегающее применение.
Полное содержание японской заявки на патент №2004-305251, опубликованной 20 октября 2004, включая описание, формулу изобретения и реферат, включено здесь посредством цитирования во всей полноте.
Реферат
Описываются новые производные 3-триазолилфенилсульфида, имеющие превосходную активность при обработке грунта в качестве инсектицидов, акарицидов или нематоцидов для сельскохозяйственных и садовых растений. Производные 3-триазолилфенилсульфида представлены формулой [1]: ! ! где R представляет собой циклопропилметильную группу или трифторэтильную группу, В2 представляет собой атом водорода, атом галогена или метильную группу, В4 представляет собой атом галогена, цианогруппу или C1-С6-алкильную группу (которая может быть поли-замещена атомами галогена), и каждый из A1 и А3 выбирают из групп Группы I и Группы II, приведенных в формуле изобретения, n представляет собой целое число от 0 до 1. Описываются также производное анилина, которое является промежуточным соединением для получения соединения формулы (I), и инсектицид, акарицид или нематоцид на основе соединения формулы (I). 3 и 7 з.п. ф-лы, 18 табл.
Формула
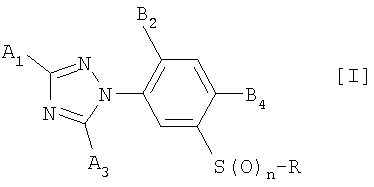
где R представляет собой циклопропилметильную группу или трифторэтильную группу;
n представляет собой целое число от 0 до 1;
A1 и А3 выбирают из групп Группы I и Группы II, при условии, что один из них выбирают из групп Группы II;
В2 представляет собой атом водорода, атом галогена или метильную группу; и
В4 представляет собой атом галогена, цианогруппу или C1-С6-алкильную группу (которая может быть полизамещена атомами галогена); при условии, что, когда А3 представляет собой NH2, B2 представляет собой атом галогена или метильную группу;
(Группа I)
атом водорода, C1-С6-алкильная группа (которая может быть полизамещена атомами галогена, цианогруппой), С3-С8-циклоалкильная группа (которая может быть монозамещена C1-С6алкильной группой), С1-С6-алкилтио группа (которая может быть полизамещена атомами галогена, С3-С8-циклоалкильной группой, замещенной атомами галогена, или цианогруппой), C1-С6-алкилсульфинильная группа (которая может быть полизамещена атомами галогена), C1-С6-алкилсульфонильная группа, С2-С6-алкинилтиогруппа;
(Группа II)
-C(=O)OR2 группа, -NR2R3 группа, -N(СOR2)R3 группа и N(СООR2)R3группа;
где R2 представляет собой атом водорода, C1-С6-алкильную группу (которая может быть моно- или полизамещена атомами галогена или цианогруппой), С3-С6-алкинильную группу, C1-С6-моноалкиламиногруппу или C2-C12-диалкиламиногруппу;
R3 представляет собой атом водорода, C1-С6-алкильную группу.
A1 представляет собой C1-С6-алкильную группу (которая может быть полизамещена атомами галогена или цианогруппой), C1-С6-алкилтиогруппу (которая может быть полизамещена атомами галогена) или C1-С6-алкилсульфинильную группу (которая может быть полизамещена атомами галогена);
А3 представляет собой -NR2R3 группу или -N(COR2)R3-группу; каждый из R2 и R3 независимо друг от друга представляют собой атом водорода, C1-С6-алкиламиногруппу, C1-С6-алкильную группу (которая может быть моно- или полизамещена атомами галогена или цианогруппой) или С3-С6-алкинильную группу, при условии, что R2 и R3 не являются одновременно атомами водорода;
B2 представляет собой атом водорода, атом галогена или метильную группу; и
В4 представляет собой цианогруппу или C1-С6-алкильную группу (которая может быть полизамещена атомами галогена).
n представляет собой целое число от 0 до 1;
A1 представляет собой C1-С6-алкильную группу (которая может быть поли-замещена атомами галогена или цианогруппой), C1-С6-алкилтиогруппу (которая может быть полизамещена атомами галогена) или C1-С6-алкилсульфинильную группу (которая может быть полизамещена атомами галогена);
А3 представляет собой аминогруппу;
В2 представляет собой атом галогена или метильную группу; и
B4 представляет собой C1-С6-алкильную группу (которая может быть полизамещена атомами галогена).
А3 представляет собой метиламиногруппу или трифторацетиламиногруппу.

где В2 представляет собой метильную группу, и В4 представляет собой C1-С6-алкильную группу и R представляет собой C1-С6-алкильную группу (которая полизамещена атомами галогена).

Комментарии