Производные триазола, способы их получения, инсектицидное и акарицидное средство - RU2131421C1
Код документа: RU2131421C1
Чертежи


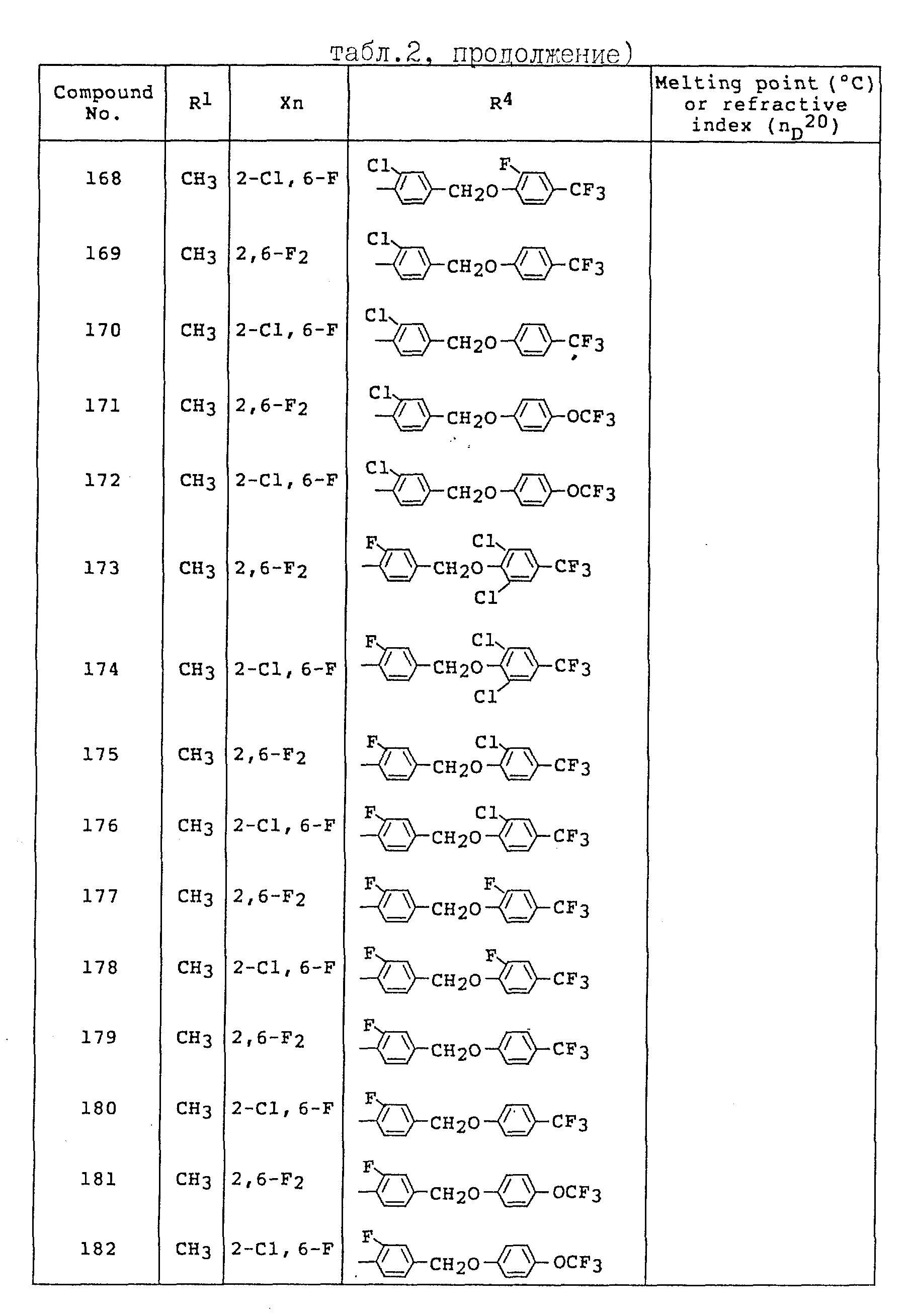
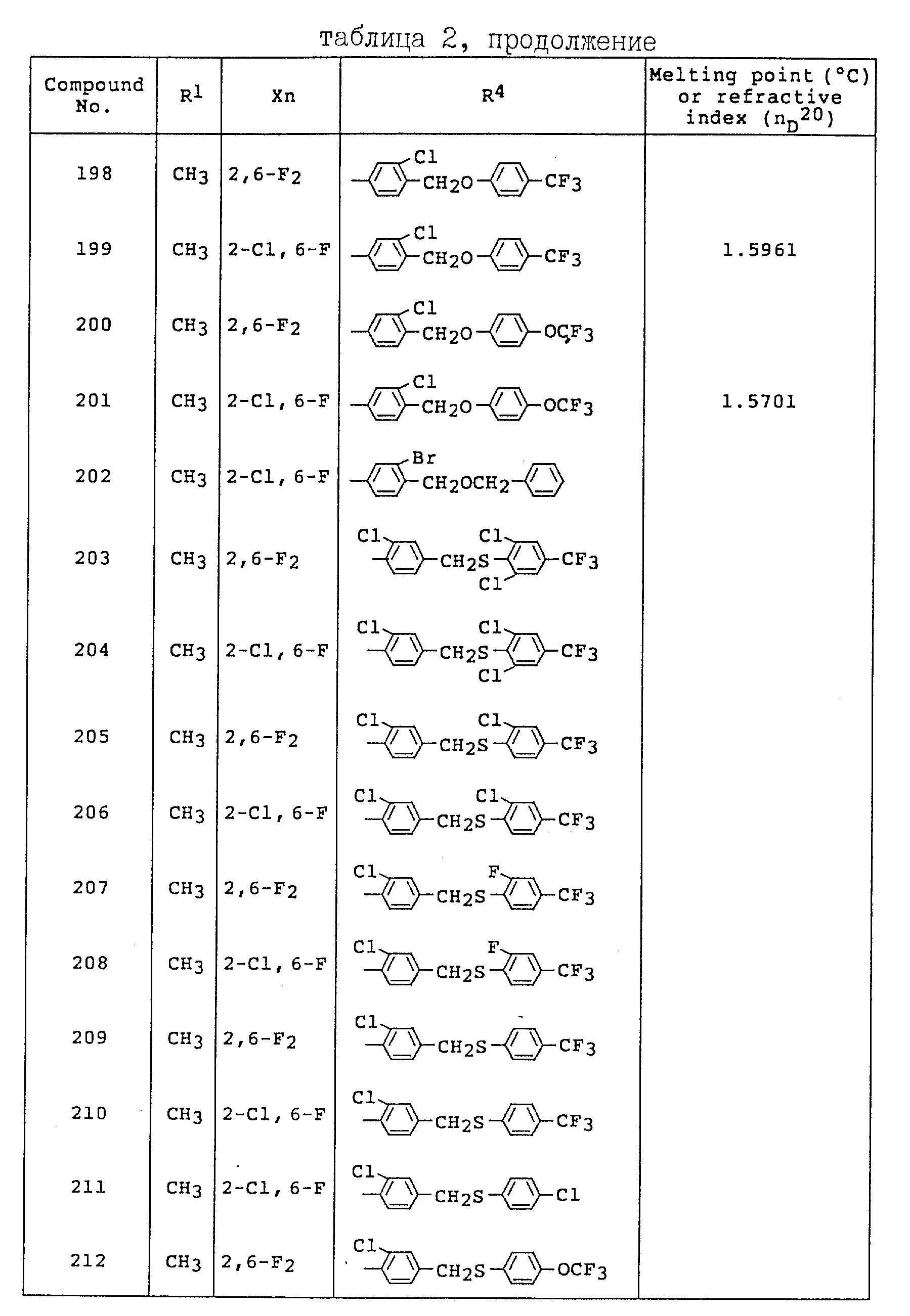
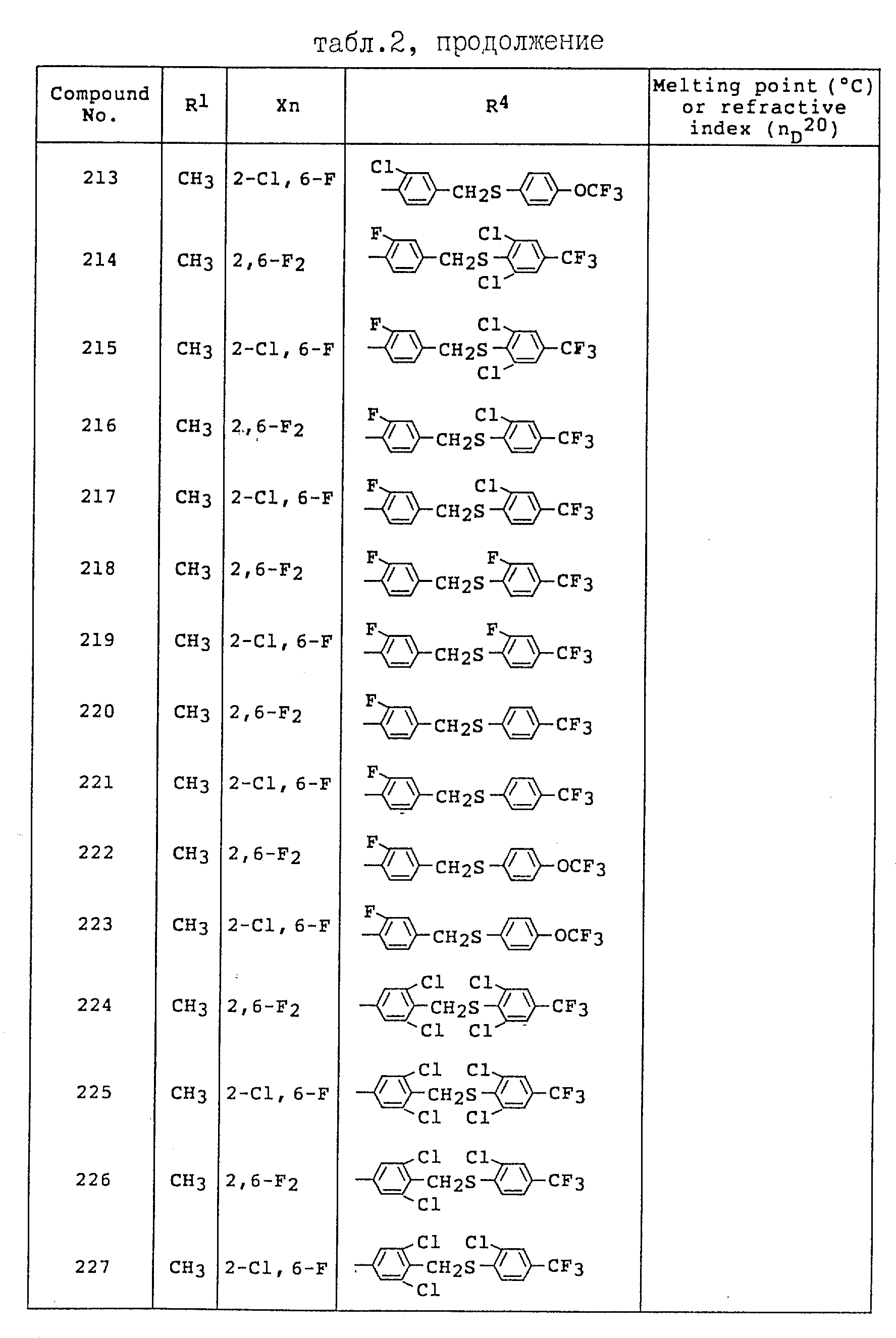
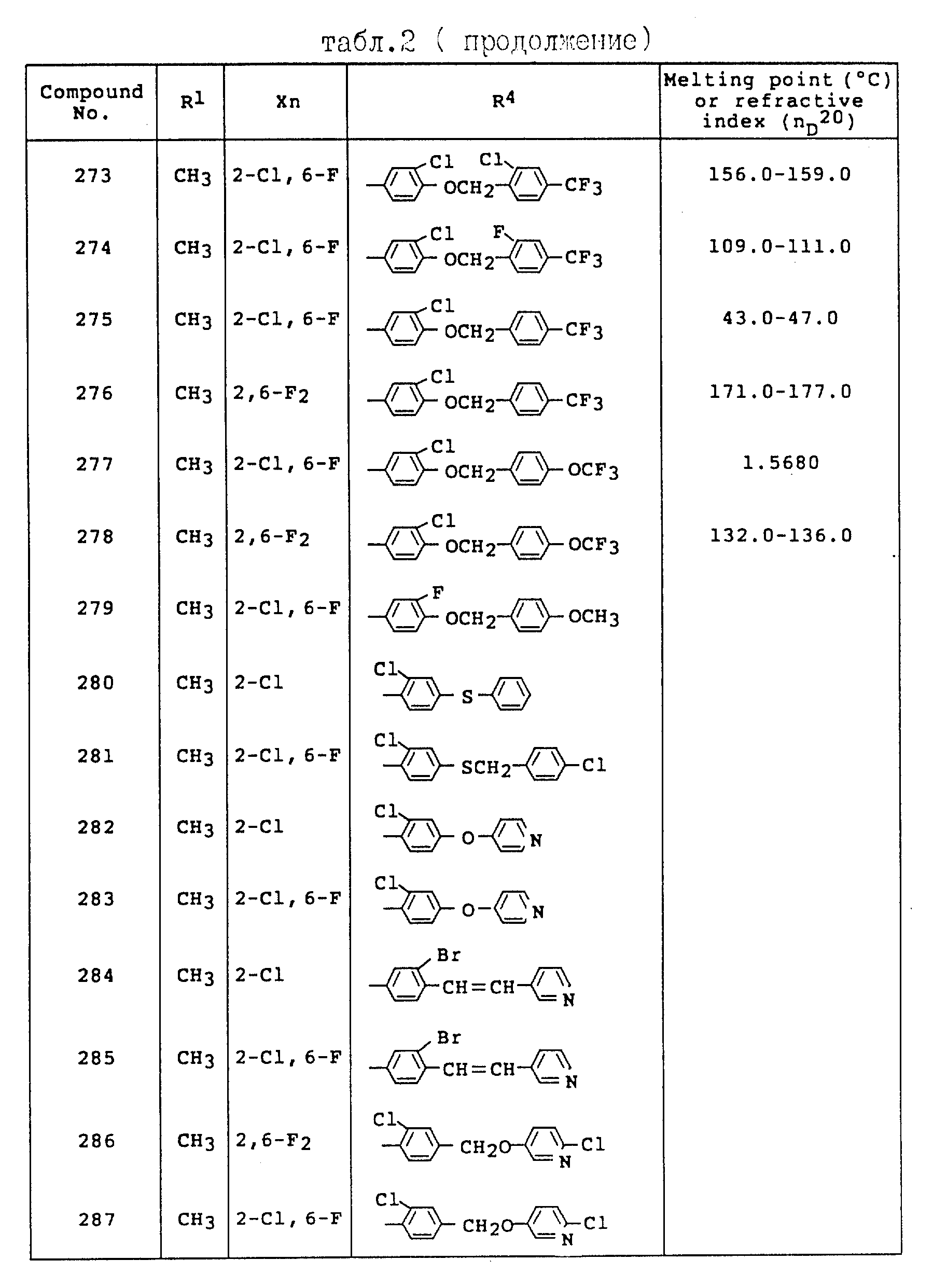

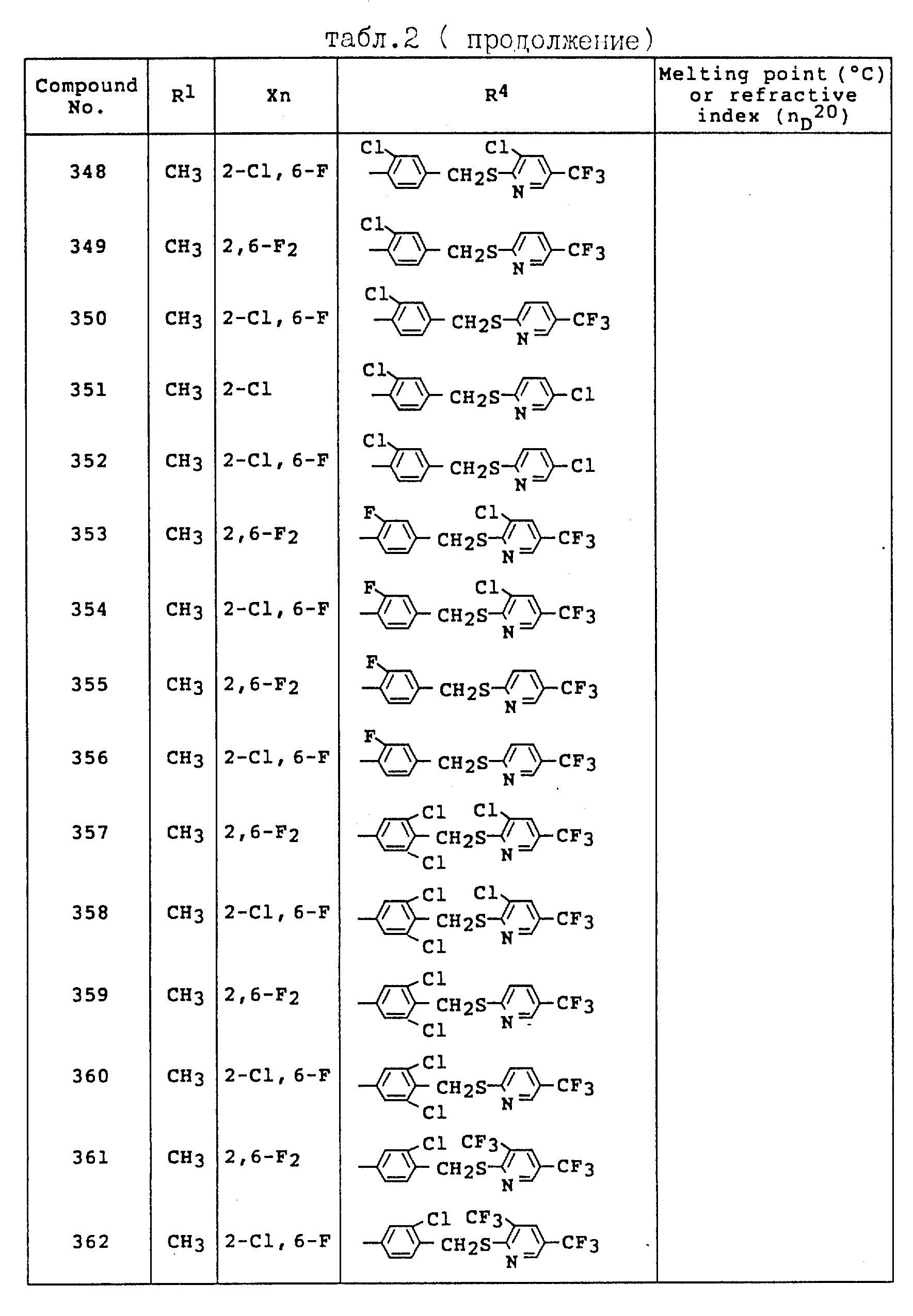
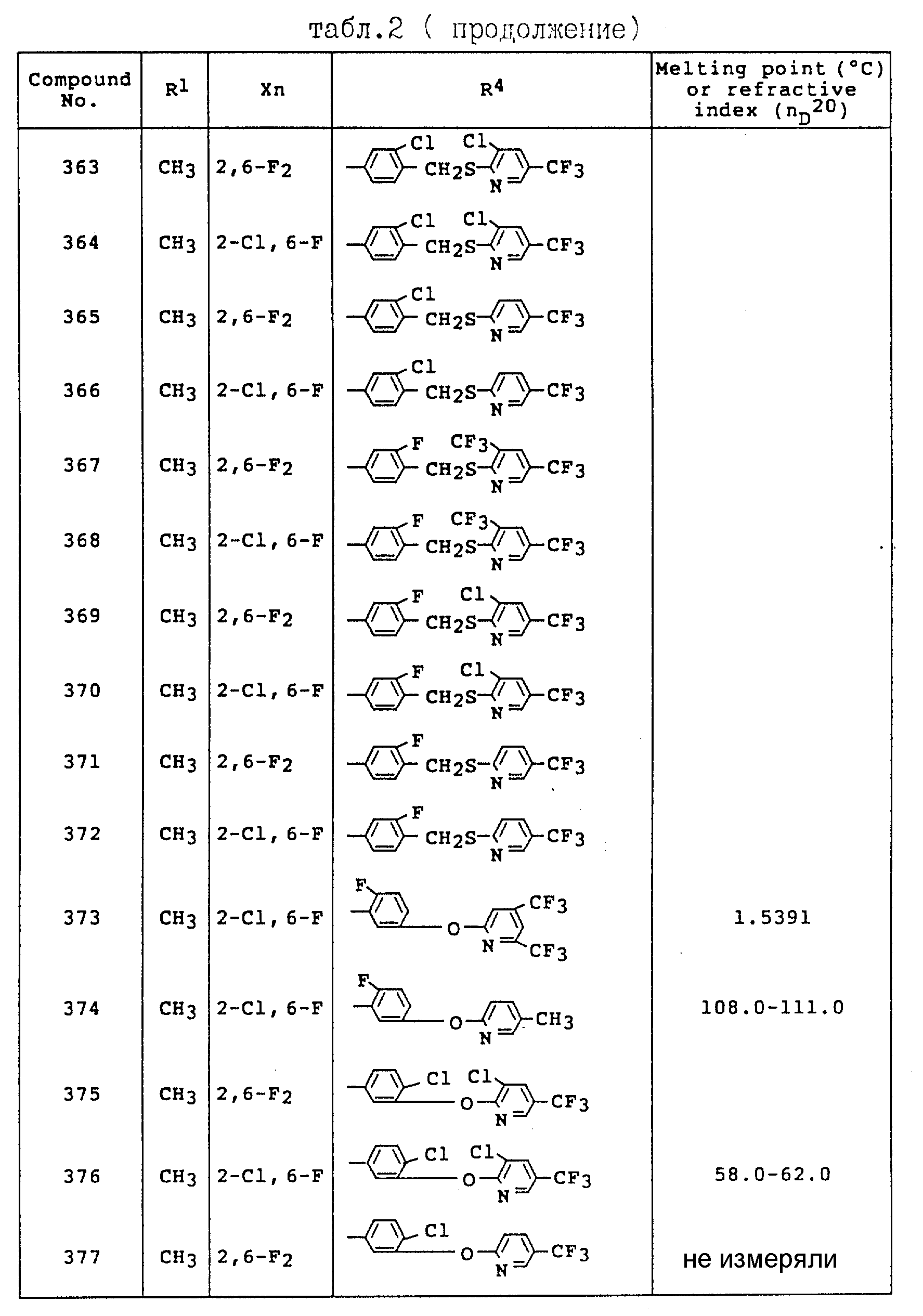
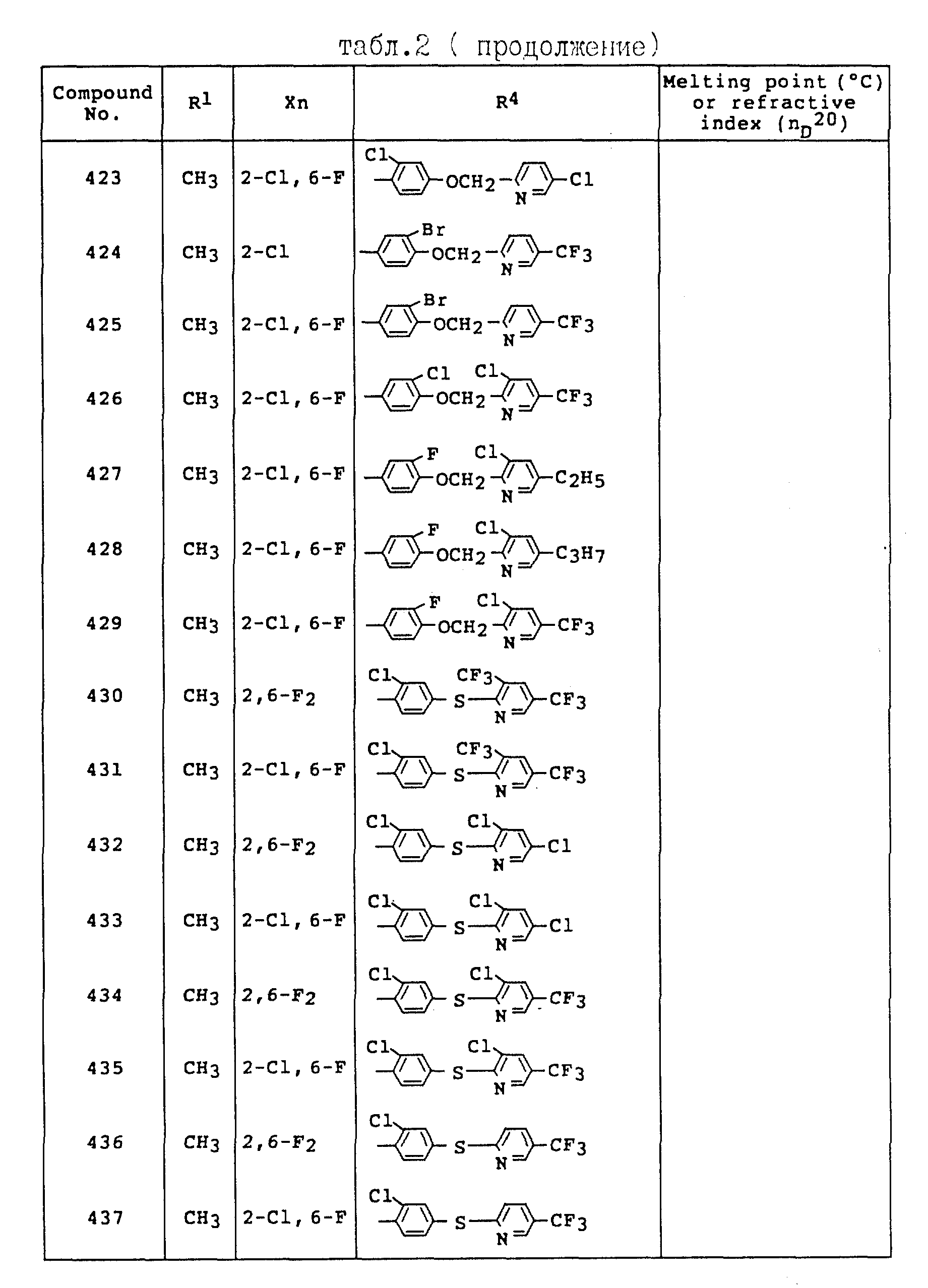


Описание
Изобретение относится к производным триазола, инсектицидам и акарицидам, содержащим такие производные в качестве активного ингредиента и способам их получения.
Уровень техники
В качестве
известных к настоящему времени технических решений, в которых описываются соединения, аналогичные по химической структуре соединению настоящего изобретения можно привести описание
IP-A-56-154464 и
технический отчет РД 278004. В этих документах отмечается, что такие соединения обладают инсектицидной и акарицидной активностями. Однако нельзя считать, что соединения, описанные в
указанных выше
открытом описании и техническом отчете обладают достаточной инсектицидной и акарицидной активностями.
Авторы настоящего изобретения синтезировали различные производные триазола с целью разработки нового и полезного инсектицида и акарицида и провели разнообразные исследования, касающиеся их физиологической активности. В результате было обнаружено, что соединения согласно настоящему изобретению обладают превосходной инсектицидной и акарицидной активностями по отношению к вредным насекомым и клещам по сравнению с соединениями конкретно описанными в описании JP-A-56-154464 и техническом отчете РД 278004. В частности было обнаружено, что такие соединения характеризуются наличием большого числа заместителей в бензольном кольце, замещенном в положении 5 триазольного кольца, и обладают превосходной инсектицидной активностью против таких клещей, как клещик паутинный двупятнистый, паутинный клещик Канзава, клещик красный цитрусовый и т.д.; таких представителей тли, как тля хлопковая и т. п. ; и таких чешуекрылых вредителей, как моль капустная и т.п., и на базе перечисленных фактов было осуществлено настоящее изобретение.
Настоящее изобретение относится к
производному триазола, отвечающему общей формуле (I):
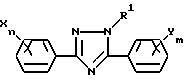
в которой R1 представляет собой алкильную группу, X представляет собой атом водорода, атом галогена, алкильную группу, алкоксигруппу, алкилтиогруппу, нитрогруппу, цианогруппу или трифторметильную группу, n - целое число, равное 1-5, при условии, что в том случае, когда n равно 2 или более, X, необязательно, может иметь одинаковые или различные значения, Y представляет собой атом галогена, нитрогруппу, алкильную группу, алкоксигруппу, алкоксиалкильную группу, алкоксиалкоксигруппу, алкилтиогруппу, алкилсульфинильную группу, алкилсульфонильную группу, алкилтиоалкильную группу, алкилсульфинилалкильную группу, алкилсульфонилалкильную группу, циклоалкильную группу, циклоалкилалкильную группу, циклоалкилалкенильную группу, циклоалкилалкинильную группу, галоалкильную группу, галоалкоксигруппу, триалкилсилилалкильную группу, триалкилсилилалкоксигруппу, алкенильную группу, алкенилоксигруппу, алкинильную группу, алкинилоксигруппу или группу, представленную общей формулой:
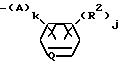
в которой A представляет собой атом кислорода, атом серы, низшую алкенильную группу, низшую алкиленоксигруппу, окси низшую алкиленовую группу, низшую алкиленокси низшую алкиленовую группу, низшую алкилентиогруппу, тио низшую алкиленовую группу, виниленовую группу или этиниленовую группу, k равно 0 или 1, O представляет собой метиновую группу или атом азота, R2 представляет собой атом водорода, атом галогена, алкильную группу, алкоксигруппу, трифторметильную группу или трифторметоксигруппу, j представляет собой целое число в интервале 1-5, причем, если j равно 2 или более, то R2, необязательно, может иметь одинаковые или различные значения, m представляет собой целое число в интервале 2-5, а Y, необязательно, может иметь одинаковые или различные значения, а также к инсектицидам и акарицидам, содержащим указанное производное в качестве активного ингредиента и способам их получения.
В настоящем описании под термином "алкильная группа" подразумевается алкильная группа нормального или разветвленного строения, содержащая 1-30 углеродных атомов, включающая, например, метильную группу, этильную группу, н-пропильную группу, изопропильную группу, н-бутильную группу, изобутильную группу, втор.-бутильную группу, трет.-бутильную группу, н-пентильную группу, изоамиловую группу, неопентильную группу, н-гексильную группу, изогексильную группу, 3,3-диметилбутильную группу, н-гептильную группу, 5-метилгексильную группу, 4-метилгексильную группу, 3-метилгексильную группу, 4,4-диметилпентильную группу, н-октильную группу, 6-метилгептильную группу, н-нонильную группу, 7-метилоктильную группу, н-децильную группу, 8-метилнонильную группу, н-ундецильную группу, 9-метилдецильную группу, н-додецильную группу, 10-метилундецильную группу, н-тридецильную группу, 11-метилдодецильную группу, н-тетрадецильную группу, 12-метилтридецильную группу, н-пентадецильную группу, 13-метил-тетрадецильную группу, н-гексадецильную группу, н-гептадецильную группу, н-октадецильную группу, н-нонадецильную группу, н-эйкозильную группу и т.д.
Алкокси группа, алкилтиогруппа, алкилсульфинильная группа и алкилсульфонильная группа представляют собой (алкил)-O-группу, (алкил)-S-группу, (алкил)-SO-группу и (алкил)-SP2-группу, в которых каждый алкильный фрагмент имеет те же значения, что указаны выше. Алкилтиоалкильная группа, алкилсульфинилалкильная группа и алкилсульфонилалкильная группа представляет собой (алкил)-S-(алкил)- группу, (алкил)-SO-(алкил)-группу и (алкил)-SO2-(алкил)-группу, в которых каждый из алкильных фрагментов имеет те же значения, что указаны выше. Под атомом галогена подразумеваются атомы фтора, хлора, брома и иода.
Термин "алкенильная группа" обозначает алкенильную группу нормального или разветвленного строения, содержащую 2-20 углеродных атомов и охватывает, например, винильную группу, пропенильную группу, изопропенильную группу, бутенильную группу, пентенильную группу, гексинильную группу, нептенильную группу, октенильную группу, 3-метил-1-бутенильную группу, 4-метил-1-пентинильную группу и т.п.
Термин "алкинильная группа" обозначает алкинильную группу нормального или разветвленного строения, содержащую 2-20 углеродных атомов и охватывает, например, этинильную группу, пропинильную группу, бутинильную группу, пентинильную группу, гексинильную группу, 3,3-диметил-1-бутинильную группу, 4-метил-пентинильную группу, 3-метил-1-пентинильную группу, 5-метил-1-гексинильную группу, 4-метил-1-гексинильную группу, 3-метил-1-гексинильную группу, гептинильную группу, октинильную группу, нонинильную группу, децинильную группу, ундецинильную группу, додецинильную группу, тридецинильную группу, тетрадецинильную группу, пентадецинильную группу, гексадецинильную группу и т.п.
Термин "циклоалкильная группа", обозначает циклоалкильную группу, содержащую 3-12 углеродных атомов и охватывает, например, циклопропильную группу, циклобутильную группу, циклопентильную группу, циклогексильную группу, циклогептильную группу, циклооктильную группу и т.п. Термин "циклоалкилальная группа" обозначает циклоалкилалкильную группу, содержащую 6-12 углеродных атомов и охватывает, например, циклопентилметильную группу, циклогексилметильную группу, циклопентилэтильную группу, циклогексилэтильную группу, циклопентилпропильную группу, циклогексилпропильную группу, циклогесилпентильную группу и т.п.
Термин "циклоалкилалкокси группа" обозначает (циклоалкилалкил)-O-группу, в которой циклоалкилалкильный фрагмент имеет указанные выше значения. Термин "циклоалкилалкенильная группа" обозначает циклоалкилалкенильную группу, содержащую 5-12 углеродных атомов, и охватывает, например, циклопентилвинильную группу, циклогексилвинильную группу, 3-циклопентил-1-пропенильную группу, 3-циклогексил-1-пропенильную группу, 5-циклогексил-1-пентинильную группу и т.п. Термин "циклоалкилалкинильная группа" обозначает циклоалкилалкинильную группу, содержащую 5-12 углеродных атомов и охватывает, например, циклопентилэтинильную группу, циклогексилэтинильную группу, 3-циклопентил-1-пропинильную группу, 3-циклогексил-1-пропинильную группу и т.п.
Термин "галоалкильная группа" обозначает алкильную группу замещенную атомом галогена и охватывает, например, трифторметильную группу, пентафторэтильную группу и т.п. Галоалкоксигруппа представляет собой (галоалкил)-O-группу, в которой галоалкильный фрагмент имеет те же значения, что указаны выше.
Термин "триалкилсилилалкильная группа" относится, например, к триметилсилилметильной группе, диметилэтилсилилметильной группе, бутилдиметилсилилметильной группе и т.п. Триалкилсилилалкокси группа представляет собой (триалкилсилилалкил)-O-группу, в которой триалкилсилилалкильный фрагмент имеет те же значения, что указаны выше.
Термин "низшая алкиленовая группа" охватывает, например, метиленовую группу, метилметиленовую группу, триметиленовую группу, 1-метилэтиленовую группу, диметилметиленовую группу, тетраметиленовую группу, 1-метилтриметиленовую группу, 2-метилтриметиленовую группу и т.п. Низшая алкиленокси группа представляет собой (низший алкилен)-O-группу, в которой низший алкиленовый фрагмент имеет те же значения, что указаны выше. Окси низшая алкиленовая группа представляет собой -O-(низший алкилен)-группу, в которой низший алкиленовый фрагмент имеет те же значения, что указаны выше.
Низший алкиленокси низшая алкиленовая группа представляет собой (низший алкилен)-O-(низшую алкиленовую)-группу, в которой низший алкиленовый фрагмент имеет те же значения, что указаны выше. Низшая алкилентио группа представляет собой (низшую алкиленовую)-S-группу, в которой низший алкиленовый фрагмент имеет те же значения, что указаны выше. Тио низшая алкиленовая группа представляет собой - S-(низший алкилен)-группу, в которой низший алкиленовый фрагмент имеет те же значения, что указаны выше.
В качестве группы предпочтительных соединений, отвечающих общей формуле /I/, можно отметить соединения, в которых R1 представляет собой
алкильную группу
нормального или изостроения, содержащую 1-6 углеродных атомов, предпочтительно, метильную группу, X представляет собой атом водорода, атом галогена, алкильную группу нормального или
разветвленного
строения, содержащую 1-4 углеродных атомов, нитрогруппу, цианогруппу или трифторметильную группу, n представляет собой целое число в интервале 1-3, причем в том случае когда n равно 2
или 3, X,
необязательно, может иметь одинаковые или различные значения, Y представляет собой атом галогена, нитрогруппу, алкильную группу нормального или разветвленного строения, содержащую 1-20
углеродных
атомов, алкоксигруппу нормального или разветвленного строения, содержащую 1-20 углеродных атомов, циклоалкильную группу, содержащую 3-12 углеродных атомов, циклоалкилалкильную группу,
содержащую 6-12
углеродных атомов, циклоалкилалкокси группу, содержащую 3-12 углеродных атомов, алкилтио группу нормального или изо-строения содержащую 1-20 углеродных атомов, алкилсульфинильную
группу,
алкилсульфонильную группу, алкинильную группу нормального или разветвленного строения, содержащую 3-16 углеродных атомов, циклоалкилалкинильную группу, содержащую 5-12 углеродных атомов,
три(алкил)силилалкильную группу, три(алкил)силилалкокси группу или группу формулы:
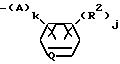
(в которой A представляет собой атом кислорода, атом серы, низшую алкиленовую группу, низшую алкиленокси группу, окси низшую алкиленовую группу или низшую алкиленокси низшую алкиленовую группу, k равно 0 или 1, Q представляет собой метиновую группу или атом азота, R2 представляет собой атом водорода; атом галогена, алкильную группу, алкоксигруппу, трифторметильную группу или трифторметокси группу, j представляет собой целое число в интервале 1-5, причем если j имеет значение, равное 2 или более, то R2, необязательно, имеет одинаковые или различные значения), m представляет собой целое число, имеющее значение в интервале 2-5, а Y, необязательно, может иметь одинаковые или различные значения.
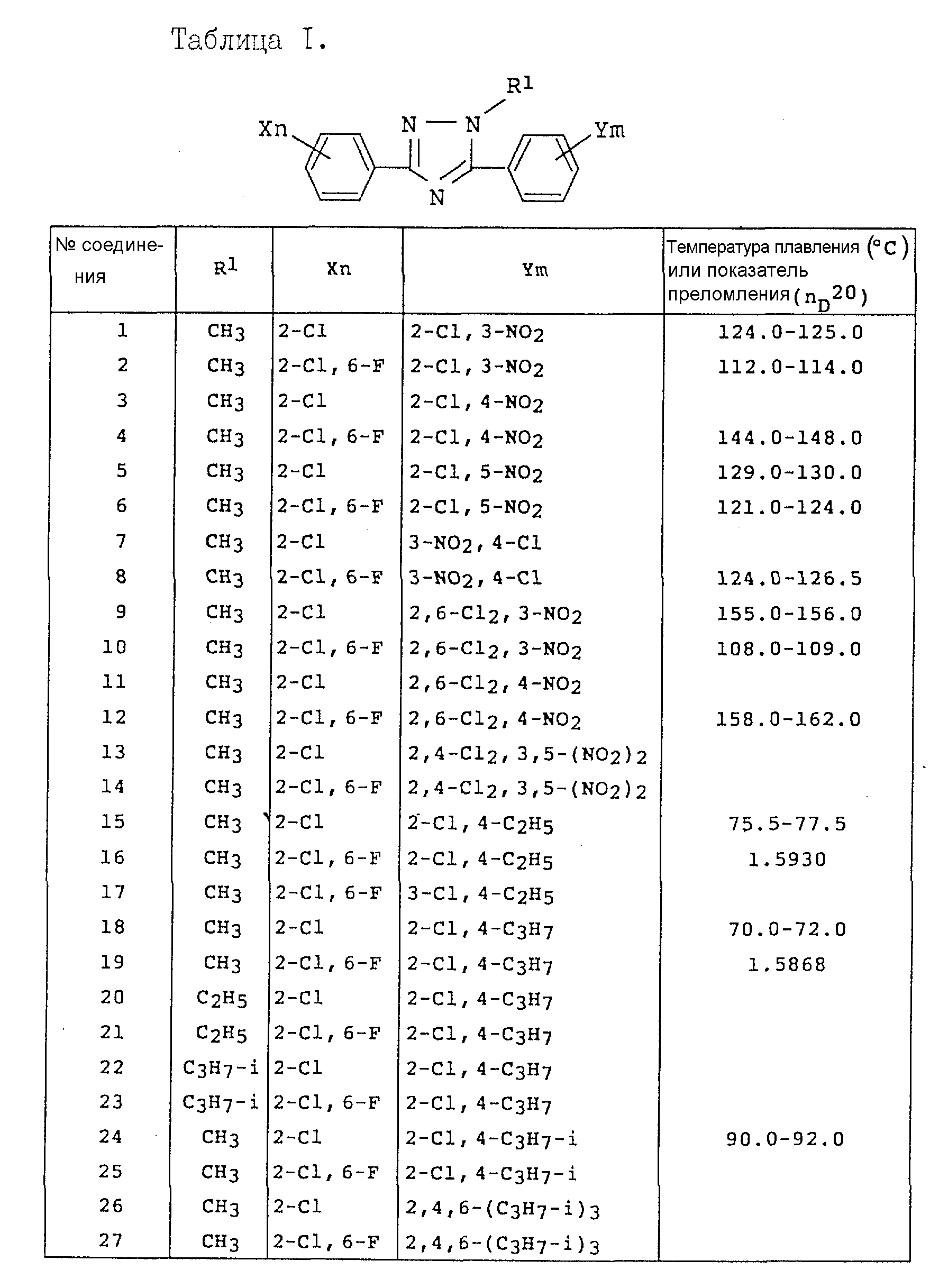
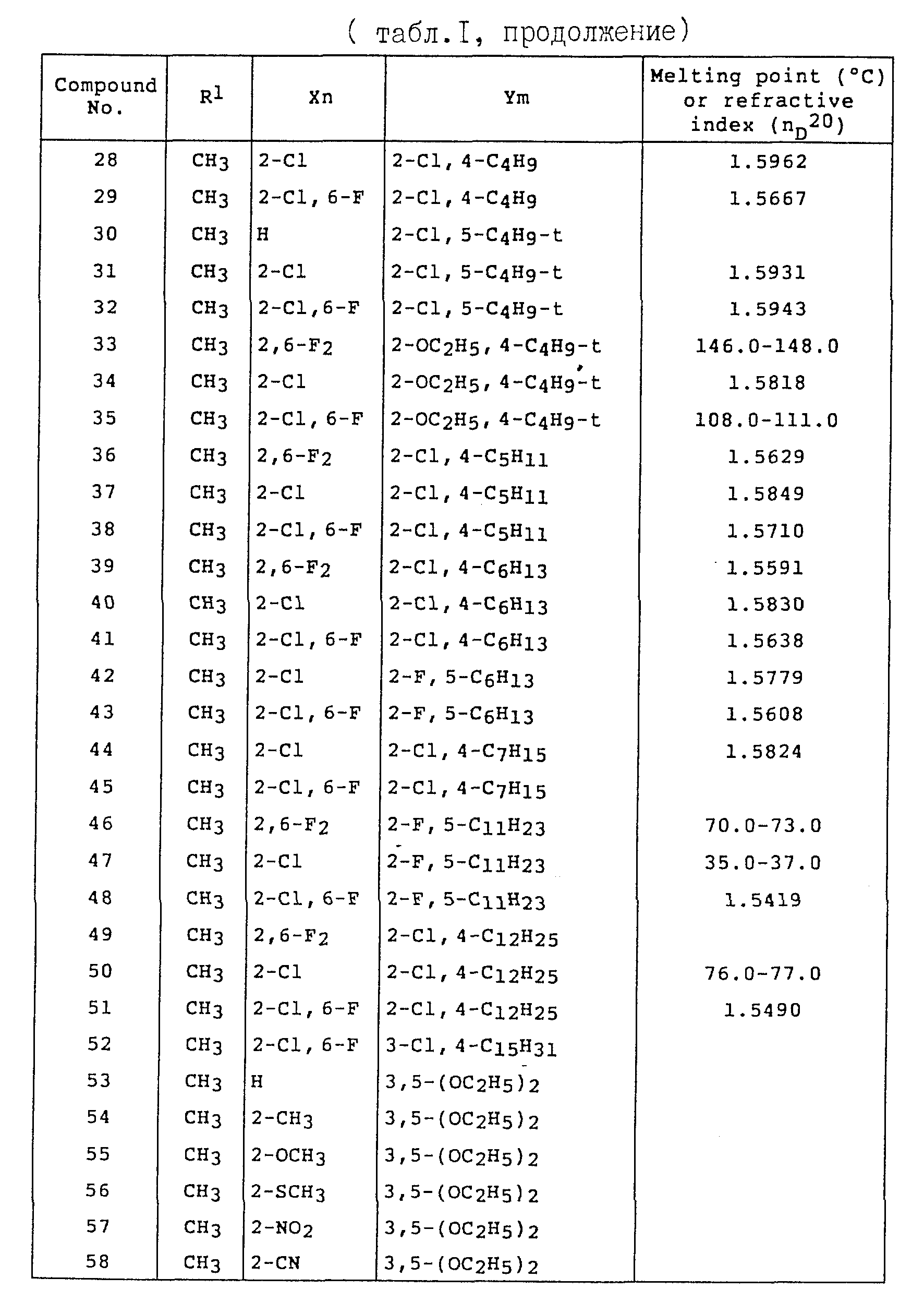
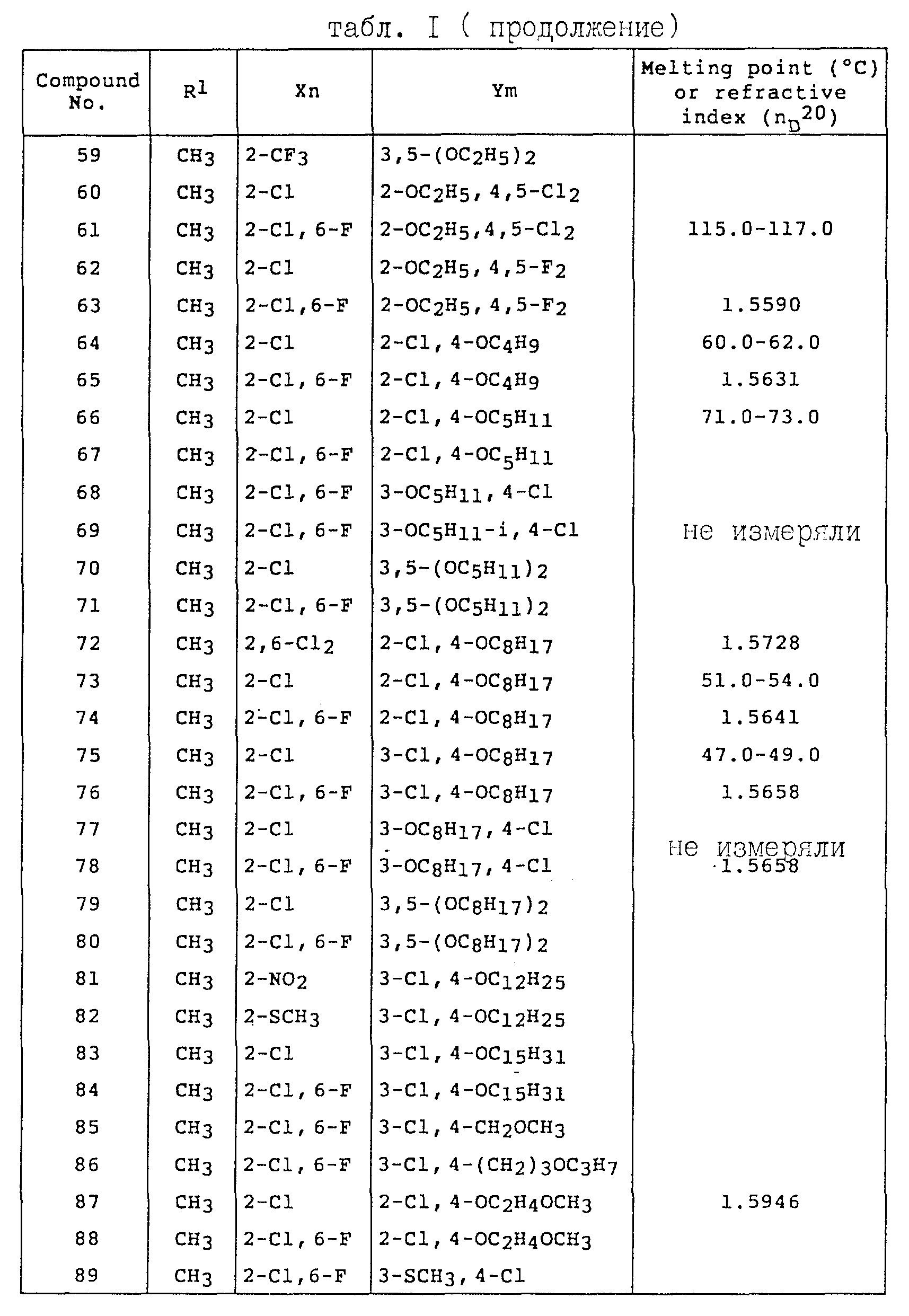
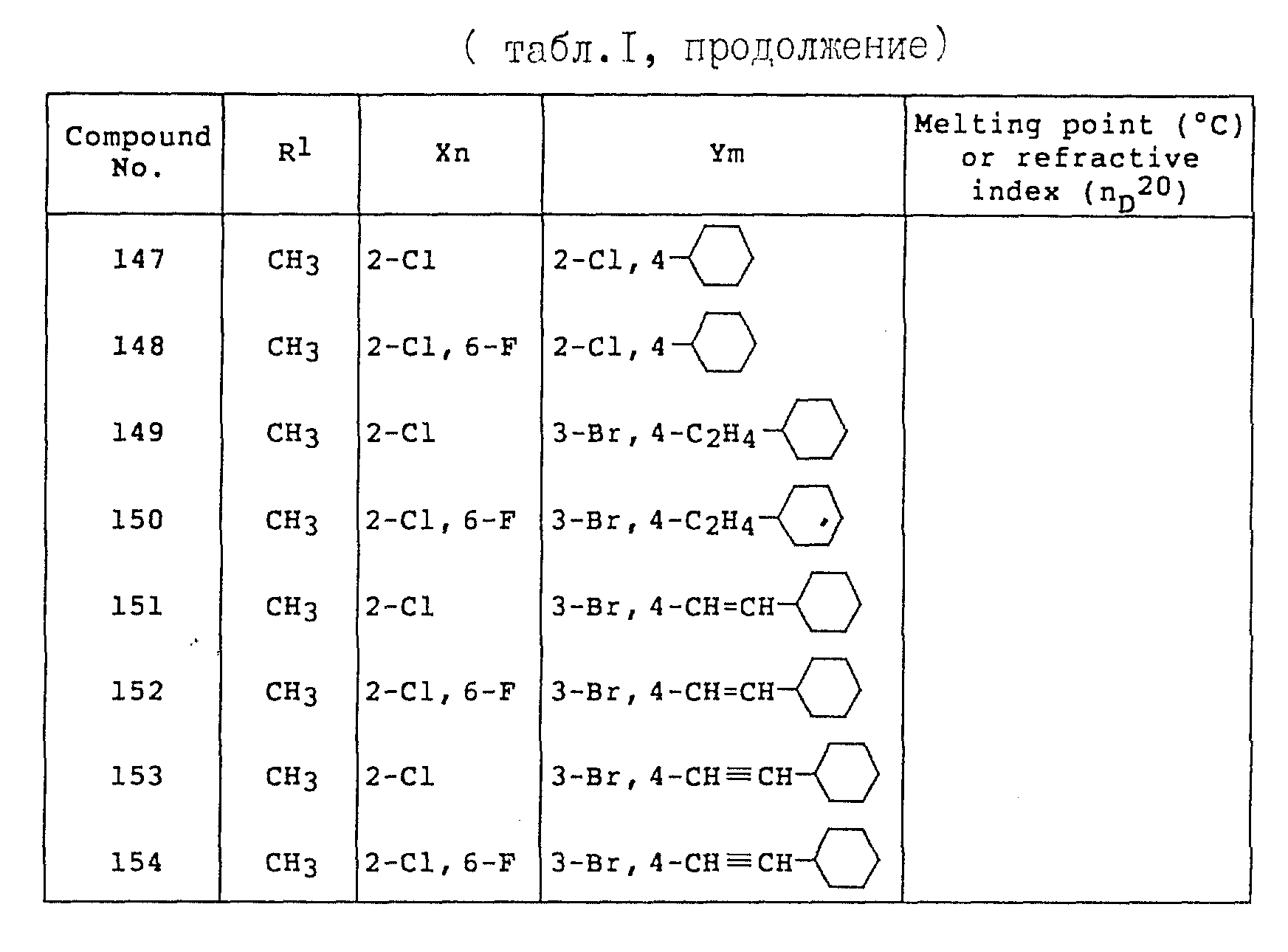
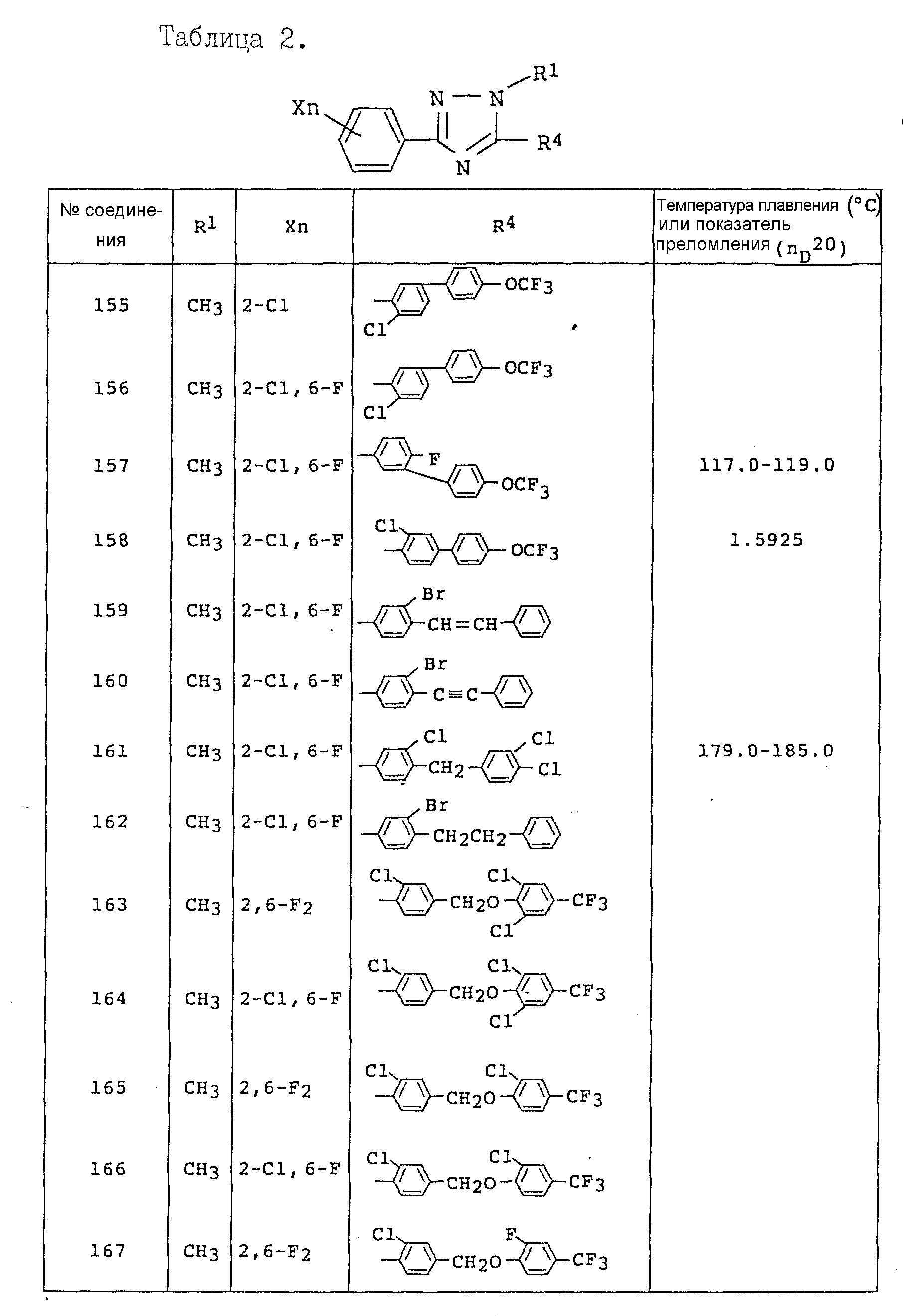
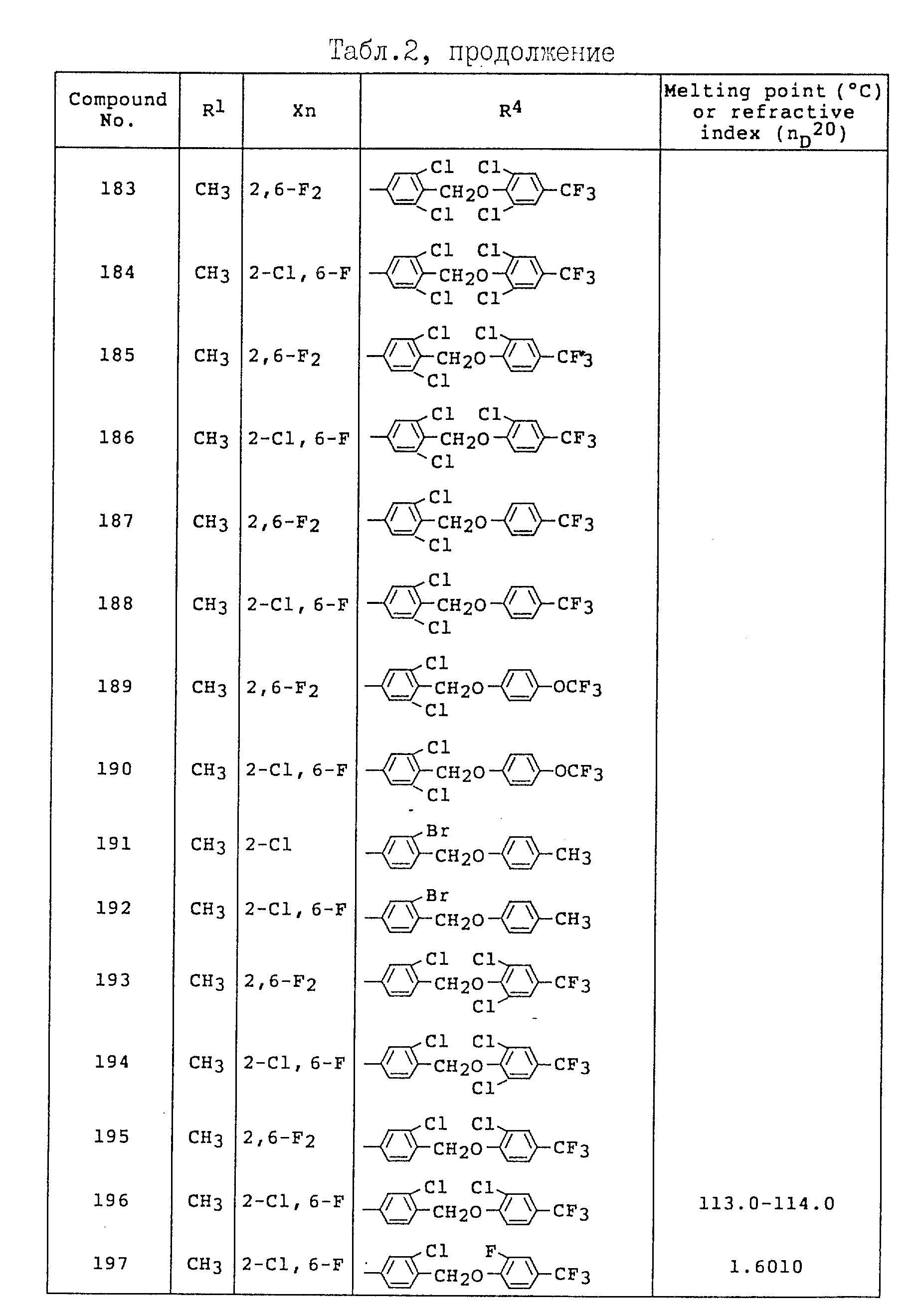
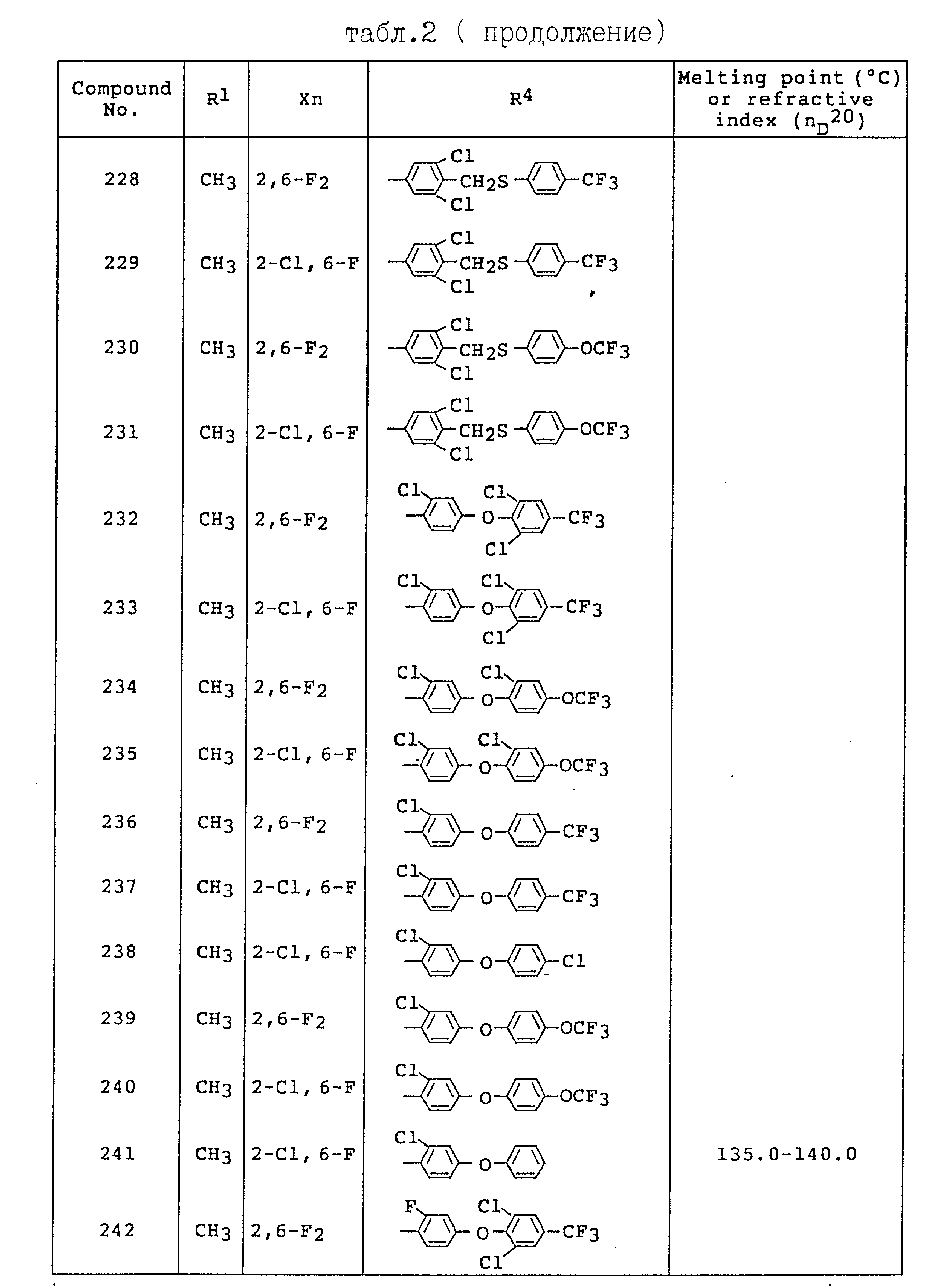
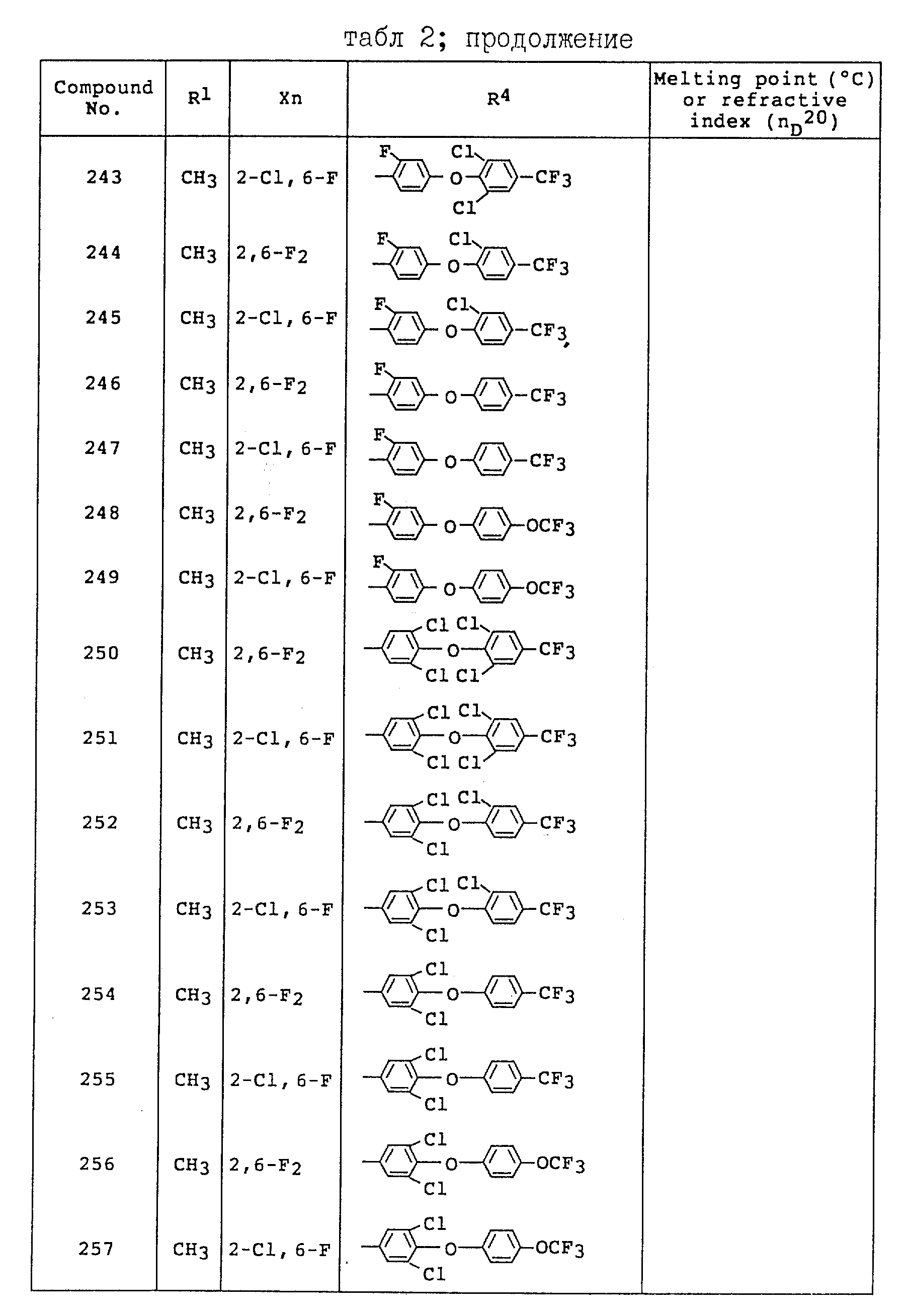
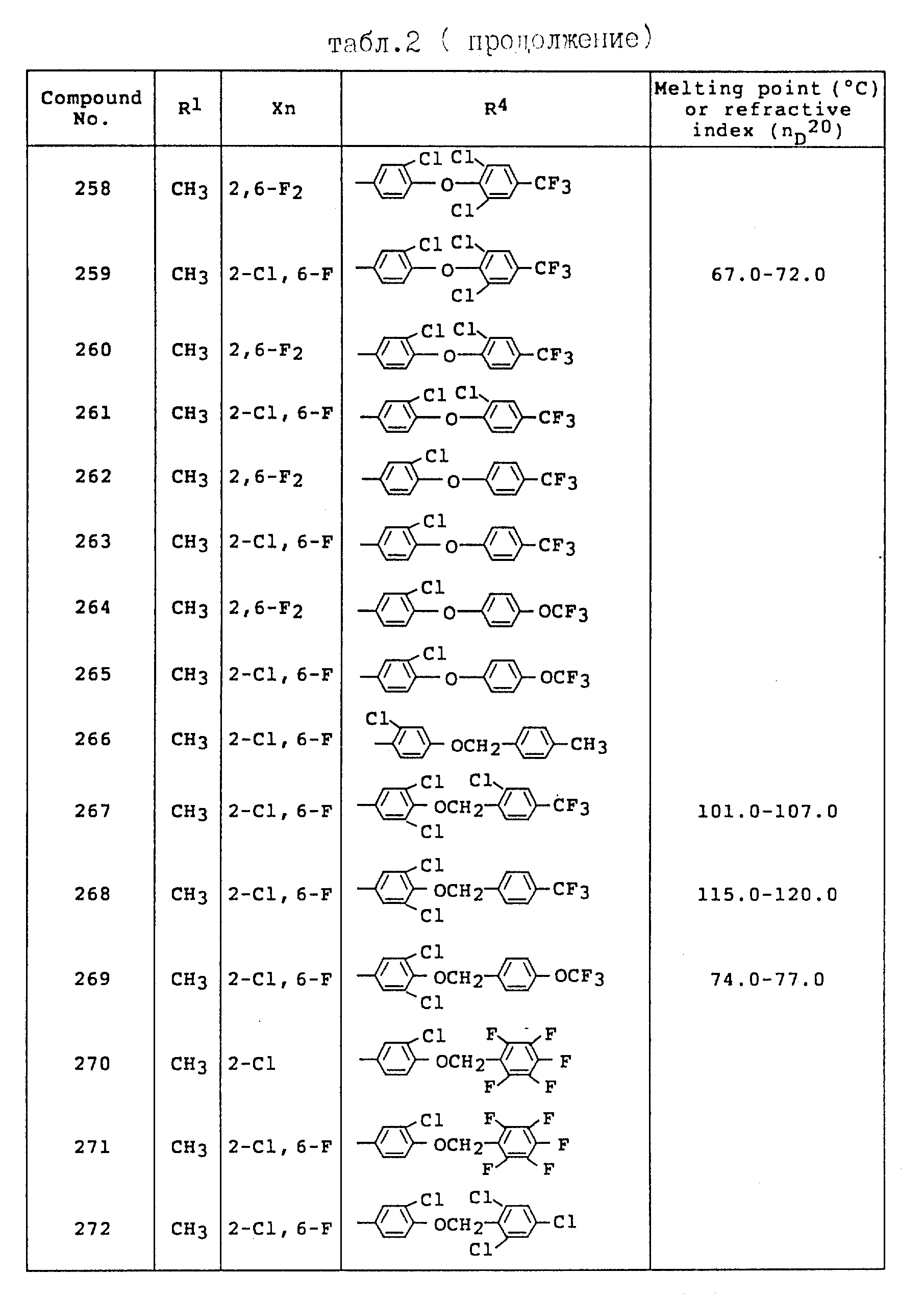
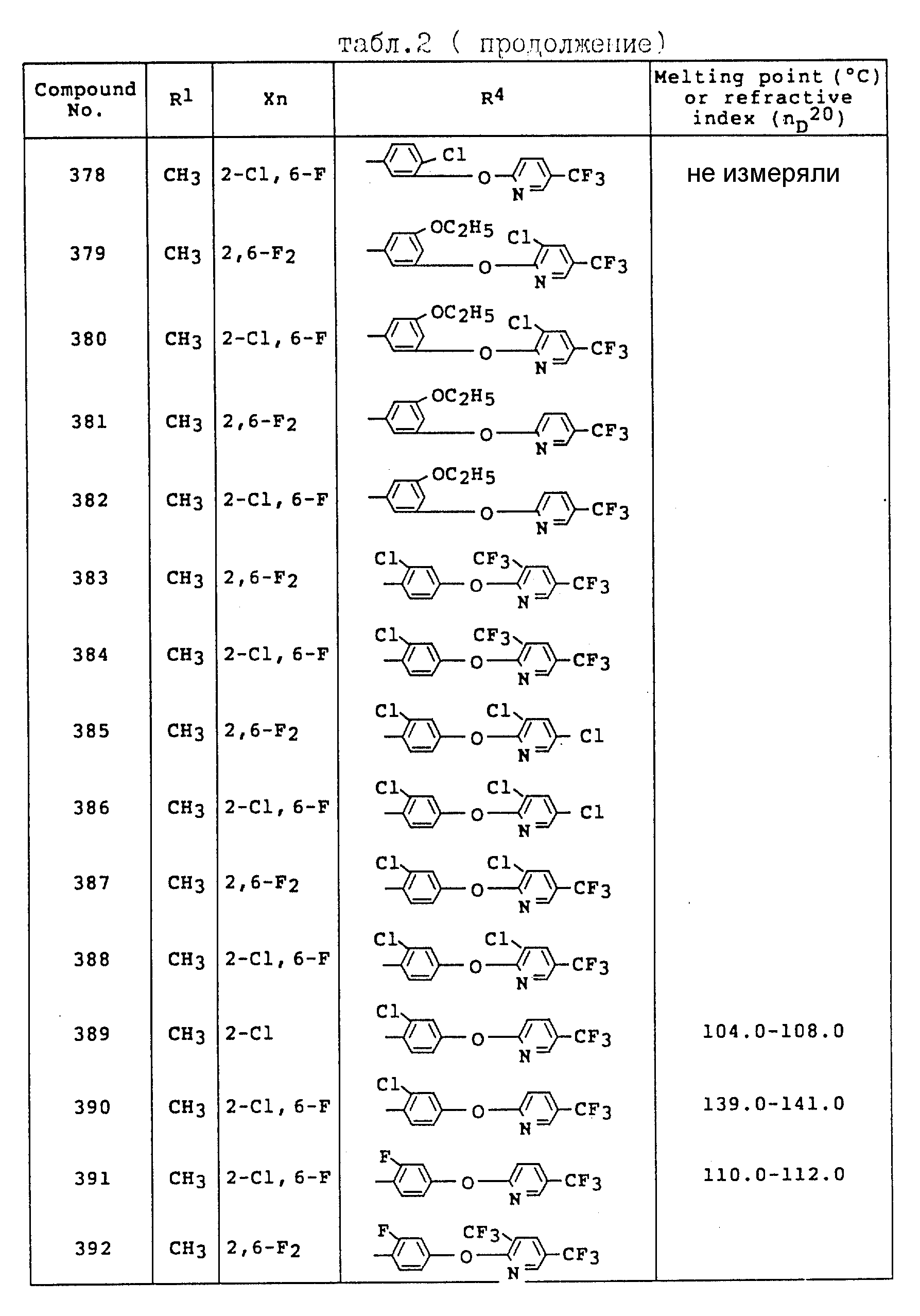
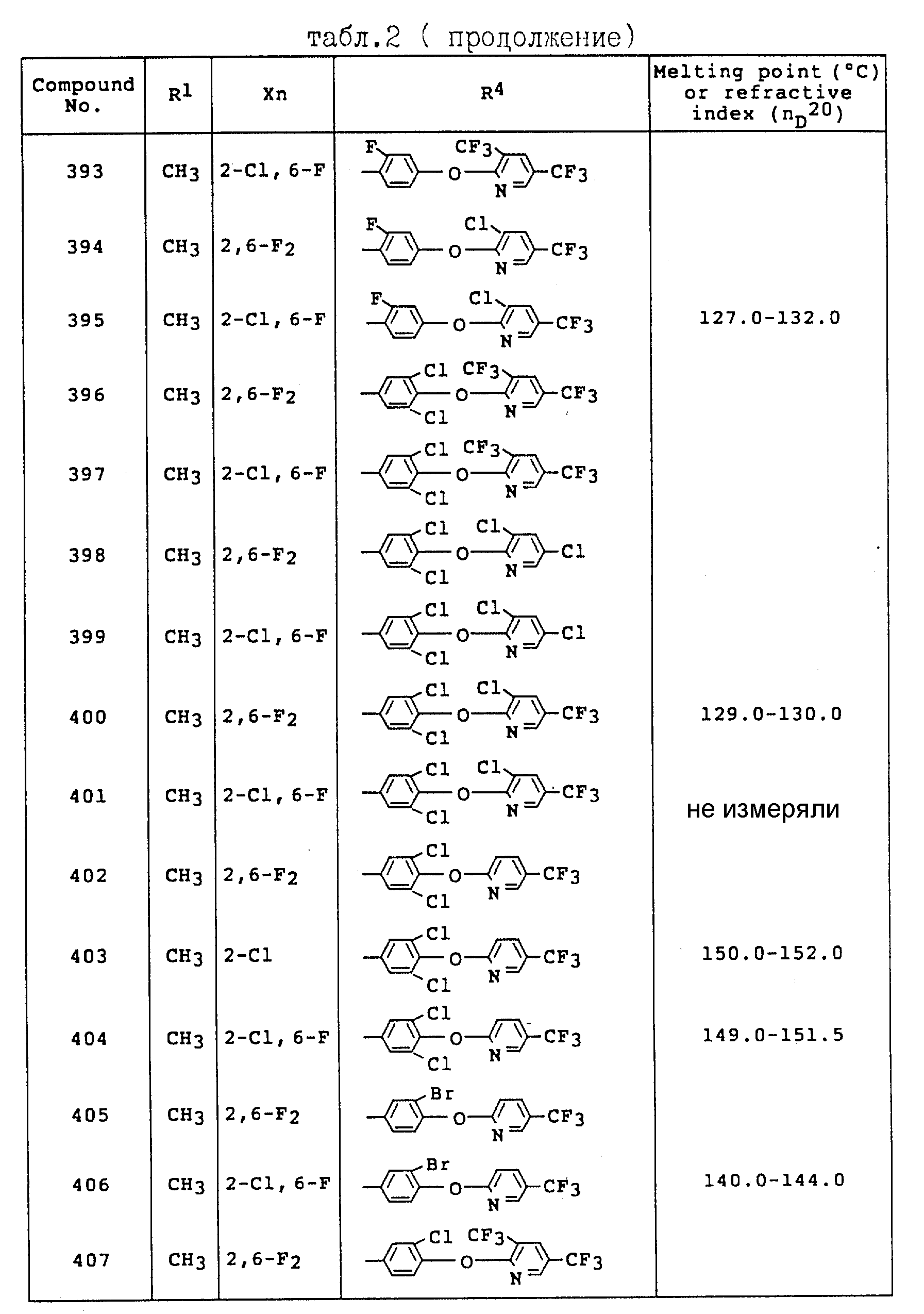
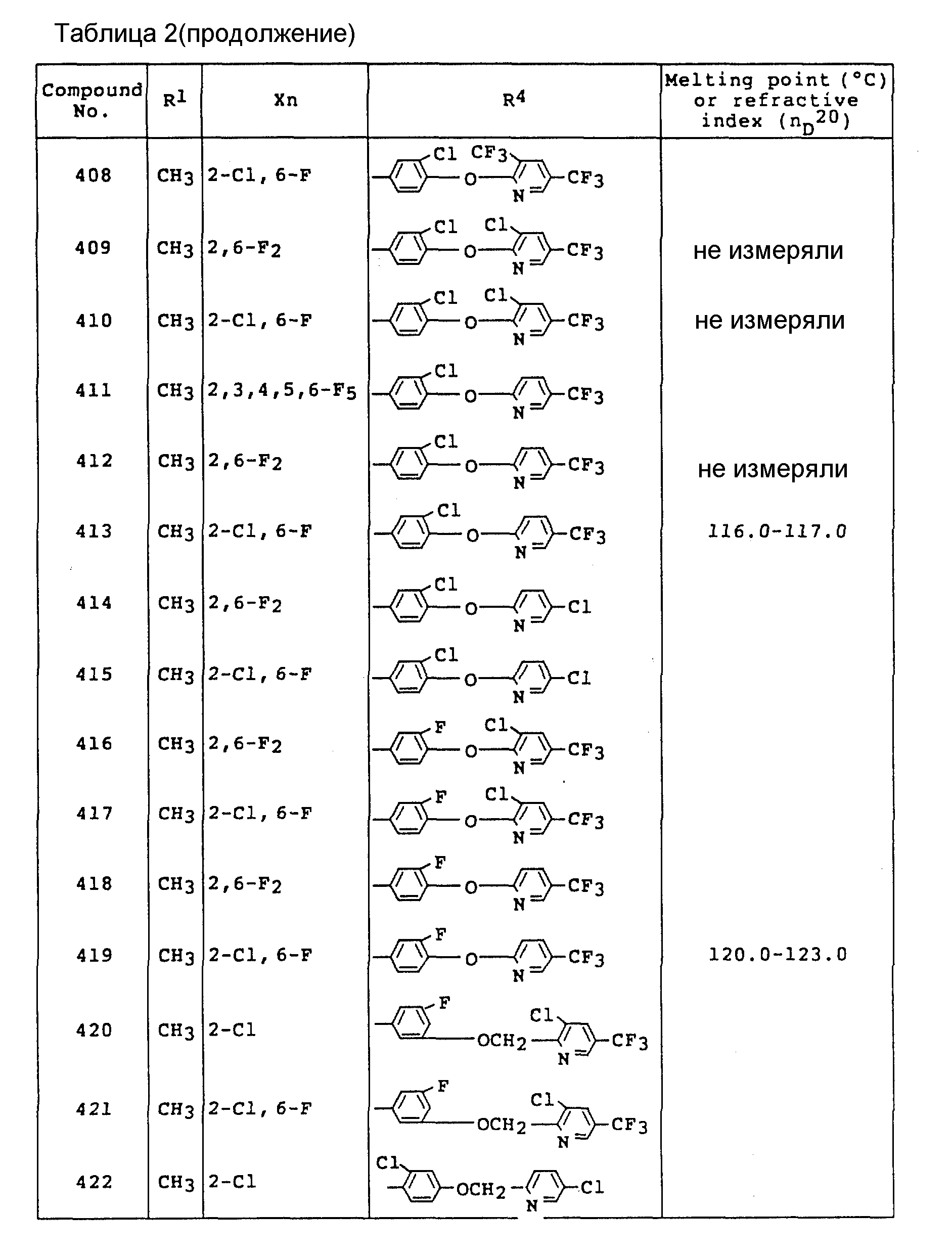
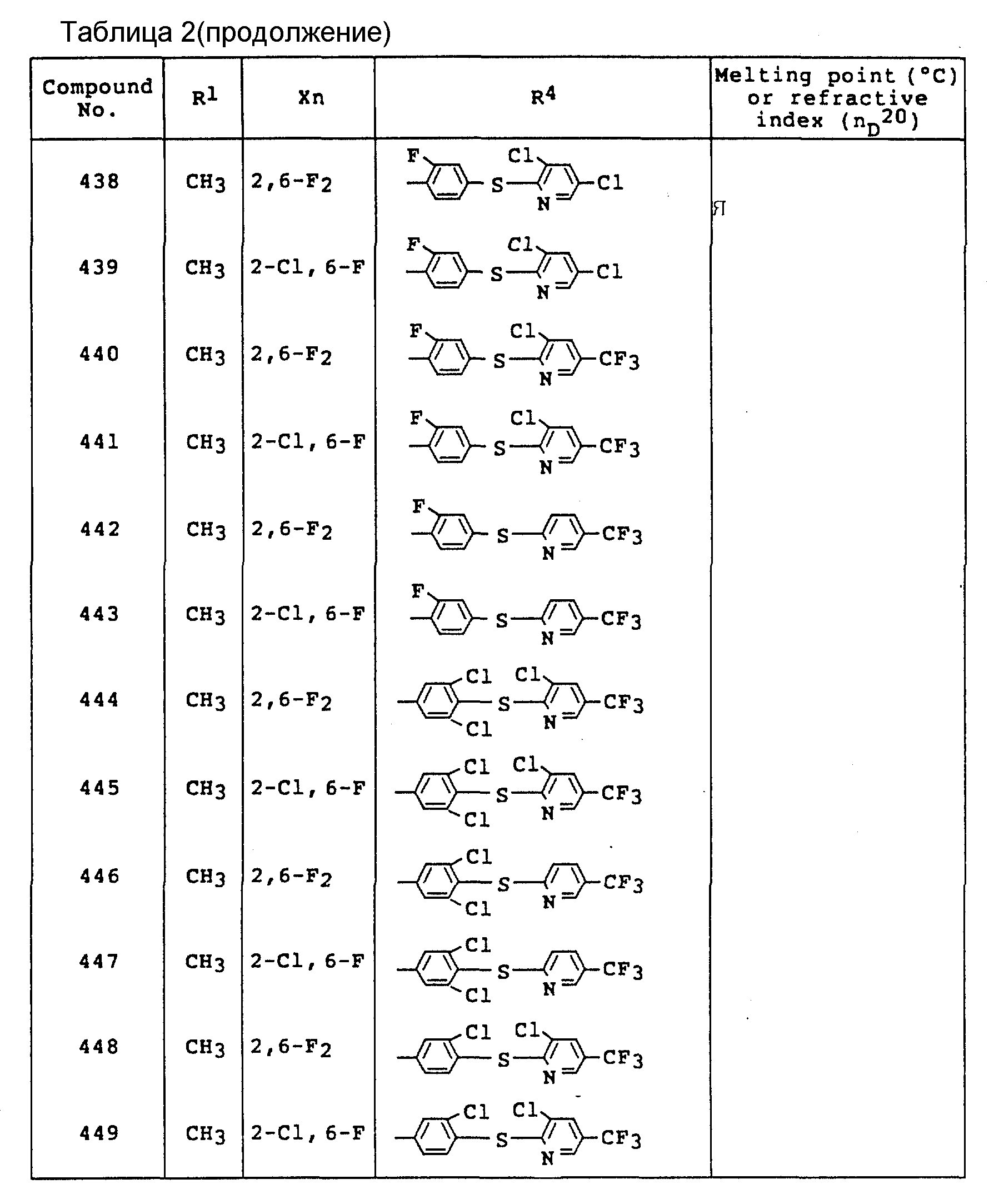
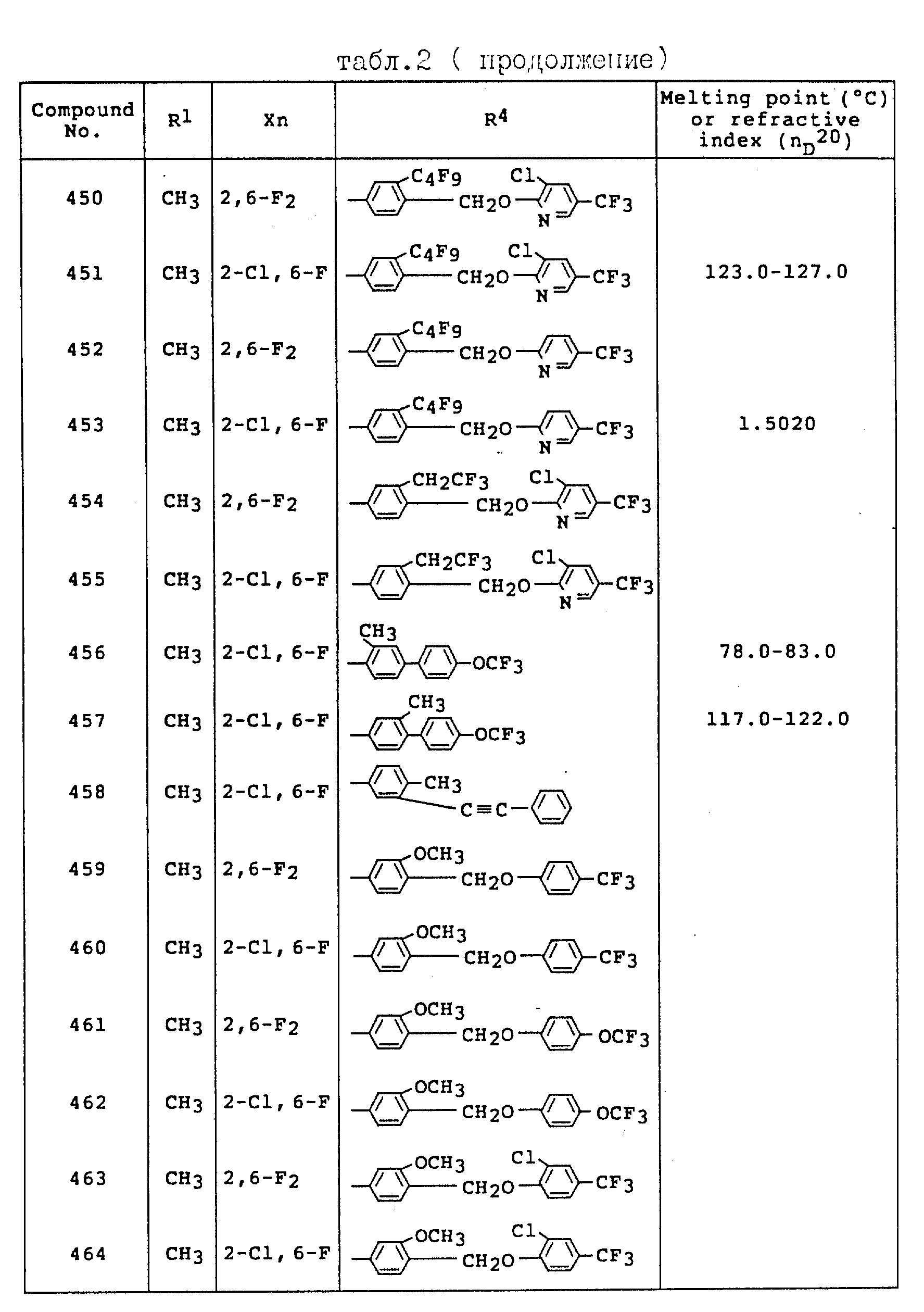
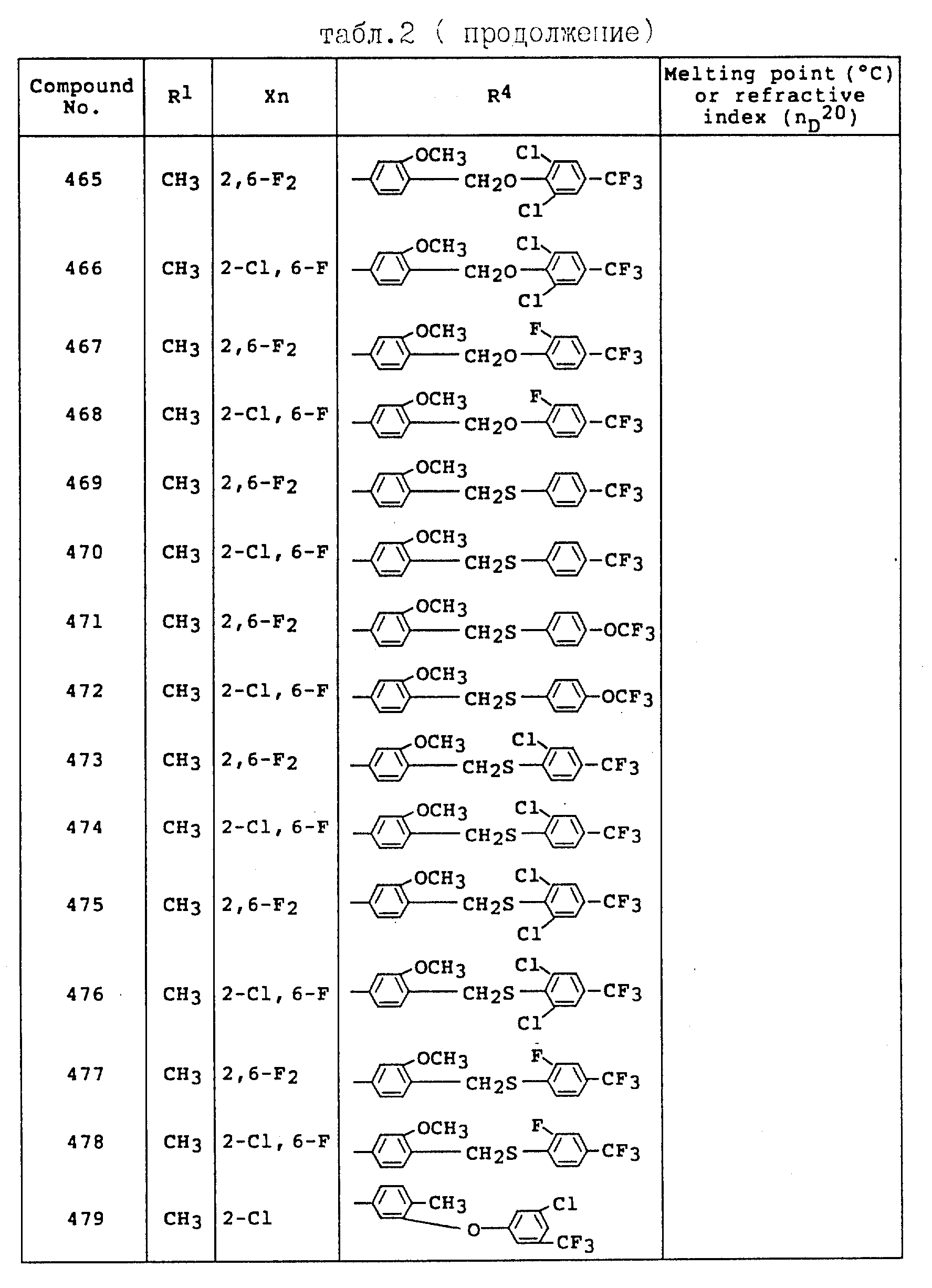
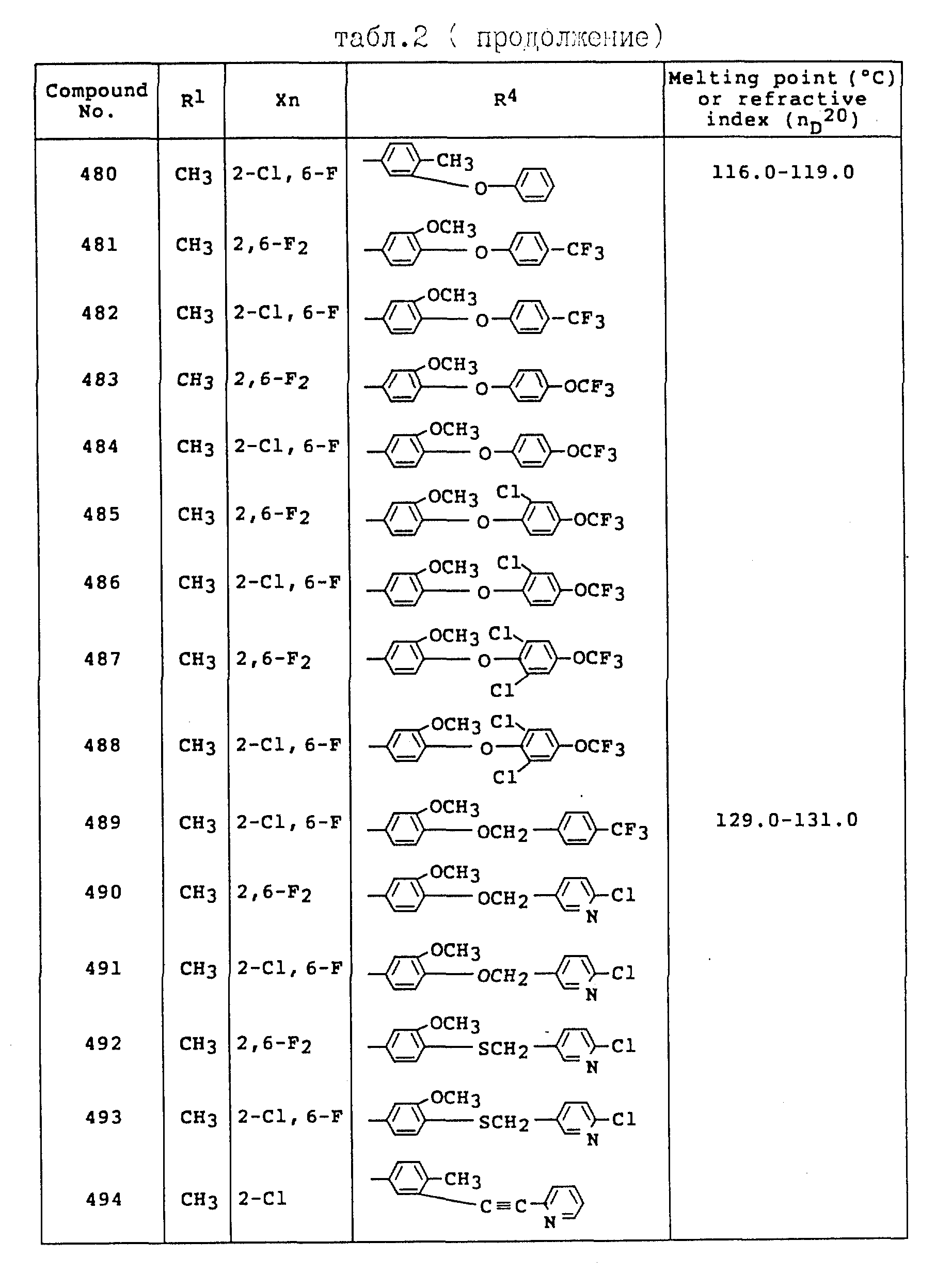
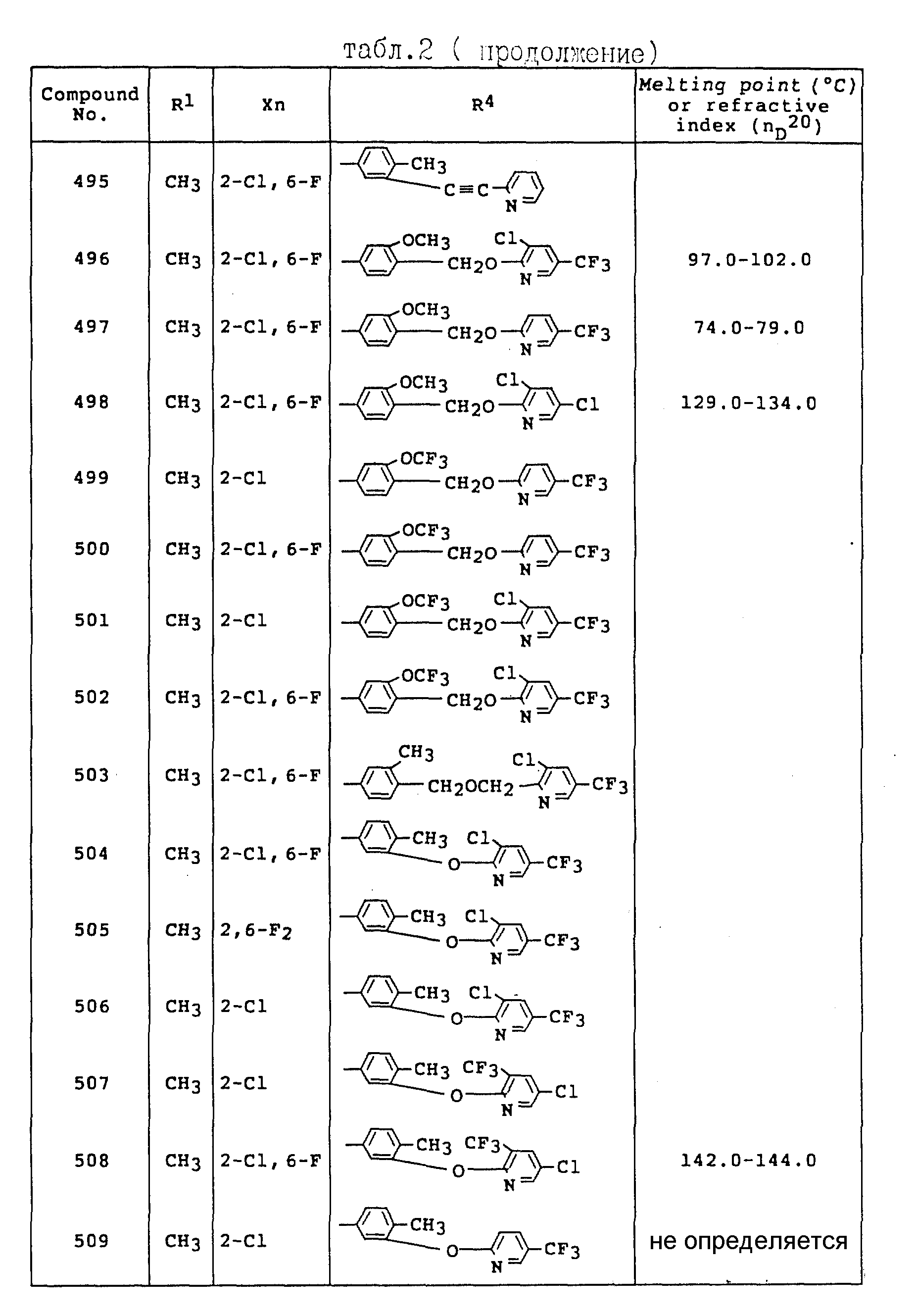
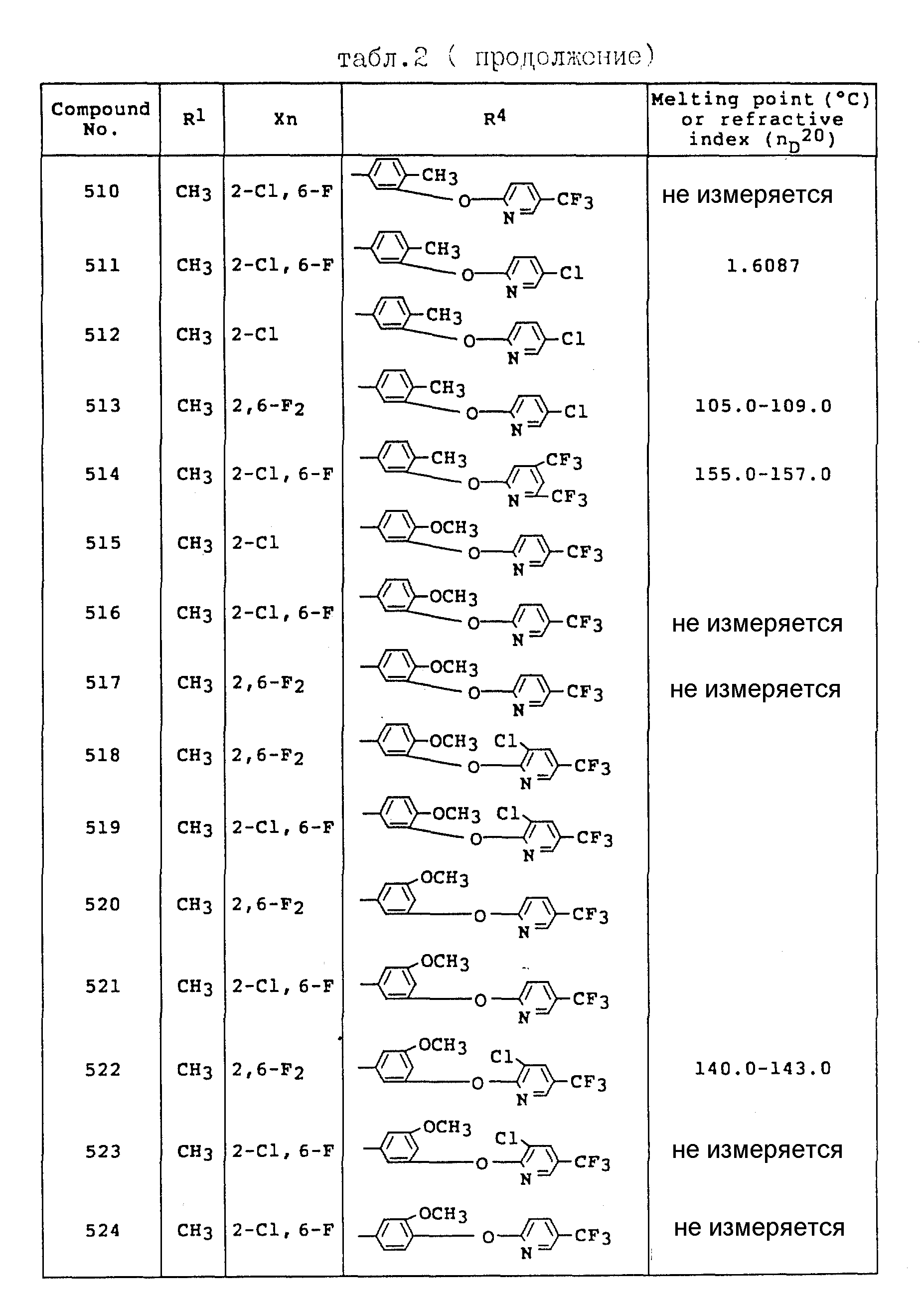
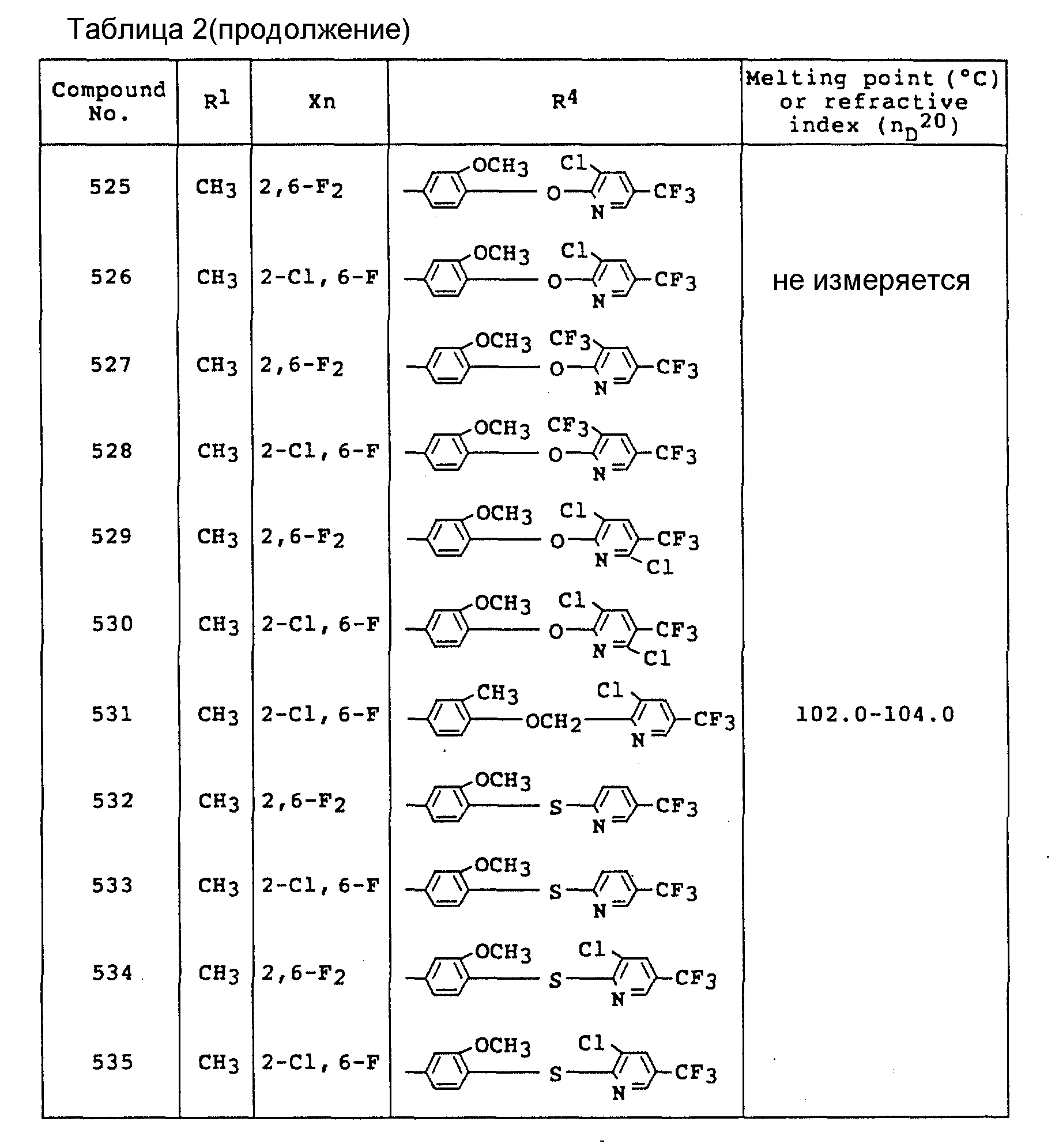
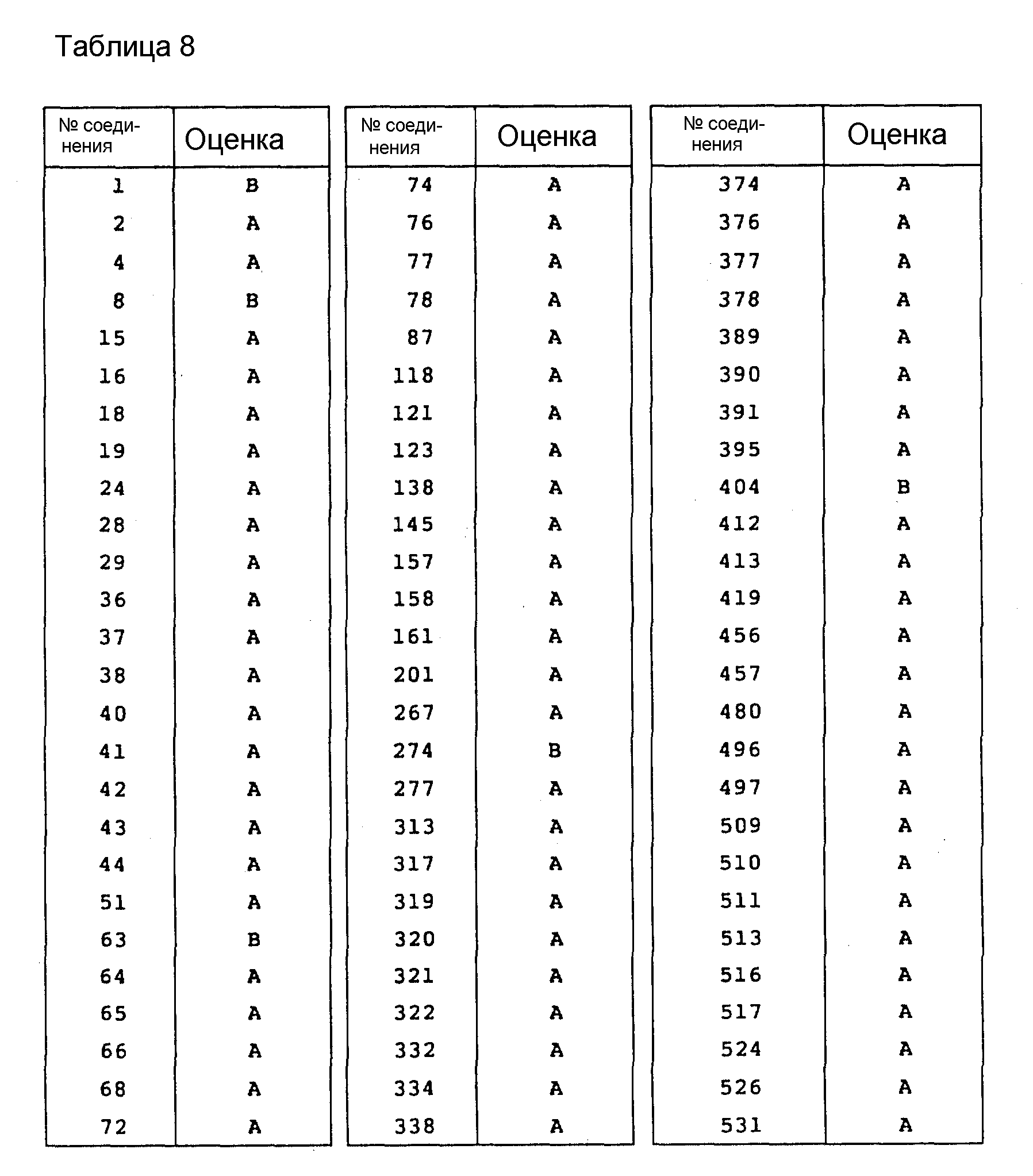
Примеры соединений общей формулы /I/ согласно настоящему изобретению представлены в Таблицах 1-2 (см. в конце описания). Далее, в описании ссылаются на номера соединений, приведенные в указанных выше таблицах.
Соединения настоящего изобретения могут быть получены согласно следующим методам.
Способ получения 1-1
(Схема реакции 1)
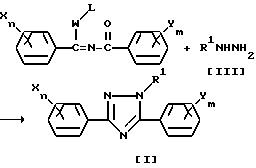
(где W представляет собой атом серы или кислорода, L представляет собой алкильную группу, содержащую 1-4 углеродных атомов, a R1, X, n, Y и m имеют указанные выше значения).
Таким образом, соединения настоящего изобретения, отвечающие общей формуле /I/, могут быть получены путем реакции N-ацилимидатного производного или N-ацилтиомидатного производного общей формулы /II/ с производным гидразина, отвечающим общей формуле /III/ в среде инертного растворителя.
В качестве растворителя могут использоваться любые растворители, не препятствующие протеканию реакции, которые, например, включают, такие спирты, как метанол, этанол и т.п.; такие простые эфиры, как диэтиловый эфир, тетрагидрофуран, диоксан, 1,2-диметоксиэтан, диглим и т.п., такие ароматические углеводороды, как бензол, толуол, хлорбензол, дихлорбензол и т.п.; такие алифатические углеводороды, как пентан, гексан, петролейный эфир и т.п.; такие галогенированные алифатические углеводороды, как дихлорметан, дихлорэтан, хлороформ, четыреххлористый углерод и т.п.; такие нитрилы, как ацетонитрил и т.п., такие апротонные полярные растворители, как диметилформамид, диметилацетамид, диметилсульфоксид и т.п.; вода и смещенные растворители, включающие комбинацию перечисленных выше растворителей. Следует отметить, что количество исходного соединения обычно составляет 1.0-5.0 моля соединений общей формулы /III/ на моль соединения общей формулы /II/.
Могут использоваться температуры реакции, лежащие в интервале от 0oC до температуры кипения растворителя. Как правило, в зависимости от природы используемого соединения время реакции может изменяться, но обычно оно составляет 1-72 часа. Конкретный пример такой реакции приведен, например, в Synthesis стр. 483(1983).
Исходное соединение общей формулы /II/ может быть получено следующим способом.
Способ получения 1-2.
(Схема реакций 2).
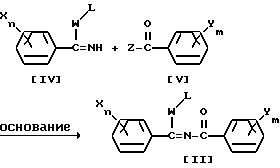
(где Z представляет собой атом галогена, а L, W, X, m, Y и n имеют значения указанные выше).
Таким образом, соединение общей формулы /II/ может быть получено по реакции соединения общей формулы /IV/ с соединением общей формулы /V/ в присутствии основания в среде инертного растворителя. Соединение общей формулы /IV/ может представлять собой такую соль присоединения кислоты, как соль присоединения с трехфтористым бором, хлористым водородом, бромистым водородом, йодистым водородом и т.п.
В качестве основания могут использоваться такие неорганические основания, как карбонат натрия, карбонат калия, кислый карбонат натрия, кислый карбонат калия, гидроксид натрия, гидроксид калия и т.п.; такие органические основания, как диэтиламин, триэтиламин, пиридин, 4-(N, N-диметиламино)пиридин и т.п.
В качестве растворителя могут использоваться такие кетоны, как ацетон, метилэтилкетон и т.п.; такие простые эфиры, как диэтиловый эфир, тетрагидрофуран, диоксан, 1,2-диметоксиэтан, диглим и т.п.; такие ароматические углеводороды, как бензол, толуол, хлорбензол, дихлорбензол и т.п.; такие алифатические углеводороды, как пентан, гексан, петролейный эфир и т.п.; такие алифатические галогенированные углеводороды, как дихлорметан, дихлорэтан, хлороформ, четыреххлористый углерод и т.п.; такие нитрилы, как ацетонитрил и т.п.; такие апротонные полярные растворители, как диметилформамид, диметилацетамид, диметилсульфоксид и т.п.; а также смешанные растворители, представляющие собой комбинацию указанных выше растворителей.
Количество используемых реагентов обычно составляет 0,8-1,3 моля соединения, отвечающего общей формуле /V/, в расчете на 1 моль соединения общей формулы /IV/. Количество применяемого основания составляет 1,0-2,0 моля на моль соединения общей формулы /IV/. Температура реакции составляет величину от 0oC до точки кипения растворителя. Время реакции может изменяться в зависимости от типа используемого соединения, но, как правило, конечный результат достигается за 1-24 часа.
Способ получения 2
(Схема реакции 3)
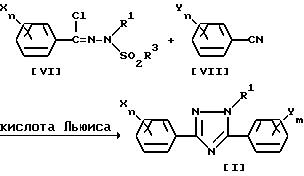
(где R1, X, n, Y и m имеют указанные выше значения, a R3 представляет собой фенильную группу, которая может быть замещена алкильной группой, содержащей 1-4 углеродных атома, или алкильную группу, содержащую 1-4 углеродных атома).
Таким образом, соединение общей формулы /I/ согласно настоящему изобретению может быть получено по реакции производного хлористого бензогидразоноила, отвечающего общей формуле /VI/, с производным бензонитрила общей формулы /VII/ в присутствии кислоты Льюиса в среде инертного растворителя.
В качестве растворителя могут использоваться любые растворители, не оказывающие вредного влияния на реакцию, например такие простые эфиры, как диэтиловый эфир, тетрагидрофуран, диоксан, 1, 2-диметоксиэтан, диглим, 1,2-диметокси этан и т. д.; такие ароматические углеводороды, как бензол, толуол, хлорбензол и т. п. ; такие алифатические углеводороды, как пентан, гексан, петролейный эфир и т.д.; такие алифатические галогенированные углеводороды, как дихлорметан, дихлорэтан, хлороформ, четыреххлористый углерод и т.д.; такие апротонные полярные растворители, как нитробензол, диметилформамид, диметилацетамид, диметилсульфоксид и т.п.; смешанный растворитель, включающий комбинацию из указанных выше растворителей.
В качестве кислоты Льюиса могут использоваться бромистый алюминий, хлористый алюминий, хлористое железо (III), трехфтористый бор, четыреххлористый титан и т. д. Используемые количества исходных веществ обычно составляют 1,0-2,0 моля соединения общей формулы /VII/ и 1,0-2,0 моля кислоты Льюиса на 1 моль соединения общей формулы /VI/. Температура реакции имеет значение в интервале от 0oC до точки кипения растворителя. Время реакции может меняться в зависимости от природы исходного соединения, но, как правило, конечный результат достигается за промежуток времени от 30 минут до 5 часов. Конкретный пример такой реакции описан, например, в Bulletin of the Chemical Society of Japan (Bull. Chem. Soc. Jap.) т.56, стр. 545 (1983).
Способ получения 3-1
(Схема
реакций 4).
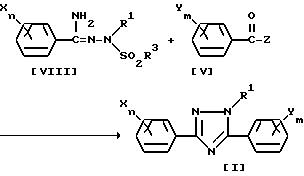
(где R1, R3, X, n, Y, m и Z имеют указанные выше значения).
Таким образом, соединение общей формулы /I/ согласно настоящему изобретению, может быть получено по реакции производного бензамидразона общей формулы /VIII/ с производным бензоилгалогенида общей формулы /I/ в отсутствии растворителя или в среде инертного растворителя.
В качестве растворителя могут использоваться любые вещества, не оказывающие вредного влияния на реакцию, например такие простые эфиры, как диэтиловый эфир, тетрагидрофуран, диоксан, 1,2-диметоксиэтан, диглим и т.п.; такие ароматические углеводороды, как бензол, толуол, хлорбензол, дихлорбензол и т. п. ; такие алифатические углеводороды, как пентан, гексан, петролейный эфир и т. п. ; такие алифатические галогенированные углеводороды, как дихлорметан, дихлорэтан, хлороформ, четыреххлористый углерод и т.п.; такие апротонные полярные растворители, как диметилформамид, диметилацетамид, диметилсульфоксид, 1-метил-2-пиролидинон и т.п.; а также смешанный растворитель, представляющий собой комбинацию указанных выше растворителей.
Обычно количество используемого исходного материала составляет 1.0-2.0 моля соединения общей формулы /V/ в расчете на моль соединения общей формулы /VIII/. Температура реакции лежит в интервале от 0oC до точки кипения растворители. Время реакции может изменяться в зависимости от природы исходного соединения, но, как правило, конечный результат достигается за время от 30 минут до 5 часов. Конкретный пример такой реакции описан в Bulletin of the Chemical Society of Japan (Bull. Chem. Soc. Jap.) т.56, стр.545 (1983).
Кроме этого, соединение общей формулы /VIII/, используемое в качестве исходного материала, может быть получено следующим способом.
Способ
получения 3-2
(Схема реакции 5).
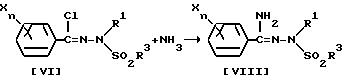
(где R1, R3, X и n имеют указанные выше значения).
Соединение общей формулы /VIII/ может быть получено по реакции соединения общей формулы /VI/ с газообразным аммиаком в среде инертного растворителя.
В качестве растворителя может использоваться любое соединение, не оказывающее вредного воздействия на ход реакции, например такие простые эфиры, как диэтиловый эфир, тетрагидрофуран, диоксан, 1,2-диметоксиэтан, диглим и т.п.; такие ароматические углеводороды, как бензол, толуол, хлорбензол, дихлорбензол и т.п.; такие алифатические углеводороды, как пентан, гексан, петролейный эфир, и т.п.; такие алифатические галогенированные углеводороды, как дихлорметан, дихлорэтан, хлороформ, четыреххлористый углерод и т.п.; такие апротонные полярные растворители, как диметилформамид, диметилацетамид, диметилсульфоксид и т.п.; а также смешанный растворитель, представляющий собой комбинацию растворителей, выбранных из числа указанных выше соединений.
Используемое количество исходного материала обычно составляет 5,0-10,0 молей аммиака на 1 моль соединения, отвечающего общей формуле /VI/. Температура реакции лежит в интервале от 0oC до точки кипения растворителя. Время реакции может изменяться в зависимости от типа используемого исходного соединения, но, как правило, конечный результат достигается за время 1-24 часа. Конкретный пример такой реакции описан, например, в Bulletin of the Chemical Society of Japan (Bull. Chem. Soc. Jhn.) т. 56, стр.545 (1983).
Способ получения 4-1
(Схема реакции 6).
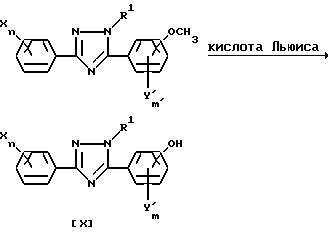
(где X, R1, Y', n и m' имеют указанные выше значения).
Соединение общей формулы /X/ может быть получено по реакции соединения общей формулы /IX/ в присутствии кислоты Льюиса и в среде инертного растворителя.
В качестве кислоты Льюиса могут использоваться бромистый алюминий, хлористый алюминий, хлористое железо (III), трехфтористый бор, тетрахлористый титан и т.п.
В качестве растворителя могут использоваться любые соединения, не оказывающие вредного влияния на ход реакции, например такие простые эфиры, как диэтиловый эфир, тетрагидрофуран, диоксан, 1,2-диметоксиэтан, диглим и т.п.; такие ароматические углеводороды, как бензол, толуол, хлорбензол, дихлорбензол и т.п.; такие алифатические углеводороды, как пентан, гексан, петролейный эфир и т.п.; такие алифатические галогенированные углеводороды, как дихлорметан, дихлорэтан, хлороформ, четыреххлористый углерод и т.п.; такие апротонные полярные растворители, как нитробензол, диметилформамид, диметилацетамид, диметилсульфоксид и т.п.; а также смешанные растворители ,включающие комбинацию перечисленных выше растворителей.
Используемое количество реагента обычно составляет 1,0-5,0 молей кислоты Льюиса на 1 моль соединения общей формулы /IX/. Температура реакции лежит в интервале от -20oC до точки кипения растворителя. Время реакции может изменяться в зависимости от природы исходного соединения, но, как правило, желаемый результат достигается за время 1-24 часа.
Способ получения 4-2
(Схема реакции 7).
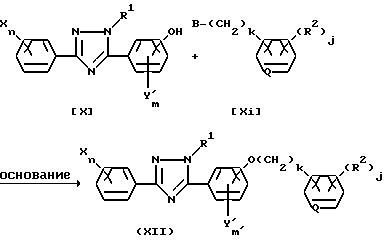
(где B представляет собой атом галогена, R4-SO2- группу или R4-SO3-группу /R4 представляет собой алкильную группу, содержащую 1-4 углеродных атомов, или фенильную группу, которая может быть замещенной/, k равно 0 или 1, а X, Y, R1, R2, Q, j, m и n имеют указанные выше значения).
Соединения общей формулы /XII/ согласно настоящему изобретению, может быть получено по реакции соединения общей формулы /X/ с соединением общей формулы /XI/ в присутствии основания и в среде инертного растворителя.
В качестве основания могут использоваться такие неорганические основания, как карбонат натрия, карбонат калия, кислый карбонат натрия, кислый карбонат калия, гидроксид натрия, гидроксид калия и т.п.; такие гидриды металлов, как гидрид натрия, гидрид калия и т.п., и такие органические основания, как триэтиламин, пиридин и т.п.
В качестве растворителя могут использоваться такие кетоны, как ацетон, метилэтилкетон и т.п., такие простые эфиры, как диэтиловый эфир, тетрагидрофуран, диоксан, 1,2-диметиоксиэтан, диглим и т.п.:, такие ароматические углеводороды, как бензол, толуол, хлорбензол, дихлорбензол и т.п.:, такие алифатические углеводороды, как пентан, гексан, петролейный эфир и т.п., такие алифатические галогенированные углеводороды, как дихлорметан, дихлорэтан, хлороформ, четыреххлористый углерод и т.п., такие нитрилы, как ацетонитрил и т.п., такие апротонные полярные растворители, как диметилформамид, диметилацетамид, диметилсульфоксид и т.п.; а также смешанный растворитель, включающий комбинацию указанных выше растворителей.
Обычно, количество используемого реагента составляет 1.0-2.0 моля соединения общей формулы /XI/ на моль соединения общей формулы /X/. Используемое количество основания составляет 1.0-2.0 моля на 1 моль соединения общей формулы /X/. Температура реакции лежит в интервале от -20oC до точки кипения растворителя. Время реакции может меняться в зависимости от типа используемого соединения, но, как правило, желаемый результат достигается за 1-24 часа.
Способ получения 5-1
(Схема реакции 8).
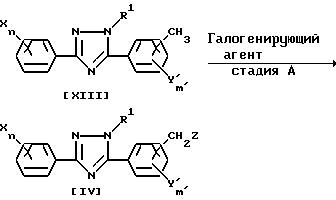
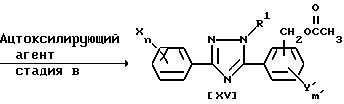
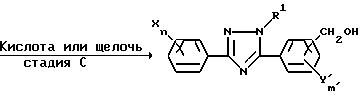
(где X, R1, Z, Y',n и m имеют указанные выше значения).
Соединение общей формулы /XIV/ может быть получено из производного триазола общей формулы /XIII/ по реакции с галогенирующим агентом. Такое соединение может реагировать с ацетоксилирующим агентом с получением соединения общей формулы /XV/. Затем соединение общей формулы /XV/ может реагировать с кислотой или щелочью с получением соединения общей формулы /XVI/.
В качестве галогенирующего соединения на стадии A могут использоваться N-хлорсукцинимид, N-бромсукцинимид, N-бромфталимид и т.п.
В качестве используемого растворителя можно отметить такие алифатические галогенированные растворители, как дихлорметан, дихлорэтан, хлороформ, четыреххлористый углерод и т. п. Кроме этого, в такой реакции необходимо использовать каталитическое количество бензоил пероксида, азобисизобутиронитрила и т.п. в качестве инициатора радикалов.
Обычно количество используемого галогенирующего агента составляет 0.8-1.5 моля на 1 моль соединения, отвечающего общей формуле /XIII/. Температура реакции лежит в интервале от 0oC до точки кипения растворителя. Время реакции может меняться в зависимости от типа используемого соединения, однако, как правило, желаемый результат достигается за время от 30 минут до 12 часов.
В качестве ацетоксилирующего агента, применяемого на стадии В, могут попользоваться ацетат лития, ацетат натрия, ацетат калия, ацетат кальция и т. п.
В качестве растворителя могут использоваться такие кетоны, как ацетон, метилэтилкетон и т.п., такие простые эфиры, как диэтиловый эфир, тетрагидрофуран, диоксан, 1,2-диметоксиэтан, диглим и т.п.; такие ароматические углеводороды, как бензол, толуол, хлорбензол, дихлорбензол и т.п., такие алифатические углеводороды, как пентан, гексан, петролейный эфир и т.п., такие алифатические галогенированные углеводороды, как дихлорметан, дихлорэтан, хлороформ, четыреххлористый углерод, и т.п., такие нитрилы, как ацетонитрил и т.п., такие апротонные полярные растворители, как диметилформамид, диметилацетамид, диметилсульфоксид и т.п., а также смешанный растворитель, представляющий собой комбинацию указанных выше растворителей.
Используемое количество ацетоксилирующего агента обычно составляет 1.0-4.0 молей на 1 моль соединения, отвечающего общей формуле /XIV/. Температура реакции лежит в интервале от 0oC до точки кипения растворителя. Время реакции может изменяться в зависимости от природы исходного соединения, но, как правило, желаемый результат достигается за 1-24 часа.
В качестве кислоты применяемой на стадии C можно использовать такие минеральные кислоты, как хлористо-водородную кислоту, серную кислоту и т.п., а также такие кислоты Льюиса, как бромистый алюминий, хлористый алюминий и т. п. В таком случае в качестве растворителя могут использоваться такие карбоновые кислоты, как уксусная кислота, муравьиновая кислота и т.п., такие кетоны, как ацетон, метилэтилкетон и т.п., такие простые эфиры, как диэтиловый эфир, тетрагидрофуран, диоксан, диметоксиэтин и т.п., такие ароматические углеводороды, как бензол, толуол и т.п., такие алифатические углеводороды, как пентан, гексан, петролейный эфир и т.п., такие алифатические галогенирующие углеводороды, как дихлорметан, дихлорэтан, четыреххлористый углерод и т. п., вода и смешанный растворитель, представляющий комбинацию из указанных выше растворителей.
Обычно, используемое каталитическое количество кислоты составляет 4.0 моля на 1 моль соединения, отвечающего общей формуле /XV/. Температура реакции лежит в интервале от 0oC до точки кипения растворителя. Время реакции может меняться в зависимости от природы используемого соединения, но, как правило, желаемый конечный результат достигается за время от 30 минут до 24 часов.
В качестве щелочи применяемой на стадии C могут использоваться водные растворы гидроксида натрия, гидроксида калия, карбоната калия, карбоната натрия и т.п. В этом случае, в качестве растворителя, могут использоваться такие спирты, как метанол, этанол, этилен гликоль и т.п., такие кетоны, как ацетон, метилэтилкетон и т.п.; такие простые эфиры, как тетрагидрофуран, диоксан, 1,2-диметоксиэтан и т.п.; вода и смешанный растворитель, состоящий из комбинации указанных выше растворителей.
Обычно, количество используемой щелочи составляет 0.5-4.0 моля на моль соединения общей формулы /XV/. Температура реакции лежит в интервале от 0oC до точки кипения растворителя. Время реакции может изменяться в зависимости от типа исходного соединения, но, как правило, желаемый результат достигается за время от 30 минут до 24 часов.
Способ получения 5-2
(Схема реакций 9).
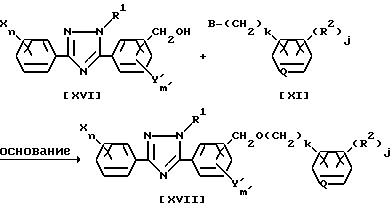
(где X, Y', B, Q, R1, R2, j, k, m' и n имеют указанные выше значения).
Соединение, отвечающее общей формуле /XVII/, согласно настоящему изобретению может быть получено по реакции соединения общей формулы /XVI/ с соединением общей формулы /XI/ в присутствии основания в среде инертного растворителя.
В качестве основания могут использоваться такие неорганические основания, как карбонат натрия, карбонат калия, кислый карбонат натрия, кислый карбонат калия, гидроксид натрия, гидроксид калия и т.п., такие гидриды металлов, как гидрид натрия, гидрид калия и т.п., такие органические основания, как триэтиламин, пиридин и т.п.
В качестве растворителя могут использоваться такие кетоны, как ацетон, метилэтилкетон и т.п.; такие простые эфиры, как диэтиловый эфир, тетрагидрофуран, диоксан, 1,2-циметоксиэтан, диглим и т.п.; такие ароматические углеводороды, как бензол, толуол, хлорбензол и т.п.; такие алифатические углеводороды, как пентан, гексан, петролейный эфир и т.п.; такие алифатические галогенированные углеводороды, как дихлорметан, дихлорэтан, хлороформ, четыреххлористый углерод и т.п.; такие нитрилы, как ацетонитрил и т.п.; такие апротонные полярные растворители, как диметилформамид, диметилацетамид, диметилсульфоксид и т.п.; а также смешанный растворитель, представляющий собой комбинацию перечисленных выше растворителей.
Обычно количество используемых реагентов составляет 1.0-2.0 моля соединения общей формулы /XI/ на моль соединения, отвечающего общей формуле /XVI/. Используемое количество щелочи составляет 1.0-2.0 моля на 1 моль соединения, отвечающего общей формуле /XVI/. Температура реакции лежит в интервале от -20oC до точки кипения растворителя. Время реакции может меняться в зависимости от типа соединения, но, как правило, желаемый результат может быть достигнут за 1-24 часа.
Способ получения 5-3
(Схема реакции 10)
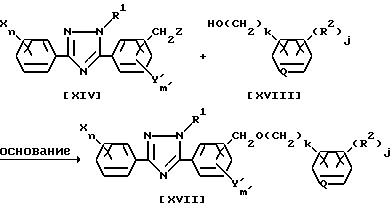
где X,Y, Q, R1, R2, Z, j, k, m' и n имеют указанные выше значения).
Соединение настоящего изобретения, отвечающее общей формуле /XVII/, может быть получено по реакции соединения общей формулы /XIV/ с соединением общей формулы /XVIII/ в присутствии основания в среде инертного растворителя.
В качестве основания можно использовать такие неорганические основания, как карбонат натрия, карбонат калия, кислый карбонат натрия, кислый карбонат калия, гидроксид натрия, гидроксид калия и т.п., такие гидриды металлов, как гидрид натрия, гидрид калия и т.п., такие органические основания, как триэтиламин, пиридин и т.п.
В качестве растворителя можно использовать такие кетоны, как ацетон, метилэтилкетон и т.п., такие простые эфиры, как диэтиловый эфир, тетрагидрофуран, диоксан, 1,2-диметоксиэтан, диглим и т.п., такие ароматические углеводороды, как бензол, толуол, хлорбензол и т.п., такие алифатические углеводороды, как пентан, гексан, петролейный эфир и т.п., такие алифатические галогенированные углеводороды, как дихлорметан, дихлорэтан, хлороформ, четыреххлористый углерод и т.п., такие нитрилы, как ацетонитрил и т.п., такие апротонные полярные растворители, как диметилформамид, диметилацетамид, диметилсульфоксид и т.п., а также смешанный растворитель, содержащий комбинацию из указанных выше растворителей.
Используемое количество реагента обычно составляет 1.0-2.0 моля соединения, отвечающего общей формуле /XVIII/, на моль соединения, отвечающего общей формуле /XIV/. Используемое количество основания составляет 1.0-2.0 моля на моль соединения отвечающего общей формуле /XIV/. Температура реакции лежит в интервале от -20oC до точки кипения растворителя. Время реакции может изменяться в зависимости от типа используемого соединения, однако, как правило, желаемый результат может достигаться за 1-24 часа.
Лучший способ осуществления настоящего изобретения.
Далее будут конкретно описаны со ссылкой на следующие ниже примеры, способ получения соединений настоящего изобретения, способ получения рецептур на их основе и способы их применения.
Пример 1. Получение 3-(2-хлорфенил)-5-(2-хлор-3-иитро-фенил)-1- метил-1H-1,2,4-триазола. (Соединение N 1).
Смесь, состоящую ив хлористого N-метил-N-(бензолсульфонил)-2- хлорбензогидразоноила (1.72 г), 2-хлор-3-нитробензонитрила (1.00 г) безводного хлористого алюминия (0.70 г) и o-дихлорбензола (20 мл), перемешивали в течение 30 минут на масляной бане при температуре 140oC. После охлаждения реакционную смесь растворяли в хлороформе (100 мл), промывали, в указанном порядке, разбавленной хлористо-водородной кислотой, разбавленным водным раствором гидроксида натрия и солевым раствором, сушили над безводным сульфатом магния и концентрировали при пониженном давлении. Концентрат очищали методом хроматографии на колонке с силикагелем, используя в качестве элюента смешанный растворитель гексанэтилацетат, с получением 1,12 г желаемого соединения (температура плавления: 124.0-125.0oC).
ЯМР-спектр (60 МГц, растворитель CDCl3, значение δ: ч/млн.): 3.83 (3H, синглет), 7.16-8.10 (7H, мультиплет).
Пример 2. Получение 3-(3-хлор-6-фторфенил)-5-(2-хлор-3- нитрофенил)-1-метил-1H-1,2,4-триазола (Соединение N 2).
Смесь, состоящую из хлористого N-метил-N-(п-толуолсульфонил)-2- хлор-6-фторбензогидразоноила (1.90 г). 2-хлор-3-нитробензонитрила (1.19 г), безводного хлористого алюминия (0.70) и o-дихлорбензола (20 мл), перемешивали в течение 30 минут на масляной бане при температуре 140oC. После охлаждения реакционную смесь растворяли в хлороформе (100 мл), в указанном порядке промывали разбавленной хлористо-водородной кислотой, разбавленным водным раствором гидроксида натрия и солевым раствором, сушили над безводным сульфатом магния и концентрировали при пониженном давлении. Концентрат очищали методом хроматографии на колонке с силикагелем, используя в качестве элюента смешанный растворитель гексанэтилацетат, с образованием 1.19 г целевого соединения (температура плавления: 112.0-114.0oC).
ЯМР-спектр (60 МГц, растворитель CDCl3, значение δ, ч/млн.: 3.90 (3H, синглет); 6.90-8.10 (6H, мультиплет).
Пример 3. Получение 3-(2-хлор-6-фторфенил)-5-(2-хлор-4- нитрофенил)-1-метил-1H-1,2,4-триазола /Соединение N 4/.
Смесь, состоящую из N-метил-N-(п-толуолсульфонил)-2-хлор-6- фторбензогидразоноилхлорида (1.90 г), 2-хлор-4-нитробензонитрила (1.80 г), безводного хлористого железа (III) /1,60 г/ и o-дихлорбензола (5 мл), перемешивали на масляной бане при температуре 140oC в течение 1 часа. После охлаждения реакционную смесь растворяли в хлороформе (100 мл), промывали, в указанном ниже порядке, разбавленной хлористо-водородной кислотой разбавленным водным раствором гидроксида натрия и солевым раствором, сушили над безводным сульфатом магния и концентрировали при пониженном давлении. Концентрат очищали методом хроматографии на колонке с силикагелем, используя в качестве элюента смешанный растворитель гексанэтилацетат, с получением 2,20 г целевого соединения (температура плавления: 144.0-148.0oC).
Спектр ЯМР (60 МГц, растворитель CDCl3, значение δ, ч/млн.): 3.88 (3H, синглет); 6.90-8.46 (6H, мультиплет).
Пример 4. Получение 5-(2-хлор-4-этилфенил)-3-(2-хлорфенил)- 1-метил-1H-1,2,4-триазола (Соединение N 15).
Этил 2-хлорбензимидат (2.75 г) и триэтиламин (1,60 г) растворяли в толуоле (30 мл) и в полученную смесь при перемешивании и при температуре 5-15oC прикапывали 2-хлор-4-этилбензоилхлорид (2,64 г), после чего полученную смесь перемешивали в течение 1 часа при комнатной температуре и снова нагревали с обратным холодильником в течение 3 часов. После охлаждения до комнатной температуры в реакционную смесь добавляли толуол (200 мл) и промывали разбавленной хлористо-водородной кислотой и солевым раствором, после чего органический слой сушили над безводным сульфатом магния. В органический слой добавляли монометилгидразин (1,00 г) и полученную смесь перемешивали в течение 16 часов при комнатной температуре. После завершения реакции реакционную смесь промывали разбавленной хлористо-водородной кислотой и солевым раствором, сушили над безводным сульфатом магния и концентрировали при пониженном давлении. Концентрат очищали методом хроматографии на колонке с силикагелем, используя в качестве элюента смешанный раствор гексанэтилацетат в результате чего получали 2,10 г желаемого соединения (температура плавления: 75,5- 77,5oC).
Спектр ЯМР (60 МГц, растворитель CDCl3, величина δ: ч/млн) 1, 27 (3H, триплет); 2.70 (2H, квартет); 3,83 (3H, синглет); 7,10-7,60 (6H, мультиплет); 7.90-8.10 (1H, мультиплет).
Пример 5. Получение 5-(2-хлор-4-этилфенил)-3-(2-хлор-6- фторфенил)-1-метил-1H-1,2,4-триазола (Соединение N 16).
Этил 2-хлор-6-фторбензимидат (3.02 г) и триэтиламин (1,60 г) растворяли в толуоле (30 мл) и при температуре 5-15oC, в условиях перемешивания, прикапывали 2-хлор-4-этилбензоилхлорид (2,64 г), после чего смесь перемешивали в течение 1 часа при комнатной температуре и снова нагревали с обратным холодильником в течение 3 часов. После охлаждения до комнатной температуры в реакционный раствор добавляли толуол (200 мл) и смесь промывали разбавленной хлористо-водородной кислотой и солевым раствором, после чего органический слой сушили над безводным сульфатом магния. В органический слой добавляли монометилгидразин (2,00 г) и полученную смесь нагревали в течение 2 часов с обратным холодильником. После завершения реакции реакционную смесь промывали разбавленной хлористо-водородной кислотой и солевым раствором, сушили над безводным сульфатом магния и концентрировали при пониженном давлении. Концентрат очищали методом хроматографии на колонке с силикагелем, используя в качестве элюента смешанный раствор гексанэтилацетат, с получением 2,63 г целевого соединения (показатель преломления: 1.5930).
Спектр ЯМР (60 МГц, растворитель CDCl3, величина δ: ч/млн.) 1,26 (3H, триплет); 2,69 (2H,квартет); 3,83 (3H, синглет); 6,90-7,50 (6H, мультиплет).
Пример 6. Получение 3-(2-хлорфенил)-5-(2-хлор-4-пропил-фенил)-1- метил-1H-1,2,4-триазола (Соединение N 18).
Этил 2-хлорбензимидат (2,75 г) и триэтиламин (1,80 г) растворяли в толуоле (30 мл) и при температуре 5-15oC, в условиях перемешивания, прикапывали 2-хлор-4-пропилбензоилхлорид (3,30 г), после чего смесь перемешивали в течение 1 часа при комнатной температуре и снова нагревали в течение 1 часа с обратным холодильником. После охлаждения до комнатной температуры в реакционный раствор добавляли толуол (200 мл) и полученную смесь промывали разбавленной хлористо-водородной кислотой и солевым раствором, после чего органический слой сушили над безводным сульфатом магния. В органический слой добавляли монометилгидразин (0,80 г) и смесь перемешивали в течение 18 часов при комнатной температуре. После завершения реакции реакционную смесь промывали разбавленной хлористо-водородной кислотой и солевым раствором, сушили над безводным сульфатом магния и концентрировали при пониженном давлении. Концентрат очищали методом хроматографии на колонке с силикагелем, используя в качестве элюента смешанный раствор гексанэтилацетат, с получением целевого соединения (температура плавления: 70.0-72.0oC).
Спектр ЯМР (60 МГц, растворитель CDCl3, величина, δ: ч/млн.) 0,95 (3H, триплет); 1,66 (2H, мультиплек); 2,63 (2H, триплет); 3,83 (3H, синглет); 6,90-7,10 (1H, мультиплет); 7,10-7,50 (6H, мультиплет).
Пример 7. Получение 3-(2-хлор-6-фторфенил)-5-(2-хлор-4- пропилфенил)-1-метил-1H,1,2,4-триазола (Соединение N 19).
Этил 2-хлор-6-фторбензимидат (3,02 г) и триэтиламин (1,80 г) растворяли в толуоле (30 мл) и при температуре 5-15oC, в условиях перемешивания, прикапывали 2-хлор-4-пропилбензоилхлорид (3.30 г), после чего смесь перемешивали в течение 1 часа при комнатной температуре и снова нагревали в течение 1 часа с обратным холодильником. После охлаждения до комнатной температуры в реакционный раствор добавляли толуол (200 мл) и смесь промывали разбавленной хлористо-водородной кислотой и солевым раствором, после чего органический слой сушили над безводным сульфатом магния. В органический слой добавляли монометилгидразин (1,80 г) и смесь нагревали в течение 4 часов с обратным холодильником. После завершения реакции реакционную смесь промывали разбавленной хлористо-водородной кислотой и солевым раствором, сушили над безводным сульфатом магния и концентрировали при пониженном давлении. Концентрат очищали методом хроматографии на колонке с силикагелем, используя в качестве элюента смешанный раствор гексанэтилацетат, с получением 0,41 г целевого соединения (показатель преломления: 1,5868).
Спектр ЯМР (60 МГц, растворитель CDCl3, величина δ: ч/млн.). 0,95(3H, триплет); 1,65 (2H, мультиплет); 2,62 (2H, триплет); 3,83 (3H, синглет); 6,80-7,50 (6H, мультиплет).
Пример 8. Получение 5-(4-бутил-2-хлорфенил)-3-(2-хлор-6- фторфенил)-1-метил-1H-1,2,4-триазола (Соединение N 29).
N-метил-N-(фенилсульфонил)-2-хлор-6-фторбензогидразоноилхлорид (1,10 г), 4-бутил-2-хлорбензонитрил (0,60 г) и безводный хлористый алюминий (0,50 г) добавляли к o-дихлорбензолу (10 мл) и полученную смесь перемешивали в течение 1 часа при 120oC. После завершения реакции добавляли хлороформ (100 мл) полученную смесь промывали разбавленной хлористо-водородной кислотой. После промывания водой органический слой сушили над безводным сульфатом магния и концентрировали при пониженном давлении. Концентрат очищали методом хроматографии на колонке с силикагелем, используя в качестве элюента смешанный раствор гексанэтилацетат, в результате чего получали 0,70 г целевого соединения (показатель преломления: 1,5667).
Спектр ЯМР (60 МГц, растворитель CDCl3, величина δ: ч/млн.) 0,75-1,12 (3H, мультиплет); 1,15-2,00 (4H, мультиплет); 2,65 (2H, триплет); 3,85 (3H, синглет); 6,83-7,60 (6H, мультиплет).
Пример 9. Получение 5-(4-трет.бутил-2-этоксифенил)-3-(2-хлор-6- фторфенил)-1-метил-1H-1,2,4-триазола. (Соединение N 35).
Смесь, состоящую из N-метил-N-(бензолсульфонил)-2-хлор-6- фторбензогидразоноилхлорида (1,60 г), 4-трет.бутил-2-эток- сибензонитрила (1.00 г), безводного хлористого алюминия (0,60 г) и o-дихлорбензола (5 мл), перемешивали в течение 30 минут на масляной бане при температуре 140oC. После охлаждения реакционную смесь растворяли в хлороформе (100 мл), промывали в указанном ниже порядке, разбавленной хлористо-водородной кислотой, разбавленным водным раствором гидроксида натрия и солевым раствором, сушили над безводным сульфатом магния и концентрировали при пониженном давлении. Концентрат очищали методом хроматографии на колонке с силикагелем, используя в качестве элюента смешанный раствор гексанэтилацетат, в результате чего получали 0,20 г целевого соединения (температура плавления: 108.0-111.0oC).
Спектр ЯМР (60 МГц, растворитель CDCl3, величина δ, ч/млн.): 1,15 (9H, синглет); 1,36 (3H, триплет); 3,87 (3H, синглет); 4,10 (2H, квартет); 6,83-7,58 (6H, мультиплет).
Пример 10. Получение 3-(2-хлорфенил)-5-(2-фтор-5-гексилфенил)- 1-метил-1H-1,2,4-триазола (Соединение N 42).
Смесь,
состоящую из N-метил-N-(бензолсульфонил)-2- хлорбензогидразоноилхлорида (2,06 г), 2-фтор-5-гексилбензо-нитрила (1,23 г), безводного хлористого алюминия (0,88 г) и
o-дихлорбензола (5 мл), перемешивали
в течение 30 минут на масляной бане при температуре 140oC. После охлаждения реакционную смесь растворяли в хлороформе (200 мл), промывали, в указанном
ниже порядке, разбавленной
хлористо-водородной кислотой, разбавленным водным раствором гидроксида натрия и солевым раствором, сушили над безводным сульфатом натрия и концентрировали при пониженном
давлении. Концентрат очищали
методом хроматографии на колонке с силикагелем, используя в качестве элюента смешанный растворитель гексанэтилацетат, в результате чего получали 1,60 г целевого соединения
(показатель преломления: 1,
5779).)
Спектр ЯМР (60 МГц, растворитель CDCl3, величина δ: ч/млн.) 0,87 (3H, триплет); 1,00-1,90 (8H, мультиплет); 2,62 (2H, триплет); 3,87 (3H,
дублет); 6,90-8,00 (7H,
мультиплет).
Пример 11. Получение 3-(2-хлор-6-фторфенил)-5-(2-фтор-5- гексилфенил)-1-метил-1H-1,2,4-триазола (Соединение N 43).
Смесь, состоящую из N-метил-N-(бензолсульфонил)-2-хлор-6- фторбензогидразоноилхлорида (2,17 г), 2-фтор-5-гексил-бензонитрила (1,23 г), безводного хлористого алюминия (0,88 г) и o-дихлорбензола (10 мл), перемешивали в течение 30 минут на масляной бане при температуре 140oC. После охлаждения реакционную смесь растворяли в хлороформе (200 мл), промывали, в указанном ниже порядке, разбавленной хлористо-водородной кислотой, разбавленным водным раствором гидроксида натрия и солевым раствором, сушили над безводным сульфатом магния и концентрировали при пониженном давлении. Концентрат очищали методом хроматографии на колонке с силикагелем, используя в качестве элюента смешанный растворитель гексанэтилацетат, в результате чего получали 1, 11 г целевого соединения (показатель преломления: 1, 5608).
Спектр ЯМР (60 МГц, растворитель CDCl3, величина δ: ч/млн.) 0,87 (3H, триплет); 1,00-1,80 (8H, мультиплет); 2,61 (2H, триплет); 3, 89 (3H, дублет); 6,80-7,40 (6H, мультиплет).
Пример 12. Получение 3-(2,6-дифторфенил)-5-(2-фтор-5- ундецилфенил)-1-метил-1H-1,2,4-триазола (Соединение N 46).
Смесь, состоящую из N-метил-N-(бензолсульфонил)-2,6- дифторбензогидразоноилхлорида (1,28 г), 2-фтор-5-ундецилбензонитрила (1,09 г), безводного хлористого алюминия (0,55 г) и o-дихлорбензола (10 мл), перемешивали в течение 30 минут на масляной бане при температуре 140oC. После охлаждения реакционную смесь растворяли в хлороформе (200 мл), промывали разбавленной хлористо-водородной кислотой, разбавленным водным раствором гидроксида натрия и солевым раствором, сушили над безводным сульфатом магния и концентрировали при пониженном давлении. Концентрат очищали методом хроматографии на колонке с силикагелем, используя в качестве элюента смешанный растворитель гексанэтилацетат, с получением 1,08 г целевого соединения (температура плавления: 70.3-73.0oC).
Спектр ЯМР (60 МГц, растворитель CDCl3, величина δ: ч/млн.) 0,88 (3H, триплет); 1,10-1,80 (18H, мультиплет); 2,63 (2H,триплет); 3,93 (3H, дублет); 6,90-7,60 (6H, мультиплет).
Пример 13. Получение 3-(2-хлорфенил)-5-(2-фтор-5-ундецилфенил)- 1-метил-1H-1,2,4-триазола (Соединение N 47).
Смесь, состоящую из N-метил-N-(бензолсульфонил)-2- хлорбензогидразоноилхлорида (1,27 г), 2-фтор-5-ундецилбензонитрила (1,09 г), безводного хлористого алюминия (0,55 г) и о-дихлорбензола (5 мл), перемешивали в течение 30 минут на масляной бане при температуре 140oC. После охлаждения реакционную смесь растворяли в хлороформе (200 мл), в указанном ниже порядке, промывали разбавленной хлористо-водородной кислотой, разбавленным водным раствором гидроксида натрия и солевым раствором, сушили над безводным сульфатом магния и концентрировали при пониженном давлении. Концентрат очищали методом хроматографии на колонке с силикагелем, используя в качестве элюента смешанный растворитель гексанэтилацетат, в результате чего получали 0,85 г целевого соединения (температура плавления: 35,0-37, 0o C).
Спектр ЯМР (60 МГц, растворитель CDCl3, величина δ: ч/млн.) 0,88 (3H, триплет); 1,10-1,70 (18H, мультиплет); 2,66 (2H, триплет); 3,93 (3H, дублет); 6,90-7,60 (6H, мультиплет); 7,90-8,00 (1H, мультиплет).
Пример 14 Получение 3-(2-хлор-6-фторфенил)-5-(2-фтор-5- ундецилфенил)-1-метил-1H-1,2,4-триазола (Соединение N 48).
Смесь, состоящую из N-метил-N-(бензолсульфонил)-2-хлор-6- фторбензогидразоноилхлорида (1,34 г), 2-фтор-5-ундецилбензонитрила (1,09 г), безводного хлористого алюминия (0,55 г) и o-дихлорбензола (10 мл), перемешивали в течение 30 минут на масляной бане при температуре 140oC. После охлаждения реакционную смесь растворяли в хлороформе (200 мл), в указанном ниже порядке, промывали разбавленной хлористо-водородной кислотой, разбавленным водным раствором гидроксида натрия и солевым раствором, сушили над безводным сульфатом магния и концентрировали при пониженном давлении. Концентрат очищали методом хроматографии на колонке с силикагелем, используя в качестве элюента смешанный растворитель гексанэтилацетат, с получением 1,04 г целевого соединения (показатель преломления: 1.5419).
Спектр ЯМР (60 МГц, растворитель CDCl3, величина δ: ч/млн.) 0,87 (3H, триплет); 1,10-1,80 (18H, мультиплет); 2,63 (2H,триплет); 3, 94 (3H, дублет); 6,90-7,60 (6H, мультиплет).
Пример 15. Получение 3-(2-хлор-6-трифторфенил)-5-(2-хлор-4- додецилфенил)-1-метил-1H-1,2,4-триазола (Соединение N 51).
Смесь, состоящую из N-метил-N-(бензолсульфонил)-2-хлор-6- фторбензогидразоноилхлорида (1,50 г), 2-хлор-4-додецил-бензонитрила (1,20 г), безводного хлористрго алюминия (0,60 г) и o-дихлорбензола (5 мл), перемешивали в течение 30 минут на масляной бане при температуре 140oC. После охлаждения реакционную смесь растворяли в хлороформе (100 мл), в указанном ниже порядке, промывали разбавленной хлористо-водородной кислотой, разбавленным водным раствором гидроксида натрия, солевым раствором, сушили над безводным сульфатом магния и концентрировали при пониженном давлении. Концентрат очищали методом хроматографии на колонке с силикагелем, используя в качестве элюента смешанный растворитель гексанэтилацетат, в результате чего получали 0,80 г целевого соединения (показатель преломления: 1, 5490).
Спектр ЯМР (60 МГц, растворитель CDCl3, величина 0,50-2,03 (23H, мультиплет); 2.65 (2H, триплет); 3.83 (3H, синглет); 6.82-7.52 (6H, мультиплет).
Пример 16. Получение 5-(4-бутокси-2-хлорфенил)-3-(2-хлор- фенил)-1-метил-1H-1,2,4-триазола (Соединение N 64).
Этил 2-хлорбензимидат (2,40 г) и триэтиламин (1,20 г) растворяли в толуоле (100 мл) и при температуре ниже 10oC, в условиях перемешивания, прикапывали 4-бутокси-2-хлорбензоилхлорид (2,60 г). Подученную смесь перемешивали в течение 2 часов при комнатной температуре и дополнительно нагревали с обратным холодильником в течение 2 часов. После завершения реакции реакционный раствор промывали солевым раствором, дополнительно промывали водой и органический слой сушили над безводным сульфатом магния. В толуольный слой добавляли монометилгидразин (1,50 г) и проводили реакцию в течение 24 часов при комнатной температуре. После завершения реакции полученную смесь промывали разбавленной хлористо-водородной кислотой, снова промывали водой и органический слой сушили над безводным сульфатом магния, после чего концентрировали при пониженном давлении. Концентрат очищали методом хроматографии на колонке с силикагелем, используя в качестве элюента смешанный растворитель гексанэтилацетат, в результате чего получали 1,00 г целевого соединения (температура плавления: 60,0-62,0oC).
Спектр ЯМР (60 МГц, растворитель CDCl3, величина, δ: ч/млн.) 0,80-1,16 (3H, мультиплет); 1.20-2.10 (4H, мультиплет); 3.84 (3H, синглет); 4.02 (2H, триплет); 6.76-7.95 (6H, мультиплет); 7.83-8.12 (1H, мультиплет).
Пример 17. Получение 3-(2-хлор-6-фторфенил)-5-(4-хлор-3- пентилоксифенил)-1-метил-1H-1, 2,4-триазола (Соединение N 68).
Смесь, состоящую из N-метил-N-(п-толуолсульфонил)-2-хлор-6- фторбензогидразоноилхлорида (1,10 г), 4-хлор-3- пентилоксибензонитрила (0,70 г), безводного хлористого железа (III) /0,60 г/ и o-дихлорбензола (5 мл), перемешивали в течение 30 минут на масляной бане при температуре 140oC. После охлаждения реакционную смесь растворяли в хлороформе (100 мл), в указанном ниже порядке промывали разбавленной хлористо-водородной кислотой, разбавленным водным раствором гидроксида натрия и солевым раствором, сушили над безводным магния и концентрировали при пониженном давлении. Концентрат очищали методом хроматографии на колонке с силикагелем, используя в качестве элюента смешанный растворитель гексан - этилацетат, в результате чего получали 0,50 г целевого соединения.
Спектр ЯМР (60 МГц, растворитель CDCl3, величина δ: ч/млн.) 0.72-2.16 (9H, мультиплет); 4.06 (3H, синглет); 4.10 (2H, триплет); 6.85-7,60 (6H, мультиплет).
Пример 18. Получение 5-(4-хлор-3-октилоксифенил)-3-(2-хлорфенил)- 1-метил-1H-1,2,4-триазола (Соединение N 77).
Смесь, состоящую из N-метил-N-(бензолсульфонил)-2- хлорбензогидразоноилхлорида (1,50 г), 4-хлор-3-октилоксибензонитрила (1,30 безводного хлористого железа (III) /0,80 г/ и o-дихлорбензола /5 мл/, в течение 30 минут перемешивали на масляной бане при температуре 140oC. После охлаждения реакционную смесь растворяли в хлороформе (100 мл), в указанном ниже порядке промывали разбавленной хлористо-водородной кислотой, разбавленным водным раствором гидроксида натрия и солевым раствором, сушили над безводным сульфатом магния и концентрировали при пониженном давлении. Концентрат очищали методом хроматографии на колонке с силикагелем, используя в качестве элюента смешанный растворитель гексанэтилацетат, в результате чего получали 0,80 г целевого соединения.
Спектр ЯМР (60 МГц, растворитель CDCl3, величина δ: ч/млн.) 0,65-2.13 (15H, мультиплет); 4.07 (3H, синглет); 4.13 (2H, триплет); 6.92-7.66 (7H, мультиплет).
Пример 19. Получение 3-(2-хлорфенил)-5-(2-хлор-4- метоксиэтоксифенил-1-метил-1H-1,2,4-триазола (Соединение N 87).
Этил 2-хлорбензимидат (4,00 г) и триэтиламин (2,60 г) растворяли в толуоле (20 мл) и при температуре 5-10oC, в условиях перемешивания, прикапывали 2-хлор-4-метоксиэтоксибензоилхлорид (4,20 г). Полученную смесь перемешивали в течение 1 часа при комнатной температуре и дополнительно нагревали с обратным холодильником в течение 30 минут. После охлаждения до комнатной температуры в реакционный раствор добавляли толуол (20 мл) и полученную смесь промывали разбавленной серной кислотой и солевым раствором, после чего органический слой сушили над безводным сульфатом магния. В органический слой добавляли монометилгидразин (2,00 г) и полученную смесь перемешивали в течение 4 часов при комнатной температуре. После завершения реакции реакционную смесь промывали разбавленной серной кислотой и солевым раствором, сушили над безводным сульфатом магния и концентрировали при пониженном давлении. Концентрат очищали методом хроматографии на колонке с силикагелем, используя в качестве элюента смешанный растворитель гексанэтилацетат, с получением 0,70 г целевого соединения (показатель преломления: 1,5946).
Спектр ЯМР (60 МГц, растворитель CDCl3, значение δ: ч/млн.) 3,45 (3H, синглет); 3.60-3.97 (4H, мультиплет); 4.00 (3H, синглет); 6.83-8.13 (7H, мультиплет).
Пример 20. Получение 3-(2-хлор-6-фторфенил)-5-(2-хлор-5- перфторбутилфенил)-1-метил-1H-1,2,4-триазола (Соединение N 116).
Смесь, состоящую из N-метил-N-(бензолсульфонил)-2-хлор-6- фторбензогидразоноилхлорида (1.70 г), 2-хлор-5- перфторбутилбензонитрила (1,75 г), безводного хлорида железа (III) /0,73 г) и o-дихлорбензола (10 мл), в течение 2 часов перемешивали на масляной бане при температуре 130oC. После охлаждения реакционную смесь растворяли в хлороформе (100 мл), в указанном ниже порядке промывали разбавленной хлористо-водородной кислотой, разбавленным водным раствором гидроксида натрия и солевым раствором, сушили над безводным сульфатом магния и концентрировали при пониженном давлении. Концентрат очищали методом хроматографии на колонке с силикагелем, используя в качестве элюента смешанный растворитель гексанэтилацетат, в результате чего получали 0,68 г целевого соединения (показатель преломления: 1, 5110).
Спектр ЯМР (60 МГц, растворитель CDCl3, значение δ, ч/млн.) 3.87 (3H, синглет); 6.80-7.97 (6H, мультиплет).
Пример 21. Получение
3-(2-хлорфенил)-5-(2-хлор-5- перфторгексилфенил)-1-метил-1H-1,2,4-триазола (Соединение N 119)
Смесь, состоящую из
N-метил-N-(п-толуолсульфонил)-2- хлорбензогидразоноилхлорида (0,51 г),
2-хлор-5- перфторгексилбензонитрила (0,70 г), безводного хлористого алюминия (0,20 г) и o-дихлорбензола (5 мл), перемешивали в
течение 1 часа на масляной бане, имеющей температуру 140oC.
После охлаждения реакционную смесь растворяли в хлороформе (100 мл), в указанной ниже последовательности, промывали разбавленной
хлористо-водородной кислотой, разбавленным водным раствором гидроксида
натрия и солевым раствором, сушили над безводным сульфатом магния и концентрировали при пониженном давлении. Концентрат очищали
методом хроматографии на колонке с силикагелем, используя в качестве
элюента смешанный растворитель гексанэтилацетат, в результате чего получали 0,15 г целевого соединения (температура плавления:
70.0-76.0oC).
Спектр ЯМР (60 МГц, растворитель CDCl3, величина δ, ч/млн.) 3,85 (3H, синглет); 7.13-8.06 (7H, мультиплет).
Пример 22. Получение 3-(2-хлор-6-фторфенил)-5-(2-хлор-5- перфторгексилфенил)-1-метил-1H-1,2,4-триазола (Соединение N 120).
Смесь, состоящую из N-метил-N-(п-толуолсульфонил)-2-хлор-6- фторбензогидразоноилхлорида (0,73 г), 2-хлор-5- перфторгексилбензонитрила (1,00 г), безводного хлорида железа (III) (0,36 г) и o-дихлорбензола (5 мл), в течение 1 часа перемешивали на масляной бане при температуре 140oC. После охлаждения реакционную смесь растворяли в хлороформе (100 мл), в указанной ниже последовательности, промывали разбавленной хлористо-водородной кислотой, разбавленным водным раствором гидроксида натрия и солевым раствором, сушили над безводным сульфатом магния и концентрировали при пониженном давлении. Концентрат очищали методом хроматографии на колонке с силикагелем, используя в качестве элюента смешанный растворитель гексанэтилацетат, в результате чего получали 0,15 г целевого соединения (температура плавления: 78.0-82.0oC).
Спектр ЯМР (60 МГц, растворитель CDCl3, значение δ: ч/млн.) 3.86 (3H, синглет); 6.86-7.86 (6H, мультиплет).
Пример 23. Получение 3-(2-хлорфенил)-5-(2-хлор-4- аллилоксифенил)-1-метил-1H-1,2,4-триазола (Соединение N 138).
Этил 2-хлорбензимидат (2.60 г) и триэтиламин (1.10 г)
растворяли в толуоле (20 мл)
и при температуре 5-10oC, в условиях перемешивания прикапывали 2-хлор-4-аллилоксибензоилхлорид (2.20 г). Полученную смесь перемешивали в течение 1 часа при
комнатной температуре и
дополнительно нагревали в течение 30 минут с обратным холодильником. После охлаждения до комнатной температуры в реакционный раствор добавляли толуол (20 мл) и полученную
смесь промывали разбавленной
серной кислотой и солевым раствором, после чего органический слой сушили над безводным сульфатом магния. В органический слой добавляли монометилидразин (2.00 г) и
подученную смесь перемешивали в
течение 5 часов при комнатной температуре. После завершения реакции реакционную смесь промывали разбавленной серной кислотой и солевым раствором сушили над безводным
сульфатом магния и концентрировали
при пониженном давлении. Концентрат очищали методом хроматографии на колонке с силикагелем, используя в качестве элюента смешанный растворитель гексанэтилацетат, с
получением 0,60 г целевого
соединения (показатель преломления : 1.6083)
Спектр ЯМР (60 МГц, растворитель CDCl3, значение δ, ч/млн.) 3.85 (3H, синглет); 4.50-4.80 (2H,
мультиплет); 5.25-5.62 (2H,
мультиплет); 5.77-6.40 (1H, мультиплет); 6.82-8.16 (7H, мультиплет).
Пример 24. Получение 3-(2-хлорфенил)-5-(2-хлор-4- пропаргилоксифенил-1-метил-1H-1,2, 4-триазола (Соединение N 145).
Этил 2- хлорбензимидат (3.00 г) и триэтиламин (1,50 г) растворяли в толуоле (20 мл) и при температуре 5-10oC, в условиях перемешивания, прикапывали 2-хлор-4-пропаргилоксибензоилхлорид (2.30). Подученную смесь перемешивали при комнатной температуре в течение 1 часа и дополнительно нагревали с обратным холодильником в течение 30 минут. После охлаждения до комнатной температуры в реакционный раствор добавляли толуол (20 мл) и полученную смесь промывали разбавленной серной кислотой и солевым раствором, после чего органический слой сушили над безводным сульфатом магния. В органический слой добавляли монометилгидразин (2.00 г) и полученную смесь перемешивали в течение 4 часов при комнатной температуре. После завершения реакции реакционную смесь промывали разбавленной серной кислотой и солевым раствором, сушили над безводным сульфатом магния и концентрировали при пониженном давлении. Концентрат очищали методом хроматографии на колонке с силикагелем, используя в качестве элюента смешанный растворитель гексанэтилацетат, в результате чего получали 0,60 г целевого соединения (температура плавления: 103.0-105.0o C.
Спектр ЯМР (60 МГц, растворитель CDCl3, значение δ: ч/млн.) 2.47-2.71 (1H, мультиплет); 3.83 (3H, синглет); 4.75 (2H, дублет); 6.83-8.20 (7H, мультиплет).
Пример 25. Получение 3-(2-хлор-6-фторфенил)-5-/4- фтор-3-(4-трифторметоксифенил)фенил/-1-метил-1H-1,2,4-триазола (Соединение N 157).
Смесь, состоящую из N-метил-N-(метансульфонил)-2-хлор-6- фторбензогидразоноилхлорида (1,50 г), 4-фтор-3-(4- трифторметоксифонил)бензонитрила (1,43 г), безводного хлорида железа (III) /0,90 г и o-дихлорбензола (5 мл), перемешивали в течение 30 минут на масляной бане при температуре 140oC. После охлаждения реакционную смесь растворяли в этилацетате (200 мл), промывали водой, сушили над безводным сульфатом магния и концентрировали при пониженном давлении. Концентрат очищали методом хроматографии на колонке с силикагелем, используя в качестве элюента смешанный растворитель гексанэтилацетат, в результате чего получали 1,90 г целевого соединения (температура плавления: 117.0-119.0oC).
Спектр ЯМР (60 МГц, растворитель CDCl3, значение δ, ч/млн.). 4.10 (3H, синглет), 6.80-7,90 (10H, мультиплет).
Пример 26. Получение 3-(2-хлор-6-фторфенил)-5-/2-хлор-4-(4- трифторметоксифенил)фенил/-1-метил-1H-1,2,4-триазола (Соединение N 158).
Смесь, состоящую из N-метил-N-(метансульфонил)-2-хлор-6- фторбензогидразоноилхлорида (1.50 г), 4-(4-трифторметоксифенил)- бензонитрила (1,56 г), безводного хлорида железа /III/ (0,90 г) и хлорбензола (20 мл), перемешивали в течение 1 часа на масляной бане при температуре 140oC. После охлаждения реакционную смесь растворяли в хлороформе (300 мл), в указанной ниже последовательности, промывали разбавленной хлористо-водородной кислотой, разбавленным водным раствором гидроксида натрия и солевым раствором, сушили над безводным сульфатом магния и концентрировали при пониженном давлении. Концентрат очищали методом хроматографии на колонке с силикагелем, используя в качестве элюента смешанный растворитель гексанэтилацетат, в результате чего получали 1,80 г целевого соединения (показатель преломления: 1,5925).
ЯМР спектр (60 МГц, растворитель CDCl3, значение δ, ч/млн.) 3.90 (3H, синглет), 6.90-7.70 (10H, мультивлет).
Пример 27. Получение 5-/3-хлор-4-(3,4-дихлорбензил)фенил/-3-(2- хлор-6-фторфенил)-1-метил-1H-1,2,4-триазола (Соединение N 161).
Смесь, состоящую из N-метил-N-(бензолсульфония)-2-хлор-6- фторбензогидразоноилхлорида (1.00 г), 3-хлор-4-(3,4- дихлорбензил)бензонитрила (0,93 г), безводного хлорида железа /III/ (0,50 г) и o-дихлорбензола (5 мл), в течение 1 часа перемешивали на масляной бане при температуре 140oC. После охлаждения реакционную смесь растворяли в хлороформе (300 мл), промывали, в указанной ниже последовательности, разбавленной хлористо-водородной кислотой, разбавленным водным раствором гидроксида натрия и солевым раствором, сушили над безводным сульфатом магния и концентрировали при пониженном давлении. Концентрат очищали методом хроматографии на колонке с силикагелем, используя в качестве элюента смешанный растворитель гексанэтилацетат, в результате чего получали 0,64 г целевого соединения (температура плавления: 179,0-185,0oC).
Спектр ЯМР (60 МГц, растворитель CDCl3, величина δ, ч/млн.) 4.03 (3H, синглет), 4.23 (2H, синглет), 6.67-7.86 (9H, мультиплет).
Пример 28. Получение 3-(2-хлор-6-фторфенил)-5-/3-хлор-4-(2- хлор-4-трифторметилфенокоиметил)фенил/-1-метил-1H-1,2,4-триазола (Соединение N 196).
К 30 мл N,N-диметилформамида добавляли 2-хлор-4- трифторметилфенол (0,29 г) и карбонат калия (0,25 г), после чего к полученной смеси при комнатной температуре, в условиях перемешивания, добавляли 5-(4-бромометил-3-хлорфенил)-3-(2-хлор-6-фторфенил)-1-метил- 1H-1,2,4-триазол (0,60 г) и полученную в результате смесь перемешивали в течение 1 часа при 120oC. После завершения реакции реакционный раствор охлаждали до комнатной температуры, переливали в воду и экстрагировали толуолом. Органический слой промывали водой, сушили над безводным сульфатом магния и концентрировали при пониженном давлении. Концентрат очищали методом хроматографии на колонке с силикагелем с получением 0,61 г целевого соединения (температура плавления: 113.0-114.0oC).
Спектр ЯМР (60 МГц, растворитель CDCl3, значение δ: ч/млн) 4.10 (3H, синглет), 5.30 (2H, синглет), 6.87-8.10 (9H, мультиплет).
Пример 29. Получение 3-(2-хлор-6-фторфенил)-5-/3-хлор-4-(2- фтор-4-трифторметилфенокоиметил)фенил/-1-метил-1H-1,2,4-триазола (Соединение N 197).
К 100 мл N,N-диметилформамида добавляли 5-(3-хлор-4- хлорметилфенил)-3-(2-хлор-6-фторфенил)-1-метил-1H-1,2,4-триазол (1,60 г) и карбонат калия (0,60 г), после чего к полученной смеси при комнатной температуре, в условиях перемешивания, добавляли 2-фтор-4- трифторметилфенол (0,80 г) и полученную смесь перемешивали в течение 3 часов при 70oC. После завершения реакции реакционный раствор охлаждали до комнатной температуры, переливали в воду и экстрагировали этилацетатом. Органический слой промывали водой, сушили над безводным сульфатом магния и концентрировали при пониженном давлении. Концентрат очищали методом хроматографии на колонке о силикагелем с получением 1,62 г целевого соединения (показатель преломления: 1,6010).
Спектр ЯМР (60 МГц, растворитель CDCl3, значение δ,
ч/млн) 4.10 (3H, синглет), 5.31 (2H, сингдет), 6.75-8.00 (9H, мультиплет)
Пример 30. Получение
3-(2-хлор-6-фторфенил)-6-фторфенил)-5- /3-хлор-4-(4-трифторметилфеноксиметил)фенил/-1-метил-1H-1,
2,4- триазола (Соединение N 199).
К 30 мл N,N-диметилформамида добавляли 4-трифторметилфенол (0,77 г) и карбонат калия (0,72 г), после чего к полученной смеси при комнатной температуре, в условиях перемешивания, добавляли 5-(4- бромометил-3-хлорфенил)-3-(2-хлор-6-фторфенил)-1-метил-1H-1,2,4- триазол (1,60 г) и полученную смесь перемешивали в течение 1 часа при 120oC. После завершения реакции реакционный раствор охлаждали до комнатной температуры, переливали в воду и экстрагировали толуолом. Органический слой промывали водой, сушили над безводным сульфатом магния и концентрировали при пониженном давлении. Концентрат очищали методом хроматографии на колонке с силикагелем с образованием 1,50 г целевого соединения (показатель преломления: 1, 5961).
Спектр ЯМР (60 МГц, растворитель CDCI3, величина δ, ч/млн) 4.08 (3H, синглет), 5.23 (2H, синглет), 6.87-7.47 (7H, мультиплет), 7.65 (2H, синглет), 7.83 (1H, синглет).
Пример 31 Получение 3-(2-хлор-6-фторфенил)-5-/3-хлор-4-(4- трифторметоксифеноксиметил)фенил/-1-метил-1H-1,2,4-триазол (Соединение N 201).
К 30 мл N, N-диметилформамида добавляли 4-трифторметоксифенол (0,33 г) и карбонат калия (0,25 г), после чего к полученной смеси при комнатной температуре, в условиях перемешивания, добавляли 5-(4- бромометил-3-хлорфенил)-3-(2-хлор-6-фторфенил)-1-метил-1H-1; 2,4- триазол (0,70 г) и полученную смесь перемешивали в течение 1 часа при 120oC. После завершения реакции реакционный раствор охлаждали до комнатной температуры, переливали в воду и экстрагировали толуолом. Органический слой промывали водой, сушили над безводным сульфатом магния и концентрировали при пониженном давлении. Концентрат очищали методом хроматографии на колонке с силикагелем, в результате чего получали 0,83 г целевого соединения (показатель преломления: 1,5701).
Спектр ЯМР (60 МГц, растворитель CDCl3, значение δ: ч/млн.) 4.08 (3H, синглет), 5.19 (2H, синглет), 6.70-7.40 (7H, мультиплет), 7,65 (1H, синглет).
Пример 32. Получение 3-(2-хлор-6-фторфенил)-5-(2-хлор-4- феноксифенил)-1-метил-1H-1,2,4-триазола (Соединение N 241).
Смесь, состоящую из N-метил-N-(п-толуолсульфонил)-2-хлор-6- фторбензогидразоноилхлорида (3.30 г), 2-хлор-4-феноксибензонитрила (2.30 г), безводного хлорида железа /III/ (1.60 г) и о-дихлорбензола (10 мл), перемешивали в течение 1 часа на масляной бане при температуре 140oC. После охлаждения реакционную смесь растворяли в хлороформе (100 мл), в указанной ниже последовательности, промывали разбавленной хлористо-водородной кислотой, разбавленным водным раствором гидроксида натрия и солевым раствором, сушили над безводным сульфатом магния и концентрировали при пониженном давлении. Концентрат очищали методом хроматографии на колонке с силикагелем, используя в качестве элюента смешанный растворитель гексанэтилацетат, в результате чего получали 0,15 г целевого соединения (температура плавления: 135.0- 140.0oC).
Спектр ЯМР (60 МГц, растворитель CDCl3, величина δ: ч/млн.) 3.91 (3H, синглет), 6.90-8.06 (11H, мультиплет).
Пример 33. Получение 3-(2-хлор-6-фторфенил)-5-/3-хлор-4-(2, 6- дихлор-4-трифторметилфенокси)-фенил/-1-метил-1H-1,2,4-триазола (Соединение N 259).
Этил 2-хлор-6-фторбензимидат (1,80 г) и триэтиламин (1,20 г) растворяли в толуоле (50 мл) и к полученной смеси, при комнатной температуре и в условиях перемешивания, прикапывали 3-хлор-4- (2,6-дихлор-4-трифторметилфенокси)-бензоилхлорид (3.70 г), после чего смесь перемешивали в течение 3 часов при 100oC. После охлаждения до комнатной температуры в реакционный раствор добавляли толуол (50 мл) и подученную смесь промывали разбавленной хлористо-водородной кислотой и солевым раствором и органический слой сушили над безводным сульфатом магния. В реакционный раствор добавляли монометилгидразин (0,80 г) и полученную смесь перемешивали в течение 3 часов при 100oC. После завершения реакции реакционную смесь промывали разбавленной хлористо-водородной кислотой и солевым раствором, сушили над безводным сульфатом магния и концентрировали при пониженном давлении. Концентрат очищали методом хроматографии на колонке с силикагелем, используя в качестве элюента смешанный раствор гексанэтилацетат, в результате чего получали 1,50г целевого соединения (температура плавления: 67.0-72.0oC).
Спектр ЯМР (60 МГц, растворитель CDCl3, величина δ: ч/млн.) 4.05 (3H, синглет), 6.40-7.95 (8H, мультиплет).
Пример 34. Получение 3-(2-хлор-6-фторфенил)-5-/3-хлор-4-(2- хлор-4-трифторметилбензилокси)-фенил/-1-метил-1H-1,2,4-триазола (Соединение N 273).
К 20 мл N,N-циметилформамида добавляли 3-(2-хлор-6-фторфенил) 5-(3-хлор-4-гидроксифенил)-1-метил-1H-1,2,4-триазола (0,70 г) и карбонат калия (0,31 г), после чего к полученной смеси, при комнатной температуре и в условиях перемешивания, добавляли 2-хлор-4-трифторметилбензилхлорид (0,50 г) и полученную смесь перемешивали в течение 5 часов при 120oC. После завершения реакции реакционный раствор охлаждали до комнатной температуры, переливали в воду и экстрагировали этилацетатом. Органический слой промывали водой, сушили над безводным сульфатом магния и концентрировали при пониженном давлении. Концентрат очищали методом хроматографии на колонке с силикагелем с получением 0,80 г целевого соединения (температура плавления: 156,0-159,0oC).
Спектр ЯМР (600 МГц, растворитель CDCl3, величина δ: ч/млн.) 4.05 (3H, синглет); 5.30 (2H, синглет), 6.80-7.95 (9H, мультиплет).
Пример 35. Получение 3-(2-хлор-6-фторфенил)-5-/3-хлор-4-(2- фтор-4-трифторметилбензилокси)-фенил/-1-метил-1H-1,2,4-триазола (Соединение N 274).
К 20 мл N,N-диметилформамида добавляли
3-(2-хлор-6-фторфенил) 5-/3-хлор-4-гидроксифенил)-1-метил-1H-1,2,4-триазол (0,90 г) и карбонат калия (0,40 г) и к полученной смеси, при комнатной температуре и в условиях перемешивания, добавляли
2-фтор-4-трифторметилбензилхлорид (0,50 г), после чего смесь в течение 5 часов перемешивали при 120oC. После завершения реакции реакционный раствор охлаждали до комнатной температуры,
переливали в воду и экстрагировали этилацетатом. Органический слой промывали водой, сушили над безводным сульфатом магния и концентрировали при пониженном давлении. Концентрат очищали методом
хроматографии на колонке с силикагелем с получением 0,60 г целевого соединения (температура плавления: 109,0-111,0oC)
Спектр ЯМР (60 МГц, растворитель CDCl3, величина
δ: ч/млн.) 4,00 (3H, синглет), 5.25 (2H, синглет), 6.80-7.90 (9H, мультиплет).
Пример 36. Получение
3-(2-хлор-6-фторфенил)-5-/3-хлор-4-(4- трифторметилбензилокси)фенил/-1-метил-1H-1,2,4-триазола (Соединение N 275)
Этил 2-хлор-6-фторбензимидат (2,40 г) и триэтиламин (1,20 г) растворяли в
толуоле (50 мл) и при комнатной температуре в условиях перемешивания прикапывали 3-хлор-4-(4-трифторметилбензилокси)- бензоилхлорид (3,50 г), после чего подученную смесь перемешивали в течение 3
часов
при температуре 100oC. После охлаждения до комнатной температуры в реакционный раствор добавляли толуол (50 мл) и смесь промывали разбавленной хлористо-водородной кислотой и солевым
раствором, после чего органический слой сушили над безводным сульфатом магния. В органический слой добавляли монометилгидразин (0,90 г) и смесь перемешивали в течение 3 часов при 100oC.
После завершения реакции реакционную смесь промывали разбавленной хлористо-водородной кислотой и солевым раствором, сушили над безводным сульфатом магния и концентрировали при пониженном давлении.
Концентрат очищали методом хроматографии на колонке с силикагелем, используя в качестве элюента смешанный растворитель гексанэтилацетат, с получением 2,20 г целевого соединения (температура
плавления:
43.0-47.0oC).
Спектр ЯМР (60 МГц, растворитель CDCl3, значение δ: ч/млн.) 4.05 (3H, синглет), 5.25 (2H, синглет), 6.90-7.95 (10H,
мультиплет)
Пример 37. Получение 5-/3-хлор-4-(4-трифторметилбензилокси)- фенил/-3-(2,6-дифторфенил)-1-метил-1H-1,2,4-триазола (Соединение N 276).
Этил 2,6-дифторбензамидат (2,20 г) и триэтиламин (1,20 г) растворяли в толуоле (50 мл) и к полученной смеси при комнатной температуре, в условиях перемешивания, прикапывали 3-хлор-4-(4- трифторметилбензилокси)бензоилхлорид (3, 50 г), после чего полученную смесь перемешивали в течение 3 часов при 100oC. После охлаждения до комнатной температуры в реакционный раствор добавляли толуол (50 мл) и смесь промывали разбавленной хлористо-водородной кислотой и солевым раствором и органический слой сушили над безводным сульфатом магния. В органический слой добавляли монометилгидразин (0,90 г) и смесь перемешивали в течение 3 часов при 100oC. После завершения реакции реакционную смесь промывали разбавленной хлористо-водородной кислотой и солевым раствором, сушили над безводным сульфатом магния и концентрировали при пониженном давлении. Концентрат очищали методом хроматографии на колонке с силикагелем, используя в качестве элюента смешанный растворитель гексанэтилацетат с получением 2,00 г целевого соединения (температура плавления: 171.0-177.0oC).
Спектр ЯМР (60 МГц, растворитель CDCl3, величина δ, ч/млн.) 4.00 (3H, синглет), 5.20 (2H, синглет), 6.65-7,90 (10H, мультиплет).
Пример 38. Получение 3-(2-хлор-6-фторфенил)-5-/3-хлор-4-(4- трифторметоксибензилокси)фенил/-1-метил-1H-1,2,4-триазола (Соединение N 277).
Этил 2-хлор-6-фторбензимидат (2,40 г) и триэтиламин (1,20 г) растворяли в толуоле (50 мл) и к полученной смеси, при комнатной температуре в условиях перемешивания, прикапывали 3-хлор-4-(4- трифторметоксибензилокси)бензоилхлорид (3.70 г), после чего полученную смесь перемешивали в течение 3 часов при 100oC. После охлаждения до комнатной температуры в реакционный раствор добавляли толуол (50 мл) и смесь промывали разбавленной хлористо-водородной кислотой и солевым раствором и органический слой сушили над безводным сульфатом магния. В органический слой добавляли монометилгидразин (0,90 г) и полученную смесь перемешивали в течение 3 часов при 100oC. После завершения реакции реакционную смесь промывали разбавленной хлористо-водородной кислотой, сушили над безводным сульфатом магния и концентрировали при пониженном давлении. Концентрат очищали методом хроматографии на колонке о силикагелем, используя в качестве элюента смешанный растворитель гексанэтилацетат в результате чего получали 2,50 г целевого соединения (показатель преломления: 1,5680).
Спектр ЯМР (60 МГц, растворитель CDCl3, величина 4,00 (3H, синглет); 5.10 (2H, синглет); 6.85-7.90 (10H, мультиплет).
Пример 39. Получение 5-/3-хлор-4-(4-трифторметоксибензолокси) фенил/-3-(2,6-дифторфенил)-1-метил-1H-1,2,4-триазола (Соединение N 278).
Этил 2,6-дифторбензимидат (2,20 г) и триэтиламин (1,20 г) растворяли в толуоле (50 мл) и к полученной смеси, при комнатной температуре и в условиях перемешивания прикапывали 3-хлор-4-(4- трифторметокоибензилокси)бензоилхлорид (3.70 г), после чего смесь перемешивали в течение 3 часов при 100oC. После охлаждения до комнатной температуры в реакционный раствор добавляли толуол (50 мл) и смесь промывали разбавленной хлористо-водородной кислотой и солевым раствором, а органический слой сушили над безводным сульфатом магния. В органический слой добавляли монометилгидразин (0,90 г) и смесь перемешивали в течение 3 часов при 100oC. После завершения реакции реакционную смесь промывали разбавленной хлористо-водородной кислотой и солевым раствором, сушили над безводным сульфатом магния и концентрировали при пониженном давлении. Концентрат очищали методом хроматографии на колонке с силикагелем, используя в качестве элюента смешанный растворитель гексанэтилацетат, с получением 2,50 г целевого соединения (температура плавления: 132.0-136.0oC).
Спектр ЯМР (60 МГц, растворитель CDCl3, величина δ: ч/млн.) 4.00 (3H, синглет), 5.10 (2H, синглет), 6.70-8.20 (10H, мультиплет).
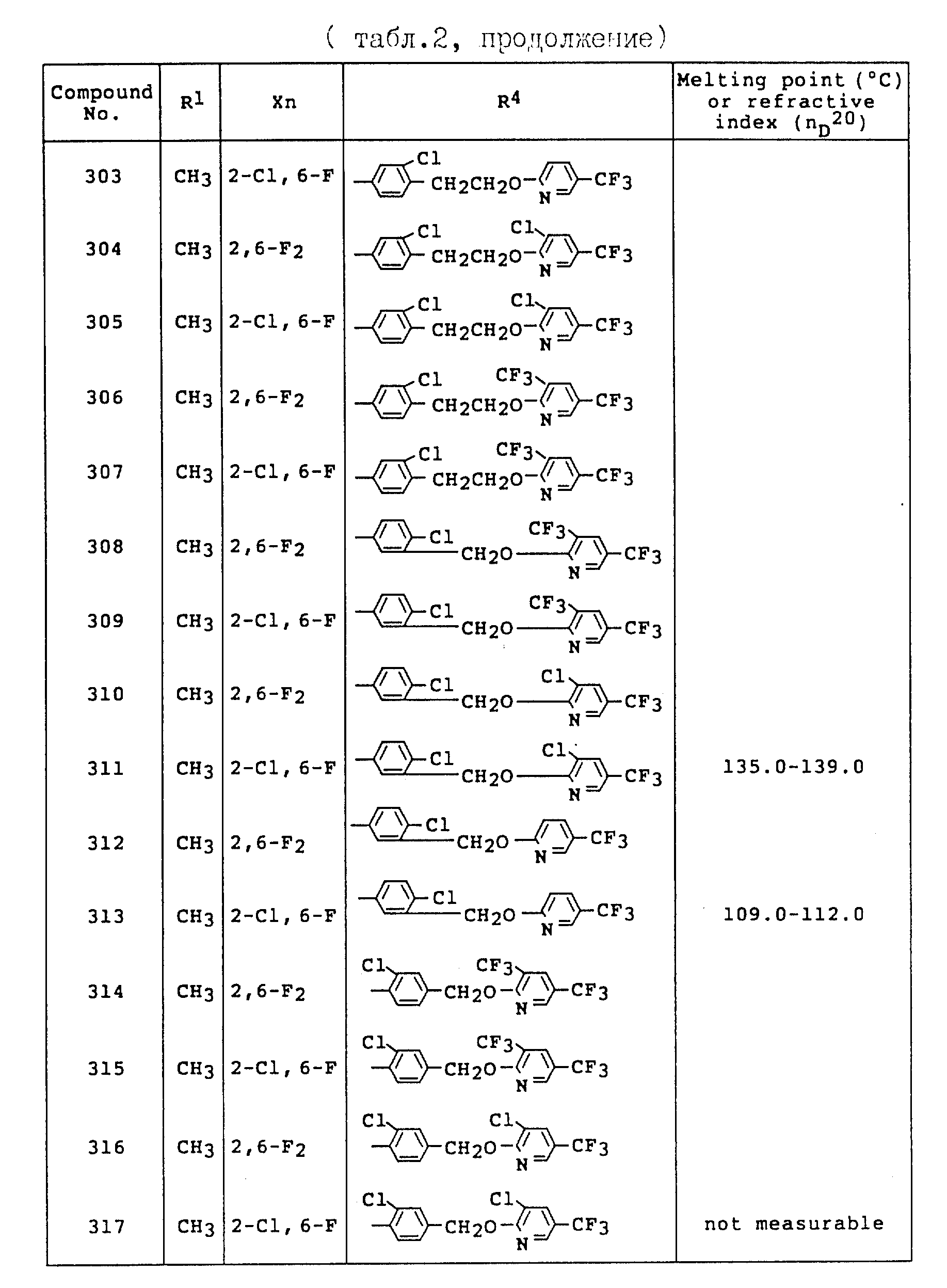
Пример 40. Получение 3-(2-хлор-6-фторфенил)-6-/2-хлор-4- (3-хлор-5-трифторметилпиридин-2-илоксиметил)фенил/-1-метил-1H- 1,2,4-триазола (Соединение N 317).
3-(2-Хлор-6-фторфенил)-5-(2-хлор-4-гидрокоиметилфенил)-1-метил- 1H-1,2,4-триазол (0,50 г) растворяли в 1,2-диметоксиэтане (20 мл) и смесь охлаждали до 0oC, после чего добавляли гидрид натрия (60%, 0,07 г) и реакционную смесь перемешивали в течение 15 минут. Затем прикапывали раствор 2,3-дихлор-5-трифторметилпиридина (0,34 г) в 1,2-диметоксиэтане (10 мл и смесь перемешивали в течение 3 часов. После завершения реакции реакционный раствор нагревали до комнатной температуры и переливали в воду, после чего проводили экстракцию эфиром. Органический слой промывали водой, сушили над безводным сульфатом магния и концентрировали при пониженном давлении. Концентрат очищали методом хроматографии на колонке с силикагелем с получением 0,62 г целевого соединения.
Спектр ЯМР (60 МГц, растворитель CDCl3, величина δ: ч/млн.) 3.83 (3H, синглет), 5.50 (2H, синглет), 6.83-8.37 (8H, мультиплет).
Пример 41. Получение 5-/3-хлор-4-(3, 5-дихлорпиридин-2- илоксиметил)фенил/-3-(2-хлор-6-фторфенил)-1-метил-1H-1,2,4-триазола (Соединение N 330).
Гидрид натрия (60%, 0,12 г) добавляли к 1,2-диметоксиэтану (50 мл и при -5oC прикапывали раствор 3-(2-хлор-6-фторфенил)-5-(3- хлор-4-гидрокоиметилфенил)-1-метил-1H-1,2,4-триазола (1,00 г) в 1,2- диметоксиэтане, после чего полученную смесь перемешивали в течение 20 минут. Полученный реакционный раствор, при температуре -5oC в течение 10 минут при перемешивании, прикапывали к раствору 2,3,5 трихлорпиридина (0,60 г) в 1,2-диметоксиэтане (20 мл). Реакционную смесь нагревали до комнатной температуры, переливали в воду и экстрагировали этилацетатом. Органический слой промывали водой сушили над безводным сульфатом магния и концентрировали при пониженном давлении. Концентрат очищали методом хроматографии на колонке с силикагелем с получением 0,40 г целевого соединения (температура плавления: 153.0-155.0oC).
Спектр ЯМР (60 МГц, растворитель CDCl3 величина δ: ч/млн.) 4.06 (3H, синглет), 5.48 (2H, синглет), 6.75-7.30 (3H, мультиплет), 7.50-8.00 (5H, мультиплет).
Пример 42. Получение 5-/3-хлор-4-(3-хлор-5-трифторметилпиридин- 2-илоксиметил)фенил/-3-(2-хлор-6-фторфенил)-1-метил-1H-1,2,4-триазола (Соединение N 332).
Гидрид натрия (60%, 0,16г ) добавляли к 1,2-диметоксиэтану (50 мл) и к полученному раствору, при температуре -5oC и перемешивании, прикапывали раствор 3-(2-хлор-6-фторфенил)-5-(3-хлор- 4- гидроксиметилфенил)-1-метил-1H-1,2, 4-триазола (1,20 г в 1,2-диметоксиэтане (20 мл). К реакционному раствору в течение 10 минут при -5oC прикапывали раствор 2,3-дихлор-5-трифторметил пиридина (0,80 г) в 1,2-диметоксиэтане (20 мл), после чего смесь дополнительно перемешивали в течение 15 минут. После завершения реакции реакционный раствор нагревали до комнатной температуры, переливали в воду и экстрагировали этилацетатом. Органический слой промывали водой, сушили над безводным сульфатом магния и концентрировали при пониженном давлении. Концентрат очищали методом хроматографии на колонке с силикагелем с получением 1,10 г целевого соединения (температура плавления: 47.0-49.0oC).
Спектр ЯМР (60 МГц, растворитель CDCl3, величина δ: ч/млн.) 4.06 (3H, синглет), 5.57 (2H, синглет), 6.84-7.50 (3H, мультиплет), 7.60- 7.75 (4H, мультиплет), 8.30 (1H, синглет).
Пример 43. Получение 5-/3-хлор-4-(5-трифторметилпиридин-2- илоксиметил)фенил/-3-(2-хлор-6-фторфенил)-1-метил-1H-1,2,4-триазола (Соединение N 334).
Гидрид натрия (60%, 0,12 г) добавляли к 1, 2-диметоксиэтану (50 мл) и к полученному раствору при -5oC прикапывали раствор 3-(2-хлор-6- фторфенил)-5-(3-хлор-4-гидроксиметилфенил)-1-метил- 1H-1,2,4-триазола (1,00 г) в 1, 2-диметоксиэтане (20 мл), после чего полученную смесь перемешивали в течение 15 минут. К реакционную раствору прикапывали раствор 2-хлор-5-трифторметилпиридина (0,60 г) в 1,2-диметоксиэтане (20 мл) при температуре -5oC, после чего смесь перемешивали в течение 15 минут. Реакционную смесь нагревали до комнатной температуры, переливали в воду и экстрагировали этилацетатом. Органический слой промывали водой, сушили над безводным сульфатом магния и концентрировали при пониженном давлении. Концентрат очищали методом хроматографии на колонке с силикагелем с получением 0,80 г целевого соединения (показатель преломления: 1,5879).
Спектр ЯМР (60 МГц, растворитель CDCl3, величина δ, ч/млн.) 4.06 (3H, синглет), 5.57 (2H, синглет), 6.75-8.42 (9H, мультиплет).
Пример 44. Получение 5-/4-хлор-3-(5-трифторметилпиридин-2- илокси)фенил/-3-(2,6-дифторфенил)-1-метил-1H-1,2,4-триазола (Соединение N 377).
Смесь, состоящую из N-метил-N-(бензолсульфонил)-2,6- дифторбензогидразоноилхлорида (0,90 г), 4-хлор-3-(5- трифторметилпиридин-2-илокси)бензонитрила (0,90 г), безводного хлорида железа (III) (0,50 г) и o-дихлорбензола (5 мл) перемешивали в течение 30 минут на масляной бане при температуре 140oC. После охлаждения смесь растворяли в хлороформе (100 мл) и промывали разбавленной хлористо-водородной кислотой, разбавленным водным раствором гидроксида натрия и солевым раствором. Затем смесь сушили над безводным сульфатом магния и концентрировали при пониженном давлении. Концентрат очищали методом хроматографии на колонке с силикагелем, используя в качестве элюента смешанный растворитель гексанэтилацетат, в результате чего получали 0,30 г целевого соединения.
Спектр ЯМР (60 МГц, растворитель CDCl3, величина δ: ч/млн.) 4.02 (3H, синглет), 6,64-7.98 (8H, мультиплет), 8.20- 8.38 (1H, мультиплет).
Пример 45. Получение 3-(2-хлор-6-фторфенил)-5-/4-хлор-3-(5- трифторметилпиридин-2-илокси)фенил/-1-метил-1H-1,2,4-триазола (Соединение N 378).
Смесь, состоящую из N-метил-N-(п-толуолсульфонил)-2-хлор-6- фторбензогидразоноилхлорида (1,00 г), 4-хлор-3-(5- трифторметилпиридин-2-илокси)бензонитрила (0,90 г), безводного хлорида железа (III) (0,50 г) и o-дихлорбензола (5 мл), в течение 30 минут перемешивали на масляной бане при температуре 140oC. После охлаждения смесь растворяли в хлороформе (100 мл) и промывали разбавленной хлористо-водородной кислотой, разбавленным водным раствором гидроксида натрия и солевым раствором. Затем смесь сушили над безводным сульфатом магния и концентрировали при пониженном давлении. Концентрат очищали методом хроматографии на колонке с силикагелем, используя в качестве элюента смешанный растворитель гексанэтилацетат, в результате чего получали 0,40 г целевого соединения.
Спектр ЯМР (60 МГц, растворитель CDCl3, величина δ, ч/млн.) 4.12 (3H, синглет), 6.92-8.11 (8H, мультиплет), 8.33-8.50 (1H, мультиплет).
Пример 46. Получение 3-(2-хлорфенил)-5-/2-хлор-4-(5- трифторметилпиридин-2-илокси)фенил/-1-метил-1H-1,2,4-триазола (Соединение N 389).
Смесь, состоящую из N-метил-N-(бензолсульфонил)-2-хлор- бензогидразоноилхлорида (2.05 г), 2-хлор-4-(5-трифторметилпиридин-2- илокси)бензонитрила (1,88 г), безводного хлорида железа /III/ (1.07 г) и o-дихлорбензола (10 мл), в течение 30 минут перемешивали на масляной бане при температуре 140oC. После охлаждения смесь растворяли в хлороформе (300 мл) и промывали разбавленной хлористо-водородной кислотой, разбавленным водным раствором гидроксида натрия и солевым раствором. Затем смесь сушили над безводным сульфатом магния и концентрировали при пониженном давлении. Концентрат очищали методом хроматографии на колонке с силикагелем, используя в качестве элюента смешанный растворитель гексанэтилацетат, в результате чего получали 1,87 г целевого соединения (температура плавления: 104.0-108.0oC).
Спектр ЯМР (60 МГц, растворитель CDCl3, величина δ: ч/млн.) 3.88 (3H, синглет), 6.90-8.40 (10H, мультиплет).
Пример 47. Получение 3-(2-хлор-6-фторфенил)-5-/2-хлор-4-(5- трифторметилпиридин-2-илокси)фенил/-1-метил-1H-1,2,4-триазола (Соединение N 390).
Смесь, состоящую из N-метил-N-(п-толуолсульфонил)-2-хлор-6- фторбензогидразоноилхлорида (2,25 г), 2-хлор-4-(5- трифторметилпиридин-2-илокси)бензонитрила (1,88 г), безводного хлорида железа /III/ (1,07) и o-дихлорбензола (5 мл), в течение 30 минут перемешивали на масляной бане при 140oC. После охлаждения полученную смесь растворяли в хлороформе (300 мл) и промывали разбавленной хлористо-водородной кислотой, разбавленным водным раствором гидроксида натрия и солевым раствором. Затем полученную смесь сушили над безводным сульфатом магния и концентрировали при пониженном давлении. Концентрат очищали методом хроматографии на силикагеле, с использованием в качестве элюента смешанного растворителя гексанэтилацетат, в результате чего получали 1,54 г целевого соединения (температура плавления: 139.0-141.0oC).
Спектр ЯМР (60 МГц, растворитель CDCl3, величина δ: ч/млн.) 3.90 (3H, синглет); 6.90-8.40 (9H, мультиплет).
Пример 48. Получение 3-(2-хлор-6-фторфенил)-5-/3,5-дихлор-4-(3- хлор-5-трифторметилпиридин-2-илокси)фенил/-1-метил-1H-1,2,4-триазола (Соединение N 401).
Смесь, состоящую из N-метил-N-(п-толуолсульфонил)-2-хлор-6- фторбензогидразоноилхлорида (1.00 г), 3,5-дихлор-4-(3-хлор-5- трифторметилпиридин-2-илокси)бензонитрила (1,00 г), безводного хлорида железа /III/ (0,50 г) и o-дихлорбензола (5 мл), в течение 30 минут перемешивали на масляной бане при 140oC. После охлаждения смесь растворяли в хлороформе (100 мл) и промывали разбавленной хлористо-водородной кислотой, разбавленным водным раствором гидроксида натрия и солевым раствором. Затем полученную смесь сушили над безводным сульфатом магния и концентрировали при пониженном давлении. Концентрат очищали методом хроматографии на колонке с силикагелем, используя в качестве элюента смешанный растворитель гексанэтилацетат, в результате чего получали 0,60 г целевого соединения.
Спектр ЯМР (60 МГц, растворитель CDCl3, величина δ: ч/млн.) 4.10 (3H, синглет), 6.73-7.52 (3H, мультиплет), 7.80 (2H, синглет), 7.97-8.10 (1H, мультиплет), 8.12-8.26 (1H, мудьтиплет).
Пример 49. Получение 5-/3-хлор-4-(3-хлор-5-трифторметилпиридин- 2-илокси)фенил/-3-(2,6-дифторфенил)-1-метил-1H-1,2,4-триазола (Соединение N 409).
Смесь, состоящую из N-метил-N-(бензолсульфонил)-2,6- дифторбензогидразоноилхлорида (0,90 г), 3-хлор-4-(3-хлор-5- трифторметилпиридин-2-илокси)бензонитрила (0,90г), безводного хлорида железа /III/ (0,50 г) и o-дихлорбензола (5 мл), в течение 30 минут перемешивали на масляной бане при температуре 140oC. После охлаждения смесь растворяли в хлороформе (100 мл) и промывали разбавленной хлористо-водородной кислотой, разбавленным водным раствором гидроксида натрия и солевым раствором. Затем полученную смесь сушили над безводным сульфатом магния и концентрировали при пониженном давлении. Концентрат очищали методом хроматографии на колонке с силикагелем, используя в качестве элюента смешанный растворитель гексанэтилацетат, в результате чего получали 0,70 г целевого соединения.
Спектр ЯМР (60 МГц, растворитель CDCl3, значение δ: ч/млн.) 4.10 (3H, синглет); 6.72-8.06 (7H, мультиплет), 8.14-8.30 (1H, мультиплет).
Пример 50. Получение 5-/3-хлор-4-(3-хлор-5-трифторметил-пиридин- 2-илокси)фенил/-3-(2-хлор-6-фторфенил)-1-метил-1H-1,2,4-триазола (Соединение N 410).
Смесь, состоящую из N-метил-N-(п-толуолсульфонил)-2-хлор-6- фторбеизогидразоноилхлорида (0,80 г), 3-хлор-4-(3-хлор-5- трифторметилпиридин-2-илокси)бензонитрила (0,80 г), безводного хлорида железа /III/ (0,40 г) и o-дихлорбензола (5 мл), в течение 30 минут перемешивали на масляной бане при температуре 140oC. После охлаждения смесь растворяли в хлороформе (100 мл) и промывали разбавленной хлористо-водородной кислотой, разбавленным водным раствором гидроксида натрия и солевым раствором. Затем смесь сушили над безводным сульфатом магния и концентрировали при пониженном давлении. Концентрат очищали методом хроматографии на колонке с силикагелем, используя в качестве элюента смешанный растворитель гексанэтилацетат, с получением 0,60 г целевого соединения.
Спектр ЯМР (60 МГц, растворитель CDCl3, значение δ: ч/млн) 4.16 (3H, синглет), 6.92-8.16 (7H, мультиплет), 8.24-8.40 (1H, мультиплет).
Пример 51. Получение 5-/3-хлор-4-(5-трифторметилпиридин-2- илокси)фенил/-3-(2,6-дифторфенил)-1-метил-1H-1,2,4-триазола (Соединение N 412).
Смесь, состоящую из N-метил-N-(бензолсульфонил)-2, 6- дифторбензогидразоноилхлорида (1,72 г), 3-хлор-4-(5-трифторметил-пиридин-2-илокси)бензонитрила (1,50 г), безводного хлорида железа /III/ (0,85 г) и о-дихлорбензола (10 мл), в течение 30 минут перемешивали на масляной бане при 140oC. После охлаждения смесь растворяли в хлороформе (200 мл) и промывали разбавленной хлористо-водородной кислотой, разбавленным водным раствором гидроксида натрия и солевым раствором. Затем смесь сушили над безводным сульфатом магния и концентрировали при пониженном давлении. Концентрат очищали методом хроматографии на колонке с силикагелем, используя в качестве элюента смешанный растворитель гексанэтилацетат и промывали гексаном с получением 1,25 г целевого соединения.
Спектр ЯМР (60 МГц, растворитель CDCl3, величина δ: ч/млн.) 3.11 (3H, синглет); 6.80-8.40 (9H, мультиплет).
Пример 52. Получение 3-(2-хлор-6-фторфенил)-5-/3-хлор-4- (5-трифторметилпиридин-2-илокси)фенил/-1-метил-1H-1, 2,4-триазола (Соединение N 413).
К N,N-диметилформамиду (50 мл) добавляли 3-(2-хлор-6- фторфенил)-5-(3-хлор-4-гидроксифенил)-1-метил-1H-1,2,4-триазол (3,04 г), 2-хлор-5-трифторметил пиридин (1,70 г) и карбонат калия (1,40 г), после чего полученную смесь в течение 2 часов и в условиях перемешивания нагревали при 120oC. После охлаждения до комнатной температуры реакционный раствор переливали в воду и экстрагировали этилацетатом и органический слой промывали водой и сушили над безводным сульфатом магния. После концентрирования при пониженном давлении, сырое твердое вещество очищали методом хроматографии на колонке с силикагелем, используя в качестве элюента смешанный растворитель гексанэтилацетат с получением 3.30 г целевого соединения (температура плавления: 116,0-117.0oC).
Спектр ЯМР (60 МГц, растворитель CDCl3, значение δ: ч/млн.) 4.10 (3H, синглет), 6.90-8.30 (9H, мультиплет).
Пример 53. Получение 3-(2-хлор-6-фторфенил)-5-/3-перфторбутил-4- (3-хлор-5-трифторметилпиридин-2-илоксиметил)фенил/-1-метил-1H-1,2,4- триазола (Соединение N 451).
3-(2-Хлор-6-фторфенил)-1-метил-5-(3-перфторбутил-4- гидроксиметилфенил)-1H-1,2,4-триазол (1.00 г) растворяли в 1,2-диметоксиэтане (20 мл) и охлаждали до 0oC. К полученной смеси добавляли гидрид натрия (60%, 0,08 г) и смесь перемешивали в течение 30 минут. Прикапывали раствор 2,3-дихлор-5-трифторметил пиридина (0,44 г) в 1,2-диметоксиэтане (10 мл) и полученную смесь перемешивали в течение 3 часов. После завершения реакции реакционный раствор нагревали до комнатной температуры, переливали в воду и экстрагировали эфиром. Органический слой промывали водой, сушили над безводным сульфатом магния и концентрировали при пониженном давлении. Концентрат очищали методом хроматографии на колонке с силикагелем с получением 1,00 г целевого соединения (температура плавления: 123.0-127.0oC).
Спектр ЯМР (60 МГц, растворитель CDCl3, величина δ: ч/млн.) 4.08 (3H, синглет); 5.73 (2H, синглет); 6.85-7.40 (4H, мультиплет); 7.75-8.27 (4H, мультиплет).
Пример 54. Получение 3-(2-хлор-6-фторфенил)-5-/3-перфторбутил-4- (5-трифторметилпиридин-2-илоксиметил)фенил/-1-метил-1H-1,2,4-триазола (Соединение N 453).
3-(2-Хлор-6-фторфенил)-1-метил-5-(3-перфторбутил-4- гидроксиметилфенил)-1H-1,2,4-триазол (1,00 г) растворяли в 1,2-диметоксиэтане (20 мл) и охлаждали до 0oC. В полученную смесь добавляли гидрид натрия (60%, 0,08 г) и смесь перемешивали в течение 30 минут. Прикапывали раствор 2-хлор-5-трифторметилпиридина (0,36 г) в 1,2-диметоксиэтане (10 мл) и смесь перемешивали в течение 5 часов. После завершения реакции реакционный раствор нагревали до комнатной температуры, переливали в воду и экстрагировали эфиром. Органический слой промывали водой, сушили над безводным сульфатом магния и концентрировали при пониженном давлении. Концентрат очищали методом хроматографии на силикагеле с получением 0,70 г целевого соединения (показатель преломления: 1,5020).
Спектр ЯМР (60 МГц, растворитель CDCl3, величина δ: ч/млн.) 4.12 (3H, синглет), 5.7 (2H, синглет), 6.80-8.53 (9H, мультиплет).
Пример 55. Получение 3-(2-хлор-6-фторфенил)-1-метил-6-/3- метил-4-(4-трифторметоксифенил)фенил/-1H-1,2,4-триазола (Соединение N 457).
Смесь, состоящую из
N-метил-N-(метансульфонил)-2-хлор-6- фторбензогидразоноилхлорида (1,50 г), 3-метил-4-(4-трифторметоксифенил бензонитрила (1,42 г), безводного хлорида железа /III/ (0,90 г) и хлорбензола (10 мл) в
течение 30 минут перемешивали на масляной бане при температуре 140oC. После охлаждения смесь растворяли в хлороформе (300 мл) и промывали разбавленной хлористо-водородной кислотой,
разбавленным водным раствором гидроксида натрия и солевым раствором. Затем смесь сушили над безводным сульфатом магния и концентрировали при пониженном давлении. Концентрат очищали методом
хроматографии на колонке с силикагелем, используя в качестве элюента смешанный растворитель гексанэтилацетат, с получением 1,64 г целевого соединения (температура плавления: 117.0-122.0o
C)
Спектр ЯМР (60 МГц, растворитель CDCl3, величина δ: ч/млн.) 2.23 (3H, синглет), 4.10 (3H, синглет); 6.90-7.70 (10H, мультиплет).
Пример 56. Получение 3-(2-хлорфенил)-1-метил-5-/4-метил-3- (5-трифторметилпиридин-2-илокси)фенил/-1H-1,2,4-триазола (Соединение N 509).
Смесь, состоящую из N-метил-N-(п-толуодсульфонил)-2-хлор- бензогидразоноилхлорида (1,1 г), 4-метил-3-(5- трифторметилпиридин-2-илокси)бензонитрила (1.00 г), безводного хлорида железа /III/ (0,60 г и o-дихлорбензола (5 мл) в течение 30 минут перемешивали на масляной бане при температуре 140oC. После охлаждения смесь растворяли в хлороформе (100 мл) и промывали разбавленной хлористо-водородной кислотой, разбавленным водным раствором гидроксида натрия и солевым раствором. Затем смесь сушили над безводным сульфатом магния и концентрировали при пониженном давлении. Концентрат очищали методом хроматографии на колонке с силикагелем, используя в качестве элюента смешанный растворитель гексанэтилацетат, в результате чего получали 0,50 г целевого соединения.
Спектр ЯМР (60 МГц, растворитель CDCl3, величина δ: ч/млн.) 2,26 (3H, синглет), 4.07 (3H, синглет), 6.96-8.16 (9H, мультиплет), 8.36-8.52 (1Н, мультиплет).
Пример 57. Получение 3-(2-хлор-6-фторфенил)-1-метил-5-/4- метил-3-(5-трифторметилпиридин-2-илокси)фенил/-1H-1,2,4-триазола (Соединение N 510).
Смесь, состоящую из N-метил-N-(п-толуолсульфонил)-2-хлор-6- фторбензогидразоноилхлорида (1,10 г), 4-метил-3-(5- трифторметилпиридин-2-илокси)бензонитрила ( δ: 90 г), безводного хлорида железа /III/ (0,60 г) и о-дихлорбензола (5 мл) перемешивали в течение 30 минут на масляной бане при температуре 140oC. После охлаждения смесь растворяли в хлороформе (100 мл) и промывали разбавленной хлористо-водородной кислотой, разбавленным водным раствором гидроксида натрия и солевым раствором. Затем смесь сушили над безводным сульфатом магния и концентрировали при пониженном давлении. Концентрат очищали методом хроматографии на колонки с силикагелем, используя в качестве элюента смешанный растворитель гексанэтилацетат с получением 0,60 г целевого соединения.
Спектр ЯМР (60 МГц, растворитель CDCl3, величина, δ: ч/млн.) 2,24 (3H, синглет), 4.12 (3H, синглет), 6.85-8.07 (8H, мультиплет), 8.36-8.52 (1H, мультиплет).
Пример 58. Получение 3-(2-хлор-6-фторфенил)-5-/4-метокси-3-(5- трифторметилпиридин-2-илокси)фенил/-1H-1,2,4-триазола (Соединение N 516).
Смесь, состоящую из N-метил-N-(п-толуолсульфонил)-2-хлор-6- фторбензогидразоноилхлорида (1.00 г), 4-метокси-3-(5- трифторметилпиридин-2-илокси)бензонитрила (0,90 г), безводного хлорида железа /III/ (0,50 г) и o-дихлорбензола (5 мл), перемешивали в течение 30 минут на масляной бане при температуре 140oC. После охлаждения смесь растворяли в хлороформе (100 мл и промывали разбавленной хлористо-водородной кислотой, разбавленным водным раствором гидроксида натрия и солевым раствором. Затем ее сушили над безводным сульфатом магния и концентрировали при пониженном давлении. Концентрат очищали методом хроматографии, используя в качестве элюента смешанный растворитель гексанэтилацетат с получением 0,50 г целевого соединения.
Спектр ЯМР (60 МГц, растворитель CDCl3, величина δ: ч/млн.) 3.85 (3H, синглет), 4.14 (3H, синглет), 6.92-8.08 (8H, мультиплет), 8.35-8.52 (1H, мультиплет).
Пример 59. Получение 3-(2, 6-дифторфенил)-5-/4-метокси-3-(5- трифторметилпиридин-2-илокси)фенил/-1-метил-1H-1,2,4-триазола (Соединение N 517).
Смесь, состоящую из N-метил-N-(бензолсульфонил)-2, 6- дифторбензогидразоноилхлорида (0,70 г), 4-метокси-3-(5- трифторметилпиридина-2-илокси)бензонитрила (0,80 г), безводного хлорида железа /III/ (0,60 г) и o-дихлорбензола (5 мл), перемешивали в течение 30 минут на масляной бане при температуре 140oC. После охлаждения смесь растворяли в хлороформе (100 мл) и промывали разбавленной хлористо-водородной кислотой, разбавленным водным раствором гидроксида натрия и солевым раствором. Затем полученную смесь сушили над безводным сульфатом магния и концентрировали при пониженном давлении. Концентрат очищали методом хроматографии на колонке с силикагелем, используя в качестве элюента смешанный растворитель гексанэтилацетат в результате чего получали 0,30 г целевого соединения.
Спектр ЯМР (60 МГц, растворитель CDCl3, величина δ: ч/млн.) 3.84 (3H, синглет); 4.10 (3H, синглет), 6.75-8.10 (8H, мультиплет), 8.30-8.47 (1H, мультиплет).
Пример 60. Получение 3-(2-хлор-6-фторфенил)-5-/3-(3-хлор-5- трифторметилпиридин-2-илокси)-5-метоксифенил/-1-метил-1H-1,2,4-триазола (Соединение N 523).
Смесь, состоящую из N-метил-N-(п-толуолсульфонил)-2-хлор-6- фторбензогидразоноилхлорида (0,90 г), 3-(3-хлор-5- трифторметилпиридин-2-илокси)-5-метоксибензонитрила (0,80 г), безводного хлорида железа /III/ (0,80 г) и o-дихлорбензола (5 мл), в течение 30 минут перемешивали на масляной бане при температуре 140oC. После охлаждения смесь растворяли в хлороформе (100 Мл) и промывали разбавленной хлористо-водородной кислотой, разбавленным водным раствором гидроксида натрия и солевым раствором. Затем смесь сушили над безводным сульфатом магнии и концентрировали при пониженном давлении. Концентрат очищали методом хроматографии на колонке с силикагелем, используя в качестве элюента смешанный растворитель гексанэтилацетат, в результате чего получали 0,60 г целевого соединения.
Спектр ЯМР (60 МГц, растворитель CDCl3 величина δ: ч/млн.) 3.92 (3H, синглет), 4.12 (3H, синглет), 6.85-7.53 (6H, мультиплет); 7.96-8.06 (1H, мультиплет), 8.23-8.40 (1H, мультиплет).
Пример 61. Получение 3-(2-хлор-6-фторфенил)-5-/3-метокси-4-(5- трифторметилпиридин-2-илокси)фенил/-1-метил-1H-1,2,4- триазола (Соединение N 524).
Смесь, состоящую из N-метил-N-(п-толуолсульфонил)-2-хлор-6- фторбензогидразоноилхлорида (3.75 г), 3-метокси-4-(5- трифторметилпиридин-2-илокси)бензонитрида (3.03), безводного хлорида железа /III/ (1.70 г) и o-дихлорбензола (5 мл), перемешивали в течение 30 минут на масляной бане при температуре 140oC. После охлаждения смесь растворяли в хлороформе (300 мл) и промывали разбавленной хлористо-водородной кислотой, разбавленным водным раствором гидроксида натрия и солевым раствором. Затем смесь сушили над безводным сульфатом магния и концентрировали при пониженном давлении. Концентрат очищали методом хроматографии на колонке с силикагелем, используя в качестве элюента смешанный растворитель гексанэтилацетат и промывали гексаном с получением 2,80 г целевого соединения.
Спектр ЯМР (60 МГц, растворитель CDCl3, величина δ: ч/млн.) 2.97 (3H, синглет), 3.07 (3H, синглет), 6.90-8.30 (9H, мультиплет).
Пример 62. Получение 3-(2-хлор-6-фторфенил)-5- трифторметилпиридин-2-илокси)-3-метоксифенил/-1-метил-1H-1,2,4- триазола (Соединение N 526).
Смесь, состоящую их N-метил-N-(п-толуолсульфонил)-2-хлор-6- фторбензогидразоноилхлорида (0,90 г), 4-(3-хлор-5-трифторметил-пиридин-2-илокси)-3-метоксибензоцитрила (0,90 г), безводного хлорида железа /III/ (0,50 г) и o-дихлорбензола (5 мл), перемешивали в течение 30 минут на масляной бане при температуре 140oC. После охлаждения смесь растворяли в хлороформе (100 мл) и промывали разбавленной хлористо-водородной кислотой, разбавленным водным раствором гидроксида натрия и солевым раствором. Затем смесь сушили над безводным сульфатом магния и концентрировали при пониженном давлении. Концентрат очищали методом хроматографии на колонке с силикагелем, используя в качестве элюента смешанный растворитель гексанэтилацетат, с получением 0,60 г целевого соединения.
Спектр ЯМР (60 МГц, растворитель CDCl3, величина δ: ч/млн.) 3.81 (3H, синглет), 4.13 (3H, синглет), 6.90-7.60 (6H, мультиплет), 7.93-8.06 (1H, мультиплет), 8.16-8.30 (1H, мультиплет).
Пример 63. Получение 5-(2-хлор-4-гексилфенил)-3-(2-хлор-фенил)-1- метил-1H-1,2,4-триазола (Соединение N 40).
Смесь, состоящую из N-метил-N-фенилсульфонил-2- хлорбензамидразона (3,24 г) и 2-хлор-4-гексилбензоилхлорида (3.37 г), в течение 4 часов перемешивали на масляной бане при температуре 170-180oC. После охлаждения до комнатной температуры в смесь добавляли этилацетат и органический слой промывали водой. Затем проводили сушку над безводным сульфатом магния и концентрирование при пониженном давлении. Концентрат очищали методом хроматографии на колонке с силикагелем, используя в качестве элюента смешанный растворитель гексанэтилацетат, в результате чего получали 0,85 г целевого соединения (показатель преломления: 1.5830).
Спектр ЯМР (60 МГц, растворитель CDCl3, значение δ: ч/млн.) 0,90 (3H, триплет), 1.00-1.90 (8H, мультиплет), 2.67 (2H, триплет), 3.87 (3H, синглет), 7,10-7.60 (6H, мультиплет), 7.90-8.05 (1H, мультиплет).
Справочный пример 1. Получение N-метил-N- (бензолсульфонил)-2-хлорбензамидоразона.
N-метил-N-(бензолсульфонил)-2-хлорбензгидразоноилхлорид (17.2 растворяли в N,N-диметилформамиде и полученную смесь перемешивали в течение 3 часов при 60-70oC, вводя в систему газообразный аммиак. После охлаждения полученную смесь растворяли в 500 мл этилацетата и промывали водой. Затем полученную систему сушили над безводным сульфатом магния и концентрировали при пониженном давлении и сырое твердое вещество промывали гексаном с получением 15,4 г целевого соединения (температура плавления: 94.0-96.0oC.
Спектр ЯМР (60 МГц, растворитель CDCl3, величина δ: ч/млн.) 2.75 (3H, синглет), 5.80 (2H, синглет), 7.10-8.00 (9H, мультиплет).
Справочный пример 2. Получение 3-(2-хлор-6-фторфенил)-5-(3-хлор- 4-метил-фенил)-1-метил-1H-1,2,4-триазола.
Смесь, состоящую из N-метил-N-(п-толуолсульфонил)-2-хлор-6- фторбензогидразоноилхлорида (7.50 г), 3-хлор-4-метил-бензонитрила (3.33 г), безводного хлорида алюминия (3.00 г) и o-дихлорбензола (20 мл), перемешивали в течение 1 часа на масляной бане при температуре 140oC. После охлаждения полученную смесь промывали солевым раствором. Затем ее сушили над безводным сульфатом магния и концентрировали при пониженном давлении. Концентрат очищали методом хроматографии на колонке с силикагелем, используя в качестве элюента смешанный растворитель гексанэтилацетат, в результате чего получали 3.70 г целевого соединения.
Справочный пример 3. Получение 5-(4-бромометил-3-хлор-фенил)- 3-(2-хлор-6-фторфенил)-1-метил-1,2,4-триазола.
К четыреххлористому углероду (50 мл) добавляли 3-(2-хлор-6- фторфенил)-5-(3-хлор-4-метилфенил)-1-метил-1H-1,2,4-триазол (3.37 г), N-бромсукцинимид (2,14 г) и азобисбутиронитрил (30 мг), после чего полученную смесь нагревали в течение 1 часа с обратным холодильником в условиях перемешивания. После охлаждения реакционной смеси, нерастворившееся вещество отфильтровывали и фильтрат концентрировали при пониженном давлении. Концентрат очищали методом хроматографии на колонке с силикагелем, используя в качестве элюента смешанный растворитель гексанэтилацетат, в результате чего получали 2,51 г целевого соединения (температура плавления 124.0-126.0oC).
Справочный пример 4. Получение 5-(4-ацетоксиметил-3-хлорфенил)- 3-(2-хлор-6-фторфенил)-1-метил-1H-1,2,4-триазола.
К N, N-диметилформамиду (200 мл добавляли 5-(4-бромометил-3- хлорфенил)-3-(2-хлор-6-фторфенил)-1-метил-1H-1,2,4-триазол (24.3 г) и ацетат калия (29.0 г), после чего полученную систему перемешивали в течение 3 часов при 130oC. Реакционную смесь охлаждали до комнатной температуры, переливали в воду и экстрагировали этилацетатом. Органический слой промывали водой, сушили над безводным сульфатом магния и концентрировали при пониженном давлении. Концентрат очищали методом хроматографии на колонке с силикагелем, используя смешанный растворитель гексанэтилацетат в качестве элюента, в результате чего получали 11,8 г целевого соединения.
Спектр ЯМР (60 МГц, растворитель CDCl3, величина δ: ч/млн.) - 2.13 (3H, синглет), 4.07 (3H, синглет), 5.24 (2H, синглет), 6.90-7.85 (6H, мультиплет).
Справочный пример 5. Получение 3-(2-хлор-6-фторфенил)-5-(3- хлор-4-гидроксиметилфенил-1-метил-1H-1,2,4-триазола.
5-(4-Ацетоксиметил-3-хлорфенил)-3-(2-хлор-6-фторфенил)-1- метил-1H-1,2,4-триазол (11,1 г) растворяли в смешанном растворителе, состоящем из этанола (50 мл) и воды (20 мл), добавляли гидроксид натрия (2,3 г) и полученную смесь нагревали в течение 1 часа с обратным холодильником в условиях перемешивания. После охлаждения до комнатной температуры, в реакционную смесь добавляли этилацетат и систему промывали водой. Затем полученную смесь сушили над безводным сульфатом магния и концентрировали при пониженном давлении с получением сырого твердого вещества. Такое сырое твердое вещество промывали смешанным растворителем гексан-этанол в результате чего получали 6,7 г целевого соединения (температура плавления: 111-113oC).
Спектр ЯМР (60 МГц, растворитель CDCl3, величина δ: ч/млн.) 3.50 (1H, триплет), 4.05 (3H, синглет), 4.75 (2H, дублет); 6.95-7.70 (6H, мультиплет).
Справочный пример 6. Получение 3-(2-хлор-6-фторфенил)-5-(3- хлор-4-гидроксифенил)-1-метил-1H-1,2,4-триазола.
К o-дихлорбензолу (200 мл) добавляли 3-хлор-4-метоксибензонитрил (40,3 г) и безводный хлорид железа /III/ (42,2 г), после чего полученную смесь нагревали при 120oC в условиях перемешивания. К такой смеси, в течение 30 минут при 120oC и в условиях перемешивания, прикапывали раствор N-метил-N-(п-толуолсульфонил)- 2-хлор-6-фторбензогидразоноилхлорида (62,2 г) в o-дихлорбензоле (300 мл) и полученную систему дополнительно перемешивали в течение 3 часов при температуре 120oC. После охлаждения до комнатной температуры реакционную смесь переливали в большое количество воды и экстрагировали хлороформом. В органический слой добавляли 10% водный раствор NaOH (200 мл) и 25% водный раствор аммиака (200 мл) и полученную систему перемешивали в течение 1 часа при температуре 50oC. После охлаждения до комнатной температуры органический слой промывали водой, сушили над безводным сульфатом магния, концентрировали при пониженном давлении, в результате чего получали 70,5 г сырого продукта, представляющего собой 3-(2-хлор-6- фторфенил)-5-(3-хлор-4-метоксифенил)-1-метил-1H-1,2,4-триазол.
В бензол (300 мл) добавляли сырой продукт, представляющий собой 3-(2-хлор-6-фторфенил)-5-(3-хлор-4-метоксифенил)-1-метил-1H-1,2,4- триазол (70,5 г) и безводный хлорид алюминия (80,0 н) и полученную смесь нагревали с обратным холодильником в течение 3 часов в условиях перемешивания. После охлаждения до комнатной температуры реакционную смесь переливали в ледяную воду и экстрагировали толуолом. Органический слой промывали водой, экстрагировали 20% водным раствором NaOH и водный слой подкисляли путем добавления небольшого количества концентрированной серной кислоты при охлаждении системы льдом, после чего систему экстрагировали этилацетатом. Органический слой промывали водой, сушили над безводным сульфатом магния и концентрировали при пониженном давлении с получением 64,2 г целевого соединения.
Спектр ЯМР (60 МГц, растворитель CDCl3, величина δ: ч/млн.) 4.10 (3H, синглет); 7.00-7.90 (6H, мультиплет), 10.85 (1H, синглет).
Инсектицид и акарицид согласно настоящему изобретению содержит в качестве активного ингредиента производное триазола, отвечающее общей формуле (I).
В том случае, когда соединения настоящего изобретения используются в качестве инсектицидов и акарицидов, эти соединения могут применяться как таковые, или могут сочетаться с функциональными добавками, такими как носитель поверхностно-активный агент, диспергирующий агент, присадки и т.п., которые обычно используются для приготовления рецептур, в результате чего получают дусты, смачиваемые порошки, эмульсии, порошки тонкого помола, грануляты и т. п. В качестве носителей, используемых для приготовления таких рецептур, можно отметить такие твердые носители, как зееклит, тальк, бентонит, глина, каолин, диатомовая земля, белая сажа, вермикулит, гидроксид кальция, кварцевый песок, сульфат аммония, мочевина и т.п., и такие жидкие носители, как изопропиловый спирт, ксилол, циклогексан, метилнафталин и т.п. В качестве поверхностно-активных агентов и диспергирующих агентов следует отметить алкилбензолсульфонаты металлов, динафтилметандисульфонаты металлов, соль сложного эфира серной кислоты и спирта, алкиларилсульфонат, лигнин сульфонат, простор эфир полиоксиэтиленгликоля, простой полиоксиэтиленалкилариловый эфир, полиоксиэтиленсорбит моноалкилат и т. п. В качестве присадок могут использоваться карбоксиметил целлюлоза, полиэтилен гликоль, аравийская камедь и т.п. При применении активный ингредиент может использоваться путем распыления растворов с требуемой концентрацией или использоваться непосредственно.
Инсектициды и акарициды настоящего изобретения могут использоваться путем распыления на стебли или листву растений, применяться на почве, на ящиках для рассады, распыляться на поверхности воды и т.п. Количество активного ингредиента в рецептуре, если это необходимо, может быть подобрано в каждом конкретном случае, однако, в случае дуста или гранул это количество может быть выбрано из интервала 0,05-20% (вес.), предпочтительны 0,1-10% (вес.). В случае эмульсий или смачиваемых порошков подходящее количество активного ингредиента лежит в интервале 0,5-80% (вес.). Предпочтительно выбирать такое количество из интервала 1-60% (вес.).
Применяемое количество инсектицида или акарицида согласно настоящему изобретению зависит от типа используемого соединения, вида вредных насекомых подлежащих уничтожению, поправимости и степени поражения насекомыми, окружающих условий, типа используемой рецептуры и т.п. В случае непосредственного применения в виде дуста или гранул, надлежащее количество активного ингредиента может выбираться из интервала 0,05 г - 5 кг, предпочтительно, 0.1 г - 1 кг в расчете на площадь в 10 аров. При использовании в жидком виде, как это имеет место в случае эмульсии или смачиваемого порошка, надлежащее количество может быть выбрано из интервала 0,1-5.000 ч/млн., предпочтительно, 1-1.000 ч/млн. Следует также отметить, что инсектициды и акарициды настоящего изобретения могут использоваться в смеси с другим инсектицидом, фунгицидом, удобрением и регулятором роста растений.
Далее следует конкретное описание рецептур со ссылкой на типичные примеры. Следует иметь в виду, что тип соединений и присадок, а также их соотношения в рецептуре не ограничиваются приведенными примерами и могут изменяться в широких интервалах. Если не указано особо, то % приведен в весовом выражении.
Рецептурный пример 1. Эмульсия.
Эмульсию готовили путем однородного растворения 30% соединения (41), 20% циклогексанона, 1% полиоксиэтилен алкиларилового эфира, 4% алкилбензолсульфоната кальция и 35% метилнафталина.
Рецептурный пример 2. Смачиваемый порошок.
Смачиваемый порошок готовили путем однородного смешивания и порошкования 40% соединения (389), 15% диатомовой земли, 15% глины, 25% белой сажи, 2% динафтилметан дисульфоната натрия и 3% лигнин сульфоната натрия.
Рецептурный пример 3. Дуст.
Дуст готовили путем однородного смешивания и порошкования 2% соединения (116), 5% диатомовой земли и 93% глины.
Рецептурный пример 4. Гранулы.
5% соединения (41), 2% натриевой соли сложного эфира лаурилового спирта и серной кислоты, 5% лигнин сульфоната натрия, 2% карбоксиметил целлюлозы и 86% глины подвергали однородному смешиванию и порошкованию. Затем 100 весовых частей такой смеси смешивали с 20 вес. частями воды, формовали в гранулы размером 14-32 меш на грануляционном устройстве экструзионного типа и сушили с целью получения гранулята.
Производные триазола согласно настоящему изобретению представляют собой эффективные средства для уничтожения таких дельфацид, как коричневая толстоголовка, бело-спинная толстоголовка, мелкая коричневая толстоголовка и т.п., таких цикадок, как зеленая рисовая цикадка, чайная заленая цикадка и т.п., такой тли, как тля хлопковая, тля персиковая, тля капустная и т.п., таких белокрылок, как белокрылка тепличная и т.п., таких вредных гемиптерановых насекомых как щитовки, например, тутовая щитовка и т.п., а также клопов, например, клоп рисовый или т.п., таких вредных чешуекрылых насекомых, как моль капустная, свекольная гусеница, совка обычная и т.п., таких двукрылых вредных насекомых, как муха домашняя, комары и т.п., таких элитровых вредных насекомых, как долгоносик рисовый, зерновка фасолевая, тыквенный листоед и т.п., таких вредных прямокрылых насекомых, как таракан американский, таракан рыжий и т.п., а также таких клещей, как клещик паутинный двупятнистый, клещик пактиннный Канзава, клещик красный цитрусовый и т.п. Особенно сильное уничтожающее действие соединения настоящего изобретения оказывают на таких клещей, как клещик паутинный двупятнистый, клещик паутинный Канзава, клещик красный цитрусовый и т.п. и на такую тлю, как тля хлопковая, тля персиковая, тля капустная и т.п.
Далее, действие соединений настоящего изобретения будет описано со ссылкой на следующие ниже испытательные примеры. В тех де рецептурах, что и тестовые соединения, использовали соединения, отвечающие химической формуле 3 в IB-A-56-154464, в качестве сравнительных химических соединений а-b и соединения, описанные в Техническом отчете РД278004, в качестве сравнительных химических соединений с-d.
Сравнительное химическое соединение: a: 3,5-бис(2-хлорфенил)- 1-метил-1H-1,2,4-триазол;
Сравнительное химическое соединение b:
3-(2-хлорфенил)-1- метил-5-(3-метилфенил)-1H-1,2,
4-триазол;
Сравнительное химическое соединение c: 3-(2-хлорфенил)-1- метил-5-(3-хлор-2-метилфенил)-1H-1,2,4-триазол;
Сравнительное
химическое соединение d:
3-(2-хлор-6-фторфенил)-1- метил-5-(2,4-дихлорфенил)-1H-1,2,4-триазол.
Испытательный пример 1. Акарицидный тест на клещика паутинного двупятнистого.
Смачиваемый порошок, полученный в соответствии с Рецептурным примером 2, разбавляли водой таким образом, чтобы концентрация активного ингредиента составила 500 ч/млн. В полученный в результате смачиваемый порошок погружали сеянцы сои, предварительно инокулированные взрослыми особями клещика паутинного двупятнистого, и затем их высушивали на воздухе. После такой обработки соевые саженцы помещали на 14 дней в термостатированную камеру при температуре 25oC и затем подсчитывали количество выживших взрослых особей с целью расчета процента эффективности уничтожения в соответствии с расчетной формулой (1). Эффективность уничтожения оценивали в соответствии со стандартом, приведенным в Таблице 3. Подученные результаты представлены в Таблице 4 (в конце описания). Все испытания дублировались.
Расчетная формула (1):
Эффективность уничтожения = 1 - число взрослых особей до обработки на необработанном участке/число взрослых особей до
обработки на
обработанном участке через определенный срок • число взрослых особей на обработанном участке/число взрослых особей через определенный срок на необработанном участке •
100
Таблица 3
Эффективность уничтожения - Оценка
Эффективность уничтожения не менее 90% - A
Эффективность уничтожения не менее 70%, но ниже 90% - B
Эффективность
уничтожения не менее 50%, но ниже 70% - C
Эффективность уничтожения менее 50% - D
Испытательный пример 2.
Инсектинидный тест на моль капустную.
Смачиваемый порошок, полученный в соответствии с Рецептурным примером 2, разбавляли водой таким образом, чтобы концентрация активного ингредиента составила 500 ч/млн. Капустные листья погружали в полученный в результате разбавления раствор, сушили на воздухе и затем помещали в хлорвиниловую чашку. В чашку выпускали гусениц моли капустной и на чашку помещали крышку. Далее, чашку помещали на 6 дней в термостатированную камеру при температуре 25oC и подсчитывали число погибших гусениц с целью расчета процента смертности в соответствии с расчетной формулой (2). Смертность оценивали в соответствии со стандартом, приведенным в Таблице 5. Полученные результаты представлены в Таблице 6 (в конце описания). Каждое испытание дублировали.
Расчетная формула
(2):
Смертность =
число погибших гусениц через определенное число дней/число гусениц до обработки • 100
Таблица 5
Смертность - Оценка
Смертность не менее
90% - A
Смертность не
менее 70%, но ниже 90% - B
Смертность не менее 50%, но ниже 70% - C
Смертность менее 50% - D
Испытательный пример 3. Инсектицидный тест на
толстоголовку коричневую.
Смачиваемый порошок, полученный в соответствии с Рецептурным примером 2 разбавляли водой таким образом, чтобы концентрация активного ингредиента составила 500 ч/млн. В полученный в результате разбавленный смачиваемый порошок погружали стебли и листву риса, после чего их сушили на воздухе и помещали в испытательную пробирку. В испытательную пробирку выпускали 10 гусениц толстоголовки коричневой и отверстие пробирки закрывали гигроскопической ватой. Затем испытательную пробирку помещали на 6 дней в термостатированную камеру при температуре 25oC и подсчитывали число погибших гусениц с целью расчета процента смертности в соответствии с расчетной формулой (2). Смертность оценивали согласно стандарту, приведенному в Таблице 5. Полученные результаты представлены в Таблице 7. Все испытания дублировали.
Таблица 7
Номер соединения - Оценка
2 - A
78 - B
116 - A
311
- B
378 - B
395 - B
517 - A
524 - A
Сравнительное химическое соединение а - D
Сравнительное химическое соединение b - C
Сравнительное
химическое
соединение d - D
Испытательный пример 4. Инсектицидный тест на тлю хлопковую.
Смачиваемый порошок подученный в соответствии с Рецептурным примером 2 разбавляли водой таким образом, чтобы концентрация активного ингредиента составила 100 ч/млн. В полученный в результате, разбавленный смачиваемый порошок погружали огуречные сеянцы, предварительно инокулированные личинками тли хлопковой и затем сеянцы сушили на воздухе. После обработки огуречные сеянцы помещали на 3 дня в термостатированную камеру при температуре 25oC, после чего подсчитывали число погибших личинок с целью расчета процента смертности в соответствии с расчетной формулой (2). Смертность оценивали согласно стандарту, приведенному в Таблице 5. Полученные результаты представлены в Таблице 8 (в конце описания). Все испытания дублировали.
Реферат
Изобретение относится к новым производным триазола, проявляющим инсектицидную и акарицидную активность. Описывается производное триазола общей формулы (I), в которой R1 представляет C1-C6алкильную группу, X представляет собой атом галогена, n целое число в интервале 1-5, Y представляет собой атом галогена, нитрогруппу, C1-C15 алкильную группу, C1-C15 алкоксигруппу, C1-C6алкокси - (C1-C6) алкоксигруппу, гало(C1-C12)алкильную группу, гало(C1-C12)алкоксигруппу, C2-C6алкинилоксигруппу или группу общей формулы (II), где A представляет атом кислорода, низшую алкиленовую группу, низшую алкиленокси (низшую) алкиленовую группу; k равно 0 или 1; Q - метиновая группа или атом азота; R2 - атом водорода, атом галогена, C1-C6 алкильная группа, трифторметильная группа или трифторметоксигруппа, j - целое число от 1 до 5, при условии, что j равно 2 или более, то R2 может иметь как одинаковые, так и различные значения; m - целое число от 2 до 5 и j может иметь как одинаковые, так и различные значения. Описывается также способ получения вышеуказанных соединений, инсектицидное и акарицидное средства на основе соединения формулы (I).
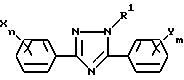
9 с. и 2 з.п.ф-лы, 8 табл.
Формула
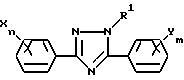
где R1 представляет собой C1-C6 алкил;
X представляет собой атом галогена;
n представляет целое число в интервале 1 - 5;
Y представляет собой атом галогена, нитрогруппу, C1-C15алкильную группу, C1-C15алкоксигруппу, C1-C6алкокси-(C1-C6)алкоксигруппу, гало(C1-C12 )алкильную группу, гало (C1-C12 )алкоксигруппу, C2-C6алкенилокси, C2-C6алкинилоксигруппу или группу общей формулы
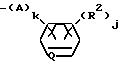
где A представляет атом кислорода, низшую алкиленовую группу, низшую алкиленоксигруппу, окси(низшую) алкиленовую группу, низшую алкиленокси (низшую) алкиленовую группу;
k - 0 или 1;
Q - представляет собой метиновую группу или атом азота;
R2 представляет собой атом водорода, атом галогена, C1-C6алкильную группу, трифторметильную группу или трифторметоксигруппу;
j представляет собой целое число от 1 до 5, при условии, что если j равно 2 или более, то R2 может иметь одинаковые, так и различные значения;
m представляет собой целое число от 2 до 5;
j может иметь как одинаковые, так и различные значения.
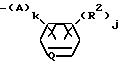
в которой A представляет собой атом кислорода, C1-C2алкиленовую группу, C1 -C2алкиленоксигруппу или C1-C2оксиалкиленовую группу;
k равно 0 или 1;
Q представляет собой метиновую группу или азотом азота;
R2 представляет собой атом водорода, атом галогена, трифторметильную группу или трифторметоксигруппу;
j представляет собой целое число от 1 до 5, при условии, что если j равно 2 или более, то R2 может иметь как одинаковые, так и различные значения;
m представляет собой целое число от 2 до 5;
Y может иметь как одинаковые, так и различные значения при условии, что если Y представляет собой атом галогена, то его значения не являются комбинацией атомов галогена.
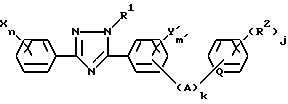
где R1 представляет собой C1-C6алкильную группу;
X представляет собой атом галогена;
n представляет целое число в интервале 1 - 5;
Y1 представляет собой атом галогена, C1-C15алкильную группу, C1-C15алкоксигруппу, C1-C8галоалкильную группу или C1-C8галоалкоксигруппу; A представляет собой атом кислорода, C1-C2алкиленовую группу, C1-C2алкиленоксигруппу или C1-C2оксиалкиленовую группу;
k = 0 или 1;
Q представляет собой метиновую группу или атом азота;
R2 представляет собой атом водорода, атом галогена, трифторметильную группу или трифторметоксигруппу;
j представляет собой целое число в интервале 1-5, при условии, что если j равно 2 или более, то R2 может иметь одинаковые или различные значения;
m' представляет собой целое число от 1 до 4;
Y' может иметь одинаковые или различные значения.
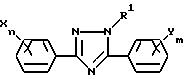
в которой R1, X, Y, m и n имеют указанные выше значения,
отличающийся тем, что осуществляют реакцию между производным N - ацилимидата или производным N - ацилтиоимидата, представленным общей формулой II
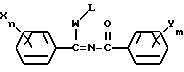
в которой W представляет собой атом серы или атом кислорода;
L представляет собой алкильную группу, содержащую 1 - 4 атома углерода;
X, Y, m и n имеют указанные выше значения,
и производным гидразина, представленным общей формулой III
R'NHNH2,
в которой R1имеет указанные выше значения.
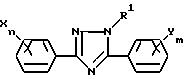
в которой R1, X, Y, m и n имеют указанные выше значения,
отличающийся тем, что проводят реакцию между производным бензогидразоноилхлорида, отвечающим общей формуле VI
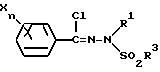
в которой R3 представляет собой фенильную группу, которая может быть замещена алкильной группой, содержащей 1 - 4 атома углерода, или алкильную группу, содержащую 1-4 атома углерода;
R1, X и n имеют указанные выше значения,
и производным бензонитрила, отвечающим общей формуле VII
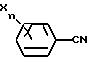
в которой Y и m и n имеют указанные выше значения.
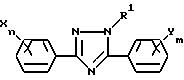
в которой R1, X, Y, m и n имеют указанные выше значения,
отличающийся тем, что проводят реакцию между производным бензамидразона общей формулы VIII
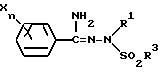
в которой R1, R3, X и n имеют указанные выше значения,
и производным бензоилгалогенида общей формулы V
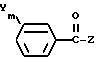
в которой Z представляет собой атом галогена и Y и m имеют указанные выше значения.
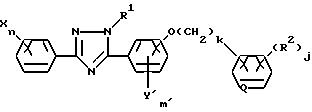
в которой R1, R2, X, Y', Q, j, k, m' и n имеют указанные выше значения,
отличающийся тем, что проводят реакцию между соединением общей формулы X
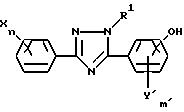
в которой R1, X, Y', m' и n имеют указанные выше значения,
и соединением общей формулы XI
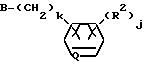
в которой B представляет собой атом галогена, R4-SO2-группу или R4 -SO-группу, где R4 представляет собой алкильную группу, содержащую 1-4 атома углерода, или фенильную группу, которая может быть замещенной;
R2, Q, j и k имеют указанные выше значения.
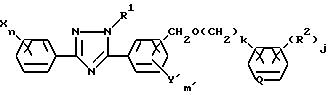
в которой R1, R2, X, Y', Q, j, k, m' и n имеют указанные выше значения,
отличающийся тем, что проводят реакцию между соединением общей формулы XVI
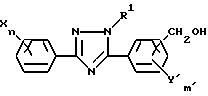
в которой R1, X, Y', m' и n имеют указанные выше значения,
и соединением общей формулы XI
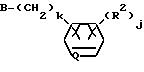
в которой B, R2, Q, j и k имеют указанные выше значения.
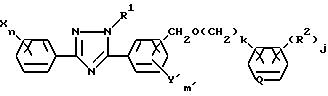
в которой R1, R2, X, Y', Q, j, k, m' и n имеют указанные выше значения,
отличающийся тем, что проводят реакцию между соединением общей формулы XIY
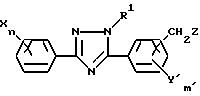
в которой R1, X, Y', Z, m' и n имеют указанные выше значения,
и соединением общей формулы XVIII
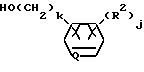
в которой R2, Q, j и k имеют указанные выше значения.

Комментарии