Способ получения сложного оксида манганита balnmno - RU2718697C1
Код документа: RU2718697C1
Чертежи
Описание
Изобретение относится к технологии получения сложных оксидов, имеющих слоистую структуру Руддлесдена-Поппера (РП) и относящихся к гомологической фазе АО⋅(ABO3)2.
Эти соединения обладают уникальными электрическими, магнитными свойствами. Актуально стоит задача разработки условий синтеза сложных оксидов, обладающих заданными физико-химическими свойствами, и исследование устойчивости этих оксидов при изменении внешних параметров. Электронные свойства этих оксидов связаны с возможностью изменения степени окисления марганца и размером иона редкоземельного элемента. Различная степень окисления марганца может быть обусловлена различным содержанием кислорода (величина δ в формуле). Варьировать содержание кислорода в образцах можно изменением давления кислорода при изотермическом отжиге материалов или изменением температуры заключительного отжига, при фиксированном давлении кислорода в газовой среде. Поэтому, основными параметрами оказывающими влияние на структуру и гомогенность соединений сложных оксидов являются температура, газовая атмосфера синтеза и его продолжительность.
Известен способ получения сверхпроводящего материала MBa2Cu3O7-х, где М - редкоземельный металл из группы Y, Nd, Sm, Eu, Dy, Ho, Er, Tm, Yb, Lu, в котором смесь нитрата бария, оксида меди и оксида редкоземельного металла из указанной группы в атомном соотношении М:Ва:Cu = 1:2:3, нагревают в тигле из золота или серебра до 850-960°C, причем, в области температур выше 600-640°C нагревание ведут со скоростью 50-100°C/ч., затем расплав выдерживают при 850-960°C 1-3 ч., охлаждают в кислородсодержащей атмосфере со скоростью 50-100°C/ч. до температуры 350-450°C и выдерживают при этой температуре 1-10 ч. Далее охлаждают до комнатной температуры, извлекают из тигля, оставляя загрязненную часть на стенках и дне. Продукт размалывают, просеивают, прессуют и отжигают при 940-960°C 1-3 ч.. Затем просеивают и охлаждают до температуры 350-450°C со скоростью 50-10°C/ч. Выдерживают при этой температуре 1-10 ч. и охлаждают до комнатной температуры (патент РФ №2104939, МПК C01F 17/00, оп. 20.02.1998).
Недостатком способа является многочисленность операций термообработки и значительная общая длительность его осуществления. Используемые температуры термообработки не позволят получить сложные оксиды общей формулы BaLn2Mn2O7+δ, где в качестве лантаноида выбраны (Nd, Pr, Gd).
Известен способ получения сложного оксида редкоземельного элемента, молибдена и теллура, состава Ln2MoTe4O14, где (Ln=Pr, Nd) (Hai-Long Jiang, En Ma, and Jiang-Gao Mao. New Luminescent Solids in the Ln-W(Mo)-Te-O-(Cl) Systems // Inorganic Chemistry. 2007, 46 (17), 7012-7023). Для его получения смесь Ln2O3 (Ln=Pr, Nd), МоО3 и TeO2, взятых в количествах 0,083:0,036:0,240 г. для получения Pr2(MoO4)(Te4O10 и 0,06:0,051:0,223 г. (для получения Nd2(MoO4)(Te4O10), соответственно, нагревают в вакуумированной кварцевой ампуле в течение 6 суток при температуре 750°C (720°C), охлаждают до температуры 350°C (300°C) скоростью 3,5°C/час (3°C/час), с последующим охлаждением до комнатной температуры с печью.
Существенными недостатками способа являются применение низкой температуры, при которой невозможно формирование сложного оксида BaLn2Mn2O7+δ (Ln=Nd, Pr, Gd), недостаточно низкое давление при синтезе и высокая продолжительность процесса.
Известен способ получения сложного оксида BaNd2Mn2O7 (J. Meng, H. Satoh, M. Ishida, N. Kamegashira Phase transition of BaNd2Mn2O7 // J. of Alloys and Compounds. 2006. 408-412. 1182-1186.). Исходные компоненты BaCO3, Nd2O3 и Mn2O3 смешивали в соответствующем молярном соотношении, прессовали в таблетки и отжигали при температуре 1423 K в течение 24 ч., затем последовательно нагревали при 1623 К в течение 72 ч. и медленно охлаждали до комнатной температуры. Процесс термообработки проводили в атмосфере аргона. Результатом синтеза является поликристаллический образец BaNd2Mn2O7, имеющий орторомбическую структуру, принадлежащий к пространственной группе Fmmn.
К недостаткам этого способа можно отнести достаточно высокую температуру отжига на обеих стадиях синтеза и значительную общую продолжительность процесса.
Наиболее близким по совокупности существенных признаков можно считать способ получения сложного оксида манганита BaLn2Mn2O7 (H. Nakano, Н. Satoh, N. Kamegashira, and N. Ishizawa Phase behavior of layered manganites BaLn2Mn2O7 (Ln = rare earth) // Phys. Stat, sol.(c). 2006. N. 8. 2812-2815.). Исходные компоненты BaCO3, Ln2O3 и Mn2O3 смешивали в соответствующем молярном соотношении, прессовали в таблетки и отжигали при температуре 1073 K в течение 12 ч. в атмосфере Ar, с одновременным удалением продукта реакции CO2, затем последовательно нагревали при 1623 К в течение 48 ч. в той же газовой атмосфере и постепенно охлаждали до комнатной температуры.
В результате были получены монокристаллы и поликристаллические образцы BaLn2Mn2O7, где (Ln=Pr, Nd, Sm, Eu, Gd, Tb), имеющие различную структуру от орторомбической до тетрагональной.
К недостаткам этого способа можно отнести достаточно высокую температуру отжига на второй стадии синтеза, образование газа CO2 и необходимость его отведения, а также невозможность формирования заданной нестехиометрии сложных оксидов.
Таким образом, перед авторами стояла задача разработки способа получения сложного оксида манганита BaLn2Mn2O7+δ в гомогенном состоянии, с определенной кристаллической структурой и возможностью изменения нестехиометрии.
Техническим результатом предлагаемого способа является сокращение трудоемкости процесса, снижение температуры отжига на второй стадии, а также расширение возможностей способа - формирование определенной кислородной нестехиометрии за счет поддержания заданного значения парциального давления кислорода в газовой атмосфере при отжиге, повышение качества получаемого соединения сложного оксида с заданным значением кислородного индекса.
Указанный технический результат достигается тем, что в способе получения сложного оксида манганита BaLn2Mn2O7+δ, где Ln выбран из группы Nd, Pr, Gd, включающем подготовку шихты, содержащей оксид марганца, оксид редкоземельного металла и барийсодержащий компонент, смешиванием исходных компонентов в определенном соотношении, прессование полученной смеси в таблетки и последующий двухстадийный отжиг в газовой среде, согласно изобретению в качестве барийсодержащего компонента в шихте используют оксид бария, указанные компоненты взяты соответственно атомному соотношению Ba:Ln:Mn=1.0:1.9:2.0, а отжиг проводят в кислородсодержащей газовой среде при поддержании заданного значения давления кислорода в диапазоне Ро2=10-5.0÷10-5,2 (атм), при этом на первой стадии нагревают до температуры 1173 К и выдерживают в течение 24 часов, а на второй стадии - до температуры 1573 К и выдерживают в течение 48 часов. Кроме того, в качестве газовой среды используют смесь из инертного газа аргона и кислорода.
В отличие от прототипа, в качестве исходного компонента смеси содержащего барий используют оксид ВаО. Это позволяет избежать образования газа CO2 в процессе синтеза и необходимости его отвода. Условия термической обработки (температура и время) подобраны экспериментально. Температура первой стадии отжига составляет 1173 К, продолжительность термической обработки - 24 ч. На этой стадии происходит образование центров основной фазы и фаз Ln0.7Ва0.3MnO3 и Ln2O3 Увеличение продолжительности прокаливания не приводит к получению гомогенного продукта синтеза или увеличению центров образования основной фазы и поэтому нецелесообразно. При температуре ниже 1173 К количество центров целевой фазы снижается. На второй стадии отжига нагрев ведут до температуры 1573 К и выдерживают в течение 48 ч., при этом происходит окончательное формирование целевой фазы.
Кислородная нестехиометрия оксидных соединений оказывает существенное влияние на их практические свойства. Формирование кислородной нестехиометрии сложного оксида BaLn2Mn2O7+δ возможно за счет изменения соотношения разновалентных ионов марганца. Одним из способов достижения требуемого соотношения Mn3+/Mn4+ является поддержание заданной величины парциального давления кислорода в процессе синтеза. Это позволяет создать продукт с необходимой величиной кислородного индекса. Кислородная нестехиометрия оксида BaLn2Mn2O7+δ (Ln=Nd, Pr, Gd), полученного при давлении в диапазоне Ро2=10-5,0÷10-5,2 (атм.) составляет δ=0.03. Выбранный интервал давления кислорода в газовой атмосфере не приводит к изменению кислородной нестехиометрии, параметры и объем ячейки при этом меняются незначительно. Дальнейшее понижение давления приводит к формированию стехиометрического по содержанию кислорода оксида, но значительное понижение в интервале Ро2=10-12,0÷10-19,0 - к диссоциации образца по схеме:
BaLn2Mn2O7+δ→Nd0.7Ba0.3MnO3+Nd2O3+↑O2→ВаО+Nd2O3+MnO+↑O2
Фазовый состав полученных образцов исследовался при помощи рентгенографического метода на дифрактометре Shimadzu XRD 7000С.
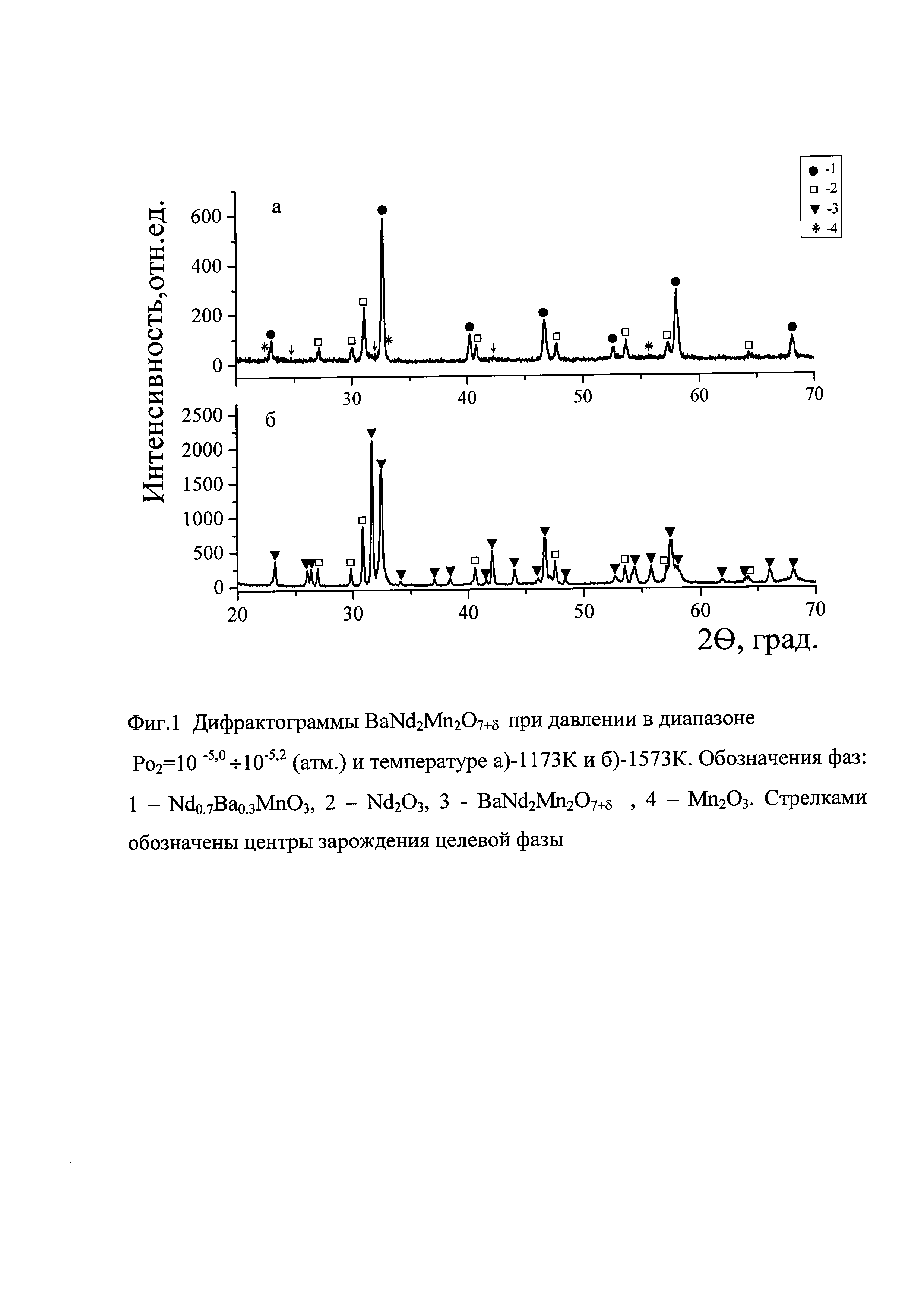
По результатам рентгенофазового анализа основным продуктом синтеза на первой стадии отжига является целевая фаза BaLn2Mn2O7+δ (Ln=Nd, Pr, Gd), а также идентифицируется примесная фаза оксида редкоземельного металла Ln2O3 и следы оксида марганца Mn2O3 (фиг. 1а, представлено на примере оксида BaNd2Mn2O7+б). Для получения гомогенного продукта необходимо изменить содержание того компонента, который присутствует дополнительно к основной фазе. Поэтому соотношение исходных компонентов скорректировано так, чтобы выполнялось условие атомного соотношения Ba:Nd:Mn=1.0:1.9:2.0 (фиг. 1 б).
Предлагаемый способ осуществляют следующим образом:
Расчет навесок исходных компонентов смеси для получения готового продукта планируемой массы 5 г. проведен согласно схеме общего вида (1)
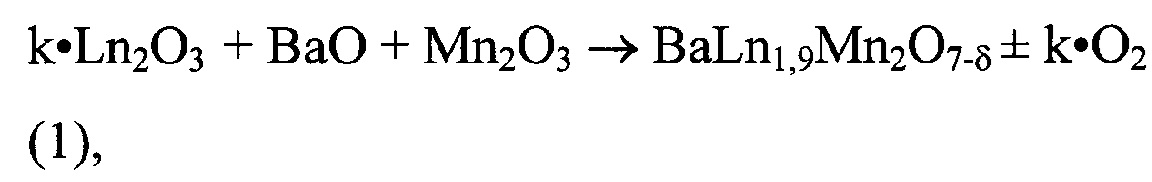
где: Ln2O3(Nd2O3, Pr6O11, Gd2O3), по формуле:
mк=mп⋅k⋅Мк/Мп,
где: mк - масса компонента (ВаО, Ln2O3, Mn2O3),
mп - масса продукта (BaLn1,9Mn2O7+δ),
k - коэффициент при компоненте,
Мк - молекулярная масса компонента,
Мп - молекулярная масса продукта.
Вычисленные массы исходных компонентов представлены в таблице 1.
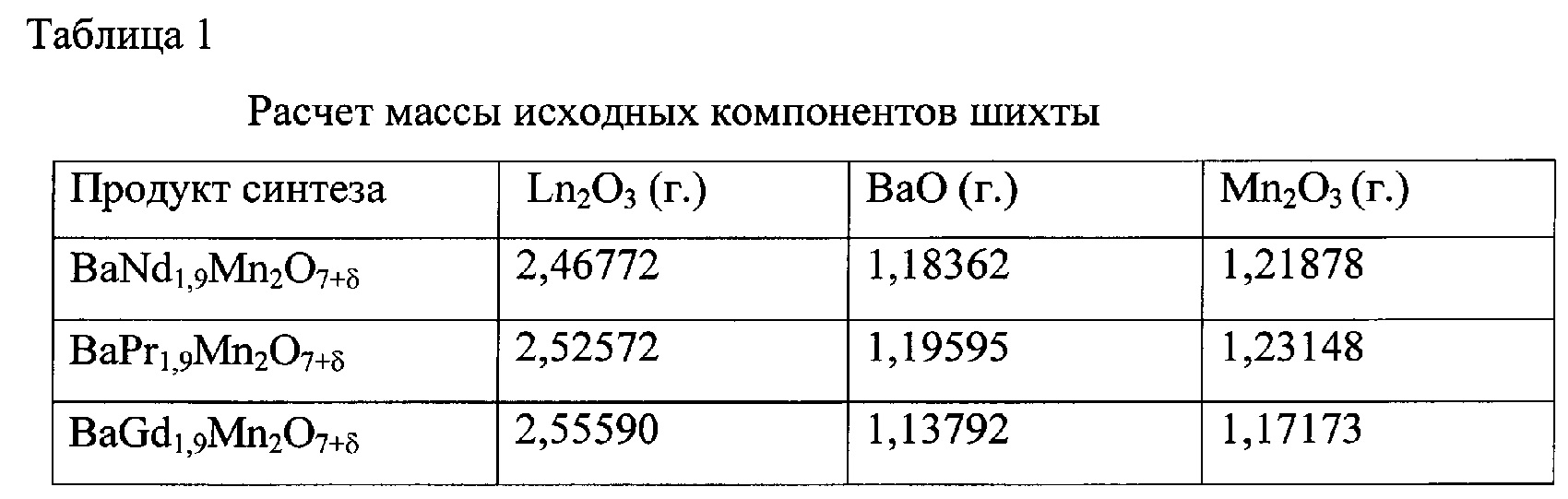
Подготовленные исходные компоненты ВаО, Ln2O3 (Ln=Nd, Pr, Gd) и Mn2O3, взятые в атомном отношении Ва:Ln:Mn=1,0:1,9:2,0 смешивали. Из полученной смеси прессовали таблетки на гидравлическом прессе под давлением 150 кПа/см2. Процесс синтеза осуществляли в герметичном реакторе из Al2O3, в котором установлен контейнер из Al2O3 с вкладышем из Pt, во избежании контакта контейнера и таблетированной смеси исходных компонентов. Для отжига реактор помещают в изотермическую зону печи. Газовую смесь с определенным, контролируемым на протяжении всего опыта значением давления кислорода подают непосредственно в реактор. Двухстадийный отжиг проводили в кислородсодержащей газовой среде при поддержании заданного значения давления кислорода в диапазоне Ро2=10-5,0÷10-5,2 (атм): на первой стадии при температуре 1173 К в течение 24 ч., затем нагревают до температуры 1573 К и выдерживают при этой температуре в течение 48 ч. Охлаждение образцов до комнатной температуры проводили с печью со скоростью 3 град/мин.
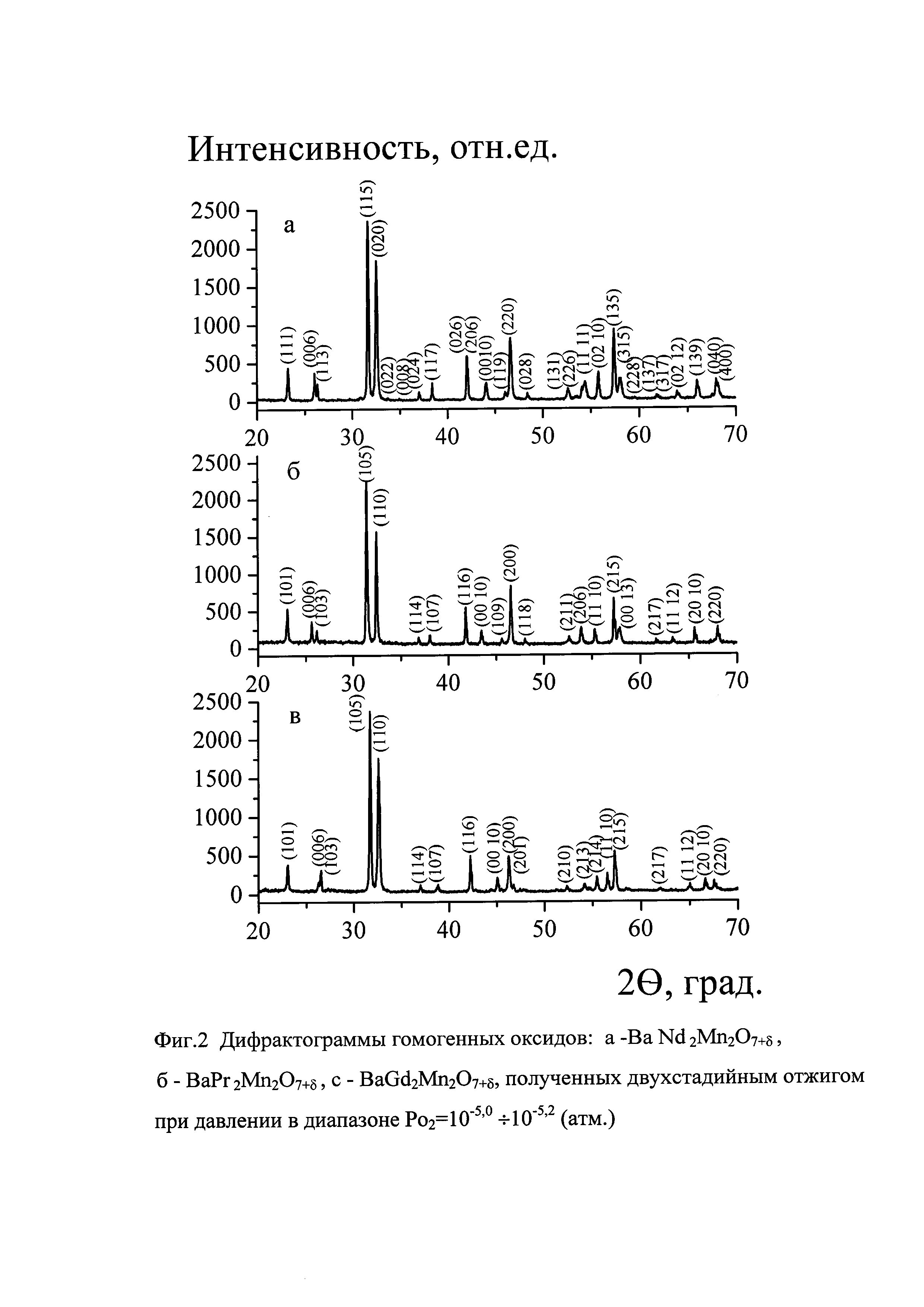
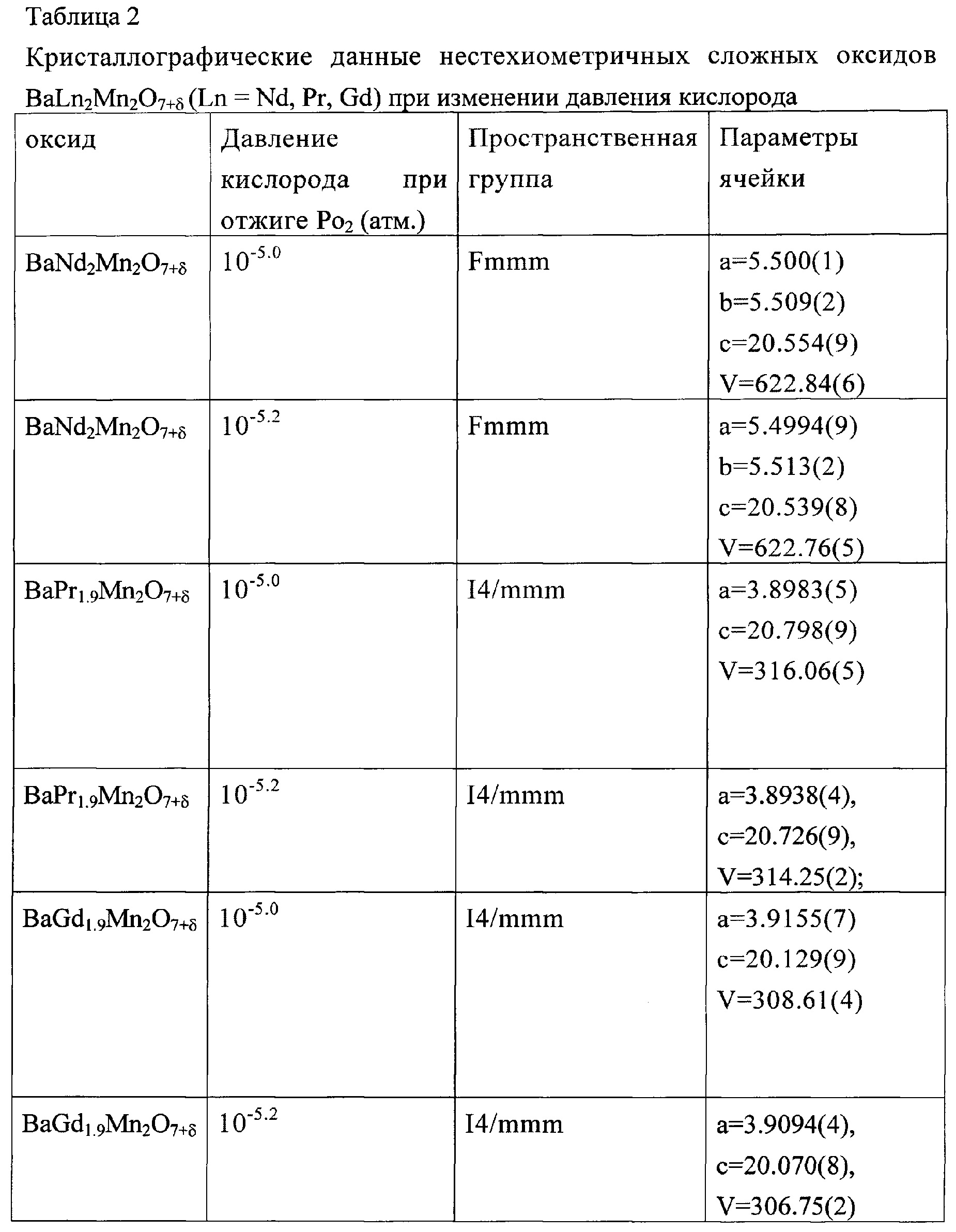
Таким образом, сложные оксиды BaLn2Mn2O7+δ, где (Ln=Nd, Pr, Gd), полученные двухстадийным отжигом при описанных условиях в кислородсодержащей газовой атмосфере с парциальным давлением кислорода Ро2=10-5.0÷10-5,2 (атм) являются гомогенными. BaNd2Mn2O7+δ, имеет орторомбическую структуру и принадлежит к пространственной группе Fmmm (фиг. 2 а). Сложные оксиды BaLn2Mn2O7+δ, где (Ln=Pr, Gd) имеют тетрагональную кристаллическую структуру, пространственная группа I4/mmm (фиг. 2 б, в). Выбранный нами интервал парциального давления кислорода при синтезе сложных оксидов манганитов BaLn2Mn2O7+δ позволяет получить оксиды с определенной устойчивой кислородной нестехиометрией (таблица 2).
Реферат
Изобретение относится к технологии получения сложных оксидов, имеющих слоистую структуру Руддлесдена-Поппера (РП) и относящихся к гомологической фазе АО⋅(АВО). Способ получения сложного оксида манганита BaLnMnO, где Ln выбран из группы Nd, Pr, Gd, включает подготовку шихты, содержащей оксид марганца, оксид редкоземельного металла и оксид бария, смешивание исходных компонентов, прессование полученной смеси в таблетки и последующий двухстадийный отжиг в газовой среде, при этом указанные компоненты взяты соответственно атомному соотношению Ba:Ln:Mn=1,0:1,9:2,0, а отжиг проводят в кислородсодержащей газовой среде при поддержании заданного значения давления кислорода в диапазоне Ро=10÷10атм, причем на первой стадии нагрев осуществляют до температуры 1173К с выдержкой в течение 24 часов, а на второй стадии - до температуры 1573К с выдержкой в течение 48 часов. В качестве газовой среды может быть использована смесь из инертного газа аргона и кислорода. Способ позволяет получать сложные оксиды с устойчивой кислородной нестехиометрией и гомогенные по химическому составу. 1 з.п. ф-лы, 2 ил., 2 табл.

Комментарии