Производные 3(2н)-пиридазинона и способ борьбы с вредными насекомыми - RU2033992C1
Код документа: RU2033992C1
Чертежи





Описание
Изобретение относится к новым 3(2Н)-пиридазиноновым производным и к способу борьбы с вредными насекомыми с их использованием.
Целью изобретения является разработка новых производных 3(2Н)-пиридазинона, которые обладают высокой инсектицидной активностью.
Другой целью изобретения является разработка способа уничтожения и/или борьбы с насекомыми в результате использования указанных выше производных или композиций.
Изобретение относится к новым производным 3(2Н)-пиридазинона общей формулы
I:
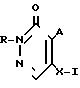
CH2CH2O
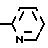
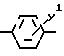
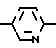
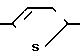
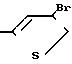
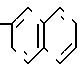
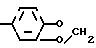
Было найдено, что соединения настоящего изобретения обладают медленной эффективностью действия, поскольку их действие основано на ингибировании метаморфоза насекомых. Кроме того, эти соединения обладают эффективностью при очень низкой концентрации в средствах, применяемых на различных видах насекомых.
Изобретение охватывает все соединения, содержащие асимметричный атом(ы) углерода, т.е. включает оптически активное (+) соединение и соединение (-).
Кроме того, соединения изобретения, существующие в стереоизомерных формах, включают цис- и транс-изомеры.
П р и м е р 1. Синтез 5-(4-трет.-бутилбензилтио)-4-хлор-2-[(2,2-дихлор-1,1-диме-тил)-этил] 3(2Н)-пиридазинона (соединение N 2). В 10 мл метанола растворяют 0,73 г 4, 5-дихлор-2-[(2,2-дихлор-1,1-диметил)-этил]-3(2Н)-пиридазинона и 0,45 г 4-трет.-бутилбензил меркаптана. Полученный в результате раствор суспендируют в присутствии 0,27 г карбоната натрия и затем в течение 3 ч перемешивают при комнатной температуре. Раствор переливают в ледяную воду и отфильтровывают. Полученные таким образом кристаллы перекристаллизовывают из смеси бензол-гексан с образованием 0,8 г целевого соединения. Температура плавления (т.пл.): 162,0-163,0оС.
П р и м е р 2. Синтез 4-бром-5-(4-хлор-бензилокси)-2-[(2,3-дихлор-2-метил)-пропил] 3(2)- пиридазинона (соединение N 12). В 10 мл N,N-диметилформамида растворяют 1,90 г 4,5-дибром-2-[(2,3-дихлор-2-метил)-пропил]-3(2)-пиридазинона и 0,71 г 4-хлорбензилового спирта. Полученный раствор суспендируют в 0,33 г порошкообразного гидроксида калия. Реакционную смесь перемешивают в течение ночи при комнатной температуре. Полученный в результате раствор переливают в ледяную воду и экстрагируют бензолом. Экстракт промывают насыщенным рассолом и затем водой и растворитель удаляют дистилляцией при пониженном давлении. Полученное таким образом масло отделяют и очищают методом колоночной хроматографии (на силикагеле проводят элюирование хлороформом) с образованием 1,10 г целевого соединения. Т.пл. 112-114оС.
П р и м е р 3. Синтез 2-(3'-бромпропил)-4-хлор-5-(4'-хлорбензилоксил)-3(2)-пирида-зинона (соединение N 19). К смешанному растворителю, состоящему из 150 мл воды и 150 мл этанола, добавляют 22,3 г 4, 5-дихлор-2-(3'-гидроксипропил)-3(2Н)-пиридази- нона (0,1 моль) и 19,6 г гидроксида калия (0,35 моль) и затем полученную смесь в течение 10 ч нагревают с обратным холодильником. После завершения реакции этанол удаляют при пониженном давлении и добавляют воду для фильтрации нерастворенного материала. Фильтрат подкисляют разбавленной хлористоводородной кислотой, и полученные кристаллы отфильтровывают. Полученные в результате кристаллы промывают водой и сушат с образованием 14,5 г 4-хлор-5-гидрокси-2(3'-гидроксипропил)-3 (2)-пиридазинона.
К 150 мл N, N-диметилформамида добавляют 10,2 г 4-хлор-5 и гидрокси-2-(3'-гидроксипропил)-3(2)-пиридазинона (0,05 моль), 8,4 г 4-хлорбензил хлорида (0,052 моль) и 10,4 г безводного карбоната калия (0,075 моль) и полученную систему нагревают в течение 3 ч при температуре 100-120оС. После завершения реакции смешанный раствор переливают в воду и экстрагируют этилацетатом. Полученный в результате раствор промывают водой, затем 5%-ным водным раствором гидроксида натрия и насыщенным раствором. Полученный раствор сушат над безводным сульфатом натрия, и растворитель удаляют дистилляцией при пониженном давлении. Полученный таким образом твердый продукт промывают н-гексаном и сушат с получением 12,3 г 4-хлор-5-(4'-хлорбензилокси)-2(3'-гидроксипропил)-3(2)-пиридазинона.
К 170 мл хлороформа добавляют 9,9 г 4-хлор-5-(4'-хлорбензилокси)-2(3'-гидрок- сипропил)3(2)-пиридазинона (0,03 моль) и медленно добавляют 9,4 г бромистого тионила (0,045 моль) при перемешивании в течение 2 ч при температуре от -5 до +5оС. После завершения реакции полученный раствор разбавляют водой и хлороформный слой отделяют. Этот слой промывают водой, 5%-ным водным раствором бикарбоната натрия и после этого промывают насыщенным рассолом и сушат над безводным сульфатом натрия, а растворитель удаляют дистилляцией при пониженном давлении. Полученный таким образом твердый продукт перекристаллизовывают из смешанного растворителя н-гексанбензола с получением 5,2 г 2-(3'-бромпропил)4-хлор-5-(4'-хлорбензилокси)-3(2)-пиридазинона. Т. пл. 83-87оС.
П р и м е р 4. Синтез 4-хлор-2[(2-хлор-2-метил)-пентил]-5-(4-йодбензилокси)-3(2)-пи- ридазинона (соединение N 33). Повторяют методику, описанную в препаративном примере 2, с использованием 1,42 г 4, 5-дихлор-2-[(2-хлор-2-метил)-пентил] -3(2)-пиридазино- на и 1,17 г 4-йодбензилового спирта с получением 1,72 г целевого соединения. Т.пл. 114-115оС.
П р и м е р 5. Синтез 4-хлор-2-[(2-дихлор-2-метил-пропил)-5][(2-йод-5-пиридил- метокси]-3(2)- пиридазинона (соединение N 20). Повторяют методику, описанную в препаративном примере 2 с использованием 1,45 г 4,5-дихлор-2/(2, 3-дихлор-2-метил)-пропил/-3(2)-пиридазинона и 1,18 г 2-йод-5-пиридинметанола с получением 1,33 г целевого соединения. Т.пл. 117-120оС.
П р и м е р 6. Синтез 4-хлор-2-(2-хлор-2-метилпропил)-5-(2-фенокси-этокси)-3(2)-пи- ридазинона (соединение N 326). 210 мл N,N-диметилформамида растворяют 1,85 г 2-(2-хлор-2-метилпропил)-4,5-дихлор-3(2)-пири-дазинона и 1,00 г 2-феноксиэтанола и в полученную смесь добавляют 0,48 г порошкобразного гидроксида калия. Полученный раствор перемешивают в течение ночи при комнатной температуре. Затем повторяют методику препаративного примера 2 с получением 1,19 г целевого соединения. Т.пл. 82-83оС.
П р и м е р 7. Синтез 5-(4-трет.бутил-метилбензилокси)-4-хлор-2-винил-3(2Н)-пири- дазинона (соединение N 129). В 60 мл N,N-диметилформамида растворяют 2,7 г 2-(2-бромэтил)-4,5-дихлор-3(2Н)-пиридазинона и 1,8 г 4-трет. бутил-а-метилбензилового спирта и в смесь добавляют 1,4 г порошкообразного гидроксида калия. Полученный раствор перемешивают в течение ночи при комнатной температуре. После завершения реакции полученный раствор переливают в воду и экстрагируют бензолом. Бензольный слой промывают водой, сушат над безводным сульфатом натрия и растворитель удаляют дистилляцией при пониженном давлении. Оставшуюся вязкую жидкость отделяют методом колоночной хроматографии (на силикагеле проводят элюирование смесью бензолэтилацетат) с получением 2,2 г целевого соединения (вязкая жидкость).
1Н-ЯМР (CDCl3, δ н/млн): 1,37 (9Н, синглет), 1,80 (3Н, дублет, I 6 Гц), 4,95 (1Н, дублет, I 9 Гц), 5,66 (1Н, квартет, I 6 Гц), 6,67 (1Н, дублет, I 15 Гц), 7,17-7,53 (4Н, мультиплет), 7,68 (1Н, дублет, дублет, I 9 Гц, 15 Гц), 7,78 (1Н, синглет).
П р и м е р 8. Синтез 4-хлор-2(2-хлор-2-метилпентил)-5-(4-этилбензилокси)-3(2Н)-пиридазинона (соединение N 85). В 20 мл N,N-диметилформамида добавляют 1,2 г 2-(2-хлор-2-метилпентил)-4,5-дихлор-3(3Н)-пиридазинона и 0,64 г 4-этилбензилового спирта и к полученной смеси добавляют 0,31 г порошкообразного гидроксида калия и полученную смесь охлаждают льдом и перемешивают в течение дня при комнатной температуре. Затем повторяют методику препаративного примера 2 с получением 600 мг целевого соединения. Т.пл. 81-83оС.
П р и м е р 9. Синтез 4-хлор-2(2-хлор-2-метилпентил)-5-(4-трифторметилбензилок-си)-3(2Н)- пиридазинона (соединение N 56). В 20 мл N,N-диметилформамида растворяют 1,2 г 2-(2-хлор-2-метилпентил)-4, 5-дихлор-3(2Н)-пиридазинона и 0,78 г 4-трифторметил бензилового спирта и к полученной смеси добавляют 1,46 г безводного карбоната калия. Полученный раствор перемешивают в течение 8 ч при 50о С. Затем повторяют методику препаративного примера 2 с получением 1,0 г целевого соединения. Т.пл.105-106оС.
П р и м е р 10. Синтез 4-хлор-2(2-хлор-2-метилпропил)-5-[(2-йод-5-пиридин)-меток- си] -3(2Н)- пиридазинона и 4-хлор-5-(2-йод-5-пиридил)-метокси-2-(2-метил-1-пропенил)-3(2Н)- пиридазинона (соединения NN 237 и 255). В 10 мл N, N-диметилформамида растворяют 1,4 г 2-(2-хлор-2-метилпропил)-4,5-дихлор-3(2Н)-пиридазинона и 1,29 г 2-йод-5-пиридил метанола и в смесь добавляют 0,33 г порошкообразного гидроксида калия при охлаждении системы льдом.
Полученный раствор перемешивают в течение дня при комнатной температуре. Затем повторяют методику примера 2 с получением 0,74 г 4-хлор-2-(2-хлор-2-метилпропил)-5-[(2-йод-5-пиридил)-метокси] -3(2Н)- пиридазинона (т.пл. 119-123оС) и 0,24 г 4-хлор-5-[(2-йод-5-пиридил)-метокси]2-(2-ме-тил-1-пропенил)-3(2Н)- пиридазинона (т.пл. 141-142оС).
П р и м е р 11. Синтез 2-(2-хлор-2-метилпропил)-5-(4-йодбензилокси)-4-метил-3(2Н)- пиридазинона (соединение N 167). В 5 мл N,N-диметилформамида растворяют 0,33 г 5-хлор-2-(2-хлор-2-метилпропил)-4-метил-3(2Н)-пиридазинона и 0,33 г 4-йодбензилового спирта и к смеси добавляют 0,1 г порошкообразного гидроксида калия при охлаждении системы льдом. Затем повторяют методику препаративного примера 2 с получением 0,3 г целевого соединения. Т.пл. 121-123оС.
П р и м е р 12. Синтез 4, 5-дихлор-2-(3-хлор-тетрагидро-2-пиранил)-3(2Н)-пирида-зинона. В 20 мл хлористого метилена растворяют 4 г 2,4,5-трихлор-3(2Н)-пиридазинона и по каплям добавляют 2,5 г 2,3-дигидропропирана при охлаждении системы льдом. Полученный раствор перемешивают в течение 30 мин и отфильтровывают побочный продукт 4,5-дихлор-3(2Н)-пиридазинон. Фильтрат подвергают дистилляции при пониженном давлении. Полученное таким образом масло отделяют методом колоночной хроматографии (на силикагеле, проводя элюирование бензолом) с образованием 1,5 г транс-формы в виде первой фракции (т. пл. 136-137о С) и 1,3 г цис-формы в виде второй фракции (т.пл. 109-110оС).
1Н-ЯМР (CDCl3, δ, ТМС): транс-форма: 1,50-2,20 (мультиплет, 4Н); 3,50-4,66 (мультиплет, 3Н); 5,86 (дублет, 1Н, 10 Гц); 7,77 (синглет, 1Н); цис-форма: 1,90-2,50 (мультиплет, 4Н); 3,50-4,60 (мультиплет, 3Н); 6,05 (дублет, 1Н, 3 Гц); 7,83 (синглет, 1Н).
П р и м е р 13. Синтез 4,5-дихлор-2-(2,3-дихлор-2-пропенил)-3(2Н)-пиридазинона. К смеси 10,8 г 4,5-дихлор-3(2Н)-пиридазинона и 9,5 г безводного карбоната калия добавляют 65 мл N,N-диметилформамида и полученную смесь перемешивают в течение 10 мин при комнатной температуре. Затем добавляют 10,0 г 1,2,3-трихлор-1-пропена (смесь Е-формы и Z-формы) и полученный раствор перемешивают в течение 6 ч при 40оС. Этот раствор переливают в большое количество воды и смесь экстрагируют бензолом, растворитель удаляют дистилляцией при пониженном давлении с получением 6,0 г целевого соединения (смесь Е-формы и Z-формы). Полученное соединение разделяют на изомеры (т.пл. 93,7-94,6оС и 112,8-114,8оС) методом колоночной хроматографии (на силикагеле, проводя элюирование бензолом).
1Н-ЯМР (CDCl3,δ ТМС): изомер 1 (т.пл. 93,7-94,6оС); 5,15 (синглет, 2Н); 6,47 (синглет: 1Н); 7,84 (синглет, 1Н); изомер 2 (т.пл. 112, 8-114,8оС): 5,00 (синглет, 2Н); 6,70 (синглет, 1Н); 7,84 (синглет, 1Н).
П р и м е р 14. Синтез 4,5-дихлор-2-(2-метил-2-пропенил)-3(2Н)-пиридазинона. В 50 мг N, N-диметилформамида суспендируют 10 г 4,5-дихлор-3(2Н)-пиридазинона, 27 г 3-хлор-2-метилпропена и 8,4 г карбоната калия. Полученный раствор перемешивают в течение 5 ч при 40оС. Затем повторяют методику препаративного примера 2 с получением 4,9 г целевого соединения. Т.пл. 52-54оС.
П р и м е р 15. Синтез 2-(2-хлор-2-метил-пропил)-4, 5-дихлор-3-(2Н)-пиридазинона. В 100 мл четыреххлористого углерода растворяют 5 г 4,5-дихлор-2-(2-метил-2-пропенил)-3-(2Н)-пиридазинона и 0,1 г хлористого трифторметил аммония и в полученную систему добавляют 30 мл концентрированной хлористоводородной кислоты. Полученный раствор перемешивают и промывают водой, сушат над безводным сульфатом натрия и удаляют растворитель путем дистилляции при пониженном давлении с получением 4,7 г целевого соединения. Т.пл. 61-66оС.
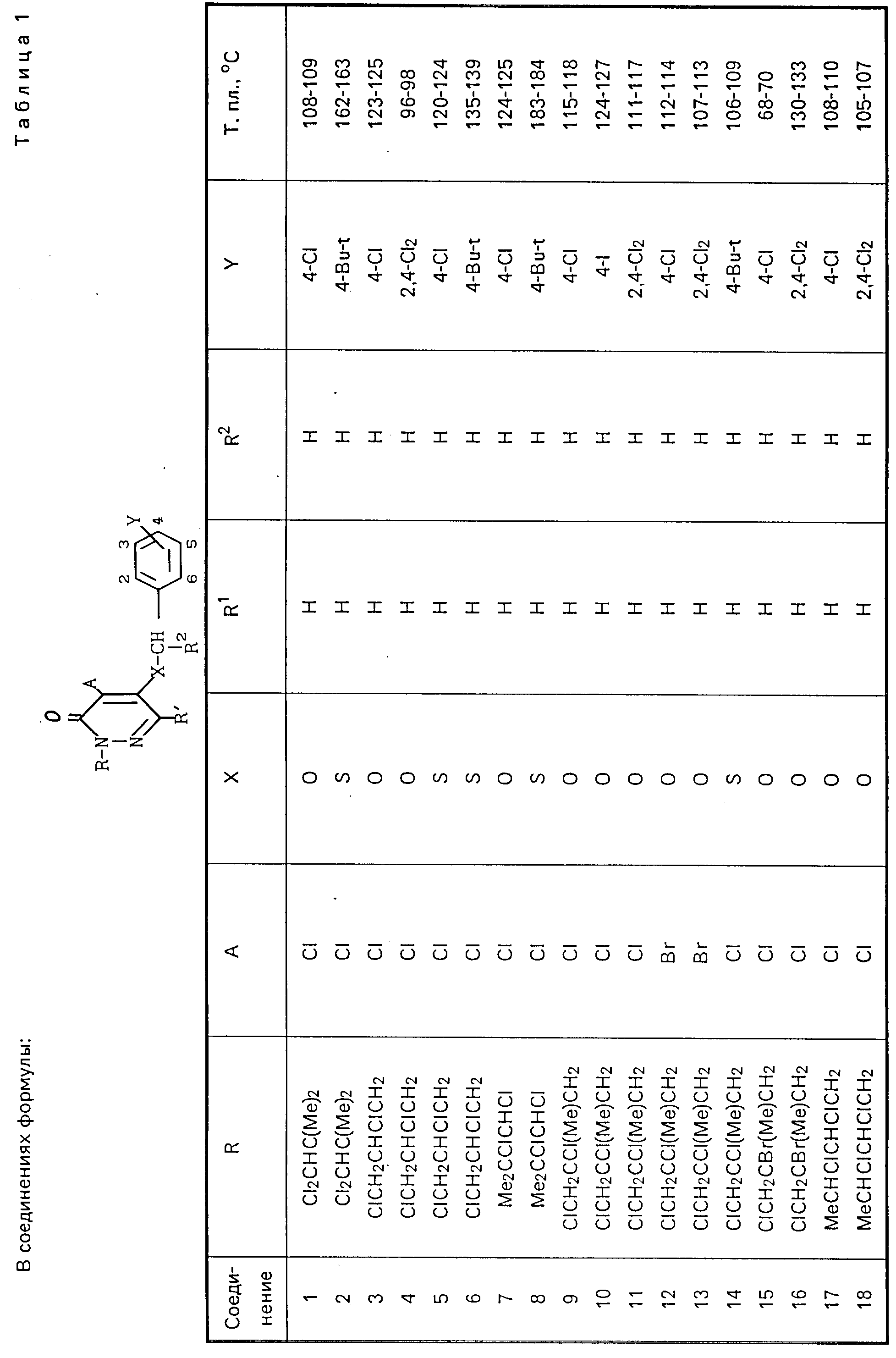
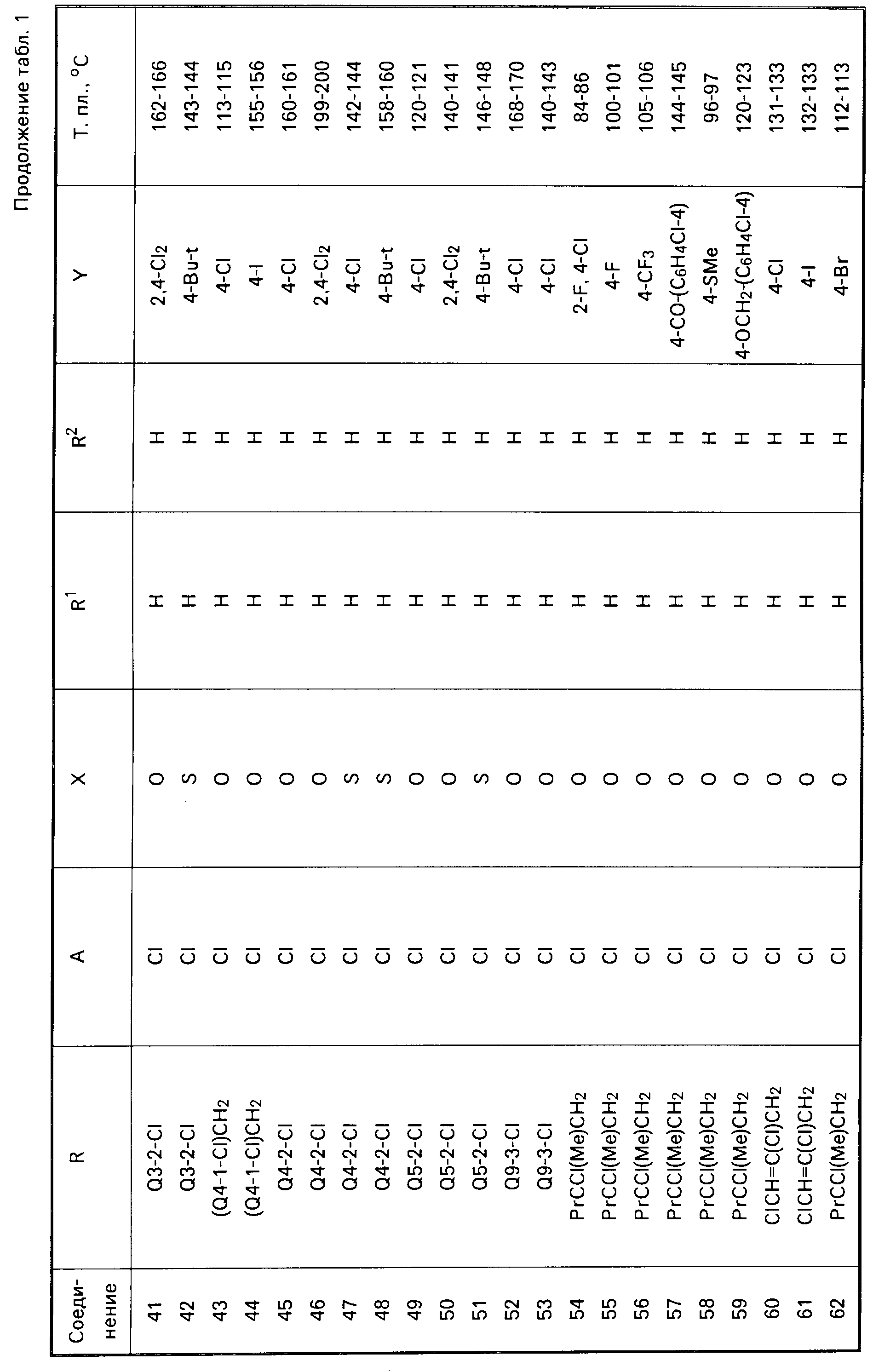
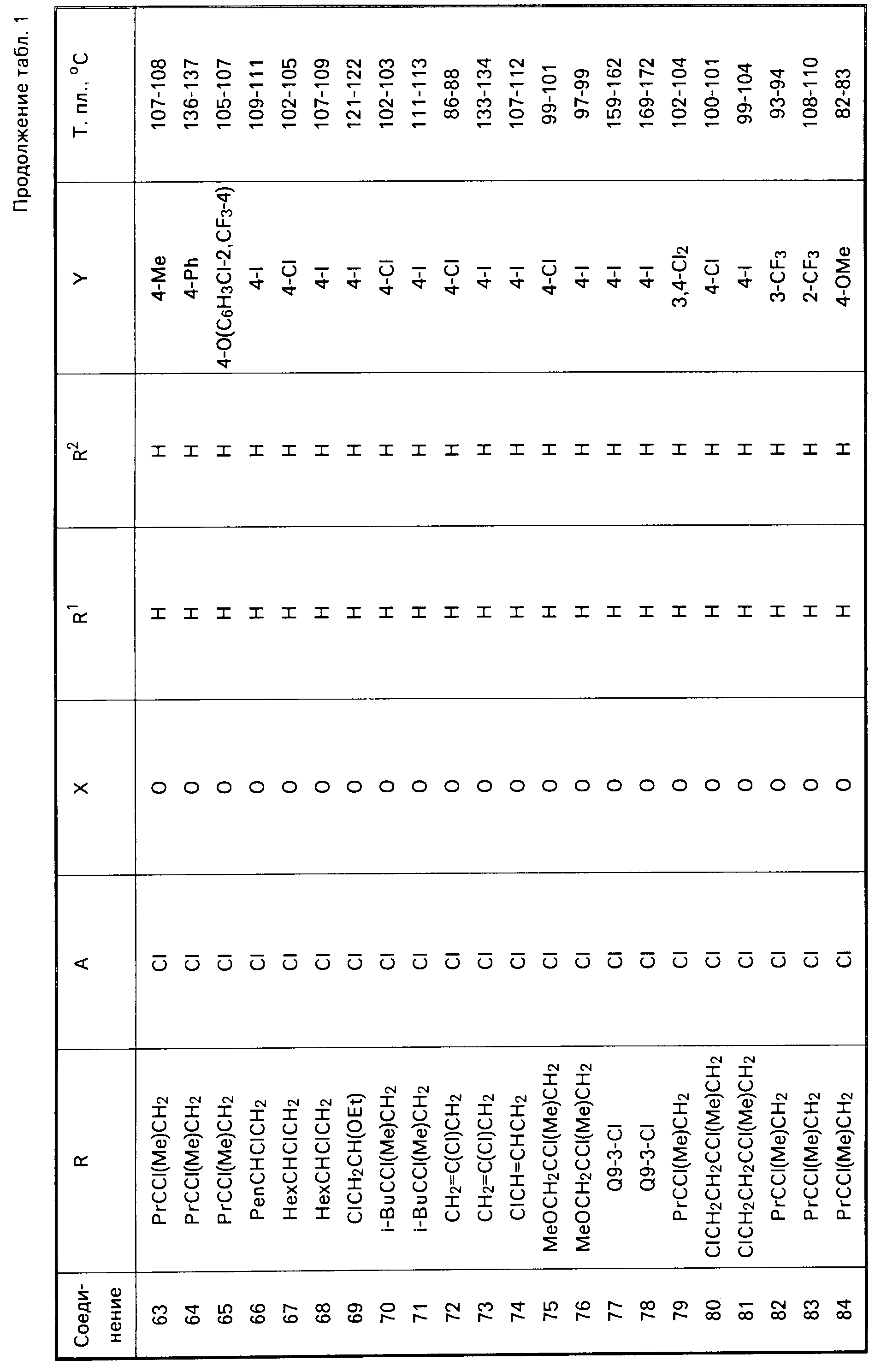
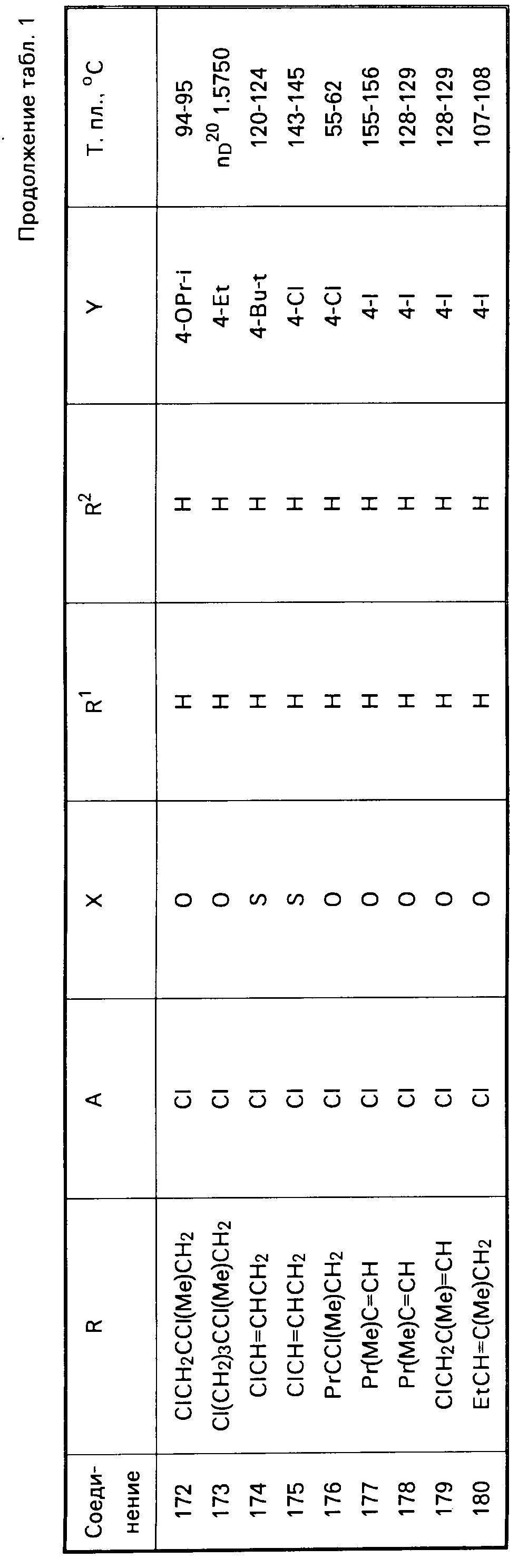
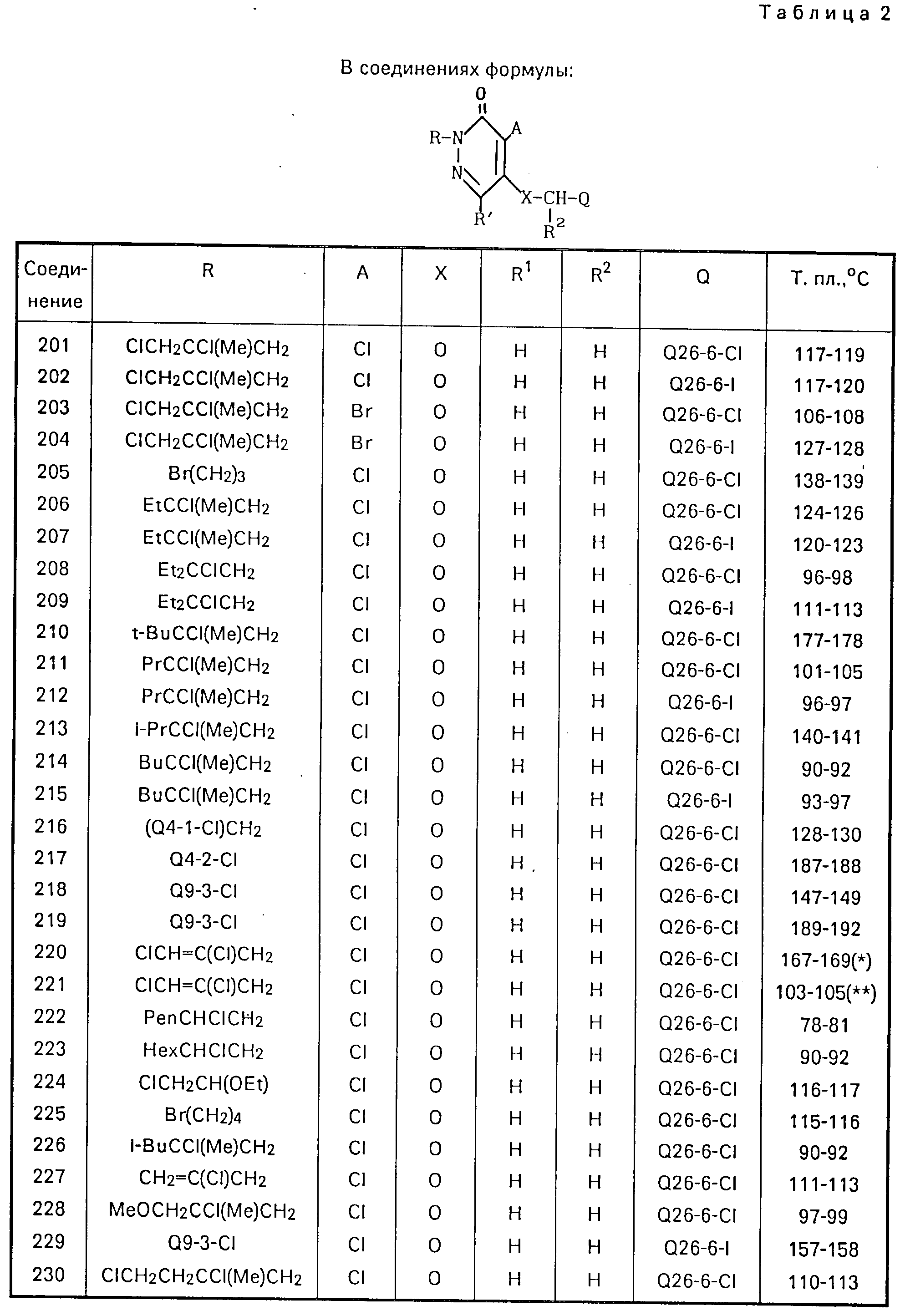
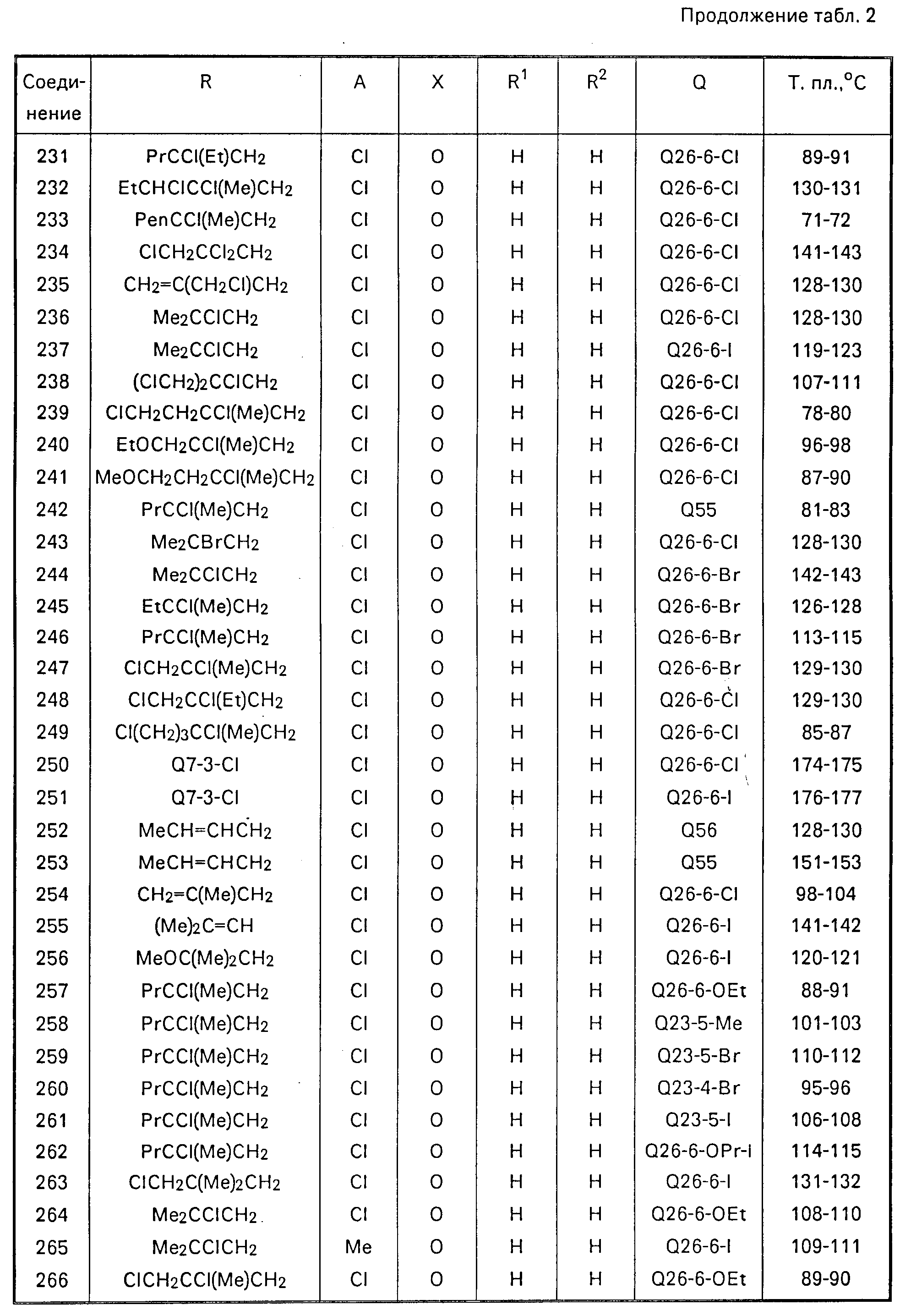
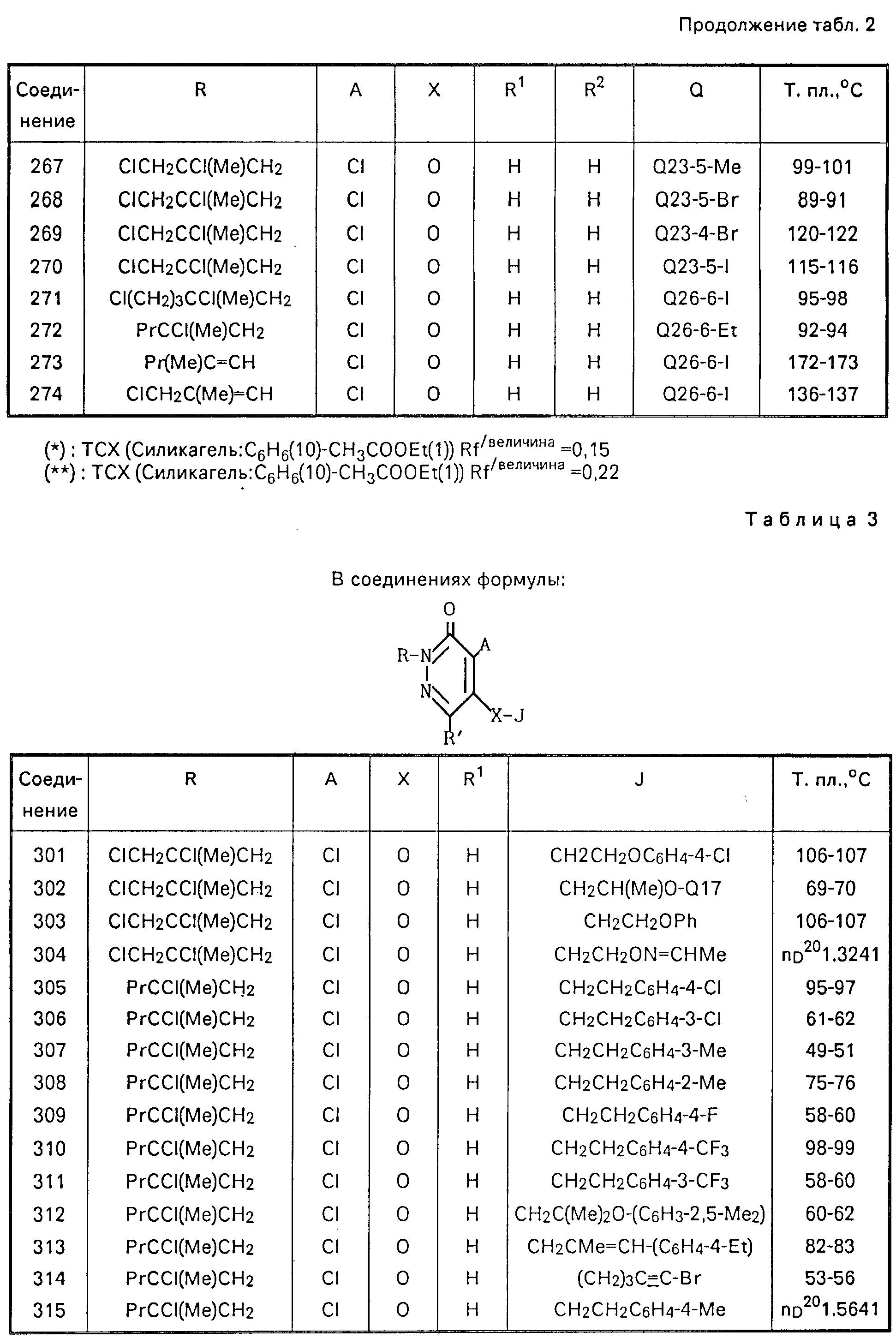
Физические свойства соединений, полученных согласно примерам 1-15, представлены в табл.1-3, где приняты следующие сокращения: Ме метил; Et этил; Pr пропил; Bu бутил; Pen пентил; Hex гексил; Ph незамещенный фенил; t третичный; δ- вторичный, i изо; с цикло.
Определения
значений Q в табл. 1-3 являются следующими:
Q3
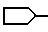
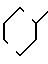
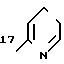
Q5
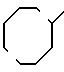
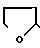
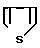
Q9
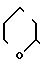
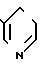
Q55
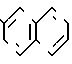
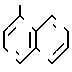
Количество соединений изобретения, используемых в качестве активного ингредиента, обычно лежит в интервале 0,005-50 кг на гектар, хотя это зависит от места применения и сезона применения, способа применения, типа заболевания и вида насекомых, подлежащих уничтожению, типа культур, подлежащих защите, и т.п.
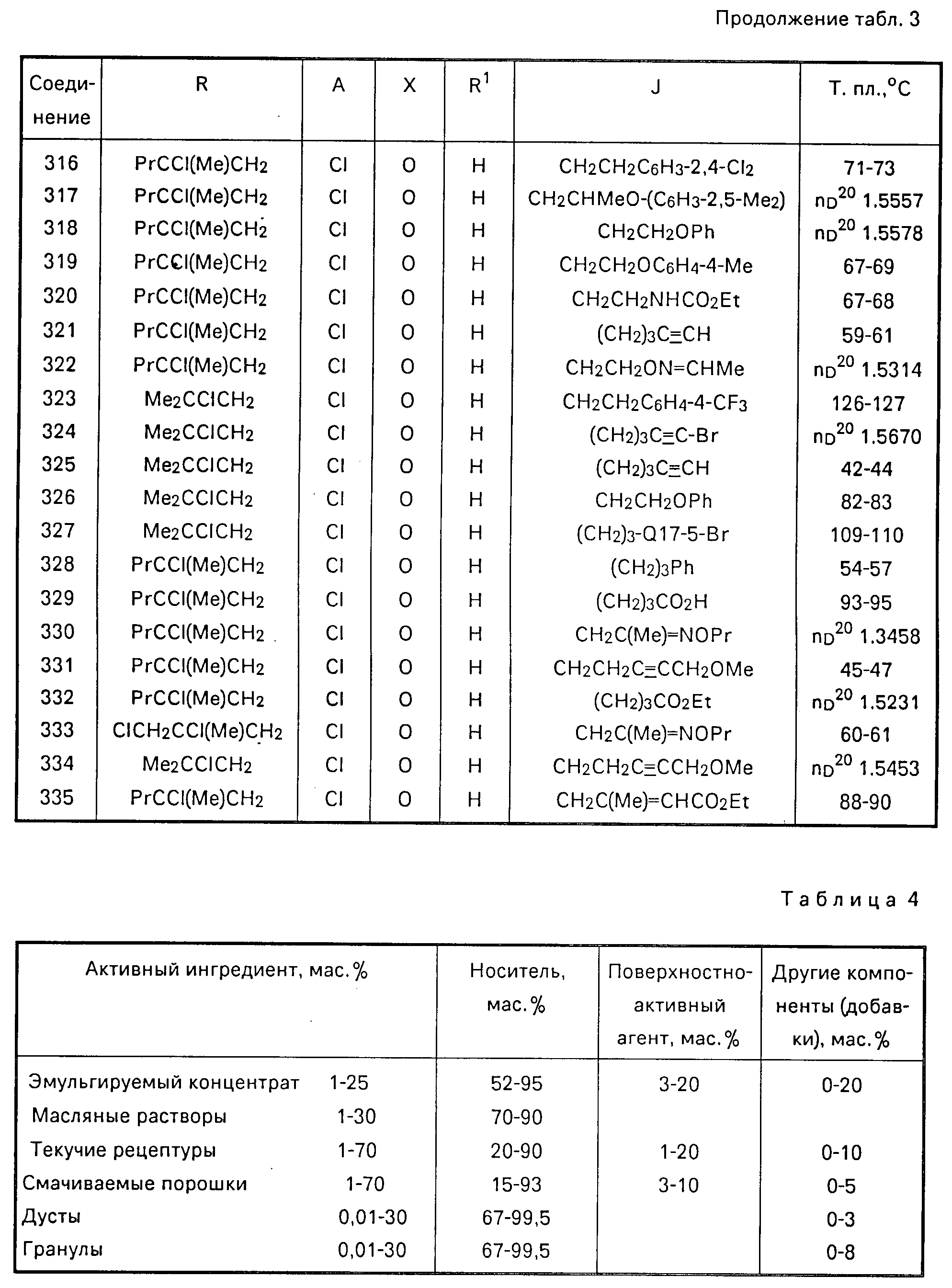
Соотношения ингредиентов в рецептурах и типы различных препаратов настоящего изобретения показаны в табл.4.
При практическом использовании эмульгируемые концентраты, масляные растворы, текучие рецептуры и смачиваемые порошки разбавляют заранее определенным количеством воды и после этого применяют. Дусты и гранулы применяют непосредственно без разбавления водой. Гранулы содержат приманки.
Далее представлены примеры рецептур инсектицидных композиций, содержащих соединения настоящего изобретения в качестве активного ингредиента. В следующих ниже рецептурах "части" приведены в весовом выражении.
Рецептурный пример 1. Эмульгируемый концентрат, ч.
Соединение изобретения 5 Ксилол 70 N,N-диметилформамид 20 Сорпол 2680 5
В соответствующем приведенном выше эмульгируемом концентрате каждый компонент такого эмульгируемого концентрата
подвергают тщательному перемешиванию с целью получения соответствующего концентрата. В ходе использования эмульгируемые концентраты разбавляют водой до соотношения 1:15000-1:20000 и применяют с нормой
0,005-50 кг активного ингредиента на гектар.
Рецептурный пример 2. Смачиваемый порошок, ч. Соединение изобретения 25 Зиклит РFP 66 Сорпол 5039 4 Карплекс 80 2 Лигнин сульфонат кальция
3
В приведенном выше смачиваемом порошке каждый компонент рецептуры тщательно размешивают и измельчают с образованием соответствующего смачиваемого порошка. Перед использованием смачиваемые
порошки разбавляют водой до концентрации порядка 1:15000-1:20000 и применяют с нормой расхода 0,005-50 кг активного ингредиента на гектар.
Рецептурный пример. Масляные растворы, ч.
Соединение изобретения 20 Метилцеллюлозы 80
Каждый компонент указанной рецептуры однородно смешивали друг с другом с получением соответствующих масляных растворов. В ходе использования
масляные растворы применяют с нормой расхода 0,005-50 кг активного ингредиента на гектар.
Пример испытания 1. Испытание на инсектицидную активность против рисовой цикадки (Nephotettix cineticeps).
5%-ный эмульгируемый концентрат (или 25 ч-смачиваемый порошок) соединения настоящего изобретения разбавляют водой, содержащей вещество, повышающее смачивающую способность, и получают 500 ppm раствора соединения.
Стебли и листья рисового растения, посаженного в горшок размером 1 м2, обрабатывают 100 мл полученного раствора, а затем сушат воздухом (500 г/га), после чего в горшок запускают 20 личинок рисовой цикадки на второй возрастной стадии (Nephotettix cineticeps), которая обладает устойчивостью к органическим фосфорным инсектицидам и карбаматным инсектицидам.
Обработанное таким образом рисовое растение накрывают цилиндрической металлической сеткой и помещают в термостат. Через 30 дней подсчитывают число
паразитов-цикадок на растениях и определяют смертность в соответствии со следующим уравнением:
Смертность/
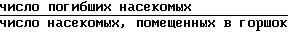
Испытания проводят для каждого соединения дважды. В результате высокий эффект (100% смертности) показывают следующие соединения.
Соединения,N: 9, 10, 12, 15, 17, 19, 24, 25, 27, 28, 32, 33, 38, 39, 45, 49, 50, 52, 53, 75,76,77,78, 80,81,85,87,92,97,104, 105, 107, 108, 109, 110, 111, 112, 113, 114, 115, 116, 117, 118, 120, 122, 124, 125, 126, 127, 155, 156, 201, 202, 203, 204, 206, 207, 208, 209, 211, 212, 218, 219, 226, 228, 229, 230, 231, 234, 236, 237, 238, 239; 240, 244, 245, 247, 250, 251, 314, 321, 324, 325.
Пример испытания 2. Испытание на инсектицидную активность против рисовых дельфицид (Nilaparvata lugens).
Повторяют процедуру, описанную в примере 1, за исключением того, что вместо личинок зеленой рисовой цикадки используют личинки второй стадии рисовых дельфицид, которые обладают устойчивостью к органическим фосфорным инсектицидам и карбаматным инсектицидам. В результате высокий эффект (100% смертности) показывают следующие соединения.
Соединения, N: 11,25,34,48,93,201, 202, 203, 204, 205, 207, 208, 209, 211, 212, 214, 215, 219, 228, 229, 230, 231, 234, 236, 237, 238, 239, 240, 243, 244, 245, 246, 247, 249, 250, 251, 254, 255, 256, 257, 259, 263, 264, 265, 271, 302.
Пример испытания 3. Испытание на инсектицидную активность против хрущака
каштанового (Tribolium castaneum)
В небольшую прозрачную пробирку помещают 5%-ный эмульгируемый концентрат соединения настоящего изобретения (или 25% смачиваемого порошка или его 20%
масляного раствора), а затем туда добавляют ацетон, в результате чего получают 500 ppm ацетонового раствора соединения. 10 см3 этого ацетонового раствора добавляют к 10 г пшеничной муки,
помещенной в чашку диаметром 9 см. После размешивания из смеси (0,5 г/кг муки) отгоняют ацетон. Затем в чашку запускают по 10 взрослых особей женского и мужского пола хрущака каштанового (Tribolium
castaneum). Чашку, содержащую взрослых насекомых, помещают в термостат. Через 90 дн проводят подсчет погибших особей.
Испытание проводят дважды для каждого соединения.
В результате в чашках, обработанных приведенными ниже соединениями, не обнаружено ни одного взрослого насекомого.
Соединения, N: 9, 10, 12, 15, 19, 24, 25, 32,33,39,70,71,75,76,77,78, 79,80,81,84,85, 86,87, 92,93,94,95,97,100, 101, 102, 103, 104, 105, 106, 107, 108, 109, 110, 111, 112, 113, 114, 115, 116, 117, 118, 119, 120, 121, 122, 123: 124, 125, 126, 127, 155, 156, 159, 160, 161, 163, 164, 168, 169, 173, 201, 202, 203, 204, 206, 207, 208, 209, 211, 212, 226, 227, 228, 229, 230, 231, 232, 233, 234, 235, 236, 237, 238, 239, 240, 241, 242, 243, 244, 245, 246, 247, 248, 249, 250, 251, 255, 257, 263, 264, 266, 271.
Пример испытания 4. Испытание на инсектицидную активность против комара-пискуна (Culex pipiens pallens)
5% -ный эмульгируемый
концентрат (или 25% смачиваемого порошка или 20% масляного раствора) соединения настоящего изобретения разбавляют деионизированной водой и получают 10 ppm раствора соединения (0,01 г/л).
200 мл указанного раствора выливают в глубокий сосуд диаметром 9 см и высотой 6 см. В указанный сосуд запускают 10 личинок комара-пискуна (Culex pipiens pallens). Сосуд, содержащий личинки, помещают в термостат при 25оС. Через 7 дн подсчитывают количество погибших особей.
Для каждого соединения испытания проводят дважды.
В результате в сосуде, обработанном любым из приведенных ниже соединений, не обнаружено ни одного взрослого насекомого.
Соединения, N: 1, 2, 3, 4, 5, 6, 9, 10, 12, 14, 15, 17, 18, 19, 24, 25, 27, 28, 30, 32, 33, 34, 35,38,39, 45, 49, 52, 53, 70, 71, 72, 73, 75,76,77,78,79,80,81,82,83,84,85,86,87,88, 89, 90,92,93,94,95,96,97,98,99,100, 101, 102, 103, 104, 105, 107, 108, 109, 110, 111, 112, 113, 114, 115, 116, 117, 118, 119, 120, 122, 123, 124, 125, 126, 127, 155, 156, 158, 160, 163, 164, 168, 169, 173, 201, 202, 203, 204, 205, 206, 207, 208, 209, 211, 212, 215, 217, 218, 219, 224, 225, 226, 227, 228, 229, 230, 231, 232, 233, 234, 236, 237, 238, 239, 240, 241, 242, 244, 245, 246, 250, 251, 255, 257, 264, 266, 301.
Пример испытания 5. Испытание на инсектицидную активность против огневки сухофруктовой (Cadra cautella).
В прозрачную небольшую пробирку помещают 5% эмульгируемого концентрата соединения настоящего изобретения (или 25% смачиваемого порошка или его 20% -ный масляный раствор) и затем добавляют ацетон, в результате чего получают 500 ppm ацетонового раствора соединения. 10 см3указанного ацетонового раствора добавляют к 10 г рисовых отрубей, помещенных в чашку диаметром 9 см. После перемешивания полученной смеси ацетон отгоняют (0,5 г/кг рис.отрубей). Затем в эту чашку запускают 10 личинок огневки (Cadra cautella). Чашку с личинками помещают в термостат. Через 30 дн проводят оценку путем подсчета числа появившихся взрослых особей.
Испытание проводят дважды для каждого соединения.
В результате в чашке, обработанной любым из приведенных ниже соединений, не обнаружено ни одного взрослого насекомого.
Соединения, N: 9, 10, 11, 12, 15, 19, 24, 25, 27, 28, 32, 33, 34, 38, 39, 52, 53, 70, 71, 73, 74,75,76,77, 78, 79, 80, 81, 84, 85, 86, 87, 89, 90,92,93,94,95,97,98,100, 101, 102, 103, 104, 105, 106, 107, 108, 109, 110, 111, 112, 113, 114, 115, 116, 117, 118, 119, 120, 124, 125, 126, 127, 155, 156, 160, 162, 163, 166, 167, 168, 169, 171, 172, 173, 201, 202, 203, 204, 206, 207, 208, 209, 211, 212, 214, 215, 217, 218, 219, 225, 226, 227, 228, 229, 230, 231, 232, 233, 234, 235, 236, 237, 238, 239, 240, 241, 242, 243, 244, 245, 246, 247, 249, 250, 251, 256, 257, 258, 259, 260, 261, 262, 263, 264, 265, 266, 268; 270, 271, 302, 314, 318, 319.
Пример испытания 6. Испытание на инсектицидную активность против тли персиковой (Myzus persical)
5% -ный эмульгируемый концентрат (или 25% смачиваемого порошка) соединения настоящего
изобретения разбавляют водой, содержащей вещество, повышающее смачивающую способность, и получают 500 ppm раствора соединения.
Рольки листьев капусты (Brassica oleralla) находились в чашках, каждая диаметром 3 см, в которые помещали увлажненную бумагу. Затем в каждую чашку запускали личинки персиковой тли (Myzus persical) на 5-возрастной стадии и опрыскивают разбрызгивателем (500 г/га). После чего чашки помещают в термостат.
Через 7 дней подсчитывают число выживших особей персиковой тли и по уравнению, приведенному в примере 1, определяют смертности. Испытание проводят для каждого соединения 4 раза.
В результате высокий эффект (100% смертности) показывают следующие соединения.
Соединения, N: 9, 10, 12, 15, 25, 27, 28, 32, 33, 34, 36, 37, 38, 39, 54, 55, 56, 58, 59,61,62,64, 75,76,84,85,87,93,95,96,97,100, 101, 102, 103, 104, 105, 107, 108, 110, 111, 115, 116, 118, 119, 120, 123, 124, 125, 126, 156, 159, 160, 161, 163, 164, 165, 167, 168, 169, 170, 173, 201, 202, 203, 204, 207, 208, 209, 211, 212, 215, 228, 231, 234, 244, 245, 246, 247, 250, 251, 255, 257, 259, 260, 261, 262, 264, 265, 266, 268, 270, 271, 301, 302, 305, 306, 307, 310, 314, 318, 319, 320, 321.
Пример испытания 7. Испытание на инсектицидную активность против моли капустной (Plutella xylostella).
5% -ный эмульгируемый концентрат (или 25% смачиваемого порошка) соединения настоящего изобретения разбавляют водой, содержащей вещество, улучшающее смачиваемость, и получают 500 ppm раствора соединения.
Листья капусты (Brassica oleracea) погружают в раствор сушат воздухом и помещают в лабораторную чашку диаметром 7 см. Затем в каждую чашку выпускают 10 личинок капустной моли (Plutella xylostella) на третьей возрастной стадии и указанные чашки с личинками помещают в термостат.
Через 20 дн подсчитывают число появившихся взрослых особей, а процент смертности подсчитывают при помощи уравнения (1). Испытание проводят дважды для каждого соединения.
В результате высокую эффективность (100% смертности) показали следующие соединения, N: 9, 10, 11, 12, 15, 17, 19, 24, 25, 27,28,32,33,34,38,39,80,81,85,104, 105, 118, 119, 124, 125, 127, 155, 156, 201, 202, 203, 204, 206, 207, 211, 212, 214, 215, 230, 231, 234, 236, 237, 243, 244, 245, 246, 247, 249, 250, 255, 256, 257, 263, 264, 265, 271.
Пример испытания 8. Испытание на инсектицидную активность против долгоносика кукурузного (Sitophilus oryzae)
5% -ный
эмульгируемый концентрат (или
25% смачиваемого порошка) соединения настоящего изобретения разбавляют водой, содержащей вещество, улучшающее смачиваемость, и получают 500 ppm раствора соединения.
10 г неразмолотого риса в лабораторной чашке погружают в полученный раствор и сушат воздухом (0,5 г/кг неразмолотого риса), а затем в эту чашку напускают по 10 взрослых особей долгоносика кукурузного, самцов и самок, после чего эти чашки помещают в термостат. Через 90 дн подсчитывают число погибших взрослых насекомых. Испытание проводят для каждого соединения дважды.
В результате во всех чашках, обработанных любым из приведенных ниже соединений, не обнаружено ни одного взрослого насекомого.
Соединения, N: 24,33,62,83,100, 104, 106, 109, 115, 116, 118, 119, 120, 155, 160, 164, 165, 168, 203, 205, 206, 207, 211, 212, 228, 231, 237, 239, 240, 243, 244, 245, 246, 247, 249, 257, 264, 266.
Пример испытания 9. Испытание на инсектицидную активность против таракана рыжего пруссака (Blatella germanica).
Во взвешенную прозрачную небольшую пробирку помещают 5%-ный эмульгируемый концентрат соединения настоящего изобретения (или 25% смачиваемого порошка или 20% масляного раствора), добавляют туда ацетон и получают 500 ppm ацетонового раствора соединения, 10 см3 этого ацетонового раствора добавляют к 10 г измельченной пищи для небольших насекомых, помещенной в лабораторный сосуд диаметром 9 см. Затем эту смесь перемешивают, а ацетон отгоняют (0,5 г/кг измельченной еды), после чего этот сосуд помещают в большую чашку диаметром 20 см для приманки. В эту большую чашку запускают 10 зародышей тараканов на 5-возрастной стадии (Blatella germanica). В указанную большую чашку помещают пропитанную водой гигиеническую вату для обеспечения насекомых влагой. Через 60 дн проводят оценку путем подсчета числа появившихся взрослых особей. Для каждого соединения испытание проводят дважды.
В результате во всех чашках, обработанных любым из приведенных ниже соединений, не обнаружено ни одного взрослого насекомого.
Соединения, N: 201, 202, 203, 204, 206, 207, 211, 212, 230, 236, 239, 243, 244, 245, 246, 247, 250, 251, 257, 265, 266.
Далее приводятся примеры, в которых описаны испытания, проведенные с соединениями настоящего изобретения и с соединениями, описанными в патентах ЕР-199281 и ЕР-183212, способами, описанными ниже и при аналогичных условиях.
Сравнительный пример 10. Испытание на инсектицидную активность против рисовых дельфицид (Nilaparnata
lugens)
5% -ный эмульгируемый концентрат (или 25% смачиваемого порошка) соединения настоящего изобретения разбавляют водой, содержащей вещество, улучшающее смачиваемость, и получают 500 ppm
раствора соединения.
Стебли и листья рисовых растений, находящихся в горшках размером 1 м2, обрабатывают 100 мл полученного раствора, а затем сушат воздухом (500 г/га), после чего в горшки с растениями запускают 20 личинок рисовых дельфицид на второй возрастной стадии (Nilaparvata lugeus), которые обладают устойчивостью к органическим фосфорным инсектицидам и карбаматным инсектицидам.
Обработанные таким образом рисовые растения накрывают цилиндрической проволочной сеткой и помещают в термостат.
Через 30 дн подсчитывают число паразитов на растениях и определяют смертность при помощи уравнения (1).
Испытания проводят для каждого соединения дважды. (Испытания проводят при условиях, аналогичных описанным в испытательном примере 2 настоящего описания).
Сравнительный пример 11. Испытание на инсектицидную активность против рисовых дельфицид (Nilaparvata lugeus)
5% -ный
эмульгируемый концентрат (или 25% смачиваемого порошка) соединения настоящего изобретения разбавляют водой, содержащей вещество, улучшающее смачиваемость, и получают 500 ppm раствора соединения.
Стебли и листья рисовых растений, находящихся в горшках размером 1 м3, обрабатывают 20 мл полученного раствора, а затем сушат воздухом (100 г/га), после чего в горшки с растениями запускают 20 личинок рисовых дельфицид на второй возрастной стадии (Nilaparvata lugeus), которые обладают устойчивостью к органическим фосфорным инсектицидам и карбаматным инсектицидам.
Обработанные таким образом рисовые растения покрывают цилиндрической проволочной сеткой и помещают в термостат. Через 30 дн подсчитывают число паразитов на растениях и определяют процент смертности при помощи уравнения (1). Испытания проводят для каждого соединения дважды.
Сравнительный пример 12. Испытание на инсектицидную активность против хрущака каштанового (Tribolium castaneum).
В небольшую прозрачную пробирку помещают 5%-ный эмульгируемый концентрат соединения настоящего изобретения или 25% смачиваемого порошка (или его 20% -ного масляного раствора), а затем добавляют ацетон, в результате чего получают 500 ppm ацетонового раствора соединения. 10 см3 указанного ацетонового раствора добавляют к 10 г пшеничной муки, помещенной в чашку диаметром 9 см. После перемешивания из смеси отгоняют ацетон (0,5 г/кг муки). Затем в чашку запускают по 10 взрослых особей самцов и самок хрущака каштанового (Tribolium castaneum). Чашку, содержащую взрослых насекомых, помещают в термостат. Через 90 дн проводят подсчет погибших особей. Испытание проводят дважды для каждого соединения. (Испытания проводят при условиях, аналогичных описанным в испытательном примере 3 настоящего описания).
Сравнительный пример 13. Испытание на инсектицидную активность против хрущака каштанового (Tribolium castaneum).
5% -ный эмульгируемый концентрат (или 25% смачиваемого порошка или 20% масляного раствора) настоящего соединения разбавляют деонизованной водой и получают 500 ppm раствора соединения (0,1 г/кг).
2 мл раствора смешивают с 10 г пшеничной муки, помещенной в чашку диаметром 9 см. После перемешивания из смеси отгоняют ацетон (0,5 г/кг муки). Затем в чашку запускают по 10 взрослых особей самок и самцов хрущака каштанового (Tribolium castaneum). Чашку, содержащую взрослых насекомых, помещают в термостат. Через 90 дн проводят оценку путем подсчета погибших особей. Испытания проводят дважды для каждого соединения.
Сравнительный пример 14. Испытание на инсектицидную активность против огневки сухофруктовой (Cadra cautella).
В прозрачную небольшую пробирку помещают 5%-ный эмульгируемый концентрат соединения настоящего изобретения (или 25%-ный смачиваемый порошок или его 20%-ный масляный раствор) и затем добавляют ацетон, в результате чего получают 500 ppm ацетонового раствора соединения. 10 см3указанного ацетонового раствора добавляют к 10 г рисовых отрубей, помещенных в чашку диаметром 9 см. После перемешивания полученной смеси ацетон отгоняют (0,5 г/кг рисовых отрубей). Затем в эту чашку запускают 10 личиной огневки (Cadra cautella). Чашку с личинками помещают в термостат. Через 30 дн проводят оценку путем подсчета числа взрослых особей. Испытания проводят дважды для каждого соединения.
(Испытания проводят при условиях, аналогичных описанным в испытательном примере 5 настоящего описания).
Сравнительный пример 15. Испытание на инсектицидную активность против огневки сухофруктовой (Cadra cautella).
В прозрачную небольшую пробирку помещают 5%-ный эмульгируемый концентрат соединения настоящего изобретения (или 25%-ный смачиваемый порошок или 20% -ный масляный раствор), затем добавляют ацетон, в результате чего получают 500 ppm ацетонового раствора соединения.
2 мл ацетонового раствора соединения, полученного в сравнительном примере 14, смешивают с 10 г рисовых отрубей, помещенных в чашку диаметром 9 см. Затем смесь перемешивают, а ацетон отгоняют (0,1 г/кг рисовых отрубей). Затем в эту чашку запускают 10 личинок огневки (Cadra cautella). Чашку с личинками помещают в термостат. Через 30 дн проводят оценку путем подсчета числа взрослых особей. Испытание проводят дважды для каждого соединения.
Сравнительный пример 16. Испытание на инсектицидную активность против комара-пискуна (Cullex pipiens pallens).
5%-ный эмульгируемый концентрат (или 25%-ный смачиваемый порошок или 20% -ный масляный раствор) соединения настоящего изобретения разбавляют деионизованной водой и получают 10 ppm раствора соединения (0,01 г/л).
200 мл указанного раствора выливают в глубокий сосуд диаметром 9 см и высотой 6 см. В указанный сосуд запускают 10 личинок комара-пискуна (Culex pipiens pallens). Сосуд, содержащий личинки, помещают в термостат при 25оС. Через 7 дн подсчитывают количество погибших особей. Для каждого соединения испытания проводят дважды. (Испытания проводят при условиях, аналогичных описанным в испытательном примере 4 настоящего описания).
Сравнительный пример 17. Испытание на инсектицидную активность против комара-пискуна (Culex pipiens pallens).
10 ppm раствора, полученного в сравнительном примере 16, десятикратно разбавляют. Раствор выливают в глубокий сосуд диаметром 9 см и 6 см высотой. В этот сосуд запускают 10 личинок комара-пискуна (Culex pipiens pallens). Сосуд, содержащий личинки, помещают в термостат при 25оС. Через 7 дн подсчитывают количество погибших особей. Для каждого соединения испытания проводят дважды.
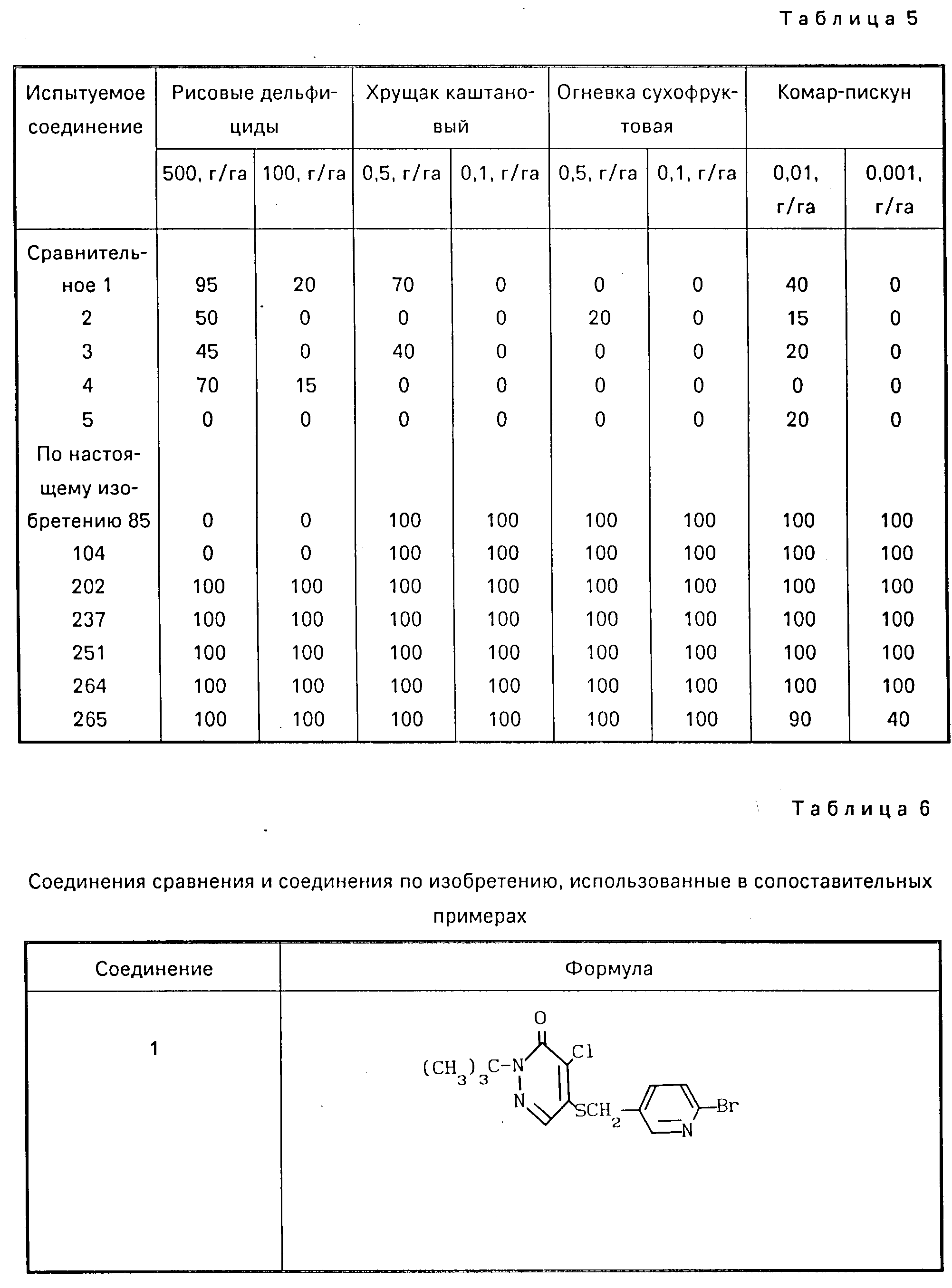
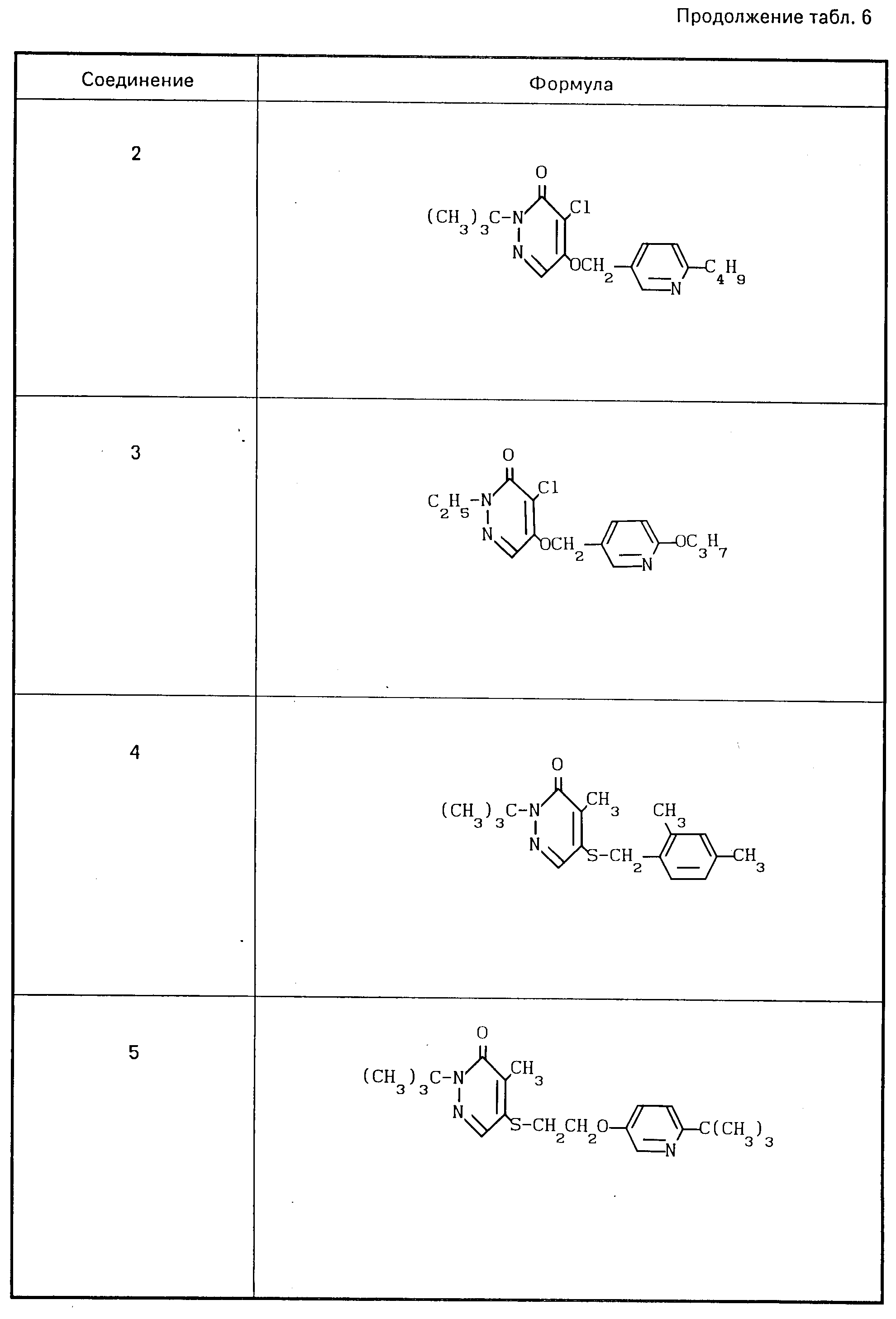
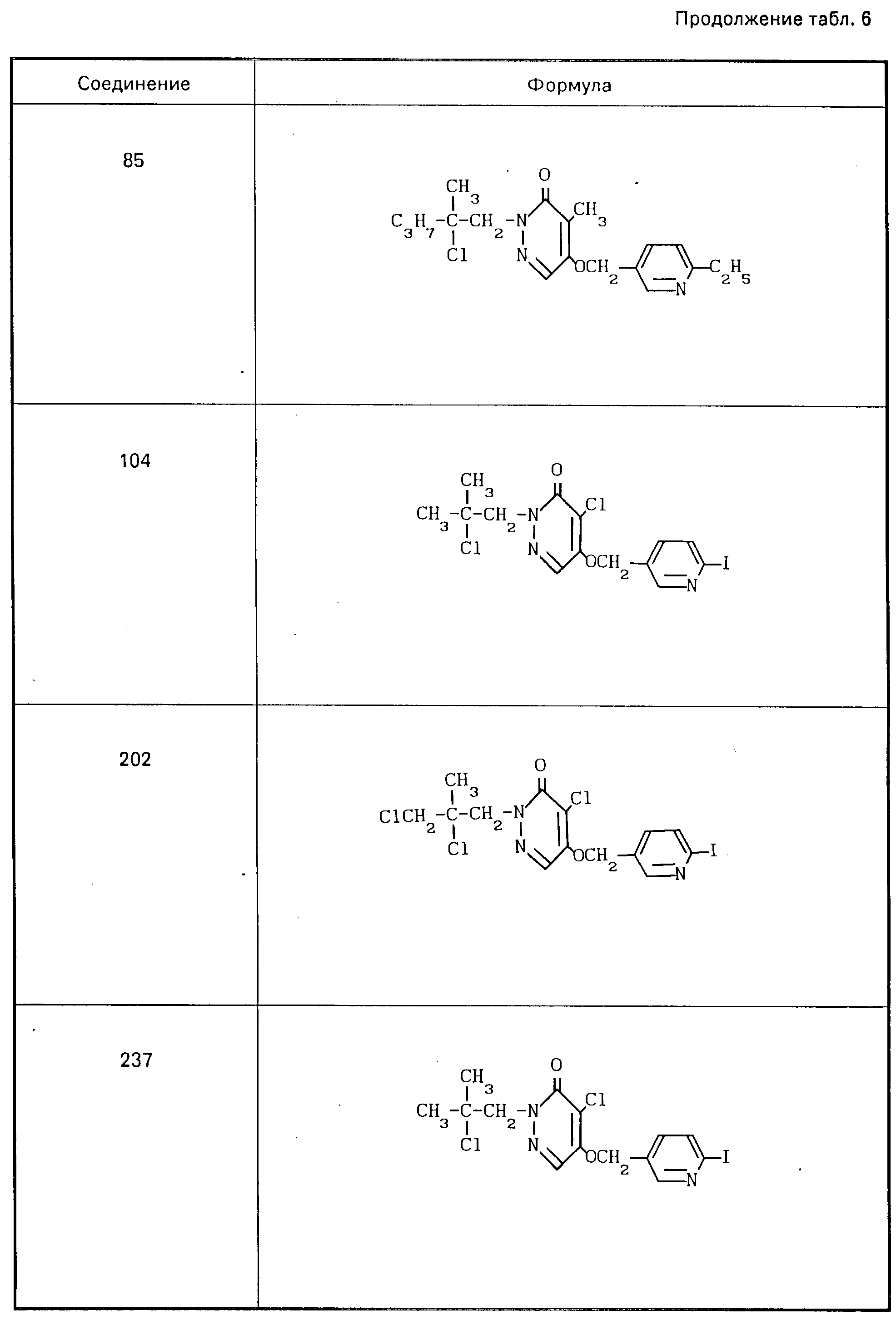
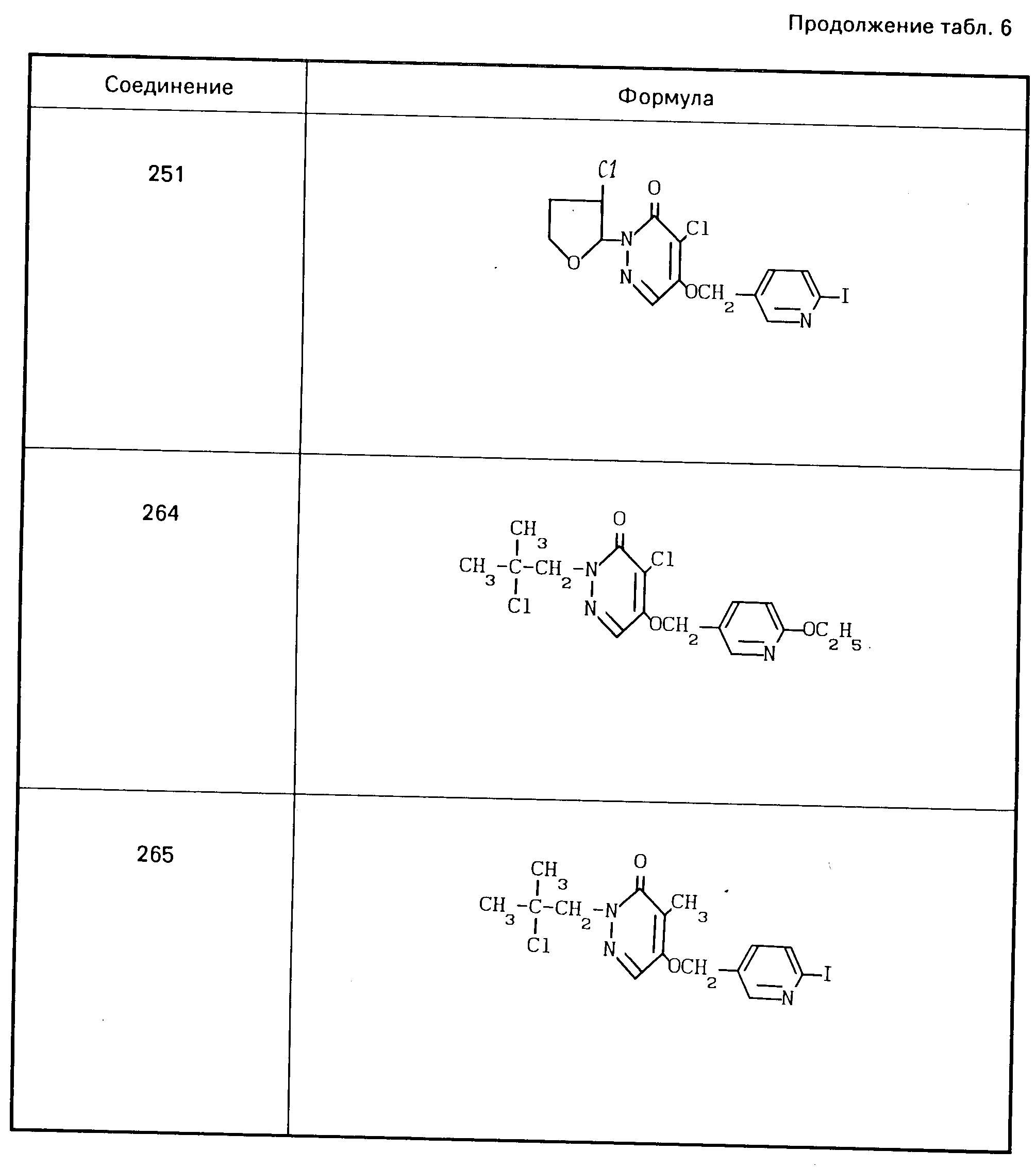
Результаты описанных сравнительных испытаний и структурные формулы соединений приведены в табл.5,6.
Реферат
Использование: сельское хозяйство, химические способы защиты растений. Сущность изобретения: продукт ф-лы (1), где R- C4-C5 -алкенил, C4 -алкил, замещенный OCH3 G-Ra, где G - h, или RbO; Rb -C1-C2 -алкил; Ra -галоид- C3-C8 -алкилен, дигалоид- C3-C6 -алкилен, тригалоид- C3-C4 -алкилен, галоид- C3-C4 -алкенилен, галоид- C6-C8 -циклоалкилен, галоид- C4-C5 -оксациклоалкилен, A-галоген или CH3, X-атом кислорода или серы, J - CH2Q′, CH2CH2OC6H4-4Y, CH2CH(CH3)OC5H4N, (CH2)3C ≡ CBr, Q′ - замещенный фенил, пиридил, тиенил, нафталин. Способ борьбы с вредными насекомыми, использующий указанный продукт в количестве 100 - 500 г/га для обработки растений, 0,1 - 0,5 г/кг для приготовления приманки и 1-10 г/м3 для обработки помещений. Структура соединения ф-лы I:
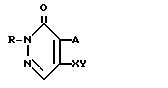
Формула
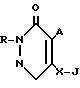
где R C4 C5-алкенильная группа, C4-алкильная группа, замещенная метокси, или группа G Ra, где G водород или RbO, в которой Rb C1 C2-алкильная группа, Ra C3 C8-галоидалкиленовая группа, C3 - C6-дигалоидалкиленовая группа, C3 C4 -тригалоидалкиленовая группа, C3 C4-галогеналкениленовая группа, C6 - C8-галоидированная циклоалкиленовая группа, C4 - C5 -галоидированная оксациклоалкиленовая группа, если G водород, и Rа С3 С5-галоидалкиленовая группа, если G обозначает RbO;
A галоген или метильная группа;
X кислород или сера;
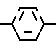
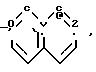
J группа формулы
CH2Q1,
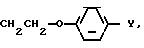
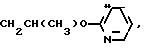
(CH2)3C ≡ CBr,
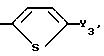
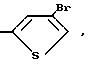
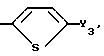
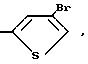
где Q1
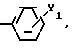
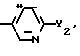
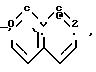
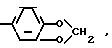
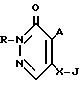
Y1 галоген, C2 C4-алкил, C1 -C3-алкоксигруппа, трифторметил, SOCH3, SO2CH3, фенокси, CN, 2, 4-дихлор, OCF3, CO2CH3;
Y водород, хлор, метил;
Y2 галоген, C2 C4 алкоксигруппа;
Y3 метил, бром, йод.
где R C4 C5-алкенильная группа, C4-алкильная группа, замещенная метокси, или группа G Ra, где G водород, или RbO, где Rb C1 C2-алкильная группа,
Ra C3 C8-галоидалкиленовая группа, C3 - C6-дигалоидалкиленовая группа, C3 C4-тригалоидалкиленовая группа, C3 C4-галогеналкениленовая группа, C6 - C8-галоидированная циклоалкиленовая группа, C4 - C5-галоидированная оксациклоалкиленовая группа, если G водород, и Ra C3 C5-галоидалкиленовая группа, если G RbO;
A галоген или метильная группа;
X кислород или сера;
J группа формулы
CH2Q1;
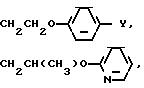
(CH2)3 ≡ CBr,
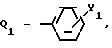
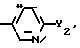
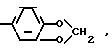
Y1 галоген, C2 C4-алкил, C1 - C3-алкоксигруппа, трифторметил, SOCH3, SO2CH3, фенокси, CN, 2,4-дихлор, OCF3, CO2CH3;
Y водород, хлор, метил;
Y2 галоген, C2 C4-алкоксильная группа;
Y3 метил, бром, йод,
в количестве 100 500 г/га для обработки растений, или 0,1 0,5 г/кг для приготовления приманки, или 1 10 г / м3 для обработки помещений.
30.07.87 при R группа, G Ra, где G водород, Ra - C3 C8-галоидалкиленовая группа, C3 C6-дигалоидалкиленовая группа, C3 C4-галогеналкениленовая группа, C6 C8-галоидированная циклоалкиленовая группа, C4 C5-галоидированная оксациклоалкиленовая группа, A галоген, X - кислород или сера, J группа формулы CH2Q1,
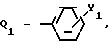
$$121 Y1 галоген, C2 C4-алкил, Y2 галоген;
17.12.87 при R RbO Ra, Ra C3 - C5-галоидалкиленовая группа, или H Ra, где Ra C3 - C4-тригалоидалкиленовая группа,
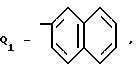
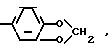
Y1 C1 C3-алкоксигруппа, трифторметил, SOCH3, SO2CH3, фенокси, CN, 2,4-дихлор;
22.06.88 при R -C4 C5-алкенильная группа, C4-алкильная группа, замещенная метокси, A метильная группа,
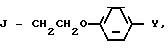
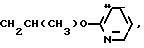
(CH2)3C≡CBr,
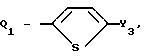
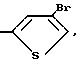
Y1 OCF3, CO2CH3, Y водород, хлор, метил, Y2 C2 C4 -алкоксильная группа, Y3 метил, бром, йод.

Комментарии