Химические реакции со сниженным содержанием влаги - RU2375298C2
Код документа: RU2375298C2
Чертежи



Описание
Настоящее изобретение относится к получению соединений по реакциям, для которых неблагоприятны высокие концентрации воды.
Одной из важных с промышленной точки зрения реакций является превращение оксида титана в субоксиды титана (TinO2n-1) в соответствии со следующей обратимой реакцией:

Ниже превращение оксида титана в субоксид будет считаться прямой реакцией со смещением равновесия вправо.
Субоксиды титана являются важными для промышленности материалами, поскольку некоторые из них электропроводны и/или обладают высокой коррозионной стойкостью. Субоксидные материалы нашли широкое применение в электрохимических устройствах, таких как датчики, реакторы электрохимического синтеза и обработки воды, топливные элементы и аккумуляторы.
В количествах приблизительно до 100 кг субоксиды титана производятся в печи периодического действия, где аликвоты порошка диоксида титана нагревают до температуры более 1000°С в восстановительной среде (в формуле (1), выше - это водород).
В ЕР 0478152 описан один из способов периодического производства субоксидов титана, в котором диоксид титана помещают в печь на графитовый лист, и при нагревании до 1200°С лропускают газообразный водород.
В патенте США 2848303 описано восстановление диоксида титана путем смешивания его с углеродом и нагревания в присутствии водорода.
Для каждого значения n константа равновесия реакции является функцией парциального давления водорода и воды, что будет принято во внимание в дальнейшем. Следовательно, путем повышения парциального давления водорода и/или снижения парциального давления воды можно сместить равновесие реакции вправо.
К тому же, реакция (1) является эндотермической, и, таким образом, для осуществления прямой реакции требуется постоянный подвод тепла.
Из рассмотрения термодинамики данной системы видно, что в любом наборе равновесных условий будут присутствовать только две твердых фазы, и что повышение температуры ускоряет прямую реакцию при малых n (преодолевая фактор энтропии).
В стандартной печи периодического действия аликвота диоксида титана статична и, следовательно, разные ее части подвергаются воздействию различных условий (температура, парциальное давление водорода и воды). Такое неоднородное воздействие означает, что продукт обычно представляет собой смесь субоксидов титана. Например, на внешней границе аликвоты (где перенос массы и энергии практически беспрепятственный) материал подвергается более значительному восстановлению, чем находящийся в центре (где подвод водорода и отвод воды затруднен). Обычно материал на поверхности стационарной аликвоты содержит Тi3O5 или Ti4O7, a в центре - Ti8O15, Ti9O17 или Ti10O19 и даже более.
Электрические и химические свойства каждого субоксида (то есть для каждого n) значительно отличаются. Обычно желательно максимально увеличить выход какого-либо одного нужного субоксида и минимизировать выход остальных. Например, Ti4O7 и Ti5O9 обладают наиболее высокой электропроводностью и, следовательно, широко применимы при производстве аккумуляторов. Электропроводность Тi3O5 и Тi2О3 низкая, при этом они уязвимы для воздействия большинства используемых в аккумуляторах электролитов (например, H2SO4), в результате образуют ионы титанатов, что нежелательно для аккумуляторов, как с точки зрения механики, так и химизма процессов. Таким образом, с целью применения в аккумуляторах желательно максимально повысить выход Ti4O7 и Ti5О9 и снизить выход Ti3O5 и Тi2О3.
Вообще, невозможно физически разделить различные субоксиды, однажды полученные в виде смеси. То есть желательно так усовершенствовать производственный процесс, условия тепло- и массопереноса, чтобы выход нужного субоксида (субоксидов) был максимально возможным.
В других процессах химики стремились облегчить тепло- и массоперенос путем создания устройств непрерывного действия, в которых твердая фаза перемещается относительно газа и/или перемешивается, что обеспечивает однородность условий по всему объему твердой фазы.
Стандартное оборудование включает вращающиеся трубчатые печи, устройства с псевдоожиженным слоем, с падающим плотным слоем, свободно падающими частицами и им подобные. Эти устройства могут предусматривать непосредственное нагревание при помощи горелки, горячие дымовые газы которой, попадая в реакционную камеру, поддерживают в ней нужную температуру реакции. Также известны способы косвенного нагревания, заключающиеся в подводе тепла, образуемого при помощи горелки или электронагрева, к стенкам реакционной камеры и поддержании за счет теплопроводности нужной температуры реакции в ней.
Вообще, не представляется возможным создать печь с косвенным нагреванием, рабочая температура которой превышала бы 1200°С, поскольку это значение выше максимальных рабочих температур большинства металлов, используемых в качестве конструкционных материалов.
Печи с рабочей температурой более 1200°С обычно ограничиваются вариантом с прямым нагреванием. Это высокоэффективный способ передачи тепла. Однако дымовые газы, полученные от сжигания обычных топлив (таких как углеводороды или водород), содержат влагу, а в случае углеводородного топлива - также оксиды углерода.
При использовании водорода (в качестве восстановителя при высоких температурах) присутствие диоксида углерода весьма нежелательно, так как идет следующая реакция:

Это означает, что горелки с прямой подачей дымовых газов в данном случае не подходят или представляют трудности для использования при высоких температурах, когда восстановителем является водород, поскольку наличие СО2 ограничивает количество расходуемого в реакции водорода. Кроме того, при сжигании углеводородов или водорода и в результате реакции СO2 и H2 образуется вода.
Таким образом, объектом настоящего изобретения является преодоление или, по меньшей мере, частичное решение одной или более проблем, возникающих на современном этапе развития техники при проведении реакций при высоких температурах и/или при проведении реакций, в которых один или более реагентов (или продуктов) чувствителен к влаге.
Более конкретным, но не исключительным объектом настоящего изобретения является реакционная печь, способная работать при температуре выше 1200°С.
Кроме того, объектом настоящего изобретения является устройство, пригодное для непрерывного производства восстановленных соединений.
Кроме того, более конкретным, но не исключительным объектом настоящего изобретения является способ получения субоксидов, например субоксидов титана, и печь для производства субоксидов.
Кроме того, неисключительным объектом настоящего изобретения являются способы более эффективного и более поддающегося управлению производства веществ по реакциям, чувствительным к присутствию воды.
Одним аспектом настоящего изобретения является способ непрерывного получения субоксида(ов) титана, включающий непрерывную подачу диоксида титана в реакционную камеру, противоточную подачу в реакционную камеру газа-восстановителя, по существу не содержащего влаги, взаимодействие поданного таким образом оксида с газом-восстановителем, удаление избытка газа, содержащего влагу, и непрерывный сбор субоксида(ов) титана.
Другим аспектом настоящего изобретения является способ получения субоксидов титана, включающий непрерывную подачу диоксида титана в реакционную камеру, нагревание газа-восстановителя, подачу нагретого газа в эту камеру, удаление избытка газа, содержащего влагу, для создания в ней не содержащей влаги восстановительной атмосферы, нагретой до температуры выше 1200°С. Окисленное соединение предпочтительно представляет собой диоксид титана, а восстановленное соединение - субоксид титана.
Используемый газ может включать один или более из следующих компонентов: водород, монооксид углерода, метан, пропан или другие углеводороды.
Данный газ нагревается, предпочтительно, при помощи плазменной горелки или СВЧ-излучения.
Такая восстановительная атмосфера предпочтительно создается газом-восстановителем. Тепло к газу может подводиться при помощи плазменной горелки или СВЧ-излучения.
Другим аспектом настоящего изобретения является устройство для получения субоксидов титана путем непрерывной реакции твердого диоксида титана (1; 10) при температурах более 1200°С, причем устройство (2; 12; 22) включает реакционную камеру, вмещающую по меньшей мере твердый оксид титана (1; 10), в которой перемещается твердый диоксид титана, и средства нагрева (4; 14; 24) для нагрева газа-восстановителя и получения источника нагретого газа-восстановителя для восстановления диоксида титана, причем газ является по существу безводным и предназначен для нагревания реакционной камеры до температуры выше 1200°С, и выход для избытка газа, содержащего влагу.
Такая реакционная камера может представлять собой вращающуюся трубчатую печь, вертикальную неподвижную трубчатую печь, устройство с псевдоожиженным слоем и другие известные специалистам типы устройств.
Данное устройство предпочтительно содержит средства для непрерывной подачи реагента в реакционную камеру. Оно может также включать приспособления для непрерывного сбора продукта реакции на выходе из реакционной камеры.
Приспособлениями для нагревания предпочтительно являются плазменная горелка или источник СВЧ-излучения.
Кроме того, данное устройство может включать источник реагента, предназначенный для подачи (например, в виде потока) реагента в реакционную камеру.
Средства для нагревания предпочтительно нагревают реагент до того, как он поступает в реакционную камеру.
В предпочтительном варианте воплощения настоящего изобретения реагентом является газ, наиболее предпочтительно - газ, создающий в реакционной камере восстановительную атмосферу, например водород и/или монооксид углерода; в любом случае не должны использоваться газы, содержащие металлы.
Одно из соединений, являющееся реагентом, может быть подано в реакционную камеру до начала реакции. Таким соединением предпочтительно является диоксид титана.
Кроме того, данное устройство может включать приспособления для подачи в реакционную камеру других веществ, которые взаимодействуют с водой, в любом виде присутствующей там, и снижают ее концентрацию, например углерода, монооксида углерода. Также возможно введение углеводородов, таких как метан, этан, пропан, бутан, этилен, пропилен, бутилен и т.д.
Для более полного понимания настоящего изобретения, далее, исключительно в качестве примера, оно будет описано со ссылкой на сопроводительные чертежи, где:
На фиг.1 схематично показано соответствующее настоящему изобретению устройство, представляющее собой вращающуюся печь.
На фиг.2 схематично показан соответствующий настоящему изобретению реактор с псевдоожиженным слоем.
На фиг.3 схематично показана соответствующая настоящему изобретению трубчатая печь со свободным падением реагента.
На фиг.1 показано устройство для непрерывного восстановления реагентов 1, включающее вращающуюся печь 2, способную вращаться вокруг своей главной оси в направлении, указанном стрелкой X. Твердый материал, например диоксид титана, непрерывно подается в печь 2 с верхнего конца 3, как показано стрелкой А. Плазменная горелка 4 предназначена для нагревания непрерывного потока газообразного водорода, обозначенного стрелкой В, который подается в печь 2 с противоположного конца 5 печи 2.
Печь 2 включает стальную обечайку, облицованную отражающей футеровкой в виде блоков из оксида алюминия (не показаны). Печь 2 также снабжена изготовленными из оксида алюминия «подъемниками» (не показаны), которые содействуют продвижению твердого материала от конца 3 к концу 5 печи 2. Толщина отражающей футеровки выбирается так, чтобы температура стальной обечайки не выходила за пределы, определяемые механическими и конструкционными параметрами (например, около 200°С).
Благодаря подаче газообразного водорода В атмосфера внутри печи 2 является восстановительной. Таким образом, в соответствии с реакцией (1), у нижнего конца 5 печи происходит выгрузка субоксида титана, как показано стрелкой С. Избыток газа, содержащий влагу, образовавшуюся в ходе реакции, выходит из печи, как указывает стрелка D.
На фиг.2 показано другое устройство для непрерывного восстановления реагентов 10, включающее реактор с псевдоожиженным слоем 12. Диоксид титана непрерывно подается в реактор 12 у верхней части 13, как показано стрелкой А′.
Реактор 12 включает стальную обечайку, облицованную отражающей футеровкой в виде блоков из оксида алюминия (не показаны). Здесь толщина отражающей футеровки тоже выбирается так, чтобы температура стальной обечайки не выходила за пределы, определяемые механическими и конструкционными параметрами (например, около 200°С).
Плазменная горелка 14 предназначена для нагревания непрерывного потока газообразного водорода, обозначенного стрелкой В′, который подается в реактор 12 через смесительную камеру 15 у основания реактора 12. Нагретый водород В′ проходит вверх по реактору 12 через массу реагента А′, которая становится при этом псевдоожиженной.
Благодаря наличию газообразного водорода В′ атмосфера в реакторе 12 является восстановительной. Таким образом, в соответствии с реакцией (1), субоксид титана выгружается из реактора 12 через выходное устройство 16, как показано стрелкой С′. Избыток газа, содержащий влагу, образовавшуюся в ходе реакции, выходит из реактора, как указывает стрелка D′.
На фиг.3 показано еще одно устройство для непрерывного восстановления реагентов 20, включающее трубчатый реактор 22 со свободным падением реагентов. Диоксид титана непрерывно подается в реактор 22 у верхней части 23, как показано стрелкой А′′, и свободно падает под действием силы тяжести к основанию реактора 22.
Реактор 22 включает стальную обечайку, облицованную отражающей футеровкой в виде блоков из оксида алюминия (не показаны). Здесь толщина отражающей футеровки тоже выбирается так, чтобы температура стальной обечайки не выходила за пределы, определяемые механическими и конструкционными параметрами (например, около 200°С).
Плазменная горелка 24 предназначена для нагревания непрерывного потока газообразного водорода, обозначенного стрелкой В′′, который подается в реактор 22 через камеру 25 у снования реактора 22. Поток нагретого водорода В′′ поднимается по реактору 22, навстречу падающему реагенту А′′.
Благодаря наличию газообразного водорода В′′ атмосфера в реакторе 22 является восстановительной. Таким образом, в соответствии с реакцией (1) субоксид титана выгружается из реактора 22 через выходное устройство 26, как показано стрелкой С′′. Избыток газа, содержащий влагу, образовавшуюся в ходе реакции, выходит из реактора, как указывает стрелка D′′.
В каждом из описанных выше устройств 1, 10 и 20 к потоку газообразного водорода В, В′ и В′′ может быть добавлен монооксид углерода. Тогда СО будет взаимодействовать с водой в соответствии с реакцией (2). Кроме того, к подаваемому TiO2 может быть добавлен углерод, который будет взаимодействовать с водой в соответствии со следующими реакциями:
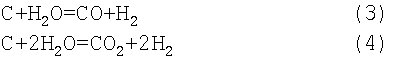
Из чертежей видно, что реагенты подаются в противотоке, также понятно, что это наиболее предпочтительный вариант, поскольку в этом случае «наиболее восстановленный» твердый реагент контактирует с «самым сухим» водородом. Однако в качестве охватываемых настоящим изобретением следует иметь в виду и другие варианты (прямоток, движение под прямым углом и т.д.).
Из термодинамических расчетов (см. Eriksson и Pelton; Mett. Trans. В.; 24 В (1993), стр.795-805) видно, что для достижения равновесного состава Тi5O9 при использовании 5 молей H2 на моль TiO2 требуется рабочая температура около 1400°С.
Для сравнения отметим, что если бы подаваемый водород содержал 5 об.% воды, а также оксиды углерода, поступающие из метановой горелки, работающей при 10% избытке воздуха, необходимая равновесная температура возросла бы до 1650°С. Это значение очень близко к температуре плавления субоксидов титана, что, вероятно, может вызвать трудности, связанные с их спеканием. Следовательно, для достижения удовлетворительного качества продукта, снижения эксплуатационных расходов и увеличения срока службы оборудования желательно снижение температуры.
Также можно показать, что в условиях равновесия в реакции с сухим водородом при 1500°С будет образовываться Ti4O7, при этом на один моль TiO2 потребуется 6,6 моль H2. При использовании упоминаемой выше горелки, представляющей известный уровень техники, при 1500°С равновесный состав будет представлять собой смесь Тi9O17 и Ti10O19. Для получения Ti4O7 с использованием этой горелки потребуется втрое большее количество водорода.
Таким образом, было показано, что путем использования источника тепла с существенно сниженным содержанием влаги можно уменьшить рабочую температуру или количество реагентов. В любом случае, настоящее изобретение делает непрерывное производство субоксидов титана более экономичным, чем это было достижимо ранее.
Следует принять во внимание, что, хотя приведенное выше описание относится к восстановлению TiO2, существует много других реакций, для осуществления которых настоящее изобретение может оказаться полезным. Это касается любого чувствительного к влаге реагента или продукта при проведении реакции в восстановительной атмосфере. В реакционную камеру может подаваться более чем один твердый реагент. Могут образовываться другие субоксиды. Могут быть использованы другие газы-восстановители, не содержащие металлов (например, магния, натрия и т.д.).
Реферат
Изобретение может быть использовано при получении субоксидов титана, применяемых в производстве топливных элементов и других областях промышленности. Способ непрерывного получения субоксидов титана включает непрерывную подачу диоксида титана в реакционную камеру, противоточную подачу в реакционную камеру газа-восстановителя, по существу не содержащего влаги, взаимодействие поданного таким образом диоксида титана с газом-восстановителем, удаление избытка газа, содержащего влагу, и непрерывный сбор субоксидов титана. Газ-восстановитель может быть подан в реакционную камеру для создания в ней не содержащей влаги восстановительной атмосферы, нагретой до температуры выше 1200°С. В качестве газа-восстановителя используют один или более из группы, включающей водород, монооксид углерода, метан, пропан или другие углеводороды. Предложено устройство для получения субоксидов титана. Изобретение позволяет повысить выход целевых субоксидов титана и уменьшить выход нежелательных субоксидов. 3 н. и 15 з.п. ф-лы, 3 ил.

Комментарии