Способ получения высокочистого нитрата натрия - RU2788906C1
Код документа: RU2788906C1
Чертежи
Описание
Заявляемое изобретение относится к технологии неорганических материалов и представляет собой способ получения высокочистого нитрата натрия примесной чистотой не ниже 99,999 мас.% для изготовления двулучепреломляющих оптических элементов. Монокристаллы нитрата натрия высокой примесной чистоты обладают высокими коэффициентами преломления, что ставит их в один ряд с такими материалами, как кальцит и β-борат бария (BBO).
В настоящее время на рынке доступен лишь химически чистый (хч) нитрат натрия, удовлетворяющий требованиям ГОСТ 4168-79, а также нитрат натрия более низкой чистоты. Это связано с тем, что нитрат натрия сегодня используют как азотное удобрение, а также в пищевой промышленности в качестве консерванта, поэтому к этому веществу не предъявляются высокие требования по чистоте. Заявляемые в ГОСТ 4168-79 требования по чистоте по калию и кальцию - основным примесям - составляют не более 0,002 мас.%. Отметим, однако, что заявленный уровень примесной чистоты по калию не всегда соблюдается, и средняя чистота по калию в исходных образцах составляет 0,01 мас.%.
Химически чистый (хч) нитрат натрия непригоден для получения монокристаллов для двулучепреломляющих элементов, что описано в статье A. Sadovskiy, E. Sukhanova, S. Belov, V. Kostikov, M. Zykova, M. Artyushenko, E. Zharikov, I. Avetissov «Axial vibration control of melt structure of sodium nitrate in crystal growth process», опубл.: 2015, и в предшествующих публикациях. В работе также указан способ получения нитрата натрия примесной чистотой 99,999 мас.% путем двойной перекристаллизации из водного раствора, но данный метод не был подробно описан, а также не был описан поэлементный примесный состав полученного вещества. На основе имеющихся литературных данных о растворимости нитрата натрия в воде при различных температурах, которая является крайне высокой (Рабинович В.А., Хавин З.Я. Краткий химический справочник. - Л.: Химия, 1977), можно сделать вывод, что самым главным минусом такого метода является крайне низкий выход целевого продукта как при кристаллизации, так и за счет потерь, возникающих при промывке вещества от маточного раствора.
В патенте RU2495825C1 подробно описан процесс очистки хлорида натрия кристаллизационным методом с добавлением соляной кислоты в процессе кристаллизации. В нем заявлена примесная чистота продукта на уровне 10-5 мас.%. Однако главным недостатком метода служит содержание примеси калия 0,001 мас.% и выше. Также не указан конечный выход продукта, что является важной информацией для промышленного получения вещества.
В диссертационной работе И.Ю. Комендо «Разработка технологии получения калия дигидрофосфата особой чистоты для лазерной техники», опубл.: 2018, описываются различные методы очистки дигидрофосфата калия, среди которых можно отметить кристаллизацию в присутствии комплексообразователя. Отмечается, что использование калиевой соли этилендиаминтетрауксусной кислоты (К2-ЭДТА) в нейтральной среде позволяет снизить примеси хрома и железа. ЭДТА и ее калиевые или натриевые соли являются крайне известными комплексообразователями, и на этом их свойстве основано комплексометрическое титрование в аналитической химии (Дятлова Н.М., Темкина В.Я., Колпакова И.Д., Попов К.И. Комплексоны и комплексонаты металлов. - М., «Химия», 1988). Дополнительно отметим, что данный способ отделения примесей можно использовать не только для снижения содержания хрома и железа в продукте, но также щелочноземельных и иных металлов при правильно подобранных условиях. Впрочем, как способ очистки от примесей, данный метод не получил широкого распространения в химической промышленности.
Задачей предлагаемого изобретения является использование кристаллизационного метода для получения высокочистого нитрата натрия и усовершенствование процесса очистки для устранения вышеописанных недостатков.
Техническим результатом предлагаемого изобретения является получение высокочистого нитрата натрия примесной чистотой не ниже 99,999 мас.% с пониженным содержанием калия (не более 0,001 мас.%) и повышенным выходом конечного продукта.
Указанный технический результат достигается за счет того, что заявлен способ очистки нитрата натрия методом кристаллизации из пересыщенного водного раствора, заключающийся в приготовлении раствора из нитрата натрия (хч) и бидистиллированной воды, соответствующего насыщенному при 90°С, выдерживании при температуре 95°С в течение часа, фильтрации и последующем охлаждении раствора с 90°С до 20°С с постоянной скоростью охлаждения, равной 0,4 град/мин, фильтрации под вакуумом и промывкой продукта от маточного раствора бидистиллированной водой.
Допустимо, что к исходному раствору нитрата натрия добавляется Na2-ЭДТА в количестве 0,005 мас.% от массы используемого нитрата натрия (хч).
Допустимо, что в качестве промывочной жидкости используют растворы бидистиллированной воды и изопропилового спирта (осч) в полном диапазоне концентраций.
Изобретение поясняется графиками.
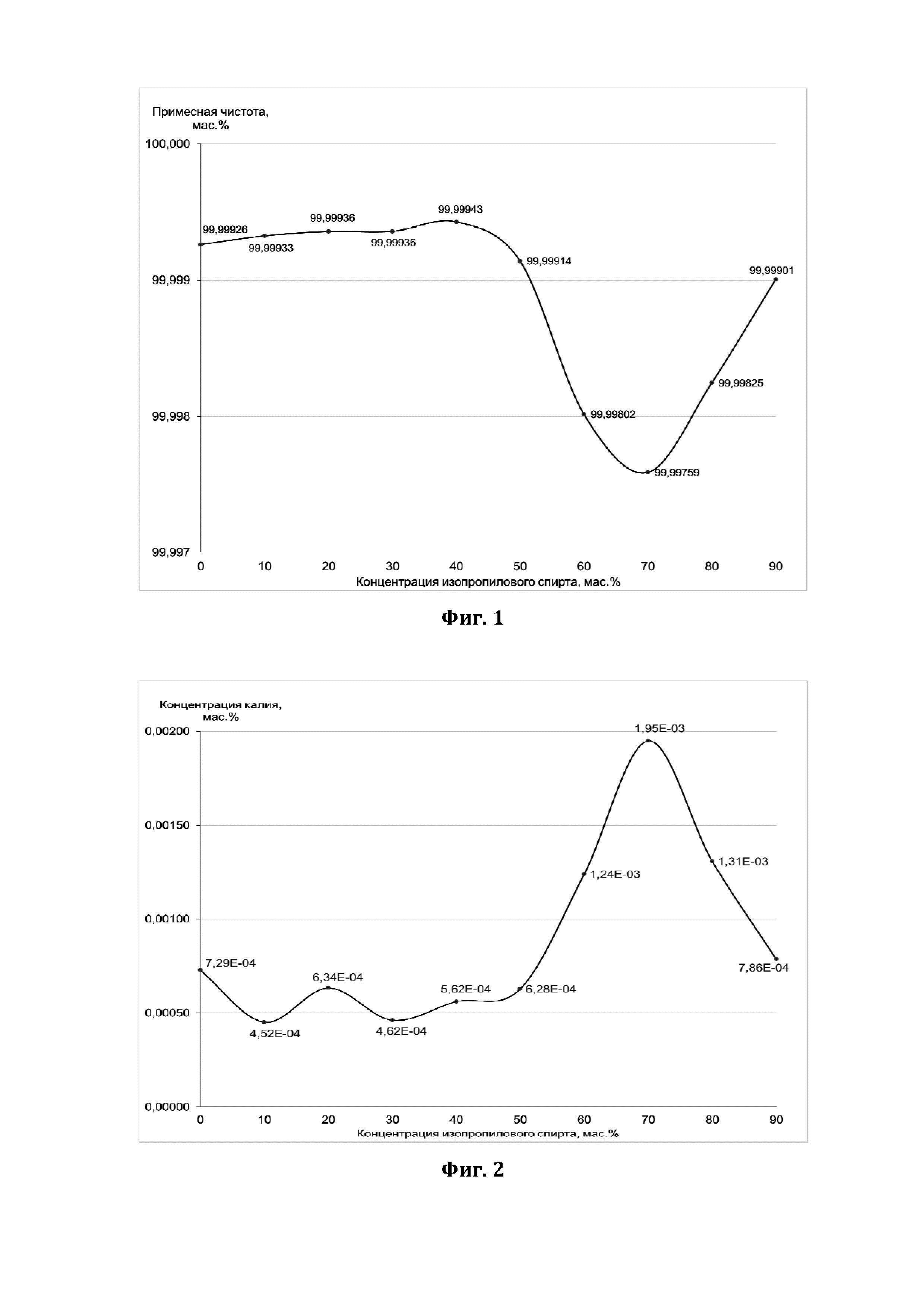
На Фиг. 1 показана примесная чистота получаемого нитрата натрия в зависимости от концентрации промывочной жидкости.
На Фиг. 2 показана концентрация калия в конечном продукте в зависимости от концентрации промывочной жидкости.
Осуществление изобретения
Для выполнения поставленной задачи и достижения технического результата к стандартному методу кристаллизации применяются добавление Na2-ЭДТА для дополнительной очистки от примесей щелочноземельных металлов и d-элементов, контролируемая скорость охлаждения раствора для равномерного осаждения и большей глубины очистки, а также промывание полученного продукта водно-спиртовым раствором для увеличения выхода продукта без потери в качестве.
Способ реализуется таким образом, что химически чистый нитрат натрия переводят в раствор, соответствующий насыщенному при 90°С, с добавлением небольшого количества (0,005 мас.% от массы нитрата натрия) Na2-ЭДТА и выдерживают в течение часа при температуре 95°С, после чего фильтруют и контролируемо кристаллизуют в термостате со скоростью охлаждения 0,4 град/мин от 90°С до 20°С в течение трех часов. Полученные кристаллы отделяют от маточного раствора фильтрацией и промывают бидистиллированной водой или спиртовым раствором, приготовленным из бидистиллированной воды и изопропилового спирта особой чистоты (ОСЧ, СТП ТУ СОМР 2-018-06), определенной концентрации.
Экспериментально обнаружено, что данные факторы влияют на степень очистки вещества, и в совокупности позволяют получать высокочистый нитрат натрия примесной чистотой не ниже 99,999 мас.% с пониженным содержанием калия (0,001 мас.% и ниже) в одну стадию кристаллизации, а также увеличить итоговый выход продукта.
Заявленный способ поясняется следующими примерами.
Пример 1: В двух стаканах из кварцевого готовятся водные растворы нитрата натрия, соответствующие насыщенным при 90°С, из нитрата натрия (ХЧ). Первый раствор (далее - I) остается неизменным, а во второй (далее - II) добавляется 0,005 мас.% Na2-ЭДТА. Оба раствора выдерживают час при 95°С, после чего отфильтровывают на горячем фильтре для удаления механических примесей. После полученные растворы отправляют в термостат, нагретый до 90°С, и начинают охлаждать со скоростью 0,4 град/мин до 20°С.Полученные кристаллы фильтруют под вакуумом, после чего дважды промывают бидистиллированной водой. Полученные образцы затем отправляют в сушильный шкаф на 12 часов, после чего анализируют при помощи ИСП-МС.Перед отбором пробы образцы взвешивались для определения выхода продукта.
Полученная примесная чистота образца I составляет 99,994 мас.%, а образца II - 99,997 мас.%. Чистота исходного образца - 99,98 мас.%.
Результаты масс-спектрометрии представлены в табл. 1.
Таблица 1. Результаты ИСП-МС для образцов, кристаллизованных из водного раствора без Na2-ЭДТА (I) и с Na2-ЭДТА (II)
По полученным результатам можно отметить, что Na2-ЭДТА значительно влияет на результат очистки нитрата натрия. Более того, можно отметить значительное снижение калия в образце II. Допускаем, что это связано с замещением Na2-ЭДТА на K2-ЭДТА, однако это подлежит отдельному изучению.
Выход сухого продукта составляет 10,2%.
Пример 2: В двух стаканах из кварцевого стекла готовятся водные растворы нитрата натрия, соответствующие насыщенным при 90°С, из нитрата натрия (ХЧ). В оба раствора добавляется 0,005 мас.% Na2-ЭДТА. Оба раствора выдерживают час при 95°С, после чего отфильтровывают на горячем фильтре для удаления механических примесей. После один раствор (далее - I) подвергается неконтролируемому охлаждение в резервуаре объемом 5 л, а второй раствор (далее - II) отправляют в термостат, нагретый до 90°С, и начинают охлаждать с постоянным шагом 0,4 град/мин до 20°С.Полученные кристаллы фильтруют под вакуумом, после чего дважды промывают бидистиллированной водой. Полученные образцы затем отправляют в сушильный шкаф на 12 часов, после чего анализируют при помощи ИСП-МС.
Результаты масс-спектрометрии представлены в табл. 2.
Таблица 2. Результаты ИСП-МС для образцов, полученных неконтролируемой (I) и контролируемой (II) кристаллизацией.
Отметим, что контролируемое охлаждение раствора нитрата натрия благотворно влияет на примесную чистоту образца.
Пример 3: В стаканах из кварцевого стекла готовятся водные растворы нитрата натрия, соответствующие насыщенным при 90°С, из нитрата натрия (ХЧ). В растворы добавляются 0,005 мас.% Na2-ЭДТА. Раствора выдерживают час при 95°С, после чего отфильтровывают на горячем фильтре для удаления механических примесей. После полученные растворы отправляют в термостат, нагретый до 90°С, и начинают охлаждать с постоянным шагом 0,4 град/мин до 20°С.Полученные кристаллы фильтруют под вакуумом. Затем один образец дважды промывается бидистиллированной водой, а последующие образцы промываются водно-спиртовыми растворами. Для девяти образцов были приготовлены девять промывочных жидкостей с шагом по содержанию изопропилового спирта в 10 мас.%. Полученные образцы затем отправляют в сушильный шкаф на 12 часов, после чего анализируют при помощи ИСП-МС. Перед отбором пробы образцы взвешивались для определения выхода продукта.
Результаты масс-спектрометрии представлены в табл. 3.
По полученным данным можно выделить, что кристаллы, промываемые спиртовыми растворами от 0 до 50 мас.%, соответствуют необходимой чистоте 99,999 мас.%. Наименьшее содержание калия и других примесей, однако, наблюдается в образце, промытым 30 мас.% спиртовым раствором. Сравнительные данные по примесной чистоте и содержанию калия приведены на фиг.1 и фиг.2 соответственно. Такой продукт имеет выход 24,3%, что является лучшим результатом в сравнении с 10,2%, полученными при промывании бидистиллированной водой.
Таблица 3. Результаты ИСП-МС для образцов, промытых различными концентрациями спиртовых растворителей
Реферат
Изобретение относится к технологии неорганических материалов. Для очистки нитрата натрия методом кристаллизации из пересыщенного водного раствора готовят раствор из нитрата натрия ХЧ и бидистиллированной воды, соответствующий насыщенному при 90°С, выдерживают при температуре 95°С в течение 1 ч, фильтруют и охлаждают раствор с 90°С до 20°С с постоянной скоростью охлаждения, равной 0,4 град/мин. Затем проводят фильтрацию под вакуумом и промывку продукта от маточного раствора бидистиллированной водой или раствором бидистиллированной воды и изопропилового спирта ОСЧ. Изобретение позволяет получить высокочистый нитрат натрия с пониженным содержанием калия, повысить выход конечного продукта. 2 з.п. ф-лы, 2 ил., 3 табл., 3 пр.

Комментарии